Результат интеллектуальной деятельности: АНТИТЕЛА К ФАКТОРУ КОМПЛЕМЕНТА Bb
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА
[0001] Настоящая заявка заявляет приоритет согласно 35 U.S.С. § 119(e) предварительной заявки на патент Соединенных Штатов №61/945613, поданной 27 февраля 2014 г., и предварительной заявки на патент Соединенных Штатов №61/947880, поданной 4 марта 2014 г., которые обе в полном объеме включены в данный документ посредством ссылки.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к антителам против комплемента и их композициям, кодирующим их полинуклеотидам, экспрессионным векторам и клеткам-хозяевам для получения антител, а также композициям и способам для диагностирования и лечения заболеваний, опосредованных комплементом. В частности, раскрыты антитела против фактора В и против фактора Bb для применения в диагностировании и лечении заболеваний, связанных с фактором В и фактором Bb, в частности, возрастной макулярной дегенерации (ВМД).
УРОВЕНЬ ТЕХНИКИ
[0003] Система комплемента состоит из около 50 отдельных белков, которые функционируют как часть врожденной иммунной системы, обеспечивая начальную стадию иммунной защиты, опсонизацию чужеродного материала и тканевый гомеостаз. (Ricklin D., 2010, Complement: a Key system for immune surveillance and homeostasis. Nature: Immunology, 785-795) Система комплемента присутствует во всех многоклеточных организмах и филогенетически предшествует формированию адаптивной иммунной системы (Zarkadis I.K., 2001 Phylogenetic aspects of the complement system. Development and Comparative Immunology, 745-762.).
[0004] Активация системы комплемента происходит тремя основными путями: классическим, лектиновым и альтернативным путями. Во время процесса активации последовательные белок-белковые взаимодействия и протеолитическая активность приводят к образованию конвертаз С3 и С5. Эти конвертазы отвечают за образование продуктов расщепления активации комплемента, которые представляют эффекторные молекулы каскада комплемента, являющиеся важными для опсонизации, образования анафилатоксинов и формирования мембраноатакующего комплекса (МАК). Последний важен для литической активности каскада комплемента (Ricklin D., 2010). В нормальных условиях активация каскадов комплемента обеспечивает защиту против патогенных бактерий, а также клиренс пораженной и поврежденной ткани. Обычно формирование МАК не влияет на окружающие ткани вследствие присутствия клеточных поверхностных и растворимых регуляторных компонентов, которые включают CFH, родственные CFH белки, С4ВР, CD46, CD55, CD59 и фактор комплемента I (CFI). Однако когда происходит излишняя активация или нарушается выработка негативных регуляторных компонентов комплемента, индуцируются как острые, так и хронические болезненные состояния. Примеры, в которых причиной патологий человека является неконтролируемая активация комплемента, включают: гломерулонефрит, системную красную волчанку, пароксизмальную ночную гемоглобинурию, болезнь Альцгеймера, наследственный ангионевротический отек, миастению гравис и возрастную макулярную дегенерацию (ВМД) (Ricklin & Lambris, 2013, Complement in Immune and inflammatory Disorders: Pthaological Mechanisms. Journal of Immunology, 3831-3838).
[0005] Фактор комплемента В представляет собой белок, который циркулирует в крови в виде одноцепочечного полипептида. После активации альтернативного пути фактор В (около 750 ак) расщепляется фактором комплемента D, что приводит к образованию двух полипептидов - меньшей некаталитической цепи Ва (около 230 ак; содержащей три домена контрольного белка комплемента (ССР)) и большей каталитической субъединицы Bb (около 510 ак; содержащей домен белкового взаимодействия и домен сериновой протеазы). Фактор Bb представляет собой сериновую протеазу, которая связывается с C3b с образованием конвертазы С3 альтернативного пути, а также второй протеазы, конвертазы С5, которая расщепляет белок С5 на С5а и C5b. Продукт расщепления C5b инициирует мембраноатакующий путь, который приводит к образованию мембраноатакующего комплекса (МАК). МАК представляет собой трансмембранный канал, который приводит к осмотическому лизису патогена-мишени. Таким образом, расщепление фактора В и образование фактора Bb способствует процессу комплемента.
[0006] Фактор В является строго регулируемой, высокоспецифической сериновой протеазой. В активированной форме он катализирует ключевой этап активации комплемента, чтобы инициировать воспалительные ответы, клеточный лизис, фагоцитоз и стимуляцию В-клеток (Carroll et al., Nat. Immunol. 5: 981-986 (2004)). Фактор В активируется через процесс сборки: он связывает поверхностно-связанный C3b или его жидкофазный аналог С3 (H2O), после чего он расщепляется фактором В на фрагменты Ва (остатки 1-234; фактор Ва, фрагмент Ва, фактор комплемента Ва) и Bb (остатки 235-739; фактор Bb, фрагмент Bb, фактор комплемента Bb). Фрагмент Ва диссоциирует из комплекса, оставляя комплекс C3b-Bb конвертазы С3 альтернативного пути, который расщепляет С3 на С3а и C3b.
[0007] Возрастная макулярная дегенерация (ВМД) является лидирующей причиной слепоты у старшего поколения в развитых странах. Только среди населения США заболеваемость запущенными формами ВМД, связанными с потерей зрения, наблюдается почти у 2 миллионов человек. Другие 7 миллионов человек с промежуточной ВМД подвержены высокому риску развития запущенных форм ВМД. Включение населения Европы практически удваивает число пораженных людей. ВМД характеризуется прогрессирующей потерей зрения вследствие паравоспалительного процесса, приводящего к прогрессирующей дегенерации нейроретины и прилегающих тканей, которые включают пигментный эпителий сетчатки (ПЭС) и хориокапилляры. Большинство случаев клинически значимой потери зрения возникают, когда нейродегенеративные изменения оказывают влияние на область центрального зрения в высокоспециализированной области глаза, отвечающей за хорошую остроту зрения, -макуле. Заболевание оказывает колоссальное влияние на физическое и умственное здоровье человека вследствие потери зрения и возрастающей зависимости от членов семьи при осуществлении повседневных задач.
[0008] Дерегуляция системы комплемента сильно коррелирует с развитием ВМД. Во-первых, генетические мутации в генах комплемента изменяют риск развития ВМД у человека. Кроме того, связанное с ВМД воспаление ассоциировано с дерегуляцией активности комплемента, о чем свидетельствует повышение количества продуктов активации комплемента в системной циркуляции и в тканях ВМД согласно данным гистопатологического анализа. Новые открытия обратили внимание на потенциальное патологическое влияние мембраноатакующего комплекса в возникновении заболевания (Whitmore S, et al. 2014, "Complement activation and choriocapillaris loss in early AMD: Implications for pathphysiology and therapy. Progress in Retinal and Eye Research, December 5. 2014 EPub ahead of print).
[0009] В настоящем изобретении предложены антитела против фактора Bb для предотвращения и лечения комплементассоциированных заболеваний, ВМД и других комплементассоциированных патологических состояний глаза.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
[0010] Изобретение включает способы и композиции, содержащие антитело против фактора Bb. В одном варианте реализации изобретения антитело против фактора Bb связывается с фактором комплемента Bb с большей аффинностью, чем с фактором комплемента В. В другом аспекте антитело против фактора Bb связывается с фактором Bb и ингибирует комплементзависимый гемолиз. В другом аспекте антитело против фактора Bb связывается с фактором комплемента Bb с Kд, меньшей чем около 1 нМ. В другом аспекте антитело против фактора Bb согласно изобретению блокирует образование мембраноатакующего комплекса (МАК).
[0011] В другом варианте реализации изобретения антитело против фактора Bb согласно изобретению содержит первую аминокислотную последовательность и вторую аминокислотную последовательность, при этом первая аминокислотная последовательность представляет собой (i) CDR1, выбранную из: (а) аминокислотной последовательности CDR1 GDIFSSHW, SEQ ID NO: 1; (b) аминокислотной последовательности CDR1, которая отличается всего не более чем на 2 аминокислотные добавки, делеции или замены от GDIFSSHW, SEQ ID NO: 1; и (с) аминокислотной последовательности CDR1 GDIFSSX1W, где X1 представляет собой гистидин, а другая аминокислота заменена аланином; (ii) CDR2, выбранную из: (а) аминокислотной последовательности CDR2 EILPRSGITHYNENFNG, SEQ ID NO: 2; (b) аминокислотной последовательности CDR2, которая отличается всего не более чем на 2 аминокислотные добавки, делеции или замены от EILPRSGITHYNENFNG, SEQ ID NO: 2; и (с) аминокислотной последовательности CDR2 X1IX2PX3SGITHYNENFNG, где X1 представляет собой глутаминовую кислоту, Х2 представляет собой лейцин, а Х3 - аргинин, и одна другая аминокислота заменена аланином; и (iii) CDR3, выбранную из: (а) аминокислотной последовательности CDR3 AINWEDS, SEQ ID NO: 3; (b) аминокислотной последовательности CDR3, которая отличается всего не более чем на 2 аминокислотные добавки, делеции или замены от AINWEDS, SEQ ID NO: 3; и (с) аминокислотной последовательности CDR3 AX1NX2X3X4S, где X1 представляет собой изолейцин, Х2 представляет собой триптофан, Х3 - глутаминовую кислоту, Х3 - аспарагиновую кислоту, и одна другая аминокислота заменена аланином; а вторая аминокислотная последовательность представляет собой (i) CDR1, выбранную из: (а) аминокислотной последовательности CDR1 HASQNVNVWL, SEQ ID NO: 4; (b) аминокислотной последовательности CDR1, которая отличается всего не более чем на 2 аминокислотные добавки, делеции или замены от HASQNVNVWL, SEQ ID NO: 4, SEQ ID NO: 4; и (с) аминокислотной последовательности CDR1 HASQNVNVX1L, где X1 представляет собой триптофан, а другая аминокислота заменена аланином; (ii) CDR2, выбранную из: (а) аминокислотной последовательности CDR2 KASNLHT, SEQ ID NO: 5; (b) аминокислотной последовательности CDR2, которая отличается всего не более чем на 2 аминокислотные добавки, делеции или замены от KASNLHT, SEQ ID NO: 5; и (с) аминокислотной последовательности CDR2 KASNLHX1, где X1 представляет собой треонин, одна другая аминокислота заменена аланином; и (iii) CDR3, выбранную из: (а) аминокислотной последовательности CDR3 QQGQSYPYT, SEQ ID NO: 6; (b) аминокислотной последовательности CDR3, которая отличается всего не более чем на 2 аминокислотные добавки, делеции или замены от QQGQSYPYT, SEQ ID NO: 6; и (с) аминокислотной последовательности CDR3 QX1GQSYPX2T, где X1 представляет собой глутаминовую кислоту, Х2 представляет собой тирозин, и одна другая аминокислота заменена аланином.
[0012] В другом варианте реализации изобретения антитело против фактора Bb согласно изобретению имеет аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 80% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO: 8-11, и аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 80% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO: 12-15. В другом варианте реализации изобретения антитело против фактора Bb согласно изобретению имеет аминокислотную последовательность вариабельного домена легкой цепи, которая по меньшей мере на 80% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO: 24-27, и аминокислотную последовательность вариабельного домена тяжелой цепи, которая по меньшей мере на 80% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO: 28-31. В другом аспекте антитело против фактора Bb согласно изобретению имеет аминокислотную последовательность вариабельного домена легкой цепи, выбранную из группы, состоящей из SEQ ID NO: 8-11, и аминокислотную последовательность вариабельного домена тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 12-15. В другом аспекте антитело против фактора Bb согласно изобретению имеет аминокислотную последовательность вариабельного домена легкой цепи, выбранную из группы, состоящей из SEQ ID NO: 24-27, и аминокислотную последовательность вариабельного домена тяжелой цепи, выбранную из группы, состоящей из SEQ ID NO: 28-31. В другом аспекте антитело против фактора Bb согласно изобретению имеет аминокислотную последовательность вариабельного домена легкой цепи SEQ ID NO: 11 и аминокислотную последовательность вариабельного домена тяжелой цепи SEQ ID NO: 15.
[0013] В другом варианте реализации изобретения антитело против фактора Bb согласно изобретению содержит вариабельный домен тяжелой цепи и легкой цепи, выбранный из аминокислотных последовательностей вариабельного домена легкой и тяжелой цепи: SEQ ID NO: 8/ SEQ ID NO: 12; SEQ ID NO: 8/ SEQ ID NO: 13; SEQ ID NO: 8/ SEQ ID NO: 14; SEQ ID NO: 8/ SEQ ID NO: 15; SEQ ID NO: 9/ SEQ ID NO: 12; SEQ ID NO: 9/ SEQ ID NO: 13; SEQ ID NO: 9/ SEQ ID NO: 14; SEQ ID NO: 9/ SEQ ID NO: 15; SEQ ID NO: 10/ SEQ ID NO: 12; SEQ ID NO: 10/ SEQ ID NO: 13; SEQ ID NO: 10/ SEQ ID NO: 14; и SEQ ID NO: 10/ SEQ ID NO: 15; SEQ ID NO: 11/ SEQ ID NO: 12; SEQ ID NO: 11/ SEQ ID NO: 13; SEQ ID NO: 11/ SEQ ID NO: 14; и SEQ ID NO: 11/ SEQ ID NO: 15.
[0014] В другом варианте реализации изобретения антитело против фактора Bb согласно изобретению содержит вариабельный домен тяжелой цепи и легкой цепи, выбранный из аминокислотных последовательностей вариабельного домена легкой и тяжелой цепи: SEQ ID NO: 24/ SEQ ID NO: 28; SEQ ID NO: 24/ SEQ ID NO: 29; SEQ ID NO: 24/ SEQ ID NO: 30; SEQ ID NO: 24/ SEQ ID NO: 31; SEQ ID NO: 25/ SEQ ID NO: 28; SEQ ID NO: 25/ SEQ ID NO: 29; SEQ ID NO: 25/ SEQ ID NO: 30; SEQ ID NO: 25/ SEQ ID NO: 31; SEQ ID NO: 26/ SEQ ID NO: 28; SEQ ID NO: 26/ SEQ ID NO: 29; SEQ ID NO: 26/ SEQ ID NO: 30; и SEQ ID NO: 26/ SEQ ID NO: 31; SEQ ID NO: 27/ SEQ ID NO: 28; SEQ ID NO: 27/ SEQ ID NO: 29; SEQ ID NO: 27/ SEQ ID NO: 30; и SEQ ID NO: 27/ SEQ ID NO: 31.
[0015] В другом аспекте антитело против фактора Bb согласно изобретению является моноклональным антителом, поликлональным антителом, рекомбинантным антителом, гуманизированным антителом, химерным антителом, мультиспецифическим антителом или фрагментом антитела. В другом аспекте антитело против фактора Bb согласно изобретению является фрагментом Fab, фрагментом Fab', фрагментом F(ab')2, фрагментом Fv, диателом или одноцепочечной молекулой антитела. В другом аспекте антитело против фактора Bb согласно изобретению принадлежит типу IgG1, IgG2, IgG3 или IgG4. В другом аспекте антитело против фактора Bb согласно изобретению сопряжено с метящей группой. Такая метящая группа может представлять собой оптическую метку, радиоизотоп, радионуклид, ферментативную группу или биотинильную группу.
[0016] В другом варианте реализации изобретение относится к процессу получения выделенного антитела согласно изобретению, который включает получение антитела согласно изобретению из клетки-хозяина, которая секретирует антитело. В одном аспекте это означает выделение или очищение антитела от клеточной культуральной среды, в которой выращивают клетку-хозяина.
[0017] В другом варианте реализации изобретение относится к молекуле нуклеиновой кислоты, кодирующей выделенное антитело согласно изобретению. В одном аспекте молекула нуклеиновой кислоты, кодирующая выделенное антитело согласно изобретению, функционально связана с регуляторной последовательностью.
[0018] В другом варианте реализации изобретение относится к фармацевтической композиции, которая содержит по меньшей мере одно антитело согласно изобретению и фармацевтически приемлемый носитель. В одном аспекте фармацевтическая композиция также может содержать дополнительный активный агент.
[0019] В другом варианте реализации изобретение относится к способу лечения или предотвращения патологического состояния у пациента, нуждающегося в лечении или предотвращении, включающему введение указанному пациенту эффективного количества по меньшей мере одного антитела против фактора Bb согласно изобретению, осуществляя тем самым лечение или предотвращение патологического состояния. В одном аспекте патологическое состояние является заболеванием глаза. В другом аспекте патологическое состояние является возрастной макулярной дегенерацией (ВМД).
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
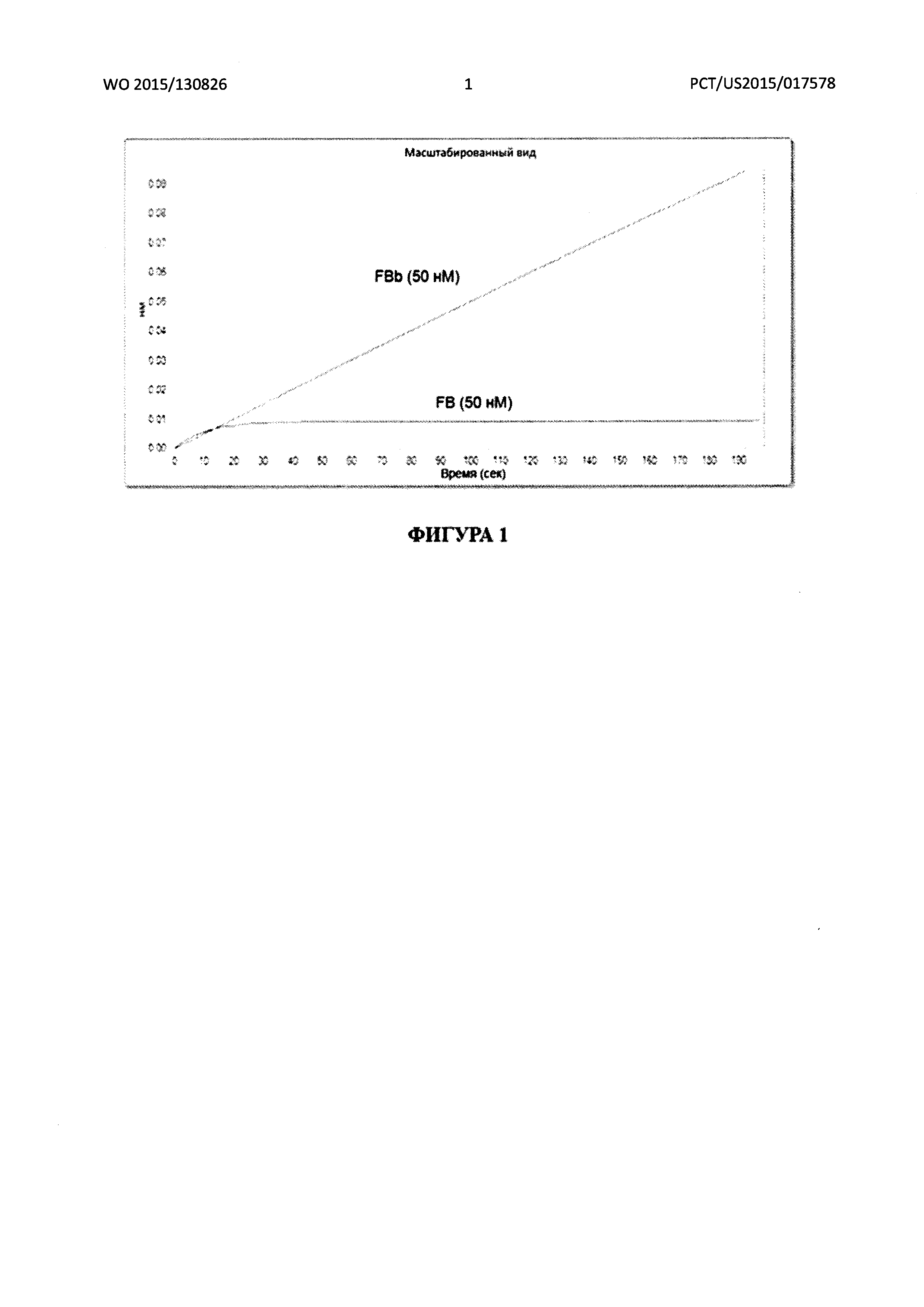
[0020] Фигура 1 иллюстрирует анализ связывания моноклонального антитела против фактора Bb с применением
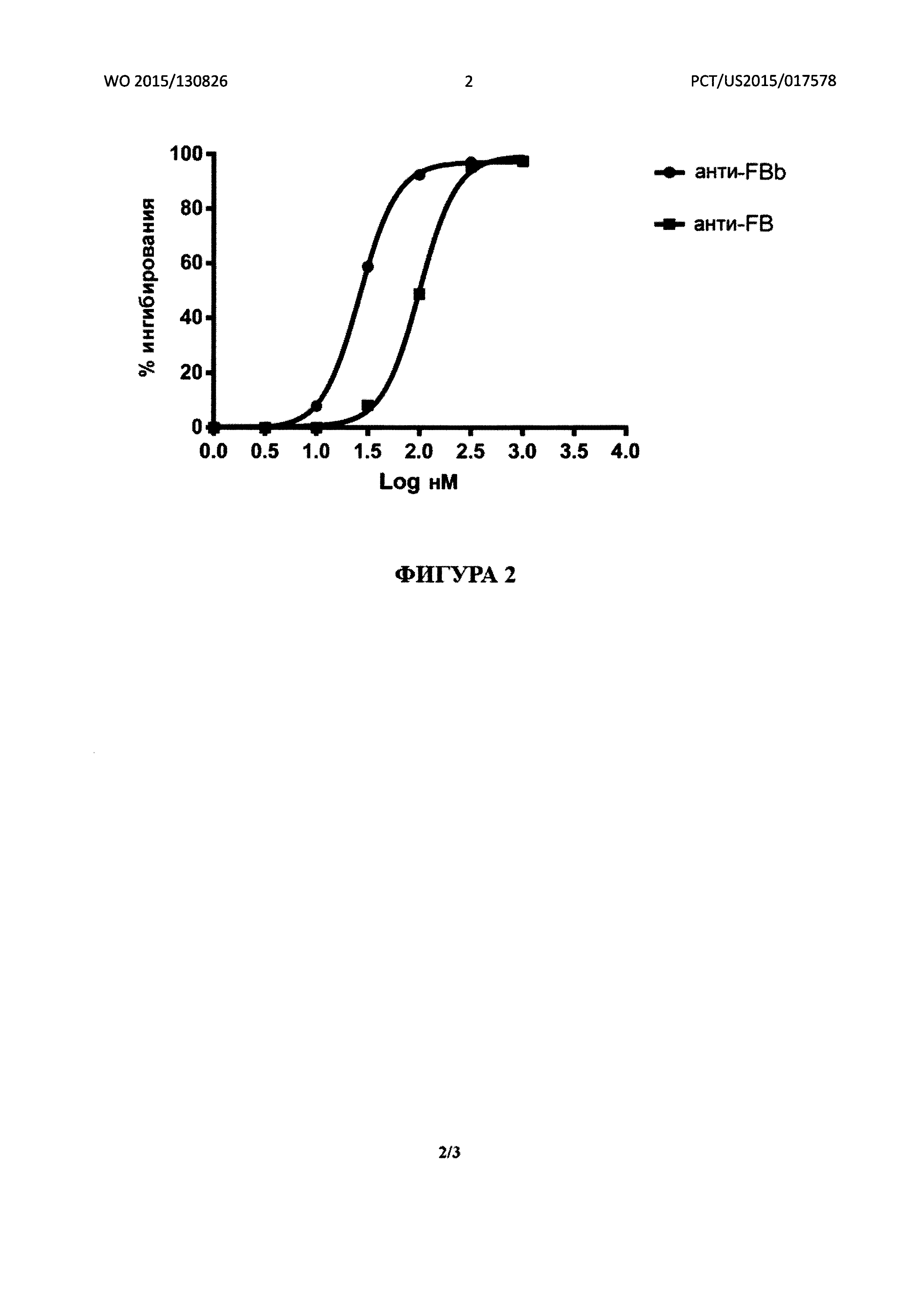
[0021] Фигура 2 иллюстрирует результаты анализа гемолиза с применением антител против фактора В или против фактора Bb в присутствии 10% нормальной человеческой сыворотки.
[0022] На Фигуре 3 приведено схематическое изображение структуры фактора комплемента В.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
[0023] Используемые в данном документе заголовки разделов предназначены исключительно для целей структурирования и не должны восприниматься как такие, которые ограничивают описываемый объект изобретения.
[0024] Для получения рекомбинантной ДНК, синтеза олигонуклеотидов, тканевого культивирования и трансформации, очистки белка и т.д. можно применять стандартные технологии. Ферментативные реакции и способы очистки можно проводить в соответствии со спецификацией производителя или так, как это обычно делают в данной области техники или как описано в данном документе. Нижеприведенные процедуры и методы в общем случае можно осуществлять в соответствии с традиционными способами, хорошо известными в данной области техники, и так, как описано в различных общих и более специализированных ссылках, которые приводятся и обсуждаются в тексте описания. Смотрите, например, Sambrook et al., 2001, Molecular Cloning: A Laboratory Manual, 3rd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., которая включена в данный документ посредством ссылки с любой целью. Если не приведены конкретные определения, номенклатура, применяемая в связи с, и лабораторные процедуры и методы молекулярной биологии, биологической химии, физической и биофизической химии, аналитической химии, органической химии и медицинской и фармацевтической химии, описанные в данном документе, являются такими, которые хорошо известны и общеприменимы в данной области техники. Для химического синтеза, химического анализа, фармацевтического приготовления, получения лекарственных препаратов и доставки и лечения пациентов можно применять стандартные методы.
[0025] В данном документе используются следующие определения:
[0026] В контексте данного документа термин «белок» относится по меньшей мере к двум ковалентно связанным аминокислотам и взаимозаменяемо употребляется с полипептидами, олигопептидами и пептидами. Две или более ковалентно связанные аминокислоты связаны пептидной связью.
[0027] «Фактор В» относится к человеческому фактору В, аминокислотная последовательность которого показана в SEQ ID NO: 16. Фактор В, белок В, фактор комплемента В, белок комплемента В относятся к той же последовательности, что и SEQ ID NO: 16. Для обозначения фактора В или вариантов фактора В могут быть использованы другие термины (например, «препропротеин В»). Фактор Ва (SEQ ID NO: 17) представляет собой один полипептидный фрагмент фактора В.
[0028] «Фактор Bb» относится к полипептидному фрагменту (SEQ ID NO: 7) человеческого фактора.
[0029] Термины «антитело» и «иммуноглобулин» употребляются взаимозаменяемо в самом широком смысле для обозначения белка, содержащего одну или более полипептидных цепей, которые взаимодействуют с конкретным антигеном путем связывания нескольких CDR и эпитопа антигена. Антитело может быть моноклональным (например, полноразмерные или интактные моноклональные антитела), поликлональным, мультивалентным и/или мультиспецифическим (например, биспецифические антитела в той мере, пока они демонстрирует желаемую биологическую активность). Антитела также могут представлять собой или включать фрагменты антител (как описано в данном документе).
[0030] Термин «эпитоп» употребляется для обозначения последовательности, структуры или молекулы, которая распознается и связывается антителом. Эпитоп может называться «антигенным участком».
[0031] «Фрагменты антитела» содержат только часть интактного антитела, при этом данная часть предпочтительно сохраняет по меньшей мере одну, предпочтительно большинство или все функции, обычно ассоциируемые с этой частью, если она присутствует в интактном антителе. Примеры фрагментов антител включают фрагменты Fab, Fab', F(ab')2 и Fv; диатела; линейные антитела; одноцепочечные молекулы антител; и мультиспецифические антитела, образуемые из фрагментов антител. В одном варианте реализации изобретения фрагмент антитела содержит антигенсвязывающий участок интактного антитела и, таким образом, сохраняет способность связывать антиген. В другом варианте реализации изобретения фрагмент антитела, например, содержащий Fc-область, сохраняет по меньшей мере одну из биологических функций, обычно ассоциируемых с Fc-областью, если она присутствует в интактном антителе, такую как связывание FcR, модуляция времени полужизни антитела, функция АЗКЦ и связывание комплемента. В одном варианте реализации изобретения фрагмент антитела представляет собой моновалентное антитело, которое имеет in vivo время полужизни, в значительной степени сходное с интактным антителом. Например, такой фрагмент антитела может содержать антигенсвязывающее плечо, связанное с последовательностью Fc, способное придавать фрагменту in vivo стабильность.
[0032] В контексте данного документа «моноклональное» антитело относится к антителу, полученному из популяции клеток, при этом популяция клеток получена при помощи клонирования из одной родительской клетки. Моноклональные антитела являются гомогенными антителами, т.е. отдельные антитела, составляющие популяцию, являются идентичными в том смысле, что они получены из одних и тех же генов и имеют одну и ту же аминокислотную последовательность и белковую структуру за исключением возможных естественных мутаций, которые могут присутствовать в малых количествах, и посттрансляционных модификаций, которые могут, в некоторых случаях, различаться. Моноклональные антитела могут, в некоторых вариантах реализации изобретения, быть высокоспецифическими. В некоторых вариантах реализации изобретения моноклональное антитело может быть направлено против одного антигенного участка. Кроме того, в отличие от других препаратов антител, которые, как правило, содержат разные антитела, направленные против разных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты на антигене. Отдельные моноклональные антитела можно получать любым конкретным способом. Например, моноклональные антитела для применения в соответствии с настоящим изобретением можно получать методом гибридомы, впервые описанным Kohler et al. (1975) Nature 256: 495, или можно получать методами рекомбинантных ДНК (смотрите, например, патент США №4816567) или из фаговых библиотек антител, используя методы, описанные в Clackson et al. (1991) Nature 352: 624-628 and Marks et al. (1991) J. Mol. Biol. 222: 581-597.
[0033] Термин «поликлональное» антитело используется для описания гетерогенной популяции антител, полученной из гетерогенной популяции родительских, вырабатывающих антитела клеток. В большинстве случаев поликлональные антитела обладают разной аффинностью в отношении разных эпитопов и получены из генов с разными последовательностями.
[0034] «Химерные» антитела представляют собой антитела, содержащие аминокислотные последовательности, полученные от двух или более разных видов.
[0035] «Гуманизированные» антитела представляют собой химерные антитела, полученные из нечеловеческого родительского антитела. Во многих случаях конкретные аминокислотные позиции в гуманизированном антителе были изменены так, чтобы соответствовать аминокислотной идентичности в соответствующей позиции в человеческом антителе. Во многих случаях позиции в вариабельной области родительского (нечеловеческого) антитела замещены аминокислотами из вариабельной области человеческого вида. Это приводит к созданию гуманизированного мышиного, крысиного, кроличьего или обезьяньего антитела, обладающего желаемой специфичностью, аффинностью и свойствами.
[0036] «Вариант» относится к последовательностям, которые содержат по меньшей мере одно отличие по сравнению с родительской последовательностью. Вариантный полипептид представляет собой белок, имеющий по меньшей мере около 75% идентичности аминокислотной последовательности с родительской последовательностью. Вариантный белок может иметь по меньшей мере около 80% идентичности аминокислотной последовательности или по меньшей мере около 85% идентичности аминокислотной последовательности, или по меньшей мере около 90% идентичности аминокислотной последовательности, или по меньшей мере около 95% идентичности аминокислотной последовательности, или по меньшей мере около 98% идентичности аминокислотной последовательности, или по меньшей мере около 99% идентичности аминокислотной последовательности с нативной аминокислотной последовательностью или аминокислотной последовательностью дикого типа. В некоторых случаях вариантные антитела представляют собой антитела, имеющие одно или более различие(ий) в аминокислотной последовательности по сравнению с родительским антителом. Гуманизированные и химерные антитела являются вариантными антителами. Следовательно, вариантные антитела имеют менее 100% идентичности последовательности с родительским антителом.
[0037] «Выделенная» или «очищенная» относится к молекуле, которая была отделена и/или избавлена по меньшей мере от одного компонента своей естественной среды, при этом указанный компонент представляет собой материал, который может препятствовать применению или активности молекулы. Компоненты включают пептиды, сахара, нуклеиновые кислоты, ферменты, гормоны и другие белковые или небелковые растворенные компоненты.
[0038] «Определяющие комплементарность области» (CDR) относятся к одной или более областям в антителе, в которых остатки одной или более CDR способствуют связыванию антигена. Во многих случаях отдельные аминокислоты CDR могут находиться в непосредственной близости к атомам антигена-мишени. В некоторых вариантах реализации изобретения CDR могут находиться в иммуноглобулине, который может состоять из трех областей CDR. В некоторых случаях, например, в случае наличия более одной последовательности CDR в более крупной аминокислотной последовательности, CDR могут быть разделены другими последовательностями, а сами CDR пронумерованы. В некоторых случаях несколько CDR определены как CDR1, CDR2 и CDR3. Каждая CDR может содержать аминокислотные остатки из определяющей комплементарность области согласно определению Кабата. Kabat et al., Sequences of Proteins of Immunological Interest, 5th Ed. Public Health Service, National Institutes of Health, Bethesda, Md. (1991)). Нумерация аминокислот CDR, а также других последовательностей антитела или фрагмента антитела соответствует нумерации Кабата. Во многих случаях CDR можно определить по их позиции в последовательности вариабельной области (нумерация по Кабату), например, CDR 1 легкой цепи может содержать аминокислотную последовательность между позицией 24 и позицией 33; между позицией 50 и позицией 56 в случае LC CDR2; и между позицией 89 и позицией 97 в случае LC CDR 3; a CDR тяжелой цепи могут находиться между позицией 26 и позицией 33 в случае CDR1; позицией 50 и позицией 66 в случае НС CDR 2; и между позицией 97 и позицией 103 в случае НС CDR 3, и/или гипервариабельные петли могут находиться между остатками легкой цепи 26-32 (LC CDR1), остатками 50-52 (LC CDR2) и остатками 91-96 (LC CDR3); и остатками тяжелой цепи 26-32 (НС CDR1), остатками 53-55 (НС CDR2) и остатками 97-101 (НС CDR3). В некоторых случаях определяющая комплементарность область может включать аминокислотные остатки как из области CDR, определяемой по Кабату, так и гипервариабельной петли. В некоторых вариантах реализации изобретения, например, в которых антитело представляет собой одноцепочечный иммуноглобулин, может присутствовать более одной CDR, более двух CDR, более трех CDR, более четырех CDR или более пяти CDR. В некоторых вариантах реализации изобретения антитело может состоять из шести CDR.
[0039] «Каркасные области», FR, представляют собой остатки вариабельного домена, отличные от остатков CDR. В большинстве вариантов реализации изобретения вариабельный домен содержит от двух до четырех FR, определяемых последовательно. Например, вариабельная область, содержащая три CDR, содержит четыре FR: FR1, FR2, FR3 и FR4. Если CDR определены по Кабату, расположение остатков FR легкой цепи соответствует приблизительно остаткам 1-23 (LCFR1), 34-49 (LCFR2), 57-88 (LCFR3) и 98-107 (LCFR4), а расположение остатков FR тяжелой цепи соответствует приблизительно остаткам 1-25 (HCFR1), 34-49 (HCFR2), 67-96 (HCFR3) и 104-113 (HCFR4) из остатков тяжелой цепи. Если CDR содержат аминокислотные остатки из гипервариабельных петель, расположение остатков FR легкой цепи соответствует приблизительно остаткам 1 -23 (LCFR1), 34-49 (LCFR2), 57-88 (LCFR3) и 98-107 (LCFR4) из легкой цепи, а расположение остатков FR тяжелой цепи соответствует приблизительно остаткам 1-25 (HCFR1), 34-49 (HCFR2), 67-96 (HCFR3) и 104-113 (HCFR4) из остатков тяжелой цепи. В некоторых случаях, когда CDR содержит аминокислотные остатки как из CDR согласно определению Кабата, так и остатки гипервариабельной петли, остатки FR будут соответственно скорректированы. Например, если НС CDR1 содержит аминокислоты Н26-Н35, остатки FR1 тяжелой цепи соответствуют позициям 1-25, а остатки FR2 соответствуют позициям 36-49.
[0040] «Вариабельный домен» соответствует позициям легкой цепи и тяжелой цепи традиционной молекулы антитела, которая содержит аминокислотные последовательности определяющих комплементарность областей (CDR) и каркасных областей (FR). VH относится к вариабельному домену тяжелой цепи. VL относится к вариабельному домену легкой цепи.
[0041] «Fv» или «фрагмент Fv» относится к фрагменту антитела, который содержит полный участок распознавания и связывания антигена, содержащий последовательности FR и CDR. Во многих вариантах реализации изобретения Fv состоит из димера вариабельного домена одной тяжелой и одной легкой цепи, находящихся в тесной связи, которая по природе может быть ковалентной, например в одноцепочечной молекуле Fv (scFv). Взаимодействие трех CDR каждого вариабельного домена определяет антигенсвязывающий участок на поверхности полипептида VH-VL. Вместе шесть CDR или их подгруппа придаются антителу антигенсвязывающую специфичность. При этом даже один вариабельный домен (или половина Fv, содержащая только три CDR, специфических в отношении антигена) обладает в некоторых случаях способностью распознавать и связывать антиген, хотя обычно с более низкой аффинностью, чем целый связывающий участок.
[0042] «Fab» или «фрагмент Fab» содержит вариабельный и константный домен (CL) легкой цепи и вариабельный домен и первый константный домен (СН1) тяжелой цепи. Фрагменты антитела F(ab')2 содержат пару фрагментов Fab, которые в общем случае ковалентно связаны вблизи своего карбокси-конца посредством шарнирных цистеинов между ними. Также в данной области техники известны другие химические сопряжения фрагментов антител.
[0043] «Процент (%) идентичности аминокислотных последовательностей» определяется как процент аминокислотных остатков в кандидатной последовательности, которые являются идентичными с аминокислотными остатками в контрольной последовательности, после выравнивания последовательностей и внесения, в случае необходимости, гэпов для достижения максимального процента идентичности последовательностей, и без учета каких-либо консервативных замен как части идентичности последовательностей. Выравнивание в целях определения процента идентичности аминокислотных последовательностей можно проводить различными способами, находящимися в компетенции данной области техники, например, используя общедоступное программное обеспечение, такое как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить подходящие параметры для проведения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания на протяжении полной длины сравниваемых последовательностей. Затем рассчитывают идентичность последовательностей по отношению к более длинной последовательности, т.е., даже если более короткая последовательность демонстрирует 100% идентичности последовательностей с частью более длинной последовательности, общая идентичность последовательностей будет меньше 100%.
[0044] «Процент (%) гомологии аминокислотных последовательностей» определяется как процент аминокислотных остатков в кандидатной последовательности, которые являются гомологичными с аминокислотными остатками в контрольной последовательности, после выравнивания последовательностей и внесения, в случае необходимости, гэпов для достижения максимального процента гомологии последовательностей. Это способ учитывает консервативные замены. Консервативными заменами являются такие замены, в которых возможна замена аминокислоты сходной аминокислотой. Аминокислоты могут иметь сходство в нескольких характеристиках, например, размере, форме, гидрофобности, гидрофильности, заряде, изоэлектрической точке, полярности, ароматичности и т.д. Выравнивание в целях определения процента гомологии аминокислотных последовательностей можно проводить различными способами, находящимися в компетенции специалистов в данной области техники. В некоторых случаях аминокислотные последовательности можно выравнивать, используя общедоступное программное обеспечение, такое как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить подходящие параметры для проведения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания на протяжении полной длины сравниваемых последовательностей. Затем рассчитывают гомологию последовательностей по отношению к более длинной последовательности, т.е., даже если более короткая последовательность демонстрирует 100% идентичности последовательностей с частью более длинной последовательности, общая идентичность последовательностей будет меньше 100%.
[0045] «Процент (%) идентичности нуклеотидных последовательностей» определяется как процент нуклеотидов в кандидатной последовательности, которые являются идентичными с нуклеотидами в контрольной последовательности, после выравнивания последовательностей и внесения, в случае необходимости, гэпов для достижения максимального процента идентичности последовательностей. Выравнивание в целях определения процента идентичности нуклеотидных последовательностей можно проводить различными способами, находящимися в компетенции данной области техники, например, используя общедоступное программное обеспечение, такое как программное обеспечение BLAST, BLAST-2, ALIGN или Megalign (DNASTAR). Специалисты в данной области техники могут определить подходящие параметры для проведения выравнивания, включая любые алгоритмы, необходимые для достижения максимального выравнивания на протяжении полной длины сравниваемых последовательностей. Затем рассчитывают идентичность последовательностей по отношению к более длинной последовательности, т.е., даже если более короткая последовательность демонстрирует 100% идентичности последовательностей с частью более длинной последовательности, общая идентичность последовательностей будет меньше 100%.
[0046] «Активность» или «биологическая активность» молекулы может зависеть от типа молекулы и доступности методов для анализа данной активности. Например, в контексте антитела к фактору Bb активность относится к его способности частично или полностью ингибировать биологическую активность фактора Bb, например, связывание с другими белками комплемента, активность сериновых протеаз или образование МАК. Предпочтительной биологической активностью заявляемого антитела к фактору Bb является возможность достигать определяемого улучшения состояния, например, патологии, ассоциированного с фактором заболевания или патологического состояния, такого как, например, комплементассоциированное патологическое состояние глаз. В некоторых случаях активность, ингибируемая раскрытым антителом к фактору Bb, является протеазной или расщепляющей активностью. В других случаях активность является способностью связывать другие белки комплемента в комплекс. В некоторых вариантах реализации изобретения активность раскрытого антитела к фактору Bb определяется по его способности ингибировать гемолиз. Активность можно определить, используя in vitro или in vivo методы, включая анализ связывания, использование релевантной животной модели или человеческие клинические исследования.
[0047] Выражение «комплементассоциированное патологическое состояние глаз» употребляется в самом широком смысле и включает все патологические состояния глаз, в патологию которых вовлечен комплемент, активируемый классическим, лектиновым, альтернативным или внешним путями. Комплементассоциированные патологические состояния глаз включают, без ограничений, макулярные дегенеративные заболевания, такие как все стадии возрастной макулярной дегенерации (ВМД), включая сухую и экссудативную (неэкссудативную и экссудативную) формы, хориоидальную неоваскуляризацию (ХНВ), увеит, диабетические и другие связанные с ишемией ретинопатии, включая диабетическую макулярную эдему, окклюзию центральной вены сетчатки (ОЦВС), разветвленную окклюзию вены сетчатки (РОВС) и другие внутриглазные неоваскулярные заболевания, такие как диабетическая макулярная эдема, патологическая миопия, болезнь фон Гиппеля-Линдау, гистоплазмоз глаза, неоваскуляризация роговицы и неоваскуляризация сетчатки. Предпочтительная группа комплементассоциированных патологических состояний глаз включает возрастную макулярную дегенерацию (ВМД), включая сухую и влажную (неэкссудативную и экссудативную) ВМД, хориоидальную неоваскуляризацию (ХНВ), макулярную телеангиэктазию, увеит, диабетические и другие связанные с ишемией неоваскулярные ретинопатии или клеточную дегенеративную диабетическую макулярную эдему, патологическую миопию, болезнь фон Гиппеля-Линдау, гистоплазмоз глаза, коллоидную дистрофию сетчатки Дойна/Malattia Leventinese, болезнь Штаргардта, глаукому, окклюзию центральной вены сетчатки (ОЦВС), РОВС, неоваскуляризацию роговицы, неоваскуляризацию сетчатки.
[0048] «Фармацевтически приемлемый» относится к препарату, утвержденному или утверждаемому регуляторным органом федеральной власти или власти штата или приведенному в фармакопее США или другой общепризнанной фармакопее для использования на животных и, в частности, на людях.
[0049] «Фармацевтически приемлемая соль» относится к соли соединения, которое обладает необходимой фармакологической активностью родительского соединения. Такие соли включают кислотно-аддитивные соли, образуемые с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и тому подобные; или образуемые с органическими кислотами, такими как уксусная кислота, пропионовая кислота, капроновая кислота, циклопентанпропионовая кислота, гликолевая кислота, пировиноградная кислота, молочная кислота, малоновая кислота, янтарная кислота, яблочная кислота, малеиновая кислота, фумаровая кислота, винная кислота, лимонная кислота, бензойная кислота, 3-(4-гидроксибензоил)бензойная кислота, коричная кислота, миндальная кислота, метансульфоновая кислота, этансульфоновая кислота, 1,2-этандисульфоновая кислота, 2-гидроксиэтансульфоновая кислота, бензолсульфоновая кислота, 4-хлорбензолсульфоновая кислота, 2-нафталинсульфоновая кислота, 4-толуолсульфоновая кислота, камфорсульфоновая кислота, 4-метилбицикло[2.2.2]-окт-2-ен-1-карбоновая кислота, глюкогептоновая кислота, 3-фенилпропионовая кислота, триметилуксусная кислота, третичная капроновая кислота, лаурил серная кислота, глюконовая кислота, глутаминовая кислота, гидроксинафтойная кислота, салициловая кислота, стеариновая кислота, муконовая кислота и тому подобные; и соли, образуемые, когда кислотный протон, присутствующий в родительском соединении, замещается ионом металла, например, ионом щелочного металла, ионом щелочноземельного металла или ионом алюминия; или координационные комплексы с органическим основанием, таким как этаноламин, диэтаноламин, триэтаноламин, N-метилглюкамин и тому подобные. В определенных вариантах реализации изобретения фармацевтически приемлемая соль является хлористоводородной солью. В определенных вариантах реализации изобретения фармацевтически приемлемая соль является натриевой солью.
[0050] «Фармацевтически приемлемое вспомогательное вещество» относится к фармацевтически приемлемому разбавителю, фармацевтически приемлемому адъюванту, фармацевтически приемлемому раствору, фармацевтически приемлемому носителю или комбинации любого из вышеперечисленных компонентов, с которым соединение, предложенное в настоящем изобретении, можно вводить пациенту, который не нарушает его фармакологическую активность и который является нетоксичным при введении в дозах, достаточных для обеспечения терапевтически эффективного количества соединения или его фармакологически активного метаболита.
[0051] «Лечением» называется введение по меньшей мере одного терапевтического агента для предотвращения развития или изменения патологии нарушения, или облегчения или уменьшения симптома нарушения. Соответственно, лечение относится как к терапевтическому лечению, так и к профилактическим или превентивным мерам. Нуждающиеся в лечении включают тех, кто уже имеет нарушение, а также тех, для кого необходимо предотвращение нарушения. Как раскрыто в данном документе, предпочтительный агент для введения содержит по меньшей мере одно из раскрытых антител против фактора Bb. При лечении связанного с комплементом заболевания терапевтический агент, содержащий по меньшей мере одно из раскрытых в настоящем изобретении антител или кодирующую последовательность для такого антитела, может прямым или непрямым образом менять интенсивность ответа компонента пути комплемента или делать заболевание более восприимчивым к лечению другими терапевтическими агентами, например, антибиотиками, противогрибковыми средствами, противовоспалительными агентами, химиотерапевтическими средствами и т.д.
[0052] «Терапевтически эффективное количество» относится к количеству агента, которое при введение субъекту в целях лечения заболевания или по меньшей мере одного из клинических симптомов заболевания является достаточным для осуществления такого лечения заболевания или его симптома. Конкретное терапевтически эффективное количество может варьироваться в зависимости, например, от агента, заболевания и/или симптомов заболевания, тяжести заболевания и/или симптомов заболевания, возраста, массы и/или здоровья пациента, лечение которого проводят, и предписаний лечащего врача. Подходящее количество любого заданного компонента может быть установлено специалистами в данной области техники и/или его можно определить при помощи рутинных экспериментов.
[0053] «Терапевтически эффективная доза» относится к дозе, которая обеспечивает эффективное лечение заболевания у пациента. Терапевтически эффективная доза может варьироваться от агента к агенту и/или от пациента к пациенту и может зависеть от факторов, таких как состояние пациента и тяжесть заболевания. Терапевтически эффективную дозу можно определить в соответствии с рутинными фармакологическими процедурами, известными специалистам в данной области техники.
[0054] «Патология» заболевания, такого как комплементассоциированное заболевание глаз, включает все явления, которые мешают хорошему самочувствию пациента. Они включают, без ограничений, аномальный или неконтролируемый рост клеток, выработку белка, аномальную или неконтролируемую гибель клеток, выработку аутоантител, выработку комплемента, активацию комплемента, образование МАК, препятствование нормальному функционированию соседних клеток, высвобождение цитокинов или других секреторных продуктов на аномальных уровнях, супрессию или усиление любых воспалительных или иммунологических ответов, инфильтрацию воспалительных клеток в межклеточное пространство и т.д.
[0055] В контексте данного документа «млекопитающее» относится к любому животному, классифицируемому как млекопитающее, включая, без ограничений, людей, высших приматов, домашних и сельскохозяйственных животных, а также животных из зоопарков, спортивных или домашних животных, таких как лошади, свиньи, крупный рогатый скот, собаки, кошки и хорьки и т.д. В предпочтительном варианте реализации изобретения млекопитающее является человеком.
[0056] Введение «в комбинации с» одним или более дополнительными терапевтическими агентами включает одновременное (параллельное) введение и последовательное введение в любом порядке.
[0057] В настоящем изобретении предложены антитела, которые связывают белок фактора Bb.
[0058] Описанные в данном документе антитела содержат каркасную структуру с одной или более определяющими комплементарность областями (CDR). В определенных вариантах реализации изобретения CDR содержат не более двух аминокислотных добавок, делеций или замен по сравнению с одной или более из CDR1 CDR2 и CDR3 тяжелой цепи и CDR1 CDR2 и CDR3 легкой цепи родительской последовательности. В других вариантах реализации изобретения CDR определяются по консенсусной последовательности, содержащей общие консервативные аминокислотные последовательности и вариабельные аминокислотные последовательности, как описано в данном документе.
[0059] В определенных вариантах реализации изобретения в основе каркасной структуры антител к фактору Bb согласно изобретению могут лежать антитела, включая, но не ограничиваясь этим, моноклональные антитела, биспецифические антитела, минитела, доменные антитела, синтетические антитела (например, миметики антител), химерные антитела, гуманизированные антитела, продукты слияния антител (например, конъюгаты антител) и фрагменты каждого из перечисленных антител, соответственно. Различные структуры дополнительно описаны и определены ниже. Антитела к фактору Bb применимы в лечении последствий, симптомов и/или патологий, связанных с активностью фактора Bb. Они включают, но не ограничиваются этим, атеросклероз, ишемию-реперфузию после острого инфаркта миокарда, нефрит при пурпуре Шенлейна-Геноха, геморрагический васкулит, ревматоидный артрит, артериит, аневризму, инсульт, кардиомиопатию, геморрагический шок, повреждение с размозжением тканей, полиорганную недостаточность, гиповолемический шок и кишечную ишемию, отторжение трансплантата, кардиохирургию, ЧКТА, самопроизвольный выкидыш, нейрональное повреждение, повреждение спинного мозга, миастению гравис, болезнь Хантингтона, амиотрофический боковой склероз, множественный склероз, синдром Гийена-Барре, болезнь Паркинсона, болезнь Альцгеймера, синдром острой дыхательной недостаточности, астму, хроническое обструктивное заболевание легких, острое посттрансфузионное повреждение легких, острое повреждение легких, болезнь Гудпасчера, инфаркт миокарда, воспаление после применения искусственного кровообращения, искусственное кровообращение, септический шок, отторжение трансплантата, ксенотрансплантацию, ожоговые повреждения, системную красную волчанку, мембранозный нефрит, болезнь Бергера, псориаз, пемфигоид, дерматомиозит, антифосфолипидный синдром, воспалительное заболевание кишечника, гемодиализ, лейкоферез, плазмаферез, гепарин-индуцированную экстракорпоральную преципитацию ЛПНП с мембранной оксигенацией, экстракорпоральный лейкоферез с мембранной оксигенацией, плазмаферез, гепарин-индуцированную экстракорпоральную преципитацию ЛПНП с мембранной оксигенацией, экстракорпоральную мембранную оксигенацию и тому подобное.
[0060] Другие применения раскрытых антител включают, например, диагностирование комплемент и фактор Bb-ассоциированных заболеваний.
[0061] В аспектах настоящего изобретения предложены антитела к фактору Bb, в частности, антитела, которые содержат по меньшей мере одну CDR, в том числе CDR тяжелой и/или легкой цепи, как более полно описано ниже, или их комбинации. [0062] В одном аспекте антитела к фактору Bb ингибируют активность фактора Bb или ингибируют способность фактора Bb образовывать белковые комплексы. Не ограничиваясь конкретным механизмом или теорией, можно сказать, что в некоторых вариантах реализации изобретения антитела нарушают путь комплемента, тем самым нарушая каскад комплемента, образование МАК и лизис клеток. Это нарушение может включать, но не ограничивается этим, сухую и влажную (неэкссудативную и экссудативную) ВМД, хориоидальную неоваскуляризацию (ХНВ), увеит, диабетические и другие связанные с ишемией ретинопатии, диабетическую макулярную эдему, патологическую миопию, болезнь фон Гиппеля-Линдау, гистоплазмоз глаза, окклюзию центральной вены сетчатки (ОЦВС), неоваскуляризацию роговицы, неоваскуляризацию сетчатки и тому подобное.
[0063] Таким образом, антитела согласно изобретению могут служить для выявления патологических состояний, связанных с системой комплемента, или заболеваний или патологических состояний, связанных с фактором Bb. Кроме того, антитела можно применять для регуляции и/или супрессии эффектов, опосредованных фактором В и/или другими нижерасположенными белками комплемента, как такие, которые проявляют эффективность в лечении и предотвращении различных заболеваний или патологических состояний, связанных с комплементом и/или фактором Bb. Это нарушение может включать, но не ограничивается этим, атеросклероз, ишемию-реперфузию после острого инфаркта миокарда, нефрит при пурпуре Шенлейна-Геноха, геморрагический васкулит, ревматоидный артрит, артериит, аневризму, инсульт, кардиомиопатию, геморрагический шок, повреждение с размозжением тканей, полиорганную недостаточность, гиповолемический шок и кишечную ишемию, отторжение трансплантата, кардиохирургию, ЧКТА, самопроизвольный выкидыш, нейрональное повреждение, повреждение спинного мозга, миастению гравис, болезнь Хантингтона, амиотрофический боковой склероз, множественный склероз, синдром Гийена-Барре, болезнь Паркинсона, болезнь Альцгеймера, синдром острой дыхательной недостаточности, астму, хроническое обструктивное заболевание легких, острое посттрансфузионное повреждение легких, острое повреждение легких, болезнь Гудпасчера, инфаркт миокарда, воспаление после применения искусственного кровообращения, искусственное кровообращение, септический шок, отторжение трансплантата, ксенотрансплантацию, ожоговые повреждения, системную красную волчанку, мембранозный нефрит, болезнь Бергера, псориаз, пемфигоид, дерматомиозит, антифосфолипидный синдром, воспалительное заболевание кишечника, гемодиализ, лейкоферез, плазмаферез, гепарин-индуцированную экстракорпоральную преципитацию ЛПНП с мембранной оксигенацией, экстракорпоральный лейкоферез с мембранной оксигенацией, плазмаферез, гепарин-индуцированную экстракорпоральную преципитацию ЛПНП с мембранной оксигенацией, экстракорпоральную мембранную оксигенацию и тому подобное.
[0064] В частности, в изобретении предложены антитела против фактора Bb и полинуклеотиды, которые их кодируют. В различных аспектах антитела против фактора Bb ингибируют по меньшей мере один из биологических ответов, опосредуемых фактором Bb и/или другими белками комплемента, и, таким образом, могут применяться для уменьшения проявления комплементассоциированных и фактор Bb-ассоциированных заболеваний или нарушений. Также в изобретении предложены экспрессионные системы, включая клеточные линии млекопитающих и бактериальные клетки, для получения антител к фактору Bb и способы лечения заболеваний, связанных с фактором Bb.
[0065] Антитела согласно изобретению содержат каркасную структуру с одной или более определяющими комплементарность областями (CDR), которые связываются с фактором Bb. В одном варианте реализации изобретения аминокислотная последовательность содержит любую из SEQ ID NO: 1-6 или SEQ ID NO: 18-23.
[0066] В различных вариантах реализации изобретения антитело содержит первую и/или вторую аминокислотную последовательность. В одном варианте реализации изобретения первая и/или вторая аминокислотная последовательность выбрана из группы, состоящей из SEQ ID NO: 8-15 или SEQ ID NO: 24-31.
[0067] В различных вариантах реализации изобретения антитела могут содержать одну или обе из первой и второй аминокислотных последовательностей. Первая и вторая аминокислотные последовательности могут представлять собой одну линейную аминокислотную последовательность, могут быть ковалентно связаны дисульфидными мостиками или могут быть нековалентно связанными.
Фактор Bb
[0068] Фактор комплемента В представляет собой гликозилированный белок, состоящий из одной полипептидной цепи в 93000 Да, кодируемой геном CFB. Он является важным компонентом альтернативного пути активации комплемента и содержится в человеческой плазме в концентрации приблизительно 200 мкг/мл. В присутствии Mg++ фактор В связывается с C3b, а комплекс C3b:В может активироваться фактором D, сериновой протеазой, которая циркулирует в виде активной трипсин-подобной сериновой протеазы. Расщепление фактора В фактором D приводит к высвобождению фрагмента Ва (33000 Да) и оставляет фрагмент Bb (60000 Да) связанным с C3b. Эта Bb-субъединица представляет собой сериновую протеазу, называемую конвертазой С3 и С5, так как она конвертирует оба этих белка в активную форму путем отщепления небольших пептидов С3а и С5а, соответственно.
[0069] Фактор В является строго регулируемой, высокоспецифической сериновой протеазой. В активированной форме он катализирует ключевой этап активации комплемента, чтобы инициировать воспалительные ответы, клеточный лизис, фагоцитоз и стимуляцию В-клеток. Фактор В активируется путем сборки с поверхностно-связанным C3b или его жидкофазным аналогом С3 (Н2О). После связывания с С3 фактор В расщепляется фактором D на малый фрагмент, фактор Ва (остатки 1-234) и большой фрагмент, фактор Bb (остатки 235-739). Фрагмент Ва диссоциирует из комплекса, оставляя комплекс C3b-Bb конвертазы С3 альтернативного пути, который расщепляет С3 на С3а и C3b. Комплекс протеазы C3b-Bb является нестабильным, и после диссоциации из комплекса фактор Bb повторно не ассоциирует с C3b.
[0070] Профермент фактор В состоит из трех N-концевых доменов контрольного белка комплемента (ССР), соединенных линкером из 45 остатков с доменом VWA, и С-концевого домена сериновой протеазы (SP), который несет каталитический центр. В активном центре фактора В наблюдаются резкие отличия от других сериновых протеаз. Фактор Bb содержит С-концевой домен сериновой протеазы, а домены ССР находятся в факторе Ва.
[0071] Аминокислотная последовательность человеческого фактора В приведена в SEQ ID NO: 16. Другие формы фактора В, применимые в настоящем изобретении, включают мутантов и вариации, которые являются по меньшей мере на 70% или по меньшей мере на 90% гомологичными последовательности человеческого нативного фактора В SEQ ID NO: 16.
[0072] Аминокислотная последовательность человеческого фактора Bb представлена SEQ ID NO: 7. Другие формы фактора Bb, применимые в настоящем изобретении, включают мутантов и вариации, которые являются по меньшей мере на 70% или по меньшей мере на 90% гомологичными последовательности человеческого нативного фактора Bb SEQ ID NO: 7.
[0073] Аминокислотная последовательность человеческого фактора Ва представлена SEQ ID NO: 17. Другие формы фактора Ва, применимые в настоящем изобретении, включают мутантов и вариации, которые являются по меньшей мере на 70% или по меньшей мере на 90% гомологичными последовательности человеческого нативного фактора Ва SEQ ID NO: 17.
[0074] Ингибирующая функция/активность фактора В, фактора Bb или фактора Ва, как описано в данном документе, представляет ингибирование фактора Bb. Одним из примеров анализа альтернативного пути комплемента является анализ гемолиза: активация альтернативного пути (АП) требует более высоких концентраций сыворотки, чем в случае классического пути. В общем случае для анализа используют конечную концентрацию, составляющую 5 мМ Mg++ в присутствии 5 мМ ЭДТУ, при этом ЭДТУ преимущественно хелатирует Са++. АП у большинства видов млекопитающих активируется спонтанно при помощи кроличьих эритроцитов, следовательно, они являются удобной мишенью. Кроличьи эритроциты (Complement Technology, Inc.) готовят путем 3-разовой промывки GVB0 (продукт CompTech) и пересуспендирования в 5×108 /мл. Разные количества антитела против фактора Bb разводили GVB0. Смешивают 100 мкл реакции на льду из ряда серийных разведений антитела против фактора Bb, 0,1 MgЭДТУ (продукт CompTech), 1/2 НЧС (нормальная человеческая сыворотка, разведенная 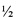 GVB0) и кроличьи эритроциты. Затем инкубируют реакцию при 37°С в течение 30 минут в шейкере. Добавляют 1,0 мл холодного GVBE. Смешивают и центрифугируют в течение 3 мин приблиз. при 1000×g или выше, чтобы осадить клетки. Переносят 100 мкл супернатанта в 96-луночный планшет и считывают на 412 ни (SoftMax Pro 4.7.1). Данные анализируют при помощи GraphPad Prism 6.
GVB0) и кроличьи эритроциты. Затем инкубируют реакцию при 37°С в течение 30 минут в шейкере. Добавляют 1,0 мл холодного GVBE. Смешивают и центрифугируют в течение 3 мин приблиз. при 1000×g или выше, чтобы осадить клетки. Переносят 100 мкл супернатанта в 96-луночный планшет и считывают на 412 ни (SoftMax Pro 4.7.1). Данные анализируют при помощи GraphPad Prism 6.
Антитела к фактору Bb.
[0075] В одном аспекте предложены антитела, которые связывают фактор Bb с большей аффинностью, чем они связывают фактор В.
[0076] В определенных аспектах в изобретении предложены рекомбинантные антитела, которые связывают фактор Bb, т.е. антитела к фактору Bb или антитела против фактора Bb. В этом контексте рекомбинантные антитела можно получать при помощи рекомбинантных методов, т.е. путем экспрессии рекомбинантной нуклеиновой кислоты, как описано ниже. Способы и методы для получения рекомбинантных белков хорошо известны в данной области техники.
[0077] В некоторых вариантах реализации антитела согласно изобретению являются выделенными или очищенными. Выделенное или очищенное антитело может быть избавлено от по меньшей мере некоторого материала, с которым оно обычно связано в естественном состоянии (загрязняющего материала). В предпочтительном варианте реализации изобретения загрязняющий материал составляет менее чем около 50%, более предпочтительно менее чем около 20% и более предпочтительно менее чем около 10% по массе относительно общей массы заданного образца. В некоторых вариантах реализации изобретения загрязняющим материалом может быть белок или пептид.
[0078] Чистый белок составляет по меньшей мере около 50% по массе от общего белка, предпочтительно по меньшей мере около 80% и наиболее предпочтительно по меньшей мере около 90%. Во многих вариантах реализации изобретения очищенное антитело против фактора Bb получают от организма, отличного от того, в который его доставляют. В некоторых вариантах реализации изобретения антитело против фактора Bb может быть получено в значительно более высокой концентрации, чем оно обыкновенно наблюдается, посредством применения индуцибельного промотора или промотора высокой экспрессии так, что получают повышенные концентрационные уровни антитела.
[0079] В некоторых вариантах реализации изобретения выделенное или очищенное антитело можно освобождать от компонентов, которые могут препятствовать диагностическому и/или терапевтическому применению антитела. В предпочтительных вариантах реализации изобретения антитело очищено более чем до 90% по массе антитела согласно определению по методу Лоури и, наиболее предпочтительно, более чем до 99% по массе до степени, достаточной для получения по меньшей мере 15 остатков N-концевой или внутренней аминокислотной последовательности при помощи общепринятых методов аминокислотного секвенирования (например, расщепления по Эдману и масс-спектрометрии), или до гомогенности по ДСН-ПААГ в восстановительных или невосстановительных условиях с применением окрашивания голубым кумасси или серебром. Выделенные антитела включают антитела in situ в рекомбинантных клетках в случае, если отсутствует по меньшей мере один компонент естественной среды антитела. При этом, как правило, выделенное антитело получают при помощи по меньшей мере одного этапа очистки.
[0080] Раскрытое антитело может специфически связываться с фактором Bb и использоваться для ингибирования или модуляции биологической активности фактора Bb. В определенных вариантах реализации изобретения раскрытые антитела создают при помощи иммунизации животного, в других случаях антитела можно получать при помощи технологии рекомбинантных ДНК. В дополнительных вариантах реализации изобретения антитела против фактора Bb можно получать при помощи ферментативного или химического расщепления антител природного происхождения. В некоторых вариантах реализации изобретения антитело может составлять тетрамер. В некоторых из этих вариантов реализации изобретения каждый тетрамер, как правило, состоит из двух идентичных пар полипептидных цепей, при этом каждая пара содержит одну легкую цепь (как правило, имеющую молекулярную массу около 25 кДа) и одну тяжелую цепь (как правило, имеющую молекулярную массу около 50-70 кДа). Амино-концевая часть каждой цепи содержит вариабельную область от около 100 до 110 или более аминокислот и может отвечать за распознавание антигена. Карбокси-концевая часть каждой цепи может определять константную область, которая отвечает главным образом за эффекторную функцию. Человеческие легкие цепи классифицируются как каппа и лямбда легкие цепи. Тяжелые цепи классифицируются как мю, дельта, гамма, альфа или эпсилон и определяют изотип антитела, соответственно, как IgM, IgD, IgG, IgA и IgE. IgG имеет несколько подклассов, включая, но не ограничиваясь этим, IgG1, IgG2, IgG3 и IgG4.
[0081] Некоторые антитела природного происхождения, например, антитела, которые можно обнаружить у верблюдов и лам, могут представлять собой димеры, состоящие из двух тяжелых цепей, и не включать легкие цепи. Muldermans et al., 2001, J. Biotechnol. 74: 277-302; Desmyter et al., 2001, J. Biol. Chem. 276: 26285-26290. Кристаллографические исследования антител верблюдов выявили, что области CDR3 этих антител образуют поверхность, которая взаимодействует с антигеном и, таким образом, является критической для связывания антигена, как и в более типичных тетрамерных антителах. Изобретение включает димерные антитела, состоящие из двух тяжелых цепей, или их фрагменты, которые могут связываться с и/или ингибировать биологическую активность фактора Bb.
[0082] Антитела согласно изобретению специфически связываются с белком фактора Bb, предпочтительно человеческого фактора Bb. Антитело может специфически связываться с антигеном-мишенью, если антитело обладает более высокой аффинностью связывания в отношении этого антигена-мишени, чем в отношении любого другого антигена или белка. Таким образом, описанные в данном документе антитела связываются с более высокой аффинностью с фактором Bb, чем с любым другим белком. Как правило, аффинность связывания измеряют путем определения равновесной константы связывания, например, Kд (или Kд) или Kа (или Kа). В некоторых вариантах реализации изобретения раскрытое антитело связывается с антигеном-мишенью с Kд от около 10-7 М до около 10-12 М или от около 10-8 М до около 10-11 М, или от около 10-9 М до около 10-10 М. В большинстве случаев Kд раскрытого антитела в отношении нецелевого антигена может быть выше, чем Kд в отношении антигена-мишени, например, когда Kд в отношении мишени составляет 10-10 М, а Kд в отношении не-мишени составляет 10-8 М. В некоторых случаях Kд в отношении другого антигена более чем 1X превышает Kд антигена-мишени, более чем 2Х превышает Kд антигена-мишени, более чем 3Х превышает Kд антигена-мишени, более чем 4Х превышает Kд антигена-мишени, более чем 5Х превышает Kд антигена-мишени, более чем 6Х превышает Kд антигена-мишени, более чем 7Х превышает Kд антигена-мишени, более чем 8Х превышает Kд антигена-мишени, более чем 9Х превышает Kд антигена-мишени, более чем 10Х превышает Kд антигена-мишени (например, когда Kд антитела составляет X-09 М в отношении антигена-мишени, Kд антитела в отношении другого антигена может быть 10Х больше или составлять X-08 М) или более чем 100Х (например, когда Kд антитела составляет X-10 М в отношении антигена-мишени, Kд антитела в отношении другого антигена может быть 10Х больше или составлять X-08 М). В некоторых случаях равновесная константа связывания может быть выражена в виде равновесной константы ассоциации Kа или Kа.
[0083] Равновесную константу связывания можно определить разными способами. В некоторых случаях равновесную константу связывания для раскрытого антитела определяют путем измерения скоростей ассоциации (k1) и диссоциации (k-1) в анализе связывания белка. Одним типовым способом измерения равновесной константы связывания является биослойная интерферометрия (BLI). BLI является технологией без применения меток, дающей возможность определять кинетику связывания в растворе. В одном типовом способе антитело может быть человеческим IgG, а захват антитела может происходить на захватывающих наконечниках биосенсора с античеловеческим IgG Fc (АНС) ( , Menlo Park, CA, USA) в соответствии с указаниями производителя. Другие типы анализа связывания белка включают: совместную иммунопреципитацию; бимолекулярную комплементацию флуоресценции; аффинный электрофорез; анализ с осаждением; перенос метки; дрожжевой двугибридный скрининг; фаговый дисплей; in vivo перекрестное связывание белковых комплексов с применением фотореактивных аминокислотных аналогов; тандемную аффинную очистку; химическое перекрестное связывание; химическое перекрестное связывание с последующей высокой массовой масс-спектрометрией MALDI; SPINE (эксперимент с взаимодействием со стреппротеином); количественную преципитацию в комбинации с нокдауном; метод близкого лигирования с биослойной интерферометрией; двойную интерферометрию поляризации; статическое светорассеяние; динамическое светорассеяние; поверхностный плазмонный резонанс; поляризацию/анизотропию флуоресценции; флуоресцентную корреляционную спектроскопию; резонансный перенос энергии флуоресценции; определение активности белка по ЯМР-измерениям многоядерной релаксации или 2D-ПФ ЯМР-спектроскопию в растворах в комбинации с нелинейным регрессионным анализом ЯМР-релаксации или групп данных 2D-ПФ-спектроскопии; стыковку белое-белок; изотермическую титрационную калориметрию; и микромасштабный термофорез.
, Menlo Park, CA, USA) в соответствии с указаниями производителя. Другие типы анализа связывания белка включают: совместную иммунопреципитацию; бимолекулярную комплементацию флуоресценции; аффинный электрофорез; анализ с осаждением; перенос метки; дрожжевой двугибридный скрининг; фаговый дисплей; in vivo перекрестное связывание белковых комплексов с применением фотореактивных аминокислотных аналогов; тандемную аффинную очистку; химическое перекрестное связывание; химическое перекрестное связывание с последующей высокой массовой масс-спектрометрией MALDI; SPINE (эксперимент с взаимодействием со стреппротеином); количественную преципитацию в комбинации с нокдауном; метод близкого лигирования с биослойной интерферометрией; двойную интерферометрию поляризации; статическое светорассеяние; динамическое светорассеяние; поверхностный плазмонный резонанс; поляризацию/анизотропию флуоресценции; флуоресцентную корреляционную спектроскопию; резонансный перенос энергии флуоресценции; определение активности белка по ЯМР-измерениям многоядерной релаксации или 2D-ПФ ЯМР-спектроскопию в растворах в комбинации с нелинейным регрессионным анализом ЯМР-релаксации или групп данных 2D-ПФ-спектроскопии; стыковку белое-белок; изотермическую титрационную калориметрию; и микромасштабный термофорез.
[0084] В вариантах реализации изобретения, в которых антитело используют в терапевтических применениях, одной из характеристик антитела к фактору Bb является то, что оно может модулировать и/или ингибировать один или более видов биологической активности фактора Bb или опосредованных фактором Bb. В этом случае антитело может специфически связываться с фактором Bb, может в значительной степени модулировать активность фактора Bb и/или может ингибировать связывание фактора Bb с другими белками (например, фактором С3). В некоторых случаях антитело может ингибировать сериновую протеазную активность фактора Bb по меньшей мере на около 20%, 40%, 60%, 80%, 85% или более.
[0085] Во многих вариантах реализации изобретения активность фактора Bb и способность антитела ингибировать эту активность определяют, анализируя лизис красных кровяных телец в присутствии 10% человеческой сыворотки. Активация альтернативного пути (АП) требует более высоких концентраций сыворотки, чем в случае классического пути. В общем случае для анализа используют конечную концентрацию, составляющую 5 мМ Mg++ в присутствии 5 мМ ЭДТУ, при этом ЭДТУ преимущественно хелатирует Са++. АП у большинства видов млекопитающих активируется спонтанно при помощи кроличьих эритроцитов, следовательно, они являются удобной мишенью. Кроличьи эритроциты (Complement Technology, Inc.) готовят путем 3-разовой промывки GVB0 (продукт CompTech) и пересуспендирования в 5×108/мл. Разные количества антитела против фактора Bb разводили GVB0. Смешивают 100 мкл реакции на льду из ряда серийных разведений антитела против фактора Bb, 0,1 М MgЭДТУ (продукт CompTech), 1/2 НЧС (нормальная человеческая сыворотка, разведенная  GVB0) и кроличьи эритроциты. Затем инкубируют реакцию при 37°С в течение 30 минут в шейкере. Добавляют 1,0 мл холодного GVBE. Смешивают и центрифугируют в течение 3 мин приблиз. при 1000×g или выше, чтобы осадить клетки. Переносят 100 мкл супернатанта в 96-луночный планшет и считывают на 412 ни (SoftMax Pro 4.7.1). Данные анализировали при помощи GraphPad Prism 6.
GVB0) и кроличьи эритроциты. Затем инкубируют реакцию при 37°С в течение 30 минут в шейкере. Добавляют 1,0 мл холодного GVBE. Смешивают и центрифугируют в течение 3 мин приблиз. при 1000×g или выше, чтобы осадить клетки. Переносят 100 мкл супернатанта в 96-луночный планшет и считывают на 412 ни (SoftMax Pro 4.7.1). Данные анализировали при помощи GraphPad Prism 6.
[0086] Не каждое антитело, которое специфически связывается с антигеном, может блокировать связывание антигена с его обычным лигандом и таким образом ингибировать или модулировать биологические действия антигена. Как известно в данной области техники, такое действие может зависеть от того, с какой частью антигена связывается антитело, а также от абсолютной и относительной концентраций антигена и антитела, в данном случае, антитела к фактору Bb. Чтобы считаться способным ингибировать или модулировать биологическую активность фактора Bb, как подразумевается в данном документе, антитело может быть способно, например, ингибировать сериновую протеазную активность фактора Bb или опосредованный человеческой сывороткой гемолиз по меньшей мере на около 20%, 40%, 60%, 80%, 85%, 90%, 95%, 99% или более.
[0087] Концентрация антитела, необходимая для ингибирования активности фактора Bb может сильно варьироваться и может зависеть от того, насколько сильно антитело связывается с фактором Bb. Например, для ингибирования биологической активности может быть достаточно одной молекулы антитела или менее на молекулу фактора Bb. В некоторых вариантах реализации изобретения для ингибирования биологической активности фактора Bb может требоваться соотношение антитела к фактору Bb, составляющее от около 1000:1 до около 1:1000, включая около 2:1, 1:1, 1:2, 1:4, 1:6, 1:8, 1:10, 1:20, 1:40, 1:60, 1:100, 1:500, 1:1000 или более. Во многих случаях способность ингибировать активность фактора Bb может зависеть от концентрации фактора Bb и/или концентрации антитела к фактору Bb.
[0088] В некоторых вариантах реализации антитела согласно изобретению содержат (а) каркас и (b) одну или несколько CDR, областей, которые определяют антигенсвязывающую специфичность и аффинность. Определяющие комплементарность области или CDR представляют собой области антитела, которые составляют основные поверхностные точки контакта для связывания антигена. В каркасную структуру антитела включена одна или более CDR. Каркасная структура антител согласно изобретению может являться каркасом антитела или его фрагментом или вариантом или может быть полностью синтетической по природе. В данном документе дополнительно описаны различные каркасные структуры антител согласно изобретению.
[0089] В предпочтительном варианте реализации раскрытых антител антитело может являться вариантным антителом, имеющим аминокислотную последовательность с по меньшей мере 75% идентичности или сходства последовательностей с аминокислотной последовательностью родительского антитела. Например, в некоторых вариантах реализации изобретения последовательность вариабельного домена легкой или тяжелой цепи варианта антитела на 75% идентична исходной последовательности вариабельного домена тяжелой или легкой цепи, в альтернативном варианте по меньшей мере на 80%, в альтернативном варианте по меньшей мере на 85%, в альтернативном варианте по меньшей мере на 90% и в альтернативном варианте меньшей мере на 95%. В большинстве случаев вариантное антитело содержит несколько или не содержит изменений в последовательности CDR и, следовательно, в большинстве случаев будет связываться с антигеном-мишенью с такой же аффинностью. Идентичность или сходство по отношению к этой последовательности определяется в данном документе как процент аминокислотных остатков в вариантной последовательности, которые являются идентичными (т.е. такой же остаток) или сходными (т.е. аминокислотный остаток, принадлежащий той же группе на основании общих свойств боковых цепей, смотрите ниже) с аминокислотной последовательностью родительского антитела после выравнивания последовательностей и внесения, в случае необходимости, гэпов для достижения максимального процента идентичности последовательностей. Никакие из N-концевых, С-концевых или внутренних продлений, делеций или инсерций в последовательности антитела за пределами вариабельного домена не следует считать такими, которые влияют на идентичность или сходство последовательностей.
CDR
[0090] Антитела согласно изобретению содержат каркасные области и одну или более CDR. Антитело согласно изобретению может содержать от одной до шести CDR (как обычно содержат антитела природного происхождения), например, одну CDR1 тяжелой цепи («НС CDR1» или «НС CDR1»), и/или одну CDR2 тяжелой цепи («НС CDR2» или «НС CDR2»), и/или одну CDR3 тяжелой цепи («НС CDR3» или «НС CDR3»), и/или одну CDR1 легкой цепи («LC CDR1» или «LC CDR1»), и/или одну CDR2 легкой цепи («LC CDR2» или «LC CDR2»), и/или одну CDR3 легкой цепи («LC CDR3» или «LC CDR3»). Употребляемый в тексте описания термин «природного происхождения» в связи с биологическими материалами, такими как полипептиды, нуклеиновые кислоты, клетки-хозяева и тому подобное, относится к материалам, которые можно обнаружить в природе. В антителах природного происхождения CDR1 тяжелой цепи, как правило, содержит от около пяти (5) до около семи (7) аминокислот, CDR2 тяжелой цепи, как правило, содержит от около шестнадцати (16) до около девятнадцати (19) аминокислот, a CDR3 тяжелой цепи, как правило, содержит от около трех (3) до около двадцати пяти (25) аминокислот.CDR1 легкой цепи, как правило, содержит от около десяти (10) до около семнадцати (17) аминокислот, CDR2 легкой цепи, как правило, содержит около семи (7) аминокислот, a CDR3 легкой цепи, как правило, содержит от около семи (7) до около десяти (10) аминокислот.
[0091] Аминокислоты согласно настоящему изобретению включают природные и синтетические аминокислоты (например, гомофенилаланин, цитруллин, орнитин и норлейцин). Такие синтетические аминокислоты могут быть включены, в частности, когда антитело синтезируют in vitro традиционными способами, хорошо известными в данной области техники. Кроме того, можно применять любую комбинацию пептидомиметических, синтетических и природных остатков/структур. Аминокислоты включают иминокислотные остатки, такие как пролин и гидроксипролин. Аминокислотная «R-группа» или «боковая цепь» может находиться как в (L)-, так и в (S)-конфигурации. В конкретном варианте реализации изобретения аминокислоты находятся в (L)- или (S)-конфигурации. В некоторых вариантах реализации изобретения аминокислоты могут образовывать пептидомиметические структуры, т.е. пептидные или белковые аналоги, такие как пептоиды (смотрите, Simon et al., 1992, Proc. Natl. Acad. Sci. U.S.A. 89: 9367, включенную в данный документ посредством ссылки), которые могут быть устойчивыми к протеазам или другим физиологическим условиям и/или условиям хранения.
[0092] Структура и свойства CDR в антителе природного происхождения описаны ниже. Вкратце, в традиционном каркасе антитела CDR включены в рамках каркасной области в вариабельную область тяжелой и легкой цепи, где они образуют области, отвечающие за связывание и распознавание антигена. Вариабельная область содержит по меньшей мере три CDR тяжелой или легкой цепи (Kabat et al., 1991, Sequences of Proteins of Immunological Interest, Public Health Service N.I.H., Bethesda, MD; смотрите также Chothia and Lesk, 1987, J. Mol. Biol. 196: 901-917; Chothia et al., 1989, Nature 342: 877-883) в пределах каркасной области (каркасные области обозначаются как 1-4, FR1, FR2, FR3 и FR4 согласно Kabat et al., 1991; смотрите также Chothia and Lesk, 1987). При этом CDR, предложенные в настоящем изобретении, могу использоваться не только для определения антигенсвязывающего домена традиционной структуры антитела, но также могут быть включены в большое количество других каркасных структур, как описано в данном документе.
[0093] Аланиновое сканирование применяли для определения аминокислотных позиций в последовательностях CDR, которые в случае модификации меняют аффинность связывания антител против фактора Bb.
[0094] Конкретные CDR для применения в раскрытых антителах представлены в Таблице 1, подчеркнуты аминокислоты, замещение которых аланином существенно снижало связывание.
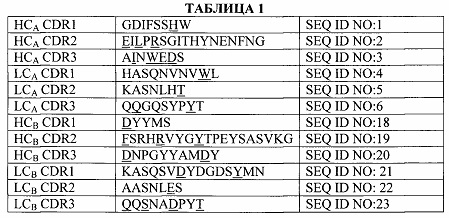
[0095] Последовательности фактора В, фактора Ва и фактора Bb показаны в Таблице 2.


[0096] В другом варианте реализации в изобретении предложено антитело, которое связывает фактор Bb (SEQ ID NO: 7), при этом указанное антитело содержит по меньшей мере одну область НС CDR, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 1-3 или SEQ ID NO: 18-20, и/или по меньшей мере одну область LC CDR, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 4-6 или SEQ ID NO: 21-23. Различные вариабельные области тяжелой цепи и легкой цепи согласно изобретению проиллюстрированы в ТАБЛИЦЕ 3 и SEQ ID NO: 8-15 или SEQ ID NO: 24-31. В некоторых вариантах реализации изобретения применяют конкретно антитела с областью НС CDR3 или LC CDR3. Кроме того, в некоторых вариантах реализации изобретения антитела могут содержать одну CDR, содержащую не более двух (2) аминокислотных добавок, делеций или замен последовательности, выбранной из областей НС CDR любой из SEQ ID NO: 1-3 или SEQ ID NO: 18-20, и LC CDR, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 4-6 или SEQ ID NO: 21-23 (например, антитело содержит две области CDR, одну НС CDR и одну LC CDR, а конкретный вариант реализации изобретения представляют антитела с обеими НС CDR3 и LC CDR3, например, SEQ ID NO: 3 и 6).



Вариантные последовательности CDR
[0097] В дополнительном аспекте изобретения предложено выделенное антитело, которое связывает фактор Bb, при этом выделенное антитело содержит аминокислотную последовательность тяжелой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 12-15 или SEQ ID NO: 28-31, или аминокислотную последовательность легкой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 8-11 или SEQ ID NO: 24-27.
[0098] В дополнительном аспекте изобретения предложено выделенное антитело, которое связывает фактор Bb, при этом выделенное антитело содержит аминокислотную последовательность тяжелой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 12-15 или SEQ ID NO: 28-31, и аминокислотную последовательность легкой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 8-11 или SEQ ID NO: 24-27. Следует отметить, что любую из последовательностей тяжелой цепи можно комбинировать и спаривать с любой из последовательностей легкой цепи.
[0099] В другом варианте реализации в изобретении предложено антитело, которое связывает фактор Bb, при этом указанное антитело содержит по меньшей мере одну область НС CDR, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из областей НС CDR1, НС CDR2 или НС CDR3 (как описано выше) SEQ ID NO: 1-3 или SEQ ID NO: 18-20, и/или по меньшей мере одну область LC CDR, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из областей LC CDR1, LC CDR2 или LC CDR3 (как описано выше) SEQ ID NO: 4-6 или SEQ ID NO: 21-23. В этом варианте реализации применяют конкретно антитела с областью НС CDR3 или LC CDR3. В дополнительных вариантах реализации изобретения применяют антитела с одной CDR, содержащей не более 2 аминокислотных добавок, делеций или замен последовательности, выбранной из областей НС CDR любой из SEQ ID NO: 1-3 или SEQ ID NO: 18-20, и областью LC CDR, содержащей не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 4-6 или SEQ ID NO: 21-23 (например, антитело содержит две области CDR, одну НС CDR и одну LC CDR, а конкретный вариант реализации изобретения представляют антитела с обеими областями НС CDR3 и LC CDR3, например, SEQ ID NO: 3 и 6).
[00100] Как понятно специалистам в данной области техники, для любого антитела с одной или более CDR из проиллюстрированных последовательностей можно применять любую комбинацию CDR, независимо выбранных из проиллюстрированных последовательностей. Таким образом, можно создавать антитела с одной, двумя, тремя, четырьмя, пятью или шестью независимо выбранными CDR. При этом, как понятно специалистам в данной области техники, в конкретных вариантах реализации изобретения применяют комбинации CDR, которые не повторяются, например, в общем случае не получают антитела с двумя областями НС CDR2 и т.д.
[00101] В дополнительном аспекте изобретения предложено выделенное антитело, которое связывает фактор Bb, при этом выделенное антитело содержит аминокислотную последовательность тяжелой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 12-15 или SEQ ID NO: 28-31, или аминокислотную последовательность легкой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 8-11 или SEQ ID NO: 24-27.
[00102] В дополнительном аспекте изобретения предложено выделенное антитело, которое связывает фактор Bb, при этом выделенное антитело содержит аминокислотную последовательность тяжелой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 12-15 или SEQ ID NO: 28-31, и аминокислотную последовательность легкой цепи, содержащую не более двух (2) аминокислотных добавок, делеций или замен любой из SEQ ID NO: 8-11 или SEQ ID NO: 24-27. Следует отметить, что любую из последовательностей тяжелой цепи можно комбинировать и спаривать с любой из последовательностей легкой цепи.
[00103] В общем случае аминокислотная гомология, сходство или идентичность между отдельными вариантными CDR, описанными в данном документе, составляет по меньшей мере 80% при сравнении с раскрытыми в данном документе последовательностями. В различных случаях аминокислотная гомология, сходство или идентичность составляет по меньшей мере 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% и 99%.
Идентичность/гомология последовательностей
[00104] Как известно в данной области техники, для определения степени идентичности или сходства последовательностей, которой обладает белок или нуклеиновая кислота по отношению к известной последовательности, можно использовать большое количество разных программ.
[00105] В случае аминокислотных последовательностей идентичность и/или сходство последовательностей определяют, применяя стандартные методы, известные в данной области техники, включая, но не ограничиваясь этим, алгоритм локальной идентичности последовательностей авторства Smith and Waterman, 1981, Adv. Appl. Math. 2: 482, алгоритм выравнивания для определения идентичности последовательностей авторства Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443, метод поиска сходства авторства Pearson and Lipman, 1988, Proc. Nat. Acad. Sci. U.S.A. 85: 2444, компьютеризованные воплощения этих алгоритмов (GAP, BESTFIT, FASTA и TFASTA в пакете программного обеспечения Wisconsin Genetics, Genetics Computer Group, 575 Science Drive, Madison, Wis.), программу для последовательностей Best Fit, описанную Devereux et al., 1984, Nucl. Acid Res. 12: 387-395, предпочтительно используемую с установленными по умолчанию параметрами или методом подбора. Предпочтительно процент идентичности рассчитывают при помощи FastDB на основании следующих параметров: штраф за несовпадение 1; штраф за гэп 1; штраф за размер гэпа 0,33; и штраф за соединение 30, "Current Methods in Sequence Comparison and Analysis," Macromolecule Sequencing and Synthesis, Selected Methods and Applications, pp 127-149 (1988), Alan R. Liss, Inc.
[00106] Примером применяемого алгоритма является PILEUP. PILEUP создает множественное выравнивание последовательностей из группы родственных последовательностей, используя прогрессивное попарное выравнивание. Также существует возможность построения дерева, показывающего групповые взаимосвязи, используемые для создания выравнивания. В PILEUP используется упрощение метода прогрессивного выравнивания авторства Feng & Doolittle, 1987, J. Mol. Evol. 35: 351-360; указанный метод сходен с описанным Higgins and Sharp, 1989, CABIOS 5: 151-153. Применяемые параметры PILEUP включают вес гэпа по умолчанию 3,00, вес длины гэпа по умолчанию 0,10 и взвешенные концевые гэпы.
[00107] Другим примером применяемого алгоритма является алгоритм BLAST, описанный в: Altschul et al., 1990, J. Mol Biol. 215: 403-410; Altschul et al., 1997, Nucleic Acids Res. 25: 3389-3402; и Karin et al., 1993, Proc. Natl. Acad. Sci. U.S.A. 90: 5873-5787. В частности, применяемой программой BLAST является программа WU-BLAST-2, которая была получена из Altschul et al., 1996, Methods in Enzymology 266: 460-480. WU-BLAST-2 использует несколько поисковых параметров, большинство из которых установлены по умолчанию. Корректируемые параметры для белков устанавливают со следующими величинами: длина перекрывания = 1, доля перекрывания = 0,125, пороговая длина сегмента, Т=11. Параметры HSP S и HSP S2 являются динамическими величинами и устанавливаются самой программой в зависимости от состава конкретной последовательности и состава конкретной базы данных, против которой проводится поиск представляющей интерес последовательности; при этом данные величины можно корректировать для повышения чувствительности.
[00108] Дополнительным применяемым алгоритмом является BLAST с гэпами, описанный Altschul et al., 1993, Nucl Acids Res. 25: 3389-3402. BLAST с гэпами использует матрицу весовых оценок замен BLOSUM-62; пороговый параметр Т установлен на 9; метод двух совпадений для запуска продлений без гэпов, затраты на длину гэпа k стоимостью 10+k; Xu установлен на 16, a Xg установлен на 40 на этапе поиска по базе данных и на 67 на выходном этапе алгоритмов. Выравнивание с гэпами запускается при оценке, соответствующей приблизительно 22 битам.
[00109] В общем случае аминокислотная гомология, сходство или идентичность между отдельными вариантными CDR или вариабельными областями составляет по меньшей мере 80% по отношению к проиллюстрированным в данном документе последовательностям и, как правило, с предпочтительно возрастающей гомологией или идентичностью, составляющей по меньшей мере 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и практически 100%.
[00110] Аналогично, процент (%) идентичности нуклеотидных последовательностей по отношению к нуклеотидной последовательности раскрытого антитела представляет собой процентную долю нуклеотидных остатков в кандидатной последовательности, которые идентичны нуклеотидным остаткам в кодирующей последовательности антитела. В конкретном способе используют модуль BLASTN WU-BLAST-2 с установленными по умолчанию параметрами, с длиной перекрытия и долей перекрытия, установленными на 1 и 0,125, соответственно.
[00111] В общем случае нуклеотидная гомология, сходство или идентичность между нуклеотидными последовательностями, кодирующими отдельные вариантные CDR, и вариантными последовательностями вариабельного домена составляет по меньшей мере 80% и, как правило, с предпочтительно возрастающей гомологией или идентичностью, составляющей по меньшей мере 85%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и практически 100%. Во многих случаях неидентичные нуклеотидные последовательности вследствие вырожденности генетического кода могут кодировать одну и ту же аминокислотную последовательность.
[00112] Гомологию между нуклеотидными последовательностями часто определяют по их способности гибридизироваться друг с другом. В некоторых вариантах реализации изобретения селективная гибридизация может относиться к связыванию с высокой специфичностью. Полинуклеотиды, олигонуклеотиды и их фрагменты в соответствии с изобретением избирательно гибридизируются с цепями нуклеиновой кислоты в условиях гибридизации и промывки, которые минимизируют значительное количество выявляемого связывания с неспецифическими нуклеиновыми кислотами. Как известно в данной области техники и как обсуждается в данном документе, для получения условий избирательной гибридизации можно использовать условия высокой жесткости.
[00113] Специалист в данной области техники легко определит жесткость гибридизации, которая в общем случае рассчитывается эмпирически в зависимости от длины зонда, температуры промывки и концентрации соли. В общем случае для более длинных зондов необходимы более высокие температуры для надлежащего отжига, в то время как для более коротких зондов необходимы более низкие температуры. В общем случае гибридизация зависит от способности денатурированной ДНК к повторному отжигу, когда комплементарные цепи находятся в среде ниже их температуры плавления. Чем выше степень необходимой гомологии между зондом и гибридизируемой последовательностью, тем более высокую относительную температуру можно использовать. Из этого следует, что более высокие относительные температуры имеют тенденцию к повышению жесткости реакционных условий, в то время как низкие температуры - к понижению. Дополнительные детали и объяснение жесткости реакций гибридизации смотрите в Ausubel et al., Current Protocols in Molecular Biology, Wiley Interscience Publishers, (1995).
[00114] Условия высокой жесткости известны в данной области техники; смотрите, например, Sambrook et al., 2001, выше, и Short Protocols in Molecular Biology, Second Edition, Ausubel et al. eds., John Wiley & Sons, 1992, которые обе включены в данный документ посредством ссылки. Жесткие условия зависят от последовательностей и будут различаться в разных обстоятельствах. Более длинные последовательности специфически гибридизируются при более высоких температурах. Расширенное руководство по гибридизации нуклеиновых кислот можно найти в Tijssen, Techniques In Biochemistry and Molecular Biology-Hybridization with Nucleic Acid Probes, "Overview of principles of hybridization and the strategy of nucleic acid assays" (1993).
[00115] В некоторых вариантах реализации изобретения условия жесткости или высокой жесткости можно определить по тому, что: (1) применяют низкую ионную силу и высокую температуру для промывки, например, 0,015 М хлорида натрия/0,0015 М цитрата натрия/0,1% додецилсульфата натрия при 50°С; (2) во время гибридизации применяют денатурирующий агент, такой как формамид, например, 50% (об/об) формамида с 0,1% бычьего сывороточного альбумина/0,1% фиколл/0,1% пол ивинилпирро ли дона/50 мМ натрий-фосфатного буфера при рН 6,5 с 750 мМ хлорида натрия, 75 мМ цитрата натрия при 42С; или (3) применяется 50% формамида, 5Х SSC (0,75 М NaCl, 0,075 М цитрата натрия), 50 мМ фосфата натрия (рН 6,8), 0,1% пирофосфата натрия, 5Х раствора Денхардта, фрагментированную ДНК из молок лососевых (50 мкг/мл), 0,1% ДСН и 10% декстран сульфата при 42°C с промывками при 42°С в 0,2Х SSC (хлорид натрия/цитрат натрия) и 50% формамиде при 55°C с последующей промывкой с высокой жесткостью, состоящей из 0,1X SSC, содержащего ЭДТУ, при 55°С.
[00116] В общем случае жесткие условия выбирают так, чтобы температура была на около 5-10°С ниже чем температура плавления (Tm) для конкретной последовательности при определенной ионной силе и рН. Tm представляет температуру (при определенных ионной силе, рН и концентрации нуклеиновой кислоты), при которой 50% зондов, комплементарных последовательности-мишени, гибридизируются с последовательностью-мишенью в состоянии равновесия (если последовательности-мишени присутствуют в избытке, при Tm наблюдается занятость 50% зондов в состоянии равновесия). Жесткими условиями являются те, при которых концентрация соли составляет менее чем около 1,0 М ионов натрия, как правило, от около 0,01 до 1,0 М ионов натрия (или других солей) при рН от 7,0 до 8,3, а температура составляет по меньшей мере около 30°С для коротких зондов (например, от 10 до 50 нуклеотидов) и по меньшей мере около 60°С для длинных зондов (например, более 50 нуклеотидов). Жесткие условия также могут быть достигнуты путем добавления дестабилизирующих агентов, таких как формамид.
[00117] В другом варианте реализации изобретения применяют менее жесткие условия; например, как известно в данной области техники, можно применять условия умеренной или низкой жесткости; смотрите, Sambrook et al., 2001, выше; Ausubel et al., 1992, выше, и Tijssen, 1993, выше.
[00118] В некоторых случаях условия умеренной жесткости могут включать применение промывочного раствора и гибридизационных условий (например, температуры, ионной силы и % ДСН), менее жестких, чем вышеописанные. Примером условий умеренной жесткости является инкубация в течение ночи при 37°С в растворе, содержащем: 20% формамида, 5Х SSC (150 мМ NaCl, 15 мМ тринатриевого цитрата), 50 мМ фосфата натрия (рН 7,6), 5Х раствора Денхардта, 10% декстран сульфата и 20 мг/мл фрагментированной ДНК из молок лососевых, с последующей промывкой фильтров в 1X SSC при около 37-50°С. Специалисту в данной области техники известно, как проводить корректировку температуры, ионной силы и т.д. в случае необходимости учитывать такие факторы, как длина зондов и тому подобное.
[00119] В некоторых вариантах реализации изобретения раскрытые антитела и их варианты можно получать при помощи сайт-специфического мутагенеза нуклеотидов в последовательности ДНК, кодирующей антитело. Это можно осуществить, используя кассету или ПЦР-мутагенез или другие методы, хорошо известные в данной области техники, для получения ДНК, кодирующей вариант, и экспрессируя после этого рекомбинантную ДНК в клеточной культуре, как описано в данном документе. В некоторых случаях фрагменты антител, содержащие вариантные CDR, содержащие до около 100-150 остатков, можно получать путем/и vitro синтеза, используя известные методы. Эти вариантные фрагменты могут демонстрировать такую же качественную биологическую активность, что и аналог природного происхождения, например, связывание с фактором Bb и ингибирование комплемента, хотя также можно выбирать варианты, которые имеют модифицированные характеристики, как более полно описано ниже.
[00120] В то время как участок или область внесения вариации аминокислотной последовательности является определенным, нет необходимости в предопределении мутации per se. Например, чтобы оптимизировать мутацию в заданном участке, можно проводить случайный мутагенез в кодоне-мишени или области-мишени и скрининг экспрессируемой последовательности CDR или вариабельной области антитела в отношении оптимальной необходимой активности антитела. Методы введения мутаций замещения в предопределенные участки в ДНК, имеющие известную последовательность, хорошо известны, например, это мутагенез с праймером М13 и ПЦР-мутагенез. Скрининг мутантов проводят, используя анализ активности антитела, такой как связывание фактора Bb.
[00121] Аминокислотные замены, как правило, проводят в одном остатке; инсерции обычно занимают от около одного (1) до около двадцати (20) аминокислотных остатков, хотя допустимы и значительно большие инсерции. Диапазон делеций составляет от около одного (1) до около двадцати (20) аминокислотных остатков, хотя в некоторых случаях делеции могут быть намного крупнее.
[00122] Для получения конечного производного или варианта можно использовать замены, делеции, инсерции или любые их комбинации. В общем случае эти изменения проводят в нескольких аминокислотах, чтобы минимизировать изменение молекулы, в частности, иммуногенности и специфичности антитела. Однако в определенных обстоятельствах допустимы большие изменения. Консервативные замены в общем случае осуществляют в соответствии со следующей схемой, приведенной в виде Таблицы 4.
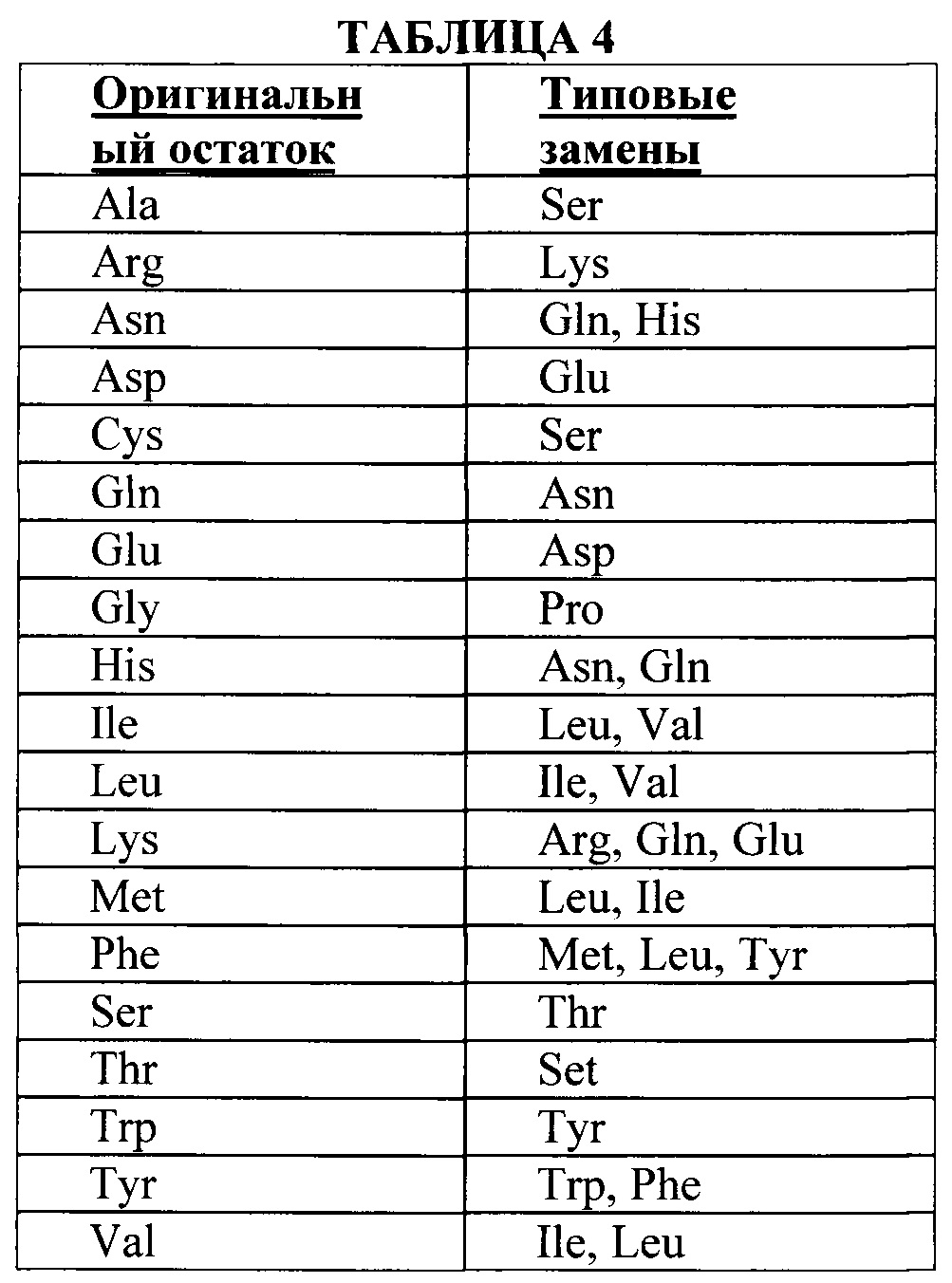
[00123] Изменения функций или иммунологических особенностей можно получить, выбирая замены, которые являются менее консервативными, чем приведенные в Таблице 4. Например, можно делать замены, которые более существенно влияют на: структуру полипептидного скелета в участке изменения, например, альфа-спиральную или бета-складчатую структуру; заряд или гидрофобность молекулы в целевом участке; или объем боковой цепи. Заменами, которые в общем случае должны приводить к наибольшим изменениям в свойствах полипептида, являются те, в которых (а) гидрофильный остаток, например, серил или треонил, замещен гидрофобным остатком, например, лейцилом, изолейцилом, фенилаланилом, валилом или аланилом; (b) цистеин или пролин замещен на любой другой остаток; (с) остаток, имеющий электроположительную боковую цепь, например, лизил, аргинил или гистидил, замещен электроотрицательным остатком, например, глутамилом или аспартилом; или (d) остаток, имеющий объемную боковую цепь, например, фенилаланин, замещен остатком без боковой цепи, например, глицином.
[00124] Варианты, как правило, демонстрируют такую же качественную биологическую активность и вызывают такой же иммунный ответ, что и аналог природного происхождения, хотя в случае необходимости можно выбирать варианты так, чтобы модифицировать характеристики раскрытого антитела к фактору Bb. В альтернативном варианте может быть выбран вариант, в котором изменена биологическая активность раскрытого антитела. Например, могут быть изменены или удалены участки гликозилирования, как обсуждается в данном документе.
[00125] В данном документе раскрыты полипептидные последовательности, гомологичные SEQ ID NO: 1-6 и 8-15 и SEQ ID NO: 18-23, и SEQ ID NO: 24-31. Раскрытые в данном документе полипептиды могут содержать аминокислотные последовательности, идентичные раскрытым аминокислотным последовательностям. В других случаях заявляемые полипептиды содержат аминокислотные последовательности, которые могут содержать консервативные аминокислотные замены по сравнению с раскрытой последовательностью. Консервативные аминокислотные замены могут включать аминокислоты, которые обладают сходными характеристиками с заменяемой аминокислотой. В различных случаях консервативную замену можно проводить без существенного изменения структуры или функции полипептида.
[00126] Консервативные аминокислотные замены можно проводить на основании относительного сходства боковой цепи, размера, заряда, гидрофобности, гидрофильности, изоэлектрической точки и т.д. В различных случаях влияние замен на функцию белка можно оценить при помощи рутинных исследований. Консервативные аминокислотные замены включают аминокислоты со сходной величиной гидрофильности, например, когда аминокислоты имеют индекс гидрофобности, который может быть основан на гидрофобности и заряде аминокислоты. В различных случаях консервативные аминокислотные замены можно проводить между двумя аминокислотами одного класса, например, неполярными аминокислотами, кислотными аминокислотами, основными аминокислотами и нейтральными аминокислотами. Консервативные замены также могут быть основаны на размере или объеме. Аминокислоты также можно классифицировать на основании их способности образовывать или разрушать заданную структуру, такую как альфа-спираль, бета-складчатость или меж- или внутримолекулярное взаимодействие. В различных случаях консервативные аминокислотные замены основаны на более чем одной характеристике.
[00127] Раскрытые в настоящей заявке полипептиды могут содержать аминокислоты как природного, так и неприродного происхождения. В различных случаях боковые цепи аминокислот природного происхождения можно замещать боковыми цепями неприродного происхождения. В различных случаях аминокислоты могут быть дериватизированы.
[00128] Раскрытые полипептиды включают полипептиды, которые являются гомологичными последовательностям SEQ ID NO: 1-6 и 8-15, и SEQ ID NO: 18-31. Гомология может быть выражена в виде % идентичности или % сходства, или % положительных результатов. В различных случаях % идентичности представляет процентную долю аминокислот, являющихся идентичными для двух выравниваемых последовательностей, а % сходства или % положительных результатов представляет процентную долю аминокислот, являющихся неидентичными, но представляющих консервативные замены. Консервативной заменой может быть замена аминокислоты с подобным зарядом, аминокислоты с подобным размером, аминокислоты с подобной полярностью и т.д. Например, если учитывать заряд, то консервативной заменой можно считать замену лизина на аргинин.
[00129] В различных случаях выравнивание двух полипептидов можно проводить при помощи алгоритмов, например, BLASTp. В различных случаях параметры BLASTp могут быть установлены с максимальной длиной последовательности-мишени, эквивалентной, большей или меньшей чем длина наиболее длинного из двух полипептидов, ожидаемый порог может быть установлен на 10, длина сегмента на 3, а матрицей замен может быть BLOSUM62 со стоимостью гэпа 11 за внесение и 1 за продление. BLASTp может представлять гомологию выровненных полипептидов в виде «идентичности» или «количества положительных результатов». Выровненные последовательности могут включать гэпы для достижения выравнивания.
[00130] В различных случаях гомология аминокислотных последовательностей может отображать процентную долю идентичности или положительных результатов при оптимальном выравнивании, как описано выше. В различных случаях % гомологии (% положительных результатов) или % идентичности можно рассчитать, разделив количество выровненных аминокислот в окне сравнения. Окно сравнения может составлять полную длину одного или другого полипептида, если длина двух полипептидов не одинакова. В других случаях окно сравнения может составлять часть одного из полипептидов. В различных случаях окно сравнения для определения гомологии или идентичности двух полипептидных последовательностей составляет более чем около 40 ак (аминокислот), 45 ак, 50 ак, 55 ак, 60 ак, 65 ак, 70 ак, 75 ак, 80 ак, 85 ак, 90 ак, 95 ак, 100 ак, 150 ак или 200 ак, и/или менее чем около 200 ак, 150 ак, 100 ак, 95 ак, 90 ак, 85 ак, 80 ак, 75 ак, 70 ак, 65 ак, 60 ак, 55 ак, 50 ак или 45 ак. В некоторых вариантах реализации изобретения, как в случае с последовательностями CDR, окно сравнения может составлять менее чем 40 ак, например, между менее чем около 25 ак, 24 ак, 23 ак, 22 ак, 21 ак, 20 ак, 19 ак, 18 ак, 17 ак, 16 ак, 15 ак, 14 ак, 13 ак, 12 ак, 11 ак, 10 ак, 9 ак, 8 ак, 7 ак, 6 ак, 5 ак или 4 ак, и более чем около 3 ак, 4 ак, 5 ак, 6 ак, 7 ак, 8 ак, 9 ак, 10 ак, 11 ак, 12 ак, 13 ак, 14 ак, 15 ак, 16 ак, 17 ак, 18 ак, 19 ак, 20 ак, 21 ак, 22 ак, 23 ак или 24 ак.
[00131] В различных случаях заявляемые аминокислотные последовательности могут иметь % идентичности или % гомологии (% положительных результатов) в заданном окне сравнения, который составляет больше чем около 60%, 65%, 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% и/или меньше чем около 100%, 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 85%, 80%, 75% или 70%.
[00132] В различных случаях выравнивание последовательностей можно проводить, используя различные алгоритмы, включая динамическое, локальное и глобальное выравнивание. Например, алгоритм Smith and Waterman, 1981, Adv. Appl. Math 2: 482; алгоритм выравнивания Needleman and Wunsch, 1970, J. Mol. Biol. 48: 443; метод сходства Pearson and Lipman, 1988, Proc. Natl. Acad. Sci. USA 85: 2444. В различных случаях эти алгоритмы могут быть реализованы компьютерными программами (такими как EMBOSS, GAP, BESTFIT, FASTA, TFASTA BLAST, BLOSUM и т.д.).
[00133] В альтернативных случаях можно проводить консервативные аминокислотные замены, в которых аминокислотный остаток замещен другим из того же класса, например, в которых аминокислоты делятся на неполярный, кислотный, основной и нейтральный классы следующим образом: неполярные: Ala, Val, Leu, Ile, Phe, Trp, Pro, Met; кислотные: Asp, Glu; основные: Lys, Arg, His; нейтральные: Gly, Ser, Thr, Cys, Asn, Gln, Tyr.
[00134] В некоторых случаях можно проводить консервативные аминокислотные замены, в которых аминокислотный остаток замещен другим, имеющим сходную величину гидрофильности (например, в пределах плюс или минус 2,0), когда следующей может быть аминокислота с индексом гидрофобности около -1,6, такой как Tyr (-1,3) или Pro (-1,6). Аминокислотам приписаны такие значения: Arg (+3;0); Lys (+3,0); Asp (+3,0); Glu (+3,0); Ser (+0,3); Asn (+0,2); Gln (+0,2); Gly (O); Pro (-0,5); Thr (-0,4); Ala (-0,5); His (-0,5); Cys (-1,0); Met (-1,3); Val (-1,5); Leu (-1,8); Ile (-1,8); Tyr (-2,3); Phe (-2,5); и Trp (-3,4).
[00135] В альтернативных случаях можно проводить консервативные аминокислотные замены, в которых аминокислотный остаток замещен другим, имеющим сходный индекс гидрофобности (например, в пределах плюс или минус 2,0). В таких случаях каждой аминокислоте может быть приписан индекс гидрофобности на основании ее гидрофобности и зарядовых характеристик следующим образом: Ile (+4,5); Val (+4,2); Leu (+3,8); Phe (+2,8); Cys (+2,5); Met (+1,9); Ala (+1,8); Gly (-0,4); Thr (-0,7); Ser (-0,8); Trp (-0,9); Tyr (-1,3); Pro (-1,6); His (-3,2); Glu (-3,5); Gln (-3,5); Asp (-3,5); Asn (-3,5); Lys (-3,9); и Arg (-4,5).
[00136] В альтернативных случаях консервативные аминокислотные замены включают изменения с учетом гидрофильности или гидрофобности, размера или объема или заряда. В общем случае аминокислоты можно охарактеризовать как гидрофобные или гидрофильные в зависимости, главным образом, от свойств аминокислотной боковой цепи. Гидрофобные аминокислоты демонстрируют гидрофобность больше нуля, а гидрофильные аминокислоты демонстрируют гидрофильность меньше нуля на основании нормированной консенсусной оценки гидрофобности по Eisenberg et al. (J. Mol. Bio. 179: 125-142, 184). Генетически кодируемые гидрофобные аминокислоты включают Gly, Ala, Phe, Val, Leu, Ile, Pro, Met и Trp, а генетически кодируемые гидрофильные аминокислоты включают Thr, His, Glu, Gin, Asp, Arg, Ser и Lys. He кодируемые генетически гидрофобные аминокислоты включают t-бутилаланин, в то время как не кодируемые генетически гидрофильные аминокислоты включают цитруллин и гомоцистеин.
[00137] Гидрофобные или гидрофильные аминокислоты можно дополнительно разделить на основании характеристик их боковых цепей. Например, ароматической аминокислотой является аминокислота с боковой цепью, содержащей по меньшей мере одно ароматическое или гетероароматическое кольцо, которое может содержать один или более заместителей, таких как -ОН, -SH, -CN, -F, -Cl, -Br, -I, -NO2, -NO, -NH2, -NHR, -NRR, -C(O)R, -С(O)ОН, -C(O)OR, -C(O)NH2, -C(O)NHR, -C(O)NRR и т.д., где R независимо представляет собой (C1-С6) алкил, замещенный (C1-С6) алкил, (С0-С6) алкенил, замещенный (C1-С6) алкенил, (С1-С6) алкинил, замещенный (С0-С6) алкинил, (С5-С20) арил, замещенный (С0-С20) арил, (С6-С26) алкарил, замещенный (С6-С26) алкарил, 5-20-членный гетероарил, замещенный 5-20-членный гетероарил, 6-26-членный алкгетероарил или замещенный 6-26-членный алкгетероарил. Генетически кодируемые ароматические аминокислоты включают Phe, Tyr и Trp.
[00138] Неполярной или аполярной аминокислотой является гидрофобная аминокислота с боковой цепью, которая является незаряженной при физиологическом уровне рН и которая содержит связи, в которых пара электронов, общая для двух атомов, в общем случае удерживается одинаково каждым из этих двух атомов (т.е. боковая цепь не является полярной). Генетически кодируемые неполярные аминокислоты включают Gly, Leu, Val, Ile, Ala и Met. Неполярные аминокислоты можно дополнительно разделить, чтобы выделить алифатические аминокислоты, которые являются гидрофобными аминокислотами с алифатической углеводной боковой цепью. Генетически кодируемые алифатические аминокислоты включают Ala, Leu, Val и Ile.
[00139] Полярной аминокислотой является гидрофильная аминокислота с боковой цепью, которая является незаряженной при физиологическом уровне рН, но которая содержит одну связь, в которой пара электронов, общая для двух атомов, более близко удерживается одним из атомов. Генетически кодируемые полярные аминокислоты включают Ser, Thr, Asn и Gln.
[00140] Кислотной аминокислотой является гидрофильная аминокислота с величиной pKa боковой цепи менее 7. Кислотные аминокислоты, как правило, имеют отрицательно заряженные боковые цепи при физиологическом уровне рН вследствие нехватки иона водорода. Генетически кодируемые кислотные аминокислоты включают Asp и Glu. Основной аминокислотой является гидрофильная аминокислота с величиной pKa боковой цепи более 7. Основные аминокислоты, как правило, имеют положительно заряженные боковые цепи при физиологическом уровне рН вследствие ассоциации с ионом гидрония. Генетически кодируемые основные аминокислоты включают Arg, Lys и His.
[00141] Величина % идентичности аминокислотных последовательностей определяется как число совпадающих идентичных остатков, разделенное на общее число остатков «более длинной» последовательности в окне сравнения. «Более длинной» последовательностью является последовательность, содержащая большее количество фактических остатков в окне сравнения (гэпы, вносимые WU-Blast-2 для максимизации счета выравнивания, игнорируются).
[00142] Выравнивание может включать внесение гэпов в последовательности, предназначенные для выравнивания. Кроме того, понятно, что для последовательностей, которые содержат больше или меньше аминокислот, чем белок, кодируемый последовательностью раскрытого полипептида, в одном случае процент идентичности последовательностей определяется на основании числа идентичных аминокислот по отношению к общему числу аминокислот. При расчете процента идентичности разным проявлениям вариативности последовательностей, таким как инсерции, делеции, замены и т.д., не приписывают относительную массу.
[00143] В одном случае положительное значение (+1) приписывается только идентичным остаткам, а всем формам вариативности последовательностей, включая гэпы, приписывается значение «0», что устраняет необходимость во взвешенной шкале или параметрах, как описано ниже для расчета сходства последовательностей. Процент идентичности последовательностей можно рассчитать, например, разделив число совпадающих идентичных остатков на общее число остатков «более короткой» последовательности в выровненной области и умножив на 100. «Более длинной» последовательностью является последовательность, содержащая большее количество фактических остатков в выровненной области.
Каркасы
[00144] Как отмечено в данном документе, антитела согласно настоящему изобретению могут содержать каркасную структуру, в которую можно прививать описанные выше CDR. В одном варианте реализации изобретения каркасная структура является традиционной структурой антитела, что означает, что антитело содержит последовательности вариабельных доменов двух тяжелых и двух легких цепей. В некоторых случаях описанные в данном документе комбинации антител могут содержать дополнительные компоненты (каркасную область, J- и D-области, константные области и т.д.), которые составляют тяжелую и/или легкую цепь. Некоторые варианты реализации изобретения включают применение человеческих каркасных компонентов.
[00145] Соответственно, в различных вариантах реализации антитела согласно изобретению содержат каркасы традиционных антител. В некоторых вариантах реализации изобретения раскрытые антитела могут быть человеческими и моноклональными антителами, биспецифическими антителами, диателами, минителами, доменными антителами, синтетическими антителами, химерными антителами, слитыми антителами и фрагментами каждого из перечисленных компонентов, соответственно. Вышеописанные CDR и комбинации CDR можно прививать в любой из следующих каркасов.
[00146] Химерные антитела согласно настоящему изобретению могут содержать последовательность тяжелой и/или легкой цепи, идентичную или гомологичную соответствующим последовательностям, полученным от конкретного вида. Например, в одном варианте реализации изобретения антитело против фактора Bb является химерным антителом, содержащим человеческий Fc-домен, в то время как оставшаяся часть антитела может быть идентичной или гомологичной соответствующим последовательностям мыши или грызуна. Химерные антитела могут представлять фрагменты таких антител до тех пор, пока эти фрагменты демонстрируют необходимую биологическую активность и содержат последовательность, полученную от другого вида, класса антител или подкласса антител (патент США №4816567; и Morrison et al. (1984) Proc. Natl. Acad. Sci. USA 81: 6851-6855).
[00147] В некоторых вариантах реализации изобретения вариабельная область раскрытого антитела против фактора Bb содержит по меньшей мере три CDR тяжелой или легкой цепи, смотрите выше (Kabat et al., 1991, Sequences of Proteins of Immunological Interest, Public Health Service N.I.H., Bethesda, MD; смотрите также Chothia and Lesk, 1987, J. Mol Biol 196: 901-917; Chothia et al., 1989, Nature 342: 877-883), в пределах каркасной области (каркасные области обозначаются как 1-4, FR1, FR2, FR3 и FR4 согласно Kabat et al., 1991, выше; смотрите также Chothia and Lesk, 1987, выше).
[00148] В некоторых случаях антитело может состоять из последовательности вариабельного домена тяжелой цепи и последовательности вариабельного домена легкой цепи. В некоторых случаях последовательность вариабельного домена тяжелой или легкой цепи может содержать последовательность, выбранную из последовательностей из Таблицы 3.
[00149] Структурные единицы традиционного антитела в большинстве случаев составляют тетрамер. Каждый тетрамер, как правило, состоит из двух идентичных пар полипептидных цепей, при этом каждая пара содержит одну легкую цепь (как правило, имеющую молекулярную массу около 25 кДа) и одну тяжелую цепь (как правило, имеющую молекулярную массу около 50-70 кДа). Амино-концевая часть каждой цепи содержит вариабельную область от около 100 до 110 или более аминокислот, отвечающих, главным образом, за распознавание антигена. Карбокси-концевая часть каждой цепи определяет константную область, причем тяжелая цепь может содержать всего три константные области (CH1, СН2 и СН3), при этом константные области могут способствовать регуляции эффекторной функции. Человеческие легкие цепи классифицируются как каппа и лямбда легкие цепи. Тяжелые цепи классифицируются как мю, дельта, гамма, альфа или эпсилон и определяют изотип антитела, соответственно, как IgM, IgD, IgG, IgA и IgE. IgG имеет несколько подклассов, включая, но не ограничиваясь этим, IgG1, IgG2, IgG3 и IgG4. IgM имеет подклассы, включая, но не ограничиваясь этим, IgM1 и IgM2.
[00150] В легких и тяжелых цепях вариабельные и константные области соединены посредством «J»-области длиной около двенадцати (12) или более аминокислот, а тяжелая цепь также содержит «D»-область длиной около десяти (10) или более аминокислот. В общем случае смотрите Paul, W., ed., 1989, Fundamental Immunology Ch. 7, 2nd ed. Raven Press, N.Y. Вариабельные области каждой пары легкой и тяжелой цепей образуют связывающий участок антитела.
[00151] Некоторые антитела природного происхождения, например, которые можно обнаружить у верблюдов и лам, представляют собой димеры, состоящие из двух тяжелых цепей, и не включают легкие цепи. Muldermans et al., 2001, J. Biotechnol. 74: 277-302; Desmyter et al., 2001, J. Biol. Chem. 276: 26285-26290. Кристаллографические исследования антител верблюдов выявили, что области CDR3 образуют поверхность, которая взаимодействует с антигеном и, таким образом, является критической для связывания антигена, как и в более типичных тетрамерных антителах. Изобретение включает димерные антитела, состоящие из двух тяжелых цепей, или их фрагменты, которые могут связываться с и/или ингибировать биологическую активность фактора Bb.
[00152] Вариабельные области тяжелой и легкой цепей, как правило, имеют одинаковую общую структуру из относительно консервативных каркасных областей (FR), соединенных тремя определяющими комплементарность областями или CDR. CDR содержат гипервариабельные области антитела, которые отвечают за распознавание и связывание антигена. CDR из двух цепей каждой пары ориентированы и поддерживаются каркасными областями, что обеспечивает возможность связывать конкретный эпитоп. От N-конца к С-концу как тяжелые, так и легкие цепи содержат домены FR1, CDR1, FR2, CDR2, FR3, CDR3 и FR4. Отнесение аминокислот к каждому домену проводят в соответствии с определениями из Kabat Sequences of Proteins of Immunological Interest. Chothia et al., 1987, J. Mol. Biol. 196: 901-917; Chothia et al., 1989. Nature 342: 878-883.
[00153] CDR составляют основные поверхностные контактные точки для связывания антигена. Смотрите, например, Chothia and Lesk, 1987, J. Mol. Biol. 196: 901-917. Кроме того, CDR3 легкой цепи и в особенности CDR3 тяжелой цепи могут составлять наиболее важные детерминанты в связывании антигена в вариабельных областях легкой и тяжелой цепей. Смотрите, например, Chothia and Lesk, 1987, выше; Desiderio et al., 2001, J. Mol Biol 310: 603-615; Xu and Davis, 2000, Immunity 13: 37-45; Desmyter et al., 2001, J. Biol. Chem. 276: 26285-26290; и Muyldermans, 2001, J. Biotechnol. 74: 277-302. В некоторых антителах CDR3 тяжелой цепи составляет основную площадь контакта между антигеном и антителом. Desmyter et al., 2001, выше. Схемы in vitro отбора, в которых варьируется только CDR3, можно использовать, чтобы варьировать связывающие свойства антитела. Muyldermans, 2001, выше; Desiderio et al., 2001, выше.
[00154] Антитела природного происхождения, как правило, содержат сигнальную последовательность, которая направляет антитело в клеточный путь для секреции белка и которая не присутствует в зрелом антителе. Полинуклеотид, кодирующий антитело согласно изобретению, может кодировать сигнальную последовательность природного происхождения или гетерологичную сигнальную последовательность, как описано ниже.
[00155] В одном варианте реализации изобретения антитело против фактора Bb представляет собой моноклональное антитело с от одной (1) до шести (6) CDR, как описано в данном документе. Антитела согласно изобретению могут принадлежать любому типу, включая антитела IgM, IgG (включая IgG1, IgG2, IgG3, IgG4), IgD, IgA или IgE. В конкретном варианте реализации изобретения антитело является антителом типа IgG. В более конкретном варианте реализации изобретения антитело является антителом типа IgG2.
[00156] В некоторых вариантах реализации изобретения антитело может содержать полные тяжелые и легкие цепи со всеми CDR от одного вида, например, человека. В альтернативном варианте, например, в вариантах реализации изобретения, в которых антитело содержит менее шести CDR из вышеприведенных последовательностей, дополнительные CDR могут принадлежать как другому виду (например, мышиные CDR), так и могут являться человеческими CDR, отличными от приведенных в последовательностях. Например, человеческие области НС CDR3 и LC CDR3 из соответствующих определенных в данном документе последовательностей можно использовать с НС CDR1, НС CDR2, LC CDR1 и LC CDR2, необязательно выбранными из других видов или из других последовательностей человеческих антител, или их комбинациями. Например, CDR согласно изобретению могут замещать области CDR коммерчески релевантных химерных или гуманизированных антител.
[00157] В конкретных вариантах реализации изобретения применяют каркасные компоненты антител, являющиеся человеческими компонентами.
[00158] В некоторых вариантах реализации изобретения, однако, каркасные компоненты могут представлять смесь от разных видов. Следовательно, антитело может быть химерным антителом и/или гуманизированным антителом. В общем случае как химерные, так и гуманизированные антитела могут являться антителами, в которых скомбинированы области или аминокислоты из более чем одного вида. Например, химерные антитела в большинстве вариантов реализации изобретения содержат вариабельную(ые) область(и) от мыши, крысы, кролика или другого подходящего отличного от человека животного и константную(ые) область(и) от человека.
[00159] Гуманизированными антителами являются антитела, которые изначально получены из нечеловеческих антител, например, мышиного антитела. В различных вариантах реализации гуманизированного антитела против фактора Bb каркасные области вариабельного домена или каркасные аминокислоты, которые получены из нечеловеческого антитела, можно заменить на идентичные аминокислоты, находящиеся в соответствующих позициях в человеческих антителах. В некоторых вариантах реализации гуманизированного антитела целое антитело за исключением CDR может кодироваться полинуклеотидом человеческого происхождения или быть идентичным такому антителу за исключением участков CDR. В других вариантах реализации изобретения гуманизированное антитело может содержать конкретные аминокислотные позиции, остатки в которых были заменены на остатки такой же или сходной позиции в соответствующем человеческом антителе. CDR, некоторые или все из которых могут кодироваться нуклеиновыми кислотами, принадлежащими нечеловеческому организму, прививают в бета-складчатый каркас вариабельной области человеческого антитела для создания антитела, специфичность которого определяется привитыми CDR. Создание таких антител описано, например, в WO 92/11018, Jones, 1986, Nature 321: 522-525, Verhoeyen et al., 1988, Science 239: 1534-1536. Гуманизированные антитела также можно получить, используя мышей с генетически сконструированной иммунной системой. Roque et al., 2004, Biotechnol Prog. 20: 639-654. В некоторых вариантах реализации изобретения CDR могут быть человеческими и, таким образом, в этом контексте как гуманизированные, так и химерные антитела содержат некоторые нечеловеческие CDR. В некоторых случаях можно получить гуманизированные антитела, которые содержат области НС CDR3 и LC CDR3 с одной или более других областей CDR отличного видового происхождения.
[00160] В одном варианте реализации изобретения антитело к фактору Bb может быть мультиспецифическим антителом, а именно, биспецифическим антителом (например, диателом). Это антитела, которые связываются с двумя (или более) разными антигенами, например, фактором Bb и другим антигеном, или двумя разными эпитопами фактора Bb. Диатела можно получать множеством известных в данной области техники способов (Holliger and Winter, 1993, Current Opinion Biotechnol. 4: 446-449), например, получать химическим путем или из гибридных гибридом.
[00161] В одном варианте реализации изобретения антитело к фактору Bb является минителом. Минитела представляют собой минимизированные антитело-подобные белки, содержащие scFv, соединенный с доменом СН3. Нu et al., 1996, Cancer Res. 56: 3055-3061.
[00162] В одном варианте реализации изобретения антитело к фактору Bb является доменным антителом; смотрите, например, патент США №6248516. Доменные антитела (dAb) представляют собой функциональные связывающие домены антител, соответствующие вариабельным участкам тяжелой (VH) или легкой (VL) цепей человеческих антител. dAB имеют молекулярную массу приблизительно 13 кДа или менее чем одна десятая от размера полного антитела. dAB хорошо экспрессируются во множестве хозяев, включая клеточные системы бактерий, дрожжей и млекопитающих. Кроме того, dAb являются высокостабильными и сохраняют активность даже после подвержения жестким условиям, таким как лиофилизация или тепловая денатурация. Смотрите, например, патент США 6291158; 6582915; 6593081; 6172197; США, серийный №2004/0110941; Европейский патент 0368684; патент США 6696245, WO 04/058821, WO 04/003019 и WO 03/002609, которые все в полном объеме включены посредством ссылки.
[00163] В одном варианте реализации изобретения антитело к фактору Bb является фрагментом антитела, который является фрагментом любого из приведенных в данном документе антител, который сохраняет специфичность связывания с фактором Bb. В различных вариантах реализации изобретения антитела являются фрагментами F(ab), F(ab'), F(ab')2, Fv или одноцепочечными фрагментами Fv. В контексте данного документа антитело, как минимум, содержит полипептид, который может специфически связываться с антигеном, при этом полипептид содержит всю или часть вариабельной области тяжелой и/или легкой цепи.
[00164] Конкретные фрагменты антител включают, но не ограничиваются этим, (i) фрагмент Fab, состоящий из доменов VL, VH, CL и СН1, (ii) фрагмент Fd, состоящий из доменов VH и CH1, (iii) фрагмент Fv, состоящий из доменов VL и VH одного антитела; (iv) фрагмент dAb (Ward et al., 1989, Nature 341: 544-546), который состоит из одной вариабельной области, (v) выделенные области CDR, (vi) фрагмент F(ab')2, бивалентный фрагмент, содержащий два связанных фрагмента Fab (vii) одноцепочечные молекулы Fv (scFv), в которых домен VH и домен VL связаны пептидным линкером, который обеспечивает ассоциацию двух доменов с образованием антигенсвязывающего участка (Bird et al., 1988, Science 242: 423-426, Huston et al., 1988, Proc. Natl Acad. Sci. U.S.A. 85: 5879-5883), (viii) биспецифические одноцепочечные димеры Fv (PCT/US92/09965) и (ix) диатела или триатела, мультивалентные или мультиспецифические фрагменты, сконструированные путем генного слияния (Tomlinson et. al, 2000, Methods Enzymol. 326: 461-479; WO 94/13804; Holliger et al., 1993, Proc. Natl. Acad. Sci. U.S.A. 90: 6444-6448). Фрагменты антител могут быть модифицированы. Например, молекулы можно стабилизировать путем включения дисульфидных мостиков, связывающих домены VH и VL (Reiter et al., 1996, Nature Biotech. 14: 1239-1245). Снова, как указано в данном документе, отличные от CDR компоненты этих фрагментов предпочтительно представлены человеческими последовательностями.
[00165] В одном варианте реализации изобретения антитело к фактору Bb является традиционным антителом, например, человеческим иммуноглобулином. В этом варианте реализации изобретения, как указано выше, конкретные структуры содержат полные тяжелые и легкие цепи, содержащие области CDR. В дополнительных вариантах реализации изобретения применяют одну или более CDR согласно изобретению с другими CDR, каркасными областями, областями J и D, константными областями и т.д., принадлежащими другим человеческим антителам. Например, CDR согласно изобретению могут замещать CDR любого числа человеческих антител, в частности, коммерчески релевантных антител.
[00166] В одном варианте реализации изобретения антитело к фактору Bb является слитым белком антитела (например, конъюгатом антитела). В этом варианте реализации изобретения антитело слито с партнером по конъюгации. Партнер по конъюгации может быть белковым или небелковым; последнее в общем случае получают при помощи функциональных групп на антителе (смотрите обсуждение ковалентных модификаций антител) и на партнере по конъюгации. Например, линкеры являются известными в данной области техники; например, хорошо известны гомо- или гетеро-бифункциональные линкеры (смотрите, каталог Pierce Chemical Company, технический раздел по кросс-линкерам, страницы 155-200, включенный в данный документ посредством ссылки).
[00167] В одном варианте реализации изобретения антитело к фактору Bb является аналогом антитела. В некоторых случаях аналоги антител могут называться синтетическими антителами. Например, во многих недавних работах используют альтернативные белковые каркасы или искусственные каркасы с привитыми CDR. Такие каркасы включают, но не ограничиваются этим, мутации, введенные для стабилизации трехмерной структуры антитела, а также полностью синтетические каркасы, состоящие, например, из биосовместимых полимеров. Смотрите, например, Korndorfer et al., 2003, Proteins: Structure, Function, and Bioinformatics, Volume 53, Issue 1: 121-129. Roque et al., 2004, Biotechnol. Prog. 20: 639-654. Кроме того, можно использовать пептидные миметики антител (ПМА), а также работу на основании миметиков антител с применением фибронектиновых компонентов в качестве каркаса.
VH- и VL-варианты
[00168] Как указано выше, в некоторых вариантах реализации в изобретении предложены антитела, содержащие или состоящие из вариабельной области тяжелой цепи, содержащей SEQ ID NO: 1-3, и/или вариабельной области легкой цепи, содержащей SEQ ID NO: 4-6, соответственно, или их фрагменты согласно определению выше. Таким образом, в этих вариантах реализации изобретения антитело содержит не только по меньшей мере одну CDR или вариант, но также по меньшей мере часть приведенной каркасной последовательности. Кроме того, изобретение включает варианты таких вариабельных последовательностей тяжелой цепи или вариабельных последовательностей легкой цепи.
[00169] Вариантная вариабельная область в общем случае обладает аминокислотной гомологией, сходством или идентичностью, составляющей по меньшей мере 80%, с родительской вариабельной областью, такой как области, раскрытые в данном документе. В некоторых вариантах реализации изобретения гомология или идентичность вариантной и родительской последовательностей составляет по меньшей мере 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и практически 100%. Гомология, сходство или идентичность нуклеотидных последовательностей между нуклеотидными последовательностями, кодирующими отдельные вариантные VH и VL, и нуклеотидными последовательностями, приведенными в данном документе, составляет по меньшей мере 70%, и, как правило, с предпочтительно возрастающей гомологией или идентичностью, составляющей по меньшей мере 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% и практически 100%. Кроме того, вариантная вариабельная область может во многих вариантах реализации изобретения обладать биологической функцией, включая, но не ограничиваясь этим, составляющей 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% от специфичности и/или активности родительской CDR. В некоторых случаях гомологию и/или идентичность определяют только за пределами последовательностей CDR, которые могут быть идентичными. В других случаях гомологию и/или идентичность определяют на полной длине последовательности, включая последовательности CDR. В некоторых вариантах реализации изобретения также могут быть включены варианты константных областей.
[00170] В различных случаях гомология аминокислотных последовательностей может отображать процентную долю идентичности или положительных результатов при оптимальном выравнивании, как описано выше. В различных случаях % гомологии (% положительных результатов) или % идентичности можно рассчитать, разделив количество выровненных аминокислот в окне сравнения. Окно сравнения может составлять полную длину одного или другого полипептида, если длина двух полипептидов не одинакова. В других случаях окно сравнения может составлять часть одного из полипептидов. В различных случаях окно сравнения для определения гомологии или идентичности двух полипептидных последовательностей составляет более чем около 40 ак (аминокислот), 45 ак, 50 ак, 55 ак, 60 ак, 65 ак, 70 ак, 75 ак, 80 ак, 85 ак, 90 ак, 95 ак, 100 ак, 150 ак или 200 ак, и/или менее чем около 200 ак, 150 ак, 100 ак, 95 ак, 90 ак, 85 ак, 80 ак, 75 ак, 70 ак, 65 ак, 60 ак, 55 ак, 50 ак или 45 ак. В некоторых вариантах реализации изобретения, как в случае с последовательностями CDR, окно сравнения может составлять менее чем 40 ак, например, между менее чем около 25 ак, 24 ак, 23 ак, 22 ак, 21 ак, 20 ак, 19 ак, 18 ак, 17 ак, 16 ак, 15 ак, 14 ак, 13 ак, 12 ак, 11 ак, 10 ак, 9 ак, 8 ак, 7 ак, 6 ак, 5 ак или 4 ак, и более чем около 3 ак, 4 ак, 5 ак, 6 ак, 7 ак, 8 ак, 9 ак, 10 ак, 11 ак, 12 ак, 13 ак, 14 ак, 15 ак, 16 ак, 17 ак, 18 ак, 19 ак, 20 ак, 21 ак, 22 ак, 23 ак или 24 ак.
[00171] В различных случаях заявленные аминокислотные последовательности могут иметь % идентичности или % гомологии (% положительных), превышающий заданное окно сравнения, т.е. больший чем около 70%, 75%, 80%, 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% и/или меньший чем около 100%, 99%, 98%, 97%, 96%, 95%, 94%, 93%, 92%, 91%, 90%, 85%, 80% или 75%.
Ковалентные модификации антител к фактору Bb
[00172] Ковалентные модификации антител включены в объем данного изобретения и в общем случае, но не всегда, происходят после трансляции. Например, в молекулу вносят несколько типов ковалентных модификаций антитела путем приведения конкретных аминокислотных остатков антитела в реакцию с органическим дериватизирующим агентом, который способен вступать в реакцию с выбранными боковыми цепями N- или С-концевых остатков.
[00173] Остатки цистеинила наиболее часто приводят в реакцию с α-галогенацетатами (и соответствующими аминами), такими как хлоруксусная кислота или хлорацетамид, чтобы получить карбоксиметильные или карбоксиамидометильные производные. Остатки цистеинила также дериватизируют посредством реакции с бромтрифторацетоном, α-бром-β-(5-имидозоил)пропионовой кислотой, хлорацетилфосфатом, N-алкилмалеимидами, 3-нитро-2-пиридилдисульфидом, метил-2-пиридилдисульфидом, п-хлорртутьбензоатом, 2-хлорртуть-4-нитрофенолом или хлор-7-нитробензо-2-окса-1,3-диазолом.
[00174] Остатки гистидила дериватизируют посредством реакции с диэтилпирокарбонатом при рН 5,5-7,0, поскольку этот агент является относительно специфичным в отношении боковой цепи гистидила. Также применим пара-бромфенацилбромид; реакцию предпочтительно проводят в 0,1 М растворе какодилата натрия при рН 6,0.
[00175] Лизиниловые и амино-концевые остатки приводят в реакцию с янтарным ангидридом или ангидридами других карбоновых кислот. Дериватизация этими агентами может приводить к изменению заряда остатков лизинила. Другие подходящие реагенты для дериватизации альфа-аминосодержащих остатков включают имидоэфиры, такие как метилпиколинимидат; пиридоксальфосфат; пиридоксаль; хлорборогидрид; тринитробензолсульфоновую кислоту; О-метилизомочевина; 2,4-пентандион; и катализируемую трансаминазой реакцию с глиоксилатом.
[00176] Остатки аргинила модифицируют путем реакции с одним или несколькими традиционными реагентами, среди которых фенилглиоксаль, 2,3-бутандион, 1,2-циклогександион и нингидрин. Для дериватизации остатков аргинина необходимо, чтобы реакцию проводили в щелочной среде из-за высокой pKa гуанидиновой функциональной группы. Кроме того, такие реагенты могут взаимодействовать с группами лизина, а также с эпсилон-амино-группой аргинина.
[00177] Можно проводить конкретные модификации остатков тирозила, в особенности интересны случаи введения спектральных меток в остатки тирозила при помощи реакции с ароматическими соединениями диазония или тетранитрометаном. Наиболее часто применяют N-ацетилимидизол и тетранитрометан для образования видов О-ацетил тирозила и 3-нитропроизводных, соответственно. Остатки тирозила йодируют, применяя 125I или 131I, для получения меченых белков для применения в радиоиммунологическом анализе, при этом подходящим является описанный выше метод с хлорамином Т.
[00178] Карбоксильные боковые группы (аспартил или глутамил) селективно модифицируют при помощи реакции с карбодиимидами (R'-N=C=N--R'), где R и R' необязательно представляют собой разные алкильные группы, такие как 1-циклогексил-3-(2-морфолинил-4-этил)карбодиимид или 1-этил-3-(4-азониа-4,4-диметилфенил)карбодиимид. Кроме того, остатки аспартила и глутамила превращают в остатки аспарагинила и глутаминила при помощи реакции с ионами аммония.
[00179] Дериватизацию с бифункциональными агентами применяют для перекрестного сшивания антител с нерастворимой в воде матричной подложной или поверхностью для применения в различных способах. Обычно применяемые перекрестносшивающие агенты включают, например, 1,1-бис(диазоацетил)-2-фенилэтан, глутаральдегид, N-гидроксисукцинимид эфиры, например, сложные эфиры с 4-азидосалициловой кислотой, гомобифункциональные сложные имидоэфиры, включая дисукцинимидилэфиры, такие как 3,3'-дитио-бис-(сукцинимидилпропионат), и бифункциональные малеимиды, такие как бис-N-малеимидо-1,8-октан. При помощи дериватизирующих агентов, таких как метил-3-[(п-азидофенил)дитио]пропиоимидат, получают фотоактивируемые промежуточные соединения, которые способны образовывать перекрестные связи в присутствии света. В альтернативном варианте для иммобилизации белка применяют нерастворимые в воде матрицы, такие как активируемые бромистым цианогеном углеводы и реактивные субстраты, описанные в патентах США №3969287; 3691016; 4195128; 4247642; 4229537; и 4330440.
[00180] Остатки глутаминила и аспарагинила часто деамидируют до соответствующих остатков глутамила и аспартила, соответственно. В альтернативном варианте эти остатки деамидируют в умеренно кислых условиях. Любая форма этих остатков входит в объем настоящего изобретения.
[00181] Другие модификации включают гидроксилирование пролина и лизина, фосфорилирование гидроксильных групп остатков серила или треонила, метилирование α-аминогрупп лизина, аргинина и боковых цепей гистидина (Т.Е. Creighton, Proteins: Structure and Molecular Properties, W.H. Freeman & Co., San Francisco, 1983, pp. 79-86), ацетилирование N-концевого амина и амидирование любой С-концевой карбоксильной группы.
Гликозилирование
[00182] Другой тип ковалентной модификации антител, входящий в объем данного изобретения, включает изменение профиля гликозилирования белка. Как известно в данной области техники, профили гликозилирования могут зависеть как от последовательности белка (например, присутствия или отсутствия конкретных аминокислотных остатков гликозилирования, обсуждаемых ниже), так и от клетки-хозяина или организма-хозяина, в которых вырабатывается белок. Конкретные экспрессионные системы обсуждаются ниже.
[00183] Гликозилирование полипептидов, как правило, бывает N-связанным или О-связанным. N-связанное гликозилирование относится к присоединению углеводного компонента к боковой цепи остатка аспарагина. Трипептидные последовательности аспарагин-Х-серин и аспарагин-Х-треонин, где X является любой аминокислотой за исключением пролина, представляют последовательности распознавания для ферментативного присоединения углеводного компонента к боковой цепи аспарагина. Следовательно, присутствие любой из этих трипептидных последовательностей создает потенциальный участок гликозилирования. О-связанное гликозилирование относится к присоединению одного из сахаров N-ацетилгалактозамина, галактозы или ксилозы к гидроксиаминокислоте, наиболее часто серину или треонину, хотя также можно использовать 5-гидроксипролин или 5-гидроксилизин.
[00184] Добавление участков гликозилирования к раскрытому антителу удобно осуществлять путем изменения аминокислотной последовательности так, чтобы она содержала одну или более из вышеописанных трипептидных последовательностей (для N-связанных участков гликозилирования). Изменение также можно проводить путем добавления или замещения на один или более остатков серина или треонина в исходной последовательности (для О-связанных участков гликозилирования). Для удобства аминокислотную последовательность антитела предпочтительно изменяют на уровне ДНК, в частности, мутируя ДНК, кодирующую полипептид-мишень, в предварительно выбранных основаниях так, чтобы сгенерированные кодоны транслировались в необходимые аминокислоты.
[00185] Другим способом повышения числа углеводных компонентов в антителе является химическое или ферментативное сопряжение гликозидов с белком. Эти процедуры являются преимущественными, так как они не требуют выработки белка в клетке-хозяине, которая обладает способностью осуществлять N- или О-связанное гликозилирование. В зависимости от применяемого способа сопряжения, сахар(а) можно присоединить к (а) аргинину и гистидину, (b) свободным карбоксильным группам, (с) свободным сульфгидрильным группам, таким как группы цистеина, (d) свободным гидроксильным группам, таким как группы серина, треонина или гидроксипролина, (е) ароматическим остаткам, таким как остатки фенилаланина, тирозина или триптофана, или (f) амидной группе глутамина. Эти способы описаны в WO 87/05330, опубликованной 11 сентября 1987 г., и в Aplin and Wriston, 1981, CRC Crit. Rev. Biochem., pp. 259-306.
[00186] Удаление углеводных компонентов, присутствующих на исходном антителе, можно осуществлять химически или ферментативно. Для химического дегликозилирования необходимо подвергнуть белок действию соединения трифторметансульфоновой кислоты или эквивалентного соединения. Эта обработка приводит к расщеплению большинства или всех сахаров, кроме связующего сахара (N-ацетилглюкозамина или N-ацетилгалактозамина), при этом полипептид остается интактным. Химическое дегликозилирование описано в Hakimuddin et al., 1987, Arch. Biochem. Biophys. 259: 52 and by Edge et al., 1981, Anal. Biochem. 118: 131. Ферментативное расщепление углеводных компонентов на полипептиде можно осуществлять, применяя различные эндо- и экзогликозидазы, как описано в Thotakura et al., 1987, Meth. Enzymol 138: 350. Гликозилирование в потенциальных участках гликозилирования можно предотвратить, используя соединение туникамицин, как описано в Duskin et al., 1982, J. Biol. Chem. 257: 3105. Туникамицин блокирует образование связей белок-N-гликозид.
ПЭГилированние
[00187] Другой тип ковалентной модификации антитела включает присоединение к антителу различных небелковых полимеров, включая, но не ограничиваясь этим, различные полиолы, такие как полиэтиленгликоль, полипропиленгликоль, или полиоксиалкилены, способом, приведенным в патентах США №4640835; 4496689; 4301144; 4670417; 4791192 и/или 4179337, которые все в полном объеме включены посредством ссылки. Кроме того, как известно в данной области техники, в различных позициях антитела можно проводить аминокислотные замены, чтобы облегчить добавление полимеров, таких как ПЭГ.
Метки
[00188] В некоторых вариантах реализации изобретения ковалентная модификация антител согласно изобретению включает добавление одной или более меток.
[00189] Термином «метящая группа» обозначают любую выявляемую метку. Примеры подходящих метящих групп включают, но не ограничиваются этим, следующие: радиоизотопы или радионуклиды (например, 3Н, 14С, 15N, 35S, 90Y, 99Тс, 111In, 125I, 131I), флуоресцентные группы (например, ФИТЦ, родамин, люминофоры на основе комплексов лантанидов), ферментативные группы (например, пероксидаза хрена, β-галактозидаза, люцифераза, щелочная фосфатаза), хемилюминесцентные группы, биотинильные группы или предопределенные полипептидные эпитопы, распознаваемые вторичным репортером (например, парные последовательности лейциновых молний, участки связывания вторичных антител, металлсвязывающие домены, эпитопные метки). В некоторых вариантах реализации изобретения метящая группа сопряжена с антителом посредством спейсерных ножек различной длины для снижения потенциального стерического несоответствия. В данной области техники известны различные способы мечения белков, которые можно применять для осуществления настоящего изобретения.
[00190] В общем случае метки делятся на различные классы в зависимости от метода их выявления: а) изотопные метки, которые могут быть представлены радиоактивными или тяжелыми изотопами; b) магнитные метки (например, магнитные частицы); с) редокс-активные компоненты; d) оптические красители; ферментативные группы (например, пероксидаза хрена, β-галактозидаза, люцифераза, щелочная фосфатаза); е) биотинилированные группы; и f) предопределенные полипептидные эпитопы, распознаваемые вторичным репортером (например, парные последовательности лейциновых молний, участки связывания вторичных антител, металлсвязывающие домены, эпитопные метки и т.д.). В некоторых вариантах реализации изобретения метящая группа сопряжена с антителом посредством спейсерных ножек различной длины для снижения потенциального стерического несоответствия. В данной области техники известны различные способы мечения белков, которые можно применять для осуществления настоящего изобретения.
[00191] Конкретные метки включают оптические красители, включая, но не ограничиваясь этим хромофоры, люминофоры и флуорофоры, при этом последние в различных случаях являются специфическими. Флуорофоры могут быть как «низкомолекулярными» флуорофорами, так и белковыми флуорофорами.
[00192] Флуоресцентная метка может представлять собой любую молекулу, которую можно выявить вследствие присущих ей флуоресцентных свойств. Подходящие флуоресцентные метки включают, но не ограничиваются этим, флуоресцеин, родамин, тетраметилродамин, эозин, эритрозин, кумарин, метилкумарины, пирен, малахитовый зеленый, стильбен, желтый люцифер, каскад голубой J, техасский красный, IAEDANS, EDANS, BODIPY FL, LC Red 640, Cy 5, Cy 5.5, LC Red 705, зеленый Орегон, красители Alexa-Fluor (Alexa Fluor 350, Alexa Fluor 430, Alexa Fluor 488, Alexa Fluor 546, Alexa Fluor 568, Alexa Fluor 594, Alexa Fluor 633, Alexa Fluor 660, Alexa Fluor 680), каскад голубой, каскад желтый и R-фикоэритрин (ФЭ) (Molecular Probes, Eugene, OR), ФИТЦ, родамин и техасский красный (Pierce, Rockford, IL), Cy5, Cy5.5, Cy7 (Amersham Life Science, Pittsburgh, PA). Подходящие оптические красители, включая флуорофоры, описаны в Molecular Probes Handbook by Richard P. Haugland, явным образом включенной в данный документ посредством ссылки.
[00193] Подходящие белковые флуоресцентные метки также включают, но не ограничиваются этим, зеленый флуоресцентный белок, включая виды ЗФБ Renilla, Ptilosarcus или Aequorea (Chalfie et al., 1994, Science 263: 802-805), УЗФБ (Clontech Laboratories, Inc., Genbank Accession Number U55762), голубой флуоресцентный белок (ГФБ, Quantum Biotechnologies, Inc. 1801 de Maisonneuve Blvd. West, 8th Floor, Montreal, Quebec, Canada H3H 1J9; Stauber, 1998, Biotechniques 24: 462-471; Heim et al., 1996, Curr. Biol 6: 178-182), еусиленный желтый флуоресцентный белок (УЖФБ, Clontech Laboratories, Inc.), люциферазу (Ichiki et al., 1993, J. Immunol 150: 5408-5417), β-галактозидазу (Nolan et al., 1988, Proc. Natl. Acad. Sci. U.S.A. 85: 2603-2607) и Renilla (WO 92/15673, WO 95/07463, WO 98/14605, WO 98/26277, WO 99/49019, патенты США №5292658, 5418155, 5683888, 5741668, 5777079, 5804387, 5874304, 5876995, 5925558), которые все в полном объеме включены посредством ссылки.
Полинуклеотиды, кодирующие антитела против фактора Bb
[00194] В определенных аспектах в изобретении предложены молекулы нуклеиновых кислот, кодирующие описанные в данном документе антитела. В некоторых случаях раскрытые нуклеиновые кислоты кодируют IgG, вариабельные области или CDR, описанные в данном документе. Нуклеиновые кислоты включают молекулы как ДНК, так и РНК. Нуклеиновые аминокислоты могут быть нуклеиновыми кислотами как природного, так и синтетического происхождения. Нуклеиновые кислоты согласно настоящему изобретению, как правило, являются полинуклеиновыми кислотами; что означает полимеры из отдельных нуклеотидов, которые ковалентно соединены посредством 3', 5' фосфодиэфирных связей. В различных случаях полинуклеотидные последовательности могут быть одноцепочечными, двухцепочечными или комбинированными. В некоторых вариациях нуклеотидные последовательности могут содержать природные нуклеиновые кислоты, синтетические нуклеиновые кислоты, неприродные нуклеиновые кислоты и/или аналоги нуклеиновых кислот. Нуклеотидные последовательности могут дополнительно содержать другие, отличные от нуклеиновых кислот молекулы, такие как аминокислоты и другие мономеры.
[00195] Во многих вариантах реализации изобретения кодирующая последовательность может представлять собой выделенную молекулу нуклеиновой кислоты. Выделенная молекула нуклеиновой кислоты выявлена и отделена по меньшей мере от одного компонента, с которым она обычно связана в естественном источнике. В некоторых случаях этот компонент может быть нуклеотидной последовательностью, белком или небелковой молекулой. Выделенная молекула нуклеиновой кислоты, кодирующая антитело против фактора Bb, отличается от той формы, в которой она находится в природе. Следовательно, выделенные молекулы нуклеиновых кислот, кодирующие антитела против фактора Bb, отличаются от кодирующей(их) молекул(ы) нуклеиновых кислот, присутствующих в природных клетках. При этом, выделенная молекула нуклеиновой кислоты, кодирующая антитело против фактора Bb, включает молекулы нуклеиновых кислот, кодирующие антитела против фактора Bb, содержащиеся в клетках, которые обычно экспрессируют антитело против фактора Bb, где, например, молекула нуклеиновой кислоты находится в хромосомной локации, отличной от локации в природных клетках. Следовательно, выделенные молекулы нуклеиновых кислот отличаются от молекулы нуклеиновой кислоты, присутствующей в организме. При этом в некоторых случаях выделенная молекула нуклеиновой кислоты может быть нуклеиновой кислотой, содержащейся в клетке, например, если выделенную молекулу нуклеиновой кислоты внесли в клетку, и она находится во внехромосомной локации или в хромосомной локации, отличной от ее нативной локации.
[00196] В зависимости от применения нуклеиновая кислота может быть двухцепочечной, одноцепочечной или содержать части как двухцепочечной, так и одноцепочечной последовательности. Как понятно специалистам в данной области техники, описание одной цепи («Уотсон») также определяет последовательность другой цепи («Крик»). Рекомбинантная нуклеиновая кислота может быть аминокислотой, изначально образуемой in vitro, в общем случае путем обработки нуклеиновой кислоты эндонуклеазами в форме, которая обычно не встречается в природе. Таким образом, выделенное антитело может кодироваться нуклеиновой кислотой в линейной форме или экспрессионным вектором, образуемым in vitro путем лигирования молекул ДНК, которые обычно не соединены, и в обоих случаях считается рекомбинантным в целях данного изобретения. Понятно, что если рекомбинантная нуклеиновая кислота со всеми необходимыми регуляторными элементами получена и внесена в организм-хозяина, она может реплицироваться нерекомбинантно, т.е. при помощи in vivo клеточного аппарата клетки-хозяина, а не in vitro манипуляций; при этом такие нуклеиновые кислоты после рекомбинантного получения, хотя впоследствии и реплицируются нерекомбинантно, все равно считаются рекомбинантными в целях данного изобретения.
[00197] В некоторых вариантах реализации изобретения рекомбинантная нуклеиновая кислота может содержать один или более регуляторных элементов или регуляторных последовательностей. Регуляторные элементы и регуляторные последовательности относятся к нуклеотидным последовательностям, необходимым для экспрессии функционально связанной кодирующей последовательности в конкретном организме-хозяине. Регуляторные последовательности, которые подходят для прокариотов, например, включают промотор, последовательность оператора и участок связывания рибосомы. Известно, что в эукариотических клетках используются промоторы, сигналы полиаденилирования и энхансеры. В контексте данного документа функционально связанной последовательностью является нуклеотидная последовательность, находящаяся в функциональной взаимосвязи с другой нуклеотидной последовательностью. Например, кодирующие нуклеотидные последовательности могут быть функционально связаны с регуляторными нуклеотидными последовательностями. Например, ДНК для предпоследовательности или секреторной лидерной последовательности функционально связаны с ДНК для полипептида, если он экспрессируется в виде белка-предшественника, который принимает участие в секреции полипептида; промотор или энхансер функционально связан с кодирующей последовательностью, если он влияет на транскрипцию последовательности; или участок связывания рибосомы функционально связан с кодирующей последовательностью, если он расположен так, чтобы облегчить трансляцию. В большинстве вариантов реализации изобретения функционально связанная последовательность представляет собой последовательность ДНК, ковалентно связанную, например, с секреторной лидерной последовательностью. Во многих вариантах реализации изобретения нет необходимости, чтобы энхансерные последовательности были смежными с кодирующей последовательностью, наоборот, две последовательности могут быть разделены одной или более нуклеиновыми кислотами.
[00198] В различных случаях нуклеиновые кислоты раскрытых нуклеотидных последовательностей могут содержать нуклеотиды, которые метаболизируются сходным образом с нуклеотидами природного происхождения. Также включены подобные нуклеиновым кислотам структуры с синтетическими аналогами скелета, включая, без ограничений, фосфодиэфирные, тиофосфатные, дитиофосфатные, метилфосфонатные, фосфорамидатные, алкил фосфодиэфирные, сульфаматные, 3'-тиоацетальные, метилен(метилимино), 3'-N-карбаматные, морфолино карбаматные и пептидные нуклеиновые кислоты (ПНК) (смотрите, например: "Oligonucleotides and Analogues, а Practical Approach," edited by F. Eckstein, IRL Press at Oxford University Press (1991); "Antisense Strategies," Annals of the New York Academy of Sciences, Volume 600, Eds. Baserga and Denhardt (NYAS 1992); Milligan (1993) J. Med. Chem. 36: 1923-1937; and "Antisense Research and Applications" (1993, CRC Press)). ПНК содержат неионные скелеты, такие как N-(2-аминоэтил)глициновые единицы. Тиофосфатные связи описаны в: WO 97/03211; WO 96/39154; и Mata (1997) Toxicol. Appl. Pharmacol. 144: 189-197. Другие синтетические скелеты, подпадающие под этот термин, включают метилфосфонатные связи или чередующиеся метилфосфонатные и фосфодиэфирные связи (Strauss-Soukup (1997) Biochemistry 36: 8692-8698) и бензилфосфонатные связи (Samstag (1996) Antisense Nucleic Acid Drug Dev 6: 153-156).
[00199] Как понятно специалистам в данной области техники, вследствие вырожденности генетического кода можно получить намного большее число нуклеиновых кислот, которые все кодируют CDR (а также тяжелые и легкие цепи или другие компоненты антитела) согласно настоящему изобретению. Таким образом, после определения конкретной аминокислотной последовательности специалисты в данной области техники могут получить любое количество разных нуклеиновых кислот, просто модифицируя последовательность одного или более кодонов так, чтобы не изменять аминокислотную последовательность кодируемого белка.
[00200] В различных случаях включены нуклеотидные последовательности, кодирующие полипептидные последовательности SEQ ID NO: 1-6 и 8-15, и 18-31. Эти кодирующие нуклеотидные последовательности могут транслироваться в полипептид, имеющий аминокислотную последовательность, идентичную раскрытой полипептидной последовательности. Во многих случаях нуклеотиды, кодирующие идентичные полипептиды, могут не иметь идентичные нуклеотидные последовательности. Это происходит вследствие вырожденности генетического кода. Раскрытые кодирующие последовательности могут дополнительно содержать нетранслируемые последовательности, например, последовательности полиаденилирования. Кодирующие последовательности согласно изобретению также могут содержать интрон или промежуточную нетранслируемую последовательность, которые вырезаются из транскрибируемой мРНК перед трансляцией. В различных случаях транскрибируемая мРНК может быть кэпирована концевым 7-метилгуанозином. В некоторых вариантах реализации изобретения кодирующие последовательности включают кодирующие последовательности аминокислот, которые не присутствуют в конечном антителе, например, последовательности, необходимые для экспортирования антитела.
[00201] В некоторых вариациях вследствие вырожденности генетического кода несколько кодирующих нуклеотидных последовательностей могут кодировать одну полипептидную последовательность. Такие кодирующие нуклеотидные последовательности согласно изобретению также могут быть гомологичными нуклеотидным последовательностям, которые кодируют раскрытые полипептиды. Выравнивание кодирующих нуклеотидных последовательностей можно проводить при помощи BLASTn, как описано выше. В различных случаях гомология (или идентичность в BLASTn) этих выровненных нуклеотидных последовательностей может составлять больше чем около 40%, 45%, 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90% или 95% и/или меньше чем около 100%, 95%, 90%, 85%, 80%, 75%, 70%, 65%, 60%, 55%, 50% или 45%. В различных случаях выровненные гомологичные последовательности могут составлять меньше чем около 700 нуклеотидов, 600 нуклеотидов, 500 нуклеотидов, 400 нуклеотидов, 300 нуклеотидов, 200 нуклеотидов, 100 нуклеотидов, 90 нуклеотидов, 80 нуклеотидов, 70 нуклеотидов, 60 нуклеотидов, 50 нуклеотидов или 40 нуклеотидов и/или больше чем около 50 нуклеотидов, 60 нуклеотидов, 70 нуклеотидов, 80 нуклеотидов, 90 нуклеотидов, 100 нуклеотидов, 200 нуклеотидов, 300 нуклеотидов, 400 нуклеотидов, 500 нуклеотидов или 600 нуклеотидов.
[00202] В различных случаях кодирующая последовательность управляет транскрипцией рибонуклеотидной последовательности, которая может быть транслирована в аминокислотную последовательность в соответствии со стандартным генетическим кодом. В различных случаях код может включать вариации канонического кода. В некоторых вариациях кодирующая последовательностью может содержать интроны или промежуточные последовательности, которые не кодируют аминокислоты, но могут быть транскрибированы и впоследствии удалены перед трансляцией рибонуклеиновой кислоты в полипептид.
Способы получения антител
[00203] Также в настоящем изобретении предложены экспрессионные системы и конструкции в форме плазмид, экспрессионных векторов, транскрипционных или экспрессионных кассет, которые содержат по меньшей мере один из вышеуказанных полинуклеотидов. Кроме того, в изобретении предложены клетки-хозяева, содержащие такие экспрессионные конструкции.
[00204] Как правило, экспрессионные векторы, применяемые в любых клетках-хозяевах, содержат последовательности для поддержания плазмид и для клонирования и экспрессии экзогенных нуклеотидных последовательностей. Такие последовательности, вместе называемые фланкирующими последовательностями, в определенных вариантах реализации изобретения, как правило, содержат одну или более из следующих нуклеотидных последовательностей: промотор, одну или более энхансерных последовательностей, точку начала репликации, последовательность терминации транскрипции, полную интронную последовательность, содержащую донорный и акцепторный участки сплайсинга, последовательность, кодирующую лидерную последовательность для секреции полипептида, участок связывания рибосомы, последовательность полиаденилирования, полилинкерную область для вставки нуклеиновой кислоты, кодирующей предназначенный для экспрессии полипептид, и элемент селективного маркера. Каждая из этих последовательностей обсуждается ниже.
[00205] Необязательно, вектор может содержать последовательность, кодирующую «метку», т.е. молекулу олигонуклеотида, расположенную в 5' или 3' конце кодирующей последовательности антитела к фактору Bb; олигонуклеотидная последовательность может кодировать метку полиHis (такую как гексаHis) или другую «метку», такую как FLAG, НА (гемагглютинин вируса гриппа) или myc, для которых существуют коммерчески доступные антитела. Такая метка обычно сливается с полипептидом после экспрессии полипептида и может служить в качестве средства для аффинной очистки или выявления антитела к фактору Bb в клетке-хозяине. Аффинную очистку можно проводить, например, при помощи колоночной хроматографии, используя антитела против метки в качестве аффинной матрицы. Необязательно, метку можно впоследствии удалять из очищенного антитела к фактору Bb разными способами, такими как использование определенных пептидаз для расщепления.
[00206] Фланкирующие последовательности могут быть гомологичными (т.е. принадлежать тому же виду и/или штамму, что и клетка-хозяин), гетерологичными (т.е. принадлежать виду, отличному от вида или штамма клетки-хозяина), гибридными (т.е. комбинация фланкирующих последовательностей из более чем одного источника), синтетическими или нативными. Следовательно, источником фланкирующей последовательности может быть любой прокариотический или эукариотический организм, любой позвоночный или беспозвоночный организм или любое растение, при условии, что фланкирующая последовательность является функциональной и может быть активирована аппаратом клетки-хозяина.
[00207] Фланкирующие последовательности, применяемые в векторах согласно данному изобретению, можно получить любым из нескольких способов, хорошо известных в данной области техники. Как правило, фланкирующие последовательности, применяемые в данном документе, были предварительно идентифицированы при помощи картирования и/или расщепления рестрикциоными эндонуклеазами и, следовательно, могут быть выделены из соответствующего тканевого источника, используя подходящие рестрикционные эндонуклеазы. В некоторых случаях может быть известна полная нуклеотидная последовательность фланкирующей последовательности. Или фланкирующая последовательность может быть синтезирована при помощи описанных в данном документе способов для синтеза и клонирования нуклеиновых кислот.
[00208] Вне зависимости от того, известна вся или только часть фланкирующей последовательности, ее можно получить при помощи полимеразной цепной реакции (ПЦР) и/или при скрининга геномной библиотека с подходящим зондом, таким как олигонуклеотид и/или фрагмент фланкирующей последовательности от того же или другого вида. Если фланкирующая последовательность неизвестна, фрагмент ДНК, содержащий фланкирующую последовательность, можно выделить из более крупного участка ДНК, который может содержать, например, кодирующую последовательность и даже другой ген или гены. Выделение можно проводить путем расщепления рестрикциоными эндонуклеазами для получения надлежащего фрагмента ДНК с последующим выделением при помощи очистки в агарозном геле, колоночной хроматографии Qiagen® (Chatsworth, СА) или других способов, известных специалисту в данной области техники. Выбор подходящих ферментов для осуществления этой цели очевиден для специалиста в данной области техники.
[00209] Точка начала репликации, как правило, является частью приобретенных на коммерческой основе прокариотических экспрессионных векторов и способствует амплификации вектора в клетке-хозяине. Если выбранный вектор не содержит точку начала репликации, ее можно химически синтезировать на основании известной последовательности и лигировать в вектор. Например, точка начала репликации из плазмиды pBR322 (New England Biolabs, Beverly, MA) подходит для большинства грамотрицательных бактерий, а различные вирусные источники (например, SV40, полиомы, аденовируса, вируса везикулярного стоматита (ВВС) или папилломавирусов, таких как ВПЧ или ВПКРС) подходят для клонирования векторов в клетках млекопитающих. В общем случае компонент точки начала репликации необязателен в экспрессионных векторах млекопитающих (например, точку SV40 часто используют только потому, что она также содержит ранний вирусный промотор).
[00210] Последовательность терминации транскрипции обычно расположена 3' к концу кодирующей полипептид области и служит для терминации транскрипции. Обычно последовательность терминации транскрипции в прокариотических клетках представляет собой G-C-богатый фрагмент, за которым следует последовательность поли-Т. Хотя последовательность легко клонировать из библиотеки или даже приобрести на коммерческом основании в качестве части вектора, ее также нетрудно синтезировать, используя способы для синтеза нуклеиновых кислот, такие как описанные в данном документе.
[00211] Ген селективного маркера кодирует белок, необходимый для выживания и роста клетки-хозяина в селективной культуральной среде. Типичные гены селективных маркеров кодируют белки, которые (а) придают устойчивость к антибиотикам или другим токсинам, например, ампициллину, тетрациклину или канамицину в случае прокариотических клеток-хозяев; (b) восполняют ауксотрофный дефицит в клетке; или (с) обеспечивают необходимые питательные вещества, недоступные из комплексной или определенной среды. Конкретными селективными маркерами являются ген устойчивости к канамицину, ген устойчивости к ампициллину, глутаминсинтетаза (GS) и ген устойчивости к тетрациклину. Предпочтительно можно также использовать ген устойчивости к неомицину для селекции как в прокариотических, так и в эукариотических клетках-хозяевах.
[00212] Для амплификации гена, предназначенного для экспрессии, можно использовать другие селективные гены. Амплификацией называется процесс, в котором гены, необходимые для выработки белка, критического для роста или выживания клетки, реитерируются в тандеме в хромосомах последующих поколений рекомбинантных клеток. Примеры подходящих селективных маркеров для клеток млекопитающих включают ген дигидрофолатредуктазы (DHFR) и беспромоторный ген тимидинкиназы. Трансформанты клеток млекопитающих помещают в условия селекционного давления, в которых только трансформанты однозначно способны к выживанию благодаря селективному гену, присутствующему в векторе. Селекционное давление создают путем культивирования трансформированных клеток в условиях, в которых последовательно увеличивается концентрация селекционного агента в среде, тем самым приводя к амплификации как селективного гена, так и ДНК, которая кодирует другой ген, такой как ген антитела, которое связывается с полипептидом фактора Bb или эпитопом фактора Bb. В результате из амплифицированной ДНК синтезируется повышенное количество полипептида, такого как антитело к фактору Bb.
[00213] Участок связывания рибосомы обычно необходим для инициации трансляции мРНК и характеризуется наличием последовательности Шайна-Дальгарно (прокариоты) или последовательности Козака (эукариоты). Этот элемент обычно расположен 3' к промотору и 5' к кодирующей последовательности предназначенного для экспрессии полипептида.
[00214] В некоторых случаях, например, когда в экспрессионной системе эукариотической клетки-хозяина необходимо гликозилирование, можно манипулировать с разными пре- или пропоследовательностями для улучшения состояния гликозилирования или выхода. Например, можно изменять участок расщепления пептидазами конкретного сигнального пептида или добавлять пропоследовательности, которые также могут влиять на гликозилирование. Конечный белковый продукт может содержать в позиции -1 (по отношению к первой аминокислоте зрелого белка) одну или более дополнительных аминокислот, связанных с экспрессией, которые могли быть не полностью удалены. Например, конечный белковый продукт может содержать один или более аминокислотных остатков, находящихся в участке расщепления пептидазами, присоединенных к амино-концу. В альтернативном варианте применение некоторых участков расщепления может приводить к слегка усеченной форме необходимого полипептида, если фермент делает надрез в такой области зрелого полипептида.
[00215] Экспрессионные и клонирующие векторы согласно изобретению, как правило, содержат промотор, который распознается органимом-хозяином и функционально связан с молекулой, кодирующей антитело к фактору Bb. Промоторы представляют собой нетранскрибируемые последовательности, расположенные выше (т.е. 5') стартового кодона структурного гена (в общем случае в пределах от около 100 до 1000 п.о.), которые регулируют транскрипцию структурного гена. Традиционно промоторы делят на два класса: индуцибельные промоторы и конститутивные промоторы. Индуцибельные промоторы инициируют повышенные уровни транскрипции из ДНК, находящейся под их управлением, в ответ на некоторые изменения в культуральных условиях, такие как присутствие или отсутствие питательных веществ или изменение температуры. С другой стороны конститутивные промоторы равномерно транскрибируют ген, с которым они функционально связаны, что означает слабую или отсутствующую регуляцию генной экспрессии. Хорошо известно большое число промоторов, распознаваемых различными потенциальными клетками-хозяевами. Подходящий промотор функционально связывают с ДНК, кодирующей тяжелую цепь или легкую цепь, принадлежащую антителу к фактору Bb согласно изобретению, при помощи удаления промотора из источника ДНК путем расщепления рестрикционными ферментами и вставки необходимой промоторной последовательности в вектор.
[00216] В некоторых вариантах реализации изобретения для получения раскрытых в данном документе антител к фактору Bb можно использовать дрожжевые клетки. Также в данной области техники хорошо известны промоторы, подходящие для применения с дрожжевыми хозяевами. Дрожжевые энхансеры предпочтительно используют с дрожжевыми промоторами. Подходящие промоторы для применения с клетками-хозяевами млекопитающих хорошо известны и включают, но не ограничиваются этим, полученные из геномов вирусов, таких как вирус полиомы, вирус оспы кур, аденовирус (такой как аденовирус 2), вирус папилломы крупного рогатого скота, вирус саркомы птиц, цитомегаловирус, ретровирусы, вирус гепатита В и, наиболее предпочтительно, вирус обезьян 40 (SV40). Другие подходящие промоторы млекопитающих включают гетерологичные промоторы млекопитающих, например, промоторы теплового шока и промотор актина.
[00217] Дополнительные промоторы, которые могут представлять интерес, включают, но не ограничиваются этим: ранний промотор SV40 (Benoist and Chambon, 1981, Nature 290: 304-310); промотор ЦМВ (Thornsen et al., 1984, Proc. Natl. Acad. U.S.A. 81: 659-663); промотор, содержащийся в 3' длинном концевом повторе вируса саркомы Рауса (Yamamoto et al., 1980, Cell 22: 787-797); промотор тимидинкиназы герпеса (Wagner et al., 1981, Proc. Natl. Acad. Sci. U.S.A. 78: 1444-1445); промотор и регуляторные последовательности из гена металлотионина (Prinster et al., 1982, Nature 296: 39-42); и прокариотические промоторы, такие как промотор бета-лактамазы (Villa-Kamaroff et al., 1978, Proc. Natl. Acad. Sci. U.S.A. 75: 3727-3731); или промотор tac (DeBoer et al., 1983, Proc. Natl Acad. Sci. U.S.A. 80: 21-25). Также интерес представляют следующие транскрипционные регуляторные области животных, которые демонстрируют тканевую специфичность и применялись в трансгенных животных: регуляторная область гена эластазы I, активная в панкреатических ацинарных клетках (Swift et al., 1984, Cell 38: 639-646; Ornitz et al., 1986, Cold Spring Harbor Symp. Quant. Biol. 50: 399-409; MacDonald, 1987, Hepatology 7: 425-515); регуляторная область гена инсулина, активная в панкреатических бета-клетках (Hanahan, 1985, Nature 315: 115-122); регуляторная область гена иммуноглобулина, активная в лимфоидных клетках (Grosschedl et al., 1984, Cell 38: 647-658; Adames et al., 1985, Nature 318: 533-538; Alexander et al., 1987, Mol. Cell. Biol. 7: 1436-1444); регуляторная область вируса опухоли молочной железы мышей, активная в клетках яичек, молочной железы, лимфоидных и тучных клетках (Leder et al., 1986, Cell 45: 485-495); регуляторная область гена альбумина, активная в печени (Pinkert et al., 1987, Genes and Devel. 1: 268-276); регуляторная область гена альфа-фетопротеина, активная в печени (Krumlauf et al., 1985, Mol. Cell. Biol. 5: 1639-1648; Hammer et al., 1987, Science 253: 53-58); регуляторная область гена альфа-1-антитрипсина, активная в печени (Kelsey et al., 1987, Genes and Devel 1: 161-171); регуляторная область гена бета-глобина, активная в миелоидных клетках (Mogram et al., 1985, Nature 315: 338-340; Kollias et al., 1986, Cell 46: 89-94); регуляторная область гена основного белка миелина, активная в клетках олигодендроцитов головного мозга (Readhead et al., 1987, Cell 48: 703-712); регуляторная область гена легкой цепи-2 миозина, активная в скелетных мышцах (Sani, 1985, Nature 314: 283-286); и регуляторная область гена гонадотропного рилизинг-гормона, активная в гипоталамусе (Mason et al., 1986, Science 234: 1372-1378).
[00218] Энхансерную последовательность можно вставлять в вектор для повышения транскрипции ДНК, кодирующей легкую цепь или тяжелую цепь, принадлежащую антителу к фактору Bb согласно изобретению, высшими эукариотами. Энхансеры представляют собой цис-действующие элементы ДНК, длиной обычно 10-300 п.о., которые воздействуют на промотор для повышения транскрипции. Энхансеры являются относительно ориентационно и позиционно независимыми и могут находиться в позициях как 5', так и 3' к транскрипционной единице. Известно несколько энхансерных последовательностей, доступных из генов млекопитающих (например, глобина, эластазы, альбумина, альфа-фетопротеина и инсулина). При этом, как правило, используют энхансеры из вирусов. Известные в данной области техники энхансер SV40, энхансер раннего промотора цитомегаловируса, энхансер полиомы и энхансер аденовируса представляют собой типовые энхансерные элементы для активации эукариотических промоторов. Хотя энхансер может находиться в векторе как 5', так и 3' к кодирующей последовательности, как правило, он расположен 5' от промотора. Для стимуляции внеклеточной секреции антитела в экспрессионный вектор может быть включена последовательность, кодирующая соответствующую нативную или гетерологичную последовательность (лидерную последовательность или сигнальный пептид). Выбор сигнального пептида или лидерной последовательности зависит от типа клеток-хозяев, в которых должно вырабатываться антитело, а гетерологичная сигнальная последовательность может заменить нативную сигнальную последовательность. Примеры сигнальных пептидов, которые функциональны в клетках-хозяевах млекопитающих, включают следующие: сигнальную последовательность интерлейкина-7 (IL-7), описанную в патенте США №4965195; сигнальную последовательность рецептора интерлейкина-2, описанную в Cosman et al., 1984, Nature 312: 768; сигнальный пептид рецептора интерлейкина-4, описанный в патенте ЕР №0367566; сигнальный пептид рецептора интерлейкина-1 типа I, описанный в патенте США №4968607; сигнальный пептид рецептора интерлейкина-1 типа II, описанный в патенте ЕР №0460846.
[00219] Экспрессионные векторы для экспрессии заявляемых антител согласно изобретению можно сконструировать из исходного вектора, такого как коммерчески доступный вектор. Такие векторы могут содержать или не содержать все необходимые фланкирующие последовательности. Если одна или более из описанных в данном документе фланкирующих последовательностей изначально не присутствует в векторе, их можно получить отдельно и лигировать в вектор. Способы, применяемые для получения каждой из фланкирующих последовательностей, хорошо известны специалисту в данной области техники.
[00220] После того, как вектор был сконструирован, а молекула нуклеиновой кислоты, кодирующая легкую цепь, тяжелую цепь или легкую цепь и тяжелую цепь, составляющие антигенсвязывающую последовательность для фактора Bb, были вставлены в соответствующий участок вектора, полный вектор можно вносить в подходящую клетку-хозяина для амплификации и/или экспрессии полипептида. Перенос экспрессионного вектора для антитела к фактору Bb в выбранную клетку-хозяина можно осуществлять хорошо известными способами, включая трансфекцию, инфицирование, совместное осаждение фосфатом кальция, электропорацию, микроинъекцию, липофекцию, опосредованную ДЭАЭ-декстраном трансфекцию или другие известные методы. Выбранный способ частично будет зависеть от применяемого типа клетки-хозяина. Эти способы и другие подходящие способы хорошо известны специалисту в данной области техники и приведены, например, в Sambrook et al., 2001, выше.
[00221] При культивировании в соответствующих условиях клетка-хозяин синтезирует антитело к фактору Bb, которое впоследствии можно собрать из культуральной среды (если клетка-хозяин секретирует в среду) или непосредственно из вырабатывающей его клетки-хозяина (если не секретирует). Выбор подходящей клетки-хозяина будет зависеть от различных факторов, таких как необходимые уровни экспрессии, полипептидные модификации, желательные или необходимые для активности (такие как гликозилирование или фосфорилирование) и легкость сворачивания в биологически активную молекулу. Клетка-хозяин может быть эукариотической или прокариотической.
[00222] Доступные в качестве хозяев клеточные линии млекопитающих хорошо известны в данной области техники и включают, но не ограничиваются этим, иммортализованные линии клеток, доступные от Американской коллекции типовых культур (АТСС), включая, но не ограничиваясь этим, клетки яичника китайского хомяка (СНО), клетки HeLa, клетки почки новорожденного хомяка (BHK), клетки почки обезьяны (COS), клетки гепатоцеллюлярной карциномы человека (например, Hep G2) и большое количество других клеточных линий. В определенных вариантах реализации изобретения клеточные линии можно выбирать, определяя, какие клеточные линии имеют высокие уровни экспрессии и конститутивно вырабатывают антитела со свойством связывания фактора Bb. В другом варианте реализации изобретения может быть выбрана клеточная линия из линии дифференцировки В-клеток, которая не вырабатывает свое антитело, но обладает способностью вырабатывать и секретировать гетерологичное антитело.
Применение антител к фактору Bb в диагностических и терапевтических целях
[00223] Антитела согласно изобретению применимы для выявления фактора Bb в биологических образцах и определения клеток или тканей, которые вырабатывают белок фактора Bb. Например, антитела к фактору Bb согласно изобретению можно применять в диагностических методах анализа, например, анализе связывания, для выявления и/или количественной оценки фактора Bb, экспрессируемого в ткани или клетке. Повышенные уровни фактора Bb могут указывать на наличие заболеваний, таких как нарушения зрения, рак, инфекция и/или язвенный колит. Пониженные уровни фактора Bb могут указывать на наличие цирроза, гломерулонефрита, наследственного ангионевротического отека, гепатита, отторжения трансплантата почки, волчаночного нефрита, неправильное питание и/или системную красную волчанку.
[00224] В некоторых вариантах реализации изобретения антитела согласно изобретению, которые специфически связываются с фактором Bb, можно применять в лечение опосредованных фактором Bb заболеваний у нуждающегося в этом пациента. Кроме того, антитело к фактору Bb согласно изобретению можно применять для ингибирования формирования фактором Bb комплекса с другими белками комплемента, тем самым модулируя биологическую активность фактора Bb в клетке или ткани. Антитела, которые связываются с фактором Bb, могут таким образом модулировать и/или блокировать взаимодействие с другими связывающими соединениями и, следовательно, могут иметь терапевтическое применение в облегчении опосредованных фактором Bb заболеваний.
[00225] В некоторых вариантах реализации изобретения антитела к фактору Bb могут блокировать протеазную активность фактора Bb. В некоторых случаях связывание фактора Bb антителами к фактору Bb может приводить к нарушению индуцированного фактором Bb каскада сигнальной трансдукции.
Диагностические способы
[00226] Антитела согласно изобретению можно применять в диагностических целях для выявления, диагностирования или мониторинга заболеваний и/или патологических состояний, связанных с фактором Bb или фактором В. В изобретении предложено выявление присутствия фактора Bb в образце при помощи классических иммуногистологических способов, известных специалистам в данной области техники (например, Tijssen, 1993, Practice and Theory of Enzyme Immunoassays, vol 15 (Eds R.H. Burdon and P.H. van Knippenberg, Elsevier, Amsterdam); Zola, 1987, Monoclonal Antibodies: A Manual of Techniques, pp. 147-158 (CRC Press, Inc.); Jalkanen et al., 1985, J. Cell. Biol. 101: 976-985; Jalkanen et al., 1987, J. Cell Biol. 105: 3087-3096). Выявление фактора Bb можно проводить in vivo или in vitro.
[00227] Предложенные в данном документе диагностические применения включают применение антител для выявления экспрессии фактора Bb и/или связывания с фактором Bb. Примеры способов, применяемых в выявлении присутствия фактора Bb, включают методы иммуноанализа, такие как ферментный иммуносорбентный анализ (ELISA) и радиоиммуноанализ (RIA).
[00228] Для диагностических применений антитело, как правило, может быть помечено выявляемой метящей группой. Подходящие метящие группы включают, но не ограничиваются этим, следующие: радиоизотопы или радионуклиды (например, 3Н, 14С, 15N, 35S, 90Y, 99Тс, 111In, 125I, 131I), флуоресцентные группы (например, ФИТЦ, родамин, люминофоры на основе комплексов лантанидов), ферментативные группы (например, пероксидаза хрена, β-галактозидаза, люцифераза, щелочная фосфатаза), хемилюминесцентные группы, биотинильные группы или предопределенные полипептидные эпитопы, распознаваемые вторичным репортером (например, парные последовательности лейциновых молний, участки связывания вторичных антител, металлсвязывающие домены, эпитопные метки). В некоторых вариантах реализации изобретения метящая группа сопряжена с антителом посредством спейсерных ножек различной длины для снижения потенциального стерического несоответствия. В данной области техники известны различные способы мечения белков, которые можно применять для осуществления настоящего изобретения.
[00229] В одном аспекте изобретения предложен способ определения клетки или клеток, которые экспрессируют фактор Bb. В конкретном варианте реализации изобретения антитело метят метящей группой и определяют связывания меченого антитела с фактором Bb. В другом конкретном варианте реализации изобретения связывание антитела с фактором Bb можно определять in vivo. В другом конкретном варианте реализации изобретения выделяют комплекс антитело/фактор Bb и проводят измерения при помощи известных в данной области техники методов. Смотрите, например, Harlow and Lane, 1988, Antibodies: A Laboratory Manual, New York: Cold Spring Harbor (ed. 1991 и периодические дополнения); John E. Coligan, ed., 1993, Current Protocols In Immunology New York: John Wiley & Sons.
[00230] В другом аспекте изобретения предложен способ определения присутствия тестовой молекулы, которая конкурирует с антителами согласно изобретению за связывание с фактором Bb. Пример такого анализа включает определение количества свободного антитела в растворе, содержащем некоторое количество фактора Bb, в присутствии или отсутствии тестовой молекулы. Повышение количества свободного антитела (т.е. антитела, не связанного с фактором Bb) указывает на то, что тестовая молекула способна конкурировать с антителом за связывание с фактором Bb. В одном варианте реализации изобретения антитело метят метящей группой. В альтернативном варианте метят тестовую молекулу и отслеживают количество свободной тестовой молекулы в присутствии или отсутствии антитела.
Показания
[00231] Было показано, что система комплемента связана с несколькими острыми и хроническими патологическими состояниями, включая атеросклероз, ишемию-реперфузию после острого инфаркта миокарда, нефрит при пурпуре Шенлейна-Геноха, геморрагический васкулит, ревматоидный артрит, артериит, аневризму, инсульт, кардиомиопатию, геморрагический шок, повреждение с размозжением тканей, полиорганную недостаточность, гиповолемический шок и кишечную ишемию, отторжение трансплантата, кардиохирургию, ЧКТА, самопроизвольный выкидыш, нейрональное повреждение, повреждение спинного мозга, миастению гравис, болезнь Хантингтона, амиотрофический боковой склероз, множественный склероз, синдром Гийена-Барре, болезнь Паркинсона, болезнь Альцгеймера, синдром острой дыхательной недостаточности, астму, хроническое обструктивное заболевание легких, острое посттрансфузионное повреждение легких, острое повреждение легких, болезнь Гудпасчера, инфаркт миокарда, воспаление после применения искусственного кровообращения, искусственное кровообращение, септический шок, отторжение трансплантата, ксенотрансплантацию, ожоговые повреждения, системную красную волчанку, мембранозный нефрит, болезнь Бергера, псориаз, пемфигоид, дерматомиозит, антифосфолипидный синдром, воспалительное заболевание кишечника, гемодиализ, лейкоферез, плазмаферез, гепарин-индуцированную экстракорпоральную преципитацию ЛПНП с мембранной оксигенацией, экстракорпоральную мембранную оксигенацию и макулярную дегенерацию.
[00232] Макулярные дегенеративные заболевания, такие как все стадии возрастной макулярной дегенерации (ВМД), включая сухую и влажную (неэкссудативную и экссудативную) формы, хориоидальную неоваскуляризацию (ХНВ), увеит, диабетические и другие связанные с ишемией ретинопатии, а также другие внутриглазные неоваскулярные заболевания, такие как диабетическая макулярная эдема, патологическая миопия, болезнь фон Гиппеля-Линдау, гистоплазмоз глаза, окклюзия центральной вены сетчатки (ОЦВС), разветвленная окклюзия вены сетчатки (РОВС), неоваскуляризация роговицы и неоваскуляризация сетчатки. Предпочтительная группа комплементассоциированных патологических состояний глаза включает возрастную макулярную дегенерацию (ВМД), включая неэкссудативную (влажную) и экссудативную (сухую или атрофическую) ВМД, хориоидальную неоваскуляризацию (ХНВ), диабетическую ретинопатию (ДР) и эндофтальмит.
[00233] Раскрытые в настоящем изобретении антитела против фактора Bb можно применять в комбинации с одним или более цитокинами, лимфокинами, гемопоэтическими факторами и/или противовоспалительными агентами.
[00234] Лечение перечисленных в данном документе заболеваний и нарушений может включать применение лекарственных препаратов первой линии для контроля боли и воспаления в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с лечением одним или более из предложенных в данном документе антител. Эти лекарственные препараты классифицируются как нестероидные противовоспалительные препараты (NSAID). Вторичное лечение включает кортикостероиды, медленно действующие противоревматические препараты (SAARD) или препараты, модифицирующие течение заболевания (DM). Информацию по следующим соединениям можно найти в The Merck Manual of Diagnosis and Therapy, Sixteenth Edition, Merck, Sharp & Dohme Research Laboratories, Merck & Co., Rahway, N.J. (1992) and in Pharmaprojects, PJB Publications Ltd.
[00235] В конкретном варианте реализации настоящее изобретение относится к применению антитела и любого одного или более NSAID для лечения перечисленных в данном документе заболеваний и нарушений. Противовоспалительное действие NSAID связано, по меньшей мере частично, с ингибированием синтеза простагландина (Goodman and Gilman в "The Pharmacological Basis of Therapeutics," MacMillan 7th Edition (1985)). NSAID можно разделить на следующие девять групп: (1) производные салициловой кислоты; (2) производные пропионовой кислоты; (3) производные уксусной кислоты; (4) производные фенаминовой кислоты; (5) производные карбоновой кислоты; (6) производные масляной кислоты; (7) оксикамы; (8) пиразолы и (9) пиразолоны.
[00236] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более производными салициловой кислоты, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Такие производные салициловой кислоты, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: ацетаминосалол, алоксиприн, аспирин, бенорилат, бромосалигенин, кальция ацетилсалицилат, холин-магний трисалицилат, магния салицилат, холина салицилат, дифлунизал, этерсалат, фендозал, гентизиновая кислота, гликольсалицилат, имидазолсалицилат, лизинацетилсалицилат, мезаламин, морфолинсалицилат, 1-нафтил салицилат, парсалмид, парсалмид, фенилацетилсалицилат, фенилсалицилат, салацетамид, салициламин, О-уксусную кислоту, салсалат, натрия салицилат и сульфасалазин. Структурно родственные производные салициловой кислоты, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00237] В дополнительным конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более производными пропионовой кислоты, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Производные пропионовой кислоты, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: алминопрофен, беноксапрофен, буклоксовую кислоту, капрофен, дексиндопрофен, фенопрофен, флуноксапрофен, флупрофен, флурбипрофен, фурклопрофен, ибупрофен, ибупрофен-алюминий, ибупроксам, индопрофен, кетопрофен, локсопрофен, миропрофен, напроксен, напроксен-натрий, оксапрозин, пикетопрофен, пимепрофен, пирпрофен, пранопрофен, протициновую кислоту, пиридоксипрофен, супрофен, тиапрофеновую кислоту и тиоксапрофен. Структурно родственные производные пропионовой кислоты, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00238] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более производными уксусной кислоты, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Производные уксусной кислоты, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: ацеметацин, аклофенак, амфенак, буфексамак, цинметацин, клопирак, делметацин, диклофенак кальция, диклофенак натрия, этодолак, фелбинак, фенклофенак, фенклорак, фенклозовую кислоту, фентиазак, фурофенак, глюкаметацин, ибуфенак, индометацин, изофезолак, изоксепак, лоназолак, метиациновую кислоту, оксаметацин, окспинак, пиметацин, проглуметацин, сулиндак, талметацин, тиарамид, тиопинак, толметин, толметин натрия, зидометацин и зомепирак. Структурно родственные производные уксусной кислоты, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00239] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более производными фенаминовой кислоты, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Производные фенаминовой кислоты, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: энфенаминовую кислоту, этофенамат, флуфенаминовую кислоту, изонексин, меклофенаминовую кислоту, меклофенамат натрия, медофенаминовую кислоту, мефенаминовую кислоту, нифлумовую кислоту, талнифлумат, терофенамат, толфенаминовую кислоту и уфенамат. Структурно родственные производные фенаминовой кислоты, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00240] В дополнительном конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более производными карбоновой кислоты, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Производные карбоновой кислоты, их пролекарственные сложные эфиры или фармацевтически приемлемые соли, которые можно использовать, включают: клиданак, дифлунизал, флуфенизал, иноридин, кеторолак и тиноридин. Структурно родственные производные карбоновой кислоты, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00241] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более производными масляной кислоты, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Производные масляной кислоты, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: бумадизон, бутибуфен, фенбуфен и ксенбуцин. Структурно родственные производные масляной кислоты, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00242] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более оксикамами, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Оксикамы, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: дроксикам, эноликам, изоксикам, пироксикам, судоксикам, теноксикам и 4-гидроксил-1,2-бензотиазин-1,1-диоксид-4-(N-фенил)-карбоксамид. Структурно родственные оксикамы, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00243] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более пиразолами, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Пиразолы, их пролекарственные сложные эфиры или фармацевтически приемлемые соли, которые можно использовать, включают: дифенамизол и эпиризол. Структурно родственные пиразолы, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00244] В дополнительном конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более пиразолонами, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями. Пиразолоны, их пролекарственные сложные эфиры или фармацевтически приемлемые соли, которые можно использовать, включают: апазон, азапропазон, бензпиперилон, фепразон, мофебутазон, моразон, оксифенбутазон, фенилбутазон, пипебузон, пропилфеназон, рамифеназон, суксибузон и тиазолинобутазон. Структурно родственные пиразолоны, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00245] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более из следующих NSAID: ε-ацетамидокапроновой кислотой, S-аденозилметионином, 3-амино-4-гидроксимасляной кислотой, амиксетрином, анитразафеном, антрафенином, бендазаком, бендазак лизинатом, бензидамином, бепрозином, броперамолом, буколомом, буфезолаком, ципроквазоном, клоксиматом, дазидамином, дебоксаметом, детомидином, дифенпайрамидом, дифенпирамидом, дифисаламином, дитазолом, эморфазоном, фанетилизолом, месилатом, фенфлумизолом, флоктафенином, флумизолом, флуниксином, флупроквазоном, фопиртолином, фосфозалом, гваймезалом, гвайзоленом, изониксирном, лефетамином, HCl, лефлуномидом, лофемизолом, лотифазолом, лизин клониксинатом, мезеклазоном, набуметоном, никтиндолом, нимесулидом, орготеином, опраноксином, оксацепролом, оксападолом, паранилином, перизоксалем, перизоксаль цитратом, пифоксимом, пипроксеном, пиразолаком, пирфенидоном, проквазоном, проксазолом, тиелавином В, тифламизолом, тимегадином, толектином, толпадолом, триптамидом и препаратами, обозначаемые фирменным кодом 480156S, АА861, AD1590, AFP802, AFP860, AI77B, АР504, AU8001, ВРРС, BW540C, CHINOIN 127, CN100, ЕВ382, EL508, F1044, FK-506, GV3658, ITF182, KCNTEI6090, KME4, LA2851, MR714, MR897, MY309, ONO3144, PR823, PV102, PV108, R830, RS2131, SCR152, SH440, SIR133, SPAS510, SQ27239, ST281, SY6001, ТА60, TAI-901 (4-бензоил-1-инданкарбоновая кислота), TVX2706, U60257, UR2301 и WY41770. Структурно родственные NSAID, имеющие сходные анальгезирующие и противовоспалительные свойства с NSAID, также входят в эту группу.
[00246] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более кортикостероидами, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями для лечения перечисленных в данном документе заболеваний и нарушений, включая острые и хронические воспаления, такие как ревматические заболевания, болезнь «трансплантат против хозяина» и множественный склероз. Кортикостероиды, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают гидрокортизон и соединения, полученные из гидрокортизона, такие как 21-ацетоксипрегненолон, алкломеразон, альгестон, амцинонид, беклометазон, бетаметазон, бетаметазон валерат, буденизонид, хлорпреднизон, клобетазол, клобетазол пропионат, клобетазон, клобетазон бутират, клокортоколон, клопреднол, кортикостерон, кортизон, кортивазол, дефлазакон, дезонид, дезоксимеразон, дексаметазон, дифлоразон, дифлукортолон, дифлупреднат, эноксолон, флуазакорт, флуклоронид, флуметазон, флуметазон пивалат, флуцинолон ацетонид, флунизолид, флуоцинонид, флуороцинолон ацетонид, флуорокортин бутил, флуорокортолон, флуорокортолон гексаноат, дифлукортолон валерат, флуорометолон, флуперолон ацетат, флупредниден ацетат, флупреднизолон, флуранденолид, формокортал, гальцинонид, галометазон, галопредон ацетат, гидрокортамат, гидрокортизон, гидрокортизон ацетат, гидрокортизон бутират, гидрокортизон фосфат, гидрокортизон 21-натрий сукцинат, гидрокортизон тебутат, мазипредон, медризон, мепреднизон, метилпредниколон, мометазон фуроат, параметазон, предникарбат, преднизолон, преднизолон 21-диэдриаминоацетат, преднизолон натрий фосфат, преднизолон натрий сукцинат, преднизолон натрий 21-m-сульфобензоат, преднизолон натрий 21-стеарогликолат, преднизолон тебутат, преднизолон 21-триметилацетат, преднизон, преднивал, преднилиден, преднилиден 21-диэтиламиноацетат, тиксокортол, триамцинолон, триамцинолон ацетонид, триамцинолон бенетонид и триамцинолон гексацетонид. Структурно родственные кортикостероиды, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00247] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более медленнодействующими противоревматическими препаратами (SAARD) или модифицирующими заболевание противоревматическими препаратами (DMARD), их пролекарственными сложными эфирами или фармацевтически приемлемыми солями для лечения перечисленных в данном документе заболеваний и нарушений, включая острые и хронические воспаления, такие как ревматические заболевания, болезнь «трансплантат против хозяина» и множественный склероз. SAARD или DMARD, их пролекарственные сложные эфиры или фармацевтически приемлемые соли включают: аллокупреид натрия, ауранофин, ауротиоглюкозу, ауротиоглюканид, азатиоприн, бреквинар натрия, буцилламин, кальций 3-ауротио-2-пропанол-1-сульфонат, хлорамбуцил, хлороквин, клобузарит, купроксолин, циклофосфамид, циклоспорин, дапзон, 15-дезоксиспергуалин, диацереин, глюкозамин, соли золота (например, золотая соль циклоквина, золотая соль тиомалата, золотая соль тиосульфата), гидроксихлороквин, гидроксихлороквин сульфат, гидроксимочевина, кебузон, левамизол, лобензарит, меллитин, 6-меркаптопурин, метотрексат, мизорибин, микофенолат мофетил, майорал, азотистый иприт, D-пенницилламин, такие имидазолы пиридинола, как SKNF86002 и SB203580, рапамицин, тиолы, тимопоэтин и винкристин. Структурно родственные SAARD или DMARD, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу.
[00248] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более ингибиторами СОХ2, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями для лечения перечисленных в данном документе заболеваний и нарушений, включая острые и хронические воспаления. Примеры ингибиторов СОХ2, их пролекарственных сложных эфиров или фармацевтически приемлемых солей включают, например, целекоксиб. Структурно родственные ингибиторы СОХ2, имеющие сходные анальгезирующие и противовоспалительные свойства, также входят в эту группу. Примеры селективных ингибиторов СОХ-2 включают, но не ограничиваются этим, эторикоксиб, вальдекоксиб, целекоксиб, ликофелон, люмиракоксиб, рофекоксиб и тому подобные.
[00249] В другом конкретном варианте реализации настоящее изобретение относится к применению антитела в комбинации (предварительное лечение, последующее лечение или одновременное лечение) с любым одним или более противомикробными препаратами, их пролекарственными сложными эфирами или фармацевтически приемлемыми солями для лечения перечисленных в данном документе заболеваний и нарушений, включая острые и хронические воспаления. Противомикробные препараты включают, например, широкий класс пенициллинов, цефалоспоринов и других бета-лактамов, аминогликозидов, азолов, квинолонов, макролидов, рифамицинов, тетрациклинов, сульфонамидов, линкозамидов и полимиксинов. Пенициллины включают, но не ограничиваются этим, пенициллин G, пенициллин V, метициллин, нафциллин, оксациллин, клоксациллин, диклоксациллин, флоксациллин, ампициллин, ампициллин/сульбактам, амоксициллин, амоксициллин/клавуланат, гетациллин, циклациллин, вакампициллин, карбенициллин, карбенициллин инданил, тикарциллин, тикарциллин/клавуланат, азлоциллин, мезлоциллин, пеперациллин и мециллинам. Цефалоспорины и другие бета-лактамы включают, но не ограничиваются этим, цефалотин, цефапирин, цефалексин, цефрадин, цефазолин, цефадроксил, цефаклор, цефамандол, цефотетан, цефокситин, церуроксим, цефоницид, цефорадин, цефиксим, цефотаксим, моксалактам, цефтизоксим, цетриаксон, цефоперазон, цефтазидим, имипенем и азтреонам. Аминогликозиды включают, но не ограничиваются этим, стрептомицин, гентамицин, тобрамицин, амикацин, нетилмицин, канамицин и неомицин. Азолы включают, но не ограничиваются этим, флуконазол. Квинолоны включают, но не ограничиваются этим, налидиксовую кислоту, норфлоксацин, эноксацин, ципрофлоксацин, офлоксацин, спарфлоксацин и темафлоксацин. Макролиды включают, но не ограничиваются этим, эритомицин, спирамицин и азитромицин. Рифамицины включают, но не ограничиваются этим, рифампин. Тетрациклины включают, но не ограничиваются этим, спициклин, хлортетрациклин, кломоциклин, демеклоциклин, дезоксициклин, гуамециклин, лимециклин, меклоциклин, метациклин, миноциклин, окситетрациклин, пенимепициклин, пипациклин, ролитетрациклин, санциклин, сеноциклин и тетрациклин. Сульфонамиды включают, но не ограничиваются этим, сульфаниламид, сульфаметоксазол, сульфацетамид, сульфадиазин, сульфисоксазол и ко-тримоксазол (триметоприм/сульфаметоксазол). Линкозамиды включают, но не ограничиваются этим, клиндамицин и линкомицин. Полимиксины (полипептиды) включают, но не ограничиваются этим, полимиксин В и колистин.
Способы лечения Фармацевтические препараты, пути введения
[00250] Раскрыты композиции, содержащие терапевтически эффективное количество одного или множества антител согласно изобретению вместе с фармацевтически приемлемым разбавителем, носителем, солюбилизатором, эмульсификатором, консервантом и/или адъювантом. Кроме того, в изобретении предложены способы лечения пациента путем введения такой фармацевтической композиции. Пациент может быть как субъектом-человеком, так и субъектом-животным.
[00251] Фармацевтические композиции, содержащие одно или более антител, можно применять для снижения активности фактора Bb. Фармацевтические композиции, содержащие одно или более антител, можно применять для лечения последствий, симптомов и/или патологий, связанных с активностью фактора Bb. Фармацевтические композиции, содержащие одно или более антител, можно применять в способах ингибирования пути комплемента и/или связывания фактора Bb с другими белками комплемента. В определенных вариантах реализации изобретения антитело ингибирует протеазную активность фактора Bb. В дополнительных вариантах реализации изобретения фармацевтические композиции, содержащие одно или более антител, можно применять в способах ингибирования протеазной активности фактора Bb. Фармацевтические композиции, содержащие одно или более антител, можно применять в способах лечения последствий, симптомов и/или патологий, связанных с активностью фактора Bb. Фармацевтические композиции, содержащие одно или более антител, можно применять в способах ингибирования выработки МАК. Фармацевтические композиции, содержащие одно или более антител, можно применять в способах ингибирования макулярной дегенерации.
[00252] Предпочтительно приемлемые материалы для препаратов являются нетоксичными для реципиентов в применяемых дозировках и концентрациях. В конкретных вариантах реализации изобретения предложены фармацевтические композиции, содержащие эффективное количество антител к фактору Bb.
[00253] В определенных вариантах реализации изобретения приемлемые материалы для препаратов являются нетоксичными для реципиентов в применяемых дозировках и концентрациях. В определенных вариантах реализации изобретения фармацевтическая композиция может содержать материалы для препаратов для модификации, поддержания или сохранения, например, рН, осмолярности, вязкости, прозрачности, цвета, изотоничности, запаха, стерильности, стабильности, скорости растворения или высвобождения, всасывания или проникновения композиции. В таких вариантах реализации изобретения подходящие материалы для препаратов включают, но не ограничиваются этим, аминокислоты (такие как глицин, глутамин, аспарагин, аргинин или лизин); противомикробные препараты; антиоксиданты (такие как аскорбиновая кислота, сульфит натрия или гидросульфит натрия); буферы (такие как борат, бикарбонат, Трис-HCl, цитраты, фосфаты или другие органические кислоты); объемообразующие агенты (такие как маннит или глицин); хелатирующие агенты (такие как этилендиаминтетрауксусная кислота (ЭДТУ)); комплексообразующие агенты (такие как кофеин, поливинилпирролидон, бета-циклодекстрин или гидроксипропил-бета-циклодекстрин); наполнители; моносахариды; дисахариды; и другие углеводы (такие как глюкоза, манноза или декстрины); белки (такие как сывороточный альбумин, желатин или иммуноглобулины); красители, ароматизаторы и разбавители; эмульсифицирующие агенты; гидрофильные полимеры (такие как поливинилпирролидон); низкомолекулярные полипептиды; солеобразующие противоионы (такие как натрий); консерванты (такие как бензалконий хлорид, бензойная кислота, салициловая кислота, тимеросал, фенетиловый спирт, метилпарабен, пропилпарабен, хлоргексидин, сорбиновая кислота или перекись водорода); растворители (такие как глицерин, пропиленгликоль или полиэтиленгликоль); сахарные спирты (такие как маннит или сорбит); суспендирующие агенты; сурфактанты или смачивающие агенты (такие как плюроники, ПЭГ, сложный эфир сорбитана, полисорбаты, такие как полисорбат 20, полисорбат, тритон, трометамин, лецитин, холестерин, тилоксапал); агенты, повышающие стабильность (такие как сахароза или сорбит); агенты, повышающие тоничность (такие как галиды щелочных металлов, предпочтительно хлорид натрия или калия, маннит, сорбит); средства для доставки; разбавители; вспомогательные вещества и/или фармацевтические адъюванты. Смотрите, REMINGTON'S PHARMACEUTICAL SCIENCES, 18th Edition, (A.R. Genrmo, ed.), 1990, Mack Publishing Company.
[00254] В определенных вариантах реализации изобретения оптимальную фармацевтическую композицию определяет специалист в данной области техники в зависимости, например, от способа введения, формата доставки и необходимой дозировки. Смотрите, например, REMINGTON'S PHARMACEUTICAL SCIENCES, выше. В определенных вариантах реализации изобретения такие композиции могут влиять на физическое состояние, стабильность, скорость in vivo высвобождения и скорость in vivo выведения антител согласно изобретению. В определенных вариантах реализации изобретения базовый раствор или носитель в фармацевтической композиции может быть как водным, так и неводным по природе. Например, подходящим базовым раствором или носителем может быть вода для инъекций, физиологический солевой раствор или искусственная цереброспинальная жидкость, возможно, дополненные другими материалами, обычными в композициях для парентерального введения. Дополнительными типовыми базовыми растворами являются забуференный солевой раствор или солевой раствор, смешанный с сывороточным альбумином. В конкретных вариантах реализации изобретения фармацевтические композиции содержат Трис-буфер с рН около 7,0-8,5 или ацетатный буфер с рН около 4,0-5,5, и могут дополнительно содержать сорбит или его подходящий заместитель. В определенных вариантах реализации изобретения композиции, содержащие антитело к фактору Bb, можно подготовить к хранению путем смешивания выбранной композиции, имеющей необходимую степень очистки, с необязательными агентами (REMINGTON'S PHARMACEUTICAL SCIENCES, выше) в форме лиофилизированной таблетки или водного раствора. Кроме того, в определенных вариантах реализации изобретения продукт антитела к фактору Bb можно получать в виде лиофилизата, используя соответствующие вспомогательные вещества, такие как сахароза.
[00255] Фармацевтические композиции согласно изобретению могут быть предназначены для парентеральной доставки. В альтернативном варианте композиции могут быть предназначены для ингаляции или для доставки через пищеварительный тракт, например, пероральной. Приготовление таких фармацевтически приемлемых композиций находится в компетенции данной области техники.
[00256] Компоненты препарата предпочтительно присутствуют в концентрациях, которые являются приемлемыми с учетом места введения. В определенных вариантах реализации изобретения для поддержания композиции при физиологическом уровне рН или немного меньшем рН, как правило, в диапазоне рН от около 5 до около 8, используют буферы.
[00257] Если предусмотрено парентеральное введение, терапевтические композиции для применения в данном изобретении могут находиться в форме апирогенного, парентерально приемлемого водного раствора, содержащего необходимое антитело к фактору Bb в фармацевтически приемлемом базовом растворе. В особенности подходящим базовым раствором для парентеральной инъекции является стерильная дистиллированная вода, в которую добавлено антитело к фактору Bb, в виде стерильного, изотонического раствора с надлежащим консервантом. В определенных вариантах реализации изобретения приготовление может включать смешивание необходимой молекулы с агентом, таким как инъецируемые микросферы, биоразлагаемые частицы, полимерные соединения (такие как полимолочная кислота или полигликолиевая кислота), гранулы или липосомы, которые могут обеспечивать контролируемое или пролонгированное высвобождение продукта, который может быть доставлен посредством депо-инъекции. В определенных вариантах реализации изобретения также можно использовать гиалуроновую кислоту, которая способствует продлению периода циркуляции. В определенных вариантах реализации изобретения можно использовать имплантируемые устройства для доставки лекарственных препаратов для внесения необходимого антитела.
[00258] Фармацевтические композиции согласно изобретению могут быть получены для ингаляции. В этих вариантах реализации изобретения антитела к фактору Bb предпочтительно приготовлены в виде сухого, вдыхаемого порошка. В конкретных вариантах реализации изобретения ингаляционные растворы, содержащие фактор Bb, также могут быть приготовлены с пропеллентом для аэрозольной доставки. В определенных вариантах реализации изобретения растворы можно распылять. Ингаляционное введение и способы получения препаратов для него дополнительно описаны в Международной патентной заявке № PCT/US94/001875, которая включена посредством ссылки и описывает ингаляционную доставку химически модифицированных белков. Также предусматривается, что препараты можно вводить перорально. Антитела к фактору Bb, которые вводят таким образом, можно готовить с или без носителей, обычно применяемых в составлении твердых дозировочных форм, таких как таблетки и капсулы. В определенных вариантах реализации изобретения капсула может быть приготовлена так, чтобы обеспечивать высвобождение активной части препарата в точке желудочно-кишечного тракта с максимальной биодоступностью и минимальной пресистемной деградацией. Для облегчения всасывания антитела к фактору Bb могут быть включены дополнительные агенты. Также можно применять разбавители, ароматизаторы, тугоплавкие воски, растительные масла, лубриканты, суспендирующие агенты, вещества для улучшения распадаемости таблеток и связующие вещества.
[00259] Фармацевтические композиции согласно изобретению предпочтительно содержит эффективное количество одного или нескольких антител к фактору Bb в смеси с нетоксичными вспомогательными веществами, которые подходят для производства таблеток. Растворяя таблетки в стерильной воде или другом подходящем базовом растворе, можно получить раствор в форме единичной дозы. Подходящие вспомогательные вещества включают, но не ограничиваются этим, инертные разбавители, такие как карбонат кальция, карбонат натрия или бикарбонат, лактоза или фосфат кальция; или связующие агенты, такие как крахмал, желатин или аравийская камедь; или лубриканты, такие как стеарат магния, стеариновая кислота или тальк.
[00260] Существование дополнительных фармацевтических композиций очевидно для специалистов в данной области техники, включая препараты антител к фактору Bb с пролонгированной или контролируемой доставкой. Способы приготовления различных других средств с пролонгированной или контролируемой доставкой, таких как липосомные носители, биоразлагаемые микрочастицы или пористые гранулы и депо-инъекции, также известны специалистам в данной области техники. Смотрите, например, Международную патентную заявке № PCT/US93/00829, которая включена посредством ссылки и описывает контролируемое высвобождение пористых полимерных микрочастиц для доставки фармацевтических композиций. Препараты с пролонгированным высвобождением могут включать полупроницаемые полимерные матрицы в виде формованных изделий, например, пленок или микрокапсул. Матрицы для пролонгированного высвобождения могут включать полиэфиры, гидрогели, полилактиды (как раскрыто в патенте США №3773919 и опубликованной заявке на Европейский патент № ЕР 058481, которые включены посредством ссылки), сополимеры L-глутаминовой кислоты и гамма этил-L-глутамата (Sidman et al., 1983, Biopolymers 2: 547-556), поли(2-гидроксиэтил-инетакрилат) (Langer et al., 1981, J. Biomed. Mater. Res. 15: 167-277 и Langer, 1982, Chem. Tech. 12: 98-105), этиленвинилацетат (Langer et al., 1981, выше) или поли-D(-)-3-гидроксимасляную кислоту (опубликованная заявка на Европейский патент № ЕР 133988). Композиции с пролонгированным высвобождением также могут включать липосомы, которые можно изготовить любым из нескольких известных в данной области техники способов. Смотрите, например, Eppstein et al., 1985, Proc. Natl. Acad. Sci. U.S.A. 82: 3688-3692; опубликованные заявки на Европейский патент № ЕР 036676; ЕР 088046 и ЕР 143949, включенные посредством ссылки.
[00261] Фармацевтические композиции, применяемые для in vivo введения, как правило, предоставлены в виде стерильных препаратов. Стерилизацию можно осуществлять путем фильтрации через стерильные фильтровальные мембраны. Если композиция лиофилизирована, стерилизацию можно проводить как до, так и после лиофилизации и восстановления. Композиции для парентерального введения можно хранить в лиофилизированной форме или в растворе. Парентеральные композиции в общем случае помещают в емкость со стерильным входным отверстием, например, пакет для внутривенных растворов или флакон с пробкой, прокалываемой гиподермической иглой для инъекций.
[00262] После приготовления фармацевтической композиции ее можно хранить в стерильных флаконах в виде раствора, суспензии, геля, эмульсии, твердого препарата, кристалла или в виде обезвоженного или лиофилизированного порошка. Такие препараты можно хранить как в готовой для использования форме, так и в форме (например, лиофилизированные), которую восстанавливают перед введением. Также в изобретении предложены наборы для получения единичной дозы для введения. Наборы согласно изобретению могут каждый содержать первый контейнер, содержащий сухой белок, и второй контейнер, содержащий водный раствор. В определенных вариантах реализации данного изобретения также предложены наборы, содержащие одно- и многокамерные предварительно наполненные шприцы (например, шприцы с жидкостью и шприцы с лиофилизатом).
[00263] Применяемое терапевтически эффективное количество содержащей антитело к фактору Bb фармацевтической композиции зависит, например, от терапевтического контекста и обстоятельств. Специалисту в данной области техники понятно, что подходящие для лечения дозировочные уровни будут варьироваться в зависимости, частично, от доставляемой молекулы, показаний, по которым применяется антитело к фактору Bb, пути введения, а также размеров (массы тела, площади поверхности тела или размеров органов) и/или состояния (возраста и общего состояния здоровья) пациента. В определенных вариантах реализации изобретения лечащий врач может титровать дозировку и модифицировать путь введения для достижения оптимального терапевтического эффекта. Типичная дозировка может соответствовать диапазону от около 0,1 мкг/кг до около 30 мг/кг или более в зависимости от вышеуказанных факторов. В конкретных вариантах реализации изобретения дозировка может соответствовать диапазону от 0,1 мкг/кг до около 30 мг/кг, необязательно, от 1 мкг/кг до около 30 мг/кг или от 10 мкг/кг до около 5 мг/кг.
[00264] Дозирование часто зависит от фармакокинетических параметров конкретного используемого в препарате антитела к фактору Bb. Как правило, лечащий врач вводит композицию до достижения такой дозировки, при которой достигается необходимый эффект. Следовательно, композицию можно вводить в виде одной дозы или в виде двух или более доз (которые могут содержать или могут не содержать одинаковое количество необходимой молекулы) в течение времени или в виде длительной инфузии посредством имплантированного устройства или катетера. Дополнительная корректировка подходящей дозировки обычно проводится специалистами в данной области техники и соответствует диапазону осуществляемых ими задач. Подходящие дозировки можно уточнять путем применения соответствующих данных доза-ответ. В определенных вариантах реализации изобретения антитела согласно изобретению можно вводить пациентам в течение продолжительного периода времени. Постоянное введение антитела согласно изобретению минимизирует нежелательные иммунные или аллергические ответы, обычно связанные с антителами, которые являются не полностью человеческими, например, антителом, полученным против человеческого антигена в организме отличного от человека животного, например, не полностью человеческим антителом или нечеловеческим антителом, полученным в организме отличного от человека вида.
[00265] Путь введения фармацевтической композиции соответствует известным способам, например, пероральный, посредством внутривенной инъекции, внутрибрюшинный, внутрицеребральный (интрапаренхиматозный), интрацеребровентрикулярный, внутримышечный, внутриглазной, интравитреальный, субретинальный, внутриартериальный, интрапортальный или внутриочаговый пути; при помощи систем для пролонгированного высвобождения или имплантируемого устройства. В определенных вариантах реализации изобретения композиции можно вводить путем болюсной инъекции или продолжительно путем инфузии или при помощи имплантируемого устройства.
[00266] Также композицию можно вводить местно посредством имплантации мембраны, губки или другого подходящего материала, в котором абсорбирована или инкапсулирована необходимая молекула. В определенных вариантах реализации изобретения, в которых применяют имплантируемое устройство, указанное устройство может быть имплантировано в любую подходящую ткань или орган, а доставка необходимой молекулы может происходить посредством диффузии, болюса с длительным высвобождением или постоянного введения. В случае глазных имплантатов, имплантат можно имплантировать при помощи внутриглазной инъекции, интравитреальной инъекции, субретинальной инъекции, супрахориоидальной инъекции, ретробульбарной инъекции или инъекции в субтеноновое пространство.
[00267] Также может возникать необходимость в применении фармацевтических композиций, содержащих антитело к фактору Bb согласно изобретению, ex vivo. В таких случаях клетки, ткани или органы, которые были удалены из организма пациента, обрабатывают фармацевтическими композициями, содержащими антитело к фактору Bb, после чего клетки, ткани и/или органы имплантируют обратно пациенту.
[00268] В частности, антитела к фактору Bb можно доставлять путем имплантации определенных клеток, которые были генетически сконструированы при помощи способов, таких как те, что описаны в данном документе, для экспрессии и секреции антитела к фактору Bb. В определенных вариантах реализации изобретения такие клетки могут быть клетками животного или человека и могут быть аутологичными, гетерологичными или ксеногенными. В определенных вариантах реализации изобретения клетки могут быть иммортализованными. В других вариантах реализации изобретения с целью снижения вероятности иммунологического ответа клетки могут быть инкапсулированы, чтобы избежать инфильтрации окружающих тканей. В дополнительных вариантах реализации изобретения материалы для инкапсуляции, как правило, являются биосовместимыми, полупроницаемыми полимерными капсулами или мембранами, которые допускают высвобождение белковых продуктов, но предотвращают разрушение клеток иммунной системой пациента или другими вредоносными факторами из окружающих тканей.
[00269] Все перечисленные в тексте данного описания ссылки явным образом и в полном объеме включены в данный документ посредством ссылки.
ПРИМЕРЫ
[00270] Нижеприведенные примеры, включая проведенные эксперименты и полученные результаты, приведены исключительно в иллюстративных целях и не ограничивают данное изобретение.
Пример 1 - Анализ связывания антитела против фактора Bb в сравнении с антителом против фактора В
[00271] Для определения кинетики связывания фактора Bb (CompTech®) и человеческого антигена фактора В (CompTech®) с моноклональным антителом против фактора Bb использовали метод биослойной интерферометрии (BLI) без применения меток. Измерения аффинности проводили при помощи Octet QKe, оборудованного биосенсорными наконечниками для захвата с античеловеческим IgG Fc (АНС) ( ®, Menlo Park, CA, USA). Анализ проводили при 30°С в 1х буфере ФСБ (Gibco®, ФСБ, рН 7,2). Образцы перемешивали при 1000 об/мин. Перед проведением анализа сенсоры увлажняли в течение 15 минут.
®, Menlo Park, CA, USA). Анализ проводили при 30°С в 1х буфере ФСБ (Gibco®, ФСБ, рН 7,2). Образцы перемешивали при 1000 об/мин. Перед проведением анализа сенсоры увлажняли в течение 15 минут.
[00272] Очищенное антитело против фактора Bb исследовали в отношении его связывающей способности с сенсорными наконечниками АНС. Наконечники загружали, используя 20 мкг/мл антитела против фактора Bb. Загрузка продолжалась 300 с до достижения уровня захвата между 1,8 и 2 нм. Антигены фактора Bb или фактора В готовили для анализа связывания путем разведения до концентрации 50 нМ в 1х ФСБ. Инициировали ассоциацию и отслеживали в течение 200 с, после чего наконечники переносили в 1х ФСБ-буфер без белка фактора (Gibco, ФСБ, рН 7,2), чтобы отследить диссоциацию. Сенсорные данные получали на протяжении экспериментов, обрабатывали и анализировали при помощи программного обеспечения для анализа данных Octet 7 (Forte Bio).
[00273] Избирательность антитела против фактора Bb исследовали сначала путем сравнения скорости ассоциации при связывании для белков фактора Bb и фактора В. Этот анализ проводили при помощи системы Octet QKe от Forte Bio®. Связывание, измеренное в течение 200 с в 50 нМ белковых препаратах, указывает на то, что антитело против фактора Bb специфически связывается с фактором Bb, а связывание с фактором В существенно ниже (Фигура 1).
Пример 2 - Функциональный анализ моноклонального антитела против фактора Bb
[00274] Анализ гемолиза - Активация альтернативного пути (АП) требует более высоких концентраций сыворотки, чем в случае классического пути. В общем случае для анализа используют конечную концентрацию, составляющую 5 мМ Mg++ в присутствии 5 мМ ЭДТУ, при этом ЭДТУ преимущественно хелатирует Са++. АП у большинства видов млекопитающих активируется спонтанно при помощи кроличьих эритроцитов, следовательно, они являются удобной мишенью. Кроличьи эритроциты (Complement Technology, Inc.) готовят путем 3-разовой промывки GVB0 (продукт CompTech) и пересуспендирования в 5×108/мл. Разные количества антитела против фактора Bb разводили GVB0. Смешивают 100 мкл реакции на льду из ряда серийных разведений антитела против фактора Bb, 0,1 М MgЭДТУ (продукт CompTech), 1/2 НЧС (нормальная человеческая сыворотка, разведенная  GVB0) и кроличьи эритроциты. Затем инкубируют реакцию при 37°С в течение 30 минут в шейкере. Добавляют 1,0 мл холодного GVBE. Смешивают и центрифугируют в течение 3 мин приблиз. при 1000×g или выше, чтобы осадить клетки. Переносят 100 мкл супернатанта в 96-луночный планшет и считывают на 412 ни (SoftMax Pro 4.7.1). Данные анализировали при помощи GraphPad Prism 4.
GVB0) и кроличьи эритроциты. Затем инкубируют реакцию при 37°С в течение 30 минут в шейкере. Добавляют 1,0 мл холодного GVBE. Смешивают и центрифугируют в течение 3 мин приблиз. при 1000×g или выше, чтобы осадить клетки. Переносят 100 мкл супернатанта в 96-луночный планшет и считывают на 412 ни (SoftMax Pro 4.7.1). Данные анализировали при помощи GraphPad Prism 4.
[00275] Результаты - Чтобы определить эффективность антител против фактора Bb, проводили анализ гемолиза АП и IC50 нМ (количества антитела, необходимого для ингибирования 50% реакции гемолиза). Данные указывают на то, что IC50 раскрытого в настоящем изобретении антитела против фактора Bb составляет около 40 нМ, в то время как IC50 антитела против фактора В составляет около 100 нМ (Фигура 2). Следовательно, антитело против фактора Bb является в около десяти раз более эффективным, чем антитело против фактора В согласно данным анализа гемолиза АП.
Пример 3 - Модель in vivo эффективности
[00276] Гуманизированное антитело H4L4 99А12 (SEQ ID NO: 15 и 11, соответственно) исследовали в обезьяньей модели легкого повреждения. Интравитреальное дозирование антителом H4L4 99А12 обеспечивало эффективное блокирование депонирования комплемента в сетчатке по сравнению с контролем. Эти данные указывают на то, что местная доставка антитела H4L4 99А12 является эффективной в in vivo модели, релевантной лечению людей с макулярной дегенерацией и другими глазными показаниями.