Результат интеллектуальной деятельности: Способ анализа последовательности нуклеотидов
Вид РИД
Изобретение
Изобретение относится к области анализа ДНК, последовательности нуклеотидов, а также может быть использовано для целей распознавания структуры любых макромолекул и агломератов с использованием флуоресцирующих или фосфоресцирующих маркеров (или праймеров) - так называемого скрининга.
Изобретение может быть использовано для целей диагностики и анализов для выявления определенных веществ. В частности, изобретение относится к средствам и реагентам, включая биочипы, для выявления присутствия или дифференцирования одного или нескольких анализируемых веществ в образце для выявления, например, токсинов в окружающей среде и скрининге лекарственных средств.
Как правило, скрининг, в том числе и анализ структуры ДНК, производится путем обработки образца флуоресцирующими праймерами с соответствующей выдержкой для связывания маркеров с отдельными участками макромолекул, воздействием излучения в оптическом диапазоне для возбуждения флуоресценции и регистрации последней методом проточной цитометрии (см. Патент РФ 2480732, G01N 15/00, 05.04.2007).
Однако выделение полезного сигнала на уровне шумов представляет в известном способе значительные трудности, несмотря на применение маркеров с максимальной флуоресценцией и регистрацией только максимального отклика, так что способ характеризуется низкой точностью и производительностью.
С целью снижения погрешности при регистрации слабого излучения маркеров в патенте США 2010057369, G06F 19/20, 2010 маркеры предварительно группируют по свойствам и эту априорную информацию используют при выделении полезного сигнала. Данный способ анализа последовательности нуклеотидов также включает обработку образца флуоресцирующими маркерами, воздействие на обработанный образец электромагнитным излучением, возбуждающим флуоресценцию, регистрацию флуоресценции образца и обработку результатов с целью выделения полезного сигнала и является наиболее близким к предлагаемому. Однако, во-первых, необходимость использовать только определенные праймеры ограничивает возможность использования способа и его производительность, а во-вторых, выигрыш в точности по сравнению с традиционными способами является незначительным.
Техническим результатом, ожидаемым от использования предлагаемого способа, является повышение точности и производительности, возможность применения маркеров с меньшим откликом, а также повышение достоверности данных исследования.
Указанный результат достигается тем, что в способе анализа, преимущественно последовательности нуклеотидов, включающем обработку присоединением к образцу люминесцирующих маркеров, воздействие на обработанный образец электромагнитным излучением, возбуждающим люминесценцию (как частный случай, флуоресценцию), регистрацию люминесценции (флуоресценции) образца и обработку результатов - с целью выделения полезного сигнала на обработанный образец воздействуют модулированным излучением, а при обработке результатов в качестве полезного сигнала соответствующим образом выделяют модулированный.
Кроме того, при воздействии электромагнитным излучением можно использовать ШИМ или ИКМ.
Далее, при уменьшении длины импульса целесообразно регистрировать изменение величины отклика (фосфоресценции, например) и по полученной зависимости судить о достоверности полученных данных и параметрах реактивов.
Также при воздействии электромагнитным излучением может быть использована частотная модуляция.
Кроме того, воздействие электромагнитным излучением целесообразно производить в двух и более спектральных областях, а модуляцию при этом выполнять с условием, что максимумы интенсивности воздействия в разных спектральных областях при этом не совпадают по времени.
Это означает, что модуляция источников сигнала возбуждения (накачки) организована таким образом, что их максимальная мощность (максимум получаемого образцом потока энергии от них) разнесена во времени, что, в свою очередь, раздвигает во времени и позволяет лучше различить сигналы отклика. Это тем более важно, что частотный (оптический) спектр одного источника возбуждения может частично перекрываться, например, со спектром флуоресцентного отклика маркеров, возбужденных другим источником, и данный способ позволяет значительно улучшить условия выделения полезного сигнала, или, например, снизить требования к оптическим фильтрам.
Наконец, по каждому из спектральных воздействий можно независимо анализировать сигналы отклика маркеров и по их взаимному соотношению судить о достоверности полученных данных и параметрах реактивов. Это касается как соотношения откликов каждого маркера на различные воздействия, так и взаимного соотношения отклика разных маркеров на одно воздействие. Таким образом, анализ соотношений откликов маркеров на различные (в том числе по спектру, длительности и другим условиям воздействия) сигналы возбуждения дает (при сравнении этих результатов с априорными данными, например) дополнительную информацию о качестве реактивов, достоверности результатов и пр.
Кроме того, при выделении модулированного полезного сигнала может быть использована общая синхронизация с источником электромагнитного излучения, преимущественно лазером.
При этом можно фиксировать (регистрировать, измерять) также фазовый сдвиг между воздействующим электромагнитным излучением и принятым сигналом и по его величине судить о достоверности полученных данных и параметрах реактивов.
Также воздействие на образец электромагнитным излучением можно производить в двух и более спектральных областях так, что максимумы интенсивности воздействия в объеме образца пространственно (геометрически) не совпадают.
Это означает, например, что в области воздействия на образец лазерным или другим излучением можно выделить несколько зон для нескольких источников воздействия, при том, что эти зоны частично или полностью не будут пересекаться и, тем самым, их максимумы будут территориально разделены (что учитывается соответственно при приеме сигнала люминесценции от них). В случае капиллярной сборки такие зоны для разных источников возбуждения удобно располагать, например, последовательно вдоль движения по капилляру.
И, наконец, дополнительно, при выделении полезного сигнала целесообразно учитывать люминесценцию (флуоресценцию) образца во всем диапазоне амплитуд сигнала.
Поясним также, что говоря выше о выделении модулированного сигнала «соответствующим образом», мы имеем в виду осуществление детектирования средствами и методами, свойственными именно тому типу модуляции возбуждающего излучения, которое используется в рассматриваемом варианте реализации, учитывая, что эти средства и методы широко используются в технике, но по иному назначению. В частности, в нашем случае наибольший интерес представляют методы выделения сигнала из шумов с возможностью получения оценки энергии сигнала с минимальной погрешностью на заданном интервале времени, и по отношению к разным типам модуляции данные методы широко описаны в технической литературе.
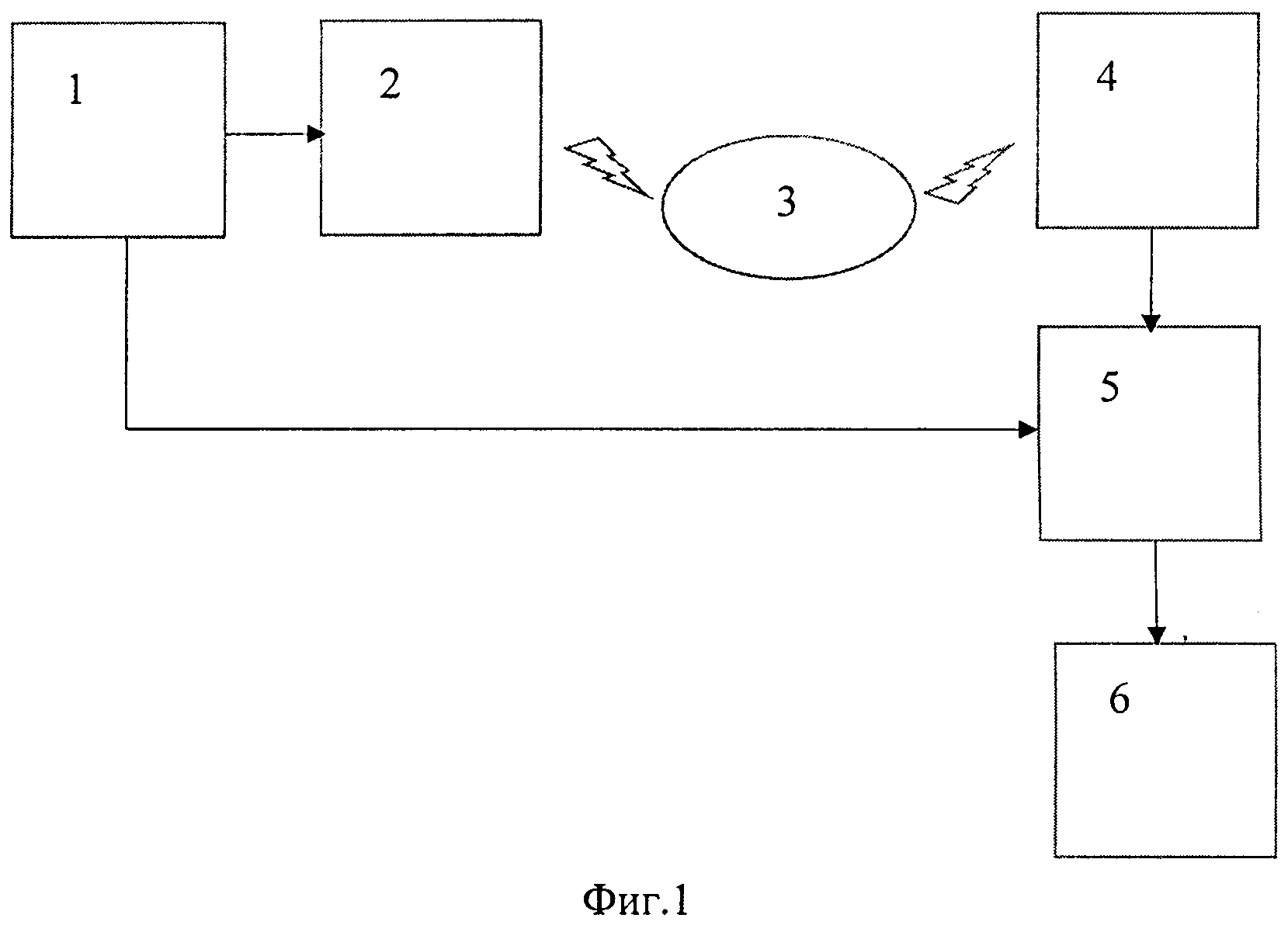
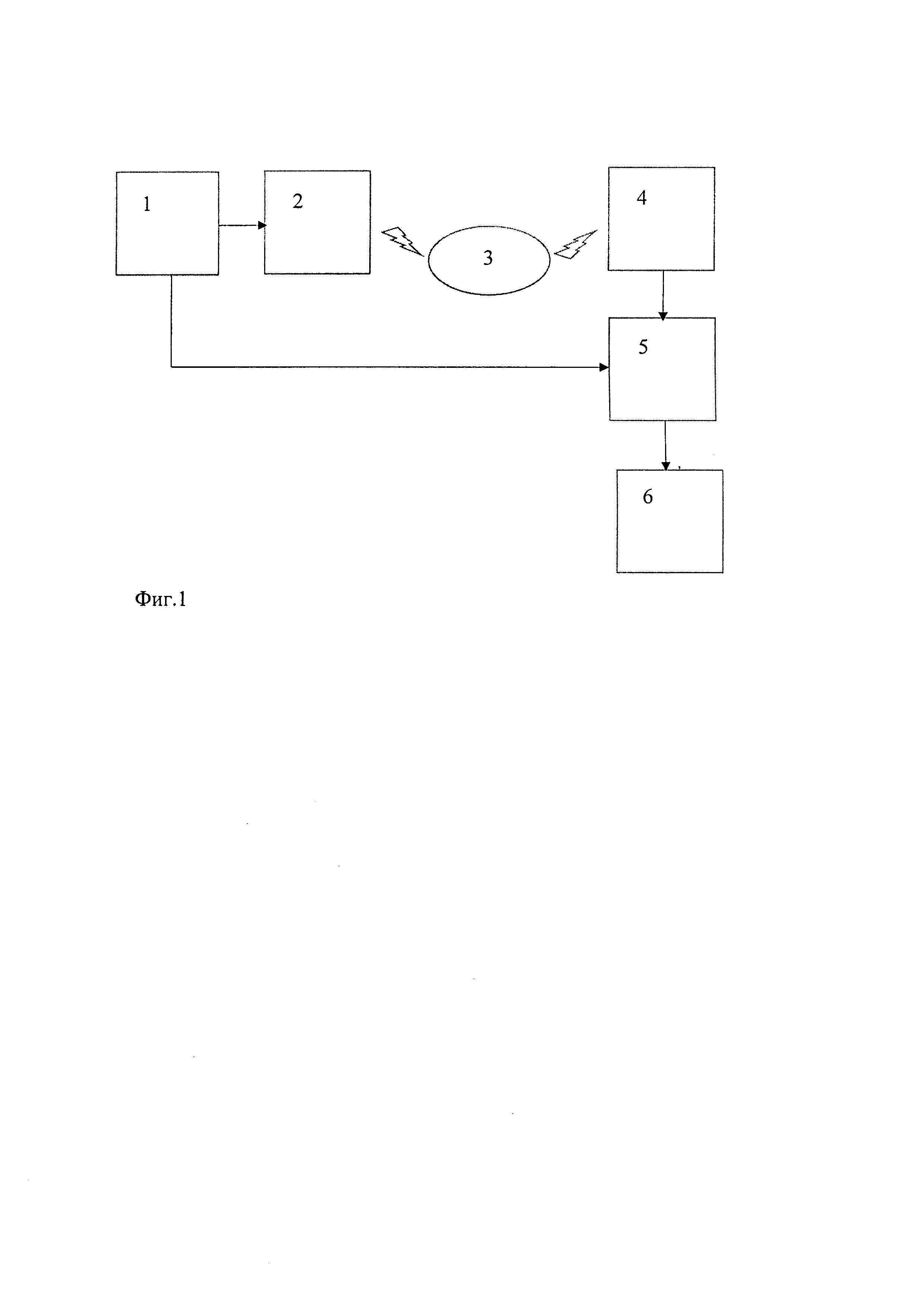
На фиг. 1 приведена функциональная схема устройства для осуществления способа путем регистрации сигнала флуоресценции и последующего дешифрования (распознавания полученных данных) с целью определения структуры макромолекулы, наличия отдельных характерных участков или веществ, последовательностей нуклеотидов и т.п.
Следует подчеркнуть, что предлагаемый способ в части воздействующих на образец факторов (праймеры, температура, напряженность поля, выдержка, поток излучения), а также регистрируемых величин (интенсивность люминесценции, или, как частный случай, флуоресценции) не отличается от известного. То же относится в целом и к используемым аппаратным средствам. Поэтому осуществление способа поясним только в той части, которая отличает его от известных способов скрининга и сделаем это на примере работы устройства, представленного на фиг. 1.
Модулированный сигнал (сигналы) с выхода генератора 1 модулированного сигнала поступает на управляющий вход источника (источников) 2 электромагнитного излучения (оптический лазер, LED, лазер или лампа с оптическим LCD затвором, и т.п.). Излучение источника (источников) 2 воздействует на обработанный образец (образцы) в проточной камере 3 (например, капиллярной сборке), возбуждая люминесцентное излучение маркеров. Это излучение вместе с шумовым сигналом регистрируется сенсором 4 (фотоприемником), выход которого соединен с информационным входом детектора 5 модулированного сигнала, выход которого соединен с входом процессора 6 (либо детектор/демодулятор в цифровой реализации является частью алгоритма процессора). Управляющий вход детектора 5 может быть подключен к выходу синхронизации генератора 1. Последний может формировать модулированный сигнал любого вида, в том числе и амплитудно-модулированный, однако в этом случае отношение сигнал/шум на выходе устройства оказывается ниже, чем при ШИМ (широтно-импульсной модуляции), ИКМ (импульсно-кодовой модуляции) или ЧИМ (частотно-импульсной модуляции), так как при снижении средней амплитуды излучения слабее оказывается и отклик люминесценции.
Как уже было отмечено выше, использование модулированного возбуждающего излучения позволяет на приемном конце, в процессе регистрации сигнала от маркеров, отстроиться от влияния помех, низкочастотного шума сигнала возбуждения, случайных флуктуаций и пр. Это не только повышает достоверность полученных данных, но и ускоряет процесс исследования за счет того, что отпадает необходимость длительное время накапливать данные, упрощает и удешевляет способ за счет возможности применения маркеров с меньшим откликом, уменьшает время выдержки.
Предлагаемый способ открывает еще одну возможность повышения достоверности анализа в случае наличия синхронизации детектора 5 и генератора 1: в детекторе 5, помимо фильтрации (выделения) полезного (информационного) сигнала, может осуществляться регистрация фазового сдвига сигнала люминесценции относительно опорного сигнала генератора 1, по фазе совпадающего с возбуждающим излучением. Величина этой задержки (фазового сдвига) оказывается зависящей практически исключительно от качества используемых маркеров (праймеров), так что изменение их состава в ходе приготовления или хранения немедленно отражается на величине задержки, по которой, таким образом, оказывается возможным судить о проведении анализа с применением нормированных препаратов, а следовательно, и о получении достоверных результатов, и наоборот. При выделении сигнала фосфоресценции ключевой становится длина импульса возбуждения, от которой может зависеть также величина отклика, что дает аналогичную информацию о качестве и составе маркера.
Модуляция существенно облегчает изучение величины отклика маркеров при использовании нескольких источников сигнала возбуждения с различным спектральным диапазоном, либо перестраиваемых источников. Результаты обработки полученных соотношений величин отклика могут являться дополнительным критерием достоверности результата анализа, что важно для таких ответственных применений, как, например, криминалистика.