Результат интеллектуальной деятельности: Способ автоматического отбора и упаковки микробиологических объектов
Вид РИД
Изобретение
Способ может быть использован для работы с классом биологических объектов размером от 0.1 мм до 0.5 мкм, находящихся в водной среде, таких, как хромосомы, сперматозоиды, бактерии, фрагменты растительных и животных тканей, споры грибов, пыльца и другие объекты, видимые в оптический микроскоп. Способ позволяет осуществлять автоматический отбор и упаковку микробиологических объектов с целью их транспортировки, реализации и хранения.
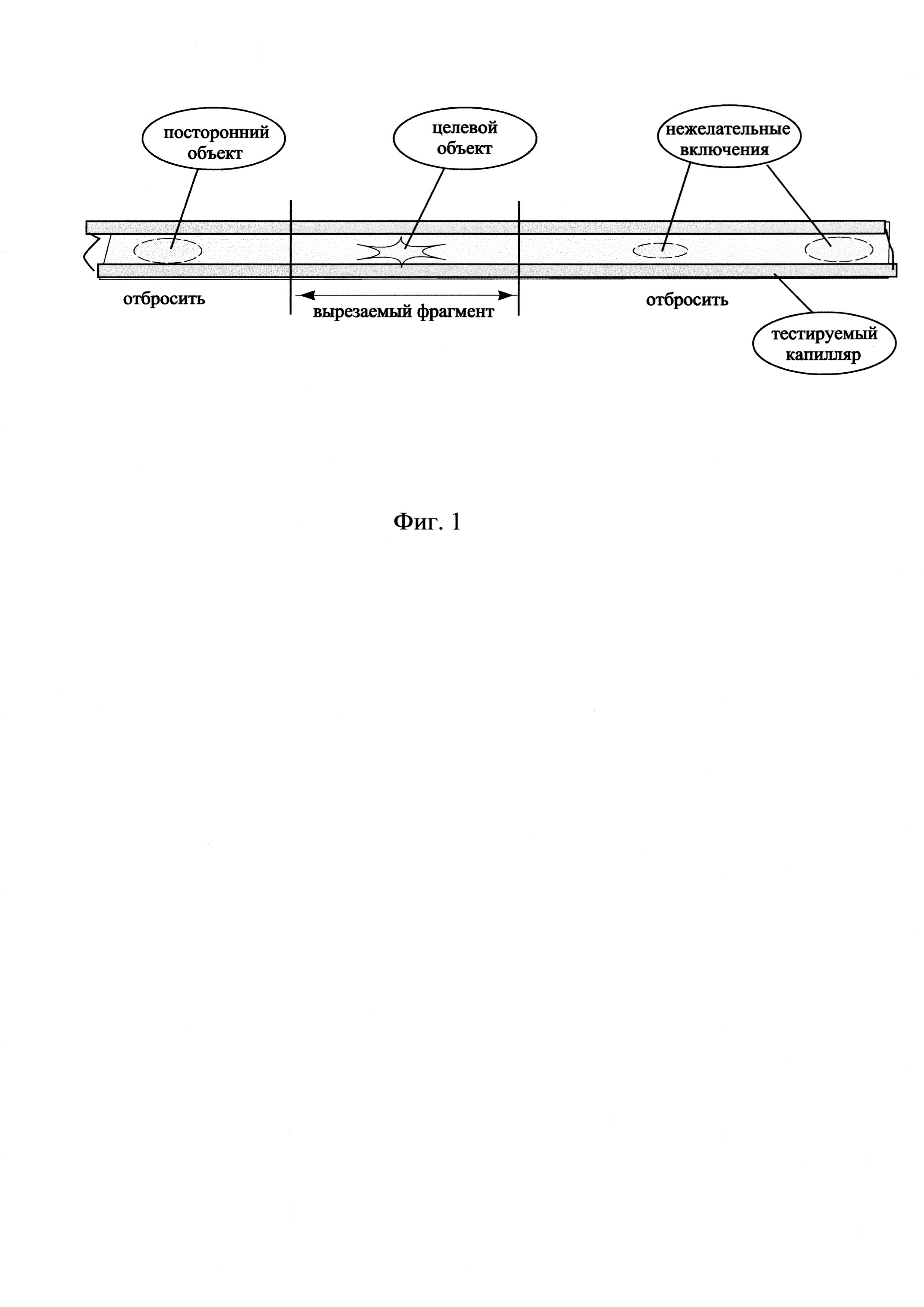
По заявляемой методике микробиологические объекты упаковываются в стеклянные или пластмассовые капилляры, внутренний диаметр которых соответствует размеру объекта. Прозрачная стенка капилляра в процессе поиска и идентификации позволяет рассмотреть в микроскоп целевой объект.
Сохраняемые биологические объекты находятся в свойственной для них по составу водной среде. Высушивание, а также любые консервирующие среды искажают и портят многие биологические объекты.
С целью остановки текущих биологических процессов, а также фиксации их положения объекты в процессе отбора, упаковки и хранения находятся в замороженном состоянии. Глубокая заморозка при транспортировке и хранении позволяет препаратам оставаться в пригодном для использования состоянии в течении длительного времени.
В процессе отбора раствор с микробиологическими объектами помещается в длинные капилляры, которые после их замораживания просматриваются под микроскопом с целью поиска и отбора нужных объектов. Пакет трубок опускается в целевой раствор, происходит их заполнение за счет гидрофильности внутренней поверхности капилляров, при необходимости возможно использование гидростатической, гидродинамической и электрокинетической методик заполнения. Таким образом, весь объем поглощенного раствора будет в дальнейшем просмотрен на предмет наличия подходящих объектов.
В процессе поиска и отбора объектов очередной капилляр в поле зрения микроскопа продвигается вдоль своей оси и при нахождении потенциального объекта поворачивается с целью его идентификации и оценки. Вместе с раствором в капилляры попадает мусор, посторонние включения, поврежденные и неполноценные объекты, - их в процессе поиска нужно исключить, а не нужные участки капилляров отбросить.
Ручной просмотр капилляров требует больших затрат времени, эту рутинную работу предполагается исключить. Идентификация и оценка микробиологического объекта производится автоматически компьютером путем сравнения видимого изображения с рядом хранимых в памяти компьютера графических образов.
В качестве таких графических образов могут использоваться несколько типовых изображений с микроскопа, отобранных оператором при ручном просмотре объектов данной партии.
В случае достаточного сходства изображения очередного объекта с эталонным образом компьютер запоминает изображение и линейную координату найденного объекта. В особых случаях окончательное решение о пригодности препарата принимает оператор после просмотра файла изображения.
После просмотра всего капилляра участки с выбранными объектами автоматически вырезаются, помещаются на упаковочную ленту и снабжаются идентификационной меткой. Не использованные отрезки капилляров выбрасываются.
Для особо ценных и редких объектов идентификационная метка сопровождается файлом с изображением конкретного запакованного объекта.
Обычно биологические микро-образцы рассматриваются в оптический микроскоп на предметном столике под покровным стеклом. Это удобно, но отбор таких образцов затруднен, особенно автоматический отбор. Между тем есть опыт просмотра мелких биологических объектов в тонких стеклянных капиллярах. Искажения, возникающие при просмотре объекта через цилиндрическую стенку капилляра носят закономерный характер и могут быть устранены программно при переносе изображения на монитор.
Кроме того, целью автоматического просмотра является не исследование, а лишь идентификация и оценка биологических объектов, и это упрощает задачу. При необходимости можно наладить производство плоских (сплюснутых) капилляров или капилляров из пластика. Известно, что температура замерзания воды в тонких капиллярах, изготовленных из гидрофильного материала, существенно ниже, чем в открытом сосуде. Это связано с физикой взаимодействия молекул воды со стеклянной стенкой трубки. Чем меньше внутренний диаметр капилляра, тем ниже температура замерзания воды в нем. Так из практики известно, что в порах и капиллярах хорошего бетонного камня вода не замерзает при самых сильных морозах, а в тонких стеклянных капиллярах удавалось сохранять воду жидкой при температуре минус 70 градусов по Цельсию. Кроме того, для сохранения механической прочности у капилляра с малым внутренним диаметром приходится наружный диаметр сохранять достаточно большим так, что соотношение диаметров увеличивается. А это значит, возникающее при замерзании воды относительное увеличение внутреннего диаметра не способно разрушить толстостенную трубку. Так сперматозоид в капилляре внутренним диаметром 10 мкм может сохраняться и при температуре жидкого азота.
Области применения методики.
Сперма. Наиболее выигрышным является использование описываемой технологии в области искусственного оплодотворения метода интрацитоплазматической инъекции спермы (ICSI).
- способ упаковки позволяет извлекать из банка спермы всего несколько образцов, необходимых для проведения процедуры, не размораживая основной массив биологического материала.
- размороженный образец оценивается на жизнеспособность и непосредственно переносится в рабочий инструмент (размеры капилляра и операционной иглы согласованы).
- заказчику изначально поставляются только полноценные здоровые клетки, оцененные по морфологическим признакам.
- в случае затрудненного получения спермы от пациента, все сперматозоиды могут быть сохранены и последовательно использованы для нескольких попыток оплодотворения.
- сперма от добровольных доноров, расфасованная по предлагаемой методике, может быть заложена на долговременное хранение. Проверка генетических достоинств биологического материала может быть проведена по результатам рождения и развития ребенка и удачный материал можно использовать в дальнейшем длительное время.
- в животноводстве при осеменении животных пока мало используется методика ICSI, обычный способ требует большого количества спермы, а высокая стоимость элитной спермы замедляет развитие отрасли. Прогрессивная методика на два - три порядка сокращает потребность в элитном материале, а возможность длительного хранения позволяет отслеживать особенности наследственных признаков производителей.
- коммерческий интерес представляет создание банка спермы знаменитостей и людей, достигших выдающихся результатов.
- сохранение спермы по редким и вымирающим видам животных.
Меристемы и протокормы. Заявляемая методика упаковки и хранения биологических микрообъектов может быть использована в области микроклонального размножения растений - вегетативного выращивания в условиях.
- автоматическая криоконсервация верхушечных меристем в пластмассовые капилляры соответствующего размера позволит сократить затраты ручного труда в подготовке элитного посадочного материала.
- появляется возможность создавать банки первичных недифференцированных растительных клеток растений многих видов для научных и практических целей.
Базы хранения ДНК. Для надежного хранения ДНК удобно использовать в качестве носителя небольшие кусочки ткани объекта, из клеток которой при необходимости извлекается наследственный материал.
Научные базы биологических образцов. Простота консервации и удобство хранения позволяют создавать единые базы биологических материалов разного назначения.
- в работах по сохранению редких и вымирающих видов животных.
- образцы тканей по ископаемым биологическим материалам.
- сайты отдельных генов и фрагменты ДНК, предназначенные для мультипликации методами ПРЦ (без просмотра в микроскоп).
- учебный процесс. Может быть создан мобильный парк микробиологических образцов по широкому спектру направлений - клеточные препараты, полученные центрифугированием фракции клеток, бактерии, насекомые, мелкая водная фауна.
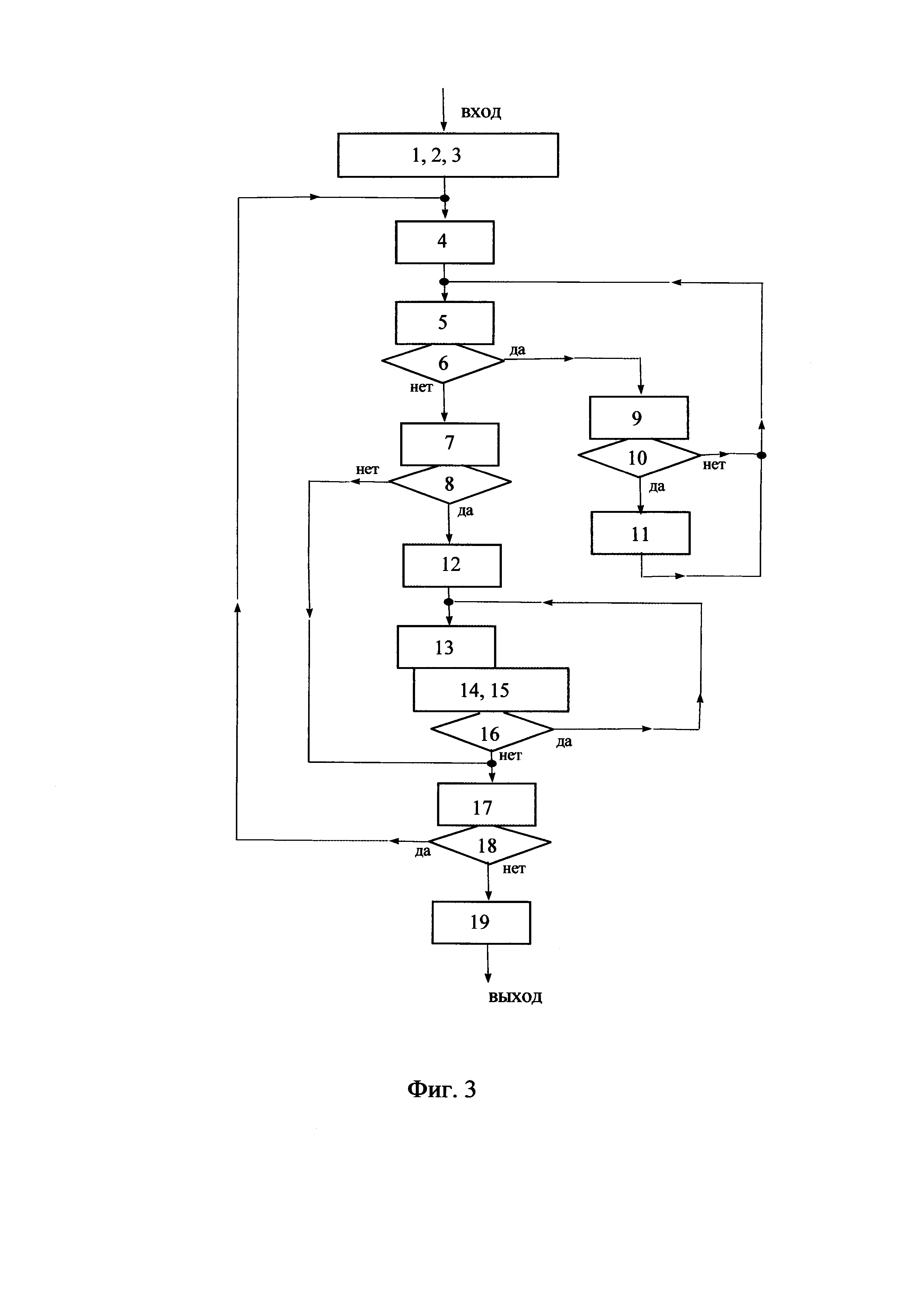
На фиг. 1 показан капилляр, который просматривается под микроскопом с целью идентификации нужных биологических объектов. На фиг. 3 приводится логическая диаграмма, иллюстрирующая пример реализации предлагаемого способа.
1. Разбавление раствора, подкрашивание (если необходимо).
2. Заполнение капилляров раствором.
3. Загрузка партии капилляров в приемную кассету устройства.
4. Установка очередного капилляра на стол.
5. Продвижение капилляра до обнаружения очередного объекта.
6. Объект обнаружен?
7. Просмотр записей по текущему капилляру.
8. В капилляре есть найденные объекты?
9. Попытка идентификации найденного объекта.
10. Объект удовлетворяет заданным условиям?
11. Запись изображения и фиксация линейной координаты.
12. Перемещение капилляра в зону разделки.
13. Установка капилляра в позицию очередного объекта по ранее сохраненной линейной координате.
14. Отделение от капилляра фрагмента, содержащего объект.
15. Закрепление фрагмента на транспортной ленте, печать идентификационной метки.
16. Есть ли в оставшейся части капилляра еще объекты?
17. Удаление капилляра в мусорный контейнер.
18. Есть ли в приемной кассете еще капилляры?
19. Приведение установки в исходное состояние.
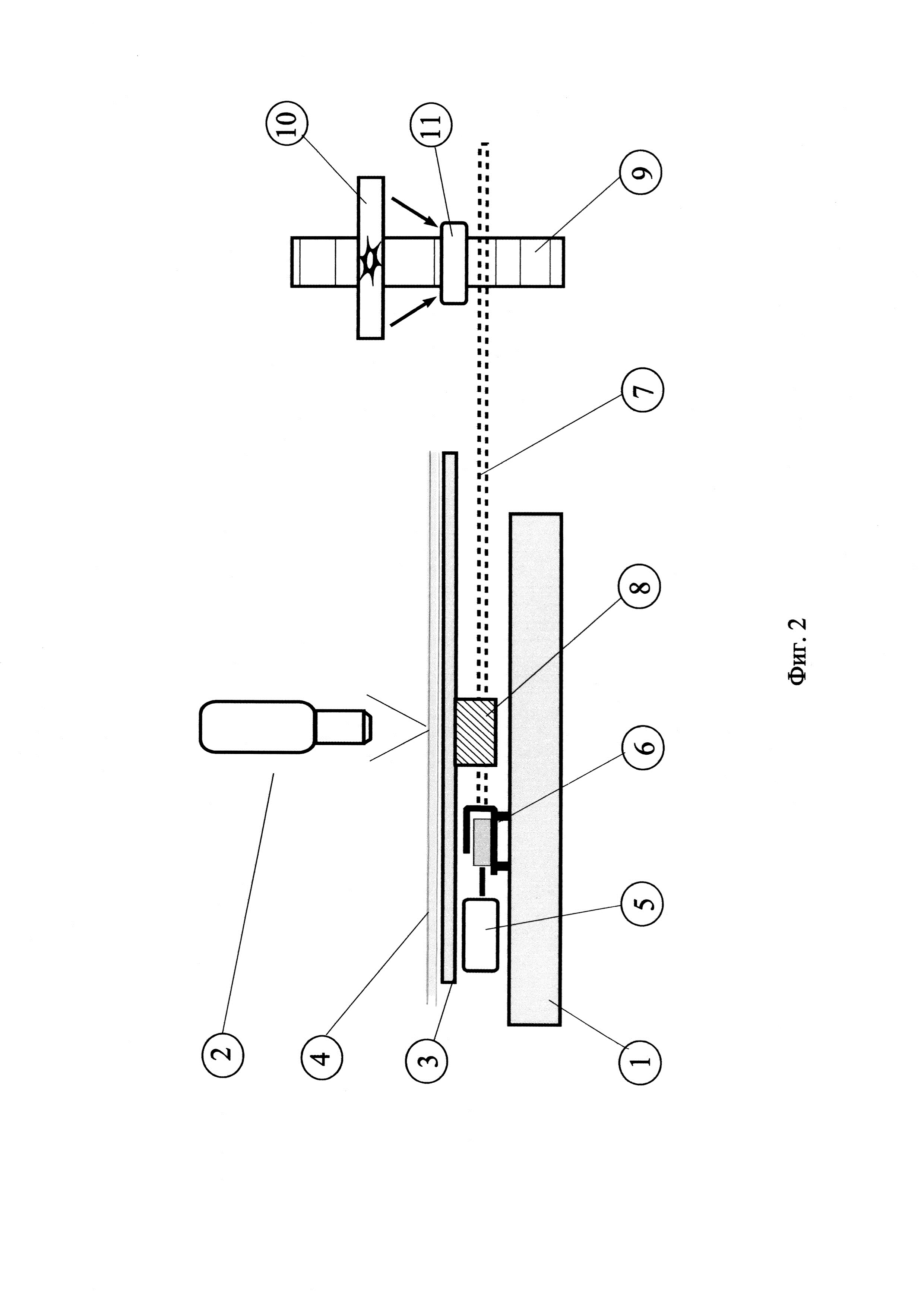
Пример устройства для реализации метода. (смотри фиг. 2)
1 - предметный столик микроскопа
2 - микроскоп
3 - подвижный стол
4 - исследуемый капилляр
5 - шаговый двигатель
6 - волновая передача
7 - ходовой винт
8 - гайка
9 - транспортная лента
10 - лазерный резак
11 - зона разделки.
На предметно столике микроскопа 1 закреплен подвижный стол 3. На этот стол устанавливается исследуемый капилляр 4. Стол может медленно или ускорено перемещаться под объективом микроскопа 2. Привод стола осуществляется от шагового двигателя 5 через волновую передачу 6. После анализа содержания капилляра подвижный стол перемещается в зону разделки 11. Здесь капилляр с помощью лазера 10 разрезается на отдельные микроконтейнеры, которые закрепляются на транспортной ленте 9.
На фиг. 3 представлена схема алгоритма работы устройства по описываемому методу. На блок-схеме обозначены отдельные операции по работе с объектами и указаны связи, характеризующие последовательность действий по реализации описываемого способа.