Результат интеллектуальной деятельности: СОДЕРЖАЩИЕ РЕТИНОИД ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ ДЛЯ МЕСТНОГО ПРИМЕНЕНИЯ ТИПА ЭМУЛЬСИИ "МАСЛО В ВОДЕ"
Вид РИД
Изобретение
Настоящее изобретение относится к фармацевтической композиции для местного применения, содержащей в качестве фармацевтически активного вещества ретиноид в физиологически приемлемой среде, к способу ее получения и к ее применению в дерматологии.
В области дерматологии и при составлении фармацевтических композиций специалистам в данной области техники приходится готовить композиции, которые должны быть стабильны физически и химически. Они должны также обеспечивать высвобождение активного вещества и благоприятствовать его проникновению через слои кожи для улучшения его эффективности.
Роговой слой или stratum corneum представляет собой самую верхнюю часть эпидермиса. Слой, традиционно сравниваемый со стеной из "кирпичей и строительного раствора", состоит из мертвых клеток, то есть корнеоцитов, вставленных в межкорнеоцитарные липиды. Роговой слой лежит на эпидермисе, представляющем собой первый живой слой кожи. Он содержит клетки многих типов и лишен сосудов. Наконец, дерма состоит из малого числа клеток, многих белков, обеспечивающих опору ткани, и сосудистой сети. Если роговой слой принципиально имеет липофильную природу в силу присутствия межкорнеоцитарных липидов, то эпидермис и дерма принципиально имеют гидрофильную природу, кроме того, присутствие сосудов в дерме в большей степени обеспечивает очистку этого слоя.
Обычно допускают, что механизмы чрескожного проникновения и проницаемости зависят, с одной стороны, от коэффициентов распределения соединений между применяемым наполнителем и различными отделами кожи (роговой слой, эпидермис и васкуляризованная дерма), а с другой стороны, от коэффициента диффузии этих соединений в каждом слое кожи. Благодаря своим физико-химическим характеристикам, в частности, благодаря своему липофильному характеру некоторые соединения обладают высокой аффинностью и большим коэффициентом диффузии в роговом слое, таким образом, они накапливаются больше в роговом слое и в меньшей мере в эпидермисе. В противоположность этому, их содержание в васкуляризированной дерме, имеющей более гидрофильную природу, чем эпидермис или роговой слой, будет низким. Таким образом, в этом случае верхние слои кожи и, в частности, роговой слой образуют настоящий резервуар, позволяющий аккумулировать фармацевтически активное вещество. Как правило, кинетика проникновения таких соединений демонстрирует с течением времени увеличение количества активного вещества в роговом слое и в меньшей мере в эпидермисе с последующим плато, в пределах которого это количество больше не изменяется. При этом достигается состояние равновесия между проникновением активного вещества в отдел и его клиренсом.
В некоторых случаях важно иметь возможность регулировать эту типичную кинетику так, чтобы фармацевтически активное вещество могло проникать в кожу в режиме небольшого, продолжительного и регулируемого потока. При этом такого типа проникновение и аккумулирование в коже может приближаться к кинетике нулевого порядка с учетом линейной кинетики чрескожной диффузии и проницаемости нулевого порядка, наблюдаемых в случае некоторых лекарственных средств, применяемых через мембрану или на коже.
Активные молекулы, от которых требуется проход к их цели, редко бывают изолированными, они наиболее часто находятся во внутренней структуре более или менее сложной композиции, которая, в зависимости от случая, может представлять собой крем, мазь, лосьон, порошок или гель. После фазы контакта между молекулой и поверхностью кожи активное вещество должно будет покинуть свой носитель, чтобы проникнуть во внутреннюю структуру рогового слоя с большей или меньшей легкостью.
В общем случае фармацевтические композиции для местного применения, такие как гели, кремы, лосьоны, растворы, высвобождают одно или несколько активных веществ за счет диффузии прямо пропорционально градиенту концентрации в фазе композиции. Иными словами, после нанесения на кожу одно или несколько активных веществ высвобождаются почти сразу, а затем кинетика высвобождения стремится к нулю с формированием плато. При этом одно или несколько активных веществ больше не абсорбируются на коже.
Для получения кинетики высвобождения, которая не зависит от градиента концентрации, существует несколько типов композиций для местного применения, таких как:
- композиции супернасыщенных растворов, то есть композиции, в которых одно или несколько активных веществ находятся в растворе с большими концентрациями;
- системы чрескожной доставки (пластыри), в которых высвобождение одного или нескольких активных веществ регулируется мембраной, которая является проницаемой и в общем случае клейкой и находится непосредственно в контакте с кожей.
Супернасыщенные растворы часто бывают нестабильными и не позволяют получать хорошую физическую стабильность композиции, которая может представлять собой гель, крем, лосьон или мазь.
Системы чрескожной доставки, напротив, являются более стабильными, но имеют недостаток, заключающийся в более сложном применении с поверхностью нанесения, ограниченной размером пластыря.
Таким образом, проблема, которую в данном случае предлагается решить настоящим изобретением, состоит в разработке фармацевтической композиции типа эмульсии "масло в воде", которая является стабильной физически и химически и содержит по меньшей мере одно активное вещество, представляющее собой один или несколько ретиноидов и имеющее нетрадиционный профиль высвобождения. Она должна также обеспечивать легкость применения и косметическую приемлемость для применения на любых частях тела, которые могут быть затронуты патологией.
Таким образом, существует потребность в фармацевтической композиции для местного применения, которая позволяет отвечать одному или нескольким следующим требованиям:
- обеспечивать хорошую физическую стабильность без риска кристаллизации одного или нескольких активных веществ;
- допускать нанесение без ограничения поверхности и с хорошей переносимостью;
- обеспечивать постепенное проникновение одного или нескольких активных веществ на уровень их целей.
Таким образом, намерением заявителя является улучшение этих параметров за счет настоящего изобретения.
Под химической стабильностью понимают, в частности, стабильность активного вещества.
Под физической стабильностью понимают, в частности, отсутствие кристаллизации или выпадения осадка активного вещества или также отсутствие разделения фаз или изменение цвета в фазе композиции.
Композиция, являющаяся по настоящему изобретению стабильной физически, представляет собой, следовательно, композицию, в которой не выявляются какие-либо изменения ни при внешнем осмотре (разделение фаз, изменение цвета, внешнего вида и т.д.), ни при исследовании под микроскопом (кристаллизация активных веществ) после хранения при температуре 25, 4 и 40°C в течение 1, 2, 3 и 6 месяцев.
Композиция, являющаяся по настоящему изобретению химически стабильной, представляет собой, следовательно, композицию, в которой содержание активного вещества остается стабильным через шесть месяцев хранения при комнатной температуре (tкомн) и 40°C. Стабильное содержание активного вещества означает по настоящему изобретению, что содержание очень мало изменяется по сравнению с начальным содержанием, то есть измененное содержание активного вещества в момент времени T не должно быть меньше 90% и более предпочтительно 95% от начального содержания в момент T0.
При выборе ингредиентов фармацевтической композиции специалистам в данной области техники надлежит принимать в расчет также и другие параметры. На практике фармацевтическая композиция, приемлемая для применения по настоящему изобретению в качестве лекарственного средства, должна быть составлена также с учетом патологии, подлежащей лечению.
В порядке неограничительного примера композиция, предназначенная для лечения угрей, должна быть в косметическом отношении нежирной, тогда как композиция, предназначенная для лечения ихтиозов, ихтиозиформных состояний, ладонно-подошвенного гиперкератоза или псориаза, должна быть смягчающей, увлажняющей и может содержать больше жировых веществ, но в любом случае в косметическом отношении не создавать эффект жирной кожи.
Настоящим изобретением заявителем неожиданным образом было показано, что можно было получить содержащую ретиноид композицию типа эмульсии "масло в воде", которая является стабильной физически и химически и характеризуется кинетикой проникновения активного вещества нулевого порядка.
Под композицией, характеризующейся кинетикой проникновения нулевого порядка, понимают композицию, для которой после нанесения на поверхность кожи характерен постепенный и регулируемый профиль проникновения активного вещества на уровень их мишеней.
Как неограничительный пример, мишень ретиноида находится, в частности, на уровне эпидермиса в случае лечения угрей, ихтиозов, ихтиозиформных состояний, ладоннно-подошвенного кератоза и псориаза.
Под солюбилизированной формой активного вещества понимают дисперсию активного вещества в жидкости в молекулярном состоянии, причем какая-либо кристаллизация активного вещества не видна ни невооруженным глазом, ни даже под оптическим микроскопом в перекрестной поляризации.
3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновая кислота (называемая далее по тексту соединением A) принадлежит к группе ретиноидов, которые представляют собой агонисты рецептора RAR-гамма. Поскольку рецепторы RAR-гамма расположены в эпидермисе, то важно, чтобы высвобождение ретиноидов осуществлялось в этой части кожи с целью получения клинической эффективности. Профиль высвобождения в коже соединений такого типа является очень важным для достижения места действия и получения оптимальной эффективности.
С учетом физико-химических характеристик активного вещества заявитель был вынужден преодолеть некоторые трудности при применении соединения A:
- соединение A малорастворимо в растворителях, обычно используемых в масляных фазах эмульсий для местного применения;
- соединение A разрушается химически во многих растворителях, растворяющих его;
- соединение A разрушается химически в присутствии многих эмульгаторов.
Таким образом, хорошая химическая стабильность соединения A не является очевидной в случае, когда оно солюбилизировано или присутствуют эмульгаторы.
Для получения эмульсии "масло в воде" (O/W) по настоящему изобретению были осуществлены исследования предварительных композиций с целью нахождения эксципиентов, обеспечивающих хорошую солюбилизацию, а также хорошую стабильность активного вещества.
Стабильность соединения A в основных масляных растворителях (определенная способом ВЭЖХ)
|
|
Пределы, установленные для хорошей стабильности, составляют 95-105% относительно процентной доли в момент T0.
Из этих исследований стабильности соединения A в основных растворителях, видно, что соединение A разрушается химически во многих растворителях, растворяющих его (химическая нестабильность). Результаты этого исследования позволили выбрать основной растворитель активного вещества и масляные вспомогательные растворители из растворителей, показавших хорошие результаты стабильности, что и было целью разработки эмульсий O/W, в которых активное вещество солюбилизировано в масляной фазе.
- (3) Стабильность соединения A в смесях эксципиентов (растворитель/поверхностно-активные вещества), определенная способом ВЭЖХ
Были осуществлены исследования стабильности соединения A, солюбилизированного в масляных растворителях, в которых оно стабильно, как было показано ранее, в присутствии поверхностно-активных веществ.
|
Пределы, установленные для хорошей стабильности, составляют 95-105% относительно процентной доли в момент T0.
В этих исследованиях было показано, что соединение A разрушается химически в присутствии многих поверхностно-активных веществ, традиционно используемых в эмульсии типа "масло в воде" (O/W).
Целью настоящего изобретения является разработка содержащих ретиноид фармацевтических композиций в форме эмульсий типа O/W ("масло в воде") на основе эмульгаторов типа сложных эфиров сахарозы, в которых активное вещество солюбилизировано в масляной фазе. В этих фармацевтических композициях ретиноид имеет хорошую физическую и химическую стабильность. Из этих композиций ретиноид проникает на уровень своих целей постепенно.
Заявителем найдено, что в случае, когда соединение A солюбилизировано растворителями и вспомогательными растворителями, в которых оно является стабильным, и в случае, когда используют сложные эфиры сахарозы в качестве эмульгаторов, композиции по настоящему изобретению стабильны по меньшей мере в течение 6 месяцев при комнатной температуре и при +40°C.
Настоящее изобретение относится к фармацевтической композиции для местного применения типа эмульсии "масло в воде", которая содержит липофильную фазу, одно или несколько поверхностно-активных веществ и находится в форме предварительного концентрата, который после разбавления водной фазой позволяет получить микронные и субмикронные эмульсии.
Компоненты масляной фазы должны быть выбраны так, чтобы они растворяли активное вещество и могли сочетаться с другими маслами или жировыми веществами с целью получения композиции, имеющей требуемые свойства.
Таким образом, композиция по настоящему изобретению относится к композиции для местного применения типа эмульсии "масло в воде", содержащей:
- масляную фазу, содержащую по меньшей мере одно активное вещество, выбранное из ретиноидов, по меньшей мере один основной растворитель активного вещества, один или несколько масляных вспомогательных растворителей и минеральное масло;
- водную фазу, содержащую по меньшей мере одно поверхностно-активное вещество из группы сложных эфиров сахарозы, по меньшей мере один полиол и очищенную воду.
Под ретиноидом в смысле настоящего изобретения понимают, гидрофобный ретиноид, такой как соединения, заявленные в WO 2006/066978, такие, как 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновая кислота.
Таким образом, композиция по настоящему изобретению относится к композиции для местного применения типа эмульсии "масло в воде", содержащей:
- масляную фазу, содержащую 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновую кислоту, по меньшей мере один основной растворитель активного вещества, один или несколько масляных вспомогательных растворителей и минеральное масло;
- водную фазу, содержащую по меньшей мере одно поверхностно-активное вещество из группы сложных эфиров сахарозы, по меньшей мере один полиол и по меньшей мере 5 масс. % воды.
Согласно предпочтительному варианту композиция по настоящему изобретению относится к композиции для местного применения типа эмульсии "масло в воде", содержащей:
- масляную фазу, содержащую по меньшей мере одно активное вещество, выбранное из ретиноидов, по меньшей мере один основной растворитель активного вещества, один или несколько масляных вспомогательных растворителей и минеральное масло;
- водную фазу, содержащую по меньшей мере одно поверхностно-активное вещество из группы сложных эфиров сахарозы, по меньшей мере один полиол, по меньшей мере один гелеобразователь и по меньшей мере 5 масс. % воды.
Под гелеобразователем понимают полимерное соединение, способное придавать композиции структуру геля. Речь может идти о гелеобразователях растительного происхождения, таких как камеди, пектины, целлюлозы и ее производные, о гелеобразователях микробиологического происхождения, таких как ксантановая камедь, о гелеобразователях синтетического происхождения.
В более предпочтительном варианте композиция находится в форме эмульсии и содержит:
- масляную фазу, содержащую от 0,00001 до 1% по меньшей мере одного ретиноида;
- водную фазу, содержащую от 0,1 до 15% сложных эфиров сахарозы, от 1 до 40% полиола, от 0,005 до 10% гидрофильного гелеобразователя и по меньшей мере 5% воды;
- от 0 до 15% одной или нескольких добавок.
Согласно предпочтительному варианту настоящего изобретения композиция состоит из:
- масляной фазы, содержащей от 0,00001 до 1% по меньшей мере одного ретиноида; от 0,1 до 10% основного растворителя ретиноида; от 0,5 до 60% масляных вспомогательных растворителей ретиноида; от 0,5 до 20% минеральных масел; от 0,1 до 10%, от 0,5 до 3% загустителя масляной фазы; от 0 до 20% силиконового масла;
- водной фазы, содержащей от 0,1 до 15% эмульгаторов из группы сложных эфиров сахарозы; от 1 до 40%, от 4 до 10% полиола; от 0,005 до 10% гелеобразователя водной фазы;
- от 0,01 до 5 масс. % системы консервантов;
- от 0 до 15%, от 0,1 до 10% добавок.
Согласно предпочтительному варианту настоящего изобретения композиция, более предпочтительно адаптированная для лечения угрей, состоит из:
- масляной фазы, содержащей от 0,00001 до 1% 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновой кислоты (соединение A); от 0,2 до 5% основного растворителя соединения A; от 0,5 до 60% масляных вспомогательных растворителей соединения A; от 0,5 до 20% минеральных масел; от 0,1 до 10% загустителя масляной фазы; от 0 до 20% силиконового масла;
- водной фазы, содержащей от 0,1 до 15% эмульгаторов из группы сложных эфиров сахарозы; от 1 до 40% полиола; от 0,005 до 10% гелеобразователя водной фазы;
- от 0,01 до 5 масс. % системы консервантов;
- от 0,001 до 15% добавок.
В случае фармацевтических композиций, адаптированных для лечения угрей, масляная фаза предпочтительно состоит из:
- от 0,0001 до 1% по меньшей мере одного ретиноида;
- 1% феноксиэтанола;
- 1,980% цетеарилового спирта;
- 3% минеральных масел;
- от 15 до 22% масляных вспомогательных растворителей.
Согласно предпочтительному варианту настоящего изобретения композиция, более предпочтительно адаптированная для лечения ихтиозов, ихтиозиформных состояний, ладонно-подошвенного гиперкератоза или псориаза, состоит из:
- масляной фазы, содержащей от 0,00001 до 1% 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновой кислоты (соединение A); от 0,2 до 5% растворителя соединения A; от 0,5 до 60% масляных вспомогательных растворителей соединения A; от 0,5 до 20% минеральных масел; от 0,1 до 10% загустителя масляной фазы; от 0 до 20% силиконового масла;
- водной фазы, содержащей от 0,1 до 15% эмульгаторов из группы сложных эфиров сахарозы; от 1 до 40% полиола; от 0,005 до 10% гелеобразователя водной фазы;
- от 0,01 до 5 масс. % системы консервантов;
- от 0,001 до 15% добавок.
Система поверхностно-активных веществ содержит по меньшей мере одно основное поверхностно-активное вещество, выбранное из категории сложных эфиров сахарозы, таких как стеарат сахарозы и пальмитат сахарозы. Один или несколько из этих сложных эфиров сахарозы могут сочетаться с любым другим поверхностно-активным веществом, которое может играть роль вспомогательных поверхностно-активных веществ.
Водная фаза может неограничительным образом содержать один или несколько полиолов, один или несколько гелеобразователей гидрофильной фазы и добавок различных типов.
Данные в % выражены по массе по отношению к общей массе композиции за исключением особых указаний.
По настоящему изобретению композиции содержат 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновую кислоту, называемую соединение A, с концентрацией в интервале от 0,00001 до 1% и предпочтительно от 0,0001 до 0,1 масс. % по отношению к общей массе композиции.
Как было указано ранее, водная фаза содержит по меньшей мере одно поверхностно-активное вещество из группы сложных эфиров сахарозы.
По настоящему изобретению композиции содержат поверхностно-активные вещества типа сложных эфиров сахарозы, которые были выбраны заявителем из-за их хорошей совместимости с соединением A, а также из-за того, что они позволяют получать очень тонко диспергированные эмульсии, которые имеют очень деликатные структуры и превосходно переносятся кожей.
Сложные эфиры сахарозы представляют собой неионогенные поверхностно-активные вещества, содержащие гидрофильную группу, которая представляет собой часть сахарозы, и липофильную группу, которая представляет собой часть жирной кислоты. Поскольку сахарозы в общем случае содержат всего 8 гидроксигрупп, то, таким образом, есть возможность получать сложные эфиры сахарозы в интервале от "моно"-эфира сахарозы до "окта"-эфира сахарозы. "Сложные эфиры сахарозы" или "эфиросахарозы" представляют собой сложные эфиры жирных кислот и сахарозы, причем сахароза представляет собой дисахаридное соединение глюкозы и фруктозы. Под сложным эфиром сахарозы понимают, как неограничительный пример, миристат сахарозы, реализуемый под названием Surfhope C-1416 и поставляемый компанией GATTEFOSSE, пальмитат сахарозы, реализуемый под названиями Surfhope C-1615, Surfhope C-1616 и Surfhope SE Pharma D-1616 и поставляемый компанией GATTEFOSSE, а также реализуемый под названием Sisterna PS750-C и поставляемый компанией UNIPEX, стеарат сахарозы, реализуемый под названиями Surfhope C-1811, Surfhope SE Pharma D-1816, Surfhope C-1815 и Surfhope C-1816 и поставляемый компанией GATTEFOSSE, а также реализуемый под названиями Sisterna SP50-C, Sisterna SP70-C и поставляемый компанией UNIPEX.
В предпочтительном варианте настоящего изобретения композиция содержит пальмитат сахарозы или стеарат сахарозы или их смесь с концентрацией в интервале от 0,1 до 15% и предпочтительно от 0,5 до 5 масс. % по отношению к общей массе композиции.
Масляная фаза по настоящему изобретению должна быть выбрана так, чтобы содержать по меньшей мере один основной растворитель соединения A, один или несколько масляных вспомогательных растворителей и минеральное масло.
Под основным растворителем понимают жидкость, обладающую способностью растворять, разбавлять или экстрагировать другие вещества, не вызывая химического изменения этих веществ и не изменяя саму себя.
По настоящему изобретению основной растворитель представляет собой жидкость, в которой растворимость ретиноидов (и более предпочтительно соединения A) при комнатной температуре и атмосферном давлении превышает или равна 0,1 масс. %.
Основной растворитель предпочтительно содержится с концентрацией в интервале от 0,1 до 10%.
В случае, когда активное вещество в композиции по настоящему изобретению представляет собой соединение A, основной растворитель может представлять собой, например, феноксиэтанол, реализуемый компанией Clariant под названием Phenoxetol и содержащийся с концентрацией в интервале от 0,2 до 5% и предпочтительно от 0,5 до 2%.
Под вспомогательным растворителем понимают вещество, исполняющее функцию растворителя в сочетании с другим веществом.
Масляная фаза по настоящему изобретению содержит также:
- один или несколько масляных вспомогательных растворителей и предпочтительно следующих масляных вспомогательных растворителей, в числе которых триглицериды каприловой/каприновой кислот (Miglyol 812N), поставляемые компанией IMCD, масло Prunus Amygdalus Dulcis (миндальное масло), поставляемое компанией SICTIA, пропиленгликольмонокаприлат (Capryol 90), поставляемый компанией GATTEFOSSE, пропиленгликольлаурат (Lauroglycol FCC) поставляемый компанией GATTEFOSSE, стеариловый эфир PPG-15 (Arlamol PS15E-LQ), поставляемый компанией CRODA, сорбитансесквиолеат (Arlacel 83VPharma), поставляемый компанией CRODA, сложный эфир масла из косточек абрикоса и PEG-6 (Labrafil M1944CS), поставляемый компанией GATTEFOSSE, рафинированное кокосовое масло, поставляемое компанией OLVEA, с содержанием в интервале от 0,5 до 60% и предпочтительно от 10 до 20% в случае угрей и в интервале от 20 до 40% в случае ихтиоза, ладонно-подошвенного гиперкератоза и псориаза;
- одно или несколько минеральных масел, таких как парафиновые масла с различной вязкостью, такие как Marcol 152, Marcol 52 или Primol 352, реализуемые компанией UNIVAR, с содержанием в интервале от 0,5 до 20% и предпочтительно от 2 до 6%.
Другие масла или жировые вещества могут быть прибавлены к масляной фазе композиции различным образом, варьируемым специалистами в данной области техники, с целью получения композиции, имеющей требуемые свойства, например, консистенции или структуры.
Композиция по настоящему изобретению может содержать, например:
- одно или несколько силиконовых масел, позволяющих улучшить свойства наносимых композиций, таких как циклометикон (St-Cyclomethicone 5NF) или диметикон (жидкий силикон Q7 9120 с вязкостью от 20 до 12500 сСт, поставляемый компанией Dow Corning), в количестве от 0 до 20% и предпочтительно от 0 до 6%;
- один или несколько загустителей масляной фазы типа жирного спирта, такого как цетиловый спирт (Crodacol C70, поставляемый компанией CRODA/Kolliwax CA, поставляемый компанией BASF), цетеариловый спирт (Crodacol 1618, поставляемый компанией CRODA, Tego Alkanol 1618, поставляемый компанией EVONIK, а также Kolliwax CSA 50), стеариловый спирт (Crodacol S95, поставляемый компанией CRODA, Kolliwax SA, поставляемый компанией BASF, Tego Alkanol 18, поставляемый компанией EVONIK), а также бегениловый спирт (Nacol 22-98, поставляемый компанией SASOL, а также Behenyl Alcohol 65 80, поставляемый компанией NIKKO CHEMS), или типа карнаубского воска, поставляемого компанией BAERLOCHER, а также пчелиного воска, реализуемого под названием CERABEIL BLANCHIE DAB и поставляемого компанией UNIVAR, с содержанием в интервале от 0,1 до 10% и предпочтительно в интервале от 0,5 до 6%.
Таким образом, количество масляной фазы в эмульсии по настоящему изобретению может находиться в интервале от 1 до 95 масс. %, предпочтительно от 5 до 85% и более предпочтительно в интервале от 15 до 50 масс. % по отношению к общей массе композиции.
Хорошую химическую и физическую стабильность композиции по настоящему изобретению предпочтительно обеспечивает выбор поверхностно-активных веществ. Таким образом, композиция по настоящему изобретению содержит также по меньшей мере одно основное поверхностно-активное вещество, выбранное из категории сложных эфиров сахарозы.
Поскольку композиция по настоящему изобретению представляет собой эмульсию "масло в воде", то она содержит водную фазу, содержащую по меньшей мере 5% и предпочтительно от 5 до 90% воды по отношению к общей массе композиции.
В предпочтительном варианте настоящего изобретения водная фаза содержит также полиол (по меньшей мере один трехатомный спирт), который предпочтительно выбран из глицерина, диглицеринового спирта или сорбита (Neosorb, поставляемый компанией ROQUETTE, Parteck SI, поставляемый компанией Merck, а также Sorbitol USP Powder, поставляемый компанией LIPO CHEMICALS) и количество которого по отношению к общей массе композиции находится в интервале от 1 до 40 масс. % и предпочтительно в интервале от 4 до 10% в случае угрей и в интервале от 10 до 25% в случае ихтиоза, ладонно-подошвенного гиперкератоза и псориаза.
В предпочтительном варианте композиция по настоящему изобретению содержит глицерин в количестве в интервале от 1 до 20% и содержанием воды в интервале от 5 до 90%.
В одном из вариантов осуществления композиция по настоящему изобретению содержит также один или несколько гелеобразователей для гидрофильных фаз. В качестве неограничительных примеров гелеобразователей, которые могут входить в композиции по настоящему изобретению, можно назвать сетчатый полимер "акрилаты/C10-30-алкилакрилат", реализуемый компанией Lubrizol под названием Pemulen TR-1 или Pemulen TR-2, карбомеры, реализуемые компанией Lubrizol под названием Ultrez 20®, Ultrez 10®, Carbopol 1382® или Carbopol ETD2020NF®, Carbopol 981 или также Carbopol 980, полисахариды с ксантановой камедью (в качестве неограничительных примеров), такие как Xantural180®, реализуемый компанией Kelco, или Satiaxane UCX 911, реализуемый компанией Cargill, поливиниловый спирт, такой как Polyvinil alcohol 40-88, реализуемый компанией Merck, геллановая камедь, реализуемая компанией Kelco под названием Kelcogel, гуаровая камедь, целлюлоза и ее производные, такой, как микрокристаллическая целлюлоза и карбоксиметилцеллюлоза натрия, реализуемые компанией FMC Biopolymer под названием Avicel CL-611, гидроксипропилметилцеллюлоза, в частности, продукт, реализуемый компанией Dow Chemical под названием Methocel E4M premium, или гидроксиэтилцеллюлоза, в частности, продукт, реализуемый компанией Ashland под названием Natrosol HHX 250®, группу алюмосиликатов магния, таких как Veegum K, реализуемый компанией Vanderbilt, группу акриловых полимеров, соединенных гидрофобными цепями, таких, как сополимер "PEG-150/децил/SMDI", реализуемый под названием Aculyn 44 (поликонденсат, содержащий по меньшей мере в качестве элементов полиэтиленгликоль со 150 или 180 моль этиленоксидных звеньев, дециловый спирт и метилен-бис-4-циклогексилизоцианат (SMDI), с содержанием 35 масс. % в смеси с пропиленгликолем (39%) и водой (26%)), группу модифицированных крахмалов, таких, как модифицированный картофельный крахмал, реализуемый под названием Structure Solanace, или их смеси и гелеобразователи из группы полиакриламидов, такие как смесь "сополимер акрилоилдиметилтаурата натрия/изогексадекан/полисорбат-80", реализуемая компанией Seppic под названием Sepineo P600® (или Simulgel 600 PHA®), смесь "полиакриламид/изопарафин C13-14/лаурет-7", такая как, например, смесь, реализуемая компанией Seppic под названием Sepigel 305, группу каррагинанов, разделенных, в частности, на четыре большие группы κ, λ, β, ω, таких как Viscarin® и Gelcarin®, реализуемые компанией IMCD.
Предпочтительно могут быть использованы гелеобразователи типа полиакриламидов, такие как "сополимер акрилоилдиметилтаурата натрия/изогексадекан/полисорбат-80", ввиду их хорошей совместимости с активным веществом и хорошей способности стабилизировать эмульсии с предпочтительными концентрациями в интервале от 0,005 до 10% и более предпочтительно от 0,5 до 4%.
В более предпочтительном варианте осуществления композиция по настоящему изобретению содержит также один или несколько консервантов, таких как метилпарабен, пропилпарабен, хлорид бензалкония, феноксиэтанол, реализуемый компанией Clariant под названием Phenoxetol, бензиловый спирт, реализуемый компанией Merck под названием "бензиловый спирт", бензоат натрия, реализуемый компанией Unipex под названием Probenz SP, сорбат калия, реализуемый компанией VWR под названием "сорбат калия", бензойная кислота, реализуемая компанией VWR под названием "бензойная кислота", 2-бром-2-нитропропан-1,3-диол, реализуемый компанией Jan Dekker International под названием Bronopol, хлоргексидин, реализуемый компанией Arnaud Pharmacie под названием "хлоргексидиндиглюконат, 20%-й раствор", хлоркрезол и его производные, этиловый спирт и диазолидинилмочевина. Эти консерванты могут быть использованы индивидуально или в сочетании для того, чтобы эффективно защищать композиции от любого бактериального загрязнения.
Под консервантом понимают любое вещество, способное противодействовать ухудшению продукта вследствие химического или микробиологического воздействия.
Консерванты, предпочтительно используемые по настоящему изобретению, представляют собой метилпарабен, пропилпарабен, бензиловый спирт, феноксиэтанол и сорбат калия. Они могут быть использованы в количестве от 0,01 до 5% и предпочтительно от 0,05 до 2%.
Композиция по настоящему изобретению может также содержать добавки, обычно используемые в области фармацевтических и косметических средств и позволяющие придавать указанной композиции специфические свойства. Специалисты в данной области техники могут адаптировать выбор этих добавок в зависимости от требуемого эффекта.
Среди добавок можно, например, неограничительным образом назвать добавки, используемые индивидуально или в сочетании:
- хелатообразующие агенты, такие как ЭДТА (этилендиаминтетрауксусная кислота) и ее производные или соли, дигидроглицерин, лимонная и винная кислоты, глюконолактон, реализуемый компанией Jungbunzlauer под названием "D-(+)-глюконо-дельта-лактон", или их смеси;
- антиоксиданты, такие как витамин E и его производные, такие как DL-альфа-токоферол или ацетат токоферола компании Roche, витамин C и его производные, такие как аскорбилпальмитат компании Roche, бутилгидрокситолуол, реализуемый компанией Clariant под названием Nipanox BHT;
- успокаивающие и/или снимающие раздражение средства, такие как сополимер PPG-12/SMDI, реализуемый компанией Bertek pharmaceuticals под торговым названием Polyolprepolymer-2, глицирретиновая кислота или ее производные, такие как, например, Enoxolone, реализуемый компанией BASF, гиалуроновая кислота в виде кислоты или в виде гиалуроната натрия, реализуемых компанией Contipro под торговым названием Hyal. Na PWD PH 15-51-45, аллантоин, реализуемый компанией Merck под названием Ronacare allantoine;
- любые другие добавки, обычно используемые в области фармацевтических и косметических средств и позволяющие придавать указанной композиции специфические свойства.
Добавки могут содержаться во внутренней структуре композиции по настоящему изобретению в количестве от 0 до 15% и предпочтительно от 0,1 до 10 масс. % от общей массы композиции.
Использованная технология позволяет получать очень тонко диспергированные эмульсии, причем получаемые масляные глобулы имеют размер преимущественно меньше 5 мкм. Способ получения состоит из двух основных стадий:
- первая стадия представляет собой стадию формирования промежуточной "гелевой" фазы, при этом речь идет об эмульсии типа O/W, содержащей увеличенное количество масляной фазы и имеющей вид прозрачного геля, состоящего из активного вещества, масляной фазы, сложного эфира сахарозы, полиола и воды;
- вторая стадия представляет собой стадию произвольного разбавления промежуточной "гелевой" фазы водной фазой для получения очень тонко диспергированной эмульсии "масло в воде". Конечная вязкость эмульсии зависит от степени разбавления. Стабильность эмульсии может быть усилена прибавлением гелеобразователя.
Способ получения является особенно чувствительным. Скорость и температура введения некоторых ингредиентов оказывают существенное действие на физическую стабильность эмульсий по настоящему изобретению.
Настоящее изобретение относится также к способу получения композиции по настоящему изобретению.
Общий способ получения эмульсии на основе "сложных эфиров сахарозы" описан далее.
A) Получение фазы "сложных эфиров сахарозы"
Солюбилизируют "сложные эфиры сахарозы" в части очищенной воды и части полиола.
B) Получение масляной/активной фазы
Солюбилизируют ретиноид в основном растворителе активного вещества, одном или нескольких масляных вспомогательных растворителей, одном или нескольких загустителях масляной фазы и минеральном масле. Для получения лучших результатов может быть рекомендовано нагревание масляной фазы во время ее получения.
C) Получение промежуточной "гелевой" фазы
Промежуточную "гелевую" фазу получают смешиванием фазы "сложных эфиров сахарозы" и масляной/активной фазы.
D) Получение водной фазы
К оставшемуся количеству воды прибавляют остаток полиола, а также другие водорастворимые добавки.
E) Получение крема
Конечную эмульсию получают разбавлением промежуточной фазы водной фазой. Специалисты в данной области техники могут адаптировать этот способ для прибавления требуемых ингредиентов или добавок.
Более предпочтительный способ получения эмульсий на основе "сложных эфиров сахарозы" описан далее.
A) Получение фазы "сложных эфиров сахарозы"
Солюбилизируют "сложные эфиры сахарозы" в части очищенной воды и части глицерина.
B) Получение масляной/активной фазы
Солюбилизируют соединение A в комплексе липофильных ингредиентов за исключением бензилового спирта и циклометикона, которые прибавляют в конце получения.
Для получения лучших результатов может быть рекомендовано нагревание масляной фазы во время ее получения.
C) Получение промежуточной "гелевой" фазы
Промежуточную "гелевую" фазу получают смешиванием фазы "сложных эфиров сахарозы" и масляной/активной фазы.
D) Получение водной фазы
К оставшемуся количеству воды прибавляют остаток глицерина, а также другие водорастворимые добавки.
К этой фазе может быть прибавлена гиалуроновая кислота в виде кислоты или в виде соли.
E) Получение крема
Конечную эмульсию получают разбавлением промежуточной фазы водной фазой и прибавлением бензилового спирта, циклометикона и гелеобразователя полиакриламидного типа.
Настоящее изобретение относится также к фармацевтической композиции для применения при лечении следующих патологий, в числе которых:
1) дерматологические заболевания, связанные с нарушением кератинизации, влияющей на дифференциацию и клеточную пролиферацию, предпочтительно для лечения простых, юношеских, полиморфных, розовых, узелково-кистозных, шаровидных, старческих угрей и угрей вторичного происхождения, таких как солнечные, медикаментозные или профессиональные угри;
2) нарушения кератинизации, в частности, ихтиозы, ихтиозиформные состояния, ламеллярный ихтиоз, болезнь Дарье, ладонно-подошвенные кератозы, лейкоплазии, красный отрубевидный волосяной лишай и лейкоплазиформные состояния, лишай кожи или слизистых оболочек (щеки);
3) дерматологические заболевания с иммуноаллергическим воспалительным компонентом, с нарушением или без нарушения клеточной пролиферации, и, в частности, любые формы псориаза, как кожи, так и слизистых оболочек или ногтей, и даже псориатический ревматизм, или также атопический дерматит и различные формы экземы;
4) кожные заболевания, вызванные облучением УФ-лучами, а также для лечения или борьбы с фотоиндуцированным или возрастным старением кожи или для уменьшения пигментации и актинических кератозов, или любых патологий, ассоциированных с возрастным или актиническим старением, таких как ксероз, пигментация и морщины;
5) любые состояния, связанные с доброкачественной пролиферацией кожи или эпидермиса, имеющей вирусное или невирусное происхождение, такие как простые бородавки, плоские бородавки, контагиозный моллюск и бородавчатая эпидермодисплазия, оральные или цветущие папилломатозы;
6) дерматологические нарушения, такие как дерматозы иммунного происхождения, такие как красная волчанка, буллезные заболевания иммунного происхождения и коллагенозы, такие как склеродермия;
7) следы атрофии эпидермиса и/или кожи, индуцированной кортикостероидами локального или системного действия, или любые другие формы атрофии кожи;
8) нарушения рубцевания, или для профилактики или лечения рубцов от растяжения кожи, или также для улучшения заживления рубцов;
9) заболевания грибкового происхождения на уровне кожи, такие, как эпидермофития стоп и отрубевидный лишай;
10) нарушения пигментации, такие как гиперпигментация, меланодермия, гипопигментация или витилиго;
11) раковые или предраковые состояния кожи или слизистых оболочек, такие, как актинические кератозы, болезнь Кейра, карциномы in-situ, кератоакантома и онкологические заболевания кожи, такие как базально-клеточная карцинома (BCC), спиноцеллюлярная карцинома (SCC) и лимфомы кожи, такие как лимфома T.
Композиция предпочтительно представляет собой фармацевтическую композицию для применения при лечении дерматологических заболеваний, связанных с нарушением кератинизации, влияющим на дифференцировку и пролиферацию клеток, нарушений кератинизации и дерматологических заболеваний с иммуноаллергическим воспалительным компонентом, с нарушением или без нарушения клеточной пролиферации.
Более предпочтительно композиция по настоящему изобретению представляет собой фармацевтическую композицию для применения при лечении угрей, ихтиозов, ихтиозиформных состояний, ладонно-подошвенного гиперкератоза или псориаза.
Согласно этим предпочтительным вариантам осуществления композиция по настоящему изобретению предпочтительно содержит соединение A.
В частности, композиция предпочтительно представляет собой фармацевтическую композицию для применения при лечении угрей, содержащую:
- масляную фазу, содержащую от 0,00001 до 1% 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновой кислоты (соединение A); от 0,2 до 5% основного растворителя соединения A; от 0,5 до 60% масляных вспомогательных растворителей соединения A; от 0,5 до 20% минеральных масел; от 0,1 до 10% загустителя масляной фазы; от 0 до 20% силиконового масла;
- водную фазу, содержащую от 0,1 до 15% эмульгаторов из группы сложных эфиров сахарозы; от 1 до 40% полиола; от 0,005 до 10% гелеобразователя водной фазы;
- от 0,01 до 5 масс. % системы консервантов;
- от 0,001 до 15% добавок.
Альтернативным образом, композиция предпочтительно представляет собой фармацевтическую композицию для применения при лечении ихтиозов, ихтиозиформных состояний, ладонно-подошвенного гиперкератоза или псориаза, состоящую из:
- масляной фазы, содержащей от 0,00001 до 1% 3''-трет-бутил-4'-(2-гидроксиэтокси)-4''-пирролидин-1-ил-[1,1';3',1'']-терфенил-4-карбоновой кислоты (соединение A); от 0,2 до 5% растворителя соединения A; от 0,5 до 60% масляных вспомогательных растворителей соединения A; от 0,5 до 20% минеральных масел; от 0,1 до 10% загустителя масляной фазы; от 0 до 20% силиконового масла;
- водной фазы, содержащей от 0,1 до 15% эмульгаторов из группы сложных эфиров сахарозы; от 1 до 40% полиола; от 0,005 до 10% гелеобразователя водной фазы;
- от 0,01 до 5 масс. % системы консервантов;
- от 0,001 до 15% добавок.
I - Примеры композиций
В приведенных далее примерах были определены характеристики полученных композиций в момент T0. Физическую и химическую стабильность композиций определяли после хранения при комнатной температуре (tкомн) и при +40°C через T+1 месяц и/или T+2 месяца, или T+3 месяца, или T+6 месяцев. Приборы, материалы и способы, использованные для определения этих характеристик, описаны далее.
- Количественное определение соединения A
- Приборы и материалы: ВЭЖХ
- Обработка результатов: содержание активного вещества выражено в относительных % по отношению к исходному содержанию в %, определенному в момент T0. Пределы, установленные для хорошей стабильности, составляют 95-105%.
- Осмотр внешнего вида
- Осмотр внешнего вида позволяет установить физическую целостность продуктов в момент T0 и после испытания на стабильность.
- Микроскопическое исследование
- Микроскопическое исследование позволяет оценить качество солюбилизации соединения A в момент T0, отсутствие кристаллизации с течением времени, а также размер глобул масляной фазы.
- Измерение pH
- Методика: измерения pH осуществляют при комнатной температуре после стабилизации всех проб в течение 24 ч в камере при 25°C.
- Вязкость
- Измерение вязкости позволяет оценить консистенцию полученных композиций.
- Приборы и материалы: Brookfield RV DVII+Pro.
- Методика: измерения осуществляют при комнатной температуре после стабилизации всех проб в течение 24 ч в камере при 25°C. Значение считывают через 1 минуту. Выбор шпинделя и скорости описаны далее для каждого примера композиций. Полученные значения выражены в сантипуазах (сП).
- Центрифугирование
- Центрифугирование позволяет оценить сопротивляемость композиций механическим напряжениям.
- Методика: в течение 30 минут при 5000 об/мин.
- Результат "соответствует" означает, что ни разделение фаз, ни выделение экссудата не выявлено.
Приведенные далее примеры неисчерпывающим образом представляют собой примеры составов композиций по настоящему изобретению, а также результаты по химической и физической стабильности.
I-1 - Примеры композиций, адаптированных для лечения угрей
Композиции примеров 1-11 могут быть изготовлены с содержанием от 0,001 до 0,03% соединения A.
Пример 1
|
|
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 2
|
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 3
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 4
|
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 5
|
|
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 6
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 7
|
|
Пример 8
|
|
Пример 9
|
|
Пример 10
|
|
Пример 11
|
I-2 - Примеры композиций, адаптированных для лечения ихтиозов, ихтиозиформных состояний, ладонно-подошвенного гиперкератоза или псориаза
Пример 12
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
Пример 13
|
|
|
|
Полученные результаты свидетельствуют о хорошей физической и химической стабильности активного вещества и композиции в целом во времени.
II. Чрескожное проникновение в случае кожи человека
II-1 - Методика оценки in vitro
Испытания in vitro осуществляют в диффузионных ячейках из стекла (называемых "ячейки Франца") или из тефлона в статическом или динамическом режиме. Ячейки состоят из двух отделений, при этом донорское отделение и рецепторное отделение разделено мембраной, которая может быть ориентирована вертикально или горизонтально.
Площадь поверхности мембран в общем случае находится в интервале от 1 до 4 см2, при этом они могут быть синтетическими (целлюлоза, полидиметилсилоксан и т.д.), но биопсийные образцы кожи животных или человека являются предпочтительными.
Отбор рецепторной жидкости может осуществляться через регулярные промежутки в течение 24 часов для обеспечения установления кинетики диффузии через кожу в случае, когда это оказывается необходимым. По истечении максимум 24 ч после нанесения в случае фармацевтических и косметических продуктов ячейки Франца демонтируют и исследуемое вещество определяют количественно в следующих отделах: остаток композиции, роговой слой, эпидермис, дерма и рецепторная жидкость. В этом случае может быть установлен массовый баланс, что позволяет определить "абсорбированное" количество (присутствующее в рецепторной жидкости), "проникшее" количество (присутствующее в живом эпидермисе и дерме) и "неабсорбированное" количество (присутствующее в остатке композиции и в роговом слое).
Исследование кинетики проникновения в кожу позволяет получить информацию, представляющую интерес в отношении поведения композиций с течением времени, и лучше охарактеризовать полученные композиции.
Таким образом, осуществляли два типа исследований на чрескожное проникновение в случае кожи человека ex vivo. В этих исследованиях соединение A испытывали в фазе композиции примера 1.
II-2 - Исследование на чрескожное проникновение в течение "унифицированного времени"
В этом исследовании композицию наносят для выдержки в течение 16 ч на поверхность кожи человека, полученной при абдоминальной хирургии и внесенной в ячейку Франца. По окончании выдержки соединение A количественно определяют в различных отделах кожи: в роговом слое, эпидермисе, дерме и рецепторной жидкости по аттестованной методике биоанализа.
Композицию примера 1 (эмульсия сложного эфира сахарозы, содержащая 100 мкг/г соединения A) по настоящему изобретению сопоставляли со сравнительным гелем, композиция которого состояла из 30% пропиленгликоля, 67,99% 95-96%-го этанола, 2% препарата Klucel HF и 0,01% соединения A.
Биоанализ осуществляли масс-спектрометрией в сочетании с электрораспылением в режиме ионизации положительных ионов на приборе Xevo (Waters).
Разработанные условия ЖХ/МС/МС позволили детектировать до 0,1% от нанесенной дозы в каждом из отделов (неабсорбированная доза, роговой слой, эпидермис, дерма и рецепторная жидкость).
Технические условия представлены в таблице, приведенной далее.
В "унифицированном по времени" исследовании этого типа приняты во внимание следующие параметры:
a. профиль распределения в различных отделах (количественные данные);
b. Проникновение в отдел "эпидермис+дерма" (количественные данные).
a - Профиль распределения в различных отделах
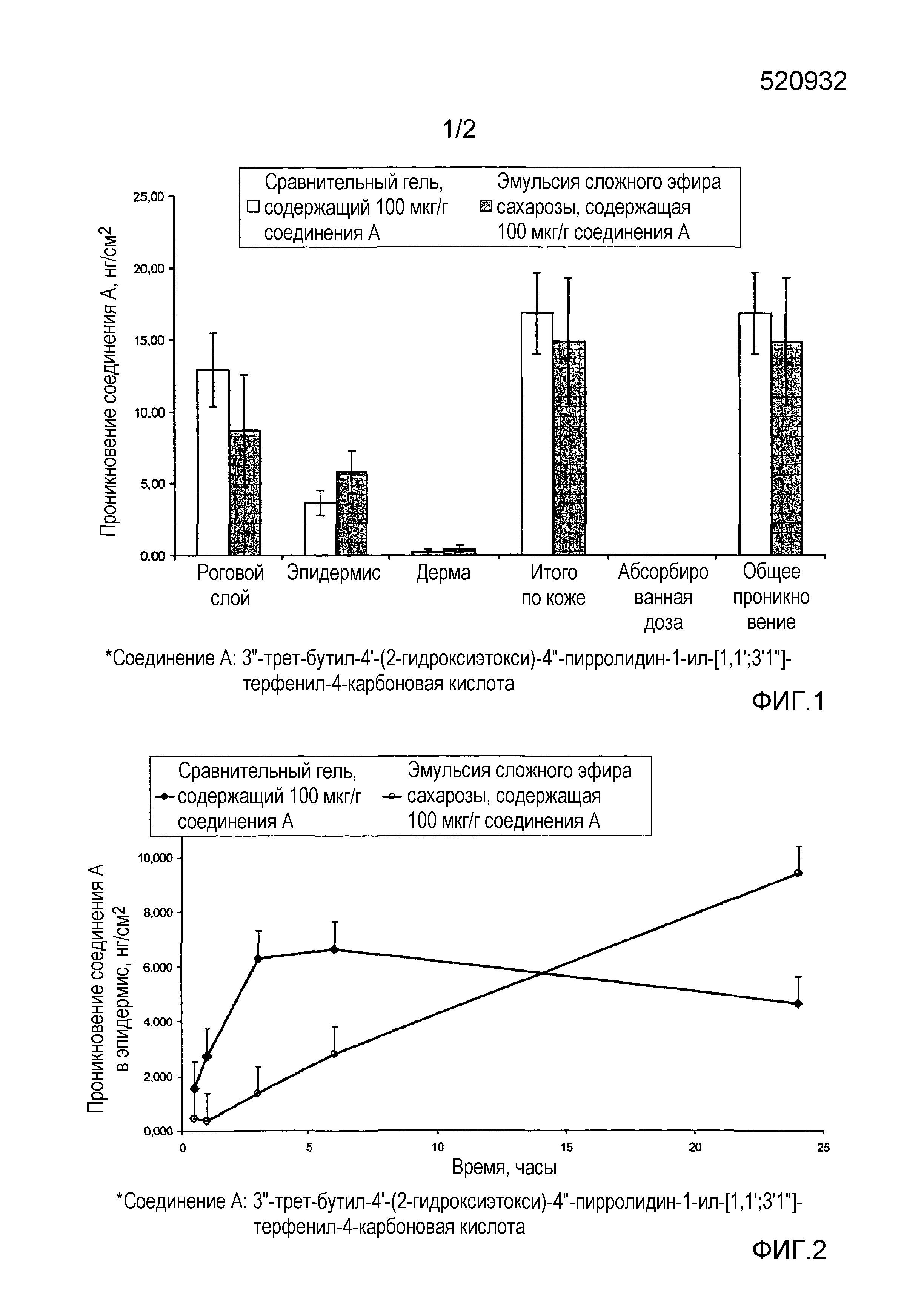
Результаты, полученные для профиля распределения соединения A в различных отделах кожи, представлены на фиг. 1.
Из фиг. 1 видно, что распределение между различными отделами имеет один и тот же порядок величин для 2 оцениваемых композиций.
Эти данные показывают предпочтительную локализацию и аккумулирование соединения A в роговом слое и в меньшей степени в эпидермисе.
b - Уровни проникновения в отдел "эпидермис+дерма"
Уровни проникновения для эмульсии по настоящему изобретению, содержащей 100 мкг/г (0,01%), находятся в интервале от 0,73 до 1,93 нг/см2. Эти значения имеют один и тот же порядок величин, что и для сравнительного геля.
Таким образом, можно сделать заключение, что соединение A хорошо высвобождается после нанесения на кожу и проникает в эпидермис.
II-3 - Исследование кинетики проникновения
В исследовании этого типа количественно определяют проникновение активного вещества в каждом отделе кожи через 0,5, 1, 3, 6 и 24 ч после нанесения. Затем определяют характеристики кинетики проникновения в каждом отделе.
Композицию примера 1 (эмульсия сложного эфира сахарозы, содержащая 100 мкг/г соединения A) по настоящему изобретению сопоставляли со сравнительным гелем, композиция которого состояла из: 30% пропиленгликоля, 67,99% 95-96%-го этанола, 2% препарата Klucel HF и 0,01% соединения A.
Подробности нанесения на кожу представлены в таблице, приведенной далее.
|
Количество активного вещества в каждом отделе в каждый момент времени определяли способом ЖХ/УФ или способом ЖХ/МС. Способ биоанализа был аттестован с целью определения не менее 0,1% от нанесенной дозы в каждом отделе.
В исследовании этого типа приняты во внимание следующие параметры:
a. профиль кинетики проникновения в эпидермис (количественные данные);
b. начальная скорость проникновения в эпидермис;
c. максимальное количество, проникшее в эпидермис.
a. Профиль кинетики проникновения в эпидермис (фиг. 2)
Профиль кинетики проникновения соединения A, использованного в сравнительной композиции (гель) и в эмульсии по настоящему изобретению, представлен на фиг. 2. В частности, на фиг. 2 представлено количество соединения A, которое проникает в эпидермис в зависимости от времени.
Проникновение соединения A, полученное для сравнительной композиции (гель), демонстрирует обычную кинетику с аккумулированием в отделе в ходе первых часов с последующим достижением плато. В противоположность этому, кинетика проникновения, наблюдаемая после нанесения эмульсии по настоящему изобретению, стремится быть возрастающей и линейной во времени.
Как видно из параграфа II.2 ("Исследование на чрескожное проникновение в течение "унифицированного времени"), эти две композиции обладают уровнями проникновения через 16 ч одного и того же порядка величин. Это исследование кинетики показывает, что даже с уровнями проникновения, близкими к уровням в исследовании кинетики в течение унифицированного времени, композиция по настоящему изобретению имеет профиль кинетики проникновения, отличающийся от сравнительного геля, с постепенным аккумулированием соединения A с течением времени. Таким образом, нанесение эмульсии по настоящему изобретению позволяет значительно изменять кинетику проникновения соединения A в кожу. Эта кинетика проникновения является возрастающей и линейной и приближается к кинетике нулевого порядка с учетом кинетики диффузии активного вещества через синтетическую мембрану или кожу после нанесения лекарственного средства.
b. Начальная скорость кинетики
Значения начальной скорости кинетики или наклон находятся в интервале от 0,45 до 0,54 нг/см2/ч.
c. Максимальное количество, проникшее в эпидермис
Максимальное количество, проникшее в эпидермис, находится в интервале от 9,40 до 15,50 нг/см2.
Это исследование проникновения неожиданным образом показало, что композиции по настоящему изобретению обладали особыми характеристиками чрескожного проникновения с кинетикой проникновения соединения A в эпидермис, стремящейся быть линейной, что позволяет обеспечивать высвобождение ретиноида в эпидермисе после нанесения постепенным образом.
II-4 - Переносимость кожей
В этом исследовании:
- 10 пациентов получали по 2 г сравнительного геля, наносимого на 1000 см2 в течение 4 недель;
- 10 пациентов получали по 2 г крема A (пример 1 по настоящему изобретению), наносимого на 1000 см2 в течение 4 недель.
В ходе исследования исследователи имели возможность менять зону нанесения в случае слишком сильного раздражения.
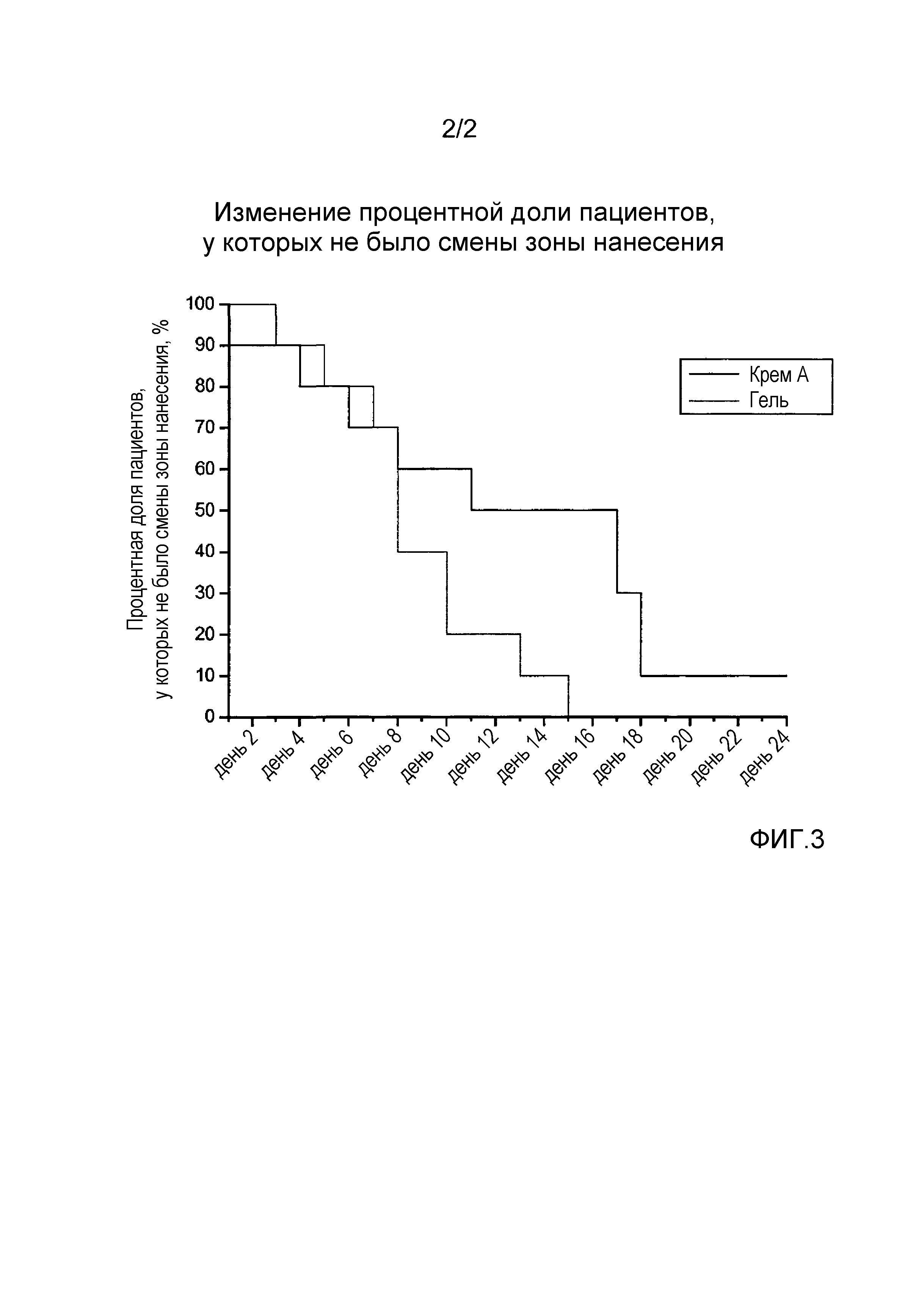
Графики на фиг. 3 отображают процентную долю пациентов, у которых не было смены зоны нанесения, в зависимости от дня нанесения. Например, в день 5 для 80% субъектов, получавших крем A, не было необходимости менять зону нанесения. Иначе говоря, у 20% пациентов, получавших крем A, появилось раздражение, требовавшее смены зоны нанесения.
Изменение процентной доли пациентов, у которых не было смены зоны нанесения
|
|
Таким образом, установлено, что раздражение появляется более быстро у пациентов, которые получали сравнительный гель, чем у пациентов, которым получали крем по настоящему изобретению. Начиная с дня 9, наблюдается четкая разница. Таким образом, композиция по настоящему изобретению переносится лучше, чем сравнительный гель.