ХИМИЧЕСКИЙ ПУТЬ СИНТЕЗА МАТЕРИАЛОВ ДЛЯ ЛИТИЙ-ИОННОГО АККУМУЛЯТОРА
Вид РИД
Изобретение
Перекрестная ссылка на родственную заявку
Эта заявка заявляет притязания на приоритет заявки на патент US № 13/865,963, поданной 18 апреля 2013.
Область техники, к которой относится изобретение
Данная заявка относится к технологии производства материалов для литий-ионных аккумуляторов.
Уровень техники
Обычный LiMnPO4 является материалом, показывающим низкую электропроводность. В результате этот материал ограничен или требователен к условиям синтеза и способам получения электродов для применения в литий-ионных аккумуляторах. Даже если использовать углеродное покрытие, чтобы улучшить электрохимические свойства, одно только углеродное покрытие не может по существу решить вопрос о природе низкой электропроводности материала LiMnPO4.
Кроме того, углеродное покрытие может ограничить время хранения конечного материала, и природа покрытия может быть разрушена во время суспензионного способа изготовления особенно, когда используют растворитель на водной основе. Так как покрытие находится только на поверхности материала, при изготовлении электродов всегда требуется целостность покрытия, и это увеличивает шанс нестабильных (несогласованных) характеристик конечной батареи.
Краткое описание чертежей
Множество аспектов изобретения могут быть лучше поняты с отсылкой к следующим фигурам. Компоненты на чертежах не обязательно выполнены в масштабе, особое внимание при размещении обращено на ясность пояснения принципов определенных вариантов осуществления данного изобретения. Кроме того, на чертежах ссылочные номера определяют соответствующие части для нескольких видов.
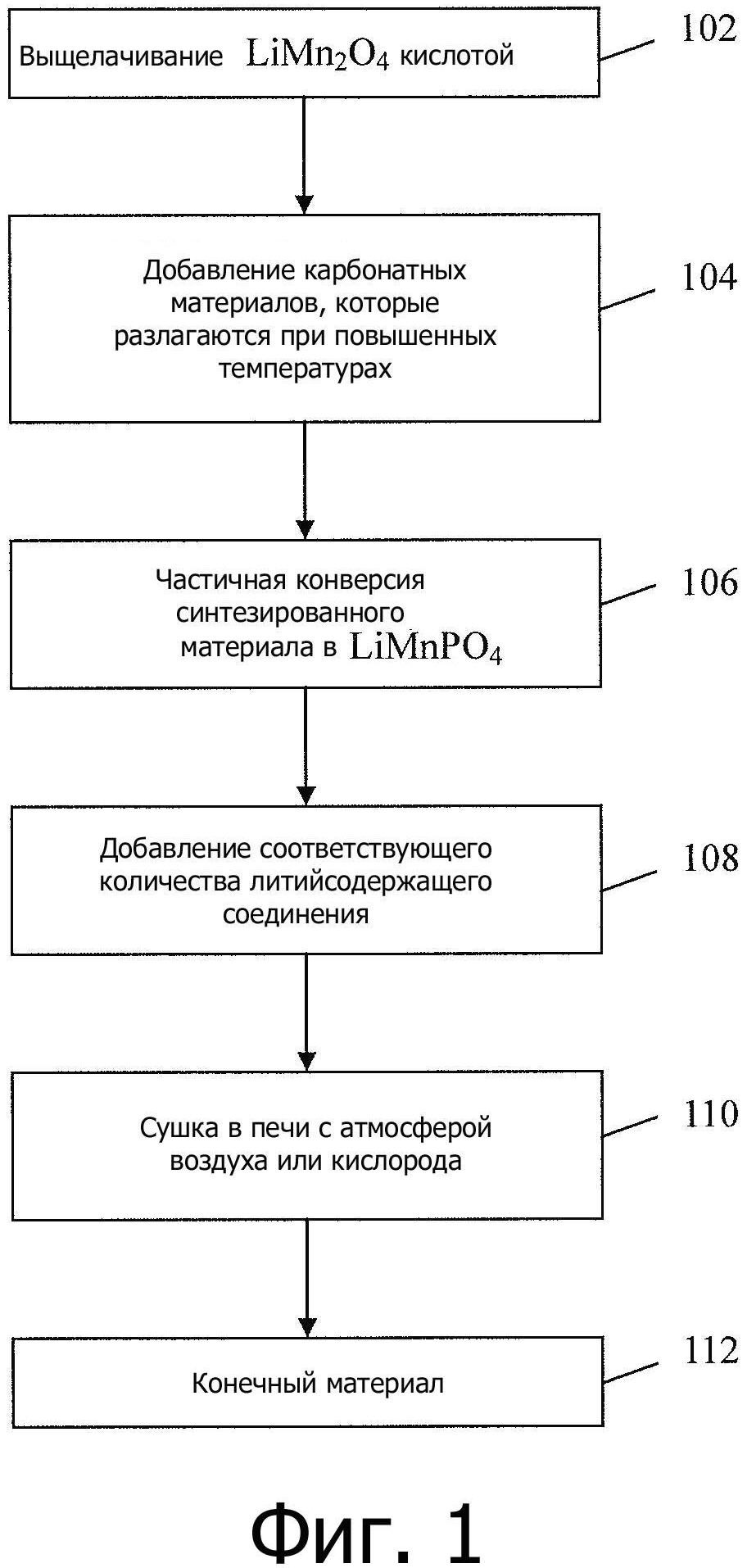
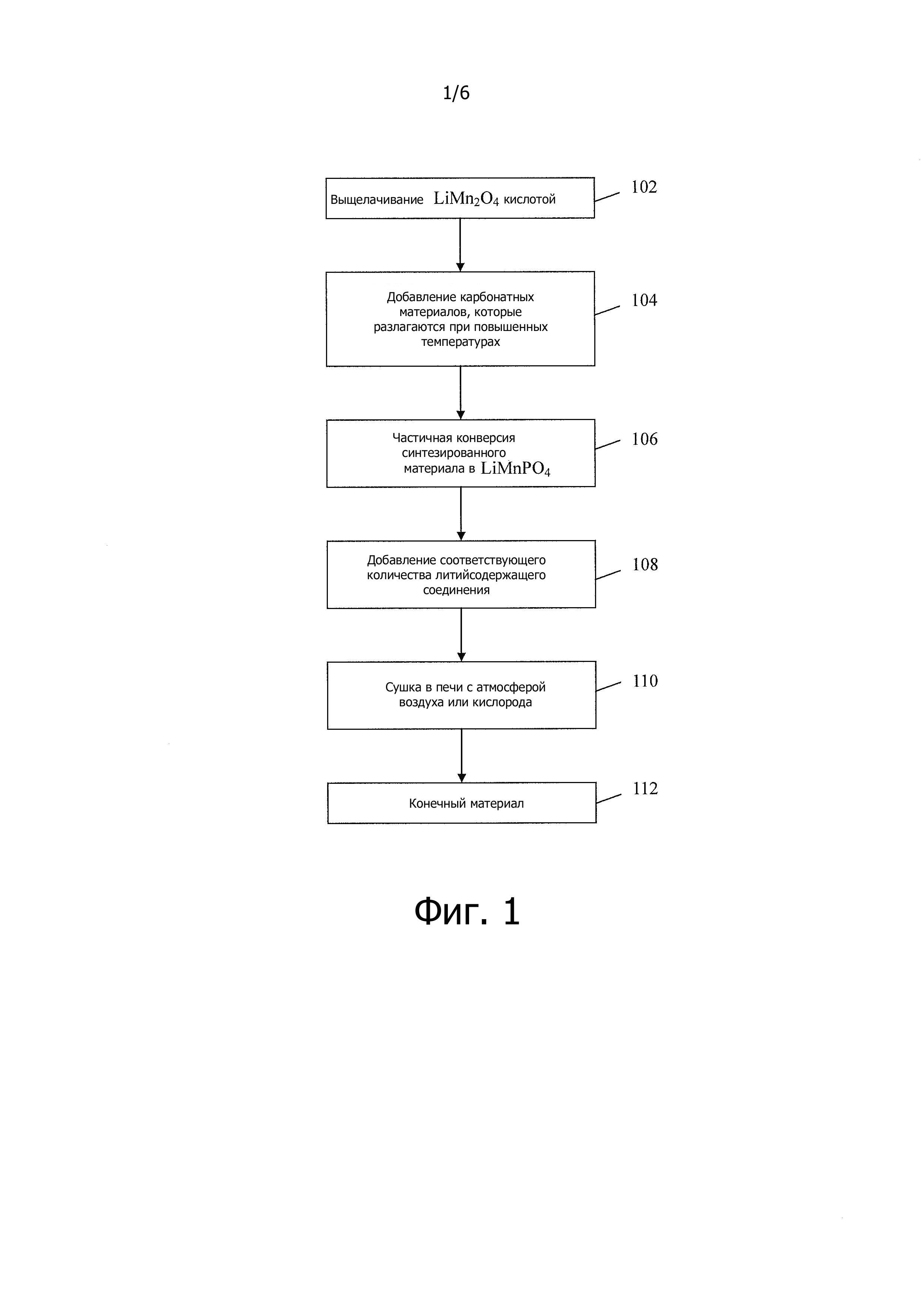
Фиг. 1 показывает схему последовательности технологического процесса, поясняющую вариант осуществления типичного процесса синтеза материалов для литий-ионных аккумуляторов в соответствии с данным изобретением.
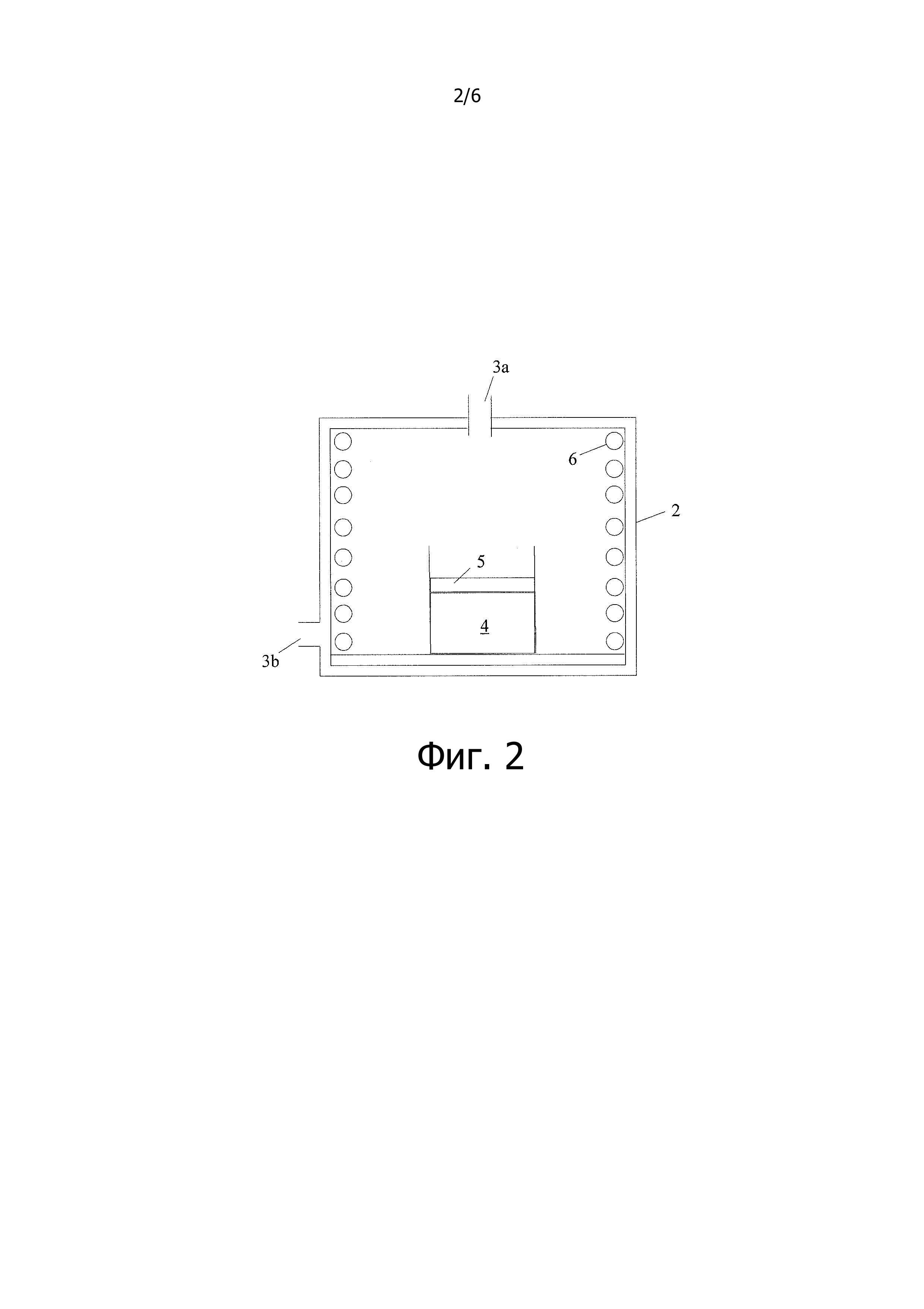
Фиг. 2 показывает схему типичной печи и окружающей среды термической обработки для синтеза материалов в соответствии с данным изобретением.
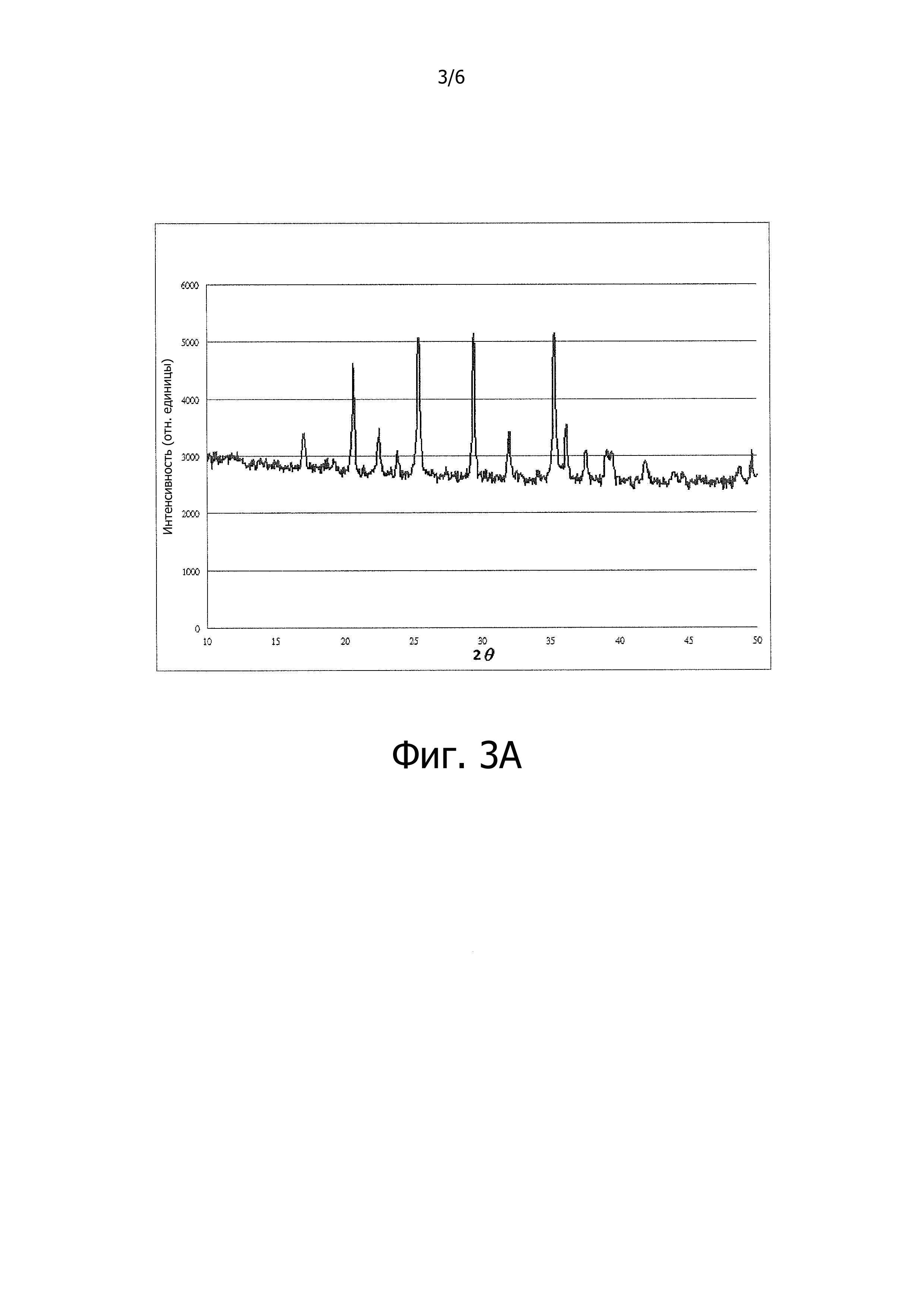
Фиг. 3A-3B показывают диаграммы, поясняющие результаты исследования синтезированных материалов, используя дифракцию рентгеновских лучей в соответствии с вариантами осуществления данного изобретения.
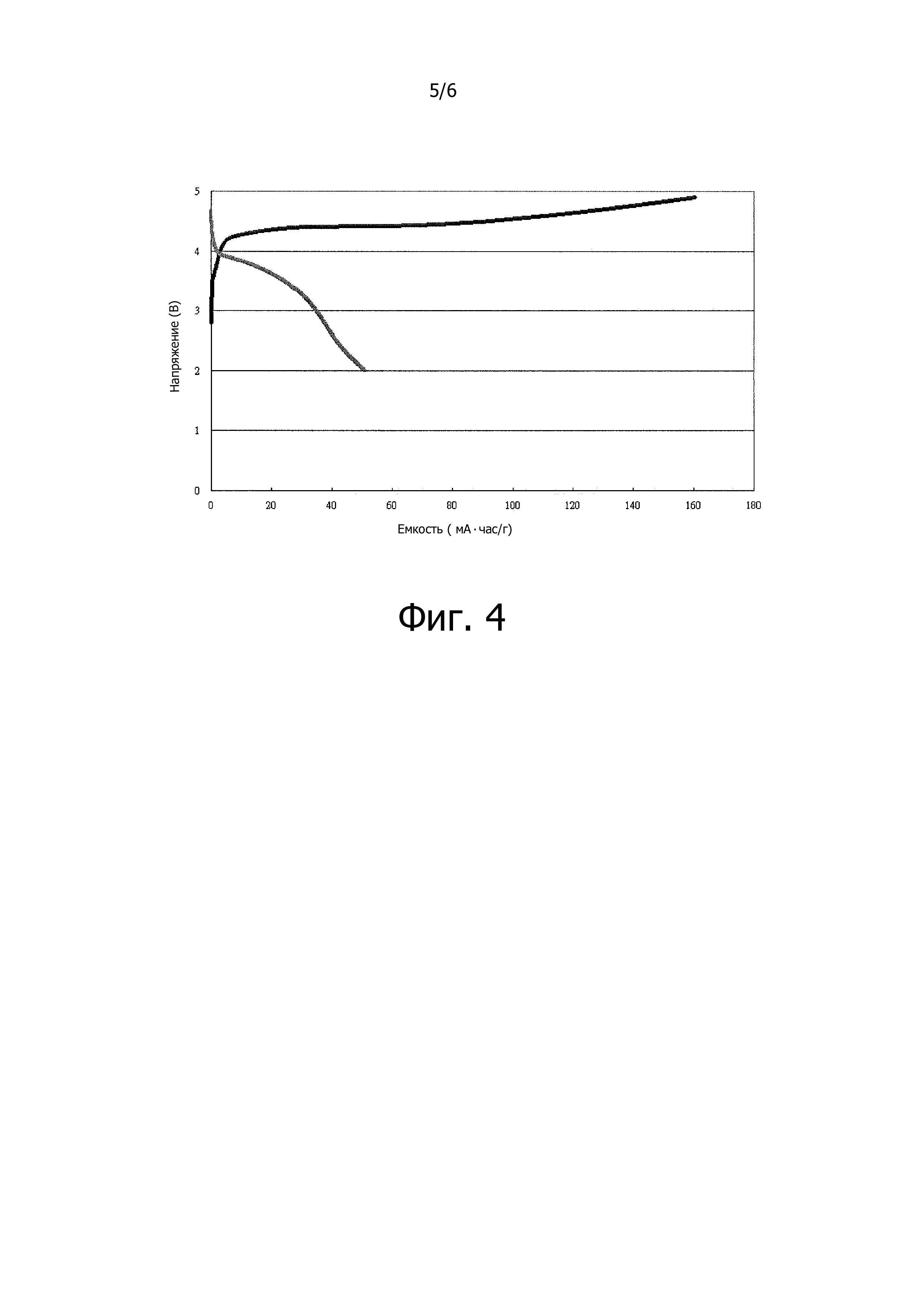
Фиг. 4 показывает результаты изучения емкости заряда синтезированных материалов в соответствии с вариантами осуществления данного изобретения.
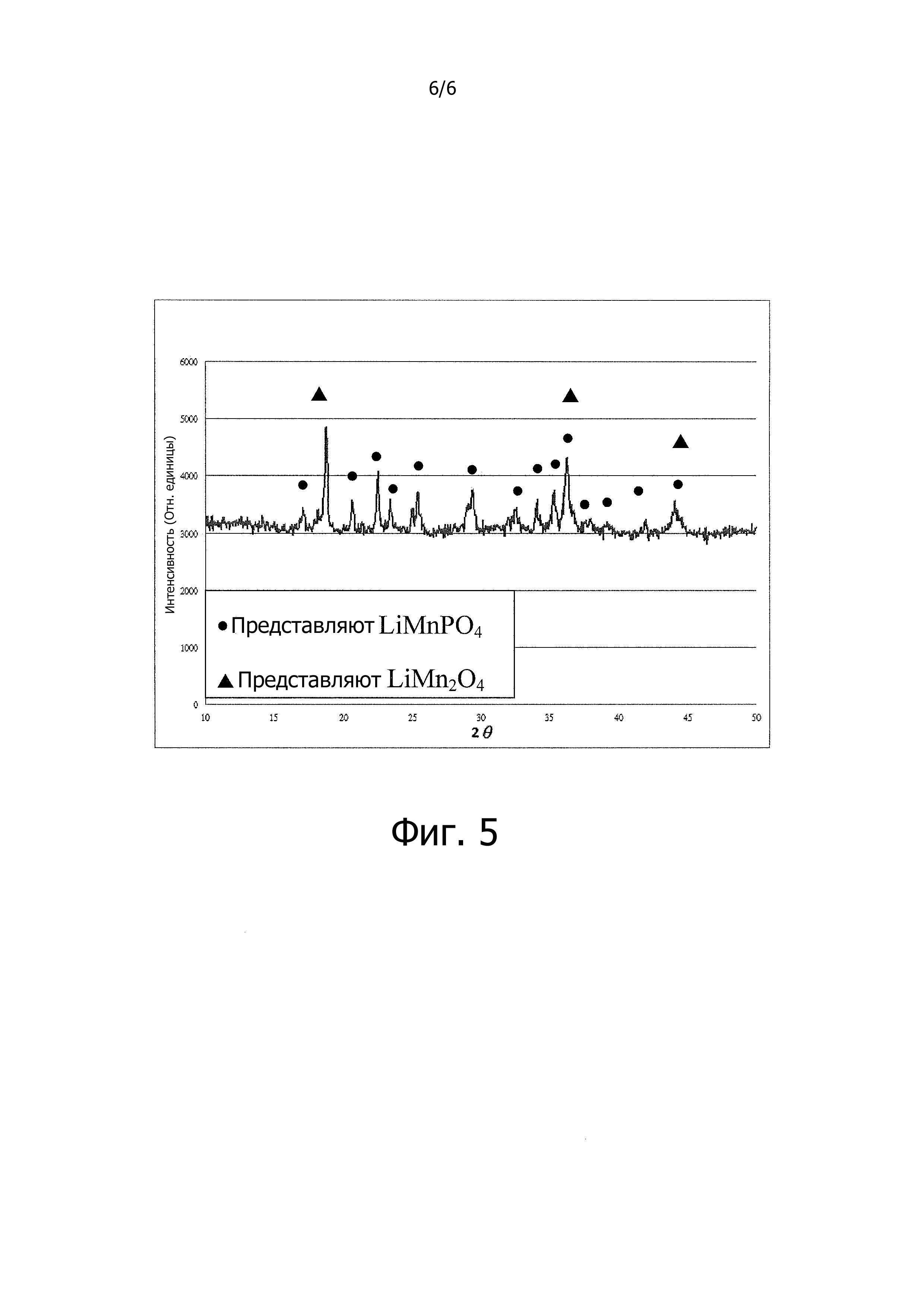
Фиг. 5 показывает диаграмму, поясняющую результаты исследования синтезированных материалов, используя дифракцию рентгеновских лучей в соответствии с вариантами осуществления данного изобретения.
Подробное описание
Здесь раскрыты определенные варианты осуществления нового химического пути синтеза материалов для литий-ионных аккумуляторов. В одном таком варианте осуществления активный материал батареи LiMn2O4 используют в качестве исходного предшественника. Соответственно, предложен новый путь синтеза, показывающий, как сделать композиционные материалы LiMnPO4 при низких температурах, используя LiMn2O4 в качестве предшественника синтеза. Осуществляя этот путь, электропроводность конечного материала увеличивают в присутствии остаточного LiMn2O4. Далее, при помощи синтеза фосфатного материала при низких температурах можно синтезировать материалы с двойным активным материалом батареи, таким образом достигая возможности адаптации физических и электрохимических свойств синтезированных материалов. Кроме того, варианты осуществления данного изобретения рассматривают и учитывают системы материалов с многократно активным материалом в применении батареи.
В соответствии с данным изобретением, LiMn2O4 со структурой шпинели может использоваться в качестве материала-предшественника в различных вариантах осуществления. Считают, что, так как LiMn2O4 со структурой шпинели устойчив при высоких температурах, легко синтезировать смешанный оксид-фосфатный материал, используя материал со структурой шпинели в качестве предшественника. Например, синтез Li(Mn1/2Fe1/2)PO4 может быть достигнут, используя Li(Mn1/2Fe1/2)2O4 в качестве исходного предшественника.
Дополнительно, для различных вариантов осуществления контроль содержания фосфора может определять отношение предшественника к конечному материалу. Это может быть полезно для адаптации электропроводности, а также электрохимической емкости конечного материала. Например, легкий контроль содержания фосфора в конечном материале придает гибкость при адаптации физических и электрохимических свойств конечного материала.
Как обсуждается ниже, раскрыт вариант осуществления нового пути синтеза, показывающий, как сделать LiMnPO4 или композиционные материалы LiMnPO4- LiMn2O4 при низких температурах (например, меньше чем 400°C, и может быть даже столь низкой как 120°C), используя LiMn2O4 в качестве предшественника при синтезе. Низкотемпературный синтез создает возможность поддержания структуры материалов-предшественников (и таким образом, электрохимической активности) в конечном материале.
В общем, вариант осуществления нового способа синтеза материалов содержит несколько важных стадий, как показано на фиг. 1. Способ начинается с выщелачивания LiMn2O4, с использованием кислоты на стадии 102. Затем карбонатные материалы, которые разлагаются при повышенных температурах, добавляют на стадии 104. Здесь термин «повышенные температуры» означает, что используют температуры, которые достаточны для разложения карбонатных материалов, тем самым увеличивая электропроводность материалов.
Если вернутся к чертежам, синтезированный материал частично преобразуют в LiMnPO4 на стадии 106; и соответствующее количество литийсодержащего соединения добавляют на стадии 108, как обсуждается далее ниже. Затем синтезированный материал высушивают, используя печь с атмосферой воздуха или кислорода на стадии 110, чтобы получить или генерировать конечный материал на стадии 112.
Фиг. 2 показывает конструкцию печи и среду термической обработки для синтеза материалов. Фиг. 2 показывает реактор 1, который открыт для воздуха в печи 2. Печь открывают для атмосферы в 3a и 3b, чтобы поддержать, в основном, атмосферное давление в печи. Поток газов, поступающий в печь или выходящий из печи, зависит от циклов нагревания и охлаждения печи и материалы в них вступают в химические реакции. Воздух свободно поступает в печь, и воздух и/или продукты химической реакции материалов 4 в реакторе 1 свободно выходят из печи. Материалы 4 в реакторе 1 реагируют химически во время стадий нагревания, чтобы получить катодные материалы в соответствии с данным изобретением. Материалы 4 в реакторе 1, которые встречаются с воздухом, находящимся в печи, покрываются слоем высокотемпературного инертного отложения 5, которое является пористым для воздуха и улетучивающихся газов, вызванных стадией нагревания. Нагревательные змеевики печи указаны как 6.
Далее следуют примеры путей синтеза в соответствии с вариантами осуществления данного изобретения.
Пример 1
Синтез LiMnPO4 - LiMn2O4 = 1,8:0,1 мольное отношение (эквивалентно 95 мол. % LiMnPO4 и 5 мол. % LiMn2O4)
Суммарная реакция может быть просто описана ниже как:
1 LiMn2O4 + 1,8 H3PO4 + 0,9 Li ------> 1,8 LiMnPO4 + 0,1 LiMn2O4 + (H и O).
Методики синтеза детализированы ниже:
1. Первоначально растворяют щавелевую кислоту (например, 22,5 г) (0,25 моль) в КМЦ (карбоксилметилцеллюлоза раствор 1 вес. %) 40 г при 60°C.
2. Добавляют LiMn2O4 (например, 181 г) (1 моль) к раствору. При этом фиолетовый оттенок пены указывает на растворения Mn в растворе. Выдерживают раствор при 80°C в течение двух часов до завершения реакции.
3. Добавляют соответствующее количество карбонатных материалов. В типичном случае в раствор добавляют сахарозу (например, 67,5 г).
4. Затем охлаждают раствор, используя ледяную ванну.
5. Затем добавляют фосфорную кислоту (например, 207 г) (1,8 моль, 85% в H3PO4) к раствору медленно (за два часа) в ледяной ванне.
6. Затем нагревают раствор до 50°C в течение двух часов (в этот момент образуется зеленоватый порошок).
7. Охлаждают раствор снова и добавляют (например, 50 г) (1,1 моль) муравьиной кислоты. Затем добавляют Li2CO3 (например, 33,3 г) (0,9 моля лития) в раствор. Во время добавления Li2CO3 к раствору образуются пузырьки и раствор становится суспензией.
8. После добавления Li2CO3 температуру суспензии поднимают снова до 50°C. В это время наблюдают вспенивание.
9. После 2 часов вспенивания очень вязкий раствор высушивают при 120°C в течение 10 часов.
Стадию 1 и 2 (выше) используют для выщелачивания Mn из LiMn2O4. Кислота, использованная на стадии 1, не ограничивается щавелевой кислотой. Возможны муравьиная кислота, уксусная кислота, соляная кислота и азотная кислота. Однако органические кислоты предпочтительны в некоторых вариантах осуществления.
Стадию 3 (выше) используют при добавлении карбонатного материала. Карбонатный материал не ограничивают сахарозой. Метилцеллюлоза (МЦ), метилкарбоксиметилцеллюлоза (КМЦ), ацетилцеллюлоза, крахмал, стирол-бутадиеновый каучук - все возможны для достижения той же самой цели (увеличения электропроводности материала после разложения). Фактически, синтез материалов может не включать добавление карбонатного материала, если соответствующее количество и распределение LiMn2O4 присутствуют в конечном материале.
Стадии 4, 5, и 6 (выше) используют для получения MnPO4. Эти стадии управляют процентом остающегося LiMn2O4 или процентом образующегося MnPO4. Стадии 7, 8, и 9 используют для получения LiMnPO4 в форме пены. Вспенивание может быть полезным для создания материалов с открытой пористостью.
Для сравнительного анализа конечный материал был исследован дифракцией рентгеновских лучей (XRD), и результат XRD показан на фиг. 3A-3B. Уточнение по Ритвельду проводили по результатам XRD, используя пространственную группу Pmnb(62). Как определено, параметры кристаллической решетки были a = 6.10287, b = 10.4603, и c = 4.74375 с объемом кристаллической ячейки = 302.8 (Е3) и плотностью = 3.4401 г/см3. В этом случае след фазы LiMn2O4 не очевиден на графике XRD. Размер частиц и анализы БЭТ предшественника LiMn2O4 и конечного материала также показан в таблице 1 для сравнений развития физических свойств, показанных материалом во время пути синтеза.
Tаблица 1
|
† Конечный материал получали после сушки образца при 120°C в течение 10 часов.
‡ После тепловой обработки 260°C в течение 2 часов.
Из таблицы 1 можно увидеть, что распыление материала-предшественника имело место во время синтеза. Размер частиц уменьшался с увеличением удельной поверхности. Дальнейшая термическая обработка конечного материала при 260°C в течение 2 часов на воздухе показала, что умеренное увеличение размера частиц сопровождается значительным увеличением удельной поверхности (пожалуйста, см. таблицу 1). Этот результат указывает, что агломерация материала не была обязательной при 260°C, но разложение карбонатного материала способствует значительному увеличению удельной поверхности. Следует заметить, что разложение при 260°C могло помочь электропроводности материала вследствие наличия электропроводящего углерода, возникающего при карбонатном разложении материалов.
Пример 2
Электрохимическая характеристика LiMnPO4 - LiMn2O4 = 1,8:0,1 мольное отношение (эквивалентно 95 мол. % LiMnPO4 и 5 мол. % LiMn2O4)
Для получения электродов, 5 г активного материала, 1 г сажи Супер-П (Super-P), и 0,3 г СБК (стирол-бутадиеновый каучук) используют при создании суспензии. После нанесения покрытия с использованием ракли покрытый электрод высушивают при 110°C в течение 3 часов, затем следует штамповка электрода. После вакуумной сушки снова при 110°C в течение ночи, электроды переносят в перчаточный бокс для испытания сборки ячеек. Тестовая ячейка является ячейкой с тремя электродами и с литием в качестве электрода сравнения. Нагрузка электрода составляет 6 мг, и содержание активного вещества составляет 81,3%. Используемая С-скорость составляет около C/10, и комнатная температура составляет около 23°C.
Получают емкость заряда 160,5 мАч/г и емкость разряда 51 мАч/г, как показано в результатах исследования на Рис. 4. Считают, что соответствующий коэффициент использования тока составляет 31,7%. Так как испытательная ячейка была заряжена до 4,9 В, большее или меньшее разложение электролита во время зарядки может привести к низкому коэффициенту использования тока.
Пример 3
Синтез LiMnPO4-LiMn2O4 = 1:0,5 мольное отношение (эквивалентно 67 мол. % LiMnPO4 and 33 мол % LiMn2O4)
Полная реакция может быть просто описана ниже как:
1 LiMn2O4 + 1 H3PO4 ------> 1Li(1-0,5x)MnPO4 + 0,5 LixMn2O4 , где
х представляет недостаток лития. Методики синтеза детализированы ниже:
1. Первоначально растворяют щавелевую кислоту (например, 11,25 г) (0,125 моль) в КМЦ (карбоксилметилцеллюлоза раствор 1 вес. %) (например, 40 г) при 80°C.
2. Добавляют LiMn2O4 (например, 90,5 г) (0,5 моль) к раствору. При этом фиолетовый оттенок пены указывает на растворение Mn в растворе. Раствор выдерживают при 80°C в течение двух часов, до завершения реакции.
3. Добавляют соответствующее количество карбонатных материалов. В типичном случае в раствор добавляют сахарозу (например, 33,75 г).
4. Затем охлаждают раствор, используя ледяную ванну.
5. Затем добавляют фосфорную кислоту (например, 57,65 г) (0,5 моля, содержание 85% в H3PO4) к раствору медленно (за два часа) в ледяной ванне.
6. Затем нагревают раствор до 50°C в течение двух часов (в этот момент образуется зеленоватый порошок).
7. Ожидают до тех пор, пока раствор не станет клейким.
8. Термическую обработку проводят, направляя материал-предшественник непосредственно в печь при 380°C в течение 10 часов в атмосфере кислорода.
Для сравнительного анализа конечный материал был исследован XRD, и результат XRD показан на фиг. 5. Из результата XRD можно идентифицировать, что конечный материал состоит из двух фаз (сосуществуют LiMnPO4 и LiMn2O4), которые присутствуют одновременно.
Из приведенного выше ясно, что низкотемпературный синтез в соответствии с вариантами данного изобретения позволяет сосуществование LiMnPO4 и LiMn2O4. Электрохимические данные показывают потенциал синтеза LiMnPO4 в присутствии LiMn2O4, с использованием LiMn2O4 в качестве исходного предшественника. Преимущественно, присутствие LiMn2O4 в композиционном материале LiMnPO4/LiMn2O4 обеспечивает электрохимическую активность, наряду с электропроводящей способностью в композиционном материале. Типичный композиционный материал для литий-ионного аккумулятора в соответствии с данным изобретением может быть в форме (x)LiMnPO4/(1-x) LiMn2O4, где x изменяется от 0,67 мол. % до 0,99 мол. %.
Любые описания способа технологического процесса следует понимать как примеры стадий способа и альтернативные воплощения включены в рамки данного изобретения, в котором стадии могут быть выполнены в порядке, отличном от показанного или обсужденного, включая по существу тот же или обратный порядок, в зависимости от функциональности, что ясно для специалистов в области техники.
Следует подчеркнуть, что вышеописанные варианты осуществления являются просто возможными примерами выполнения, сформулированными для ясного понимания принципов данного изобретения. Различные изменения и модификации могут быть сделаны в вышеописанных вариантах осуществления без отклонения в основном от сущности и принципов данного изобретения. Все такие изменения и модификации предназначены для включения в рамки этого изобретения и защищены следующей формулой изобретения.