Результат интеллектуальной деятельности: N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ
Вид РИД
Изобретение
Изобретение относится к органической химии, конкретно к новым бис(фуранолабданоидам), формулы (Iа, б)
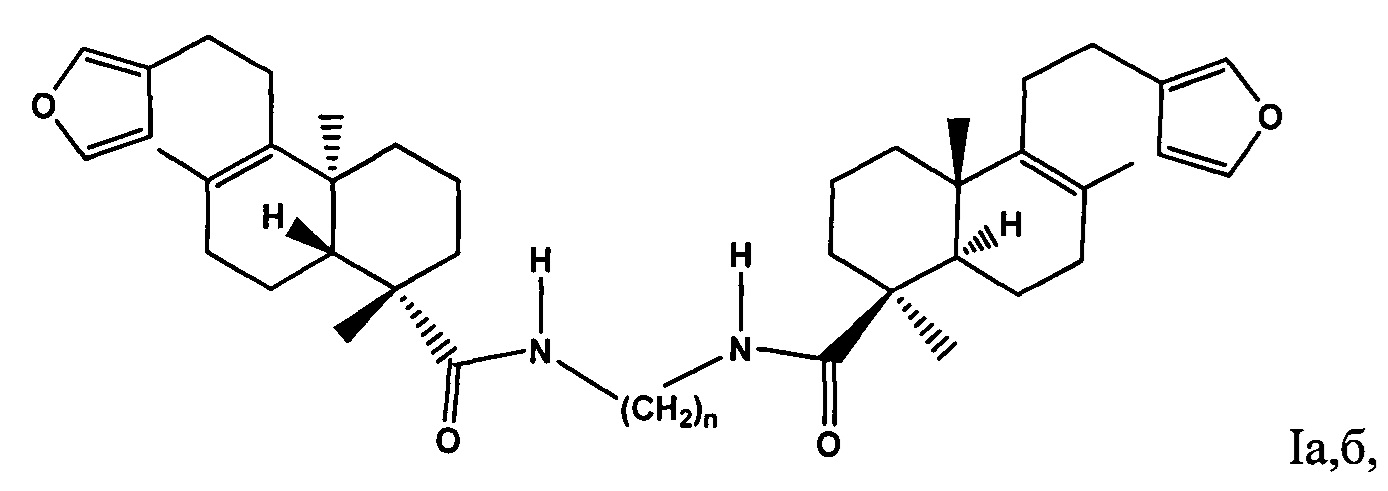
где n=2 (Ia); n=6 (Iб),
обладающим противоопухолевой активностью.
Указанные свойства позволяют предполагать возможность использования соединений в медицине в качестве фармацевтического препарата.
Химическая терапия онкологических заболеваний является одной из основных проблем современной медицины, что связано как с недостаточной эффективностью многих препаратов, так и с сопутствующими их применению побочными эффектами. Кроме того, опухолевые клетки, пережившие химиотерапию, нередко проявляют лекарственную устойчивость к широкому спектру препаратов. Таким образом, поиск химиотерапевтических лекарственных средств новых структурных типов остается важной и актуальной задачей. Не менее актуальной является проблема изыскания агентов, способных предотвращать малигнизацию доброкачественных опухолей путем снижения их инвазивного потенциала.
Полезными соединениями в профилактике и лечении ряда заболеваний, включая рак, признаны растительные дитерпеноиды, обладающие также противомикробными, противогрибковыми, противопаразитарными, противовирусными, антиаллергенными, спазмолитическими, гипогликемическими, противовоспалительными, иммуномодулирующими свойствами [Rabi Т., Bishayee A. Breast Cancer Res. Treat. - 2009. - V. 115. - P. 223-239]. В последние годы они привлекают внимание как ингибиторы тканевой инвазии и индукторы апоптоза опухолевых клеток, что делает перспективным поиск в этом ряду цитостатических агентов для противоопухолевой терапии [Fenteany G., Zhu S. Cur. Top. Med. Chem. - 2003, - V. 3. - P. 593-616]. Соединения обоих типов найдены в ряду сестертерпеноидов и лабдановых дитерпеноидов. В качестве перспективных ингибиторов инвазии опухолевых клеток рассматриваются хинон- и гидрохинонсодержащие ди- и сестертерпеноиды морских губок - стронгулофорин-26 (II) [Warabi К., Patrik В.О., Austin P., Roskelley C.D., Roberge М., Andersen R.J. J. Nat. Prod. - 2007. - V. 70. - P. 736-740] и авинозол (III) [Diaz-Marrero A.R., Austin P., Van Soest R., Matainaho Т., Roskelley C.D., Roberge M, Andersen R.J. Org. Lett. 2006. - V. 8. - P. 3749-3752]. Соединения проявляют значительную цитотоксичность в отношении опухолевых клеток, а также обладают антиинвазивной активностью в тестах связывания: IC50 (доза, в которой ингибируется инвазия 50% опухолевых клеток) соединений (II, III) составляет 1-50 мкг/мл (клетки рака груди MDA-MB-231) и 20-50 мкг/мл (клетки карциномы LS 174Т) [Diaz-Marrero A.R., Austin P., Van Soest R., Matainaho Т., Roskelley C.D., Roberge M., Andersen R.J. Org. Lett. - 2006. - V. 8. - P. 3749-3752]. Однако соединения (II, III) являются малодоступными метаболитами.
Активным противоопухолевым агентом является природный лабданоид пинусолид (IV). Это соединение является аналогом по свойствам заявляемых соединений. Пинусолид (IV) содержится в нейтральной части живицы кедра сибирского Pinus sibirica R. Mayr.
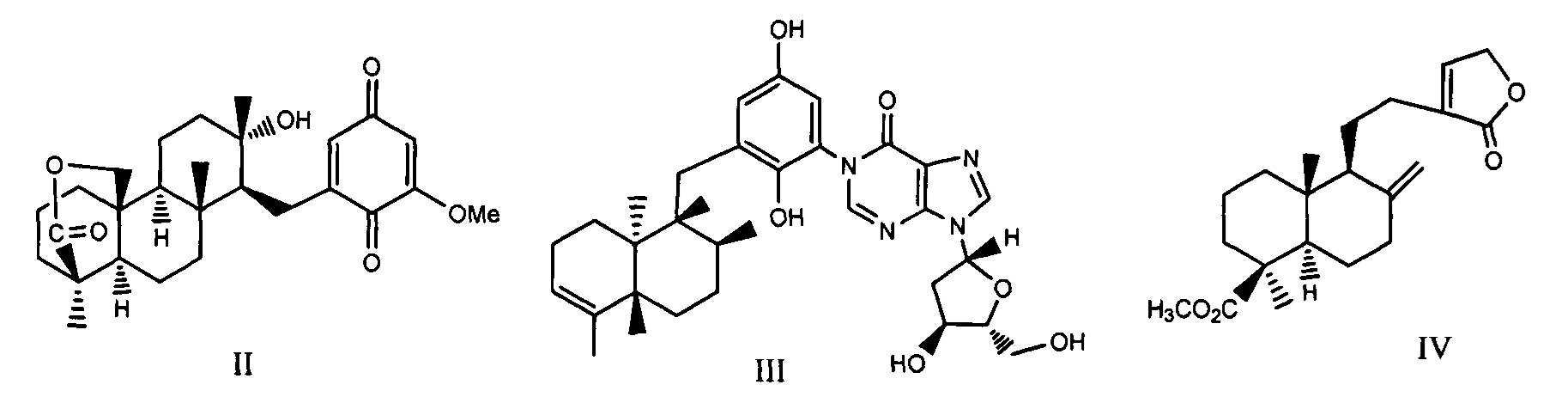
Антилейкемический потенциал пинусолида был изучен in vitro на клеточной линии лимфомы Беркитта BJAB. Было показано, что пинусолид не только снижает пролиферативную активность опухолевых клеток в относительно низких концентрациях, но и специфично индуцирует апоптоз у 70% клеток в концентрации 100 мкМ. Апоптоз клеток BJAB опосредован потерей потенциала митохондриальной мембраны. В сущности, пинусолид в концентрации 100 мкМ приводит к потере потенциала митохондриальной мембраны, что указывает на внутренний митохондриальный механизм апоптоза в соответствующем сигнальном пути гибели клетки. Значительная индукция апоптоза пинусолидом (100 мкМ) наблюдалась также в эксперименте ex vivo. При этом фрагментация ДНК происходила как в первичных лимфобластных клетках, так и в лейкемических. Пинусолид ex vivo преодолевал устойчивость к антрациклину первичных лимфобластов, полученных от пациентов с высоким риском ОЛЛ (острая лимфобластная лейкемия) и слабым ответом на химиотерапию [Shults Е.Е., Velder J., Schmalz H.-G., Chernov S.V.,. Rubalova T.V, Gatilov Y.V., Henze G., Tolstikov G.A., Prokop A. Bioorg. Med. Chem. Lett. - 2006. - V. 16. - P. 4228-4232.].
Авторы работы [Han B.H., Yang H.O., Kang Y.-H., Suh D.-Y., Go H.J., Song W.-J., Kim Y.Ch., Park M.K. J. Med. Chem. - 1998. - V. 41. - P. 2626-2630] охарактеризовали пинусолид (IV) в качестве нового антагониста фактора агрегации тромбоцитов. В опытах с использованием тромбоцитов кролика было получено значение IC50 пинусолида при агрегации тромбоцитов, вызванной ФАТ (фактор агрегации тромбоцитов), от 19 до 5 мкМ, а при снижении концентрации ФАТ - от 500 до 5 нМ. Величина ЕД50 пинусолида in vivo составила 1.1 мг/кг для внутривенного введения и 69.0 мг/кг для перорального (per os).
Основным недостатком биологического действия пинусолида (IV) является его использование в значительных дозах (IC50 100 мкМ). Однако в связи селективностью фармакологического (антипролиферативного и апоптозиндуцирующего) эффектов, связанных с активацией каспазы-3, получение структурных аналогов указанного эпоксилабданоида представляет значительный интерес для создания противоопухолевых агентов с направленным цитостатическим действием.
Аналогом по строению заявляемых соединений является амид ламбертиановой кислоты (V), обладающий анальгетической активностью и центральным стимулирующим действием [Патент RU 2534987 от 08.10.2014. Заявка №2013147550/04(073981). Амиды ламбертиановой кислоты, обладающие анальгетической активностью и стимулирующим действием, авторы Шульц Э.Э., Харитонов Ю.В., Морозова Е.А., Фомина Е.К., Толстикова Т.Г. Опубликовано: 10.12.2014. Бюл. №34]. В работе [Вечкапова C.O., Запара Т.А., Морозова Е.А., Проскура А.Л., Шульц Э.Э., Толстикова Т.Г., Ратушняк А.С. Бюлл. эксперимент, биол. мед. - 2016. - №6. - С. 736-739] показано, что амид ламбертиановой кислоты подавляет гиперактивацию ионотропных глутаматных рецепторов. Противоопухолевая активность соединения не изучалась.
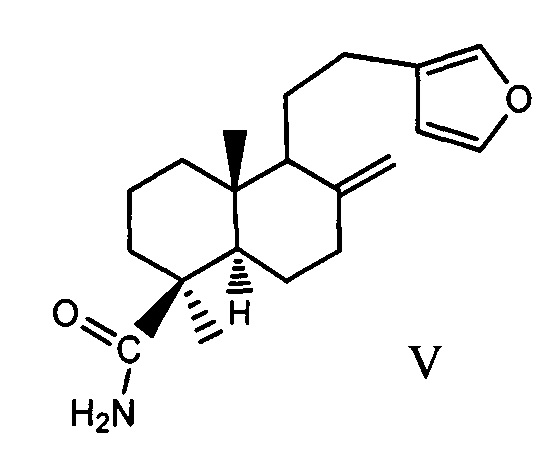
Задачей изобретения является создание нового эффективного средства с цитостатической активностью, обладающего противоопухолевым действием in vivo на основе доступного растительного метаболита ламбертиановой кислоты (VI). Это соединение легко выделяется из хвои, живицы или побегов кедра сибирского [Патент RU 2436781 от 10.06.2010. Заявка 2010123753/04. Способ получения ламбертиановой кислоты из экстрактивных веществ древесной зелени кедра сибирского. Авторы Попов С.А., Козлова Л.П., Шпатов А.В., Шульц Э.Э., Толстиков Г.А. Опубликовано: Бюл. №35, 20.12.2011].
Поставленная задача решается новыми химическими соединениями - N,N'-(алкандиил)бис[лабда-7(9),13,14-триен-4-карбоксамидами] формулы (Iа, б), обладающими способностью к подавлению роста опухолевых клеток человека в культурах МТ-4, MDA-MB-231 и ВТ-474 и задерживающими рост опухолевых трансплантатов у животных.
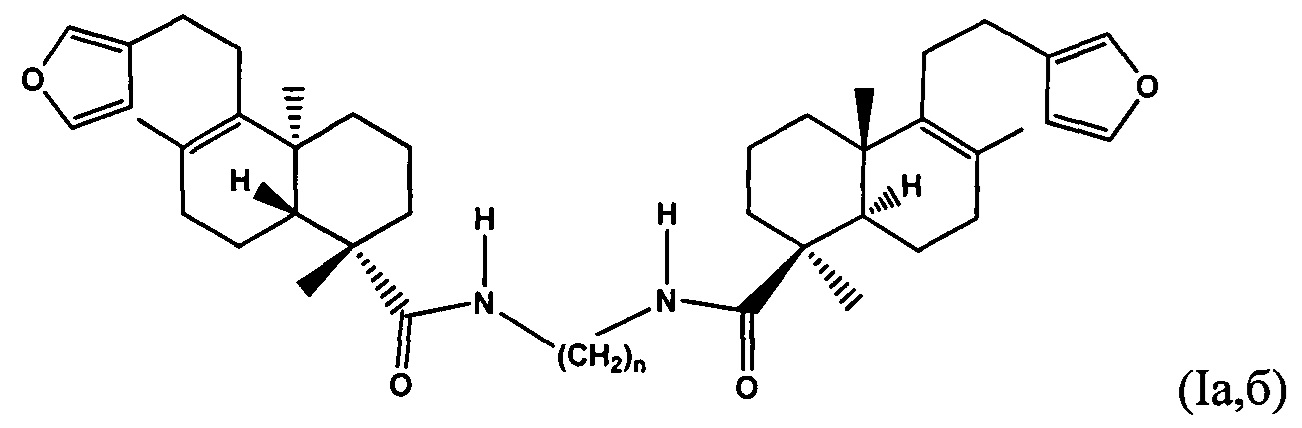
где n=2 (Iа); n=6 (Iб).
Способ получения соединений (Iа, б) реализуется по показанной на схеме последовательности превращений ламбертиановой кислоты (VI) (рис. 1). При действии p-толуолсульфокислоты ламбертиановая кислота (VI) гладко претерпевает изомеризацию с образованием фломизоиковой кислоты (VII), обработка которой хлористым оксалилом в хлористом метилене в условиях работы [Миронов М.Е., Харитонов Ю.В., Шульц Э.Э., Шакиров М.М., Багрянская И.Ю., Толстиков Г.А. Химия природных соединений. - 2010. - №2. - С. 194-200] приводит к хлорангидриду (VIII) (выход 89%). При конденсации хлорангидрида фломизоиковой кислоты (VIII) с диаминами - этилендиамином (IХа) или гексаметилендиамином (IX,), гладко образуются соответствующие бис(лабдатриенкарбоксамидо)алканы (Iа, б) (выход 81-89%).
Цитостатическая активность соединений (Iа, б) изучалась по способности подавлять рост опухолевых клеток в культурах: МТ-4 (лимфоциты Т-клеточной лейкемии), ВТ-474 с высокой экспрессией HER-2 (рак молочной железы), MDA-MB-231 и MCF-7 с низким уровнем экспрессии HER-2 (рак молочной железы), клетки меланомы MEL-8. Для этого определяли GI50 - концентрацию, ингибирующую на 50% жизнеспособность опухолевых клеток. Для определения GI50 использовали стандартный МТТ тест, как описано в рекомендациях [Mosmann. J Immunol. Methods, 1983. - V. 16. - P. 55-63; Wilson J.K., Sargent J.M., Elgie A.W., Hill J.G., Taylor C.G. Br. J. Cancer. - 1990. - V. 62. - P. 189-194].
Результаты изучения цитотоксической активности приведены в табл. 1. Из данных таблицы 1 видно, что заявляемые соединения (Iа, б) обладают способностью подавлять рост опухолевых клеток человека. Наибольшей цитотоксической активностью обладало соединение (Iб) для опухолевых клеток MEL-8 (4.16 мкМ). Соединение (Iб) оказалось в 5 раз более активным ингибитором жизнеспособности опухолевых клеток меланомы MEL-8 по сравнению с соединением (Iа) и в 8-10 раз - по сравнению с пинусолидом (IV) и исходным соединением фломизоиковой кислотой (VII). Соединение (Iб) активнее, чем другие лабданоиды, снижало рост клеток рака молочной железы MDA-MB-231. Соединение (Iб) проявляло ингибирующую активность для клеток Т-клеточной лейкемии МТ-4 (7.17 мкМ) и являлось в 5-7 раз более активным ингибитором жизнеспособности этих клеток, чем соединение (1а) и агент сравнения пинусолид (IV). Новые бислабданоиды (Iа, б) оказались в 3 раза более активными по сравнению с пинусолидом (IV) в отношении клеток рака молочной железы ВТ-474. При этом для соединения (Iа) наблюдалась селективность по отношению к опухолевым клеткам ВТ-474. Цитотоксическая концентрация соединения (Iб) на опухолевых клетках меланомы MEL-8 и рака молочной железы MDA-MB-231 оказалась на уровне таковой доксорубицина.
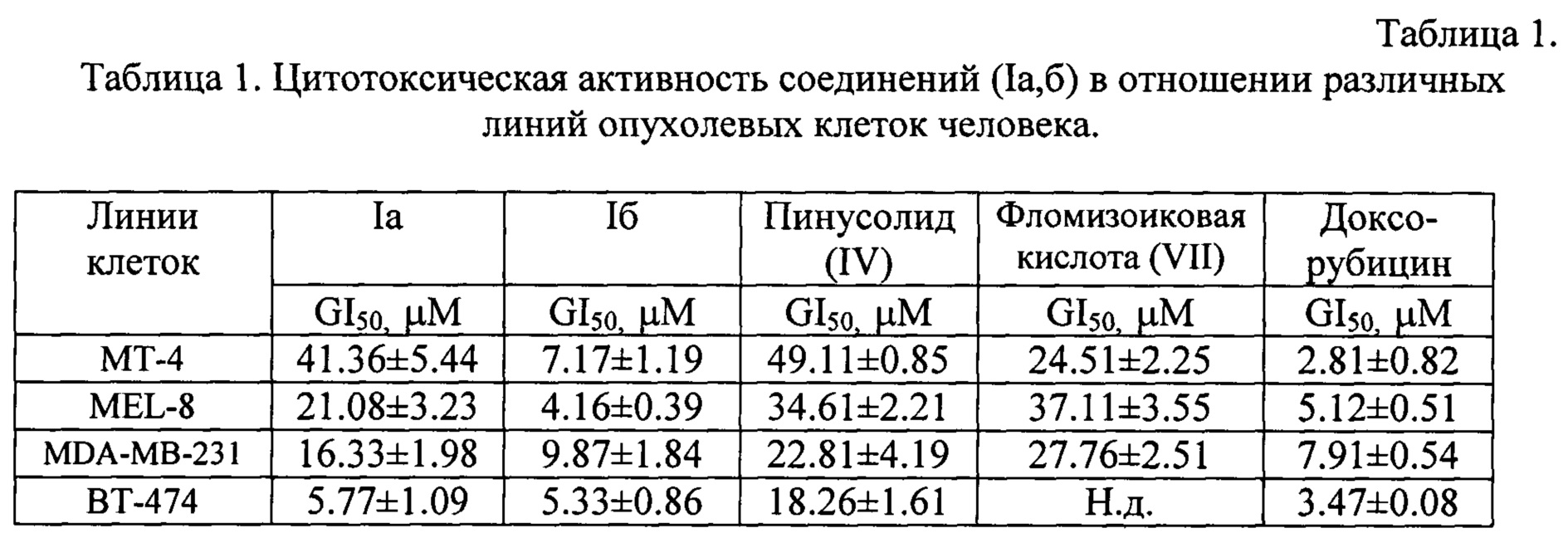
[a] GI50: концентрация вещества, при которой наблюдалось 50% ингибирование роста опухолевых клеток после 72 ч инкубирования.
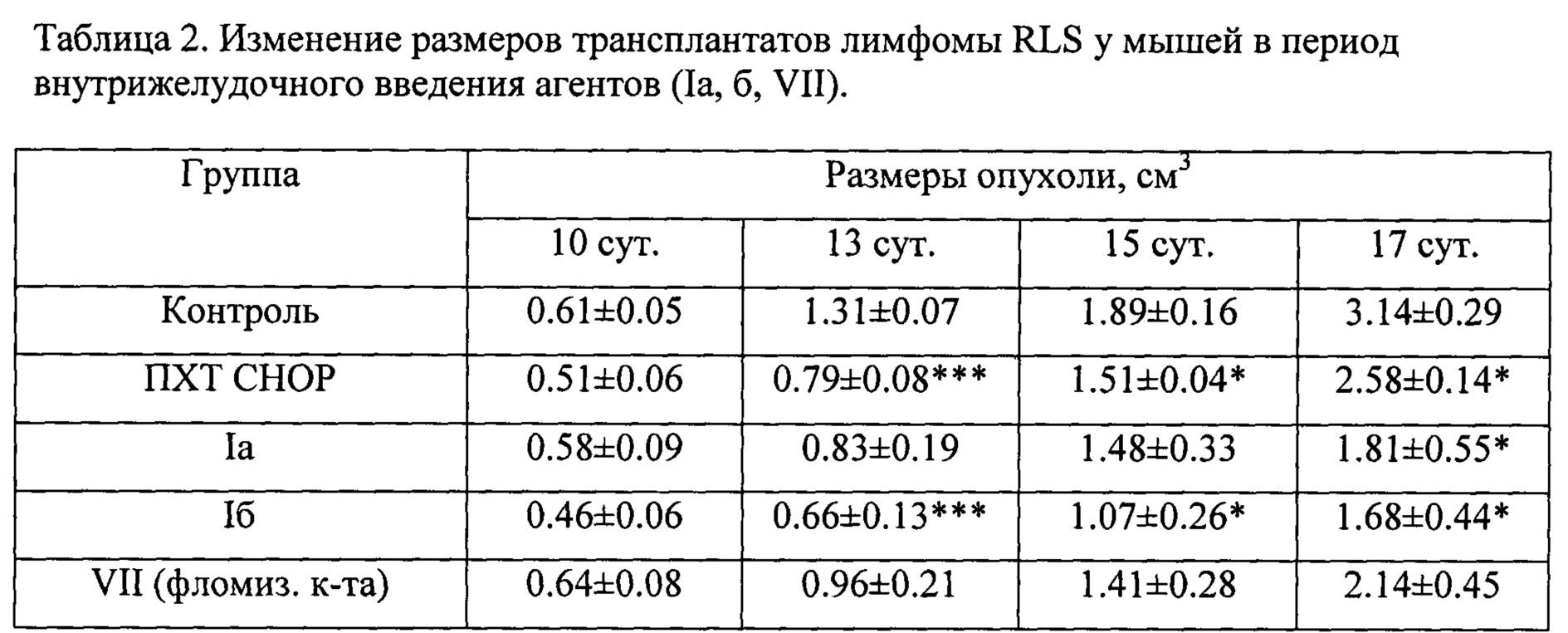
Противоопухолевое действие бислабданоидов (Iа, б) и фломизоиковой кислоты (VII) исследовали на мышах линии СВА массой 25-30 г, которым трансплантировали внутримышечно клетки злокачественной мышиной лимфомы RLS, резистентной к циклофосфану (500 тысяч клеток). Данный штамм лимфомы растет в виде солидного узла, характеризуется быстрым прогрессивным ростом. Изучаемые соединения (Iа, б, VII) вводили в курсовом режиме внутрижелудочно, начиная с пятого дня после перевивки в режиме четыре раза через день в дозе 100 мг/кг в виде суспензии в воде с Твином-80 (общая курсовая доза - 400 мг/кг). В качестве эталона противоопухолевого эффекта являлся эффект комплекса цитостатических препаратов, вводимых однократно референсной группе мышей по стандартной схеме полихимиотерапии CHOP (ПХТ) [Грек О.Р., Мишенина С.В., Пупышев А.Б. Бюлл. экспер. биол. мед. 2002. - Т. 134. - №10. - С. 413-417]: циклофосфан (50 мг/кг), доксорубицин (4 мг/кг), винкристин (0.1 мг/кг) и преднизолон (5 мг/кг). Контролем являлись животные с опухолью без лечения. Размеры опухолевых узлов измеряли в динамике на стадии прогрессивного роста опухоли. Результаты измерений размеров опухоли в период введения агентов представлены в таблице 2. На основе данных табл. 2 были рассчитаны значения показателя торможения роста опухоли (ТРО), приведенные на рис. 1. Установлено, что в ранние сроки наблюдения (13 день после перевивки) заявленные агенты не уступали ПХТ по противоопухолевому эффекту, а в конце этого периода (17 день) агент (Iб) достоверно превосходили его. При этом наиболее стабильно высокий эффект продемонстрировал бис(амидолабданоид) (Iб), имеющий линкерную цепь из шести атомов углерода (рис. 1). Данные для фломизоиковой кислоты (VII) были недостоверными в течение всего периода наблюдения (табл. 2).
На рис. 2 приведено изменение показателей торможения роста лимфомы RLS у мышей после введения лабданоидов (Iа, б, VII) в сравнении с ПХТ.
*p<0.05, ** p<0.01 различия с контролем достоверны
#p<0.05, ###p<0.001 различия с ПХТ достоверны
Таким образом, бислабданоиды (Iа, Iб), а также исходное соединение (VII) при курсовом внутрижелудочном введении мышам оказывают противоопухолевое действие, выражающееся в задержке роста злокачественной опухоли. При этом соединение (Iа) не уступает, а соединение (Iб) превосходит по эффективности цитостатическую ПХТ по стандартной схеме CHOP. Результаты, достигнутые на перевиваемой лимфоме, резистентной к циклофосфану, свидетельствуют о потенциальной способности бислабданоидов преодолевать феномен лекарственной устойчивости опухолевых штаммов.
В дополнительном эксперименте на мышах, которым имплантировали ту же опухоль, как указано выше, изучали противоопухолевый эффект соединения (Iб) при внутрижелудочном введении в масляном растворе в курсовой дозе 300 мг/кг в более ранние сроки (через 2 дня после перевивки). Контрольной группе мышей вводили подсолнечное масло в эквивалентном объеме, референсной группе - однократно внутрибрюшинно водный раствор паклитаксела в дозе 30 мг/кг. Установлено, что в этих условиях соединение (Iб) оказывает противоопухолевое действие, выражающееся в достоверной задержке ее роста на 13-ые и 15-ые сутки. При этом наиболее высокий противоопухолевый эффект наблюдался на 13-й день после перевивки (через 4 дня после отмены агента) в виде уменьшение размеров трансплантатов в 1.7 раз относительно контроля. Сравнимый с паклитакселом эффект наблюдался также на 15-й день после перевивки опухоли (через 6 дней после отмены препарата) (таблица 3).
Из анализа показателей выживаемости следует, что введение изучаемого соединения и референсного препарата не оказало существенного влияния на среднюю продолжительность жизни мышей по сравнению с контролем: соответственно 19.7±0.4 и 20.7±0.9 дней против 19.0±0.6 дней в контроле.

*p<0.05, ** p<0.01 различия с контролем достоверны
Таким образом, бислабданоид (Iб) при курсовом внутрижелудочном введении в масляном растворе мышам в ранние сроки после перевивки злокачественной опухоли оказывает противоопухолевое действие, выражающееся в достоверной задержке ее роста. При этом соединение (Iб) по выраженности эффекта не уступает паклитакселю, но имеет более короткую продолжительность действия после прекращения введения в организм.
Техническим результатом изобретения является создание новых производных лабданоидов (Iа, б), обладающих способностью к подавлению роста опухолевых клеток человека. Новые соединения получают путем химической модификации доступного растительного метаболита Pinus sibirica R. Mayr. - ламбертиановой кислоты (VI), которая легко выделяется из лесопромышленного продукта - кедровой живицы или из хвои кедра, являющейся многотоннажным отходом лесосеки [Толстикова Т.Г., Сорокина И.В., Долгих М.П., Харитонов Ю.В., Чернов С.В., Шульц Э.Э., Толстиков Г.А. Химико-фармацевтический журнал. - 2004. - Т. 38. - С. 13-15]. Физико-химические константы новых, впервые полученных соединений приведены в примерах 1, 2.
Пример 1. Получение (1S,1'S,4aS,4a'S,8aR,8a'R)-N,N,-(этaн-1,2-диил)биc{5-[2-(фуран-3-ил)этил]-1,4а,6-триметил-1,2,3,4,4а,7,8,8а-октагидронафталин-1-карбоксамида} (Iа)
К раствору 1.10 г (3.2 ммоль) хлорангидрида 15,16-эпокси-8(9),13(16),14-лабдатриен-18-овой кислоты (VIII) в 15 мл хлористого метилена добавляли 0.21 г (3.2 ммоль) этилендиамина (IХа) и по каплям 0.73 мл (6.4 ммоль) триэтиламина. Реакционную смесь перемешивали при комнатной температуре 24 ч, растворитель упаривали в вакууме, к остатку добавляли диэтиловый эфир. Выпавший осадок гидрохлорида триэтиламина отфильтровывали, маточный раствор упаривали, остаток хроматографировали на силикагеле (элюент - хлороформ). Получили 0.82 г (81%) соединения (Iа) в виде бесцветного маслообразного вещества. 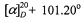 (с 0.50, СНСl3). ИК спектр, ν, см-1: 600, 755, 874, 1025, 1064, 1164, 1192, 1233, 1255, 1377, 1462, 1519, 1643, 1759, 2871, 2932, 3392. Спектр ЯМР 1H, δ, м.д.: 0.84 с (6Н, С20Н3), 1.08 д.т (2Н, H3, J 13.5, 4.4 Гц), 1.17 с (6Н, С19Н3), 1.20 д.т (2Н, Н1, J 14.1, 4.0 Гц), 1.34 д (2Н, H5, J 12.1 Гц), 1.57 м (2Н, Н2), 1.62 с (6Н, С17Н3), 1.71-1.84 м (4Н, H6,2), 1.88-2.02 м (6Н, H1,6,7), 2.05-2.15 м (2Н, H7,11), 2.10 д.м (2Н, H3, J 9.6 Гц), 2.24 м (2Н, Н11), 2.43 м (4Н, H12,12), 3.34 уш.с (4Н, 2СН2), 6.28 д.д (1H, H14, J 1.6, 0.8 Гц), 6.35 уш.с (2Н, NH), 7.22 уш.с (1Н, H16), 7.33 д.д (1Н, H15, J 1.6, 0.8 Гц). Спектр ЯМР 13С, δ, м.д.: 17.86 к (С20), 19.51 к (С17), 19.62 т (С2), 21.09 т (С6), 25.48 т (С12), 28.66 т (С11), 29.44 к (С19), 34.22 т (С7), 37.27 т (С1), 37.60 т (С3), 39.49 с (С10), 40.10 т (СН2), 43.43 с (С4), 53.50 д (С5), 110.54 д (С14), 125.24 с (С13), 126.72 с (С8), 138.07 д (С15), 138.77 с (С9), 142.36 д (С16), 178.01 с (С18). Найдено, %: С 77.09, Н 9.64, N 3.89. C44H64N2O4. Вычислено, %: С 77.14, Н 9.42, N 4.09.
(с 0.50, СНСl3). ИК спектр, ν, см-1: 600, 755, 874, 1025, 1064, 1164, 1192, 1233, 1255, 1377, 1462, 1519, 1643, 1759, 2871, 2932, 3392. Спектр ЯМР 1H, δ, м.д.: 0.84 с (6Н, С20Н3), 1.08 д.т (2Н, H3, J 13.5, 4.4 Гц), 1.17 с (6Н, С19Н3), 1.20 д.т (2Н, Н1, J 14.1, 4.0 Гц), 1.34 д (2Н, H5, J 12.1 Гц), 1.57 м (2Н, Н2), 1.62 с (6Н, С17Н3), 1.71-1.84 м (4Н, H6,2), 1.88-2.02 м (6Н, H1,6,7), 2.05-2.15 м (2Н, H7,11), 2.10 д.м (2Н, H3, J 9.6 Гц), 2.24 м (2Н, Н11), 2.43 м (4Н, H12,12), 3.34 уш.с (4Н, 2СН2), 6.28 д.д (1H, H14, J 1.6, 0.8 Гц), 6.35 уш.с (2Н, NH), 7.22 уш.с (1Н, H16), 7.33 д.д (1Н, H15, J 1.6, 0.8 Гц). Спектр ЯМР 13С, δ, м.д.: 17.86 к (С20), 19.51 к (С17), 19.62 т (С2), 21.09 т (С6), 25.48 т (С12), 28.66 т (С11), 29.44 к (С19), 34.22 т (С7), 37.27 т (С1), 37.60 т (С3), 39.49 с (С10), 40.10 т (СН2), 43.43 с (С4), 53.50 д (С5), 110.54 д (С14), 125.24 с (С13), 126.72 с (С8), 138.07 д (С15), 138.77 с (С9), 142.36 д (С16), 178.01 с (С18). Найдено, %: С 77.09, Н 9.64, N 3.89. C44H64N2O4. Вычислено, %: С 77.14, Н 9.42, N 4.09.
Пример 2. Получение (1S,1'S,4аS,4а'S,8аR,8а'R)-N,N-(гексан-1,6-диил)бис{5-[2-(фуран-3-ил)этил]-1,4а,6-триметил-1,2,3,4,4а,7,8,8а-октагидронафталин-1-карбоксамида} (Iб)
К раствору 1.10 г (3.2 ммоль) хлорангидрида 15,16-эпокси-8(9),13(16),14-лабдатриен-18-овой кислоты (VII) в 15 мл хлористого метилена добавляли 0.44 г (3.2 ммоль) гексаметилен-1,6-диамина (IХа) и по каплям 0.73 мл (6.4 ммоль) триэтиламина. Реакционную смесь перемешивали при комнатной температуре 24 ч, растворитель упаривали в вакууме, к остатку добавляли диэтиловый эфир. Выпавший осадок гидрохлорида триэтиламина отфильтровывали, маточный раствор упаривали, остаток хроматографировали на силикагеле (элюент - хлороформ). Получили 1.06 г (89%) соединения (Iб) в виде бесцветного аморфного порошка. 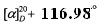 (с 1.06, СНСl3). ИК спектр, ν, см-1: 756, 1024, 1066, 1167, 1180, 1256, 1377, 1459, 1520, 1643, 1759, 2873, 2935, 3391. Спектр ЯМР 1Н, δ, м.д.: 0.84 с (6Н, С20Н3), 1.06 д.т (2Н, H3, J 13.6, 4.1 Гц), 1.15 с (6Н, С19Н3), 1.18 с (2Н, Н1), 1.30 м (4Н, СН2), 1.31 м (2Н, Н5), 1.30 т (4Н, СН2, J 6.7 Гц), 1.53 м (2Н, Н2), 1.61 с (6Н, С17Н3), 1.72-1.82 м (4Н, Н6,2), 1.87 м, 1.91 м, 1.99 м (6Н, Н1,6,7), 2.07 м (2Н, Н7,11), 2.10 д.м (2Н, H3, J 9.6 Гц), 2.21 м (2Н, Н11), 2.41 м (4Н, H12,12), 3.15 д (2Н, СН2, J6.7 Гц), 3.20 д (2Н, СН2, J 6.7 Гц), 5.62 т (2Н, NH, J 6.1 Гц), 6.26 д.д (1H, H14, J 1.5, 0.9 Гц), 7.21 т (1H, H16, J 0.9 Гц), 7.33 д.д (1H, H15, J 1.5, 0.9 Гц). Спектр ЯМР 13С, δ, м.д.: 17.87 к (С20), 19.46 к (С17),19.60 т (С2), 21.15 т (С6), 25.42 т (С12), 26.23 т (СН2), 28.63 т (С11), 29.03 т (СН2), 29.54 к (С19), 34.23 т (С7), 37.31 т (С1), 37.70 т (С3), 38.89 т (СН2), 39.50 с (С10), 43.46 с (С4), 53.44 д (С5), 110.52 д (С14), 125.21 с (С13), 126.63 с (С8), 138.03 д (С15), 138.84 с (С9), 142.32 д (С16), 176.52 с (C18). Масс-спектр, m/z. (Iотн, %): 712 (35), 632 (19), 631 (39), 539 (40), 538 (100), 495 (24), 494 (76), 410 (11), 305 (16), 189 (16), 121 (11). Найдено: m/z 712.5172 [М]+. C46H68N2O4. Вычислено: М 712.5174.
(с 1.06, СНСl3). ИК спектр, ν, см-1: 756, 1024, 1066, 1167, 1180, 1256, 1377, 1459, 1520, 1643, 1759, 2873, 2935, 3391. Спектр ЯМР 1Н, δ, м.д.: 0.84 с (6Н, С20Н3), 1.06 д.т (2Н, H3, J 13.6, 4.1 Гц), 1.15 с (6Н, С19Н3), 1.18 с (2Н, Н1), 1.30 м (4Н, СН2), 1.31 м (2Н, Н5), 1.30 т (4Н, СН2, J 6.7 Гц), 1.53 м (2Н, Н2), 1.61 с (6Н, С17Н3), 1.72-1.82 м (4Н, Н6,2), 1.87 м, 1.91 м, 1.99 м (6Н, Н1,6,7), 2.07 м (2Н, Н7,11), 2.10 д.м (2Н, H3, J 9.6 Гц), 2.21 м (2Н, Н11), 2.41 м (4Н, H12,12), 3.15 д (2Н, СН2, J6.7 Гц), 3.20 д (2Н, СН2, J 6.7 Гц), 5.62 т (2Н, NH, J 6.1 Гц), 6.26 д.д (1H, H14, J 1.5, 0.9 Гц), 7.21 т (1H, H16, J 0.9 Гц), 7.33 д.д (1H, H15, J 1.5, 0.9 Гц). Спектр ЯМР 13С, δ, м.д.: 17.87 к (С20), 19.46 к (С17),19.60 т (С2), 21.15 т (С6), 25.42 т (С12), 26.23 т (СН2), 28.63 т (С11), 29.03 т (СН2), 29.54 к (С19), 34.23 т (С7), 37.31 т (С1), 37.70 т (С3), 38.89 т (СН2), 39.50 с (С10), 43.46 с (С4), 53.44 д (С5), 110.52 д (С14), 125.21 с (С13), 126.63 с (С8), 138.03 д (С15), 138.84 с (С9), 142.32 д (С16), 176.52 с (C18). Масс-спектр, m/z. (Iотн, %): 712 (35), 632 (19), 631 (39), 539 (40), 538 (100), 495 (24), 494 (76), 410 (11), 305 (16), 189 (16), 121 (11). Найдено: m/z 712.5172 [М]+. C46H68N2O4. Вычислено: М 712.5174.
Пример 3. Определение цитотоксичности соединений (Iа, б), исходного лабданоида (VII) и агента сравнения пинусолида (IV) в отношении различных опухолевых клеток
Для определения 50% цитотоксической концентрации для опухолевых клеток in vitro использовали стандартный МТТ тест. Клетки МТ-4, ВТ-474, MDA-MB-231, MEL-8 культивировали в термоинактивированной среде RPMI-1640 (30 мин при температуре 65°C), содержащей 10% эмбриональной сыворотки крупного рогатого скота, 2 ммоль/л L-глютамина, 80 мкг/мл гентамицина при температуре 37°C в СO2 инкубаторе. Для эксперимента использовали клетки на 3 сутки культивирования после оценки морфологии, подсчета концентрации и жизнеспособности клеток. Клетки МТ-4, СЕМ-13 и U-937 помещали в лунки 96-луночного планшета («Cel-Cult», Англия) по 100 мкл в лунку, в посевной концентрации 0.5×106 клеток в мл. Исследуемые вещества добавляли к клеткам, получая конечные концентрации 0.01-1000 мкМ, используя по 3 лунки на каждую концентрацию. Клетки, инкубируемые в тех же условиях без добавления исследуемых соединений, являлись контрольными. Клетки культивировали 72 часа. Водный раствор МТТ (5 мг/мл) профильтровывали через 0.22 мкм фильтр («Flow laboratories)), Англия) добавляли в каждую исследуемую культуру в соотношении 1:10 к ее объему, смесь инкубировали 4 часа при температуре 37°C в CO2 инкубаторе. По окончании инкубации супернатант осторожно удаляли, затем в каждую анализируемую лунку добавляли по 100 мкл ДМСО. Осадок ресуспендировали и 30 мин инкубировали в темноте при комнатной температуре до полного растворения кристаллов формазана.
Оптическую плотность (OD) образцов измеряли на мультилуночном спектрофотометре BioRad 680 (США) при длине волны, равной 490 нм. Процент ингибирования роста клеток определяли по формуле 100 - (среднее значение OD в опыте/среднее значение OD в контроле) × 100. Полученное значение для контрольного триплета (первые три лунки без добавления соединений, параллельных для каждого исследуемого экспериментального агента) принималось за 100%. Рассчитывали среднее значение и ошибку среднего для каждой концентрации анализируемого соединения. По результатам строили диаграмму зависимости жизнеспособности клеток (%) от концентрации исследуемого цитотоксического вещества, определяли 50% цитотоксическую дозу (ЦД50), а также стандартную ошибку (SE) показателя ЦД50.
Соединение (Iа) ингибировало рост опухолевых клеток человека МТ-4, MEL8, MDA-MB-231, ВТ474 в концентрациях 41.36, 21.08 16.33 и 5.77 мкМ соответственно. Цитотоксическая активность этого соединения выше, чем у аналога по свойствам пинусолида (IV), у которого ингибирующие концентрации в этих же условиях составляет 49.1, 34.6, 22.81 и 18.26 мкМ.
Соединение (Iб) проявляет свой цитотоксический эффект в концентрациях 7.17,4.16, 9.87 и 5.33 мкМ соответственно, что значительно меньше эффективных концентраций пинусолида (IV) и исходного соединения (VII). При этом цитотоксическая доза соединения (Iб) для опухолевых клеток MEL-8, MDA-MB-231 сравнима с эффективной цитотоксической дозой лекарственного препарата доксорубицина.
Пример 4. Изучение противоопухолевого действия соединений (Iа, б, VII) в сравнении с цитостатической полихимиотерапией на мышах с перевиваемой опухолью
Противоопухолевое действие бислабданоидов (Iа, б) и исходного лабданоида (VII) исследовали на мышах-самцах линии СВА массой 25-30 г, которым перевивали внутримышечно клеточную суспензию злокачественной мышиной лимфомы RLS, резистентной к циклофосфану (500 тысяч клеток в 0.1 мл физ. раствора). После перевивки опухоль растет в виде солидного узла, характеризуется быстрым прогрессивным ростом. Перевивочный материал получен из банка опухолевых штаммов Института цитологии и генетики СО РАН.
После перевивки животных делили на 5 групп по 10 особей. Изучаемые соединения вводили внутрижелудочно, начиная с пятого дня после перевивки в режиме четыре раза через день в дозе 100 мг/кг в виде суспензии в воде с Твином-80 (общая курсовая доза - 400 мг/кг). Эталоном противоопухолевого эффекта являлась группа животных, получавшая однократно на 5-й день опыта цитостатическую полихимиотерапию (ПХТ) по стандартной схеме CHOP в модификации [Грек О.Р., Мишенина С.В., Пупышев А.Б. Бюлл. экспер. биол. мед. 2002. - Т. 134. - №10. - С. 413-417]: парентеральное введение циклофосфана (50 мг/кг), доксорубицина (4 мг/кг), винкристина (0.1 мг/кг) и преднизолона (5 мг/кг). Контролем являлись животные с опухолью без лечения. Контроль и группа с ПХТ получали внутрижелудочно в течение опыта водно-твиновую смесь. Опухолевые узлы измеряли штангенциркулем с момента визуализации опухоли до начала гибели мышей (на 10, 13, 15 и 17 сутки после перевивки). Противоопухолевый эффект определяли по индексу торможения роста опухоли (ТРО): разность средних размеров опухолей в контрольной и опытной группах, отнесенная к среднему размеру опухолей в контроле.
Результаты измерений размеров опухоли в период введения агентов представлены в таблице 2. Согласно данным табл. 2, внутрижелудочное курсовое введение бислабданоидов (Iа, б) вызывает уменьшение размеров опухолевых узлов относительно контроля в течение всего периода наблюдений. На 17-й день после перевивки размеры опухолевых трансплантатов в группах с введением соединений Iа, Iб были меньше, чем в контроле соответственно в 1.7 и 1.9 раз, тогда как в группе с ПХТ различия в размерах опухолей с контролем были незначительными (в 1.2 раза). Фломизоиковая кислота (VII) также снижала размеры опухолевых трансплантатов, но меньше, чем бис-лабданоиды (Iа, б) (эффект не достоверен). Наиболее выраженный и достоверный противоопухолевый эффект отмечен у агента (Iб), который уже к 13-му дню опыта достоверно снизил объем опухолевых трансплантатов в 2 раза, в то время как после ПХТ они уменьшились не более чем в 1.7 раза. На основе данных табл. 2 были рассчитаны значения показателя торможения роста опухоли (ТРО), приведенные на рис. 1. Показано, что соединение (Iб) проявляет наиболее высокий противоопухолевый эффект, превосходящий ПХТ в течение всего периода наблюдений. Агент (Iа) в ранние сроки не уступал ПХТ по выраженности противоопухолевого действия, а к концу наблюдений превзошел ее эффект (рис. 2).
Пример 5. Изучение противоопухолевого действия соединения (Iб) по сравнению с паклитакселем на мышах с перевиваемой опухолью
В опыте использовали 30 мышей самок СВА массой 25-30 г, которым производили перевивку клеток лимфомы RLS как указано выше. Изучаемый агент (Iб) вводили внутрижелудочно в виде раствора в подсолнечном масле в дозе 100 мг/кг трижды через день (первый раз - через два дня после перевивки опухолевых клеток). Суммарная доза составила 300 мг/кг. Контролем являлась группа животных с опухолью, получавшая внутрижелудочно подсолнечное масло в эквивалентном объеме. Референсной группе животных вводили однократно внутрибрюшинно водный раствор паклитаксела в дозе 30 мг/кг. Динамику роста опухолевых трансплантатов определяли через два дня после отмены испытуемых соединений или с 11 по 18 день после перевивки (до начала гибели животных в группах). Измерение каждого опухолевого узла проводили штангенциркулем в трех взаимно перпендикулярных направлениях. О состоянии животных судили по изменению продолжительности жизни в течение всего опыта, которую рассчитывали в среднем на одно животное. В каждой группе было не менее 10 мышей. Данные о размерах трансплантатов (табл. 3) показывают, что при курсовом внутрижелудочном введении в масляном растворе в ранние сроки после перевивки агент (Iб) проявляет противоопухолевую активность, сравнимую с паклитакселем. При этом наиболее высокий противоопухолевый эффект наблюдался на 13-й день после перевивки (через 4 дня после отмены агента) в виде уменьшения размеров трансплантатов в 1.7 раз относительно контроля. Сравнимый с паклитакселом эффект наблюдался также на 15-й день после перевивки опухоли. Паклитаксел снижал объем опухолевых узлов в 1.4 раза, при этом его эффект имел отсроченный характер.
Таким образом, заявляемое изобретение обладает следующими преимуществами, а именно:
- новые алкандиил(бикарбоксамиды) бифуронолабданоидов (Iа, б) обладают способностью ингибировать рост опухолевых клеток человека в микромолярных концентрациях;
- заявленные соединения обладают противоопухолевым эффектом in vivo, сравнимым с эффектом традиционных цитостатиков (паклитаксел, комплексная химиотерапия по схеме CHOP).
- заявляемые соединения (Iа, б) синтезируются из доступного растительного сырья - хвои или живицы кедра сибирского.
![N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ](https://fips.edrid.ru/images/rid/5c/d7/9e/ce8826490cd9c28bd6ef16e2c190a8b0.png)
![N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ](https://fips.edrid.ru/images/rid/5c/d7/9e/a7228a4d0d216d6b7db33dac22d4c3cb.jpg)
![N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ](https://fips.edrid.ru/images/rid/5c/d7/9e/e3629cdb66868372cfb388a344a6feac.png)
![N,N'-(АЛКАНДИИЛ)БИС[ЛАБДА-7(9),13,14-ТРИЕН-4-КАРБОКСАМИДЫ], ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ](https://fips.edrid.ru/images/rid/5c/d7/9e/a6875b3fa3f8c03d252a448d53877508.jpg)

