Результат интеллектуальной деятельности: Комбинированный способ гистохимического выявления дезоксирибонуклеопротеинов, полисахаридов и углеводных компонентов биополимеров в полутонких срезах тканей и органов
Вид РИД
Изобретение
Изобретение относится к экспериментальной медицине и биологии, а именно к гистологическим исследованиям. Наиболее часто используемыми гистохимическими реакциями для световой микроскопии являются реакция Фельгена и ШИК-реакция (реактив Шиффа-йодная кислота) [3]. ШИК-реакция выявляет в срезах полисахариды и углеводные компоненты гликопротеинов и заключается в окислении перйодатом калия или натрия полисахаридов с образованием из гидроксильных групп альдегидных, дающих реакцию с фуксинсернистой кислотой (реактив Шиффа) с образованием продуктов малинового цвета [4]. Реакция Фельгена выявляет пентозы в составе дезоксирибонуклеопротеинов и также основана на применении реактива Шиффа. Ее особенностью является предварительный кислотный гидролиз нуклеопротеинов при температуре 60°С вместо использования перйодата [4]. При кислотном гидролизе в дезоксирибонуклеиновой кислоте (ДНК) разрываются гликозидные связи, соединяющие пентозу с азотистым основанием, вследствие чего в пентозах освобождаются реакционно-способные альдегидные группы у первого атома углерода, которые затем реагируют с реактивом Шиффа. Многие полимеры, содержащие углеводы, при этом гидролизуются, деполимеризуются и экстрагируются, вследствие чего реакция положительная Фельгена и ШИК-реакция одновременно не могут проявляться, и их совместное проведение нецелесообразно из-за высокой вероятности ложноотрицательных результатов.
Особую сложность представляет гистохимическое выявление дезоксирибонуклеопротеинов и углеводных структур в полутонких срезах тканей и органов, залитых в смолы для электронно-микроскопического исследования. Изготовление полутонких срезов толщиной 1-2 мкм предшествует электронно-микроскопическому исследованию биологических препаратов и необходимо для выявления клеток и неклеточных структур, интересующих исследователя, для последующего изготовления ультратонких срезов. Гистохимические методики, широко применяемые при исследовании гистологических препаратов, изготовленных из обезвоженных в спиртах и залитых в парафин кусочков ткани, не всегда воспроизводятся на полутонких срезах, так как при подготовке ткани для электронно-микроскопического исследования образцы контрастируются оксидом осмия, уранилацетатом, что существенно влияет на течение гистохимических реакций, а затем заливаются в эпоксидные смолы, которые, полимеризуясь, изменяют свойства биополимеров [1]. Проведение гистохимических реакций, направленных на выявление основных биополимеров в клетках, таких как нуклеиновые кислоты, полисахариды и гликопротеины позволило бы существенно повысить точность выявления органелл и включений, а также дифференцировки сходных по строению структур, таких как фрагментированные ядра, секреторные гранулы, лизосомы, что значительно повысило бы точность отбора участков тканей и органов для электронной микроскопии, избавило от необходимости заливки и исследования большего количества объектов, а соответственно, снизило стоимость исследования. Помимо этого данные методики позволили бы существенно расширить использование полутонких срезов в гистологических и цитологических исследованиях с использованием световой микроскопии, так как полутонкие срезы позволяют визуализировать структуры, недоступные для исследования классических гистологических препаратов. Использование гистохимических реакций, выявление и дифференцировка внутриклеточных образований могли бы в ряде случаев проводиться и без использования электронной микроскопии, что также существенно позволяет снизить стоимость исследования.
Реакция Фельгена на полутонких срезах затруднена, так как смолы и контрастирующие вещества ингибируют проявление окраски [2]. Наиболее близким аналогом реакции Фельгена в полутонких срезах является методика, разработанная для неконтрастированных препаратов [9]. Образцы для исследований фиксируют в глутаровом альдегиде без постфиксации оксидом осмия и заливают в Эпон. Изготавливают полутонкие срезы толщиной 1-2 мкм. Кислотный гидролиз проводят в течение 1 ч при комнатной температуре в 5 н. растворе соляной кислоты. Затем на срезы наносят реактив Шиффа и инкубируют в темноте в течение 1-2 ч. Ядра окрашиваются в ярко-розовый цвет.
Недостатком метода является получение аналогичного окрашивания и без кислотного гидролиза, который является определяющим фактором в развитии реакции Фельгена, только за счет реакции реактива Шиффа с глутаровым альдегидом, присутствующим в образце, то есть окрашивание является неспецифической реакцией, что было установлено самим разработчиком метода [9]. Помимо этого подготовка образцов не позволяет использовать их в дальнейшем для электронно-микроскопических исследований.
Известно несколько способов проведения ШИК-реакции на полутонких срезах [5, 6]. Их общими недостатками являются сильное повреждающее воздействие на ткань дополнительных окислителей, например перекиси водорода, а также способность давать специфическое окрашивание препаратов только при использовании определенного типа заливочной смолы (метакрилат, Эпон, Аралдит). В настоящее время, как правило, для изготовления препаратов применяется комбинированная смесь смол Эпон и Аралдит, а метакрилат практически не применяется в электронной микроскопии.
Наиболее близким аналогом к заявляемому способу является способ, предложенный R. DiBella и K. Hashimoto [7], по проведению ШИК-реакции на полутонких срезах. На препараты биологических образцов, залитых в Аралдит, наносят несколько капель 0,5%-ного перйодата калия на 10 мин и нагревают стекла на нагревательном столике до 65°C. Чтобы избежать испарения по мере надобности перйодат добавляют на срезы. Затем погружают стекла в дистиллированную воду, а затем снова прогревают до испарения воды. На прогретый до 65°C препарат наносят капельно реактив Шиффа на 5 мин, периодически добавляя для предупреждения испарения. Реактив изменяет цвет на пурпурный, после чего срезы отмываются в дистиллированной воде.
Недостатком данного метода является необходимость неоднократного инкубирования срезов при повышенной температуре, которая вызывает пересушивание препарата, а в дальнейшем при отмывании в дистиллированной воде отклеивание и потерю срезов. Метод не окрашивает биологические образцы, залитые в другие заливочные смолы. Не комбинируется с другими гистохимическими методиками.
Задача изобретения - разработать методику, позволяющую одновременно проводить гистохимическое выявление ДНК, полисахаридов и углеводных компонентов различных классов биополимеров (гликопротеинов) в полутонких срезах образцов, залитых в комбинированные смолы, дающую специфическое окрашивание различных тканей и органов, с минимальным повреждающим воздействием на срезы.
Заявленный способ одновременного гистохимического выявления ДНК, полисахаридов и углеводных компонентов биополимеров в полутонких срезах биологических образцов, залитых в смесь смол эпона и аралдита, заключается в погружение срезов в 0,5 М раствор гидроксида калия в абсолютном метаноле на 10 мин при комнатной температуре, переносе срезов в первый абсолютный этиловый спирт на 3 мин, затем - во второй и третий абсолютный этанол также с инкубацией 3 мин. Затем срезы промываются в трех сменах дистиллированной воды по 3 мин. После третьей промывки избыток воды осторожно удаляется со стекол вокруг срезов фильтровальной бумагой, и предметные стекла со срезами оставляют для подсушивания при комнатной температуре на 3-4 мин. Затем на срезы капельно наносят 1%-ный водный раствор перйодата калия и инкубируют при комнатной температуре 8 мин. Погружают стекла в дистиллированную воду на несколько секунд для удаления перийодата. Затем избыток воды удаляют со стекол вокруг срезов фильтровальной бумагой. Срезы подсушивают при комнатной температуре в течение 3-4 мин. На срезы капельно наносят реактив Шиффа и помещают срезы в темноту на 30 мин. После окончания инкубации срезы погружают на 2-3 мин в проточную холодную воду. В это время приготовляют сернистую воду добавлением к 100 мл дистиллированной воды 0,5 г метабисульфита натрия и 5-6 капель 1 н. соляной кислоты. Затем переносят на 1 мин в сернистую воду, после чего промывают в дистиллированной воде в течение 1 мин. Удаляют избыток воды со стекол фильтровальной бумагой, оставляют срезы при комнатной температуре на 5 мин для высыхания, затем наносят среду для заключения препаратов и покрывают покровным стеклом.
Технический результат заключается в появлении стабильного специфического окрашивания структур, содержащих ДНК и углеводы, в оттенки от розово-сиреневого до малиново-фиолетового в различных органах и тканях, залитых в смесь Эпона и Аралдита, без потери и термического повреждения полутонких срезов.
Указанный технический результат достигается тем, что в предлагаемом способе кислотный гидролиз ДНК при повышенной температуре заменен на обработку спиртовым раствором щелочи. Для выявления ДНК в полутонких срезах образцов необходимо было сделать пентозы ДНК доступными для проведения ШИК-реакции, как с другими полисахаридами и гликопротеинами, то есть освободить их гидроксильные группы для реакции с перйодатом, что позволит избежать разрыва гликозидных связей и окисления пентоз кислотой. Для образования в пентозах реакционно-способных альдегидных групп провели щелочной гидролиз в 0,5 М растворе гидроокиси калия в метаноле. Воздействие щелочи вызывает отщепление от нуклеотидов остатков фосфорной кислоты с образованием нуклеозидов. Разрыва гликозидных связей при этом не происходит, но освобождается гидроксильная группа у третьего атома углерода пентозы. Это дает возможность окислить ее перйодатом, а затем провести реакцию с реактивом Шиффа. Выбор в качестве растворителя абсолютного метанола обусловлен следующим: спирты облегчают проникновение реактива в срезы, но при приготовлении водно-спиртового раствора может произойти реакция Каниццаро с образованием из углеводов спиртов и кислот [4], что может помешать выявлению ДНК. Поэтому был выбран абсолютный спирт. Выбор метанола обусловлен тем, что он не способен вступать в реакцию с щелочами, но понижает рН раствора, что важно для сохранности биополимеров. Одновременно это позволяет также увеличить реакционную способность углеводов в ДНК и в других сложных соединениях за счет растворения смол, а также облегчить взаимодействие перйодата калия с гидроксилами углеводов. Известно, что некоторые полисахариды, например гликозаминогликаны, плохо реагируют с перийодатом, так как их карбоксильные и сульфатные группировки вызывают отталкивание перйодат-иона, вследствие чего ШИК-реакция может их не выявлять [8]. Обработка срезов щелочью должна была минимизировать эти явления. Для повышения специфичности после щелочного гидролиза использовали многократную отмывку препарата сначала в полярных (абсолютном этаноле), затем в неполярных растворителях (дистиллированной воде) для удаления органических и неорганических гидрофобных и гидрофильных соединений, в том числе фиксатора, так как ШИК-реакция может давать ложноположительные результаты на биологических образцах, фиксированных глутаровым альдегидом (наиболее распространенным фиксатором для электронно-микроскопических исследований), поскольку считается, что свободные альдегидные группы могут вступать в реакцию с реактивом Шиффа. Концентрацию перийодата калия повысили с 0,5 до 1% для повышения эффективности окисления при комнатной температуре. Усиление реакции с реактивом Шиффа за счет повышения температуры реакционной среды заменили увеличением длительности инкубации с реактивом Шиффа при комнатной температуре.
Для оценки эффективности заявленного способа провели следующие исследования.
Пример 1. Определение специфичности развивающейся окраски
Для установления специфичности одновременного определения углеводных компонентов и ДНК провели гистохимические реакции заявленным способом в образцах органов, имеющих биологические структуры, которые должны давать положительную реакцию на углеводные компоненты и ДНК, а также отрицательную реакцию на ДНК и углеводы. Объектом исследования были полутонкие срезы щитовидной железы и сосудов. Препараты щитовидной железы являются положительной пробой на ШИК-реакцию из-за содержания в полостях фолликулах большого количества коллоида - высокогликозилированного белка тироглобулина. Также положительную ШИК-реакцию дают базальные мембраны фолликулярных тироцитов и капилляров. Одновременно ядра клеток щитовидной железы дают положительную реакцию Фельгена. Плазма крови в просветах сосудов содержит большое количество гликопротеинов, дающих ШИК-положительную реакцию. Эритроциты не имеют ядер и не содержат большого количества углеводов в цитоплазме, вследствие чего не дают ни ШИК-реакции, ни реакции Фельгена, то есть являются отрицательным контролем.
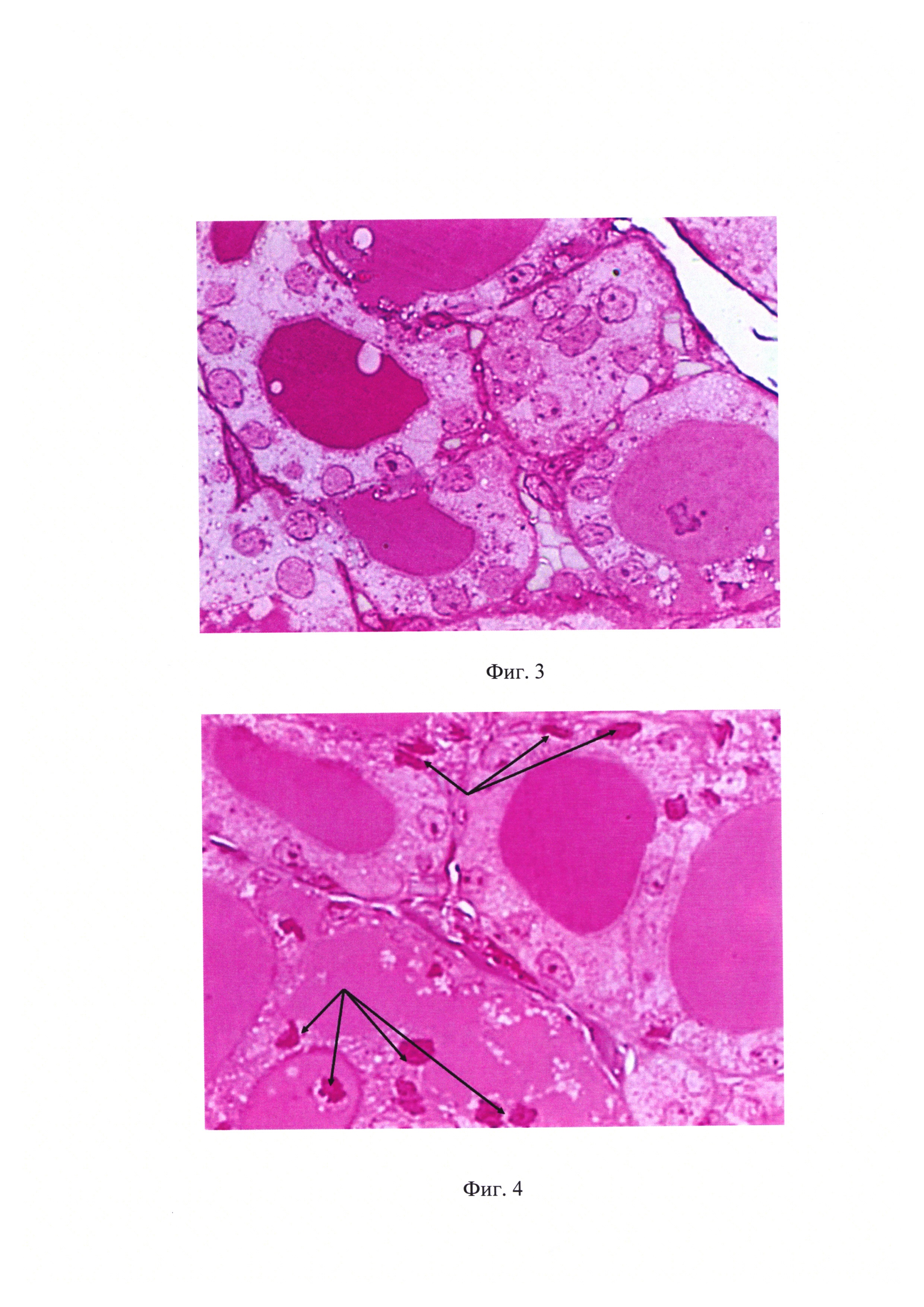
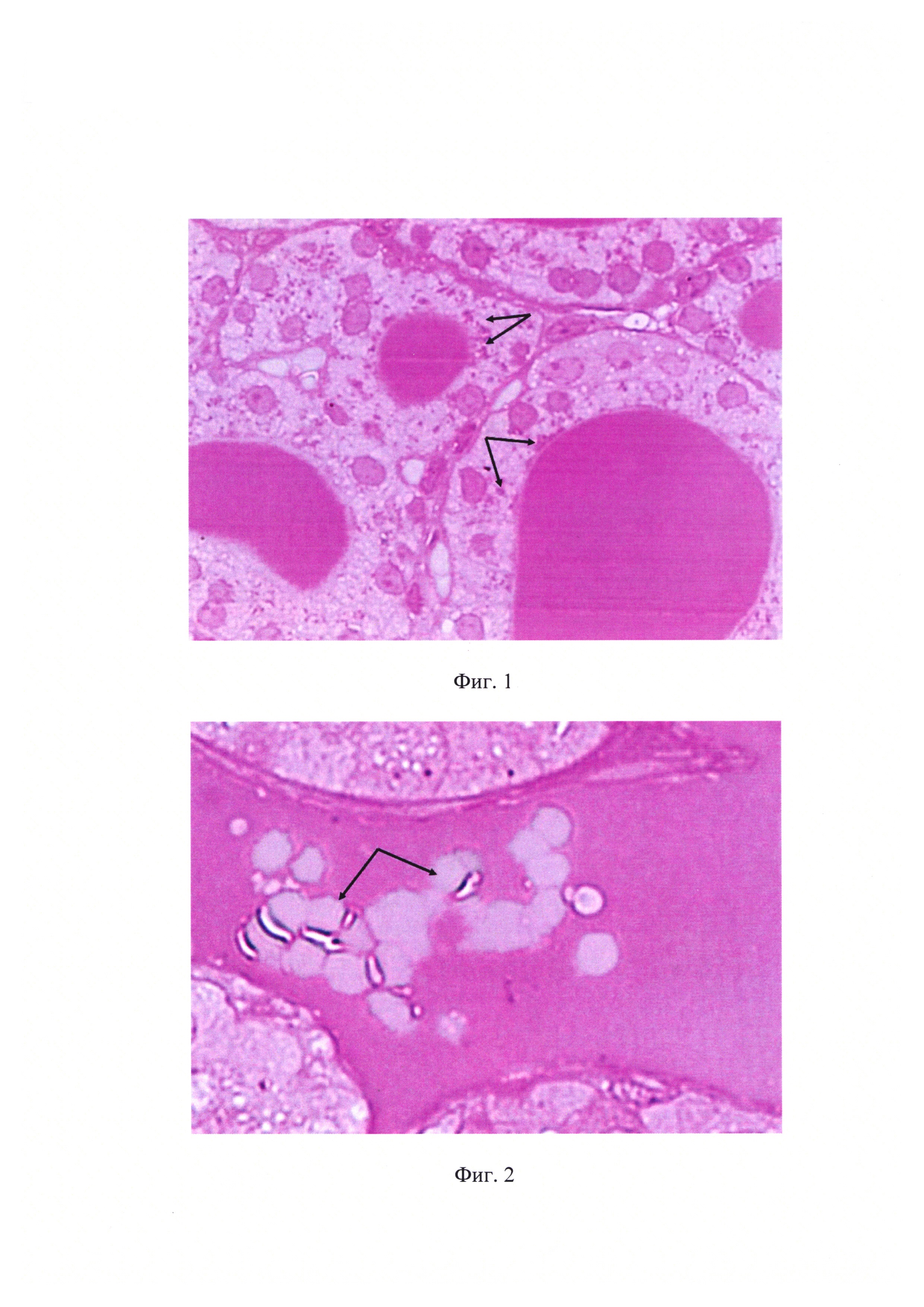
Материал фиксировали 1%-ным глутаровым альдегидом с постфиксацией 1%-ным раствором тетраокиси осмия в какодилатном буфере и 5%-ным водным раствором уранилацетата и заливали в смесь Эпона и Аралдита с добавлением дибутилфталата в качестве пластификатора и додецил-янтарнокислого ангидрида в качестве уплотнителя и DMP30 в качестве катализатора. Провели окрашивание изготовленных полутонких срезов по заявленной методике. На фиг. 1 представлены результаты гистохимических реакций в щитовидной железе. Коллоид в просвете фолликулов окрашен в малиново-фиолетовый цвет, ядра тироцитов - в сиренево-розовый цвет с более интенсивной окраской ядрышек, цитоплазма клеток не окрашена, в цитоплазме видны ШИК-положительные включения тироглобулина (указаны стрелками), в просветах сосудов неокрашенные эритроциты. На фиг. 2 представлены результаты окрашивания срезов сосуда, в виде окрашенной в розово-малиновый цвет плазмы в просвете сосуда и неокрашенных эритроцитов (указаны стрелками). Сохранность срезов была стопроцентной.
Таким образом, заявленный способ характеризуется эффективностью при постановке реакции на образцах, залитых в комбинированные эпоксидные смолы, не дает ложноположительных и ложноотрицательных реакций и, следовательно, является специфичным методом выявления углеводных компонентов и ДНК.
Пример 2. Определение чувствительности выявления ДНК и углеводного компонента
Яркость развивающейся окраски ядер зависит от количества гетерохроматина, имеющего высокую компактизацию нуклеопротеинов, и более рыхлого эухроматина, соответственно, дающего более слабую окраску дезоксирибонуклеопротеинов. Аналогично насыщенность окраски углеводных компонентов зависит от их количества в исследуемом объекте, что дает возможность при необходимости для спектрофотометрического определения количества данных соединений. Для определения чувствительности заявленного способа провели гистохимическое выявление гликопротеинов и ДНК в щитовидной железе в фолликулах с различным функциональным состоянием клеток. Фиксация и заливка материала проводилась аналогичным способом, как и в примере 1.
На фиг. 3 представлены результаты выявления тироглобулина в группе фолликулов щитовидной железы с различным содержанием этого гликопротеина с соответствующей окраской содержимого полостей фолликулов от светлого розово-сиренево до насыщенного малинового цвета. Эухроматин ядер дает слабую положительную реакцию, гетерохроматин вдоль ядерной оболочки и ядрышки окрашиваются более интенсивно. Цитоплазма клеток не окрашивается. Положительная ШИК-реакция наблюдается в базальных мембранах фолликулярных тироцитов.
На фиг. 4 представлены результаты гистохимической реакции в клетках щитовидной железы с различным состоянием ядер. Пикнотизированные ядра погибающих, десквамированных в полость фолликулов, клеток (указаны стрелками) дают более интенсивную окраску за счет более высокой концентрации нуклеопротеинов.
Таким образом, заявленный способ гистохимического выявления обладает чувствительностью.
Пример 3. Выявление полисахаридов, затрудняющих протекание ШИК-реакции
К углеводам, в структуре которых имеются группировки, препятствующие образованию альдегидных групп в углеводах, относятся гликозаминогликаны. Для определения эффективности заявленного метода провели гистохимическое выявление гепарина тучных клеток - протеогликана, состоящего из белка и гликозаминогликанов. Для избежания неправильной трактовки отрицательных результатов провели реакцию вышеописанным способом на полутонких срезах дающей положительную ШИК-реакцию щитовидной железы, в соединительнотканных перегородках которой часто встречаются тучные клетки.
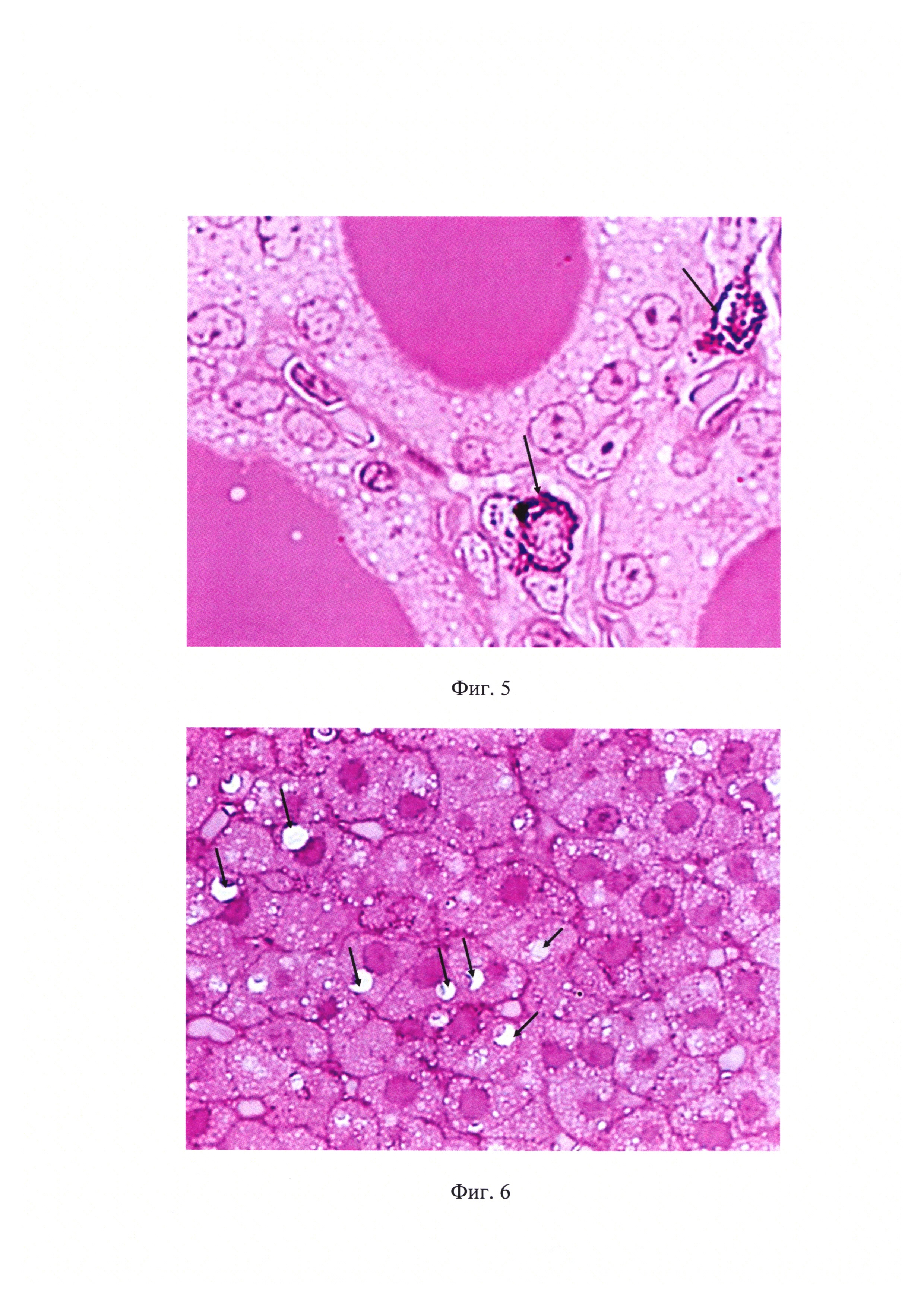
На фиг. 5 показаны результаты в виде резко положительной реакции с развитием насыщенной малиново-фиолетовой окраски гранул в цитоплазме тучных клеток, ярким розово-сиреневым окрашиванием коллоида в фолликулах и малиново-фиолетовым окрашиванием гетерохроматина и ядрышек ядер фолликулярных тироцитов.
Таким образом, заявленный способ позволяет выявлять гликозаминогликаны, что повышает применимость ШИК-реакции.
Пример 4. Отсутствие органоспецифичности заявленного способа
Для установления эффективности заявленного метода провели выявление ДНК и углеводов в различных органах. Препараты коркового вещества надпочечников и семенников крыс были изготовлены вышеописанным в примере 1 способом. Корковое вещество надпочечников представлено клетками, в цитоплазме которых содержится большое количество крупных митохондрий овальной формы и единичные липидные капли, не дающие положительной реакции с реактивом Шиффа. Клетки окружены капиллярами, чья базальная мембрана ШИК-положительна. В семенниках сперматогенный эпителий содержит крупные ядра с деконденсированным хроматином низкой плотности, дающим слабую реакцию Фельгена. Сперматозоиды содержат в головке сильно конденсированный хроматин, а в хвостике - большое количество гликопротеинов на плазмолемме, вследствие чего дают резко положительную ШИК-реакцию и реакцию Фельгена.
На фиг. 6 показаны результаты реакции на корковом веществе надпочечников. Ядра клеток имеют сиренево-розовую окраску, в цитоплазме видны крупные неокрашенные капли липидов (указаны стрелками) и более мелкие неокрашенные митохондрии. Яркую окраску дают базальные мембраны капилляров.
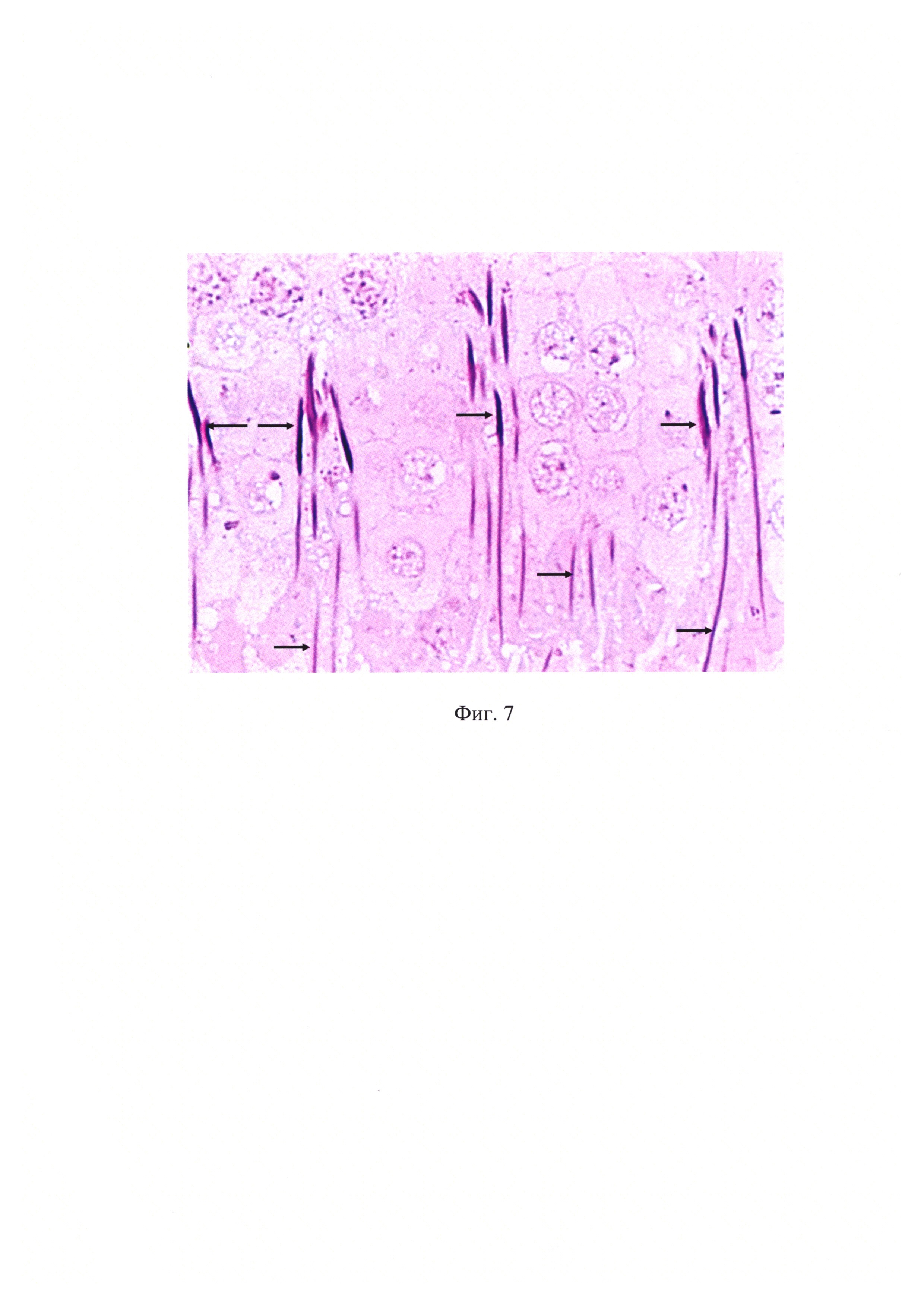
На фиг. 7 представлены результаты гистохимических реакций заявленным способом в препаратах семенников. В сперматогенном эпителии розово-сиреневую окраску дают хромосомы, яркую малиново-фиолетовую окраску - головки, и малиново-сиреневую - хвостики сперматозоидов (указаны стрелками).
Следовательно, заявленный способ характеризуется отсутствием органоспецифичности положительных реакций, то есть является универсальным для выявления ДНК и углеводных компонентов в органах и тканях.
Таким образом, заявленный способ является эффективным методом выявления ДНК, полисахаридов и углеводных компонентов биополимеров в полутонких срезах образцов разнообразных тканей и органов, залитых в смесь различных эпоксидных смол. Данный метод отличается также высокой сохранностью материала и простотой исполнения, так как не требует использования термостатов и нагревательных столиков.
Литература
1. Гайер Г. Электронная гистохимия. - М.: Мир, 1974. - 488 с.
2. Конарев В.Г., Тютерев С.Л. Методы биохимии и цитохимии нуклеиновых кислот растений. - Л.: Колос, 1970. - 204 с.
3. Петрова А.С., Полонская Н.Ю. Глава 17. Основные методы окрашивания цитологических препаратов // Микроскопическая техника: руководство / Под ред. Д.С. Саркисова, Л.Ю. Перова. - М.: Медицина, 1996. - 544 с.
4. Пирс Э. Гистохимия. Пер. с англ. - М.: Издательство иностранной литературы, 1962. - 962 с.
5. Carson F., Hladik С. Histotechnology: A Self-Instructional Text (3 ed.). - Hong Kong: American Society for Clinical Pathology Press, 2009. - P. 137-139.
6. Cerri PS, Sasso-Cerri E. Staining methods applied to glycol methacrylate embedded tissue sections // Micron - 2003. - Vol. 34. - No 8. - P. 365-372.
7. DiBella R., Hashimoto K. A new method for PAS stain of osmium-fixed Araldite-embedded thick tissue section // J. Invest. Dermatol. - 1966. - Vol. 47. - P. 503-505.
8. Scott J., Harbinson R. Periodate oxidation of acid polysaccharides. II. Rates of oxidation of uronic acids in hyalyuronides and acid mucopolysaccharides // Histochemie. - 1969. - Vol. 19. - P. 155-161.
9. Stockert J. Feulgen positive nucleoli in Epon semithin sections: Fact or artifact? // Experientia. 1978. - Vol. 33. - No 12. - P. 1669-1670.
Способ одновременного гистохимического выявления дезоксирибонуклеопротеинов, полисахаридов и углеводных компонентов биополимеров в полутонких срезах тканей и органов, заключающийся в окислении срезов 1%-ным водным раствором перйодата калия в течение 7-10 мин с последующей отмывкой срезов в дистиллированной воде и подсушиванием срезов; инкубации в темноте с реактивом Шиффа в течение 25-40 мин с последующей отмывкой в течение 2-3 мин в проточной, по 1 мин в сернистой и дистиллированной воде и получением розово-фиолетового окрашивания в образцах, отличающийся тем, что образцы, предварительно залитые в смесь эпона и аралдита, гидролизуют 0,5-0,7 М раствором гидроксида калия в абсолютном метаноле при комнатной температуре с последующим удалением продуктов гидролиза при отмывании абсолютным этанолом и дистиллированной водой.