Результат интеллектуальной деятельности: Композиции длительного действия на основе кетопрофена
Вид РИД
Изобретение
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Данное изобретение относится к новой композиции длительного действия, содержащей сложноэфирную пролекарственную форму кетопрофена и по меньшей мере один ветеринарно приемлемый триглицерид и возможно консервант и/или ветеринарно приемлемый эксципиент. В изобретении также описан способ лечения животного, страдающего лихорадкой, болью и/или воспалением, указанной композицией длительного действия.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Настоящее изобретение относится к новой композиции длительного действия, содержащей сложноэфирную пролекарственную форму кетопрофена и по меньшей мере один ветеринарно приемлемый триглицерид и возможно по меньшей мере один консервант и/или по меньшей мере один ветеринарно приемлемый эксципиент. В изобретении также описан способ лечения животного, страдающего лихорадкой, болью и/или воспалением, путем введения указанной композиции длительного действия. Пролекарственные формы кетопрофена, а также кетопрофен хорошо известны в данной области техники. Так же существует много известных композиций для местного применения, пероральных и инъекционных композиций, которые можно использовать вместе с кетопрофеном и его пролекарственными формами. Согласно настоящему изобретению предложена улучшенная композиция длительного действия, содержащая по меньшей мере одну сложноэфирную пролекарственную форму кетопрофена. В частности, композиция длительного действия представляет собой инъекционную композицию.
Нестероидные противовоспалительные лекарственные средства (NSAID) ингибируют ферменты циклооксигеназы СОХ-1 и СОХ-2, тем самым ингибируя синтез простагландинов, которые участвуют в развитии как лихорадки, так и боли. Кетопрофен, 2-(3-бензоилфенил)-пропионовая кислота (рацемат),
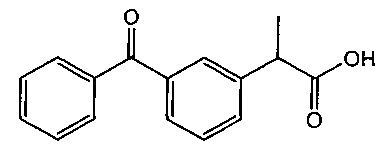
представляет собой NSAID, которое уже давно признано как полезное средство для лечения лихорадки, боли и/или воспаления (т.е. как жаропонижающий и аналгезирующий агент). В качестве аналгезирующего агента кетопрофен по меньшей мере так же эффективен, как и другие доступные высокоэффективные соединения, представляющие собой NSAID, такие как индометацин, мелоксикам, флуниксина меглумин и фенилбутазон. В качестве жаропонижающего агента кетопрофен более эффективен, чем мелоксикам.
Современные схемы лечения с применением NSAID разработаны для введения один раз в сутки, и при их использовании достигают различных степеней успеха по результатам измерений эффективности, включая продолжительность действия и токсичность. Таким образом, существует потребность в стабильной и эффективной жаропонижающей и/или аналгезирующей композиции длительного действия, в частности, композиции, которая может обеспечить эффективное действие в течение от 2 до 5 суток после введения однократной инъекционной дозы.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В настоящем изобретении описана композиция длительного действия на основе кетопрофена для применения в лечении боли, воспаления и/или лихорадки у животных. Композиция длительного действия содержит а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид, и возможно в) по меньшей мере один консервант, и возможно г) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент. Согласно другому аспекту изобретения композиция длительного действия содержит а) сложноэфирную пролекарственную форму кетопрофена и б) по меньшей мере один ветеринарно приемлемый триглицерид. Согласно еще одному аспекту изобретения композиция длительного действия содержит а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид и в) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент. Согласно еще одному аспекту изобретения композиция длительного действия содержит а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид и в) по меньшей мере один консервант. Согласно еще одному аспекту изобретения композиция длительного действия содержит а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид, в) по меньшей мере один консервант и г) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент.
Согласно другому аспекту изобретения сложноэфирная пролекарственная форма кетопрофена представляет собой алкиловый эфир (например, метиловый, этиловый, пропиловый, изопропиловый и тому подобное), бензиловый эфир, никотинамидный эфир, гликолевый эфир (например, полиэтиленгликолевый эфир, пропиленгликолевый моноэфир и пропиленгликолевый диэфир и их смеси). Согласно другому аспекту изобретения сложный эфир представляет собой алкиловый эфир (например, метиловый, этиловый, пропиловый, изопропиловый и их смеси). Согласно другому аспекту изобретения сложный эфир представляет собой метиловый эфир. Согласно другому аспекту изобретения сложный эфир представляет собой этиловый эфир. Согласно другому аспекту изобретения сложный эфир представляет собой пропиловый эфир. Согласно другому аспекту изобретения сложный эфир представляет собой изопропиловый эфир. Согласно другому аспекту изобретения сложный эфир представляет собой бензиловый эфир. Согласно другому аспекту изобретения сложный эфир представляет собой никотинамидный эфир. Согласно другому аспекту изобретения сложный эфир представляет собой гликолевый эфир (например, полиэтиленгликолевый эфир, пропиленгликолевый моноэфир, пропиленгликолевый диэфир и их смеси). Согласно другому аспекту изобретения сложный эфир представляет собой полиэтиленгликолевый эфир. Согласно другому аспекту изобретения сложный эфир представляет собой пропиленгликолевый моноэфир, пропиленгликолевый диэфир и их смеси. Согласно другому аспекту изобретения сложный эфир представляет собой пропиленгликолевый моноэфир. Согласно другому аспекту изобретения сложный эфир представляет собой пропиленгликолевый диэфир. Согласно другому аспекту изобретения сложный эфир представляет собой диастереомер пропиленгликолевого эфира.
Согласно другому аспекту изобретения композиция длительного действия представляет собой ветеринарную композицию. Согласно еще одному аспекту изобретения композиция длительного действия представляет собой инъекционную ветеринарную композицию. Согласно еще одному аспекту изобретения ветеринарная инъекционная композиция длительного действия представляет собой инъекционную композицию для внутримышечного введения. Согласно еще одному аспекту изобретения ветеринарная инъекционная композиция длительного действия представляет собой инъекционную композицию для подкожного введения.
Согласно другому аспекту изобретения ветеринарно приемлемый триглицерид (в том числе триглицеридоподобное вещество) выбран из группы, состоящей из триглицерида каприловой/каприновой кислоты, дикаприлата/дикапрата пропиленгликоля (триглицеридоподобного вещества), триглицерида каприловой/каприновой/линолевой кислоты, триацетата глицерина (триацетина), касторового масла, хлопкового масла, кунжутного масла и их смесей. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид выбран из группы, состоящей из триглицерида каприловой/каприновой кислоты, дикаприлата/дикапрата пропиленгликоля, триацетата глицерина, касторового масла, хлопкового масла и их смесей. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид выбран из группы, состоящей из триглицерида каприловой/каприновой кислоты, триацетата глицерина и касторового масла и их смесей. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид выбран из группы, состоящей из триглицерида каприловой/каприновой кислоты и триацетина и их смесей. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид выбран из группы, состоящей из триглицерида каприловой/каприновой кислоты и касторового масла и их смесей. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид представляет собой триглицерид каприловой/каприновой кислоты. Согласно еще одному аспекту изобретения триглицерид каприловой/каприновой кислоты представляет собой миглиол 812. Согласно еще одному аспекту изобретения триглицерид представляет собой триацетат глицерина. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид представляет собой касторовое масло. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид выбран из дикаприлата/дикапрата пропиленгликоля, триацетата глицерина, касторового масла и их смесей. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид представляет собой смесь двух триглицеридов, включающую дикаприлат/дикапрат пропиленгликоля и триацетин. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид представляет собой смесь двух триглицеридов, включающую дикаприлат/дикапрат пропиленгликоля и касторовое масло. Согласно еще одному аспекту изобретения ветеринарно приемлемый триглицерид представляет собой дикаприлат/дикапрат пропиленгликоля, в частности, миглиол 840.
Согласно еще одному аспекту изобретения композиция дополнительно содержит по меньшей мере один консервант. Согласно еще одному аспекту изобретения консервант выбран из группы, состоящей из бутилированного гидрокситолуола, бутилированного гидроксианизола, бензилового спирта и их смесей. Согласно еще одному аспекту изобретения консервант выбран из группы, состоящей из бутилированного гидрокситолуола и бутилированного гидроксианизола и их смесей. Согласно еще одному аспекту изобретения консервант представляет собой бутилированный гидрокситолуол. Согласно еще одному аспекту изобретения консервант представляет собой бутилированный гидроксианизол. Согласно еще одному аспекту изобретения консервант представляет собой бензиловый спирт.
Согласно еще одному аспекту изобретения композиция дополнительно содержит по меньшей мере один ветеринарно приемлемый эксципиент. Согласно еще одному аспекту изобретения этот дополнительный ветеринарно приемлемый эксципиент выбран из группы, состоящей из тетрагликоля, транскутола, коллифора HS15, полиэтиленгликоля, пропиленгликоля, пирролидонов, этанола, бензилового спирта, глицерилмоностеарата, глицерилмоноолеата, этилолеата, изопропилмиристата, бензилбензоата и их смесей.
Согласно еще одному аспекту изобретения предложен способ лечения животного от лихорадки, боли и/или воспаления, включающий введение указанному животному, нуждающемуся в этом, ветеринарной композиции длительного действия, содержащей а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид, и возможно в) по меньшей мере один консервант, и возможно г) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент. Согласно еще одному аспекту изобретения предложен способ лечения животного от лихорадки, боли и/или воспаления, включающий введение указанному животному, нуждающемуся в этом, ветеринарной композиции длительного действия, содержащей а) сложноэфирную пролекарственную форму кетопрофена и б) по меньшей мере один ветеринарно приемлемый триглицерид. Согласно еще одному аспекту настоящего изобретения предложен способ лечения животного от лихорадки, боли и/или воспаления, включающий введение указанному животному, нуждающемуся в этом, ветеринарной композиции длительного действия, содержащей а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид и в) по меньшей мере один консервант. Согласно еще одному аспекту настоящего изобретения предложен способ лечения животного от лихорадки, боли и/или воспаления, включающий введение указанному животному, нуждающемуся в этом, ветеринарной композиции длительного действия, содержащей а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид и в) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент. Согласно еще одному аспекту настоящего изобретения предложен способ лечения животного от лихорадки, боли и/или воспаления, включающий введение указанному животному, нуждающемуся в этом, ветеринарной композиции длительного действия, содержащей а) сложноэфирную пролекарственную форму кетопрофена, б) по меньшей мере один ветеринарно приемлемый триглицерид, в) по меньшей мере один консервант и г) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент.
Согласно еще одному аспекту изобретения предложен способ лечения животного от лихорадки, боли и/или воспаления, включающий введение указанному животному, нуждающемуся в этом, ветеринарной композиции длительного действия, где сложноэфирная пролекарственная форма кетопрофена выбрана из группы, состоящей из метилового эфира, этилового эфира, бензилового эфира, никотинамидного эфира, полиэтиленгликолевого эфира, пропиленгликолевого моноэфира, пропиленгликолевого диэфира, пропиленгликолевого моно- и диэфира и диастереомеров пропиленгликолевого эфира.
Согласно другому аспекту изобретения предложен способ лечения боли у животного путем введения животному, нуждающемуся в этом, эффективного количества ветеринарной композиции длительного действия по настоящему изобретению. Согласно другому аспекту изобретения предложен способ лечения лихорадки у животного путем введения животному, нуждающемуся в этом, эффективного количества ветеринарной композиции длительного действия по настоящему изобретению. Согласно другому аспекту изобретения предложен способ лечения воспаления у животного путем введения животному, нуждающемуся в этом, эффективного количества ветеринарной композиции длительного действия по настоящему изобретению.
Согласно другому аспекту изобретения композицию длительного действия вводят посредством инъекции. Согласно еще одному аспекту изобретения композиция представляет собой инъекционную композицию. Согласно еще одному аспекту изобретения инъекционная композиция представляет собой вводимую внутримышечно (в.м.) инъекционную композицию. Согласно еще одному аспекту изобретения ветеринарная инъекционная композиция представляет собой вводимую подкожно инъекционную композицию.
Согласно другому аспекту изобретения количество пролекарственной формы кетопрофена вводят животному в дозе от примерно 0,5 до 12 мг/кг. Согласно еще одному аспекту изобретения количество пролекарственной формы кетопрофена находится в диапазоне от примерно 10 мг/мл до примерно 300 мг/мл.
Согласно еще одному аспекту изобретения предложено применение композиции длительного действия по настоящему изобретению для изготовления лекарственного средства для лечения боли, лихорадки и/или воспаления у животного, нуждающегося в этом.
Согласно другому аспекту изобретения предложено применение композиции длительного действия, содержащей а) пролекарственную форму кетопрофена, выбранную из группы, состоящей из соединений формулы 1, формулы 2, формулы 3, формулы 4, формулы 5, формулы 6 и формулы 7 и их смесей, б) по меньшей мере один ветеринарно приемлемый триглицерид, и возможно в) по меньшей мере один консервант, и возможно г) по меньшей мере один дополнительный ветеринарно приемлемый эксципиент, для лечения или предупреждения боли, лихорадки и/или воспаления у животного, нуждающегося в этом.
ОПРЕДЕЛЕНИЯ
Для задач настоящего изобретения, описанного и заявленного в данном документе, приведенные ниже термины и фразы определены следующим образом.
«Примерно», при использовании вместе с поддающейся количественному измерению численной переменной, относится к указанному значению этой переменной и ко всем значениям этой переменной, которые находятся в пределах экспериментальной ошибки данного указанного значения (например, в пределах 95%-ного доверительного интервала для среднего значения) или в пределах 10 процентов от данного указанного значения, но не более.
«Животное», при использовании в данном описании, если не указано иное, относится к отдельному животному, и этим указанным отдельным животным является млекопитающее. Конкретно, «млекопитающее» относится к позвоночным животным, являющимся человеком и не являющимся человеком, которые считаются представителями таксономического класса млекопитающих. Неисключающие примеры не являющихся человеком млекопитающих включают домашних и сельскохозяйственных животных. Неисключающие примеры домашних животных включают: собаку, кошку и лошадь. Неисключающие примеры сельскохозяйственных животных включают: свинью, козу, овцу и крупный рогатый скот. Предпочтительными сельскохозяйственными животными являются крупный рогатый скот и свиньи. Предпочтительным животным является свинья, и только вторым предпочтительным животным является крупный рогатый скот.
«Возможно», при использовании в данном описании, если не указано иное, относится к рекомендательному включению по меньшей мере одного консерванта и/или по меньшей мере одного дополнительного ветеринарно приемлемого эксципиента; т.е. эти дополнительные ингредиенты могут не потребоваться.
«Терапевтически эффективное количество», при использовании в данном описании, если не указано иное, относится к количеству одной из пролекарственных форм кетопрофена в композиции длительного действия по настоящему изобретению, которое (1) лечит или предупреждает конкретное сопровождающееся повышением температуры тела, воспалительное и/или вызывающее боль состояние, (2) ослабляет, уменьшает интенсивность симптомов или устраняет один или более симптомов этого конкретного сопровождающегося повышением температуры тела, воспалительного и/или вызывающего боль состояния либо (3) предупреждает или задерживает начало возникновения одного или более симптомов этого конкретного сопровождающегося повышением температуры тела, воспалительного и/или вызывающего боль состояния, описанного в данной заявке. Терапевтически эффективное количество охватывает диапазон доз от примерно 0,5 до 12 мг/кг.
«Лечение», «подвергание лечению» и тому подобное, при использовании в данном описании, если не указано иное, относится к реверсированию, облегчению или подавлению сопровождающегося повышением температуры тела, воспалительного и/или вызывающего боль состояния. При использовании в данном описании эти термины также охватывают, в зависимости от состояния животного, предупреждение начала возникновения расстройства или состояния либо симптомов, ассоциированных с расстройством или состоянием, включая ослабление тяжести расстройства или состояния либо ассоциированных с ними симптомов, перед поражением указанным сопровождающимся повышением температуры тела, воспалительным и/или вызывающим боль состоянием. Таким образом, «подвергание лечению» может относиться к введению композиции длительного действия по настоящему изобретению животному, которое в момент введения не поражено данным сопровождающимся повышением температуры тела, воспалительным и/или вызывающим боль состоянием, например, в качестве профилактического лечения. «Лечение» также охватывает предупреждение рецидива сопровождающегося повышением температуры тела, воспалительного и/или вызывающего боль состояния либо ассоциированных с ними симптомов.
«Ветеринарно приемлемый», при использовании в данном описании, если не указано иное, указывает на то, что пролекарственная форма кетопрофена и композиция длительного действия должны быть совместимы химически и/или токсикологически с другими ингредиентами, содержащимися в композиции, и/или с животным, подвергаемым лечению ими. Этот термин является синонимом термина «фармацевтически приемлемый».
ПОДРОБНОЕ ОПИСАНИЕ
Среднему специалисту в данной области техники следует понимать, что настоящее обсуждение представляет собой описание только иллюстративных воплощений и не предназначено для ограничения более широких аспектов настоящего изобретения, которые воплощаются в данной иллюстративной интерпретации. Действительно, специалистам в данной области техники будет очевидно, что в настоящем изобретении могут быть выполнены различные модификации и варианты без отклонения от объема или сущности изобретения. Например, признаки, проиллюстрированные или описанные как часть одного из воплощений, можно использовать в другом воплощении, получая еще одно воплощение. Подразумевается, что настоящее изобретение охватывает такие модификации и варианты, которые попадают в объем прилагаемой формулы изобретения, и их эквиваленты.
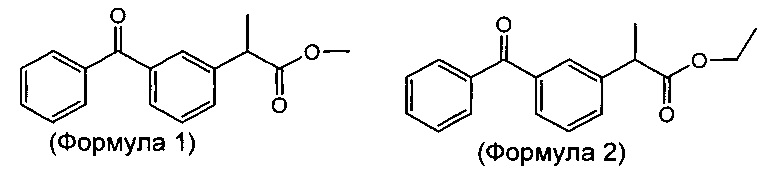
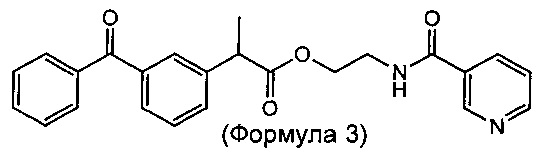
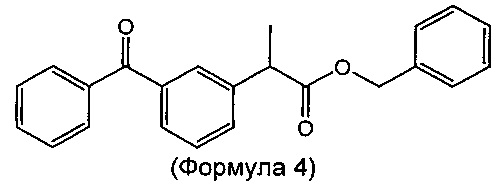
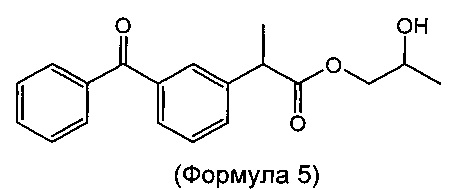
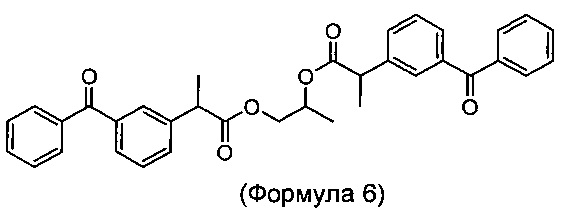
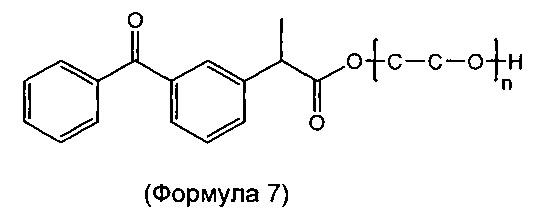
Согласно изобретению предложена стабильная ветеринарная композиция длительного действия для лечения лихорадки, боли и/или воспаления у животного, нуждающегося в этом, включающего введение эффективного количества сложноэфирной пролекарственной формы кетопрофена, выбранной из группы, состоящей из а) метилового эфира (соединения формулы 1, метил-2-(3-бензоилфенил)пропаноата), б) этилового эфира (соединения формулы 2, этил-2-(3-бензоилфенил)пропаноата), в) никотинамидного эфира (соединения формулы 3, 2-(никотинамидо)этил-2-(3-бензоилфенил)пропаноата), г) бензилового эфира (соединения формулы 4, (бензил-2-(3-бензоилфенил)пропаноата), д) пропиленгликолевого моноэфира (соединения формулы 5, 2-гидроксипропил-2-(3-бензоилфенил)пропаноата), е) пропиленгликолевого диэфира (соединения формулы 6, пропан-1,2-диил-бис(2-(3-бензоилфенил)пропаноата), ж) смеси соединения формулы 5 и соединения формулы 6 и з) полиэтиленгликолевого эфира (соединения формулы 7). Сложные пропиленгликолевые эфиры по настоящему изобретению также включают все свои диастереомеры.
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 .
.
После инъекции сложноэфирная пролекарственная форма кетопрофена постепенно высвобождается из композиции в месте инъекции. После высвобождения в системный кровоток (например, кровь/плазму) это сложноэфирное пролекарство гидролизуется ферментами печени. Исходная (активная) форма лекарственного средства, кетопрофен, является преобладающим циркулирующим в крови NSAID соединением, которое обеспечивает установленную эффективность.
Кетопрофен может быть получен в соответствии с методиками, описанными в US 3641127. Пролекарственные формы в виде алкиловых эфиров кетопрофена могут быть получены в соответствии с методиками, описанными в International Journal of Pharmaceutics, 43 (1988), pp. 101-110. Кроме того, метиловый эфир можно получить, используя обычные реагенты для этерификации, как описано в Liang, Yu-Feng, et. al., Highly Efficient C-H Hydroxylation of Carbonyl Compounds with Oxygen under Mild Conditions, Angewandte Chemie, International Edition, Volume 53, Issue 2, pages 548-552, 2014; схема 5. Пролекарственная форма кетопрофена в виде никотинамидного эфира может быть получена в соответствии с методиками, описанными в European Journal of Medicinal Chemistry, 39 (2004), pp. 715-727. Бензиловый эфир может быть получен посредством реакции этерификации по Фишеру, которая включает обработку карбоновой кислоты (кетопрофена) спиртом (например бензиловым спиртом) в присутствии дегидратирующего агента, например серной кислоты, как описано в Med. Chem. Res., 21 (2012), pp. 3361-3368. Сложные алкиловые эфиры также могут быть получены этим способом с использованием алифатического спирта. Сложные эфиры гликолей могут быть получены в соответствии со способами, описанными в патенте США 4560785.
Кетопрофен демонстрирует мощное противовоспалительное, аналгезирующее и жаропонижающее действие, которое ассоциировано с ингибированием синтеза простагландинов и антагонизмом действия брадикинина. Кетопрофен неселективно ингибирует активность СОХ-1 и СОХ-2, что приводит к блокированию образования простагландинов, в частности PGE2, предупреждая развитие гипералгезии. Значение IC50 для кетопрофена составляет 4-8 нМ по результатам анализа неселективного действия в отношении СОХ человека, что соответствует в 6-12 раз более сильному функциональному действию по сравнению с другими оцененными NSAID (например напроксеном или индометацином). Kantor, Т., Pharmacotherapy, 6: 93-103 (1986). Значения IC50 для кетопрофена в отношении свиных ферментов-ортологов СОХ-1 и СОХ-2 аналогичны таковым для человека и находятся в диапазоне 6-7 нМ, как изложено в данном описании. В противоположность этому, кетопрофен оказывает менее сильное действие в отношении бычьих ферментов-ортологов СОХ-1 и СОХ-2, демонстрируя значение IC50, составляющее 30 нМ в отношении СОХ-1, и значение IC50, составляющее 220 нМ в отношении СОХ-2, как изложено в данном описании. Кетопрофен также обладает функциональной антагонистической активностью в отношении брадикинина, причем его эффективность в 8 раз превышает таковую, показанную при использовании классического NSAID индометацина. Julou, L., et al., Scand. J. Rheumatol. Suppl. 0: 33-44 (1976). Считается, что помимо ингибирования циклооксигеназы кетопрофен оказывает дополнительный противовоспалительный эффект, ингибируя липоксигеназу.
Композиции, в частности ветеринарные композиции, более конкретно ветеринарные композиции длительного действия, подходящие для доставки по меньшей мере одной из пролекарственных форм кетопрофена по настоящему изобретению, и способы их изготовления будут легко понятны специалистам в данной области техники. Такие композиции и способы их изготовления можно найти, например, в "Remington's Pharmaceutical Sciences", 19th Edition (Mack Publishing Company, 1995).
В настоящем изобретении ветеринарно приемлемый триглицерид также охватывает моно- и ди-глицериды. Кроме того, триглицерид охватывает масла природного происхождения и полусинтетические/синтетические масла, например касторовое масло, хлопковое масло, кунжутное масло, льняное масло, сафлоровое масло, арахисовое масло, соевое масло, кокосовое масло, оливковое масло, кукурузное масло, миндальное масло, маковое масло, подсолнечное масло, растительное масло и их смеси. Триглицериды также включают: трикаприлин, триглицерид каприловой/каприновой кислоты (например, миглиол 801, миглиол 812, каптекс 355 и тому подобное), триглицерид каприловой/каприновой/линолевой кислоты, триглицерид каприловой/каприновой/янтарной кислоты, дикаприлат/дикапрат пропиленгликоля (например, миглиол 840 и каптекс 200 и тому подобное), триацетат глицерина (триацетин), глицерилстеараты и тому подобное, включая их смеси. Предпочтительным триглицеридом является касторовое масло, триацетат глицерина, триглицерид каприловой/каприновой/линолевой кислоты, триглицерид каприловой/каприновой/янтарной кислоты, дикаприлат/дикапрат пропиленгликоля (например, миглиол 840 и каптекс 200), триглицерид каприловой/каприновой кислоты и их смеси. Более предпочтительным триглицеридом является триглицерид каприловой/каприновой кислоты, триацетат глицерина, дикаприлат/дикапрат пропиленгликоля, касторовое масло и их смеси. Еще более предпочтительным триглицеридом является триглицерид каприловой/каприновой кислоты. Другим более предпочтительным триглицеридом является триацетат глицерина. Другим более предпочтительным триглицеридом является дикаприлат/дикапрат пропиленгликоля. Другим более предпочтительным триглицеридом является касторовое масло. Если триглицеридом в композиции является касторовое масло, то нет необходимости в других глицеридах и/или триглицеридах, например пропил-дикаприлатах/дикапратах, триглицеридах каприловой/каприновой кислоты или ацилированных моноглицеридах либо их смесях. Еще более предпочтительным триглицеридом каприловой/каприновой кислоты является миглиол 812. Другим еще более предпочтительным триглицеридом типа дикаприлата/дикапрата пропиленгликоля является миглиол 840.
В настоящем изобретении композиция длительного действия возможно содержит по меньшей мере один консервант. В настоящем изобретении композиция длительного действия дополнительно содержит по меньшей мере один консервант. Консервант может представлять собой антимикробный, противогрибковый и/или антиоксидантный консервант. Неограничивающие примеры консервантов включают: бензойную кислоту, сорбиновую кислоту, аскорбиновую кислоту, лимонную кислоту, бензиловый спирт, токоферолы, этанол, бисульфат натрия, хлорбутанол, 2-этоксиэтанол, метил-, этил-, пропил- и бутил-парабены и их комбинации, хлоргексидин, фенол, бутилированный гидрокситолуол (ВНТ), бутилированный гидроксианизол (ВНА), бензоат натрия, их смеси и тому подобное. Предпочтительный консервант выбран из группы, состоящей из ВНА, ВНТ, бензилового спирта и их смесей.
В настоящем изобретении композиция длительного действия возможно содержит по меньшей мере один дополнительный ветеринарно приемлемый эксципиент. В настоящем изобретении композиция длительного действия дополнительно содержит по меньшей мере один дополнительный ветеринарно приемлемый эксципиент. Например, дополнительный(е) ветеринарно приемлемый(е) эксципиент(ы) может(гут) включать буферные агенты (например ацетат натрия, ацетат аммония, аспарагиновую кислоту, диэтаноламин, карбонат натрия, фосфат калия и тому подобное), модификаторы вязкости (например стеараты алюминия (моно- и ди-стеараты), натриевую соль карбоксиметилцеллюлозы, метилцеллюлозу и тому подобное), растворители (например бензилбензоат, полиэтиленгликоль (например ПЭГ200, ПЭГ 400 и тому подобное), N,N-диметилацетамид, пропиленгликоль, этанол, бензиловый спирт, диметилсульфоксид, N-метилпирролидон, 2-пирролидон, глицеролформаль, глицерин, изопропилмиристат, тетрагликоль (гликофурол, простой эфир тетрагидрофурфурилового спирта и полиэтиленгликоля), простой моноэтиловый эфир диэтиленгликоля (DEGMEE, например транскутол), простой монометиловый эфир диэтиленгликоля (DEGMME) и тому подобное, эмульгатор (например полиэтоксилированные простые эфиры, сложные эфиры и масла, такие как макроголы, и фосфолипиды, среди которых типичным является лецитин, сложные эфиры сорбитана (например полисорбат 80 (спан 80), спан 40, спан 60 и тому подобное)), кремофоры (например кремофор EL, кремофор RH40 и тому подобное), полисорбаты (например твин 20, твин 80 и тому подобное), 15-гидроксистеараты полиэтиленгликоля (например коллифор HS15, кродасол HS15 и тому подобное), 15-гидроксистеарат макрогола, сополимеры полиоксиэтилена-полиоксипропилена и полиоксиэтиленовые производные витамина Е, такие как сукцинат токоферил-полиэтиленгликоля 1000 и тому подобное) и модификатор тоничности (например сорбит, ксилит, маннит, декстрозу, глюкозу, пропиленгликоль, сахарозу, неорганические соли, такие как хлорид натрия, и лактозу и тому подобное).
Такие композиции готовят традиционным образом в соответствии со стандартной медицинской или ветеринарной практикой.
Количества этих сложноэфирных пролекарственных форм кетопрофена легко определяются специалистом в данной области и, кроме того, зависят от количества дозы и объема дозы конечной композиции длительного действия. Подразумевается, что указанные дозовые количества и дозовые объемы являются терапевтически эффективными дозовыми количествами и дозовыми объемами. Репрезентативные количества терапевтически эффективного количества пролекарственной формы кетопрофена формулы 1, формулы 2 или формулы 3, формулы 4, формулы 5, формулы 6, формулы 5 и формулы 6, и формулы 7 и их смесей находятся в диапазоне от примерно 0,1 до 20 мг/кг. Более предпочтительные репрезентативные количества терапевтически эффективного количества сложноэфирной пролекарственной формы кетопрофена находятся в диапазоне от примерно 0,25 до 15 мг/кг. Еще более предпочтительные репрезентативные количества терапевтически эффективного количества сложноэфирной пролекарственной формы кетопрофена находятся в диапазоне от примерно 0,5 до 12 мг/кг. Еще более предпочтительные репрезентативные количества терапевтически эффективного количества сложноэфирной пролекарственной формы кетопрофена находятся в диапазоне от примерно 0,5 до 10 мг/кг. Репрезентативные количества сложноэфирной пролекарственной формы кетопрофена в композиции находятся в диапазоне от примерно 1 мг/мл до примерно 500 мг/мл. Более предпочтительное количество сложноэфирной пролекарственной формы кетопрофена в композиции находится в диапазоне от примерно 10 мг/мл до примерно 400 мг/мл. Еще более предпочтительное количество сложноэфирной пролекарственной формы кетопрофена в композиции находится в диапазоне от примерно 20 мг/мл до примерно 300 мг/мл.
Композиция длительного действия по настоящему изобретению полезна в качестве противовоспалительного агента, жаропонижающего агента и аналгезирующего агента. Композицию длительного действия можно использовать в области ветеринарии, животноводства и для поддержания общественного здоровья, а именно, для обеспечения безопасности и здоровья годных в пищу животных, в частности сельскохозяйственных животных, например свиней и крупного рогатого скота.
Системная доставка пролекарственной формы кетопрофена посредством внутримышечной инъекции или подкожной инъекции обеспечивает получение животным (а именно, представителем крупного рогатого скота) всей лечебной дозы. Композицию длительного действия можно вводить посредством инъекции в ухо или в область, расположенную на стыке ушной раковины и черепа животного. Например, подкожную инъекцию вводят в область, расположенную на стыке ушной раковины с черепом, используя стерильную иглу (например, 16-го калибра, от 1,5 до 2,0 см), прикрепленную к такому устройству, как шприц, инжектор для многоразового введения, многоразовый шприц и тому подобное. Иглу направляют каудально по отношению к возвышению хряща ушной раковины на проксимальном конце хряща ушной раковины у основания обратной поверхности ладьевидной ямки (antiscaphal surface) и направляют рострально от каудальной стороны уха. Предпочтительно, чтобы инъекцию выполняли каудально по отношению к шейно-ушным мышцам и дорсокаудально по отношению к околоушной слюнной железе. После того, как игла введена полностью, вводящий лекарственное средство может оттянуть назад поршень шприца, чтобы убедиться, что игла не попадает в кровеносный сосуд. Как только игла оказывается в подкожной ткани, через нее выпускают соответствующий объем инъекционной композиции длительного действия и затем иглу извлекают. Чтобы свести к минимуму обратный ток введенной инъекцией композиции, к месту введения иглы предпочтительно прикладывается постоянное давление. Даже если нет необходимости во введении иглы параллельно коже, этот способ все же считается подкожной инъекцией ввиду использования короткой иглы и расположения места инъекции.
Инъекция через иглу представляет собой предпочтительный способ доставки, хотя аналогичным образом также можно использовать шприцы, шприцы-автоматы, шприцы для многоразового введения и шприцы-пистолеты.
Например, согласно современным схемам лечения Metacam® (мелоксикам) вводят инъекцией один раз в сутки для сдерживания боли и/или воспаления, ассоциированных с артритом. Последующие дозы должны быть введены через 24 часа после предшествующей дозы. Аналогичным образом, для лошадей рекомендовано вводить дозу флуниксина меглумина инъекционного один раз в сутки с повторным введением вплоть до 5 суток. Представителям крупного рогатого скота можно вводить дозу один раз в сутки в виде разовой дозы или дозы, разделенной на две дозы, вводимые один раз за промежуток времени 12 часов в течение вплоть до 3 суток. Кетопрофен (Anafen®) инъекционный также вводят посредством инъекции один раз в сутки в течение от 1 (свиньям) до пяти (лошадям) суток.
Согласно настоящему изобретению композицию длительного действия, содержащую по меньшей мере одну из сложноэфирных пролекарственных форм кетопрофена, по меньшей мере один ветеринарно приемлемый триглицерид, и возможно по меньшей мере один консервант, и возможно по меньшей мере один дополнительный ветеринарно приемлемый эксципиент, можно использовать один раз в течение каждых двух, трех, четырех или пяти суток, как будет необходимо. Композиция длительного действия предусмотрена для лечения боли, воспаления и/или ослабления лихорадки в течение вплоть до 48 часов, 72 часов, 96 часов и в некоторых случаях в течение вплоть до 120 часов после введения однократной инъекционной дозы. Таким образом, применение композиции длительного действия обеспечивает животному пролонгированное облегчение заболевания и также уменьшает число инъекций, выполняемых человеком, ухаживающим за животными.
Согласно настоящему изобретению композиция длительного действия, содержащая по меньшей мере одну из сложноэфирных пролекарственных форм кетопрофена, по меньшей мере один ветеринарно приемлемый триглицерид, и возможно по меньшей мере один консервант, и возможно по меньшей мере один дополнительный ветеринарно приемлемый эксципиент, может дополнительно содержать дополнительный биологически активный агент, например антибактериальный агент. Имеется целый ряд антибактериальных агентов, приемлемых для применения на животных. Эти антибактериальные агенты включают, без ограничения, следующие: макролиды, например тулатромицин (Draxxin®), тилдипирозин (Zuprevo®), тилмикозин (Micotil®), тилозина фосфат (Tylan®) и гамитромицин (Zactran®); цефалоспорины, например цефтиофур натрия (например Naxcel® и Excenel®), цефтиофура гидрохлорид (например Excenel RTU®, Excenel RTU EZ®, Spectramast®), цефтиофур кристаллический в форме свободной кислоты (Excede®), цефовецин натрия (Convenia®) и цефподоксима проксетил (Simplicef®); антибиотики группы линкозамидов, например линкомицин (Lincomix®), пирлимицина гидрохлорид (Pirsue®) и клиндамицина гидрохлорид (Antirobe®); фторхинолоны, например данофлоксацин (Advocin®), энрофлоксацин (Baytril®) и марбофлоксацин (Zeniquin®); и тетрациклины, например хлортетрациклин, окситетрациклин и доксициклин. Другие антибактериальные агенты включают, без ограничения, амоксициллина тригидрат и клавулановую кислоту (Clavamox®), спектиномицин (Adspec®), потенцированные сульфаниламиды, включая триметоприм/сульфадиазин (Tucoprim®) и сульфадиметоксин/орметоприм (Primor®); и флорфеникол (например Nuflor® и Nuflor® Gold).
Помимо все прочего, исходный агент, кетопрофен, также можно комбинировать с любым из антибактериальных агентов, описанных в данной заявке, например, кетопрофен и Draxxin®. Композиция, содержащая как кетопрофен, так и Draxxin® или кетопрофен и любой другой антибактериальный агент, описанный в данной заявке, может представлять собой или может не представлять собой композицию, содержащую ветеринарно приемлемый триглицерид и/или консервант, но может содержать по меньшей мере один ветеринарно приемлемый эксципиент, который описан в данной заявке, и/или любой(ые) дополнительный(ые) ветеринарно приемлемый(ые) эксципиент(ы), известный(ые) в данной области техники, для изготовления стабильной инъекционной композиции для животных.
Согласно настоящему изобретению композицию длительного действия, содержащую по меньшей мере одну сложноэфирную пролекарственную форму кетопрофена, по меньшей мере один ветеринарно приемлемый триглицерид, и возможно по меньшей мере один консервант, и возможно по меньшей мере один дополнительный ветеринарно приемлемый эксципиент, можно вводить одновременно или последовательно с антибактериальным агентом, т.е. в виде двух отдельных стандартных лекарственных форм. Иным образом, композиция длительного действия может дополнительно содержать антибактериальный агент, который можно вводить совместно в виде однократной инъекционной стандартной лекарственной формы. Аналогичным образом, кетопрофен можно вводить одновременно или последовательно с антибактериальным агентом независимо от того, приготовлены ли они вместе в виде однократной инъекционной стандартной лекарственной формы или в виде отдельных стандартных лекарственных форм.
Экспериментальный раздел
Сложные эфиры кетопрофена могут быть получены в соответствии со способами и методами, изложенными в данном описании. Альтернативно, метиловый эфир может быть получен согласно следующей схеме:
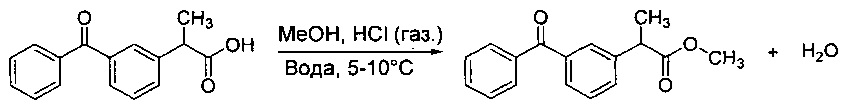
Кетопрофен (50 г) добавляли к метанолу (200 мл) при комнатной температуре и перемешивали до полного растворения. Раствор охлаждали до температуры примерно 5-10°С. Через этот раствор пропускали газообразный HCl, получая увеличение реакционной массы примерно на 23 г. Раствор нагревали до комнатной температуры при перемешивании. Затем раствор охлаждали до температуры примерно 0-5°С. По каплям добавляли охлажденную воду (200 мл), поддерживая температуру реакции примерно 0-20°С. Затем раствор перемешивали при комнатной температуре в течение примерно 30 минут. Твердые вещества отфильтровывали и промывали водой. Твердые вещества сушили под вакуумом при температуре примерно 40°С, получая примерно 52 г метилового эфира кетопрофена (98,6%).
ПРИМЕРЫ
В приведенных далее примерах композиции длительного действия сложноэфирная пролекарственная форма кетопрофена (КЕР) может представлять собой любое соединение из соединений формулы 1 (Ф1) - формулы 7 (Ф7) и их смеси. Неограничивающие ветеринарно приемлемые композиции длительного действия показаны ниже.
Композиция 1
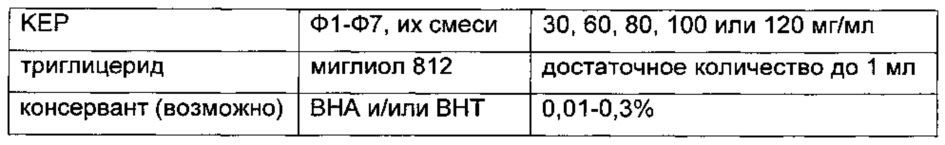
Композиция 2

Композиция 3
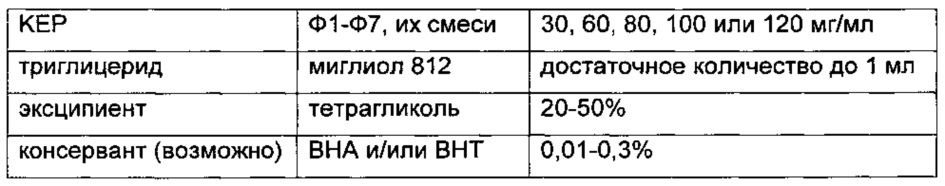
Композиция 4

Композиция 5

Композиция 6

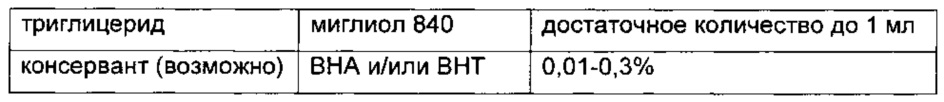
Композиция 7

Композиция 8
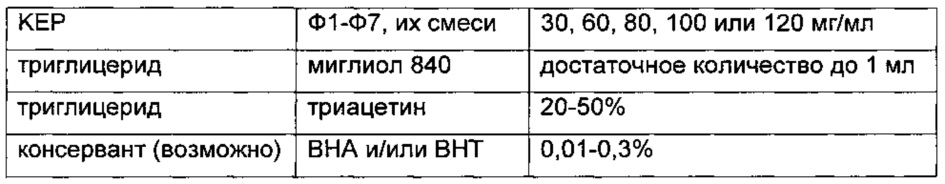
Композиция 9

Композиция 10

Композиция 11
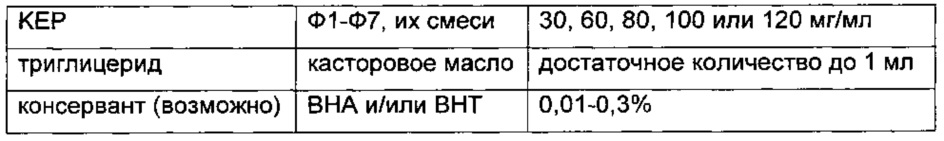
Композиция 12

Композиция 13
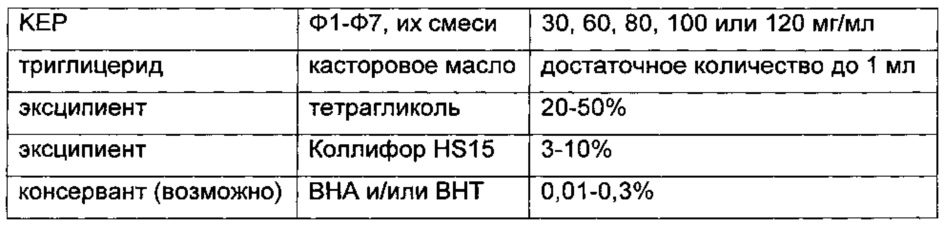
Композиция 14
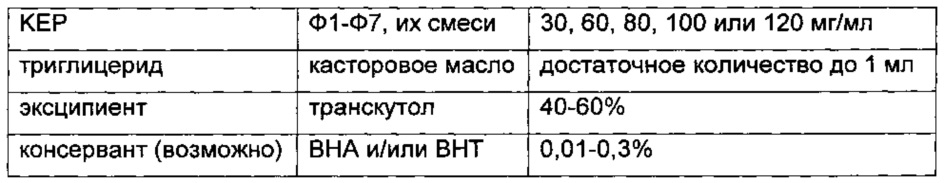
Показано, что соединение формулы 1 (60 мг/мл или 120 мг/мл) в композиции 1 (без консерванта) оставалось стабильным при хранении в прозрачных или желтых стеклянных флаконах или белых флаконах из полиэтилена высокой плотности (HDPE; high density polyethylene) при 25°С и 40°С и в условиях ускоренного определения стабильности при относительной влажности 60% и 75%. В результате добавления консерванта (например бензилового спирта или бутилгидрокситолуола (ВНТ)) получали аналогичные результаты по стабильности. Кроме того, композиция «60 мг/мл» также была стабильна при 4°С, 25°С, 40°С, 50°С и 60°С, независимо от того, было ли свободное пространство во флаконе заполнено воздухом или азотом.
БИОЛОГИЧЕСКИЙ РАЗДЕЛ
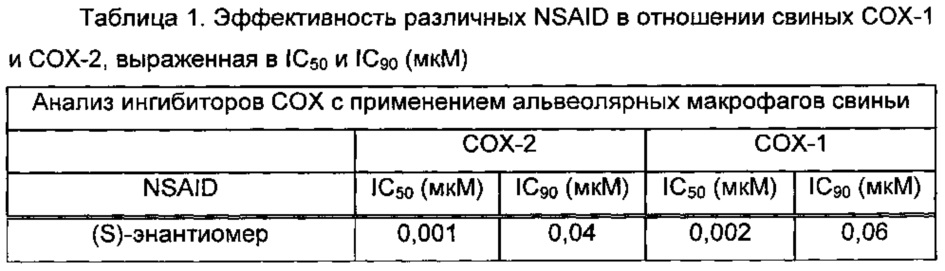
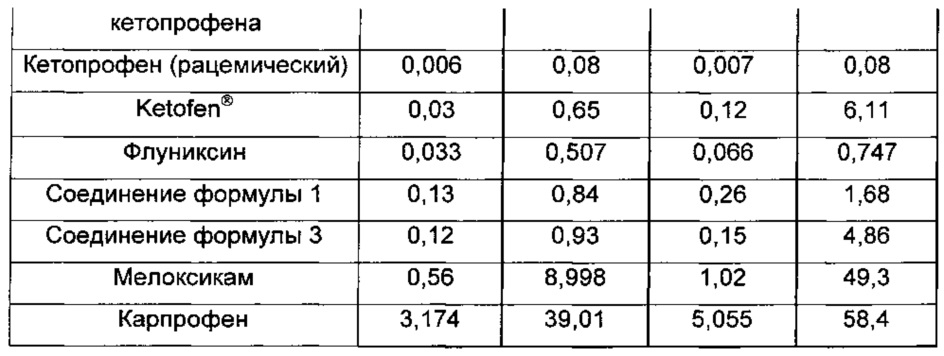
Активность in vitro ряда NSAID оценивали в отношении свиных ферментов СОХ-1 и СОХ-2, используя подходящий анализ на первичных клетках с применением альвеолярных макрофагов свиней. Использовали следующие NSAID: флуниксина меглумин (Banamine-S®), мелоксикам (Metacam®), кетопрофен (Ketofen®, инъекционный), S-энантиомер кетопрофена, кетопрофен (рацемический), карпрофен и пролекарственные формы кетопрофена (соединения формулы 1 и формулы 3). Альвеолярные макрофаги обрабатывали липополисахаридом (LPS) в присутствии различных количеств ингибиторов с целью продуцирования тромбоксана В2 (ТХВ2) и/или простагландина Е2 (PGE2). Супернатанты клеток собирали через 21-24 часа после инкубации и замораживали при -80°С до проведения количественного определения посредством иммуноферментного твердофазного анализа (ELISA). Полученные в анализе данные относительно ТХВ2 использовали в качестве индикатора ингибирования СОХ-1. Полученные в анализе данные относительно PGE2 использовали в качестве индикатора ингибирования СОХ-2. Каждое лекарственное средство тестировали в трех разных экспериментах, проведенных в три разных дня (как минимум). Процент ингибирования СОХ-1 или СОХ-2 рассчитывали для каждой концентрации лекарственного средства по среднему значению обнаруженной концентрации ТХВ2 или PGE2, соответственно. Усредненные кривые % ингибирования (зависимость % ингибирования от концентрации лекарственного средства) анализировали методом нелинейной регрессии, получая отдельно значения IC50 и IC90, которые приведены в порядке ранжирования эффективности в отношении СОХ-2, выраженной в IC50. Значения IC50 для рацемического кетопрофена в отношении свиных ферментов СОХ (Таблица 1) аналогичны значениям, приведенным в литературе для человека. Как показано в Таблице 1, кетопрофен (рацемат) проявляет слегка более сильное действие, чем флуниксин, и эффективность их обоих оказывается на порядок больше, чем у метилового эфира кетопрофена, который проявляет примерно в 5 раз более сильное действие по сравнению с мелоксикамом - классическим эталонным ингибитором СОХ-2.
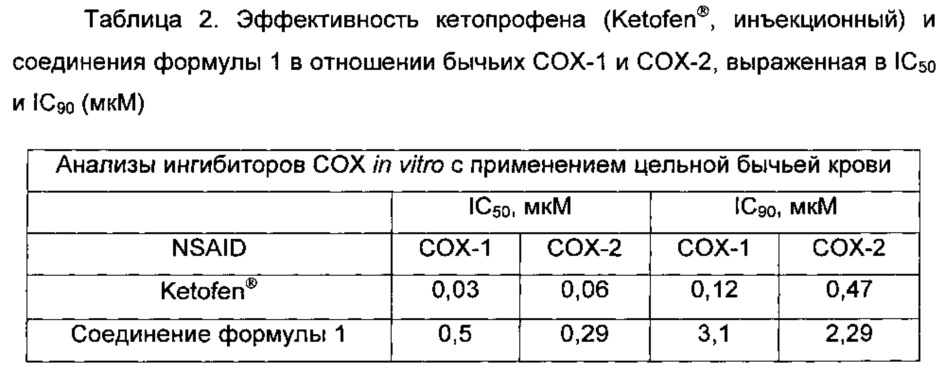
Кроме этого, активность in vitro кетопрофена и соединения формулы 1 оценивали в отношении бычьих ферментов СОХ-1 и СОХ-2, используя анализ с применением бычьей цельной крови. Кратко, для обоих анализов готовили образцы гепаринизированной крови. Анализ для СОХ-1 включал обработку крови протамином для аннулирования антикоагулянтных эффектов гепарина, приводящую в результате к коагуляции и образованию тромбоксана В2 (ТХВ2). Анализ для СОХ-2 включал обработку крови LPS для образования PGE2. Оба анализа проводили в присутствии различных количеств ингибиторов для ингибирования ТХВ2 или PGE2. И кетопрофен (Ketofen® инъекционный), и сложноэфирную пролекарственную форму кетопрофена, соединение формулы 1, тестировали в трех разных экспериментах, проведенных в три разных дня (как минимум). Процент ингибирования рассчитывали из начальных данных для каждой дозы лекарственного средства по среднему значению концентраций ТХВ2 или PGE2. Затем усредненные кривые % ингибирования (зависимость % ингибирования от концентрации лекарственного средства) анализировали методом нелинейной регрессии, получая отдельно значения IC50 и IC90. Как показано в Таблице 2, кетопрофен (рацемат) проявляет более сильное действие, чем соединение формулы 1, в отношении ингибирования бычьего фермента СОХ-1, но демонстрирует сходную с соединением формулы 1 эффективность в отношении фермента СОХ-2. При сравнении со свиными ферментами СОХ обнаружено, что и кетопрофен, и соединение формулы 1 демонстрируют более низкую эффективность в отношении бычьих СОХ-1 и СОХ-2.
Фармакокинетику кетопрофена у подсвинков (примерно 15 кг) оценивали в водной композиции после внутривенного и внутримышечного введения в дозе 0,5 мг/кг. Кетопрофен демонстрировал низкий системный клиренс (1,49±0,50 мл/мин/кг), низкое значение объема распределения (0,199±0,027 л/кг), конечный период полувыведения 2,29±0,87 часа и высокую биодоступность (121±9%) после внутримышечного введения. Основываясь на этих фармакокинетических результатах, в доклинических исследованиях использовали модель лихорадки, включающую интратрахеальное введение вируса свиного гриппа (SIV), для оценки жаропонижающего эффективного действия кетопрофена (рацемического) с немедленным высвобождением и для установления фармакокинетических-фармакодинамических (ФК-ФД) закономерностей в отношении ослабления лихорадки у подсвинков после отъема от свиноматки. В результате интратрахеального введения SIV (4 мл 7,0±0,5 log10 средней цитопатогенной дозы (инфицирующей 50% клеток) (TCID50)/4 мл) лихорадка у свиней постепенно усиливалась, достигая пика примерно через 24 часа после введения, и ослабевала примерно через 40 часов после введения. Пять групп молодых подсвинков (N=10 в каждой группе) в возрасте приблизительно 28 суток получали SIV путем интратрахеального введения, затем следовало внутримышечное (в.м.) введение кетопрофена в различных дозах (0; 0,03; 0,1; 0,3 и 1 мг/кг). Кетопрофен (рацемический) вводили через 23 часа после введения SIV. Показания ректальной температуры снимали непосредственно перед введением SIV (t=0 часов), за 1 час до (t=22 часа) и через 1 час после (t=24 часа) введения кетопрофена, а также в моменты времени t=6, 27, 29, 32 и 35 часов. Рацемический кетопрофен дозозависимым образом ослаблял лихорадку в модели SIV-индуцированной лихорадки, при этом даже для самой низкой тестируемой дозы (0,03 мг/кг, в.м.) было продемонстрировано статистически значимое отличие от разбавителя. Сильную жаропонижающую активность связывали с концентрациями в плазме крови уже при 500 нМ. Эти данные указывают на то, что рацемический кетопрофен представляет собой сильнодействующий жаропонижающий агент для свиней.
Модель LPS-индуцированного синовита у свиней использовали для оценки аналгезирующей эффективности кетопрофена с немедленным высвобождением и установления ФК-ФД закономерностей в отношении ослабления боли (которые могут отличаться от таковых, связанных с ослаблением лихорадки) у подсвинков после отъема от свиноматки. Подвергнутые анестезии животные получали по 2 мл LPS инъекцией в коленный сустав. По истечении времени, достаточного для выхода из наркоза, животных оценивали в отношении хромоты, перенося их из мест содержания на открытую площадку и позволяя им двигаться самостоятельно. Для оценки клинической хромоты наблюдатель присваивал балл по визуальной аналоговой шкале (VAS). Возможные баллы для оценки хромоты изменяются в диапазоне от 0 см (что соответствует отсутствию отклонения от движения в норме) до 10 см (что соответствует самому худшему из возможных вариантов хромоты). Наблюдения повторяли в течение вплоть до 5 часов после индуцирования синовита, после чего хромота идет на убыль, и к животным возвращается способность нормально передвигаться. В валидационных исследованиях, как флуниксина меглумин (2,2 мг/кг, в.м.), представляющий собой продукт, часто используемый не по прямому назначению для лечения боли у свиней, так и мелоксикам (0,2 мг/кг, в.м.), представляющий собой соединение, одобренное к применению в Европе в качестве аналгезирующего средства для свиней, были эффективны для уменьшения степени LPS-индуцированной хромоты.
Оценивали способность кетопрофена с немедленным высвобождением ослаблять степень LPS-индуцированной хромоты. На этой модели проводили два отдельных исследования для определения и корректирования зависимости доза-ответ для кетопрофена. Кроме того, отбирали образцы крови для определения корреляции концентраций кетопрофена в плазме крови с эффективностью (т.е. оценку ФК-ФД). Методология этих двух исследований была одинаковой. В каждом исследовании использовали 36 свиней (М=9/обрабатываемая группа); синовит индуцировали в момент времени t=-1 час, а кетопрофен вводили в момент времени t=0 ч. Свиней исследовали в моменты времени t=1, 2, 3 и 4 часа и определяли балл для оценки клинической хромоты в соответствии с VAS. В первом исследовании проводили сравнение кетопрофена в широком диапазоне уровней доз (0,01; 0,1; 1,0 мг/кг, в.м.) с разбавителем. Кетопрофен в дозах 0,1 и 1,0 мг/кг вызывал статистически значимые уменьшения степени хромоты по сравнению с разбавителем в течение вплоть до 3 часов после введения. По концентрациям в плазме крови было определено, что в результате введения этих доз общие концентрации в плазме крови составляли приблизительно IC90 in vitro для обоих ферментов СОХ. Через некоторый промежуток времени проводили второе исследование для корректировки кривой зависимости доза-ответ, проводя изучение кетопрофена с уровнями доз 0,01; 0,03 и 0,1 мг/кг, в.м., по сравнению с разбавителем. В этом исследовании вновь продемонстрировано, что кетопрофен в дозе 0,1 мг/кг вызывал максимальные уменьшения степени хромоты в течение 3 часов после введения. Такой уровень доз соответствовал концентрациям кетопрофена в плазме крови от 0,5 до 0,7 мкМ. Помимо этого было определено, что биодоступность кетопрофена составляла 100% после в.м. инъекции.
Описанные выше результаты in vitro и in vivo демонстрируют, что кетопрофен 1) представляет собой сильнодействующий ингибитор свиных изоферментов СОХ, 2) имеет благоприятные фармакокинетические свойства для свиней и 3) является высокоэффективным средством против и лихорадки, и боли у свиней при общей концентрации в плазме крови уже при 500 нМ. Кетопрофен считается гидрофильным агентом, который, как правило, непригоден для композиций на основе триглицеридов. Поэтому рассматривалась композиция на основе триглицеридов со сложноэфирной пролекарственной формой кетопрофена, которая имеет более низкую растворимость в воде.
Пролекарственные формы кетопрофена, соединения формулы 1, формулы 2 и формулы 3, оценивали при гидролизе в плазме крови и микросомах печени свиней. Тестируемые соединения всех формул (1-3) быстро гидролизовались в микросомах печени свиней и умеренно или медленно в плазме крови свиней. Процессы гидролиза этих сложных эфиров кетопрофена оценивали in vivo после однократного внутривенного и внутримышечного введения свиньям в дозе 0,5 мг/кг. Свиньям вводили кетопрофен или его сложные эфиры (соединения формул 1-3) в дозе 0,5 мг/кг либо путем внутривенной (в.в.), либо путем внутримышечной инъекции. Образцы плазмы крови оценивали в отношении содержания кетопрофена, и значения площади под кривой (AUC), нормированные к дозе в мкмоль/кг (нмоль*ч/мл/мкмоль/кг) (n=3 или 4), представлены в Таблице 3.
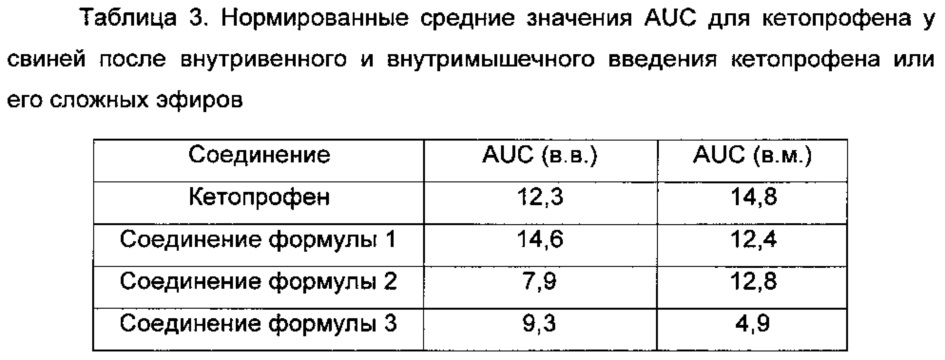
Как можно видеть из Таблицы 3, воздействие кетопрофена после введения его метилового эфира (соединения формулы 1) эквивалентно воздействию после введения самого кетопрофена.
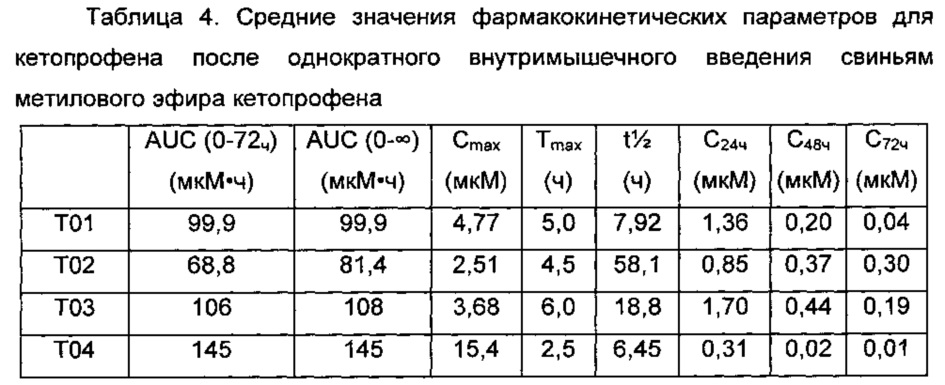
На основании нормированных результатов воздействия для оценки фармакокинетики кетопрофена были разработаны четыре композиции длительного действия, содержащие соединение формулы 1. Эти композиции содержали сорастворители, которые будут медленно распространяться из места инъекции и/или внутримышечного пространства в течение от примерно 1 суток до примерно 1 недели, и использовали следующие композиции: Т01 (глицеролформаль : триацетин (25:75 об./об.)); Т02 (миглиол 812); Т03 (хлопковое масло : триацетин (90:10 об./об.)); и Т04 (самоэмульгирующая микросистема доставки лекарственных средств), что теоретически обеспечивает по меньшей мере два преимущества: 1) придает кинетике относительно гидрофобного соединения характер, подобный характеру кинетики раствора и/или 2) пролонгирует продолжительность времени, в течение которого активный агент остается в растворе, а также сводит к минимуму осаждение в месте инъекции благодаря присутствию значительных уровней эмульгирующих агентов вместе с триглицеридом. Подсвинки (n=4), самки свиней, которые еще не были беременными, массой примерно 15 кг каждая, получали разовую внутримышечную инъекцию в дозе 3 мг/кг (30 мг/мл). Как можно видеть из Таблицы 4, содержащая миглиол 812 композиция давала самое низкое значение Cmax и самую высокую концентрацию кетопрофена в плазме крови в момент времени 72 часа (С72ч). Величина С24ч, С48ч и С72ч представляет собой концентрацию кетопрофена в плазме крови на момент времени 24, 48 и 72 часа после введения дозы, соответственно.
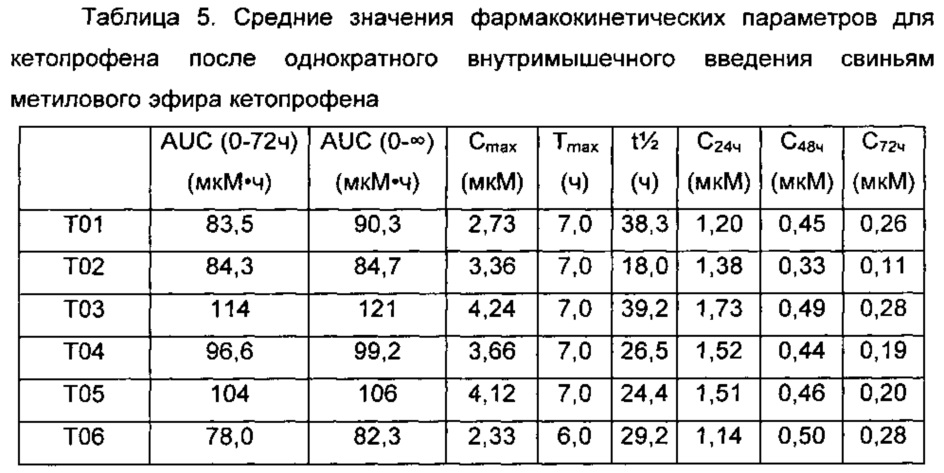
Второе исследование композиций проводили для оценки композиций на основе соединения формулы 1 (30 мг/мл или 60 мг/мл) вместе с дополнительными компонентами. Например, для увеличения вязкости к содержащей миглиол 812 композиции добавляли моностеарат алюминия, уменьшая тем самым область истечения лекарственного средства из внутримышечного пространства. Аналогичным образом к миглиолу 812 добавляли поверхностно-активное вещество (спан 80; 0,5% или 1%) для уменьшения времени задержки начала истощения триглицерида, и касторовое масло, благодаря которому можно обеспечить получение разных коэффициентов распределения между триглицеридом и сложным эфиром. Использовали следующие композиции: Т01 (миглиол 812, 30 мг/мл), Т02 (миглиол 812 с моностеаратом алюминия, 30 мг/мл), Т03 (миглиол 812, 60 мг/мл), Т04 (миглиол 812 с 0,5% спана 80, 30 мг/мл), Т05 (миглиол 812 с 1% спана 80, 30 мг/мл) и Т06 (касторовое масло, 30 мг/мл). Как можно видеть из Таблицы 5, увеличение дозы метилового эфира кетопрофена не оказывало никакого влияния на фармакокинетический профиль кетопрофена. Добавление модификатора вязкости и/или поверхностно-активных веществ не оказывало заметного влияния на Cmax или продолжительность действия для кетопрофена. Кроме того, действие касторового масла оказывалось аналогичным действию миглиола 812.
В дополнительных фармакокинетических исследованиях на свиньях анализировали соединение формулы 1 в составе разных инъекционных композиций длительного действия. Используемые композиции включают: композицию 1: миглиол 812; композицию 3: миглиол 812 : тетрагликоль (67:33, об./об.); композицию 4: миглиол 812 : триацетин (75:25, об./об.); композицию 5: миглиол 812 : тетрагликоль : коллифор HS15 (67:28:5, об./об./об.). Эти композиции не включали возможный консервант. В Таблице 6 показаны средние значения фармакокинетических параметров после однократной внутримышечной инъекции в дозе 1 мг/кг для каждой из композиций, содержащих соединение формулы 1 (80 мг/мл), свиноматкам (n=4) массой от 184 до 233 кг каждая.
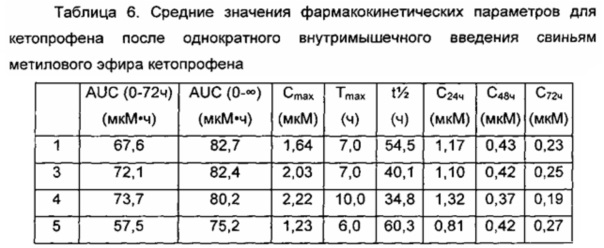
В дополнительных фармакокинетических исследованиях на свиньях анализировали соединения формулы 1 в составе разных инъекционных композиций длительного действия. Используемые композиции включают: композицию 6: миглиол 840; композицию 7: миглиол 840 : тетрагликоль (67:33); композицию 8: миглиол 840 : триацетин (75:25); и композицию 10: миглиол 840 : тетрагликоль : коллифор HS15 (67:28:5). Эти композиции не включали возможный консервант. В Таблице 7 показаны средние значения фармакокинетических параметров после однократной внутримышечной инъекции в дозе 1 мг/кг для каждой из композиций, содержащих соединение формулы 1 (80 мг/мл), свиноматкам (n=4) массой от 184 до 233 кг.
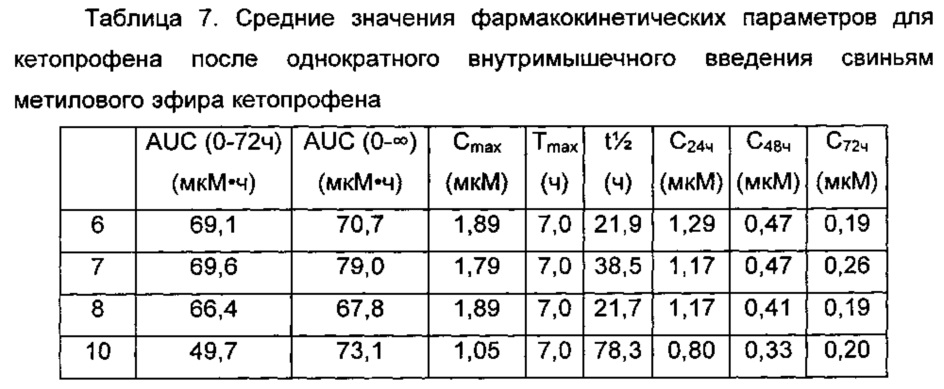
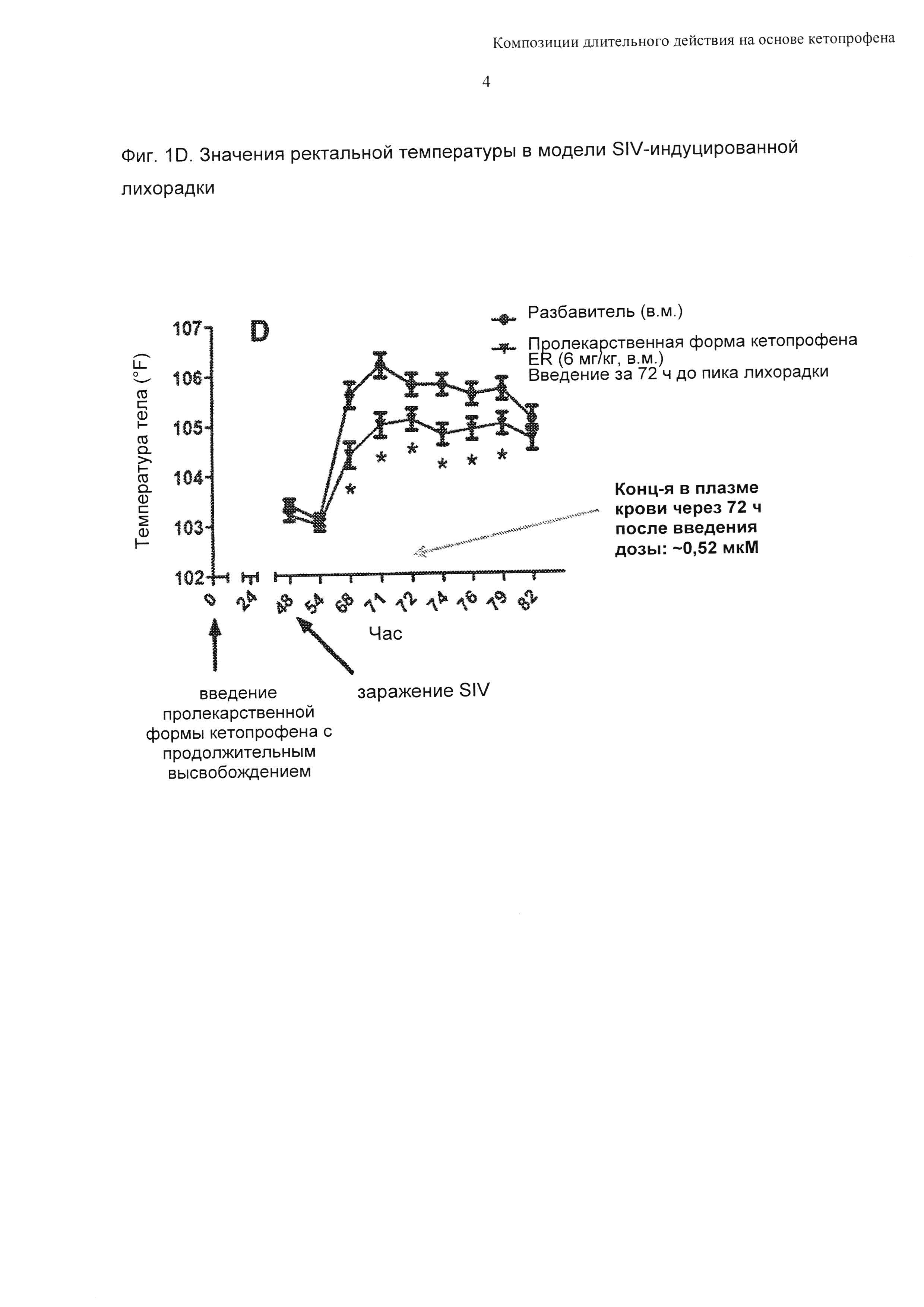
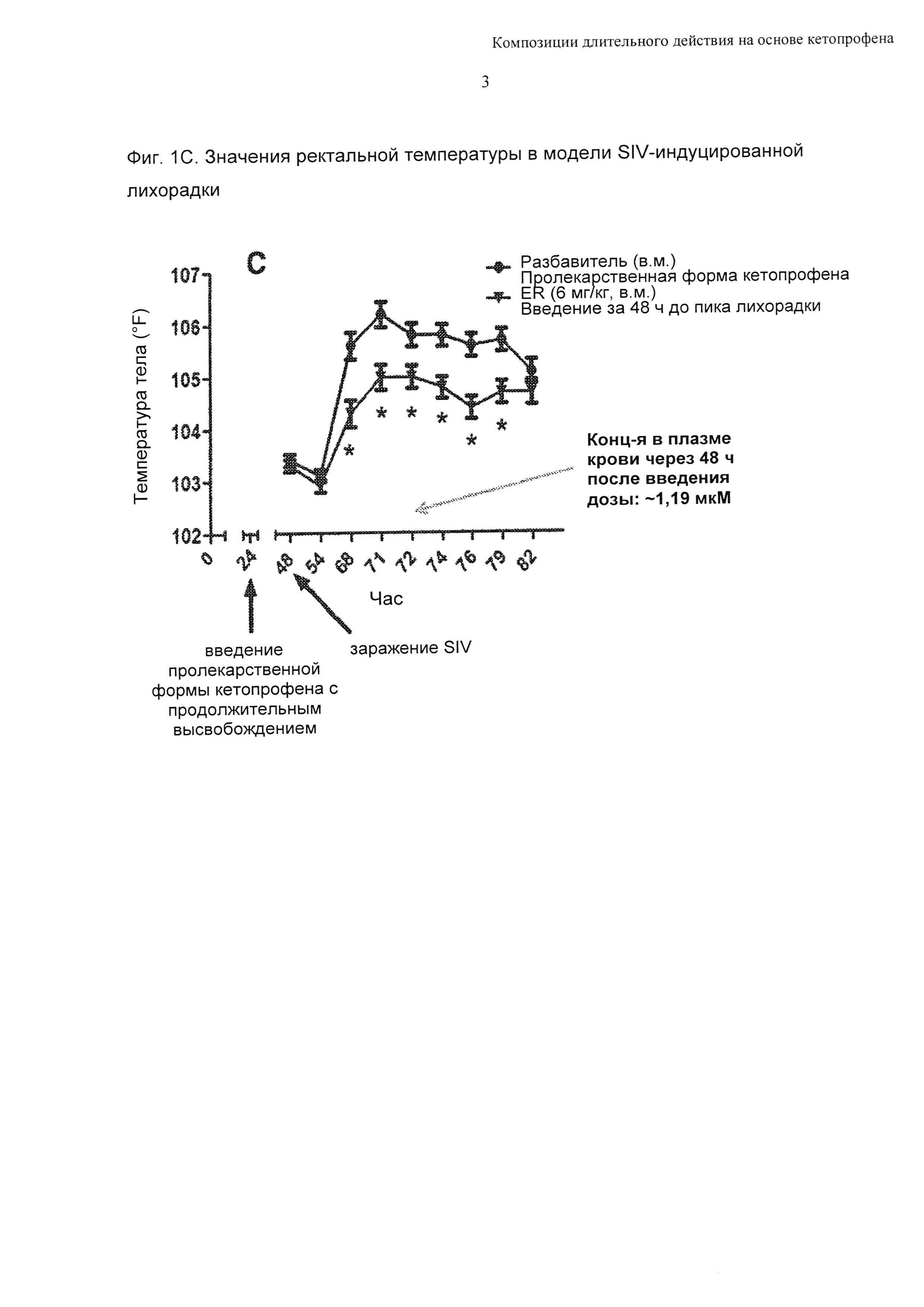
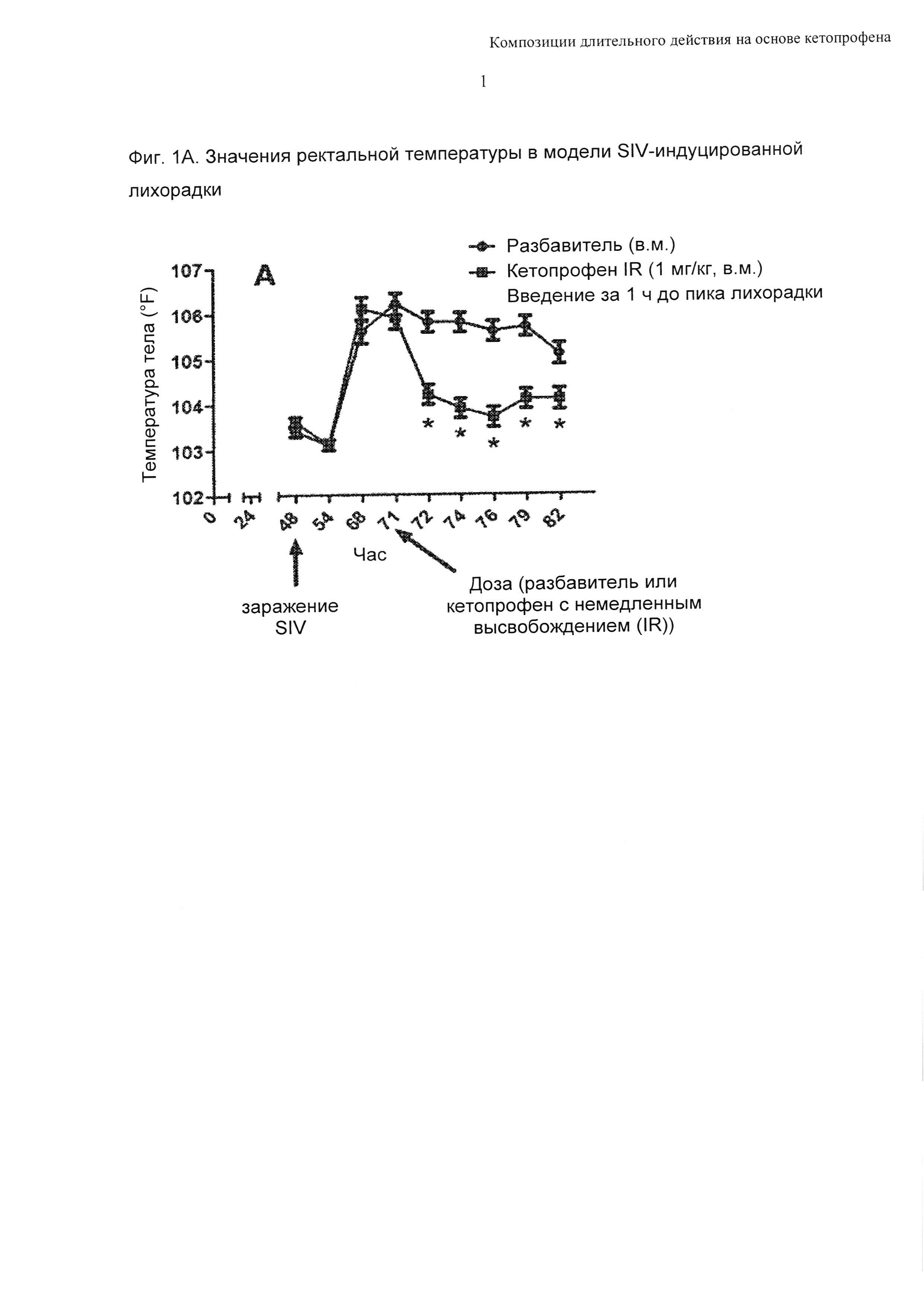
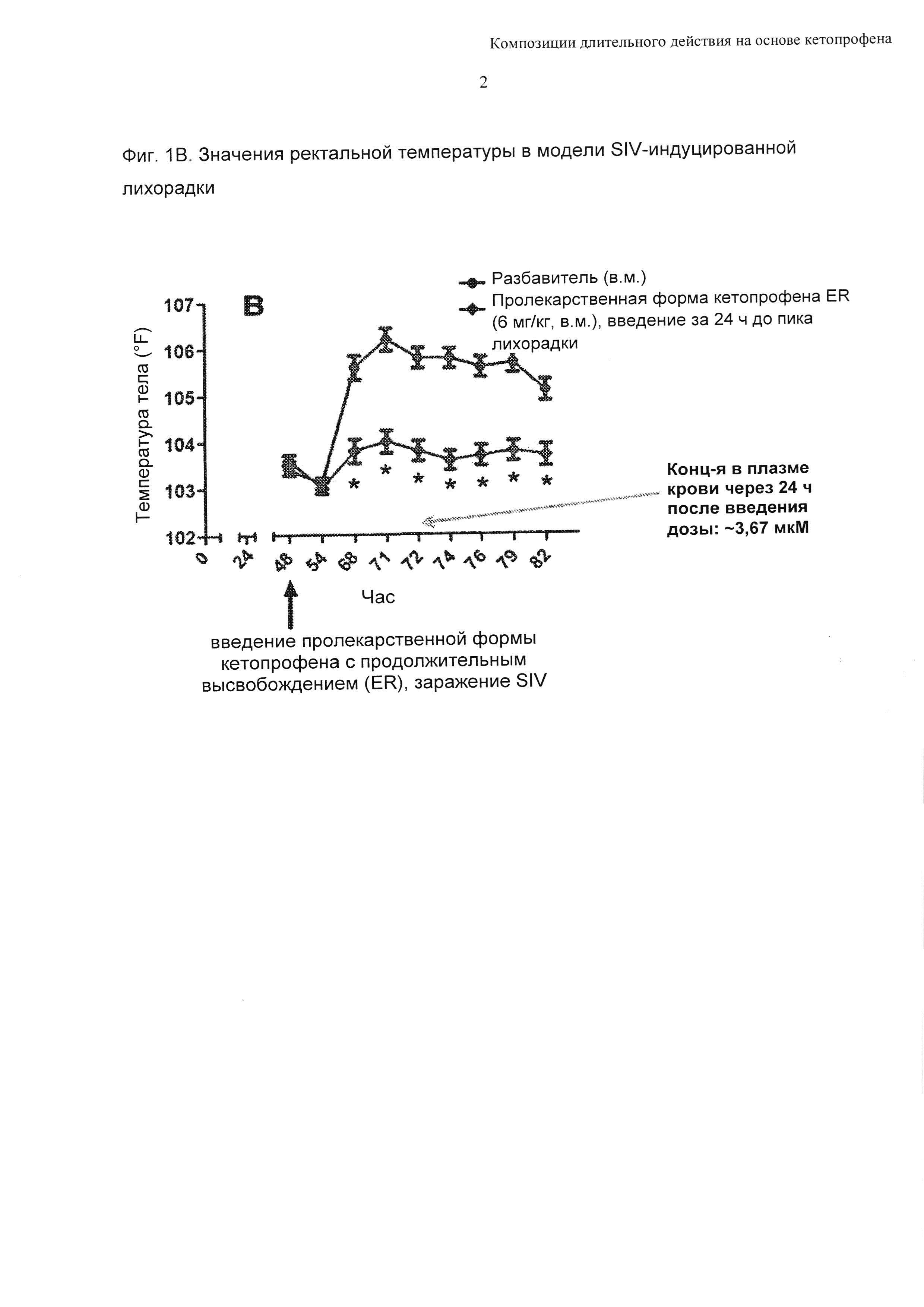
В попытке оценить величину и продолжительность эффективного действия соединения формулы 1 в миглиоле 812 (30 мг/мл) против лихорадки у свиней (в частности подсвинков) животным давали дозу 6 мг/кг путем внутримышечной инъекции, за исключением специально описанных случаев. На основании ФК-ФД исследований, проведенных ранее для кетопрофена с немедленным высвобождением в модели SIV-индуцированной лихорадки у свиней, было предсказано, что доза 6 мг/кг обеспечивает общую концентрацию кетопрофена в плазме крови не меньше 500 нМ в течение 72 часов. Четыре обрабатываемых группы сравнивали с группой, получавшей разбавитель, и они включали: Т01 (кетопрофен с немедленным высвобождением (1 мг/кг, в.м., введенный за 1 час до пика лихорадки), Т02 (соединение формулы 1, введенное за 24 часа до заражения SIV (т.е. в пик лихорадки), Т03 (соединение формулы 1, введенное за 48 часов до заражения SIV) и Т04 (соединение формулы 1, введенное за 72 часа до заражения SIV). Во всех случаях ректальные температуры измеряли на моменты времени 6, 20, 23, 24, 26, 28, 31 и 34 часа после заражения SIV. Данные представлены на Фиг. 1. Данные представлены графически в виде полученных методом наименьших квадратов средних значений ± SEM с величинами ошибки, представляющими собой стандартную ошибку среднего (SEM). Показаны значения средней концентрации кетопрофена в плазме крови, определенной через 24 часа, 48 часов и 72 часа после введения доз (сателлитная ФК группа): Фиг. 1А: кетопрофен (с немедленным высвобождением), введенный через 23 часа после заражения SIV; Фиг. 1В: метиловый эфир кетопрофена в миглиоле 812 (6 мг/кг, в.м.), введенный одновременно с заражением SIV (т.е. за 24 часа до пика лихорадки); Фиг. 1С: метиловый эфир кетопрофена в миглиоле 812 (6 мг/кг, в.м.), введенный за 24 часа до заражения SIV (т.е. за 48 часов до пика лихорадки); Фиг. 1D: метиловый эфир кетопрофена в миглиоле 812 (6 мг/кг, в.м.), введенный за 48 часов до заражения SIV (т.е. за 72 часа до пика лихорадки). На Фиг. 1 знаком «*» отмечены точки статистической значимости (Р<0,05) по сравнению с разбавителем. N=10/группа.
Как можно видеть из Фиг. 1В, 1С и 1D, введение соединения формулы 1 в миглиоле 812 приводило к статистически значимым снижениям ректальной температуры на моменты времени 10-79 часов после введения доз. В испытании с участием сателлитной ФК группы, проводимом параллельно с исследованием эффективности, продемонстрировано, что средние значения концентрации в плазме крови, обусловленные введением композиций, составляли 3,67; 1,19 и 0,52 мкМ на моменты времени 24 часа, 48 часов и 72 часа после введения доз, соответственно; это согласовывалось с предположением, что дозы 6 мг/кг будет достаточно для поддержания концентраций в плазме крови не менее 500 нМ в течение 72 часов.
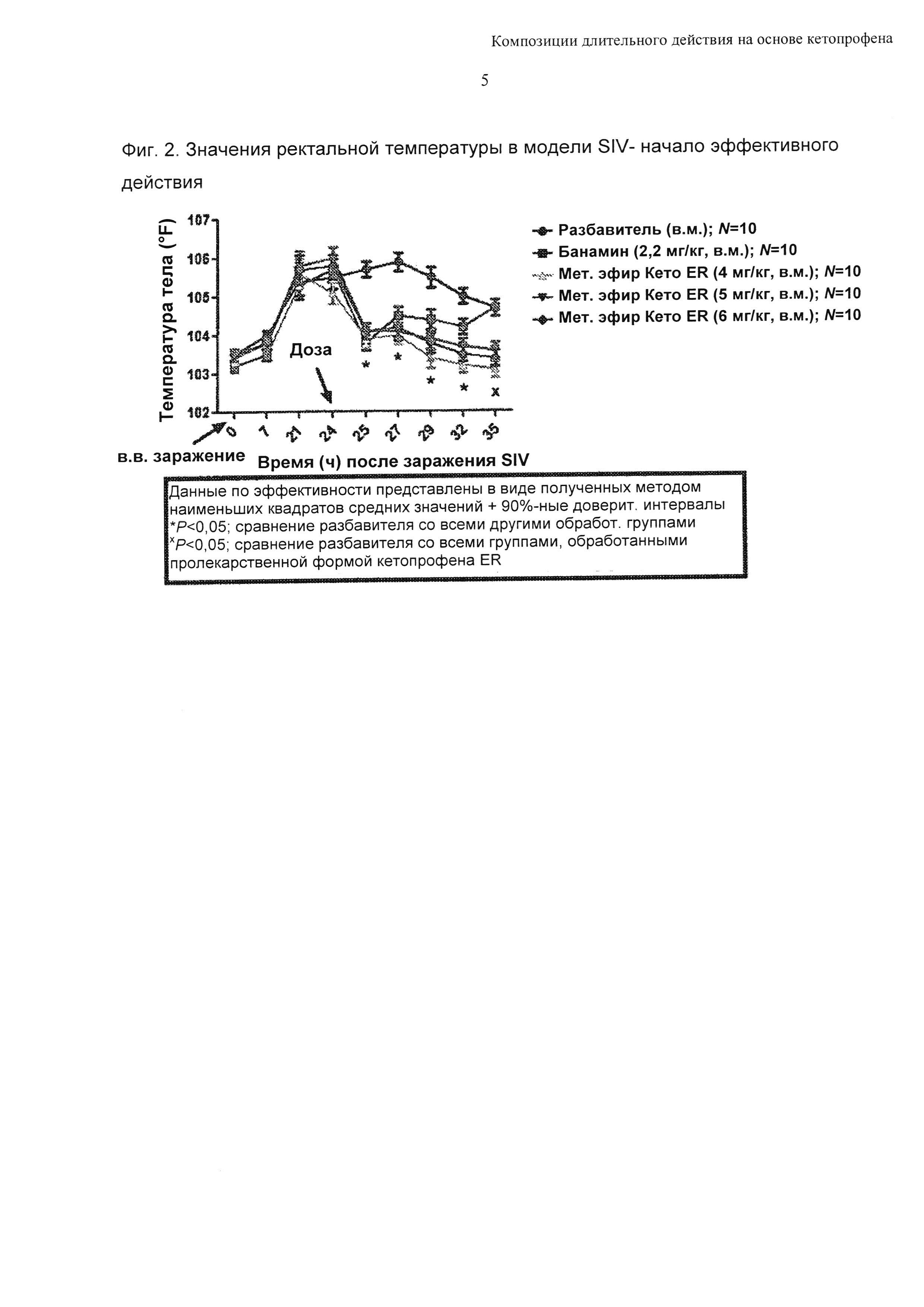
Чтобы определить начало жаропонижающего действия, соединение формулы 1 в миглиоле 812 оценивали в первые часы после введения дозы в модели SIV-индуцированной лихорадки. Пять групп молодых подсвинков (N=10 в каждой группе) получали SIV путем интратрахеального введения с последующим внутримышечным введением соединения формулы 1 в различных дозах (0, 4, 5, 6 мг/кг) или банамина (2,2 мг/кг, в.м.) в качестве положительного контроля. Всем получающим дозу группам вводили тестируемый агент через 24 часа после введения SIV. Показания ректальной температуры снимали непосредственно перед введением SIV (t=0 часов), за 3 часа до (t=21 час) и через 1 час после (t=25 часов) введения дозы, а также в моменты времени t=7, 27, 29, 32 и 35 часов (эффекты метилового эфира кетопрофена в миглиоле 812 (4, 5, 6 мг/кг; в.м.), по сравнению с разбавителем в первые часы после введения дозы). Результаты показаны на Фиг. 2. Данные представлены графически в виде полученных методом наименьших квадратов средних значений ± SEM с величинами ошибки, также представляющими собой SEM. Зависимость концентраций в плазме крови, обусловленных разными уровнями доз, от времени оценивали в моменты времени 0,5, 1 и 3 часа после введения дозы (сателлитная ФК группа).
Как можно видеть на Фиг. 2, для всех доз соединения формулы 1 наблюдали существенное ослабление лихорадки по сравнению с разбавителем, начинающееся через 1 час после введения дозы и продолжающееся для всех исследуемых моментов времени. Важно, что по сравнению с разбавителем все получающие дозу группы оставались активными на момент времени t=35 часов (т.е. через 11 часов после введения дозы), в то время как для банамина такого не наблюдали. В соответствии с ФК профилем, относящимся к композиции, содержащей миглиол 812, для сателлитной ФК группы было продемонстрировано, что уровни воздействия для всех доз значительно превышали значения IC90 in vitro для СОХ-1 и СОХ-2 на моменты времени 0,5, 1 и 3 часа после введения доз. В заключение, жаропонижающие эффекты композиции, содержащей миглиол 812, у молодых подсвинков можно обобщить так, как приведено ниже: соединение формулы 1, введенное в дозе 1) 4, 5 и 6 мг/кг, в.м., демонстрирует эффективность жаропонижающего действия, начиная с момента времени 1 час после введения доз; 2) 6 мг/кг, в.м., продолжает демонстрировать жаропонижающее действие в течение 72 часов после введения доз, однако введение более низких доз демонстрирует соответствующее уменьшение продолжительности жаропонижающего эффективного действия. На Фиг. 2 знаком «*» отмечены точки статистической значимости (Р<0,05) по сравнению с разбавителем. N=10/группа.
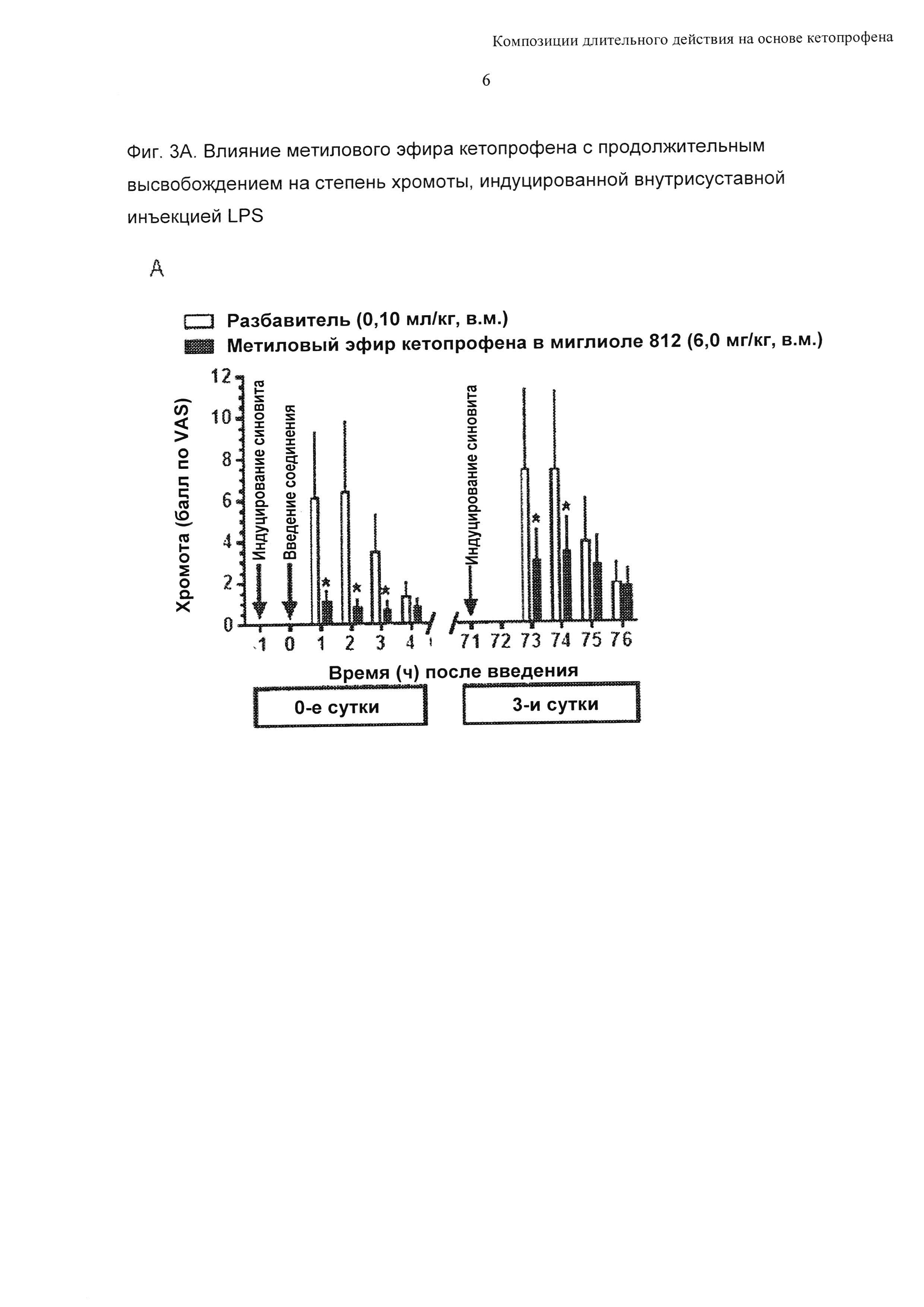
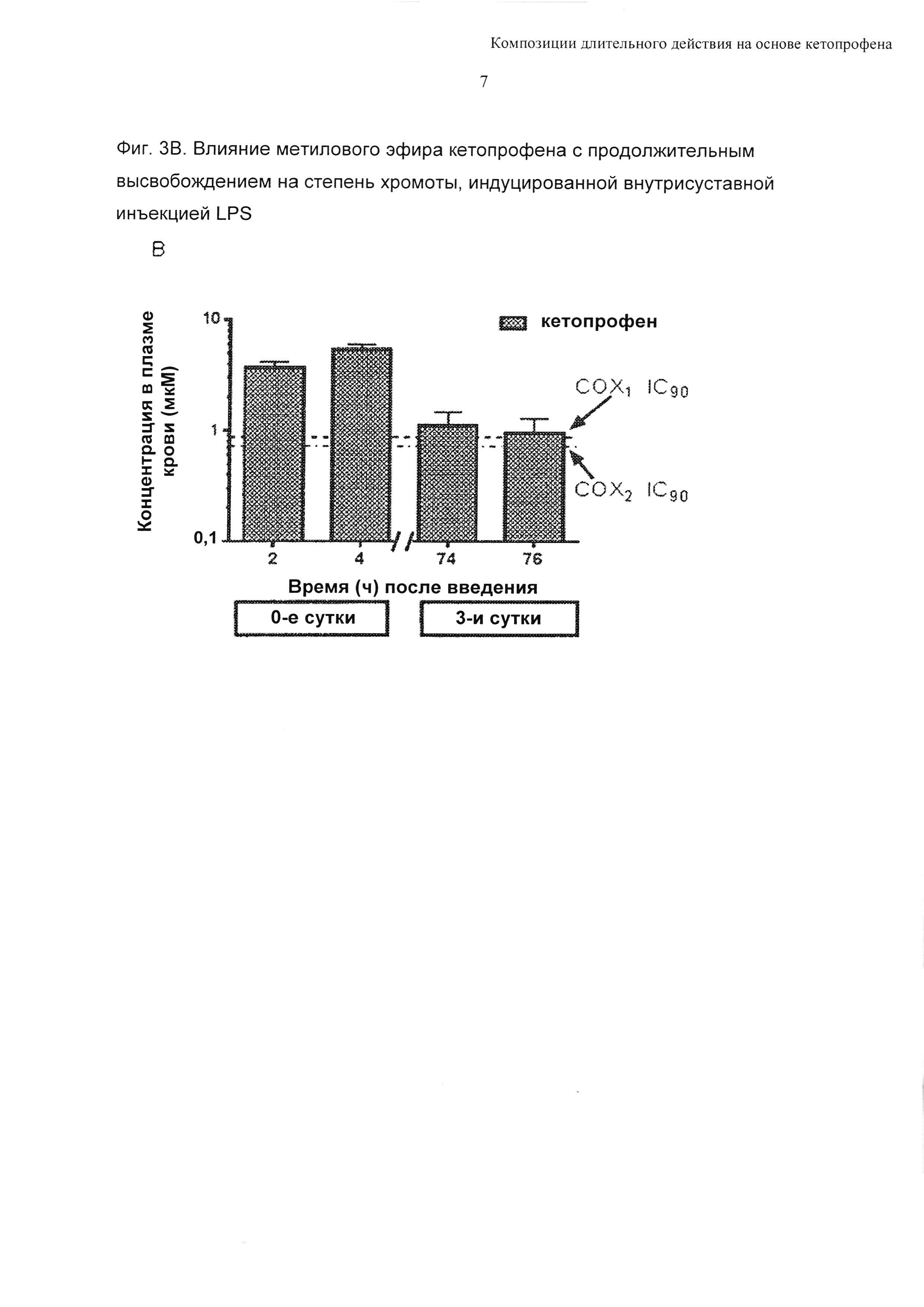
Начало и продолжительность действия метилового эфира кетопрофена в миглиоле 812 (6,0 мг/кг, в.м.) тестировали на модели синовита у свиней. Для этого конкретного исследования у каждого подсвинка дважды индуцировали синовит: один раз в 0-е сутки и еще раз на 3-й сутки. В 0-е сутки, t=-1 час, синовит индуцировали посредством инъекции LPS в правый коленный сустав, затем в момент времени t=0 часов вводили либо композицию соединения формулы 1 и миглиола 812 (N=9), либо разбавитель (N=9). Обследование степени хромоты проводили через 1-4 часа после введения доз. На 3-й сутки у каждого подсвинка индуцировали синовит еще раз посредством инъекции LPS в левый коленный сустав (т.е. в момент времени t=71 час). Обследование степени хромоты на 3-й сутки соответствовало 73-76 часам после введения доз. Результаты показаны на Фиг. 3. Данные выражены в виде полученных методом наименьших квадратов средних значений с 90%-ными доверительными интервалами (N=9/группа). *Р<0,05 по сравнению с разбавителем. Величины ошибки на диаграмме «А» Фиг. 3 иллюстрируют 95%-ные доверительные интервалы, а величины ошибки на диаграмме «В» Фиг. 3 представляют собой SEM. В результате применения метилового эфира кетопрофена в миглиоле 812 (6 мг/кг, в.м.) получили значительное уменьшение степени хромоты в течение 1 часа с момента введения в 0-е сутки. На 3-й сутки хромота все еще была значительно меньше по сравнению с плацебо к 74 часам после введения доз (Фиг. 3А). Кроме того, полученные уровни в плазме крови являлись подтверждением того, что значения IC90 in vitro были превышены для обоих СОХ ферментов на протяжении этого исследования (Фиг. 3В).
Фармакокинетику кетопрофена в плазме крови после внутримышечного введения метилового эфира кетопрофена также оценивали на здоровых быках. Использовали следующие композиции: композицию 1: метиловый эфир кетопрофена в миглиоле 812 без консерванта в концентрации 120 мг/мл; композицию 2: метиловый эфир кетопрофена в смеси миглиол 812 : транскутол (50:50, об./об.) в концентрации 160 мг/мл; и композицию 4: метиловый эфир кетопрофена в смеси миглиол 812 : триацетин (80:20, об./об.) в концентрации 160 мг/мл. В случае композиций 1 и 2 использовали трех телят (220-300 кг), при этом каждый из них получал внутримышечную дозу 6 мг/кг, а в случае композиции 4 использовали двух телят (180-240 кг), при этом каждый из них получал внутримышечную дозу 6 мг/кг. После однократной внутримышечной инъекции метилового эфира кетопрофена средняя концентрация кетопрофена в плазме крови оставалась выше, чем IC90 in vitro для кетопрофена, для ингибирования бычьего фермента СОХ-1 в течение 120 часов, и оставалась выше, чем IC90 in vitro для кетопрофена, для ингибирования бычьего фермента СОХ-2 в течение почти 72 часов. Результаты показаны в Таблице 8.
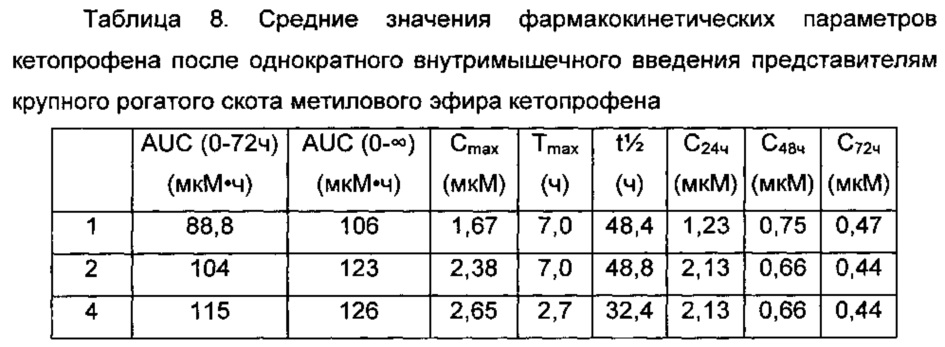
Приведенные в Таблице 8 данные указывают на то, что в случае однократного введения метилового эфира кетопрофена в миглиоле 812 путем внутримышечной инъекции представителям крупного рогатого скота, такая композиция приобретает свойства препарата с продолжительным высвобождением, аналогичные наблюдаемым у свиней, что приводит к пролонгированному нахождению кетопрофена в плазме крови с уровнями, достаточными для ингибирования бычьих ферментов СОХ в течение 3-5 суток.
В качестве сравнения, средние значения фармакокинетических параметров для кетопрофена в случае инъекционной композиции на основе кетопрофена с непролонгированным действием (3 мг/кг; Neoprofen®, 100 мг/мл), введенной представителям крупного рогатого скота (телятам, в возрасте от 6 до 12 месяцев) со средней массой тела примерно 91 кг, представлены в Таблице 9. Singh, R., et al., Wayamba Journal of Animal Science, 6, 2014, pp. 820-823.
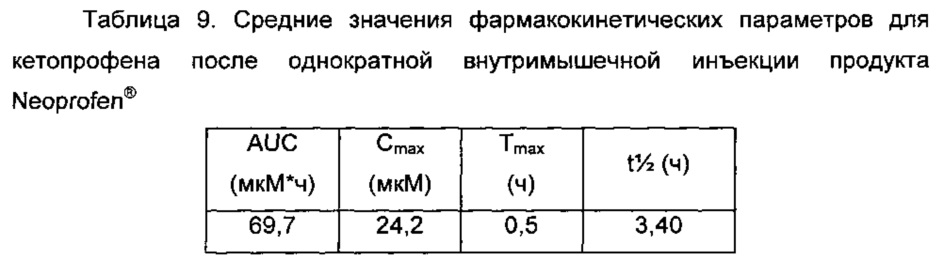
Как можно видеть из Таблиц 8 и 9, значения 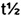 для кетопрофена после введения представителям крупного рогатого скота пролекарственной формы в виде метилового эфира (соединения формулы 1) оказываются приблизительно в 14 раз (композиции 1 и 2) больше и приблизительно в 9,5 раз больше (композиция 4) по сравнению с коммерческим инъекционным продуктом Neoprofen®. Соответственно, большее значение
для кетопрофена после введения представителям крупного рогатого скота пролекарственной формы в виде метилового эфира (соединения формулы 1) оказываются приблизительно в 14 раз (композиции 1 и 2) больше и приблизительно в 9,5 раз больше (композиция 4) по сравнению с коммерческим инъекционным продуктом Neoprofen®. Соответственно, большее значение 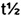 будет коррелировать с более высокими терапевтическими концентрациями в плазме крови и, следовательно, с большей продолжительностью эффективного действия после введения однократной инъекционной дозы.
будет коррелировать с более высокими терапевтическими концентрациями в плазме крови и, следовательно, с большей продолжительностью эффективного действия после введения однократной инъекционной дозы.