Результат интеллектуальной деятельности: 1,3-Бис(4-метоксибензоил)пиримидин-2,4(1Н,3Н)-дион, обладающий разрывающей поперечные сшивки гликированных белков активностью
Вид РИД
Изобретение
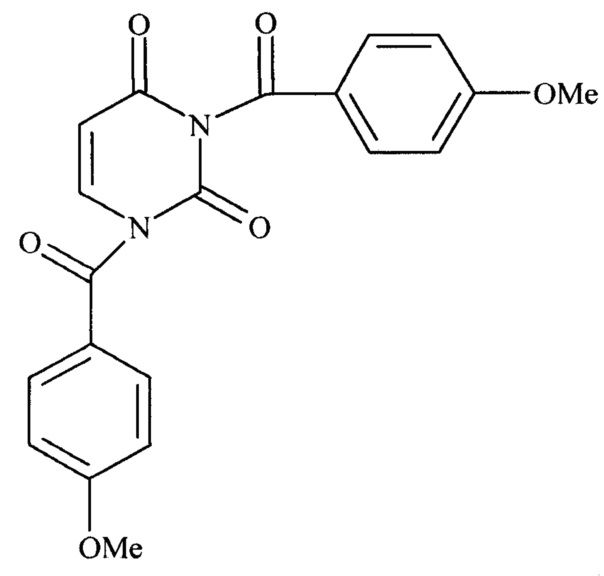
Изобретение относится к области органической химии и медицины и касается нового биологически активного химического соединения, конкретно 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-диона формулы
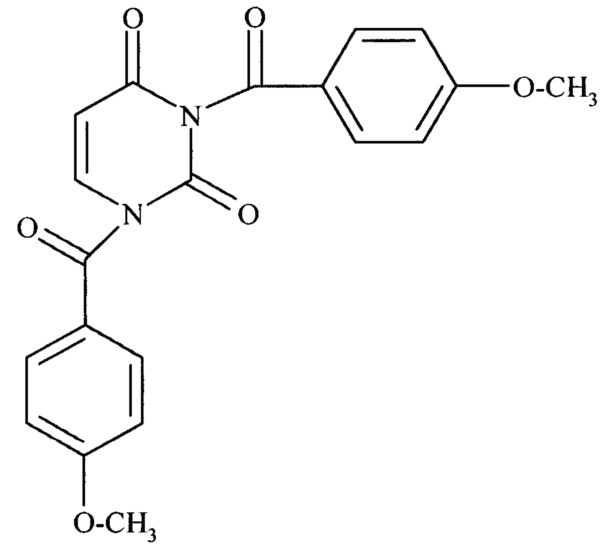 ,
,
обладающий разрывающей поперечные сшивки гликированных белков активностью. Указанное соединение и его свойства в литературе не описаны.
Долгоживущие структурные белки подвергаются постоянному неферментативному сшиванию с глюкозой в процессе старения у больных сахарным диабетом. Неферментативное гликирование усиливается при диабете благодаря гипергликемии и приводит к различным осложнениям данной болезни [Ансари Н.А., Рашид З. Неферментативное гликирование белков: от диабета до рака // Биомедицинская химия. - 2010. - Т. 56. - №.2. - С. 168-178].
Неферментативное гликирование является классической ковалентной реакцией, в которой посредством N-гликозидного связывания образуется сахар-протеиновый комплекс через серию химических реакций, описанных Майяром. Неферментативное гликирование белков, пептидов и других макромолекул связывают с рядом патологий, наиболее часто с диабетом [Ahmed N. Advanced glycation endproducts - role in pathology of diabetic complications // Diabetes research and clinical practice. - 2005. - T. 67. - №.1. - C. 3-21], нормальным старением и нейродегенеративной амилоидной болезнью, такой как болезнь Альцгеймера. Многочисленные исследования доказывают определенную связь между гипергликемией и патогенезом диабетических осложнений, таких как ретинопатией, нефропатией, нейропатией и васкулопатией [Щеглова Т., Маккер С.П., Трамонтано А. Ковалентно-связывающиеся антитела подавляют глубокое гликирование: врожденный компонент системы приобретенного иммунитета // Acta Naturae (русскоязычная версия). - 2009. - Т. 1. - №.2].
Способность разрывателей поперечных сшивок разрушать конечные продукты гликирования является возможным терапевтическим подходом к восстановлению эластичности коллагенового каркаса сердечно-сосудистой системы, а также к лечению других осложнений сахарного диабета. В 1996 году впервые были опубликованы данные о N-фенацилтиазол бромиде (ФТБ) [Vasan S. et al. An agent cleaving glucose-derived protein crosslinks in vitro and in vivo. - 1996.]. Купер и др. [Thornalley P.J., Minhas H.S. Rapid hydrolysis and slow α,β-dicarbonyl cleavage of an agent proposed to cleave glucose-derived protein cross-links // Biochemical pharmacology. - 1999. - T. 57. - №.3. - C. 303-307] исследовали влияние ФТБ на сосудистую гипертрофию у крыс со стрептозотоцин-индуцированным диабетом. Внутрибрюшинное введение ФТБ привело к снижению количества конечных продуктов гликирования, накопленных в кровеносных сосудах.
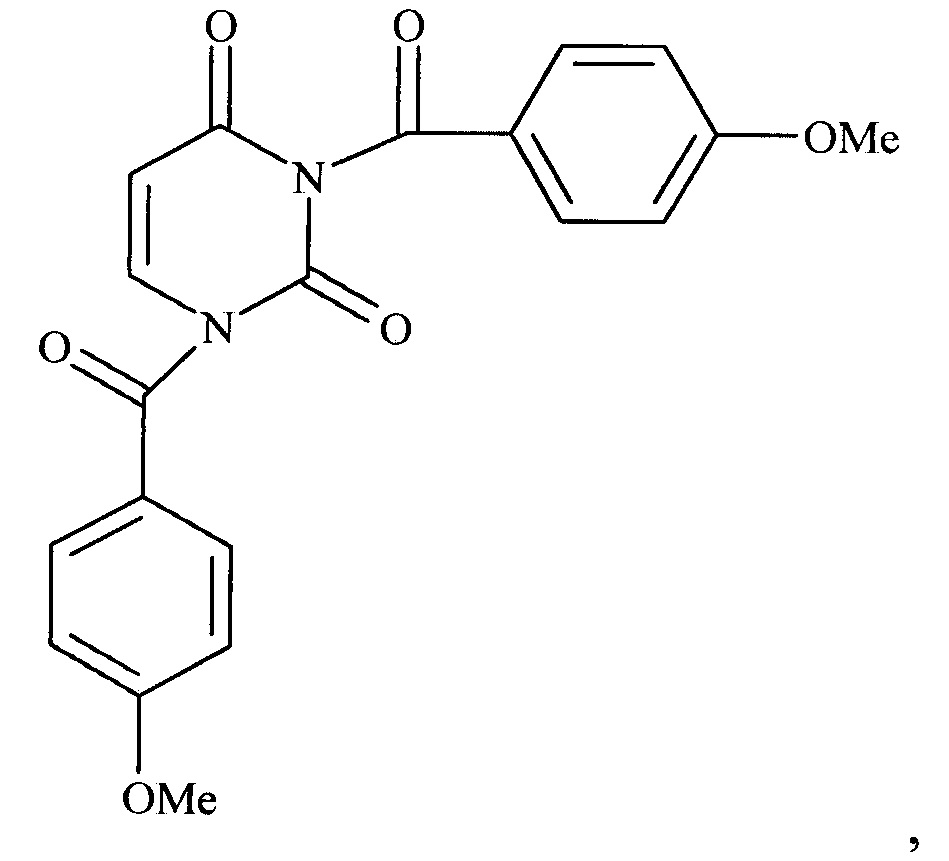
Ввиду нестабильности фенилтиазолбромида в физиологических буферах, был протестирован его аналог - ALT-711 (алагебриум) - который является наиболее близким по свойствам к патентуемому соединению. Исследования, проведенные на лабораторных животных, указывают на то, что ALT-711 приводит к нормализации сердечно-сосудистой системы после осложнений, вызванных старением и диабетом [Vasan S., Foiles P., Founds H. Therapeutic potential of breakers of advanced glycation end product-protein crosslinks // Archives of Biochemistry and Biophysics. - 2003. - T. 419. - №.1. - C. 89-96]. Фаза 2 клинических испытаний ALT-711 была начата в 1998 с участием добровольцев обоих полов и разных возрастных групп. Было показано, что алагебриум хорошо переносится участниками исследования. Кроме того, наблюдалось увеличение эластичности сосудов у 93% пациентов старше 50 лет, а также отмечалось статистически значимое снижение пульса по сравнению с пациентами, принимающими плацебо [Chelation: A Fundamental Mechanism of Action of AGE Inhibitors, AGE Breakers, and Other Inhibitors of Diabetes Complications R. Nagai, D.B. Murray, Т.O. Metz, J.W. Baynes // Diabetes, V. 61, 2012, pp. 549-559].
Задача, на решение которой направлено данное изобретение, заключается в поиске новых соединений, обладающих повышенной разрывающей поперечные сшивки гликированных белков активностью.
Сущность изобретения заключается в синтезе нового химического соединения 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-диона формулы
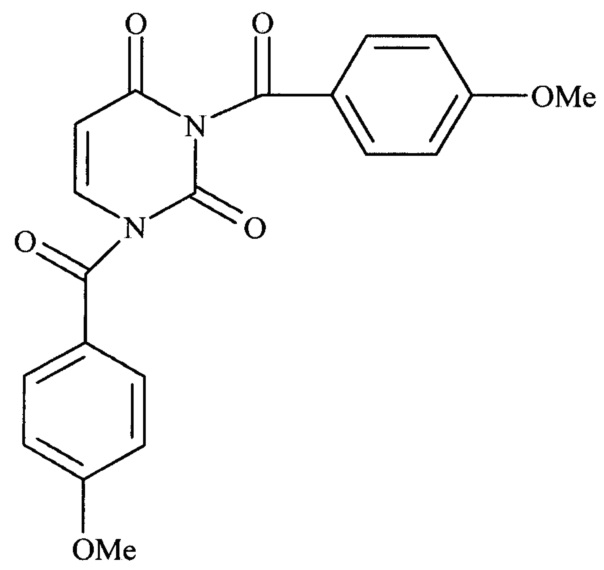 ,
,
обладающий разрывающей поперечные сшивки гликированных белков активностью.
Пример 1. 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-дион.
К раствору урацила (100 ммоль) в сухом пиридине (30 мл) прибавляют медленно по каплям в течение 15 мин раствор 4-метоксибензоилхлорида (200 ммоль) в хлороформе (10 мл), в результате чего происходит осаждение продукта и хлоргидрата пиридина. Смесь перемешивают в течение 1 ч при комнатной температуре. Затем раствор фильтруют, осадок промывают холодной водой и перекристаллизовывают из бензола. Получают 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-дион в виде белого кристаллического вещества. Выход 31,19 г (82%). Т.пл.=319-322°С. Rf 0,36 (изопропанол : вода 7:3). C20H16N2O6: вычислено, %: С63.16, Н4.24, N7.37, найдено, %: С63.19, Н4,25, N7.39. ПМР-спектр (ДМСО-d6, 300 МГц), δ, м.д.: 7.88д (1Н, урацил), 7.73-7.68 м (4Н, Ph), 7.33 д (1Н, урацил), 7.05-7.01 м (4Н, Ph), 3.85 с (6Н, -СН3).
Пример 2. Исследование влияния 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-диона на поперечные сшивки гликированных белков.
Получение коллагена. Нормальные крысы Вистар (масса тела 200±20 г) умерщвлялись, после чего иссекали хвосты и получали коллаген при температуре 4°С следующим образом: вынимали коллагеновые волокна сухожилия хвоста, промывали физиологическим солевым раствором, удаляли ткани неколлагеновых волокон, трижды промывали дистиллированной деионизованной водой, разрезали на куски и погружали в 0,1% уксусную кислоту при 4°С на одну неделю, в течение которой иммерсионную жидкость часто взбалтывали. Иммерсионную жидкость подвергали обработке на центрифуге при 8000 g в течение 30 минут и собирали супернатантный раствор коллагена. После разбавления измеряли содержание протеина. 96-Луночный микропланшет (Costar) тщательно покрывали раствором коллагена в количестве 70 мкг/лунку при 4°С в течение 24 часов, затем пленкообразующий раствор удаляли. Пластины высушивали на воздухе, покрывали пленкой для сохранения свежести и хранили при 4°С до использования.
Получение конечных продуктов гликирования (гликированного бычьего сывороточного альбумина). Раствор, содержащий 50 мг/мл бычьего сывороточного альбумина (БСА) (V) (Roch) и 0,5 М глюкозы в 0,2 М забуференном фосфатом физиологическом растворе (фосфатный буферный раствор pH 7,4), инкубировали при 37°С в стерильных условиях в течение 3-4 месяцев для образования гликозилированного БСА. В то же время готовили негликозилированный БСА со свободным от глюкозы БСА. Затем БСА-AGE раствор диализировали против 0,01 М фосфатный буферный раствор (pH 7,4) для удаления непрореагировавшей глюкозы. Использовали флуоресцентное сканирование (Exi/Em (395/460 нм)).
Исследование активности патентуемого соединения 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-диона. Покрытый коллагеном из хвоста 96-луночный микропланшет тщательно обрабатывали фосфатным буферным раствором (pH 7,4) в течение 1 часа для нейтрализации кислого коллагена. Планшет блокировали Superblock (PIERCE) при 37°С в течение 1 часа и промывали фосфатным буферным раствором с Tween-20, трижды встряхивая в течение 1 минуты при каждом промывании. 100 мкл раствора гликированного белка добавляли в лунки в ряды 96-луночного планшета, маркированные как А, В, С и D, и раствор БСА такой же концентрации добавляли в лунки в ряды, маркированные как Е, F, G и Н. Лунки инкубировали при 37°С в течение 4 часов, чтобы обеспечить сшивание коллагена, и промывали фосфатным буферным раствором с Tween-20 четыре раза при встряхивании в течение 1 минуты при каждом промывании. Патентуемое соединение 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-дион добавляли к выполненным в четырех экземплярах лункам с гликированным белком и к выполненным в четырех экземплярах лункам с БСА в количестве 100 мкл/лунку. В первые три лунки в каждом ряду вместо вещества добавляли 100 мкл/лунку фосфатный буферный раствор или другой растворитель (например, диметилсульфоксид). Лунки инкубировали при 37°С в течение 16 часов и промывали фосфатным буферным раствором с tween-20, встряхивая в течение 1 минуты во время каждого промывания. В лунки добавляли антитела кролика против-БСА (1:500) 80 мкл/лунку и планшет инкубировали при 37°С в течение 50 минут. Далее в лунки добавляли 80 мкл/лунку меченных пероксидазой хрена козьих IgG против кроличьих (1:1000). Лунки инкубировали при 37°С в течение 50 минут. После этого добавляли субстрат 3,3',5,5'-тетраметилбензидин (ТМВ) 100 мкл/лунку. Планшет инкубировали при комнатной температуре в темноте в течение 20 минут. Для прекращения реакции использовали 2 М H2SO4. В течение 10 минут после реакции регистрировали оптическую плотность при 450 нм на планшет-ридере TECAN M200Pro.
Для каждого определения вычисляли среднюю оптическую плотность (ОП). Корректированная ОП = средняя ОП лунки с гликированным белком - средняя ОП лунки БСА. Процент разрушения выражали в виде относительного уменьшения ОП: [(средняя ОП лунки фосфатный буферный раствор - средняя ОП лунки исследуемого соединения)/средняя ОП лунки фосфатный буферный раствор]×100%.
Обработка результатов выполнялась в программе Microsoft Excel (Microsoft, США) с расчетом базовых статистических показателей: среднего арифметического М, стандартного отклонения s, стандартной ошибки среднего арифметического m. Статистическая обработка с применением парного t-критерия Стьюдента в программе Statistika 10.0 (StatSoft, США).
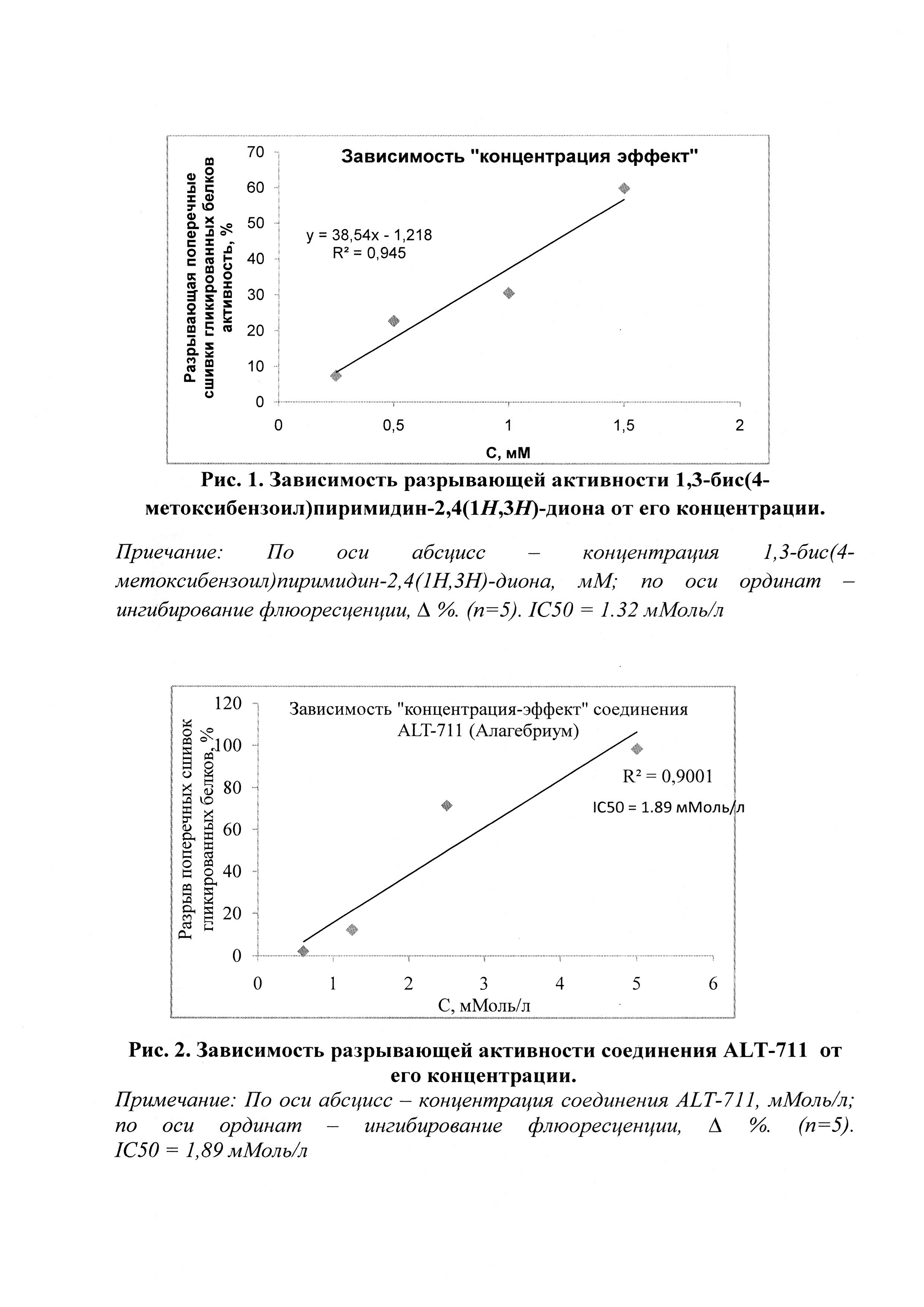
В результате проведенных исследований in vitro установлено, что патентуемое соединение 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-дион характеризуется разрывающей поперечные сшивки гликированных белков активностью. Так, было выявлено, что для патентуемого соединения, 1,3-бис(4-метоксибензоил)пиримидин-2,4(1H,3H)-диона, характерно значение IC50=1.32 мМоль/л. В процессе исследования было установлено значение IC50 препарата сравнения алагебриума (ALT-711), которое составило 1,89 мМоль/л (по литературным данным 1,67 мМ).