N-ацетил-L-цистеин для применения в экстракорпоральном оплодотворении
Вид РИД
Изобретение
Область изобретения
Настоящее изобретение относится к новому применению N-ацетил-L-цистеина в экстракорпоральном оплодотворении.
Предпосылки изобретения
Экстракорпоральное оплодотворение (ЭКО) представляет собой метод, посредством которого одну яйцеклетку оплодотворяют при помощи сперматозоида вне организма. ЭКО является основным лечением бесплодия, тогда как другие способы вспомогательной репродуктивной технологии не имели успеха. Этот метод включает в себя отслеживание овуляционного процесса женщины, извлечение яйцеклетки или яйцеклеток из яичников женщины и предоставление возможности сперме оплодотворять их в жидких средах в лаборатории. В том случае, когда отслеживают естественный цикл женщины с целью сбора отобранной в естественных условиях женской зародышевой клетки (яйцеклетки) для оплодотворения, его называют ЭКО в естественном цикле. Оплодотворенную яйцеклетку (зиготу) затем переносят в матку пациентки с намерением вызывания успешной беременности. Первое успешное рождение "ребенка из пробирки", Луизы Браун, имело место в 1978 г. Луиза Браун родилась в результате ЭКО в естественном цикле. Роберту Дж. Эдвардсу, физиологу, разработавшему лечение, была присуждена Нобелевская премия по физиологии или медицине в 2010 (S.K. Kalra et al. Fertility and Sterility Vol 95, no 6, p. 1888-1889. In vitro fertilization and adverse Childhood outcomes: what we know, where we are going, and how we will get there. A glimpse into what lies behind and beckons ahead. В Almog et al. Fertility and Sterility Vol 94, N 6, p 2026-2028. Promoting implantation by local injury to the endometrium).
Несмотря на значительный прогресс во вспомогательной репродуктивной технологии в течение последних 25 лет, общая эффективность даже наиболее передовых лечений, таких как ЭКО/перенос эмбриона (ЭКО/ПЭ), является относительно низкой, в среднем примерно 20-30% рождения живых детей на цикл лечения (Nyboe-Andersen et al., Hum Reprod. 2009; 24(6): 1267-87).
Перенос эмбриона является независимым фактором, влияющим на результат лечения. Определяющие успех факторы при переносе эмбриона включают в себя качество эмбриона(ов), рецептивность матки и качество внутриматочной среды (Cavagna and Mantese, Placenta. 2003; 24 Suppl В: S39-47).
Маточные сокращения являются наиболее существенными составляющими рецептивности матки. Сократительная активность матки играет важную роль в имплантации эмбриона. Чрезмерные маточные сокращения могут снижать коэффициенты имплантации в циклах ЭКО, так как сократительная активность может выталкивать эмбрионы из матки (Fanchin et al. Hum Reprod, 1998; 13: 1968-74). До настоящего времени стратегии лечения для уменьшения маточных сокращений перед переносом эмбриона, такие как применение бета-агонистов или нестероидных противовоспалительных лекарственных средств, не продемонстрировали обеспечения существенного преимущества (Moon et al., Fertil Steril 2004; 82:816-20; Tsirigotis et al. Human Reproduction and Embryology, June 25-28, 2000; Bologna, Italy).
Циклы лечения вызывают избыточное повышение концентраций эстрадиола, которые составляют примерно 10-20 нмоль/л в конце стимуляции яичников по сравнению с концентрацией менее 2 нмоль/л перед овуляцией в естественном цикле. Предполагают, что супрафизиологические концентрации эстрадиола индуцируют локальное (эндометриальное) продуцирование окситоцина, образование окситоциновых рецепторов, и, опосредственно, образование/высвобождение PGF2a (простагландин F2a), что фактически аналогично предродовому состоянию. Также, окситоцин и вазопрессин вовлечены в индуцирование и сохранение маточных сокращений во время родов.
Было показано, что сократительная активность матки в циклах ЭКО увеличивается приблизительно 6-кратно при измерении перед переносом эмбриона по сравнению с ситуацией перед овуляцией в естественном цикле. Маточные сокращения играют важную роль в репродукции человека, будучи активно вовлеченными в скорый и направленный транспорт спермы и имплантацию эмбриона в высшей точке дна матки.
В ходе ЭКО-лечения/ПЭ наблюдают постепенное снижение маточных сокращений после сбора яйцеклеток, достигающее почти неподвижного состояния во время переноса бластоцисты (5-6 сутки после сбора яйцеклеток) (Fanchin et al., Fertil Steril 2001; 75: 1136-40). Полагают, что такое снижение сократительной активности дополнительно увеличивает более высокие коэффициенты имплантации, достигаемые при помощи переноса бластоцисты. Однако большую часть эмбрионов по-прежнему переносят на 2 или 3 сутки после оплодотворения во время периодов заметной сократительной активности матки.
Предполагают, что сама процедура переноса эмбриона повышает локальное высвобождение окситоцина и простагландинов. Любая дополнительная манипуляция с влагалищем или шейкой матки, такая как применение расширителя, дает дополнительный стимул для высвобождения окситоцина/простагландина (Dorn et al., 1999), который связан с усилением маточных сокращений. Mansour et al. продемонстрировали, что у более половины пациенток, имеющих ложный перенос эмбриона с красителем метиленовым синим, после процедуры обнаруживается перенесенный во влагалище краситель (Mansour et al., Hum Reprod 1994; 9: 1257-9). Также было продемонстрировано, что менее 50% перенесенных эмбрионов оставалось в матке через 1 час после переноса и примерно 15% эмбрионов можно было обнаружить во влагалище после переноса эмбриона (Poindexter et al. Fertil Steril, 1986; 46:262-7).
С учетом вышесказанного предположили, что сократительная активность матки во время переноса эмбриона и особенно сокращения от дна матки к шейке могут выталкивать эмбрионы из матки. Fanchin et al., Human Reprod 1998; 13:1968-74 оценили, что примерно 30% пациенток, подвергающихся переносу эмбриона, имеет резко выраженные маточные сокращения. В этой группе коэффициенты успеха ЭКО-лечения/ПЭ были в три раза меньше по сравнению с популяцией пациенток с «молчащей маткой» (16% и 53% клинических беременностей, соответственно). Различие не зависело от направления маточных сокращений, замеченных во время анализов. Это могло означать, что фармакологическое подавление возросших сокращений во время переноса эмбриона может являться привлекательной мишенью для потенциального лечения.
Вмешательство в системы PGF2a/окситоцин и, возможно, улучшение эндометриальной перфузии могли бы представлять собой один механизм, посредством которого могли быть снижены маточные сокращения и улучшена рецептивность матки.
Эффективность экстракорпорального оплодотворения-переноса эмбриона (ЭКО-ПЭ) обычно не превышает 30% на цикл лечения (Nyboe Andersen A., Gianaroli L., Felberbaum R., de Mouzon J., Nygren K. Assisted reproductive technology in Europe, 2001. Results generated from European registers by ESHRE. Hum Reprod 2005; 20:1158-76) и дополнительно снижается у женщин старше 36 лет (Stolwijk A., Wetzels A., Braat D. Cumulative probability of achieving an ongoing pregnancy after in vitro fertilization and intracytoplasmic sperm injection according to a woman's age, subfertility diagnosis and primary or secondary subfertility. Hum Reprod 2000; 15: 203-9).
Хорошее качество эмбрионов и оптимальная внутриматочная среда являются основными определяющими факторами успеха для ПЭ и всей процедуры ЭКО-ПЭ. Идеальные внутриматочные условия, которые делают возможной имплантацию, включают подходящий статус эндометрия, достаточную перфузию эндометрия и отсутствие чрезмерных маточных сокращений. В частности, повышенная сократительная активность матки может выталкивать эмбрионы из матки (Mansour R., Aboulghar M.A., Serour G.I., Amin Y.M. Dummy embryo transfer using methylene blue dye. Hum Reprod 1994; 9: 1257-9) (Poindexter A, Thompson D., Gibbons W. Residual embryos in failed embryo transfer. Fertil Steril 1986; 46: 262-7).
Коэффициенты имплантации и беременности обратно пропорционально коррелируются с частотой маточных сокращений и синтезом простагландина (синтез PG). Высокую сократительную активность матки при ПЭ (пять или более сокращений в минуту) обнаруживают примерно у одной трети пациенток, и у этих женщин коэффициенты клинической беременности достигают 13% на цикл, в отличие от 53% успешных беременностей у женщин с более низкой активностью матки (три или меньше сокращений в минуту) (Fanchin R., Righini С., Olivennes F., Taylor S., de Ziegler D., Frydman R. Uterine contractions at the time of embryo transfer alter pregnancy rates after in-vitro fertilization. Hum Reprod 1998; 13: 1968-74). Кроме того, раздражение шейки матки посредством катетера для ПЭ вероятно индуцирует дополнительный синтез PG и сократительные рефлексы и дополнительно снижает шансы успешной имплантации эмбриона (Lesny P., Killick S., Tetlow R., Robinson J., Maguiness S. Embryo transfer - can we learn anything new from the observation of junctional zone contractions? Hum Reprod 1998; 13: 1540-6).
Однако сократительная активность матки, являющаяся важной составляющей рецептивности матки, в настоящее время не является предметом специальной диагностики или лечения у реципиентов ПЭ. Добавление прогестерона, даже при влиянии на рецептивность матки, улучшении эндометриального статуса и уменьшении маточных сокращений, не демонстрирует преимуществ в отношении коэффициентов беременности после ЭКО-ПЭ. (Fanchin R, Righini С, de Ziegler D, Olivennes F, Ledee N, Frydman R. Effects of vaginal progesteron administration on uterine contractility at the time of embryo transfer. Fertil Steril 2001; 75:1136-40).
Исследования по оценке эффективности пироксикама (ингибитор циклооксигеназы) и ритодрина (агонист β2-адренорецептора) продемонстрировали положительное влияние на коэффициенты беременности. (Moon Н., Park S., Lee J., Kim K., Joo В. Treatment with piroxicam before embryo transfer increases pregnancy rate after in-vitro fertilization и embryo transfer. Fertil Steril 2004; 82: 816-20; Tsirigotis M., Pelekanos M., Gilhespie S., Gregorakis S., Pistofidis G. Ritodrine use during the peri-implantation period reduces uterine contractility and improves implantation and pregnancy rates post-implantation. Presented at the 16th annual meeting of the European Society of Human Reproduction and Embryology; June 25-28, 2000; Bologna, Italy). Лекарствам, упомянутым выше, было отказано в регистрации для обычного клинического применения из-за опасений по поводу безопасности.
Недавно было описано рандомизированное плацебо-контролируемое исследование с общей в/в дозой 37,5 мг атосибана (антагонист окситоцина), введенной посредством инфузии перед переносом эмбриона и вплоть до 2 часов после него у 160 пациенток (Moraloglu et al. Treatment with окситоцин antagonists before embryo transfer may increase implantation rates after IVF. Reproductive biomedicine online 09/2010; 21(3): 338-43). Авторы отметили значительное улучшение как коэффициентов имплантации, так и коэффициентов клинических беременностей. Коэффициенты имплантации на перенесенный эмбрион равнялись 20,4% по сравнению с 12,6% и коэффициенты клинической беременности на цикл равнялись 46,7% по сравнению с 28,9% (атосибан в сравнении с плацебо). В группе исследования отмечали меньшее количество преждевременных самопроизвольных абортов (16,7% по сравнению с 24,4%, атосибан по сравнению с плацебо).
N-ацетил-L-цистеин (в дальнейшем обозначается NAC) представляет собой хорошо известное лекарство, которое использовалось главным образом в качестве муколитического агента и в лечении отравления парацетамолом. В последние годы было признано, что он также обладает другими благоприятными свойствами, такими как противовоспалительные и антипролиферативные свойства, и он был рекомендован для лечения целого ряда различных расстройств и симптомов, включающих, помимо эндометриоза, шизофрению, диабет и раковые заболевания.
До настоящего времени NAC не считался лекарственным средством в лечении фертильности, хотя его применяли для перорального лечения эндометриоза, как описано в ЕР 2305238. В этом исследовании отсутствуют выводы о вызванных искусственным путем беременностях. Наоборот, при лечении эндометриоза не предполагали, что могут иметь место какие-либо беременности. Хотя, это не было раскрыто раньше, при анализе данных авторы изобретения заметили, что один человек, который получал NAC перорально при эндометриозе, имел успешное ЭКО-лечение. К тому же два предыдущих исследования ЭКО не имели успеха и имели результатом аборт. Это была одна из причин, по которой авторы настоящего изобретения начали исследование того, можно ли использовать NAC применительно к ЭКО.
Действительно было подтверждено, что у мышей NAC поддерживает имплантацию эмбриона. В животной модели коэффициент имплантации эмбриона снижался, когда мышам давали окситоцин. В зависимости от дозы NAC восстанавливал коэффициенты имплантации у мышей, которых лечили окситоцином, что является доказательством вовлечения окситоцина в имплантацию эмбриона.
Предшествующий уровень техники
Предшествующий уровень, описывающий молекулярный эффект NAC в лечении ракового заболевания, включает: Т. Parasassi et al. Cell Death and Differentiation (2005), Vol. 12, N10, pages 1285-1296; E. K. Krasnowska et al. Free Radicals Biology and Medicine 2008, 45(11): 1566-72; A.C. Gustafsson et al. BMC Cancer (2005), 5:75. NAC в лечении эндометриоза описан в Pittaluga et al. More than an antioxidant: N-acetyl-L-Cysteine in a murine model of endometriosis. Fertil & Steril 2010; 94(7): 2905-8. Кроме того, C.H. Kim et al. (Abstracts of the 22nd Annual Meeting of the ESHRE, Prague, Czech Republic, 18-21 June 2006, P-463) описывают лечение при помощи N-ацетил-цистеина для улучшения чувствительности к инсулину. Композиции, содержащие N-ацетил-L-цистеин (NAC) сам по себе или вместе с (2) селеном в форме селенометионина и/или (3) мелатонином и/или их физиологически приемлемыми солями, описаны в ЕР 12710062.6. Такие композиции также можно применять для ЭКО-лечения.
Цели изобретения
Уже с момента появления ЭКО существует проблема низкого клинического результата в ЭКО-лечении. Так как стоимость ЭКО является высокой, и лечение обычно дает только 20-30% рождения живых детей на цикл лечения, много различных видов лечения было испытано с целью получения более высокого процента рождения живых детей. В настоящее время неожиданно было обнаружено, что введение NAC предпочтительно за несколько суток перед ЭКО-лечением дает более высокий процент рождения живых детей. Кроме того, в случаях, когда многие более ранние случаи ЭКО-лечения были безуспешными, предварительное введение NAC, связанное с новым ЭКО-лечением приводило к рождению живых детей.
Клинический результат NAC-лечения, как определено в формуле изобретения настоящей заявки, в экстракорпоральном оплодотворении (ЭКО) не был, насколько известно авторам изобретения, определен в предшествующем уровне техники, также эффективная схема приема для ЭКО-лечения или применение NAC для лечения ассоциированных с ЭКО симптомов не были предложены.
По этой причине главная цель настоящего изобретения заключается в решения проблемы обеспечением фармацевтической композиции, содержащей N-ацетил-L-цистеин (NAC), для ЭКО-лечения и лечения ассоциированных с ЭКО симптомов у людей и млекопитающих.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Согласно настоящему изобретению предложена фармацевтическая композиция, содержащая N-ацетил-L-цистеин (NAC), используемая для внутривенного и/или перорального введения. Композиция содержит N-ацетил-L-цистеин (NAC) сам по себе или вместе с (2) селеном в форме селенометионина и/или (3) мелатонином и/или их физиологически приемлемыми солями.
Композиция, содержащая NAC сам по себе, содержит от 70 до 150 мг/кг массы тела NAC и вводится один раз в сутки в течение 1-3 суток при ЭКО-лечении. Можно также вводить только один раз, а именно в день проведения ЭКО. В таком случае введение имеет место за 1 час перед ЭКО.
Примеры Эмбриотоксичность
Предварительно испытывали NAC на возможное присутствие эмбриотоксичности. Для проверки эмбриотоксичности NAC при применении проводили два теста на эмбриотоксичность - биотест на эмбрионе кролика и биотест на подвижность спермы человека (см. Pierzynski et al., 2007а). Оба не имели успеха в обнаружении эмбриотоксичного эффекта NAC в концентрациях вплоть до 50-кратных терапевтических концентраций в крови. Показано, что NAC не оказывает воздействия на выживание 1-клеточных эмбрионов кролика, а также не снижает процент выведенных искусственно бластоцист кролика. Тесты, выполненные на сперматозоидах человека, также не имели успеха в установлении вредного влияния.
Тест на токсичность - Биотест на подвижность спермы человека
Тесты подвижности спермы человека выполняли на свежих образцах, взятых от 3 здоровых доноров с хорошими параметрами спермы, включая подвижность и скорость спермы. Перемещение или "Swim-up" в средах препарата спермы человека использовали для отбора подвижных сперматозоидов. После отбора каждый образец семени разделяли на 3 аликвоты и переносили в пробирки Eppendorf. В дополнение к одной контрольной пробирке в две пробирки добавляли NAC в концентрациях 100 и 1000 нМ. Пробирки инкубировали в среде с 5% CO2 в условиях постоянной температуры и влажности в течение 24 часов. Подвижность спермы оценивали, используя контрастно-фазовый микроскоп при 400-кратном увеличении, после 1 и 24 часов подвергания воздействию NAC. Анализ выполняли в течение фиксированного интервала времени 2 минуты. Девять образцов оценивали на подвижность и скорость спермы путем 36 измерений (2 измерения в 1 и 24 часы на образец).
В ходе биотеста на подвижность спермы человека не обнаружили воздействия NAC на подвижность или скорость спермы человека по сравнению с контрольными группами. Однако продолжительность эксперимента влияла на подвижность, обнаруживаясь в виде постепенного снижения активности и скорости сперматозоидов. Это снижение наблюдали как в контрольных группах, так и в группах, обработанных NAC, и между группами не было различия. Обнаружили отсутствие взаимосвязи между временем и концентрацией, так что эффект времени не отличался значительно в 2 группах с концентрациями 100 и 1000.
In vitro
Во время имплантации в трансплацентарном барьере интегрины экспрессируются крайне упорядоченным образом. Однако значение лигандов внеклеточного матрикса (ЕСМ) во время опосредованного интегрином присоединения эмбриона к эндометрию понятно не полностью. Таким образом, исследовали во время имплантации распределение фибронектина в матке крысы и бластоцисте. Фибронектин отсутствовал в люминальных эпителиальных клетках матки, но интенсивно экспрессировался в клетках трофобласты и в зародышевом узелке, из чего можно заключить, что фибронектин, секретируемый из бластоцисты, может представлять собой возможный мостиковый лиганд для интегринов, экспрессирующихся в трансплацентарном барьере. Пептид Arg-Gly-Asp (RGD) использовали для блокировки сайтов распознавания RGD на интегринах, и изучали воздействие на присоединения бластоцисты крысы к клеткам Ishikawa. Обнаружили значительное снижение присоединения бластоцисты, когда либо бластоцисту, либо клетки Ishikawa предварительно инкубировали с RGD-блокирующим пептидом. Таким образом, успешное присоединение эмбриона к эндометрию требует взаимодействия интегринов как на эндометрии, так и на бластоцисте с последовательностью RGD лигандов ЕСМ, таких как фибронектин. Предварительная обработка бластоцист и клеток Ishikawa при помощи пептида RGD также ингибировала присоединение бластоцисты, но не полностью, из чего следует, что мостиковые лиганды ЕСМ, которые не содержат последовательность RGD, также вовлечены в присоединение эмбриона (Kaneko Y., Murphy C.R., Day M.L. Extracellular matrix proteins secreted from both the endometrium and the embryo are required for attachment: A study using a co-culture model of rat blastocysts and Ishikawa cells. J Morphol. 2013; 274 (1): 63-72).
Эксперимент 1
Данные эксперименты осуществляли, чтобы прояснить, влияет ли обработка при помощи NAC на соединение (прилипание) белков, включая интегрин/фибронектин.
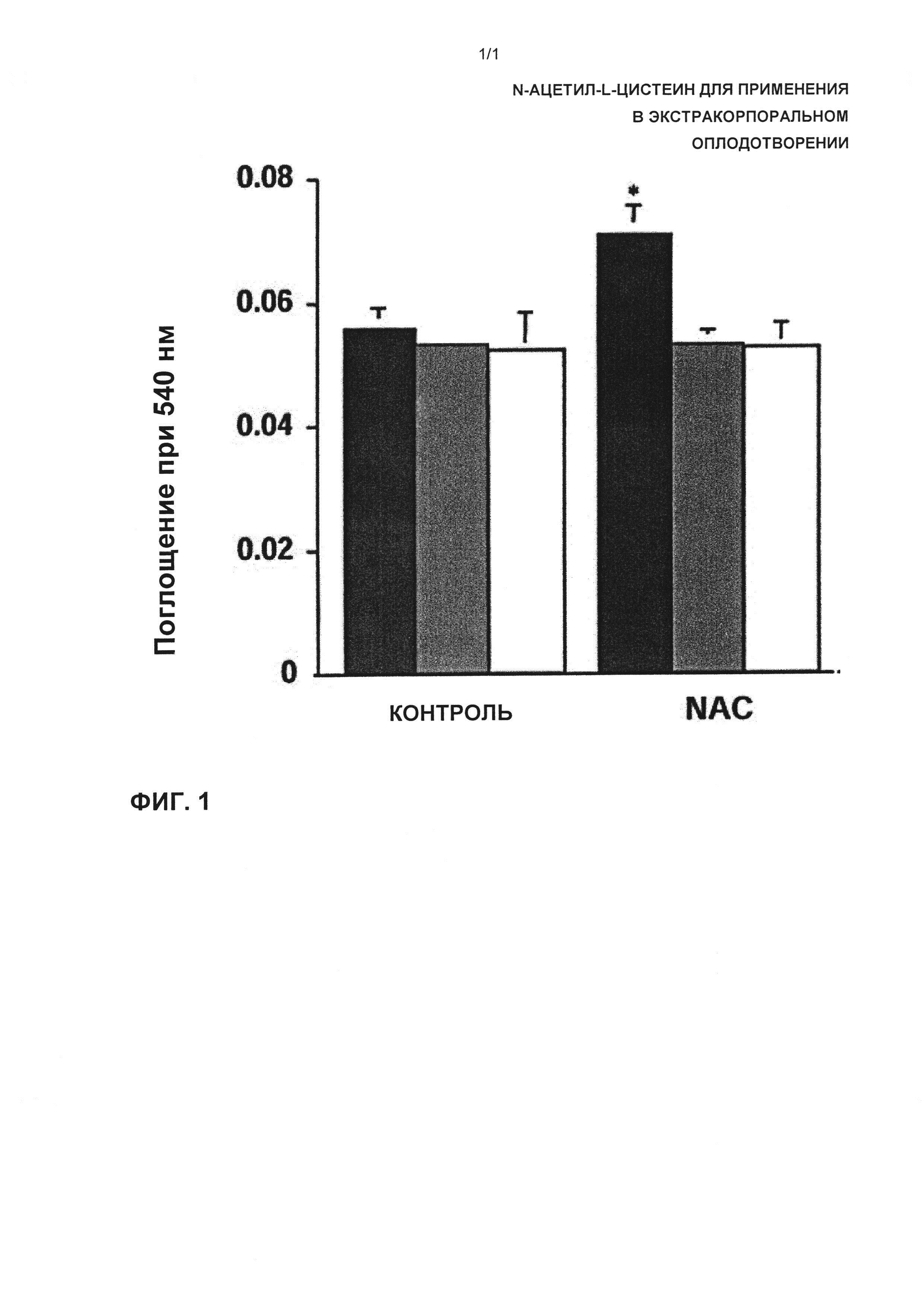
Анализ клеточной адгезии. Семь мкг/мл фибронектина человека (Sigma Aid rich Chem Co) насыщали 2% бычьим сывороточным альбумином (БСА) в течение 30 мин при 37°С и промывали дважды фосфатно-солевым буферным раствором (PBS). Затем делали посев клеток Jurkat в лунки в течение 2 часов при 37°С, затем неприлипшие клетки отсасывали, и лунки прополаскивали при помощи PBS. Прилипшие клетки фиксировали в течение ночи при помощи 2% формальдегида и окрашивали эозином Y в течение 30 мин. Затем эозин Y извлекали путем добавления смеси 1% ледяной уксусной кислоты и 50% этанола и поглощение измеряли при 540 нм.
Экспрессия интегрина альфа-4 (VLA-4). Экспрессию антигена VLA-4 обнаруживали в клетках Jurkat путем непрямой иммунофлуоресценции при помощи моноклональных антител против VLA-4 (клон НР1/7) и проточной цитометрии. Окрашивание клеток выполняли согласно стандартным протоколам и анализ проточной цитометрией выполняли с применением цитометра FACS-Calibur (Becton Dickinson).
Результаты со ссылкой на Фиг. 1
NAC повышает адгезию клеток Jurkat на фибронектине. Анализ адгезии выполняли при использовании контроля или клеток Jurkat, обработанных при помощи NAC (5 мМ в течение 2 часов). Клетки фотографировали после окрашивания эозином Y. Инкубирование клеток после обработки при помощи NAC с антителами против VLA-4 подавляло прилипание. Затем адгезию клеток оценивали количественно путем окрашивания клеток, присоединенных к планшетам, покрытым соединенными белками, при помощи эозина Y и считывали поглощение в микропланшетном ридере. Как показано на Фиг. 1, предварительная обработка при помощи NAC усиливала адгезию клеток приблизительно на 35%, этот эффект аннулировали посредством антител против VLA-4.
Клетки солюбилизировали и добавляли эозин Y и поглощение количественно оценивали при 540 нм. Отсутствие антител показано черными полосками; антитела против VLA-4 (10 нг/мл) показаны серыми полосками; и антитела против VLA-4 (10 мкг/мл) показаны белыми полосками. Данные представляют собой средние значения +/-SE (стандартная ошибка) (n=3).*, Р меньше, чем 0,01 по сравнению с контролем. На основании Фиг. 1 можно прийти к выводу, что обработка при помощи NAC увеличивает адгезию (молекулы соединенных белков).
Эксперимент 2
Настоящие эксперименты осуществляли, чтобы прояснить, влияет ли обработка при помощи NAC на экспрессию генов интегрина и фибронектина, посредством анализ экспрессии гена, используя платформу Affymetrix GeneChip.
Анализ экспрессии гена нормальных эпидермальных кератиноцитов человека в микропланшетах осуществляли через 1 и 12 часов после добавления NAC, сравнивали с необработанными образцами (то есть контрольными образцами в те же самые моменты времени). Данные, полученные из анализа GeneChip, обрабатывали, применяя способ с анализом РНК, и образцы нормализовали к их соответствующим контролям. Фильтрование выполняли на основе двух критериев (р-значение менее чем 0,1 и более чем 1,5-кратное повышение или более чем 0,5-кратное снижение экспрессии) в течение каждого момента времени. Маркирование и гибридизацию выполняли в двух повторностях.
Через 1 час после обработки при помощи NAC интегрина альфа 2, обнаружили повышение экспрессии. Через 12 часов обнаруживали повышение уровня фибронектина. Эти результаты свидетельствуют о том, что обработка при помощи NAC приводит к повышенной адгезии за счет непрерывного повышения экспрессии интегрина и фибронектина, и что некоторые из эффектов видны уже через один час после обработки.
Эксперимент 3
На мышах подтвердили, что NAC оказывает поддержку имплантации эмбриона. В животной модели коэффициент имплантации эмбриона снижался, когда мышам давали окситоцин. В зависимости от дозы NAC восстанавливал коэффициенты имплантации у мышей, которым вводили окситоцин, что доказывает участие окситоцина в имплантации эмбриона.
Для проверки эмбриотоксичности NAC при применении использовали два испытания на эмбриотоксичность - биотест на эмбрионе кролика и биотест на подвижность спермы человека. Оба не имели успеха в обнаружении эффекта эмбриотоксичности NAC в концентрациях вплоть до 50-кратных терапевтических концентраций в крови. Показано, что NAC не воздействует на выживание 1-клеточных эмбрионов кролика, а также не снижает процент выведенных искусственно бластоцист кролика. Тесты, выполненные на сперматозоидах человека, также не имели успеха в установлении вредного влияния.
Эксперимент 4
Исследование на животных, демонстрирующее, что NAC ослабляет сокращения матки
План эксперимента
Животных содержали при 22°С, поселяли по 3 особи в клетку и кормили без ограничений. Использовали извлеченные матки от девственных крыс Wistar (200-280 г) при эструсе, который определяли при помощи анализа влагалищного мазка ежедневно.
Реагенты
Протамина сульфат (PS) и NAC растворяли в чистой воде.
Исследования при помощи инкубатора изолированных органов
Всех крыс умерщвляли посредством смещения шейных позвонков. Рога матки иссекали, осторожно очищали и закрепляли вертикально в инкубаторе органов объемом 10 мл, содержащем среду де Жалона (NaCl 154 мМ, KCl 5,6 мМ, CaCl2 × 2H2O 0,41 мМ, NaHCO2 5,9 мМ и глюкоза 2,8 мМ), при напряжении 1 q, аэрировали при помощи 95% кислорода и 5% углекислого газа при 37°С. После достижения периода равновесия (45 мин), когда матки демонстрировали стабильные сокращения (самопроизвольные или индуцированные ионами кальция), добавляли индометацин (1 мкг/мл), а затем PS. Через 10 мин добавляли PS в возрастающих концентрациях до тех пор, пока не наблюдали полное прекращение сокращений.
Миометральное напряжение регистрировали изометрически при помощи инкубатора органов и датчика-преобразователя.
Анализ данных и статистические процедуры
Эффекты лечения на сокращения матки вычисляли в виде процентов относительно контроля, необработанного состояния и состояния с сокращениями. Каждое значение данных выражали в виде среднего ±SEM (стандартная ошибка среднего значения). Различия между группами анализировали посредством двухфакторного дисперсионного анализа. Значения ЕС50 (полумаксимальная эффективная концентрация) сравнивали, используя однофакторный дисперсионный анализ.
Результаты
PS вызывал дозозависимую релаксацию самопроизвольно возбуждаемых маток. Предварительная обработка при помощи NAC (1 мкг/мл) увеличивала индуцируемую PS релаксацию. PS также вызывал дозозависимую релаксацию, индуцированную ионами кальция маточных сокращений. Предварительная обработка при помощи NAC модулировала индуцируемую PS релаксацию маточных сокращений и изменяла кривые индуцируемой PS релаксации.
Проанализировали значения ЕС50 для обработанных при помощи PS маток. Обнаружили значимые различия среди значений ЕС50 в части, касающейся типа применяемого сокращения и применяемой обработки. ЕС50 была ниже у самопроизвольно возбуждаемых маток, чем у маток, индуцированных ионами кальция. Значения ЕС50 для самопроизвольно возбуждаемых маток, предварительно обработанных при помощи индометацина (1 мкг/мл), были значительно ниже, чем другие два полученных значения ЕС50. Однако матки с индуцированным ионами кальция возбуждением, предварительно обработанные при помощи индометацина, демонстрировали более высокие значения ЕС50 при сравнении с матками, обработанными при помощи PS.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Общая информация о NAC
N-ацетил-L-цистеин (NAC) представляет собой хорошо известное низкомолекулярное фармацевтическое лекарственное средство с химической формулой
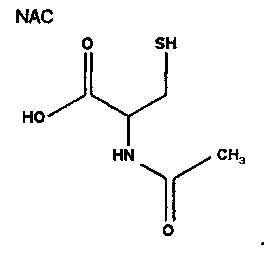
Свойства NAC связаны главным образом с его тиоловой группой, которая делает его эффективным в большинстве биохимических путей, где действует трипептид глютатион (GSH), присутствующий во всех тканях человека в относительно высоких концентрациях, даже выше 10 мМ. Цистеин, несомненно, является одной из трех аминокислот, входящих в состав GSH, поэтому NAC считают предшественником GSH с деацетилированным цистеином. NAC использовался и по-прежнему широко используется в качестве муколитического агента, механизм действия которого обычно объясняется окислительно-восстановительным разрывом чувствительных дисульфидных мостиков цистеина в белках слизи. Фактически, NAC принимает участие в сложном окислительно-восстановительном циклическом изменении тиоловых групп, где действует несколько ферментов. Более того, исключительной физиологической важностью является цикл образования и разрыва дисульфида, представляющий собой общий механизм, посредством которого регулируется активность белка и передача сигнала в клетке. Ферменты, такие как протеинтирозинфосфатазы и тирозинкиназы, например, играют ключевые роли в контроле клеточного цикла, пролиферации и дифференцировке клеток, и многие из них регулируются посредством состояния окисления-восстановления их цистеинов.
В общем и целом, хотя подробные механизмы действия не были окончательно объяснены, NAC, по-видимому, действует во всех биохимических путях, где участвует GSH. Ферменты и белки, чья активность модулируется посредством GSH, работают в нескольких процессах или непосредственно, или через сеть путей сигнальной трансдукции. В этой ситуации NAC может действовать либо параллельно с GSH, либо может быть даже более эффективным, чем GSH.
GSH, например, обычно конъюгируется с реакционноспособными метаболитами, образованными парацетамолом, и помогает его нейтрализовать. При передозировке парацетамола GSH, однако, истощается, и метаболиты парацетамола начинают взаимодействовать с клеточными белками, приводя, в конечном счете, к некрозу клеток. Во время лечения внезапно и быстро развивающейся печеночной недостаточности после отравления парацетамолом NAC действует вместо GSH в нейтрализации метаболитов парацетамола. Полагают, что у NAC в сущности отсутствуют нежелательный побочный эффект, на что также указывают высокие дозы NAC, которые используют в лечении отравления парацетамолом, предположительно, для субъекта с массой 70 кг, примерно 40 г/сутки.
В противоположность трипептиду GSH, который может распадаться уже в желудке, простая молекула NAC легко диффундирует почти во всех тканях и клетках. В фармакокинетических исследованиях NAC определили пиковую концентрацию в плазме, достигаемую примерно в течение одного часа с периодом полувыведения примерно три часа. Общий клиренс длится от шести до двенадцати часов.
NAC в качестве антипролиферативного дифференцирующего агента Авторы изобретения недавно обнаружили, что N-ацетил-L-цистеин (NAC) обладает заметным антипролиферативным воздействием на раковые клетки эпителиального происхождения (Cell Death and Differentiation 2005, 12(10): 1285-1296).
NAC использовали для задержки пролиферации и индуцирования дифференцировки на двух клеточных линиях аденокарциномы и на первичных клетках нормального кератиноцита (все клетки эпителиального происхождения). В этих системах дифференцировку характеризовали морфологически, биохимически и посредством анализа экспрессии гена (анализ экспрессии гена подробно описан в ВМС Cancer 2005, 5: 75).
В исследовании ракового заболевания антипролиферативный эффект NAC не был связан с некрозом клеток или с токсичностью, но, вместо этого, являлся результатом активации пути физиологической дифференцировки, что можно рассматривать как нормализацию клеточных функций по отношению к первичной ткани.
В дополнение к сниженной пролиферации, морфология обработанных при помощи NAC раковых клеток также изменялась. Эпителиальные клетки при активной пролиферации проявляют in vitro несимметричную морфологию, а именно мезенхимальную морфологию, и часто образуют несколько многоклеточных слоев. Наоборот, когда клетки подвергаются процессу дифференцировки по отношению к структуре и функции их конечной целевой ткани, они прекращают пролиферацию, их морфология становится симметрично полигональной, каждая в отдельности клетка иногда толще, и они образуют один слой примыкающих друг к другу клеток. Этот процесс сопровождается увеличением числа соединений клетка-клетка и клетка-субстрат, которые согласуются с изменением фенотипа с пролиферирующего мезенхимального на адгезивный, менее подвижный и дифференцированный фенотип.
В целом, после добавления NAC к раковым клеткам обнаруживали сложный комплекс метаболических изменений, сводящихся к задерживанию неконтролируемой пролиферации и индуцированию их терминальной дифференцировки. А именно, обработка NAC индуцировала значительное возрастание комплексов адгезии клетка-клетка и клетка-субстрат. Неконтролируемую пролиферацию можно рассматривать как состояние, когда клетки утратили контактное торможение и свою способность отвечать на сигналы дифференцировки. Клетки, входящие в путь дифференцировки, проявляют ощутимое увеличение комплексов соединений клетка-клетка, и обычно этот процесс также обозначают как контактное торможение. Некоторые факты показывают, что сигналы клеткам входить в начальную точку дифференцировки возникают из компонентов комплексов клетка-клетка. Эти соединения также являются путем для распространения сигналов между клетками.
Схема приема
Из исследования лечения при помощи NAC на клеточных линиях аденокарциномы и на первичных нормальных кератиноцитах (Cell Death and Differentiation 2005, 12(10): 1285-1296), пришли к выводу, что эффективная доза NAC для индуцирования антипролиферативного-дифференцирующего эффекта варьировала и зависела от типа клеток. Первичная ткань, таким образом, определяет эффективную концентрация NAC, требующуюся для наблюдения полного блокирования пролиферации, которая должна определяться для каждой ткани. Кроме того, доза NAC также была связана со злокачественностью клеток. Более подробно, в то время как нормальным клеткам требовалась низкая доза для остановки пролиферации и начала дифференцировки, клеткам карциномы с характерным неблагоприятным прогнозом требовалась более высокая концентрация NAC.
Для цели настоящего изобретения схему приема NAC для ЭКО-лечения у млекопитающего, включая человека, разрабатывали на основе следующих критериев:
1) суточная дозировка NAC, которая согласуется с другими текущими клиническими лечениями и рассматривается как не имеющая нежелательных побочных эффектов;
2) установление описанного снижения уровня NAC в плазме после длительных лечений (Pendyala L, Creaven PJ. Cancer Epidemiol Biomarkers Prev. 1995; 4:245-51), приостановка лечения в течение примерно половины каждой недели рассматривали относительно оптимального биологического ответа на лечение в течение двух месяцев или больше.
Композиция по настоящему изобретению, содержащая NAC, для ЭКО-лечения согласно одному воплощению подлежит введению внутривенно в дозе от приблизительно 50 до 150 мг/кг/сутки. Было показано, что нижний предел является эффективным при ЭКО, а верхний предел фактически не имеет побочных эффектов.
В еще одном воплощении настоящего изобретения композиция содержит NAC для перорального введения в дозе приблизительно 30-45 мг/кг/сутки. Неожиданно было показано, что эта низкая дозировка является эффективной в лечении эндометриоза и также дает эффект применительно к ЭКО.
В одном воплощении пероральная композиция подлежит введению в течение периода времени, который равен двум месяцам или более, или предпочтительно трем месяцам или более. Чтобы противодействовать снижению уровня NAC в плазме крови после длительного лечения, NAC можно вводить в заданной дозировке в прерывистом режиме, то есть по прерывистой(ом) схеме приема/лечении. Под прерывистым введением или лечением подразумевается, что лечение периодически приостанавливают, то есть, что фармацевтическую композицию вводят в течение периода времени, например, нескольких суток, с последующей приостановкой введения, когда фармацевтическую композицию не вводят в течение периода времени, например, нескольких суток. Прерывистое лечение может представлять собой регулярное лечение, например, лечение в течение фиксированного количества суток или недель с последующей приостановкой на фиксированное количество суток или недель. Примеры включают повторяющиеся схемы с лечением в течение 4 суток с последующей приостановкой на 3 суток каждую неделю или лечение в течение 2 недель с последующей приостановкой на 1 неделю. Особенный случай регулярного прерывистого лечения представляет собой лечение в импульсном режиме, то есть с регулярной продолжительностью лечения и приостановки, например введение каждые вторые сутки или введение в течение двух суток с последующими двумя сутками приостановки, и так далее. Схемы нерегулярного прерывистого лечения, которое не является регулярно повторяющимся или имеет более сложную схему, которая повторяется, также являются возможными, например, в зависимости от ответа на лечение. В различных воплощениях настоящего изобретения прописанную дозу NAC вводят в течение 3-5 суток подряд с последующими 2-4 сутками приостановки или вводят в течение 1-3 суток подряд с последующими 1-2 сутками приостановки.
В одном воплощении при массе тела, приблизительно равной 60 кг, доза NAC находится в диапазоне от 1,2 до 5,4 г/сутки, предпочтительно от 1,8 до 3,6 г/сутки. Эту дозу можно разделять на два или более, предпочтительно на три или четыре, ежедневных введения одной или двух доз (например, пилюлей) при каждом введении, где каждая доза может содержать, например, 0,15-2,7 г NAC или предпочтительно 0,6-1,2 г NAC. Лечение включает введение вышеупомянутых доз в импульсном режиме или прерывисто, например каждые вторые сутки или в течение трех-четырех суток подряд каждую неделю с временным прекращением на четверо-трое суток, соответственно. Минимальная общая продолжительность лечения составляет два месяца, без ограничения максимальной продолжительности. Для пациенток с другими массами, например лиц с избытком или недостатком массы, ежедневную дозу необходимо соответственно корректировать.
В одном воплощении настоящего изобретения фармацевтическая композиция для ЭКО-лечения, содержащая NAC в дозе 150-5400 мг, подлежит двум или более введениям в сутки в течение периода по меньшей мере 2 месяца, такого как по меньшей мере 3 месяца. В предпочтительном воплощении настоящего изобретения фармацевтическая композиция с содержанием NAC в дозе 230-3600 мг подлежит двум или более введениям в сутки в течение периода по меньшей мере 2 месяца, такого как максимум по меньшей мере 3 месяца. Лечение включает введение вышеупомянутых доз в импульсном режиме или прерывисто, например каждые вторые сутки или в течение трех-четырех суток подряд каждую неделю с временным прекращением на четверо-трое суток, соответственно.
NAC можно также вводить вместе с селеном в форме селенометионина и/или мелатонином. Такие комбинации дополнительно описаны в ЕР 12710062.6.
Фармацевтические композиции
Фармацевтическая композиция по настоящему изобретению может быть получена способом, по существу известным специалисту в фармацевтической области техники. Композиция может содержать эффективное количество NAC в соответствии с изобретением, а также подходящий носитель или эксципиент, которые служат в качестве средства доставки или среды для активного ингредиента. Такие носители или эксципиенты известны в данной области техники. Фармацевтическая композиция предназначается предпочтительно для в/в введения. Другие формы, такие как таблетки, капсулы, суппозитории, суспензии, сиропы или тому подобные, также являются возможными. Изобретение требует строгого анализа фармацевтического качества препарата NAC для получения эффективной дозы. По этой причине должны применяться брендовые или сертифицированные дженериковые препараты. NAC не является стабильной молекулой, его активный тиоловый остаток может легко окисляться кислородом, светом и посредством других излучений, так что эффективная доза может быть не достигнута. Препарат, таким образом, предпочтительно защищают от света в растворимых таблетках с гидрокарбонатом натрия, который помогает частичному удалению кислорода из воды во время растворения.
Было замечено, что высокие пероральные дозы NAC могут вызывать боль в животе. Для преодоления этого в случаях перорального введения решением является предложение NAC в композиции с защитой желудка, подходящей для предупреждения высвобождения/растворения NAC в желудке. Такие композиции хорошо известны в данной области техники и могут применяться в настоящем изобретении. Например, можно использовать оболочки для таблеток, которые являются устойчивыми к желудочному соку и делают возможным высвобождение лекарственного средства только в кишечнике после его прохождения через желудок. Применяемые обычно композиции содержат полимеры, такие как производные целлюлозы, сополимеры метакрилат/сложные аминоэфиры. Оболочка защищает ядро таблетки от расщепления в кислой среде желудка путем использования чувствительного к рН полимера, который разбухает или солюбилизируется после завершения прохождения через желудок в ответ на повышение рН для высвобождения лекарства.
Другое решение представляет собой снижение дозы NAC, поступающего в кровоток одновременно. Введение NAC три или более раза ежедневно может быть трудновыполнимым для пациента. Однако повторяющееся введение может быть желательным для достижения приблизительно постоянной концентрации NAC в сыворотке крови. Для преодоления этих проблем введение один раз или дважды-в-сутки может быть более легким для выполнения пациентом, например, утром и вечером. Одно решение представляет собой обеспечение NAC в композиции с замедленным высвобождением (также называемым длительным высвобождением или контролируемым высвобождением). Будучи способной снижать скорость диффузии и поглощения NAC в кровотоке, такая композиция дает возможность введения большей дозы в более продолжительных интервалах. Затем доза распределяется в крови в течение продолжительного времени в небольших количествах, например в течение 12+12 часов в случае схемы лечения дважды-в-сутки. Много различных технологий и композиций для замедленного высвобождения уже давно известны в данной области техники и могут применяться в настоящем изобретении. В таких технологиях активное вещество, например, инкапсулируют в оболочку или матрицу, которая нерастворима или малорастворима в жидкости тела, куда ее вводят.
Композиции, обладающие комбинированным эффектом замедленного высвобождения и защиты желудка, также являются возможными и могут применяться в настоящем изобретении.
Примеры на человеке
Введение применительно к ЭКО-лечению
Недавно был документально подтвержден самый первый случай клинического применения NAC до переноса эмбриона. NAC вводили в концентрации 50 мг/кг пациентке возрастом 42 года, которая раньше подвергалась пяти переносам эмбрионов, включающим общее количество эмбрионов высокого качества, равное 8. Непосредственно перед переносом эмбриона наличие повышенной сократительной активности матки подтверждали при помощи ультразвука. NAC в концентрации 50 мг/кг массы тела вводили в ходе внутривенной инфузии в течение 60 мин. Перенос эмбриона выполняли через 60 мин после окончания 60-минутного введения NAC в концентрации 50 мг/кг массы тела. Как перед началом инфузии, так и непосредственно перед переносом эмбриона осуществляли трансвагинальное сагиттальное сканирование. Посредством этого можно было подтвердить, что маточные сокращения снижались с 10 сокращений за 3 мин до пяти сокращений за 3 мин, а также регистрировали явное снижение их амплитуды. Терапевтический успех был подтвержден рождением здоровой дочери.
Введение в импульсном режиме
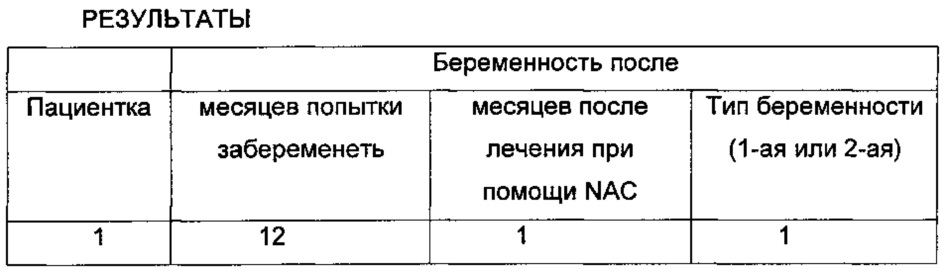
Ниже представлены результаты, полученные при введении NAC в импульсном режиме 15 пациенткам, 8 из которых забеременели.
Согласно этому, NAC вводили пациенткам перорально в течение 3 месяцев или более согласно следующему графику: 600 мг три раза в сутки, трое суток подряд в неделю. Выбор этой процедуры основан на следующих соображениях: (1) ежедневная общая доза NAC 1,8 мг фактически не имеет побочных эффектов и уже рассматривалась для других клинических показаний [K.R. Atkuri, J.J. Mantovani, L.A. Herzenberg, and L.A. Herzenberg, "N-acetylcysteine-a safe antidote for cystein/glutathione deficiency," Current Opinion in Pharmacology, vol. 7, no 4, pp. 355-359, 2007]; (2) разделение суммарной дозы на 3 несложно для пациенток и, с учетом известной фармакокинетики NAC [L. Pendyala and P.J. Creaven, "Pharmacokinetic and pharmacodynamic studies of N-acetylcysteine, a potential chemopreventive agent during a phase I trial," Cancer Epidemiology Biomarkers and Prevention, vol. 4, no. 3, pp. 245-251, 1995], обеспечивает приблизительно постоянный уровень лекарственного средства в плазме крови; (3) четырехсуточный интервал без введения лекарственного средства обеспечивает период вымывания, пригодный для ограничения описанного снижения уровня NAC в плазме, наблюдаемого во время длительных лечений.

Композиции, используемые применительно к изобретению
В одном воплощении изобретения предложена фармацевтическая композиция, содержащая N-ацетил-L-цистеин (NAC) для внутривенного введения в дозе от 50 до 150 мг/кг массы тела NAC один раз в сутки в течение 1-3 суток, связанная с ЭКО-лечением.
Один аспект представляет собой фармацевтическую композицию, содержащую NAC для использования в дозе 150 мг/кг в течение 1-3 суток.
Другой аспект представляет собой фармацевтическую композицию, содержащую NAC для применения только в те же самые сутки, что и ЭКО-лечение.
В еще одном воплощении настоящего изобретения композицию, содержащую NAC, вводят перорально в дозе приблизительно 30-45 мг/кг/сутки.
Когда NAC комбинируют с селеном и/или мелатонином, то NAC вводят в дозе 5-45 мг/кг/сутки, селен в форме селенометионина для введения в дозе 0,4-1,2 мкг/кг/сутки и мелатонин для введения в дозе 0,02-0,08 мг/кг/сутки. Медицинский продукт в одном воплощении представляет собой фармацевтическую композицию, содержащую NAC, селен в форме селенометионина и мелатонин.
Также импульсное или прерывистое пероральное введение в течение периода времени три месяца с дозой N-ацетил-L-цистеина, которая составляет от 20 до 90 мг/кг/сутки, в те сутки, когда ее вводят, будет оказывать благоприятное воздействие на успех ЭКО. В этом случае композиция предназначена для непрерывного введения в течение трех месяцев или более, или 3-5 суток подряд с последующими 2-4 сутками приостановки. В другом воплощении фармацевтическая композиция, содержащая N-ацетил-L-цистеин, предназначена для введения в течение 1-3 суток подряд с последующими 1-2 сутками приостановки.
Согласно примерам, описанным в описании изобретения, 15 пациенток лечили при помощи импульсного перорального введения N-ацетил-L-цистеина для применения в ЭКО в дозе 600 мг три раза сутки в течение трех суток подряд с последующими четырьмя сутками приостановки в течение 3 месяцев или более.
Другие возможные режимы введения, такие как следующие ниже, описаны в ЕР 2305238.
В одном воплощении предложена фармацевтическая композиция, содержащая N-ацетил-L-цистеин, для вышеупомянутого использования, где композиция предназначена для введения дозы N-ацетил-L-цистеина, которая составляет от 30 до 60 мг/кг/сутки, в те сутки, когда ее вводят. В другом воплощении фармацевтическая композиция предназначена для введения дозы N-ацетил-L-цистеина, которая составляет от 30 до 45 мг/кг/сутки, в те сутки, когда ее вводят.
В одном воплощении изобретения предложена фармацевтическая композиция, содержащая N-ацетил-L-цистеин, для использования, описанного выше, когда фармацевтическую композицию защищают от света. В другом воплощении фармацевтическая композиция представляет собой водорастворимую таблетку. В еще одном воплощении фармацевтическая композиция содержит натрия гидрокарбонат. В одном воплощении фармацевтическая композиция представляет собой композицию с замедленным высвобождением и/или композицию для защиты желудка.
В одном аспекте изобретения предложен способ лечения млекопитающего, связанный с ЭКО, включающий внутривенное введение фармацевтической композиции, содержащей N-ацетил-L-цистеин (NAC), указанному млекопитающему от 50 до 150 мг/кг массы тела NAC один раз в сутки в течение 1-3 суток совместно с ЭКО-лечением.
Один аспект представляет собой способ, включающий внутривенное введение NAC в дозе 150 мг/кг в течение 1-3 суток.
Другой аспект представляет собой способ, включающий внутривенное введение NAC только в те же самые сутки, что и ЭКО-лечение.