Результат интеллектуальной деятельности: Способ и реагент-индикатор для рН-метрии вагинальной жидкости
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к акушерству и гинекологии к способам и реагентам для рН-метрии вагинальной жидкости и может быть использовано для диагностики дисбиотических и инфекционных процессов во влагалище.
Известен способ измерения вагинального рН (1983 г.), предложенный R. Amsel Бактериальный вагиноз диагностировали на основе 4 критериев: вида выделений, запаха, рН более 4,5 и обнаружения ключевых клеток.
В рекомендациях FDA 2014 года определение рН влагалищной жидкости позиционируется как полезный способ доклинической диагностики. Последняя редакция Европейского руководства сообщества специалистов по заболеваниям передающимся половым путем под эгидой ВОЗ определяет повышение рН влагалищной жидкости одним из четырех основных критериев диагностики бактериального вагиноза.
Золотым стандартом рН метрии является использование ионометра. Считается, что эффективность использования ручного рН метра превосходит бумажные индикаторы, нивелируя отклонения измерений за счет цвета и консистенции вагинальной жидкости (1). Есть альтернативное мнение. Проведя сравнение бумажных, пластиковых индикаторов различных производителей, подтвердили их равную аппаратной рН-метрии достоверность в определении значения Н+. В качестве преимуществ пластиковой полоски названа большая комплаентность применения in vivo и значимость дискретности шага 0,2-0,3-0,5 (2).
Также известно применение несколько видов тестовых прокладок и шпателей. Результаты изучения их диагностической ценности показали, что при использовании встречается достаточно высокий процент как ложноположительных, так и ложноотрицательных результатов. Несмотря на то что данные тест-системы удобны в применении, они имеют много недостатков. На прокладку могут попадать не только вагинальные выделения, но и капельки мочи, выделения желез, что искажает истинные результаты и снижает чувствительность метода (2).
Наиболее близким к предлагаемому является способ определения рН с помощью Кольпо-тест рН (Биосенсор АН, Россия) - от 3,5 до 7,5, с шагом деления 0,2-0,3-0,5 (Регистрационное удостоверение на медицинское изделие №РЗН 2013/1370 от 31 декабря 2013 года). Индикаторные полоски являются высокоточным, простым и доступным средством для определения кислотности влагалища у женщин. Полученные результаты свидетельствуют о высокой диагностической эффективности Кольпо-теста рН (чувствительность 90% и специфичность 85%) при исследовании влагалищной жидкости в случаях бактериального вагиноза. Недостатком существующего метода является использование дополнительных средств диагностики, что удорожает и усложняет процесс, необходимость переноса жидкости из влагалища на индикатор, что не всегда возможно вследствие индивидуальных различий в консистенции вагинального секрета.
Для экспрессного (с погрешностью ~ ±0,5-1) определения рН неизвестного раствора, применяют т.н. универсальные индикаторы. Универсальные индикаторы представляют собой смеси индивидуальных индикаторов, с различными, но примыкающими друг к другу зонами перехода окраски.
Например, известен универсальный индикатор (по Богену) следующего состава: фенолфталеин (0,2 г), метиловый красный (0,4 г), диметиламинобензол (0,6 г), бромтимоловый синий (0,8 г), тимоловый синий (1,0 г), спирт этиловый (1 л), гидроксид натрия (до появления желтой окраски).
Изменение окраски описанного индикатора представлено в таблице

Известен коммерческий жидкий универсальный индикатор UNISOL 410 (заявленный диапазон работы 4-10). Согласно паспорту безопасности (MSDS) в состав индикатора входит: Этанол - 90-98%, Фенолфталеин -<0,1%, Химические индикаторы - 0,01-0,1%.
Представленный образец - жидкий универсальный индикатор Munktell Visual Color Test имеет диапазон работы 4-8.
Существует универсальный индикатор ЗИВ-1 (водно-спиртовой), состав и способ приготовления которого описаны в ГОСТ 4919.1-77, диапазон работы 1-10.
Новый технический результат - упрощение способа при сохранении точности и информативности, а также разработка более доступного и удобного для использования индикатора для рН-метрии вагинальной жидкости.
Для достижения технического результата в способе определения рН вагинальной жидкости, путем забора биоматериала вагинальной жидкости и формирования контактного слоя с реагентом, контактный слой получают смешиванием образца биоматериала с предварительно размещенной каплей реагента-индикатора на предметном стекле, при этом определяют рН путем сравнения окраски слоя материала с цветом стандартной шкалы.
Реагент-индикатор включает следующие компоненты, вес.ч.:
|
Также в качестве растворителя можно использовать изопропанол или н-пропанол.
Способ осуществляют следующим образом.
Каплю реагента-индикатора наносят на предметное стекло, приготовленное для забора материала для бактериоскопии. Биоматериал из влагалища забирают универсальным зондом. При нанесении на стекло слоя биологического материала и смешивания его с каплей индикатора-реагента он приобретают окраску, соответствующую значению рН на стандартной цветовой шкале.
Подбор компонентов и их количественного соотношения для создания реагента-индикатора производили эмпирическим способом.
Задачей исследований явилась разработка жидкого универсального индикатора рН для диапазона 3.0-8.0, при этом:
- индикатор должен позволять гарантированно идентифицировать следующие точки рН: 3,0-3,5- 4,5-5,0-6,0-7,0-8,0->8,0;
- изменение цвета в течение не более 1 минуты;
- стабильность окрашивания в течение не менее 30 минут (при высыхании);
- адекватность оценки рН вне зависимости от примесей слизи, мицелия гриба, лейкоцитарной массы;
- отсутствие влияния на последующую цитологическую окраску по Грамму (Карболовый раствор генциана фиолетового, Раствор Люголя, водный раствор фуксина Циля);
- отсутствие токсического влияния на медицинский, персонал при работе на открытом столе в условиях смотровой;
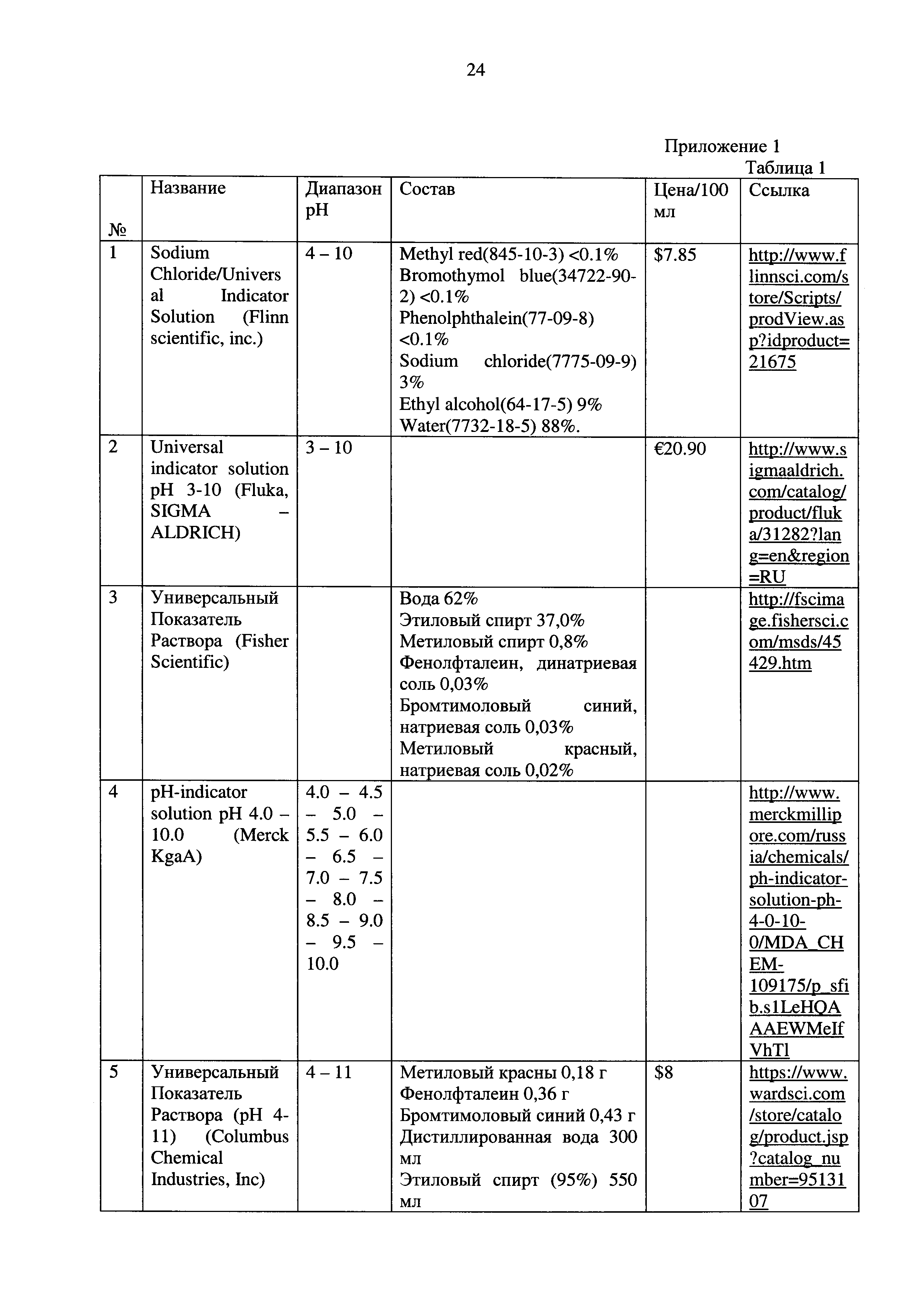
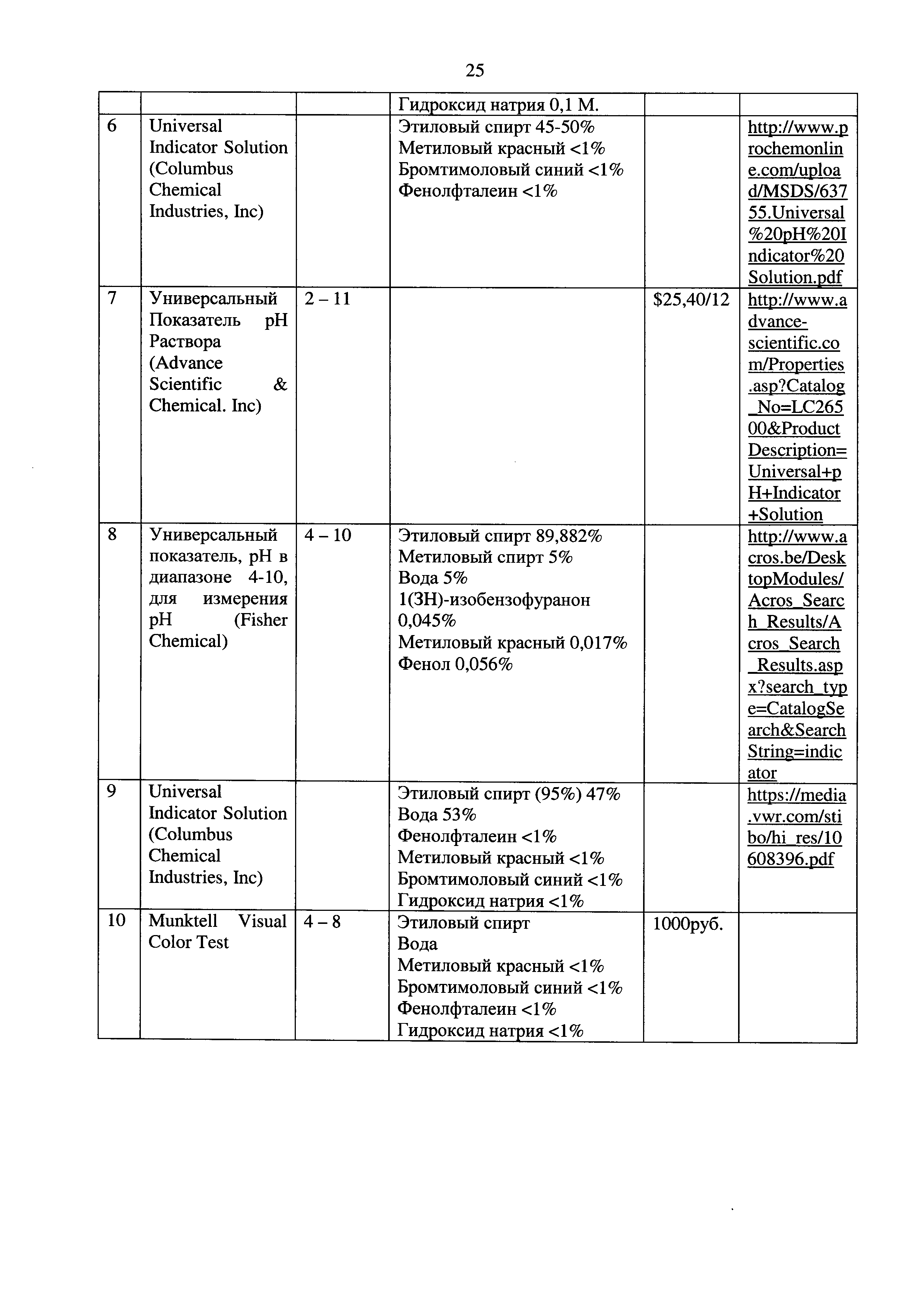
Было рассмотрено 9 аналогов универсального индикатора (Табл. 1 Приложения). В 6 из них в составе имеется этиловый спирт с процентным содержанием не менее 40% и метиловый спирт с процентным содержанием около 5-6%. Содержание воды во всех аналогах более 50%.
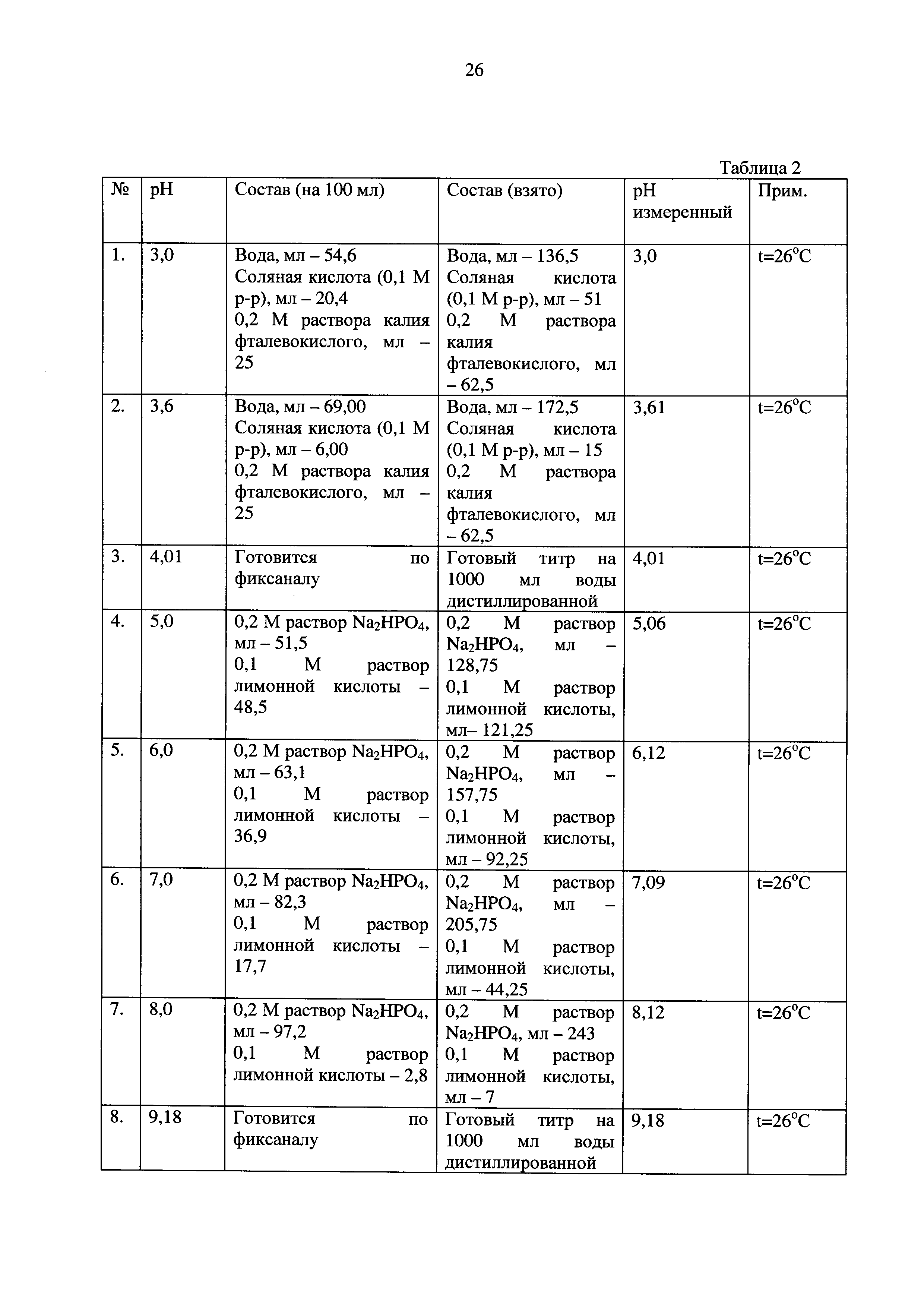
Были приготовлены буферные растворы (Табл. 2 Приложения) согласно ГОСТ 4919.2-77 и растворы индивидуальных индикаторов (Табл. 3 Приложения). Контроль рН осуществлялся с помощью рН-метра рН-150МИ ТУ 4215-051-89650280-2009 (погрешность определения рН 0,05).
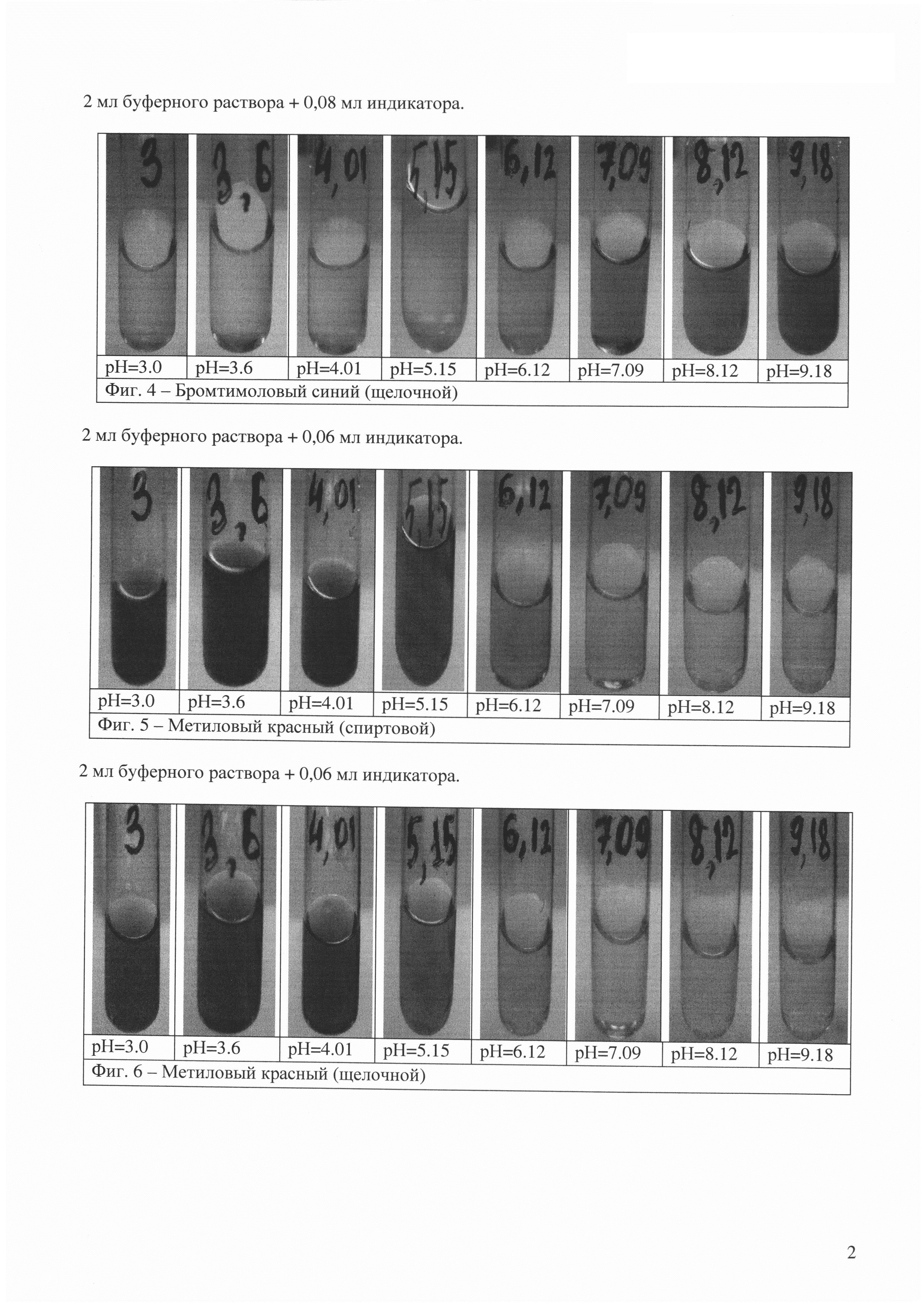
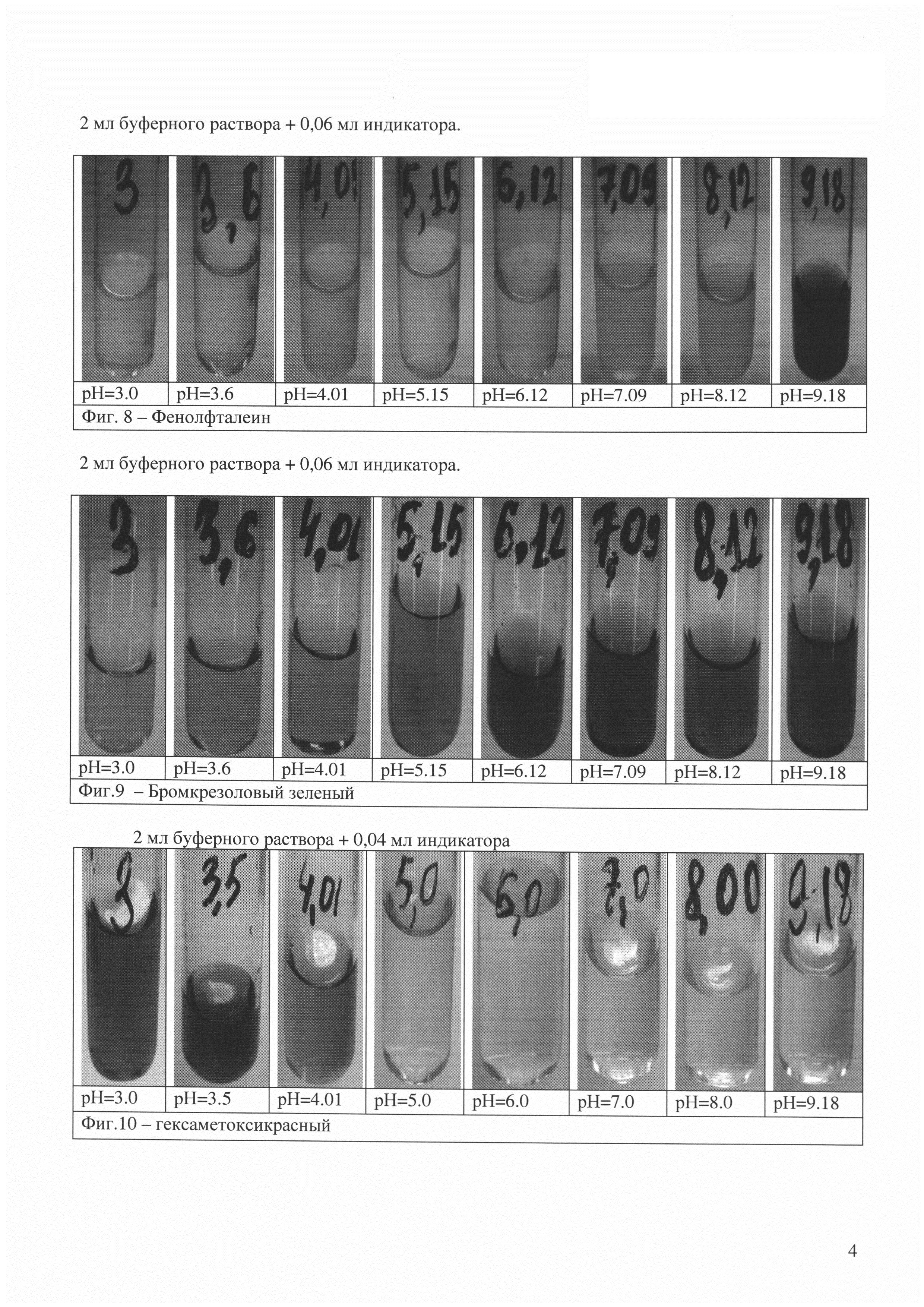
Затем было проведено тестирование растворов индивидуальных индикаторов и аналога (Фиг. 1-13).
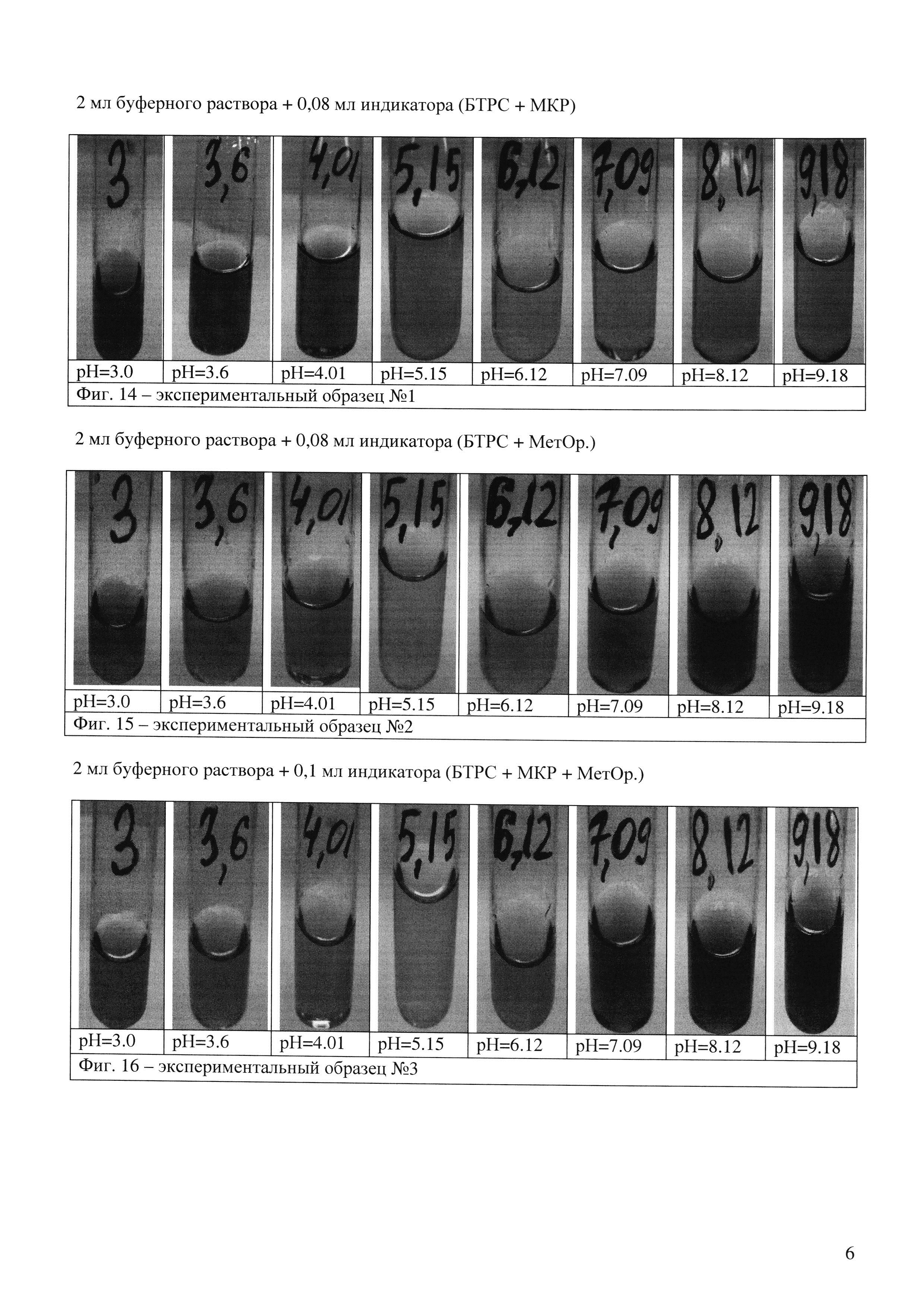
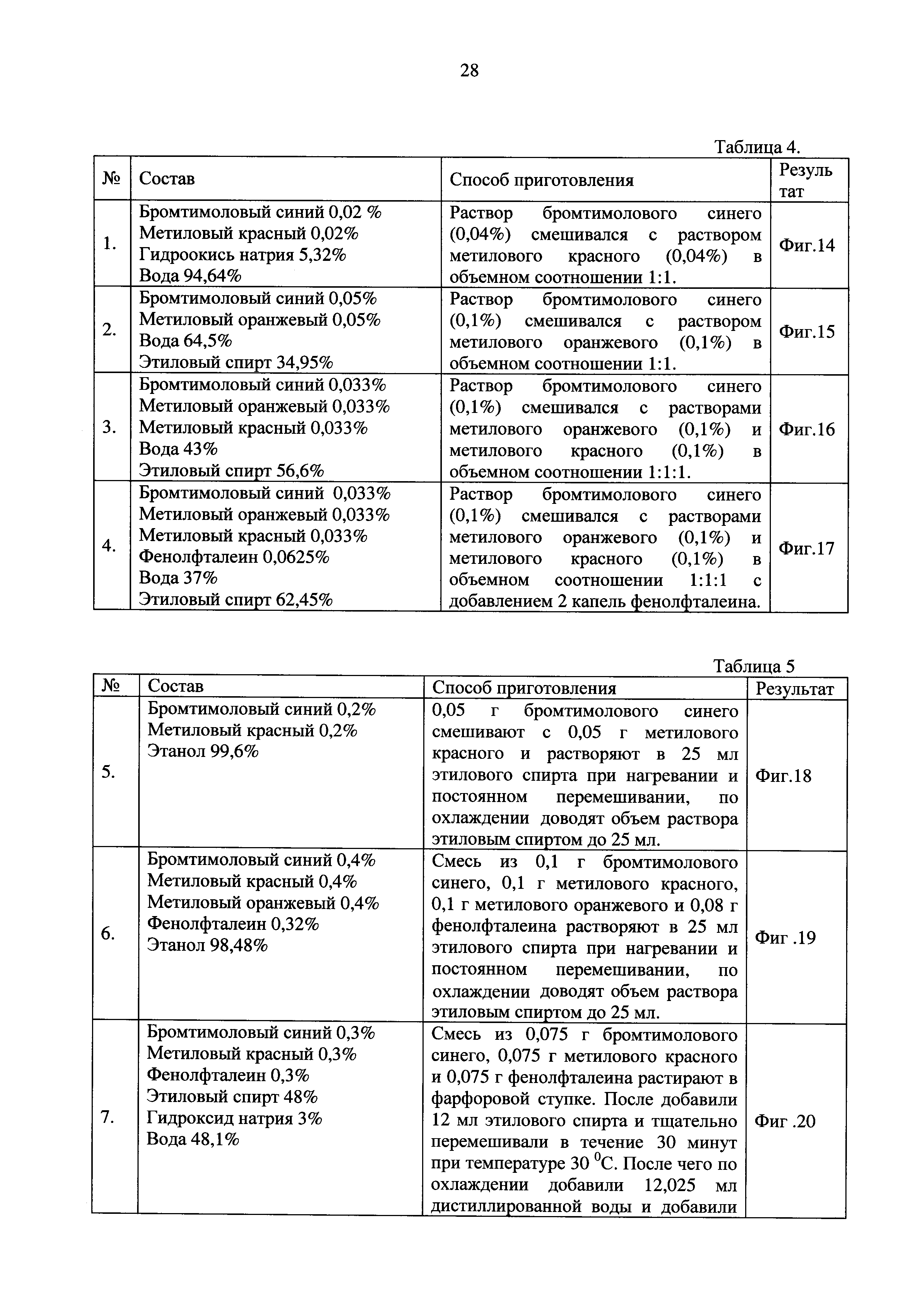
Для приготовления экспериментальных образцов №№1-4 использовались растворы индикаторов приведенных в Таблице 3. Состав экспериментальных образцов универсальных индикаторов приведен Таблице 4.
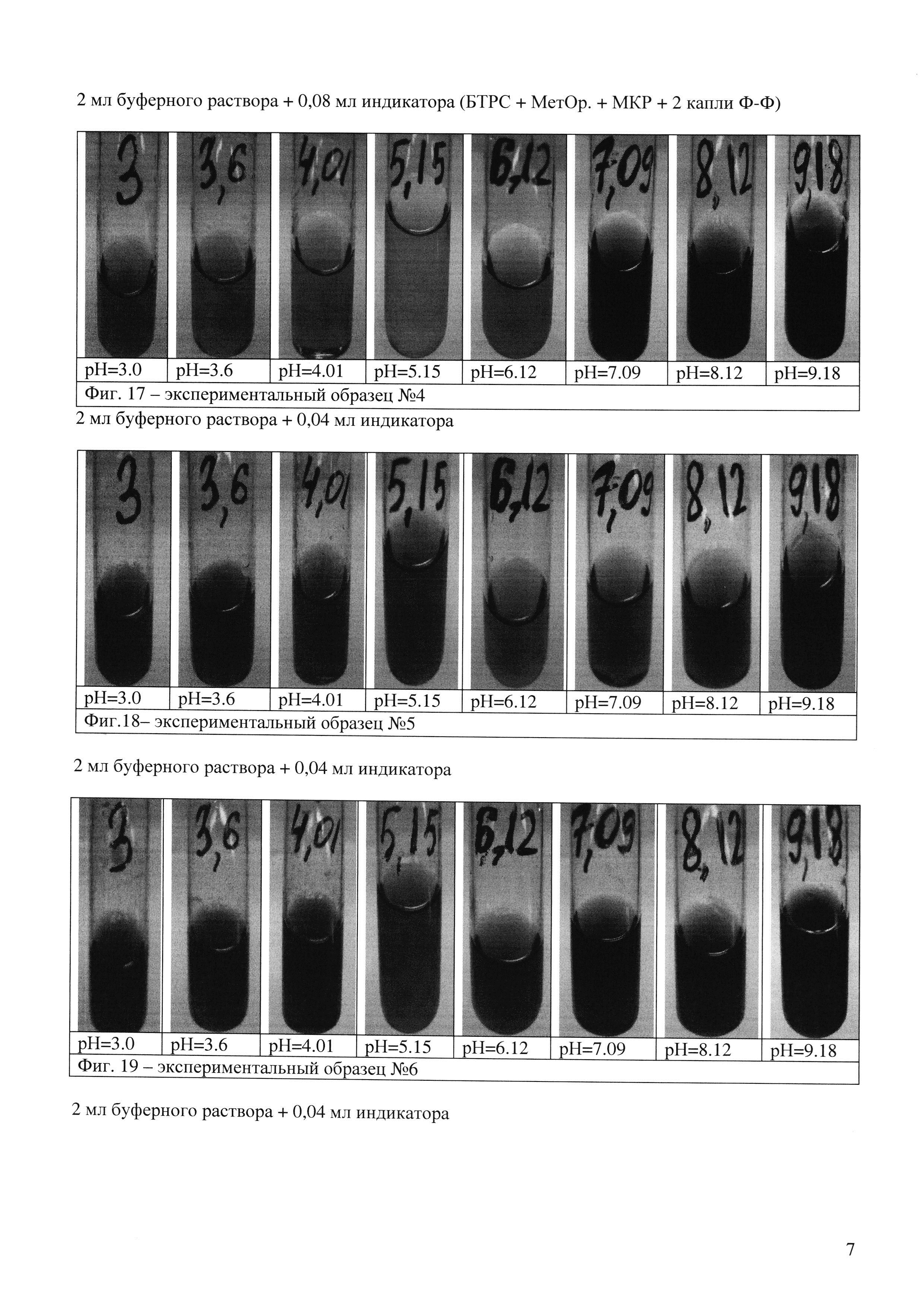
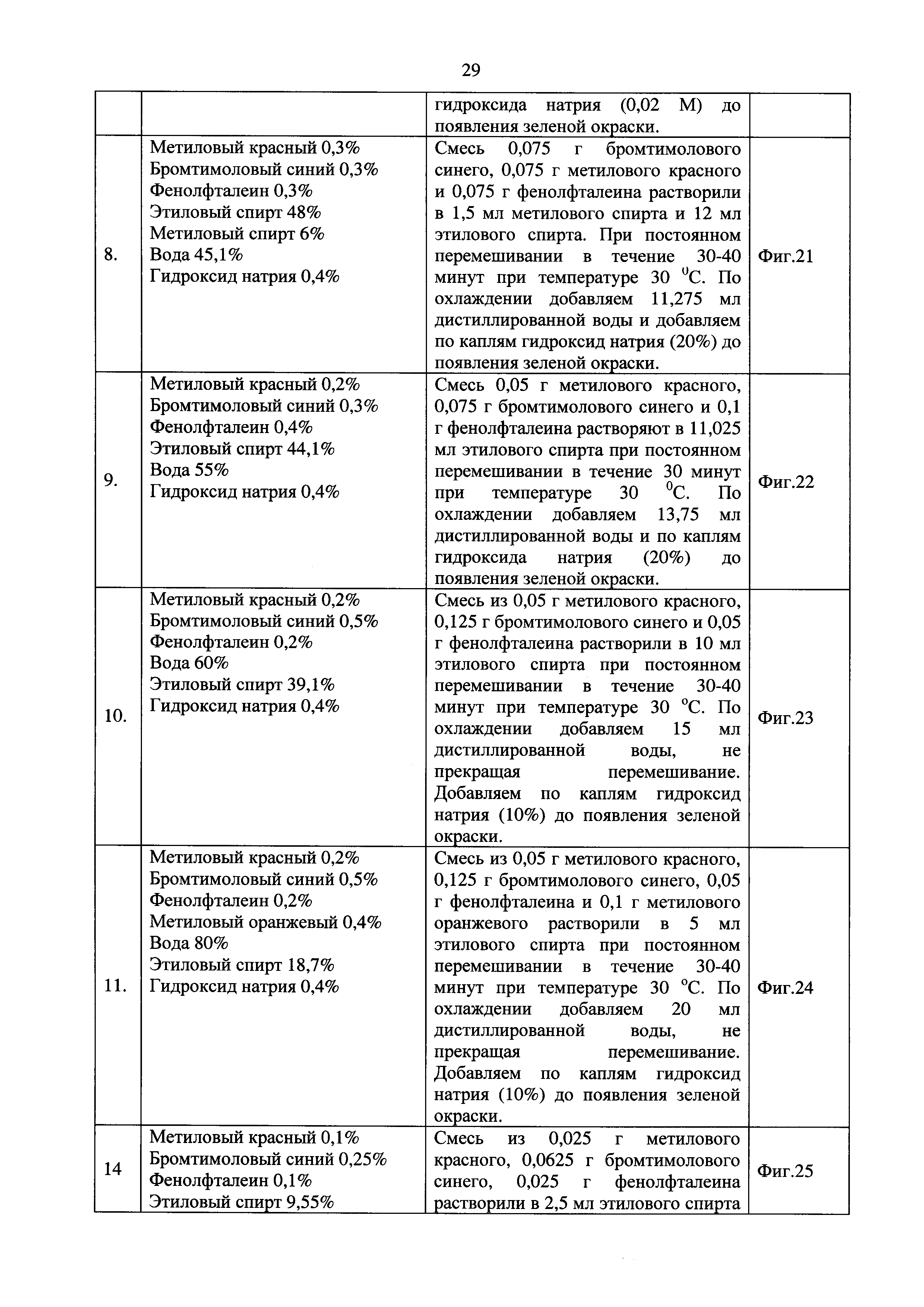
Вывод по образцам №1-4 (фиг. 14, 15, 16, 17): данные образцы имели низкую концентрацию индикаторов в своем составе, посредством чего имели ненасыщенную окраску. При этом в экспериментальном образце №1 был виден переход между точками 4,01-5,15-6,12-7,09. Предположили, что при увеличении концентрации индикаторов в составе раствора переход между точками 4,01-5,15-6,12-7,09 будет более ярким и проявятся переходы между остальными точками. В образце состава №4 увеличили концентрацию фенолфталеина, ожидая получить более четкое разделение между точками 3-3,6-4,0 и 7,09-8,12-9,18.
В результате данных предположений получили образцы №5 и №6. Для приготовления экспериментальных образцов №5 и №6 использовались сухие препараты индикаторов в соотношении (Таблица 5,6 Приложения).
Вывод по образцам №5-6 (фиг. 18, 19): данные образцы готовились с учетом того, что метиловый красный хуже всего растворим в воде, по причине чего все образцы были приготовлены с большим содержанием этанола, образец №5 имеет яркие почти не различимые цвета в точках 3,0-3,6-4,01-5,15 и 7,09-8,12-9,18. что не удовлетворило поставленным целям. Появилось предположение, что при уменьшении концентрации этанола в составе раствора насыщенность индикатора не изменится, но повысится различимость точек. В образце №6 цвет получился грязным и точки малоразличимы. Принято решение уменьшить концентрацию этанола.
В образцы №7-8 добавляем гидроксид натрия, для придания зеленого цвета раствору индикатора, добавляя воду, уменьшаем концентрацию этанола.
Вывод по образцам №7-8 (фиг. 20, 21): по приготовлению данного образца можно сделать вывод, что щелочь можно добавлять концентрированную, несколько капель, для придания индикатору темно-зеленой окраски. Цвета стали более различимыми и светлыми. Но точки 3-3,6-4,01. так и невозможно различить. Экспериментальный образец №8 не дал возможность различить точки 3-3,6-4,01. при этом имеет насыщенный цвет, но не четкое разделение цветов в точках 7,09-8,12-9,18. Принято решение уменьшить концентрацию метилового красного и убрать из состава метанол.
Вывод по образцу №9 (фиг. 22): уменьшение концентрации метилового красного и увеличении фенолфталеина никак не повлияло на цвет. Решено попробовать увеличить концентрацию бромтимолового синего и сровнять фенолфталеина и метилового красного. Так же уменьшить концентрацию гидроксида натрия вдвое.
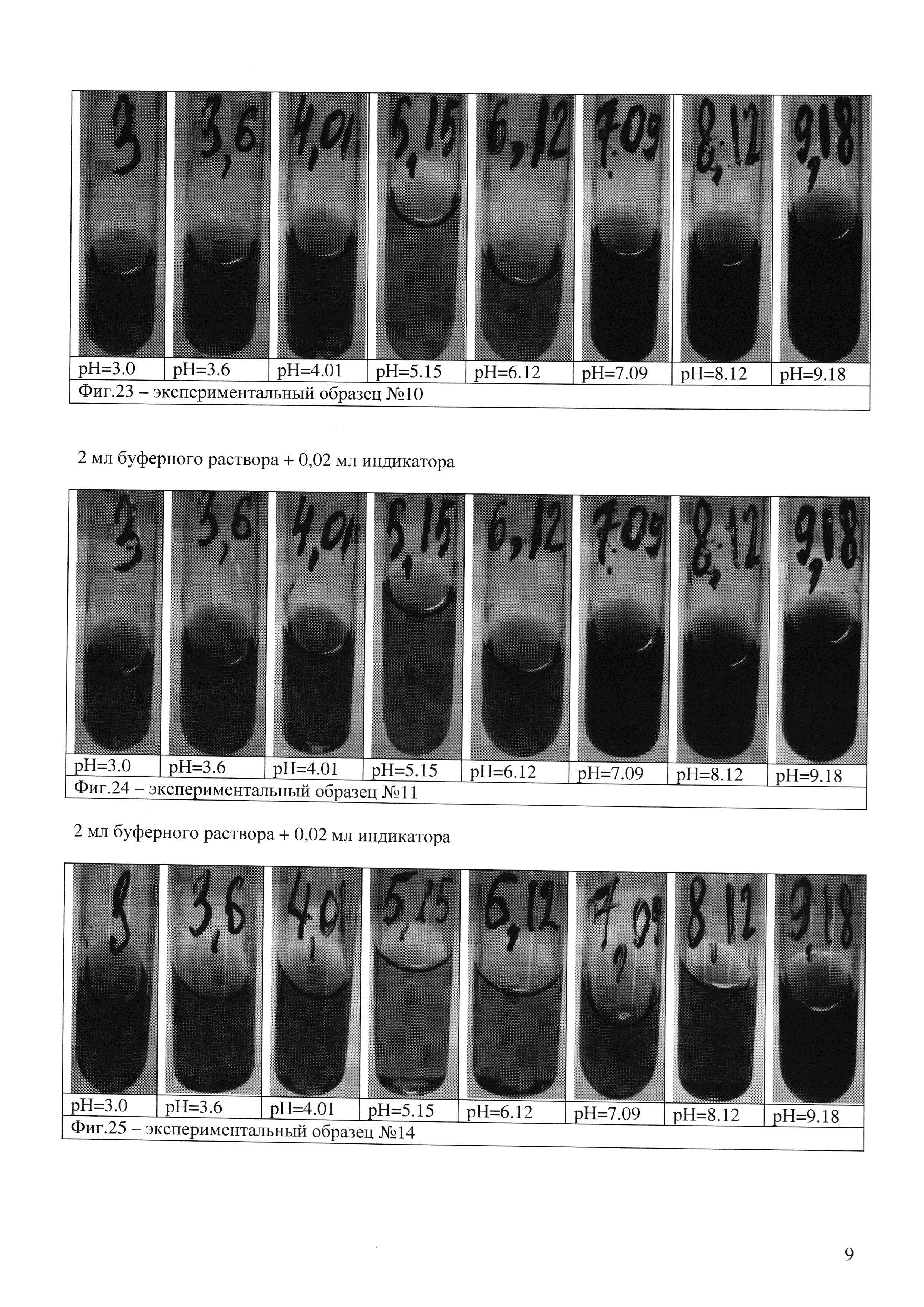
Вывод по образцу №10 (фиг. 23): данный образец дает достаточно точное разделение всех точек, кроме 3-3,6-4,01. Имеет насыщенный цвет и обретает его после добавления всего 1 капли индикатора. Выдвинуто предположение, что для того чтобы различить точки 3-3,6-4,01, необходимо добавить бромкрезоловый зеленый.
Вывод по образцам с добавлением бромкрезолового зеленого: данные образцы не дали ожидаемых результатов в точках 3.0-3,6-4,01. Различия цветов не наблюдались, плюс была нарушена расцветка в остальных точках.
Вывод по образцу №11 (фиг. 24): образец с добавлением метилового оранжевого не дал большие различия в цвете в точках 3 - 4,01, но все цвета очень темные и не дают остальных точек. Индикаторы растворились не до конца, возможно на это повлияло большое количество воды (80%). Возможно, добавление меньшего количества метилового оранжевого даст различие в точках 3-4,01 и не повлияет на остальные точки. При этом концентрация метилового оранжевого должна быть не на много больше метилового красного и на много меньше бромтимолового синего.
Добавление метилового оранжевого не дало положительных результатов.
В процессе работы по техническим и экономическим расчетам, было принято решение уменьшить концентрацию спирта в образце №10, но в связи с тем, что метиловый красный не растворяется в дистиллированной воде, приготовили 2 экспериментальных образца с концентрациями спирта 19,1% и 4,1%. экспериментальный образец №12 с концентрацией 4,1% дал отрицательный результат, а экспериментальный образец №13 с концентрацией 19,1% не соответствовал по цветовым характеристикам аналогу. Для соответствия аналогу экспериментальный образец №13 был разбавлен дистиллированной водой в 2 раза и протестирован на буферных растворах. Полученный экспериментальный образец №14 соответствовал по всем характеристикам своему аналогу.
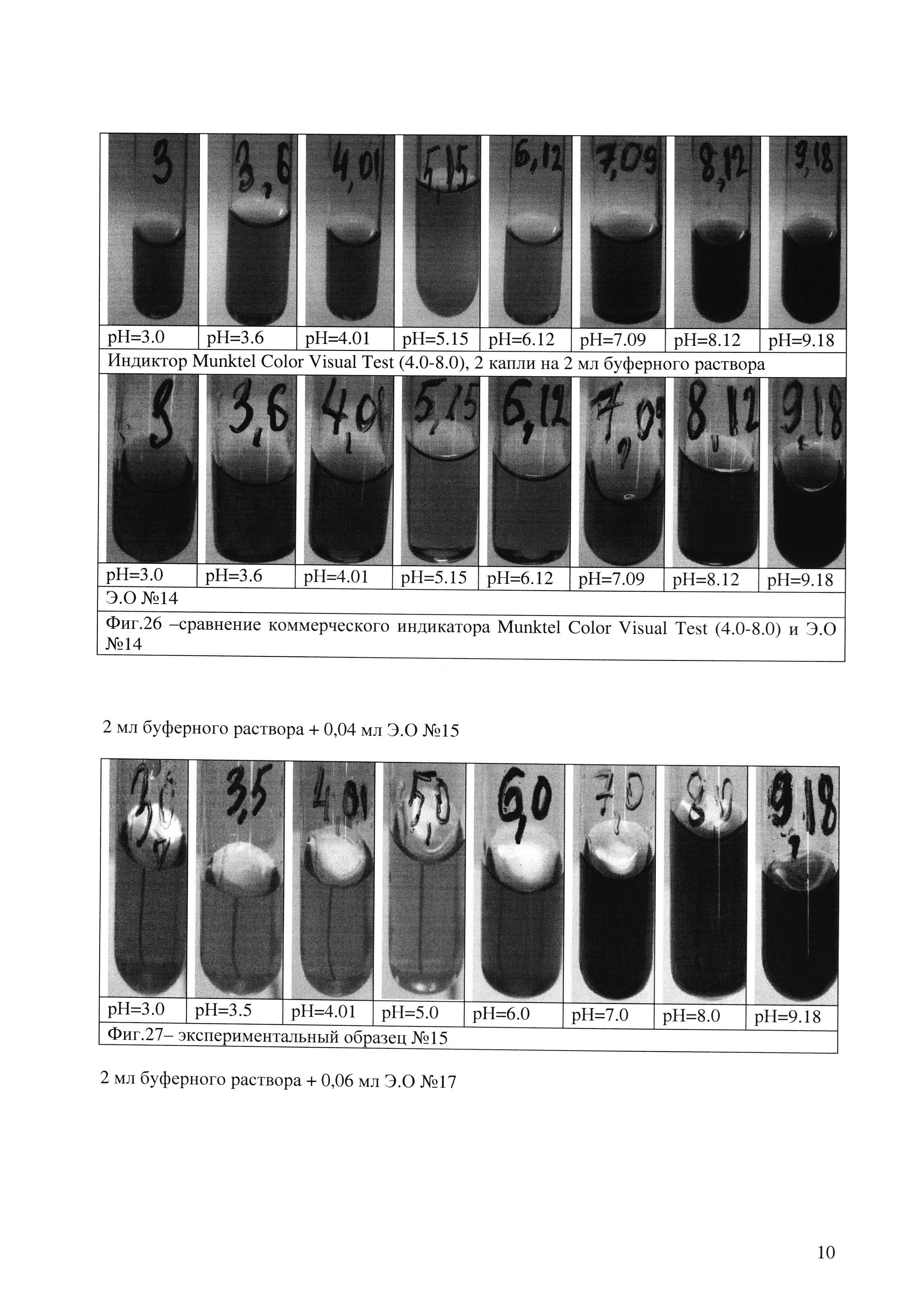
Исходя из имеющегося набора индикаторов метиловый красный, бромтимоловый синий и фенолфталеин был разработан универсальный индикатор, аналогичный по целевым характеристикам коммерческому индикатору Munktell Visual Color Test 4.0-8.0. Сравнение экспериментального образца №14 (Фиг. 25) и коммерческого индикатора Munktell Visual Color Test (Фиг. 26).
Для разделения точек 3 и 3.5 было предложено попробовать 4 индикатора: ализариновый красный С (1,2-диоксиантрахинон сульфокислоты натриевая соль), с интервалом рН перехода окраски 3,6 - 5,2;
гексаметоксикрасный (гексаметокситрифенилкарбинол), с интервалом рН перехода окраски 2,8 - 5,0;
диметиловый желтый (метиловый желтый), с интервалом рН перехода 3,0 - 4,0 и
2,4-динитрофенол (альфа-динитрофенол), с интервалом рН перехода 2,8 - 4,4.
Сравнительный анализ клинического применения индикаторов ЭО-14 и Munktell.
На базе Центра Перинатального Здоровья (ЦПЗ) г. Томск, в период с 13 по 23 сентября 2013 г., врачом Юрьевым С.Ю. выполнено 50 исследований с параллельным использованием 2-х индикаторов. Были сделаны следующие выводы:
- жидкие индикаторы удобны в практическом использовании на рабочем месте врача;
- индикаторы идентичны по исходному цвету и консистенции;
- скорость, цвет и интенсивность окрашивания у обоих индикаторов при контакте с биологическими средами с различной кислотностью идентична;
- индикаторы в равной степени не влияют на последующую окраску мазка по Граму, метиленовой синью.
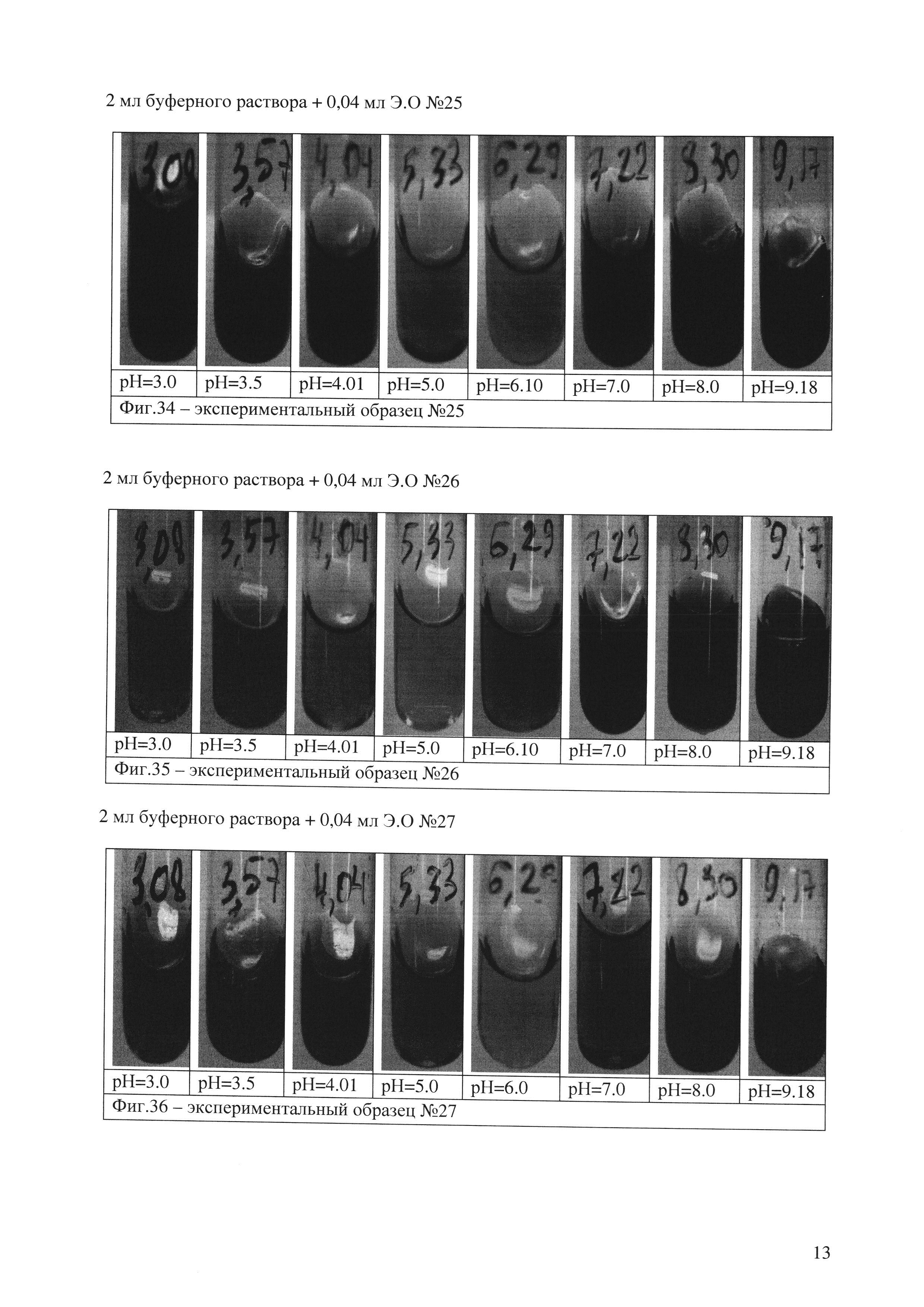
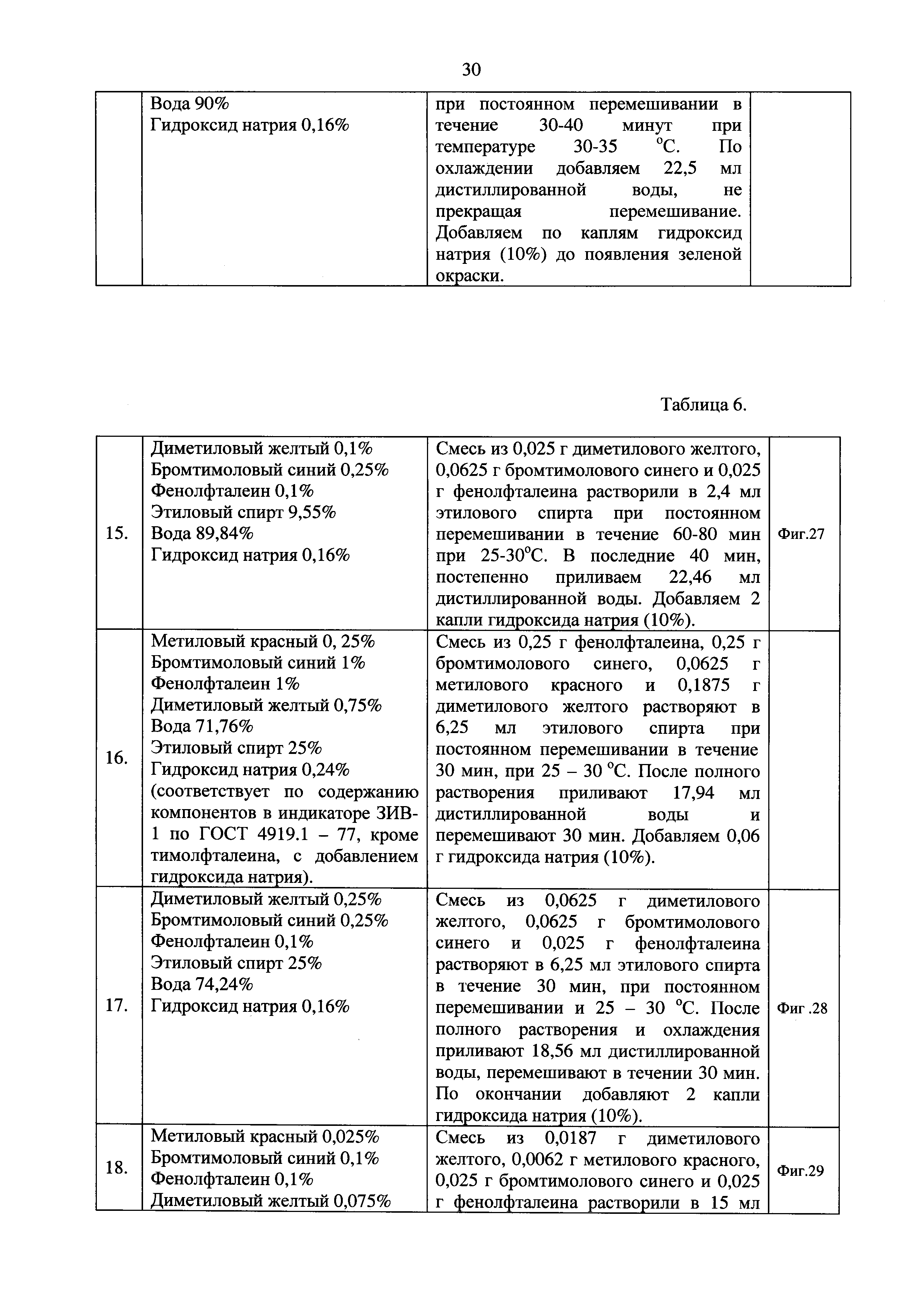
Недостатки: необходимы точки 3,0; 3,5; 4,0; 4,5; 5,0; 6,0; 7,0; 8,0. Опираясь на состав универсального индикатора ЗИВ-1 и полученные результаты тестирования индивидуальных индикаторов, было принято решение приготовить экспериментальные образцы следующего состава, приведенные в таблице 6. Сравнение образцов Э.О №20 и Э.О №25, состав образцов идентичен.
Вывод по образцу Э.О №15(Фиг. 27): данный экспериментальный образец хорошо растворился в процессе приготовления. Имеет точные различия цвета в точках 5,0 - 6,0 -7,0 - 8,0 - 9,18. цвета чистые и насыщенные. В точках 3,0 - 3,5 - 4,01, различия цветов выражены не так ярко. На основании состава данного образца и фото индивидуального индикатора диметилового желтого, принято решение о работе с составом Э.О №15, а именно формирование состава Э.О №17.
Вывод по образцу Э.О №16: данный образец хорошо растворился в процессе приготовления, но через сутки выпал в осадок. Э.О №16 не дал ожидаемого результата в плане разделения цветов и из-за осадка является не пригодным для эксперимента. Данный экспериментальный образец не содержал достаточного количества спирта. На основании Э.О №16 и универсального индикатора ЗИВ - 1 (ГОСТ 4919.1 - 77), был подобран состав Э.О №18(Фиг. 29).
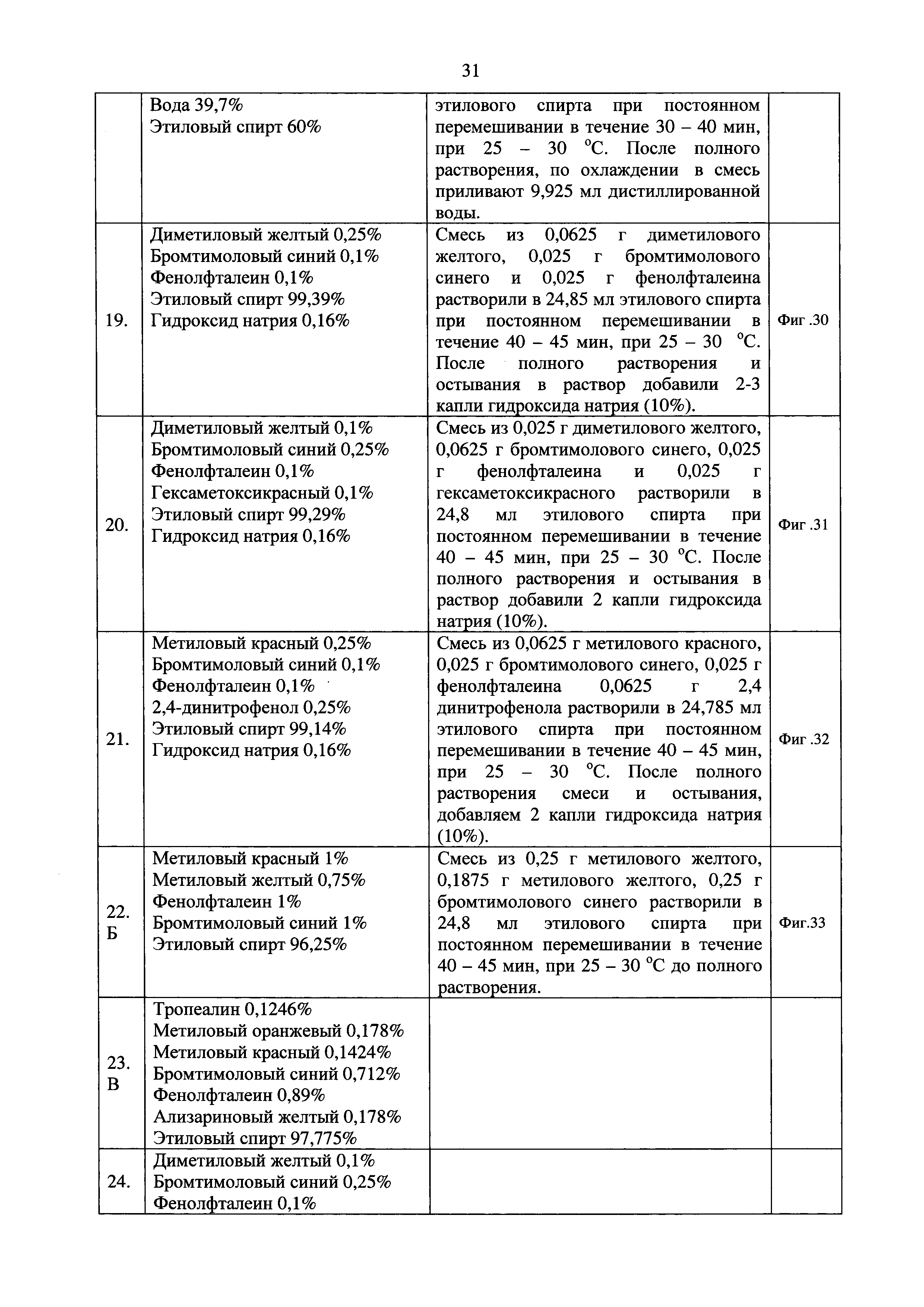
Вывод по образцу Э.О №17(Фиг. 28): опираясь на данные по образцу, принято решение приготовить спиртовой раствор, не содержащий воды и уменьшить концентрацию бромтимолового синего, данному составу соответствует образец Э.О №19(Фиг. 30).
Описание задачи эксперимента по образцам:
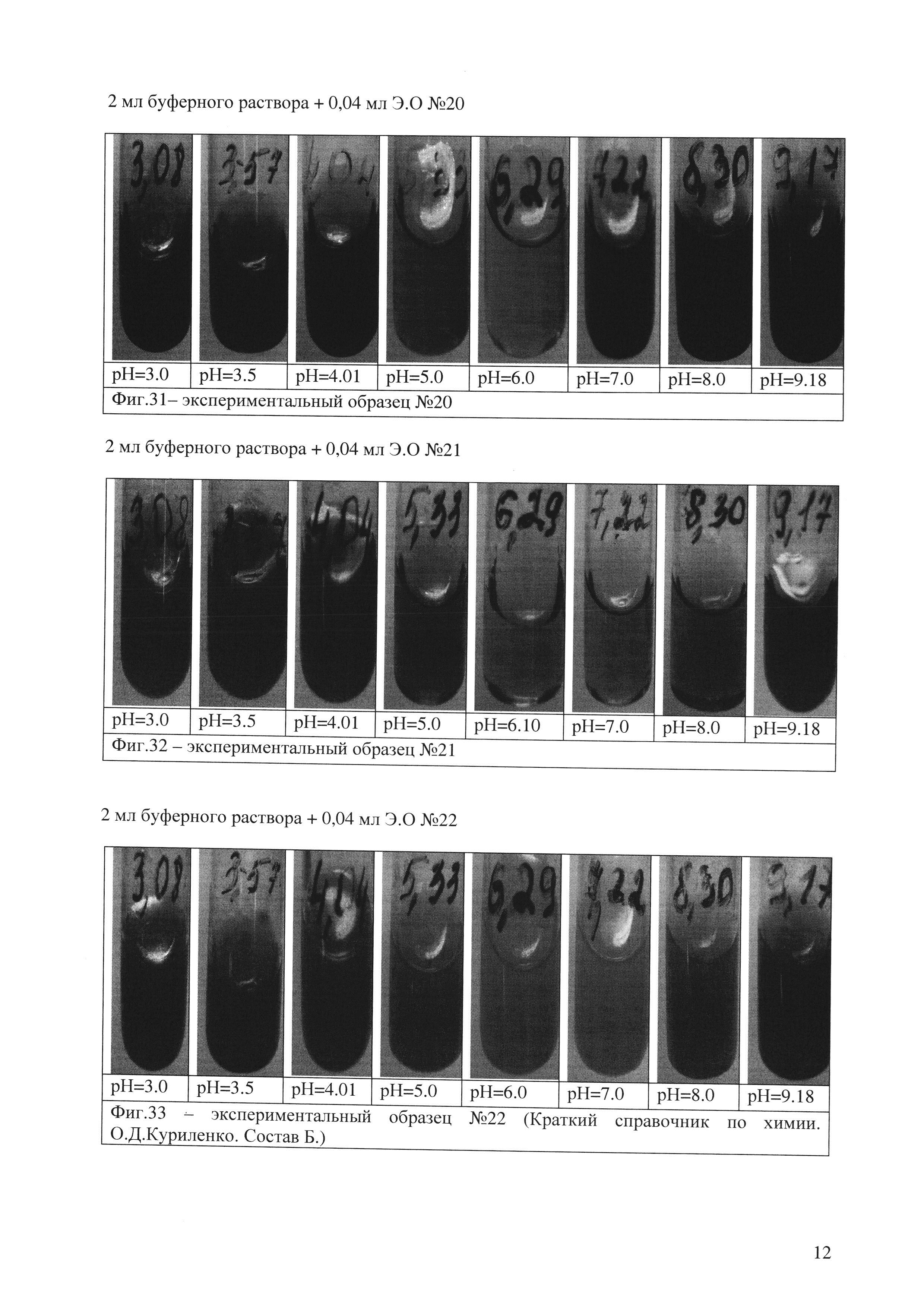
Э.О №20 (Фиг. 31): принято решение добавить в состав образца Э.О №15 гексаметоксикрасный, для различия в точках 3,0 - 3,5 - 4,01.
Э.О №21(Фиг. 32): в состав Э.О №14 решено добавить 2,4-динитрофенол для проверки индикатора в зонах кислой среды, 3,0 - 3,5 - 4,01.
Э.О №22(Фиг. 33): имеет состав, близкий к Э.О №15,отличия заключаются в содержании воды и компонентов. Состав взяли из краткого справочника по химии, О.Д. Куриленко. Состав Б.
Э.О №23: данный образец в составе имеет тропеалин с областью определения рН среды от 1,4 - 3,2, а также ализариновый красный, чтобы определить дают ли индикатора с рН выходящей за пределы 9, фон на точках от 3,0 до 9,18. Состав взяли из краткого справочника по химии, О.Д. Куриленко. Состав В.
Описание задачи по образцам Э.О №24-25: образец Э.О №24 имеет состав соответствующий образцу Э.О №15 с добавлением гексаметоксикрасного. В свою очередь, образец Э.О №25 (фиг. 34) имеет состав, соответствующий образцу Э.О №15 с добавлением гексаметоксикрасного, но приготовленный на спиртовой основе (не содержит воду).
Цель: получить четкий переход цвета в диапазоне рН 3-8 для получения универсального индикатора. Задачи:
1. Приготовить буферные растворы с рН 3 4 5 6 7 8.
2. Подобрать индикаторы с контрастным переходом цвета в диапазоне рН 3-4, 4-5, 5-6, 6-7, 7-8.
3. Подобрать концентрации индикаторов для раствора универсального индикатора. Повторение эксперимента по созданию экспериментального образца №14
Приготовление ЭО№14: 
Вывод: точки 3 и 4 не различимы.
Для создания рецептуры универсального индикатора было принято решение использовать 0,1% спиртовые растворы индикаторов, приготовленных по ГОСТ и далее модифицировать этот состав для разделения точек 3,0 4,0 5,0 6,0 7,0 8,0.
Приготовление буферов проводилось по ГОСТ- 4919-1-77.
Получены буферные растворы со значением 3,0 4,01 5,02 6,0 7,0 8,0.
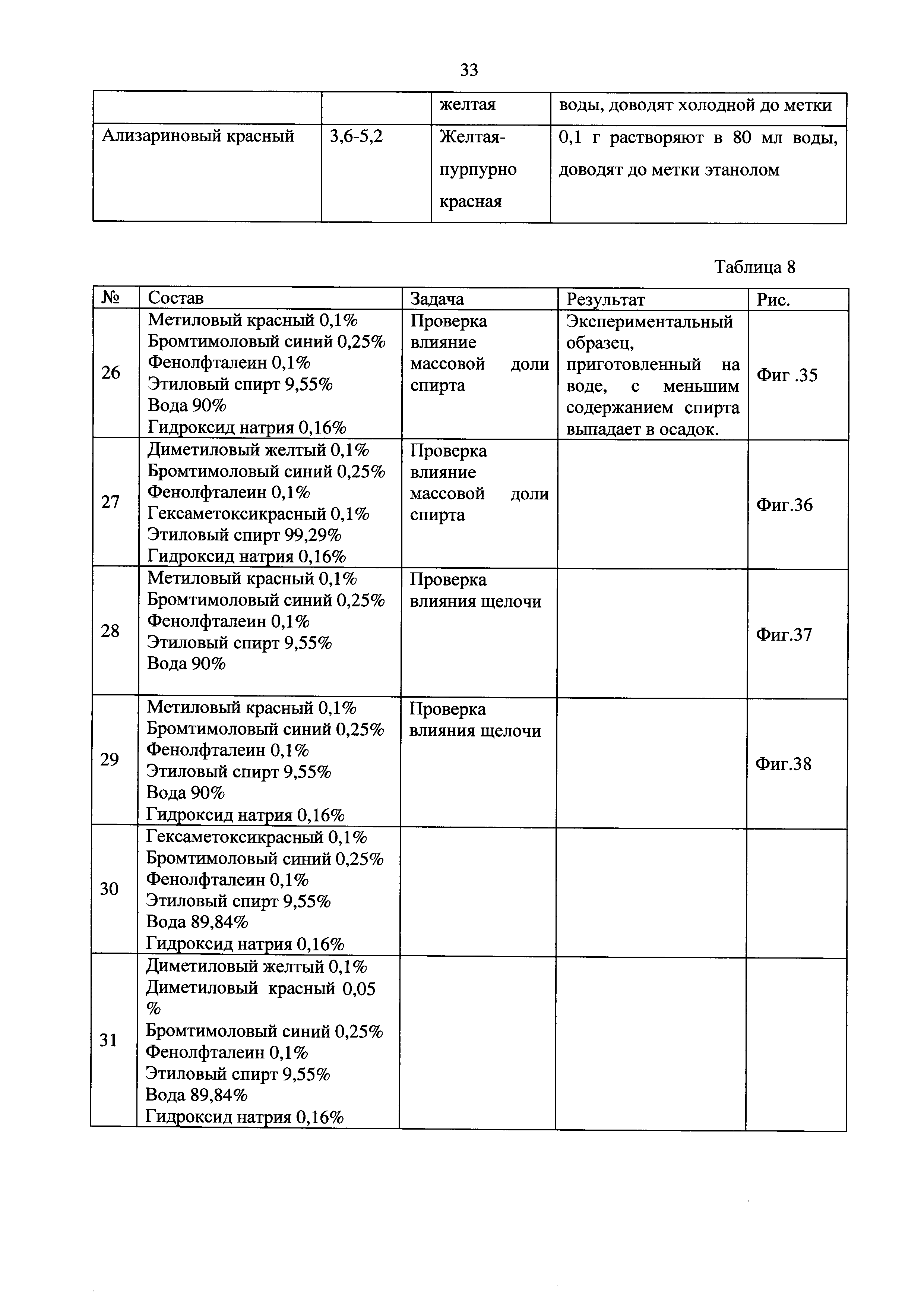
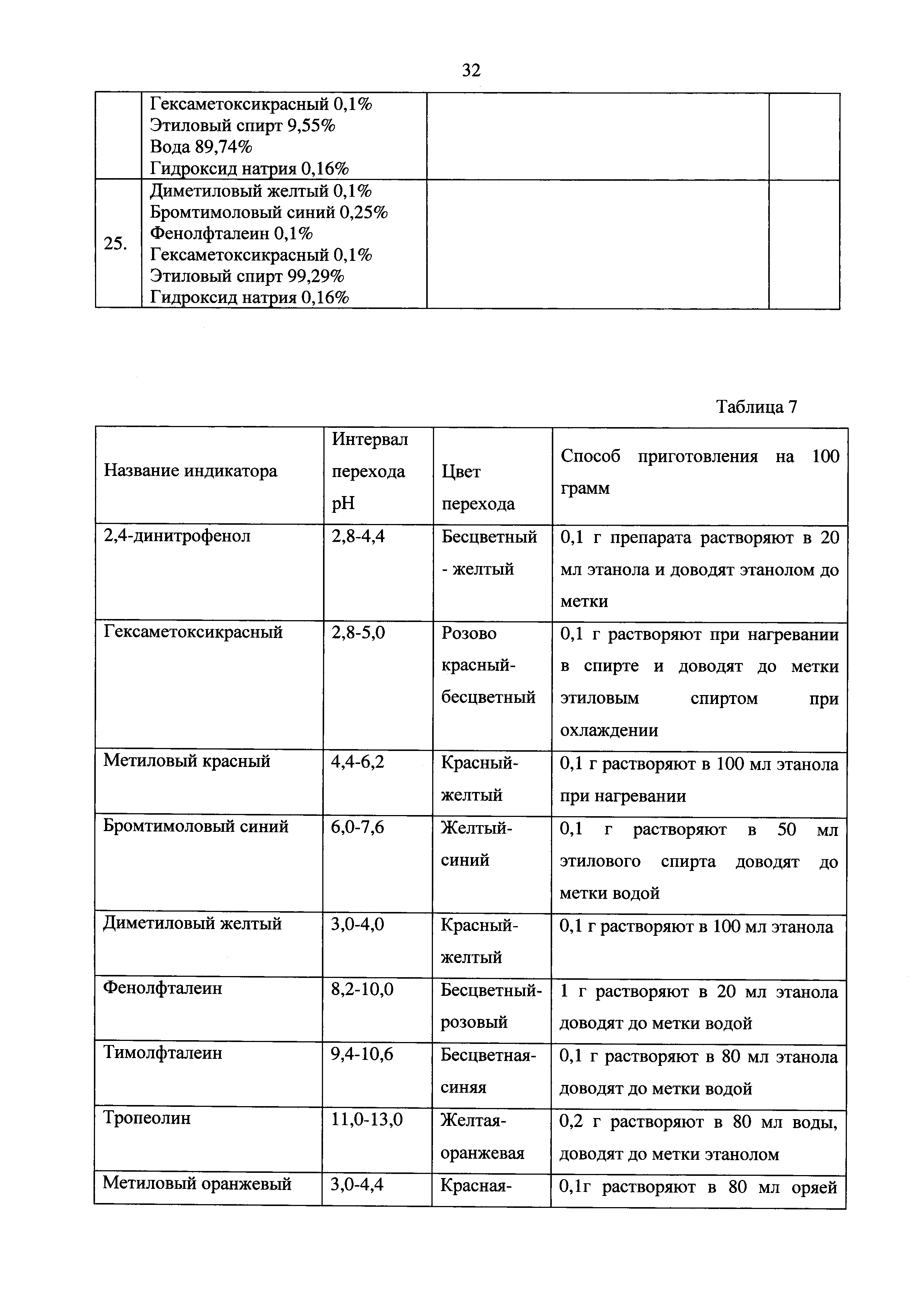
Для работы были выбраны индикаторы, указанные в Таблице 7 Приложения. В таблице 8 приведены составы индикаторов №№26, 27, 28, 30, 31(Фиг. 35, 36, 37, 38, 39).
Опыт 1. (индикатор 28)(фиг. 37)
Опыт с контрольным индикатором ЗИВ 1.
Согласно плану был приготовлен состав, соответствующий индикатору ЗИВ 1 (по методике ГОСТ 4919 1-77), но без добавки тимолфталеина, так как он работает в более щелочной области рН (9,4-10,6) и его исходный цвет не влияет на окраску индикатора. Состав индикатора №28
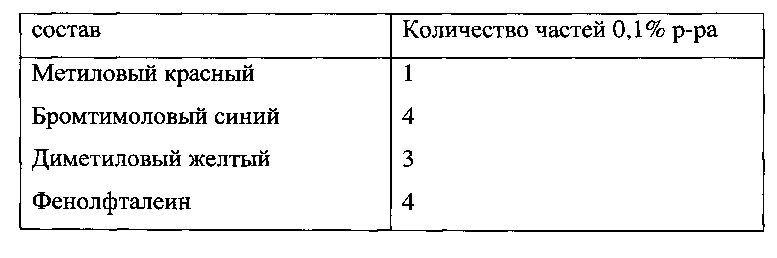
Выводы:
Данный индикатор не дает четкого разделения точек 3,0-4,0 и точки 4,0-5,0 при увеличении концентрации индикатора будут сливаться. Также будет не заметно различие в точках 3 и 4.
Опыт 2. (Индикатор 29)
За основу индикатора №29 был взят ЗИВ 1. Принято решение использовать индикаторы в следующих частях:
Состав индикатора №29

В результате установлено, что у данного индикатора нет четкого перехода в области рН 3-4 и 7-8.
Вывод: Попробовать добавить гексаметоксикрасный и 2,4-динитрофенол для придания точке 3 более розовой окраски.
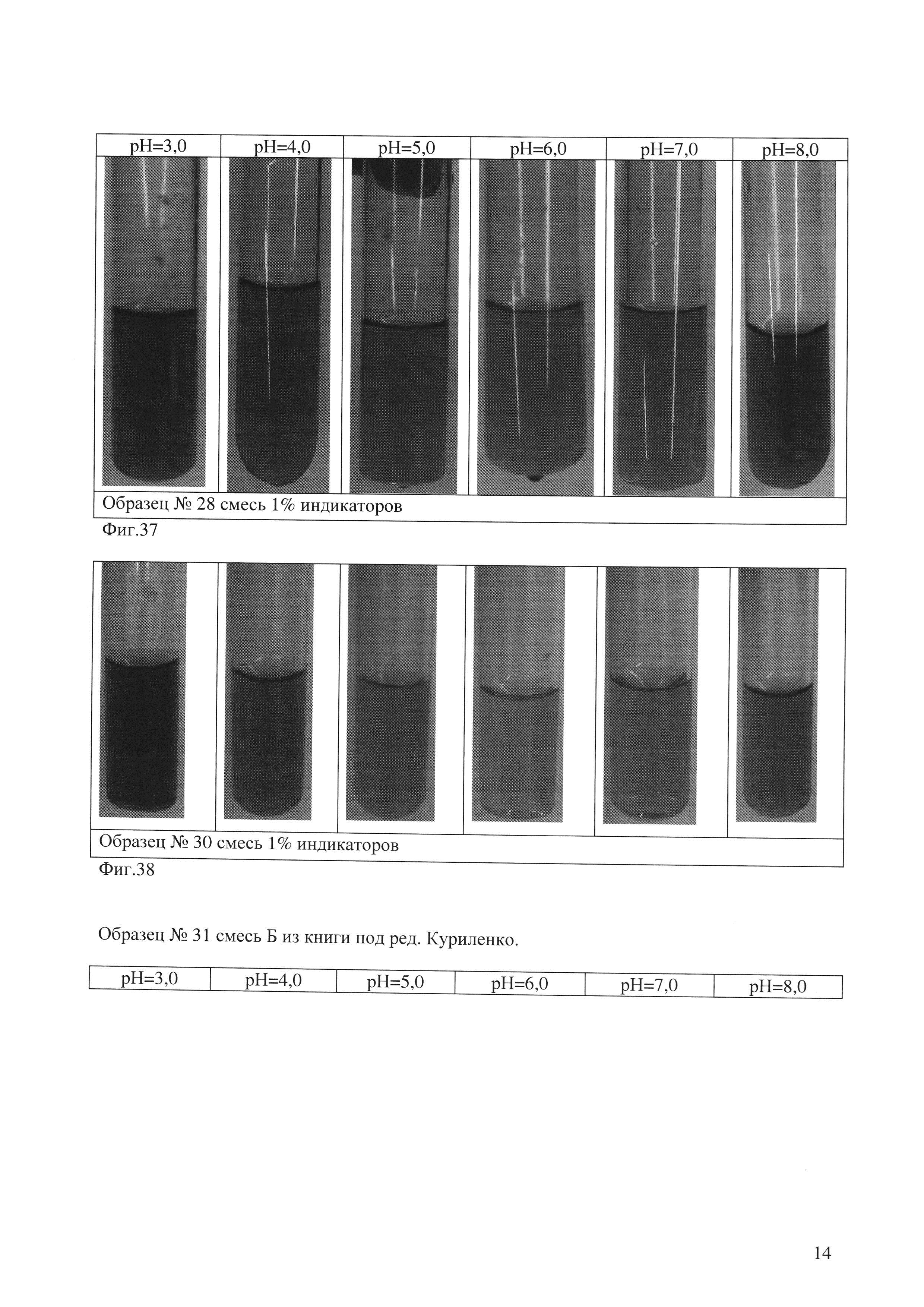
Опыт 3. (индикатор 30) (Фиг.38) Данный состав получен при добавлении гексаметоксикрасного и 2,4-динитрофенола к составу №29
Состав индикатора №30

Вывод:
Получено более четкое разделение точек 3 и 4, необходимо подобрать процентное количество гексаметоксикрасного и метилового красного для получения разделения точек 3 и 4.
Проверить влияние добавок:
1) добавить метиловый оранжевый,
2) добавить больше БТС,
3) уменьшить содержание этанола,
4) проверить растворимость индикаторов в смеси этанол /вода 50/50, (т.к. индикатор имеет спиртовую основу, в ходе испытаний была выявлена высокая летучесть).
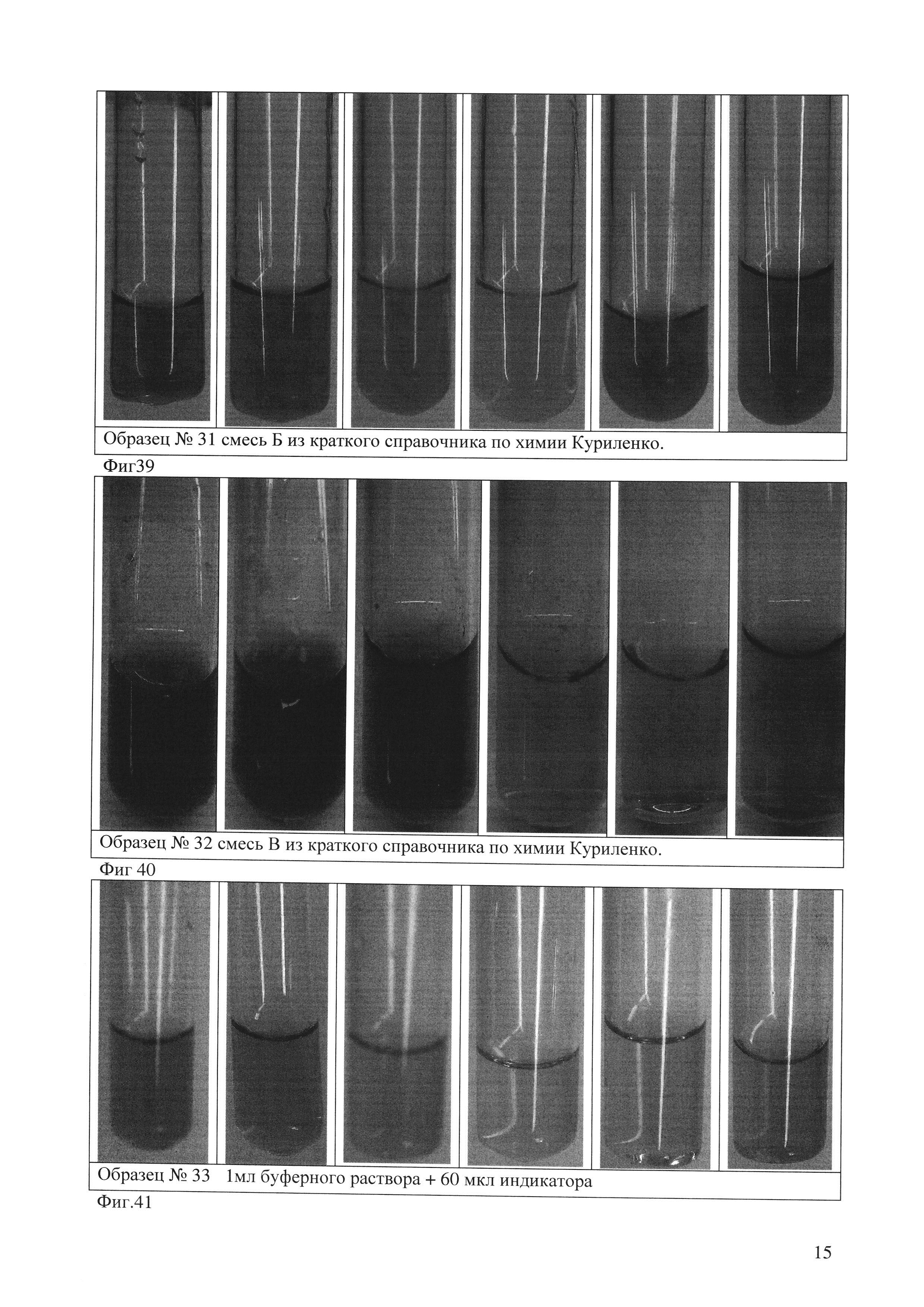
Опыт 4. (индикатор 31)(фиг. 39)
Приготовление универсального индикатора состава Б по книге: Куриленко. Краткий справочник по химии.
Состав индикатора №31: 
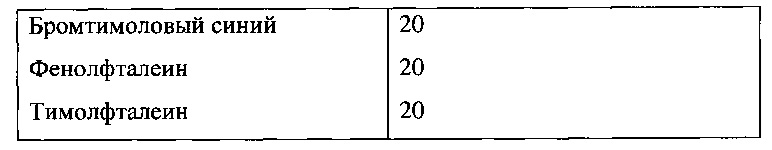
Образец №31 смесь Б из книги под ред. Куриленко.
Вывод: получен индикатор схожий по цветовой шкале с ЭО№28, но различие в цветах точек 3,0 и 4,0 наблюдается только для разбавленных растворов, при увеличении концентрации цвета этих точек сливаются.
Опыт 5. (индикатор 32)(фиг. 40)
Приготовление универсального индикатора состава В по книге: Куриленко. Краткий справочник по химии.
Приготовлен индикатор данного состава:
Растворение проводили при температуре 75 градусов, в течение 2 часов, при постоянном перемешивании. Образец №31 смесь В по книге Куриленко.
Вывод:
Данный состав индикатора совершенно не делит точки 3-4-5 и 6-7. Также при контакте индикатора с буфером выпадает осадок. Вероятно, это составляющая индикатора, которая не растворяется в воде. Возможно, это повлияло на окрашивание буферных растворов.
Вывод по опытам 1-5;
Получены составы, которые позволяют разделять все точки рН по цветам (опыты 3 и 4). Данные составы имеют различие в подборе индикаторной составляющей, но дают приблизительно одинаковый результат. Оба индикатора, взятый из литературы и полученный в результате разработки, состоят на более чем 80% из спирта, они не дают осадка при контакте с буфером, в отличие от состава №31, который на 50% состоит из воды.
Следует попробовать уменьшить концентрацию спирта в составах 30, 31.
Уменьшить летучесть образца 30, попробовать приготовить его на водно-спиртовой основе (с минимально возможным содержанием этанола).
Опыт 6 (индикатор 33) (фиг. 41)
С целью уменьшения летучести решено в индикатор добавить глицерин.
Приготовление индикатора:

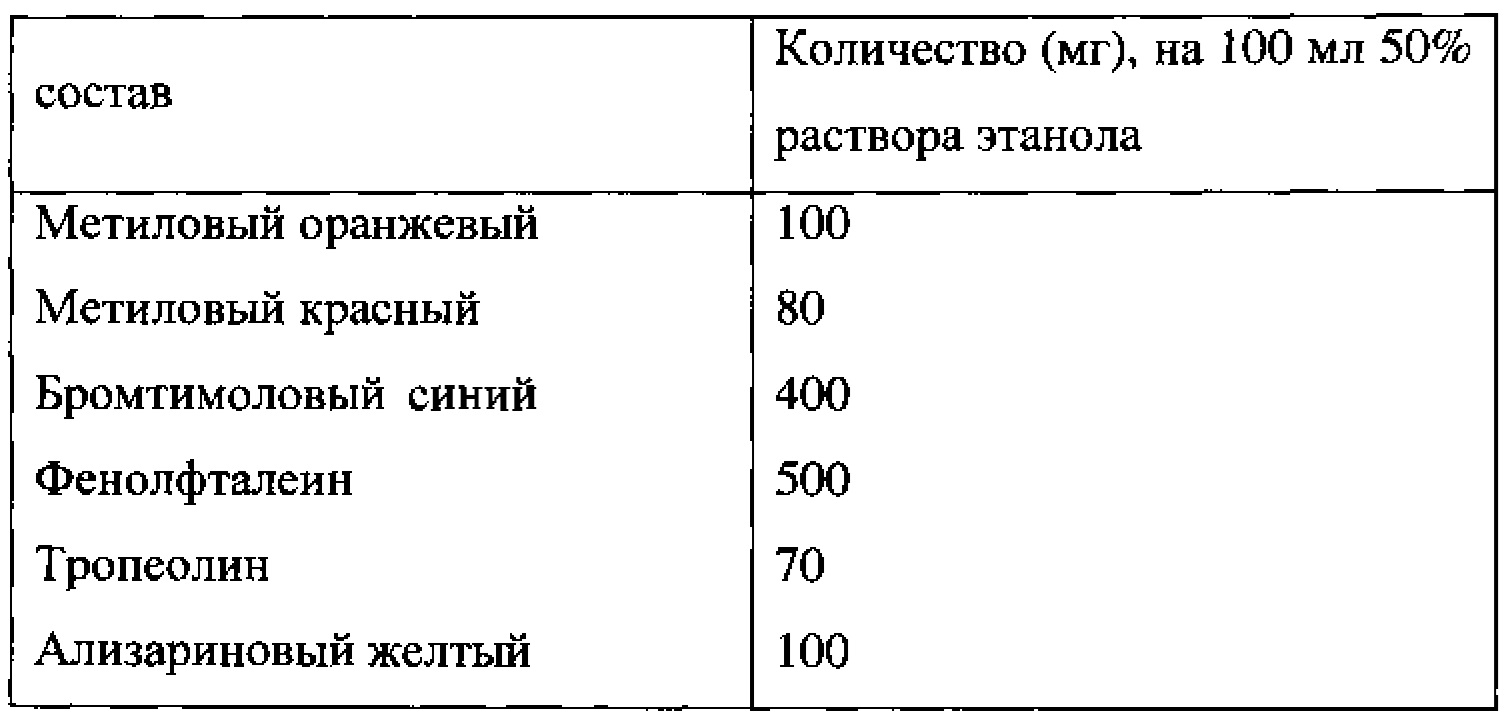
Вывод: образец высыхает за 5-6 минут. Цвета четко разделяются, но не насыщенны. Рецептура приготовления ЭО №33 на 100 мл:
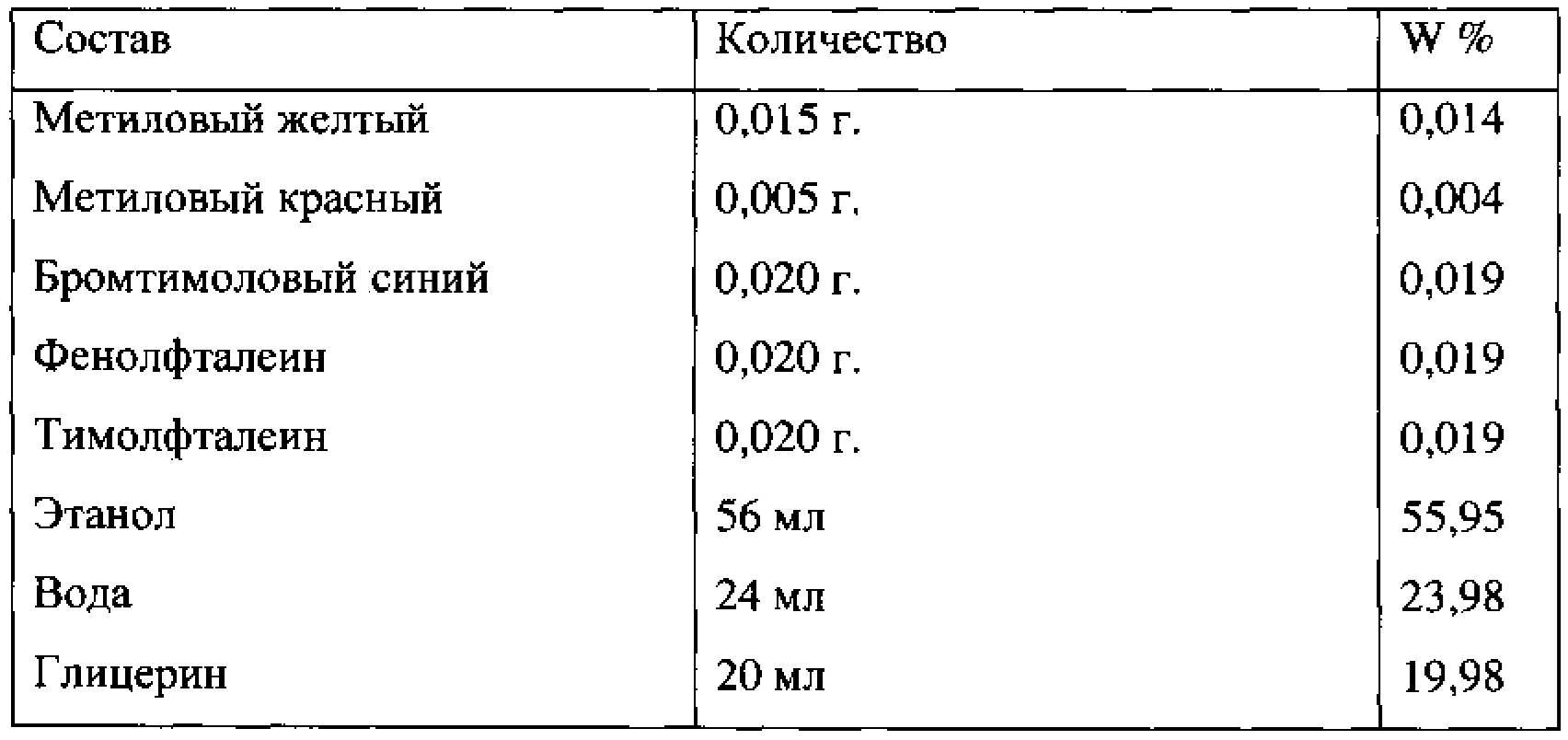
Смесь из кристаллических индикаторов высыпать в коническую колбу, добавить спирт этиловый. Смесь непрерывно перемешивать при нагревании (150°С) до растворения.
Добавить воду, не охлаждая раствор.
К полученной смеси после остывания добавить глицерин. Тщательно перемешать. Принято решение приготовить растворы индикаторов с концентрацией 0,3г/100 мл с добавлением глицерина.
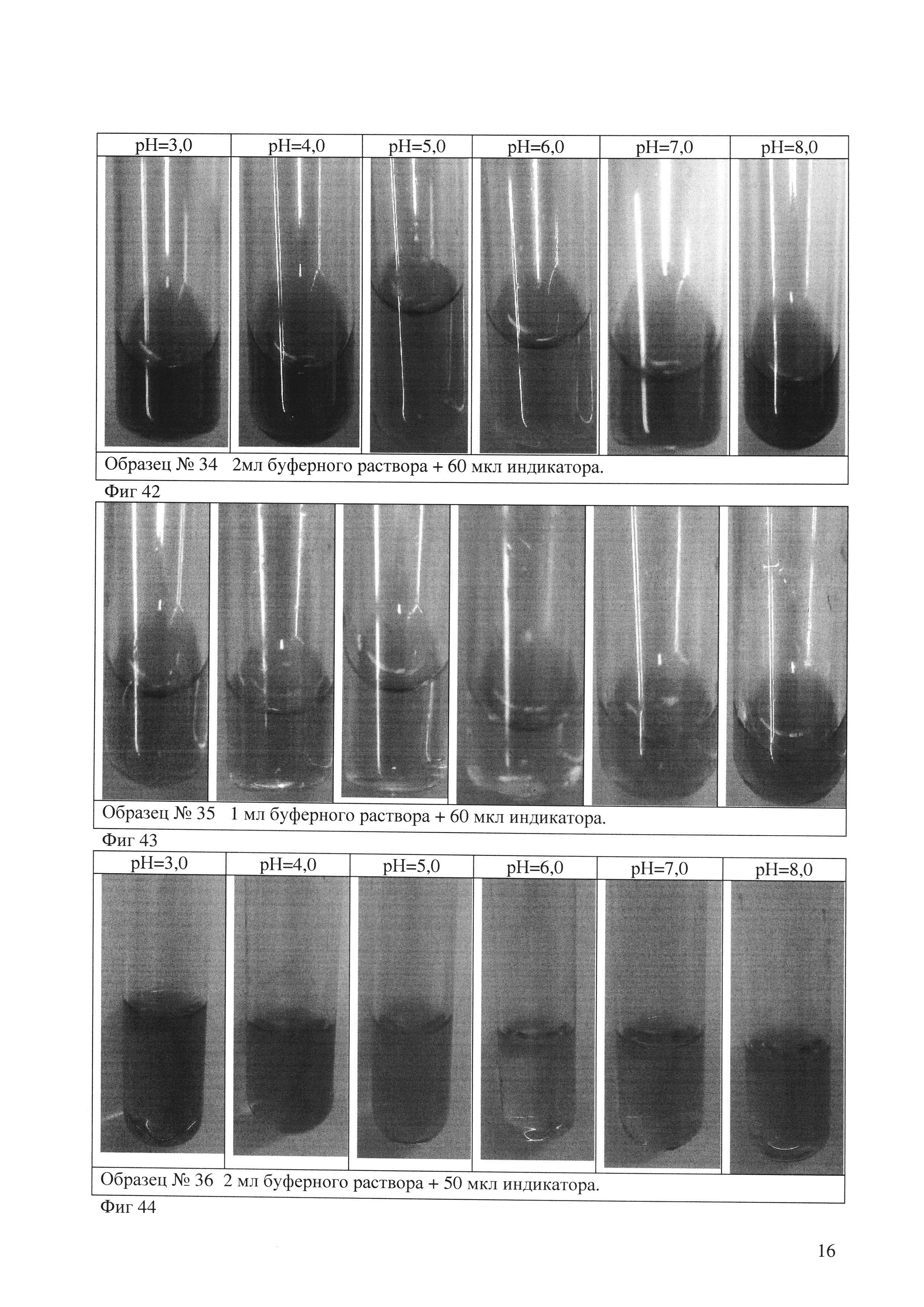
Опыт 7. (индикатор 34)(фиг. 42)
С целью увеличения насыщенности окраски цветовой шкалы увеличиваем исходную концентрацию индикаторов до 0,3 г/100 мл:

Увеличение концентрации исходных индикаторов привело к большей насыщенности цветов, точки 3 и 4 различимы только при нормальном освещении. Точка 3 имеет розоватый цвет, 4 - красный.
В 0,3% растворе метилового красного выпали кристаллы, умеренно растворим в этаноле.
Вывод:
1. Исходя из имеющихся в наличии индикаторов, можно сказать, что лучший результат не может быть достигнут, используя в качестве растворителей только этиловый спирт воду.
2. Добавить щелочь к рецептуре индикатора №33.
3. Попробовать добавить в образец №28 глицерин.
4. Закупить индикаторы:
Конго красный (3-5,2 синфиол.-красн.)
П- нитрофенол (5,6-7,6 6 цв.-желт.).
Опыт 8. (индикатор 35)(фиг. 43) 
Вывод:
Добавление щелочи привело к ухудшению в различии цветов точек 3-6, оттенки очень близки различить сложно.
Опыт 9. (индикатор 36)(фиг. 44)
Были приготовлены 0,1% растворы индивидуальных индикаторов в изопропиловом спирте по ГОСТ 4919_1-77, отступление в приготовлении фенолфталеина. 0,1 г Фенолфталеина растворен в смеси ИПС/вода в соотношении 50/50.

Вывод: полученный индикатор хорошо разделяет все точки шкалы от 3 до 8. Скорость высыхания 50 мкл около 5 минут с выпаданием составляющих в осадок.
Но входящий в состав изопропиловый спирт имеет резкий раздражающий запах из-за чего, вероятно, индикатор на основе ИПС-а не может быть применен в помещении с отсутствием приточно-вытяжной системы.
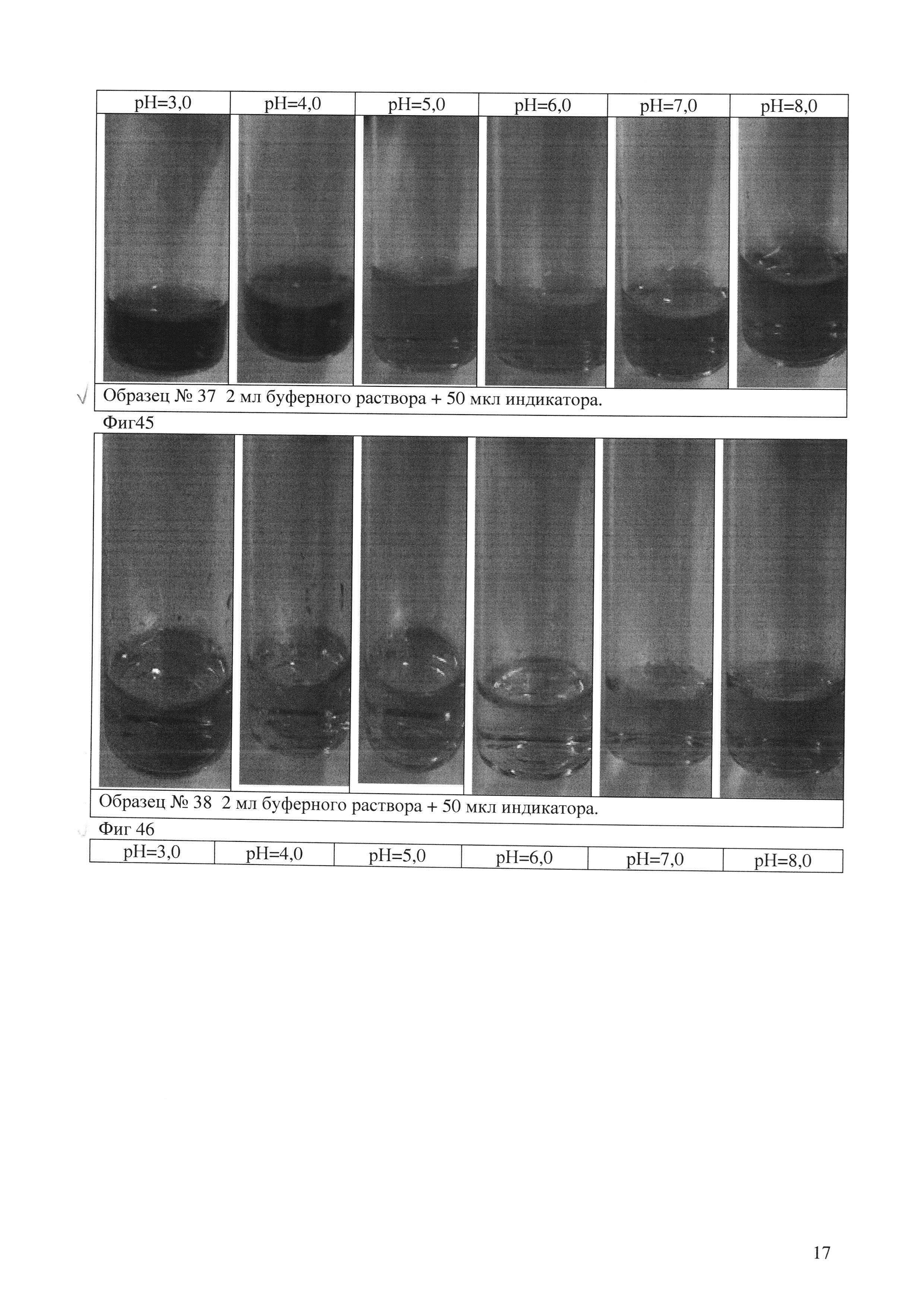
Опыт 10. (индикатор 37)(фиг. 45)
Приготовлен индикатор на основе н-пропилового спирта:

Результат: полученный индикатор хорошо разделяет все точки шкалы от 3 до 8.
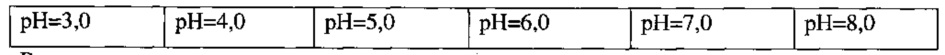
Вывод: результаты не отличаются от растворов на основе ИПС и этанола. Запах менее резок, чем при использовании ИПС-а. Отдан на исследование.
Опыт 11. (индикатор 38)(фиг. 46)
Приготовлен индикатор на основе н-бутилового спирта: 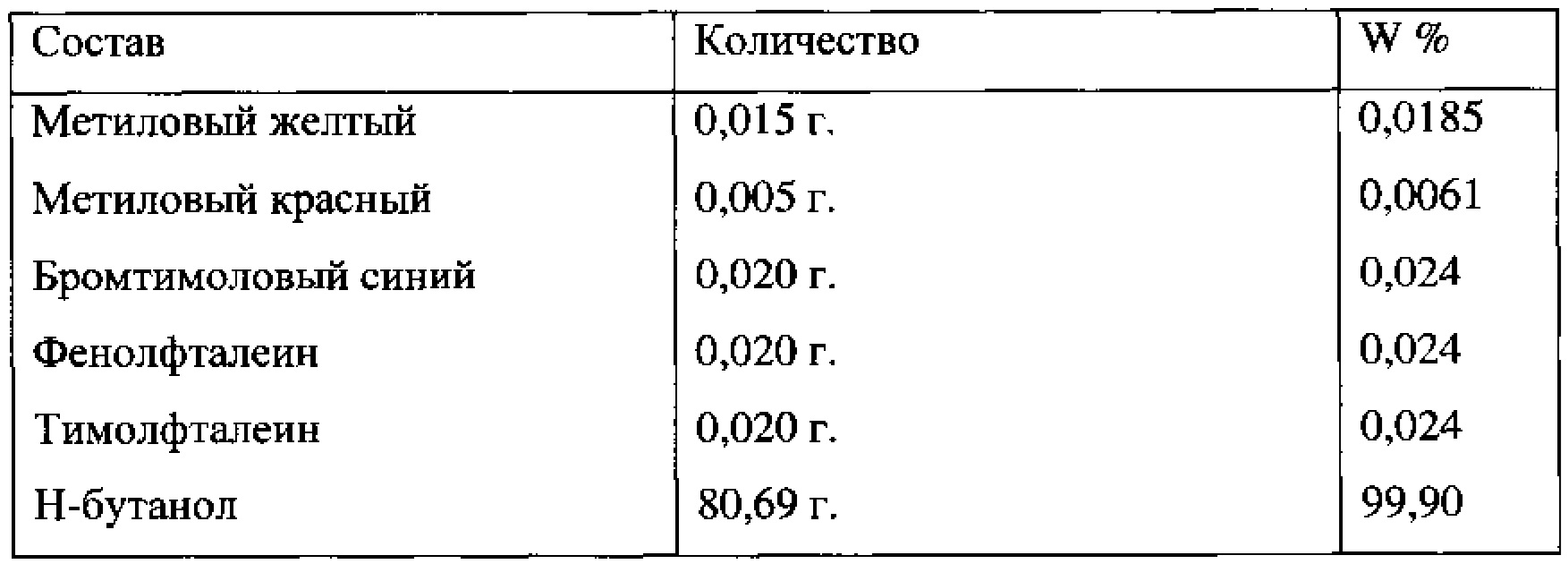
Результат: полученный индикатор не смешивается с водой, но компоненты индикаторной системы частично переходят в буферные растворы, окрашивая их хаотично. Вывод: бутанол-н не пригоден для разработки индикатора.
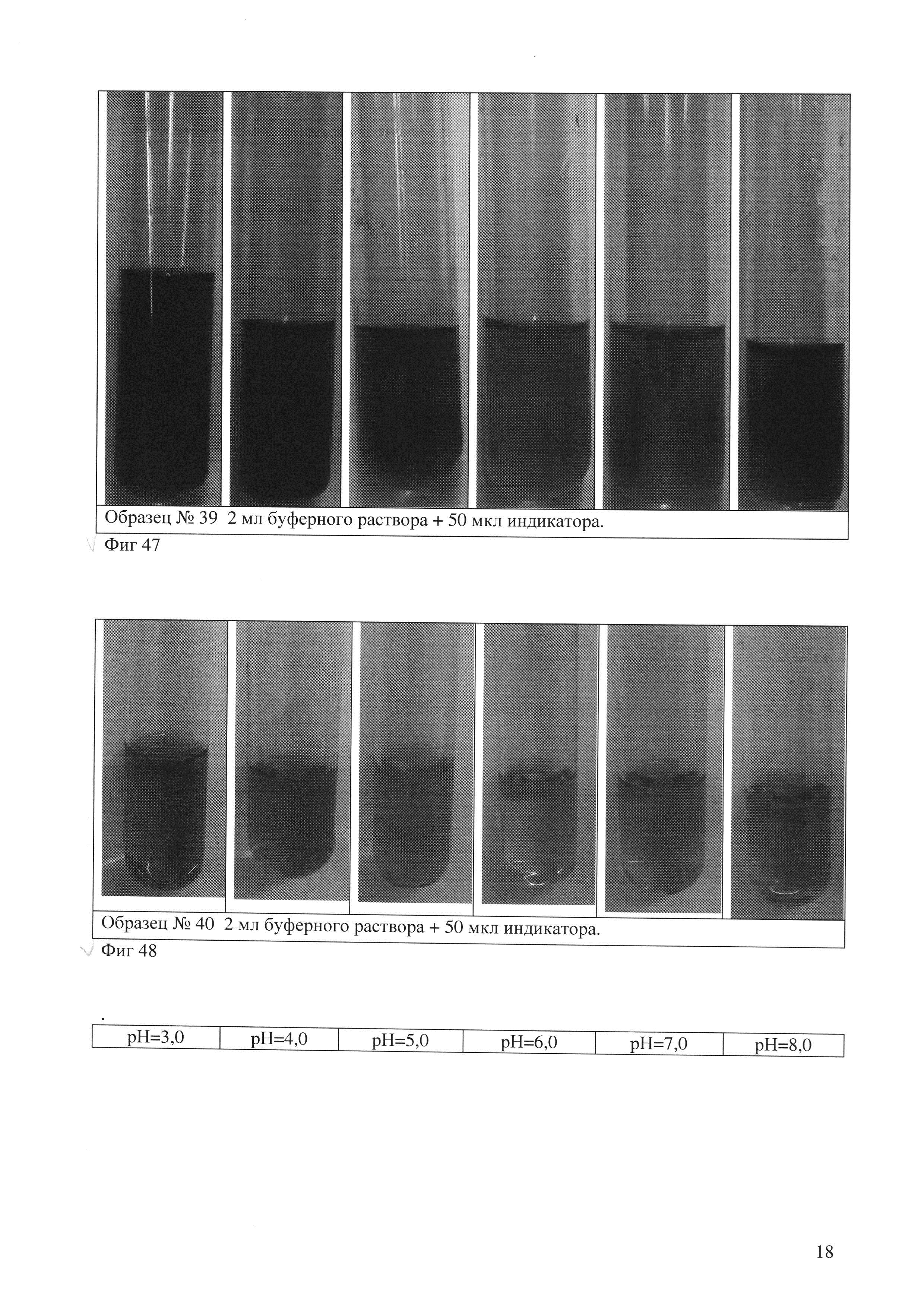
Опыт 12. (индикатор 39)(фиг. 47)
Приготовлен индикатор с двойной концентрацией реагентов на основе н-пропилового спирта:
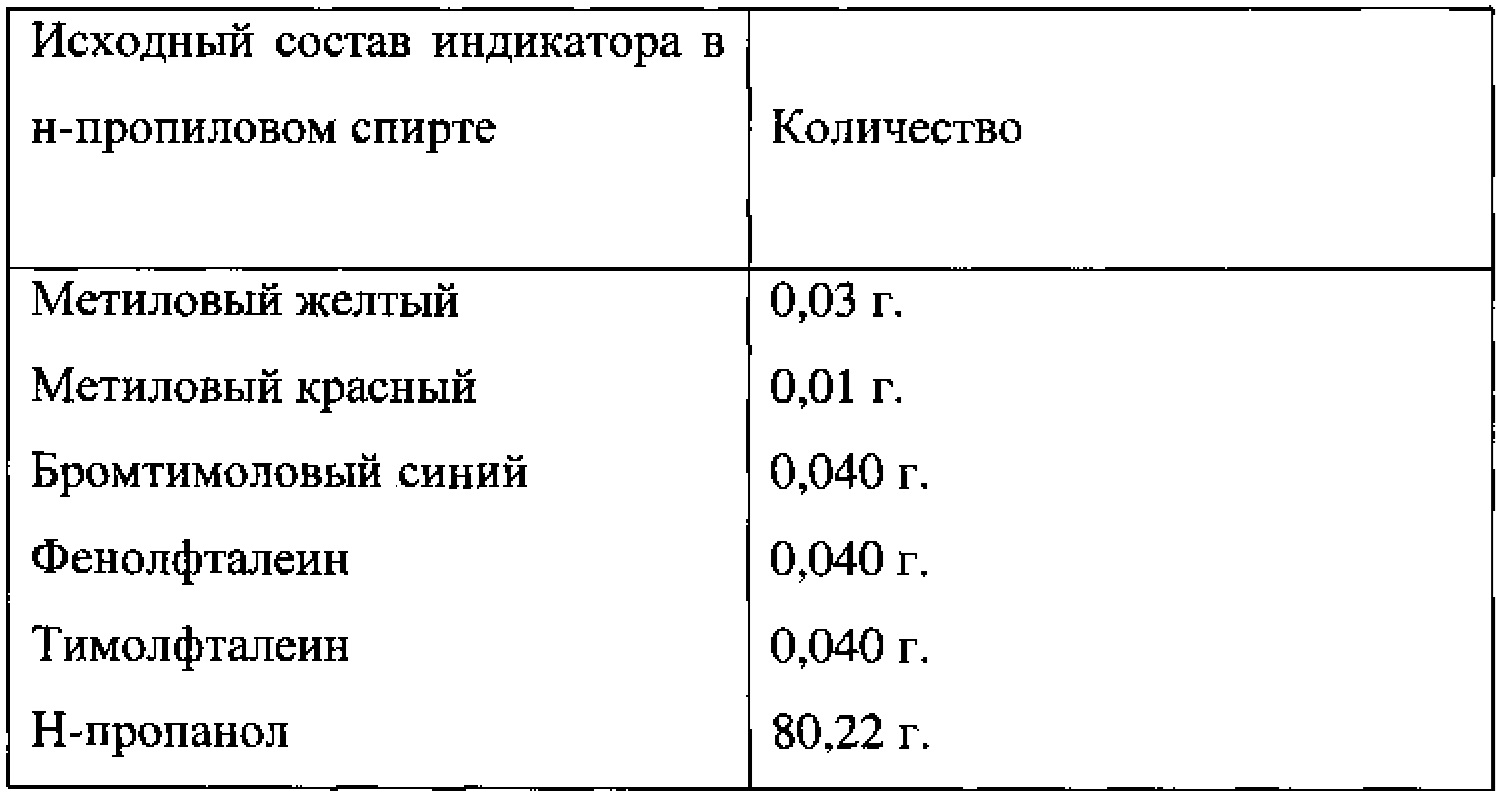
Далее, с целью уменьшения летучести и взрыво-пожароопасности исходный раствор разбавлен водой в соотношении 50:50: 
Результат: полученный индикатор смешивается с водой, компоненты индикаторной системы не выпадают в осадок. 20 мкл образца высыхают более чем за 10 минут с выпадением составляющих в осадок.
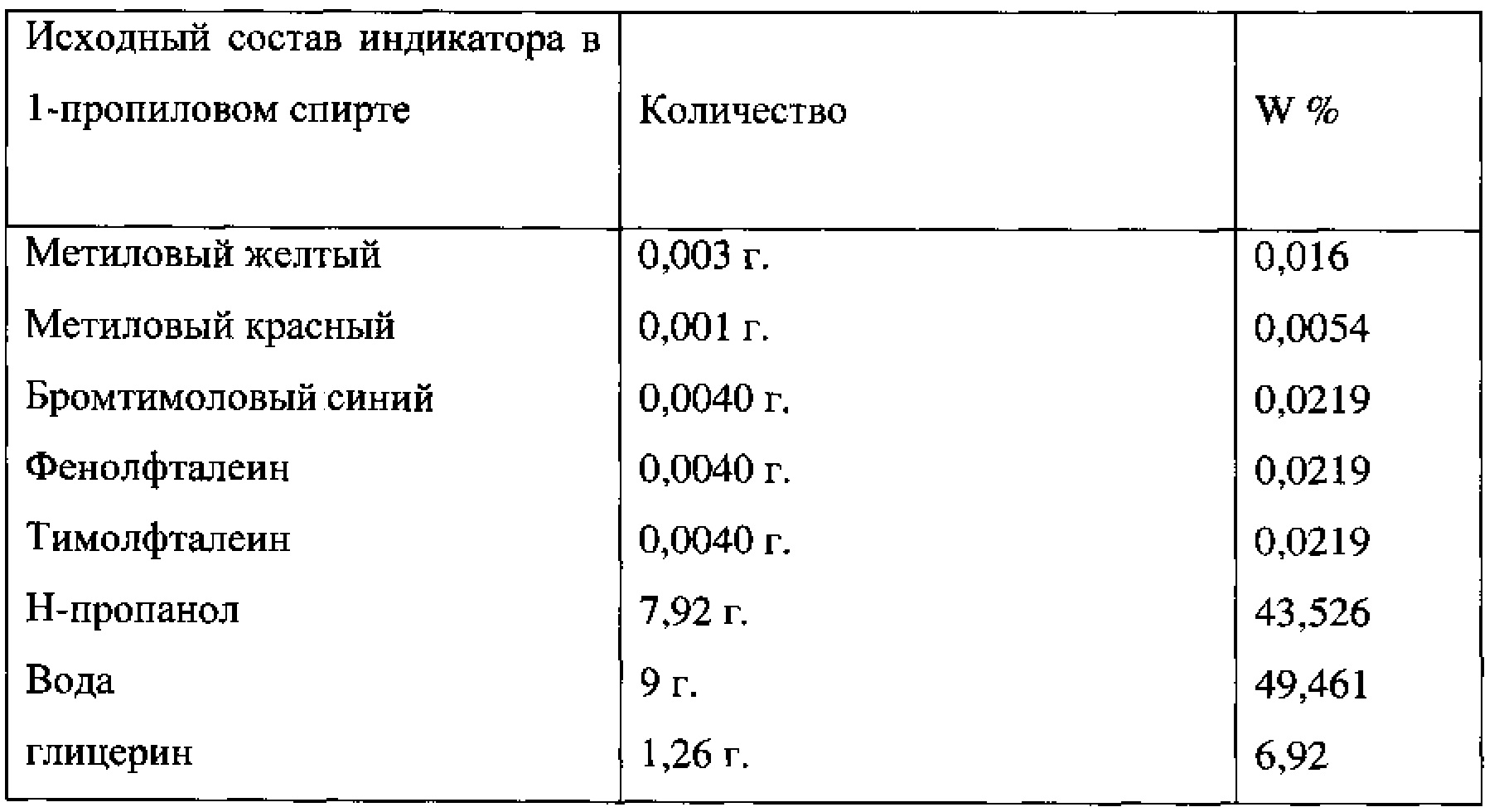
Опыт 13. (индикатор 40) (фиг. 48)
Приготовлено 10 мл 0.2% раствора индикатора в пропаноле. 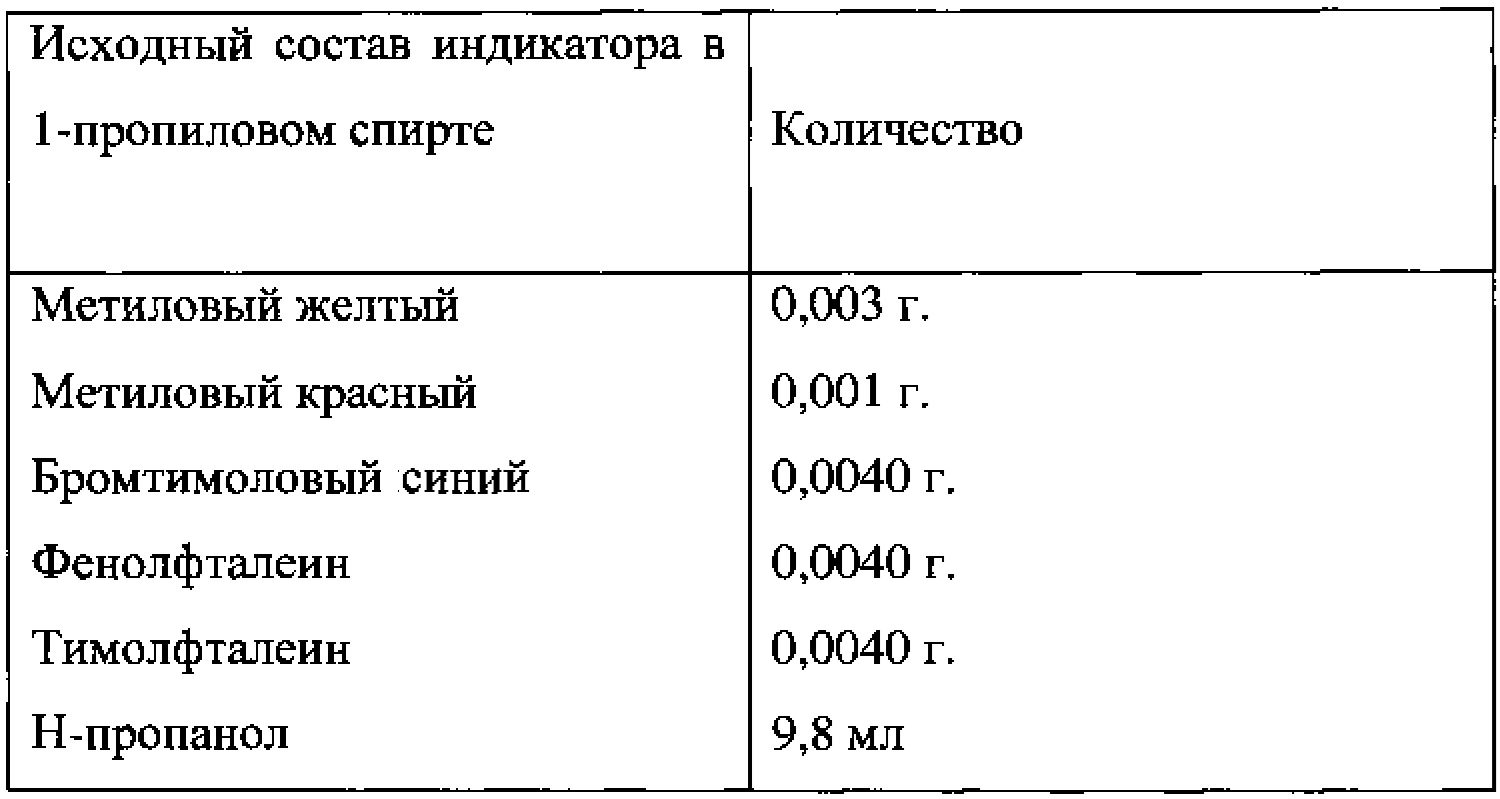
В полученный раствор добавили 9 мл воды и 1 мл глицерина.
Опыт 14. (индикатор 41)
Попытка приготовить раствор индикаторов на этиленгликоле не удалась. Компоненты не растворяются.
Опыт 15. (индикатор 42) (фиг. 49)
Приготовлено 50 мл 0.2% раствора индикатора в изопропаноле.
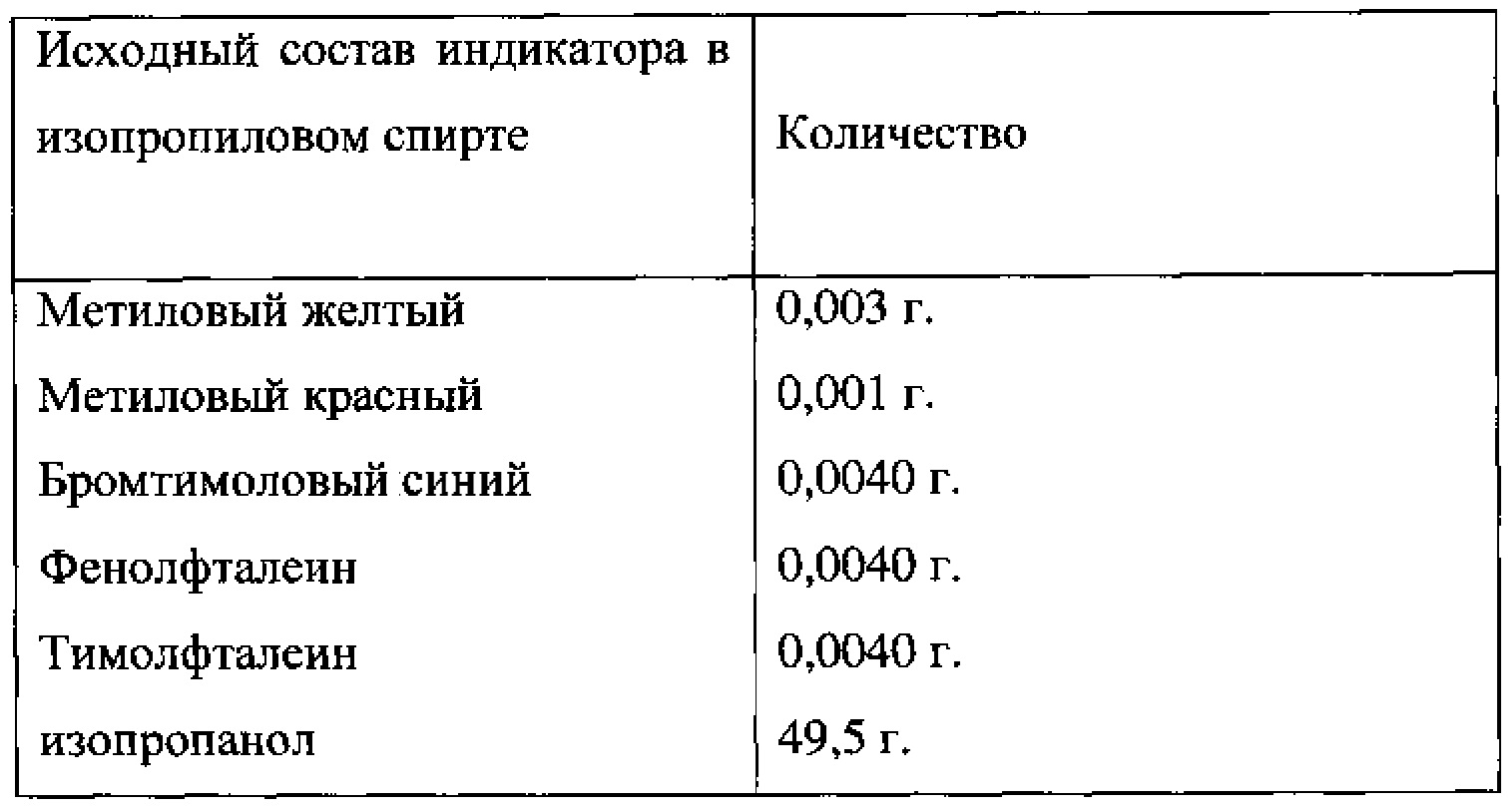
В полученный раствор добавили 48 мл воды и 2 г глицерина.
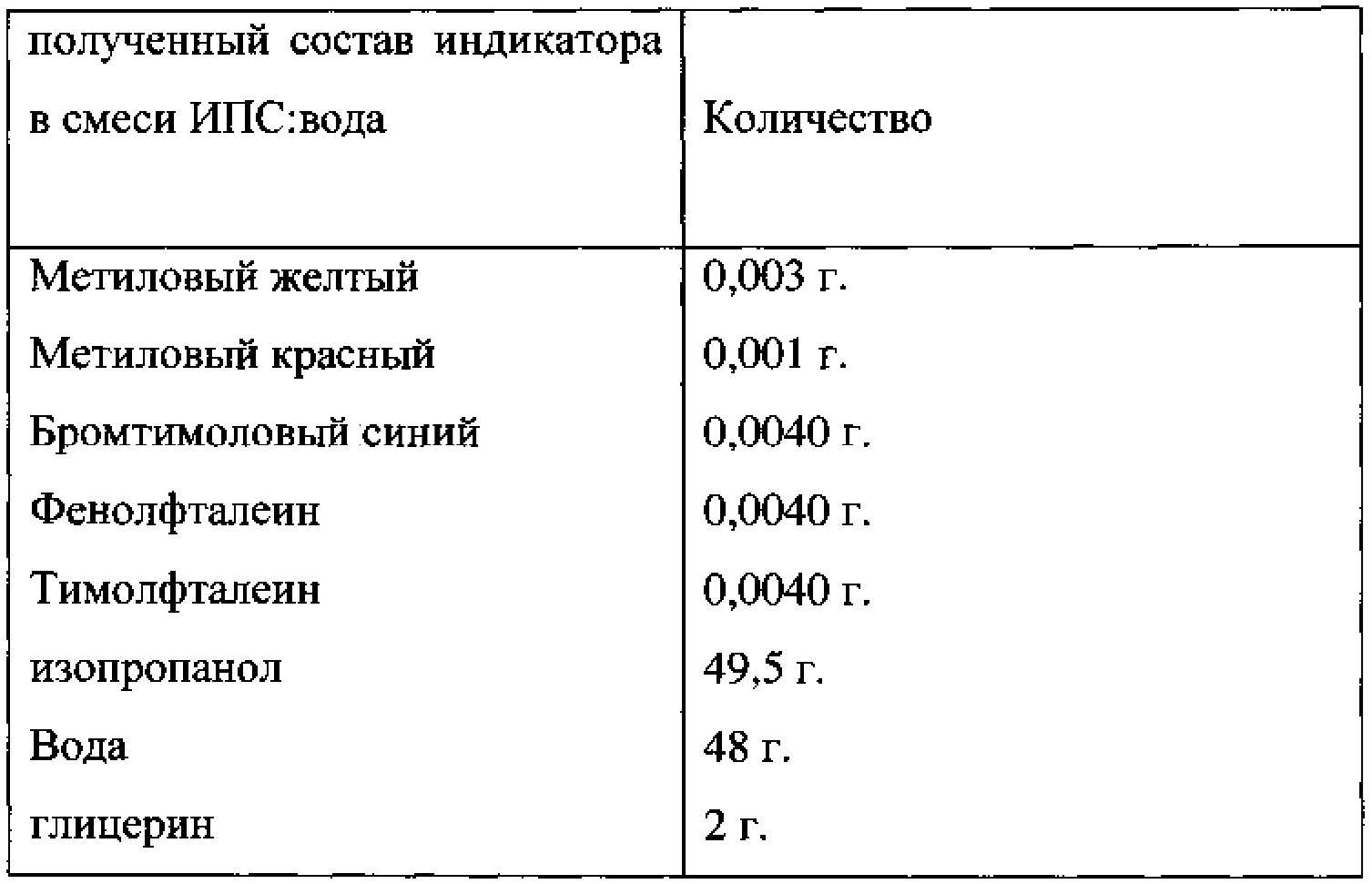
Полученный раствор передан на испытания. До передачи раствор стоял на протяжении приблизительно 1 месяца на свету при комнатной температуре плотно закрытым.
После подбора химических составляющих к испытанию были представлены три состава, отличающиеся растворителем.
Индикатор, содержащий:
|
Этанол, выбранный в качестве растворителя, создает на стекле устойчивую каплю, не высыхает в течение 10 минут, равномерно окрашивает препарат и зонд. Цвет четко соответствует шкале. Последующая окраска препарата для бактериоскопии не имеет различий с копией, не обработанной индикатором.
Индикатор, содержащий в качестве растворителя изопропанол:
|
Изопропанол создает на стекле пленку, высыхающую в течение минуты, что иногда приводит к неравномерному окрашиванию препарата. Цвет четко соответствует шкале. Последующая окраска препарата для бактериоскопии не имеет различий с копией, не обработанной индикатором.
Индикатор, содержащий растворитель н-пропанол:
|
Н-пропанол создает на стекле устойчивую каплю, не высыхает в течение 10 минут, равномерно окрашивает препарат и зонд. Цвет нечетко соответствует шкале, образуя полутона, сложные для интерпретации. Последующая окраска препарата для бактериоскопии не имеет различий с копией, не обработанной индикатором. Следующие примеры иллюстрируют предлагаемые изобретения
ПРИМЕР 1.
ФИО: Ш.О.Н., 32 года Пол: женский
Первичное обращение
Anamnesis vitae
Развитие: родилась доношенным ребенком, росла и развивалась согласно возрасту и полу
Условия жизни и работы: Жилищно-бытовые условия удовлетворительные Профессия: дизайнер.
Семейный анамнез: со стороны отца: тромбозы: инфаркт до 50 лет,
со стороны матери: онкозаболевания: рак молочной железы в 60 лет.
Заболевания: Перенесенные заболевания: железодефицитная анемия в детстве, хронический отит с обострениями 1-2 раза в год, хронический дисбактериоз кишечника с 10 лет, лечение лямблиоза в 2004 году. В последние годы хронические запоры Гемотрансфузионнный анамнез: A(II)Rh положительный. Переливаний крови не было. Anamnesis gynecologycae
Менструация с 13 лет
Характеристика менструального цикла: регулярный
Длительность менструации: 5 дней
Характер менструаций: обильные безболезненные
Последняя менструация: 29.03.2014
Контрацепция: барьерный метод
Гинекологические заболевания: острый гнойный сальпингит 2007 г. сальпингоэктомия слева.
ИППП: облигатные патогены: хламидийная инфекция диагностирована в 2005 году, лечение азитромицином. Контроль ПЦР через месяц зарегистрировал выздоровление. Условно - патогенная флора: вагинальные кандидозы 1-2 раза в год. Местная и системная терапия с временным клиническим эффектом. Генитальные микоплазмы (Ureaplasma urealyticum) обнаружены в 2013 году. Проведена антибактериальная терапия без контроля. Предыдущие беременности; 2003: артифициальный аборт на сроке до 6 недель, осложненный эндометритом, 2006: срочные роды, 2010: срочные роды. Дети растут и развиваются нормально.
Anamnesis morbi
Жалобы; серые выделения с запахом в течение месяца, периодические зуд и жжение вульвы во второй фазе цикла. Обследование с супругом на облигатные ИППП месяц назад дало отрицательный результат. Лечение метронидазол и миконазол местно+метронидазол per os дало кратковременный эффект.
Объективно:
Рост: 165
Вес: 64
ИМТ: 23,51
Кожа, слизистые чистые. Язык влажный, обложен белым налетом, имеет «географическую» исчерченность. Дыхание везикулярное. Шумов нет. Тоны сердца ритмичны. Пульс 72 удара в минуту. АД 120/70. Живот мягкий, безболезненный, несколько вздут. Аускультативно - повышенная перистальтика. Печень по краю реберной дуги. Симптом поколачивания отрицателен в обеих поясничных областях.
Мочеиспускание свободное, безболезненное.
Status genitalis (20-й день менструального цикла)
Лимфатические узлы: интактны
Наружные пол.органы: сформированы правильно,
Вульва: чистая,
Промежность: средняя,
Влагалище: рожавшей, гиперемии стенок нет
Выделения во влагалище: обильные серые пенистые с характерным рыбным запахом
Шейка матки: цилиндрическая, слизистая визуально не изменена.
Цервикальный секрет: мутная слизь в умеренном количестве
Матка: подвижная, расположена в anteversio, размер нормальный, поверхность ровная, консистенция плотно-эластическая, болезненность при пальпации отсутствует
Придатки матки: не увеличены, область их безболезненная при пальпации,
Спаечный процесс в малом тазу: не выражен
Диагноз предварительный:
Бактериальный вагиноз?
Лабораторное обследование:
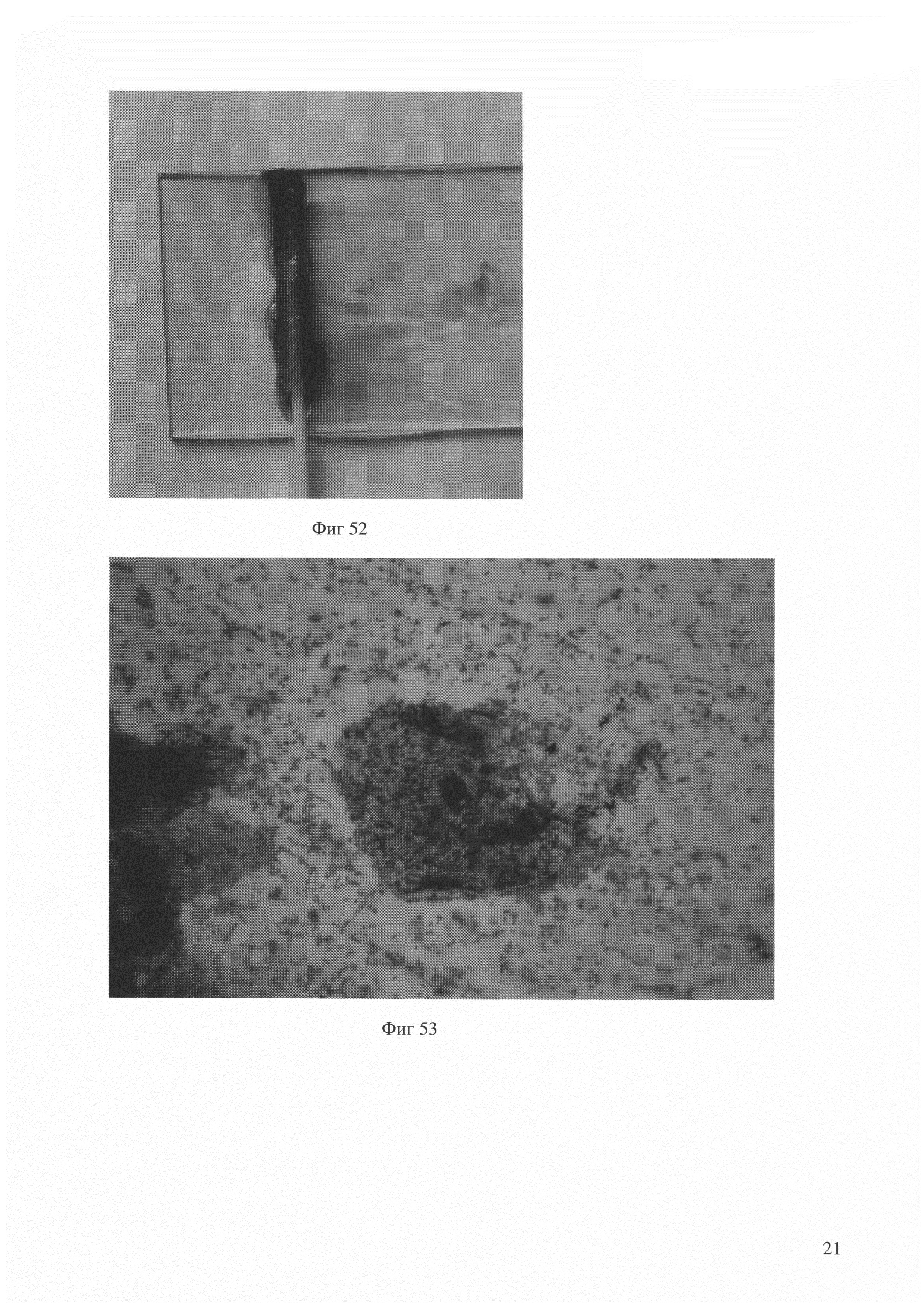
Забор мазка проведен на 3-секционное стекло. Для каждой локализации использован отдельный универсальный зонд для взятия биоматериала. На секцию для влагалищной порции помещена капля индикатора. При нанесении материала на стекло индикатор моментально изменил окраску как на стекле, так и на рабочей части зонда.
рН метрия - 6,0 (Фиг. 52).
Анализ мазка на флору с окраской по Романовскому: Во влагалищной порции мазка обнаружены ключевые клетки, снижение количества лактобацилл, 2-3 лейкоцита в поле зрения.
Посев на селективную среду для идентификации Ureaplasma urealyticum и Mycoplasma hominis - роста генитальных микоплазм нет
Консультации специалистов:
Гастроэнтеролог: Хронический гастродуоденит. Хронический холецистит. Хронический дисбактериоз кишечника. Назначена терапия.
Эндокринолог: Субклинический гипотиреоз. Назначена терапия.
Диагноз клинический:
Бактериальный вагиноз. Код по МКБ10: [N89.8] Другие невоспалительные болезни влагалища.
Лечение (проведено одновременно со схемами по рекомендациям гастроэнтеролога и эндокринолога):
1 этап: нео-пенотран форте 1 свеча вагинально на ночь 7 дней
2 этап, непосредственно за первым: гинофлор Э 1 свеча вагинально на ночь 6 дней.
ПРИМЕР 2.
ФИО: Ш.О.Н., 32 года Пол: женский
Контрольное обследование (проведено через 2 недели после окончания терапии): Лечение перенесла без осложнений. Клинически зарегистрировано выздоровление. Жалоб не предъявляет.
Лабораторное обследование:
Забор мазка осуществлялся идентично первичному.
рН метрия - 3,5 (фиг. 53)
Анализ мазка на флору с окраской по Романовскому: Во влагалищной порции мазка ключевые клетки не обнаружены, нормализовалось количество лактобацилл, 2-3 лейкоцита в поле зрения (фиг. 54)
Status genitalis (18-й день менструального цикла)
Лимфатические узлы: интактны
Вульва: чистая,
Влагалище: рожавшей, гиперемии стенок нет
Выделения во влагалище: умеренные слизистые
Шейка матки: цилиндрическая, слизистая визуально не изменена.
Цервикальный секрет: прозрачная слизь в умеренном количестве
Матка: подвижная, расположена в anteversio, размер нормальный, поверхность ровная, консистенция плотно-эластическая, болезненность при пальпации отсутствует
Придатки матки: не увеличены, область их безболезненная при пальпации,
Диагноз:
Реконвалесценция.
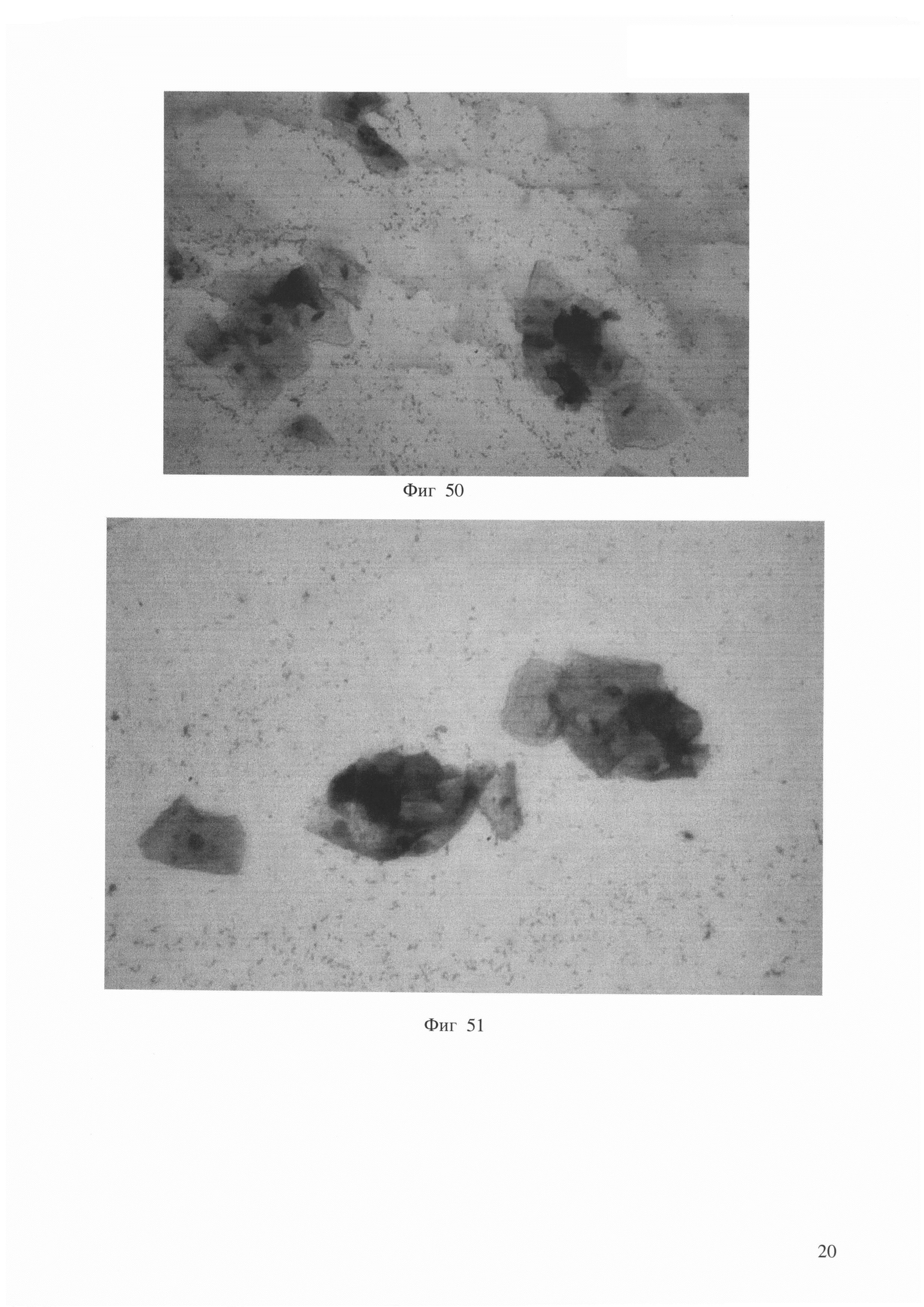
Заключение: Новый способ и реагент-индикатор для определения рН влагалищного секрета отличаются удобством применения в практической работе, позволяет адекватно оценивать рН, что доказано соответствием клинических признаков и результатовизмерения, не влияет на качество последующей окраски мазков. В приложении подтверждение идентичности окрашивания (окраска азур - эозин): на фиг. 50 (без индикатора), на фиг. 51 (с индикатором) подтверждение идентичности последующего окрашивания.
Таким образом, предложен наиболее доступные способ и реагент-индикатор, использование которых дает возможность определять рН вагинальной жидкости in vitro при рутинном заборе вагинальной жидкости для бактериоскопии в ходе гинекологического приема. Предлагаемый способ отличается простотой и может широко применяться в гинекологической практике. Возможно, также аналогичным способом определять рН цервикальной слизи, что может найти большое практическое значение в репродуктологии, в частности в области вспомогательных репродуктивных технологий.
Источники информации
1. De Los Santos G.E., Zuniga S. Comparison of pH measurement devices for determining vaginal pH in cynomolgus macaques / Contemp Top Lab Anim Sci. 2004 Sep;43(5):39-40.
2. Гинекология №02 2014., стр 9-13 Роль рН-метрии в диагностике вагинальных инфекций / Е.Ф.Кира, К.Е.Семенова, А.М.Маркарян.