Результат интеллектуальной деятельности: Средство, обладающее гастропротекторной активностью
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к фармакологии, может быть использовано в качестве гастропротекторного средства для повышения защитной функции слизистого барьера и устойчивости слизистой оболочки гастродуоденальной зоны к повреждающему действию стресса и нестероидных противовоспалительных средств.
Заболевания органов пищеварения отличаются широким распространением и по частоте занимают третье место среди причин летальности после патологий сердечнососудистой системы и онкозаболеваний. Существует многообразие этиопатогенетических факторов, обусловливающих ульцерогенные процессы, при этом нет доказательств приоритетного значения какого-либо из них в развитии язвенной болезни и других кислотозависимых заболеваний [1, 3, 6]. В настоящее время считается доказанным фактом значимая роль стресса в качестве «пускового механизма» и фактора хронизации ульцерогенеза [1, 4, 5]. Ульцерогенное действие нестероидных противовоспалительных средств, применяемых по жизненным показаниям в рамках кардиальной и противоревматической терапии, определяет актуальность разработки профилактических и лечебных гастроэнтерологических мероприятий. Кроме того, существующие схемы стандартной терапии язвенной болезни желудка и двенадцатиперстной кишки сопровождаются побочными эффектами, в том числе и атрофическими изменениями слизистой оболочки желудка, и не всегда предотвращают развитие хронических вариантов течения заболевания [2]. Детальная информация о причинах и механизмах инициации и формирования язвенной болезни желудка и двенадцатиперстной кишки позволяет определять наиболее эффективные способы лечения в конкретном случае. Поэтому при терапии язвенной болезни и других кислотозависимых заболеваний необходимо воздействовать не только на причину болезни, ведущие патогенетические механизмы, воспалительный процесс, болевой синдром, но корригировать уровень секреции, обменные нарушения, репаративные процессы. Все вышесказанное обусловливает целесообразность поиска и разработки лекарственных препаратов, способных повышать резистентность клеток гастродуоденальной слизистой к ульцерогенным факторам и регенеративную способность слизистой оболочки желудка и кишечника. Создание лекарственных средств с таким комплексным фармакологическим действием является насущным и перспективным направлением для отечественной фармацевтической промышленности.
Широко используется группа противоязвенных средств - гастропротекторов, повышающих резистентность слизистой оболочки гастродуоденальной зоны к воздействию агрессивных факторов. Подобная гастропротекция может быть осуществлена или путем активации естественных механизмов защиты слизистой оболочки, или за счет образования дополнительного защитного барьера в области эрозии или язвы. Однако, существуют противопоказания и ограничения к назначению большинства гастропротекторов [6, 10, 11].
Одним из наиболее часто используемых гастропротекторов и наиболее близким по техническому результату к предлагаемому средству является метилурацил, который выбран в качестве препарата сравнения [10]. Метилурацил - аналог пиримидиновых оснований, стимулирует белковый синтез при язвенной болезни, ускоряет регенерацию клеток, способствует заживлению язв, но в отношении данного препарата существуют противопоказания и ограничения к назначению.
Результаты экспериментов, ранее проведенных нами на моделях нейрогенного и аспиринового ульцерогенеза, свидетельствуют об однонаправленном и выраженном противоязвенном действии цельного экстракта Lychnis chalcedonica L., содержащего комплекс мажорных и редких экдистероидов, тритерпеновых гликозидов, алкалоидов, полифенолов и флавоноидов [8, 12]. Полученные данные позволяют рассматривать вышеперечисленные фитокомплексы в качестве источников для создания на их основе субстанций для гастроэнтерологической клиники.
Нами впервые выявлена выраженная гастропротекторная активность комплекса флавоноидов, выделенного из надземной части растения Lychnis chalcedonica L., в условиях экспериментального стрессорного и индометациного повреждения.
Задачей изобретения является расширение арсенала гастропротекторных средств, способных повышать устойчивость слизистой оболочки гастродуоденальной зоны к ульцерогенному действию нестероидных противовоспалительных средств и стрессорного повреждения.
Поставленная задача достигается применением выделенного вещества - комплекса флавоноидов из надземной части растения Lychnis chalcedonica L. - в качестве гастропротекторного средства.
Впервые показано, что средство, содержащее комплекс флавоноидов из надземной части растения Lychnis chalcedonica L., оказывает гастропротекторное действие. Авторы не нашли в проанализированной литературе сведений о самостоятельной активности флавоноидов из надземной части растения Lychnis chalcedonica L. в условиях моделей стрессорного и индометациного повреждения. Гастропротекторное действие комплекса флавоноидов Lychnis chalcedonica L. явным образом не вытекает из уровня техники в данной области и не является очевидным для специалиста. Экспериментально установлено новое свойство и возможность использования комплекса флавоноидов из надземной части растения Lychnis chalcedonica L. в качестве средства, обладающего гастропротективной активностью, в практическом здравоохранении.
Таким образом, предлагаемое изобретение соответствует критериям патентоспособности "новизна", "изобретательский уровень", "промышленная применимость".
Средство, обладающее гастропротективым действием, представляет собой комплекс флавоноидов, выделенный из надземной части растений Lychnis chalcedonica L.
Изобретение будет понятно из следующего описания и приложенных к нему фигур.
На фиг. 1 - ВЭЖХ комплекса флавоноидов, выделенного из Lychnis chalcedonica L.;
На фиг. 2 - УФ-спектры выделенных флавоноидов:
1. УФ-спектр флавоноида с tr=10.40 мин;
2. УФ-спектр флавоноида с tr=12.45 мин;
3. УФ-спектр флавоноида с tr=13.29 мин;
4. УФ-спектр флавоноида с tr=15.47 мин;
Предлагаемое нами средство получают следующим образом.
Экстракцию воздушно-сухого сырья (200 г) надземной части в фазе цветения растения Lychnis chalcedonica L. проводили 5 раз 70% этиловым спиртом (4500 мл). Затем для удаления экстрагента объединенный экстракт концентрировали при температуре 50°C с помощью вакуумного ротационного испарителя IKA НВ 10 digital (Германия). Концентрированный экстракт разбавляли водой до соотношения 1:3 (v:v) и фильтровали. Затем фильтрат очищали от липофильных веществ при помощи н-гексана. Извлечение суммы биологически активных веществ из очищенного фильтрата осуществляли многократной экстракцией н-бутанолом. При этом из водной фракции выпадает осадок желто-коричневого цвета, который отделяли. Контроль содержания БАВ во фракциях осуществляли методом ТСХ. Выход бутанольной фракции составил 5.8%, флавоноидной фракции - 0.7% (в расчете на сырье). В последующем комплекс флавоноидов подвергали очистке селективной экстракцией системой растворителей этилацетат : этанол в соотношении 3:1. Полученный порошок имел желтоватую окраску.
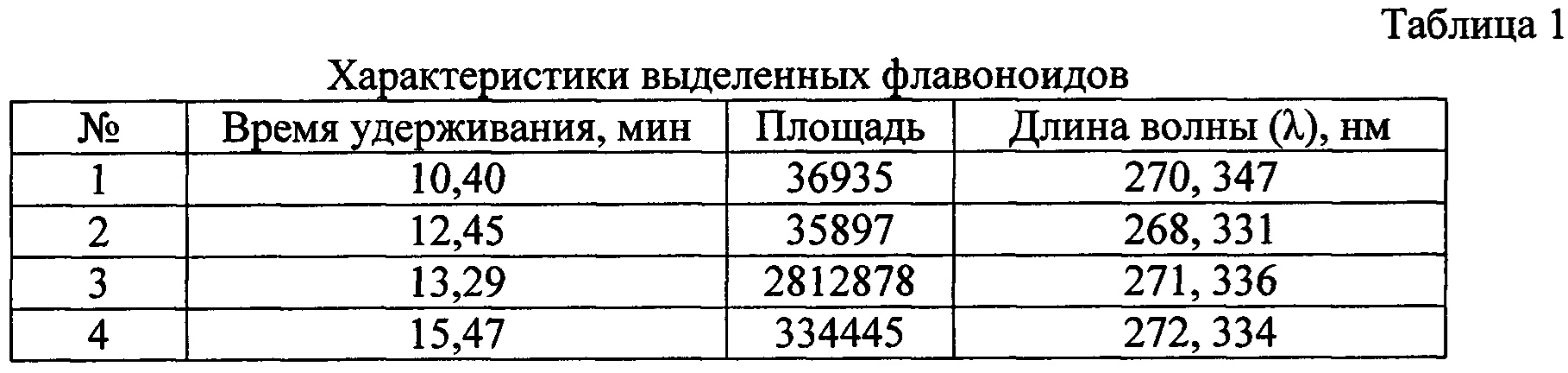
Мажорным компонентом флавоноидного комплекса является пик с tr=13.29 мин, площадь которого составила 87.4%.
Идентификация флавоноидной фракции, выделенной из надземной части растения Lychnis chalcedonica L., проведена методами ВЭЖХ и УФ-спектроскопии. ВЭЖХ анализ (фиг. 1) свидетельствует о том, что очищенный порошок представляет собой комплекс 4-х флавоноидов. В УФ-спектрах этих соединений, разделенных ВЭЖХ, с временами удерживания 10.40,12.45; 13.29 и 15.47 мин присутствуют по два максимума поглощения - 270 и 347; 268 и 331, 271 и 336; 272 и 334 нм, обусловленные присутствием двух ароматических колец А и В (фиг. 2). Такие спектральные характеристики свойственны флавоноидам.
Технический результат заключается в расширении арсенала гастропротекторных средств, повышающих защитную функцию слизистого барьера и устойчивость слизистой оболочки гастродуоденальной зоны к развитию стрессорных язв и ятрогенного повреждения желудка вследствие приема нестероидных противовоспалительных средств.
Возможность осуществления заявляемого изобретения подтверждается примером результатов экспериментального исследования гастрозащитной активности заявляемого средства в сравнении с действием экстракта элеутерококка и метилурацила на моделях нейрогенного и индометациного повреждения слизистой желудка.
Эксперименты выполнены на 108 аутбредных мышах-самцах CD1 (10-12 недель, массой 25-26 г) первой категории, которые были получены из отдела экспериментальных биологических моделей НИИФиРМ имени Е.Д.Гольдберга. Содержание животных и дизайн экспериментов были одобрены Этическим комитетом НИИФиРМ имени Е.Д. Гольдберга и соответствовали правилам, принятым Европейской конвенцией по защите позвоночных животных (Страсбург, 1986); Приказу МЗ РФ №199н от 1 апреля 2016 г.; Руководству по проведению доклинических исследований лекарственных средств (2012) [11, 13].
Дозы 12, 16, 20, 24 мкг/кг экспериментального образца (мажорное содержание флавоноидов 87,4%) были выбраны согласно результатам ранее проведенных экспериментов. Предлагаемая доза элеутерококка экстракта жидкого (5 мл/кг) и метилурацила (500 мг/кг) в исследовании противоязвенной активности выбрана на основании ранее проведенных экспериментов и данных литературы.
В механизме генеза модели нейрогенного повреждения ведущее место занимает нейро-гуморальный фактор, поэтому данная модель является наиболее адекватной среди быстровоспроизводимых «острых» экспериментальных язв [4, 5]. Мышей подвешивали корнцангами за кожную шейную складку, в результате 24-часовой частичной иммобилизации у животных развивалось язвенное поражение слизистой оболочки желудка.
Ульцерогенное действие нестероидных противовоспалительных средств (НПВС), применяемых по жизненным показаниям в рамках кардиальной и противоревматической терапии, определяет актуальность разработки профилактических и лечебных гастроэнтерологических мероприятий [3, 6]. Среди НПВС индометацин обладает наиболее выраженным ульцерогенным действием, что послужило основанием для выбора данного препарата в качестве повреждающего агента [6]. Индометациновое повреждение слизистой желудка у мышей вызывали внутрижелудочным введением препарата в дозе 20 мг/кг в физиологическом растворе дважды с интервалом 4 ч [7]. Последнее введение исследуемых вещества осуществляли дважды за 1 ч до начала действия язвообразующего фактора. Эффективность лечебных воздействий оценивали через 16 ч после введения индометацина.
Для оценки полученных результатов использовали следующие критерии эффективности. В конце экспериментов мышей умерщвляли методом кранио-цервикальной дислокации, желудки извлекали, вскрывали по малой кривизне, промывали холодным физиологическим раствором и макроскопически с помощью лупы при ярком освещении определяли число и площадь деструкций, которые дифференцировали на точечные (менее 0,5 мм) и крупные (более 0,5 мм), полосовидные. Подсчитывали среднее количество изъязвлений на одно животное в группе, процент животных с язвами [4, 5]. Индекс Паулса (ИП) определяли как интегральный показатель количества деструкций по формуле: % (среднее количество язв × % животных с язвами):100. Противоязвенную активность (ПА) препаратов определяли как отношение индекса Паулса в контрольной группе к индексу Паулса в опытной группе. Исследуемое средство считали активным, если ПА составляло 2 и более единиц [4, 14].
Статистическая обработка результатов производилась путем расчета средней (X) и стандартной ошибки (m) с использованием непараметрических методов Вилкоксона-Манна-Уитни (U) и углового преобразования Фишера (ϕ). Различие считали достоверным при P<0,05 [9].
Пример 1
Изучение гастропротекторной активности комплекса флавоноидов из надземной части растения Lychnis chalcedonica L. - лихниса халцедонского в сравнении с экстрактом элеутерококка жидкого при курсовом введении на модели нейрогенного повреждения слизистой желудка у аутбредных мышей-самцов CD1.
Мышей распределяли на группы рандомизированно, используя в качестве критерия массу тела, так, чтобы индивидуальное значение массы не отклонялось от среднего значения в пределах одного пола более чем на ±10%. В экспериментах использовали следующие группы аутбредных мышей-самцов CD1:
1. Животным вводили дистиллированную воду в объеме 0,5 мл/мышь внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз за 1 ч до иммобилизации на 24 ч (n=9);
2. Животным вводили элеутерококка экстракт жидкий в дозе 5 мл/кг (в объеме 0,5 мл/мышь диет, воды) внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз за 1 ч до иммобилизации на 24 ч (n=9);
3. Животным вводили раствор флавоноидов лихниса в дозе 12 мкг/кг (в объеме 0,3 мл/мышь диет, воды) внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз за 1 ч до иммобилизации на 24 ч (n=10);
4. Животным вводили раствор флавоноидов лихниса в дозе 16 мкг/кг (в объеме 0,4 мл/мышь диет, воды), внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз за 1 ч до иммобилизации на 24 ч (n=10);
5. Животным вводили раствор флавоноидов лихниса 20 мкг/кг (в объеме 0,5 мл/мышь диет, воды), внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз за 1 ч до иммобилизации на 24 ч (n=10);
6. Животным вводили раствор флавоноидов лихниса 24 мкг/кг (в объеме 0,6 мл/мышь диет, воды), внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз за 1 ч до иммобилизации на 24 ч (n=10).
Препарат сравнения - элеутерококка экстракт жидкий проявил выраженную противоязвенную активность на модели нейрогенного повреждения. Статистически значимое снижение в 2,5 раза среднего количества деструкций обусловлено подавлением генеза полосовидных и значительным уменьшением числа крупных язв (p<0,01) относительно таковых значений у мышей группы стресс-контроля (табл. 2, 3). Следует отметить статистически достоверное снижение числа животных со всеми видами язвенных поражений (70% против 100% контроля) и количества животных с крупными деструкциями (10% против 88,9% контроля, p<0,01). В результате выявленных изменений противоязвенная активность препарата сравнения составила 3,6 балла (табл. 2).
Антиульцерогенная активность флавоноидов в дозе 12 мкг/кг реализовалась в снижении среднего количества животных с язвами (70% против 100% контроля, p<0,01) и числа мышей с крупными деструкциями (20% против 88,9% контроля, p<0,01). В пользу противоязвенного действия флавоноидов в этой дозе свидетельствует статистически значимое уменьшение (в 6,2 раза) количества тяжелых повреждений слизистой желудка - крупных язв. Выявленные позитивные изменения обусловили значимую противоязвенную активность, которая составила 2,2 балла (табл. 2, 3).
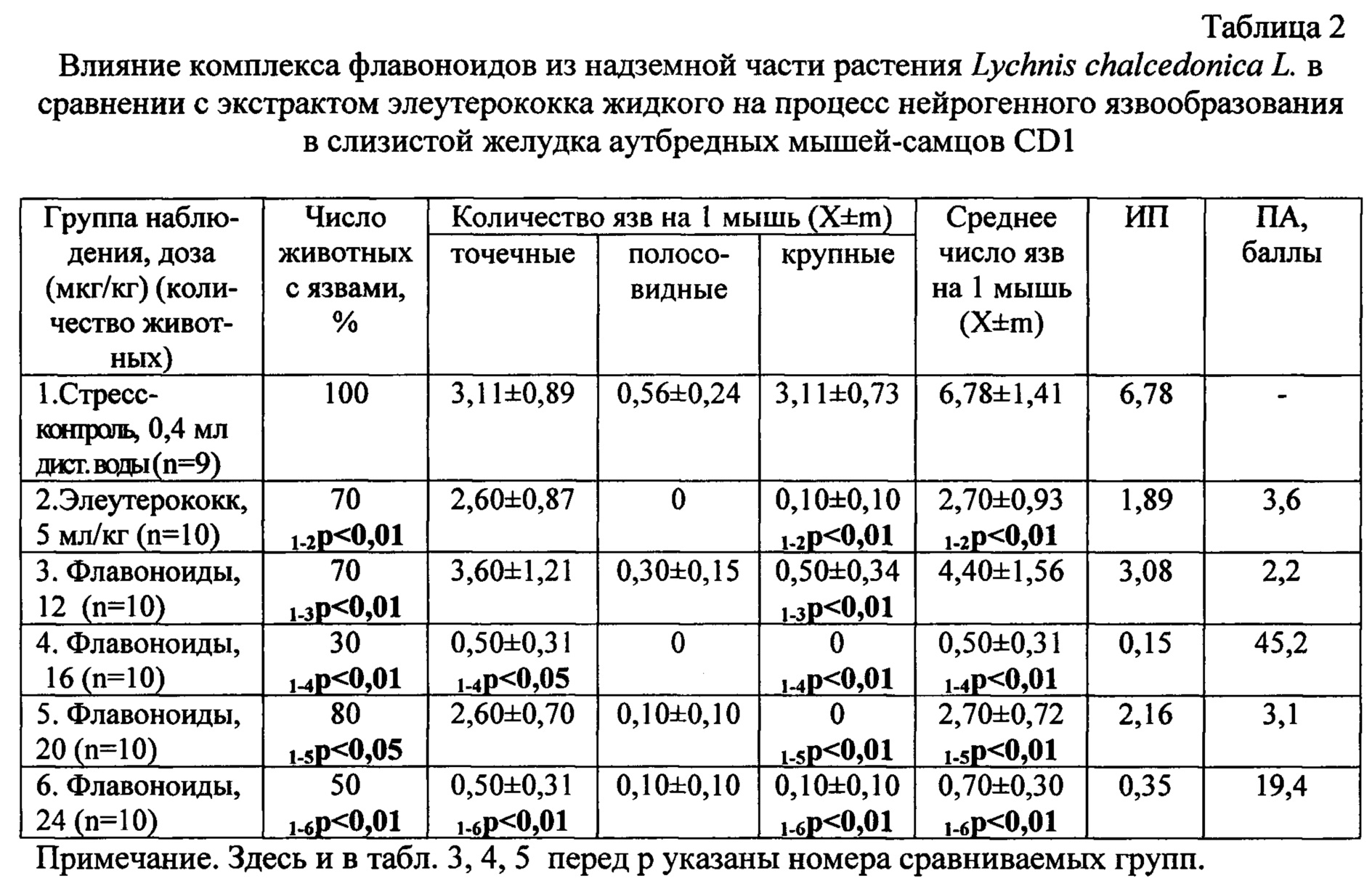
Применение флавоноидов в дозе 16 мкг/кг приводило к значительному снижению всех видов язвенных деструкций в слизистой желудка животных (табл. 2, 3). Отмечалось статистически значимое уменьшение количества мышей с язвами (30% против 100% контроля, p<0,01), числа животных с точечными повреждениями (30% против 77,8% контроля, p<0,01), подавление генеза полосовидных и крупных деструкций (табл. 2). При этом среднее количество язв оказалось в 13,6 раза (p<0,01) ниже аналогичного значения у нелеченых мышей, а противоязвенная активность составила 45,2 балла (табл. 2, 3).
В результате введения флавоноидов лихниса халцедонского в дозе 20 мкг/кг выявлено снижение количества животных со всеми видами деструкций (80% против 100%, p<0,05), уменьшение числа мышей с полосовидными язвами (10% против 55,6%, p<0,01), подавление образования крупных повреждений (табл. 2, 3). Кроме того, отмечено статистически достоверное снижение среднего количества язв в 2,5 раза по сравнению с соответствующим показателем стресс-контроля. Однако противоязвенная активность флавоноидов в дозе 20 мкг/кг составила 3,1 балла, что оказалось значительно ниже эффективности вещества в дозе 16 мкг/кг (табл. 2).
Введение флавоноидов в дозе 24 мкг/кг приводило к значительному снижению количества деструкций и степени язвенного повреждения слизистой желудка мышей (табл. 2, 3). Выявлено статистически достоверное уменьшение числа животных с язвами всех видов (50% против 100% стресс-контроля), количества мышей с точечными деструкциями (30% против 77,8%, p<0,01), полосовидными язвами (10% против 55,6%, p<0,01), крупными повреждениями (10% против 88,9%, p<0,01). Следует отметить значительное снижение количества точечных язв в 6,2 раза (p<0,01), крупных деструкций - в 31,1 (p<0,01) раза, вследствие чего произошло уменьшение среднего количества язв в 9,7 раза (p<0,01) относительно соответствующих значений у нелеченых мышей. Необходимо подчеркнуть повышение активности флавоноидов в дозе 24 мкг/кг, что превысило эффективность вещества в дозе 20 мкг/кг и составило 19,4 балла (табл. 2, 3).
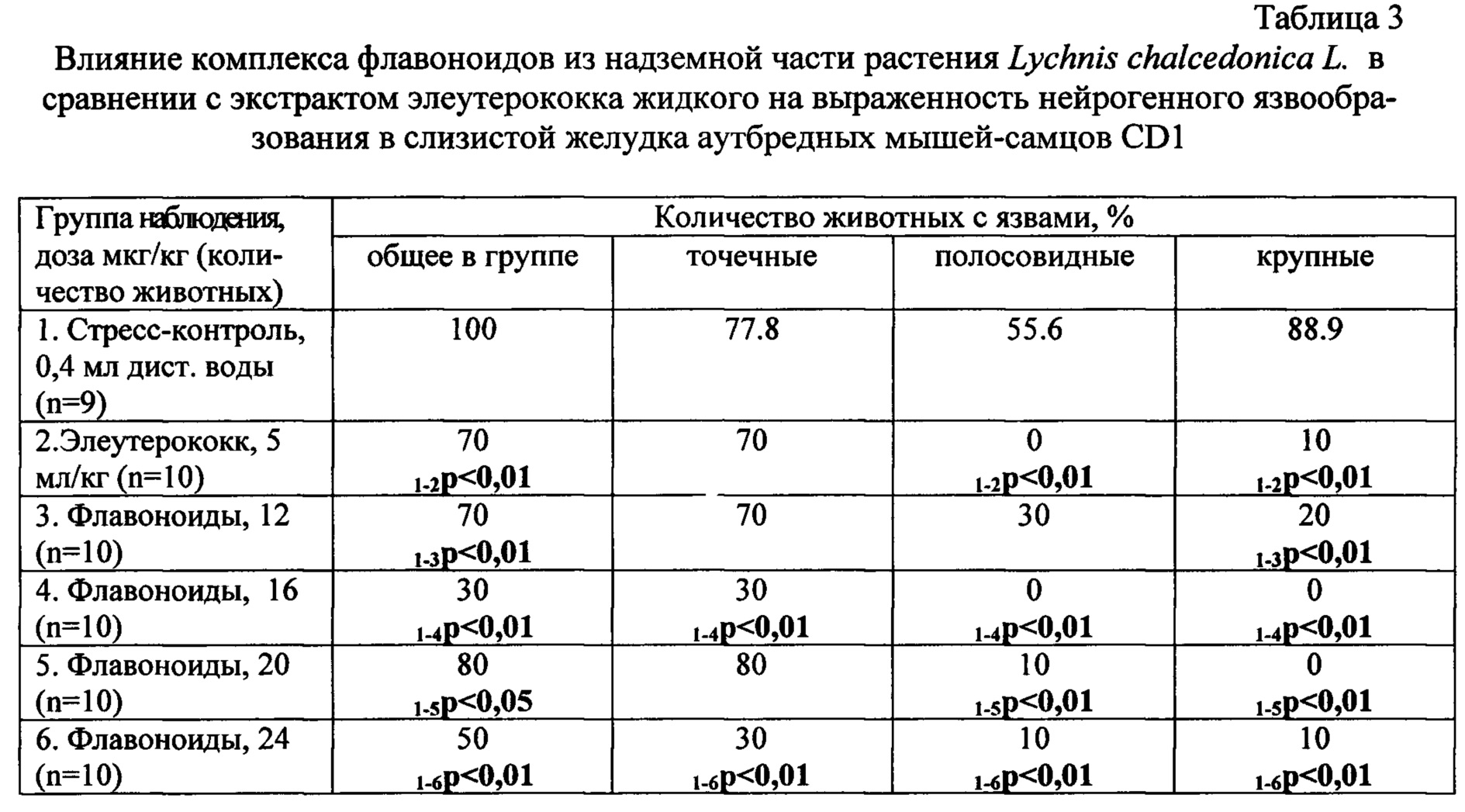
Таким образом, профилактическое курсовое введение флавоноидов во всех использованных дозах (12, 16, 20 и 24 мкг/кг) приводило к существенному повышению резистентности слизистой оболочки желудка мышей к повреждающему действию иммобилизационного стресса. Антиульцерогенное действие комплекса флавоноидов Lychnis chalcedonica L. в дозах 16 и 24 мкг/кг превышало активность препарата сравнения - адаптогена элеутерококка экстракта жидкого (5 мл/кг) на модели нейрогенного повреждения.
Пример 2
Изучение гастропротекторной активности комплекса флавоноидов из надземной части растения Lychnis chalcedonica L.- лихниса халцедонского в сравнении с метилурацилом при курсовом введении на модели индометацинового повреждения слизистой желудка у аутбредных мышей-самцов CD1.
Мышей распределяли на группы рандомизированно, используя в качестве критерия массу тела, так, чтобы индивидуальное значение массы не отклонялось от среднего значения в пределах одного пола более чем на ±10%.
В экспериментах использовали следующие группы аутбредных мышей-самцов CD1:
1. Животным вводили дистиллированную воду в объеме 0,3 мл/мышь внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз - по схеме (n=10);
2. Животным вводили метилурацил в дозе 500 мг/кг (в объеме 0,3 мл/мышь диет, воды) внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз - по схеме (n=10);
3. Животным вводили раствор флавоноидов лихниса в дозе 1600 мкг/кг (в объеме 0,3 мл/мышь диет, воды) внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз - по схеме (n=10);
4. Животным вводили раствор флавоноидов лихниса в дозе 160 мкг/кг (в объеме 0,3 мл/мышь диет, воды), внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз - по схеме (n=10);
5. Животным вводили раствор флавоноидов лихниса 32 мкг/кг (в объеме 0,3 мл/мышь диет, воды), внутрижелудочно через зонд в течение 4 сут однократно ежесуточно, последний раз - по схеме (n=10).
Представлена схема введения испытуемого вещества и ульцерогена: препарат - через 1 ч индометацин, 20 мг/кг - через 4 ч препарат - через 1 ч индометацин, 20 мг/кг. Введение индометацина вызывало развитие всех видов язвенных деструкций у 100% животных контрольной группы (табл. 4).
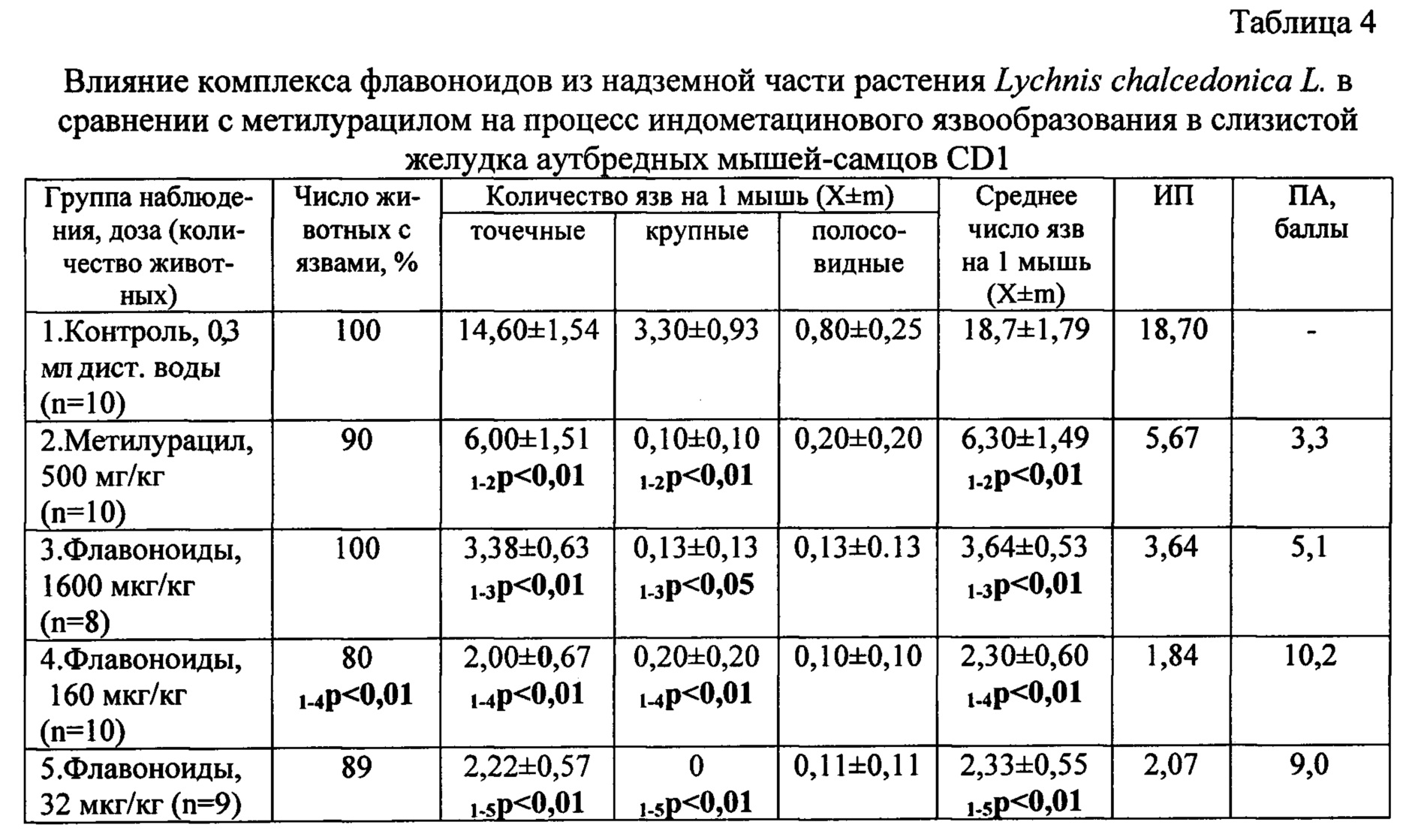
Препарат сравнения - метилурацил - проявил выраженную противоязвенную активность на модели индометацинового повреждения слизистой желудка у мышей. Статистически значимое снижение в 3,0 раза среднего количества язв обусловлено подавлением генеза крупных деструкций в 33,0 раза (p<0,01) и уменьшением числа точечных язв в 2,4 раза (p<0,01) по сравнению с соответствующими значениями у мышей контрольной группы (табл. 4). Следует отметить снижение числа животных с полосовидными поражениями (10% против 60% контроля, p<0,01) и количества животных с крупными деструкциями (10% против 80% контроля, p<0,01). В результате выявленных изменений противоязвенная активность препарата сравнения составила 3,3 балла (табл. 4, 5).
Антиульцерогенная активность флавоноидов в максимальной дозе 1600 мкг/кг реализовалась в снижении среднего количества язвенных деструкций в 5,1 раза (p<0,01), точечных повреждений - в 4,3 раза (p<0,01), числа крупных деструкций - в 25,4 (p<0,05) относительно аналогичных значений у нелеченых животных. В пользу противоязвенного действия флавоноидов в этой дозе свидетельствует статистически значимое уменьшение количества животных с полосовидными и крупными повреждениями слизистой желудка. Выявленные позитивные изменения обусловили значимую противоязвенную активность (5,1 балла) флавоноидов в дозе 1600 мкг/кг (табл. 4, 5).
Применение флавоноидов в дозе 160 мкг/кг приводило к значительному снижению язвенных деструкций в слизистой желудка животных (табл. 4, 5). Отмечалось статистически значимое уменьшение количества мышей с язвами (80% против 100% контроля, p<0,01), числа животных с точечными повреждениями (60% против 100% контроля, p<0,01), снижение генеза полосовидных (10% против 60% контроля, p<0,01) и крупных деструкций (10% против 80% контроля p<0,01). При этом число точечных повреждений статистически достоверно снизилось в 7,3 раза, крупных язв - в 16,5 раза (p<0,01), а среднее количество язв уменьшилось в 8,1 раза (p<0,01) ниже аналогичных значений у нелеченых мышей. Снижение дозы флавоноидов в 10 раз привело к увеличению активности до 10,2 балла (табл. 4).
В результате введения флавоноидов лихниса халцедонского в дозе 32 мкг/кг выявлено тенденция к снижению (89%) количества животных со всеми видами деструкций. При этом отмечалось уменьшение числа мышей с полосовидными язвами (11% против 60% контроля, p<0.01), подавление образования крупных деструкций (табл. 5). Кроме того, выявлено статистически достоверное снижение числа точечных деструкций в 6,6 раза, среднего количества язв - в 8,0 раза по сравнению с соответствующими показателями у животных контрольной группы. Противоязвенная активность флавоноидов в дозе 32 мкг/кг составила 9,0 балла, что оказалось ниже эффективности вещества в дозе 160 мкг/кг (табл. 4).

Таким образом, профилактическое курсовое введение флавоноидов во всех использованных дозах (1600, 160, 32 мкг/кг) приводило к существенному повышению резистентности слизистой оболочки желудка мышей к повреждающему действию нестероидного противовоспалительного средства. Антиульцерогенное действие флавоноидов Lychnis chalcedonica L. в дозах 1600, 160 и 32 мкг/кг превышало активность препарата сравнения - метилурацила (500 мг/кг) на модели индометацинового повреждения слизистой желудка.
Резюмируя полученные результаты двух серий экспериментов можно считать, что предлагаемое средство, содержащее комплекс флавоноидов Lychnis chalcedonica L. оказывает выраженное противоязвенное (гастропротективное) действие.
Источники информации
1. Бутов М.А. Об этиологии и патогенезе язвенной болезни // Экспериментальная и клиническая гастроэнтерология. - 2003. - №5. - С. 23-27.
2. Васильев Ю.В. Современная терапия язвенной болезни, ассоциируемой с Helicobacter pilori // Трудный пациент. - 2007. - №6-7. - С. 35-41.
3. Васильев Ю.В. Язвенная болезнь // Избранные главы клинической гастроэнтерологии / под ред. Л.Б. Лазебника. М.: Анахарсис, 2005. - С. 82-112.
4. Добряков Ю.И. Скрининговый метод оценки антистрессорного действия препаратов // Стресс и адаптация: Тез. Всесоюзного симпозиума. - Кишинев, 1978. - С. 172-173.
5. Заводская И.С., Морева Е.В. Фармакологический анализ механизмов стресса и его последствий. - Л.: Медицина, 1981. - 212 с.
6. Кривошеев А.Б., Хван Л.А., Филиппова О.А. Прогноз и профилактика осложнений язвенной болезни // Сибирский вестник гепатологии и гастроэнтерологии. - 2006. -№20. - С.60-62.
7. Крылова С.Г. Растения Сибири и Дальнего Востока в терапии язвенной болезни желудка и двенадцатиперстной кишки: автореф. дис. … д-ра. мед. наук. - Томск, 2005. - 50 с.
8. Крылова С.Г., Зуева Е.П., Зибарева Л.Н., Амосова Е.Н., Разина Т.Г. Противоязвенная активность экстрактов экдистероидсодержащих растений родов Lychnis и Silene семейства Caryophyllaceae // Бюллетень экспериментальной биологии и медицины. - 2014. - Т. 158., №8. - С. 190-194.
9. Лакин Г.Ф. Биометрия. - М.: Высшая школа, 1980. - 293 с.
10. Машковский М.Д. Лекарственные средства: 15-е изд. - М.: ОО «Издательство Новая Волна», 2008. - 1206 с.
11. Руководство по проведению доклинических исследований лекарственных средств / Под ред. А.Н. Миронова. - М., 2012. - Часть первая. - 944 с.
12. Смолякова И.М., Авдеенко С.Н., Калинкина Г.И., Зибарева Л.Н. Исследование химического состава Лихниса Халцедонского, культивируемого в Западной Сибири. Сообщение 1. Хроматографическое исследование фенольных соединений и экдистероидов // Химия растительного сырья. - 2010. - №3. - С. 91-93.
13. European Convention for the Protection of Vertebrate Animals used for Experimental and other scientific purposes. - Strasburg: Council of Europe, 1986. - 51 p.
14. Pauls F., Wick A.M., Mac. Key E.M. et al. An assau method for antiulcer substances // Gastroenterology. - 1947. - №8. - P. 774-782
Средство, обладающее гастропротекторной активностью, представляющее собой комплекс 4-х флавоноидов, выделенный из надземной части растения Lychnis chalcedonica L. 5-кратной экстракцией 70% этанолом в соотношении сырье:экстрагент 1:22.5, с последующей экстракцией н-бутанолом, очисткой выпавшего осадка из водной фракции системой растворителей этил ацетат : этанол в соотношении 3:1.