Результат интеллектуальной деятельности: СРЕДСТВО С АНТИТРОМБОТИЧЕСКОЙ АКТИВНОСТЬЮ
Вид РИД
Изобретение
Сердечно-сосудистые заболевания - главная причина смертности во всем мире; среди них тромбоэмболические осложнения, связанные с формированием тромба в сердечно-сосудистой системе. К формированию тромба приводят - застой крови, изменения в свертывании крови, повреждения сосудистой стенки и изменения в концентрациях лейкоцитов или тромбоцитов. Изобретение относится к области медицины и может быть использовано для создания эффективного средства для профилактики и лечения у людей венозных тромбозов разного происхождения (тромбозы глубоких вен, инфаркты, инсульты).
Система гемостаза организма млекопитающих выполняет защитную функцию. Последовательная активация на фосфолипидных поверхностях (тканевый фактор на клетках или активированные тромбоциты) факторов свертывания крови, сопровождающаяся включением механизмов положительной и отрицательной обратной связи, приводит к образованию тромбина, при этом антикоагулянтная система ингибирует избыточную генерацию тромбина, а система фибринолиза обеспечивает лизис сгустка. Нарушение баланса прокоагулянтных и антикоагулянтных механизмов приводит к тромбозам или кровотечениям. При тромбозах в сосудах появляются сгустки крови, содержащие в основном фибрин-тромбоциты (артериальный тромбоз) или фибрин-эритроциты (венозный тромбоз) [1].
В настоящее время для профилактики и лечения тромбозов, наряду с другими лекарственными средствами, используют и антикоагулянты, обладающие и антитромботической активностью. Однако все современные антикоагулянты, независимо от механизма действия (прямые ингибиторы активности тромбина или активированного фактора X и активаторы антитромбина - препараты гепаринов, по структуре это сульфатированные полисахариды), обладают рядом побочных эффектов, основным из которых является способность вызывать кровотечения. Поиск новых соединений в дополнение к препаратам гепарина (нефракционированный гепарин с одинаковой антитромбин-опосредованной ингибиторной активностью против тромбина и фактора Ха; низкомолекулярные гепарины с меньшей, чем у нефракционированного гепарина, антитромбин-опосредованной ингибиторной активностью в отношении тромбина; синтетический пентасахарид - фондапаринукс - с высокой антитромбин-опосредованной ингибиторной активностью в отношении фактора Ха, без активности против тромбина), но с меньшей геморрагической активностью, осуществляют и в ряду сульфатированных полисахаридов растительного, животного происхождения, например среди морских беспозвоночных или водорослей, а также среди тканей наземных растений [2, 3]. Однако структурная неоднородность полисахаридов из водорослей затрудняет получение соединений с программируемой постоянной высокой активностью. Поэтому некоторые авторы выбирают в качестве субстанции для последующего химического модифицирования полисахариды с линейной структурой, выделенные из наземных растений [4]. Например, целлюлоза - это полисахарид, макромолекула которого построена из повторяющихся звеньев - остатков β-D- глюкопиранозы с общей формулой (С6Н10О5)n, являющийся самым распространенным органическим соединением, которое выделяют из травянистых и древовидных растений.
Наиболее близким по сущности и назначению к предлагаемому изобретению является антитромботическое средство - сульфат целлюлозы с молекулярной массой 80000 Да [5], полученный из частично гидролизованной целлюлозы пихты сульфатированием комплексом пиридина и хлорсульфоновой кислоты, гидролиз целлюлозы осуществляли по методике, описанной в патенте РФ №2203995 [6].
Недостатком данного изобретения является невысокая антитромботическая активность сульфатированного полисахарида. Недостаток изобретения обусловлен видом растительного сырья, используемого для выделения целлюлозы, и недостаточной величиной молекулярной массы сульфата целлюлозы (80000 Да), что связано с жесткими условиями проведения частичного гидролиза исходной целлюлозы.
Известно, что антикоагулянтная активность полисахаридов зависит от ряда структурных параметров - степени сульфатирования, расположения функционально активных групп, плотности заряда, молекулярной массы сульфатов полисахаридов, с увеличением которой антикоагулянтная активность полисахаридов, полученных из растительного сырья, иногда увеличивается [7].
Задача изобретения - расширение ассортимента антитромботических средств на основе растительного полисахарида с высокой антитромботической активностью.
Технический результат - получено средство с высокой антитромботической активностью на основе химически модифцированной целлюлозы соломы пшеницы.
Технический результат достигается тем, что антитромботическое средство на основе сульфатированного целлюлозного материала представляет собой сульфат целлюлозы с молекулярной массой 116000 Да, полученный из частично гидролизованной целлюлозы соломы пшеницы путем сульфатирования хлорсульфоновой кислотой в пиридине.
В отличие от прототипа в предлагаемом изобретении при получении антитромботического средства частичный гидролиз целлюлозы соломы пшеницы осуществляют при температуре 100°C в течение 1 ч, в прототипе - более жесткие условия: температура 120°C, продолжительность гидролиза 2 ч.
Сульфатирование частично гидролизованной целлюлозы соломы пшеницы для получения антитромботического средства осуществляли по методике, описанной в патенте РФ №2426746 [8], следующим образом.
Целлюлозу, выделенную из соломы пшеницы, предварительно подвергали мягкому гидролитическому воздействию водного раствора состава: 6,4% перекиси водорода; 23,6% уксусной кислоты, 2%-ной серной кислоты, при гидромодуле, равном 10; температуре 100°C в течение 1 ч. Затем целлюлозу подвергали предварительному набуханию в среде пиридина не менее 12 ч. Подготовленную таким образом целлюлозу при 10-15°C добавляли к комплексу пиридина и хлорсульфоновой кислоты. Сульфатирование проводили при 80-85°C в течение 2-2,5 ч. Натриевую соль сульфата целлюлозы соломы пшеницы выделяли из реакционной массы путем декантации пиридина, нейтрализацией промытого ледяной водой вязкого остатка 6%-ным водным раствором гидроксида натрия до рН 8-9, декантацией от образовавшейся гелеобразной натриевой соли сульфата целлюлозы водного раствора, растворением соли в воде и высаживанием 3-кратным объемом этанола. В результате получали водорастворимую натриевую соль сульфата целлюлозы с содержанием основного вещества 98% (масс.), содержанием серы (ωs) 14,1% (масс.); степенью замещения (CЗs) 1,3 и молекулярной массой ММ 116000 Да. Установлено методом ЯМР 13С, что все гидроксильные группы целлюлозы при атоме углерода С6 замещены на сульфатные группы, а при атоме С2 - частично замещены на сульфатные группы.
Степень замещения в образцах находили по уравнению: CЗs=162⋅ωs/3200-ωs⋅103, где ωs - содержание серы, % [9]. Содержание серы определяли на элементном анализаторе Flash ЕА-1112 (Thermo Quest Italia).
ЯМР 13С спектры исходной и сульфатированной целлюлозы соломы пшеницы сняты при температуре 25°С с использованием спектрометра Bruker Avance III 600 МГц в D2O с привязкой к дейтериевому резонансу растворителя.
Молекулярно-массовое распределение (ММР) исследовали на хроматографе Agilent 1200с колонкой PL aguagel - ОН 40, 300⋅7,5; детектор рефтактометрический. В качестве растворителя и элюента использовали водный раствор 0,1 М LiNO3.
Специфические антикоагулянтные активности полученной субстанции сульфата целлюлозы (СЦ) оценивали по времени свертывания плазмы крови человека в коагулологических тестах активированного частичного тромбопластинового времени (АЧТВ) и с использованием теста РеаКлот-Гепарин (НПО «Ренам», Москва). Для расчета антитромбиновой (aIIa) и антифактора Ха (аХа) активностей использовали калибровочные кривые Международного стандарта нефракционированного гепарина (НФГ).
Высокая антитромбиновая активность СЦ позволила провести оценку антитромботической активности. Исследование проводили с использованием лабораторных животных (крыс), которых получали из питомника РАМН «Столбовая2». Все опыты осуществляли с соблюдением «Правил для проведения работ с использованием экспериментальных животных» (Приказ Минздрава СССР от 12.08.1977 №755 «О мерах по дальнейшему совершенствованию организационных форм работы с использованием экспериментальных животных) и «Правил лабораторной практики» (приложение к Приказу Минздравсоцразвития России от 23 августа 2010 г. N 708н). В качестве препарата сравнения использовали Международный стандарт НФГ. Для оценки антитромботической активности использовали модель венозного тромбоза у крыс по S.Wessler [10]. С увеличением дозы СЦ и НФГ увеличивалась антитромботическая активность. Для достижения 50% ингибирование роста тромба СЦ требовалось в 2 раза больше, чем НФГ.
Изобретение поясняется следующими примерами.
Пример 1. Определение антитромбиновой активности субстанции СЦ. К смеси плазмы и АЧТВ-реагента (0,15 мл) (НПО "Ренам") добавляли раствор СЦ или НФГ (Международный стандарт) в конечных концентрациях 0,0005-0,0025 мкг/мл. Через 3 мин инкубирования при 37°C добавляли 0,02 мл 0,025 М раствора CaCl2 и на коагулометре «Минилаб 701-М» фиксировали время (сек) появления фибринового сгустка. Показано влияние разных концентраций СЦ на время свертывания плазмы человека в тесте АЧТВ. Сравнивая показания кривых СЦ концентрация-время свертывания плазмы в 15 независимых определениях с калибровочными кривыми НФГ, определяли антитромбиновую (aIIa) активность СЦ [10]; aIIa активность СЦ составила 93,8±1,0 ЕД/мг.
Пример 2. Определение антифактора Ха активности субстанции СЦ. К смеси плазмы и раствора фактора Ха (0,16 мл; тест РеаКлот-Гепарин, НПО "Ренам") добавляли СЦ или НФГ (Международный стандарт НФГ) в конечных концентрациях 0,0002-0,001 мкг/мл. Через 2 мин инкубирования при 37°C добавляли 0,02 мл 0,035 М раствора CaCl2 и на коагулометре «Минилаб 701-М» фиксировали время (сек) появления фибринового сгустка. Показано влияние СЦ на время свертывания плазмы человека в тесте РеаКлот-Гепарин. Сравнивая показания кривых СЦ концентрация-время свертывания плазмы в 15 независимых определениях с калибровочными кривыми НФГ, определяли антифактор Ха (аХа) активности СЦ [10]; аХа активность СЦ составила 9,9±0,6 ЕД/мг.
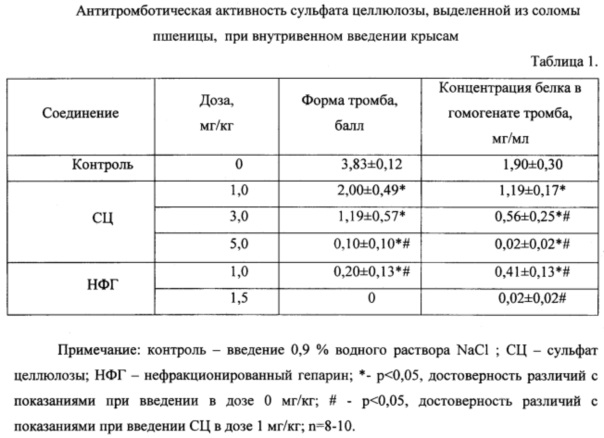
Пример 3. Антитромботическую активность СЦ оценивали, моделируя венозный тромбоз по Wessler S. и др. [11] у 55 крыс самцов Wistar массой 180-350 г. Для наркоза крысам внутрибрюшинно вводили нембутал в дозе 60 мг/кг. Растворы СЦ в дозах 1, 3 и 5 мг/кг вводили в левую яремную вену (препарат сравнения НФГ вводили в дозах 1 и 1,5 мг/кг), а через 15 мин - активированную стеклом сыворотку человека. Затем перевязывали нитью участок противоположной вены, не использованной для введения антикоагулянтов, через 15 мин вырезали перевязанный участок вены и извлекали содержимое в небольшую емкость. Эффективность антитромботической активности оценивали: 1) в баллах от 0 (тромба нет) до 4 (один большой тромб) по форме тромба, извлеченного из перевязанного участка вены; 2) по концентрации белка в гомогенате тромба, измеренной по Лоури; содержание белка в испытуемой пробе устанавливали по калибровочной кривой, построенной с раствором фибриногена человека (Sigma Aldrich). С увеличением дозы СЦ снижались: форма тромбов с 2,00±0,49 до 0,10±0,10 баллов и концентрация белка в гомогенатах тромбов с 1,19±0,17 до 0,02±0,02 мг/мл (табл. 1). Отмечали достоверные различия формы тромбов между показаниями при введении физиологического раствора и СЦ, начиная с дозы 3 мг/кг.
Преимуществом заявляемого средства в сравнении с прототипом является большая на 10 ЕД/мг антитромбиновая активность и меньшая в 2 раза аХа активность, что может привести к меньшей геморрагической активности при внутривенном введении сульфата целлюлозы крысам.
Список литературы
1. Nakamura М., Yamada N., Ito М. Current management of venous thromboembolism in Japan: Current epidemiology and advances in anticoagulant therapy. // J Cardiol., 2015. - 66(6). - 451-459.
2.  P.A. Perspective on the use of sulfated polysaccharides from marine organisms as a source of new antithrombotic drugs. // Mar Drugs. - 2015. - 13(5). - 2770-2784.
P.A. Perspective on the use of sulfated polysaccharides from marine organisms as a source of new antithrombotic drugs. // Mar Drugs. - 2015. - 13(5). - 2770-2784.
3.  K., Kovac Besivic E., Njksic H. et al. Anticoagulant activity of some Artemisia dracunculus leaf extracts // Bosn J Basic Med Sci. - 2015. - 15(2). - 9-14.
K., Kovac Besivic E., Njksic H. et al. Anticoagulant activity of some Artemisia dracunculus leaf extracts // Bosn J Basic Med Sci. - 2015. - 15(2). - 9-14.
4. Ehmann H.M., Mohan Т., Koshanskaya M. et al. Design of anticoagulant surfaces based on cellulose nanocrystals // Chem. Commun. (Camb.). 2014.- 50 (86). - P. 13070-13072.
5. Патент РФ №2571555. Антитромботическое средство из целлюлозы пихты сибирской // Кузнецова С.А., Дрозд Н.Н., Савчик Е.Ю., Мифтахова Н.Т., Васильева Н.Ю., Макаров В.А., Кузнецов Б.Н. Опубл. 20.12.2015.
6. Патент РФ №2203995. Способ получения микрокристаллической целлюлозы // Данилов В.Г., Яценкова О.В., Кузнецова С.А., Кузнецов Б.Н. Опубл. 10.05.2003.
7. Arata P., Quintana I., Canelon D. et al. Chemical structure and anticoagulant activity of highly pyruvylated Chemical structure and anticoagulant activity of highly pyruvylated sulfated galactans from tropical green seaweeds of the order Bryopsidales // Carbohydr Polym. 2015. - 122. - P. 376-386.
8. Патент РФ №2426746. Способ получения сульфатированной целлюлозы // Васильева Н.Ю., Кузнецова С.А., Кузнецов Б.Н., Скворцова Г.П., Данилов В.Г. Опубл. 20.08.2011.
9. Торлопов М.А. Получение порошковых материалов деструкцией целлюлозы кислотами Льюиса и их модификация. Сульфатирование порошковых материалов, полученных деструкцией целлюлозы кислотами Льюиса // М.А. Торлопов, С.В. Фролова // Химия растительного сырья. - 2008. - №3. - С 63-67.
10. Макаров В.А., Спасов А.А., Плотников М.Б., Чернышева Г.А., Блозерская Г.М., Васильева Т.М., Дрозд Н.Н. и др. // Методические указания по изучению фармакологических веществ, влияющих на гемостаз. С. 453-479 // Руководство по проведению доклинических исследований лекарственных средств. Часть первая // Под ред. А.Н. Миронова.- М.: Гриф и К. 2012. - 944 с.
11. Wessler S., Reimer S.M., Sheps М.С. Biologic assay of a thrombosis-inducing activity in human serum // J. Appl Physiol 1959. - V.14. - №1. - P. 943-946.