Результат интеллектуальной деятельности: Способ комбинированного термохимиолучевого лечения больных местнораспространенным раком шейки матки
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к онкологии, и может быть использовано для лечения больных местнораспространенным раком шейки матки (МРРШМ).
Рак шейки матки (РШМ) занимает второе место в структуре онкологических заболеваний у женщин, уступая лишь раку молочной железы (WHO, 2013). В Российской Федерации на долю данной патологии приходится 5,3% [1], причем 68% из них составляет МРРШМ [2]. Стоит отметить, что за последние 5 лет в России неуклонно растет число заболевших МРРШМ в возрасте до 40 лет [3].
В настоящее время основным методом лечения МРРШМ является химиолучевое лечение. Доказано, что цитостатики усиливают лучевое повреждение опухолевых клеток за счет нарушения механизма репарации ДНК, синхронизации вступления опухолевых клеток в фазы клеточного цикла, которые наиболее чувствительны к лучевому воздействию. Также было отмечено, что цитостатики уменьшают число опухолевых клеток, находящихся в фазе покоя, и способствуют девитализации резистентных к лучевой терапии опухолевых клеток, находящихся в гипоксии [7]. Широко обсуждается вопрос о неоадъювантной химиотерапии (НАХТ).
По данным разных авторов наиболее эффективны схемы с применением препаратов платины [5]. Установлено, что у больных МРРШМ в результате использования химиолучевого лечения с включением схемы цисплатин + гемцитабин в неоадъювантном режиме с последующей сочетанной лучевой терапией по радикальной программе достигается более эффективный регресс первичного очага (общий эффект химиотерапии составляет 58%) [8].
В то же время, результаты лечения больных МРРШМ остаются неудовлетворительными, 5-летняя выживаемость у этих больных составляет 65%, варьируя от 15 до 80% в зависимости от распространения опухолевого процесса [4].
В связи с этим, в последние годы для повышения эффективности как химиотерапии, так и лучевой терапии, широко используются модификаторы биологических реакций. Общепризнанным и самым мощным радиомодификатором является локальная гипертермия, то есть нагрев опухоли в определенном температурно-экспозиционном режиме. В большинстве исследований термолучевое лечение в 1,5-2 раза чаще приводит к местному излечению, чем только СЛТ. Привлекает универсальность этого модификатора. При нагреве до 39-40°С, гипертермия приводит к усилению кровотока, тем самым улучшая оксигенацию опухоли. При достижении в опухоли температуры свыше 42°С происходит подавление процессов репарации - частичная или полная блокировка восстановления сублетальных и потенциально летальных постлучевых повреждений. Анализ результатов лечения онкологических больных показал, что гипертермическое воздействие при сочетании с лучевой терапией предотвращает диссеминацию опухолевых клеток и усиливает метастазирование опухоли [9].
В то же время имеются лишь единичные исследования I-II фазы, посвященные химиолучевому лечению больных РШМ в условиях локальной гипертермии. Рандомизированное клиническое исследование III фазы (AnInternationalMultiCenterPhase IIIStudyofChemoradiotherapyVersusChemoradiotherapyPlusHyperthermiaforLocallyAdvancedCervicalCancer) инициировано в 2004, закрыто в 2013 из-за медленного набора пациентов [10].
Неудовлетворительные результаты лечения МРРШМ предопределяют продолжение совершенствования способов комбинированного лечения, поиска новых радиомодификаторов и дополнительных факторов воздействия на опухоль.
Наиболее близким к заявленному является способ, характеризующийся тем, что за 2 недели до проведения сочетанной лучевой терапии проводят 2 курса неоадъювантной (предлучевой) химиотерапии с перерывом в 14 дней по схеме цисплатин в дозе 75 мг/м2 в 1 день и гемцитабин в дозе 1250 мг/м2 в 1 и 8 дни с последующей стандартной лучевой терапией по радикальной программе - дистанционная гамма-терапия на область малого таза и зону регионарного лимфооттока в стандартном режиме фракционирования, РОД 2,0 Гр, до суммарной очаговой дозы 46-48 Гр, внутриполостная лучевая терапия в РОД 5,0 Гр до суммарной дозы 50 Гр. [6]. При этом отрицательным моментом данного метода является наличие побочных эффектов от химиотерапии, которые требуют корригирующей терапии после проведения лечения.
Новый технический результат - повышение непосредственной эффективности за счет увеличения удельного веса полных ответов на лечение, благодаря более быстрому регрессу первичного очага, и повышение качества жизни больных за счет более быстрого купирования болевого синдрома и прекращения кровотечения из опухоли.
Для достижения нового технического результата в способе комбинированного лечения больных местно-распространенным раком шейки матки, включающем проведение курса СЛТ - дистанционной гаммы-терапии в стандартном режиме фракционирования дозы РОД 2 Гр, 5 фракций в неделю, 20-23 сеанса с СОД 46 Гр, внутриполостной лучевой терапии с энергией 1,25 МэВ в режиме крупного фракционирования дозы РОД 5 Гр, 2 фракции в неделю, 10 сеансов с СОД 50 Гр, введение цисплатина в дозе 40 мг/м2, 1 раз в неделю, с достижением суммарной дозы не менее 300 мг, внутриполостной лучевой терапии с энергией 1,25 МэВ в режиме крупного фракционирования дозы РОД 5 Гр, 2 фракции в неделю, 10 сеансов с СОД 50 за 2 часа до сеанса внутриполостной лучевой терапии проводят локальную гипертермию при температуре 42-43°C в течение 40-60 минут, 10 сеансов.
Новым в способе является использование локальной гипертермии, как дополнительного модификатора лучевой терапии при лечении местнораспространенного рака шейки матки, что позволяет улучшить показатели непосредственной эффективности, за счет более быстрого регресса первичного очага и достижения более высокого удельного веса полных ответов на лечение, повышения качества жизни за счет быстрого купирования клинической симптоматики - болевого синдрома и кровотечения.
Предлагаемый способ был разработан и апробирован на базе гинекологического отделения ФГБНУ «Томский НИИ онкологии». Клиническая апробация метода была проведена у 12 больных местно-распространенным раком шейки матки II-III стадий. Средний возраст пациенток составил 47,7±1,2 лет (31-73 года). У всех больных был выявлен плоскоклеточный рак шейки матки II-III стадии, умеренной и низкой степени дифференцировки. Группой сравнения послужили 42 больных местнораспространенным плоскоклеточным раком шейки матки умеренной и низкой степени дифференцировки опухоли, средний возраст больных составил 48,0±1,6 лет (25-74 года). Все пациентки проходили химиолучевое лечение, включающее СЛТ с еженедельным введением цисплатина. Дистанционную гамма-терапию проводили на линейном ускорителе 6,0 МэВ, в стандартном режиме фракционирования дозы - РОД 2 Гр, 5 фракций в неделю, 20-23 сеанса с СОД 46 Гр, внутриполостную на аппарате MultiSourse UDR с энергией 1,25 МэВ в режиме крупного фракционирования дозы - РОД 5 Гр, 2 фракции в неделю, 10 сеансов с СОД 50 Гр. Введение цисплатина проводилось в дозе 40 мг/м2, 1 раз в неделю, с достижением суммарной дозы не менее 300 мг. В основной группе всем пациенткам 2 раза в неделю, за 2 часа до сеанса внутриполостной лучевой терапии проводили локальную гипертермию при температуре 42-43°C в течение 40-60 минут, 10 сеансов.
У всех больных исследуемых групп до начала лечения и при завершении лечения проводили оценку объема первичной опухоли шейки матки. При первичном осмотре у 57,2% больных МРРШМ размер шейки матки с опухолью превышал 4 см в диаметре. Размеры опухоли от 2-х до 4-х см имели 37,1% пациенток, шейка матки с опухолью размером до 2-х см диагностирована у 9 больных (5,7%). Во всех группах преимущественно встречались опухоли более 4-х см, причем в основной группе больных удельный вес шейки матки с опухолью более 4-х см был выше по сравнению с контрольной группой. Опухоль шейки матки до 2-х см наблюдалась у 10%.
Оценку эффективности проведенного лечения проводили у всех больных (Фиг. 1). В основной группе объективный ответ составил 100%, полная регрессия отмечалась у 40% пациенток, частичная у 60%. В контрольной группе у 7% больных отмечалось прогрессирование заболевания, а в 5% случаев стабилизация процесса.
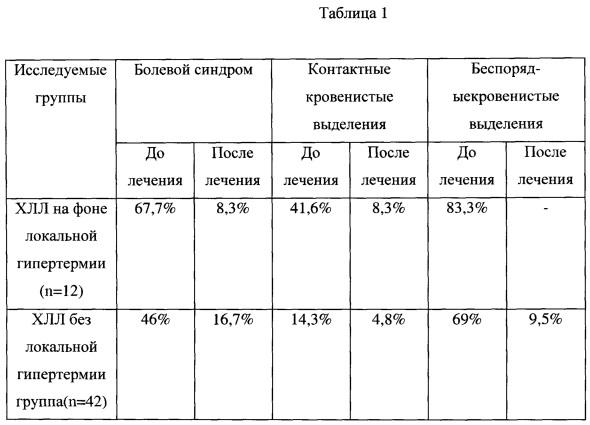
У всех больных была проведена оценка качества жизни больных по клиническим проявлениям МРРШМ - болевому синдрому и кровянистым выделениям из половых путей (таблица 1).
Как видно из представленных данных, болевой синдром у пациенток основной группы сохранился только у 8,3% больных, в контрольной группе этот процент был в 2 раза больше и составил 16,7%. Контактные кровянистые выделения из половых путей у пациенток основной группы после лечения сохранялись у 8,3% больных, беспорядочные же кровянистые выделения из половых путей после лечения вообще не отмечались ни у одной пациентки основной группы, в отличие от контрольной, где они определялись у 9.5% больных. Результаты свидетельствуют о лучшем качестве жизни больных, получивших химиолучевое лечение в условиях локальной гипертермии. Более высокие показатели, по-видимому, связаны с лучшим воздействием ХЛЛ в условиях локальной гипертермии на опухоль, что способствует устранению симптомов, вызванных наличием опухолевого процесса, и тем самым обуславливает лучшее качество жизни больных.
Учитывая, что все больные получили сочетанную лучевую терапию, проведена оценка частоты и степени выраженности лучевых реакций, которые оценивались по шкале лучевых повреждений RTOG/EORTC (1995). Лучевые реакции, развившиеся у больных МРРШМ изучаемых групп, представлены в табл. 2.
Было выявлено, что хотя у больных основной группы имеются несколько более выраженные острые лучевые реакции, но их удельный вес достоверно не отличался от контрольной группы. В большинстве случаев тяжесть осложнений не превышала 1-2 степени. Лучевые реакции хорошо купировались на фоне коррекции уросептическими препаратами, иммуномодуляторами, обработки слизистой влагалища антисептиками и мазями, обладающими противовоспалительным и регенерирующим эффектами, и не требовали прекращения лечения.
Таким образом, предлагаемый способ позволяет повысить эффективность лечения за счет увеличения удельного веса полных ответов на лечение, в результате, более быстрого регресса первичного очага и улучшения качества жизни больных за счет купирования болевого синдрома и прекращения кровянистых выделений из половых путей, без увеличения удельного веса лучевых реакций. Способ малозатратен, легкодоступен и является перспективным для применения в специализированных стационарах.
Предлагаемый способ иллюстрируется клиническим примером
Больная К., 47 года, находилась на лечении в гинекологическом стационаре НИИ онкологии с диагнозом: рак шейки матки IIb стадии (T2bNxMo), эндофитная форма роста, маточно-параметральный вариант. Из анамнеза: больную беспокоят кровянистые выделения из половых путей в течение 3-х месяцев. В 1997 г. у пациентки была выявлена эрозия шейки матки, лечение которой не проводилось. При поступлении локальный статус: шейка матки бочкообразно раздута, с язвенно-некротическим дефектом, более 4 см в диаметре, обильно кровоточащем при контакте. Матка отклонена кзади, крупная. Имеется инфильтрация сводов, не доходящая до стенок таза.
Морфологическая верификация биопсийного материала шейки матки: плоскоклеточный умеренно дифференцированный рак шейки матки.
Проведено комплексное обследование, включающее УЗИ и МРТ органов малого таза, органов брюшной полости и забрюшинных лимфатических узлов, рентгенографию легких и молочных желез, ректороманоскопию, цистоскопию. Отдаленных метастазов и поражения соседних органов не обнаружено.
Пациентке проведено лечение согласно предлагаемому способу: СЛТ - дистанционной гаммы-терапии в стандартном режиме фракционирования дозы - РОД 2 Гр, 5 фракций в неделю, 23 сеанса с СОД 46 Гр, внутриполостной лучевой терапии с энергией 1,25 МэВ в режиме крупного фракционирования дозы - РОД 5 Гр, 2 фракции в неделю, 10 сеансов с СОД 50 Гр, введение цисплатина в дозе 40 мг/м2, что составило 55 мг/м2, 1 раз в неделю, с достижением суммарной дозы не менее 220 мг, внутриполостную лучевую терапию, за 2 часа до сеанса внутриполостной лучевой терапии проводят локальную гипертермию при температуре 42-43°C, в течение 40-60 минут проводят процедуру локальной гипертермии, 2 раза в неделю, 10 сеансов. При присоединении в/п лучевой терапии, с сеансами гипертермии отмечалась лейкопения 2-3 степени, анемия 1 степени. Лучевой цистит. Проводилась медикаментозная коррекция. Пациентка перенесла лечение удовлетворительно. Клинический эффект после окончания химиолучевого лечения наблюдался в виде полной регрессии опухоли. В настоящее время срок наблюдения составляет 15 месяцев, прогрессирования заболевания нет.
Приложение
Фиг. 1 Эффективность проведенного лечения у больных МРРШМ исследуемых групп У всех больных была проведена оценка качества жизни больных по клиническим проявлениям МРРШМ- болевому синдрому и кровянистым выделениям из половых путей (таблица 2).
Таблица 1. Динамика изменений основных клинических проявлений МРРШМ у больных исследуемых групп
Таблица 2. Лучевые реакции у больных изучаемых групп
тоящее время срок наблюдения составляет 15 месяцев, прогрессирования заболевания нет.

Источники информации
1. Статистика злокачественных новообразований в России и странах СНГ в 2012 году / Под ред. академика РАН и РАМН М.И. Давыдова и д.б.н. Е.М. Аксель. - М.: Ассоциация директоров центров и институтов онкологии, радиологии и рентгенологии государств-участников Содружества Независимых Государств - Российский онкологический научный центр имени Н.Н. Блохина. - 2014. - ил. – 226.
2. Крейнина Ю.М., Титова В.А., Добровольская Н.Ю., Болтенко А.И. Современные подходы к терапии рецидивов и метастазов рака шейки матки // Мед. радиол, и радиац. безопасность. 2007. - Т. 52. - №5. - С. 36-45.
3. Злокачественные новообразования в России в 2014 году (заболеваемость и смертность) / Под ред. А.Д. Каприна, В.В. Старинского, Г.В. Петровой. - М.: МНИОИ им. П.А. Герцена - филиал ФГБУ «ФМИЦ им. П.А. Герцена» Минздрава России. - 2015. - илл. - 250 с.
4. Марьина Л.А., Кравец О.А., Нечушкин М.И. Сочетанная лучевая терапия местно-распространенных форм рака шейки матки // Опухоли женской репродуктивной системы. 2007. - №1-2. - С. 77-79.
5. Шакирова Э.Ж., Муллагалиева А.М., Хасанов Р.Ш., Сухорукова Л.К. Местно-распространенный рак шейки матки: проблемы диагностики и лечения // Казанский медицинский журнал. 2007. - Т. - 88. - №6. - С. 627-630.
6. Коломиец Л.А., Чуруксаева О.Н. «Неоадъювантная химиотерапия при лечении местнораспространенного рака шейки матки» СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2013. №2 (56).
7. Lukka Н, Hirte Н, Fyles A, Thomas G, Elit L, Johnston M, Fung MF, Browman G. Concurrent cisplatin-based chemotherapy plus radiotherapy for cervical cancer - a meta-analysis. J Clin Oncol. 2002;14: 203-212.
8. Rose, P.G., Ali, S., Watkins, E., Thigpen, J.Т., Deppe, G., Clarke-Pearson, D.L., & Insalaco, S. (2007). Long-term follow-up of a randomized trial comparing concurrent single agent cisplatin, cisplatin-based combination chemotherapy, or hydroxyurea during pelvic irradiation for locally advanced cervical cancer: A gynecologic oncology group study. Journal of Clinical Oncology, 25(19), 2804-2810.
9. K Franke, M Kettering, K Lange, WA Kaiser, I Hilger (2013). The exposure of cancer cells to hyperthermia, iron oxide nanoparticles, and mitomycin С influences membrane multidrug resistance protein (MRP) expression levels. International Journal of Nanomedicine 8: 351-363.
10. Franckena M, Fatehi D, de Bruijne M, Canters RA, van Norden Y, Mens JW, van Rhoon GC, van der Zee J. Eur J Cancer. 2009 Hyperthermia dose-effect relationship in 420 patients with cervical cancer treated with combined radiotherapy and hyperthermia. Jul; 45(11): 1969-78. doi: 10.1016/j.ejca.2009.03.009. Epub 2009 Apr 8.
Способ комбинированного лечения больных местно-распространенным раком шейки матки, включающий проведение курса сочетанной лучевой терапии - дистанционной гаммы-терапии в стандартном режиме фракционирования дозы РОД 2 Гр, 5 фракций в неделю, с СОД 46 Гр, внутриполостной лучевой терапии с энергией 1,25 МэВ в режиме крупного фракционирования дозы РОД 5 Гр, 2 фракции в неделю, с СОД 50 Гр, введение цисплатина в дозе 40 мг/м2, 1 раз в неделю, до суммарной дозы не менее 220 мг, отличающийся тем, что за 2 ч до сеанса внутриполостной лучевой терапии проводят локальную гипертермию при температуре 42-43°С в течение 40-60 мин, 10 сеансов.

