Результат интеллектуальной деятельности: КОМПОЗИЦИИ И СПОСОБЫ ДИАГНОСТИКИ И ЛЕЧЕНИЯ ГИПЕРТИРЕОЗА У ЖИВОТНЫХ-КОМПАНЬОНОВ
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
По данной заявке испрашивается приоритет по предварительной заявке США № 61/577373, зарегистрированной 19 декабря 2011 года, включенной в настоящее описание в качестве ссылки.
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к выделенной молекуле ДНК, кодирующей часть белка NIS кошек, а также применению этого фрагмента гена в способах получения пищевых композиций для животных, подходящих для введения животным-компаньонам из семейства кошачьих, страдающих гипертиреозом, а также композициям и способам лечения гипертиреоза у животных-компаньонов из семейства кошачьих.
СПИСОК ПОСЛЕДОВАТЕЛЬНОСТЕЙ
Настоящая заявка включает список последовательностей, поданный с помощью EFS-Web и включенный, таким образом, в настоящее описание в качестве ссылки в полном объеме. Указанная копия ASCII, созданная 15 декабря 2011 года, названа 9344P-00-HL_Sequence_Listing_ST25.txt и имеет размер 3 KB.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Гипертиреоз является относительно распространенным эндокринным нарушением, в частности, преобладающим у пожилых кошек. Он является опасным состоянием здоровья, являющимся результатом гиперпластического роста тиреоидной ткани и гиперпродукции тиреоидного гормона. Общепринятые способы лечения гипертиреоза включают постоянное введение антитиреоидного лекарственного средства, хирургическое удаление щитовидной железы и/или терапию радиоактивным йодом. Эти способы лечения являются дорогостоящими и имеют ограничения и побочные эффекты. Например, т.к. большинство антитиреоидных лекарственных средств вводят перорально, соблюдение режима лечения часто нарушается. Для хирургического вмешательства необходима анестезия, и это часто невозможно для пожилых кошек, в частности, кошек, страдающих также и другими заболеваниями. Терапия радиоактивным йодом доступна только в учреждениях, лицензированных для использования радиоактивных материалом, и для нее необходима госпитализация кошек до тех пор, пока их уровни радиоактивности не станут безопасными.
Т.к. для продукции тиреоидного гормона необходим поступающий с пищей йод, разрабатывают способы лечения гипертиреоза у кошек, включающие кормовые рационы с ограниченным содержанием йода. Желательно дополнять такие рационы с ограниченным содержанием йода ингредиентами, снижающими захват йода щитовидной железой, и ингредиентами, ингибирующими синтез тиреоидного гормона.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и реагентам для определения пищевых ингредиентов, снижающих захват йода щитовидной железой и ингибирующих синтез тиреоидного гормона. Способы, представленные в настоящем описании, включают использование выделенного фрагмента гена, кодирующего часть натрий-йодного симпортерного белка кошек (белка NIS), для получения данных профиля экспрессии гена в присутствии и отсутствие тестовых материалов. Используя эти способы, можно определять материалы, которые можно включать в рацион кошки, страдающей гипертиреозом, для лечения этого состояния.
Настоящее изобретение относится к выделенному фрагменту гена, кодирующему часть натрий-йодного симпортерного белка кошек (белка NIS), имеющему нуклеотидную последовательность SEQ ID NO:1 и кодирующему пептид, имеющий аминокислотную последовательность SEQ ID NO:2.
Настоящее изобретение также относится к рекомбинантным векторам и трансформированным клеткам, содержащим выделенный фрагмент гена NIS кошек. Настоящее изобретение также относится к способам, включающим использование таких выделенных молекул ДНК для определения профилей экспрессии гена для гена NIS кошек у здоровых и больных животных и измерения профилей экспрессии гена NIS в присутствии и отсутствие пищевых ингредиентов и их экстрактов для получения пищевых композиций для животных, подходящих для введения животным-компаньонам из семейства кошачьих, страдающим гипертиреозом. Настоящее изобретение также относится к композициям и способам лечения гипертиреоза у кошек.
Настоящее изобретение также относится к способу получения корма для домашних животных, подходящего для введения животному-компаньону из семейства кошачьих, страдающему гипертиреозом, включающему: (a) осуществление доступа по меньшей мере к одной первой базе данных, содержащей первый набор данных, относящий функциональный профиль гена в образце биологической жидкости или ткани животного к физиологическому состоянию и, необязательно, генотипу животного, где функциональный профиль гена является функциональным профилем гена NIS кошек, (b) осуществление доступа по меньшей мере к одной второй базе данных, содержащей второй набор данных, относящийся к эффектам биоактивных компонентов рациона на функциональный профиль гена из этапа (a); (c) обработку исходных данных, определяющих физиологическое состояние и, необязательно, генотип субпопуляции, например, кошек, страдающих гипертиреозом, с помощью первого алгоритма, использующего первый и второй наборы данных, для получения пищевого состава, применимого для выбора и получения пищевой композиции для этой субпопуляции животных; и (d) получение пищевой композиции на основе пищевого состава, где эта пищевая композиция подходит для введения животному-компаньону из семейства кошачьих, страдающему гипертиреозом.
В определенных аспектах этого варианта изобретения первый набор данных получают из образцов, собранных от множества отдельных животных, представляющих диапазон генотипов и физиологических состояний, включающих животных-компаньонов из семейства кошачьих, страдающих гипертиреозом. В одном из аспектов каждый такой образец от отдельного животного связан с записью о происхождении, содержащей зоографические данные отдельного животного, относящиеся к определению генотипа и физиологического состояния, на момент забора образца. В другом аспекте этого варианта осуществления зоографические данные содержат один или несколько элементов данных, относящихся к генотипу, выбранных из группы, состоящей из породы, пород родителей, родословной, пола, типа шерстного покрова и очевидных наследственных состояний и нарушений, в частности, гипертиреоза. В другом аспекте этого варианта осуществления зоографические данные содержат один или несколько элементов данных, относящихся к физиологическому состоянию, выбранному из группы, состоящей из возраста, массы, ветеринарного анамнеза, репродуктивного анамнеза, состояния здоровья в настоящее время или состояния заболевания, аппетита, уровня физической активности, умственной деятельности, поведенческих аномалий и характера, и, в частности, наличия и степени гипертиреоза.
В конкретном аспекте этого способа первый набор данных содержит данные, относящиеся к анализу образца в отношении одного или нескольких компонентов, выбранных из группы, состоящей из ДНК, РНК, белков, метаболитов в качестве биомаркеров, в то время как второй набор данных получают при контролируемых экспериментах, включающих подвергание модели на животных воздействию различных уровней одного или нескольких биоактивных компонентов рациона.
Настоящее изобретение также относится к композициям и способам диагностики гипертиреоза у кошек, а также способам определения материалов и составления пищевых композиций, содержащих эти материалы, которые будут применимыми для лечения гипертиреоза у кошек.
В другом конкретном аспекте этого способа исходные данные содержат зоографические данные, относящиеся к определению генотипа и физиологического состояния животных-компаньонов из семейства кошачьих, страдающих гипертиреозом. В другом аспекте этого способа исходные данные содержат аналитические данные для образца биологической жидкости или ткани, полученного от животных-компаньонов из семейства кошачьих, не страдающих гипертиреозом. В других конкретных аспектах этого способа исходные данные содержат аналитические данные для образца биологической жидкости или ткани, полученного от животных-компаньонов из семейства кошачьих, страдающих легким гипертиреозом, а также от животных-компаньонов из семейства кошачьих, страдающих тяжелым гипертиреозом.
Настоящее изобретение также относится к пищевым композициям для животных, полученным указанным выше способом, для получения корма для домашних животных, иллюстративные примеры которого представлены в настоящем описании ниже, применимого для введения животным-компаньонам из семейства кошачьих, страдающим гипертиреозом.
Таким образом, настоящее изобретение относится к способам рационального получения рациона для животного, страдающего заболеванием или состоянием, включающим определение биоактивных компонентов рациона, применимых в снижении эффектов заболевания или состояния, которым страдает животное. В конкретном иллюстративном аспекте этого варианта осуществления заболеванием или состоянием является гипертиреоз, а страдающим животным является животное-компаньон из семейства кошачьих.
В одном из вариантов осуществления настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона. В одном из аспектов настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона из семейства кошачьих.
В другом варианте осуществления настоящее изобретение относится к композициям, применимым в способе лечения гипертиреоза у животного-компаньона. В одном из аспектов настоящее изобретение относится к композициям, применимым в способе лечения гипертиреоза у животного-компаньона из семейства кошачьих.
В конкретных аспектах этих вариантов осуществления животное-компаньон с гипертиреозом, нуждающееся в лечении, кормят пищевой композицией для домашних животных, содержащей эффективное количество биоактивного компонента рациона, достаточное для подавления экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или их обоих, в качестве неограничивающих примеров, таких как активность гена NIS кошек, представленного в настоящем описании.
В определенных вариантах осуществления полипептид, ингибируемый биоактивными компонентами рациона, выбран из группы, состоящей из тиреоидной пероксидазы, натрий-йодного симпортера (NIS), тиреоидной оксидазы, интратиреоидной 5'-дейодиназы типа I, рецептора тиреотропного гормона, пендрина, монокарбоксилат-транспортера 8 и их комбинаций.
Настоящее изобретение также относится к способу составления рациона, подходящего для лечения заболевания или состояния у животного.
Дополнительные области применения настоящего изобретения станут очевидными из подробного описания, представленного далее в настоящем описании. Следует понимать, что, хотя в подробном описании и конкретных примерах указан предпочтительный вариант осуществления изобретения, они предназначены исключительно для иллюстративных целей, а не для ограничения объема изобретения.
Дополнительные варианты осуществления и цели настоящего изобретения будут очевидны специалистам в этой области.
В другом варианте осуществления изобретение относится к способу лечения гипертиреоза у нуждающейся в этом кошки, включающему диагностику наличия гипертиреоза, например, с использованием описываемых выше способов, и контроль состояния, например, исключительно с помощью рациона или в комбинации с соответствующим лекарственным средством. В одном из аспектов этого варианта осуществления рацион включает один или несколько компонентов, определяемых способами, представленными в настоящем описании, применимых для снижения захвата йода щитовидной железой или для ингибирования синтеза тиреоидного гормона, включая, в том числе, компоненты, способные подавлять или ингибировать экспрессию гена NIS или снижать или ингибировать функцию белка NIS.
В дополнительном варианте осуществления изобретение относится к реагентам, необязательно меченым, применимым в определении уровня экспрессии биомаркера NIS у кошки. Такие реагенты могут включать, например, антитела, например, моноклональные антитела, одноцепочечные антитела и функциональные фрагменты антител, избирательно распознающие белок NIS кошек, например, антитела, например, моноклональные антитела, одноцепочечные антитела и функциональные фрагменты антител, избирательно распознающие пептид SEQ ID NO:2. Другие такие реагенты включают аптамеры, например, аптамеры нуклеиновых кислот или пептидные аптамеры, распознающие или избирательно распознающие белок NIS кошек или пептид SEQ ID NO:2, а также олигонуклеотидные зонды, способные избирательно гибридизоваться с геном NIS кошек или нуклеотидной последовательностью SEQ ID NO:1.
В дополнительном варианте осуществления настоящее изобретение относится к набору для диагностики, прогнозирования или мониторинга гипертиреоза у кошки, содержащему средства для измерения экспрессии гена NIS кошек в биологическом образце от кошки и инструкции по использованию таких средств для измерения экспрессии гена NIS в биологическом образце от кошки и оценки наличия процесса, приводящего к гипертиреозу у кошки. Набор предназначен для измерения одного или нескольких биомаркеров с помощью одного или нескольких нуклеиновых кислот-зондов, с помощью которых можно определять экспрессию гена NIS, способных избирательно гибридизоваться с нуклеиновой кислотой SEQ ID NO:1 в строгих условиях.
В других аспектах этих вариантов изобретения средствами для измерения одного или нескольких биомаркеров являются одно или несколько антител, с помощью которых можно определять экспрессию гена NIS посредством избирательного распознавания экспрессируемого белка NIS или посредством избирательного распознавания пептида SEQ ID NO:2. Такие наборы могут находиться в формате ELISA, содержащем антитело, с помощью которого можно определять белок NIS, включая выделенный, очищенный или рекомбинантный белок NIS, соответствующий экспрессируемому белку или пептидной последовательности SEQ ID NO:2, и буфер.
В других аспектах этого варианта осуществления средствами для измерения биомаркера NIS являются один или несколько аптамеров, например, как представлено в настоящем описании выше, с помощью которых можно определять экспрессию гена, кодирующего белок NIS, или посредством распознавания экспрессируемого белка NIS.
Дополнительные области применения настоящего изобретения станут очевидными из подробного описания, представленного далее в настоящем описании. Следует понимать, что, хотя в подробном описании и конкретных примерах указан предпочтительный вариант осуществления изобретения, они предназначены исключительно для иллюстративных целей, а не для ограничения объема изобретения.
ПОДРОБНОЕ ОПИСАНИЕ
Следующее описание предпочтительных вариантов осуществления носит исключительно иллюстративный характер и никоим образом не предназначено для ограничения изобретения или его применения.
Определения
Как применяют в настоящем описании и формуле изобретения, термины в единственном числе включают множественное число, если контекст четко не указывает на иное, например, упоминание "варианта" включает множество вариантов. Кроме того, определенные термины включают варианты терминов, используемые в соответствующем грамматическом контексте, например, термин "специфически связывается" включает "специфическое связывание" и другие формы термина. Аналогично, слова "содержат", "содержит" и "содержащий" следует интерпретировать включительно, а не исключительно.
Термин "антитело" означает любой иммуноглобулин, связывающийся с конкретным антигеном, включающий антитела IgG, IgM, IgA, IgD и IgE. Термин включает поликлональные, моноклональные, моновалентные, гуманизированные антитела, гетероконъюгат, композиции антител с полиэпитопной специфичностью, химерные, биспецифические антитела, диатела, одноцепочечные антитела и фрагменты антител, такие как Fab, Fab', F(ab')2 и Fv, или другие антигенсвязывающие фрагменты. Специфичность антител можно определять с использованием способов и анализов, известных в этой области, включая, в качестве неограничивающих примеров, конкурентные анализы и использование систем фагового дисплея. Таким образом, антитело, специфически связывающееся, например, с белком NIS кошек, является антителом со скоростью ассоциации/диссоциации и/или аффинностью связывания, значительно большей для пептида SEQ ID NO:2 или его части, субфрагмента или части пептида, чем для гомологичного белка другого вида, например, для белка NIS человека. В этом контексте термин "значительно" означает, что скорости ассоциации/диссоциации и/или аффинность связывания субъекта отличается по меньшей мере в 1,1, 1,2, 1,5, 2, 5, 10, 50, 100, 1000 или 10000 раз или более.
Термин "чип" означает упорядоченное расположение по меньшей мере двух зондов на субстрате. По меньшей мере один из зондов является контролем или стандартом, и по меньшей мере один из зондов является диагностическим зондом. Расположение от приблизительно двух до приблизительно 40000 зондов на субстрате гарантирует, что размер и интенсивность сигнала каждого меченого комплекса, образующегося между зондом и полинуклеотидом или полипептидом в образце, являются индивидуально различимыми. Коллекцию молекул, нанесенных на чип, можно получать синтетически или биосинтетически. Чип может иметь множество форм, включая библиотеки растворимых молекул, библиотеки соединений, связанных с зернами смолы, чипами из диоксида кремния или другими твердыми подложками. Чип с нуклеиновой кислотой может включать библиотеки нуклеиновых кислот, которые можно получать нанесением в виде пятен нуклеиновых кислот по существу любой длины (например, от 1 до приблизительно 1000 нуклеотидов в длину) на субстрат. Чип с нуклеиновыми кислотами-зондами предпочтительно содержит нуклеиновые кислоты, связанные с субстратом в известных местах. В других вариантах осуществления система может включать твердую подложку или субстрат, такой как мембрана, фильтр, предметное стекло, лунка микропланшета, пробирка для образца, бусина, цепочка бусин или т.п. Твердую подложку можно получать из различных материалов, включая бумагу, целлюлозу, нейлон, полистирол, поликарбонат, пластмассу, стекло, керамику, нержавеющую сталь или т.п. Твердая подложка предпочтительно может иметь жесткую или полужесткую поверхность и предпочтительно может являться сферической (например, бусиной) или по существу плоской (например, плоской поверхностью) с подходящими лунками, выпуклыми областями, вытравленными канавками или т.п. Твердая подложка также может включать гель или матрицу, в которые можно погружать нуклеиновые кислоты.
Термин "биомаркеры" относится к генам и продуктам генов, кодируемым геном по изобретению или его гомологом, в частности, его гомологом у кошек, где определено, что ген дифференциально экспрессируется в результате заболевания, состояния, нарушения или введения вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций, и где такие гены и продукты генов по изобретению определены, например, в SEQ ID NO:1. Биомаркер может являться полинуклеотидом, полипептидом, белком, РНК, включая РНК-транскрипт или продукт ее транскрипции, ДНК, кДНК, метаболит одной или нескольких из указанных выше молекул или применимый вариант любой из указанных выше молекул, дифференциальная экспрессия которого ассоциирована с гипертиреозом кошек, где корреляцию такой дифференциальной экспрессии в образце, взятом у тестового животного, с дифференциальной экспрессией в образце, взятом у контрольного животного, можно использовать в диагностике, прогнозировании, мониторинге или лечении состояния, заболевания или нарушения у нуждающегося в этом животного. Кроме того, биомаркер, как правило, можно использовать в отношении любой части или сегмента такого гена или белка, с помощью которой можно определять полноразмерный ген или белок, или которая может коррелировать с полноразмерным геном или белком, например, в анализе или другом способе по изобретению. Экспрессию биомаркера также можно определять посредством определения трансляции биомаркера (т.е. определения биомаркерного белка в образце). Способы, подходящие для определения биомаркерных белков, включают любой подходящий способ определения и/или измерения белков из клетки или клеточного экстракта. Такие способы включают, в качестве неограничивающих примеров, иммуноблоттинг (например, Вестерн-блоттинг), твердофазный иммуноферментный анализ (ELISA), радиоиммунологический анализ (RIA), иммунопреципитацию, иммуногистохимию и иммунофлуоресценцию. Особенно предпочтительные способы определения белков включают любой клеточный анализ, включая иммуногистохимию и иммунофлуоресценцию. Такие способы хорошо известны в этой области.
Термин "по сравнению", используемый для сравнения экспрессии в тестовом образце и контрольном образце, должен означать признаки такого свойства и количество и должен включать, в качестве неограничивающих примеров, значения в пределах одного стандартного отклонения от среднего значения, с которым осуществляют указанное сравнение, и значения, включающие дифференциальную экспрессию между тестовым образцом и контрольным образцом.
Термины "дифференциально экспрессирующийся ген", "дифференциальная экспрессия гена", "дифференциальная экспрессия" или "дифференциально экспрессируемый" и их синонимы, используемые взаимозаменяемо, относятся к гену, экспрессия которого активируется до более высокого или более низкого уровня у субъекта, страдающего заболеванием, состоянием или нарушением, или в результате введения вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций, относительно его экспрессии у нормального или контрольного субъекта. Термины также включают гены, экспрессия которых активируется до более высокого или более низкого уровня на разных стадиях одного заболевания. Также следует понимать, что дифференциально экспрессируемый ген можно активировать или ингибировать на уровне нуклеиновой кислоты или уровне белка, или можно подвергать альтернативному сплайсингу, приводящему к другому полипептидному продукту. Такие различия можно подтверждать изменением уровней мРНК, поверхностной экспрессии, секреции или, например, другим разделением полипептида. Дифференциальная экспрессия гена может включать сравнение экспрессии двух или более генов или их продуктов, или сравнение соотношений экспрессии двух или более генов или их продуктов, или даже сравнение двух по-разному процессирующихся продуктов одного и того же гена, отличающихся среди нормальных субъектов и субъектов, страдающих заболеванием, состоянием или нарушением, или в результате введения вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций, или между разными стадиями одного и того же заболевания, состояния или нарушения, или в результате введения различных количеств вещества, лекарственного средства, питательного вещества или компонента рациона или их комбинаций. Дифференциальная экспрессия включает и количественные, и качественные различия временного или клеточного профиля экспрессии гена или продуктов его экспрессии, например, в нормальных и пораженных клетках или в клетках, прошедших различные события в течение заболевания или стадии заболевания. В целях настоящего изобретения считают, что присутствует "дифференциальная экспрессия гена", если существует изменение количества транскрибированных полинуклеотидов или транслируемого белка в образце по меньшей мере приблизительно в 2,0, 1,9, 1,8, 1,7, 1,6, 1,5, 1,4, 1,3, 1,25 раз.
При использовании в качестве меры дифференциальной экспрессии гена термин "кратный" означает уровень экспрессии гена у кошки, являющийся кратным количеством или долей экспрессии гена, сравниваемым с уровнем экспрессии гена у кошки сравнения, например, у кошки, страдающей гипертиреозом, по сравнению с животным, не демонстрирующим такого состояния. Например, ген, экспрессирующийся у животного в 2 раза сильнее, чем у животного сравнения, имеет 2-кратную дифференциальную экспрессию гена, и ген, экспрессирующийся у животного вполовину слабее, чем у животного сравнения, также имеет 2-кратную дифференциальную экспрессию гена.
Термин "фрагмент" означает (1) олигонуклеотид или полинуклеотидную последовательность, являющуюся частью полной последовательности или содержащую ее, и имеющую ту же или схожую активность для конкретного использования в качестве полной полинуклеотидной последовательности, или (2) пептид или полипептидную последовательность, являющуюся частью полной последовательности или содержащую ее, и имеющую ту же или схожую активность для конкретного использования в качестве полной полипептидной последовательности. Такие фрагменты могут содержать любое количество нуклеотидов или аминокислот, считающихся подходящими для конкретного использования. Как правило, олигонуклеотидные или полинуклеотидные фрагменты содержат по меньшей мере приблизительно 10, 15, 20, 25, 30, 35, 40, 45, 50, 60, 70, 80, 90, 100, 200, 400, 600, 800 или 1000 или более нуклеотидов, и полипептидные фрагменты содержат по меньшей мере приблизительно 4, 6, 8, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28, 30, 32, 34, 36, 38, 40, 42, 44, 46, 48 или 50 или более последовательных аминокислот из полной последовательности. Термин включает полинуклеотидные и полипептидные варианты фрагментов. Например, полинуклеотид можно разбивать или фрагментировать на множество сегментов.
Различные способы фрагментирования нуклеиновых кислот хорошо известны в этой области. Например, эти способы могут являться по своей природе химическими или физическими. Химическая фрагментация может включать частичную деградацию ДНКазой; частичную депуринизацию кислотой; использование ферментов рестрикции; использование кодируемых интронами эндонуклеаз; способы расщепления на основе ДНК, такие как способы с образованием триплекса и гибрида, основанные на специфической гибридизации сегмента нуклеиновой кислоты для локализации расщепляющего средства в конкретном месте в молекуле нуклеиновой кислоты; или другие ферменты или соединения, расщепляющие ДНК в известном или неизвестном месте. Способы физической фрагментации могут включать подвергание ДНК воздействию высокой скорости сдвига. Высокие скорости сдвига можно получать, например, перемещая ДНК через камеру или канал с углублениями или шипами, или пропуская образец ДНК через канал ограниченного размера, например, отверстие, имеющее поперечный размер микронного или субмикронного порядка. Другие физические способы включают обработку ультразвуком и распыление. Аналогично можно использовать комбинации физических и химических способов фрагментации, такие как фрагментация нагреванием и ион-опосредованный гидролиз. См., например, Sambrook et al., "Molecular Cloning: A Laboratory Manual," 3rd Ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y. (2001) ("Sambrook et al"), включенную в настоящее описание в качестве ссылки для всех целей. Эти способы можно оптимизировать для расщепления нуклеиновой кислоты на фрагменты с выбранным диапазоном размеров. Применимые диапазоны размеров могут составлять от 25, 50, 100, 200, 400, 700 или 1000 до 500, 800, 1500, 2000, 4000 или 10000 пар оснований. Однако большие диапазоны размеров, такие как от 4000, 10000 или 20000 до 10000, 20000 или 500000 пар оснований, также могут являться применимыми.
Термин "ген" или "гены" означает полный или частичный сегмент ДНК, участвующий в продукции полипептида, включая области перед и после кодирующей области (лидерную и трейлерную последовательность) и промежуточные последовательности (интроны) между отдельными кодирующими сегментами (экзонами). Термин включает любую последовательность ДНК, гибридизующуюся с комплементарной цепью кодирующих последовательностей гена.
Термин "гомолог" означает (1) полинуклеотид, включая полинуклеотиды из того же или другого вида животных, имеющий более чем 30%, 50%, 70%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99%-ое сходство последовательности с полинуклеотидом, имеющий те же или по существу те же свойства и осуществляющий ту же или по существу ту же функцию, что и полный полинуклеотид, или имеющий способность специфически гибридизоваться с полинуклеотидом в строгих условиях, или (2) полипептид, включая полипептиды из того же или другого вида животных, имеющий более чем 30%, 50%, 70%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% сходство последовательности с полипептидом, идентифицированным по экспрессирующимся полинуклеотидам, и имеющий те же или по существу те же свойства и осуществляющий ту же или по существу ту же функцию, что и полный полипептид, или имеющий способность специфически связываться с полипептидом, идентифицированным по экспрессии полинуклеотидов. Сходство последовательности двух полипептидных последовательностей или двух полинуклеотидных последовательностей определяют с использованием способов, известных специалистам в этой области, например, алгоритма Karlin и Altschul (Proc. Natl. Acad. Sci. USA 87: 2264-2268 (1990)). Такой алгоритм включен в программы NBLAST и XBLAST Altschul et al. (J. Mol. Biol. 215: 403-410 (1990)). Для получения выравнивания с пропусками в целях сравнения можно использовать Gapped Blast, как описано в Altschul et al. (Nucl. Acids Res. 25: 3389-3402 (1997)). При использовании программ BLAST и Gapped BLAST используют программы по умолчанию соответствующих программ (например, XBLAST и NBLAST). См. http://www.ncbi.nlm.nih.gov.
Термин "гибридизация" относится к процессу, в котором два одноцепочечных полинуклеотида нековалентно связываются с образованием стабильного двухцепочечного полинуклеотида. Термин "гибридизация" также может относиться к трехцепочечной гибридизации. Получаемый (как правило) двухцепочечный полинуклеотид является "гибридом". Доля популяции полинуклеотидов, образующих стабильные гибриды, в настоящем описании обозначают как "степень гибридизации".
Реакции гибридизации можно осуществлять в абсолютных или дифференциальных форматах гибридизации. В абсолютном формате гибридизации полинуклеотиды, полученные из одного образца, гибридизуют с зондами в чипе с нуклеиновыми кислотами. Сигналы, определяемые после образования гибридизационных комплексов, коррелируют с уровнями полинуклеотида в образце. В формате дифференциальной гибридизации полинуклеотиды, полученные из двух образцов, метят различными веществами для мечения. Смесь этих по-разному меченых полинуклеотидов добавляют на чип с нуклеиновыми кислотами. Затем чип с нуклеиновыми кислотами исследуют в условиях, в которых излучение от двух разных меток определяют по отдельности. В одном из вариантов осуществления для формата дифференциальной гибридизации в качестве веществ для мечения используют флуорофоры Cy3 и Cy5 (Amersham Pharmacia Biotech, Piscataway, N.J.).
Сигналы, полученные от чипов с нуклеиновыми кислотами, можно анализировать с использованием коммерчески доступного программного обеспечения, такого как программное обеспечение, поставляемое Affymetrix или Agilent Technologies. Предпочтительно, в эксперименты по гибридизации включают контроли, такие как контроли чувствительности сканирования, мечения зонда и квантования кДНК или кРНК. Сигналы гибридизации можно масштабировать или нормировать до проведения дальнейшего анализа. Например, сигналы гибридизации для каждого отдельного зонда можно нормировать для учета изменений интенсивностей гибридизации при использовании нескольких чипов в аналогичных условиях тестирования. Также сигналы гибридизации можно нормировать с использованием интенсивностей, полученных от внутренних контролей для нормирования, содержащихся в каждом чипе. Кроме того, гены с относительно постоянными уровнями экспрессии среди образцов можно использовать для нормирования уровней экспрессии других генов. В одном из вариантов осуществления зонды для конкретных генов "домашнего хозяйства" включают в чип с нуклеиновыми кислотами по настоящему изобретению. Эти гены выбирают потому, что они демонстрируют стабильные уровни экспрессии в различных тканях. Сигналы гибридизации можно нормировать и/или масштабировать, учитывая уровни экспрессии этих генов "домашнего хозяйства".
Термин "гибридизационный комплекс" означает комплекс, образующийся между полинуклеотидами в образце, когда пурины одного полинуклеотида образуют водородные связи с пиримидинами комплементарного полинуклеотида, например, 5'-A-G-T-C-3' образует пары оснований с 3'-T-C-A-G-5'. Степень комплементарности и использование аналогов нуклеотида влияет на эффективность и точность реакций гибридизации.
Термин "зонды для гибридизации" включает нуклеиновые кислоты (такие как олигонуклеотиды), способные связывать с комплементарной цепью нуклеиновой кислоты с образованием пар оснований. Такие зонды включают пептид-нуклеиновые кислоты, как описано в Nielsen et al., Science 254: 1497-1500 (1991), Nielsen Curr. Opin. Biotechnol., 10: 71-75 (1999), и другие аналоги нуклеиновых кислот и имитации нуклеиновых кислот. См. патент США № 6156501, зарегистрированный 3 апреля 1996 года.
"Последовательность нуклеиновой кислоты" означает олигонуклеотид, нуклеотид или полинуклеотид и его фрагменты или части, и относится к ДНК или РНК геномного или синтетического происхождения, которая может являться одно- или двухцепочечной, и представляет смысловую или антисмысловую цепь.
Термин "полинуклеотид" или "олигонуклеотид" означает полимер нуклеотидов. Термин включает молекулы ДНК и РНК (включая кДНК и мРНК), одно- или двухцепочечные, и, в случае одноцепочечной молекулы, ее комплементарную последовательность в линейной или кольцевой форме. Термин также включает фрагменты, варианты, гомологи и аллели, при необходимости, в случае последовательностей, имеющих те же или по существу те же свойства и осуществляющих ту же или по существу ту же функцию, что и исходная последовательность. Последовательности могут являться полностью комплементарными (без несовпадений) при выравнивании или могут иметь несовпадения до приблизительно 30% последовательности. В случае полинуклеотидов цепь содержит от приблизительно 20 до 10000, от 50 до 8000, от 100 до 5000 или от 150 до 3500 нуклеотидов. В случае олигонуклеотидов цепь содержит от приблизительно 2 до 100, от 3 до 80, от 4 до 60, от 5 до 40 или от 6 до 30 нуклеотидов. Точный размер полинуклеотида или олигонуклеотида будет зависеть от различных факторов и от конкретного использования полинуклеотида или олигонуклеотида. Термин включает нуклеотидные полимеры, синтезированные и выделенные и очищенные из природных источников. Термин "полинуклеотид" включает "олигонуклеотид".
Термин "полипептид", "пептид" или "белок" означает полимер аминокислот. Термин включает природные и неприродные (синтетические) полимеры и полимеры, в которых искусственными химическими имитациями замещают одну или несколько аминокислот. Термин также включает фрагменты, варианты и гомологи, имеющие те же или по существу те же свойства и осуществляющие ту же или по существу ту же функцию, что и исходная последовательность. Термин включает полимеры любой длины, предпочтительно полимеры, содержащие от приблизительно 2 до 1000, от 4 до 800, от 6 до 600 и от 8 до 400 аминокислот. Термин включает полимеры аминокислот, синтезированные и выделенные и очищенные из природных источников. В некоторых случаях в настоящем описании термины "полипептид", "пептид" или "белок" используют взаимозаменяемо.
Термин "зонд" означает (1) олигонуклеотид или полинуклеотид РНК или ДНК, существующий в природе в виде очищенного продукта расщепления ферментами рестрикции или полученный синтетически, способный отжигаться или специфически гибридизоваться с полинуклеотидом с последовательностями, комплементарными зонду; или (2) пептид или полипептид, способный специфически связываться с конкретным белком или фрагментом белка, по существу, для исключения других белков или фрагментов белков. Олигонуклеотидный или полинуклеотидный зонд может являться одно- или двухцепочечным. Точная длина зонда будет зависеть от многих факторов, включая температуру, источник и использование. Например, в случае диагностического применения в зависимости от сложности последовательности-мишени, олигонуклеотидный зонд, как правило, содержит от приблизительно 10 до 100, от 15 до 50 или от 15 до 25 нуклеотидов. В случае конкретного диагностического применения полинуклеотидный зонд содержит приблизительно 100-1000 нуклеотидов, 300-600 нуклеотидов, предпочтительно - приблизительно 300 нуклеотидов. В настоящем описании зонды выбраны так, что они являются "по-существу" комплементарными различным цепям конкретной последовательности-мишени. Это означает, что зонды должны являться в достаточной степени комплементарными для специфической гибридизации или отжига с соответствующими последовательностями-мишенями в заранее определенных условиях. Таким образом, нет необходимости в том, чтобы последовательность зонда отражала точную комплементарную последовательность мишени. Например, к 5'- или 3'-концу зонда можно присоединять некомплементарный нуклеотидный фрагмент, в то время как остальная часть последовательности зонда будет комплементарной последовательности-мишени. Альтернативно, в зонд можно включать некомплементарные основания или более длинные последовательности при условии, что последовательность зонда обладает достаточной комплементарностью с последовательностью полинуклеотида-мишени для специфического отжига на полинуклеотиде-мишени. Пептидным или полипептидным зондом может являться любая молекула, с которой белок или пептид специфически связывается, включая ДНК (в случае ДНК-связывающих белков), антитела, рецепторы клеточной мембраны, пептиды, кофакторы, лектины, сахара, полисахариды, клетки, клеточные мембраны, органеллы и мембраны органелл.
Термин "образец" означает любую ткань или жидкость животного, содержащую полинуклеотиды, включая клетки и другую ткань, содержащую ДНК и РНК. Примеры включают тиреоидную ткань, кровь, соединительную, эпителиальную, лимфоидную, мышечную, нервную ткань, мокроту и т.п. Образец может являться твердым или жидким и может содержать ДНК, РНК, кДНК, например, биологические жидкости, такие как кровь или моча, клетки, клеточные препараты или их растворимые фракции или аликвоты сред, хромосомы, органеллы и т.п.
Термин "специфически связывается" означает специальное и точное взаимодействие между двумя молекулами, зависящее от их структуры, в частности, их молекулярных боковых групп. Например, интеркаляция регуляторного белка в большую бороздку молекулы ДНК, образование водородных связей вдоль остова между двумя одноцепочечными нуклеиновыми кислотами или связывание между эпитопом белка и агонистом, антагонистом или антителом.
Термин "специфически гибридизуется" означает ассоциацию между двумя одноцепочечными полинуклеотидами достаточно комплементарной последовательности, делающую возможной такую гибридизацию в заранее определенных условиях, как правило, используемых в этой области (иногда обозначаемой как "по существу комплементарной"). Например, термин может относиться к гибридизации полинуклеотидного зонда с по существу комплементарной последовательностью, содержащейся в одноцепочечной молекуле ДНК или РНК по одному из аспектов изобретения, для значительного исключения гибридизации полинуклеотидного зонда с одноцепочечными полинуклеотидами некомплементарной последовательности.
Термин "строгие условия" означает (1) гибридизацию в 50% (об./об.) формамиде с 0,1% бычьим сывороточным альбумином, 0,1% фиколлом, 0,1% поливинилпирролидоном, буфером 50 мМ фосфата натрия при pH 6,5 с 750 мМ NaCl, 75 мМ цитратом натрия при 42°C, (2) гибридизацию в 50% формамиде, 5-кратном SSC (0,75 M NaCl, 0,075 M цитрат натрия), 50 мМ фосфате натрия (pH 6,8), 0,1 % пирофосфате натрия, 5-кратном растворе Денхардта, ДНК из обработанной ультразвуком спермы лосося (50 мг/мл), 0,1% SDS и 10% декстрана сульфат при 42°C; при промывании при 42°C в 0,2-кратном SSC и 0,1% SDS или промывании с использованием 0,015 M NaCl, 0,0015 M цитрата натрия, 0,1% Na2SO4 при 50°C или аналогичных известных в этой области способов с использованием промывочных средств с аналогичной низкой ионной силой и высокой температурой и аналогичных денатурирующих средств.
Термин "применимые варианты" означает: (1) в случае полинуклеотида, комплементарные цепи полинуклеотида; гомологи полинуклеотида и их комплементарные цепи; варианты полинуклеотида, их комплементарные цепи и их гомологи; и фрагменты полинуклеотида, их комплементарные цепи, их гомологи и их варианты; и (2) в случае полипептида, гомологи полипептида; варианты полипептида и их гомологи; и фрагменты полинуклеотида, их гомологи и их варианты.
Термин "вариант" означает (1) полинуклеотидную последовательность, содержащую любую замену, изменение, модификацию, делецию или добавление одного или нескольких нуклеотидов из или в полинуклеотидную последовательность, имеющую те же или по существу те же свойства и осуществляющую ту же или по существу ту же функцию, что и исходная последовательность, и (2) полипептидную последовательность, содержащую любую замену, изменение, модификацию, делецию или добавление одной или нескольких аминокислот из или в полипептидную последовательность, имеющую те же или по существу те же свойства и осуществляющую ту же или по существу ту же функцию, что и исходная последовательность. Таким образом, термин включает однонуклеотидные полиморфизмы (SNP) и аллельные варианты и консервативные и неконсервативные аминокислотные замены в полипептидах. Термин также включает химическую дериватизацию полинуклеотида или полипептида и, при необходимости, замену нуклеотидов или аминокислот нуклеотидами или аминокислотами, не существующими в природе.
Если не указано иначе, все процентные доли и количества, выраженные здесь и где-либо еще в настоящем описании, необходимо понимать как относящиеся к процентным долям в пересчете на сухую массу. Указанные количества основаны на активной массе материала.
Как применяют в настоящем описании, способы "лечения" животного, страдающего заболеванием, нарушением или состоянием, также предназначены для включения способов профилактики или излечения, реверсирования, ослабления, облегчения, улучшения, минимизации, супрессии или прекращения вредных воздействий заболевания, нарушения или состояния.
Композиции, представленные в настоящем описании, могут содержать, по существу состоять из или состоять из любого из компонентов, представленных в настоящем описании.
Изобретение не ограничено конкретной методологией, протоколами и реагентами, представленными в настоящем описании, т.к. они могут варьироваться. Кроме того, используемая в настоящем описании терминология предназначена исключительно для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения.
Гипертиреоз
Гипертиреоз отличается повышенным метаболизмом щитовидной железы и избыточной продукцией гормонов щитовидной железы трийодтиронина (T3) и тетрайодтиронина (тироксина или T4). Большая часть T3 и T4 связывается с белками сыворотки. Часть T3 и T4, распадающуюся в сыворотке и не связанную с белком, называют свободным T3 (fT3) и T4 (fT4). Специалист в этой области может точно диагностировать гипертиреоз у кошки, используя исследования функции щитовидной железы, исследуя клинические признаки и наблюдая ответ животного на пробное введение тиреоидного гормона. Исследования функции щитовидной железы известны специалистам в этой области и включают, например, тесты для определения концентраций общего и свободного T3 и T4 в сыворотке, тесты для определения концентрации тиреотропного гормона (TSH), и тесты пертехнетата натрия и супрессии T3. См., например, Small Animal Nutrition, стр. 863-868 (2000). Как указано выше, как применяют в настоящем описании, лечение гипертиреоза включает улучшение, супрессию и эрадикацию гипертиреоза.
Биосинтез тироксина (T4) осуществляется в фолликулярных клетках щитовидной железы. В этом процессе сначала йод транспортируется через базальную мембрану фолликулярных клеток с помощью Na+/I- (натрий-йодного) симпортера, а затем перемещается через апикальную мембрану в коллоид фолликула с помощью транспортера пендрина. Полипептид тиреоглобулин (TG) синтезируется в эндоплазматическом ретикулуме фолликулярной клетки и секретируется в коллоид. Тиреоидная пероксидаза (PTO) окисляет йод (I-) до I0, более реакционноспособной частицы, йодирующей тирозильные остатки полипептида тиреоглобулина в опосредуемой пероксидом водорода реакции. Полагают, что продукция пероксида водорода опосредуется тиреоидной оксидазой (ThOX). Реакция между фенольными остатками йодированных тирозильных остатков приводит к образованию предшественников T4-тироксина и T3-трийодтиронина с двойным кольцом. Также считают, что последняя реакция опосредуется системой тиреоидной пероксидазы/H2O2, в которой йодированное тирозильное феноловое кольцо расщепляется и соединяется с йодированным тирозином эфирной связью.
Тиреотропный гормон (TSH), высвобождаемый из гипофиза, связывается с рецептором тиреотропного гормона (TSHR), трансмембранным сопряженным с G-белком рецептором базолатеральной мембраны клетки, стимулируя, в том числе, накопление цАМФ, йодирование белка и эндоцитоз коллоида. Подвергнутые эндоцитозу везикулы сливаются с лизосомами в клетке, в которой тиреоглобулин, несущий йодированные предшественники T4-тироксина и T3-трийодтиронина с двойным кольцом, подвергается протеолитической деградации для высвобождения T4-тироксина и T3-трийодтиронина.
Интратиреоидная 5'-дейодиназа является селеносодержащим ферментом, который может превращать T4-тироксин в активный гормон T3-трийодтиронин. Также необходимо отметить, что щитовидная железа активно захватывает йод для обеспечения достаточного запаса тиреоидных гормонов.
Первичным регулятором синтеза T4-тироксина и T3-трийодтиронина, как указано выше, является тиреотропный гормон (TSH). Его стимуляторная активность подчиняется механизму обратной связи, посредством которой уровни TSH подавляются циркулирующими T4-тироксином и T3-трийодтиронином. Таким образом, одним из биологических маркеров гипертиреоза (более высоких уровней циркулирующих T4-тироксина и T3-трийодтиронина) является более низкий уровень тиреотропного гормона (TSH). Хемилюминесцентные анализы позволяют определять TSH на уровнях 0,05 Ед/мл или ниже, которые являются уровнями, как правило, диагностическими для гипертиреоза.
Трийодтиронин, T3, воздействует на большинство тканей организма, повышая уровень основного метаболизма и, таким образом, потребление организмом кислорода и энергии. Одним из механизмов действия трийодтиронина (T3) является стимуляция экспрессия генов. Например, среди прочих его биологических действий, трийодтиронин (T3) связывает белок, молекулу активатора рецептора тиреоидного гормона, и образованный таким образом комплекс, по-видимому, участвует в стимуляции транскрипции гена, кодирующего рецептор тиреоидного гормона (TR).
Используя способы и реагенты, представленные в настоящем описании, наблюдали, что у животных с гипертиреозом экспрессия и активность ряда указанных выше белков и полипептидов является по существу повышенной (см. таблицу 1).
|
Как показывают данные в таблице 1, у кошек с гипертиреозом экспрессия натрий-йодного транспортера (NIS) повышена в 2,7 раз, активность тиреоидной пероксидазы (TPO) повышена в 1,9 раз, активность рецептора тиреотропного гормона (TSHR) повышена в 1,6 раз, активность транспортера йода (IT; пендрина) повышена в 1,4 раз, и активность тиреоидной оксидазы (ThOX) повышена в 1,4 раз.
Учитывая данные в таблице 1, например, можно предполагать, что гены, транскрипты, белки и полипептиды, идентифицированные как вовлеченные в заболевание или состояние у одного рода или вида, также вовлечены в сравнимое заболевание или состояние у другого рода или вида. Подтверждение таких предположений легко получить посредством выявления соответствующих генов, транскриптов, белков и полипептидов у второго вида и измерения уровней их экспрессии у нормальных и больных животных с использованием способов и материалов, хорошо известных в этой области. Такие способы включают, в качестве неограничивающих примеров, анализ генома и сравнительные анализы генома (например, человека и кошки), биоинформатические, протеомные и транскриптомные анализы нормальных и больных животных. Гомологичные гены можно определять и выделять, используя способы гибридизации и амплификацию посредством полимеразной цепной реакции (ПЦР), а также другие способы и подходы, известные специалистам в этой области.
Определение полипептидов, вовлеченных в этиологию заболевания, можно обнаруживать в литературе, или оно может включать, например, осуществление транскрипции и протеомных анализов тканей здоровых животных в сравнении с тканями животных, страдающих целевым заболеванием. Такие анализы будут показывать, какие белки могут быть вовлечены в этиологию целевого заболевания, а также то, повышение или снижение экспрессии может коррелировать с наличием и тяжестью заболевания или состояния. Дополнительную информацию можно получать с использованием, например, инбредных животных (мышей), страдающих или генетически сконструированных страдающими целевым заболеванием или состоянием. В дополнительных аспектах определение полипептида, вовлеченного в этиологию, лежащую в основе целевого заболевания или состояния, и определение того, повышение ли или снижение активности или экспрессии указанного идентифицированного полипептида будет улучшать целевое заболевание или состояние, можно облегчать с использованием культур клеток, выращиваемых из здоровой ткани, а также соответствующей ткани от больного животного. В таких системах активность белка-мишени в здоровой и поврежденной тканях можно определять с помощью биохимических анализов с использованием способов, как правило, известных в этой области или легко разрабатываемых с использованием реагентов и способов, как правило, известных в этой области.
В практическом осуществлении настоящего изобретения можно использовать многие общепринятые способы молекулярной биологии, включая конструирование рекомбинантных векторов, систем экспрессии и трансформированные клетки и клеточные линии, содержащие такие рекомбинантные векторы, системы экспрессии, содержащие и экспрессирующие, например, ген NIS кошек, ген ядерного рецептора тиреоидного гормона и гены, кодирующие репортерные полипептиды, в частности, находящиеся в функциональной связи с элементом, чувствительным к тиреоидному гормону. Иллюстративные репортерные полипептиды включают, в качестве неограничивающих примеров, β-галактозидазу, HcRed, DsRed, мономер DsRed, ZsGreen, AmCyan, ZsYellow, люциферазу светлячка, lac Z, люциферазу Renilla, SEAP, усиленный зеленый флуоресцентный белок (eGFP), d2EGFP, усиленный синий флуоресцентный белок (eBFP), усиленный желтый флуоресцентный белок (eYFP) и GFPuv, усиленный циановый флуоресцентный белок (eCFP), циановый, желто-зеленый, красный флуоресцентный белок рифовых кораллов и флуоресцентный белок рифовых кораллов дальнего красного спектра, альфа-1-антитрипсин человека (hAAT) и/или их фрагменты, модификации или функциональные варианты.
Как применяют в настоящем описании, в определенных вариантах осуществления определение "уровней экспрессии белка", "экспрессии гена" или "уровней экспрессии гена" включает, в качестве неограничивающих примеров, определение уровней соответствующих РНК, белка или пептида (или их комбинаций). Способы по настоящему изобретению не ограничены конкретным способом определения уровней белка, пептида или РНК, все из которых хорошо известны в этой области. Кроме того, экспрессию гена и уровни экспрессии гена можно оценивать в любой клетке или ткани, подходящей для экспрессии интересующего гена. В одном из вариантов осуществления, при необходимости, экспрессию гена оценивают в клетках крови. Другие типы клеток включают, в качестве неограничивающих примеров, клетки щитовидной железы, мышечные клетки, нервные клетки, глиальные клетки, эндотелиальные клетки, клетки кожи, клетки печени, клетки почек и костные клетки. Клетки могут являться первичными клетками, т.е. взятыми непосредственно у животного, такими как клетки, выделенные из недавно забранной крови или биопсийных тканей. Клетки также могут являться не первичными, т.е. устойчивой клеточной линией посредством пассажей или даже иммортализованной клеточной линией, таким образом, что способы определения уровней экспрессии гена можно осуществлять на устойчивых линиях клеток животных, например, клетках CHO, перед введением композиции животному.
Мультивариантный анализ профилей экспрессии генов у кошек с диагнозом гипертиреоз, а также здоровых, соответствующих по возрасту кошек без гипертиреоза позволил выявить, что эти две группы животных можно различать в зависимости от набора дифференциально экспрессирующихся генов. В этом большем наборе генов было пять генов, участвующих в биосинтезе тиреоидных гормонов, экспрессирующихся на более высоких уровнях у кошек с гипертиреозом. Среди них геном с наибольшим уровнем экспрессии в тиреоидной ткани у кошек с гипертиреозом являлся натрий-йодный симпортер (NIS).
Таким образом, настоящее изобретение относится к выделенному фрагменту гена, кодирующему часть натрий-йодного симпортерного белка кошек (белка NIS), имеющему нуклеотидную последовательность SEQ ID NO:1 и кодирующему пептид, имеющий аминокислотную последовательность SEQ ID NO:2.
Также настоящее изобретение относится к рекомбинантным векторам и трансформированным клеткам, содержащим выделенный фрагмент гена NIS кошек. Настоящее изобретение также относится к способам, включающим использование таких выделенных молекул ДНК для определения профилей экспрессии гена NIS кошек у здоровых и больных животных и измерения профилей экспрессии гена NIS в присутствии и в отсутствие пищевых ингредиентов и их экстрактов для этих генов для получения пищевых композиций для домашних животных, подходящих для введения животным-компаньонам из семейства кошачьих, страдающих гипертиреозом. Настоящее изобретение также относится к композициям и способам лечения гипертиреоза у кошек.
Экспрессия гена NIS у кошек с гипертиреозом и основанные на ней способы
Способы по настоящему изобретению частично основаны на обнаружении того, что конкретные профили экспрессии гена у кошек коррелируют с изменением состояния таких животных от нормального к гипертиреозу. Корреляцию конкретного профиля экспрессии гена с наличием и тяжестью гипертиреоза можно прогнозировать, определять и диагностировать у кошки без постановки общепринятого клинического диагноза на основе общепринятых в этой области клинических признаков и симптомов.
В одном из вариантов осуществления настоящее изобретение относится к одному или нескольким генам или сегментам генов (определенных в настоящем описании как "гены"), дифференциально экспрессирующимся у больных животных по сравнению с нормальными животными. Изобретение зависит от обнаружения полинуклеотидов, дифференциально экспрессирующихся у больных животных по сравнению с нормальными животными. Гены определяли, сравнивая экспрессию генов в образцах тканей, взятых у диагностированных больных животных, с экспрессией генов в образцах тканей от диагностированных нормальных животных с использованием технологии Affymetrix GeneChip®.
Полинуклеотиды и гены определяют посредством измерения различий экспрессии гена из образцов тканей, взятых у диагностированных больных кошек, т.е. с гипертиреозом, и экспрессии генов в образцах тканей от диагностированных нормальных кошек. Изменения экспрессии генов можно определять любым способом, известным специалистам в этой области. Как правило, изменения экспрессии генов определяют посредством измерения транскрипции (определяя количество мРНК, продуцируемой с этого гена) или измерения трансляции (определяя количество белка, продуцируемого с этого гена). Количество РНК или белка, продуцируемого с этого гена, можно определять с использованием любого способа, известного специалистам в этой области, для количественного анализа полинуклеотидов и белков.
Как правило, экспрессию мРНК определяют с использованием полимеразной цепной реакции (ПЦР) (включая, в качестве неограничивающих примеров, ПЦР с обратной транскрипцией (RT-ПЦР) и количественную ПЦР в реальном времени (qPCR)), чипы с короткими или длинными олигонуклеотидами, кДНК-чипы, EST-секвенирование, "нозерн"-блоттинг, SAGE, MPSS, MS, анализы с использованием микрочастиц и другие способы гибридизации. Измеряемая РНК, как правило, находится в форме мРНК или обратно транскрибированной мРНК.
Экспрессию белка или полипептида определяют с использованием различных колориметрических и спектроскопических анализов и способов, таких как количественный вестерн-блоттинг, ELISA, 2D-гели, газовая или жидкостная хроматография, масс-спектроскопия.
Генетические чипы делают возможным крупномасштабное исследование биологических процессов и измерение активности в клетке в конкретный момент времени. Анализ с использованием микрочипов позволяет оценивать различия фенотипов на крупномасштабной генетической основе. Точное измерение продуктов экспрессии гена является более точным индикатором функции гена, чем определение последовательностей per se. Анализ с использованием микрочипов зависит от количественного анализа концентрации транскрипта мРНК гена в клетке в указанное время. ДНК иммобилизуют на носителе, и меченая мРНК-мишень гибридизуется с зондами на чипе. Связывание меченой мРНК с зондами измеряют с помощью лазерного анализа. Измерение представляет собой подсчет испускаемых фотонов. Весь чип сканируют и визуализируют цифровым способом. Изображение обрабатывают для локализации зондов и приписывания измеренных интенсивностей каждому зонду. Таким образом, можно определять гены с пониженной и повышенной регуляцией. Анализ позволяет специалисту обнаруживать группы генов со схожими профилями экспрессии и обнаруживать ткани со схожими профилями экспрессии. Таким образом, можно определять гены, с помощью которых можно объяснять наблюдаемые различия в образцах тканей.
В генетических чипах Affymetrix, как правило, используют зонды длиной 25 п. н. и наборы зондов от 11 до 20 зондов, соответствующих конкретному гену или EST. Конструируют чип с полным совпадением и зонд с несовпадением длиной 25 п. н. каждый, первый из которых полностью комплементарен конкретной области гена, а последний содержит замененную 13-ую п. н. не получения несовпадения. Алгоритм суммирования зондов используют для определения поправки на фон, нормирования и суммирования зондов, представляющего собой конвертирования значений зондов в значения экспрессии набора зондов. RMA является одним из алгоритмов, которые можно использовать для этой цели. С использованием алгоритма осуществляют последние два этапа анализа, нормирование и суммирование измерений зонд-уровень интенсивности. Таким образом, значения полного совпадения являются скорректированными по фону, нормированными и суммированными в набор измерений экспрессии.
Исходные данные анализируют с использованием программного обеспечения GeneSpring версии 7.0 (GS) (Agilent Corporation) и валидируют с использованием бесплатного программного обеспечения R-Bioconductor (RB). Оба пакета программ используют для вычисления зонд интенсивности из файлов CEL, генерируемых устройством Affymetrix. Сигналы Present/Absent/Marginal на зонд и значения P вычисляют с использованием программного обеспечения R-Bioconductor и GeneSpring раздельно.
Как правило, дифференциальную экспрессию гена у больных животных по сравнению с нормальными животными определяют посредством измерения экспрессии по меньшей мере одного гена. В определенных вариантах осуществления экспрессию двух или более дифференциально экспрессирующихся генов измеряют для получения профиля экспрессии гена. В других вариантах осуществления для получения дополнительной информации для более значимого профиля экспрессии гена измеряют экспрессию множества дифференциально экспрессирующихся генов.
В другом аспекте настоящее изобретение относится к устройству, подходящему для определения экспрессии множества генов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками. Устройство включает субстрат, содержащий множество олигонуклеотидных или полинуклеотидных зондов по настоящему изобретению, прикрепленных к субстрату в известных местах. Устройство по существу является иммобилизованной версией олигонуклеотидных или полинуклеотидных зондов, представленных в настоящем описании. Устройство применимо для быстрого и специфичного определения генов и полинуклеотидов и профилей их экспрессии. Как правило, такие зонды присоединяют к субстрату или аналогичной твердой подложке, а образец, содержащий один или несколько полинуклеотидов (например, ген, продукт ПЦР, продукт лигазной цепной реакции (LCR), последовательность ДНК, синтезированную с использованием способов амплификации, или их смесь), подвергают воздействию зондов таким образом, что полинуклеотиды в образце могут гибридизоваться с зондами. Зонды, полинуклеотиды в образце или и то, и другое метят, как правило, флуорофором или другой меткой, такой как стрептавидин, и определяют с использованием способов, известных специалистам в этой области. Если полинуклеотиды в образце являются мечеными, гибридизацию можно определять посредством детекции флуоресценции при связывании. Если зонды являются мечеными, гибридизацию, как правило, определяют по тушению метки. Если и зонд, и полинуклеотиды в образце являются мечеными, гибридизацию, как правило, определяют, контролируя цветовой сдвиг, являющийся результатом сближения двух связанных меток. Специалистам в этой области известно множество стратегий мечения и меток, в частности, для флуоресцентного мечения. Предпочтительно, зонды иммобилизуют на субстратах, подходящих для образования чипа (известного под несколькими названиями, включая ДНК-микрочип, генетический чип, биочип, ДНК-чип), сравнимого с известными в этой области.
Специалистам в этой области известны способы определения количества или концентрации белка в образце. Такие способы включают радиоиммунологические анализы, анализы конкурентного связывания, анализ вестерн-блоттинга и анализы ELISA. Для способов с использованием антител подходят поликлональные и моноклональные антитела. Такие антитела могут являться иммунологически специфичными для белка, эпитопа белка или фрагмента белка.
В некоторых вариантах осуществления изобретения используют антитела для определения и количественного анализа белков, образующихся в результате экспрессии полинуклеотидов по настоящему изобретению. Хотя белки можно определять с помощью иммунопреципитации, аффинного разделения, анализа вестерн-блоттинга, белковых чипов и т.п., в предпочтительном способе используют технологию ELISA, где антитело иммобилизуют на твердой подложке, а белок- или пептид-мишень подвергают воздействию иммобилизованного антитела. Зонд или мишень, или и то, и другое можно метить с использованием известных способов.
В дополнительном аспекте изобретение относится к способу определения дифференциальной экспрессии одного или нескольких генов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками в образце. Способ включает (a) гибридизацию комбинации, содержащей множество полинуклеотидных зондов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками, с полинуклеотидами в образце для образования одного или нескольких гибридизационных комплексов; (b) необязательно, гибридизацию комбинации, содержащей множество полинуклеотидных зондов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками, с полинуклеотидами в стандарте для образования одного или нескольких гибридизационных комплексов; (c) определение гибридизационных комплексов из образца и, необязательно, стандарта из этапа (b); и (d) сравнение гибридизационных комплексов из образца с гибридизационными комплексами из стандарта, где различие в количестве гибридизационных комплексов между стандартом и образцом свидетельствует о дифференциальной экспрессии генов, дифференциально экспрессирующихся у больных животных по сравнению с нормальными животными в выборке.
Этап (b) и часть этапа (c) являются необязательными, и их используют, если проводят относительно одновременное сравнение двух или более тестовых систем. Однако в предпочтительном варианте осуществления стандарт, используемый для сравнения, зависит от данных, полученных ранее с использованием способа.
Эти зонды подвергают воздействию образца для образования гибридизационных комплексов, определяемых и сравниваемых с гибридизационными комплексами в стандарте. Различия между гибридизационными комплексами из образца и стандарта свидетельствуют о дифференциальной экспрессии полинуклеотидов и, таким образом, о генах, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками в выборке. В определенных вариантах осуществления получают зонды для специфического определения полинуклеотидов или их фрагментов, являющихся продуктами одного или нескольких генов или фрагментов генов, определенных с помощью настоящего изобретения. Способы определения гибридизационных комплексов известны специалистам в этой области.
В другом аспекте изобретение относится к способу определения дифференциальной экспрессии генов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками в выборке. Способ включает (a) реакцию комбинации, содержащей множество полипептидных зондов, с белками в образце в условиях, делающих возможным осуществление специфического связывания между зондами и белками, где белки, связываемые зондами, дифференциально экспрессируются у больной кошки по сравнению с нормальной кошкой; (b) необязательно, реакцию комбинации, содержащей множество полипептидных зондов, с белками в стандарте в условиях, делающих возможным осуществление специфического связывания между зондами и белками, где белки, связываемые зондами, дифференциально экспрессируются у больной кошки по сравнению с нормальной кошкой; (c) определение специфического связывания в образце и, необязательно, стандарте из этапа (b); и (d) сравнение специфического связывания в образце и стандарте, где различия между специфическим связыванием в стандарте и образце свидетельствуют о дифференциальной экспрессии генов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками в выборке.
Эти зонды подвергают воздействию образца для осуществления специфического связывания, определяемого и сравниваемого с таковым в стандарте. Различия между специфическим связыванием в образце и стандарте свидетельствуют о дифференциальной экспрессии белков и, таким образом, о генах, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками, в частности, ассоциированных с заболеванием генов, в выборке. В предпочтительном варианте осуществления получают зонды для специфического определения белков или их фрагментов, являющихся продуктами одного или нескольких генов или фрагментов генов, определяемых с помощью настоящего изобретения.
В одном из вариантов осуществления способ дополнительно включает подвергание кошки или образца воздействию тестового вещества перед реакцией полипептидов с белками. Затем сравнение свидетельствует о том, изменяет ли тестовое вещество экспрессию генов, дифференциально экспрессирующихся у больных кошек по сравнению с нормальными кошками, в частности, ассоциированных с заболеванием генов, в выборке.
Таким образом, изобретение относится к способу диагностики наличия и тяжести гипертиреоза у кошки, включающему измерение уровня экспрессии биомаркеров NIS в биологическом образце, взятом у кошки, где различия в экспрессии гена NIS относительно контрольного значения экспрессии в образце от нормального животного свидетельствуют о наличии гипертиреоза и отражают его тяжесть, по любому из следующих иллюстративных способов:
По этому способу уровень экспрессии биомаркера NIS определяют посредством измерения экспрессии гена с использованием (i) ДНК-микрочипа, содержащего один или несколько олигонуклеотидов, комплементарных мРНК или кДНК, соответствующей гену NIS, или (ii) количественной полимеразной цепной реакции с олигонуклеотидными праймерами к мРНК или кДНК, соответствующей гену NIS.
По этому способу этап измерения экспрессии гена биомаркера NIS включает (i) выделение РНК из образца ткани, (ii) обратную транскрипцию РНК для получения соответствующей кДНК, (iii) выделение и фрагментацию полученной, таким образом, кДНК, (iv) приведение фрагментов кДНК в контакт с ДНК-микрочипом, содержащим один или несколько олигонуклеотидов, комплементарных кДНК, соответствующей одному или нескольким биомаркерам, подлежащим измерению, и (v) определение гибридизации между фрагментами кДНК и одним или несколькими олигонуклеотидами на ДНК-микрочипе. В определенном аспекте этого варианта осуществления гибридизацию между фрагментами кДНК и одним или несколькими олигонуклеотидами на ДНК-микрочипе проводят в строгих условиях.
В другом варианте осуществления уровень экспрессии биомаркера NIS определяют с помощью антитела к экспрессируемому белку. В этом варианте осуществления биомаркер NIS определяют с помощью иммунологического анализа, выбранного из анализа конкурентного связывания, анализа неконкурентного связывания, радиоиммунологического анализа, твердофазного иммуноферментного анализа (ELISA), сэндвич-анализа, реакции преципитации, гель-диффузии, анализа иммунодиффузии, анализа агглютинации, флуоресцентного иммунологического анализа, хемилюминесцентного иммунологического анализа, иммуно-ПЦР, иммунологического анализа с использованием протеина A или протеина G и иммуноэлектрофореза.
В одном из аспектов этого варианта осуществления указанный выше способ является твердофазным иммуноферментным анализом (ELISA) или иммунохроматографическим анализом по принципу бокового сдвига. В других аспектах этого варианта изобретения уровень экспрессии биомаркера определяют с помощью количественной масс-спектроскопии с измерением экспрессирующегося белка в биологическом образце, или биомаркер NIS определяют с помощью аптамера, распознающего экспрессирующийся белок, где аптамер может являться олигонуклеотидом или пептидом.
В определенных аспектах уровень экспрессии биомаркеров NIS в биологическом образце животного с гипертиреозом относительно контрольного значения экспрессии в образце от здорового животного повышается у больного животного по сравнению со здоровым животным в 1,25, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9 или 3 раза или более. В других аспектах уровень экспрессии биомаркеров NIS в биологическом образце больного животного снижается, например, в 1,25, 1,3, 1,4, 1,5, 1,6, 1,7, 1,8, 1,9, 2,0, 2,1, 2,2, 2,3, 2,4, 2,5, 2,6, 2,7, 2,8, 2,9 или 3 раза или более. В определенном варианте осуществления биомаркер NIS определяют in vitro в подходящей модельной системе культуры клеток.
В других аспектах этих вариантов изобретения уровень экспрессии биомаркера NIS в биологическом образце на одно или по меньшей мере одно стандартное отклонение выше или ниже, чем средняя экспрессия этого биомаркера в нормальном образце. В других аспектах этих вариантов осуществления уровень экспрессии биомаркера NIS в биологическом образце нормируют относительно экспрессии одного или нескольких генов, о которых известно, что они имеют относительно постоянную экспрессию.
В другом варианте осуществления изобретение относится к способу лечения гипертиреоза у нуждающейся в этом кошки, включающему диагностику наличия гипертиреоза с использованием, например, описываемых выше способов, и регуляцию состояния, например, только с помощью рациона или в комбинации с подходящим лекарственным средством. В одном из аспектов этого варианта осуществления рацион включает один или несколько компонентов, определенных способами, представленными в настоящем описании, где компоненты применимы для снижения захвата йода щитовидной железой или для ингибирования синтеза тиреоидного гормона, включая, в том числе, компоненты, способные снижать или ингибировать экспрессию гена NIS или снижать или ингибировать функцию белка NIS.
В дополнительном варианте осуществления изобретение относится к реагентам, необязательно меченым, применимым в определении уровня экспрессии биомаркера NIS у кошки. Такие реагенты могут включать, например, антитела, например, моноклональные антитела, одноцепочечные антитела и функциональные фрагменты антител, избирательно распознающие белок NIS кошек, например, антитела, например, моноклональные антитела, одноцепочечные антитела и функциональные фрагменты антител, избирательно распознающие пептид SEQ ID NO:2. Другие такие реагенты включают аптамеры, например, аптамеры нуклеиновых кислот или пептидов, избирательно распознающие белок NIS кошек или пептид SEQ ID NO:2, а также олигонуклеотидные зонды, способные избирательно гибридизоваться с геном NIS кошек или нуклеотидной последовательностью SEQ ID NO:1.
В дополнительном варианте осуществления настоящее изобретение относится к набору (набор 1) для диагностики, прогнозирования или мониторинга гипертиреоза у кошки, содержащему средства для измерения экспрессии гена NIS кошек в биологическом образце от кошки и инструкции по использованию таких средств для измерения экспрессии гена NIS в биологическом образце от кошки и оценки наличия процесса, приводящего к гипертиреозу у кошки. Средства в наборе для измерения одного или нескольких биомаркеров являются одним или несколькими нуклеиновыми кислотами-зондами, с помощью которых можно определять экспрессию гена NIS, где зонды способны избирательно гибридизоваться с нуклеиновой кислотой SEQ ID NO:1 в строгих условиях.
В других аспектах этих вариантов изобретения средства для измерения одного или нескольких биомаркеров являются одним или несколькими антителами, с помощью которых можно определять экспрессию гена NIS посредством избирательного распознавания экспрессирующегося белка NIS или посредством избирательного распознавания пептида SEQ ID NO:2. Такие наборы могут находиться в формате ELISA, содержащем антитело, с помощью которого можно определять белок NIS, включая выделенный, очищенный или рекомбинантный белок NIS, соответствующий экспрессирующемуся белку или пептидной последовательности SEQ ID NO:2, и буфер.
В других аспектах этого варианта осуществления средства для измерения биомаркера NIS являются одним или несколькими аптамерами, например, описываемыми выше, с помощью которых можно определять экспрессию гена белка NIS, или они могут распознавать экспрессирующийся белок NIS.
В одном из вариантов осуществления настоящее изобретение относится к способу диагностики гипертиреоза у кошки. Этот способ включает определение уровня пептида SEQ ID NO:2, обнаруживаемого в биологическом образце кошки, подвергнутой тестированию на предмет гипертиреоза, и затем сравнение этого уровня с референсным уровнем этого пептида, определенным у здоровых кошек, т.е. тех, о которых известно, что они не страдают гипертиреозом. Повышенный уровень пептида SEQ ID NO:2 у тестируемой кошки является диагностическим для гипертиреоза, и степень этого повышения свидетельствует о тяжести состояния.
В определенных аспектах этого варианта изобретения уровень пептида SEQ ID NO:2 можно определять способами, представленными в настоящем описании, а также известными в этой области. В конкретных аспектах этого варианта осуществления определение уровня пептида SEQ ID NO:2 осуществляют с использованием антитела, фрагмента антитела или аптамера в качестве индикатора. В конкретных аспектах индикатор является моноклональным антителом, в то время как в других он является Fab-фрагментом, F(ab')2-фрагментом, Fv-фрагментом или аптамером.
В дополнительном варианте осуществления настоящее изобретение относится к способу диагностики гипертиреоза у кошки, включающему определение уровня нуклеиновой кислоты, кодирующей пептид SEQ ID NO:2, в биологическом образце кошки, и затем сравнение этого значения с референсным уровнем этой нуклеиновой кислоты, определенным у контрольных кошек без гипертиреоза. По этому способу повышенный уровень нуклеиновой кислоты в образце от кошки по сравнению с референсным уровнем является диагностическим для гипертиреоза у кошки. В определенных аспектах этого варианта изобретения уровень нуклеиновой кислоты определяют с использованием способов, включающих использование количественной RT-ПЦР. В другом аспекте этого варианта осуществления уровень нуклеиновой кислоты определяют с использованием способов, включающих использование микрочипов, включая те, в которых микрочип содержит множество выделенных полинуклеотидов, выбранных из группы, состоящей из РНК, ДНК, кДНК, продуктов ПЦР или EST, в которых полинуклеотид кодирует, по меньшей мере, часть пептида SEQ ID NO:2. В конкретном аспекте этого варианта осуществления нуклеиновая кислота является РНК.
Настоящее изобретение также относится к способу мониторинга гипертиреоза у больной кошки. Этот способ включает определение первого уровня пептида SEQ ID NO:2 в биологическом образце от кошки в первый момент времени с последующим определением второго уровня пептида SEQ ID NO:2 в биологическом образце от кошки во второй, последующий момент времени. Два уровня сравнивают, и повышение уровня пептида SEQ ID NO:2 с течением времени свидетельствует о прогрессировании гипертиреоза, а снижение уровня пептида SEQ ID NO:2 с течением времени свидетельствует о регрессировании гипертиреоза.
В другом варианте осуществления настоящее изобретение также относится к способу мониторинга гипертиреоза у больной кошки, включающему определение первого уровня нуклеиновой кислоты, кодирующей пептид SEQ ID NO:2, в биологическом образце от кошки с последующим определением второго уровня нуклеиновой кислоты, кодирующей пептид SEQ ID NO:2, в биологическом образце от кошки, во второй, более поздний момент времени. Два значения сравнивают, и повышение уровня нуклеиновой кислоты, кодирующей пептид SEQ ID NO:2, с течением времени свидетельствует о прогрессировании гипертиреоза, а снижение уровня нуклеиновой кислоты, кодирующей пептид SEQ ID NO:2, с течением времени свидетельствует о регрессировании гипертиреоза.
Настоящее изобретение также относится к наборам, применимым в этих способах. В одном из вариантов осуществления настоящее изобретение относится к набору, содержащему средства для измерения уровня экспрессии гена NIS кошек в биологическом образце от кошки. Средства, используемые для этого определения, могут включать по меньшей мере один индикатор, выбранный из группы, состоящей из нуклеиновых кислот-зондов, антител, фрагментов антител и аптамеров, где с помощью индикатора можно определять экспрессию гена NIS кошек в биологическом образце от кошки с использованием способов, представленных в настоящем описании, а также известных в этой области. В одном из аспектов этого варианта осуществления набор включает инструкции по использованию указанных выше средств для измерения экспрессии гена NIS кошек в биологическом образце от указанной кошки. В конкретных аспектах этого варианта осуществления используемые средства включают антитело или фрагмент антитела, специфически распознающий пептид SEQ ID NO:2. В другом аспекте этого варианта осуществления используемые средства включают первый и второй олигонуклеотид, где первый олигонуклеотид специфически гибридизуется с некодирующей цепью нуклеиновой кислоты SEQ ID NO:1, и где второй олигонуклеотид специфически гибридизуется с кодирующей цепью нуклеиновой кислоты SEQ ID NO:1. Комбинацию этих двух олигонуклеотидов можно использовать для ПЦР-амплификации части молекулы ДНК SEQ ID NO:1, кодирующей пептид SEQ ID NO:2.
Можно разрабатывать дополнительные диагностические способы, наборы и композиции в зависимости от описываемых последовательностей нуклеиновой кислоты и пептида с использованием реагентов и способов, описываемых в совместной заявке № 12/600064 и заявке № 13/054745, обе из которых, таким образом, включены в настоящее описании в качестве ссылки в полном объеме.
Дополнительные области применения настоящего изобретения будут очевидны из подробного описания, представленного далее в настоящем описании. Следует понимать, что подробное описание и конкретные примеры, хотя и демонстрируют предпочтительный вариант осуществления изобретения, предназначены исключительно для иллюстративных целей, а не для ограничения объема изобретения.
Функциональный профиль гена
Настоящее изобретение относится к выделенным генам и способам использования этих генов для рационального получения композиций, применимых для улучшения здоровья животного-компаньона из семейства кошачьих, страдающего гипертиреозом.
Нутритивная геномика ("нутригеномика") является относительно новым направлением геномных исследований у людей, возникшим на рубеже условий питания и клеточных и генетических процессов. С помощью нутригеномики стремятся достичь генетического понимания того, как компоненты рациона и/или питание влияет на баланс между здоровьем и заболеванием, например, изменяя экспрессию и/или структуру набора генов индивидуума. Показано, что некоторые компоненты рациона изменяют экспрессию генов различными путями. Например, они могут действовать как лиганды для белков, таких как факторы транскрипции или рецепторы, могут метаболизироваться с помощью первичных или вторичных метаболических путей, таким образом, изменяя концентрации субстратов или промежуточных продуктов, или могут участвовать в путях передачи сигнала.
Функциональный геномный профиль: Как применяют в настоящем описании, термин "фенотип" относится к совокупности, или любой ее части, наблюдаемых характеристик, функциональных или других, организма, определяемых генотипом организма. Термин "генотип" относится к общей генетической структуре организма или любой ее части. Генотип содержит генетическую информацию, хранящуюся в хромосомах или экстрахромосомно.
Как применяют в настоящем описании, фраза "функциональный профиль гена" относится к совокупности или любой части функциональных последствий экспрессии определенных последовательностей гена, включая продукцию и функцию мРНК, белков и метаболитов, относящихся к активности конкретных генов. Функциональный профиль гена (FGP) можно определять с использованием геномных, протеомных или метаболомных подходов или любой их комбинации.
Функциональный профиль гена каждого гена, представленного в настоящем описании, ген NIS кошек, таким образом, можно определять по его экспрессии и активности, отражающихся в транскрибирующейся с него мРНК, количестве кодируемого белка, биологической активности этого белка и метаболитах, продуцируемых в результате его активности. Каждый из этих индикаторов можно измерять с использованием способов, представленных в настоящем описании, а также известных в этой области. Эти профили генов определяют у здоровых кошек, а также у кошек, страдающих гипертиреозом, что позволяет определять корреляцию между экспрессией гена и наличием и тяжестью гипертиреоза у кошек. Эти профили генов также определяют у здоровых кошек, а также кошек, страдающих гипертиреозом, и с введением биоактивного компонента рациона и без него.
Данные, лежащие в основе функционального профиля гена, можно получать из биологической жидкости и/или образцов ткани любым способом, известным в области функциональной геномики. Примеры способов, применимых в осуществлении функционального геномного анализа, включают, в качестве неограничивающих примеров, следующие способы, которые можно использовать отдельно или в комбинации: (a) одно- и многоцветные генетические и белковые чипы и микрочипы в формате низкой и высокой плотности, например, на подложке из стекла, диоксида кремния, пластика, мембраны или микрочастиц или их комбинаций, включая, например анализ нозерн-блоттинга и анализ вестерн-блоттинга; (b) способы масс-спектрометрии с использованием квадрупольных масс-спектрометров, масс-спектрометров с временем пролета, квадрупольной ионной ловушкой или ионным циклотронным резонансом с Фурье-преобразованием или их комбинаций с различными источниками ионизации, включая, в качестве неограничивающих примеров, лазерную десорбцию-ионизацию в присутствии матрицы, ионизацию электрораспылением, ионизацию с нанораспылением и поверхностно-усиленную лазерную десорбцию-ионизацию; (c) способы полимеразной цепной реакции (ПЦР), включая одиночные и мультиплексные способы количественной ПЦР в реальном времени; (d) электрофорез в геле (одно- или многомерный), включая способы двухцветного электрофореза в 2D-геле, SDS-электрофорез в полиакриламидном геле (SDS-PAGE) и 2D PAGE; и (e) жидкостную хроматографию (одно- или многомерную) в отдельности или вместе с масс-спектрометрией.
Функциональный профиль гена можно получать из изображения формата RAW, набора числовых и/или текстовых данных, как правило, после нормирования и предварительной обработки для снижения или удаления данных фона. Способы, которые можно использовать для распознавания функционального профиля гена, включают, в качестве неограничивающих примеров, распознавание ближайшего соседа, нейронные сети, скрытые Марковские модели, Байесовы сети, генетические алгоритмы, способ опорных векторов и их комбинации.
Функциональный профиль генов кошек, представленных в настоящем описании, который можно измерять у здоровых кошек, кошек, страдающих легким гипертиреозом, кошек, страдающих тяжелым гипертиреозом, или модели на животных, или в их тканях или клетках, таким образом, может находиться в "нормальном" или "ненормальном" состоянии. "Нормальный" функциональный профиль гена для описываемых генов является профилем, определяемым у животного, демонстрирующего состояние здоровья, как определено в настоящем описании, и, как правило, свидетельствующим о таком состоянии. Как правило, "нормальный" функциональный профиль гена ассоциирован с гомеостазом, т.е. тенденции к стабильности функций организма, возникающей, например, в результате действия внутренних систем контроля, активированных отрицательной обратной связью. "Ненормальным" функциональным профилем гена является профиль, выходящий за рамки диапазона, определенного как "нормальный", и который может коррелировать с наличием гипертиреоза у тестируемых кошек. Такой "ненормальный" функциональный профиль гена может быть ассоциирован с ухудшением гомеостаза; таким образом, в случае "ненормального" функционального профиля гена часто существует тенденция к дальнейшему смещению относительно нормальности с течением времени и прогрессированию гипертиреоза, например, от слабого к тяжелому, в отсутствие вмешательства (например, с помощью способа по настоящему изобретению) для прекращения или реверсирования такого смещения. При отсутствии контроля это прогрессирующее смещение относительно нормальности в конечном итоге может приводить к гибели. Таким образом, "ненормальный" функциональный профиль гена часто свидетельствует о состоянии, неблагоприятном состоянии заболевания или физиологического нарушения у животного, которое в данном контексте является гипертиреозом. Такое состояние может являться внешне очевидным или латентным (т.е. бессимптомным). В некоторых ситуациях "ненормальный" функциональный профиль гена может свидетельствовать о предрасположенности, наследственной или иной, к заболеванию, например, гипертиреозу, и в таких ситуациях сдвиг функционального профиля гена в сторону более нормального состояния (например, с помощью способа по настоящему изобретению) может являться эффективным в профилактике заболевания.
В определенных вариантах осуществления субпопуляцию кошек можно определять, например, как легко или тяжело страдающую гипертиреозом, по меньшей мере, относительно физиологического состояния. Термин "физиологическое состояние" в настоящем описании относится к любому физическому, патологическому, поведенческому и биохимическому показателю животного, включая его размер, массу, возраст, уровень активности, характер и состояние здоровья или заболевания, или их комбинации, например, как определяют по уровням трийодтиронина (T3) или тетрайодтиронина (тироксина или T4), или их обоих. Физиологическое состояние является результатом взаимодействия генотипа с окружающей животное средой.
Образцы биологической жидкости и тканей: Образец биологической жидкости или ткани, применимый в настоящем описании, может являться любым образцом, поддающимся генетическому, протеомному и/или метаболомному анализу. Для генетического анализа образец должен содержать ДНК в количестве, которое может потребовать или не потребовать амплификации, например, посредством способов ПЦР. Из образцов с недостатком ДНК или РНК, как это часто случается в случае, например, образцов мочи, никоим образом нельзя получать протеомную и/или метаболомную информацию.
Биологические жидкости, которые можно подвергать забору, включают экскреты (фекалии и мочу), кровь, слюну, амниотическую жидкость и т.д. Образцы ткани можно получать после смерти из любой части тела животного, но для настоящих целей более применимы образцы от живых животных, например, полученные посредством биопсии, удаления хирургическим путем (например, при хирургическом вмешательстве, осуществляемом с иной целью), буккального мазка или выщипывания нескольких волосков.
Первый набор данных: Системы и способы по изобретению, как указано выше, включают по меньшей мере два набора данных, обозначаемых в настоящем описании как "первый" (или выборочный) и "второй" (или тестовый) наборы данных. Эти наборы данных, как правило, хранят в цифровой форме и систематизируют в от одной до множества баз данных, находящихся в среде интерфейса пользователя, такой как любой компьютер, или периферийное устройство памяти или устройство для хранения данных. База данных может являться "виртуальной", т.е. существующей только в сети множества устройство.
Первый и второй наборы данных могут являться частями одной базы данных или могут находиться в отдельных базах данных. Любой или оба из первого и второго набора данных, при желании, можно сконфигурировать в несколько баз данных при условии, что можно осуществлять доступ к данным для обработки, как более подробно описано ниже.
Первый набор данных (выборочный набор данных) содержит данные, полученные при функциональном анализе генов многочисленных образцов биологических жидкостей и/или тканей, полученных из животных, представляющих широкий диапазон генотипов и фенотипов или физиологических состояний кошек, включая здоровых животных (как правило, демонстрирующих "нормальный" функциональный профиль гена) и животных с различными состояниями заболевания, например, с легким или тяжелым гипертиреозом, и, таким образом, демонстрирующих "ненормальный" функциональный профиль гена в отношении гена NIS кошек. Данные конфигурируют реляционно, т.е. таким образом, который делает возможной корреляцию функциональных параметров гена с генотипическими и фенотипическими признаками. Таким образом, первый набор данных можно использовать для определения функционального профиля гена не только для здоровых кошек, но также и для страдающих легким и тяжелым гипертиреозом, т.е. для конкретных субпопуляций, имеющих генотип и физиологическое состояние, включенные в набор данных. Т.к. первый набор данных повышается экстенсивно, среди прочих преимуществ, можно достигать ряда благоприятных результатов: (1) включается диапазон субпопуляций, например, определяемых по тяжести гипертиреоидного состояния, т.к. набор данных становится более обширным; (2) данные функционального профиля гена для этих конкретных субпопуляций становятся более достоверными; и (3) можно использовать данные с большей надежностью для получения прогнозируемого функционального профиля гена для субпопуляции, конкретно не представленной в данных. Таким образом, можно определять изменения экспрессии гена NIS кошек, как следствия показателей, иных, чем наличие и степень гипертиреоза, и это становится возможным при определении аспектов функционального профиля гена, коррелирующих с наличием и тяжестью состояния, например, гипертиреоза кошек.
Функциональный анализ гена, представленного в настоящем описании, для каждого образца, как отражено в первом наборе данных, может включать анализ в отношении одного или нескольких из ДНК, РНК (например, мРНК), белков, метаболитов и биомаркеров, таких как ферменты.
Данные, которые можно использовать для получения прогнозируемого функционального профиля гена NIS кошек, представленного в настоящем описании, можно получать из информации и данных из источников, иных, чем функциональный анализ гена в образцах биологических жидкостей и/или ткани, как описано выше, или дополнять ими. Например, в некоторых вариантах осуществления данные можно получать из исследований, опубликованных в литературе. В определенных вариантах осуществления данные можно получать из публично или коммерчески доступных банков данных, например, доступных через веб-сайт. В некоторых вариантах осуществления данные можно получать при интеллектуальном анализе данных о геноме вида исследуемого животного, и в других вариантах осуществления гомологичные функциональные геномные данные можно получать из видов, иных, чем исследуемое животное, таких как человек, крыса или мышь. В определенных вариантах осуществления данные можно получать посредством интеллектуального анализа данных о геномах видов, иных, чем исследуемое животное.
В определенном варианте осуществления, где способ направлен на сравнительно ограниченную мишень, например, гипертиреоз у кошек, набор данных можно получать с использованием относительно небольшого количества образцов. Таким образом, в одной серии вариантов осуществления первый набор данных получают из образцов, собранных от множества животных, представляющих диапазон генотипов и физиологических состояний, достаточно широкий для включения интересующей субпопуляции, например, кошек, страдающих гипертиреозом.
В определенных вариантах осуществления первый набор данных позволяет получать нормальный и ненормальный функциональные профили генов, представленных в настоящем описании, подлежащих определению для животных, имеющих диапазоны генотипов и физиологических состояний, включающих генотип и физиологическое состояние, соответственно, животного, для которого получали исходные данные. В отношении физиологических состояний в данном контексте, слово "включает" означает, что животные, отдельно и в совокупности имеющие схожие физиологические состояния относительно субъекта, представлены в наборе данных, даже если конкретную комбинацию физиологических состояний субъекта не обнаруживают ни в одном животном в наборе данных. Аналогично, диапазоны генотипов и физиологических состояний, представленных в первом наборе данных, рассматривают в настоящем описании как "включающие" генотип и физиологическое состояние субъекта, если такой генотип и физиологическое состояние независимо находят в наборе данных, даже если и не у одного и того же животного.
Каждый образец от отдельного животного, подлежащий использованию, должен быть связан с записью о происхождении, становящейся частью первого набора данных. Запись о происхождении содержит зоографические данные в отношении определения генотипа и физиологического состояния животного, от которого получают образец, на момент забора образца.
Термин "зоографические данные" в настоящем описании относится к любой и всей информации, количественной или качественной, собранной в отношении животного, от которого получают образец биологической жидкости или ткани, из источников, иных, чем анализ или эксперимент над самим образцом. Источники зоографических данных могут включать банк знаний собственника, зарегистрированный, например, в результате ответов на запросы, записи ветеринара, включая записи, свидетельствующие о прошлом и настоящем состоянии здоровья или заболевания, родословную животного, если она у него есть, биометрические данные (рост, массу и т.д.) на момент забора образца и т.д.
Зоографические данные, включенные в первый набор данных, могут содержать один или несколько элементов данных, относящихся к генотипу. Примеры таких элементов данных включают, в качестве неограничивающих примеров: породу животного, племенную, зарегистрированную организацией, такой как AKC или другой; родословную, если известна; в случае животных смешанной породы происхождение животного, включая породы его родителей и, по возможности, предков из более ранних поколений; пол; и тип шерстного покрова (например, длинная, короткая, жесткая, кудрявая, гладкая шерсть) и окрас; очевидные наследственные состояния и нарушения, включая, в качестве неограничивающих примеров, гипертиреоз.
Зоографические данные, включенные в первый набор данных, могут содержать один или несколько элементов данных, относящихся к физиологическому состоянию. Примеры таких элементов данных включают, в качестве неограничивающих примеров: возраст (хронологический и, если определим, физиологический); массу; размеры (например, высоту в холке, длину ног, длину спины и т.д.); ветеринарный анамнез; репродуктивный анамнез, включая стерилизацию, количество и размер потомства; состояние здоровья в настоящее время или состояние заболевания и любые его недавние изменения, включая любое диагностированное состояние или нарушение, и любые симптомы, поставлен ли диагноз или нет; наличие паразитов, включая блох; аппетит и любые его недавние изменения; уровень физической активности; умственную деятельность; поведенческие аномалии и характер (например, пугливый, агрессивный, послушный, возбужденный). Такие данные могут облегчать определение изменений экспрессии гена NIS кошек, подверженных воздействию показателей, иных, чем наличие и степень гипертиреоза, а также определение фенотипических признаков, которые могут коррелировать с наличием или тяжестью гипертиреоза.
"Хронологический возраст" животного представляет собой точное время, прошедшее с момента рождения (например, в годах или месяцах). "Физиологический возраст" животного является вычисленным средним хронологическим возрастом животных аналогичной породы, демонстрирующих то же возраст-зависимое физиологическое состояние (подвижность, умственная деятельность, износ зубов и т.д.), что и животное.
Зоографические данные дополнительно могут относиться к аспектам окружающей среды, в которой тестируемые животные живут. Такие аспекты включают, в качестве неограничивающих примеров, климат, время года, географическое местоположение и жилище. Например, для разработки пищевой композиции для животного может быть важным знать, живет ли животное во влажном или сухом климате, или сухом или влажном климате; в настоящее время весна, лето, осень или зима; содержат ли животное в помещении или вне помещения; находится ли животное в доме, питомнике, на рабочем месте (например, в случае сторожевых собак, полицейских собак и т.д.) или в некотором другом месте обитания; содержат ли его в отдельности или с другими животными; живет ли оно в городе или сельской местности; почтовый код, страну и/или город проживания; воздействуют ли на его место проживания загрязнения окружающей среды (например, табачный дым) и до какой степени; и т.д.
Второй набор данных: Второй набор данных (тестовый набор данных) содержит данные об эффектах биоактивных компонентов рациона (BDC) в отдельности и в комбинациях на функциональную экспрессию гена, т.е. на функциональную экспрессию генов, представленных в настоящем описании. Эти данные могут включать публично или коммерчески доступную информацию из любого источника и/или результатов исследований, осуществленных специально для получения второго набора данных.
Исторически, совокупные эффекты конкретных биоактивных компонентов рациона на здоровье определяют с помощью исследований с введением препарата с пищей с использованием животных интересующего вида, например, собак или кошек. По настоящему изобретению эффекты биоактивных компонентов рациона на субклеточном уровне, т.е. на функциональную экспрессию генов, представленных в настоящем описании, в клетках, можно определять с помощью контролируемых экспериментов, где модель на животных подвергают воздействию различных уровней и/или различной длительности воздействия одного или нескольких биоактивных компонентов рациона. В данном контексте "различные уровни" биоактивного компонента рациона включают нулевой уровень биоактивного компонента рациона. Если в тест включают множество уровней биоактивного компонента рациона, можно выявлять эффект дозы.
В определенных вариантах осуществления модель на животных может являться живым животным интересующего вида. Однако исчерпывающий набор данных легче и экономически выгоднее можно получать, используя одну или несколько альтернативных тестовых моделей, пример чего приведен ниже.
В одном из вариантов осуществления альтернативная тестовая модель является моделью на позвоночном животном, например, небольшого вида, хорошо адаптированного для функциональных геномных исследований, таких как мыши, крысы, морские свинки, кролики или курицы. В другом варианте осуществления альтернативная тестовая модель является моделью на непозвоночном животном, например, вида непозвоночных, такого как круглый червь Caenorhabditis elegans или плодовая мушка Drosophila melanogaster, геном которых по существу определен. В дополнительном варианте осуществления альтернативной тестовой моделью, которую можно получать, является неживотная модель, в частности, генетически сконструированная модель на основе, например, дрожжей, таких как Candida albicans или Saccharomyces cerevisiae, или бактерий, таких как Escherichia coli. Другой альтернативной тестовой моделью является модель культуры клеток, например, с использованием линий первичных и/или иммортализованных клеток интересующего вида кошачьих или другого вида, включая человека. В другом варианте осуществления альтернативная тестовая модель является моделью ex vivo с использованием эксплантатов ткани, полученных из животного и поддерживаемых вне организма животного.
Не будучи связанными в теории, на клеточном уровне биоактивный компонент рациона может действовать как лиганд для белка, такого как фактор транскрипции или рецептор, может метаболизироваться посредством первичных или вторичных метаболических путей, таким образом, изменяя концентрации субстратов и/или промежуточных продуктов, участвующих в регуляции гена или сигнальной системе клетки, или может изменять пути передачи сигнала, положительно или отрицательно воздействуя на сигнальный путь.
Второй набор данных может включать данные не только о химических или биологических веществах, известных как биоактивные компоненты рациона, но и о множестве материалов, о пищевом, нутрицевтическом или фармакологическом эффекте которых ранее не было известно. В настоящем описании все такие материалы считают биоактивными компонентами рациона, если для гена NIS кошек обнаружен применимый эффект в отношении экспрессии по меньшей мере одного гена, функции по меньшей мере одного белка или продукции по меньшей мере одного метаболита. В одном из вариантов осуществления интересующие биоактивные компоненты рациона в настоящем описании являются материалами, имеющими GRAS (как правило, считаются безопасными) или эквивалентный статус по инструкциям FDA (Управления по санитарному надзору за качеством пищевых продуктов и медикаментов) США или соответствующим инструкциям в других странах, или имеющими право на такой статус. В других вариантах осуществления биоактивный компонент рациона может являться терапевтически или фармакологически эффективным соединением, например, лекарственным средством или средством из растительного сырья.
Многие биоактивные компоненты рациона являются химическими веществами, как правило, природными в пище, из которой их можно экстрагировать. Во многих случаях биоактивные компоненты рациона также можно получать микробиологическими (например, ферментацией) или синтетическими способами. Их примерами являются химические вещества, включающие, в качестве неограничивающих примеров: аминокислоты; простые сахара; сложные сахара; среднецепочечные триглицериды (MCT); триацилглицериды (TAG); n-3 (омега-3)-жирные кислоты, включая α-линоленовую кислоту (ALA), эйкозапентаеновую кислоту (EPA) и докозагексаеновую кислоту (DHA); n-6 (omega-6)-жирные кислоты, включая линолевую кислоту (LA), γ-линоленовую кислоту (GLA) и арахидоновую кислоту (ARA); источники холина, такие как лецитин; жирорастворимые витамины, включая витамин A и его предшественников, таких как каротиноиды {например, β-каротин), источники витамина D, такие как витамин D2 (эргокальциферол) и витамин D3 (холекальциферол), источники витамина E, такие как токоферолы (например, α-токоферол) и токотриенолы, и источники витамина K, такие как витамин K1 (филлохинон) и витамин K2 (менадион); водорастворимые витамины, включая витамины группы B, такие как рибофлавин, ниацин (включая никотинамид и никотиновую кислоту), пиридоксин, пантотеновую кислоту, фолиевую кислоту, биотин и кобаламин; и витамин C (аскорбиновую кислоту); антиоксиданты, включая некоторые из указанных выше витаминов, в частности, витамины E и C; а также биофлавоноиды, такие как катехин, кверцетин и теафлавин; хиноны, такие как убихинон; каротиноиды, такие как ликопин и ликоксантин; ресвератрол; и α-липоевую кислоту; L-карнитин; D-лимонен; глюкозамин; S-аденозилметионин; и хитозан.
Что касается включения аминокислот в представленный выше иллюстративный список биоактивных компонентов рациона, почти все продукты питания содержат белок, как правило, восполняющий все незаменимые аминокислоты. Однако содержание белка в пище не обязательно восполняет незаменимые аминокислоты в пропорциях, оптимальных для здоровья конкретных субпопуляций животных, таким образом, желательным может являться восполнение одной или нескольких аминокислот или восполнение с использованием источников белка, богатых такими аминокислотами.
Аналогичные соображения применимы в случае простых и сложных сахаров, которые являются биоактивными компонентами рациона и могут являться или не являться компонентами углеводной фракции пищи, и конкретных жирных кислот, включая n-3- и n-6-жирные кислоты, которые являются биоактивными компонентами рациона и могут являться или не являться компонентами липидной фракции пищи.
В ином случае макронутриенты, необходимые для сбалансированного рациона животного (белки, углеводы, жиры и волокна), рассматривают отдельно от биоактивных компонентов рациона, таких как указанные выше в получении пищевого состава, как будет описано ниже.
Конкретные биологические материалы, в частности, растительные материалы, можно считать биоактивными компонентами рациона и, при желании, их можно включать во второй набор данных. Среди многих из них идентифицированы биоактивные химические вещества; даже если биоактивный компонент известен, могут присутствовать другие, неизвестные, биоактивные компоненты и вносить свой вклад в биоактивный эффект биологического материала.
Иллюстративные растительные материалы, которые могут являться применимыми в качестве биоактивных компонентов рациона, включают, в качестве неограничивающих примеров, алоэ вера, дягиль лекарственный, эхинацею, энотеру, льняное семя, чеснок, имбирь, гинкго билоба, женьшень, зеленый чай, сою, куркуму, ростки пшеницы и падуб парагвайский.
Таким образом, второй набор данных содержит данные, относящиеся к эффектам функционального профиля генов в модели на животных в отношении биоактивных компонентов рациона, тестируемых в модели. Используя подходящий алгоритм, из этого набора данных можно выбирать биоактивный компонент рациона или комбинацию биоактивных компонентов рациона, имеющих желаемый эффект на функциональный профиль гена, например, экспрессию или активность гена NIS кошек, или и то, и другое.
Исходные данные: Исходные данные, обрабатываемые способами по изобретению, содержат данные, определяющие генотип и физиологическое состояние субпопуляции, для которой составляют рацион, предписанный пищевой состав или получаемую пищевую композицию. Исходные данные могут содержать зоографические данные, включая любой из указанных выше типов зоографических данных, как часть записи о происхождении образцов в первом наборе данных. В определенных вариантах осуществления исходные данные для исследуемого животного включают данные о функциональном профиле гена, полученные из одного или нескольких образцов ткани и/или биологической жидкости, взятых у субъекта. По этим вариантам осуществления в исходных данных можно указывать функциональный профиль гена в нормальном или ненормальном диапазоне.
Компьютеризированная система по изобретению, как правило, содержит интерфейс пользователя, позволяющий вносить исходные данные.
Ввод зоографических исходных данных в систему можно осуществлять с помощью интерфейса оператора на основе печатного или электронного опросника, заполняемого хозяином исследуемого животного. Альтернативно, ввод таких данных может осуществляться в интерфейсе непосредственно хозяином.
Интерфейс пользователя для ввода зоографических данных может являться удаленным относительно главного процессора (где исходные данные обрабатываются способом по изобретению), но связанным с ним через сеть, такую как Интернет. Альтернативно, интерфейс пользователя может являться локальным (например, с проводным соединением) для главного процессора, например, установленным в магазине розничной торговли или ветеринарной клинике. В различных вариантах осуществления интерфейс пользователя, в качестве иллюстративного и неограничивающего примера, может включать клавиатуру и монитор; персональный компьютер, например, в доме хозяина животного; терминал с сенсорным экраном; кнопочный телефон; или систему с голосовой активацией. Альтернативно, зоографические данные можно предварительно вносить на машиночитаемый носитель, такой как напечатанный штрих-код или машиночитаемые буквенно-цифровые обозначения; дискету; CD-ROM; карту памяти; чип и т.д., и сканировать или загружать в терминале, оборудованном для считывания с такого носителя. В некоторых вариантах осуществления носитель можно прикреплять к исследуемому животному, например, на ошейник, ушную бирку или прикрепленный к ошейнику медальон, или, в случае конкретных типов чипа, хирургически имплантировать под кожу животного. В качестве еще одного варианта, зоографические данные можно предварительно вносить в саму компьютеризированную систему и хранить в базе данных, откуда их можно получать при введении кода, уникального для исследуемого животного, для которого исходно вводили зоографические данные. Такой код можно вводить с помощью любого типа интерфейса и на любом подходящем носителе, включая указанные выше.
Обработка исходных данных для получения пищевого состава: Обработку исходных данных для субпопуляции (которая, как указано выше, может являться одним исследуемым животным, например, кошкой, страдающей гипертиреозом) осуществляют с помощью алгоритма, иногда в настоящем описании обозначаемого как "первый" алгоритм, в котором используют первый и/или второй наборы данных, описываемые выше, для получения из исходных данных пищевого состава, улучшающего здоровье одного или нескольких животных в субпопуляции.
Алгоритм, по меньшей мере, в случае вариантов осуществления изобретения, где в алгоритме используют первый и второй набор данных, как описано выше, можно иллюстративно воплощать в компьютерной программе, включающей, по меньшей мере, следующие задачи. Обработку необязательно проводят в последовательности, представленной ниже. В компьютеризированной системе по изобретению необязательно могут использовать параллельную обработку, где две или более задач выполняют одновременно.
В одной задаче исходные данные от субъекта заносят в память. В другой - в первом наборе данных осуществляют поиск зоографических данных и/или данных о функциональном профиле гена, как можно больше соответствующих исходным данным. Для получения от одного до множества "совпадений", которые в совокупности обеспечивают наилучшее совпадение с генотипом и физиологическим состоянием субъекта, можно использовать известные в этой области способы поиска и статистического анализа. Если функциональный профиль гена представлен как часть исходных данных о субъекте, алгоритм снова идентифицирует любое отклонение от нормального состояния. В еще одной задаче во втором наборе данных осуществляют поиск для тестирования данных, относящихся к функциональному профилю гена, установленных для субъекта ранее. Тестовые данные, указывающие на биоактивный компонент рациона или комбинацию биоактивных компонентов рациона, являющихся эффективными для поддержания такого функционального профиля гена в нормальном состоянии или сдвига такого функционального профиля гена от ненормального состояния к большей нормальности, получают, например, с использованием известных в этой области способов поиска и статистического анализа для получения наилучшего совпадения с функциональным профилем гена субъекта. В другой задаче вычисляют пищевой состав, включающий эффективные количества одного или нескольких биоактивных компонентов рациона, определенных, как описано выше. Пищевой состав можно вычислять в виде полного рациона, включающего требования по основному обмену, содержанию белка и волокон (которые легко можно определять из исходных зоографических данных) вместе с идентифицированными биоактивными компонентами рациона. Альтернативно, пищевой состав можно вычислять в виде пищевой добавки, исключающей требования по основному обмену, содержанию белка и волокон.
Необязательно, пищевой состав можно выводить через интерфейс пользователя, такой как монитор компьютера, принтер, речевой синтезатор и т.д. Код, представляющий пищевой состав, можно загружать на читаемый пользователем или машиночитаемый носитель, например, напечатанный штрих-код, напечатанный числовой код, полосу данных на карте, устройство памяти, диск, чип и т.д. В одном из вариантов осуществления такой код загружают на чип, адаптированный для имплантации животному, в частности, животному-компаньону.
В вариантах осуществления, где пищевой состав обрабатывают дополнительно, например, для получения пищевой композиции, может не требоваться вывод самого пищевого состава.
В определенных вариантах осуществления пищевую композицию составляют, непосредственно объединяя первый алгоритм со вторым алгоритмом (для состава), как описано ниже. По таким вариантам осуществления можно осуществлять или не осуществлять вычисление пищевого состава как промежуточный этап.
Если пищевой состав является выходными данными, биоактивные компоненты рациона и другие компоненты можно выражать в любой подходящей форме. Например, компоненты можно выражать в терминах их содержания в пищевой композиции (например, в % или в мг/г, как правило, в пересчете на сухую массу), в терминах суточной дозы или рациона (например, в г/день), необязательно, в пересчете на живой вес (например, в мг/кг/день).
В иллюстративном способе по изобретению для получения пищевого состава ключевым этапом является обработка исходных данных для получения пищевого состава, например, как непосредственно описано ниже. На этапе обработки вводят три подсистемы.
В первой подсистеме определяют животных с различными состояниями здоровья и заболевания, т.е. здоровых кошек и страдающих легким или тяжелым гипертиреозом. Как предполагалось выше, часто желательно, чтобы этот набор животных являлся как можно большим и включал как можно более широкий диапазон состояния заболевания и физиологического нарушения, а также широкий диапазон генотипов. Собирают набор зоографических данных для каждого животного. Каждое животное является источником от одного до множества образцов тканей и/или биологических жидкостей. Каждый образец подвергают функциональному анализу генов (включая один или несколько из анализа экспрессия гена, протеомного и метаболомного анализа), например, с помощью общепринятого способа с использованием микрочипов, для определения функционального профиля гена для животного, от которого получен образец, отражающего генотип и физиологическое состояние животного на момент забора образца, относящегося к генам кошек, представленным в настоящем описании, а именно, гену NIS кошек. Данные, определяющие функциональный профиль гена, становятся частью первого набор данных, как определено в настоящем описании, вместе с зоографическими данными, относящимися к животному.
Во второй подсистеме биоактивные компоненты рациона тестируют в одной или нескольких моделях на животных, как описано выше. Чем больше биоактивных компонентов рациона тестируют, тем лучше; и чем больше доз каждого биоактивного компонента рациона тестируют, тем лучше. Тестирование может включать комбинации биоактивных компонентов рациона, а также отдельные биоактивные компоненты рациона. Во всех этих тестах можно определять эффекты биоактивных компонентов рациона на функциональную экспрессию гена в модели на животных. Результаты тестов используют для получения второго набора данных, как определено в настоящем описании.
Как правило, первый и второй наборы данных систематизируют в одной или нескольких соответствующих базах данных, адаптированных для поиска и получения информации с помощью первого алгоритма, т.к. с помощью него обрабатывают исходные данные.
В третью подсистему вводят исходные данные для исследуемого животного или субпопуляции. Как указано выше, исходные данные, как правило, включают зоографические данные и могут включать или не включать данные о функциональном профиле гена. Для обработки исходных данных для получения пищевого состава необходим доступ алгоритма обработки к первому и второму наборам данных. Полученный пищевой состав является составом, для которого данные, хранящиеся в системе, свидетельствуют или позволяют предполагать то, что он будет улучшать здоровье исследуемого животного или одного или нескольких животных в субпопуляции, например, будет применимым для лечения кошек, страдающих гипертиреозом. Некоторые аспекты "улучшения здоровья" более подробно представлены в настоящем описании ниже. Необязательно, исходные данные, содержащие и зоографические данные, и данные о функциональном профиле гена, добавляют в первый набор данных, и они могут быть доступны в будущих итерациях способа.
В одном из вариантов осуществления такие исходные данные связаны с идентификатором или кодом для конкретного животного, к которому они относятся. Если то же животное является субъектом последующей итерации способа, можно программировать алгоритм обработки данных для получения предыдущих данных о функциональном профиле гена для этого животного. Таким образом, можно отслеживать тенденции и изменения функционального профиля генов животного. Среди других преимуществ, такое отслеживание может делать возможным периодический мониторинг эффективности пищевого состава в поддержании нормального функционального профиля гена, в смещении ненормального функционального профиля гена в сторону большей нормальности и/или в любом аспекте улучшения здоровья, как более подробно представлено в настоящем описании ниже.
Итеративное использование способа для конкретного животного может создать основу плана питания, контролируемого на протяжении всей жизни животного или существенной ее части. Можно осуществлять корректирующее воздействия, корректируя пищевой состав во всех случаях ухудшения состояния здоровья животного или смещения его функционального профиля генов в сторону ненормального состояния, свидетельствующего, например, о прогрессировании гипертиреоидного состояния.
Получение пищевой композиции: Конечным продуктом одного из вариантов осуществления изобретения является пищевой состав, полученный, как указано выше. Например, ветеринарный врач или диетолог может прописывать пищевой состав для исследуемого животного с помощью способа, представленного в настоящем описании. Можно получать пищевой состав для обеспечения комплексного решения относительно состояния заболевания или физиологического нарушения, или можно адаптировать его для использования в комбинации с фармацевтическим средством (например, введением лекарственного средства или другим лечением), как описано ниже, или хирургическим вмешательством.
В другом варианте осуществления пищевой состав используют в качестве основы для получения пищевой композиции, становящейся конечным продуктом этого варианта осуществления. Второй алгоритм или алгоритм составления можно использовать для получения пищевой композиции из пищевого состава. Как указано выше, такой алгоритм можно объединять с первым алгоритмом для получения пищевой композиции, непосредственно обрабатывая исходные данные. Раскрытие в настоящем описании пищевого состава как промежуточной стадии получения пищевой композиции не ограничивает настоящее изобретение способами и системами, где такая стадия является определимой.
Алгоритмы для составления пищевых композиций на основе a пищевого состава хорошо известны в этой области. Такие алгоритмы осуществляют доступ к набору данных, анализируя различные пищевые ингредиенты и используя этот набор данных для вычисления количеств таких ингредиентов в пищевой композиции, имеющей желаемый пищевой состав.
Необязательно, набор данных, которые обрабатывают с помощью второго алгоритма, дополнительно включает данные о стоимости различных пищевых ингредиентов, и второй алгоритм содержит операцию для включения стоимости как критерия выбора ингредиентов. Это может позволить получать пищевую композицию со сниженной стоимостью, например, с наименьшей стоимостью, соответствующей получению желаемого пищевого состава.
При желании можно включать другие критерии. Например, ингредиенты можно определять как "органические" или другие, таким образом, что, если желательным является "органический" пищевой продукт, выбирают только "органические" ингредиенты.
В одном из вариантов осуществления можно выбирать пищевую композицию из диапазона уже существующих опций, например, существующей линии пищевых продуктов для домашних животных, для наилучшего совпадения пищевого состава, получаемого при практическом осуществлении изобретения. Например, можно использовать алгоритм, сравнивающий вычисленную пищевую композицию или пищевой состав с доступными продуктами и выбирающий продукт, наиболее совпадающий с композицией или составом.
В другом варианте осуществления производят корм для домашних животных, соответствующий композиции, приведенной выше. Таким образом, такой корм для домашних животных адаптирован для отдельного животного, для которого получены исходные данные, или для субпопуляции животных, представленной животным, для которого получены исходные данные. Такое производство может являться автономным, т.е. не контролируемым компьютеризированной системой. Альтернативно, такое производство может частично или полностью находиться под контролем и/или управляться компонентом компьютеризированной системы, генерирующей пищевой состав и вычисляющей композицию корма, как описано выше.
Произведенный таким образом продукт может являться полным рационом или добавкой, адаптированной для добавления или смешивания с основным рационом для получения полного рациона. Продукт может быть жидким, полутвердым или твердым; в случае твердого продукта он может быть влажным (например, стерилизуемым влажным кормом для домашних животных), полувлажным или сухим (например, гранулой). Можно получать добавку для использования, например, в качестве подливки, дополняющей основной корм, или в качестве соуса для основного корма в гранулах.
В этой области известны подходящие управляемые компьютером устройства для производства пищевого продукта, имеющего определенную композицию.
Необязательно, пищевой продукт, получаемый способом по изобретению, упаковывают в подходящий контейнер. Например, влажный пищевой продукт можно упаковывать в консервную банку, банку или запаиваемый пакет; сухой пищевой продукт можно упаковывать в мешок, коробку или мешок в коробке. При желании, этот этап также может находиться под контролем компьютеризированной системы.
Компьютеризированную систему по изобретению дополнительно можно приспосабливать для распечатывания ярлыка или вкладыша в упаковку пищевого продукта, содержащего любую или всю информацию, удовлетворяющую требованиям государственного регулирования и общепринятой в коммерческой практике. Например, ярлык или вкладыш в упаковку может включать списки ингредиентов и/или гарантированный состав.
Производство пищевого продукта, включая упаковку и нанесение ярлыка, можно осуществлять в общепринятом месте производства, таком как фабрика. Альтернативно, более удобной может являться организация производства пищевого продукта ближе к конечному пользователю, например, в месте продажи в помещениях дистрибьютора или распространителя, таких как зоомагазин. В одном из вариантов осуществления пищевую композицию получают в месте распространения и доставляют конечному потребителю, например, в ответ на заказ, размещенный конечным потребителем, например, с помощью телефона или через веб-сайт, доступный в интернете.
В одном из вариантов осуществления пищевую композицию получает заводчик, составляющий корма, при получении рецепта от ветеринарного врача или диетолога, указавшего пищевой состав, полученный с помощью первого алгоритма.
В другом варианте осуществления конечный потребитель в терминале в пункте продажи вводит код, представляющий пищевой состав, выбранный ранее для конкретного животного, например, с помощью проведения картой или сканирования чипа, содержащего такой код. Затем компьютеризированное устройство для смешивания, например, устройство для смешивания и продажи, находящееся в месте продажи, готовит пищевую композицию на основе пищевого состава, закодированного таким образом, и выдает ее конечному потребителю.
Пищевая композиция, получаемая способом по любому варианту осуществления настоящего изобретения, сама по себе является дополнительным вариантом осуществления изобретения.
В одном из вариантов осуществления способ по изобретению повторяют с интервалами для одного или нескольких отдельных животных в субпопуляции, корректируя пищевой состав по мере необходимости для изменений физиологического состояния или функционального профиля гена с течением времени. Такие изменения можно осуществлять, по меньшей мере частично, с помощью пищевых составов пищевых композиций, получаемых с помощью предыдущих итераций способа. С помощью итеративного способа можно получать план питания, например, для перехода от исправления проблем со здоровьем к профилактике рецидива проблемы.
Банк данных: Термин "банк данных" в настоящем описании относится к физическому варианту осуществления коллекции данных, содержащей от одного до множества наборов данных, которые можно сконфигурировать в от одной до множества баз данных. Таким образом, банк данных содержит носитель, где или на котором такие данные хранят. Банк данных может содержать несколько таких носителей; однако, в таком случае, носители являются функционально связанными. Носители, применимые в настоящем изобретении, могут являться читаемыми пользователем, как в случае напечатанной электронной таблицы, но, как правило, и особенно, в связи с большим объемом данных, предусматриваемых в настоящее время, такие носители являются машиночитаемыми.
Банк данных по изобретению может содержать от одного до множества носителей, находящихся в компьютере или связанных с ними электронно, на которых хранят данные, относящиеся к функциональному геномному профилю вида животного или модели для по меньшей мере одного из (a) генотипа и/или физиологического состояния животного, от которого получали один или несколько образцов тканей и/или биологических жидкостей, из которых определяли указанный функциональный геномный профиль; и (b) воздействия вида животного или модели на один или несколько биоактивных компонентов рациона. Данные конфигурируют в виде от одной до множества баз данных. При представлении запроса, относящегося к функциональному геномному профилю и/или биоактивным компонентам рациона, с помощью компьютера, информацию в ответ на соответствующий запрос получают из одной или нескольких баз данных.
По одному из вариантов осуществления с помощью такого запроса запрашивают выходные данные о функциональном геномном профиле, относящиеся к исходным данным о генотипе и/или физиологическом состоянии исследуемого животного. По другому варианту осуществления с помощью такого запроса запрашивают выходные данные о биоактивном компоненте рациона, относящиеся к исходным данным о функциональном геномном профиле исследуемого животного. Информацию, выдаваемую в ответ на такой запрос, можно выражать в виде пищевого состава для исследуемого животного.
В типичном банке данных по изобретению данные содержат первый набор данных, относящийся к функциональному геномному профилю, о генотипе и/или физиологическом состоянии животного, от которого получали один или несколько образцов тканей и/или биологических жидкостей, из которых определяют указанный функциональный геномный профиль; и второй набор данных, относящийся к функциональному геномному профилю, о подвергании модели на животных воздействию одного или нескольких биоактивных компонентов рациона. По этому варианту осуществления информацию получают в ответ на соответствующий запрос, с помощью которого запрашивают выходные данные о пищевом составе для исследуемого животного, соответствующие исходным данным о генотипе и/или физиологическом состоянии субъекта.
Данные в таком банке данных, необязательно, дополнительно содержат третий набор данных, включающий содержание биоактивных компонентов рациона в ингредиентах для пищевой композиции. По этому варианту осуществления информацию получают в ответ на соответствующий запрос, с помощью которого запрашивают выходные данные о пищевой композиции для исследуемого животного, соответствующие исходным данным о генотипе и/или физиологическом состоянии субъекта.
По родственному варианту осуществления третий набор данных дополнительно содержит стоимость ингредиентов, и информацию получают в ответ на соответствующий запрос, помощью которого запрашивают выходные данные об оптимизированной по стоимости пищевой композиции для исследуемого животного, соответствующие исходным данным о генотипе и/или физиологическом состоянии субъекта.
В банке данных по дополнительному варианту осуществления изобретения информацию получают в ответ на соответствующий запрос, с помощью которого запрашивают выходные данные, относящиеся к исходным данным о функциональном геномном профиле исследуемого животного относительно нормального функционального геномного профиля.
В банке данных по еще одному варианту осуществления информацию получают в ответ на соответствующий запрос, с помощью которого запрашивают выходные данные о пищевом составе для исследуемого животного, эффективном (a) для поддержания нормального функционального геномного профиля или (b) для модификации ненормального функционального геномного профиля в сторону более нормального состояния.
Дополнительные варианты осуществления изобретения представлены ниже. Одним таким вариантом осуществления является способ выбора пищевой композиции для исследуемого животного, предпочтительно исследуемого животного-компаньона. Способ включает (a) осуществление доступа к базе данных, заполненной данными о нормальных и ненормальных функциональных геномных профилях; (b) оценку функционального профиля генов субъекта относительно нормального профиля с учетом указанных данных; (c) определение одного или нескольких биоактивных компонентов рациона, демонстрирующих тенденцию к смещению функционального профиля гена в более нормальное состояние, с помощью базы данных, заполненной результатами тестирования функционального профиля генов в модели на животных, подвергнутых воздействию по меньшей мере одного биоактивного компонента рациона; и (d) выбор пищевой композиции, содержащей указанные один или несколько биоактивных компонентов рациона.
В одном из аспектов изобретения пищевую композицию выбирают с учетом базы данных, заполненной данными о стоимости пищевых ингредиентов и биоактивных компонентов рациона. В другом - пищевая композиция является эффективной в смещении функционального профиля генов в более нормальное состояние, и ее составляют с плановой стоимостью или ниже ее. В другом - базы данных хранят на одном или нескольких носителях. В другом - для оценки функциональных геномных данных используют компьютер, способный осуществлять доступ к одному или нескольким носителям. В дополнительном аспекте способ дополнительно включает кормление композицией исследуемого животного для профилактики развития состояния заболевания у субъекта, для улучшения здоровья субъекта, для смещения функционального профиля генов субъекта из ненормального в нормальное состояние или для осуществления изменения функционального профиля генов субъекта. В другом - нормальные и ненормальные функциональные геномные данные получают с помощью анализа тканей и/или биологических жидкостей популяции животных в состояниях здоровья и заболевания. Такую популяцию можно определять, по меньшей мере частично, по фенотипическим параметрам, включая тяжесть гипертиреоза.
Другим вариантам осуществления является способ составления пищевой композиции для исследуемого животного. Способ включает (a) осуществление доступа к первому набору данных, содержащему данные, относящиеся к функциональному профилю генов субъекта для гена NIS кошек, определяемого в одном или нескольких образцах тканей и/или биологических жидкостей, относительно нормального функционального профиля генов; (b) осуществление доступа ко второму набору данных, содержащему информацию об эффектах отдельных биоактивных компонентов рациона и/или их комбинаций на функциональный профиль генов в одной или нескольких тестовых модельных системах; и (c) вычисление состава, содержащего биоактивный компонент рациона или их комбинацию, эффективные при использовании в качестве пищевой композиции для реверсирования или ослабления смещения функционального профиля генов субъекта из нормального функционального профиля генов.
В одном из вариантов осуществления состав является эффективным для перехода функционального профиля генов субъекта в нормальный функциональный профиль генов. В другом - способ дополнительно включает осуществление доступа к набору данных, содержащему информацию, относящуюся к фенотипу субъекта. Такую информацию, например, можно выбирать из группы, состоящей из возраста, типа шерстного покрова, размера и массы. В дополнительном аспекте способ дополнительно включает осуществление доступа к набору данных, содержащему информацию об источнике и стоимости активной формы, прекурсора или метаболита каждого биоактивного компонента рациона в составе. В другом - состав, вычисляемый таким способом, является экономически эффективным. В другом - нормальный функциональный профиль генов определяют с помощью анализа тканей и/или биологических жидкостей от популяции животных. Такую популяцию снова можно определять, по меньшей мере частично, по генотипическим параметрам, по меньшей мере частично, по фенотипическим параметрам. В дополнительном аспекте по меньшей мере один из наборов данных хранят на одном или нескольких носителях. В другом - для вычисления состава используют компьютер, способный осуществлять доступ к одному или нескольким носителям.
Получение пищевых композиций для кошек с гипертиреозом
В одном из вариантов осуществления в настоящем описании представлен способ получения пищевой композиции для животных. Один из аспектов этого варианта осуществления включает выбор целевого заболевания или состояния животного-компаньона и идентификацию белков и полипептидов, вносящих вклад или лежащих в основе этого заболевания или состояния, включая, в качестве неограничивающих примеров, ген NIS кошек. После этого осуществляют определение того, повышение ли или снижение экспрессии или активности одного или нескольких из этих белков и полипептидов будет ожидаемо улучшать, модулировать или устранять целевое заболевание или состояние. Осуществляя скрининг компонентов (макронутриентов) пищевых композиций для домашних животных, как представлено в настоящем описании, можно определять биоактивные компоненты рациона, которыми можно кормить животное-компаньона для лечения целевого заболевания или состояния, например, эффективно снижая экспрессию или активность гена NIS кошек.
Таким образом, в одном из вариантов осуществления настоящее изобретение относится к способу получения пищевой композиции, подходящей для лечения заболевания или состояния животного, включающему: (a) определение целевого заболевания или состояния, (b) определение полипептида, вносящего вклад в этиологию, лежащую в основе этого заболевания, например, гена NIS кошек, (c) определение того, повышение ли или снижение активности или экспрессии указанного идентифицированного полипептида будет улучшать целевое заболевание или состояние, (d) осуществление по меньшей мере одного мультивариантного анализа для определения биоактивных компонентов рациона, способных модулировать активность или экспрессию указанного идентифицированного полипептида способом, необходимым для улучшения целевого заболевания или состояния, и (e) составление пищевой композиции, содержащей биоактивный компонент рациона. В данном контексте, например, гипертиреоз может являться ассоциированным с существенными повышениями уровня экспрессии гена NIS кошек.
Настоящее изобретение относится к способам и реагентам для определения ингредиентов рациона, снижающих захват йода щитовидной железой и ингибирующих синтез тиреоидного гормона. Способы, представленные в настоящем описании, включают использование выделенного фрагмента гена, кодирующего часть натрий-йодного симпортерного белка кошек (белка NIS), для получения данных профиля экспрессии гена в присутствии и отсутствие тестовых материалов. Используя эти способы, можно определять материалы, которые можно включать в рацион кошки, страдающей гипертиреозом, для лечения этого состояния.
Настоящее изобретение также относится к способу дизайна пищевой композиции для домашних животных, подходящей для введения животному-компаньону из семейства кошачьих, страдающему гипертиреозом, включающему: (a) осуществление доступа по меньшей мере к одной первой базе данных, содержащей первый набор данных, относящийся к функциональному профилю генов в образце биологической жидкости или ткани от животного, о физиологическом состоянии и, необязательно, генотипе животного, где функциональный профиль гена является профилем гена NIS кошек, (b) осуществление доступа по меньшей мере к одной второй базе данных, содержащей второй набор данных, относящийся к эффектам биоактивных компонентов рациона на функциональный профиль гена по этапу (a); (c) использование первого алгоритма, использующего первый и второй наборы данных, обрабатывающего исходные данные, в которых определено физиологическое состояние и, необязательно, генотип субпопуляции, например, кошек, страдающих гипертиреозом, для получения пищевого состава, применимого для выбора и получения пищевой композиции для этой субпопуляции животных; и (d) получение пищевой композиции на основе пищевого состава, где эта пищевая композиция подходит для введения животному-компаньону из семейства кошачьих, страдающему гипертиреозом.
Настоящее изобретение также относится к композициям и способам диагностики гипертиреоза у кошек, а также способам определения материалов и составления пищевых композиций, содержащих эти материалы, которые будут применимыми для лечения гипертиреоза у кошек.
В определенных аспектах этого варианта изобретения первый набор данных получают из образцов, собранных из множества отдельных животных, представляющих диапазон генотипов и физиологических состояний, включающих животных-компаньонов из семейства кошачьих, страдающих гипертиреозом. В одном из аспектов каждый образец от отдельного животного связан с записью о происхождении, содержащей зоографические данные, относящиеся к определению генотипа и физиологического состояния на момент забора образца от отдельного животного. В другом аспекте этого варианта осуществления зоографические данные содержат один или несколько элементов данных, относящихся к генотипу, выбранным из группы, состоящей из породы, пород родителей, родословной, пола, типа шерстного покрова и очевидных наследственных состояний и нарушений, в частности, гипертиреоза. В другом аспекте этого варианта осуществления зоографические данные содержат один или несколько элементов данных, относящихся к физиологическому состоянию, выбранных из группы, состоящей из возраста, массы, ветеринарного анамнеза, репродуктивного анамнеза, состояния здоровья в настоящее время или состояния заболевания, аппетита, уровня физической активности, умственной деятельности, поведенческих аномалий и характера и, в частности, наличия и степени гипертиреоза.
В конкретном аспекте этого способа первый набор данных содержит данные, относящиеся к анализу образца в отношении одного или нескольких компонентов, выбранных из группы, состоящей из ДНК, РНК, белков, метаболитов и биомаркеров, в то время как второй набор данных получают при контролируемых экспериментах, включающих подвергание модели на животных воздействию различных уровней одного или нескольких биоактивных компонентов рациона.
В другом конкретном аспекте этого способа исходные данные содержат зоографические данные, относящиеся к определению генотипа и физиологического состояния животных-компаньонов из семейства кошачьих, страдающих гипертиреозом. В другом аспекте этого способа исходные данные содержат аналитические данные, полученные из образца биологической жидкости или ткани, полученного из животных-компаньонов из семейства кошачьих, не страдающих гипертиреозом. В других конкретных аспектах этого способа исходные данные содержат аналитические данные, полученные из образца биологической жидкости или ткани, полученного из животных-компаньонов из семейства кошачьих, страдающих легким гипертиреозом, а также животных-компаньонов из семейства кошачьих, страдающих тяжелым гипертиреозом.
Настоящее изобретение также относится к пищевым композициям, полученным указанным выше способом, для получения пищевой композиции для домашних животных, иллюстративные примеры которой представлены в настоящем описании ниже, являющейся применимой для введения животным-компаньонам из семейства кошачьих, страдающих гипертиреозом.
Таким образом, настоящее изобретение относится к способам получения пищевой композиции для животного, страдающего заболеванием или состоянием, включающим определение биоактивных компонентов рациона, применимых в снижении эффектов заболевания или состояния, которым страдает животное. В конкретном иллюстративном аспекте этого варианта осуществления заболеванием или состоянием является гипертиреоз, и страдающим животным является животное-компаньон из семейства кошачьих.
В одном из вариантов осуществления настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона. В одном из аспектов настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона из семейства кошачьих.
В другом варианте осуществления настоящее изобретение относится к композициям, применимым в способе лечения гипертиреоза у животного-компаньона. В одном из аспектов настоящее изобретение относится к композициям, применимым в способе лечения гипертиреоза у животного-компаньона из семейства кошачьих.
В конкретных аспектах этих вариантов осуществления животного-компаньона с гипертиреозом, нуждающегося в лечении, кормят пищевой композицией для домашних животных, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, в качестве неограничивающих примеров, такой как активность гена NIS кошек, представленного в настоящем описании.
В определенных вариантах осуществления полипептид, ингибируемый биоактивными компонентами рациона, выбран из группы, состоящей из тиреоидной пероксидазы, натрий-йодного симпортера (NIS), тиреоидной оксидазы, интратиреоидной 5'-дейодиназы типа I, рецептора тиреотропного гормона, пендрина, монокарбоксилат-транспортера 8 и их комбинаций.
Также изобретение относится к способу получения пищевой композиции, подходящей для лечения заболевания или состояния у животного.
Зонды
Зонды, применимые в практическом осуществлении изобретения и используемые в определении биомаркеров кошек в образцах от кошек, содержат от 10 до 50, от 15 до 40, от 20 до 30 последовательных нуклеотидов SEQ ID NO:1 или комплементарной ей последовательности. В конкретных вариантах осуществления зонд содержит приблизительно последовательных 25 нуклеотидов SEQ ID NO:1 или комплементарной ей последовательности. Последовательности зонда соответствуют идентификационному номеру зонда, используемому в патентованном генетическом чипе для кошек, производимому Affymetrix, определяемом как Affymetrix Feline GeneChip®, как более подробно представлено в настоящем описании ниже. HP06947_at соответствует SEQ ID NO:1, применимой в гибридизации с последовательностью мРНК гена NIS кошек.
Биомаркеры
Биомаркером, применимым в практическом осуществлении настоящего изобретения, является фрагмент гена NIS кошек SEQ ID NO:1 и кодируемый им пептид SEQ ID NO:2, как более подробно описано ниже и в списках последовательностей, прилагаемых к этому описанию.
В конкретных вариантах осуществления настоящего изобретения кошка может иметь нормальную функцию щитовидной железы, как определяют с помощью общепринятых в этой области клинических измерений, и способы по изобретению можно использовать для прогнозирования, определения и диагностики у такой кошки изменения с нормального состояния на аномальное состояние, приводящее к состоянию гипертиреоза.
В другом варианте осуществления способ по изобретению можно осуществлять практически с использованием чипа, с помощью которого определяют изменения экспрессии гена, например, изменения уровня экспрессии гена NIS. В одном способе такой чип является ДНК-микрочипом. Уровень активности или экспрессии можно определять посредством измерения продукта экспрессии этого гена, который может являться полинуклеотидом или полипептидом, или белком.
В другом варианте осуществления способ по изобретению можно осуществлять практически с использованием чипа, с помощью которого определяют изменения экспрессии гена, или уровень активности одного или нескольких генов, или их продукты экспрессии, выбранные из группы, состоящей из натрий-йодного транспортера (NIS), тиреоидной пероксидазы (TPO), рецептора тиреоидного гормона (TSHR), транспортера йода (IT; пендрина), тиреоидной оксидазы (ThOX), дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8) и молекулы-активатора рецептора тиреоидного гормона. В одном из аспектов этого способа такой чип является ДНК-микрочипом. Уровень активности или экспрессии одного или нескольких генов можно определять посредством измерения продукта экспрессии таких генов, которые могут являться полинуклеотидом или полипептидом, или белком.
В одном из аспектов изобретение включает приведение образца ткани или образца биологической жидкости в контакт со средством, с помощью которого у кошки определяют один или несколько генов или продуктов экспрессии такого одного или нескольких генов, выбранных из группы, состоящей из натрий-йодного транспортера (NIS), тиреоидной пероксидазы (TPO), рецептора тиреоидного гормона (TSHR), транспортера йода (IT; пендрина), тиреоидной оксидазы (ThOX), дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8) и молекулы-активатора рецептора тиреоидного гормона. Средство может являться антителом или нуклеиновой кислотой-зондом, используемым в комбинации с общепринятыми средствами анализа, такими как иммобилизация на твердой фазе, лунках планшета для микротитрования, пробирках, тест-полосках или другие общепринятые средства.
В другом аспекте изобретение включает приведение образца ткани или образца биологической жидкости в контакт со средством, с помощью которого у кошки определяют один или несколько генов или продуктов экспрессии такого одного или нескольких генов, выбранных из группы, состоящей из натрий-йодного транспортера (NIS), тиреоидной пероксидазы (TPO), рецептора тиреоидного гормона (TSHR), транспортера йода (IT; пендрина), тиреоидной оксидазы (ThOX), дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8) и молекулы-активатора рецептора тиреоидного гормона. Средство может являться антителом или нуклеиновой кислотой-зондом, используемым в комбинации с общепринятыми средствами анализа, такими как иммобилизация на твердой фазе, лунках планшета для микротитрования, пробирках, тест-полосках или другие общепринятые средства.
Другой вариант осуществления способа по настоящему изобретению относится к использованию общепринятых средств анализа для определения экспрессии гена у кошки в отдельности или в комбинации с чипами для анализа экспрессии гена с использованием полипептидов и/или полинуклеотидов, такие общепринятые средства анализа включают один или несколько из ELISA, RIA, анализов иммуноблоттинга, гибридизации in situ, анализа нозерн-блоттинга, анализа вестерн-блоттинга и анализа Luminex X-Map®.
В дополнительном аспекте изобретение относится к композициям, содержащим одну или несколько нуклеиновых кислот-зондов, специфически гибридизующихся с нуклеиновой кислотой или ее фрагментом, кодирующим биомаркер по настоящему изобретению, например, SEQ ID NO:1. В конкретном аспекте этого варианта осуществления нуклеиновая кислота-зонд специфически гибридизуется с кодирующей последовательностью (или комплементарной ей последовательностью) SEQ ID NO:1, т.е. кодирует последовательность пептида, включенную в SEQ ID NO:2. В другом аспекте этого варианта осуществления изобретение относится к композициям, содержащим одну или несколько таких нуклеиновых кислот-зондов, специфически гибридизующихся с нуклеиновой кислотой или ее фрагментом, кодирующим белок NIS или его часть.
В дополнительном аспекте настоящее изобретение относится к композициям, содержащим антитела, специфически связывающиеся с полипептидом, кодируемым геном, экспрессирующим биомаркер по настоящему изобретению. В частности, настоящее изобретение относится к композициям, содержащим антитела, избирательно связывающиеся с белком NIS кошек, по сравнению, например, с его гомологами у человека или собаки. В другом аспекте настоящее изобретение относится к композициям, содержащим антитела, избирательно связывающиеся с пептидной последовательностью SEQ ID NO:2, по сравнению, например, с ее гомологами у человека или собаки.
В настоящем описании также предполагают, что способы по настоящему изобретению можно использовать в комбинации с общепринятыми способами диагностики, с помощью которых можно определять физические и морфологические характеристики гипертиреоза.
Дополнительным аспектом изобретения является способ диагностики и/или прогнозирования гипертиреоза у кошки, включающий этапы: получения по меньшей мере одного образца ткани или образца биологической жидкости от животного; определения количества одного или нескольких биомаркеров, например, гена NIS, в указанном по меньшей мере одном образце, полученном от животного, где указанным биомаркером является его полипептид, белок, РНК, ДНК, полинуклеотид или метаболит.
Другие и дополнительные цели, характерные черты и преимущества настоящего изобретения будут очевидны специалистам в этой области.
В практическом осуществлении настоящего изобретения, если не указано иначе, можно использовать общепринятые способы и описания по органической химии, технологии полимеров, молекулярной биологи (включая рекомбинантные способы), клеточной биологии, биохимии и иммунологии, известные специалистам в этой области. Такие общепринятые способы включают синтез полимерного чипа, гибридизацию, лигирование и определение гибридизации с использованием метки. Конкретные иллюстративные примеры подходящих способов можно получить по ссылке в примере, приведенном в настоящем описании ниже. Однако, конечно, также можно использовать другие эквивалентные общепринятые способы.
Настоящее изобретение также включает многочисленные способы использования полимеров, прикрепленных к твердым подложкам. Эти способы использования включают мониторинг экспрессии генов, профилирование, скрининг библиотек, генотипирование и диагностику. Мониторинг и профилирование экспрессии можно найти в патентах США №№ 5800992, 6013449, 6020135, 6033860, 6040138, 6177248, 6309822 и 6344316. Генотипирование и его использование представлено в патентах США №№ 60319253, 10013598 и патентах США №№ 5856092, 6300063, 5858659, 6284460, 6361947, 6368799 и 6333179. Другие способы использования воплощены в патентах США №№ 5871928, 5902723, 6045996, 5541061 и 6197506.
Специалистам в этой области понятно, что продукты и способы, воплощенные в настоящем изобретении, можно использовать для множества систем, включая коммерчески доступные системы мониторинга экспрессии генов, включающие чипы с нуклеиновыми кислотами-зондами, блоттинг на мембранах, лунки микропланшетов, микрочастицы и пробирки для образцов, полученные с использованием различных материалов с использованием различных известных в этой области способов. Таким образом, настоящее изобретение не ограничено любым конкретным вариантом осуществления, и следующее ниже описание конкретных вариантов осуществления настоящего изобретения предназначено исключительно для иллюстративных целей.
В предпочтительном варианте осуществления система мониторинга экспрессии генов может содержать чип с нуклеиновыми кислотами-зондами (включая олигонуклеотидный чип, кДНК-чип, a чип с нанесенными пятнами и т.п.), блоттинг на мембранах (такой как используемый в анализе гибридизации, такой как нозерн-блоттинг, Саузерн-блоттинг, дот-блоттинг и т.п.) или лунки микропланшетов, пробирки для образцов, микрочастицы или волокна (или любую твердую подложку, содержащую связанные нуклеиновые кислоты). Система мониторинга экспрессии генов также может содержать нуклеиновые кислоты-зонды в растворе.
Настоящее изобретение также включает получение образцов, включающее амплификацию. Образец генома также можно амплифицировать множеством способов, в некоторых из которых можно использовать ПЦР. Образец можно амплифицировать на чипе. См., например, патент США № 6300070 и патентную заявку США с серийным № 09/513300.
Другие подходящие способы амплификации включают лигазную цепную реакцию (LCR) (например, Wu and Wallace, Genomics 4, 560 (1989), Landegren et al., 241 Science 1077 (1988) и Barringer et al. Gene 89:117 (1990)), транскрипционную амплификацию (Kwoh et al., Proc. Natl. Acad. Sci. USA 86, 1173 (1989), и WO88/10315), самоподдерживающуюся репликацию последовательностей (Guatelli et al, Proc. Nat. Acad. Sci. USA, 87, 1874 (1990), и WO 90/06995), селективную амплификацию полинуклеотидных последовательностей-мишеней (патент США № 6410276), полимеразную цепную реакцию с консенсусной последовательностью (CP-ПЦР) (патент США № 4437975), полимеразную цепную реакцию с произвольными праймерами (AP-ПЦР) (патенты США №№ 5413909, 5861245) и реакцию транскрипционной амплификации (NASBA). (См. патенты США №№ 5409818, 5554517 и 6063603, содержание каждого из которых включено в настоящее описание в качестве ссылки). Другие способы амплификации, которые можно использовать, описывают в патентах США №№ 5242794, 5494810, 4988617, 6344316 и в патентной заявке США № 09854317, содержание каждого из которых включено в настоящее описание в качестве ссылки.
Дополнительные способы получения образца и методики описывают в Dong et al., Genome Research 11, 1418 (2001), в патентах США №№ 6361947, 6391592 и патентных заявках США №№ 09/916135, 09/920491, 09/910292 и 10/013598.
Систему мониторинга экспрессии генов по настоящему изобретению можно использовать для облегчения сравнительного анализа экспрессии в различных клетках или тканях, различных субпопуляциях этих клеток или тканей, различных физиологических состояниях этих клеток или тканей, различных стадиях развития этих клеток или тканей или различных популяциях клеток этой ткани. В предпочтительном варианте осуществления с помощью пропорциональных способов амплификации по настоящему изобретению можно получать воспроизводимые результаты (т.е. в статистически значимых пределах ошибки или степеней достоверности), достаточные для облегчения измерения количественных, а также качественных различий в тестируемых образцах.
В этой области хорошо известны анализы гибридизации полинуклеотидов. Способы и условия анализа гибридизации будут варьироваться в зависимости от применения, и их выбирают согласно известным общим способам связывания, включая приведенные в Maniatis et al. Molecular Cloning: A Laboratory Manual (2nd Ed. Cold Spring Harbor, N.Y, 1989); Berger and Kimmel Methods in Enzymology, Vol. 152, Guide to Molecular Cloning Techniques (Academic Press, Inc., San Diego, Calif., 1987); Young and Davis, P.N.A.S, 80: 1194 (1983).
Способы и устройства для осуществления повторных и контролируемых реакций гибридизации описывают в патентах США №№ 5871928, 5874219, 6045996, 6386749 и 6391623, содержание каждого из которых включено в настоящее описание в качестве ссылки. Определение сигнала гибридизации между лигандами в конкретных предпочтительных вариантах осуществления. См. патенты США №№ 5143854, 5578832, 5631734, 5834758, 5936324, 5981956, 6025601, 6141096, 6185030, 6201639, 6218803 и 6225625, в патентной заявке США № 60/364731 и в заявке PCT № PCT/US99/06097 (опубликованной как W099/47964), содержание каждой из которых, таким образом, включено в настоящее описание в качестве ссылки в полном объеме для всех целей. Способы и устройства для определения сигнала и обработки данных об интенсивности описывают, например, в патентах США №№ 5143854, 5547839, 5578832, 5631734, 5800992, 5834758; 5856092, 5902723, 5936324, 5981956, 6025601, 6090555, 6141096, 6185030, 6201639; 6218803 и 6225625, в патентной заявке США № 60/364731 и в заявке PCT № PCT/US99/06097 (опубликованной как W099/47964), содержание каждой из которых, таким образом, включено в настоящее описание в качестве ссылки в полном объеме для всех целей.
Дизайн пищевых композиций для животных
Настоящее изобретение относится к способам дизайна пищевой композиции для животного, страдающего заболеванием или состоянием, включающим определение биоактивных компонентов рациона, применимых в снижении эффектов заболевания или состояния, которым страдает животное. В конкретном иллюстративном аспекте этого варианта осуществления заболеванием или состоянием является гипертиреоз, и страдающим животным является животное-компаньон из семейства кошачьих. Способы, представленные в настоящем описании и приведенные в примерах, относятся к способам и материалам для определения биоактивных компонентов рациона. Также в настоящем описании представлены иллюстративные пищевые композиции для домашних животных, содержащие эти биоактивные компоненты рациона, которые можно вводить кошкам, страдающим гипертиреозом, для лечения этого заболевания.
Терапевтические пищевые композиции для домашних животных для кошек с гипертиреозом
В одном иллюстративном варианте осуществления пищевой композиции для больных животных определяют животных-компаньонов из семейства кошачьих с диагнозом гипертиреоз и базальные уровни T4. Кроме того, каждому животному делают биопсию щитовидной железы и определяют базальные уровни экспрессии для каждого из натрий-йодного транспортера (NIS), тиреоидной пероксидазы (TPO), рецептора тиреоидного гормона (TSHR), транспортера йода (IT; пендрина), тиреоидной оксидазы (ThOX), дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8) и молекулы-активатора рецептора тиреоидного гормона. Составляют серию пищевых композиций, каждой из них кормят животных в течение соответствующего периода времени, и берут образцы крови для определения уровней тиреотропного гормона (TSH). Получают пищевые композиции и данные с использованием анализа основных компонентов, т.е. формы мультивариантного анализа, для определения макронутриентов пищи, коррелирующих с повышением тиреотропного гормона (TSH), свидетельствующим о повышении уровней циркулирующих T4-тироксина и T3-трийодтиронина. Обработанным животным, демонстрирующим значительное повышение уровней тиреотропного гормона (TSH), проводят биопсию, и определяют уровни экспрессии для каждого из натрий-йодного транспортера (NIS), тиреоидной пероксидазы (TPO), рецептора тиреоидного гормона (TSHR), транспортера йода (IT; пендрина), тиреоидной оксидазы (ThOX), дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8) и молекулы-активатора рецептора тиреоидного гормона. Компоненты (макронутриенты) корма для домашних животных, коррелирующие со снижением экспрессии одного или нескольких из TSH, TPO, TSHR, IT/пендрина, ThOX, дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8), обозначают в настоящем описании как биоактивные компоненты рациона.
Каждый из растительной смеси, пшена и томатного жмыха определяют как содержащий биоактивные компоненты рациона, приводящие к снижению экспрессии натрий-йодного транспортера (NIS). Т.е., в другом аспекте этого варианта осуществления, указанные выше биоактивные компоненты рациона измельчают или фракционируют для определения одной или нескольких молекул или субкомпонентов с повышенной специфической активностью в отношении модуляции активности молекулы-мишени. В другом аспекте тестирование на интактных животных можно дополнять, расширять или, возможно, заменять с использованием систем культур тканей in vitro, в которых используют соответствующие клеточные линии. Такие клеточные линии или индикаторные системы, например, можно генетически конструировать для получения легко измеряемых сигналов после ингибирования или стимуляции уровней экспрессии или активности одного или нескольких генов и кодируемых ими белков. В конкретном аспекте биоактивный компонент рациона экстрагируют и/или фракционируют для получения препарата, тестируемого на способность изменять экспрессию гена, например, изменять экспрессию гена NIS кошек в клетках культуры ткани.
В определенных вариантах осуществления животному-компаньону с гипертиреозом вводят пищевую композицию, содержащую эффективное количество первого биологически эффективного питательного вещества, достаточное для супрессии экспрессии или активности первого полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого. В другом аспекте этого варианта осуществления пищевая композиция дополнительно содержит эффективное количество второго биологически эффективного питательного вещества, достаточного для супрессии экспрессии или активности второго полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого. В дополнительных аспектах этих вариантов осуществления, пищевая композиция содержит ограниченные количества солей йода или селена, или и того, и другого. Еще в одном дополнительном аспекте страдающему животному-компаньону также вводят антитиреоидное средство, которое, например, можно выбирать из метимазола, пропилтиоурацила, карбимазола и их комбинаций.
Таким образом, в некоторых вариантах осуществления пищевые композиции по изобретению содержат от приблизительно 0,1 до менее чем приблизительно 1 мг/кг йода в пересчете на сухую массу. В некоторых таких вариантах осуществления пищевые композиции содержат от приблизительно 0,1 до приблизительно 0,5 мг/кг йода в пересчете на сухую массу. В других таких вариантах осуществления пищевые композиции по изобретению содержат от приблизительно 0,1 до приблизительно 0,3 мг/кг йода в пересчете на сухую массу. В других таких вариантах осуществления пищевые композиции по изобретению содержат от приблизительно 0,15 до приблизительно 0,25 мг/кг йода в пересчете на сухую массу. И в дополнительных таких вариантах осуществления пищевые композиции по изобретению содержат от приблизительно 0,1 до приблизительно 0,2 мг/кг йода в пересчете на сухую массу. Как указано выше, йод является компонентом T3 и T4. Как применяют в настоящем описании, йод относится к атому йода без ссылки на его молекулярную или ионную форму и включает йод, присутствующий в одной или нескольких химических формах, таких как, например, йодид, йодат и периодат.
В других вариантах осуществления пищевые композиции по изобретению содержат от приблизительно 0,1 до менее чем приблизительно 1 мг/кг селена в пересчете на сухую массу. В некоторых таких вариантах осуществления пищевые композиции содержат от приблизительно 0,1 до приблизительно 0,8 мг/кг селена в пересчете на сухую массу. В других таких вариантах осуществления пищевые композиции содержат от приблизительно 0,15 до приблизительно 0,65 мг/кг селена в пересчете на сухую массу. В других таких вариантах осуществления пищевые композиции содержат от приблизительно 0,4 до приблизительно 0,7 мг/кг селена в пересчете на сухую массу. В дополнительных таких вариантах осуществления пищевые композиции содержат от приблизительно 0,3 до приблизительно 0,65 мг/кг селена в пересчете на сухую массу. Как указано выше, селен играет роль в поддержании нормального метаболизма в щитовидной железе и метаболизма йода, в частности, посредством контроля ферментов дейодиназ, регулирующих превращение T4 в T3. Как применяют в настоящем описании, селен относится к атому селена без ссылки на его молекулярную или ионную форму и включает селен, присутствующий в одной или нескольких химических формах, таких как, например, селенид, селенит и селенат.
В дополнительных вариантах осуществления пищевые композиции по изобретению содержат от приблизительно 0,1 до менее чем приблизительно 1 мг/кг йода в пересчете на сухую массу и от приблизительно 0,1 до менее чем приблизительно 1 мг/кг селена в пересчете на сухую массу. В некоторых таких вариантах осуществления пищевые композиции содержат от приблизительно 0,1 до приблизительно 0,5 мг/кг йода в пересчете на сухую массу и от приблизительно 0,1 до приблизительно 0,8 мг/кг селена в пересчете на сухую массу. В других таких вариантах осуществления пищевые композиции содержат от приблизительно 0,1 до приблизительно 0,3 мг/кг йода в пересчете на сухую массу и от приблизительно 0,15 до приблизительно 0,65 мг/кг селена в пересчете на сухую массу. В дополнительных таких вариантах осуществления пищевые композиции содержат (1) от приблизительно 0,1, приблизительно 0,15 или от приблизительно 0,2 до приблизительно 0,25, приблизительно 0,3 или приблизительно 0,5 мг/кг йода в пересчете на сухую массу, и (2) от приблизительно 0,1, приблизительно 0,15, приблизительно 0,3 или от приблизительно 0,4 до приблизительно 0,65, приблизительно 0,7 или приблизительно 0,8 мг/кг селена в пересчете на сухую массу.
Как указано выше, животному, особенно кошке-компаньону с гипертиреозом, также можно вводить антитиреоидное средство. Антитиреоидные средства, подходящие для описываемых выше способов лечения, включают, например, тиоурейлены, производные анилина, многоатомные фенолы и соли лития. В некоторых вариантах осуществления способ включает введение кошке антитиреоидного средства, содержащего тиоурейлен. В некоторых вариантах осуществления способ включает введение антитиреоидного средства, содержащего метимазол. В некоторых вариантах осуществления способ включает введение кошке антитиреоидного средства, содержащего пропилтиоурацил. В некоторых вариантах осуществления способ включает введение антитиреоидного средства, содержащего карбимазол. В некоторых вариантах осуществления способ включает введение терапевтически эффективного количества антитиреоидного средства в комбинации с кормлением кошки пищевой композицией для домашних животных по изобретению. В некоторых вариантах осуществления пищевая композиция для домашних животных, которой кормят кошку, содержит антитиреоидное средство, вводимое кошке. В некоторых таких вариантах осуществления способ включает кормление кошки пищевой композицией по изобретению, содержащей терапевтически эффективное количество антитиреоидного средства. Антитиреоидные средства можно вводить, например, в форме солей, полученных из неорганических или органических кислот. В зависимости от конкретного соединения соль соединения может являться предпочтительной по причине одного или нескольких физических свойств солей, например, повышенной фармацевтической стабильности при различных температурах и влажности или желаемой растворимости в воде или масле. Предпочтительно, соль является фармацевтически приемлемой солью.
Предпочтительная общая суточная доза антитиреоидного средства (вводимого в одной или разделенной дозах) составляет, как правило, от приблизительно 0,001 до приблизительно 100 мг/кг массы тела, более предпочтительно - от приблизительно 0,01 до приблизительно 30 мг/кг массы тела, и даже более предпочтительно - от приблизительно 0,01 до приблизительно 10 мг/кг массы тела. Композиции в единицах дозирования могут содержать такие количества и их дольные единицы для получения суточной дозы. Во многих случаях введение антитиреоидного средства будут повторять множество раз. Многократные дозы в сутки, как правило, можно использовать для повышения общей суточной дозы, при желании. Факторы, влияющие на предпочтительный режим дозирования, включают, например, возраст, массу и состояние кошки; тяжесть заболевания; путь введения; фармакологические аспекты, такие как активность, эффективность, фармакокинетический и токсикологический профили конкретного используемого антитиреоидного средства; используют ли систему доставки лекарственного средства; и вводят ли антитиреоидное средство как часть комбинации лекарственных средств. Таким образом, режим дозирования может варьироваться в широких пределах, и, таким образом, он может отличаться от предпочтительного режима дозирования, описываемого выше.
В конкретных вариантах осуществления способ лечения можно адаптировать в зависимости от тяжести заболевания и скорости восстановления больного животного. Например, что касается лечения кошки-компаньона с гипертиреозом, при такой адаптации можно учитывать выбор одного или нескольких биоактивных компонентов рациона, представленных в настоящем описании, концентрацию каждого из них в пищевой композиции, уровни йода и селена в пищевой композиции, а также вводят ли больному животному антитиреоидное соединение или нет. В частности, это очевидно, учитывая синергизм, ожидаемый при использовании способов по настоящему изобретению, обеспечивающих многочисленные точки вмешательства, каждая из которых, как ожидают, будет улучшать, модулировать или устранять один или несколько основополагающих факторов, участвующих в развитии гипертиреоза у кошки-компаньона.
Таким образом, способы лечения по изобретению являются удобными и легкими в практическом осуществлении. В некоторых вариантах осуществления достаточно кормить композицией по изобретению кошку с диагнозом гипертиреоз. В некоторых таких вариантах осуществления композиция не содержит какие-либо антитиреоидные средства, и такие средства не вводят кошке в комбинации с кормлением кошки композицией. Таким образом, такие способы обеспечивают экономически эффективные альтернативы лечению антитиреоидными средствами. Кроме того, такие способы не вызывают побочных эффектов, приписываемых лечению антитиреоидными средствами, например, повреждение почек. Наконец, такие способы приводят к лучшему соблюдению режима, т.к. необходимо только кормить кошку композицией по изобретению, а не вводить, например, пероральное или местное антитиреоидное лекарственное средство. Как указано выше, в некоторых вариантах осуществления способы лечения по изобретению включают кормление кошки композицией, содержащей антитиреоидное средство. Такие способы лечения более удобны и легки в практическом осуществлении, т.к. они устраняют необходимость, например, перорального или местного введения антитиреоидных средств. В некоторых вариантах осуществления способы лечения по изобретению позволяют вводить меньше антитиреоидного средства, чем вводили бы при исключительно медикаментозном лечении, т.к. введение антитиреоидного средства в комбинации с кормлением кошки композицией по изобретению приводит к синергичному действию антитиреоидного средства, вводимого кошке, и композиции по изобретению, которой кормят кошку. Кроме того, специалисту в этой области будет известно, что кошку можно кормить одной композицией по изобретению или кошку можно кормить различными композициями по изобретению в течение различных временных интервалов.
В одном из вариантов осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% растительной смеси;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В другом варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% томатного жмыха;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В одном из вариантов осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% пшена;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В одном из вариантов осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% растительной смеси и от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% соевого жмыха.
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 5% соевого жмыха и приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 5% соевого жмыха, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 5% соевого жмыха, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В другом варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% томатного жмыха; и от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% соевого жмыха;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 5% соевого жмыха, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 5% соевого жмыха, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 5% соевого жмыха, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В одном из вариантов осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% пшена; и от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% соевого жмыха;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 5% соевого жмыха, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 5% соевого жмыха, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 5% соевого жмыха, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В другом варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% растительной смеси, и от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% томатного концентрата;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 5% томатного концентрата и приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 5% томатного концентрата, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% растительной смеси, приблизительно 5% томатного концентрата, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В другом варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% томатного жмыха; и от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% томатного концентрата;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 5% томатного концентрата, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 5% томатного концентрата, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% томатного жмыха, приблизительно 5% томатного концентрата, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
В одном из вариантов осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого, содержащей:
(a) от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% пшена; и от приблизительно 0,1% до приблизительно 20%, от приблизительно 0,25% до приблизительно 15%, от приблизительно 0,75% до приблизительно 12,5%, от приблизительно 1% до приблизительно 10%, от приблизительно 2% до приблизительно 8%, от приблизительно 3% до приблизительно 7%, от приблизительно 4% до приблизительно 6% или приблизительно 5% томатного концентрата;
(b) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% белка;
(c) от приблизительно 10% до приблизительно 50%, от приблизительно 15% до приблизительно 45%, от приблизительно 20% до приблизительно 40% или от приблизительно 25% до приблизительно 35% жира; и
(d) от приблизительно 10% до приблизительно 60%, от приблизительно 20% до приблизительно 50%, от приблизительно 25% до приблизительно 45% или от приблизительно 30% до приблизительно 40% углеводов.
В конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 35% томатного концентрата, приблизительно 30% белка, приблизительно 27% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 5% томатного концентрата, приблизительно 35% белка, приблизительно 20% жира и приблизительно 35% углеводов.
В другом конкретном варианте осуществления способы по настоящему изобретению включают кормление кошки, страдающей гипертиреозом, композицией, содержащей приблизительно 5% пшена, приблизительно 5% томатного концентрата, приблизительно 20% белка, приблизительно 15% жира и приблизительно 57% углеводов.
Описываемая выше растительная смесь может содержать материал, получаемый из любого или всех следующих растений: брюссельская капуста, кочанная капуста, цветная капуста, кормовая капуста, кольраби, брюква, турнепс, редис и их комбинации. В одном из аспектов этого варианта осуществления растительная смесь может дополнительно содержать горчицу, персики, арахис и клубнику.
В других вариантах осуществления настоящее изобретение относится к пищевой композиции, пригодной для использования в способе лечения гипертиреоза у животного-компаньона, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого. Таким образом, пищевые композиции включают каждую из описываемых выше композиций, применимых в описываемых выше способах.
В других вариантах осуществления, как указано выше, композиция по изобретению является пищевой композицией для домашних животных (т.е. композиция может содержать одну или несколько пищевых композиций). В некоторых таких вариантах осуществления композиция удовлетворяет требованиям AAFCO к минимальному содержанию питательных веществ, их уровню для репродукции или поддержания. См. официальную публикацию AAFCO, стр. 159-162 (2005). В других таких вариантах осуществления пищевая композиция для домашних животных содержит меньше минимальных требований AAFCO для репродукции или поддержания (например, пищевая композиция для домашних животных содержит меньше йода и/или селена, чем количество, рекомендуемое AAFCO). В некоторых вариантах осуществления пищевую композицию для домашних животных составляют в виде сухого корма. В некоторых вариантах осуществления пищевую композицию для домашних животных составляют в виде полувлажного корма. В некоторых вариантах осуществления пищевую композицию для домашних животных составляют в виде влажного корма. В некоторых вариантах осуществления пищевую композицию для домашних животных составляют и получают в виде добавки, лакомства, закуски или частично или полностью съедобной игрушки. В некоторых вариантах осуществления пищевая композиция для домашних животных содержит смесь двух или более кормов.
В определенных аспектах этих вариантов изобретения пищевые композиции для домашних животных по изобретению также могут содержать дополнительные ингредиенты, включая незаменимые аминокислоты и питательные вещества. В одном из вариантов осуществления "незаменимые аминокислоты", как применяют в настоящем описании, относятся к аминокислотам, которые не могут синтезироваться de novo в организме, и, таким образом, ими необходимо дополнять рацион. Специалисту в этой области будет понятно, что незаменимые аминокислоты варьируются от вида к виду в зависимости от метаболизма организма. Например, как правило, следует понимать, что незаменимыми аминокислотами для собак и кошек являются фенилаланин, лейцин, метионин, лизин, изолейцин, валин, треонин, триптофан, гистидин и аргинин. В других вариантах осуществления описываемые пищевые композиции для домашних животных также дополняют аминокислотой лизин.
В другом варианте осуществления пищевые композиции для домашних животных, представленные в настоящем описании, также могут содержать "незаменимые питательные вещества", относящиеся, как применяют в настоящем описании, к питательным веществам, необходимым для нормального функционирования организма, которые не могут синтезироваться в организме. Категории незаменимых питательных веществ включают витамины, минеральные вещества, жирные кислоты и аминокислоты. Специалисту в этой области будет понятно, что питательные вещества, считающиеся незаменимыми, варьируются от вида к виду в зависимости от метаболизма организма. Например, незаменимые питательные вещества для собак и кошек включают витамины A, D, E, K, B1, B6, B12, рибофлавин, ниацин, пантотеновую кислоту, фолиевую кислоту, кальций, фосфор, магний, натрий, калий, хлор, железо, медь, цинк, марганец, селен и йод. Как указано выше, количества йода и селена в пищевых композициях для домашних животных, представленных в настоящем описании, могут быть ниже рекомендуемых уровней, представленных AAFCO.
Холин, как правило, рассматриваемый как комплекс витамина B, можно включать среди полунезаменимых питательных веществ. Кроме того, таурин, хотя формально является не аминокислотой, а производным цистеина, является незаменимым питательным веществом для кошек. В другом аспекте пищевые композиции для домашних животных по настоящему изобретению также могут содержать карнитин, также известный как L-карнитин (левокарнитин), являющийся четвертичным соединением аммония, синтезируемым из аминокислот лизина и метионина и ответственным за транспорт жирных кислот из цитозоля в митохондрии.
Таким образом, в одном конкретном варианте осуществления пищевая композиция для домашних животных, применимая в описываемом способе лечения гипертиреоза, может содержать один или несколько определенных выше биоактивных компонентов рациона в описываемых количествах, а также йод и селен (например, в виде йодата кальций, йодированной соли и селенита натрия) на описываемых выше уровнях, и может дополнительно содержать: свиную печень, куриные, свиные субпродукты, вареный рис, кукурузный крахмал, глюкозу, куриный жир (законсервированный с использованием смеси токоферолов и лимонной кислоты), цитрат калия, карбонат кальция, рыбий жир, сульфат кальция, DL-метионин, хлорид холина, таурин, добавку витамина E, L-цистеин, глицин, мононитрат тиамина, аскорбиновую кислоту, оксид цинка, сульфат железа, ниацин, бета-каротин, оксид марганца, сульфат меди, гидрохлорид пиридоксина, пантотенат кальция, добавку витамина B12, рибофлавин, биотин, добавку витамина D3 и фолиевую кислоту.
В другом варианте осуществления пищевая композиция для домашних животных, применимая в описываемом способе лечения гипертиреоза, может содержать один или несколько указанных выше биоактивных компонентов рациона в описываемых количествах, а также йод и селен (например, в виде йодата кальция, йодированной соли и селенита натрия) на определенных выше уровнях, и может дополнительно содержать: воду, свиную печень, куриные, свиные субпродукты, вареный рис, кукурузный крахмал, глюкозу, куриный жир (законсервированный с использованием смеси токоферолов и лимонной кислоты), цитрат калия, карбонат кальция, рыбий жир, сульфат кальция, DL-метионин, хлорид холина, таурин, добавку витамина E, L-цистеин, глицин, мононитрат тиамина, аскорбиновую кислоту, оксид цинка, сульфат железа, ниацин, бета-каротин, оксид марганца, сульфат меди, гидрохлорид пиридоксина, пантотенат кальция, добавку витамина B12, рибофлавин, биотин, добавку витамина D3 и фолиевую кислоту.
В другом конкретном варианте осуществления пищевая композиция для домашних животных, применимая в описываемом способе лечения гипертиреоза, может содержать один или несколько описываемых выше биоактивных компонентов рациона в описываемых количествах, а также йод и селен (например, в виде йодата кальций, йодированной соли и селенита натрия) на описываемых выше уровнях, и может дополнительно содержать: измельченные куриные субпродукты, кукурузную глютеновую муку, вареный рис, животный жир (законсервированный с использованием смеси токоферолов и лимонной кислоты), L-лизин, молочную кислоту, измельченную куриную печень, хлорид калия, хлорид холина, добавку витамина E, сульфат кальция, витамины (L-аскорбил-2-полифосфат (источник витамина C), добавку витамина E, ниацин, мононитрат тиамина, добавку витамина A, пантотенат кальция, рибофлавин, биотин, добавку витамина B12, гидрохлорид пиридоксина, фолиевую кислоту, добавку витамина D3), таурин, натуральный ароматизатор, карбонат кальция, рыбий жир, минеральные вещества (сульфат железа, оксид цинка, сульфат меди, оксид марганца), L-карнитин, законсервированный с использованием смеси токоферолов и лимонной кислоты, фосфорную кислоту, бета-каротин и экстракт розмарина.
В другом конкретном варианте осуществления пищевая композиция для домашних животных, применимая в описываемом способе лечения гипертиреоза, может содержать один или несколько из описываемых выше биоактивных компонентов рациона в описываемых количествах, а также йод и селен (например, в виде йодата кальция, йодированной соли и селенита натрия) на указанных выше уровнях, и может дополнительно содержать: измельченные куриные субпродукты, животный жир (законсервированный с использованием смеси токоферолов и лимонной кислоты), измельченную куриную печень, молочную кислоту, кукурузную глютеновую муку, хлорид калия, L-лизин, хлорид холина, добавку витамина E, витамины (L-аскорбил-2-полифосфат (источник витамина C), добавку витамина E, ниацин, мононитрат тиамина, добавку витамина A, пантотенат кальция, биотин, добавку витамина B12, гидрохлорид пиридоксина, рибофлавин, фолиевую кислоту, добавку витамина D3), карбонат кальция, дифосфат кальция, минеральные вещества (сульфат железа, оксид цинка, сульфат меди и оксид марганца), L-триптофан, таурин, гидрохлорид глюкозамина, L-карнитин, законсервированный с использованием смеси токоферолов и лимонной кислоты, хондроитинсульфат, фосфорную кислоту, бета-каротин и экстракт розмарина.
Примеры подходящих источников белка, которые можно включать в композиции, представленные в настоящем описании, включают, в качестве неограничивающих примеров, животные источники, такие как изолят мясного белка, изолят белка молочной сыворотки, их смеси и т.п., а также растительные источники, такие как кукурузная глютеновая мука, пшеничная клейковина, их смеси и т.п. Примеры подходящих источников жира, который можно включать в композиции, представленные в настоящем описании, включают, в качестве неограничивающих примеров, птичий жир, говяжий жир, лярд, белый жир, соевое масло, кукурузное масло, каноловое масло, подсолнечное масло, их смеси и т.п. Жир можно полностью включать в пищевую композицию, его можно хранить вне пищевой композиции или комбинировать эти два способа. Примеры подходящих источников углеводов, которые можно включать в композиции, представленные в настоящем описании, включают, в качестве неограничивающих примеров, компонент другого ингредиента, такого как источник белка, а также крахмалы и зерна, такие как кукуруза, пшеница, сорго, ячмень, рис, их смеси и т.п.
В конкретных вариантах осуществления пищевые композиции для домашних животных, применимые в способах, представленных в настоящем описании, также могут содержать волокнистую добавку, как правило, составляющую от приблизительно 1% до приблизительно 5% композиции. Подходящие источники таких волокон включают, в качестве неограничивающих примеров, цельные зерна кукурузы, овсяные волокна, оболочки семян подорожника, гуаровую камедь, льняное семя, соевые отруби и их комбинации.
Иллюстративные варианты осуществления описываемых способов лечения и пищевых композиций для домашних животных приведены в следующих параграфах.
В одном из вариантов осуществления настоящее изобретение относится к способу лечения гипертиреоза у животного-компаньона, включающему кормление нуждающегося в этом животного-компаньона пищевой композицией для домашних животных, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого.
В одном из аспектов этого варианта осуществления полипептид является биосинтетическим ферментом, выбранным из группы, состоящей из тиреоидной пероксидазы, натрий-йодного симпортера, тиреоидной оксидазы и интратиреоидной 5'-дейодиназы типа I и их комбинаций.
В одном из аспектов этого варианта осуществления полипептид выбран из группы, состоящей из тиреотропного гормона, рецептора тиреоидного гормона, молекулы-активатора рецептора тиреоидного гормона, пендрина и монокарбоксилат-транспортера-8 и их комбинаций.
В одном из аспектов этого варианта осуществления животное-компаньон является кошкой.
В одном из аспектов этого варианта осуществления вводимая пищевая композиция для домашних животных содержит биоактивный компонент рациона, выбранный из группы, состоящей из томатного жмыха, растительной смеси, пшена, соевого жмыха, томатного концентрата и их комбинаций. В одном из аспектов этого варианта осуществления биологически активный материал составляет от приблизительно 0,1% до приблизительно 20% пищевой композиции для домашних животных в пересчете на сухую массу. В другом аспекте этого варианта осуществления биологически активный материал составляет от приблизительно 1% до приблизительно 10% пищевой композиции для домашних животных в пересчете на сухую массу.
В одном из аспектов этого варианта осуществления вводимая пищевая композиция для домашних животных содержит от приблизительно 15% до приблизительно 45% белка, от приблизительно 15% до приблизительно 45% жира, от приблизительно 20% до 50% углеводов в пересчете на сухую массу и от приблизительно 2% до приблизительно 8% биологически активного материала в пересчете на сухую массу.
В одном из аспектов этого варианта осуществления вводимая пищевая композиция для домашних животных содержит от приблизительно 25% до приблизительно 35% белка, от приблизительно 25% до приблизительно 35% жира, от приблизительно 30% до 40% углеводов и от приблизительно 2% до приблизительно 8% биологически активного материала в пересчете на сухую массу.
В одном из аспектов этого варианта осуществления вводимая пищевая композиция для домашних животных содержит от 0,1 до менее чем приблизительно 1 мг/кг йода в пересчете на сухую массу.
В одном из аспектов этого варианта осуществления вводимая пищевая композиция для домашних животных содержит от 0,1 до приблизительно 1 мг/кг селена в пересчете на сухую массу.
В одном из аспектов этого варианта осуществления способ дополнительно включает введение терапевтически эффективного количества антитиреоидного средства, например, где антитиреоидное средство выбрано из группы, состоящей из метимазола, пропилтиоурацила, карбимазола и их комбинаций.
В другом варианте осуществления настоящее изобретение относится к пищевой композиции для домашних животных, где пищевая композиция для домашних животных пригодна для использования в способе лечения гипертиреоз у животного-компаньона, содержащей эффективное количество биоактивного компонента рациона, достаточное для супрессии экспрессии или активности по меньшей мере одного полипептида, необходимого для биосинтеза, транспорта или активности тироксина или трийодтиронина, или и того, и другого.
В одном из аспектов этого варианта осуществления полипептид является биосинтетическим ферментом, выбранным из группы, состоящей из тиреоидной пероксидазы, натрий-йодного симпортера, тиреоидной оксидазы и интратиреоидной 5'-дейодиназы типа I и их комбинаций.
В одном из аспектов этого варианта осуществления полипептид выбран из группы, состоящей из молекулы-активатора рецептора тиреоидного гормона, рецептора тиреоидного гормона, пендрина, монокарбоксилат-транспортера-8 и их комбинаций.
В одном из аспектов этого варианта осуществления животное-компаньон является кошкой.
В одном из аспектов этого варианта осуществления биоактивный компонент рациона выбран из группы, состоящей из томатного жмыха, растительной смеси, пшена, соевого жмыха, томатного концентрата и их комбинаций.
В одном из аспектов этого варианта осуществления биологически активный материал составляет от приблизительно 0,1% до приблизительно 20% пищевой композиции для домашних животных в пересчете на сухую массу.
В одном из аспектов этого варианта осуществления биологически активный материал составляет от приблизительно 1% до приблизительно 10% пищевой композиции для домашних животных в пересчете на сухую массу.
В другом аспекте этого варианта осуществления композиция содержит от приблизительно 15% до приблизительно 45% белка, от приблизительно 15% до приблизительно 45% жира, от приблизительно 20% до 50% углеводов и от приблизительно 2% до приблизительно 8% биологически активного материала в пересчете на сухую массу.
В другом аспекте этого варианта осуществления композиция содержит от приблизительно 25% до приблизительно 35% белка, от приблизительно 25% до приблизительно 35% жира, от приблизительно 30% до 40% углеводов и от приблизительно 2% до приблизительно 8% биологически активного материала в пересчете на сухую массу.
В другом аспекте этого варианта осуществления композиция содержит от приблизительно 0,1 до менее чем приблизительно 1 мг/кг йода в пересчете на сухую массу.
В другом аспекте этого варианта осуществления композиция содержит от приблизительно 0,1 до приблизительно 1 мг/кг селена в пересчете на сухую массу.
В другом аспекте этого варианта осуществления композиция содержит терапевтически эффективное количество антитиреоидного средства, где антитиреоидное средство выбрано из группы, состоящей из метимазола, пропилтиоурацила, карбимазола и их комбинаций.
Таким образом, настоящее изобретение включает способ получения пищевой композиции, подходящей для лечения заболевания или состояния у животного, включающий: (a) определение целевого заболевания или состояния; (b) определение полипептида, вносящего вклад в этиологию, лежащую в основе этого заболевания; (c) определение, повышение ли или снижение активности или экспрессии указанного определенного полипептида будет улучшать целевое заболевание или состояние; (d) осуществление по меньшей мере одного мультивариантного анализа для определения биоактивных компонентов рациона, способных модулировать активность или экспрессию указанного определенного полипептида способом, необходимым для улучшения целевого заболевания или состояния; и (e) составление пищевой композиции, содержащей биоактивный компонент рациона.
Изобретение не ограничено конкретной методологией, протоколами и реагентами, представленными в настоящем описании, т.к. они могут варьироваться. Кроме того, терминология, используемая в настоящем описании, представлена исключительно в целях описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения.
Все патенты, патентные заявки, публикации и другие ссылки, цитируемые или упоминаемые в настоящем описании, включены в настоящее описание посредством ссылок в пределах, разрешенных законом. Описание таких ссылок предназначено исключительно для обобщений утверждений, сделанных в них.
Как применяют на всем протяжении описания, диапазоны используют в качестве условного обозначения для описания каждого значения, попадающего в диапазон. В качестве границы диапазона можно выбирать любое значение в пределах диапазона. Кроме того, все цитируемые в этом описании ссылки включены, таким образом, в него в качестве ссылок в полном объеме. В случае противоречия определения, представленного в настоящем описании и в цитируемом источнике, настоящее описание обладает приоритетом.
ПРИМЕРЫ
Пример 1: Определение генов с измененной экспрессией у кошек с гипертиреозом
В следующих ниже примерах, касающихся кошек, для которых данные об экспрессии гена получают с помощью анализа с использованием ДНК-микрочипа, для определения конкретных генов и экспрессируемых белков в качестве подходящих биологических маркеров гипертиреоза у кошек устанавливают критерии выбора. Специалист в этой области может выбирать из ряда алгоритмов для анализа данных, полученных с помощью генетического чипа. Они включают статистический алгоритм MASS, Probe logarithmic intensity error estimation (PLIER) и Robust multi-chip analysis (RMA). Алгоритмы обработки подробно описаны в следующих источниках: Li, C. Mo, 2001, Model-based analysis of oligonucleotide arrays: expression index computation and outlier detection, Proc. Acad. Sci. USA, Vol. 98: 31-36; Irizarry R.A. et al., Exploration, normalization and summaries of high density oligonucleotide array probe level data, Biostatistics, 2003, Vol. 4: 249-264; Irizarry et al., Summaries of Affymetrix GeneChip probe level data, Nucleic Acid Res., 2003, Vol. 31(4): e15; and Fan, W., A. et al., A class of models for analyzing GeneChip gene expression analysis array data, BMC Genomics, 2005, Vol. 16: 6-16; Zhou, L. et al., An expression index for Affymetrix GeneChips based on the generalized logarithm, Bioinformatics, 2005, Vol. 21(21): 3983-3989 and Hein A.K. et al., BGX: a fully Bayesian integrated approach to the analysis of Affymetrix GeneChip data, Biostatistics, 2005, Vol. 6: 349-373.
Исходные данные в следующих примерах анализируют с использованием программного обеспечения GeneSpring версии 7.0 (GS) (Agilent Corporation) и валидируют с использованием бесплатного программного обеспечения R-Bioconductor (RB). Оба пакета программ используют для вычисления интенсивности зондов из файлов CEL, генерируемых устройством Affymetrix. Сигналы Present/Absent/Marginal на зонд и значения P вычисляют с использованием программного обеспечения R-Bioconductor и GeneSpring раздельно.
Данные об экспрессии гена для любого указанного анализа определяют "положительно" или "отрицательно" регулируемые. Решение о том, является ли ген "положительно" или "отрицательно" регулируемым, основывается на кратном изменении, вычисляемом как интенсивность при лечении/контрольная интенсивность для каждого отдельного зонда. Кратное изменение считают отрицательно регулируемым, если его значение снижается на величину приблизительно 10%, приблизительно 15%, приблизительно 20%, приблизительно 25%, приблизительно 30%, приблизительно 35%, приблизительно 40%, приблизительно 45% или приблизительно 50% или более, и положительно регулируемым, если оно повышается на величину приблизительно 10%, приблизительно 15%, приблизительно 20%, приблизительно 25%, приблизительно 30%, приблизительно 35%, приблизительно 40%, приблизительно 45% или приблизительно 50% или более. Кроме того, зонд считают важным для дальнейшего изучения, если его называют "Present" только в одних условиях сравнения (при лечении или в контроле) и "Absent" или "Marginal" в других, и кратное изменение считают значимым согласно используемому программному обеспечению.
Пример 2: Сбор образцов крови и выделение РНК
Кровь собирали и обрабатывали по инструкциям производителя в руководстве PAXgene. Пробирки PAXgene хранят при -20°C перед выделением РНК. РНК выделяют из пробирок для крови PAXgene (VWR, кат. № 77776-026) с использованием набора для выделения РНК из крови PAXgene (Qiagen, кат. № 762164) по инструкциям производителя. Количество и качество РНК определяют с использованием биоанализатора Agilent 2100 (Agilent Technologies) и набора RNA 6000 Nano chip (Agilent, кат. № 5067-1511) по инструкциям производителя. Целостность РНК определяют по соотношению рибосомальной РНК 28S:18S и показателю целостности РНК (RIN; бета-версия программного обеспечения Agilent 2100 RIN). Очищенные образцы РНК хранят при -80°C.
Пример 3: Выделение РНК из ткани
Собирают образцы тканей кошек и рассекают на небольшие куски, помещают в сосуды для криогенной заморозки и сразу замораживают в жидком азоте. Образцы тканей гомогенизируют с использованием Tissue Lyser (SOP №: LAB-LS-028.3). РНК выделяют с использованием набора для выделения РНК RNeasy по инструкциям производителя. Все образцы выделенной РНК количественно анализируют по показаниям оптической плотности при 260 и 280 нм с использованием спектрофотометра NanoDrop 1000 (Thermo Scientific). Качество РНК определяют с помощью биоанализатора 2100 Bioanalyzer (Agilent Technologies) по инструкциям производителя. Целостность РНК определяют по соотношению рибосомальной РНК 28S:18S и показателю целостности РНК (RIN; с помощью бета-версии программного обеспечения Agilent 2100 RIN). Очищенные образцы РНК хранят при -80°C.
Пример 4: Получение зондов
Реагенты для мечения и амплификации получают из NuGEN Technologies, Inc. (San Carlos, CA, USA), и они включают систему для амплификации РНК Ovation RNA Amplification System V2 (кат. № 3100-A01), раствор Ovation® Whole Blood Solution (кат. № 1300-A01) и модуль Encore Biotin Module (кат. № 4200-A01). Биотинилированные кДНК-мишени получают по инструкциям производителя. Двухцепочечную кДНК синтезируют из 50 нг тотальной РНК с последующим этапом линейной изотермальной амплификации (SPIA Amplification™) для получения одноцепочечной кДНК. После фрагментации проводят прямое мечение, при котором биотин прикрепляют к амплифицированному зонду. Очистку зонда осуществляют с использованием RNAClean XP, продукта на основе магнитных микрочастиц, которые используют для очистки синтезированной кДНК (Beckman Genomics, кат. № A63987).
Пример 5: Гибридизация на чипе и обработка
После предварительной гибридизации в течение 10 минут при 45°C 4,4 мкг каждой кДНК-мишени смешивают с контролями для гибридизации Affymetrix (Affymetrix, кат. № 900454) в гибридизационном буфере и гибридизуют с чипом Affymetrix Feline-2 GeneChip® в течение 16-18 часов при 45°C. После удаления гибридизационных смесей чип GeneChips® промывают в струйной установке с использованием буфера низкой жесткости (6-кратный стандартный фосфатно-солевой буфер с ЭДТА, 0,01% Tween 20) и буфера высокой жесткости (100 мМ N-морфолино-этансульфоновая кислота (MES), 0,1 M NaCl и 0,01% Tween 20) и окрашивают SAPE (стрептавидин-фикоэритрин, Invitrogen, кат. № S-866). После этого проводят инкубацию с нормальным IgG козла и биотинилированным антителом мыши против стрептавидина (Vector Lab, BA-0500) с последующим повторным окрашиванием SAPE. Чипы сканируют с помощью GeneChip® Scanner 3000 7G (Affymetrix Inc., Santa Clara, CA) для определения сигналов гибридизации. Изучение изображений осуществляют вручную непосредственно после каждого сканирования (GeneChip® Expression Analysis Technical Manual. кат. № 702232 Rev. 3, главы II и III).
Пример 6: Анализ данных
Для анализа данных используют программное обеспечение Partek® GS (Partek Inc., St. Charles, MO) для анализа данных об экспрессии генов (Partek Incorporated, 12747 Olive Blvd., Suite 205, St. Louis, Missouri 63141, U.S.A. http://www.partek.com/partekgs_geneexpression). Алгоритм Robust Multichip Average (RMA) (Rafael. A. Irizarry, Benjamin M. Bolstad, Francois Collin, Leslie M. Cope, Bridget Hobbs and Terence P. Speed (2003), Summaries of Affymetrix GeneChip probe level data Nucleic Acids Research 31(4):e15) используют для коррекции фона, нормирования и суммаризации зонда-уровня в образцах GeneChip®. Осуществляют анализ ANOVA для обнаружения значимых дифференциально экспрессирующихся генов в любых двух группах с минимальным контролем FDR при 0,1 и кратном изменении в 1,25 раз в каждом направлении. Эмпирические исследования показали, что Feline-2 GeneChips® имеет ассоциированный 1,3-кратный уровень фонового шума. Таким образом, во всех представленных анализах используют ±1,25-кратное граничное значение. Кроме того, выбирают предел средней доли ложных отклонений гипотезы 0,1 (означает, что 10% результатов являются результатом случая) как минимальный уровень приемлемой статистической значимости.
Пример 7: Подробное описание способов выделения РНК.
Материалы и способы. Следующие общие способы можно использовать для выделения РНК из образцов тканей кошек для определения профиля экспрессии генов с использованием генетических чипов, как более подробно описано в примерах, приведенных в настоящем описании. Специалисту в этой области будет очевидно, что эти способы или их модификации, как общепринято в этой области, можно использовать для выделения РНК из образцов тканей или биологических жидкостей для дальнейшего анализа экспрессии генов с использованием множества аналитических способов, доступных специалисту в этой области, в конкретных технологиях с использованием микрочипов.
Выделение рибонуклеиновой кислоты (РНК) из ткани. Образцы ткани можно собирать, замораживать в жидком азоте, размораживать, а затем растирать в ступке пестиком, гомогенизировать и переносить в коническую колбу емкостью 50 мл. Затем гомогенизированный образец ткани обрабатывают с использованием способа выделения РНК TRIzol® по инструкциям производителя (Invitrogen) для получения РНК хорошего качества, затем подвергаемой дальнейшему геномному анализу.
Материалы: лед, жидкий азот, замороженная ткань кошки, лизирующий реагент TRIzol®, хлороформ минимум 99%, изопропиловый спирт, 70% этанол (полученный с использованием абсолютного и деионизированного этанола, воды, не содержащей РНКаз), РНКаза Zap®, деионизированная вода, RNA Storage Solution® от Ambion.
Оборудование: гомогенизатор Ultra-Turrax T25 Power Homogenizer, центрифуга Beckman Coulter Allegra 25R, центрифуга Eppendorf, пинцет, скальпель, твердая поверхность для резки, т.е. разделочная доска, стерильные микроцентрифужные пробирки без ДНКаз и РНКаз емкостью 1,5 мл, стерильные одноразовые полипропиленовые пробирки без ДНКаз и РНКаз емкостью 50 мл, пипетки P1000, P200, P20, P10 и P2 Rainin Pipetman, наконечники для пипеток с фильтрами для пипеток P1000, P200, P20, P10 и P2, стерильные и безворсовые салфетки без ДНКаз и РНКаз.
Препараты: Получают полипропиленовые пробирки емкостью 50 мл с 4 мл TRIzol® (одна пробирка для каждой ткани, выбранной для выделения РНК).
Гомогенизация ткани: Контейнер, способный удерживать жидкий азот, наполняют 3-4 ковшами жидкого азота. Помещают кусок замороженной ткани непосредственно в указанный выше контейнер (ткань должна иметь размер приблизительно горошины) и помещают ткань в подходящую помеченную полипропиленовую пробирку емкостью 50 мл (которая уже содержит 4 мл TRIzol®). Сразу начинают гомогенизацию с использованием гомогенизатора Ultra-Turrax T25 Power Homogenizer. Гомогенизируют при самых высоких настройках (6) в течение 10-15 секунд. Охлаждают образец на льду в течение еще 10-15 секунд, а затем повторяют. Продолжают до полной гомогенизации ткани и помутнения раствора. После завершения гомогенизации пробирку емкостью 50 мл закрывают и возвращают на лед. Инкубируют гомогенизированные ткани при комнатной температуре в течение 5 минут перед проведением выделения.
Пример 8: Способы получения РНК.
Выделение РНК: В целом, следуют процедурам, представленным в инструкциях, прилагаемых Invitrogen к TRIzol®. Разделяют гомогенизированный образец на четыре аликвоты по 1 мл в четырех микроцентрифужных пробирках по 1,5 мл. Добавляют 200 мкл хлороформа в каждую аликвоту по 1 мл. Закрывают пробирки, центрифугируют на центрифуге типа вортекс в течение 15 секунд, а затем встряхивают вверх и вниз. В результате должны получать мутную розовую жидкость. Инкубируют пробирки при комнатной температуре в течение 2-3 минут. Центрифугируют пробирки в течение 15 минут при 14000 об./мин и 4°C. Переносят водную фазу (верхний слой) в стерильную микроцентрифужную пробирку по 1,5 мл. Типичный объем водной фазы, который необходимо переносить в новую пробирку, составляет приблизительно 500 мкл. Убеждаются, что не переносят какую-либо промежуточную или нижнюю фазы. Осаждают РНК из раствора, добавляя 500 мкл изопропилового спирта в каждую микроцентрифужную пробирку, содержащую водный слой. Встряхивают пробирки вверх и вниз в течение по меньшей мере 20 секунд. Инкубируют образцы при комнатной температуре в течение 10 минут. Центрифугируют образцы в течение 10 минут при 14000 об./мин и 4°C. Осторожно удаляют супернатант осторожно, отсасывая жидкость, будучи уверенными, что не теряют осадок. Добавляют 1 мл 70% этанола для промывания осадка. Перемещают осадок, встряхивая пробирку (или постукивая пробиркой по рабочей поверхности стола), и встряхивают для перемешивания. Центрифугируют в течение 5 минут при 8200 об./мин и 4°C. Осторожно удаляют супернатант, отсасывая жидкость, будучи уверенными, что не теряют осадок. Используя безворсовую салфетку, осторожно промокают избыток этанола, обеспечивая высушивание осадка. Ресуспендируют каждый осадок в 30 мкл раствора для хранения РНК. Осторожно перемешивают пипетированием до перехода РНК в раствор, а затем хранят при -80°C. Необходимым может являться центрифугирование образца на центрифуге типа вортекс в течение нескольких секунд при низкой скорости для облегчения ресуспендирования РНК. При необходимости, перед замораживанием образцы центрифугируют с использованием микроцентрифуги.
Пример 9: Очистка РНК: способы по руководству RNeasy® Mini
Выделение РНК из культивируемых клеток в камерах OptiCell с использованием набора RNeasy Mini. Для выделения РНК хорошего качества, которую затем используют для последующего геномного анализа, используют культивируемые клетки из клеточных линий млекопитающих. Все работы, относящиеся к культивированию клеток, необходимо проводить в строгих асептических условиях.
Реагенты: 10X PBS, деионизированная H2O, абсолютный этанол, раствор для хранения РНК, β-меркаптоэтанол, РНКаза Zap®, буфер RLT, буфер RW1 и буфер RPE (находящиеся в наборе RNeasy Mini).
Оборудование/Материалы: набор RNeasy Mini, центрифужные колонки QIAshredder, нож OptiCell, стерильный шприц 20 мл, наконечники OptiCell, скребок для клеток, пипетка P1000 Pipetman, Rainin, пипетка P200 Pipetman, Rainin, наконечники для пипеток с фильтрами 100-100 мкл, наконечники для пипеток с фильтрами 1-200 мкл, стерильные пипетки для переноса, почковидный тазик емкостью 55 мл для стерильного раствора, стерильные микроцентрифужные пробирки по 1,5 мл и микроцентрифуга Eppendorf.
Растворы: Буфер RLT (сток, находящийся в наборе RNeasy Mini); перед началом выполнения протокола добавляют 100 мкл β-меркаптоэтанола на 10 мл буфера RLT. 70% этанол: Получают 50 мл 70% этанола, добавляя 35 мл абсолютного этанола к 15 мл деионизированной воды, не содержащей РНКаз. 1-кратный PBS: вода, не содержащая РНКаз. Фильтруют раствор с использованием фильтра a.22 мкм.
Способ: Удаляют клетки из камеры OptiCell (используя одну OptiCell за один раз). Проверяют клетки под микроскопом для того, чтобы убедиться, что клетки являются живыми перед выделением РНК. Удаляют и выбрасывают среду для культивирования клеток. Используя нож OptiCell, отрезают верхнюю мембрану, располагая клетки на нижней мембране. Мембрану, к которой прикреплены клетки, промывают 1-кратным PBS три раза. С помощью пипетки наносят 600 мкл буферного раствора RLT (содержащего β-меркаптоэтанол) на центр мембраны, к которой прикреплены клетки. Используя скребок для клеток, осторожно покрывают буфером RLT всю поверхность мембраны, а затем собирают жидкость в одном углу. Пипеткой отбирают весь объем буфера RLT и помещают в центрифужную колонку QIAshredder.
Выделение РНК: Центрифужные колонки QIAshredder центрифугируют при 14000 об./мин в течение 2 минут. Выбрасывают центрифужную колонку, сохраняя пробирку для сбора образцов и ее содержимое. В пробирку для сбора образцов добавляют 600 мкл 70% этанола и хорошо перемешивают пипетированием (теперь общий объем =1,2 мл). 600 мкл клеточного лизата переносят на миниколонку RNeasy и центрифугируют в течение 15 секунд при 14000 об./мин. Выбрасывают фильтрат, сохраняя пробирку для сбора образцов и центрифужную колонку. Оставшийся объем клеточного лизата (~600 мкл) переносят на центрифужную колонку и повторяют центрифугирование. Выбрасывают фильтрат, сохраняя пробирку для сбора образцов и центрифужную колонку. В центрифужную колонку добавляют 100 мкл буфера RW1. Центрифугируют в течение 15 секунд при 14000 об./мин для промывания колонки. Выбрасывают фильтрат и пробирку для сбора образцов. Переносят центрифужную колонку в новую пробирку для сбора образцов по 2 мл и в колонку добавляют 500 мкл буфера RPE. Центрифугируют в течение 15 секунд при 14000 об./мин. Выбрасывают фильтрат, сохраняя пробирку для сбора образцов/колонку. В колонку добавляют еще 500 мкл буфера RPE. Центрифугируют в течение 2 минут при 14000 об./мин. Переносят центрифужную колонку в пробирку для сбора образцов по 1,5 мл. Добавляют 30 мкл раствора для хранения РНК непосредственно на силикагелевую мембрану и центрифугируют в течение 1 минуты при 14000 об./мин для элюции РНК. Хранят конечную РНК при -70°C.
Анализ RNA 6000 Nano. Используя биоанализатор Agilent 2100 Bioanalyzer и анализ RNA 6000 Nano, анализируют качество РНК, выделенной из культивируемых клеток млекопитающих, лимфоцитов или тканей.
Реагенты: гелевая матрица RNA 6000 Nano, концентрированный краситель RNA 6000 Nano, маркер RNA 6000 Nano (все указанные выше реагенты содержатся в наборе для анализа RNA 6000 Nano, Agilent), маркер молекулярных масс RNA 6000, РНКаза Zap и вода, не содержащая РНКаз, от Ambion.
Оборудование/Другие материалы: установка для прайминга чипов Agilent Chip Priming Station, Agilent, чип RNA 6000, Agilent, средства для очистки электродов, пипетки P2, P10, P200 и P1000 Rainin Pipetman, стерильные, наконечники для пипеток с фильтрами без ДНКаз и РНКаз, стерильные микроцентрифужные пробирки по 1,5 мл, центрифуга типа вортекс, вихревая мешалка IKA, микроцентрифуга и нагревательный блок.
Способ: Способ представлен в руководстве к набору реагентов для анализа RNA 6000 Nano, издание ноября 2003 г., Agilent Technologies. Способ осуществляли, как указано в руководстве, со следующими модификациями: Получение геля, стр. 17, - не разделение отфильтрованного геля на аликвоты по 65 мкл каждая, хранение стока отфильтрованного геля в оригинальной микроцентрифужной пробирке и аликвоте по 65 мкл, по мере необходимости. Загрузка маркера RNA 6000 Nano, стр. 22 - добавляют 1 мкл воды, не содержащей РНКаз (вместо маркера RNA 6000 Nano), в лунку каждого образца, не содержащего образец. Помимо того, что это позволяет экономить количество используемого маркера, но также и служит отрицательным контролем, не контаминированным ни одним из реагентов, включая воду, не содержащую РНКаз. Загрузка маркера молекулярных масс и образцов, стр. 23 - образцы и маркер молекулярных масс RNA 6000 подвергают денатурации нагреванием в течение дополнительных 30 секунд (всего 2,5 минуты) при 71°C. Запуск режима работы чипа, стр. 26 - выбирают опцию "Eukaryote Total RNA Nano" в меню анализа.
Пример 10: Анализ экспрессии с использованием Affymetrix GeneChip.
Экспрессию гена анализируют с использованием патентованного Affymetrix Feline GeneChip®. Проводят обратную транскрипцию тотальной РНК в кДНК. кДНК используют для получения кРНК, которую фрагментируют и используют в качестве зондов для гибридизации GeneChip. Генетический чип промывают и измеряют сигнал гибридизации с помощью лазерного сканера Affymetrix. Затем данные о гибридизации валидируют и нормируют для дальнейшего анализа по инструкциям производителя.
Оборудование: микроцентрифуга Eppendorf, стерильные микроцентрифужные пробирки по 1,5 мл без ДНКаз и РНКаз, стерильные одноразовые полипропиленовые пробирки по 50 мл без ДНКаз и РНКаз, пипетки P1000, P200, P20, P10 и P2 Rainin Pipetman, стерильные наконечники для пипеток с фильтрами без ДНКаз и РНКаз для пипеток P1000, P200, P20, P10 и P2, и термоциклер Пельтье PTC-200.
Способ: все следующие процедуры осуществляли точно, как описано в руководстве GeneChip Expression Analysis Technical Manual (Affymetrix Copyright 1999-2003). Для синтеза первой цепи кДНК используют 5 микрограммов тотальной РНК. Для контроля температуры реакций и денатурации зондов используют термоциклер Пельтье PTC-200 или термоблок. Контроль качества осуществляют с использованием чипов RNA NanoDrop и биоанализатор BioAnalyer 2100. Для генетического чипа для кошек используют формат 100 (средний чип).
Пример 11: Экспрессия гена у кошек с гипертиреозом
Исследования осуществляют согласно представленным выше примерам с использованием кошек, страдающих легким и тяжелым гипертиреозом, для определения лежащих в основе различий экспрессии гена между этими животными и нормальными кошками. Как описано в примерах в настоящем описании, используют способы получения образцов тканей и биологических жидкостей от статистически соответствующего количества кошек, являющихся здоровыми, страдающими легким гипертиреозом и страдающих тяжелым гипертиреозом. Эти исследования включают измерение данных об экспрессии генов при сравнении нормальных кошек с больными кошками в отношении экспрессии, в том числе одного или нескольких из натрий-йодного транспортера (NIS), тиреоидной пероксидазы (TPO), рецептора тиреоидного гормона (TSHR), транспортера йода (IT; пендрина), тиреоидной оксидазы (ThOX), дейодиназы T4-тироксина (например, интратиреоидной 5'-дейодиназы типа I), монокарбоксилат-транспортера (например, монокарбоксилат-транспортера-8) и молекулы-активатора рецептора тиреоидного гормона. В конкретном варианте осуществления эти исследования включают измерение данных об экспрессии гена при сравнении нормальных кошек с больными кошками в отношении экспрессии гена NIS кошек.
Пример 12: Способы культивирования клеток для определения биоактивных компонентов рациона
Биоактивными компонентами рациона являются пищевые компоненты, которые могут изменять экспрессию одного или нескольких генов, таким образом, приводя к снижению уровней тиреоидного гормона или другим биологическим эффектам, снижающим эффекты гипертиреоза. Эти биоактивные компоненты рациона можно определять, например, приводя соответствующие клетки в культуре ткани в контакт, например, с экстрактами пищевых компонентов и измеряя уровень экспрессии одного или нескольких генов, участвующих, в том числе продукции, транспорте или утилизации тиреоидных гормонов, включая, в качестве неограничивающих примеров, натрий-йодный транспортер (NIS), тиреоидную пероксидазу (TPO), рецептор тиреоидного гормона (TSHR), транспортер йода (IT; пендрин), тиреоидную оксидазу (ThOX), дейодиназу T4-тироксина (например, интратиреоидную 5'-дейодиназу типа I), монокарбоксилат-транспортер (например, монокарбоксилат-транспортер-8) и молекулу-активатор рецептора тиреоидного гормона. В настоящем описании измеряют экспрессию гена NIS кошек и определяют три биоактивных компонента рациона с использованием представленной выше методологии экспрессии гена.
Посев новых клеточных линий
РЕАГЕНТЫ: Полные среды (конкретные для каждой отдельной клеточной линии); 70% этанол, полученный для собственного использования; 70% пропанол, полученный для собственного использования. Одна (1) стоковая аликвота клеток собаки или кошки, ATCC (или аликвота замороженных клеток последнего пассажа).
МАТЕРИАЛЫ/ОБОРУДОВАНИЕ: Ламинарный бокс; стерильные серологические пипетки, автоматический контроллер для пипеток VWR; камеры OptiCell, BioCrystal 1004-01; наконечники OptiCell, BioCrystal 1011-01; подставка OptiCell, BioCrystal 1006-01; стерильные почковидные тазики для раствора, VWR; стерильные конические пробирки емкостью 50 мл, VWR 21008-736; водяная баня температурой 37°C; перманентный маркер.
Способ: Получают соответствующий тип среды для клеточной линии, подлежащей посеву. Прогревают среды при 37°C на водяной бане в течение 25-30 минут. Стерилизуют ламинарный бокс и все реагенты/оборудование, которые будут использовать при осуществлении способа, с использованием 70% пропанола. Помечают ячейки OptiCell, обозначая клеточную линию, тип клеток, дату и номер пассажа. Сосуд, содержащий клетки, вынимают из бака с жидким азотом и быстро размораживают (время размораживания приблизительно 2 минуты) при 37°C на водяной бане. Сосуд, содержащий клетки, помещают в стакан, содержащий небольшое количество 70% этанола, для очистки внешней поверхности и удаляют любые бактерии и/или другие загрязнения. Сосуд вынимают из 70% этанола и позволяют высушиваться в ламинарном боксе. Смешивают размороженную аликвоту клеток с соответствующим количеством полной среды для заполнения ячеек OptiCell до максимальной емкости 10 мл каждая. Пример: если объем клеток составляет 1,5 мл (и клетки будут высевать в две камеры OptiCell), добавляют клетки до 18,5 мл полной среды в стерильной пробирке емкостью 50 мл. Тщательно, но осторожно, смешивают и инъецируют 10 мл смеси клетки/среда в каждую из двух камер OptiCell. Удаляют избыток воздуха из каждой камеры OptiCell. Все внешние отверстия камер OptiCell протирают 70% пропанолом и помещают в подставку OptiCell. Помещают подставку OptiCell в инкубатор в условия правильной температуры и CO2.
Культивирование клеток с использованием камер OptiCell
МАТЕРИАЛЫ: камеры OptiCell, BioCrystal 1004-01; подставка OptiCell, BioCrystal 1006-01; стерильные наконечники OptiCell, BioCrystal 1011-01; стерильные шприцы 10cc/20cc, VWR 53548- 006/53548-008; стерильные серологические пипетки, VWR; контейнер для отходов; стерильные почковидные тазики для раствора, VWR 21007-972; стерильные конические пробирки емкостью 50 мл; стерильные сосуды для криогенной заморозки емкостью 2 мл, VWR 66021-944; подставки для пробирок по 50 мл и 2 мл; полная среда; Трипсин-ЭДТА, Gibco 25200-056; 1-кратный PBS, Gibco 20012-027; 70% спирт, полученный для собственного использования; водяная баня температурой 37°C; центрифуга Beckman Coulter Allegra 25R, SN AJC01J015; автоматизированный контроллер для пипеток Accu-jet; анализатор жизнеспособности клеток Vi-Cell XR, Beckman Coulter, SN AH391.
СПОСОБ: Изменение среды: Прикрепляют новый наконечник OptiCell к стерильному шприцу и наполняют его 10 мл воздуха. Воздух вводят в камеру OptiCell и без удаления наконечника переворачивают камеру и удаляют среду. Выбрасывают среду в подходящий контейнер для сброса. Используя новый наконечник OptiCell, новый шприц наполняют 10 мл полной среды и инъецируют в камеру OptiCell. Не удаляя наконечник, переворачивают камеру и удаляют весь воздух. Камеры OptiCell хранят в подставке OptiCell в инкубаторе при 37°C в подходящих условиях CO2.
Сбор/Посев
К шприцу прикрепляют новый наконечник OptiCell и наполняют 10 мл воздуха. В камеру OptiCell инъецируют воздух. Не удаляя наконечник, переворачивают камеру OptiCell и удаляют среду. Выбрасывают среду. Используя новый наконечник OptiCell и новый шприц, в камеру OptiCell инъецируют 10 мл стерильного 1-кратного PBS (при комнатной температуре). Не удаляя наконечник, камеру переворачивают несколько раз для промывания клеток, а затем удаляют PBS. Выбрасывают PBS. Используя новый наконечник OptiCell и новый шприц, инъецируют 4 мл трипсина-ЭДТА в камеру OptiCell. Удаляют наконечник и несколько раз переворачивают камеру для покрывания клеток. Помещают камеру OptiCell обратно на подставку для хранения. Инкубируют камеры OptiCell при 37°C в течение 2-2,5 минут. Используя микроскоп, проверяют, что все клетки являются неприкрепленными. Необходимым может являться осторожное встряхивание камер для облегчения открепления клеток. Используя новый наконечник OptiCell и шприц, в камеру OptiCell инъецируют 10 мл полной среды. Не удаляя наконечник, несколько раз переворачивают камеру для нейтрализации эффектов трипсина-ЭДТА, а затем удаляют клеточную суспензию. Суспензию помещают в стерильную коническую пробирку емкостью 50 мл. После удаления всех клеток из всех камер OptiCell, удостоверяются, что объем в каждой пробирке емкостью 50 мл является равным, а затем центрифугируют при 800×g в течение 5 минут при комнатной температуре. Осторожно удаляют супернатант и ресуспендируют клеточный осадок в полной среде. Используя цитометр, определяют общее количество собранных клеток и # жизнеспособных клеток/мл. Соответствующее количество клеток высевают в новые камеры OptiCell. Необходимо отметить, что количество среды, используемой для ресуспендирования клеток на указанных выше этапах, является произвольным и будет зависеть от осуществляемого анализа.
Сбор, замораживание и субкультивирование клеток собак и кошек
МАТЕРИАЛЫ: Полные среды (конкретные для каждой клеточной линии); 70% спирт, полученный для собственного использования; трипсин-ЭДТА, Gibco 25200-056; диметилсульфоксид, Fisher; культивируемые линии клеток собак и/или кошек, ATCC; ламинарный бокс; стерильные серологические пипетки, (50 мл, 25 мл, 10 мл, 5 мл и 2 мл), VWR; автоматизированный контроллер для пипеток; стерильные конические пробирки емкостью 50 мл, VWR 21008-736; стерильные сосуды для криогенной заморозки емкостью2 мл, VWR 66021-944; стерильные культуральные флаконы по 150 см2, VWR 15705-074; водяная баня температурой 37°C; центрифуга Beckman Coulter Allegra 25R, SN AJC01J015; подставка для пробирок емкостью 50 мл; подставка для сосудов для криогенной заморозки и перманентный маркер.
СПОСОБ: Сбор клеток. Прогревают подходящую полную среду и трипсин-ЭДТА на водяной бане температурой 37°C в течение 25-30 минут перед продолжением осуществления способа. Из каждого флакона, содержащего клетки, подлежащие сбору, удаляют полную среду и помещают ее в контейнер для отходов. В каждый из флаконов добавляют 7 мл трипсина-ЭДТА. Проверяют, что трипсин-ЭДТА покрывает дно флакона (поверхность, на которую прикрепляются клетки) и помещают в инкубатор при 37°C на 2,5 минуты. Флаконы вынимают из инкубатора и исследуют под микроскопом для определения прогрессирования прикрепления. "Похлопывают" каждый флакон и повторно проверяют под микроскопом. "Похлопывание" продолжают, пока все клетки не открепятся от дна флакона. Из каждого флакона удаляют трипсин-EDTA/клеточную суспензию и помещают в конические пробирки емкостью 50 мл. Пробирки емкостью 50 мл наполняют до полного объема полной средой для нейтрализации эффектов трипсин-ЭДТА. Центрифугируют каждую из пробирок емкостью 50 мл при 800×g в течение 5 минут при комнатной температуре. Удаляют супернатант и ресуспендируют клеточный осадок в 48 мл полной среды. Ресуспендируют только те клетки, которые будут использовать для субкультивирования в полной среде. Для тех клеток, которые будут замораживать и хранить для дальнейшего использования, следовали способу "Замораживание".
Замораживание: Получают 5% диметилсульфоксид (DMSO) в растворе полной среды (для большинства клеточных линий необходим 5% раствор, но важно проверять индивидуальные требования для каждой клеточной линии). Ресуспендируют клеточные осадки, подлежащие замораживанию (из этапа 1.10), в 2 мл 5% DMSO в растворе среды. Разделяют смесь DMSO/клетки на аликвоты по 1,5 мл в сосудах для криогенной заморозки емкостью 2 мл. Эти аликвоты помещают в морозильную камеру Styrofoam® при -70°C для замораживания в течение ночи. На следующее утро аликвоты вынимают из морозильной камеры -70°C и переносят в жидкий азот.
Субкультивирование: Определяют соответствующее соотношение субкультивирования клеточной линии и отмечают правильное количество флаконов. (Этот протокол создан для соотношения субкультивирования 1:8, и все объемы отражают это соотношение). В каждый из указанных выше флаконов добавляют 14 мл полной среды, сохраняя их в вертикальном положении. В каждый из флаконов добавляют 6 мл клеточной суспензии (этап 1.10), одновременно все еще сохраняя их в вертикальном положении. Клеточную суспензию не "капают" во флакон, вместо этого суспензии позволяют стекать по стенке флакона. Убеждаются, что смесь среда/клетки полностью покрывает дно флакона. Не допускают попадания среды на горлышко флакона. Флаконы помещают в инкубатор с температурой 37°C при подходящих условиях. Соответствующие пометки для флаконов с культурами клеток будут включать следующую информацию: клеточная линия, тип клеток, дата, количество пассажей, среда и требования к CO2. Соответствующие пометки для сосудов для криогенной заморозки будут включать следующую идентификационную информацию: клеточная линия, тип клеток, дата, количество пассажей и инициалы сотрудника.
Солюбилизация и экстракция ингредиентов для тестирования в культурах клеток
Представленные ниже способы представляют собой иллюстративные подходы для солюбилизации ингредиентов при конкретных концентрациях для тестирования в клеточных культурах. В основном, ингредиенты получали в виде сухих химических веществ, жидкостей или гранул. Активный компонент каждого ингредиента экстрагируют с использованием конкретного растворителя. Используемые в способе растворители могут включать, например, Millipore H2O, забуференную Millipore H2O, DMSO, 0,1% DMSO (в Millipore H2O), метанол и этанол. Сухие химические вещества добавляют непосредственно в конкретный растворитель и исследуют визуально, чтобы убедиться, что они полностью растворились в желаемой стоковой концентрации. Жидкости с известной концентрацией добавляют непосредственно в конкретный растворитель для получения конечной желаемой стоковой концентрации. Гранулы измельчают с использованием кофемолки, обрабатывают ультразвуком (уровень: 008 ватт) и фильтруют (0,45 мкм) до желаемой стоковой концентрации.
МАТЕРИАЛЫ/ОБОРУДОВАНИЕ: центрифуга типа вортекс; весы AT200 Mettler; pH-метр AR15 Accumet; соникатор VirSonic 100; кофемолка (Krups); стерильный шприц 20 мл (Norm-Ject); VWR 53548-008; стерильные наконечники для шприца, 18G, игла 1S'', VWR BD305196; фильтр для шприца 25 мм Acrodisc (w/0,45 мкм HT Tuffryn Membrane), VWR 28144-007; центрифужная пробирка емкостью 50 мл (Corning), Fisher 06-443-19; пипетки P10, P20, P100, P200, P1000 Rainin; стерильные наконечники для пипеток с фильтром, USA Scientific.
РАСТВОРЫ: Millipore H2O, Milli-Q Syntesis A 10; DMSO, EMD MX1458-6; 0,1% DMSO (в Millipore H2O); 1M буферный раствор HEPES, Gibco 15630-080; забуференная Millipore H2O (pH:7); метанол (99,93%, категории ВЭЖХ), Sigma-Aldrich 439193; этанол (200 Proof), Sigma-Aldrich E7023; Примечание: чистую H2O необходимо забуферить до pH 7 с использованием 1M буферного раствора HEPES.
СПОСОБ:
Тестирование растворимости: Сухое химическое вещество. Центрифужную пробирку емкостью 50 мл помещают на весы Mettler. Определяют массу тары при определении массы. Для взвешивания центрифужной пробирки на первом этапе добавляют небольшое количество сухого химического вещества, подлежащего тестированию, и помещают пробирку с крышкой обратно на весы. Записывают массу добавленного сухого химического вещества. Добавляют конкретный растворитель для получения желаемой стоковой концентрации (мг/мл). Перемешивают на центрифуге типа вортекс и визуально осматривают на предмет полного растворения.
Тестирование растворимости: Жидкий ингредиент. В центрифужную пробирку емкостью 50 мл добавляют желаемое количество жидкого ингредиента с использованием необходимой пипетки Rainin. Для получения желаемой стоковой концентрации добавляют растворитель (C1V1=C2V2). Тщательно перемешивают на центрифуге типа вортекс и проверяют однородность раствора.
Тестирование растворимости: Гранулы. Тщательно перемалывают любое количество гранул, подлежащих тестированию, в кофемолке. Проверяют наличие любых больших частиц и снова перемалывают, при необходимости. Помещают центрифужную пробирку емкостью 50 мл с крышкой на весы Mettler. Определяют массу тары при определении массы. В центрифужную пробирку, взвешенную на втором этапе, добавляют желаемое количество перемолотого ингредиента и перемещают пробирку с крышкой обратно на весы. Записывают массу ингредиента. Добавляют конкретный растворитель для получения желаемой стоковой концентрации (мг/мл). Обрабатывают ультразвуком в течение 30-60 сек в режиме 008 Ватт. Фильтруют обработанный ультразвуком раствор с использованием шприца 20 мл и фильтра 0,45 мкм в новую центрифужную пробирку емкостью 50 мл. Если обработанный ультразвуком раствор не фильтруется через фильтр 0,4 5 мкм, используют ультрацентрифугу для осаждения меньших частиц ингредиента и сливают супернатант.
Результаты
Используя описываемых выше способы, определяют три пищевых ингредиента, содержащие биоактивные компоненты рациона. Они включают томатный жмых, растительную смесь и пшено. Зонды, используемые в анализе, находящиеся на используемых генетических чипах, включают набор 25-мерных олигонуклеотидов, полученных из нуклеотидной последовательности SEQ ID NO: 1. Изменения уровней экспрессии гена NIS кошек, после подвергания клеток в культуре ткани воздействию экстрактов каждого из них, представлены в следующей таблице:
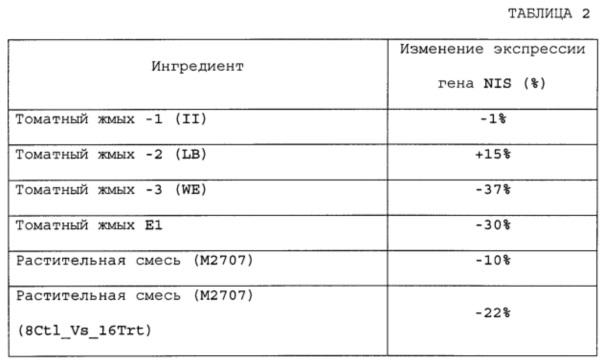
|
Данные в таблице 2 свидетельствуют о том, что способы, представленные в настоящем описании, можно использовать для определения биоактивных компонентов рациона, которые могут снижать экспрессию гена кошки и, таким образом, будут применимыми для лечения гипертиреоза у кошек. Эти данные также демонстрируют вариабельность композиций конкретных пищевых ингредиентов и их экстрактов. Несмотря на эту вариабельность, способы экстракции и анализа, представленные в настоящем описании, можно использовать, например, для "анализа" указанного ингредиента на количество и концентрацию биоактивного компонента рациона. Используя эти данные, можно составлять пищевые композиции для кошек, включающие количество пищевого ингредиента, представляющее эффективное количество биоактивного компонента рациона. Хотя для пищевых композиций для домашних животных, представленных в настоящем описании, описывают различные уровни биоактивных компонентов рациона, точное включенное количество предпочтительно будет являться количествами, представленными для иллюстративных целей; точное количество будет являться терапевтически эффективным количеством, определяемым способами, представленными в настоящем описании.
В других аспектах в описываемых выше способах и реагентах можно использовать более крупномасштабную экстракцию, фракционирование, выделение и очистку пищевых ингредиентов, чтобы сделать возможным определение молекулярных веществ, ответственных за наблюдаемую активность. Затем эти определенные соединения можно более точно включать в пищевую композицию для домашних животных или пищевую добавку, подлежащую использованию для лечения гипертиреоза у кошек.
В других дополнительных аспектах терапевтически эффективное количество пищевых ингредиентов, содержащих биоактивные компоненты рациона или выделенные и очищенные средства per se, составляют в пищевые композиции для домашних животных, содержащие низкие уровни йодидных составов, для получения улучшенного корма с дополнительной защитой от внешнего потребления йода животным, которому проводят лечение от гипертиреоза.
В другом аспекте терапевтически эффективное количество пищевых ингредиентов, содержащих биоактивные компоненты рациона или выделенные и очищенные средства per se, составляют в пищевые композиции для домашних животных, созданные для лечения заболевания или состояния, иного, чем гипертиреоз, для обеспечения рациона, применимого для лечения гипертиреоза, а также второго определенного заболевания или состояния.
Еще в одном дополнительном аспекте изобретение относится к пищевой композиции для домашних животных или пищевой добавке, содержащей, по меньшей мере, добавку, и в определенных вариантах осуществления количества нескольких синергических биоактивных компонентов рациона или нескольких выделенных и очищенных средств per se, для получения пищевой композиции для домашних животных или пищевой добавки для домашних животных, применимых для снижения продукции тиреоидного гормона и/или для лечения гипертиреоза.
Иллюстративные примеры таких пищевых композиций для кошек представлены ниже; хотя указывают количества биоактивных компонентов рациона, эти уровни можно и нужно корректировать для получения требуемых или "стандартизированных" единиц или уровней биологической активности с использованием указанных выше способов для измерения уровня биологически активных материалов.
Предполагают, что изобретение, представленное в настоящем описании, не ограничено конкретной описываемой методологией, протоколами и реагентами, т.к. их можно варьировать. Также следует понимать, что терминология, используемая в настоящем описании, предназначена для описания исключительно конкретных вариантов осуществления, и не предназначена для ограничения объема настоящего изобретения каким-либо образом.
В описании представлены типичные, иллюстративные и предпочтительные варианты осуществления изобретения и, хотя используют конкретные термины, их используют в общем и описательном смысле, а не в целях ограничения объема изобретения, приведенного в формуле изобретения. С учетом изложенных выше идей возможно множество модификаций и вариантов изобретения. Таким образом, следует понимать, что в объеме формулы изобретения можно проводить практическое осуществление, иное, чем описано конкретно.


