НОВЫЕ ПРОЛЕКАРСТВА НУКЛЕИНОВЫХ КИСЛОТ И СПОСОБЫ ИХ ПРИМЕНЕНИЯ
Вид РИД
Изобретение
ПЕРЕКРЕСТНЫЕ ССЫЛКИ
Данная заявка испрашивает приоритет по промежуточной заявке США №61/223,369, поданной 6 июля 2009 г., и промежуточной заявке США №61/242,722, поданной 15 сентября 2009 г., которые включены в данное описание путем отсылки в полном объеме.
ОБЛАСТЬ ТЕХНИКИ
В данном описании описаны пролекарства нуклеиновых кислот и пролекарства нуклеиновых кислот, содержащие хиральные фосфорсодержащие фрагменты, а также способы их получения и применения.
УРОВЕНЬ ТЕХНИКИ
Олигонуклеотиды пригодны для применения в терапевтической, диагностической, исследовательской областях, а также в области новых и наноматериалов, Применение природных последовательностей ДНК или РНК ограничено, например, уровнем их устойчивости к действию нуклеаз. Дополнительно, исследования in vitro показали, что на свойства антисмысловых нуклеотидов, такие как сродство связывания, последовательность-специфичное связывание с комплементарной РНК, устойчивость к действию нуклеаз, влияет конфигурация атомов фосфора. Таким образом, существует потребность в пролекарствах стереоопределенных олигонуклеотидов, обеспечивающих дополнительную стабильность молекулам олигонуклеотидов во множестве областей применения in vitro и in vivo. Пролекарства стереоопределенных олигонуклеотидов, которые содержат нуклеиновые кислоты с модифицированным атомом фосфора и способы их применения, описаны в данном описании.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В одном из вариантов предлагается пролекарство хиральной нуклеиновой кислоты.
В одном из вариантов предлагается пролекарство нуклеиновой кислоты следующей структуры:
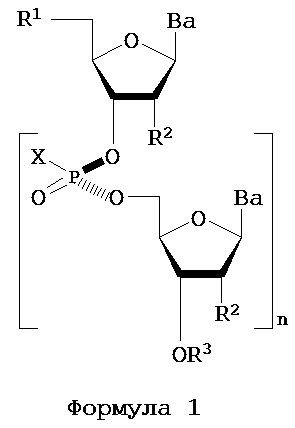
где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -Р(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ba, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере в одном случае Х представляет собой -OCH2CH2S-S(O)2R10, -OCH2CH2S-SCH2CH2OH, -OCH2CH2CO2H,  ,
,  ,
,
|
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил;
Z представляет собой S или О;
q равно 0, 1 или 3;
w равно 1, 2, 3, 4, 5 или 6;
R15 и R16 независимо представляют собой водород или метил;
R17 выбран из алкила, арила или CH2CH=CH2;
R18 выбран из N(CH3)2, 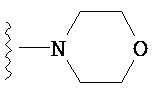 ,
, 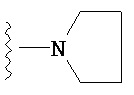 ,
, 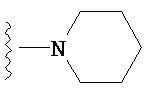 ,
, 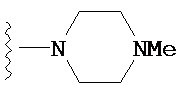 и
и 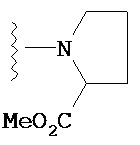 ; и
; и
n равно целому числу от 1 до приблизительно 200.
В другом варианте предлагается пролекарство нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ba, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере в одном случае Х представляет собой  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 или
или  ;
;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил; и n равно целому числу от 1 до приблизительно 200.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где диастереомерная чистота каждого Х-фосфонатного фрагмента соединения Формулы 1 составляет более 98% по данным 31P ЯМР спектроскопии или обращенно-фазовой ВЭЖХ.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где каждый Х-фосфонатный фрагмент находится в Rp конфигурации.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где каждый Х-фосфонатный фрагмент находится в SP конфигурации. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где каждый Х-фосфонат независимо находится в RP конфигурации или Sp конфигурации.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где R10 представляет собой метил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где R11 представляет собой метил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где R12 представляет собой метил.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  и
и  . В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  и
и  . В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  и
и  .
.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где каждый фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  и
и  .
.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где каждый фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из -OCH2CH2S-S(O)2R10, -OCH2CH2S-SCH2CH2OH, -OCH2CH2CO2H,  ,
,  ,
,  ,
, 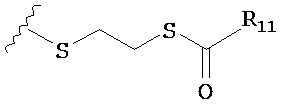 ,
, 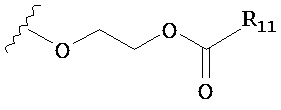 ,
, 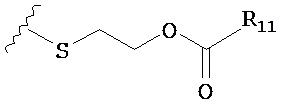 ,
, 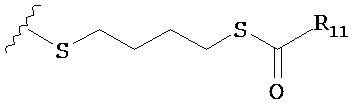 ,
, 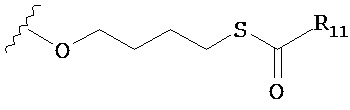 ,
, 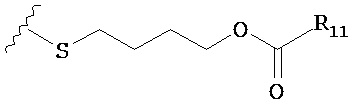 ,
, 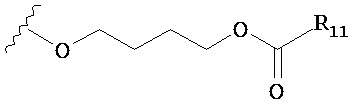 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
, 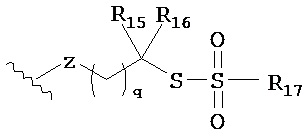 или
или
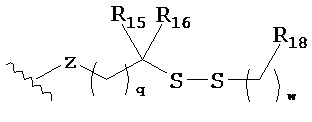 ;
;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил;
Z представляет собой S или О;
q равно 0, 1 или 3;
w равно 1, 2, 3, 4, 5 или 6;
R15 и R16 независимо представляют собой водород или метил;
R17 выбран из алкила, арила или CH2CH=СН2; и
R18 выбран из N(СН3)2,  ,
,  ,
,  ,
,  и
и  .
.
В одном из вариантов предлагается пролекарство нуклеиновой кислоты следующей структуры:
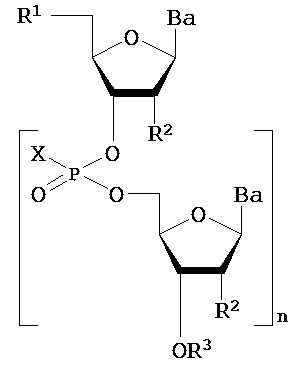
где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -НР(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере один Х представляет собой  ,
,
 ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  или
или  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой; и n равно целому числу от 1 до приблизительно 200.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где R10 представляет собой метил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где R11 представляет собой метил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где R12 представляет собой метил
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  и
и
 ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  и
и
 ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В дополнительном варианте предлагается пролекарство нуклеиновой кислоты, где каждый фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В одном из вариантов предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
где по меньшей мере один фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 и
и  ;
;
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой; и n равно целому числу от 1 до приблизительно 200;
где способ, применяемый для синтеза пролекарства нуклеиновой кислоты, включает следующие стадии: (1) реакцию молекулы, содержащей ахиральный Н-фосфонатный фрагмент, и нуклеозида, содержащего 5'-ОН фрагмент, с образованием конденсированного промежуточного соединения; и (2) превращение конденсированного промежуточного соединения в пролекарство нуклеиновой кислоты, содержащее хиральный Х-фосфонатный фрагмент.
В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где диастереомерная чистота каждого Х-фосфонатного фрагмента соединения Формулы 1 составляет более 98% по данным 3l? ЯМР спектроскопии или обращенно-фазовой ВЭЖХ. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где каждый Х-фосфонатный фрагмент находится в RP конфигурации. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где каждый Х-фосфонатный фрагмент находится в SP конфигурации. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где каждый Х-фосфонат независимо находится в RP конфигурации или Sp конфигурации.
В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где в каждом случае Х независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где R10 представляет собой метил. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где R11 представляет собой метил. В другом варианте предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты, структура которого представлена Формулой 1, где R12 представляет собой метил.
В одном из вариантов предлагается способ лечения заболевания, связанного с регуляцией вверх РНКазы L путем введения терапевтического количества пролекарства хиральной нуклеиновой кислоты. В другом варианте предлагается способ лечения заболевания, связанного с регуляцией вверх РНКазы L, где заболевание представляет собой синдром хронической усталости. В другом варианте предлагается способ лечения заболевания, связанного с регуляцией вниз РНКазы L, путем введения терапевтического количества пролекарства хиральной нуклеиновой кислоты. В другом варианте предлагается способ лечения заболевания, сопровождающегося регуляцией вниз РНКазы L, где заболевание представляет собой рак. В другом варианте, рак выбран из рака предстательной железы, ободочной и прямой кишки и поджелудочной железы. В одном из вариантов, рак с регуляцией вниз РНКазы L представляет собой рак поджелудочной железы. В другом варианте рак с регуляцией вниз РНКазы L представляет собой рак предстательной железы. Еще в одном варианте, рак с регуляцией вниз РНКазы L представляет собой рак ободочной и прямой кишки.
В одном из вариантов предлагается способ лечения рака, который включает введение терапевтического количества пролекарства нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере один фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой; и n равно целому числу от 1 до приблизительно 200;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
где способ, применяемый для синтеза пролекарства нуклеиновой кислоты, включает следующие стадии: (1) реакцию молекулы, содержащей ахиральный Н-фосфонатный фрагмент, и нуклеозида, содержащего 5'-ОН фрагмент, с образованием конденсированного промежуточного соединения; и (2) превращение конденсированного промежуточного соединения в пролекарство нуклеиновой кислоты, содержащее хиральный Х-фосфонатный фрагмент.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где в каждом случае Х независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где R10 представляет собой метил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где R11 представляет собой метил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где R12 представляет собой метил.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где диастереомерная чистота каждого Х-фосфонатного фрагмента соединения Формулы 1 составляет более 98% по данным 31Р ЯМР спектроскопии или обращенно-фазовой ВЭЖХ. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где каждый Х-фосфонатный фрагмент находится в RP конфигурации. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где каждый Х-фосфонатный фрагмент находится в SP конфигурации. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где каждый Х-фосфонат независимо находится в RP конфигурации или Sp конфигурации.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения Формулы 1, где рак представляет собой рак поджелудочной железы.
В одном из вариантов предлагается пролекарство нуклеиновой кислоты следующей структуры:
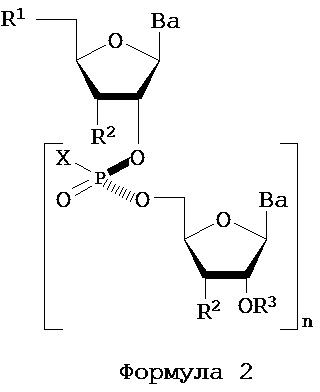
где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re)2, -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -НР(O)(Re);
в каждом случае Re представляет собой независимо водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере в одном случае Х представляет собой  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ;
;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил; и
n равно целому числу от 1 до приблизительно 200.
В одном из вариантов предлагается пролекарство нуклеиновой кислоты Формулы 2, где диастереомерная чистота каждого Х-фосфонатного фрагмента соединения Формулы 2 составляет более 98% по данным 31Р ЯМР спектроскопии или обращенно-фазовой ВЭЖХ. В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где каждый Х-фосфонатный фрагмент находится в RP конфигурации. В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где каждый Х-фосфонатный фрагмент находится в SP конфигурации. В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где каждый Х-фосфонат независимо находится в RP конфигурации или Sp конфигурации.
В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где R10 представляет собой метил. В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где R11 представляет собой метил. В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где R12 представляет собой метил.
В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
В другом варианте предлагается пролекарство нуклеиновой кислоты Формулы 2, где каждый фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  .
.
В одном из вариантов предлагается фармацевтическая композиция, содержащая пролекарство нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
где по меньшей мере один фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой; и n равно целому числу от 1 до приблизительно 200;
где способ, применяемый для синтеза пролекарства нуклеиновой кислоты, включает следующие стадии: (1) реакцию молекулы, содержащей ахиральный Н-фосфонатный фрагмент, и нуклеозида, содержащего 5'-ОН фрагмент, с образованием конденсированного промежуточного соединения; и (2) превращение конденсированного промежуточного соединения в пролекарство нуклеиновой кислоты, содержащее хиральный Х-фосфонатный фрагмент.
В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где диастереомерная чистота каждого X-фосфонатного фрагмента соединения Формулы 2 составляет более 98% по данным 31P ЯМР спектроскопии или обращенно-фазовой ВЭЖХ. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где каждый Х-фосфонатный фрагмент находится в RP конфигурации. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где каждый Х-фосфонатный фрагмент находится в SP конфигурации. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где каждый Х-фосфонат независимо находится в RP конфигурации или Sp конфигурации.
В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где в каждом случае Х независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где R10 представляет собой метил. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где R11 представляет собой метил. В другом варианте предлагается фармацевтическая композиция, содержащая соединение Формулы 2, где R12 представляет собой метил.
В одном из вариантов предлагается способ лечения рака, который включает введение терапевтического количества пролекарства нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NR1, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере один фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой; и n равно целому числу от 1 до приблизительно 200;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
где способ, применяемый для синтеза пролекарства нуклеиновой кислоты, включает следующие стадии: (1) реакцию молекулы, содержащей ахиральный Н-фосфонатный фрагмент, и нуклеозида, содержащего 5'-ОН фрагмент, с образованием конденсированного промежуточного соединения; и (2) превращение конденсированного промежуточного соединения в пролекарство нуклеиновой кислоты, содержащее хиральный Х-фосфонатный фрагмент.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где по меньшей мере 25% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где по меньшей мере 50% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где по меньшей мере 90% фрагментов Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где в каждом случае Х независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где R10 представляет собой метил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где R11 представляет собой метил. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где R12 представляет собой метил
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где диастереомерная чистота каждого Х-фосфонатного фрагмента соединения Формулы 2 составляет более 98% по данным 31P ЯМР спектроскопии или обращенно-фазовой ВЭЖХ.
В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где каждый Х-фосфонатный фрагмент находится в RP конфигурации. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где каждый Х-фосфонатный фрагмент находится в SP конфигурации. В другом варианте предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где каждый Х-фосфонат независимо находится в RP конфигурации или Sp конфигурации.
В одном из вариантов предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где рак представляет собой рак поджелудочной железы.
В одном из вариантов предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где соединение представлено следующей формулой:
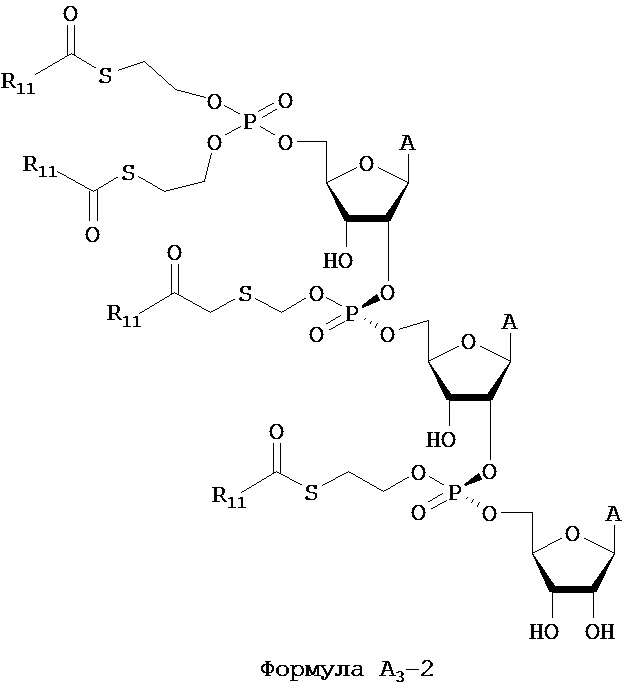
где каждый А представляет собой аденин, и каждый R11 независимо выбран из алкила, арила, гетероарила, гетероциклила и циклоалкила. В дополнительном варианте предлагается способ лечения рака поджелудочной железы, который включает введение терапевтического количества соединения Формулы А3-2.
В одном из вариантов предлагается способ лечения рака, который включает введение терапевтического количества соединения, структура которого представлена Формулой 2, где соединение представлено следующей формулой:
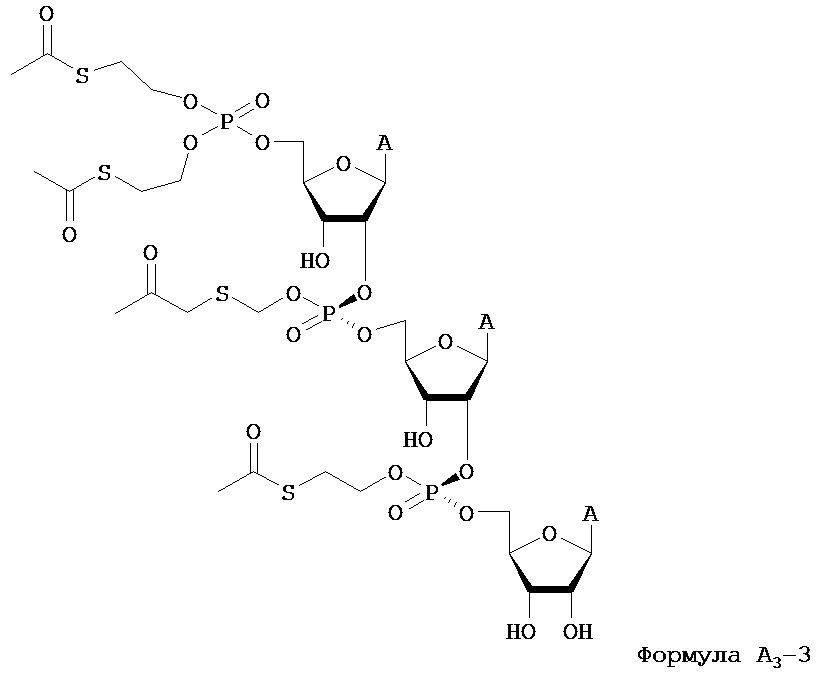
В дополнительном варианте предлагается способ лечения рака поджелудочной железы, включающий введение терапевтического количества соединения Формулы A3-3.
В одном из вариантов предлагается соединение или его фармацевтически приемлемая соль следующей формулы:
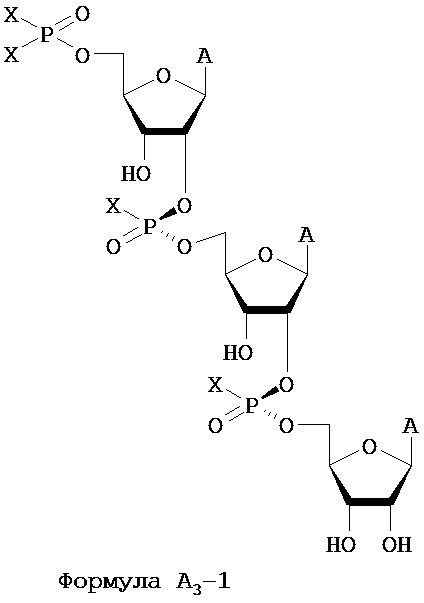
где каждый А представляет собой аденин; и по меньшей мере один фрагмент Х представляет собой
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  или
или  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается соединение или его фармацевтически приемлемая соль, представленное структурой Формулы А3-1, где по меньшей мере два фрагмента Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается соединение или его фармацевтически приемлемая соль, представленное структурой Формулы А3-1, где по меньшей мере три фрагмента Х в пролекарстве нуклеиновой кислоты независимо выбраны из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается соединение или его фармацевтически приемлемая соль, представленное структурой Формулы А3-1, где каждый фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  и
и  ,
,
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода; R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил; и R12 представляет собой водород или алкил.
В другом варианте предлагается соединение или его фармацевтически приемлемая соль, представленное структурой Формулы А3-1, где соединение представлено следующей формулой:

Все публикации и патентные заявки, раскрытые в описании данной заявки, включены в данное описание путем отсылки во всем объеме, в такой же степени, как если бы каждая отдельная публикация или патентная заявка была конкретно и отдельно указана как включенная путем ссылки.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Новые признаки изобретения конкретно определены в прилагаемой формуле изобретения. Лучшее понимание признаков и преимуществ данного изобретения будет достигнуто со ссылкой на следующее подробное описание, где приведены иллюстративные варианты, в которых применяются принципы изобретения, и сопутствующие фигуры.
На фиг.1 представлен характерный профиль, полученный методом аналитической ВЭЖХ для соединения 64 и GSH.
На фиг.2 представлен характерный профиль, полученный методом ВЭЖХ для соединения 64а, глутатионового аддукта и конечного продукта после высвобождения из про-фрагмента.
На фиг.3 представлен график превращения во времени для соединений 64а и 64b.
На фиг.4 представлено протекание реакции во времени по данным ЖХ-МС для высвобождения соединения 64а из пролекарства при содействии глутатиона.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Заголовки разделов приведены в данном описании только для целей систематизации материала и не должны интерпретироваться как ограничивающие описанный предмет. Все документы или части документов, процитированные в заявке, в том числе, не ограничиваясь ими, патенты, патентные заявки, статьи, книги, руководства и монографии, явно включены путем ссылки в полном объеме для любой цели.
Если не указано иное, следующие термины, используемые в данной заявке, включая описание и формулу изобретения, имеют определения, приведенные ниже. Следует отметить, что в описании и прилагаемой формуле изобретения, формы единственного числа "a" "an" и "the" включают множественное число, если из контекста явно не следует противоположное. Если не указано иное, применяются традиционные методы масс-спектроскопии, ЯМР, ВЭЖХ, химии белков, биохимии, техники рекомбинации ДНК и фармакологические методы. В данной заявке применение слов "или" или "и" обозначает "и/или", если не указано иное. Кроме того, применение термина "в том числе", а также других форм, таких как "включают", "включает" и "включены" не является ограничивающим.
Некоторые химические термины
Если не указано иное, применение общих химических терминов, таких как, не ограничиваясь ими, "алкил", "амин", "арил" обозначает незамещенный радикал.
В данном описании C1-Cx включает C1-С2, С1-С3.. С1-Сх. Только для примера, группа, обозначенная "C1-C4" показывает, что фрагмент содержит от 1 до 4 атомов углерода, т.е. группы, содержащие 1 атом углерода, 2 атома углерода, 3 атома углерода или 4 атома углерода, а также интервалы C1-C2 и C1-С3. Таким образом, только для примера, "C1-C4 алкил" показывает, что алкильная группа содержит от 1 до 4 атомов углерода, т.е. алкильная группа выбрана из метила, этила, пропила, изо-пропила, н-бутила, изо-бутила, втор-бутила и трет-бутила. Если указание на нее содержится в данном описании, численный интервал, например, "1-10" обозначает каждое целое число в указанном интервале; например, "1-10 атомов углерода" означает, что группа может содержать 1 атом углерода, 2 атома углерода, 3 атома углерода, 4 атома углерода, 5 атомов углерода, 6 атомов углерода, 7 атомов углерода, 8 атомов углерода, 9 атомов углерода или 10 атомов углерода.
Термины "гетероатом" или "гетеро" в данном описании отдельно или в комбинации, обозначают атом, который не является атомом углерода или водорода. Гетероатомы могут быть независимо выбраны из кислорода, азота, серы, фосфора, кремния, селена и олова, но не ограничиваются ими. В вариантах, где присутствует два или более гетероатомов, два или более гетероатомов могут быть одинаковыми, или некоторые или все из двух или более гетероатомов могут отличаться от других.
Термин "алкил" в данном описании, отдельно или в комбинации, обозначает неразветвленный или разветвленный насыщенный углеводородный монорадикал, содержащий от 1 до приблизительно 10 атомов углерода или от 1 до 6 атомов углерода. Примеры включают, не ограничиваясь ими, метил, этил, н-пропил, изопропил, 2-метил-1-пропил, 2-метил-2-пропил, 2-метил-1-бутил, 3-метил-1-бутил, 2-метил-3-бутил, 2,2-диметил-1-пропил, 2-метил-1-пентил, 3-метил-1-пентил, 4-метил-1-пентил, 2-метил-2-пентил, 3-метил-2-пентил, 4-метил-2-пентил, 2,2-диметил-1-бутил, 3,3-диметил-1-бутил, 2-этил-1-бутил, н-бутил, изобутил, втор-бутил, трет-бутил, «-пентил, изопентил, неопентил, трет-амил и гексил, а также более длинные алкильные группы, такие как гептил, октил, и т.п. При упоминании в данном описании, численный интервал, например, "С1-С6 алкил" или "C1-6 алкил", обозначает, что алкильная группа может состоять из 1 атома углерода, 2 атомов углерода, 3 атомов углерода, 4 атомов углерода, 5 атомов углерода или 6 атомов углерода. В одном из вариантов "алкил" является замещенным. Если не указано иное, "алкил" является незамещенным.
Термин "алкенил" в данном описании, отдельно или в комбинации, обозначает неразветвленный или разветвленный углеводородный монорадикал, содержащий одну или больше углерод-углеродных двойных связей и содержащий от 2 до приблизительно 10 атомов углерода или от 2 до приблизительно 6 атомов углерода. Группа может находиться в цис- или транс-конформации относительно двойной связи(ей), и предусматривается, что она включает оба изомера. Примеры включают, не ограничиваясь ими, этенил (-СН=CH2), 1-пропенил (-CH2CH=СН2), изопропенил [-C(CH3)=CH2], бутенил, 1,3-бутадиенил, и т.п. При упоминании в данном описании, численный интервал, например, "C2-C6 алкенил" или "С2-6 алкенил", обозначает, что алкенильная группа может состоять из 2 атомов углерода, 3 атомов углерода, 4 атомов углерода, 5 атомов углерода или 6 атомов углерода. В одном из вариантов "алкенил" является замещенным. Если не указано иное, "алкенил" является незамещенным.
Термин "алкинил" в данном описании, отдельно или в комбинации, обозначает неразветвленный или разветвленный углеводородный монорадикал, содержащий одну или больше углерод-углеродных тройных связей и содержащий от 2 до приблизительно 10 атомов углерода или от 2 до приблизительно 6 атомов углерода. Примеры включают, не ограничиваясь ими, этинил, 2-пропинил, 2-бутинил, 1,3-бутадиинил, и т.п. При упоминании в данном описании, численный интервал, такой как "С2-С6 алкинил" или "С2-6 алкинил", обозначает, что алкинильная группа может состоять из 2 атомов углерода, 3 атомов углерода, 4 атомов углерода, 5 атомов углерода или 6 атомов углерода. В одном из вариантов "алкинил" является замещенным. Если не указано иное, "алкинил" является незамещенным.
Термины "гетероалкил", "гетероалкенил" и "гетероалкинил" в данном описании, отдельно или в комбинации, обозначают алкильные, алкенильные и алкинильные структуры, соответственно, как описано выше, где один или больше из атомов углерода в основной цепи (и, при необходимости, любые связанные с ними атомы водорода) независимо заменены на гетероатом (т.е. атом, не являющийся атомом углерода, например, не ограничиваясь ими, кислород, азот, сера, кремний, фосфор, олово или их комбинация) или гетероатомную группу, такую как, не ограничиваясь ими, -O-O-, -S-S-, -O-S-, -S-O-, =N-N=, -N=N-, -N=N-NH-, -P(O)2, -O-P(O)2, -P(O)2-O-, -S(O)-, -S(O)2-, -SnH2-, и т.п.
Термины "галогеналкил", "галогеналкенил" и "галогеналкинил" в данном описании, отдельно или в комбинации, обозначают алкильные, алкенильные и алкинильные группы, соответственно, как определено выше, где один или больше атомов водорода заменены на атомы фтора, хлора, брома или йода или их комбинации. В некоторых вариантах два или более атомов водорода могут быть заменены одинаковыми атомами галогена (например, дифторметил); в других вариантах два или более атомов водорода могут быть заменены разными атомами галогена (например, 1-хлор-1-фтор-1-йодэтил). Неограничивающими примерами галогеналкильных групп являются фторметил, хлорметил и бромэтил.
Неограничивающим примером галогеналкенильной группы является бромэтенил. Неограничивающим примером галогеналкинильной группы является хлорэтинил.
Термин "углеродная цепь" в данном описании, отдельно или в комбинации, обозначает любую алкильную, алкенильную, алкинильную, гетероалкильную, гетероалкенильную или гетероалкинильную группу, которая является линейной, циклической или любой их комбинацией. Если цепь является частью линкера, и такой линкер включает одно или больше колец как часть скелета ядра, для целей вычисления длины цепи, "цепь" включает только те атомы углерода, которые составляют нижнюю часть или верхнюю часть данного кольца, но не обе, и где верхняя и нижняя части кольца(колец) не равны по длине, то более короткое расстояние будет использоваться для определения длины цепи. Если цепь содержит гетероатомы как часть скелета, такие атомы не считаются частью длины углеродной цепи.
Термин "циклоалкил" в данном описании, отдельно или в комбинации, обозначает монорадикал насыщенного углеводородного кольца, содержащий от 3 до приблизительно 15 атомов углерода в кольце или от 3 до приблизительно 10 атомов углерода в кольце, хотя может включать дополнительные неуглеродные атомы кольца в качестве заместителей (например, метилциклопропил). При упоминании в данном описании, численный интервал, например, "С3-С6 циклоалкил " или "С3-6 циклоалкил", обозначает, что циклоалкильная группа может состоять из 3 атомов углерода, 4 атомов углерода, 5 атомов углерода или 6 атомов углерода, т.е. представляет собой циклопропил, циклобутил, циклопентил или циклогептил, хотя данное определение также охватывает употребление термина "циклоалкил", где численный интервал не обозначен. Термин включает конденсированные, неконденсированные, соединенные мостиком и спирорадикалы. Конденсированный циклоалкил может содержать от 2 до 4 конденсированных колец, где кольцо, через которое осуществляется присоединение, представляет собой циклоалкильное кольцо, и другие отдельные кольца могут быть алициклическими, гетероциклическими, ароматическими, гетероароматическими или любой их комбинацией. Примеры включают, не ограничиваясь ими, циклопропил, циклопентил, циклогексил, декалинил и бицикло[2,2,1]гептильную и адамантильную системы колец. Иллюстративные примеры включают, не ограничиваясь ими, следующие фрагменты:
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
, 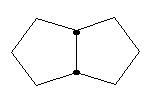 ,
, 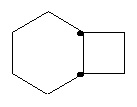 ,
, 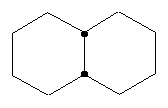 ,
, 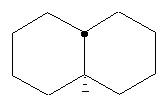 ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  и т.п.
и т.п.
В одном из вариантов "циклоалкил" является замещенным. Если не указано иное, the "циклоалкил" является незамещенным.
Термины "неароматический гетероциклил" и "гетероалициклил" в данном описании, отдельно или в комбинации, обозначают насыщенные, частично ненасыщенные или полностью ненасыщенные монорадикалы неароматического кольца, содержащего от 3 до приблизительно 12 атомов в кольце, где один или больше из атомов кольца представляют собой атом, не являющийся атомом углерода, независимо выбранный из кислорода, азота, серы, фосфора, кремния, селена и олова, не ограничиваясь указанными атомами. В вариантах, где два или более гетероатомов присутствуют в кольце, два или более гетероатомов могут быть одинаковыми или разными. Термины включают конденсированные, неконденсированные, соединенные мостиком и спирорадикалы. Конденсированный неароматических гетероциклический радикал может содержать от 2 до 4 конденсированных колец, где кольцо, через которое осуществляется присоединение, является неароматическим гетероциклом, и другие отдельные кольца могут быть алициклическими, гетероциклическими, ароматическими, гетероароматическими, или любой их комбинацией. Системы конденсированных колец могут быть конденсированными поперек одинарной связи или двойной связи, а также поперек связей, которые представляют собой связи углерод-угдерод, углерод-гетероатом или гетероатом-гетероатом. Термины также включают радикалы, содержащие от 3 до приблизительно 12 скелетных атомов в кольце, а также содержащие от 3 до приблизительно 10 скелетных атомов в кольце. Присоединение неароматической гетероциклической субъединицы к исходной молекуле может осуществляться через гетероатом или атом углерода. Подобным образом, дополнительное замещение может осуществляться при гетероатоме или атоме углерода. В качестве неограничивающего примера, имидазолидиновый неароматический гетероцикл может быть присоединен к исходной молекуле через содержащиеся в гетероцикле атомы N (имидазолидин-1-ил или имидазолидин-3-ил) или любой из атомов углерода (имидазолидин-2-ил имидазолидин-4-ил или имидазолидин-5-ил). В некоторых вариантах неароматические гетероциклы содержат одну или больше карбонильных или тиокарбонильных групп, например, таких как оксо- и тиосодержащие группы. Примеры включают, не ограничиваясь ими, пирролидинил, тетрагидрофуранил, дигидрофуранил, тетрагидротиенил, тетрагидропиранил, дигидропиранил, тетрагидротиопиранил, пиперидин, морфолино, тиоморфолино, тиоксанил, пиперазинил, азетидинил, оксетанил, тиетанил, гомопиперидинил, оксепанил, тиепанил, оксазепинил, диазепинил, тиазепинил, 1,2,3,6-тетрагидрорпиридинил, 2-пирролинил, 3-пирролинил, индолинил, 2Н-пиранил, 4Н-пиранил, диоксанил, 1,3-диоксоланил, пиразолинил, дитианил, дитиоланил, дигидропиранил, дигидротиенил, дигидрофуранил, пиразолидинил, имидазолинил, имидазолидинил, 3-азабицикло[3,1,0]гексанил, 3-азабицикло[4,1,0]гептанил, 3H-индолил и хинолизинил. Иллюстративные примеры гетероциклоалкильных групп, которые также называются неароматическими гетероциклами, включают:
 ,
,  ,
,  ,
, 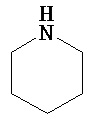 ,
, 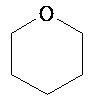 ,
, 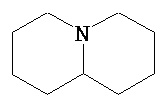 ,
, 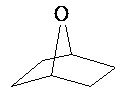 ,
,
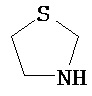 ,
, 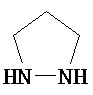 ,
, 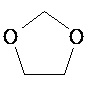 ,
, 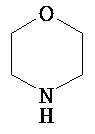 ,
, 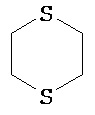 ,
, 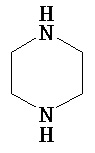 ,
, 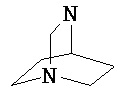 ,
,
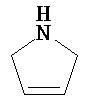 ,
, 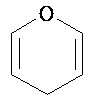 ,
, 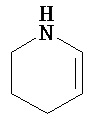 ,
, 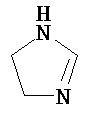 ,
, 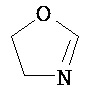 ,
, 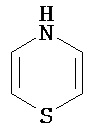 ,
, 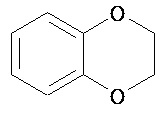 ,
,
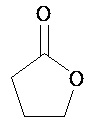 ,
, 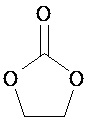 ,
, 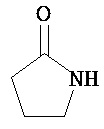 ,
, 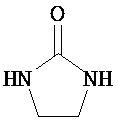 ,
, 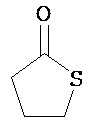 ,
, 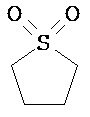 ,
, 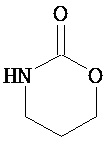 ,
, 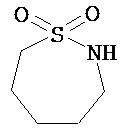 и т.д.
и т.д.
Термины также включают все кольцевые формы углеводородов, в том числе, не ограничиваясь ими, моносахариды, дисахариды и олигосахариды. В одном из вариантов "неароматический гетероциклил" или "гетероалициклил" является замещенным. Если не указано иное, "неароматический гетероциклил" или "гетероалициклил" является незамещенным.
Термин "арил" в данном описании, отдельно или в комбинации, обозначает ароматический углеводородный радикал, содержащий от 6 до приблизительно 12 атомов углерода в кольце, и включает конденсированные и неконденсированные арильные кольца. Арильный радикал, содержащий конденсированные кольца, включает от 2 до 4 конденсированных колец, где присоединение осуществляется через арильное кольцо, и другие отдельные кольца могут быть алициклическими, гетероциклическими, ароматическими, гетероароматическими, или любой их комбинацией. Кроме того, термин «арил» включает конденсированные и неконденсированные кольца, содержащие от 6 до приблизительно 12 атомов углерода в кольце, а также содержащие от 6 до приблизительно 10 атомов углерода в кольце. Неограничивающий пример арильной группы с одним кольцом включает фенил; арильные группы с конденсированными кольцами включает нафтил, фенантренил, антраценил, азуленил; и би-арильной группы с неконденсированными кольцами включает бифенил. В одном из вариантов "арил" является замещенным. Если не указано иное, "арил" является незамещенным.
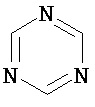
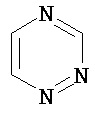
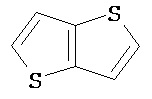
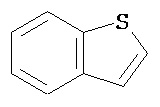
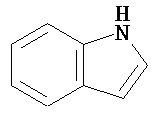
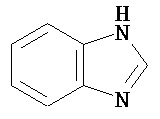
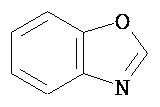
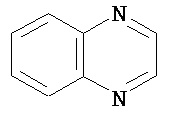
Термин "гетероарил" в данном описании, отдельно или в комбинации, обозначает ароматические монорадикалы, содержащие от приблизительно 5 до приблизительно 12 скелетных атомов в кольце, где один или больше атомов в кольце представляет собой гетероатом, независимо выбранный из кислорода, азота, серы, фосфора, кремния, селена и олова, не ограничиваясь указанными атомами, и при условии, что кольцо в указанной группе не содержит двух смежных атомов О или S. В вариантах, где два или больше гетероатомов присутствуют в кольце, два или больше гетероатомов могут быть одинаковыми, или все из двух или больше гетероатомов могут быть разными. Термин «гетероарил» включает конденсированные и неконденсированные гетероарильные радикалы, содержащие по меньшей мере один гетероатом. Термин «гетероарил» также включает конденсированные и неконденсированные гетероарилы, содержащие от 5 до приблизительно 12 скелетных атомов в кольце, а также содержащие от 5 до приблизительно 10 скелетных атомов в кольце. Присоединение к гетероарильной группе может осуществляться через атом углерода или гетероатом. Таким образом, в качестве неограничивающего примера, имидазольная группа может быть присоединена к исходной молекуле через любой из атомов углерода (имидазол-2-ил, имидазол-4-ил или имидазол-5-ил) или атомов азота (имидазол-1-ил или имидазол-3-ил). Подобным образом, гетероарильная группа дополнительно может быть замещена при любом или всех атомах углерода и/или любом или всех гетероатомах. Конденсированный гетероарильный радикал может содержать от 2 до 4 конденсированных колец, где кольцо, через которое осуществляется присоединение, представляет собой гетероароматическое кольцо, и другие отдельные кольца могут быть алициклическими, гетероциклическими, ароматическими, гетероароматическими, или любой их комбинацией. Неограничивающий пример гетероарильной группы с одним кольцом включает пиридил; гетероарильной группы с конденсированными кольцами включает бензимидазолил, хинолинил, акридинил; и неконденсированной би-гетероарильной группы включает бипиридинил. Другие примеры гетероарилов включают, не ограничиваясь ими, фуранил, тиенил, оксазолил, акридинил, феназинил, бензимидазолил, бензофуранил, бензоксазолил, бензотиазолил, бензотиадиазолил, бензотиофенил, бензоксадиазолил, бензотриазолил, имидазолил, индолил, изоксазолил, изохинолинил, индолизинил, изотиазолил, изоиндолил, оксадиазолил, индазолил, пиридил, пиридазил, пиримидил, пиразинил, пирролил, пиразинил, пиразолил, пуринил, фталазинил, птеридинил, хинолинил, хиназолинил, хиноксалинил, триазолил, тетразолил, тиазолил, триазинил, тиадиазолил, и т.п., и их оксиды, такие как, например, пиридил-N-оксид. Иллюстративные примеры гетероарильных групп включают следующие фрагменты:
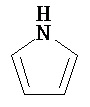 ,
, 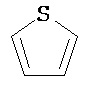 ,
, 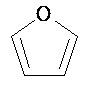 ,
, 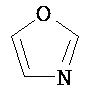 ,
, 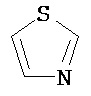 ,
, 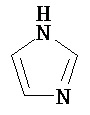 ,
, 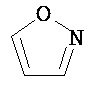 ,
, 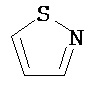 ,
, 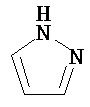 ,
, 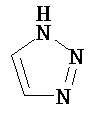 ,
,
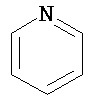 ,
, 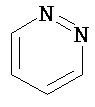 ,
, 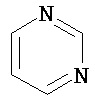 ,
, 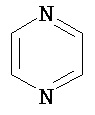 ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
, 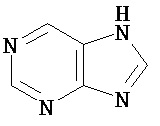 ,
, 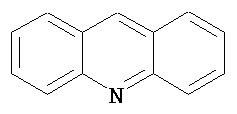 и т.д.
и т.д.
В одном из вариантов "гетероарил" является замещенным. Если не указано иное, "гетероарил" является незамещенным.
Термин "гетероциклил" в данном описании, отдельно или в комбинации, коллективно обозначает гетероалициклические и гетероарильные группы. Таким образом, независимо от указанного количества атомов углерода в гетероцикле (например, С1-С6 гетероцикл), по меньшей мере один неуглеродный атом (гетероатом) должен присутствовать в кольце. Такие обозначения, как "C1-C6 гетероцикл" касаются только количества атомов углерода в кольце и не обозначают общего количества атомов в кольце. Такие обозначения, как "4-6-членный гетероцикл" обозначают общее количество атомов, которые содержатся в кольце (т.е. 4-, 5- или 6-членное кольцо, где по меньшей мере один атом представляет собой атом углерода, по меньшей мере один атом представляет собой гетероатом, и остальные 2-4 атома представляют собой атомы углерода или гетероатомы). Для гетероциклов, содержащих два или больше гетероатомов, указанные два или больше гетероатомов могут быть одинаковыми или разными. Неароматические гетероциклические группы включают группы, содержащие только 3 атома в кольце, тогда как ароматические гетероциклические группы должны содержать по меньшей мере 5 атомов в кольце. Присоединение (т.е. присоединение к исходной молекуле или дополнительное замещение) к гетероциклу может осуществляться через гетероатом или атом углерода. В одном из вариантов "гетероциклил" является замещенным. Если не указано иное, "гетероциклил" является незамещенным.
Термины "галоген", "гало" или "галогенид" в данном описании, отдельно или в комбинации обозначают фтор, хлор, бром и/или йод.
Некоторые фармацевтические термины
Термины "субъект", "пациент" или "индивидуум" в данном описании в отношении индивидуумов, страдающих от расстройства, и т.п., включают млекопитающих и субъектов, не относящихся к млекопитающим. Примеры млекопитающих включают, не ограничиваясь ими, любого члена класс Млекопитающих: человека, негуманоидных приматов, таких как шимпанзе и другие виды обезьян и мартышек; сельскохозяйственных животных, таких как телята, лошади, овцы, козы, свиньи; домашних животных, таких как кролики, собаки и кошки; лабораторных животных, в том числе грызунов, таких как крысы, мыши и морские свинки, и т.п. Примеры субъектов, не относящихся к млекопитающим, включают, не ограничиваясь ими, птиц, рыб, и т.п. В одном из вариантов способов и композиций, предложенных в данном описании, млекопитающее представляет собой человека.
Термины "эффективное количество", "терапевтически эффективное количество" или "фармацевтически эффективное количество" в данном описании обозначают количество по меньшей мере одного агента или соединения, которое при введении является достаточным для лечения или профилактики конкретного заболевания или состояния. Результатом может быть уменьшение и/или облегчение признаков, симптомов или причин заболевания, или любое другое желательное изменение биологической системы. Например, "эффективное количество" в терапии представляет собой количество композиции, содержащей соединение, раскрытое в данном описании, необходимое для достижения клинически значимого уменьшения тяжести заболевания. Подходящее "эффективное" количество в любом отдельном случае может быть определено с использованием таких методик, как исследование повышения дозы.
В данном описании термины "лечение" или "терапия", "облегчение" или "улучшение" используются равнозначным образом. Эти термин указывают на подход для получения полезных или желательных результатов, в том числе, но не ограничиваясь ими, терапевтической выгоды и/или профилактической выгоды. Под терапевтической выгодой подразумевается устранение или облегчение основного расстройства, подлежащего лечению. Также, терапевтическая выгода достигается при устранении или облегчении одного или больше физиологических симптомов, связанных с основным расстройством, таким образом, что улучшение наблюдается у больного, несмотря на, что больной может все еще страдать основным расстройством. Для достижения профилактической выгоды композиции могут вводиться больному, подверженному риску развития конкретного заболевания, или больному, который сообщает об одном или больше физиологических симптомов заболевания, даже если диагноз этого заболевания может быть не установлен.
Термин "терапевтический эффект" используется в данном описании и включает терапевтическую выгоду и/или профилактическую выгоду, как изложено выше. Профилактический эффект включает задержку или исключение появления заболевания или состояния, задержку или исключение появления симптомов заболевания или состояния, замедление, остановку или изменение прогрессирования заболевания или состояния, или любую их комбинацию.
Термин "фармацевтически приемлемый" в данном описании обозначает материал, такой как носитель или разбавитель, который не создает помех биологической активности или свойствам соединений, описанных в данном описании, и является относительно нетоксичным, т.е. материал может вводиться индивидууму без провоцирован™ нежелательных биологических эффектов или вредного взаимодействия с любым из компонентов композиции, в которой этот материал содержится.
Термин "фармацевтическая композиция" в данном описании обозначает биологически активное соединение, необязательно смешанное по меньшей мере с одним фармацевтически приемлемым химическим компонентом, таким как, не ограничиваясь ими, носители, стабилизаторы, разбавители, диспергирующие средства, суспендирующие средства, загустители и/или вспомогательные вещества.
Термин "носитель" в данном описании обозначает относительно нетоксичные химические соединения или средства, которые облегчают проникновение соединения в клетки или ткани.
Термин "пролекарство" обозначает соединение, которое может превращаться в физиологических условиях или путем сольволиза в биологически активное соединение, описанное в данном описании. Таким образом, термин "пролекарство" обозначает прекурсор биологически активного соединения, который является фармацевтически приемлемым. Пролекарство может быть инертным при введении субъекту, но превращаться in vivo в активное соединение, например, посредством гидролиза. Пролекарство соединения часто обеспечивает преимущества растворимости, совместимости с тканями или замедленного высвобождения в организме млекопитающих (см., например, Bundgard, П., Design of Prodrugs (1985), pp.7-9, 21-24 (Elsevier, Амстердам). Обсуждение пролекарств приведено в Higuchi, Т., et al., "Pro-drugs as Novel Delivery Systems," A.C.S. Symposium Series, Vol.14, и в Bioreversible Carriers in Drug Design, ed. Edward B. Roche, American Pharmaceutical Association and Pergamon Press, 1987, оба из которых включены в данное описание путем ссылки в полном объеме. Термин "пролекарство" также предназначен включать любые ковалентно связанные носители, которые высвобождают активное соединение in vivo, при введении такого пролекарства субъекту-млекопитающему. Пролекарство активного соединения, описанного в данном описании, может быть получено путем модификации функциональных групп, присутствующих в активном соединении, таким образом, что модифицирующие группы отщепляются при шаблонном манипулировании или in vivo, с образованием исходного активного соединения. Пролекарства включают соединения, где гидрокси-, амино- или меркаптогруппа соединена с какой-либо группой, которая, при введении Пролекарства активного соединения субъекту-млекопитающему, отщепляется с образованием свободной гидрокси-, амино- или меркаптогруппы, соответственно. Примеры пролекарств включают, не ограничиваясь ими, ацилокси, тиоацилокси, 2-карбоалкоксиэтил, дисульфид, тиаминальные и енол-эфирные производные нуклеиновой кислоты с модифицированным атомом фосфора.
Термины "про-олигонуклеотид" или "пронуклеотид" или "пролекарство нуклеиновой кислоты" обозначают олигонуклеотид, модифицированный таким образом, чтобы быть пролекарством олигонуклеотида.
Некоторые термины в области нуклеиновых кислот
Природные нуклеиновые кислоты содержат фосфатный скелет;
искусственные нуклеиновые кислоты могут содержать другие виды скелета, но содержат такие же основания.
Термин "нуклеотид" в данном описании обозначает мономерную единицу полинуклеотида, которая состоит из гетероциклического основания, сахара и одной или больше фосфорнокислых групп. Природные основания (гуанин [G], аденин [А], цитозин [С], тимин [Т] и урацил [U]) - это производные пурина или пиримидина, однако, следует понимать, что природные и неприродные аналоги оснований также включены. Природные сахара - это пентоза (пятиуглеродный сахар), дезоксирибоза (которая формирует ДНК) или рибоза (которая формирует РНК), однако, следует понимать, что природные и неприродные сахара также включены. Нуклеиновые кислоты присоединены через фосфорнокислые связи, с образованием нуклеиновых кислот или полинуклеотидов, однако, множество других соединений известны из уровня техники (например, не ограничиваясь ими, фосфортиоаты, боранофосфаты, и т.п.). Искусственные нуклеиновые кислоты включают ПНК (пептид-нуклеиновые кислоты), фосфортиоаты и другие варианты фосфатного скелета природных нуклеиновых кислот.
Термин "нуклеозид" обозначает фрагмент, где нуклеиновое основание или модифицированное нуклеиновое основание связаны с сахаром или модифицированным сахаром.
Термин "сахар" обозначает моносахарид в закрытой и/или открытой форме. Сахара включают, не ограничиваясь ими, рибозный, дезоксирибозный, пентофуранозный, пентопиранозный и гексопиранозный фрагменты.
Термин "модифицированный сахар" обозначает фрагмент, который может заменить сахар. Модифицированный сахар имитирует пространственное расположение, электронные свойства или некоторое другое физико-химическое свойство сахара.
Термины "нуклеиновая кислота" и "полинуклеотид" в данном описании обозначают полимерную форму нуклеотидов любой длины, т.е. рибонуклеотиды (РНК) или дезоксирибонуклеотиды (ДНК). Эти термины обозначают первичную структуру молекул и, таким образом, включают двухцепочечные и одноцепочечные ДНК, а также двухцепочечные и одноцепочечные РНК. Эти термины включают, как эквиваленты, аналоги РНК или ДНК, полученные из нуклеотидных аналогов и модифицированных полинуклеотидов, таких как например, не ограничиваясь ими, метилированные и/или кэппированные полинуклеотиды. Термины охватывают поли- или олиго-рибонуклеотиды (РНК) и поли- или олиго-дезоксирибонуклеотиды (ДНК); РНК или ДНК, происходящие от N-гликозидов или С-гликозидов нуклеиновых оснований и/или модифицированных нуклеиновых оснований; нуклеиновые кислоты, происходящие от сахаров и/или модифицированных сахаров; и нуклеиновые кислоты, происходящие от фосфатных мостиков и/или модифицированных фосфатных мостиков. Термин включает нуклеиновые кислоты, содержащие какие-либо комбинации нуклеиновых оснований, модифицированных нуклеиновых оснований, сахаров, модифицированных сахаров, фосфатных мостиков или модифицированных фосфатных мостиков. Примеры включают, не ограничиваясь ими, нуклеиновые кислоты, содержащие рибозные фрагменты, нуклеиновые кислоты, содержащие дезоксирибозные фрагменты, нуклеиновые кислоты, содержащие как рибозные, так и дезоксирибозные фрагменты, нуклеиновые кислоты, содержащие рибозные и модифицированные рибозные фрагменты. Приставка поли- обозначает нуклеиновые кислоты, содержащие от приблизительно 1 до приблизительно 10000 мономерных нуклеотидных единиц, и приставка олиго- обозначает нуклеиновые кислоты, содержащие от приблизительно 1 до приблизительно 200 мономерных нуклеотидных единиц.
Термин "нуклеиновое основание" обозначает части нуклеиновых кислот, которые образуют водородную связь, соединяющую одну цепь нуклеиновой кислоты с другой комплементарной цепью специфичным для последовательности образом. Наиболее распространенными природными основаниями являются аденин (А), гуанин (G), урацил (U), цитозин (С) и тимин (Т).
Термин "модифицированное нуклеиновое основание" обозначает фрагмент, который может заменить нуклеиновое основание. Модифицированное нуклеиновое основание имитирует пространственное расположение, электронные свойства или некоторое другое физико-химическое свойство нуклеинового основания и сохраняет свойство образования водородных связей, соединяющих одну цепь нуклеиновой кислоты с другой специфичным для последовательности образом. Модифицированные нуклеиновые основания могут спариваться со всеми пятью природными основаниями (урацил, тимин, аденин, цитозин или гуанин), не влияя в существенной мере на поведение при плавлении, распознавание внутриклеточными ферментами или активность спаренного олигонуклеотида.
Термин "хиральный реактив" обозначает соединение, которое является хиральным или энантиомерно чистым и может использоваться для асимметрической индукции в синтезе нуклеиновых кислот.
Термины "хиральный лиганд" или "хиральный адъювант" обозначаю фрагмент, который является хиральным или энантиомерно чистым и контролирует стереохимический результат реакции.
В реакции конденсации, термин "конденсирующий реактив" обозначает реактив, который активизирует менее реакционноспособный сайт и делает его более восприимчивым к атаке нуклеофила.
Термин "блокирующая группа" обозначает группу, которая временно маскирует реакционноспособность функциональной группы. Маскировка функциональной группы может быть впоследствии отменена удалением блокирующей группы.
Термины "борирующие агенты", "серосодержащий электрофил", "селеносодержащий электрофил" обозначают соединения, пригодные на стадии модификации, используемой для введения групп BH3, S, и Se, соответственно, с целью модификации при атоме фосфора.
Термин "фрагмент" обозначает определенный сегмент или функциональную группу молекулы. Химические фрагментами часто называют химические объекты, введенные в или присоединенные к молекуле.
Термин "твердая подложка" обозначает любую подложку, которая позволяет массовое производство нуклеиновых кислот синтетическим способом и при необходимости может быть использована снова. В данном описании термин обозначает полимер, нерастворимый в средах, используемых на стадиях реакции, целью который является синтез нуклеиновых кислот, и дериватизированных для охвата реакционноспособных групп.
Термин "связывающий фрагмент" обозначает любой фрагмент, необязательно помещенный между терминальным нуклеозидом и твердой подложкой или между терминальным нуклеозидом и другим нуклеозидом, нуклеотидом или нуклеиновой кислотой.
"Молекула ДНК" обозначает полимерную форму дезоксирибонуклеотидов (аденина, гуанина, тимина или цитозина) в форме одноцепочечной или двухцепочечной спирали. Данный термин обозначает только первичную и вторичную структуру молекулы, и не ограничивается какими-либо конкретными третичными формами. Таким образом, данный термин включает двухцепочечную ДНК, среди прочего, в виде линейных молекул ДНК (например, рестрикционные фрагменты), вирусов, плазмид и хромосом. В обсуждении структуры конкретных двухцепочечных молекул ДНК, последовательности могут быть описаны согласно обычному соглашению предоставления только последовательности в 5'→3' направлении вдоль нетранскрибированной цепи ДНК (т.е. цепь, последовательность которого гомологична мРНК).
"Кодирующая последовательность" или "кодирующий участок" ДНК - это двухцепочечная последовательность ДНК, которая транскрибируется и транслируется в полипептид in vivo, при размещении под контролем подходящей последовательности для контроля экспрессии. Границы кодирующей последовательности ("открытая рамка считывания" или "ОРС") определяются стартовым кодоном на 5'-конце (амино) и кодоном остановки трансляции на 3'-конце (карбоксил). Кодирующая последовательность может включать, не ограничиваясь ими, последовательности прокариот, кДНК из мРНК эукариот, геномные последовательности ДНК эукариот (например, млекопитающих) и синтетические последовательности ДНК. Сигнал полиаденилирования и последовательность окончания транскрипции обычно размещены в направлении 3' по отношению к кодирующей последовательности. Термин "некодирующая последовательность" или "некодирующий участок" обозначает участки полинуклеотидной последовательности, которые не транслируются в аминокислоты (например, 5' и 3' нетранслируемые участки).
Термин "рамка считывания" обозначает одну из шести возможных рамок считывания, по три в каждом направлении, двухцепочечной молекулы ДНК. Используемая рамка считывания определяет, какие кодоны используются для кодирования аминокислот в пределах кодирующей последовательности молекулы ДНК.
В данном описании "антисмысловая" молекула нуклеиновой кислоты охватывает последовательность нуклеотидов, комплементарную к "смысловой" нуклеиновой кислоте, кодирующей белок, например, комплементарную к кодирующей цепи двухцепочечной молекуле кДНК, комплементарную к последовательности мРНК или комплементарную к кодирующей цепи гена. Соответственно, молекула антисмысловой нуклеиновой кислоты может образовывать водородную связь с молекулой смысловой нуклеиновой кислоты.
Термин "пара оснований" ("bp"): спаривание аденина (А) с тимином (Т) или цитозина (С) с гуанином (G) в двухцепочечной молекуле ДНК. В РНК урацил (U) замещает тимин.
В данном описании "кодон" обозначает три нуклеотида, которые при транскрибировании и трансляции кодируют одинарный остаток аминокислоты; или в случае UUA, UGA или UAG кодируют сигнал окончания. Кодоны, кодирующие аминокислоты, хорошо известны из уровня техники и для удобства приведены в табл.1.
|
В данном описании "положение качания" обозначает третье положение кодона. Мутации в молекуле ДНК в пределах положения качания кодона, в некоторых вариантах, приводят к безмолвным или консервативным мутациям на уровне аминокислоты. Например, существует четыре кодона, которые кодируют глицин, т.е. GGU, GGC, GGA и GGG, поэтому мутация какого-либо нуклеотида в «положении качания» до любого другого нуклеотида не приводит к изменению на уровне аминокислоты кодируемого белка и, таким образом, является безмолвной заменой.
Соответственно, "безмолвная замена" или "безмолвная мутация" - такая, при которой нуклеотид в пределах кодона изменен, но не приводит к изменению остатка аминокислоты, кодируемого кодоном. Примеры включают мутации в третьем положении кодона, а также в первом положении некоторых кодонов, таких как кодон "CGG", который, в случае видоизменения до AGG, все еще кодирует Arg.
Термины "ген", "рекомбинантный ген" и "генная конструкция" в данном описании обозначают молекулу ДНК, или часть молекулы ДНК, которая кодирует белок или его часть. Молекула ДНК может содержать открытую рамку считывания, кодирующую белок (как последовательности экзонов), и может дополнительно включать последовательности интрона. Термин "интрон" в данном описании обозначает наличие в представленном гене последовательности ДНК, которая не транслируется в белок и найдена в некоторых, но не во всех случаях, между экзонами. Для гена, который функционально связан (или это может включать) с одним или больше промоторами, энхансерами, репрессорами и/или другими регуляторными последовательностями, может быть желательной модуляция активности или экспрессии гена, как хорошо известно из уровня техники.
В данном описании "комплементарная ДНК" или "кДНК" включает рекомбинантные полинуклеотиды, синтезированные обратной транскрипцией мРНК, из которых исключены перемежающие последовательности (интроны).
"Гомология", "идентичность" или "сходство" обозначают сходство последовательностей между двумя молекулами нуклеиновой кислоты. Каждое из понятий «гомология и идентичность» может быть определено путем сравнения положений в каждой их последовательностей, которая может быть выровнена для целей сравнения. Если равноценное положение в сравниваемых последовательностях занято таким же основанием, то молекулы идентичны в этом положении; если равноценное положение занято таким же или подобным остатком нуклеиновой кислоты (например, со сходной стерической и/или электронной природой), то молекулы могут быть названы гомологичными (сходными) по данному положению. Выражение процента гомологии/сходства или идентичности обозначает функцию количества идентичных или сходных остатков нуклеиновых кислот в положениях, разделяемых сравниваемыми последовательностями. "Несходная" или "негомологичная" последовательность обладает менее чем 40% идентичностью, менее чем 35% идентичностью, менее чем 30% идентичностью или менее чем 25% идентичностью с последовательностью, описанной в данном описании. При сравнении двух последовательностей, отсутствие остатков (аминокислот или нуклеиновых кислот) или присутствие добавочных остатков также уменьшает степень идентичности и гомологии/сходства.
Термин "гомология" описывает математически обоснованное сравнение последовательностей на предмет сходства, которое используется для идентификации генов с подобными функциями или мотивами. Последовательности нуклеиновых кислот, описанные в данном описании, могут использоваться в качестве "последовательности запроса" для выполнения поиска в публичных базах данных, например, с целью идентификации других членов семейства, связанных последовательностей или гомологов. Такой поиск может выполняться с использованием программ NBLAST и XBLAST (версия 2.0) Altschul, et al. (1990) J. Mol. Biol. 215:403-10. Поиск нуклеотида методом BLAST может выполняться с помощью программы NBLAST, score = 100, wordlength = 12, чтобы получить последовательности нуклеотидов, гомологичные молекулам нуклеиновых кислот по изобретению. Чтобы получить выравнивание с промежутками для целей сравнения, Gapped BLAST может использоваться, как описано в Altschul, et al. (1997) Nucleic Acids Res. 25(17):3389-3402. При использовании программ BLAST и Gapped BLAST, используемые по умолчанию параметры соответствующих программ (например, XBLAST и BLAST) могут применяться (см. www.ncbi.nlm.nih.gov).
В данном описании "идентичность" подразумевает процент идентичных нуклеотидных остатков в соответствующих положениях двух или больше последовательностей, при выравнивании последовательностей с целью максимизации соответствия последовательностей, т.е. с учетом промежутком и вставок. Идентичность может быть легко вычислена известными способами, в том числе, не ограничиваясь ими, описанными в (Computational Molecular Biology, Lesk, A.M., ed., Oxford University Press, New York, 1988; Biocomputing: Informatics and Genome Projects, Smith, D.W., ed., Academic Press, New York, 1993; Computer Analysis of Sequence Data, Part I, Griffin, A.M., and Griffin, H.G., eds., Humana Press, New Jersey, 1994; Sequence Analysis in Molecular Biology, von Heinje, G., Academic Press, 1987; and Sequence Analysis Primer, Gribskov, M. and Devereux, J., eds., M Stockton Press, New York, 1991; и Carillo, H., and Lipman, D., SIAM J. Applied Math., 48: 1073 (1988). Способы определения идентичность разработаны для обеспечения наибольшего совпадения между проверяемыми последовательностями. Кроме того, способы определения идентичности заложены в публично доступных компьютерных программах. Способы определить идентичность двух последовательностей с помощью компьютерной программы включают, не ограничиваясь ими, пакеты программ GCG (Devereux, J., et al., Nucleic Acids Research 12 (1): 387 (1984)), BLASTP, BLASTN и FASTA (Altschul, S.F. et al., J. Molec. Biol. 215: 403-410 (1990) и Altschul et al. Nuc. Acids Res. 25: 3389-3402 (1997)). Программа BLAST X публично доступна от NCBI и из других источников (BLAST Manual, Altschul, S., et al., NCBI NLM NIH Bethesda, Md. 20894; Altschul, S., et al., J. Mol. Biol. 215: 403-410 (1990). Хорошо известный алгоритм Smith Waterman также может применяться для определения идентичности.
"Гетерологичный" участок последовательности ДНК - это идентифицируемый сегмент ДНК в пределах последовательности ДНК большего размера, который не найден в связи с последовательностью большего размера в природе. Таким образом, если гетерологичный участок кодирует ген млекопитающего, фланг гена обычно может быть защищен ДНК, которая не защищает фланг геномной ДНК млекопитающего в геноме исходного организма. Другой пример гетерологичной кодирующей последовательности - это последовательность, где непосредственно кодирующая последовательность не найдена в природе (например, кДНК, где геномная кодирующая последовательность содержит интроны или синтетические последовательности, включающие кодоны или другие мотивы, чем немодифицированный ген). Аллельные вариации или природные мутационные события не дают начало гетерологичному участку ДНК, в соответствии с определением в данном описании.
Термин «переходные мутации» обозначает замены оснований в последовательности ДНК, где пиримидиновое основание (цитидин [С] или тимин [Т]) заменяется на другое пиримидиновое основание или пуриновое основание (аденозин [А] или гуанозин [G]) заменяется на другое пуриновое основание.
Термин «трансверсивные мутации» обозначает замены оснований в последовательности ДНК, где пиримидиновое основание (цитидин [С] или тимин [Т]) заменяется на пуриновое основание (аденозин [А] или гуанозин [G]), или пуриновое основание заменяется на пиримидиновое основание.
Пролекарства нуклеиновых кислот, содержащие хиральный X-фосфонатный фрагмент
Общие принципы дизайна пролекарств описаны Bundgard (Design and Application of Prodrugs. В Textbook of Drug Design and Development; Krogsgaard-Larsen, P., Bundgard, H., Eds.; Harwood: Reading, UK, 1991).
Одна из стратегий улучшения фармацевтических свойств молекул с желательной биологической активностью, но недостаточными фармацевтическими свойствами состоит во введении целевой молекулы в виде производного-пролекарства. Такое пролекарство может демонстрировать одно или больше свойств: повышение биодоступности при пероральном введении, повышение проницаемости клетки, повышение растворимости в воде, уменьшение пресистемного метаболизма, повышение стабильности, активный транспорт кишечными носителями или избегание носителей, выводящих молекулы, по сравнению с исходной молекулой.
Олигонуклеотиды обладают несколькими фармацевтическими свойствами, которые могут быть улучшены с применением пролекарственных стратегий. В частности, олигонуклеотиды быстро разлагаются нуклеазами и слабо захватываются клетками через цитоплазматическую мембрану клетки (Poijarvi-Virta et al., Curr. Med. Chem. (2006), 13(28);3441-65; Wagner et al., Med. Res. Rev. (2000), 20(6):417-51; Peyrottes et al., Mini Rev. Med. Chem. (2004), 4 (4): 395-408; Gosselin et al., (1996), 43(1):196-208; Bologna et al., (2002), Antisense & Nucleic Acid Drug Development 12:33-41). В одном из примеров, Vives et al., (Nucleic Acids Research (1999), 27 (20): 4071-76) обнаружили, что трет-бугил SATE про-олигонуклеотиды демонстрируют значительное увеличение проникновения в клетку по сравнению с исходным олигонуклеотидом.
В некоторых вариантах пролекарственный фрагмент селективно удаляется эстеразами, нуклеазами или ферментом цитохром Р450, в том числе, не ограничиваясь ими, представленными в перечне ниже.
|
|
В некоторых вариантах пролекарственный фрагмент удаляется до переноса про-олигонуклеотида через мембрану клетки. В других вариантах пролекарственный фрагмент удаляется из про-олигонуклеотида только после переноса через мембрану клетки. Альтернативно, пролекарственный фрагмент удаляется только после переноса в органеллу в пределах клетки. В некоторых вариантах пролекарственный фрагмент удаляется посредством неферментативного процесса, в том числе, не ограничиваясь ими, самопроизвольное восстановление внутри клетки.
В данном изобретении описаны пролекарства нуклеиновых кислот, содержащие модификацию хирального Х-фосфоната, где модификация улучшает одно или больше физико-химических, фармакокинетических или фармакодинамических свойств нуклеиновой кислоты. Пролекарственный фрагмент соединен с атомом кислорода или серы, который присоединен к атоме фосфора фосфонатной или фосфортиоатной группы нуклеотида. Пролекарственный фрагмент включает, не ограничиваясь ими, 8-ацил-2-тиоэтильные, ацилокси, тиоацилокси, 2-карбоалкоксиэтильные, дисульфидные, тиаминальные и енол-эфирные производные.
В одном из вариантов пролекарственный фрагмент представляет собой S-ацил-2-тиоэтильный фрагмент следующей структуры:

где R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил. В некоторых вариантах R11 представляет собой метил, этил или циклопропил.
В других вариантах пролекарственный фрагмент представляет собой ацилокси фрагмент следующей структуры:

где R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил, и R12 представляет собой водород или алкил. В некоторых вариантах R11 представляет собой метил, и R12 представляет собой водород.
Альтернативно, пролекарственный фрагмент представляет собой тиоацилокси фрагмент следующей структуры:

где R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил, и R12 представляет собой водород или алкил. В некоторых вариантах R11 представляет собой метил, и R12 представляет собой водород.
В изобретении также предлагаются пролекарства 2-карбоалкоксиэтил фрагмента следующей структуры:
 или
или 
где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода. В некоторых вариантах R10 представляет собой метил или этил.
В других вариантах, пролекарственный фрагмент представляет собой дисульфидный фрагмент следующей структуры:

где R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил. В некоторых вариантах R11 представляет собой метил, этил или бензил.
В дополнительных вариантах, пролекарственный фрагмент представляет собой тиоацетальный фрагмент следующей структуры:

где R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода, и R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил. В некоторых вариантах R10 представляет собой метил, и R11 представляет собой метил или фенил.
В изобретении также предлагаются фрагменты пролекарства енольного эфира следующей структуры:
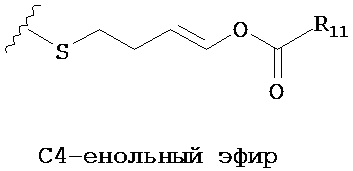 или
или 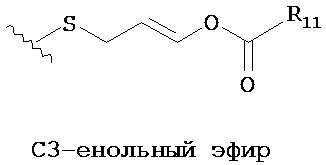
где R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил. В некоторых вариантах фрагмент пролекарства С3-енольного эфира или фрагмент пролекарства С4-енольного эфира, находящийся в цис-форме. В некоторых вариантах фрагмент пролекарства С3-енольного эфира или фрагмент пролекарства С4-енольного эфира, R11 представляет собой метил, этил или фенил.
В одном из вариантов пролекарственный фрагмент представляет собой триалкиламмонийметильный фрагмент, структура которого представлена одной из следующих формул:
 или
или  .
.
В одном из вариантов пролекарственный фрагмент представляет собой алкилгидроксаматный фрагмент, структура которого представлена одной из следующих формул:
 или
или  .
.
В одном из вариантов пролекарственный фрагмент представляет собой ацилгидроксаматный фрагмент, структура которого представлена одной из следующих формул:
 или
или  .
.
В одном из вариантов предлагается пролекарство нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, P(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, P(О)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
по меньшей мере в одном случае Х представляет собой
-OCH2CH2S-S(O)2R10, -OCH2CH2S-SCH2CH2OH, -OCH2CH2CO2H,  ,
,  ,
,
 ,
, 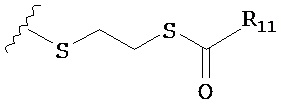 ,
, 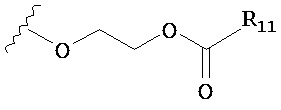 ,
,
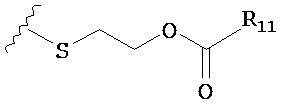 ,
, 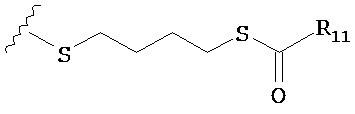 ,
, 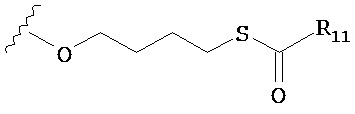 ,
,
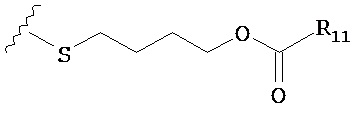 ,
, 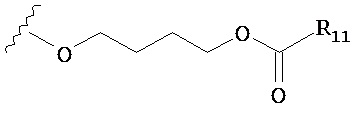 ,
,  ,
,
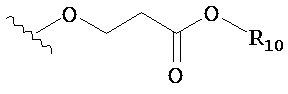 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  или
или
 ;
;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил;
Z представляет собой S или О;
q равно 0, 1 или 3;
w равно 1, 2, 3, 4, 5 или 6;
R15 и R16 независимо представляют собой водород или метил;
R17 выбран из алкила, арила или CH2CH=СН2;  ,
,  ,
,  ,
,  и
и  ; и
; и
n равно целому числу от 1 до приблизительно 200.
В одном из аспектов изобретения предлагается пролекарство нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -OP(O)(Re)2, -HP(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где R6 представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
в каждом случае X представляет собой
 ,
,  ,
,
 ,
,  ,
,  ,
,  ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  или
или

R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил; и
n равно целому числу от 1 до приблизительно 200.
В одном из аспектов изобретения предлагается пролекарство нуклеиновой кислоты следующей структуры:

где R1 представляет собой -ОН, -SH, -NRdRd, -N3, галоген, водород, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -OP(O)(Re)2, -НР(O)(Re), -ORa или -SRc;
Y1 представляет собой О, NRd, S или Se;
Ra представляет собой блокирующую группу;
Rc представляет собой блокирующую группу;
Rd, в каждом случае независимо, представляет собой водород, алкил, алкенил, алкинил, арил, ацил, замещенный силил, карбамат, -P(O)(Re)2 или -HP(O)(Re);
Re, в каждом случае независимо, представляет собой водород, алкил, арил, алкенил, алкинил, алкил-Y2-, алкенил-Y2-, алкинил-Y2-, арил-Y2- или гетероарил-Y2- или катион, который представляет собой Na+1, Li+1 или K+1;
Y2 представляет собой О, NRd или S;
R2, в каждом случае независимо, представляет собой водород, -ОН, -SH, -NRdRd, -N3, галоген, алкил, алкенил, алкинил, алкил-Y1-, алкенил-Y1-, алкинил-Y1-, арил-Y1-, гетероарил-Y1-, -ORb или -SRc, где Rb представляет собой блокирующую группу;
Ва, в каждом случае независимо, представляет собой блокированный или неблокированный аденин, цитозин, гуанин, тимин, урацил или модифицированное нуклеиновое основание;
в каждом случае Х представляет собой
 ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  или
или
 .
.
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил; и
n равно целому числу от 1 до приблизительно 200.
В дополнительном варианте предлагается пролекарство нуклеиновой кислоты Формулы 1 или Формулы 2, где каждый фрагмент Х в пролекарстве нуклеиновой кислоты независимо выбран из
-OCH2CH2S-S(O)2R10, -OCH2CH2S-SCH2CH2OH, -OCH2CH2CO2H,  ,
,  ,
,
 ,
,  ,
,  ,
,
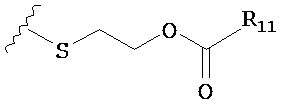 ,
,  ,
, 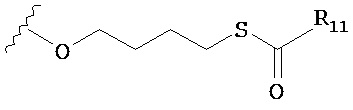 ,
,
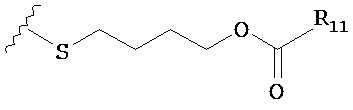 ,
, 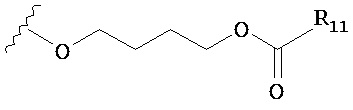 ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  ,
,
 ,
,  ,
,  или
или
 ;
;
R3 представляет собой водород, блокирующую группу, связывающий фрагмент, соединенный с твердой подложкой или соединенный с нуклеиновой кислотой;
R10 представляет собой алкильную группу, которая содержит от 1 до 4 атомов углерода;
R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил;
R12 представляет собой водород или алкил;
Z представляет собой S или О;
q равно 0, 1 или 3;
w равно 1, 2, 3, 4, 5 или 6;
R15 и R16 независимо представляют собой водород или метил;
R17 выбран из алкила, арила или CH2CH=СН2; и
R18 выбран из N(СН3)2,  ,
,  ,
,  ,
,  и
и  .
.
В некоторых вариантах n равно целому числу от 1 до приблизительно 50; от 1 до приблизительно 40; от 1 до приблизительно 30; от 1 до приблизительно 25; от 1 до приблизительно 20; от 1 до приблизительно 15; или от 1 до приблизительно 10.
В одном из вариантов предлагается нерацемический про-олигонуклеотид, где про-олигонуклеотид представляет собой аналог 2-5А, структура которого представлена следующей формулой:

где Х представляет собой любой из пролекарственных фрагментов, описанных в данном описании.
В некоторых вариантах нерацемический про-олигонуклеотид представляет собой 2-5А аналог следующей структуры:

где R11 представляет собой алкил, арил, гетероарил, гетероциклил или циклоалкил.
В одном из вариантов нерацемический про-олигонуклеотид представляет собой 2-5А аналог следующей структуры:
 .
.
ПРИМЕРЫ СПОСОБОВ СИНТЕЗА
Общее обсуждение способов синтеза пролекарств нуклеиновой кислоты, содержащих хиральный Х-фосфонатный фрагмент
Способы, описанные в данном описании, предлагают эффективный синтез пролекарств нуклеиновой кислоты, модифицированных по атому фосфора, где стереохимическая конфигурация атома фосфора контролируется таким образом, чтобы получить олигонуклеотид с заданной стереохимией. Хотя в примерах способов синтеза, описанных в данном описании, предлагается 3'-5' нуклеотидная связь, 2'-5' нуклеотидная связь также включена.
Про-олигонуклеотиды по изобретению могут быть синтезированы путем модификации хирального фосфортиоата или хирального Н-фосфоната нуклеотида или нуклеиновой кислоты.
8-Ацил-2-тиоэтил пронуклеотид может быть синтезирован из нуклеиновой кислоты или нуклеотида, содержащего хиральный Н-фосфонат, как показано на следующей схеме:
Схема 1
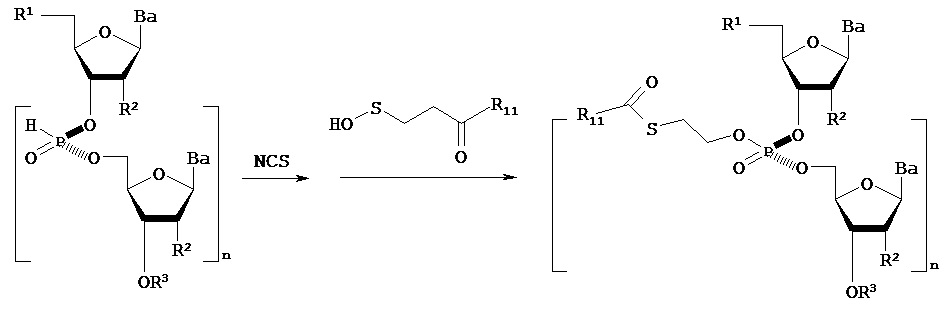
В некоторых вариантах R1 представляет собой -OP(O)(Re)2, тогда как Re представляет собой 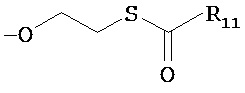 . Хиральный Н-фосфонат обрабатывают N-хлорсукцинимидом, и затем вводят в реакцию с 8-ацил-2-тиоэтилспиртом с получением 8-ацил-2-тиоэтил пролекарства. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
. Хиральный Н-фосфонат обрабатывают N-хлорсукцинимидом, и затем вводят в реакцию с 8-ацил-2-тиоэтилспиртом с получением 8-ацил-2-тиоэтил пролекарства. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
Ацилокси пролекарство нуклеиновой кислоты может быть синтезировано из нуклеиновой кислоты или нуклеотида, содержащего хиральный Н-фосфонат, как показано на следующей схеме:
Схема 2
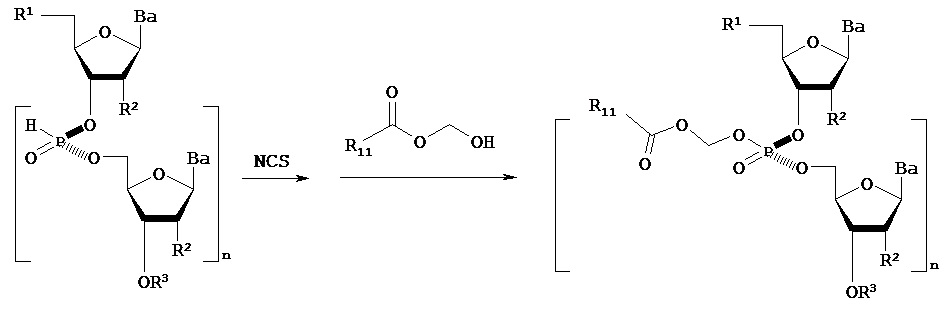
Хиральный Н-фосфонат обрабатывают N-хлорсукцинимидом, и затем вводят в реакцию с гидроксиметилацетатным соединением с получением ацилокси пролекарства. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
Тиоацилокси пролекарство нуклеиновой кислоты может быть синтезировано из нуклеиновой кислоты или нуклеотида, содержащего хиральный фосфортиоат, как показано на следующей схеме:
Схема 3
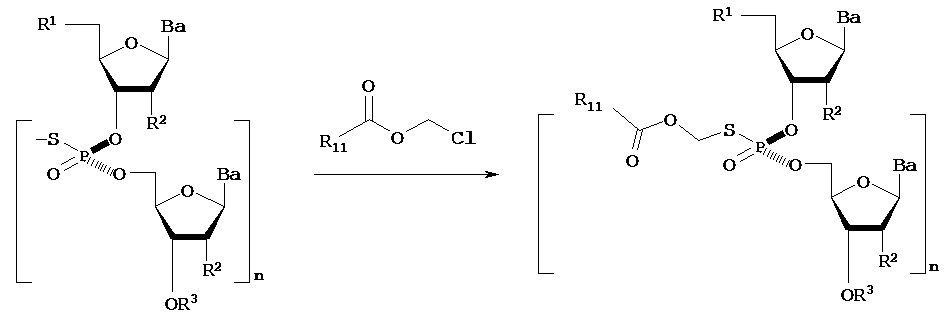
Хиральный фосфортиоат обрабатывают хлорметилацилокси соединением с получением ацилокси пролекарства. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
2-Карбоалкоксиэтил пролекарство нуклеиновой кислоты может быть синтезировано из нуклеиновой кислоты или нуклеотида, содержащего хиральный фосфортиоат, как показано на следующей схеме:
Схема 4
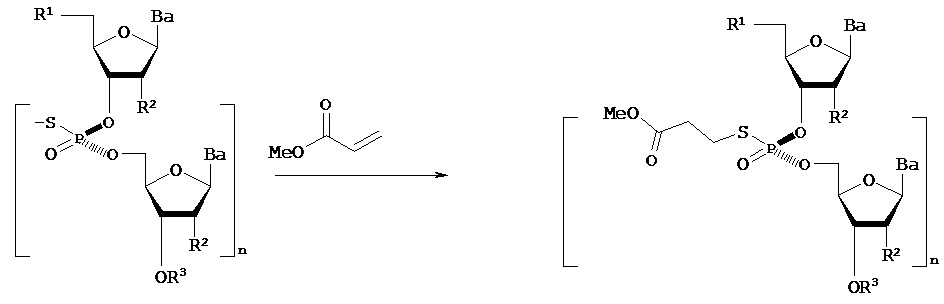
Депротонированный хиральный фосфортиоат реагирует с алкилакрилатом с образованием 2-карбоалкоксиэтил пронуклеотида. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
Дисульфидное пролекарство нуклеиновой кислоты может быть синтезировано из нуклеиновой кислоты или нуклеотида, содержащего хиральный фосфортиоат, как показано на следующей схеме:
Схема 5
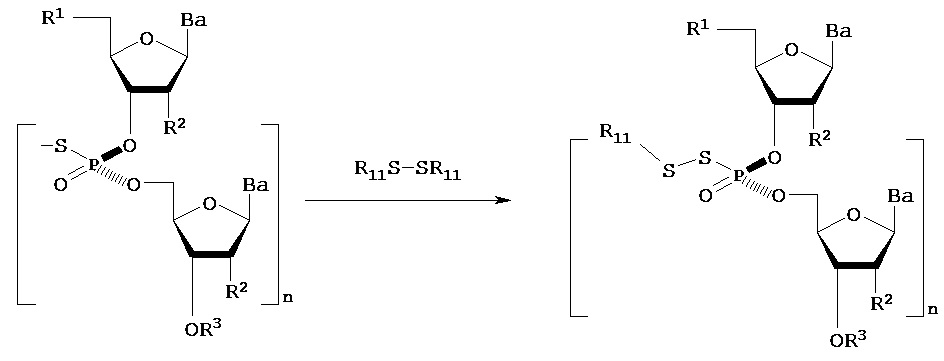
Депротонированный хиральный фосфортиоат реагирует с диалкилсульфидом с образованием алкил дисульфидного пронуклеотида. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
Тиоацетальное пролекарство нуклеиновой кислоты может быть синтезировано из нуклеиновой кислоты или нуклеотида, содержащего хиральный фосфортиоат, как показано на следующей схеме:
Схема 6
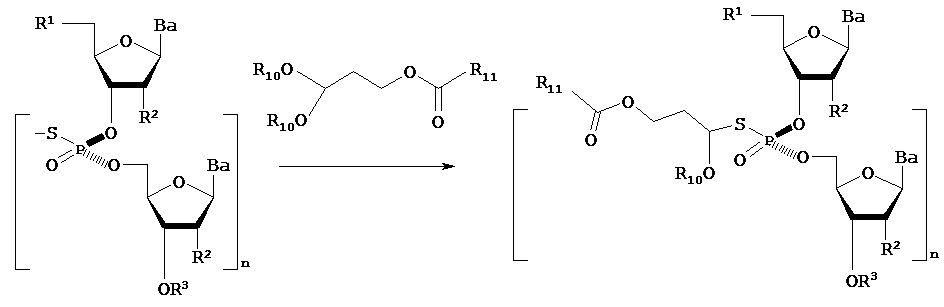
1,1-Диалкилокси 3-ацилоксипропан реагирует с триметилсилилтрифлатом, и депротонированный хиральный фосфортиоат затем добавляют к реакционной смеси с образованием тиоацетального пронуклеотида. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
Содержащее С3-енольный эфир пролекарство нуклеиновой кислоты может быть синтезирован из нуклеиновой кислоты или нуклеотида, содержащего хиральный фосфортиоат, как показано на следующей схеме:
Схема 7
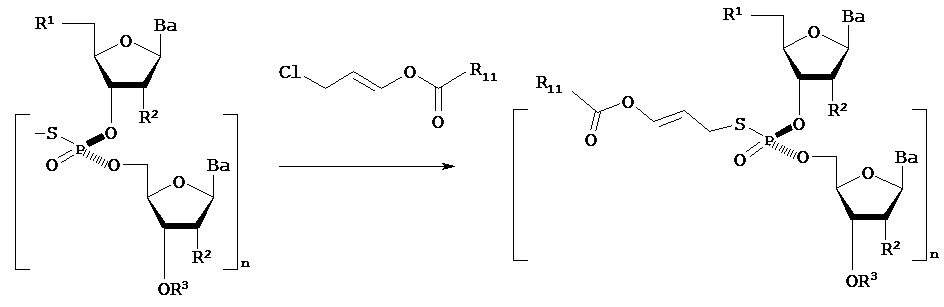
Депротонированный хиральный фосфортиоат реагирует с (Е)-3-хлор-1-ацилокси-проп-1-еновым соединением с образованием пролекарства С3-енольного эфира нуклеиновой кислоты. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
Содержащее С4-енольный эфир пролекарство нуклеиновой кислоты может быть синтезировано из нуклеиновой кислоты или нуклеотида, содержащего хиральный фосфортиоат, как показано на следующей схеме:
Схема 8
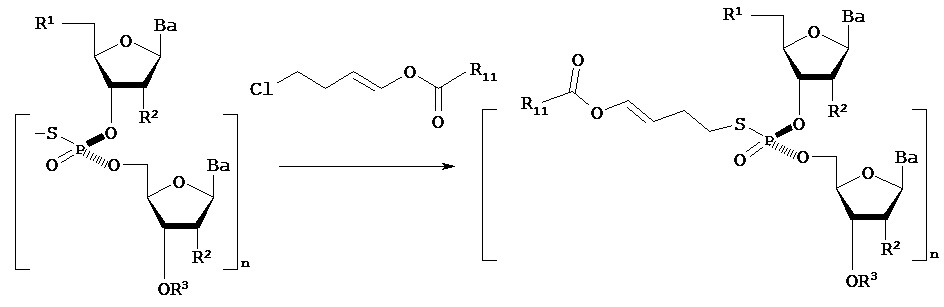
Депротонированный хиральный фосфортиоат реагирует с (Е)-3-хлор-1-ацилокси-бут-1-еновым соединением с образованием содержащего С3-енольный эфира нуклеиновой кислоты пролекарства. Защитные группы, присутствующие на R1, R2 и/или R3, в дальнейшем могут быть удалены.
В некоторых вариантах нуклеиновую кислоту, содержащую хиральный фосфортиоат или хиральный Н-фосфонат, синтезируют, как описано в данном описании. В других вариантах, другие способы синтеза могут применяться с получением нуклеиновой кислоты, содержащей хиральный фосфортиоат или хиральный Н-фосфонат.
Схема 9
Синтез содержащих хиральный фосфортиоат прекурсоров пролекарственных олигонуклеотидов по изобретению. (Путь А)
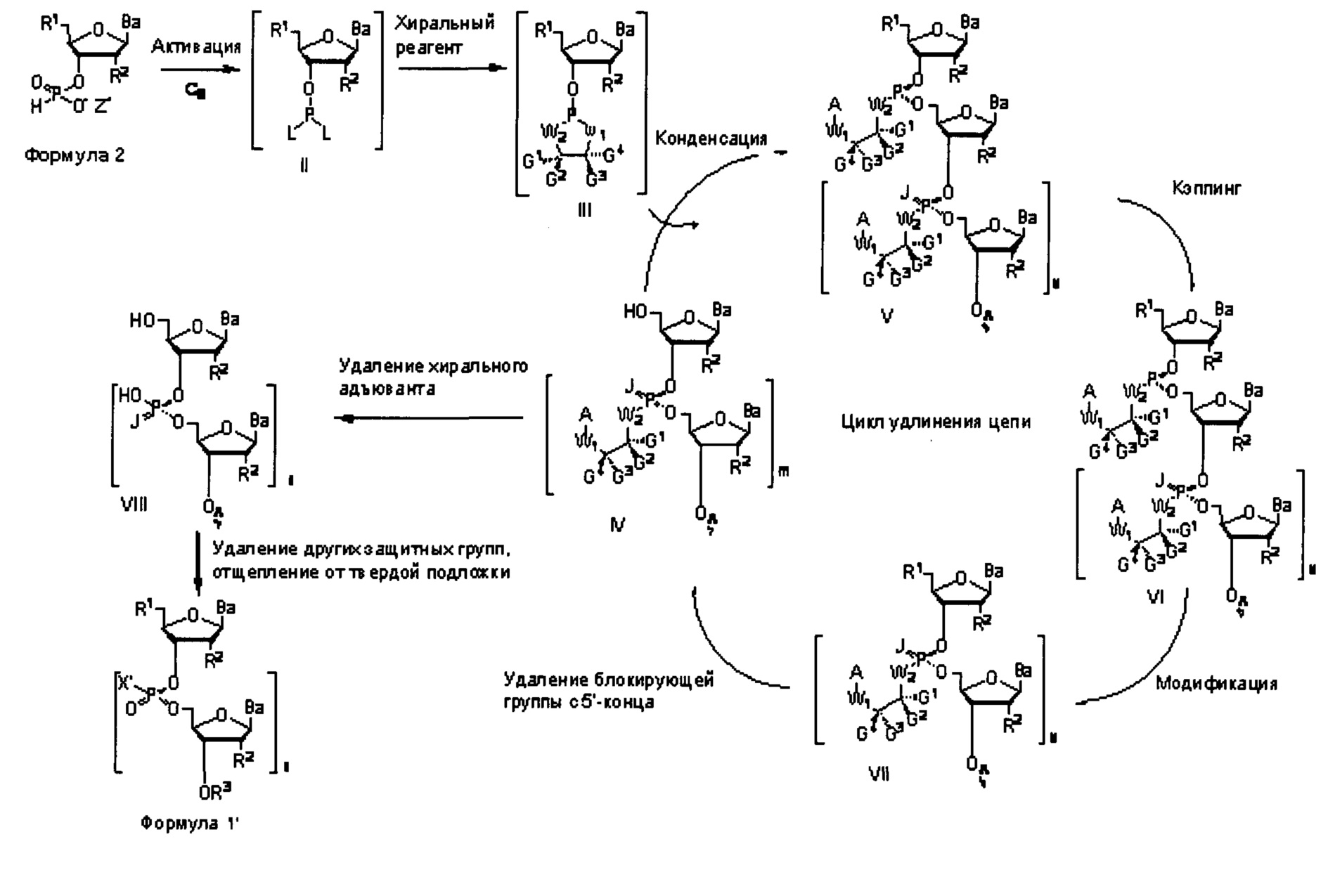
Реакция молекулы, содержащей ахиральный H-фосфонатный фрагмент Формулы 2, с нуклеозидом, содержащим нуклеофильный фрагмент Формулы IV, приводит к образованию конденсированного промежуточного соединения (V); который превращают в нуклеиновую кислоту, содержащую хиральный X'-фосфонатный фрагмент, который может быть дополнительно модифицирован для получения пролекарственного олигонуклеотида Формулы I, содержащего хиральный Х-фосфонатный фрагмент. Синтез конденсированного промежуточного соединения включает стадии (а) активации соединения Формулы 2 с помощью конденсирующего агента с образованием промежуточного соединения II, (б) реакцию с хиральным реагентом с образованием промежуточного соединения III, с последующей (в) реакцией с соединением Формулы IV.
Конденсированное промежуточное соединение может быть превращено в нуклеиновую кислоту, содержащую хиральный X'-фосфонатный фрагмент Формулы 1', путем кэппинга хиральной группы с помощью фрагмента А, который представляет собой ацильный, арильный, алкильный, аралкильный или силильный фрагмент, и модификации фосфора для введения J, который представляет собой S, Se или BH3, с получением таким образом соединения Формулы VII.
Соединение Формулы VII может быть превращено в соединение Формулы 1', где X' представляет собой S, Se или BH3 и n равно 1, путем отщепления хирального реагента и снятия блокировки блокирующей группой, при желании с отщеплением от твердой подложки. Альтернативно удлиняют цепь соединения Формулы VII путем снятия блокировки с 5'-конца и повторение стадий сочетания для получения конденсированного промежуточного соединения, как описано выше. Стадии кэппинга, модификации, снятия блокировки и удлинения цепи повторяют до тех пор, пока будет достигнуто целевое значение n. В этой точке, хиральные реагенты при каждом фосфонате отщепляют, остальные блокирующие группы отщепляют, в том числе, отщепляют от твердой подложки, при желании, с получением соединения Формулы 1', где X' представляет собой S, Se или BH3 и n≥2 и меньше приблизительно 200. Далее осуществляют превращения соединения Формулы 1', где X' представляет собой S, в соответствии со способами, описанными в данном описании, с получением про-олигонуклеотида соединения Формулы 1.
Модифицирующие агенты, используемые для введения S, Se или BH3 в положение при хиральном атоме фосфора конденсированного промежуточного соединения V в Пути А.
В некоторых вариантах модифицирующий агент представляет собой серосодержащий электрофил, селеносодержащий электрофил или борирующий агент. В некоторых вариантах серосодержащий электрофил представляет собой соединение следующей формулы:
S8 (Формула В), Z10-S-S-Z11 или Z10-S-X-Z11,
где Z10 и Z11 независимо представляют собой алкил, аминоалкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси, гетероарилокси, ацил, амид, имид или тиокарбонил, или Z10 и Z11 вместе образуют 3-8-членное алициклическое или гетероциклическое кольцо, которое может быть замещенным или незамещенным; Х представляет собой SO2, О или NRf и Rf представляет собой водород, алкил, алкенил, алкинил или арил. В других вариантах, серосодержащий электрофил представляет собой соединение Формулы В, С, D, Е или F:
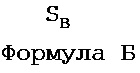
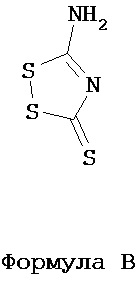
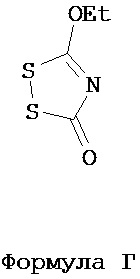
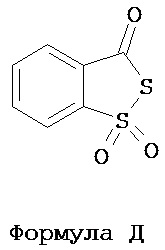
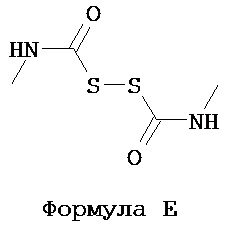
В других вариантах серосодержащий электрофил представляет собой соединение Формулы Е, Формулы Д или Формулы Б.
В некоторых вариантах селеносодержащий электрофил представляет собой соединение, структура которого представлена одной из следующих формул:
Se (Формула G), Z10-Se-Se-Z11 или Z10-Se-X-Z11,
где Z10 и Z11 независимо представляют собой алкил, аминоалкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси, гетероарилокси, ацил, амид, имид или тиокарбонил, или Z10 и Z11 вместе образуют 3-8-членное алициклическое или гетероциклическое кольцо, которое может быть замещенным или незамещенным; Х представляет собой SO2, S, О или NRf; и Rf представляет собой водород, алкил, алкенил, алкинил или арил.
В других вариантах селеносодержащий электрофил представляет собой соединение Формулы Ж, 3, И, К, Л или М.


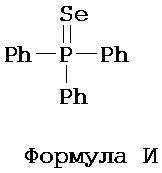
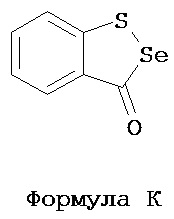
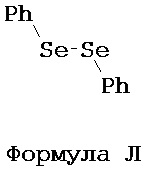
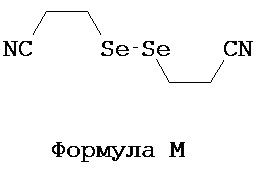
В некоторых вариантах селеносодержащий электрофил представляет собой соединение Формулы Ж или Формулы М.
В некоторых вариантах борирующий агент представляет собой боран-N,N-диизопропилэтиламин (ВН3⋅DIPEA, BH3⋅ДИПЭА), боран-пиридин (BH3⋅Ру), боран-2-хлорпиридин (BH3⋅СРу), боран-анилин (BH3⋅An), боран-тетрагидрофуран (BH3⋅THF, BH3⋅ТГФ) или боран-диметилсульфид (BH3⋅Me2S), анилин-цианоборан, трифенилфосфин-карбоалкоксибораны.
В других вариантах, борирующий агент представляет собой боран-N,N-диизопропилэтиламин (BH3⋅DIPEA, BH3⋅ДИПЭА), боран-2-хлорпиридин (BH3⋅СРу), боран-тетрагидрофуран (BH3⋅THF, BH3⋅ТГФ) или боран-диметилсульфид (BH3⋅Me2S).
Схема 10
Синтез прекурсора пролекарства олигонуклеотида через хиральные Н-фосфонаты (Путь Б).

В другом варианте, описанном на Схеме 10, ахиральный H-фосфонат Формулы 2 обрабатывают конденсирующим реагентом для получения промежуточного соединения структуры II. Промежуточное соединение структуры II в той же емкости обрабатывают без выделения хиральным реагентом с образованием хирального промежуточного соединения структуры III. Промежуточное соединение структуры III в той же емкости без выделения вводят в реакцию с нуклеозидом или модифицированным нуклеозидом структуры IX с получением хирального фосфатного соединения структуры X. В некоторых вариантах соединение структуры Х экстрагируют в растворитель для отделения его от побочных продуктов, примесей и/или реагентов. В других вариантах, если способ выполняют путем твердофазного синтеза, твердую подложку, содержащую соединение структуры X, отфильтровывают от побочных продуктов, примесей и/или реагентов. Соединение структуры Х обрабатывают кислотой для удаления блокирующей группы на 5'-конце растущей цепи нуклеиновой кислоты (структура XI). На стадии подкисления также удаляют хиральный вспомогательный лиганд с получением хирального Н-фосфоната IX. 5'-Разблокированному промежуточному соединению необязательно дают вернуться в цикл удлинения цепи для получения конденсированного промежуточного соединения, содержащего блокированный 5'-конец, который затем подкисляют для удаления блокирующей группы с 5'-конца и хирального вспомогательного лиганда.
Когда целевая длина цепи достигнута, для промежуточного соединения с удаленной с 5'-конца защитной группой проводят стадию модификации для введения фрагмента X, связанного с каждым из атомов фосфора, с получением соединения структуры XII. Модифицированное промежуточное соединение разблокируют путем удаления защитной группы, например, защитную группу в виде нуклеотидного основания, модифицированного нуклеотидного основания, сахара или модифицированного сахара удаляют, с получением нуклеиновой кислоты Формулы 1. В вариантах, где используют твердую подложку, модифицированную по атому фосфора нуклеиновую кислоту далее отщепляют от твердой подложки. В некоторых вариантах нуклеиновые кислоты остаются присоединенными к твердой подложке для последующей очистки, после которой их отщепляют от твердой подложки. В одном из вариантов синтез, описанный на Схеме 10, пригоден в случае, когда G1 и G2 в хиральном вспомогательном лиганде Формулы А не являются водородом.
Модификация соединения Формулы IX, полученного через Путь В, для введения фосфонатного фрагмента Х- или X'-.
Другие способы, применяемые для модификации соединения Формулы IX, полученного через Путь Б, проиллюстрированы на Схемах реакции 10а и 10б. Известно, что фосфонат и фосфит образуют таутомеры и существуют в равновесии. Фосфитный таутомер менее стабилен, чем фосфонатный таутомер. Равновесие сдвигается в направлении фосфонатного таутомера в нейтральных условиях вследствие очень высокой прочности связи Р=O. В кислых условиях, фосфорильная группа фосфоната становится обратимо протонированной. Расщепление связи Р-Н в промежуточном соединении происходит медленно с образованием фосфитного промежуточного соединения. Структуру IX далее модифицируют для получения структуры XII, с использованием реагентов, показанных на Схеме реакций 10а и 10б.
Схема реакции 10а
Модификация фосфорного центра промежуточных соединений, синтезированных через Путь Б, с использованием начального галогенирования при атоме фосфора.
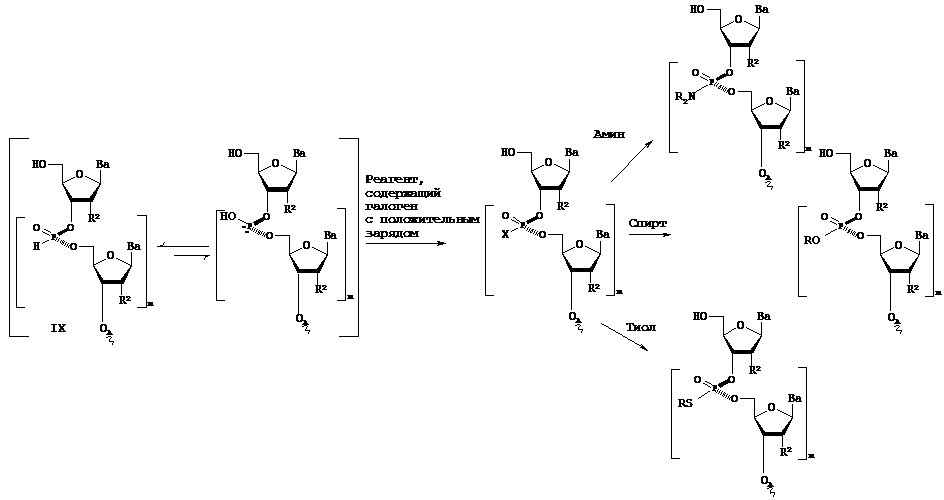
Схема реакции 10б
Модификация атома фосфора в промежуточных соединениях, синтезированных через Путь Б, с использованием начального силилирования.
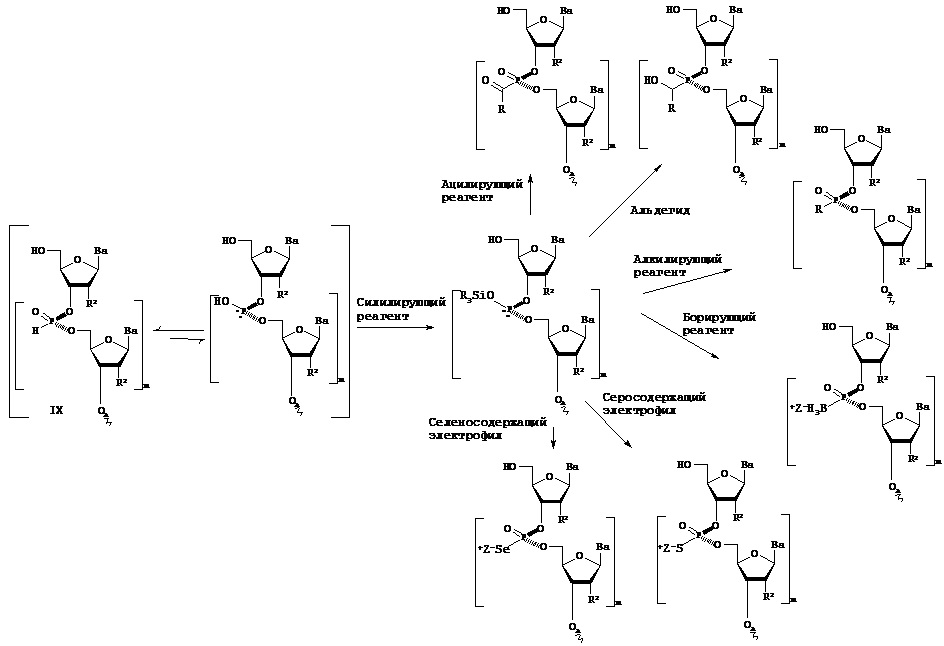
В некоторых вариантах стадию модификации выполняют путем реакции структуры IX с галогенирующим реагентом, с последующей реакцией с нуклеофилом. В конкретных вариантах, галогенирующий реагент представляет собой CCl4, CBr4, CI4, Cl2, Br2, I2, сульфурилхлорид (SO2Cl2), фосген, трифосген, серы монохлорид, серы дихлорид, хлорамин, CuCl2, N-хлорсукцинимид (NCS), N-бромсукцинимид (NBS) или N-йодсукцинимид (NIS). В других конкретных вариантах, галогенирующий реагент представляет собой CCl4, CBr4, Cl2, сульфурилхлорид (SO2Cl2) или N-хлорсукцинимид (NCS). В некоторых вариантах нуклеофил представляет собой первичные или вторичные акрилаты, спирты или тиолы. В других вариантах нуклеофил представляет собой NRfRfH, RfOH или RfSH, где Rf представляет собой водород, алкил, алкенил, алкинил или арил, и по меньшей мере один из Rf в NRfRfH не является водородом.
Стадия модификации также может быть выполнена в виде реакции структуры IX с силилирующим реагентом, с последующей реакцией с серосодержащим электрофилом, селеносодержащим электрофилом, борирующим агентом, алкилирующим агентом, альдегидом или ацилирующим агентом.
В конкретных вариантах силилирующий реагент представляет собой хлортриметилсилан (TMS-Cl, ТМС-Cl), триизопропилсилилхлорид (TIPS-Cl, ТИПС-Cl), трет-бутилдиметилсилилхлорид (TBDMS-Cl, ТБДМС-Cl), трет-бутилдифенилсилилхлорид (TBDPS-Cl, ТБДПС-Cl), 1,1,1,3,3,3-гексаметилдисилазан (HMDS, ГМДС), N-триметилсилилдиметиламин (TMSDMA, ТМСДМА), N-триметилсилилдиэтиламин (TMSDEA, ТМСДЭА), N-триметилсилилацетамид (TMSA, ТМСА), N,O-бис(триметилсилил)ацетамид (BSA, БСА) или N,O-бис(триметилсилил)трифторацетамид (BSTFA, БСТФА).
В других конкретных вариантах, серосодержащий электрофил представляет собой соединение, структура которого представлена одной из следующих формул:
S8 (Формула Б), Z10-S-S-Z11 или Z10-S-X-Z11,
где Z10 и Z11 независимо представляют собой алкил, аминоалкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси, гетероарилокси, ацил, амид, имид или тиокарбонил, или Z10 и Z11 вместе образуют 3-8-членное алициклическое или гетероциклическое кольцо, которое может быть замещенным или незамещенным; Х представляет собой SO2, О или NRf; и Rf представляет собой водород, алкил, алкенил, алкинил или арил. В других вариантах, серосодержащий электрофил представляет собой соединение Формулы Б, В, Г, Д или Е:
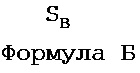




В других вариантах серосодержащий электрофил представляет собой соединение Формулы Е, Формулы Д или Формулы Б.
В некоторых вариантах селеносодержащий электрофил представляет собой соединение, структура которого представлена одной из следующих формул:
Se (Формула Ж), Z10-Se-Se-Z11 или Z10-Se-X-Z11,
где Z10 и Z11 независимо представляют собой алкил, аминоалкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси, гетероарилокси, ацил, амид, имид или тиокарбонил или Z10 и Z11 вместе образуют 3-8-членное алициклическое или гетероциклическое кольцо, которое может быть замещенным или незамещенным; Х представляет собой SO2, S, О или NRf; и Rf представляет собой водород, алкил, алкенил, алкинил или арил.
В других вариантах селеносодержащие представляет собой соединение Формулы Ж, 3, И, К, Л или М.






В некоторых вариантах селеносодержащий электрофил представляет собой соединение Формулы Ж или Формулы М.
В некоторых вариантах борирующий агент представляет собой боран-N,N-диизопропилэтиламин (ВН3⋅ДИПЭА), боран-пиридин (ВН3⋅Ру), боран-2-хлорпиридин (ВН3⋅СРу), боран-анилин (ВН3⋅An), боран-тетрагидрофуран (ВН3⋅ТГФ) или боран-диметилсульфид (BH3⋅Me2S), анилин-цианоборан, трифенилфосфин-карбоалкоксибораны. В других вариантах борирующий агент представляет собой боран-N,N-диизопропилэтиламин (ВН3⋅-ДИПЭА), боран-2-хлорпиридин (ВН3⋅CРу), боран-тетрагидрофуран (ВН3⋅ТГФ) или боран-диметилсульфид (BH3⋅Me2S).
В других вариантах алкилирующий агент представляет собой алкилгалогенид, алкенилгалогенид, алкинилгалогенид, алкилсульфонат, алкенилсульфонат или алкинилсульфонат.
В других вариантах альдегид представляет собой (пара)-формальдегид, алкилальдегид, алкенилальдегид, алкинилальдегид или арилальдегид.
В других вариантах ацилирующий агент представляет собой соединение Формулы О или П:
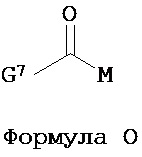
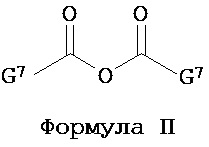
где G7 представляет собой алкил, циклоалкил, гетероцикл, циклоалкилалкил, гетероциклоалкил, арил, гетероарил, алкилокси, арилокси или гетероарилокси; и М представляет собой F, Cl, Br, I, 3-нитро-1,2,4-триазолимидазол, алкилтриазол, тетразол, пентафторбензол или 1-гидроксибензотриазол.
Схема 11
Синтез хирального динуклеозид фосфортиоата путем стереоселективного синтеза.
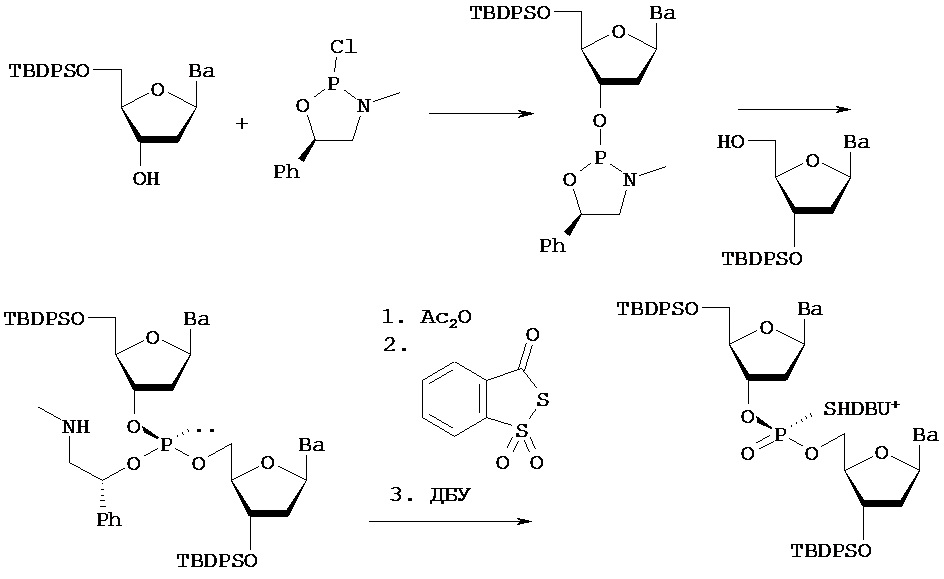
Один из способов стереоселективного синтеза динуклеозид фосфортиоата включает использовании стереохимически чистых 3'-фосфорамидитов, как описано Oka et al., (J. Am. Chem. Soc. (2003), 125:8307-17). Как показано на Схеме 6а (выше), производные 2-хлороксазафосфолидина вводят в реакцию с 5'-O-(ТБЖПС)нуклеозида с получением производного 3'-O-оксазафосфолидина. Реакция 3'-O-(ТБЖПС)нуклеозида с производным 3'-O-оксазафосфолидина в присутствии активатора, такого как N-(цианометил)пирролидин, дает динуклеозид фосфит в форме одного диастереомера. Динуклеозид фосфит может быть превращен в фосфортиоат в ходе 3-стадийного процесса, включающего ацетилирование с помощью уксусного ангидрида, сульфурирование с помощью реагента Бекаже (3Н-1,2-бензодитиол-3-он-1,1-диоксид; Iyer et al., J. Am. Chem. Soc. (1990), 112:1253-4), с отщеплением хирального вспомогательного лиганда с помощью избытка ДБУ. Защищенный динуклеозид фосфортиоат затем превращают в пролекарство способами, раскрытыми в данном описании.
Другие способы, пригодные для синтеза динуклеозид фосфортиоатов, включают ферментные способы (Hacia et al. Biochemistry (1994), 33:5367-9; Tang et al. Nucleosides Nucleotides (1995), 14:985-990), способы, включающие разделение смеси диастереомеров фосфортиоата, полученной не стереоселективными способами (Zon et al. Oligonucleotides and Analogues: A Practical Approach; IRL Press: London, 1991, pp 87-108), и способы, включающие стереоселективный синтез фосфортиоатов (Wilk et al. J. Am. Chem. Soc. 2000, 722, 2149-2156; Lu et al., Angew. Chem., Int. Ed. 2000, 39, 4521-4524; Iyer et al. Tetrahedron: Asymmetry 1995, 6, 1051-1054. Iyer et al. Tetrahedron Lett. 1998, 39, 2491-2494; Lu et al. Tetrahedron 2001, 57, 1677-1687. Stec et al. Nucleic Acids Res. 1991, 19, 5883-5888; Stec et al. J. Am. Chem. Soc. 1995, 777, 12019-12029; Uznan'ski et al. J. Am. Chem. Soc. 1992, 774, 10197-10202.
Обратный синтез нуклеиновой кислоты в направлении 5'-3'
Нуклеиновую кислоту Формулы 1, содержащую хиральный X-фосфонатный фрагмент, альтернативно синтезируют в направлении от 5' к 3’. В вариантах, где используют твердую подложку, нуклеиновую кислоту присоединяют к твердой подложке через 5'-конец растущей нуклеиновой кислоты, таким образом оставляя 3'-группу доступной для реакции, в том числе, ферментной реакции (например, дотирования и полимеризации). В некоторых вариантах такая ориентация достигается путем получения нуклеозидных мономеров, содержащих ахиральный H-фосфонатный фрагмент в положении 5' и защищенную гидроксильную группу в положении 3'. В одном из вариантов, нуклеиновую кислоту синтезируют в соответствии со Схемой 12. На Схеме 12, -R4 представляет собой -Orb, как определено выше, или, в последнем цикле синтеза, представляет собой R4, который эквивалентен R1, как определено в данном описании.
Схема 12
Синтез в направлении 5'-3' про-олигонуклеотида Формулы 1, содержащего хиральный Х-фосфонатный фрагмент.
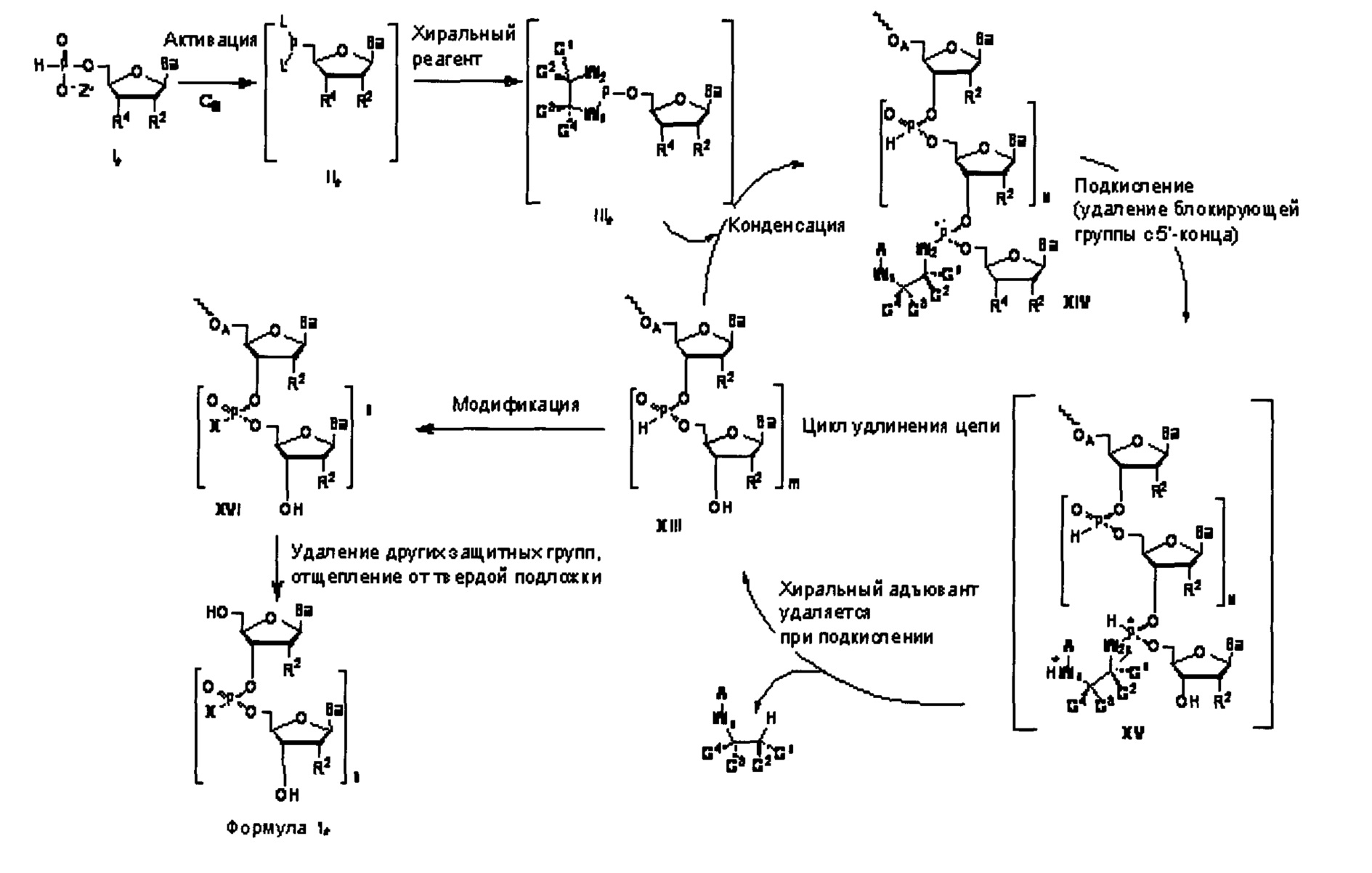
В варианте, описанном на Схеме 12, ахиральный H-фосфонат структуры Ir обрабатывают конденсирующим реагентом с образованием промежуточного соединения структуры IIr. Промежуточное соединение структуры IIr без выделения обрабатывают в той же емкости хиральным реагентом с получением промежуточного соединения структуры IIIr. Промежуточное соединение структуры IIIr без выделения вводят в той же емкости в реакцию с нуклеозидом или модифицированным нуклеозидом структуры XIII с получением хирального фосфитного соединения структуры XIV. В некоторых вариантах соединение структуры XIV экстрагируют в растворитель для отделения его от побочных продуктов, примесей и/или реагентов. В других вариантах, если способ выполняют путем твердофазного синтеза, твердую подложку, содержащую соединение структуры XIV отфильтровывают от побочных продуктов, примесей и/или реагентов. Соединение структуры XIV обрабатывают кислотой для удаления блокирующей группы на 5'-конце растущей цепи нуклеиновой кислоты (структура XV). На стадии подкисления также удаляют хиральный вспомогательный лиганд с получением хирального Н-фосфоната XIII. 3'-Разблокированному промежуточному соединению необязательно дают вернуться в цикл удлинения цепи для получения конденсированного промежуточного соединения, содержащего блокированный 3'-конец, который затем подкисляют для удаления блокирующей группы с 5'-конца и хирального вспомогательного лиганда. После по меньшей мере одного круга цикла удлинения цепи, для промежуточного соединения с удаленной с 3'-конца защитной группой проводят стадию модификации для введения фрагмента X, связанного с каждым из атомов фосфора, с получением соединения структуры XVI. Модифицированное промежуточное соединение разблокируют путем удаления защитной группы, например, защитную группу в виде нуклеотидного основания, модифицированного нуклеотидного основания, сахара или модифицированного сахара удаляют, с получением нуклеиновой кислоты Формулы 1. В других вариантах нуклеозид, содержащий фрагмент 3'-ОН, представляет собой промежуточное соединение с предыдущего цикла удлинения цепи, как описано в данном описании. В других вариантах нуклеозид, содержащий фрагмент 3'-ОН, представляет собой промежуточное соединение, полученное другим известным способом синтеза нуклеиновой кислоты. После цикла синтеза с использованием первого нуклеозида, нуклеозиды, нуклеотиды или нуклеиновые кислоты, содержащие незащищенный фрагмент -ОН, могут использоваться для последующих циклов удлинения цепи. В вариантах, где используют твердую подложку, модифицированная по атому фосфора нуклеиновая кислота далее может быть отщеплена от твердой подложки, расположенной на 5'-конце. В некоторых вариантах нуклеиновые кислоты остаются присоединенными к твердой подложке для последующей очистки, после которой их отщепляют от твердой подложки. В одном из вариантов синтез, описанный на Схеме 12, пригоден в случае, когда и G1, и G2 в хиральном вспомогательном лиганде Формулы А не являются водородом. Синтез в обратном направлении 5'-3' может быть выполнен с использованием таких же исходных материалов, как показано на Схеме 12, по механизму, аналогичному стадиям, описанным в Пути А.
Получение фосфотиотриэфиров с удаляемой защитной группой из Н-фосфоната
Фосфортиоаты могут быть синтезированы стереоспецифическим способом из Н-фосфонатов с сохранением конфигурации при атоме фосфора (J. Org. Chem. 1991, 3861-3869). Также подразумевается применение данной реакции для синтеза фосфортиотриэфиров с использованием тиолсодержащего фрагмента, который также несет биоудаляемую защитную группу, см.Схему 13. Дополнительно, также сообщалось о стереоконтролируемом твердофазном синтезе олигонуклеозид Н-фосфонатов (Angew. Chem. Int. Ed. 2009, 48, 496-499), и предусматривается сочетание указанного способа с алкилированием в ходе синтеза на твердой подложке, для получения фосфотиотриэфиров на подложке.
Схема 13
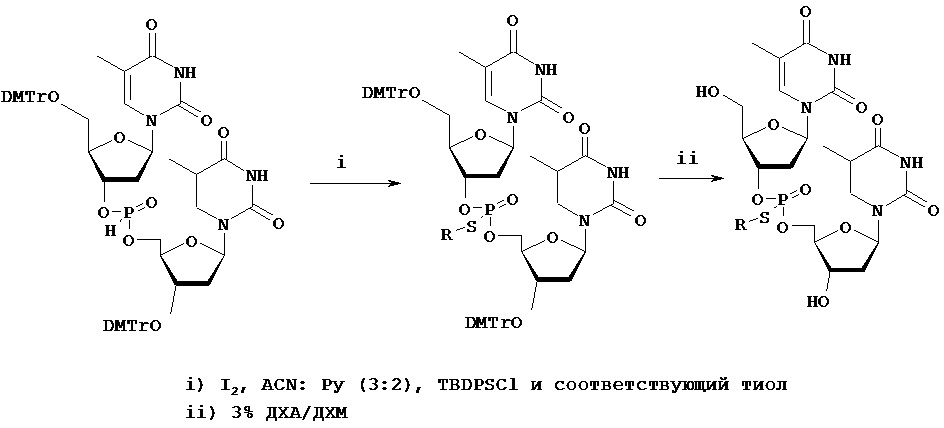
Условия реакции, применяемые в способах по изобретению. Условия
Стадии реакции молекулы, содержащей ахиральный H-фосфонатный фрагмент, и нуклеозида, содержащего фрагмент 5'-ОН, с образованием конденсированного промежуточного соединения, могут быть осуществлены без выделения каких-либо промежуточных соединений. В некоторых вариантах стадии реакции молекулы, содержащей ахиральный H-фосфонатный фрагмент, и нуклеозида, содержащего фрагмент 5'-ОН, с образованием конденсированного промежуточного соединения, могут быть проведены в одной и той же емкости. В одном из вариантов, молекулу, содержащую ахиральный H-фосфонатный фрагмент, конденсирующий реагент, хиральный реагент и соединение, содержащее свободный нуклеофильный фрагмент, добавляют к реакционной смеси в разных временных точках. В другом варианте молекула, содержащая ахиральный Н-фосфонатный фрагмент, конденсирующий реагент и хиральный реагент присутствуют в одной и той же реакционной емкости или сосуде. В другом варианте, молекула, содержащая ахиральный H-фосфонатный фрагмент, конденсирующий реагент, хиральный реагент и соединение, содержащее свободный нуклеофильный фрагмент, присутствуют в одной и той же реакционной емкости или сосуде. Это позволяет проводить реакцию без выделения промежуточных соединений и избежать требующих времени стадий, что дает возможность провести синтез экономично и эффективно. В конкретных вариантах, ахиральный H-фосфонат, конденсирующий реагент, хиральный аминоспирт и 5'-ОН нуклеозид присутствуют в реакционной смеси в одной и то же время. В дополнительном варианте, образование хирального промежуточного соединения для конденсации происходит in situ, и его не выделяют пере реакцией конденсации. В другом варианте, молекулу, содержащую ахиральный H-фосфонатный фрагмент, активируют реакцией с конденсирующим реагентом, хиральный реагентом в отдельной реакционной емкости, а не в той, которую используют для реакции хирального промежуточного соединения с соединением, содержащим свободный 5'-ОН фрагмент.
Синтез на твердой подложке
В некоторых вариантах синтез нуклеиновой кислоты проводят в растворе. В других вариантах синтез нуклеиновой кислоты проводят на твердой подложке. Реакционноспособные группы твердой подложки могут быть незащищенными или защищенными. В ходе синтеза олигонуклеотида твердую подложку обрабатывают различными реагентами в нескольких циклах синтеза для обеспечения постадийного удлинения растущей цепи олигонуклеотида отдельными нуклеотидными мономерами. Нуклеозидный мономер на конце цепи непосредственно соединенный с твердой подложкой, в данном описании называют "первым нуклеозидом". Первый нуклеозид связан с твердой подложкой посредством линкерного фрагмента, т.е. дирадикала с ковалентными связями как с полимером твердой подложки, так и с нуклеозидом. Линкер остается интактным в ходе циклом синтеза, проводимы для сборки олигонуклеотидной цепи, и расщепляется после сборки цепи для высвобождения олигонуклеотида из подложки.
Твердые подложки для твердофазного синтеза нуклеиновой кислоты включают подложки, описанные, например, патентах США 4,659,774, 5,141,813, 4,458,066; выданных Caruthers патентах США 4,415,732, 4,458,066, 4,500,707, 4,668,777, 4,973,679 и 5,132,418; выданных Andrus et al. патентах США 5,047,524, 5,262,530; и выданных Koster патентах США 4,725,677 (повторно выданных как Re34,069). В некоторых вариантах твердая фаза представляет собой подложку из органического полимера. В других вариантах твердая фаза представляет собой подложку из неорганического полимера. В некоторых вариантах органический полимер подложки представляет собой полистирол, аминометилполистирол, полиэтиленгликоль-полистирол перевитый сополимер, полиакриламид, полиметакрилат, поливиниловый спирт, полимер с высокой степенью поперечного сшивания (ВСПС) или другие синтетические полимеры, углеводы, такие как целлюлоза и крахмал, или другие полимерные углеводороды или другие органические полимеры, а также любые сополимеры, композитные материалы или комбинацию перечисленных выше неорганических или органических материалов. В других вариантах неорганический полимер подложки представляет собой кремния диоксид, алюминия оксид, контролируемое полистекло (КПС), которое представляет собой подложку из силикагеля или аминопропил-КПС. Другие пригодные твердые подложки включают фторированные твердые подложки (см., например, WO/2005/070859), твердые подложки из длинноцепочечного алкиламина (ДЦАА), стекла с контролируемым размером пор (КПП) (см., например, S.Р.Adams, K.S.Kavka, E.J.Wykes, S.В.Holder and G.R.Galluppi, J. Am. Chem. Soc., 1983, 105, 661-663; G.R.Gough, M.J.Bruden and P.T.Gilham, Tetrahedron Lett., 1981, 22, 4177-4180). Мембранные подложки и полимерные мембраны (см., например, Innovation and Perspectives in Solid Phase Synthesis, Peptides, Proteins and Nucleic Acids, ch 21 pp 157-162, 1994, Ed. Roger Epton и патент США 4,923,901) также пригодны для синтеза нуклеиновых кислот. После получения, в мембрану могут быть введены/модифицированы химическими способами функциональные группы для использования в синтезе нуклеиновой кислоты. В дополнение к присоединению функциональной группы к мембране, использование линкерной или спейсерной группы, присоединенной к мембране, может использоваться для минимизации стерического препятствия между мембраной и синтезированной цепью.
Другие подходящие твердые подложки включают широко известные в данной области как пригодные для использования в методологии твердофазного синтеза, в том числе, например, стекло, продаваемое под маркой подложки Primer™ 200, стекло с контролируемым размером пор (КПП), оксалильное стекло с контролируемым размером пор (см., например, Alul, et al., Nucleic Acids Research, 1991, 19, 1527), подложку из дериватизированного аминополиэтиленгликоля TentaGel Support (см., например, Wright, et al., Tetrahedron Lett., 1993, 34, 3373) и сополимер полистирола/дивинилбензола Poros.
Продемонстрировано использование полимеров с активированной поверхностью в синтезе природных и модифицированных нуклеиновых кислот и белков на нескольких видах твердых подложек. Материал твердой подложки может представлять собой любой полимер, пористость которого является достаточно однородной, который содержит достаточное количество аминогрупп и является достаточно гибким для проведения любых сопутствующих манипуляций без нарушения целостности. Примеры некоторых подходящих материалов включают нейлон, полипропилен, полиэфир, политетрафторэтилен, полистирол, поликарбонат и нитроцеллюлозу. Другие материалы могут служить в качестве твердой подложки, в зависимости от проекта исследователя. В комбинации с некоторыми видами проектов, например, металл с покрытием, в частности, может быть выбрано золото или платина (см., например, публикацию США №20010055761). В одном из вариантов синтеза олигонуклеотидов, например, нуклеозид заякорен на твердой подложке, которая функционализирована гидроксильными или аминными остатками. Альтернативно, твердую подложку дериватизируют с получением нестойкой к действию кислоты триалкокситритильной группы, такой как триметокситритильная группа (ТМТ). Без желания связываться с теорией, ожидается, что присутствие триалкокситритильной защитной группы будет позволять начальное детритилирование в широко используемых условиях на синтезаторах ДНК. Для более быстрого высвобождения олигонуклеотидного материала в раствор с помощью водного раствора аммиака, дигликолятный линкер необязательно вводят на подложку.
Линкерный фрагмент
Линкерный фрагмент или линкер необязательно используют для соединения твердой подложки с соединением, содержащим свободный нуклеофильный фрагмент. Подходящие линкеры известны, например, короткие молекулы, которые служат для соединения твердой подложки с функциональными группами (например, гидроксильными группами) начальных молекул нуклеозидов в техниках твердофазного синтеза. В некоторых вариантах линкерный фрагмент представляет собой линкер на основе сукцинаминовой кислоты или сукцинатный линкер (-CO-CH2-CH2-СО-) или оксалильный линкер (-CO-CO-). В других вариантах линкерный фрагмент и нуклеозид соединены вместе посредством эфирной связи. В других вариантах линкерный фрагмент и нуклеозид соединены вместе посредством амидной связи. In дополнительных вариантах линкерный фрагмент соединяет нуклеозид с другим нуклеотидом или нуклеиновой кислотой. Подходящие линкеры раскрыты, например, в Oligonucleotides And Analogues A Practical Approach, Ekstein, F. Ed., IRL Press, N.Y., 1991, Chapter 1.
Линкерный фрагмент используют для связи соединения, содержащего свободный нуклеофильный фрагмент, с другим нуклеозидом, нуклеотидом или нуклеиновой кислотой. В некоторых вариантах линкерный фрагмент представляет собой фосфодиэфирную связь. В других вариантах линкерный фрагмент представляет собой H-фосфонатный фрагмент. В других вариантах линкерный фрагмент представляет собой Х-фосфонатный фрагмент.
Растворители для синтеза
Синтез нуклеиновых кислот выполняют в апротонном органическом растворителе. В некоторых вариантах растворитель представляет собой ацетонитрил, пиридин, тетрагидрофуран или дихлорметан. В некоторых вариантах, если апротонный органический растворитель не имеет основной природы, на стадии реакции присутствует основание. В некоторых вариантах, если присутствует основание, основание представляет собой пиридин, хинолин или N,N-диметиланилин. Другие примеры оснований включают пирролидин, пиперидин, N-метилпирролидин, пиридин, хинолин, N,N-диметиламинопиридин (ДМАП) или N,N-диметиланилин. В некоторых вариантах апротонный органический растворитель является безводным. В других вариантах безводный апротонный органический растворитель является свежеперегнанным. В некоторых вариантах свежеперегнанный безводный апротонный органический растворитель представляет собой пиридин. В других вариантах свежеперегнанный безводный апротонный органический растворитель представляет собой тетрагидрофуран. В других вариантах свежеперегнанный безводный апротонный органический растворитель представляет собой ацетонитрил.
Условия подкисления для удаления блокирующей группы.
Подкисление для удаления блокирующей группы осуществляют с помощью кислоты Бренстеда или кислоты Льюиса. В некоторых вариантах подкислением применяют для удаления блокирующей R1 группы. Пригодными кислотами Бренстеда являются карбоновые кислоты, алкилсульфоновые кислоты, арилсульфоновые кислоты, фосфорная кислота и ее производные, фосфоновая кислота и ее производные, алкилфосфоновые кислоты и их производные, арилфосфоновые кислоты и их производные, фосфиновая кислота, диалкилфосфиновые кислоты и диарилфосфиновые кислоты со значением рКа (25°C в воде) от -0,6 (трифторуксусная кислота) до 4,76 (уксусная кислота) в органическом растворителе или воде (в случае 80% уксусной кислоты). Концентрация кислоты (от 1 до 80%), применяемая на стадии подкисления, зависит от кислотности кислоты. Сила кислоты должна быть принята во внимание, поскольку сильнокислые условия будут приводить к депуринированию/депиримидинированию, когда пуринильные или пиримидинильные основания отщепляются от рибозного кольца.
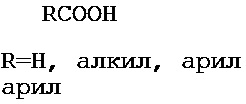
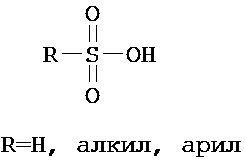
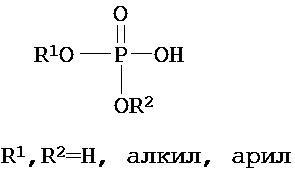
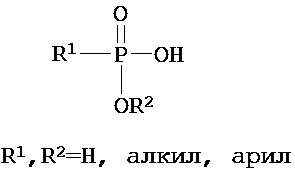
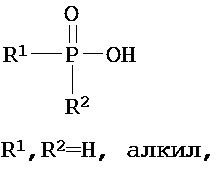
В некоторых вариантах подкисление осуществляют с помощью кислоты Льюиса в органическом растворителе. Пригодные кислоты Льюиса представляют собой ZnX2, где Х представляет собой Cl, Br, I или CF3SO3.
В некоторых вариантах подкисление включает добавление количества кислоты Бернстеда или кислоты Льюиса, эффективного для превращения конденсированного промежуточного соединения в соединение Формулы 4 без удаления пуриновых фрагментов из конденсированного промежуточного соединения.
Кислоты, пригодные для стадии подкисления также включают, не ограничиваясь ими, 10% фосфорную кислоту в органическом растворителе, 10% хлористоводородную кислоту в органическом растворителе, 1% трифторуксусную кислоту в органическом растворителе, 3% дихлоруксусную кислоту в органическом растворителе или 80% уксусную кислоту в воде. Концентрацию любой кислоты Бернстеда или кислоты Льюиса, используемой в ходе процесса, выбирают таким образом, что концентрация кислоты не превышает концентрации, вызывающей отщепления нуклеотидного основания от сахарного фрагмента.
В некоторых вариантах подкисление включает добавление 1% трифторуксусной кислоты в органический растворитель. В некоторых вариантах подкисление включает добавление от приблизительно 0,1% до приблизительно 8% трифторуксусной кислоты в органическом растворителе. В других вариантах подкисление включает добавление 3% дихлоруксусной кислоты в органическом растворителе. В других вариантах подкислением включает добавление от приблизительно 0,1% до приблизительно 10% дихлоруксусной кислоты в органическом растворителе. В других вариантах подкислением включает добавление 3% трихлоруксусной кислоты в органическом растворителе. В других вариантах подкислением включает добавление от приблизительно 0,1% до приблизительно 10% трихлоруксусной кислоты в органическом растворителе. В некоторых вариантах подкисление включает добавление 80% уксусной кислоты в воде. В некоторых вариантах подкислением включает добавление от приблизительно 50% до приблизительно 90% или от приблизительно 50% до приблизительно 80%, от приблизительно 50% до приблизительно 70%, от приблизительно 50% до приблизительно 60%, от приблизительно 70% до приблизительно 90% уксусной кислоты в воде. В некоторых вариантах подкислением включает дополнительное добавление средств для связывания катионов к кислому растворителю. В конкретных вариантах средства для связывания катионов могут представлять собой триэтилсилан или триизопропилсилан. В некоторых вариантах блокирующую группу удаляют с R1 до проведения стадии подкисления конденсированного промежуточного соединения. В некоторых вариантах блокирующую группу удаляют с R1 подкислением, которое включает добавление 1% трифторуксусной кислоты в органическом растворителе. В некоторых вариантах блокирующую группу удаляют с R1 подкислением, которое включает добавление 3% дихлоруксусной кислоты в органическом растворителе. В некоторых вариантах блокирующую группу удаляют с R1 подкислением, которое включает добавление 3% трихлоруксусной кислоты в органический растворитель.
Удаление блокирующих фрагментов или групп
Функциональные группы, такие как гидроксильный или аминный фрагмент, которые расположены на нуклеиновых основаниях или сахарных фрагментах, обычно блокируют с помощью блокирующих защитных групп (фрагментов) в ходе синтеза, и затем удаляют блокирующие группы. В целом, блокирующая группа, защищающая химическую функциональную группу в молекуле, является инертной по отношению к специфическим условиям реакции, и позже может быть удалена из такой функциональной группы в молекуле без значительного ущерба для остальной части молекулы (см., например. Green and Wuts, Protective Groups in Organic Synthesis, 2nd Ed., John Wiley & Sons, New York, 1991). Например, аминогруппы могут быть блокированы группой, блокирующей атом азота, такой как фталимидо, 9-флудренилметоксикарбонил (FMOC), трифенилметилсульфенил, трет-ВОС, 4,4'-диметокситритил (DMTr, ДМТр), 4-метокситритил (MMTr, ММТр), 9-фенилксантин-9-ил (Pixyl), тритил (Tr) или 9-(n-метоксифенил)ксантин-9-ил (MOX, МОК). Карбоксильные группы могут быть защищены в форме ацетильных групп.Гидроксильные группы могут быть защищены, например, тетрагидропиранилом (TGP, ТГП), трет-бутилдиметилсилилом (TBDMS, ТБДМС), 1-[(2-хлор-4-метил)фенил]-4-метоксипиперидин-4-илом (Ctmp), 1-(2-фторфенил)-4-метоксипиперидин-4-илом (Fpmp), 1-(2-хлорэтокси)этил, 3-метокси-1,5-дикарбометоксипентап-3-илом (MDP, МДП), бис(2-ацетоксиэтокси)метилом (FCE, АЦЕ), триизопропилсилилоксиметилом (TOM, ТОМ), 1-(2-цианоэтокси)этилом (СЕЕ, ЦЭЭ), 2-цианоэтоксиметилом (СЕМ, ЦЭМ), [4-(N-дихлорацетил-N-метиламино)бензилокси]метилом, 2-цианоэтилом (CN, ЦН), пивалоилоксиметилом (PivOM), левунилоксиметилом (ALE, АЛЕ). Описаны другие характерные блокирующие группы для гидроксильной группы (см., например, Beaucage et al., Tetrahedron, 1992, 46, 2223). В некоторых вариантах блокирующие группы для гидроксильной группы представляют собой нестойкие к действию кислоты группы, такие как тритил, монометокситритил, диметокситритил, триметокситритил, 9-фенилксантин-9-ил (Pixyl) и 9-(n-метоксифенил)ксантин-9-ил (MOX, МОК). Химические функциональные группы также могут быть блокированы, в том числе в форме прекурсора. Таким образом, азидная группа может рассматриваться как блокированная форма амина, поскольку азидная группа легко превращается в амин. Известны другие характерные защитные группы, используемые в синтезе нуклеиновых кислот, например, Agrawal et al., Protocols for Oligonucleotide Conjugates, Eds., Humana Press, New Jersey, 1994, Vol.26, pp.1-72).
Различные способы известны и применяются для удаления блокирующих групп из нуклеиновой кислоты. В некоторых вариантах все блокирующие группы удаляют. В других вариантах удаляют только часть блокирующих групп. В других вариантах, условия реакции могут быть отрегулированы для удаления блокирующих групп в некоторых фрагментах. В некоторых вариантах, где R2 представляет собой блокирующую группу, удаление блокирующей группы с R2 является ортогональным по отношению к удалению блокирующей группы с R1. Блокирующие группы в R1 и R2 остаются интактными в ходе стадий синтеза и одновременно удаляются после сборки цепи. В некоторых вариантах блокирующую группу R2 удаляют одновременно с отщеплением нуклеиновых кислот от твердой подложки и с удалением группы, блокирующей нуклеиновое основание. В конкретных вариантах блокирующую группу в R1 удаляют, тогда как блокирующие группы в R2 и нуклеиновых основаниях остаются интактными. Блокирующие группы в R1 отщепляют от твердой подложки с помощью органического основания, такого как первичный амин, вторичный амин или их смесь. Удаление блокирующей группы из положения R1 обычно называют снятием защиты с фронтального конца.
В одном из вариантов группы, блокирующие нуклеиновое основание, если они присутствуют, отщепляются после сборки соответствующей нуклеиновой кислоты, используя кислый реагент. В другом варианте одну или больше из блокирующих нуклеиновое основание групп отщепляют в условиях, не являющихся ни кислыми, ни основными, например, отщепляют с помощью соли фторида или комплексов фтороводородной кислоты. В другом варианте одну или больше из блокирующих нуклеиновое основание групп отщепляют после сборки соответствующей нуклеиновой кислоты в присутствии основание или основного растворителя, где блокирующая нуклеиновое основание группа является устойчивой к условиям стадии снятия защиты с фронтального конца с помощью акрилатов.
В некоторых вариантах нет необходимости в блокирующих группах для нуклеиновых основаниях. В других вариантах блокирующие группы для нуклеиновых оснований необходимы. В других вариантах для некоторых нуклеиновых оснований блокирующая группа необходима, тогда как для других нуклеиновых оснований блокирующая группа не является необходимой. В некоторых вариантах, если нуклеиновые основания блокированы, блокирующие группы полностью или частично удаляют в условиях, подходящих для удаления блокирующей группы на фронтальном конце. Например, R1 может обозначать ORa, где Ra представляет собой ацил, и Ва обозначает гуанин, блокированный ацильной группой, в том числе, но не ограничиваясь ими, изобутирил, ацетил или 4-(трет-бутилфенокси)ацетил. Ацильные группы в R1 и Ва будут удалены или частично удалены в ходе одной и той же стадии снятия блокировки.
Реагенты
Конденсирующий реагент
Структура конденсирующего реагента (CR), пригодного в способах по изобретению, представлена одной из следующих общих формул:
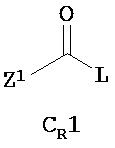 ,
, 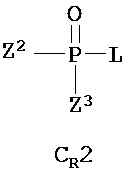 ,
, 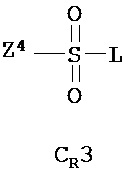 ,
, 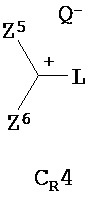 or
or 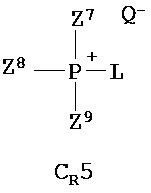
где Z1, Z2, Z3, Z4, Z5, Z6, Z7, Z8 и Z9 независимо выбраны из алкила, аминоалкила, циклоалкила, гетероцикла, циклоалкилалкила, гетероциклоалкила, арила, гетероарила, алкилокси, арилокси или гетероарилокси, или, где любая из пар Z2 и Z3, Z5 и Z6, Z7 и Z8, Z8 и Z9, Z9 и Z7 или Z7 и Z8 и Z9 вместе образуют 3-20-членное алициклическое или гетероциклическое кольцо; Q- представляет собой противоанион; и L представляет собой уходящую группу.
В некоторых вариантах противоион конденсирующего реагента CR представляет собой Cl-, Br-, 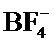 ,
, 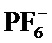 , TfO-, Tf2N-,
, TfO-, Tf2N-, 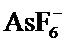 ,
, 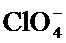 или
или 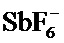 , где Tf представляет собой CF3SO2. В некоторых вариантах уходящая группа конденсирующего реагента CR представляет собой F, Cl, Br, I, 3-нитро-1,2,4-триазол, имидазол, алкилтриазол, тетразол, пентафторбензол или 1-гидроксибензотриазол.
, где Tf представляет собой CF3SO2. В некоторых вариантах уходящая группа конденсирующего реагента CR представляет собой F, Cl, Br, I, 3-нитро-1,2,4-триазол, имидазол, алкилтриазол, тетразол, пентафторбензол или 1-гидроксибензотриазол.
Примеры конденсирующих агентов, которые могут быть использованы в ходе процесса, включают, на ограничиваясь ими, пентафторбензоилхлорид, карбонилдиимидазол (CDI, КДИ), 1-мезитиленсульфонил-3-нитротриазол (MCNT, МСНТ), 1-этил-3-(3'-диметиламинопропил)карбодиимида гидрохлорид (EDCI-HCl, ЭДКИ-HCl), бензотриазол-1-илокситрис(диметиламино)фосфония гексафторфосфат (РуВОР), N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl), 2-(1H-7-азабензотриазол-1-ил)-1,1,3,3-тетраметилурония гексафторфосфат (HATU, ГАТУ) и O-бензотриазол-N,N,N',N'-тетраметилурония гексафторфосфат (HBTU, ГБТУ), DIPDCI (ДИПКДИ); N,N'-бис(2-оксо-3-оксазолидинил)фосфиния бромид (BopBr), 1,3-диметил-2-(3-нитро-1,2,4-триазол-1-ил)-2-пирролидин-1-ил-1,3,2-диазафосфолидин гексафторфосфат (MNTP, МНТП), 3-нитро-1,2,4-триазол-1-ил-трис(пирролидин-1-ил)фосфония гексафторфосфат (PyNTP), бромтрипирролидинофосфония гексафторфосфат (РуBrOP); O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония тетрафторборат (TBTU, ТБТУ); и тетраметилфторформамидиния гексафторфосфат (TFFG, ТФФГ). В некоторых вариантах противоион конденсирующего реагента CR представляет собой Cl-, Br-, 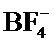 ,
, 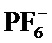 , TfO-, Tf2N-,
, TfO-, Tf2N-, 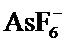 ,
, 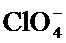 или
или 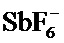 , где Tf представляет собой CF3SO2.
, где Tf представляет собой CF3SO2.
В других вариантах изобретения, конденсирующий реагент представляет собой 1-(2,4,6-триизопропилбензолсульфонил)-5-(пиридин-2-ил)тетразолид, пивалоилхлорид, бромтриспирролидинофосфония гексафторфосфат, N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl) или 2-хлор-5,5-диметил-2-оксо-1,3,2-диохафосфинан. В одном из вариантов конденсирующий реагент представляет собой N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl). Описаны другие известные конденсирующие реагенты (см., например, WO/2006/066260).
В других вариантах конденсирующий реагент представляет собой 1,3-диметил-2-(3-нитро-1,2,4-триазол-1-ил)-2-пирролидин-1-ил-1,3,2-диазафосфолидиния гексафторфосфат (МНТП) или 3-нитро-1,2,4-триазол-1-ил-трис(пирролидин-1-ил)фосфония гексафторфосфат (PyNTP).
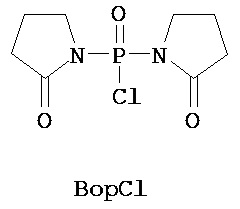
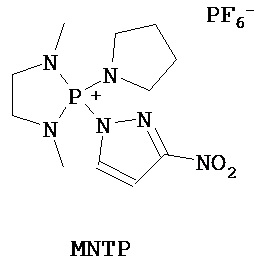
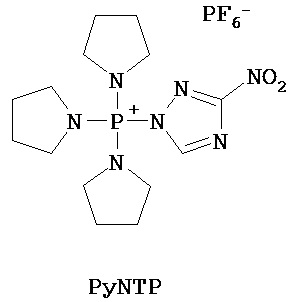
Хиральный реагент
В способах по данному изобретению, хиральные реагенты используются для обеспечения стереоселективности в образовании Х-фосфонатных связей. Множество различных хиральных вспомогательных реагентов может использоваться в данном процессе, которые представляют собой соединения Формулы 3-I, где W1 и W2 представляют собой любой из -O-, -S- или -NG5-, способные реагировать с H-фосфонатным исходным материалом, соединением Формулы 2, с образованием хирального промежуточного соединения, как показано в структуре III на Схемах 5 и 6.
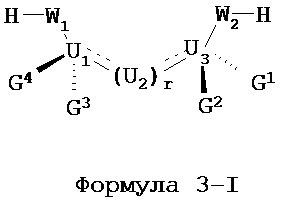
U1 и U3 представляют собой атомы углерода, соединенные с U2, если он присутствует, или друг с другом, если r равно 0, посредством одинарной, двойной или тройной связи. U2 представляет собой -С-, -CG8-, -CG8G8-, -NG8-, -N-, -О- или -S-, где r равно целому числу от 0 до 5, и не более двух гетероатомов являются смежными. Если любой один из U2 представляет собой С, тройная связь должна быть образована со вторым U2, который представляет собой С или с одним из U1 или U3. Подобным образом, если любой один из U2 представляет собой CG8, двойная связь образуется со вторым U2, который представляет собой -CG8- или -N-, или с одним из U1 или U3.
Например, в некоторых вариантах, -U1-(U2)r-U3- представляет собой -CG3G4-CG1G2-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -CG3=CG1-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -С≡С-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -CG3=C G8-CG1G2-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -CG3G4-O-CG1G2-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -CG3G4-NG8-CG1G2-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -CG3G4-N-CG2-. В некоторых вариантах -U1-(U2)r-U3- представляет собой -CG3G4-N=C G8-CG1G2-.
G1, G2, G3, G4, G5 и G8 независимо представляют собой водород, алкил, аралкил, циклоалкил, циклоалкилалкил, гетероциклил, гетарил или арил, или два из G1, G2, G3, G4 и G5 представляют собой G6 и, взятые вместе, образуют насыщенное, частично ненасыщенное или ненасыщенное карбоциклическое или содержащее гетероатом кольцо, содержащее до приблизительно 20 атомов в кольце, которое является моноциклическим или полициклическим и является конденсированным или неконденсированным. В некоторых вариантах образованное таким образом кольцо замещено оксо, тиоксо, алкильным, алкенильным, алкинильным, гетероарильным или арильным фрагментами. В некоторых вариантах, если кольцо, образованное двумя G6, является замещенным, оно замещено фрагментом, достаточно объемным для обеспечения стереоселективности в ходе реакции.
Например, в некоторых вариантах, кольцо, образованное двумя из G6 вместе, представляет собой циклопентил, пирролил, циклопропил, циклогексенил, циклопентенил, тетрагидропиранил или пиперазинил.
В некоторых вариантах изобретения хиральный реагент представляет собой соединение Формулы 3.
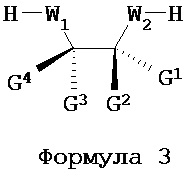
В некоторых вариантах Формулы 3, W1 и W2 независимо представляют собой -NG5-, -О- или -S-; G1, G2, G3, G4 и G5 независимо представляют собой водород, алкил, аралкил, циклоалкил, циклоалкилалкил, гетероциклил, гетарил или арил, или два из G1, G2, G3, G4 и G5 представляют собой G6 и, взятые вместе, образуют насыщенное, частично ненасыщенное или ненасыщенное карбоциклическое или содержащее гетероатом кольцо, содержащее до приблизительно 20 атомов в кольце, которое является моноциклическим или полициклическим, конденсированным или неконденсированным, и не более четырех из G1, G2, G3, G4 и G5 представляют собой G6. Подобно соединениям Формулы 3', любой из G1, G2, G3, G4 или G5 замещен оксо, тиоксо, алкильным, алкенильным, алкинильным, гетероарильным или арильным фрагментами. В некоторых вариантах такое замещение обеспечивает стереоселективность в ходе образования Х-фосфоната.
В некоторых вариантах изобретения, структура хирального реагента представлена одной из следующих Формул:
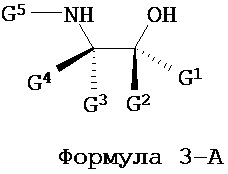
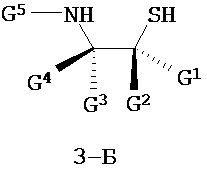
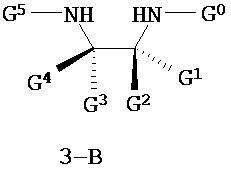
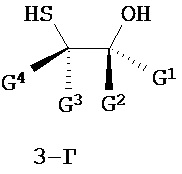
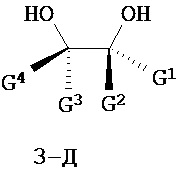
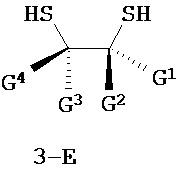
В некоторых вариантах хиральный реагент представляет собой аминоспирт. В некоторых других вариантах хиральный реагент представляет собой аминотиол. В других вариантах хиральный реагент представляет собой аминофенол. В некоторых вариантах хиральный реагент представляет собой (S)- и (-R)-2-метиламино-1-фенилэтанол, (1R, 2S)-эфедрин или (1R, 2S)-2-метиламино-1,2-дифенилэтанол.
В других вариантах по изобретению хиральный реагент представляет собой соединение, структура которого представлена одной из следующих формул:
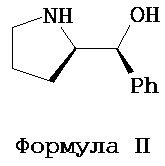
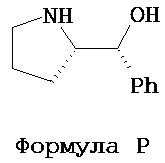
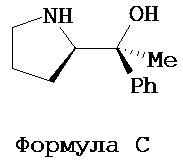
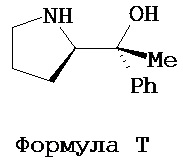
Выбор хирального реагента, например, изомера, представленного Формулой П, или его стереоизомера, представленного Формулой Р, позволяет осуществить специфический контроль хиральности атома фосфора. Таким образом, RP или SP конфигурация может быть выбрана в каждом цикле синтеза, что дает возможность контролировать общую трехмерную структуру полученной нуклеиновой кислоты. В некоторых вариантах изобретения, все стереоцентры полученной нуклеиновой кислоты находятся в RP конфигурации. В некоторых вариантах изобретения, все стереоцентры полученной нуклеиновой кислоты находятся в SP конфигурации. В некоторых вариантах выбор конфигурации центров RP и SP обеспечивает конкретную трехмерную суперструктуру цепи нуклеиновой кислоты.
Стереохимия олигонуклеозид фосфортиоатных связей
Показан терапевтический потенциал олигонуклеозид фосфортиоатов (Stein et al., Science (1993), 261:1004-12; Agrawal et al., Antisence Res. and Dev. (1992), 2:261-66; Bayever et al., Antisense Res. and Dev. (1993), 3:383-390). Олигонуклеозид фосфортиоаты, полученные без учета их стереохимии фосфортиоата, существуют в виде смеси 2n диастереомеров, где n равно количество внутринуклеотидных фосфортиоатных связей. Химические и биологические свойства указанных диастереомерных фосфортиоатов могут быть различными. Например, Wada et al. (Nucleic Acids Symposium Series No. 51 p.119-120; doi:10,1093/nass/nrm060) обнаружили, что стереоопределенный-(Rp)-(Ups)9U/(Ap)9A дуплекс показал более высокое значение Tm, чем природный-(Up)9U(Ар)9А и стереоопределенный-(Sp)-(Ups)9U, не сформировавшие дуплекс. В другом примере, в исследовании Tang et al., (Nucleosides Nucleotides (1995), 14:985-990) было обнаружено, что стереочистым Rp-олигодезоксирибонуклеозид фосфортиоатам присуща более низкая стабильность к эндогенным нуклеазам сыворотки человека по сравнению с исходными олигодезоксирибонуклеозид фосфортиоатами с неопределенной хиральностью фосфора.
Нуклеиновые основание и модифицированные нуклеиновые основания
Нуклеиновое основание Ва в Формуле 1 представляет собой природное нуклеиновое основание или модифицированное нуклеиновое основание, полученное из природных нуклеиновых оснований. Примеры включают, не ограничиваясь ими, урацил, тимин, аденин, цитозин и гуанин, в которых соответствующие аминогруппы защищены ацильной защитной группой, - 2-фторурацил, 2-фторцитозин, 5-бромурацил, 5-йодурацил, 2,6-диаминопурин, азацитозин, пиримидиновые аналоги, такие как псевдоизоцитозин и псевдоурацил, а также другие модифицированные нуклеиновые основания, такие как 8-замещенные пурины, ксантин или гипоксантин (последние два представляют собой природные продукты разложения). Модифицированные нуклеиновые основание, раскрытые в Chiu and Rana, RNA, 2003, P, 1034-1048, Limbach et al. Nucleic Acids Research, 1994, 22, 2183-2196 и Revankar and Rao, Comprehensive Natural Products Chemistry, vol. 7, 313, также включены как фрагменты Ва Формулы 1. Соединения, представленные следующими общими формулами, также включены в качестве модифицированных нуклеиновых оснований:
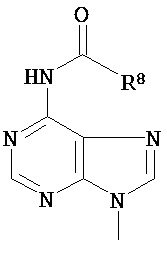
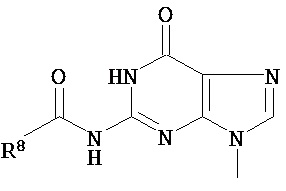
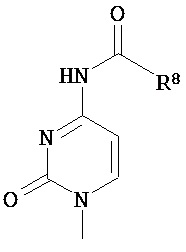
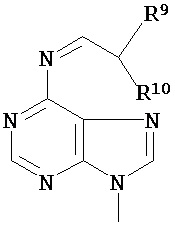
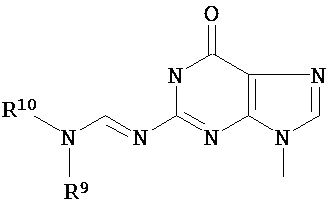
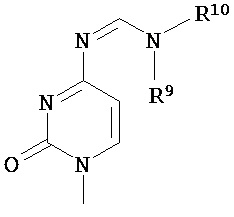
В приведенных выше формулах, R представляет собой неразветвленную или разветвленную алкильную, арильную, аралкильную или арилоксилалкильную группу, которая содержит от 1 до 15 атомов углерода, в том числе, только для примера, метальную, изопропильную, фенильную, бензильную или феноксиметильную группу; и каждый из R9 и R10 представляет неразветвленную или разветвленную алкильную группу, которая содержит от 1 до 4 атомов углерода.
Модифицированные нуклеиновые основания также включают нуклеиновые основание увеличенного размера, в которые введены одно или больше бензольных колец. Замены нуклеиновых оснований, описанный в каталоге Glen Research (www.glenresearch.com); Krueger AT et al., Ace. Chem. Res., 2007, 40, 141-150; Kool, ET, Асе. Chem. Res., 2002, 35, 936-943; Benner S.A., et al., Nat. Rev. Gent., 2005, 6, 553-543; Romesberr, F.E., et al., Curr. Opin. Chem. Biol., 2003, 7, 723-733; Hirao, I., Curr. Opin. Chem. Biol., 2006, 10, 622-627, включены в качестве пригодных для синтеза нуклеиновых кислот, описанных в данном описании. Некоторые примеры указанных нуклеиновых оснований увеличенного размера показаны ниже:
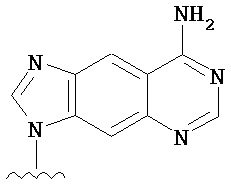
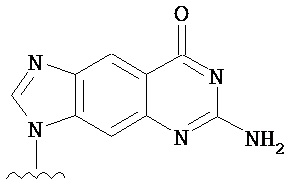
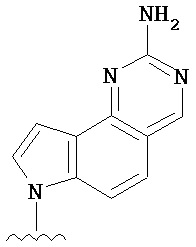
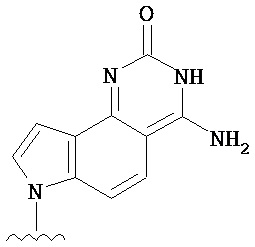
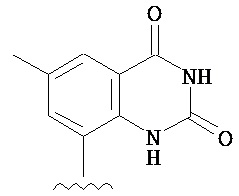
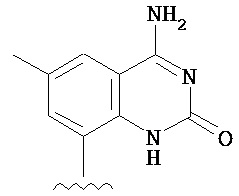
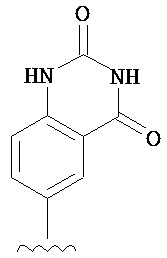
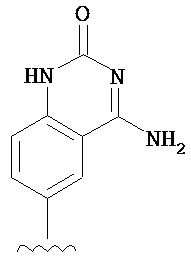
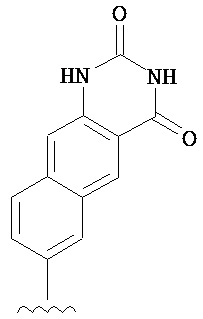
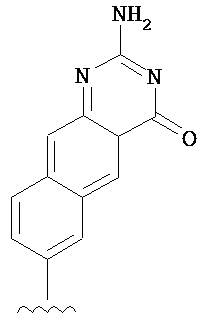
В данном изобретении, модифицированные нуклеиновые основание также охватывают структуры, которые не считаются нуклеиновыми основаниями, но представляют собой другие фрагменты, такие как, не ограничиваясь ими, кольца-производные коррина или порфирина. Замены оснований производными порфирина описаны в Morales-Rojas, H и Kool, ET, Org. Lett., 2002, 4, 4377-4380. Ниже показан пример кольца-производного порфирина, которое может использоваться в качестве замены основания:
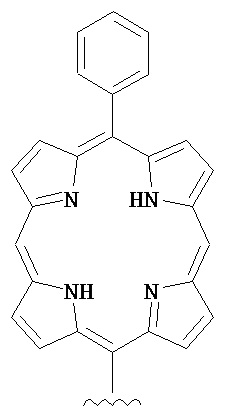
Другие модифицированные нуклеиновые основания также включают замены оснований, например, такие как показано ниже:
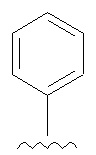
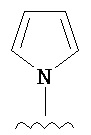
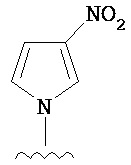
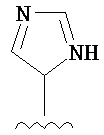
Модифицированные нуклеиновые основания, которые являются флуоресцентными, также включены. Неограничивающие примеры указанных замен оснований включают фенантрен, пирен, стильбен, изоксантин, изозантоптерин, терфенил, тертиофен, бензотертиофен, кумарин, люмазин, тетарированный стильбен, бензо-урацил и нафто-урацил, как показано ниже:
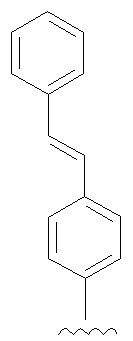
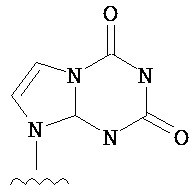
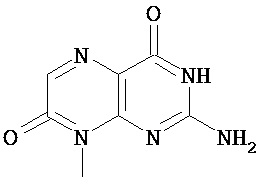
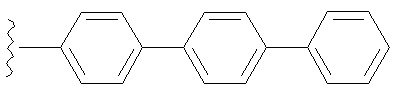
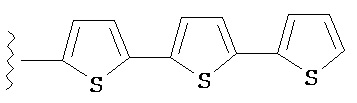
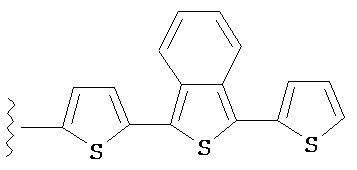
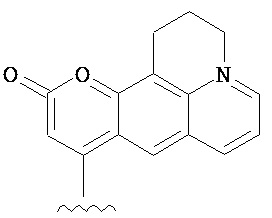
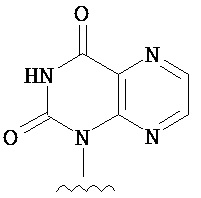
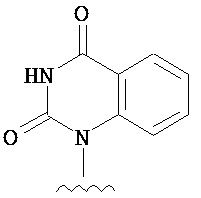
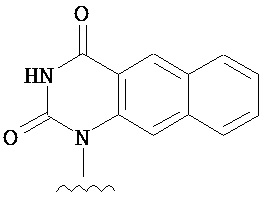
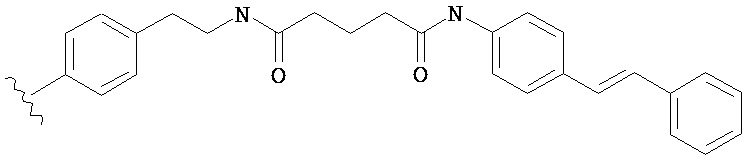
Модифицированные нуклеиновые основания могут быть незамещенными или могут содержать дополнительные заместители, такие как гетероатомы, алкильные группы или линкерные фрагменты, соединенные с флуоресцентными фрагментами, биотиновыми или авидиновыми фрагментами, или другими белками или пептидами. Модифицированные нуклеиновые основания также включают некоторые универсальные основания, которые не являются нуклеиновыми основаниями в наиболее классическом смысле, но функционируют подобно нуклеиновым основаниям. Одним из характерных примеров такого универсального основания является 3-нитропиррол.
В дополнение к нуклеозидам структуры IV или IX, другие нуклеозиды также могут быть использованы в способе, раскрытом в данном описании, которые включают нуклеозиды, содержащие модифицированные нуклеиновые основания или нуклеиновые основания, ковалентно соединенные с модифицированными сахарами. Некоторые примеры нуклеозидов, которые включают модифицированные нуклеиновые основания, включают 4-ацетилцитидин; 5-(карбоксигидроксилметил)уридин; 2'-0-метилцитидин; 5-карбоксиметиламинометил-2-тиоуридин; 5-карбоксиметиламинометилуридин; дигидроуридин; 2'-O-метилпсевдоуридин; бета,O-галактозилхеозин; 2'-O-метилгуанозин; N6-изопентениладенозин; 1-метиладенозин; 1-метилпсевдоуридин; 1-метилгуанозин; 1-метилинозин; 2,2-диметилгуанозин; 2-метиладенозин; 2-метилгуанозин; N7-метилгуанозин; 3-метил-цитидин; 5-метилцитидин; N6-метиладенозин; 7-метилгуанозин; 5-метиламиноэтилуридин; 5-метоксиаминометил-2-тиоуридин; бета,D-маннозилхеозин; 5-метоксикарбонилметилуридин; 5-метоксиуридин; 2-метилтио-N6-изопентениладенозин; N-((9-бета,D-рибофуранозил-2-метилтиопурин-6-ил)карбамоил)треонин; N-((9-бета,D-рибофуранозилпурин-6-ил)-N-метилкарбамоил)треонин; уридин-5-оксиуксусной кислоты метиловый эфир; уридин-5-оксиуксусную кислоту (v); псевдоуридин; хеозин; 2-тиоцитидин; 5-метил-2-тиоуридин; 2-тиоуридин; 4-тиоуридин; 5-метилуридин; 2'-O-метил-5-метилуридин; и 2'-O-метилуридин.
В некоторых вариантах нуклеозиды включают 6'-модифицированные бициклические аналоги нуклеозидов с (R)- или (S)-хиральностью в положении 6' и включают аналоги, описанные в патенте США 7,399,845. В других вариантах нуклеозиды включают 5'-модифицированные бициклические аналоги нуклеозидов с (R) или (S)-хиральностью в положении 5' и включают аналоги, описанные в публикации патентной заявки США №20070287831.
В некоторых вариантах нуклеиновые основания или модифицированные нуклеиновые основания включает фрагменты связывания с биологическими молекулами, такими как антитела, фрагменты антител, биотин, авидин, стрептавидин, лиганды рецепторов или хелатные фрагменты. В других вариантах Ва представляет собой 5-бромцрацил, 5-йодурацил или 2,6-диаминопурин. В других вариантах Ва модифицирован замещением флуоресцентным фрагментом или фрагментом связывания с биологической молекулой. В некоторых вариантах заместитель в Ва представляет собой флуоресцентный фрагмент. В других вариантах заместитель на В а представляет собой биотин или авидин.
Модифицированные сахара нуклеотид/нуклеозид.
Наиболее распространенные из встречающихся в природе нуклеотидов представляют собой рибозные сахара, соединенные с нуклеиновыми основаниями аденозином (А), цитозином (С), гуанином (G) и тимином (Т) или урацилом (U). Также включены модифицированные нуклеотиды, где фосфатная группа или фрагменты с модифицированные атомом фосфора в нуклеотидах могут быть присоединены к различным положениям сахара или модифицированного сахара. В качестве неограничивающих примеров, фосфатная группа или фрагмент с модифицированным атомом фосфора может быть присоединен к 2'-, 3'-, 4'- или 5'-гидроксильному фрагменту сахара или модифицированного сахара. Нуклеозиды, содержащие модифицированные нуклеиновые основания, описанные выше, также могут использоваться в способе, раскрытом в данном описании. В некоторых вариантах нуклеотиды или модифицированные нуклеотиды, содержащие незащищенный -ОН фрагмент, используются в способе, раскрытом в данном описании.
В дополнение к рибозному фрагменту, описанному на Схемах 1-4b, другие модифицированные сахара также могут быть введены в нуклеиновые кислоты, раскрытые в данном описании. В некоторых вариантах модифицированные сахара содержат один или больше заместителей в положении 2', в том числе один из следующих: F; CF3, CN, N3, NO, NO2, O-, S- или N-алкил; O-, S- или N-алкенил; O-, S- или N-алкинил; или О-алкил-O-алкил, О-алкил-N-алкил или N-алкил-О-алкил, где алкил, алкенил и алкинил могут быть замещенными или незамещенными C1-С10 алкилом или С2-С10 алкенилом и алкинилом. Примеры заместителей включают, не ограничиваясь ими, O(СН2)NOCH3 и O(CH2)nNH2, где n равно от 1 до приблизительно 10, МОЭ, ДМАОЭ, ДМАЭОЭ. Также в данное изобретение включены модифицированные сахара, описанные в WO 2001/088198; и Martin et al., Helv. Chim. Acta, 1995, 78, 486-504. В некоторых вариантах модифицированные сахара включают замещенные силильные группы, отщепляющую РНК группу, репортерную группу, флуоресцентную метку, интеркалятор, группу для улучшения фармакокинетических свойств нуклеиновой кислоты или группу для улучшения фармакодинамических свойств нуклеиновой кислоты и другие заместители с подобными свойствами. Модификации могут быть осуществлены в положениях 2', 3', 4', 5' или 6' сахара или модифицированного сахара, в том числе, в положении 3' для 3'-концевого нуклеотида или в положении 5' для 5'-концевого нуклеотида.
Модифицированные сахара также включают миметики сахаров, такие как циклобутильные или циклопентильные фрагменты, вместо пентофуранозильного сахара. Примеры патентов США, в которых раскрыто получение таких модифицированных сахарных структур, включают, не ограничиваясь ими, патенты США 4,981,957; 5,118,800; 5,319,080; и 5,359,044. Некоторые модифицированные сахара, охватываемые данным изобретением, включают:
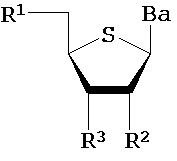
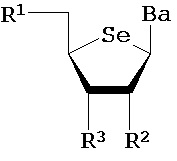
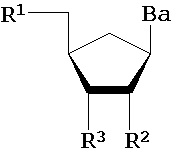 and
and 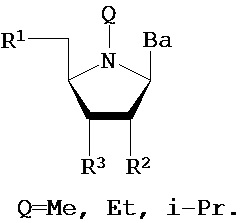
Другие неограничивающие примеры модифицированных сахаров включают глицерин, который образует аналоги глицерин-нуклеиновой кислоты (ГНК). Один из примером аналогов ГНК показан ниже и описан в Zhang, R et al., J. Am. Chem. Soc., 2008, 130, 5846-5847; Zhang L, et al., J. Am. Chem. Soc., 2005, 727, 4174-4175 и Tsai CH et al., PNAS, 2007, 14598-14603:
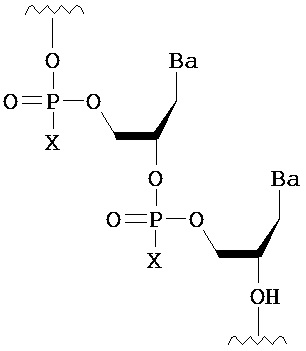 .
.
где X является таким, как определено в данном описании. Другой пример аналога-производного ГНУ, гибкой нуклеиновой кислоты (ГбНК) базирующийся на смешанном ацетальаминале формилглицерина, описан в Joyce GF et al., PNAS, 1987, 84, 4398-4402 и Heuberger BD and Switzer C, J. Am. Chem. Soc., 2008, 130, 412-413 и показан ниже:
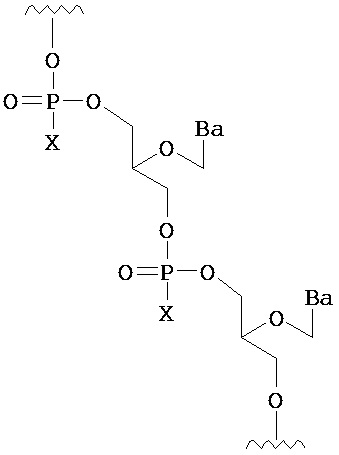 .
.
Другие неограничивающие примеры модифицированных сахаров включают гексопиранозильные (6'→4'), пентопиранозильные (4'→2'), пентопиранозильные (4'→3') или тетрофуранозильные (3'→2') сахара.
Охватываемые изобретением гексопиранозильные (6'→4') сахара включают:
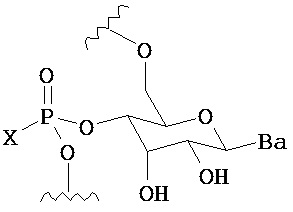
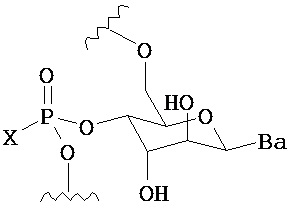
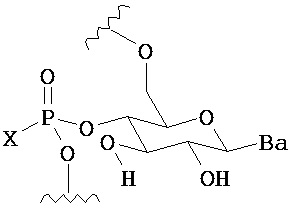
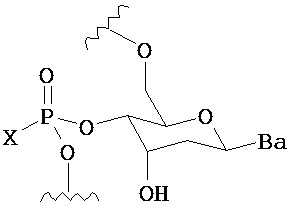
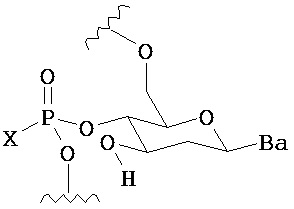
Охватываемые изобретением пентопиранозильные (4'→2') сахара включают:
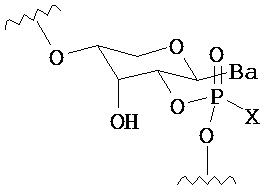
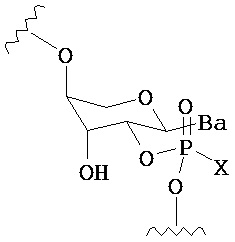
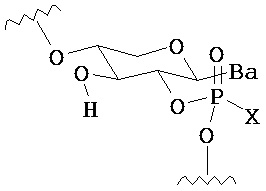
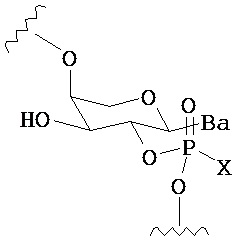 .
.
Охватываемые изобретением пентопиранозильные (4'→3') сахара включают:
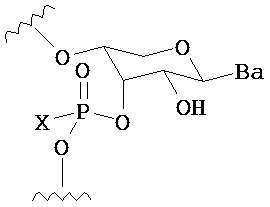
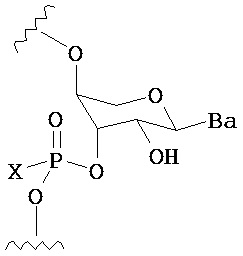 .
.
Охватываемые изобретением тетрофуранозильные (3'→2') сахара включают:
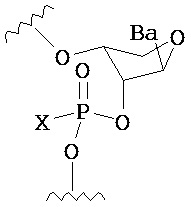
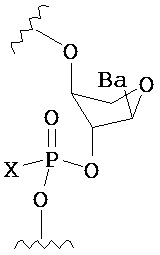
Другие охватываемые изобретением модифицированные сахара включают:
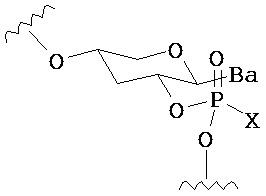
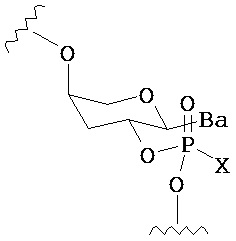
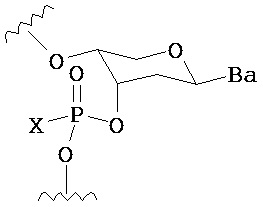
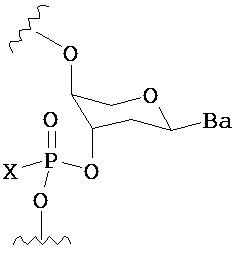
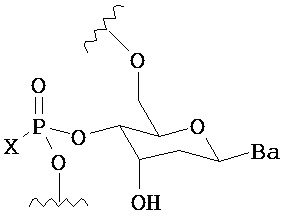
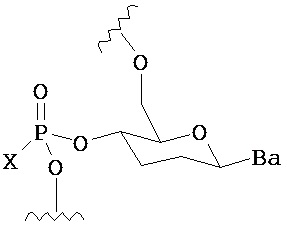
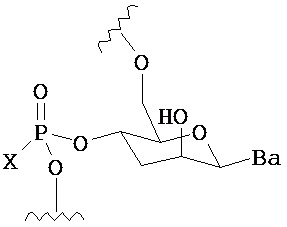
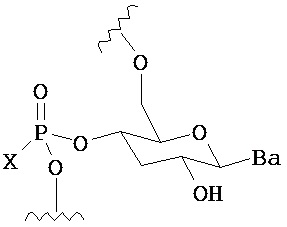
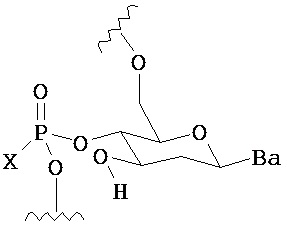 .
.
Дополнительно изобретение охватывает миметики сахаров, проиллюстрированные ниже, где Х выбран из S, Se, СН2, N-Me, N-Et или N-iPr.
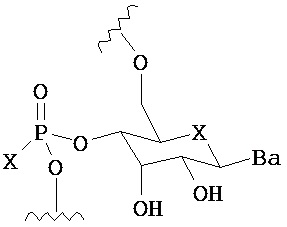
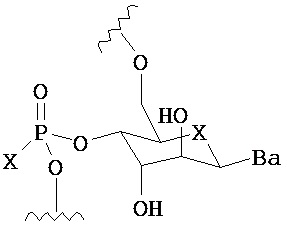
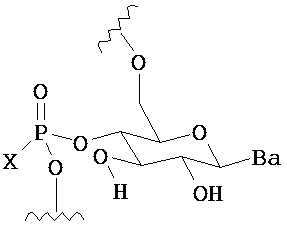
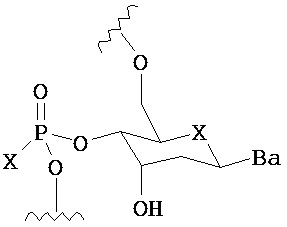
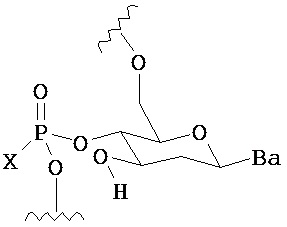
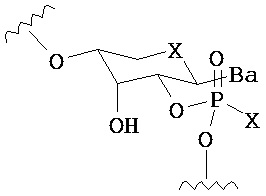
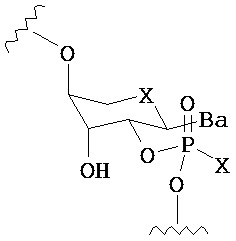
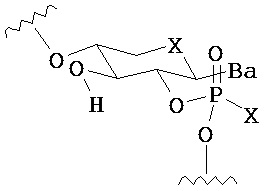
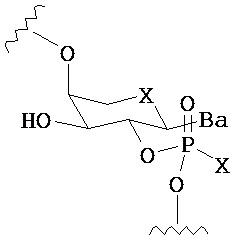
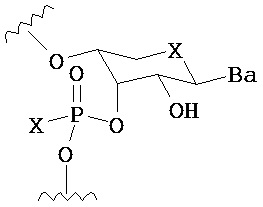
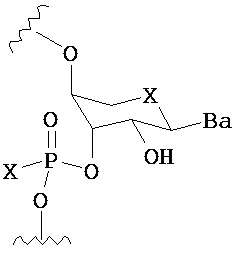
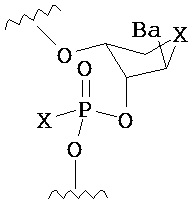
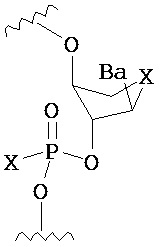
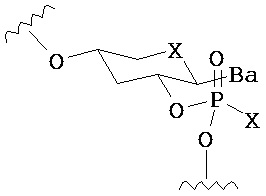
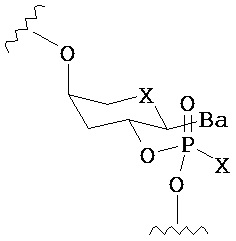
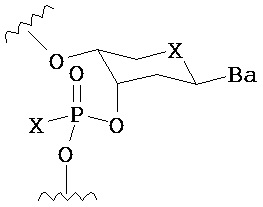
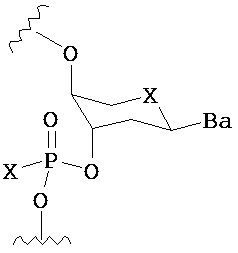
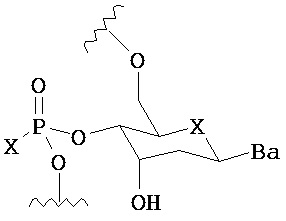
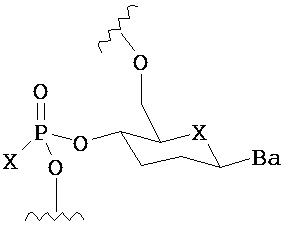
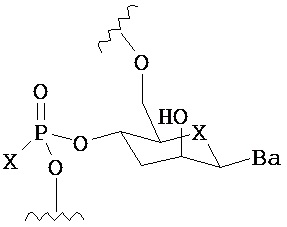
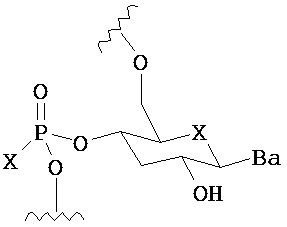
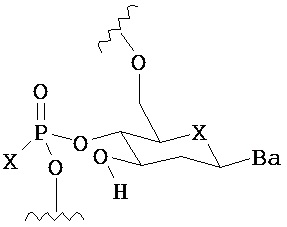 .
.
Модифицированные сахара и миметики сахаров могут быть получены по способам, известным в данной области, в том числе, не ограничиваясь ими: А. Eschenmoser, Science (1999), 284:2118; M. Bohringer et al., Helv. Chim. Acta (1992), 75:1416-1477; M. Egli et al., J. Am. Chem. Soc. (2006), 128(33):10847-56; A. Eschenmoser в Chemical Synthesis: Gnosis to Prognosis, C. Chatgilialoglu and V. Sniekus, Ed., (Kluwer Academic, Netherlands, 1996), p, 293; K.-U. Schoning et al., Science (2000), 290:1347-1351; A. Eschenmoser et al., Helv. Chim. Acta (1992), 75:218; J. Hunziker et al., Helv. Chim. Acta (1993), 76:259; G. Otting et al., Helv. Chim. Acta (1993), 76:2701; K. Groebke et al., Helv. Chim. Acta (1998), 81:375; и A. Eschenmoser, Science (1999), 284:2118.
Блокирующие группы
В некоторых вариантах описанных реакций необходимо защитить функциональные группы, например гидрокси, амино, тиольные или карбоксильные группы, если их присутствие желательно в конечном продукте, во избежание их нежелательного участия в реакциях. Защитные группы используются для блокирования некоторых или всех реакционноспособных фрагментов и предупреждения участия таких фрагментов в химических реакциях до удаления защитной группы. В одном из вариантов каждую из защитных групп удаляют другими средствами. Защитные группы, которые отщепляются в полностью различных условиях реакции, удовлетворяют требованию удаления по отдельности. В некоторых вариантах защитные группы удаляют с помощью кислоты, основания и/или гидрогенолиза. Такие группы, как тритил, диметокситритил, ацеталь и трет-бутилдиметилсилил, являются нестойкими к действию кислоты и используются в некоторых вариантах для защиты карбоксильных и гидроксильных реакционноспособных фрагментов в присутствии аминогруппы, защищенной группой Cbz, которую удаляют гидрогенолизом, и/или группы Fmoc, которая является нестойкой к действию основания. В других вариантах реакционноспособные карбоксильные и гидроксильные фрагменты блокируют нестойкими к действию оснований группами, такими как, не ограничиваясь ими, метил, этил и ацетил, в присутствии акрилатов, блокированных нестойкими к действию кислоты группами, такими как трет-бутилкарбамат, или карбаматами, которые устойчивы к действию кислот и оснований, но удаляются гидролизом.
В другом варианте, реакционноспособные гидроксильные фрагменты блокируют гидролитически удаляемыми защитными группами, такими как бензильная группа, тогда как аминогруппы, способные образовывать водородные связи с кислотами, блокируют нестойкими к действию оснований группами, такими как Fmoc. В другом варианте реакционноспособные карбоксильные фрагменты защищают превращением в простые эфира, или, в другом варианте, блокируют защитными группами, удаляемыми в окислительных условиях, такими как 2,4-диметоксибензил, тогда как сопутствующие аминогруппы блокируют нестойкими к действию фторидов силильными или карбаматными блокирующими группами.
Аллильные блокирующие группы пригодны в присутствии кислота- и основание-защитных групп, поскольку первые являются устойчивыми, и в последующем могут быть удалены с использованием металлических или пи-кислотных катализаторов. Например, с блокированных аллилом гидроксильных групп защита может быть снята с помощью катализируемой Pd(0) реакции в присутствии нестойких к действию кислоты трет-бутилкарбаматных или нестойких к действию основания ацетатаминных защитных групп. Другой формой защитной группы является смола, к которое присоединяют соединение или промежуточное соединение. До тех пор, пока остаток присоединен к смоле, функциональная группа блокирована и не может вступить в реакцию. После высвобождения из смолы, функциональная группа доступна для реакции.
Типичные блокирующие/защитные группы, пригодные для синтеза соединений, описанных в данном описании, только для примера:
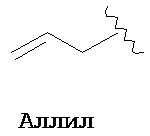
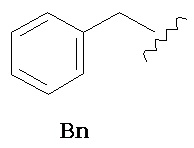
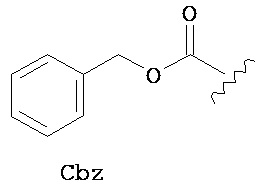
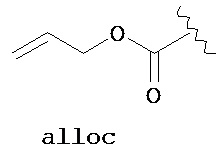
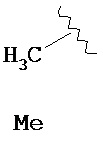
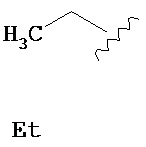
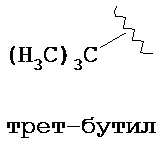
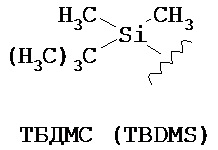
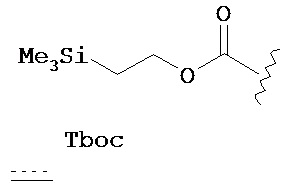
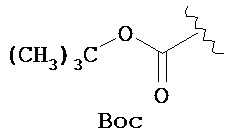
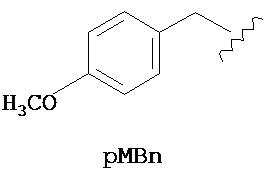
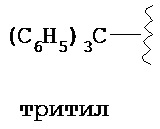
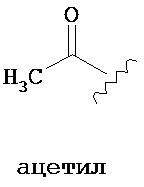
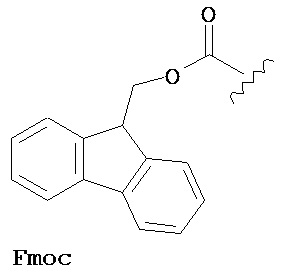
Характерные защитные группы, пригодные для защиты нуклеотидов в ходе синтеза, включают нестойкие к действию оснований защитные группы и нестойкие к действию кислоты защитные группы. Нестойкие к действию основания защитные группы используют для защиты экзоциклических аминогрупп в гетероциклических нуклеиновых основаниях. Данный вид защиты в целом достигается ацилированием. Тремя широко используемыми для ацилирования группами для данной цели являются бензоилхлорид, феноксиуксусный ангидрид и изобутирилхлорид. Указанные защитные группы устойчивы в условиях реакции, применяемых в ходе синтеза нуклеиновой кислоты, и отщепляются с приблизительно одинаковой скоростью в ходе обработки основанием в конце синтеза.
В некоторых вариантах 5'-защитная группа представляет собой тритил, монометокситритил, диметокситритил, триметокситритил, 2-хлортритил, ДАТЭ, ТБТр, 9-фенилксантин-9-ил (Pixyl) или 9-(n-метоксифенил)ксантин-9-ил (МОК).
В некоторых вариантах защищают тиольные фрагменты, включенные в соединения Формулы 1, 2, 4 или 5. В некоторых вариантах защитные группы включают, не ограничиваясь ими, пиксил, тритил, бензил, n-метоксибензил (РМВ, ПМБ) или трет-бутил (трет-Bu).
Другие защитные группы, а также подробное описание методик, применимых для введения защитных групп и их удаления, описаны в Green and Wuts, Protective Groups in Organic Синтез, 3rd Ed., John Wiley & Sons, New York, NY, 1999 и Kocienski, Protective Groups, Thieme Verlag, New York, NY, 1994, которые включены в данное описание путем ссылки для целей такого раскрытия.
СПОСОБЫ ПРИМЕНЕНИЯ ПРОЛЕКАРСТВ НУКЛЕИНОВОЙ КИСЛОТЫ, СОДЕРЖАЩИХ ХИРАЛЬНЫЙ Х-ФОСФОНАТНЫЙ ФРАГМЕНТ
Стереоопределенное пролекарство в форме олигонуклеотида, содержащего хиральный атом фосфора или фосфортиоатный фрагмент, которое получают способами по изобретению, пригодно для применения во множестве областей благодаря сочетанию стабильности, определенной хиральности и легкости синтеза. В общем, соединения, синтезированные данным способом, пригодны в качестве терапевтических, диагностических зондов и реагентов, синтетических инструментов для получения других олигонуклеотидных продуктов и наноструктурных материалов, пригодных для множества сфер применения новых материалов и вычислительных подходов.
Пролекарство в форме стереоопределенного олигонуклеотида по изобретению обладает улучшенной стабильностью в сыворотке по сравнению с природными ДНК/РНК эквивалентами и в частности, стереоопределенное олигонуклеотидное Пролекарство из класса фосфортиоатоа. Кроме того, SP изомер является более стабильным, чем RP изомер. В некоторых вариантах уровень стабильности в сыворотки модулируется путем введения всех SP центров или SP центров в выбранных положениях для обеспечения сопротивления разложению. В других вариантах введение выбранных RP и/или Sp стереоцентров может обеспечивать сочетание спаривания с конкретным основанием и эндогенной или экзогенной мишенью, таким образом защищая мишень от метаболизма или усиливая конкретную биологическую реакцию.
Активация РНКазы Н также модулируется присутствием стереоконтролируемых фосфортиоатных аналогов нуклеиновой кислоты, тогда как природная ДНК/РНК более чувствительна, чем RP стереоизомер, который, в свою очередь, более чувствителен, чем соответствующий Sp изомер.
Повышенная стабильность дуплекса по сравнению с РНК наблюдалась для RP фосфортиоатных олигонуклеотидов, демонстрирующих более высокую стабильность дуплекса, чем соответствующие SP олигонуклеотиды, которые, в свою очередь, демонстрировали более высокую стабильность по сравнению с природной ДНК/РНК. Повышенная стабильность дуплекса по сравнению с ДНК наблюдалась для 5Р, демонстрирующего более высокую стабильность дуплекса по сравнению с RP, который является более стабильным по сравнению с природной ДНК/РНК. (Р. Guga, Curr. Top Med. Chem., 2007, 7, 695-713).
Указанные молекулы могут быть пригодными в качестве терапевтических агентов, для множества конкретных областей. Они могут быть введены в олигонуклеотиды, которые также содержат стандартные ДНК/РНК нуклеозиды, или они могут быть синтезированы в виде полных последовательностей стереоконтролируемых олигонуклеотидов по изобретению. Некоторые категории терапевтических агентов включают, не ограничиваясь ими, антисмысловые олигонуклеотиды, антигенные олигонуклеотиды, которые образуют тройную спираль с целевыми последовательностями для подавления транскрипции нежелательных генов и модуляции экспрессии и/или активности белка, ложные олигонуклеотиды, ДНК вакцины, аптамеры, рибозимы, дезоксирибозимы (ДНКзимы или ДНК ферменты), миРНК, микроРНК, нкРНК (некодирующая РНК) и Р-модифицированные пролекарства. Модуляция охватывает прямое или опосредованное повышение или снижение активности белка или ингибирование или промотирование экспрессии белка. Указанные соединения нуклеиновых кислот могут применяться для контроля пролиферации клеток, репликации вирусов или любого другого процесса проведения сигнала клеткой.
В одном из примеров, сфера применения терапевтических миРНК демонстрирует потребность в молекулах олигонуклеотидов, которые обладали бы повышенной устойчивостью к действию РНКазы, с целью увеличения длительности действия по сравнению с продемонстрированной дли миРНК, состоящей из природных нуклеозидов. Дополнительно, образование спирали А-формы, по-видимому, более показательно для успеха введения иРНК, чем присутствие конкретных нативных элементов на олигонуклеотиде. Оба указанных требования могут быть удовлетворены при применении стереоконтролируемых олигонуклеотидов по изобретению, которые могут обеспечить повышенную стабильность (Y-L Chiu, T.M.Ransi RNA, 2003, 9, 1034-1048).
Способы лечения
Нуклеиновые кислоты, описанные в данном описании, пригодны в качестве терапевтических агентов против различных патологических состояний, в том числе для применения в качестве противовирусных агентов. Нуклеиновые кислоты могут применяться в качестве агентов для лечения заболеваний посредством модуляции активности ДНК и/или РНК. В некоторых вариантах нуклеиновые кислоты могут применяться для ингибирования экспрессии конкретного гена. Например, нуклеиновые кислоты могут быть комплементарными к конкретной последовательности-мишени мессенджера РНК (мРНК). Они могут применяться для ингибирования репликации множества вирусов. Примеры семейств вирусов включают ортомиксовирусы, поксвирусы, вирусы герпеса, папилломавирусы, пикорнавирусы, флавивирусы, ретровирусы, вирусы гепатита, парамиксовирусы, реовирусы, парвовирусы, филовирусы, коронавирусы, аренавирусы, рабдовирусы и аденовирусы. Дополнительные семейства вирусов известны и также включены в данное изобретение. Другие примеры включают применение в качестве антисмысловых соединений против РНК ВИЧ или РНК других ретровирусов, или для гибридизации с мРНК ВИЧ, кодирующей белок tat, или с участком TAR мРНК ВИЧ. В некоторых вариантах нуклеиновые кислоты имитируют вторичную структуру участка TAR мРНК ВИЧ и таким образом связываются с белком tat. В одном из вариантов нуклеиновые кислоты используют для ингибирования экспрессии целевого белка путем обеспечения контакта клетки с соединением Формулы 1, где экспрессия других белков в клетке не ингибируется или ингибируется минимально. В одном из вариантов ингибирование целевого белка возникает in vivo у млекопитающего. В других вариантах терапевтически эффективное количество соединения Формулы 1 вводят для ингибирования экспрессии целевого белка.
Другие примеры белков, экспрессия которых может модулироваться, включают Jun N-концевые киназные (JNK) белки, диацилглицерин ацилтрансферазу I, аполипопротеин В, рецептор глюкагона, Aurora В, ацил-КоА-холестерин ацилтрансферазу-2, с-реактивный белок, семейство белков STAT (преобразователи сигнала транскрипции) и MDR Р-гликопротеин. Нуклеиновые кислоты могут применяться для ингибирования экспрессии белка фосфатазы 1 В (РТР1 В), РНК-зависимой РНК-полимеразы вирусов. Нуклеиновые кислоты могут применяться для индуцирования таких событий, как апоптоз в раковых клетках, или для того, чтобы сделать клетки более чувствительными к апоптозу. Нуклеиновые кислоты могут применяться для модулирования активности белков. Например, они могут способствовать модуляции активности РНКазы Н, нацеливая ее на молекулы РНК, обеспечивающие резистентность ко многим лекарственным средствам (РМЛ).
В другом аспекте данного изобретения предлагаются способы лечения заболевания, опосредованного экспрессией нежелательного гена у субъекта (например, млекопитающих, таких как человек), нуждающегося в таком лечении. Под "заболеваниями" подразумеваются заболевания или симптомы заболеваний. Способ включает введение субъекту эффективного количества нерацемического про-олигонуклеотида по данному изобретению.
Примеры заболеваний, опосредованных экспрессией нежелательного гена, включают рак (например, лейкоз, опухоли и метастазы), аллергию, астму, ожирение, воспаление (например, воспалительные заболевания, такие как воспалительное заболевание дыхательных путей), гиперхолестеринемию, расстройства кроветворения, тяжелый острый дыхательный синдром (SARS), обструктивное заболевание дыхательных путей, астму, аутоиммунные заболевания, вызванные ретровирусами заболевания, такие как СПИД или ВИЧ, другие вирусные инфекции, внутриматочные инфекции, метаболические заболевания, инфекцию (например, бактериальную, вирусную, дрожжевую, грибковую), заболевания ЦНС, опухоли мозга, дегенеративные заболевания нервной системы, сердечно-сосудистые заболевания и заболевания, связанные с ангиогенезом, неоваскуляризацией и васкулогенезом.
В примерном варианте соединения пригодны для лечения рака, в том числе, рака поджелудочной железы, и других заболеваний или расстройств, включающих аномальную пролиферацию клеток.
Расположенная в верхней части брюшной полости (в ретроперитонеальной области), поджелудочная железа представляет собой железу с двойной функцией - в пищеварительной и эндокринной системе. В некоторых поджелудочная железа функционирует как эндокринная железа (например, вырабатывая некоторые важные гормоны). В некоторых случаях поджелудочная железа функционирует как экзокринная железа (например, секретируя жидкость, содержащую пищеварительные ферменты, которые попадают в тонкий кишечник).
Рак поджелудочной железы является четвертой по распространенности причиной смертности от рака в США (после рака легкого, ободочной кишки и молочной железы), на долю которого приходится 6% всех смертельных случаев, вызванных раком. В 2008 г. приблизительно 37680 новых случаев рака поджелудочной железы будет диагностировано в США, из которых 34290 будут смертельными. Встречаемость заболевания возрастает линейно после 50 лет, причем единственным определяющим фактором риска является курение (у курильщиков риск развития заболевания в 4 раза выше, чем у некурящих). Инвазивный рак поджелудочной железы практически всегда фатален. Медианное значение продолжительности жизни для всех пациентов составляет 4-6 месяцев. Относительная частота выживаемости на протяжении 1 года составляет 24%; общая частота выживаемости на протяжении 5 лет составляет <5%.
Рак поджелудочной железы характеризуется бессимптомным течением на ранней стадии и часто остается недиагностированным в течение нескольких месяцев (менее, чем для 1/3 пациентов диагноз устанавливают в пределах 2 месяцев с момента появления симптомов). В некоторых случаях поздняя диагностика приводит (частично или полностью) к метастазам раковых клеток в печень или лимфатические узлы.
В настоящее время, хирургическое вмешательство (резекция поджелудочной железы) является основным и единственным ведущим к излечению видом лечения рака поджелудочной железы. Однако, только 15-25% опухолей подлежат резекции на момент постановки диагноза, и только для 10-20% пациентов продолжительность жизни после хирургического вмешательства составляет свыше 2 лет. Как только происходит инфильтрация опухоли, и поражаются другие ткани, хирургическое вмешательство становится невозможным.
В некоторых случаях, сахарный диабет или панкреатит способствуют развитию пролиферативного расстройства множества клеток поджелудочной железы. В некоторых случаях, у лиц возникает повышенный риск развития пролиферативного расстройства множества панкреатических клеток вследствие наследственного синдрома, выбранного из группы, состоящей из: наследственный полипозный рак ободочной и прямой кишки (НПРОПК) и семейный аденоматозный полипоз (САП). В некоторых случаях повышенный риск развития пролиферативного расстройства множества панкреатических клеток является результатом мутации гена, выбранного из группы, состоящей из: МСН2, МСН6, MLH1 и APC.
В идеале, эффективное лечение рака поджелудочной железы должно (i) контролировать массу первичной опухоли, в начале лечения и в дальнейшем, и (ii) лечить метастатические опухолевые клетки. Химиопрофилактика (введения таких агентов, как лекарственные средства, биологические вещества, нутриенты, и т.п.) замедляет прогресс, обращает или ингибирует канцерогенез, таким образом снижая риск развития инвазивного или клинически значимого заболевания.
В некоторых вариантах данного изобретения раскрыт способ лечения рака поджелудочной железы. В данном описании "рак поджелудочной железы" включает формы рака поджелудочной железы. В некоторых вариантах рак поджелудочной железы представляет собой метастатический рак поджелудочной железы. В некоторых вариантах рак поджелудочной железы представляет собой карциному, саркому, рак или их комбинацию. В некоторых вариантах рак поджелудочной железы, подлежащий лечению, включает спорадический и наследственный рак поджелудочной железы. В некоторых вариантах рак поджелудочной железы представляет собой карциному клеток протока, карциному ацинозных клеток, папиллярную слизистую карциному, мукоидную карциному, аденосквамозную карциному, недифференцированную карциному, слизистую карциному, гигантско-клеточную карциному, мелкоклеточную карциному, кистозный рак, серозный кистозный рак, неклассифицированный рак поджелудочной железы, панкреатобластому или их комбинацию.
В некоторых вариантах у индивидуума, нуждающегося в лечении рака поджелудочной железы, присутствует локализованная опухоль поджелудочной железы. В некоторых вариантах у индивидуума, нуждающегося в лечении рака поджелудочной железы, отрицательные результаты биопсии регионарного лимфатического узла. В некоторых вариантах у индивидуума, нуждающегося в лечении рака поджелудочной железы, положительные результаты биопсии регионарного лимфатического узла. В некоторых вариантах у индивидуума, нуждающегося в лечении рака поджелудочной железы, присутствует узел-отрицательная опухоль поджелудочной железы (например, узел-отрицательная). В некоторых вариантах у индивидуума, нуждающегося в лечении рака поджелудочной железы, присутствует узел-положительная опухоль (например, узел-положительная).
В некоторых вариантах рак поджелудочной железы у индивидуума, нуждающегося в лечении рака поджелудочной железы, метастазировал в другие участки организма. В некоторых вариантах рак поджелудочной железы метастазировал в участок, выбранный из группы, состоящей из: лимфатического узла, желудка, желчного протока, печени, кости, яичника, брюшной полости и мозга.
В некоторых вариантах раковые клетки или предраковые клетки идентифицируют путем гистологического типирования или категоризации образца ткани (например, образца биопсии). В некоторых вариантах раковые клетки или предраковые клетки идентифицируют посредством использования подходящих молекулярных маркеров.
В некоторых вариантах стадия рака поджелудочной железы у индивидуума, нуждающегося в лечении рака поджелудочной железы, классифицирована в соответствии с системой классификации TNM Американского Объединенного комитета рака (AJCC), где опухоли (Т) присваивают стадию Тх, Т1, Т2, Т3, Т4; регионарным лимфатическим узлам (N) присваивают стадию NX, N0, N1; и удаленным метастазам (М) присваивают стадию MX, М0 или Ml. В некоторых вариантах стадия рака поджелудочной железы у индивидуума, нуждающегося в лечении рака поджелудочной железы, классифицирована как Стадия 0, I, IA, IB, II, IIA, IIB, III и IV рака поджелудочной железы. В некоторых вариантах стадия рака поджелудочной железы у индивидуума, нуждающегося в лечении рака поджелудочной железы, классифицирована как Категория GX (например, стадия не может быть оценена). Категория 1, Категория 2, Категория 3 или Категория 4.
Более конкретные примеры видов рака, поддающихся лечению соединениями по данному изобретению, включают рак молочной железы, рак легкого, меланому, рак ободочной и прямой кишки, рак мочевого пузыря, рак яичника, рак предстательной железы, рак почки, плоскоклеточный рак, глиобластому, саркому Капоши, множественную миелому и лейкоз.
Оценка и лечение рака
Термин "антиген опухолевой клетки" определен в данном описании как антиген, который присутствует в более высоких количества на опухолевой клетки или в биологических жидкостях, чем в других опухолевых клетках, нормальных клетках или в нормальной биологической жидкости. Присутствие антигена может быть обнаружено с помощью любого количества анализов, известных специалистам в данной области, в том числе, не ограничиваясь ими, отрицательная и/или положительная селекция с помощью антител, например, методом ELISA, радиоиммуноанализа или вестерн-блоттинга.
"Вызывающий апоптоз агент" определен в данном описании как индуцирующий апоптоз/запрограммированную гибель клетки и включает, например, противораковые агенты и средства лечения, где в клетках (например, опухолевых клетках) индуцируется запрограммированная гибель клетки. Примеры вызывающих апоптоз агентов описаны более подробно ниже.
Термины "апоптоз" или "запрограммированная гибель клетки" обозначают физиологический процесс, при помощи которого нежелательные или бесполезные клетки удаляются в ходе развития и других нормальных биологических процессов. Апоптоз представляет собой режим гибели клетки, которая происходит в нормальных физиологических условиях, и клетка принимает активное участие в собственной гибели («клеточный суицид»). Это чаще всего наблюдается в ходе нормального жизненного цикла клетки и гомеостаза ткани, эмбриогенеза, индуцирования и поддержания иммунной толерантности, развития нервной системы и эндокринно-зависимой атрофии тканей. Клетки, в которых возникает апоптоз, демонстрируют характерный морфологические и биохимические особенности. Указанные особенности включают агрегацию хроматина, ядерную и цитоплазматическую конденсацию, распределение цитоплазмы и ядра в соединенные с мембраной пузырьки (апоптотические тельца), которые содержат рибосомы, морфологически интактные митохондрии и ядерный материал. In vivo, такие апоптотические тельца быстро распознаются и фагоцитируются макрофагами, дендритными клетками или смежными эпителиальными клетками. Благодаря такому эффективному механизму удаления апоптотических клеток in vivo, воспалительный ответ не развивается. In vitro апоптотические тельца, также остальные фрагменты клетки набухают, и, в конечном итоге, происходит их лизис. Эта терминальная фаза клеточной гибели in vitro названа "вторичным некрозом". Апоптоз может быть измерен способами, известными специалистам в данной области, такими как фрагментация ДНК, контакт с Аннексином V, активация каспаз, высвобождения цитохром С, и т.д. Клетка, гибель которой инициирована, в данном описании называется "апоптотической клеткой".
Апоптоз также может быть обнаружен с использованием стандартного анализа апоптоза с использованием аннексина V: клетки NIH:OVCAR-3 выращивают на 6-луночных планшетах (NUNC) и облучают или обрабатывают антагонистом (или в комбинации с другим противораковым лекарственным средством) в течение 4-48 час, промывают и окрашивают Аннексином V-FITC (BD-Pharmingen) в течение 1 час. Клетки анализируют проточной цитометрией (Becton-Dickinson, CellQuest), осуществляя доокрашивание пропидия йодидом, и снова анализируют проточной цитометрией.
Состояние пациентов может быть оценено с учетом симптомов в одной или больше множественных временных точек, в том числе перед, в ходе и после проведения курсов лечения. Лечение может приводить к улучшению состояния субъекта и может быть оценено путем определения наличия одного или больше из следующих факторов: уменьшение размера опухоли, снижение клеточной пролиферации, уменьшение количества клеток, уменьшение неоваскуляризации, усиление апоптоза или уменьшение продолжительности жизни по меньшей мере части опухолевых клеток. Одно или больше из указанных явлений может, в некоторых случаях, приводить к частичному или полному устранению рака и увеличению продолжительности жизни пациента. Альтернативно, для рака в терминальной стадии, лечение может приводить к остановке прогресса заболевания, улучшению качества жизни и/или увеличению продолжительности жизни.
Способы анализа миграции клеток
Анализы миграции клеток описаны в литературе, например. Brooks, et al., J. Clin. Invest 1997, 99:1390-1398, и способы измерения миграции клеток известны специалистам в данной области. В одном из способом измерения миграции клеток, описанной в данном описании, мембраны камер транслуночной миграции покрывают субстратом, транслунки промывают, и участки неспецифического связывания блокируют альбумином телячьей сыворотки. Опухолевые клетки из субслитых культур собирают, промывают и ресуспендируют в буфере миграции в присутствии или в отсутствие антител анализа. Затем опухолевым клеткам позволяют мигрировать к нижней стороне покрытых транслуночных мембран; клетки, оставшиеся на верхней стороны мембраны, удаляют, и клетки, которые мигрировали на нижнюю сторону, окрашивают кристаллическим фиолетовым. Затем миграцию клеток количественно оценивают путем прямого подсчета клеток в поле зрения микроскопа.
Способы оценки роста опухоли
Рост опухоли можно оценить способами, известными специалистам в данной области, например, на модели с использованием мышей SCID, модели с использованием голых мышей и мышей BALB/c с сингенными опухолями. Модели роста опухоли с использованием мышей SCID получают следующим образом: субслитые клетки меланомы человека М21 (или любого целевого вида опухолевых клеток) собирают, промывают и ресуспендируют в стерильном ФБР (20×106/мл). Мышам SCID подкожно вводят 100 мкл суспензии клеток меланомы человека М21 (2×106). Через 3 дня после инъекции опухолевых клеток мышей оставляют без лечения или лечат интраперитонеально антагонистом в целевом интервале доз. Мышам вводят препарат ежедневно в течение 24 дней. Размер опухоли измеряют с помощью штангенциркуля, и объема вычисляют с использованием формулы V=(L×W2)/2, где V - объем, L - длина, и W - ширина.
Альтернативно, модели с использованием голых мышей, модели с использованием мышей SCID и/или сингенные модели с использованием мышей BALB/c также могут применяться для оценки роста опухоли и его замедления под действием гуманизированных анти-эндоглиновых антител или антигенсвязывающих фрагментов, описанных в данном описании.
Методы анализа пролиферации клеток
Пролиферация клеток может быть оценена способами, известными специалистам в данной области. Как описано в данном описании, субслитые эндотелиальные клетки человека (HUVEC) могут быть ресуспендированы в буфере пролиферации, содержащем низкую концентрацию (5,0%) сыворотки, в присутствии или в отсутствие СМ (25 мкл) из клеток ECV или ECVL, после чего позволяют пролиферацию эндотелиальных клеток в течение 24 час. Пролиферация может быть количественно оценена путем измерения активности митохондриальной дегидрогеназы с использованием коммерчески доступного набора для анализа WST-1 (Chemicon). Также, как описано в данном описании, пролиферация может быть количественно оценена путем измерения инкорпорации 3Н с использованием стандартных способов. (She et al., Int. J. Cancer, 108: 251-257 (2004)).
Другие способы оценки пролиферации клеток известны в данной области и включены в данное изобретение. Дополнительные неограничивающие примеры описаны более подробно в разделе «Примеры».
Следует понимать, что системы классификации и определения стадии, описанные в данном описании, являются одним из средств оценки лечения видов рака, описанных в данном описании; дополнительно, другие схемы оценки стадии известны в данной области и могут применяться в сочетании со способами, описанными в данном описании. Только для примера, TNM классификация злокачественных опухолей может применяться как система определения стадии рака для описания степени прогресса рака в организме пациента. Т описывает размер опухоли и наличие инвазии опухоли в окружающие ткани, N описывает степень вовлечения регионарных лимфатических узлов, и М описывает удаленные метастазы. TNM поддерживается Международным Сообществом борьбы с раком (UICC), а также применяется Американским Объединенным сообществом рака (AJCC) и Международной Федерацией Гинекологии и акушерства (FIGO). Следует понимать, что не все опухоли можно классифицировать согласно TNM, например, такие как опухоли мозга. В целом, Т (a, is, (0), 1-4) измеряют как размер или прямое распространение первичной опухоли. N (0-3) обозначает степень распространения на регионарные лимфатические узлы. N0 означает, что клетки опухоли отсутствуют в регионарных лимфатических узлах, N1 означает, что клетки опухоли распространились в ближайшие или в небольшое количество регионарных лимфатических узлов, N2 означает, что клетки опухоли распространились до степени между N1 и N3; N3 означает, что клетки опухоли распространились в наиболее отдаленные или многочисленные регионарные лимфатические узлы. М (0/1) обозначает присутствие метастазов: М0 означает отсутствие удаленных метастазов; M1 означает, что метастазы присутствуют в отдаленных органах (помимо регионарных лимфатических узлов). Другие параметры также могут оцениваться. G (1-4) обозначает категорию раковых клеток (т.е. низкая категория означает, что они сходны с нормальными клетками, и высокая категория означает, что они слабо дифференцированы). R (0/1/2) обозначает полноту хирургического вмешательства (т.е. границы поля резекции свободны от раковых клеток или нет). L (0/1) обозначает инвазию в лимфатические сосуды. V (0/1) обозначает инвазию в вену. С (1-4) обозначает индекс определенности (качества) V.
В данном изобретении предлагаются способы разложения, замедления роста или индуцирования гибели раковых клеток, которые включают обеспечение контакта клеток с количеством соединения, описанного в данном описании, эффективного для разложения, замедления роста или индуцирования гибели раковых клеток.
В данном изобретении предложены способы замедления увеличения размера опухоли, уменьшения размера опухоли, уменьшения пролиферации опухоли или предупреждения пролиферации опухоли у индивидуума, которые включают введение указанному индивидууму эффективного количества соединения, описанного в данном описании, для замедления увеличения размера опухоли, уменьшения размера опухоли, снижения пролиферации опухоли или предупреждения пролиферации опухоли. Лечение опухолей в некоторых случаях включает остановку симптомов, т.е. при лечении пациента рак не прогрессирует, и продолжительность жизни пациента увеличивается.
Состояние больных может быть оценено с учетом симптомов в одной или больше множественных временных точек, в том числе перед, в ходе и после проведения курсов лечения. Лечение может приводить к улучшению состояния субъекта и может быть оценено путем определения наличия одного или больше из следующих факторов: уменьшение размера опухоли, снижение клеточной пролиферации, уменьшение количества клеток, уменьшение неоваскуляризации и/или усиление апоптоза. Одно или больше из указанных явлений может, в некоторых случаях, приводить к частичному или полному устранению рака и увеличению продолжительности жизни пациента. Альтернативно, для рака в терминальной стадии, лечение может приводить к остановке прогресса заболевания, улучшению качества жизни и/или увеличению продолжительности жизни. Другие способы оценки лечения известны в данной области и включены в данное изобретение.
В примерном варианте соединение про-олигонуклеотид по изобретению вводят субъекту, такому как млекопитающее (например, человек), страдающему от медицинского расстройства, например, рака или злокачественного состояния, характеризующегося присутствием класса нежелательных клеток.
Измерение первичной конечной точки может быть проведено способами, описанными в данном описании, и включает, например, период до прогресса заболевания. В одном из вариантов наблюдается увеличение периода до прогресса заболевания приблизительно в 2 раза, в 5 раз, в 10 раз, в 20 раз, в 50 раз или больше по сравнению с отсутствием лечения. В другом варианте наблюдается увеличение периода до прогресса заболевания приблизительно на 3 месяца, приблизительно на 6 месяцев, приблизительно на 9 месяцев, приблизительно на 12 месяцев, приблизительно на 18 месяцев, приблизительно на 2 года, приблизительно на 3 года, приблизительно на 4 года, приблизительно на 5 лет или больше по сравнению с отсутствием лечения.
Вторичная конечная точка также может быть измерена и включает длительность ответа, период до прогрессирования опухоли, общую продолжительность жизни, легкие и тяжелые побочные эффекты. Например, лечение может предупреждать прогресс заболевания (т.е. остановка) или может приводить к улучшению. Альтернативно или дополнительно, достижение других целей может быть измерено с учетом одного или больше из следующего: снижение опухолевой нагрузки, уменьшение неоваскуляризации, уменьшение побочных реакций и/или повышение степени соблюдения пациентом предписаний врача.
Другие конкретные примеры заболеваний или расстройств, при которых лечение соединениями или композициями по изобретению пригодно для лечения или профилактики, включают, не ограничиваясь ими, отторжение трансплантата (например, почки, печени, сердца, легкого, островковых клеток, поджелудочной железы, костного мозга, роговицы, тонкой кишки, кожных аллотрансплантатов или ксенотрансклантатов и других трансплантатов), заболевание «трансплантат против хозяина», остеоартрит, ревматоидный артрит, рассеянный склероз, диабет, диабетическую ретинопатию, воспалительное заболевание кишечника (например, болезнь Крона, язвенный колит и другие заболевания кишечника) заболевания почек, кахексию, септический шок, волчанку, миастению гравис, псориаз, дерматит, экзема, себорею, болезнь Альцгеймера, болезнь Паркинсона, защиту стволовых клеток в ходе химиотерапии, селекцию ex vivo или промывание ex vivo для аутологичной или аллогенной трансплантации костного мозга, заболевание глаз, ретинопатию (например, дегенерацию желтого пятна, диабетическую ретинопатию и другие виды ретинопатии), заболевание роговицы, глаукому, инфекции(например, бактериальные, вирусные или грибковые), заболевание сердца, в том числе, не ограничиваясь им, рестеноз.
Активация РНКазы L
Путь 2'-5' олигоаденилата (2-5А)/РНКазы L представляет собой один из ферментных путей, индуцируемых интерфероном. РНКаза L активируется после связывания с 5'-фосфорилированными фрагментами 2'-5' адениловой кислоты. Указанные фрагменты 2'-5' адениловой кислоты (2-5А) образуются под контролем 2'-5' олиго(А) синтетазы. Данный путь представляет собой часть врожденной иммунной системы и играет важную роль в предупреждении вирусной инфекции. 2-5А-Индуцированное расщепление одноцепочечной РНК приводит к апоптозу. Показано, что биологически стабильные фосфортиоатные аналоги 2-5А являются мощными активаторами РНКазы L (Xianh et al., Cancer Research (2003), 63:6795-6801). В данном исследовании, аналоги 2-5А индуцируют активность РНКазы L и вызывают апоптоз в культурах линий клеток поздней стадии метастазирующего рака предстательной железы человека DU145, РС3 и LNCaP.
Непрерывная активация РНКазы L запускает митохондриальный путь апоптоза, который удаляет инфицированные вирусом клетки, а также раковые/опухолевые клетки. РНКаза L может ингибировать рост фибросаркомы, роста рака предстательной железы, рост рака ободочной и прямой кишки и рост рака поджелудочной железы. С учетом повсеместной роли РНКазы L при различных видах рака, предусматривается, что изобретение, описанное в данном описании, может применяться для лечения любого вида рака. Silverman, RH, Cytokine Growth Factor Rev, 18(5-6): 381-388 (2007); Bisbal, С. and Silverman, RH, Biochimie. 89(6-7): 789-798 (2007). Для примера, регуляция вниз РНКазы L обозначает любое снижение уровней экспрессии гена или генов, кодирующих РНКазу L, сайленсинг гена или генов, кодирующих РНКазу L, снижение уровней экспрессии/трансляции белков, включающих РНКазу L, уменьшение количества РНКазы L в пределах клетки и/или любое снижение активности РНКазы L по сравнению с предварительно определенным уровнем РНКазы L в примере здоровой популяции. Альтернативно, любое снижение уровней РНКазы L, как описано в данном описании, может быть показательным для регуляции вниз РНКазы L.
В одном из примерных вариантов соединения, описанные в данном описании, пригодны для лечения заболеваний, при которых происходит регуляция вниз РНКазы L. В другом варианте заболевания, сопровождающееся регуляцией вниз РНКазы L, представляет собой рак. В дополнительных вариантах, рак представляет собой рак поджелудочной железы, рак предстательной железы или рак ободочной и прямой кишки. Альтернативно, соединения, описанные в данном описании, пригодны для лечения заболевания, при котором происходит регуляция вверх РНКазы L. В одном из примерных вариантов заболевание, при котором происходит регуляция вверх РНКазы L, представляет собой синдром хронической усталости. Дополнительные заболевания, при которых происходит регуляция вверх РНКазы L, известны в данной области и включены в данное изобретение.
В случае применения в качестве терапевтических средств, нуклеиновые кислоты, описанные в данном описании, вводят в виде композиции фармацевтического средства. В некоторых вариантах фармацевтическая композиция включает терапевтически эффективное количество нуклеиновой кислоты, содержащей хиральный Х-фосфонатный фрагмент Формулы 1 или ее фармацевтически приемлемой соли и по меньшей мере один фармацевтически приемлемый неактивные ингредиент, выбранный из фармацевтически приемлемых разбавителей, фармацевтически приемлемых вспомогательных веществ и фармацевтически приемлемых носителей. В другом варианте фармацевтической композиции придают форму препарата для внутривенной инъекции, перорального введения буккального введения, ингаляции, назального ведения, местного применения, введения в глаза или уши. В дополнительных вариантах фармацевтическая композиция представляет собой таблетку, пилюлю, капсулу, жидкость, препарат для ингаляций, назальный спрей в форме раствора, суппозиторий, суспензию, гель, коллоидный раствор, суспензию, раствор, эмульсию, мазь, лосьон, глазные капли или ушные капли.
Фармацевтические композиции и введение
В другом аспекте данного изобретения предлагается фармацевтическая композиция, содержащая нерацемический про-олигонуклеотид в смеси с фармацевтически приемлемым вспомогательным веществом. Специалисту в данной области будет понятно, что фармацевтические композиции включают фармацевтически приемлемые соли нерацемических про-олигонуклеотидов, описанных выше.
Соединения для расширенной и целевой доставки
Про-олигонуклеотиды, описанные в данном описании, могут быть доставлены с использованием разнообразных стратегий доставки, в том числе в виде конъюгатов олигонуклеотидов с различными лигандами, а также с использованием подхода наноносителя. Любые стратегии доставки нуклеиновых кислот включены для использования с про-олигонуклеотидами, описанными в данном описании. Выбор между примерами стратегий доставки, в том числе не ограничиваясь ими, химические конъюгаты, транспортные пузырьки «катионный липид/липосома» и супрамолекулярные наноносители, зависит от терапевтического контекста и способов определения оптимального режима доставки, известен в данной области и дополнительно включен в данное описание.
Соединения, проникающие в клетку ("СПК")
Известно, что многочисленные соединения действуют в качестве носителей «груза», такого как нуклеиновые кислоты, и облегчают вхождение нуклеиновой кислоты в клетку в условиях in vivo. Примеры носителей описаны в Dietz et al., Molecular & Cellular Neuroscience, 27(2): 85-131 (2004), которые включены в данное описание путем ссылки. Прототипы СПК, производные Tat и регуляторы транскрипции Antennapedia, соединенные большим количеством новых фрагментов. В качестве примера, СПК, которые представляют собой пептиды, могут быть относительно короткими (9-30 аминокислот) поликатионными пептидами, богатыми аргинином и лизином, или взаимодействующими с мембраной в интерактивном режиме гидрофобными последовательностями. СПК могут быть соединены техниками рекомбинации ДНК или химическими способами присоединены к пептидам, олигонуклеотидам или наноносителям, которые дополнительно включают «груз» для СПК.
Нацеливающие на клетки лиганды ("НКЛ")
Другая стратегия представляет собой доставку олигонуклеотидов при помощи использования НКЛ, который связывается с высоким сродством с рецептором на поверхности клетки и способен эффективно интернализироваться. Потенциальные лиганды включают антитела, полипептиды, полученные из библиотек показа фага, и низкомолекулярные органические соединения. Дополнительные нацеливающие на клетки лиганды известны в данной области или будут созданы, и они включены для использования в изобретении, описанном в данном описании. Вследствие того, что различные рецепторы часто предпочтительно экспрессируются на конкретных видах клеток, данный подход предлагает возможность повышения селективности олигонуклеотидных реагентов. Примеры рецепторов-мишеней включают, не ограничиваясь ими, рецепторы липопротеинов (например, находящиеся в печени), интегринов, рецепторной тирозинкиназы и суперсемейство сочетанных с G-протеином рецептором (GPCR).
Наноносители
Различные супрамолекулярные наноносители могут быть использованы для доставки нуклеиновых кислот. Примеры наноносителей включают, не ограничиваясь ими, липосомы, комплексы катионных полимеров и различные полимеры. Образование комплексов нуклеиновых кислот с различными поликатионами представляет собой другой подход к внутриклеточной доставке; он включает использование пегилированных поликатионов, комплексов полиэтиленамина (ПЭА), катионных блок-сополимеров и дендримеров. Некоторые катионные наноносители, в том числе ПЭА и полиамидоаминные дендримеры, помогают высвободить содержимое эндосом. Другие подходы включают применение полимерных наночастиц, полимерных мицелл, квантовых точек и липоплексов.
Известны дополнительные стратегии доставки нуклеиновой кислоты, кроме примерных стратегий доставки, описанных в данном описании.
В терапевтическом и/или диагностическом применении, соединения по изобретению могут быть введены в различные лекарственные формы для различных видов введения, в том числе, системного и местного или локального применения. Технологии и препарата в целом можно найти в Remington, The Science and Practice of Pharmacy, (20th ed. 2000).
Соединения по изобретению эффективны в широком интервале доз. Например, в лечении взрослых людей, дозы от 0,01 до 1000 мг, от 0,5 до 100 мг, от 1 до 50 мг в сутки и от 5 до 100 мг в сутки представляют собой примеры доз, которые могут применяться. Точная доза будет зависеть от способа введения, лекарственной формы, в которой вводится соединение, подлежащего лечению субъекта, массы тела субъекта, а также опыта и предпочтений лечащего врача.
Фармацевтически приемлемые соли в целом будут известны средним специалистам в данной области и могут включать, например, не ограничиваясь ими, ацетат, бензолсульфонат, безилат, бензоат, бикарбонат, битартрат, бромид, кальция эдетат, камзилат, карбонат, цитрат, эдетат, эдизилат, эстолат, эзилат, фумарат, глюцептат, глюконат, глутамат, гликольлиларсанилат, гексилрезорцинат, гидрабамин, гидробромид, гидрохлорид, гидроксинафтоат, йодид, изетионат, лактат, лактобионат, малат, малеат, манделат, мезилат, муцат, напзилат, нитрат, памоат (эмбонат), пантотенат, фосфат/дифосфат, полигалактуронат, салицилат, стеарат, субацетат, сукцинат, сульфат, таннат, тартрат или теоклат. Другие фармацевтически приемлемые соли могут быть найдены, например, в Remington, The Science and Practice of Pharmacy (20th ed. 2000). Предпочтительные фармацевтически приемлемые соли включают, например, ацетат, бензоат, бромид, карбонат, цитрат, глюконат, гидробромид, гидрохлорид, малеат, мезилат, напзилат, памоат (эмбонат), фосфат, салицилат, сукцинат, сульфат или тартрат.
В зависимости от конкретных состояний, подлежащих лечению, такие агенты могут быть введены в жидкие или твердые лекарственные формы, и могут применяться системно или местно. Агенты могут быть доставлены, например, в форме с ускоренным или непрерывным замедленным высвобождением, известной специалистам в данной области. Технологии изготовления и введения можно найти в Remington, The Science and Practice of Pharmacy (20th ed. 2000). Подходящие способы могут включать пероральное, буккальное, ингаляцией спрея, сублингвальное, ректальное, трансдермальное, вагинальное, через слизистую оболочку, назальное или кишечное введение, парентеральное введение, в том числе внутримышечные, подкожные, интрамедуллярные инъекции, а также интратекальные, прямые интравентрикулярные, внутривенные, внутрисуставные, интрастернальные, интрасиновиальные, внутрипеченочные, в поврежденный участок, интракраниальные, интраперитонеальные, интраназальные или внутриглазные инъекции, или другие способы доставки.
Для инъекции агенты по изобретению могут быть введены и разбавлены в водных растворах, таких как растворы в физиологически совместимых буферных растворах, таких как раствор Ханка, раствор Рингера или физиологический солевой буферный раствор. Для введения через слизистую оболочку, в препаратах используют пенетранты, пригодные для проникновения сквозь соответствующий барьер. Такие пенетранты в общем известны в данной области.
Применение фармацевтически приемлемых инертных носителей для введения соединения по изобретению в лекарственную форму раскрыто для применения изобретения в лекарственных формах, подходящих для системного применения и находится в пределах изобретения. При условии правильного выбора носителя и способа введения, композиции по данному изобретению, в частности, в форме растворов, могут быть введены парентерально, например, внутривенной инъекцией. Соединения могут быть легко введены в лекарственные формы с использованием фармацевтически приемлемых носителей, хорошо известных в данной области, в дозах, подходящих для перорального введения. Такие носители позволяют введение соединений по изобретению в таблетки, пилюли, капсулы, жидкости, гели, сиропы, суспензии, и т.п., для приема внутрь субъектом (например, пациентом), который подлежит лечению.
Для назального или ингаляционного введения, агенты по изобретению также могут быть введены в лекарственные формы способами, известными специалисту в данной области, и могут включать, например, не ограничиваясь ими, примеры разбавителей, солюбилизирующих или диспергирующих веществ, таких как раствор соли, консервантов, таких как бензиловый спирт, усилители абсорбции и фторуглероды.
Фармацевтические композиции, пригодные для использования в данном изобретении, включают композиции, где активные ингредиенты содержатся в эффективном количестве для достижения предусмотренных целей. Определение эффективных количеств находится в пределах навыком специалистов в данной области, особенно в свете подробного раскрытия, приведенного в данном описании.
Кроме активных ингредиентов, такие фармацевтические композиции могут содержать подходящие фармацевтически приемлемые носители, включающие вспомогательные вещества и адъюванты, облегчающие обработку активного соединения и введение его в лекарственные формы, которые могут применяться в фармации. Лекарственные формы для перорального ведения могут приобретать форму таблеток, драже, капсул или растворов.
Фармацевтические препараты для перорального применения могут быть получены сочетанием активного соединения с твердыми вспомогательными веществами, с необязательным помолом полученной смеси и обработкой смеси гранул, после добавления подходящих вспомогательных веществ, при желании - с получением таблеток или ядер драже. Подходящими вспомогательными веществами являются, в частности, наполнители, такие как сахара, в том числе, лактоза, сахароза, маннит или сорбит; препараты целлюлозы, например, кукурузный крахмал, пшеничный крахмал, рисовый крахмал, картофельный крахмал, желатин, трагакантовая камедь, метилцеллюлоза, гидроксипропилметилцеллюлоза, натрий карбоксиметилцеллюлоза (КМЦ) и/или поливинилпирролидон (ПВП, повидон). При желании, могут быть добавлены дезинтегранты, такие как поперечно-сшитый поливинилпирролидон, агар или альгиновая кислота или ее соль, такая как натрия альгинат.
Ядра драже покрывают подходящими покрытиями. Для этой цели могут использоваться концентрированные растворы сахара, которые необязательно могут содержать аравийскую камедь, тальк, поливинилпирролидон, гель карбопол, полиэтиленгликоль (ПЭГ) и/или титана диоксид, растворы лака и подходящие органические растворители или смеси растворителей. Красители или пигменты могут быть добавлены к таблеткам или покрытиям драже для идентификации или различения разных комбинаций или доз активного соединения.
Фармацевтические препараты для перорального введения включают твердые сборные желатиновые капсулы, а также мягкие, запечатанные капсулы, изготовленные из желатина и пластификатора, такого как глицерин или сорбит. Сборные капсулы могут содержать активные ингредиенты в смеси с наполнителем, таким как лактоза, связывающими агентами, такими как различные виды крахмала, и/или любрикантами, такими как тальк или магния стеарат, и, необязательно, стабилизаторами. В мягких капсулах активные соединения могут быть растворены или суспендированы в подходящих жидкостях, таких как жирные масла, жидкий парафин или жидкий полиэтиленгликоль (ПЭГ). Кроме того, могут быть добавлены стабилизаторы.
В зависимости от конкретного состояния или заболевания, подлежащего лечению или профилактике, дополнительные терапевтические средства, которые обычно вводят для лечения или профилактики такого состояния, могут быть введены вместе с ингибиторами по данному изобретению. Например, химиотерапевтические средства или антипролиферативные средства могут сочетаться с ингибиторами по данному изобретению для лечения пролиферативных заболеваний и рака. Примеры известных химиотерапевтических средств включают, не ограничиваясь ими, адриамицин, дексаметазон, винкристин, циклофосфамид, фторурацил, топотекан, таксол, интерфероны и производные платины.
Другие примеры агентов, с которыми может сочетаться нерацемический про-олигонуклеотид по данному изобретению, могут также включать, не ограничиваясь ими, противовоспалительные агенты, такие как кортикостероиды, блокаторы опухолевого некротического фактора, IL-1 RA, азатиоприн, циклофосфамид и сульфасалазин; иммуномодуляторы и иммуносупрессивные средства. Такие как циклоспорин, такролимус, рапамицин, микофенолят мофетил, интерферон, кортикостероиды, циклофосфамид, азатиоприн и сульфасалазин, нейротрофные факторы, такие как ингибиторы ацетилхолинэстеразы, ингибиторы МАО, интерфероны, противосудорожные средства, блокаторы ионных каналов, рилузон и противопаркинсонические средства; средства для лечения сердечнососудистого заболевания, такие как бета-блокаторы, ингибиторы АПФ, диуретики, нитраты, блокаторы кальциевых каналов и статины; средства для лечения заболеваний печени, такие как кортикостероиды, холестирамин, интерфероны и противовирусные средства; средства для лечения расстройств крови, такие как кортикостероиды, противолейкозные средства и факторы роста; средства для лечения диабета, такие как инсулин, аналоги инсулина, ингибиторы альфа-глюкозидазы, бигуаниды и инсулиносенсибилизаторы; а также средства для лечения иммунодефицитных расстройств, такие как гамма-глобулин.
Указанные дополнительные средства могут быть введены отдельно, как часть многодозовой схемы, или как часть композиции, содержащей нерацемический про-олигонуклеотид. Альтернативно, указанные средства могут быть частью единой лекарственной формы, смешанные с нерацемическим про-олигонуклеотидом в единой композиции.
Приведенные ниже примеры и препаративные примеры дополнительно иллюстрируют и демонстрируют примеры соединений по данному изобретению и способов получения таких соединений. Следует понимать, что рамки данного изобретения не ограничиваются следующими примерами и препаративными примерами.
ПРИМЕРЫ
Пример 1: Синтез (SP)-1,8-диазабицикло[5,4,0]ундеу-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(SP)-4tt] проиллюстрирован на Схеме А.
Схема А
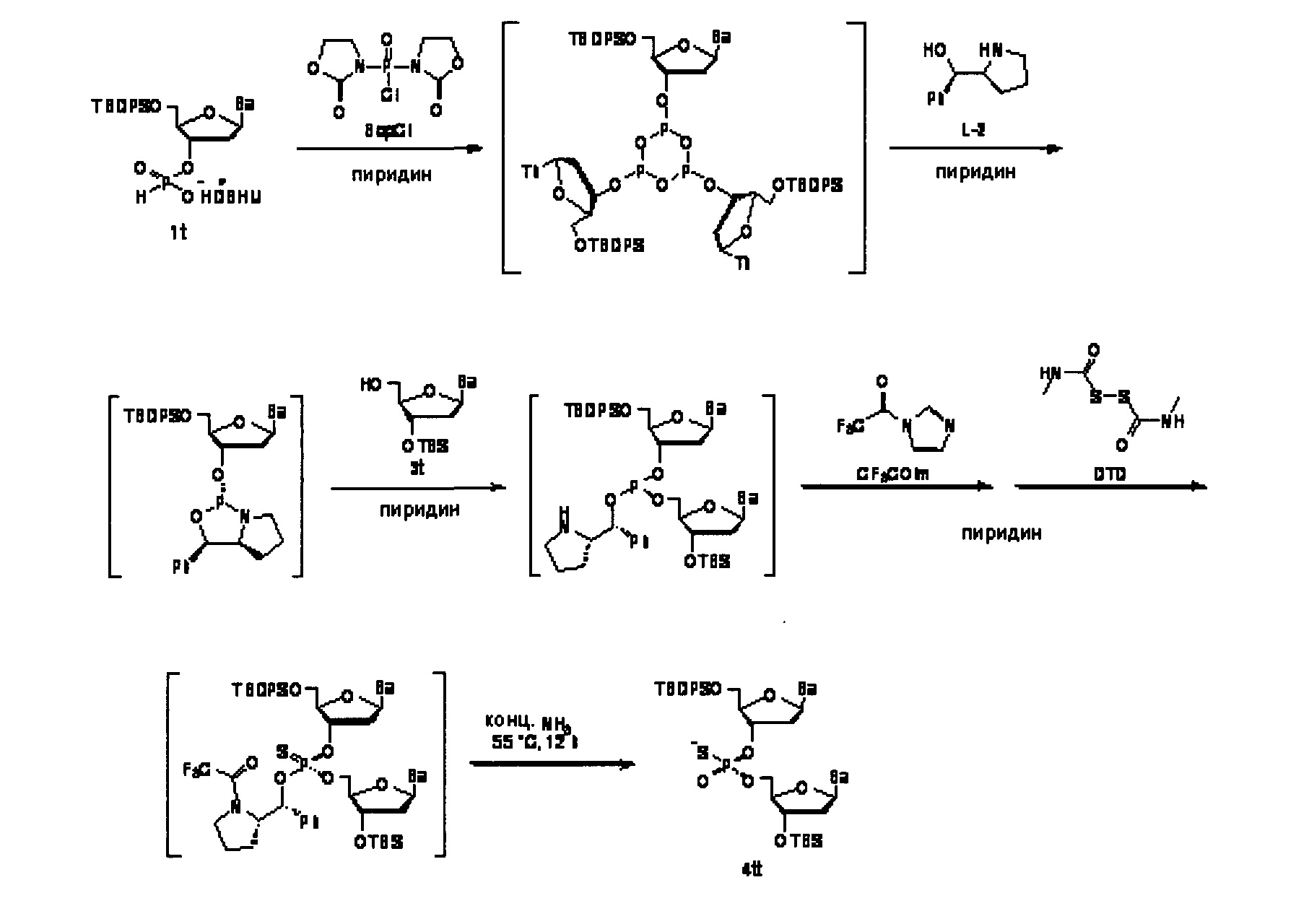
8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил фосфоната (1t) (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl; 500 мкмоль), и смесь перемешивают в течение 5 мин. Раствор аминоспирта (L-2) (100 мкмоль) повторно соупаривают с сухим пиридином и растворяют в сухом пиридине (1 мл). Аминоспирт раствор добавляют к реакционной смеси по каплям с помощью шприца, и смесь перемешивают в течение 5 мин в атмосфере аргона. 3'-O-(трет-Бутилдиметилсилил)тимидин 3t сушат с использованием повторного соупаривания с сухим пиридином и растворяют в 100 мкмоль пиридина. Полученную выше смесь добавляют через канюлю к раствору 3'-O-(трет-бутилдиметилсилил)тимидина 3t в сухом пиридине (100 мкмоль). Через 5 мин добавляют N-трифторацетилимидазол (CF3COIm; 200 мкмоль). Еще через 30 с добавляют N,N'-диметилтиурама дисульфид (ДТД; 120 мкмоль). Еще через 3 мин смесь сушат под вакуумом. Концентрированный раствор NH3 (10 мл) добавляют к остатку, и смесь нагревают до 55°C, выдерживая при этой температуре в течение 12 час. Далее смеси дают остыть до комнатной температуры, и затем упаривают до сухого состояния при сниженном давлении. Смесь разбавляют CHCl3 (5 мл) и промывают 0,2 М фосфатным буферным раствором (рН 7,0, 5 мл). Водные фракции снова экстрагируют CHCl3 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния при сниженном давлении. Остаток очищают РТСХ. Продукт растворяют в CHCl3 (5 мл), промывают 0,2 М буферным раствором 1,8-диазабицикло[5,4,0]ундец-7-ения бикарбоната (5 мл) и снова экстрагируют CHCl3 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния с получением (SP)-4tt.
Пример 2. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-дезоксиаденозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(SP)-4at].
(SP)-4at получают из 1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-дезоксиаденозин-3'-ил фосфоната (1а) вместо 1t, с использованием стадий реакции, описанных в Примере 1 и на Схеме А для (SP)-4tt.
Пример 3. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-дезоксицитидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(SP)-4ct].
(SP)-4ct получают из 1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-дезоксицитидин-3'-ил фосфоната (1с) вместо 1t, с использованием стадий реакции, описанных в Примере 1 и на Схеме A (SP)-4tt.
Пример 4. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)дезоксигуанозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(SP)-4gt].
(SP)-4gt получают из 1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)дезоксигуанозин-3'-ил фосфоната (1 г) вместо 1t, с использованием стадий реакции, описанных в Примере 1 и на Схеме A (SP)-4tt.
Пример 5. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(RP)-4tt].
(RP)-4tt получают путем превращений, описанных в Примере 1 и на Схеме А для синтеза (SP)-4tt с использованием в качестве хирального реагента аминоспирта D-2, вместо L-2.
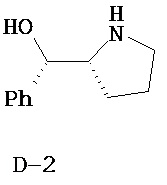
Пример 6. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)дезоксиаденозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(RP)-4at].
(RP)-4at получают путем превращений, описанных в Примере 2, с использованием соединения 1а и аминоспирта D-2 в качестве хирального реагента, вместо L-2.
Пример 7. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)дезоксицитидин-3'-ил 3'-O-{трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(RP)-4ct].
(RP)-4ct получают путем превращений, описанных выше в Примере 3 с использованием соединения 1 с и аминоспирта D-2 в качестве хирального реагента, вместо L-2.
Пример 8. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)дезоксигуанозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(RP)-4gt].
(RP)-4gt получают путем превращений, описанных выше в Примере 4, с использованием соединения 1 г и аминоспирта D-2 в качестве хирального реагента, вместо L-2.
Схема Б
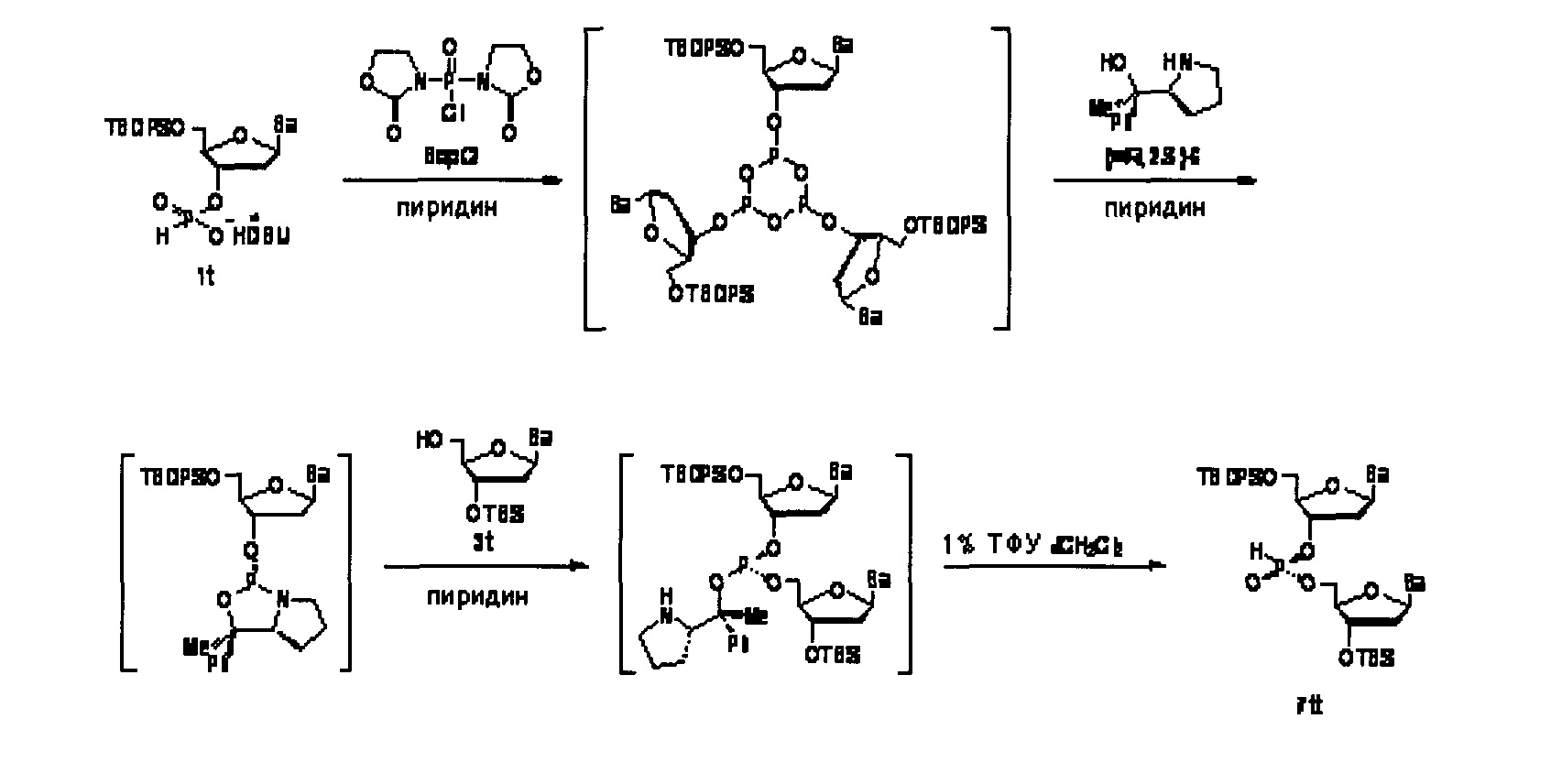
Пример 9. Синтез (RP)-5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(RP)-7tt], как описано на Схеме Б.
1t (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl; 500 мкмоль), и смесь перемешивают в течение 5 мин. К смеси с помощью шприца добавляют по каплям раствор аминоспирта ((αR, 2S)-6) (100 мкмоль), высушенный путем соупаривания с сухим пиридином, растворяют в сухом пиридине (1 мл), и смесь перемешивают в течение 5 мин в атмосфере аргона. 3'-O-(трет-Бутилдиметилсилил)тимидин сушат с использованием повторного соупаривания с сухим пиридином и растворяют в 100 мкмоль пиридина. Полученную выше смесь добавляют через канюлю к раствору 3'-O-(трет-бутилдиметилсилил)тимидина 3t в сухом пиридине (100 мкмоль). Через 15 мин смесь упаривают при сниженном давлении. Остаток разбавляют CH2Cl2 (5 мл) и промывают насыщенным раствором NaHCO3 (3×5 мл). Объединенные водные фракции снова экстрагируют CH2Cl2 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до объема приблизительно 1 мл при сниженном давлении. Остаток добавляют по каплям с помощью шприца при перемешивании к 1% раствору трифторуксусной кислоты (ТФУ) в сухом CH2Cl2 (20 мл) при 0°C. Еще через 5 мин смесь разбавляют сухим CH2Cl2 (100 мл) и промывают насыщенным водным раствором NaHCO3 (2×100 мл). Объединенные водные фракции снова экстрагируют CH2Cl2 (2×100 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния при сниженном давлении с получением неочищенного (RP)-7tt.
Пример 10. Синтез (RP)-6-N-бензоил-5'-O-(трет-бутилдифенилсилил)дезоксиаденозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(RP)-7at].
Неочищенный (RP)-7at получают, как описано в Примере 9, с использованием 1а вместо 1t.
Пример 11. Синтез (RP)-4-N-бензоил-5'-O-(трет-бутилдифенилсилил)дезоксицитидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(RP)-7ct].
Неочищенный (RP)-7ct получают, как описано в Примере 9, с использованием 1 с вместо 1t.
Пример 12. Синтез (Rp)-2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)дезоксигуанозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(RP)-7gt].
Неочищенный (RP)-7gt получают, как описано в Примере 9, с использованием 1 г вместо 1t.
Пример 13. Синтез (SP)-5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(SP)-7tt].
Неочищенный (SP)-7tt получают, как описано в Примере 9, с использованием (αS, 2R)-6 вместо (αR, 2S)-6 в качестве хирального реагента.
Пример 14. Синтез (SP)-6-N-бензоил-5'-O-(трет-бутилдифенилсилил)дезоксиаденозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(SP)-7at].
Неочищенный (SP)-7at получают, как описано в Примере 9, с использованием соединения 1а и (αS, 2R)-6 вместо (αR, 2S)-6 в качестве хирального реагента.
Пример 15. Синтез (SP)-4-N-бензоил-5'-O-(трет-бутилдифенилсилил)дезоксицитидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(SP)-7ct].
Неочищенный (SP)-7ct получают, как описано в Примере 9, с использованием соединения 1с и (αS, 2R)-6 вместо (□R, 2S)-6 в качестве хирального реагента.
Пример 16. Синтез (SP)-2-N-феноксиацетил-5'-(9-(трет-бутилдифенилсилил)дезоксигуанозин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфоната [(SP)-7gt].
Неочищенный (SP)-7gt получают, как описано в Примере 9, с использованием соединения 1 г вместо 1t и соединения (αS, 2R)-6 вместо соединения (□R, 2S)-6 в качестве хирального реагента.
Схема В
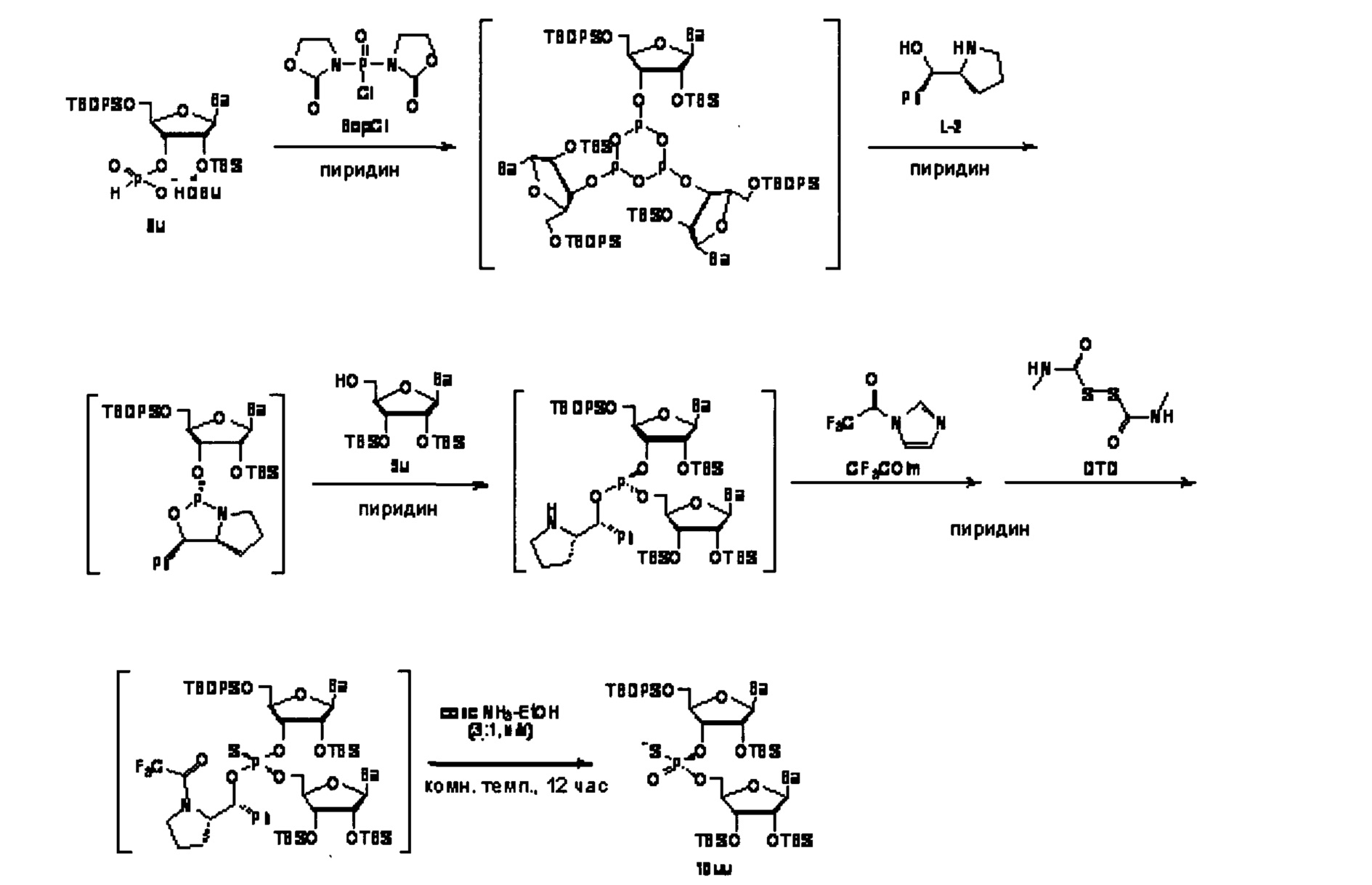
Пример 17. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)уридин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-10uu].
1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)уридин-3'-ил фосфонат (8u) (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl; 500 мкмоль), и смесь перемешивают в течение 5 мин. К смеси добавляют по каплям с помощью шприца раствор аминоспирта (L-2) (100 мкмоль), высушенный повторным соупариванием с сухим пиридином с сухим пиридином и растворяют в сухом пиридине (1 мл), и смесь перемешивают в течение 5 мин в атмосфере аргона. 2',3'-O-Бис(трет-бутилдиметилсилил)уридин 9u сушат повторным соупариванием с сухим пиридином и растворяют в 100 мкмоль пиридина. Затем полученную выше смесь добавляют через канюлю к раствору 2',3'-O-бис(трет-бутилдиметилсилил)уридина 9u (100 мкмоль). Через 10 мин добавляют N-трифторацетилимидазол (CF3COIm; 200 мкмоль). Еще через 30 с добавляют N,N'-диметилтиурама дисульфид (ДТД; 120 мкмоль). Еще через 3 мин смесь сушат под вакуумом. К остатку добавляют конц. NH3-EtOH (3:1, об/об, 10 мл), смесь перемешивают в течение 12 час, и затем упаривают до сухого состояния при сниженном давлении. Далее смесь разбавляют CHCl3 (5 мл) и промывают 0,2 М фосфатным буферным раствором (рН 7,0, 5 мл). Водные фракции снова экстрагируют CHCl3 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния при сниженном давлении. Остаток очищают РТСХ. Продукт растворяют в CHCl3 (5 мл), промывают 0,2 М буферным раствором 1,8-диазабицикло[5,4,0]ундец-7-ения бикарбоната (5 мл) и снова экстрагируют CHCl3 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния с получением (SP)-10uu.
Пример 18. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)аденозин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-10au].
(SP)-10au получают, как описано в Примере 17, с использованием 1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)аденозин-3'-ил фосфоната (8а) вместо 8u.
Пример 19. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)цитидин-3'-ил 2',3'-(9-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-10cu].
(SP)-10cu получают, как описано в Примере 17, с использованием 1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-(9-(трет-бутилдифенилсилил)-2'-(9-(трет-бутилдиметилсилил)цитидин-3'-ил фосфоната (8с) вместо 8u.
Пример 20. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-(9-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)гуанозин-3'-ил 2',3'-(9-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-10gu].
(SP)-10gu получают, как описано в Примере 17, с использованием 1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)гуанозин-3'-ил фосфоната (8 г) вместо 8u.
Пример 21. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)уридин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(RP)-10uu].
(RP)-10uu получают, как описано в Примере 17, с использованием хирального реагента D-2 вместо хирального реагента L-2.
Пример 22. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)аденозин-3'-ил 2',3'-(9-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(RP)-10au].
(RP)-10au получают, как описано в Примере 17, с использованием 8а вместо 8u и хирального реагента D-2 вместо хирального реагента L-2.
Пример 23. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-(9-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)цитидин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(RP)-10cu].
(RP)-10cu получают, как описано в Примере 17, с использованием 8 с вместо 8u и хирального реагента D-2 вместо хирального реагента L-2.
Пример 24. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)гуанозин-3'-ил 2',3'-(9-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(RP)-10gu].
(RP)-10gu получают, как описано в Примере 17, с использованием 8 г вместо 8u и хирального реагента D-2 вместо хирального реагента L-2.
Схема Г
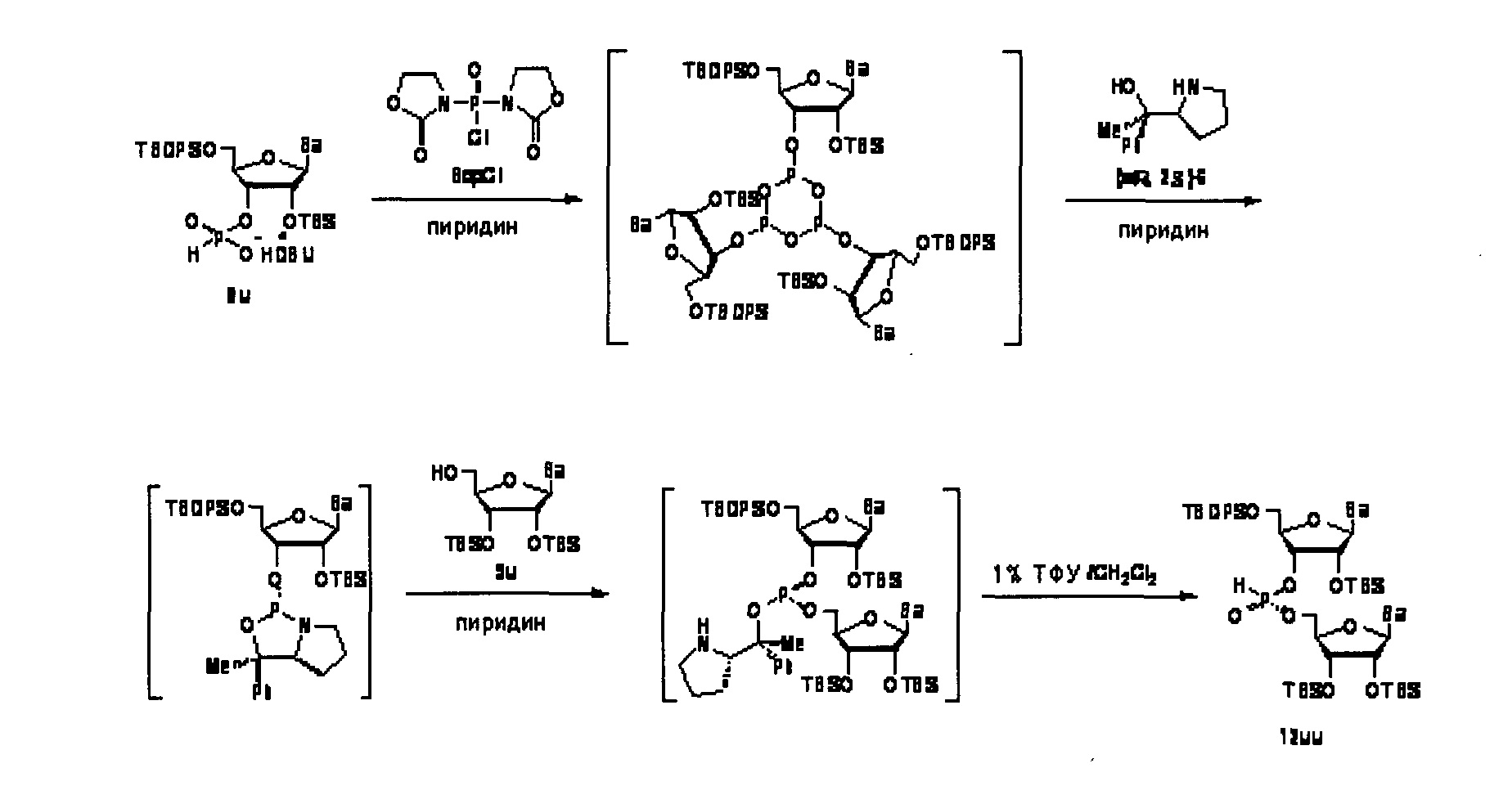
Пример 25. Синтез (RP)-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)уридин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-12uu].
8u (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl; 500 мкмоль), и смесь перемешивают в течение 5 мин. К смеси добавляют по каплям с помощью шприца раствор аминоспирта ((αR, 2S)-6) (100 мкмоль), высушенного соупариванием с сухим пиридином и растворенного в сухом пиридине (1 мл), и смесь перемешивают в течение 5 мин в атмосфере аргона. Далее смесь добавляют через канюлю к раствору 9 ч (100 мкмоль), полученному повторным соупариванием с сухим пиридином и растворением в пиридине. Через 15 мин смесь упаривают при сниженном давлении. Остаток разбавляют CH2Cl2 (5 мл) и промывают насыщенным раствором NaHCO3 (3×5 мл). Объединенные водные фракции снова экстрагируют CH2Cl2 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до объема приблизительно 1 мл при сниженном давлении. Остаток добавляют по каплям с помощью шприца при перемешивании к 1% раствору трифторуксусную кислоту (ТФУ) в сухом CH2Cl2 (20 мл) при 0°C. Еще через 5 мин смесь разбавляют сухим CH2Cl2 (100 мл) и промывают насыщенным водным раствором NaHCO3 (2×100 мл). Объединенные водные фракции снова экстрагируют CH2Cl2 (2×100 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния при сниженном давлении с получением неочищенного (Rp)-12uu, который анализируют методом 31P ЯМР.
Пример 26. Синтез (RP)-6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)аденозин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-12au].
Неочищенный (RP)-12au получают, как описано в Примере 25, с использованием 8а вместо 8u.
Пример 27. Синтез (RP)-4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)цитидин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-12 cu].
Неочищенный (RP)-12cu получают, как описано в Примере 25, с использованием 8с вместо 8u.
Пример 28. Синтез (RP)-2-N-Феноксиацетил-5'-O-(трет-бутилдифенилсилил)-2'-(9-(трет-бутилдиметилсилил)гуанозин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-12gu].
Неочищенный (RP)-12gu получают, как описано в Примере 25, с использованием 8г вместо 8u.
Пример 29. Синтез (SP)-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)уридин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-12uu].
Неочищенный (SP)-12uu получают, как описано в Примере 25, с использованием хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Пример 30. Синтез (SP)-6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)аденозин-3'-ил 2',3'-(9-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-12au].
Неочищенный (SP)-12au получают, как описано в Примере 25, с использованием 8а вместо 8u и хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Пример 31. Синтез (SP)-4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)питидин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-12cu].
Неочищенный (SP)-12cu получают, как описано в Примере 25, с использованием 8с вместо 8u и хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Пример 32. Синтез (SP)-2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)-2'-O-(трет-бутилдиметилсилил)гуанозин-3'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-12gu].
Неочищенный (SP)-12gu получают, как описано в Примере 25, с использованием 8г вместо 8u и хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Схема Д
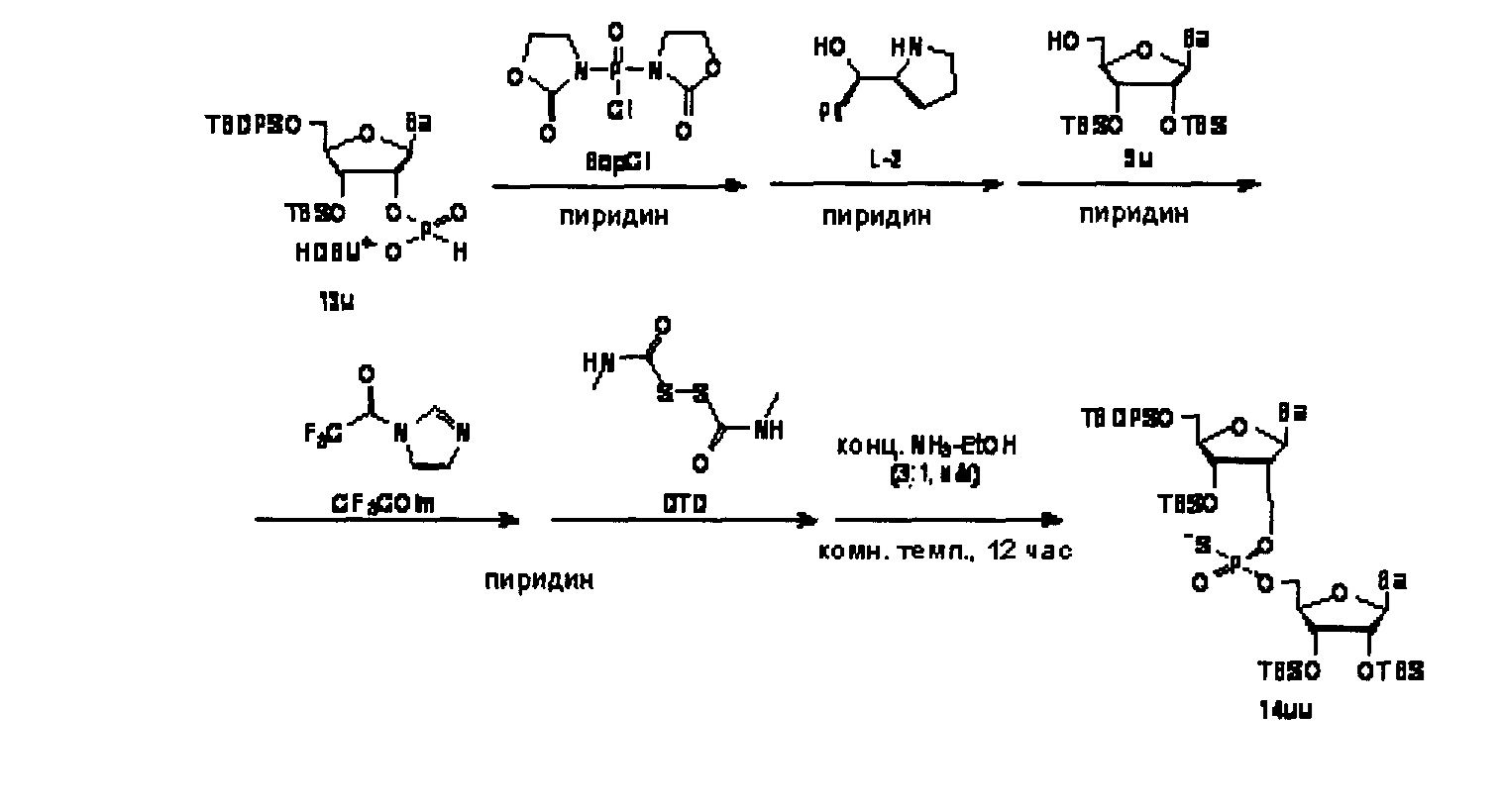
Пример 33. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)уридин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-14uu].
1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)уридин-3'-ил фосфонат (13u) (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl; 500 мкмоль), и смесь перемешивают в течение 5 мин. К смеси добавляют по каплям с помощью шприца раствор аминоспирта (L-2) (100 мкмоль), высушенного повторным соупариванием с сухим пиридином и растворенного в сухом пиридине (1 мл), и смесь перемешивают в течение 5 мин в атмосфере аргона. 2',3'-(9-Бис(трет-бутилдиметилсилил)уридин 9 ч сушат повторным соупариванием с сухим пиридином и растворяют в 100 мкмоль пиридина. Далее полученную выше смесь добавляют через канюлю к раствору 2',3'-O-бис(трет-бутилдиметилсилил)уридина 9u (100 мкмоль). Через 10 мин добавляют N-трифторацетилимидазол (CF3COIm; 200 мкмоль). Еще через 30 с добавляют N,N'-диметилтиурама дисульфид (ДТД; 120 мкмоль). Еще через 3 мин смесь сушат под вакуумом. К остатку добавляют конц. NH3-EtOH (3:1, об./об., 10 мл), смесь перемешивают в течение 12 час, и затем упаривают до сухого состояния при сниженном давлении. Далее, смесь разбавляют CHCl3 (5 мл) и промывают 0,2 М фосфатным буферным раствором (рН 7,0, 5 мл). Водные фракции снова экстрагируют CHCl3 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния при сниженном давлении. Остаток очищают РТСХ. Продукт растворяют в CHCl3 (5 мл), промывают 0,2 М буферным раствором 1,8-диазабицикло[5,4,0]ундец-7-ения бикарбоната (5 мл) и снова экстрагируют CHCl3 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния с получением (SP)-14uu.
Пример 34. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)аденозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-14au].
(SP)-14au получают, как описано в Примере 33, с использованием 1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)аденозин-2'-ил фосфоната (13а) вместо 13u.
Пример 35. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)цитидин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(SP)-14cu].
(SP)-14cu получают, как описано в Примере 33, с использованием 1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)цитидин-2'-ил фосфоната (13с) вместо 13u.
Пример 36. Синтез (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-О-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)гуанозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоат [(SP)-14gu].
(SP)-14gu получают, как описано в Примере 33, с использованием 1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)гуанозин-2'-ил фосфоната (13 г) вместо 13u.
Пример 37. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)уридин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоат [(RP)-14uu].
(RP)-14uu получают, как описано в Примере 33, с использованием хирального реагента D-2 вместо хирального реагента L-2.
Пример 38. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-(9-(трет-бутилдиметилсилил)аденозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоат [(RP)-14au].
(RP)-14au получают, как описано в Примере 33, с использованием 13а вместо 13u и хирального реагента D-2 вместо хирального реагента L-2.
Пример 39. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)цитидин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(RP)-14cu].
(RP)-14cu получают, как описано в Примере 33, с использованием 13с вместо 13u и хирального реагента D-2 вместо хирального реагента L-2.
Пример 40. Синтез (RP)-1,8-диазабицикло[5,4,0]ундец-7-ения 2-N-феноксиацетил-5'-(9-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)гуанозин-2'-ил 2',3'-(9-бис(трет-бутилдиметилсилил)уридин-5'-ил фосфортиоата [(RP)-14gu].
(RP)-14gu получают, как описано в Примере 33, с использованием 13г вместо 13u и хирального реагента D-2 вместо хирального реагента L-2.
Схема Е
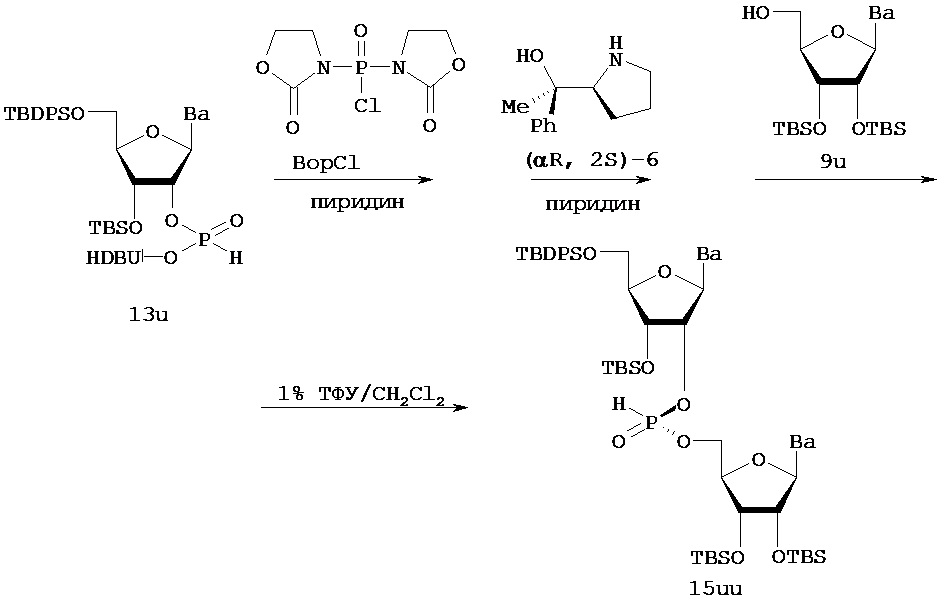
Пример 41. Синтез (RP)-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)уридин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-15uu].
13u (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N,N'-бис(2-оксо-3-оксазолидинил)фосфиния хлорид (BopCl; 500 мкмоль), и смесь перемешивают в течение 5 мин. К смеси по каплям с помощью шприца добавляют раствор аминоспирта ((αR, 2S)-6) (100 мкмоль), высушенного соупариванием с сухим пиридином и растворенного в сухом пиридине (1 мл), и смесь перемешивают в течение 5 мин в атмосфере аргона. Далее смесь добавляют через канюлю к раствору 9u (100 мкмоль), полученному повторным соупариванием с сухим пиридином и растворением в пиридине. Через 15 мин смесь упаривают при сниженном давлении. Остаток разбавляют CH2Cl2 (5 мл) и промывают насыщенным раствором NaHCO3 (3×5 мл). Объединенные водные фракции снова экстрагируют CH2Cl2 (2×5 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до объема приблизительно 1 мл при сниженном давлении. Остаток добавляют по каплям с помощью шприца при перемешивании к раствору 1% трифторуксусной кислоты (ТФУ) в сухом CH2Cl2 (20 мл) при 0°C. Еще через 5 мин смесь разбавляют сухим CH2Cl2 (100 мл) и промывают насыщенным водным раствором NaHCO3 (2×100 мл). Объединенные водные фракции снова экстрагируют CH2Cl2 (2×100 мл). Объединенные органические фракции сушат над Na2SO4, фильтруют и упаривают до сухого состояния при сниженном давлении с получением неочищенного (Rp)-15uu, который анализируют методом 31P ЯМР.
Пример 42. Синтез (RP)-6-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)аденозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-15au].
Неочищенный (RP)-15au получают, как описано в Примере 41, с использованием 13а вместо 13u.
Пример 43. Синтез (RP)-4-N-бензоил-5'-(9-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)цитидин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-15cu].
Неочищенный (RP)-15cu получают, как описано в Примере 41, с использованием 13с вместо 13u.
Пример 44. Синтез (RP)-2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)гуанозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(RP)-15gu].
Неочищенный (RP)-15gu получают, как описано в Примере 41, с использованием 13г вместо 13u.
Пример 45. Синтез (SP)-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)уридин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-15uu].
Неочищенный (SP)-15uu получают, как описано в Примере 41, с использованием хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Пример 46. Синтез (SP)-6-N-бензоил-5'-O-(трет-бутилдафенилсилил)-3'-O-(трет-бутилдиметилсилил)аденозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-15au].
Неочищенный (SP)-15au получают, как описано в Примере 41, с использованием 13а вместо 13u и хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Пример 47. Синтез (SP)-4-N-бензоил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)цитидин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-15cu].
Неочищенный (SP)-15cu получают, как описано в Примере 41, с использованием 13с вместо 13u и хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Пример 48. Синтез (SP)-2-N-феноксиацетил-5'-O-(трет-бутилдифенилсилил)-3'-O-(трет-бутилдиметилсилил)гуанозин-2'-ил 2',3'-O-бис(трет-бутилдиметилсилил)уридин-5'-ил H-фосфоната [(SP)-15gu].
Неочищенный (SP)-15gu получают, как описано в Примере 41, с использованием 13г вместо 13u и хирального реагента (αS, 2R)-6 вместо хирального реагента (αR, 2S)-6.
Схема Ж: Синтез пролекарств 8-ацил-2-тиоэтил нуклеиновой кислоты.
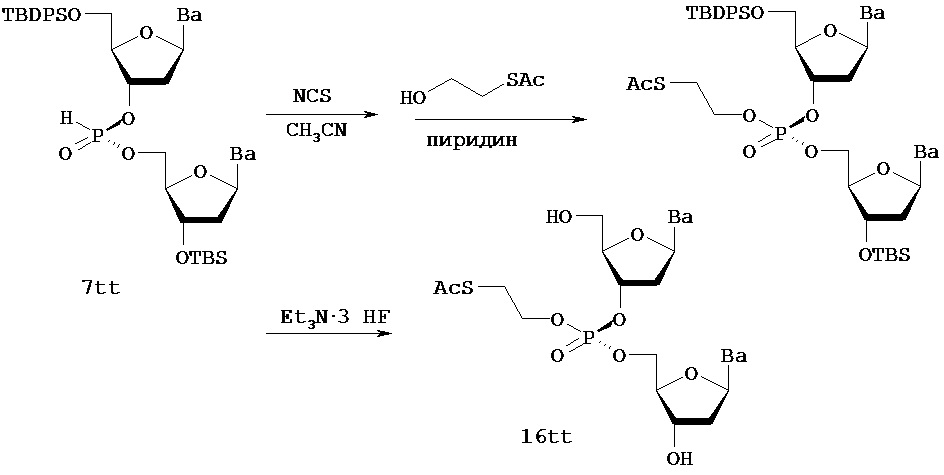
Пример 49. Синтез пролекарства 8-ацил-2-тиоэтилнуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-16tt], как описано на Схеме Ж.
(RP)-5'-O-(трет-Бутилдифенилсилил)тимидин-3'-ил 3'-O-{трет-бутилдиметилсилил)тимидин-5'-ил H-фосфонат [(RP)-7tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают 8-ацетил-2-тиоэтанолом (100 мкмоль) в сухом (100 мкмоль) пиридине. Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. А 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-16tt.
Пример 50. Синтез 8-ацил-2-тиоэтил пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(RP)-16at].
Неочищенный (RP)-16at получают, как описано в Примере 49, с использованием (RP)-7at вместо (RP)-7tt.
Пример 51. Синтез 8-ацил-2-тиоэтил пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(RP)-16ct].
Неочищенный (RP)-16ct получают, как описано в Примере 49, с использованием (RP)-7ct вместо (RP)-7tt.
Пример 52. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(RP)-16gt].
Неочищенный (RP)-16gt получают, как описано в Примере 49, с использованием (RP)-7г вместо (RP)-7tt.
Пример 53. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(SP)-16tt].
Неочищенный (SP)-16tt получают, как описано в Примере 49, с использованием (SP)-7tt вместо (RP)-7tt.
Пример 54. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(SP)-16at].
Неочищенный (SP)-16at получают, как описано в Примере 49, с использованием (SP)-7at вместо (RP)-7tt.
Пример 55. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(SP)-16ct].
Неочищенный (SP)-16ct получают, как описано в Примере 49, с использованием (SP)-7ct вместо (RP)-7tt.
Пример 56. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(SP)-16gt].
Неочищенный (SP)-16gt получают, как описано в Примере 49, с использованием (SP)-7gt вместо (RP)-7tt.
Пример 57. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфоната [(RP)-16uu].
Неочищенный (RP)-16uu получают, как описано в Примере 49, с использованием (RP)-12uu вместо (RP)-7tt.
Пример 58. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(RP)-16au].
Неочищенный (RP)-16au получают, как описано в Примере 49, с использованием (RP)-12au вместо (RP)-7tt.
Пример 59. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(RP)-16cu].
Неочищенный (RP)-16cu получают, как описано в Примере 49, с использованием (RP)-12cu вместо (RP)-7tt.
Пример 60. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(RP)-16gu].
Неочищенный (RP)-16gu получают, как описано в Примере 49, с использованием (RP)-12gu вместо (RP)-7tt.
Пример 61. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфоната [(SP)-16uu].
Неочищенный (SP)-16uu получают, как описано в Примере 49, с использованием (SP)-12uu вместо (RP)-7tt.
Пример 62. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(SP)-16au].
Неочищенный (SP)-16au получают, как описано в Примере 49, с использованием (SP)-12au вместо (RP)-7tt.
Пример 63. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(SP)-16cu].
Неочищенный (SP)-16cu получают, как описано в Примере 49, с использованием (SP)-12au вместо (RP)-7tt.
Пример 64. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(SP)-16gu].
Неочищенный (SP)-16gu получают, как описано в Примере 49, с использованием (SP)-12gu вместо (RP)-7tt.
Пример 65. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфоната [(RP)-17uu].
Неочищенный (SP)-17uu получают, как описано в Примере 49, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 66. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(RP)-17au].
Неочищенный (RP)-17au получают, как описано в Примере 49, с использованием (SP)-15au вместо (RP)-7tt.
Пример 67. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(RP)-17cu].
Неочищенный (RP)-17cu получают, как описано в Примере 49, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 68. Синтез S-ацил-2-тиоэтил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил H-фосфоната [(RP)-17gu].
Неочищенный (RP)-17gu получают, как описано в Примере 49, с использованием (SP)-15gu вместо (RP)-7tt.
Пример 69. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфоната [(SP)-17uu].
Неочищенный (SP)-17uu получают, как описано в Примере 49, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 70. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(SP)-17au].
Неочищенный (SP)-17au получают, как описано в Примере 49, с использованием (SP)-15au вместо (RP)-7tt.
Пример 71. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(SP)-17cu].
Неочищенный (SP)-17cu получают, как описано в Примере 49, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 72. Синтез S-ацил-2-тиоэтил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфоната [(SP)-17gu].
Неочищенный (SP)-17gu получают, как описано в Примере 49, с использованием (SP)-15gu вместо (RP)-7tt.
Схема 3: Синтез ацилокси пронуклеотидов.
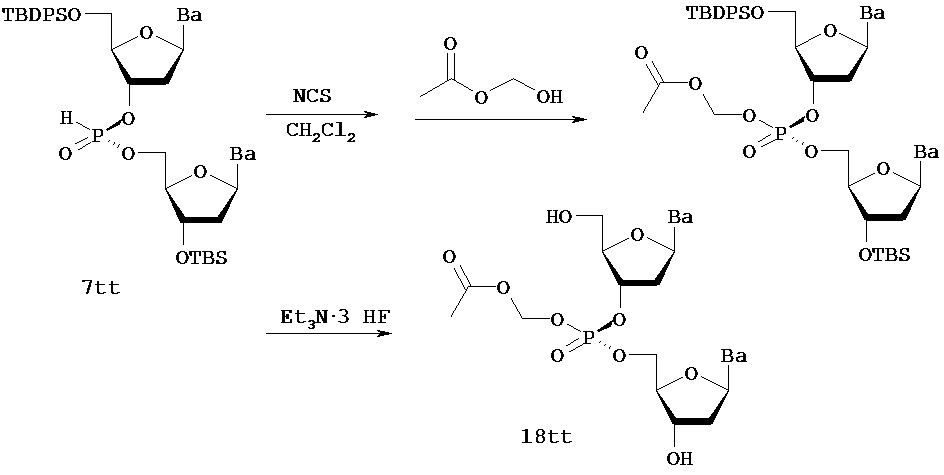
Пример 73. Синтез ацилокси пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-18tt], как описано на Схеме З.
(RP)-5'-O-(трет-Бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфонат [(RP)-7tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают гидроксиметилацетатом (100 мкмоль) в сухом (100 мкмоль) метиленхлориде. Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-18tt.
Пример 74. Синтез ацилокси пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(RP)-18at].
Неочищенный (RP)-18at получают, как описано в Примере 73, с использованием (RP)-7at вместо (RP)-7tt.
Пример 75. Синтез ацилокси пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(RP)-18ct].
Неочищенный (RP)-18ct получают, как описано в Примере 73, с использованием (RP)-7ct вместо (RP)-7tt.
Пример 76. Синтез ацилокси пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(RP)-18gt].
Неочищенный (RP)-18gt получают, как описано в Примере 73, с использованием (RP)-7г вместо (RP)-7tt.
Пример 77. Синтез ацилокси пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(SP)-18tt].
Неочищенный (SP)-18tt получают, как описано в Примере 73, с использованием (SP)-7tt вместо (RP)-7tt.
Пример 78. Синтез ацилокси пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(SP)-18at].
Неочищенный (SP)-18at получают, как описано в Примере 73, с использованием (SP)-7at вместо (RP)-7tt.
Пример 79. Синтез ацилокси пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(SP)-18ct].
Неочищенный (SP)-18ct получают, как описано в Примере 73, с использованием (SP)-7ct вместо (RP)-7tt.
Пример 80. Синтез ацилокси пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(SP)-18gt].
Неочищенный (SP)-18gt получают, как описано в Примере 73, с использованием (SP)-7gt вместо (RP)-7tt.
Пример 81. Синтез ацилокси пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфоната [(RP)-18uu].
Неочищенный (RP)-18uu получают, как описано в Примере 73, с использованием (RP)-12uu вместо (RP)-7tt.
Пример 82. Синтез ацилокси пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(RP)-18au].
Неочищенный (RP)-18au получают, как описано в Примере 73, с использованием (RP)-12au вместо (RP)-7tt.
Пример 83. Синтез ацилокси пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(RP)-18cu].
Неочищенный (RP)-18cu получают, как описано в Примере 73, с использованием (RP)-12cu вместо (RP)-7tt.
Пример 84. Синтез ацилокси пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(RP)-18gu].
Неочищенный (RP)-18gu получают, как описано в Примере 73, с использованием (RP)-12gu вместо (RP)-7tt.
Пример 85. Синтез ацилокси пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфоната [(SP)-18uu].
Неочищенный (SP)-18uu получают, как описано в Примере 73, с использованием (SP)-12uu вместо (RP)-7tt.
Пример 86. Синтез ацилокси пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(SP)-18au].
Неочищенный (SP)-18au получают, как описано в Примере 73, с использованием (SP)-12au вместо (RP)-7tt.
Пример 87. Синтез ацилокси пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(SP)-18cu].
Неочищенный (SP)-18cu получают, как описано в Примере 73, с использованием (SP)-12au вместо (RP)-7tt.
Пример 88. Синтез ацилокси пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(SP)-18gu].
Неочищенный (SP)-18gu получают, как описано в Примере 73, с использованием (SP)-12gu вместо (RP)-7tt.
Пример 89. Синтез ацилокси пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфоната [(RP)-19uu].
Неочищенный (SP)-19uu получают, как описано в Примере 73, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 90. Синтез ацилокси пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(RP)-19au].
Неочищенный (RP)-19au получают, как описано в Примере 73, с использованием (SP)-15au вместо (RP)-7tt.
Пример 91. Синтез ацилокси пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(RP)-19cu].
Неочищенный (RP)-19cu получают, как описано в Примере 73, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 92. Синтез ацилокси пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфоната [(RP)-19gu].
Неочищенный (RP)-19gu получают, как описано в Примере 73, с использованием (SP)-15gu вместо (RP)-7tt.
Пример 93. Синтез ацилокси пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфоната [(SP)-19uu].
Неочищенный (SP)-19uu получают, как описано в Примере 73, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 94. Синтез ацилокси пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(SP)-19au].
Неочищенный (SP)-19аи получают, как описано в Примере 73, с использованием (SP)-15au вместо (RP)-7tt.
Пример 95. Синтез ацилокси пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(SP)-19cu].
Неочищенный (SP)-19cu получают, как описано в Примере 73, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 96. Синтез ацилокси пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфоната [(SP)-19gu].
Неочищенный (SP)-19gu получают, как описано в Примере 73, с использованием (SP)-15gu вместо (RP)-7tt.
Схема И: Синтез тиоацилокси пронуклеотидов.
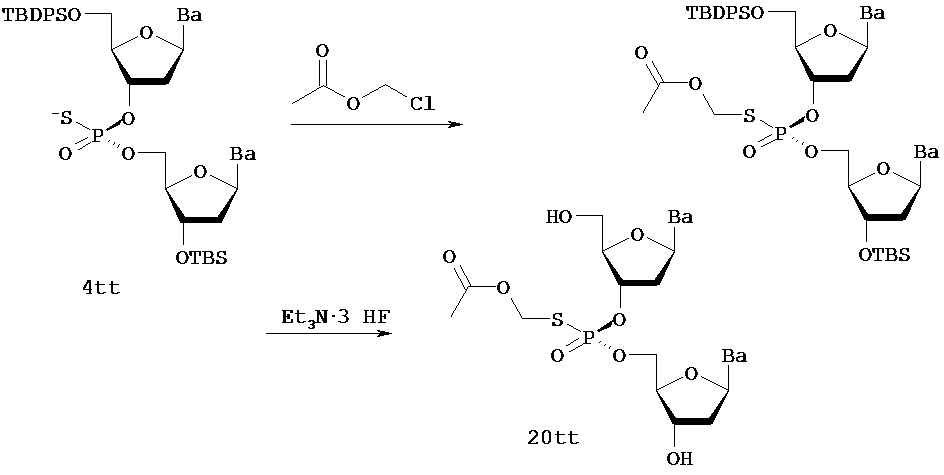
Пример 97. Синтез тиоацилокси пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-20tt], как описано на Схеме I.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоата [(SP)-4tt) (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом метиленхлориде (1 мл). Смесь обрабатывают хлорметилацетатом, полученным по способу Bodor et al. J. Org. Chem. (1983), 48:5280 (100 мкмоль) в сухом (100 мкмоль) метиленхлориде. Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-20tt.
Пример 98. Синтез тиоацилокси пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-20at].
Неочищенный (RP)-20at получают, как описано в Примере 97, с использованием (RP)-4at вместо (RP)-4tt.
Пример 99. Синтез тиоацилокси пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-20ct].
Неочищенный (RP)-20ct получают, как описано в Примере 97, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 100. Синтез тиоацилокси пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-20gt].
Неочищенный (RP)-20gt получают, как описано в Примере 97, с использованием (RP)-4 г вместо (RP)-4tt.
Пример 101. Синтез тиоацилокси пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-20tt].
Неочищенный (SP)-20tt получают, как описано в Примере 97, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 102. Синтез тиоацилокси пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-20at].
Неочищенный (SP)-20at получают, как описано в Примере 97, с использованием (SP)-4at вместо (RP)-4tt.
Пример 103. Синтез тиоацилокси пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-20ct].
Неочищенный (SP)-20ct получают, как описано в Примере 97, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 104. Синтез тиоацилокси пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-20gt].
Неочищенный (SP)-20gt получают, как описано в Примере 97, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 105. Синтез тиоацилокси пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-20uu].
Неочищенный (RP)-20uu получают, как описано в Примере 97, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 106. Синтез тиоацилокси пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-20au].
Неочищенный (RP)-20au получают, как описано в Примере 97, с использованием (RP)-10au вместо (RP)-4tt.
Пример 107. Синтез тиоацилокси пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-20cu].
Неочищенный (RP)-20cu получают, как описано в Примере 97, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 108. Синтез тиоацилокси пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-20gu].
Неочищенный (RP)-20gu получают, как описано в Примере 97, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 109. Синтез тиоацилокси пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-20uu].
Неочищенный (SP)-20uu получают, как описано в Примере 97, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 110. Синтез тиоацилокси пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-20au].
Неочищенный (SP)-20au получают, как описано в Примере 97, с использованием (SP)-10au вместо (RP)-4tt.
Пример 111. Синтез тиоацилокси пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-20cu].
Неочищенный (SP)-20cu получают, как описано в Примере 97, с использованием (SP)-10au вместо (RP)-4tt.
Пример 112. Синтез тиоацилокси пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-20gu].
Неочищенный (SP)-20gu получают, как описано в Примере 97, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 113. Синтез тиоацилокси пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-21uu].
Неочищенный (SP)-21uu получают, как описано в Примере 97, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 114. Синтез тиоацилокси пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-21au].
Неочищенный (RP)-21au получают, как описано в Примере 97, с использованием (SP)-14au вместо (RP)-4tt.
Пример 115. Синтез тиоацилокси пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-21cu].
Неочищенный (RP)-21cu получают, как описано в Примере 97, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 116. Синтез тиоацилокси пронуклеотида (RP)-2-N-феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-21gu].
Неочищенный (RP)-21gu получают, как описано в Примере 97, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 117. Синтез тиоацилокси пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-21uu].
Неочищенный (SP)-21uu получают, как описано в Примере 97, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 118. Синтез тиоацилокси пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-21au].
Неочищенный (SP)-21au получают, как описано в Примере 97, с использованием (SP)-14au вместо (RP)-4tt.
Пример 119. Синтез тиоацилокси пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-21cu].
Неочищенный (SP)-21cu получают, как описано в Примере 97, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 120. Синтез тиоацилокси пронуклеотида (SP)-2-N-феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-21gu].
Неочищенный (SP)-21gu получают, как описано в Примере 97, с использованием (SP)-14gu вместо (RP)-4tt.
Схема К: Синтез 2-карбоалкоксиэтил пронуклеотидов.
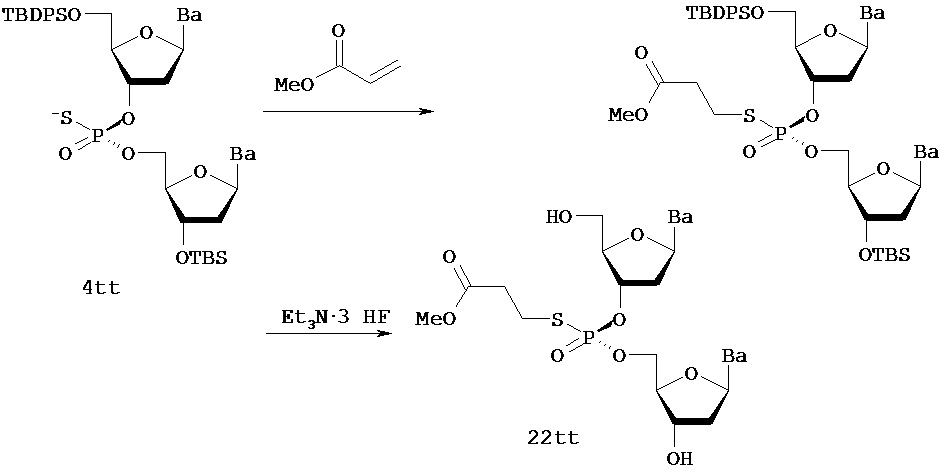
Пример 121. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-22tt], как описано на Схеме К.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом метиленхлориде (1 мл). Смесь обрабатывают метилакрилатом (100 мкмоль) в сухом (100 мкмоль) метиленхлориде. Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-22tt.
Пример 122. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-22at].
Неочищенный (RP)-22at получают, как описано в Примере 121, с использованием (RP)-4at вместо (RP)-4tt.
Пример 123. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-22ct].
Неочищенный (RP)-22ct получают, как описано в Примере 121, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 124. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-22gt].
Неочищенный (RP)-22gt получают, как описано в Примере 121, с использованием (RP)-4г вместо (RP)-4tt.
Пример 125. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-22tt].
Неочищенный (SP)-22tt получают, как описано в Примере 121, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 126. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-22at].
Неочищенный (SP)-22at получают, как описано в Примере 121, с использованием (SP)-4at вместо (RP)-4tt.
Пример 127. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-22ct].
Неочищенный (SP)-22ct получают, как описано в Примере 121, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 128. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-22gt].
Неочищенный (SP)-22gt получают, как описано в Примере 121, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 129. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-22uu].
Неочищенный (RP)-22uu получают, как описано в Примере 121, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 130. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-22au].
Неочищенный (RP)-22au получают, как описано в Примере 121, с использованием (RP)-10au вместо (RP)-4tt.
Пример 131. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-22cu].
Неочищенный (RP)-22cu получают, как описано в Примере 121, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 132. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-22gu].
Неочищенный (RP)-22gu получают, как описано в Примере 121, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 133. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-22uu].
Неочищенный (SP)-22uu получают, как описано в Примере 121, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 134. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-22au].
Неочищенный (SP)-22au получают, как описано в Примере 121, с использованием (SP)-10au вместо (RP)-4tt.
Пример 135. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-22cu].
Неочищенный (SP)-22cu получают, как описано в Примере 121, с использованием (SP)-10au вместо (RP)-4tt.
Пример 136. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-22gu].
Неочищенный (SP)-22gu получают, как описано в Примере 121, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 137. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-23uu].
Неочищенный (SP)-23uu получают, как описано в Примере 121, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 138. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-23ay].
Неочищенный (RP)-23au получают, как описано в Примере 121, с использованием (SP)-14au вместо (RP)-4tt.
Пример 139. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-23cu].
Неочищенный (RP)-23cu получают, как описано в Примере 121, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 140. Синтез 2-карбоалкоксиэтил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-23gu].
Неочищенный (RP)-23gu получают, как описано в Примере 121, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 141. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-23uu].
Неочищенный (SP)-23uu получают, как описано в Примере 121, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 142. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-23au].
Неочищенный (SP)-23au получают, как описано в Примере 121, с использованием (SP)-14au вместо (RP)-4tt.
Пример 143. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-23cu].
Неочищенный (SP)-23cu получают, как описано в Примере 121, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 144. Синтез 2-карбоалкоксиэтил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-23gu].
Неочищенный (SP)-23gu получают, как описано в Примере 121, с использованием (SP)-14gu вместо (RP)-4tt.
Схема Л: Синтез дисульфидных пронуклеотидов.
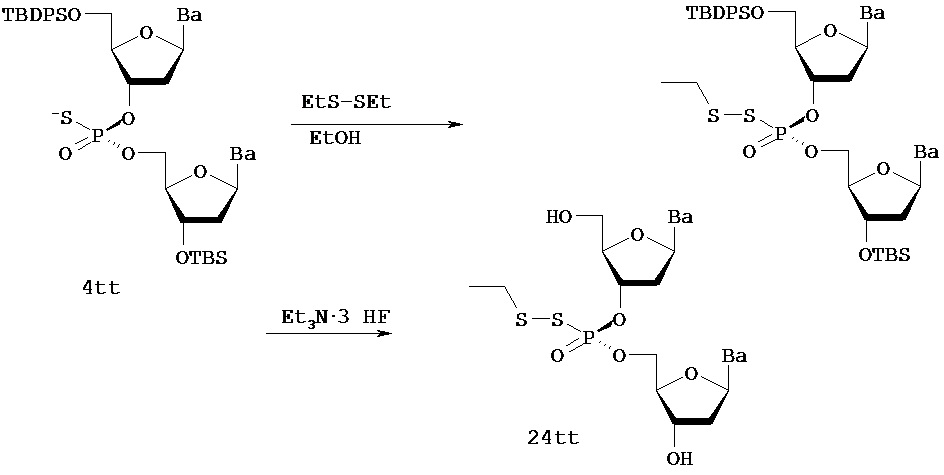
Пример 145. Синтез дисульфидного пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоат [(RP)-24tt], как описано на Схеме Л.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом этаноле (1 мл). Смесь обрабатывают диэтилдисульфидом (200 мкмоль) в сухом (100 мкмоль) этаноле. Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-24tt.
Пример 146. Синтез дисульфид пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-24at].
Неочищенный (RP)-24at получают, как описано в Примере 145, с использованием (RP)-4at вместо (RP)-4tt.
Пример 147. Синтез дисульфид пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-24ct].
Неочищенный (RP)-24ct получают, как описано в Примере 145, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 148. Синтез дисульфид пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-24gt].
Неочищенный (RP)-24gt получают, как описано в Примере 145, с использованием (RP)-4г вместо (RP)-4tt.
Пример 149. Синтез дисульфид пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-24tt].
Неочищенный (SP)-24tt получают, как описано в Примере 145, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 150. Синтез дисульфид пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-24at].
Неочищенный (SP)-24at получают, как описано в Примере 145, с использованием (SP)-4at вместо (RP)-4tt.
Пример 151. Синтез дисульфид пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-24ct].
Неочищенный (SP)-24ct получают, как описано в Примере 145, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 152. Синтез дисульфид пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-24gt].
Неочищенный (SP)-24gt получают, как описано в Примере 145, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 153. Синтез дисульфид пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-24uu].
Неочищенный (RP)-24uu получают, как описано в Примере 145, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 154. Синтез дисульфид пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-24au].
Неочищенный (RP)-24au получают, как описано в Примере 145, с использованием (RP)-10au вместо (RP)-4tt.
Пример 155. Синтез дисульфид пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [RP)-24cu].
Неочищенный (RP)-24cu получают, как описано в Примере 145, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 156. Синтез дисульфид пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-24gu].
Неочищенный (RP)-24gu получают, как описано в Примере 145, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 157. Синтез дисульфид пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-24uu].
Неочищенный (SP)-24uu получают, как описано в Примере 145, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 158. Синтез дисульфид пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-24au].
Неочищенный (SP)-24au получают, как описано в Примере 145, с использованием (SP)-10au вместо (RP)-4tt.
Пример 159. Синтез дисульфид пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-24cu].
Неочищенный (SP)-24cu получают, как описано в Примере 145, с использованием (SP)-10au вместо (RP)-4tt.
Пример 160. Синтез дисульфид пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-24gu].
Неочищенный (SP)-24gu получают, как описано в Примере 145, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 161. Синтез дисульфид пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-25uu].
Неочищенный (SP)-25uu получают, как описано в Примере 145, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 162. Синтез дисульфид пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-25au].
Неочищенный (RP)-25au получают, как описано в Примере 145, с использованием (SP)-14au вместо (RP)-4tt.
Пример 163. Синтез дисульфид пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-25cu].
Неочищенный (RP)-25cu получают, как описано в Примере 145, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 164. Синтез дисульфид пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-25gu].
Неочищенный (RP)-25gu получают, как описано в Примере 145, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 165. Синтез дисульфид пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-25uu].
Неочищенный (SP)-25uu получают, как описано в Примере 145, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 166. Синтез дисульфид пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-25au].
Неочищенный (SP)-25au получают, как описано в Примере 145, с использованием (SP)-14au вместо (RP)-4tt.
Пример 167. Синтез дисульфид пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-25cu].
Неочищенный (SP)-25cu получают, как описано в Примере 145, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 168. Синтез дисульфид пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-25gu].
Неочищенный (SP)-25gu получают, как описано в Примере 145, с использованием (SP)-14gu вместо (RP)-4tt.
Схема М: Синтез тиоацеталь пронуклеотидов.
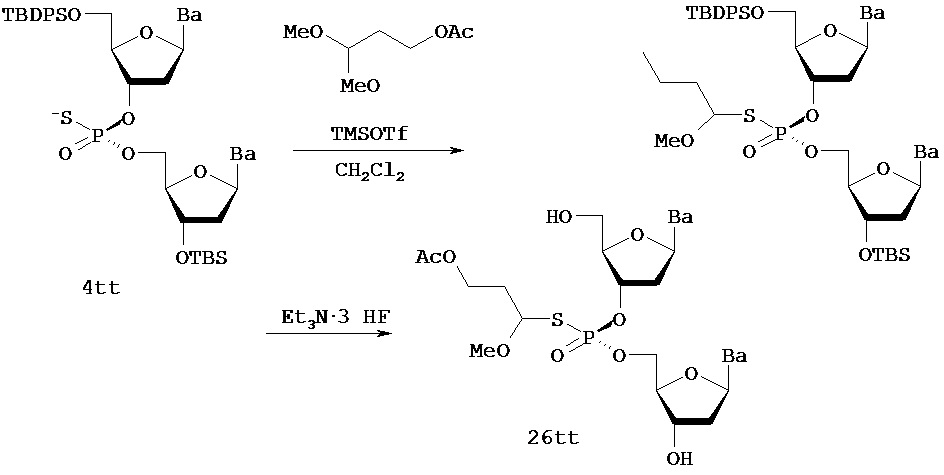
Пример 169. Синтез тиоацеталь пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-26tt], как описано на Схеме М.
3,3-Диметоксипропилацетат (100 мкмоль) добавляют к раствору триметилсилилтрифлата (100 мкмоль) в метиленхлориде (1 мл) при -78°C. После перемешивания при температуре -78°C в течение 30 мин, (SP)-1,8- добавляют диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль) в сухом метиленхлориде (1 мл). Смеси дают медленно нагреться до комнатной температуры. Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-26tt.
Пример 170. Синтез тиоацеталь пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-26at].
Неочищенный (RP)-26at получают, как описано в Примере 169, с использованием (RP)-4at вместо (RP)-4tt.
Пример 171. Синтез тиоацеталь пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-26ct].
Неочищенный (RP)-26ct получают, как описано в Примере 169, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 172. Синтез тиоацеталь пронуклеотида [(RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-26gt].
Неочищенный (RP)-26gt получают, как описано в Примере 169, с использованием (RP)-4г вместо (RP)-4tt.
Пример 173. Синтез тиоацеталь пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-26tt].
Неочищенный (SP)-26tt получают, как описано в Примере 169, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 174. Синтез тиоацеталь пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-26at].
Неочищенный (SP)-26at получают, как описано в Примере 169, с использованием (SP)-4at вместо (RP)-4tt.
Пример 175. Синтез тиоацеталь пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-26ct].
Неочищенный (SP)-26ct получают, как описано в Примере 169, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 176. Синтез тиоацеталь пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-илтимидин-5'-ил фосфортиоата [(SP)-26gt].
Неочищенный (SP)-26gt получают, как описано в Примере 169, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 177. Синтез тиоацеталь пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-26uu].
Неочищенный (RP)-26uu получают, как описано в Примере 169, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 178. Синтез тиоацеталь пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-26au].
Неочищенный (RP)-26au получают, как описано в Примере 169, с использованием (RP)-10au вместо (RP)-4tt.
Пример 179. Синтез тиоацеталь пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-26cu].
Неочищенный (RP)-26cu получают, как описано в Примере 169, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 180. Синтез тиоацеталь пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-26gu].
Неочищенный (RP)-26gu получают, как описано в Примере 169, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 181. Синтез тиоацеталь пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-26uu].
Неочищенный (SP)-26uu получают, как описано в Примере 169, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 182. Синтез тиоацеталь пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-26au].
Неочищенный (SP)-26au получают, как описано в Примере 169, с использованием (SP)-10au вместо (RP)-4tt.
Пример 183. Синтез тиоацеталь пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-26cu].
Неочищенный (SP)-26cu получают, как описано в Примере 169, с использованием (SP)-10au вместо (RP)-4tt.
Пример 184. Синтез тиоацеталь пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-26gu].
Неочищенный (SP)-26gu получают, как описано в Примере 169, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 185. Синтез тиоацеталь пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-27uu].
Неочищенный (SP)-27uu получают, как описано в Примере 169, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 186. Синтез тиоацеталь пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-27au].
Неочищенный (RP)-27au получают, как описано в Примере 169, с использованием (SP)-14au вместо (RP)-4tt.
Пример 187. Синтез тиоацеталь пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-27cu].
Неочищенный (RP)-27cu получают, как описано в Примере 169, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 188. Синтез тиоацеталь пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-27gu].
Неочищенный (RP)-27gu получают, как описано в Примере 169, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 189. Синтез тиоацеталь пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-27uu].
Неочищенный (SP)-27uu получают, как описано в Примере 169, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 190. Синтез тиоацеталь пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-27au].
Неочищенный (SP)-27au получают, как описано в Примере 169, с использованием (SP)-14au вместо (RP)-4tt.
Пример 191. Синтез тиоацеталь пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-27cu].
Неочищенный (SP)-27cu получают, как описано в Примере 169, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 192. Синтез тиоацеталь пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-27gu].
Неочищенный (SP)-27gu получают, как описано в Примере 169, с использованием (SP)-14gu вместо (RP)-4tt.
Схема Н: Синтез С3 енол эфир пронуклеотидов.
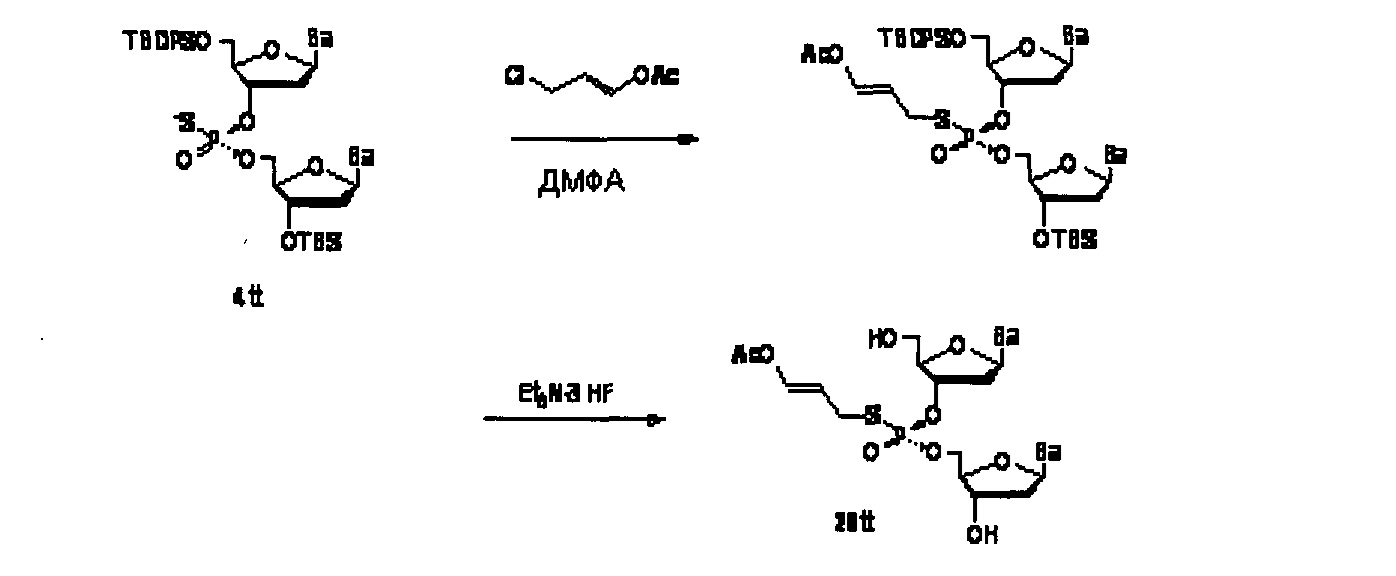
Пример 193. Синтез С3 енол эфир пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоат [(RP)-28tt], как описано на Схеме М.
К раствору (Е)-3-хлорпроп-1-енилацетата (100 мкмоль) в ДМФА (1 мл) добавляют (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферный раствор аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-28tt.
Пример 194. Синтез С3 енол эфир пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-28at].
Неочищенный (RP)-28at получают, как описано в Примере 193, с использованием (RP)-4at вместо (RP)-4tt.
Пример 195. Синтез С3 енол эфир пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-28ct].
Неочищенный (RP)-28ct получают, как описано в Примере 193, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 196. Синтез С3 енол эфир пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-28gt].
Неочищенный (RP)-28gt получают, как описано в Примере 193, с использованием (RP)-4г вместо (RP)-4tt.
Пример 197. Синтез С3 енол эфир пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-28tt].
Неочищенный (SP)-28tt получают, как описано в Примере 193, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 198. Синтез С3 енол эфир пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-28at].
Неочищенный (SP)-28at получают, как описано в Примере 193, с использованием (SP)-4at вместо (RP)-4tt.
Пример 199. Синтез С3 енол эфир пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-28ct].
Неочищенный (SP)-28ct получают, как описано в Примере 193, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 200. Синтез С3 енол эфир пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-28gt].
Неочищенный (SP)-28gt получают, как описано в Примере 193, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 201. Синтез С3 енол эфир пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-28uu].
Неочищенный (RP)-28uu получают, как описано в Примере 193, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 202. Синтез С3 енол эфир пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-28au].
Неочищенный (RP)-28au получают, как описано в Примере 193, с использованием (RP)-10au вместо (RP)-4tt.
Пример 203. Синтез С3 енол эфир пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-28cu].
Неочищенный (RP)-28cu получают, как описано в Примере 193, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 204. Синтез С3 енол эфир пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-28gu].
Неочищенный (RP)-28gu получают, как описано в Примере 193, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 205. Синтез С3 енол эфир пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-28uu].
Неочищенный (SP)-28uu получают, как описано в Примере 193, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 206. Синтез С3 енол эфир пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-28au].
Неочищенный (SP)-28au получают, как описано в Примере 193, с использованием (SP)-10au вместо (RP)-4tt.
Пример 207. Синтез С3 енол эфир пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-28cu].
Неочищенный (SP)-28cu получают, как описано в Примере 193, с использованием (SP)-10au вместо (RP)-4tt.
Пример 208. Синтез С3 енол эфир пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-28gu].
Неочищенный (SP)-28gu получают, как описано в Примере 193, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 209. Синтез С3 енол эфир пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-29uu].
Неочищенный (SP)-29uu получают, как описано в Примере 193, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 210. Синтез С3 енол эфир пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-29au].
Неочищенный (RP)-29auu получают, как описано в Примере 193, с использованием (SP)-14au вместо (RP)-4tt.
Пример 211. Синтез С3 енол эфир пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-29cu].
Неочищенный (RP)-29cu получают, как описано в Примере 193, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 212. Синтез С3 енол эфир пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-29gu].
Неочищенный (RP)-29gu получают, как описано в Примере 193, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 213. Синтез С3 енол эфир пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-29uu].
Неочищенный (SP)-29uu получают, как описано в Примере 193, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 214. Синтез С3 енол эфир пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-29au].
Неочищенный (SP)-29au получают, как описано в Примере 193, с использованием (SP)-14au вместо (RP)-4tt.
Пример 215. Синтез С3 енол эфир пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-29cu].
Неочищенный (SP)-29cu получают, как описано в Примере 193, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 216. Синтез С3 енол эфир пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-29gu].
Неочищенный (SP)-29gu получают, как описано в Примере 193, с использованием (SP)-14gu вместо (RP)-4tt.
Схема О: Синтез С4 енол эфир пронуклеотидов.
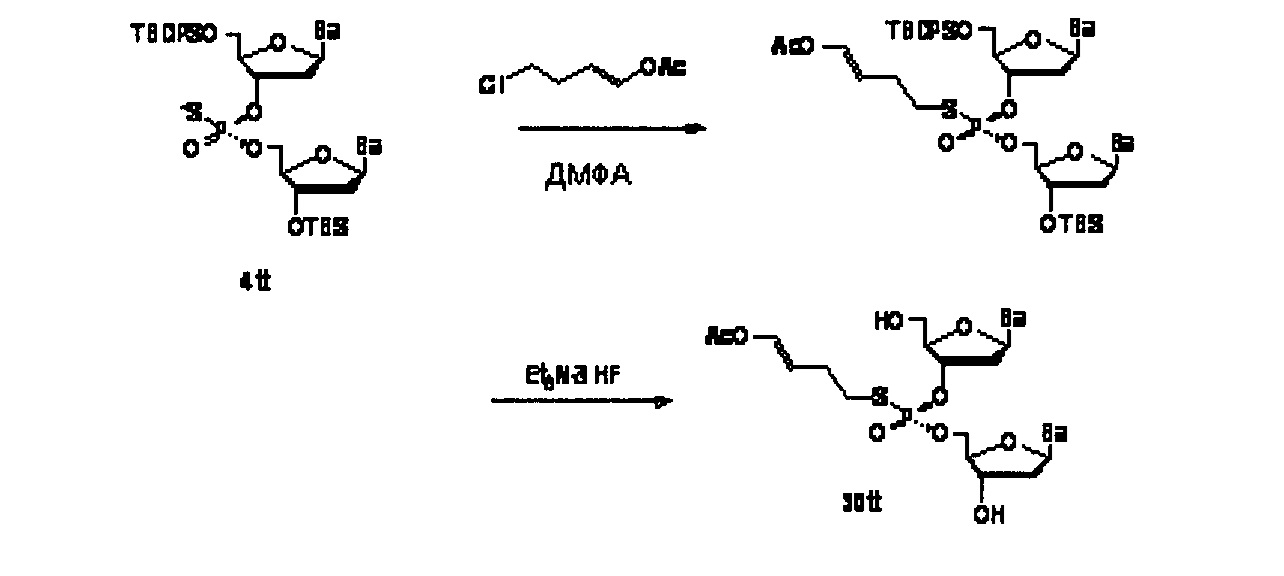
Пример 217. Синтез С4 енол эфир пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоат [(RP)-30tt], как описано на Схеме N.
К раствору (Е)-4-хлорбут-1-енилацетата (100 мкмоль) в ДМФА (1 мл) добавляют (SP)-1,8-диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-(9-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-30tt.
Пример 218. Синтез С4 енол эфир пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-30at].
Неочищенный (RP)-30at получают, как описано в Примере 217, с использованием (RP)-4at вместо (RP)-4tt.
Пример 219. Синтез С4 енол эфир пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-30ct].
Неочищенный (RP)-30ct получают, как описано в Примере 217, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 220. Синтез С4 енол эфир пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-30gt].
Неочищенный (RP)-30gt получают, как описано в Примере 217, с использованием (RP)-4 г вместо (RP)-4tt.
Пример 221. Синтез С4 енол эфир пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-30tt].
Неочищенный (SP)-30tt получают, как описано в Примере 217, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 222. Синтез С4 енол эфир пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-30at].
Неочищенный (SP)-30at получают, как описано в Примере 217, с использованием (SP)-4at вместо (RP)-4tt.
Пример 223. Синтез С4 енол эфир пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-30ct].
Неочищенный (SP)-30ct получают, как описано в Примере 217, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 224. Синтез С4 енол эфир пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-30gt].
Неочищенный (SP)-30gt получают, как описано в Примере 217, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 225. Синтез С4 енол эфир пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-30uu].
Неочищенный (RP)-30uu получают, как описано в Примере 217, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 226. Синтез С4 енол эфир пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-30au].
Неочищенный (RP)-30au получают, как описано в Примере 217, с использованием (RP)-10au вместо (RP)-4tt.
Пример 227. Синтез С4 енол эфир пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-30cu].
Неочищенный (RP)-30cu получают, как описано в Примере 217, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 228. Синтез С4 енол эфир пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-30gu].
Неочищенный (RP)-30gu получают, как описано в Примере 217, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 229. Синтез С4 енол эфир пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-30uu].
Неочищенный (SP)-30uu получают, как описано в Примере 217, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 230. Синтез С4 енол эфир пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-30au].
Неочищенный (SP)-30au получают, как описано в Примере 217, с использованием (SP)-10au вместо (RP)-4tt.
Пример 231. Синтез С4 енол эфир пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-30cu].
Неочищенный (SP)-30cu получают, как описано в Примере 217, с использованием (SP)-10au вместо (RP)-4tt.
Пример 232. Синтез С4 енол эфир пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-30gu].
Неочищенный (SP)-30gu получают, как описано в Примере 217, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 233. Синтез С4 енол эфир пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-31uu].
Неочищенный (SP)-31uu получают, как описано в Примере 217, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 234. Синтез С4 енол эфир пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-31au].
Неочищенный (RP)-31au получают, как описано в Примере 217, с использованием (SP)-14au вместо (RP)-4tt.
Пример 235. Синтез С4 енол эфир пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-31cu].
Неочищенный (RP)-31cu получают, как описано в Примере 217, с использованием (SP)-14 си вместо (RP)-4tt.
Пример 236. Синтез С4 енол эфир пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-31gu].
Неочищенный (RP)-31gu получают, как описано в Примере 217, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 237. Синтез С4 енол эфир пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-31uu].
Неочищенный (SP)-31uu получают, как описано в Примере 217, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 238. Синтез С4 енол эфир пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-31au].
Неочищенный (SP)-31au получают, как описано в Примере 217, с использованием (SP)-14au вместо (RP)-4tt.
Пример 239. Синтез С4 енол эфир пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-31cu].
Неочищенный (SP)-31cu получают, как описано в Примере 217, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 240. Синтез С4 енол эфир пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-31gu].
Неочищенный (SP)-31gu получают, как описано в Примере 217, с использованием (SP)-14gu вместо (RP)-4tt.
Схема П: Синтез защищенного 2'-5'-А3 Н-фосфоната
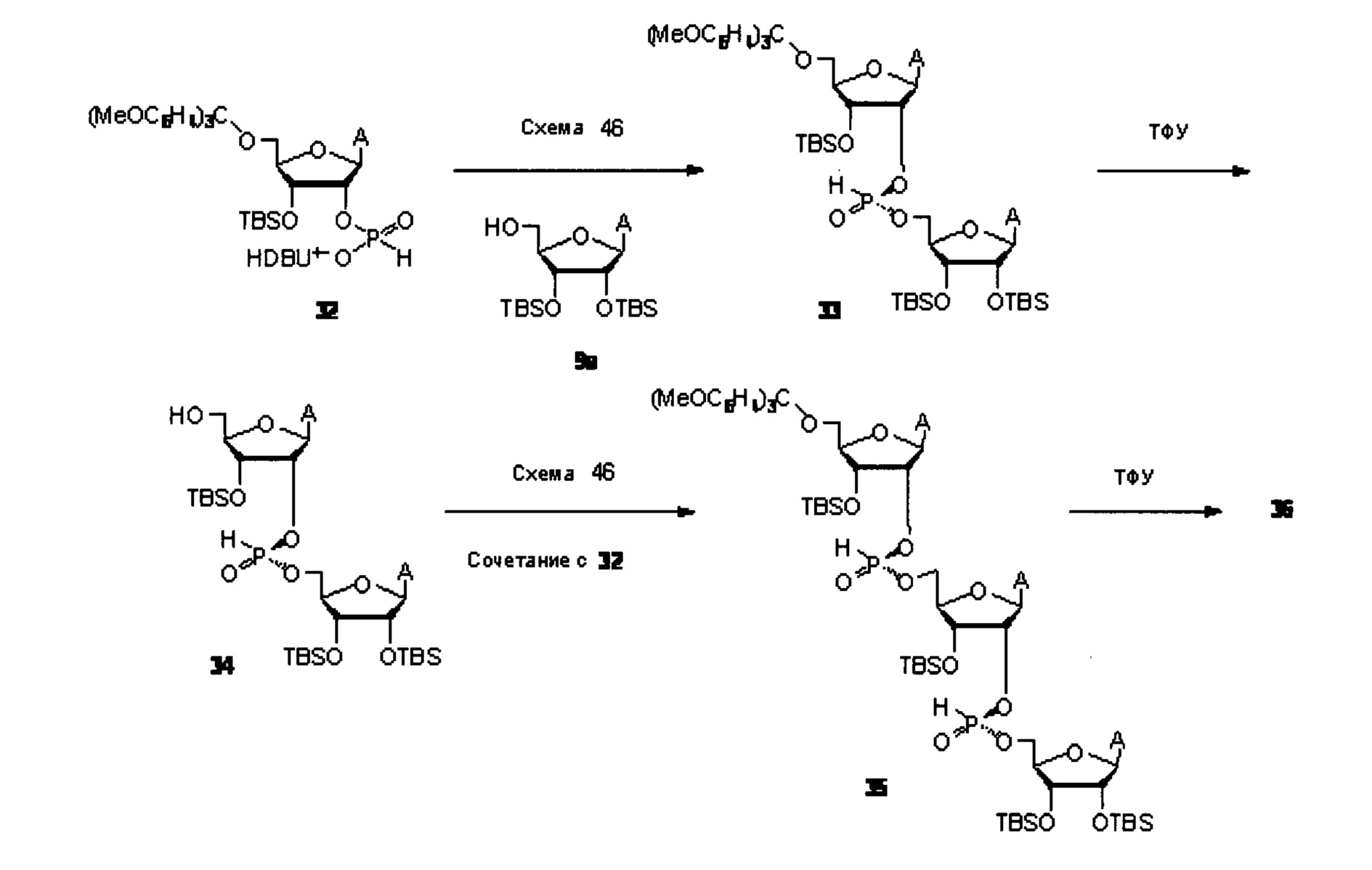
Пример 241. Синтез 5'-O-(метокситритил)-защищенного 2'-5'-А3 Н-фосфоната проиллюстрирован на Схеме П-а.
Осуществляют сочетание 5'-O-(метокситритил)-защищенного соединения 32 с 9а, как описано на Схеме 6, Пример 41. 5'-O-(Метокситритил)-защитную группу удаляют с полученного Н-фосфоната 33 обработкой 1% ТФУ в CH2Cl2 с получением 5'-ОН соединения 34. Сочетание 34 и 32, описанное на Схеме 6, Пример 41, дает Н-фосфонат тринуклеотид 35. Удаление защитной группы с группы 5'-ОН с помощью 1% ТФУ в CH2Cl2 дает Н-фосфонат тринуклеотид 36.
Схема П-б: Синтез 2'-5'-А3 S-ацетил-2-тиоэтил пронуклеотида
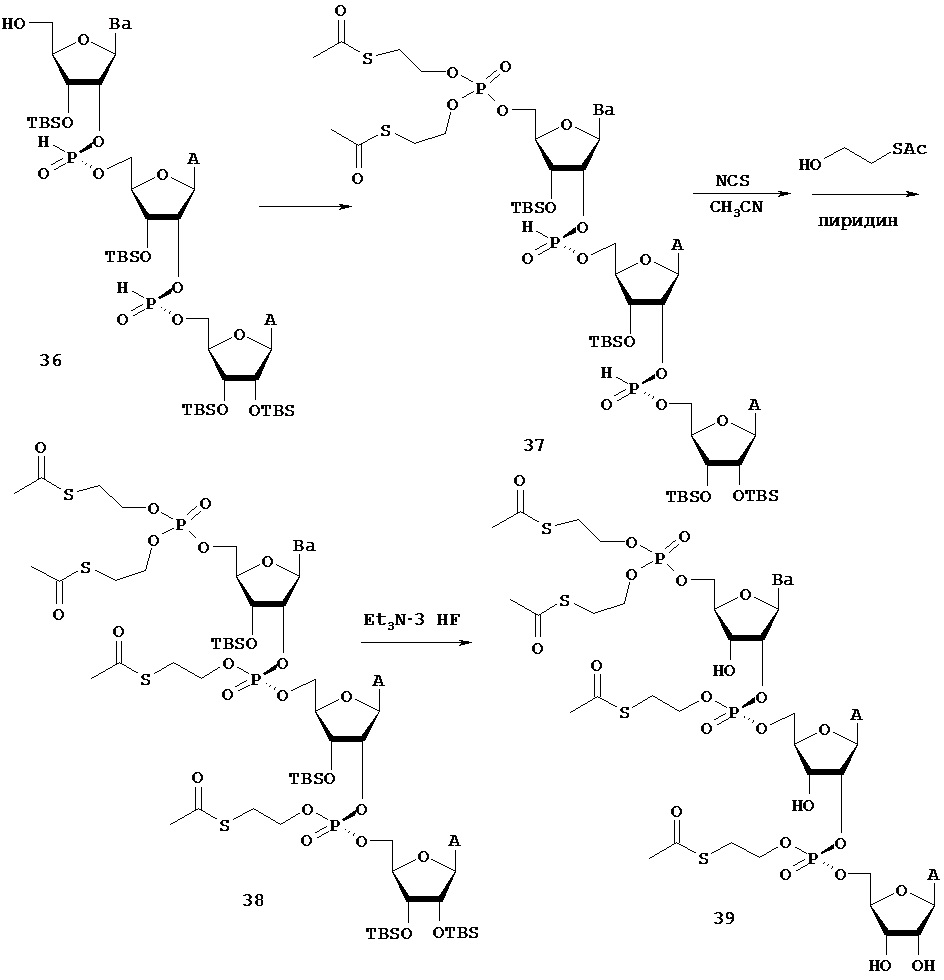
Пример 242. Синтез 2'-5'-А3 8-ацетил-2-тиоэтил пронуклеотида проиллюстрирован на Схеме П-б.
5'-ОН Н-фосфонат тринуклеотид (соединение 36) превращают в S-ацетил-2-тиоэтил пролекарство по способу Eldrup, как описано в патенте США 7,202,224. К 36 (1 ммоль) добавляют 1H-тетразол (1,1 ммоль), и смесь сушат в течение ночи над Р205. К полученной смеси добавляют сухой ацетонитрил (10 мл), с последующим добавлением бис(S-ацетил-2-тиоэтил)N,N-диизопропилфосфорамидита (1,1 ммоль), и полученную смесь перемешивают при комнатной температуре в течение 2 час. Растворитель удаляют, остаток охлаждают до -40°C, и добавляют раствор м-ХПБК (1,0 ммоль) в дихлорметане (10 мл). После перемешивания при комнатной температуре в течение 1 час, добавляют водный раствор NaHSO3, органическую фракцию отделяют, и продукт 37 выделяют хроматографически.
Соединение 37 превращают в конечный продукт 39 в соответствии с методикой Схемы 7, Пример 49. Соединение 37 (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают 3-ацетил-2-тиоэтанолом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением 39.
Схема Р: Синтез пролекарств триметиламмонийметил нуклеиновой кислоты.
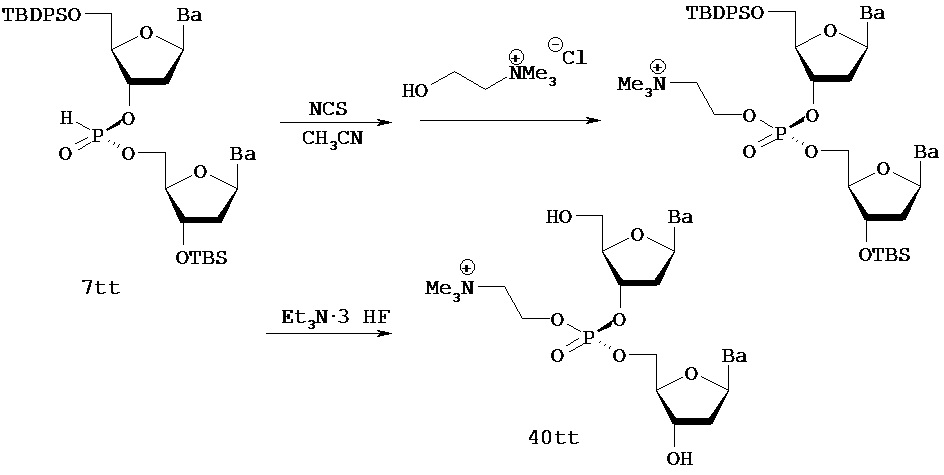
Пример 243. Синтез триметиламмонийметил пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-16tt], как описано на Схеме Р.
(RP)-5'-O-(трет-Бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфонат [(RP)-7tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл), добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают 1-(2-гидрокси)-этил-триметиламмония хлоридом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-40tt.
Пример 244. Синтез триметиламмонийметил пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(RP)-40at].
Неочищенный (RP)-40at получают, как описано в Примере 243, с использованием (RP)-7at вместо (RP)-7tt.
Пример 245. Синтез триметиламмонийметил пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(RP)-40ct].
Неочищенный (RP)-40ct получают, как описано в Примере 49, с использованием (RP)-7ct вместо (RP)-7tt.
Пример 246. Синтез триметиламмонийметил пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(RP)-40gt].
Неочищенный (RP)-40gt получают, как описано в Примере 49, с использованием (RP)-7 г вместо (RP)-7tt.
Пример 247. Синтез триметиламмонийметил пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(SP)-40tt].
Неочищенный (SP)-40tt получают, как описано в Примере 49, с использованием (SP)-7tt вместо (RP)-7tt.
Пример 248. Синтез триметиламмонийметил пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(SP)-40at].
Неочищенный (SP)-40at получают, как описано в Примере 49, с использованием (SP)-7at вместо (RP)-7tt.
Пример 249. Синтез триметиламмонийметил пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(SP)-40ct].
Неочищенный (SP)-40ct получают, как описано в Примере 49, с использованием (SP)-7ct вместо (RP)-7tt.
Пример 250. Синтез триметиламмонийметил пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(SP)-40gt].
Неочищенный (SP)-40gt получают, как описано в Примере 49, с использованием (SP)-7gt вместо (RP)-7tt.
Пример 251. Синтез триметиламмонийметил пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфоната [(RP)-40uu].
Неочищенный (RP)-40uu получают, как описано в Примере 49, с использованием (RP)-12uu вместо (RP)-7tt.
Пример 252. Синтез триметиламмонийметил пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(RP)-40au].
Неочищенный (RP)-40au получают, как описано в Примере 49, с использованием (RP)-12au вместо (RP)-7tt.
Пример 253. Синтез триметиламмонийметил пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(RP)-40cu].
Неочищенный (RP)-16 си получают, как описано в Примере 49, с использованием (RP)-12cu вместо (RP)-7tt.
Пример 254. Синтез триметиламмонийметил пронуклеотида (RP)-2-N-феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(RP)-40gu].
Неочищенный (RP)-40gu получают, как описано в Примере 49, с использованием (RP)-12gu вместо (RP)-7tt.
Пример 255. Синтез триметиламмонийметил пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфоната [(SP)-40uu].
Неочищенный (SP)-40uu получают, как описано в Примере 49, с использованием (SP)-12uu вместо (RP)-7tt.
Пример 256. Синтез триметиламмонийметил пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(SP)-40au].
Неочищенный (SP)-40au получают, как описано в Примере 49, с использованием (SP)-12au вместо (RP)-7tt.
Пример 257. Синтез триметиламмонийметил пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(SP)-40cu].
Неочищенный (SP)-40cu получают, как описано в Примере 49, с использованием (SP)-12au вместо (RP)-7tt.
Пример 258. Синтез триметиламмонийметил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(SP)-40gu].
Неочищенный (SP)-40gu получают, как описано в Примере 49, с использованием (SP)-12gu вместо (RP)-7tt.
Пример 259. Синтез триметиламмонийметил пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфоната [(RP)-41uu].
Неочищенный (RP)-41uu получают, как описано в Примере 49, с использованием (-RP)-15uu вместо (RP)-7tt.
Пример 260. Синтез триметиламмонийметил пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(RP)-41au].
Неочищенный (RP)-41au получают, как описано в Примере 49, с использованием (SP)-15au вместо (RP)-7tt.
Пример 261. Синтез триметиламмонийметил пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(RP)-41cu].
Неочищенный (RP)-41cu получают, как описано в Примере 49, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 262. Синтез триметиламмонийметил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил H-фосфоната [(RP)-41gu].
Неочищенный (RP)-41gu получают, как описано в Примере 49, с использованием (SP)-15gu вместо (RP)-7tt.
Пример 263. Синтез триметиламмонийметил пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфоната [(SP)-41uu].
Неочищенный (SP)-41uu получают, как описано в Примере 49, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 264. Синтез триметиламмонийметил пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(SP)-41au].
Неочищенный (SP)-41au получают, как описано в Примере 49, с использованием (SP)-15au вместо (RP)-7tt.
Пример 265. Синтез триметиламмонийметил пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(SP)-41cu].
Неочищенный (SP)-41cu получают, как описано в Примере 49, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 266. Синтез триметиламмонийметил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфоната [(SP)-41gu].
Неочищенный (SP)-41gu получают, как описано в Примере 49, с использованием (SP)-15gu вместо (RP)-7tt.
Схема С: Синтез пролекарств алкилгидроксамат нуклеиновой кислоты.
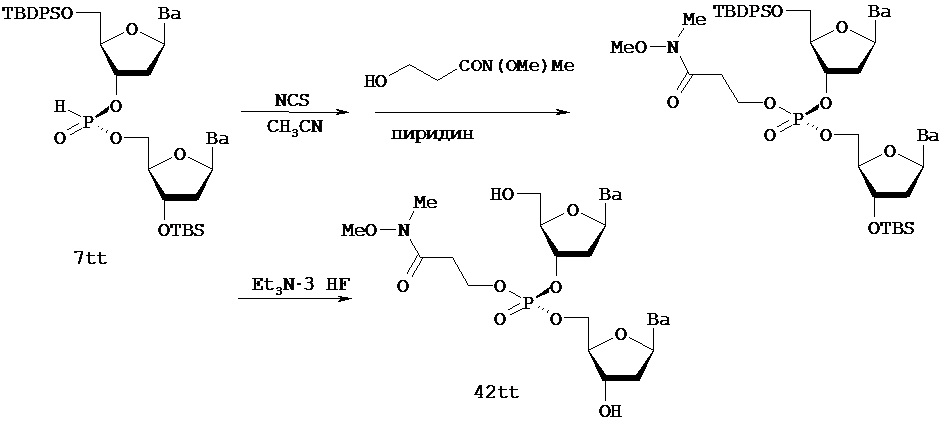
Пример 267. Синтез алкилгидроксамат пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-42tt], как описано на Схеме С.
(RP)-5'-O-(трет-Бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфонат [(RP)-7tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают N-метокси-N-метил-3-гидроксипропионамидом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-42tt.
Пример 268. Синтез алкилгидроксамат пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(RP)-42at].
Неочищенный (RP)-42at получают, как описано в Примере 267, с использованием (RP)-7at вместо (RP)-7tt.
Пример 269. Синтез алкилгидроксамат пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(RP)-42ct].
Неочищенный (RP)-42ct получают, как описано в Примере 267, с использованием (RP)-7ct вместо (RP)-7tt.
Пример 270. Синтез алкилгидроксамат пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(RP)-42gt].
Неочищенный (RP)-42gt получают, как описано в Примере 267, с использованием (RP)-7 г вместо (RP)-7tt.
Пример 271. Синтез алкилгидроксамат пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(SP)-42tt].
Неочищенный (SP)-42tt получают, как описано в Примере 267, с использованием (SP)-7tt вместо (RP)-7tt.
Пример 272. Синтез алкилгидроксамат пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(SP)-42at].
Неочищенный (SP)-42at получают, как описано в Примере 267, с использованием (SP)-7at вместо (RP)-7tt.
Пример 273. Синтез алкилгидроксамат пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(SP)-42ct].
Неочищенный (SP)-42ct получают, как описано в Примере 267, с использованием (SP)-7ct вместо (RP)-7tt.
Пример 274. Синтез алкилгидроксамат пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(SP)-42gt].
Неочищенный (SP)-42gt получают, как описано в Примере 267, с использованием (SP)-7gt вместо (RP)-7tt.
Пример 275. Синтез алкилгидроксамат пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфоната [(RP)-42uu].
Неочищенный (RP)-42uu получают, как описано в Примере 267, с использованием (RP)-12uu вместо (RP)-7tt.
Пример 276. Синтез алкилгидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(RP)-42au].
Неочищенный (RP)-42au получают, как описано в Примере 267, с использованием (RP)-12au вместо (RP)-7tt.
Пример 277. Синтез алкилгидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(RP)-42cu].
Неочищенный (RP)-42cu получают, как описано в Примере 267, с использованием (RP)-12cu вместо (RP)-7tt.
Пример 278. Синтез алкилгидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(RP)-42gu].
Неочищенный (RP)-42gu получают, как описано в Примере 267, с использованием (RP)-12gu вместо (RP)-7tt.
Пример 279. Синтез алкилгидроксамат пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфоната [(SP)-42uu].
Неочищенный (SP)-42uu получают, как описано в Примере 267, с использованием (SP)-12uu вместо (RP)-7tt.
Пример 280. Синтез алкилгидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(SP)-42au].
Неочищенный (SP)-42au получают, как описано в Примере 267, с использованием (SP)-12au вместо (RP)-7tt.
Пример 281. Синтез алкилгидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(SP)-42cu].
Неочищенный (SP)-42 си получают, как описано в Примере 267, с использованием (SP)-12au вместо (RP)-7tt.
Пример 282. Синтез алкилгидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(SP)-42gu].
Неочищенный (SP)-42gu получают, как описано в Примере 267, с использованием (SP)-12gu вместо (RP)-7tt.
Пример 283. Синтез алкилгидроксамат пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфоната [(RP)-43uu].
Неочищенный (RP)-43uu получают, как описано в Примере 267, с использованием (RP)-15uu вместо (RP)-7tt.
Пример 284. Синтез алкилгидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(RP)-43au].
Неочищенный (RP)-43au получают, как описано в Примере 267, с использованием (SP)-15au вместо (RP)-7tt.
Пример 285. Синтез алкилгидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(RP)-43cu].
Неочищенный (RP)-43 си получают, как описано в Примере 267, с использованием (SP)-15 си вместо (RP)-7tt.
Пример 286. Синтез алкилгидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил H-фосфоната [(RP)-43gu].
Неочищенный (RP)-43gu получают, как описано в Примере 267, с использованием (SP)-15gu вместо (RP)-7tt.
Пример 287. Синтез алкилгидроксамат пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфоната [(SP)-43uu].
Неочищенный (SP)-43uu получают, как описано в Примере 267, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 288. Синтез алкилгидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(SP)-43au].
Неочищенный (SP)-43au получают, как описано в Примере 267, с использованием (SP)-15au вместо (RP)-7tt.
Пример 289. Синтез алкилгидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(SP)-43cu].
Неочищенный (SP)-43cu получают, как описано в Примере 267, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 290. Синтез алкилгидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфоната [(SP)-43gu].
Неочищенный (SP)-43gu получают, как описано в Примере 267, с использованием (SP)-15gu вместо (RP)-7tt.
Схема Т: Синтез пролекарств ацилгидроксамат нуклеиновой кислоты.
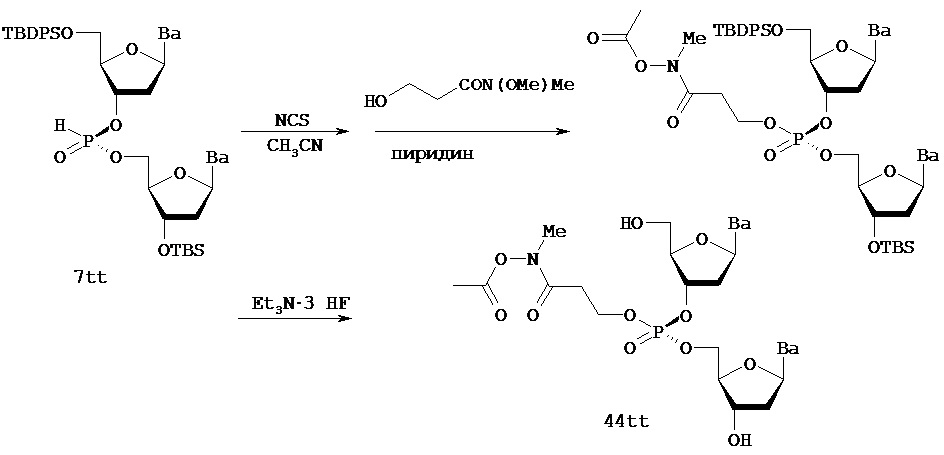
Пример 291. Синтез ацилгидроксамат пролекарство нуклеиновой кислоты of(RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-44tt], как описано на Схеме Т.
(RP)-5'-O-(трет-Бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил H-фосфонат [(RP)-7tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают N-ацилокси-N-метил-3-гидроксипропионамидом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-44tt.
Пример 292. Синтез ацилгидроксамат пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(RP)-44at].
Неочищенный (RP)-40at получают, как описано в Примере 291, с использованием (RP)-7at вместо (RP)-7tt.
Пример 293. Синтез ацилгидроксамат пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(RP)-44ct].
Неочищенный (RP)-44ct получают, как описано в Примере 291, с использованием (RP)-7ct вместо (RP)-7tt.
Пример 294. Синтез ацилгидроксамат пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(RP)-44gt].
Неочищенный (RP)-44gt получают, как описано в Примере 291, с использованием (RP)-7г вместо (RP)-7tt.
Пример 295. Синтез ацилгидроксамат пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(SP)-44tt].
Неочищенный (SP)-44tt получают, как описано в Примере 291, с использованием (SP)-7tt вместо (RP)-7tt.
Пример 296. Синтез ацилгидроксамат пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфоната [(SP)-44at].
Неочищенный (SP)-44at получают, как описано в Примере 291, с использованием (SP)-7at вместо (RP)-7tt.
Пример 297. Синтез ацилгидроксамат пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфоната [(SP)-44ct].
Неочищенный (SP)-44ct получают, как описано в Примере 291, с использованием (SP)-7ct вместо (RP)-7tt.
Пример 298. Синтез ацилгидроксамат пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфоната [(SP)-44gt].
Неочищенный (SP)-44gt получают, как описано в Примере 291, с использованием (SP)-7gt вместо (RP)-7tt.
Пример 299. Синтез ацилгидроксамат пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфоната [(RP)-44uu].
Неочищенный (RP)-44uu получают, как описано в Примере 291, с использованием (RP)-12uu вместо (RP)-7tt.
Пример 300. Синтез ацилгидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(RP)-44au].
Неочищенный (RP)-44au получают, как описано в Примере 291, с использованием (RP)-12au вместо (RP)-7tt.
Пример 301. Синтез ацилгидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(RP)-44cu].
Неочищенный (RP)-44cu получают, как описано в Примере 291, с использованием (RP)-12cu вместо (RP)-7tt.
Пример 302. Синтез ацилгидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(RP)-44gu].
Неочищенный (RP)-40gu получают, как описано в Примере 291, с использованием (RP)-12gu вместо (RP)-7tt.
Пример 303. Синтез ацилгидроксамат пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфоната [(SP)-44uu].
Неочищенный (SP)-44uu получают, как описано в Примере 291, с использованием (SP)-12uu вместо (RP)-7tt.
Пример 304. Синтез ацилгидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфоната [(SP)-44au].
Неочищенный (SP)-44au получают, как описано в Примере 291, с использованием (SP)-12au вместо (RP)-7tt.
Пример 305. Синтез ацилгидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфоната [(SP)-44cu].
Неочищенный (SP)-44cu получают, как описано в Примере 291, с использованием (SP)-12au вместо (RP)-7tt.
Пример 306. Синтез ацилгидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфоната [(SP)-44gu].
Неочищенный (SP)-44gu получают, как описано в Примере 291, с использованием (SP)-12gu вместо (RP)-7tt.
Пример 307. Синтез ацилгидроксамат пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфоната [(RP)-45uu].
Неочищенный (RP)-45uu получают, как описано в Примере 291, с использованием (RP)-15uu вместо (RP)-7tt.
Пример 308. Синтез ацилгидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(RP)-45au].
Неочищенный (RP)-45au получают, как описано в Примере 291, с использованием (SP)-15au вместо (RP)-7tt.
Пример 309. Синтез ацилгидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(RP)-45cu].
Неочищенный (RP)-45cu получают, как описано в Примере 291, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 310. Синтез ацилгидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил H-фосфоната [(RP)-45gu].
Неочищенный (RP)-45gu получают, как описано в Примере 291, с использованием (SP)-15gu вместо (RP)-7tt.
Пример 311. Синтез ацилгидроксамат пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфоната [(SP)-45uu].
Неочищенный (SP)-45uu получают, как описано в Примере 291, с использованием (SP)-15uu вместо (RP)-7tt.
Пример 312. Синтез ацилгидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфоната [(SP)-45au].
Неочищенный (SP)-45au получают, как описано в Примере 291, с использованием (SP)-15au вместо (RP)-7tt.
Пример 313. Синтез ацилгидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфоната [(SP)-45cu].
Неочищенный (SP)-45cu получают, как описано в Примере 291, с использованием (SP)-15cu вместо (RP)-7tt.
Пример 314. Синтез ацилгидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфоната [(SP)-45gu].
Неочищенный (SP)-45gu получают, как описано в Примере 291, с использованием (SP)-15gu вместо (RP)-7tt.
Схема У: Синтез тиотриалкиламмонийметил пронуклеотидов.
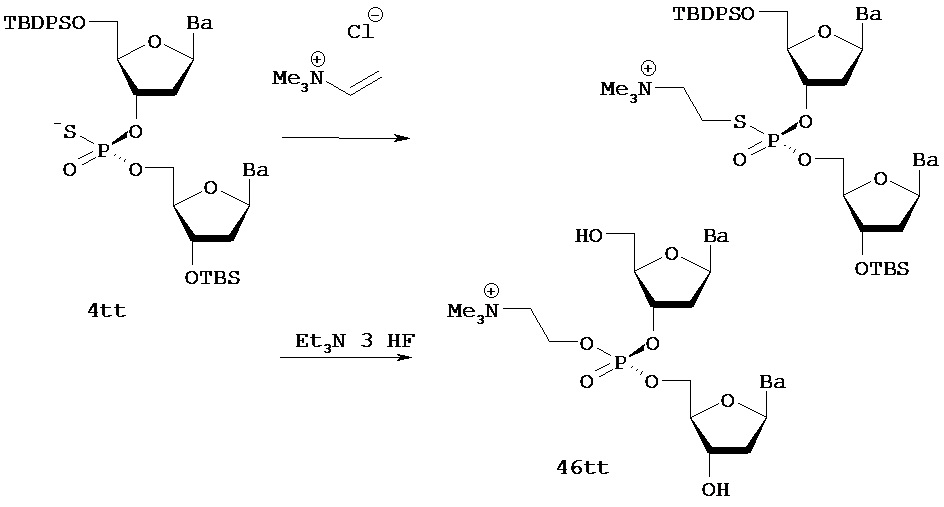
Пример 315. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-46tt], как описано на Схеме У.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом метиленхлориде (1 мл). Смесь обрабатывают винилтриметиламмония хлоридом (100 мкмоль) в сухом метиленхлориде (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-46tt.
Пример 316. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-46at].
Неочищенный (RP)-46at получают, как описано в Примере 315, с использованием (RP)-4at вместо (RP)-4tt.
Пример 317. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-46ct].
Неочищенный (RP)-46ct получают, как описано в Примере 315, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 318. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-46gt].
Неочищенный (RP)-46gt получают, как описано в Примере 315, с использованием (RP)-4г вместо (RP)-4tt.
Пример 319. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-46tt].
Неочищенный (SP)-46tt получают, как описано в Примере 315, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 320. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-46at].
Неочищенный (SP)-46at получают, как описано в Примере 315, с использованием (SP)-4at вместо (RP)-4tt.
Пример 321. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-46ct].
Неочищенный (SP)-46ct получают, как описано в Примере 315, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 322. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-46gt].
Неочищенный (SP)-46gt получают, как описано в Примере 315, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 323. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-46uu].
Неочищенный (RP)-46uu получают, как описано в Примере 315, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 324. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-46au].
Неочищенный (RP)-46au получают, как описано в Примере 315, с использованием (RP)-10au вместо (RP)-4tt.
Пример 325. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-46cu].
Неочищенный (RP)-46cu получают, как описано в Примере 315, с использованием (RP)-10 си вместо (RP)-4tt.
Пример 326. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-46gu].
Неочищенный (RP)-46gu получают, как описано в Примере 315, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 327. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-46uu].
Неочищенный (SP)-46uu получают, как описано в Примере 315, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 328. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-46au].
Неочищенный (SP)-46au получают, как описано в Примере 315, с использованием (SP)-10au вместо (RP)-4tt.
Пример 329. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-46cu].
Неочищенный (SP)-46 си получают, как описано в Примере 315, с использованием (SP)-10аи вместо (RP)-4tt.
Пример 330. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-46gu].
Неочищенный (SP)-46gu получают, как описано в Примере 315, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 331. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-47uu].
Неочищенный (SP)-47uu получают, как описано в Примере 315, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 332. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-47au].
Неочищенный (RP)-47au получают, как описано в Примере 315, с использованием (SP)-14au вместо (RP)-4tt.
Пример 333. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-47cu].
Неочищенный (RP)-47cu получают, как описано в Примере 315, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 334. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-47gu].
Неочищенный (RP)-47gu получают, как описано в Примере 315, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 335. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-47uu].
Неочищенный (SP)-47uu получают, как описано в Примере 315, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 336. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-47au].
Неочищенный (SP)-47au получают, как описано в Примере 315, с использованием (SP)-14au вместо (RP)-4tt.
Пример 337. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-47cu].
Неочищенный (SP)-47cu получают, как описано в Примере 315, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 338. Синтез тиотриалкиламмонийметил пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-47gu].
Неочищенный (SP)-47gu получают, как описано в Примере 315, с использованием (SP)-14gu вместо (RP)-4tt.
Схема Ф: Синтез тио-N-алкилгидроксамат пронуклеотидов.
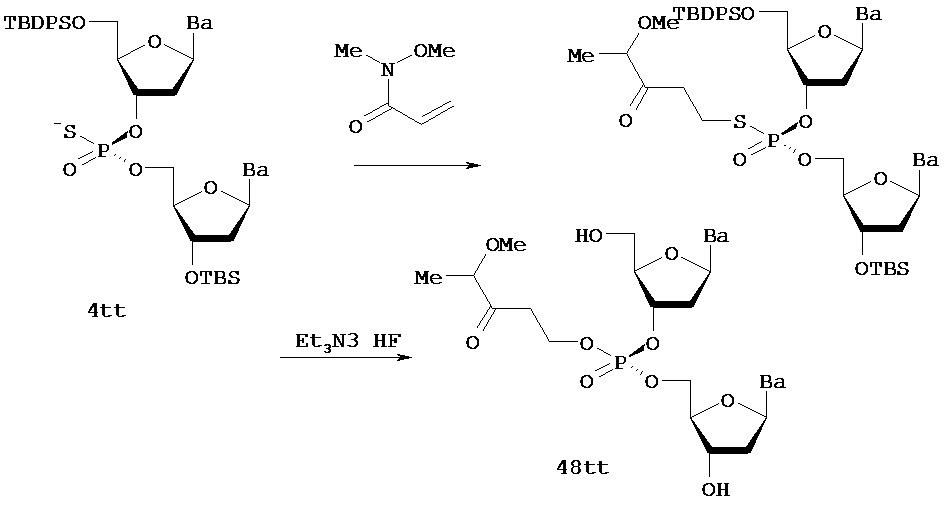
Пример 339. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоат [(RP)-48tt], как описано на Схеме Ф.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом метиленхлориде (1 мл). Смесь обрабатывают N,O-диметилакриламидом (100 мкмоль) в сухом метиленхлориде (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-48tt.
Пример 340. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-48at].
Неочищенный (RP)-48at получают, как описано в Примере 339, с использованием (RP)-4at вместо (RP)-4tt.
Пример 341. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-48ct].
Неочищенный (RP)-48ct получают, как описано в Примере 339, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 342. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-48gt].
Неочищенный (RP)-48gt получают, как описано в Примере 339, с использованием (RP)-4г вместо (RP)-4tt.
Пример 343. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-48tt].
Неочищенный (SP)-48tt получают, как описано в Примере 339, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 344. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-48at].
Неочищенный (SP)-48at получают, как описано в Примере 339, с использованием (SP)-4at вместо (RP)-4tt.
Пример 345. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-48ct].
Неочищенный (SP)-48ct получают, как описано в Примере 339, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 346. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-48gt].
Неочищенный (SP)-48gt получают, как описано в Примере 339, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 347. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-48uu].
Неочищенный (RP)-48uu получают, как описано в Примере 339, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 348. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-48au].
Неочищенный (RP)-48au получают, как описано в Примере 339, с использованием (RP)-10au вместо (RP)-4tt.
Пример 349. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-48cu].
Неочищенный (RP)-48cu получают, как описано в Примере 339, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 350. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [RP)-48gu].
Неочищенный (RP)-48gu получают, как описано в Примере 339, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 351. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(SP)-48uu].
Неочищенный (SP)-48uu получают, как описано в Примере 339, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 352. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-48au].
Неочищенный (SP)-48au получают, как описано в Примере 339, с использованием (SP)-10au вместо (RP)-4tt.
Пример 353. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-48cu].
Неочищенный (SP)-48cu получают, как описано в Примере 339, с использованием (SP)-10au вместо (RP)-4tt.
Пример 354. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-48gu].
Неочищенный (SP)-48gu получают, как описано в Примере 339, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 355. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-49uu].
Неочищенный (SP)-49uu получают, как описано в Примере 339, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 356. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-49au].
Неочищенный (RP)-49au получают, как описано в Примере 339, с использованием (SP)-14au вместо (RP)-4tt.
Пример 357. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-49cu].
Неочищенный (RP)-49cu получают, как описано в Примере 339, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 358. Синтез тио-N-алкилгидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-49gu].
Неочищенный (RP)-49gu получают, как описано в Примере 339, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 359. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-49uu].
Неочищенный (SP)-49uu получают, как описано в Примере 339, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 360. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-49au].
Неочищенный (SP)-49au получают, как описано в Примере 339, с использованием (SP)-14au вместо (RP)-4tt.
Пример 361. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-49cu].
Неочищенный (SP)-49cu получают, как описано в Примере 339, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 362. Синтез тио-N-алкилгидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-49gu].
Неочищенный (SP)-49gu получают, как описано в Примере 339, с использованием (SP)-14gu вместо (RP)-4tt.
Схема X: Синтез тио-N-ацетоксигидроксамат пронуклеотидов.
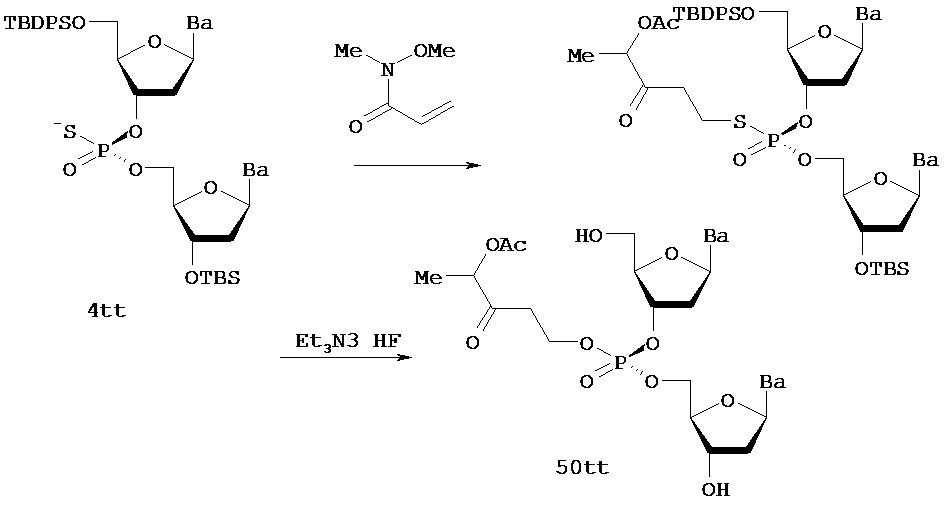
Пример 363. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоат [(RP)-50tt], как описано на Схеме X.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(трет-бутилдифенилсилил)тимидин-3'-ил 3'-O-(трет-бутилдиметилсилил)тимидин-5'-ил фосфортиоат [(SP)-4tt] (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом метиленхлориде (1 мл). Смесь обрабатывают N-метил-N-ацетокси-акриламидом (100 мкмоль) в сухом метиленхлориде (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-50tt.
Пример 364. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-50at].
Неочищенный (RP)-50at получают, как описано в Примере 363, с использованием (RP)-4at вместо (RP)-4tt.
Пример 365. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-50ct].
Неочищенный (RP)-50ct получают, как описано в Примере 363, с использованием (RP)-4ct вместо (RP)-4tt.
Пример 366. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-50gt].
Неочищенный (RP)-50gt получают, как описано в Примере 363, с использованием (RP)-4г вместо (RP)-4tt.
Пример 367. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-50tt].
Неочищенный (SP)-50tt получают, как описано в Примере 363, с использованием (SP)-4tt вместо (RP)-4tt.
Пример 368. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-6-N-бензоил-дезоксиаденозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-50at].
Неочищенный (SP)-50at получают, как описано в Примере 363, с использованием (SP)-4at вместо (RP)-4tt.
Пример 369. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-4-N-бензоил-дезоксицитидин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-50ct].
Неочищенный (SP)-50ct получают, как описано в Примере 363, с использованием (SP)-4ct вместо (RP)-4tt.
Пример 370. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-2-N-феноксиацетил-дезоксигуанозин-3'-ил тимидин-5'-ил фосфортиоата [(SP)-50gt].
Неочищенный (SP)-50gt получают, как описано в Примере 363, с использованием (SP)-4gt вместо (RP)-4tt.
Пример 371. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-уридин-3'-ил уридин-5'-ил фосфортиоата [(RP)-50uu].
Неочищенный (RP)-50uu получают, как описано в Примере 363, с использованием (RP)-10uu вместо (RP)-4tt.
Пример 372. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-50au].
Неочищенный (RP)-50au получают, как описано в Примере 363, с использованием (RP)-10au вместо (RP)-4tt.
Пример 373. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(RP)-50cu].
Неочищенный (RP)-50cu получают, как описано в Примере 363, с использованием (RP)-10cu вместо (RP)-4tt.
Пример 374. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(RP)-50gu].
Неочищенный (RP)-50gu получают, как описано в Примере 363, с использованием (RP)-10gu вместо (RP)-4tt.
Пример 375. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-уридин-3'-ил уридин-5'-ил фосфортиоат [(SP)-50uu].
Неочищенный (SP)-50uu получают, как описано в Примере 363, с использованием (SP)-10uu вместо (RP)-4tt.
Пример 376. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-50au].
Неочищенный (SP)-50au получают, как описано в Примере 363, с использованием (SP)-10au вместо (RP)-4tt.
Пример 377. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-3'-ил уридин-5'-ил фосфортиоата [(SP)-50cu].
Неочищенный (SP)-50cu получают, как описано в Примере 363, с использованием (SP)-10au вместо (RP)-4tt.
Пример 378. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-3'-ил уридин-5'-ил фосфортиоата [(SP)-50gu].
Неочищенный (SP)-50gu получают, как описано в Примере 363, с использованием (SP)-10gu вместо (RP)-4tt.
Пример 379. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(RP)-51uu].
Неочищенный (SP)-51uu получают, как описано в Примере 363, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 380. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-51au].
Неочищенный (RP)-51au получают, как описано в Примере 363, с использованием (SP)-14au вместо (RP)-4tt.
Пример 381. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(RP)-51cu].
Неочищенный (RP)-51cu получают, как описано в Примере 363, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 382. Синтез тио-N-ацетоксигидроксамат пронуклеотида (RP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(RP)-51gu].
Неочищенный (RP)-51gu получают, как описано в Примере 363, с использованием (SP)-14gu вместо (RP)-4tt.
Пример 383. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-уридин-2'-ил уридин-5'-ил фосфортиоата [(SP)-51uu].
Неочищенный (SP)-51uu получают, как описано в Примере 363, с использованием (SP)-14uu вместо (RP)-4tt.
Пример 384. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-6-N-бензоил-аденозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-51au].
Неочищенный (SP)-51au получают, как описано в Примере 363, с использованием (SP)-14au вместо (RP)-4tt.
Пример 385. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-4-N-бензоил-цитидин-2'-ил уридин-5'-ил фосфортиоата [(SP)-51cu].
Неочищенный (SP)-51cu получают, как описано в Примере 363, с использованием (SP)-14cu вместо (RP)-4tt.
Пример 386. Синтез тио-N-ацетоксигидроксамат пронуклеотида (SP)-2-N-Феноксиацетил-гуанозин-2'-ил уридин-5'-ил фосфортиоата [(SP)-51gu].
Неочищенный (SP)-51gu получают, как описано в Примере 363, с использованием (SP)-14gu вместо (RP)-4tt.
Схема Ц: Синтез тиотриалкиламмонийметил пронуклеотидов.
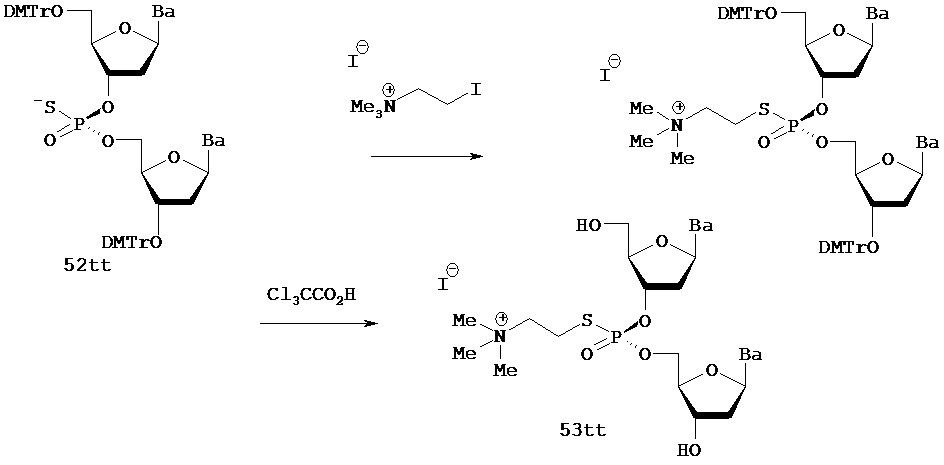
Пример 387. Синтез тиотриалкиламмонийметил пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-53tt], как описано на Схеме Ц.
(SP)-1,8-Диазабицикло[5,4,0]ундец-7-ения 5'-O-(диметокситритил)тимидин-3'-ил 3'-O-(диметокситритил)тимидин-5'-ил фосфортиоат [(SP)-52tt] получают по способу, применяемому для получения соединения 4tt в Примере 1 (Схема А). Соединение (SP)-52tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом диметилформамиде (1 мл). Смесь обрабатывают 2-йодэтилтриметиламмония йодидом (100 мкмоль) в сухом ДМФА (0,5 мл). Через 1 час смесь упаривают, затем растворяют в CH2Cl2 (1000 мкл), и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-53tt.
Схема Ч: Синтез тиотриалкиламмонийметил пронуклеотидов.
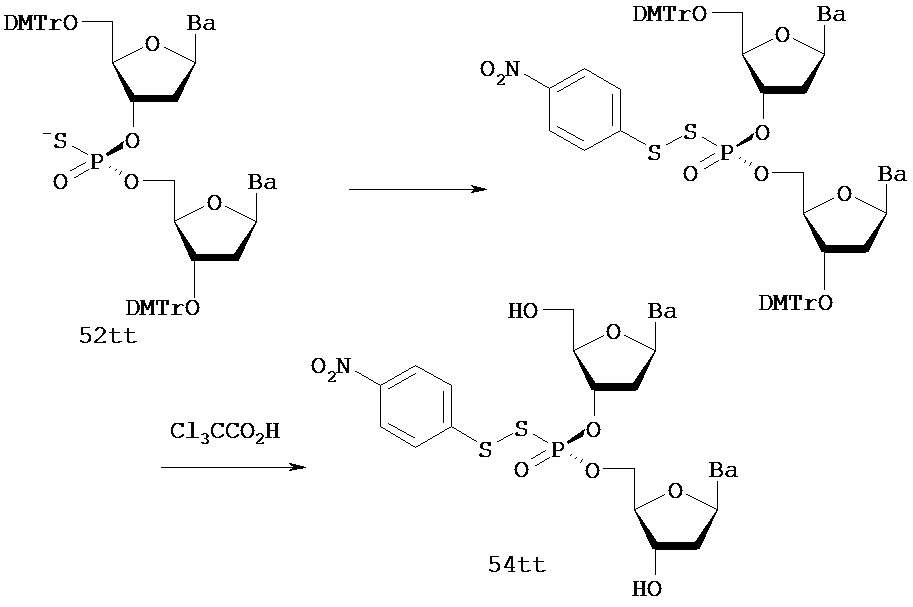
Пример 388. Синтез дисульфид пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-54tt], как описано на Схеме Ч.
Соединение (SP)-52tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом этаноле (1 мл). Смесь обрабатывают n-нитробензолсульфенилхлоридом (200 мкмоль) в сухом этаноле (100 мкмоль). Через 1 час смесь упаривают, затем растворяют в CH2Cl2 (1000 мкл), и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-54tt.
Схема Ш: Синтез 2-тиопивалилэтил пролекарств нуклеиновой кислоты.
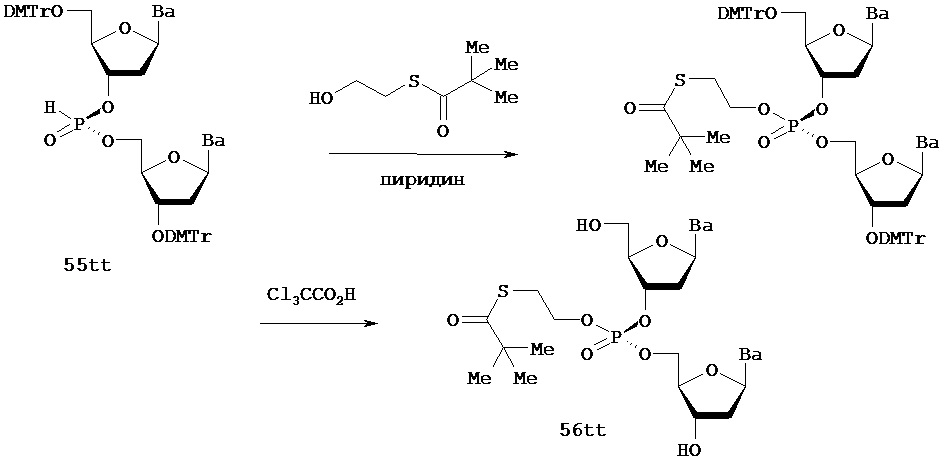
Пример 389. Синтез 2-тиопивалилэтил пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-56tt], как описано на Схеме Ш.
(RP)-5'-O-(Диметокситритил)тимидин-3'-ил 3'-O-(диметокситритил)тимидин-5'-ил H-фосфонат [(RP)-55tt] получают по способу, применяемому для получения соединения 7tt в Примере 8 (Схема В). Соединение (RP)-55tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают 2-гидроксиэтилтиопивалатом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, затем растворяют в CH2Cl2 (1000 мкл), и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-56tt.
Схема Щ: Синтез 2-карбоэтоксиэтил пролекарств нуклеиновой кислоты.
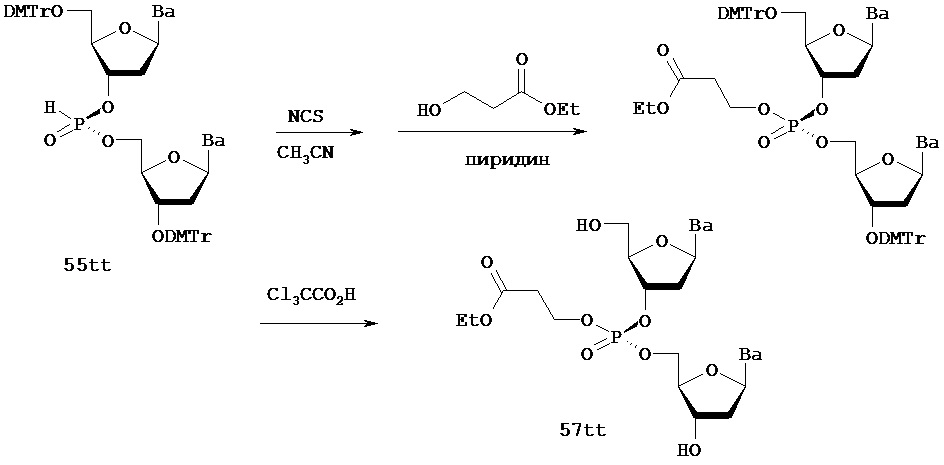
Пример 390. Синтез 2-карбоэтоксиэтил пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-57tt], как описано на Схеме Щ.
Соединение (RP)-55tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают этил-2-гидроксиэтилпропионатом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, затем растворяют в CH2Cl2 (1000 мкл), и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-57tt.
Схема Э: Синтез тио(циклогексил)ацилокси пронуклеотидов.
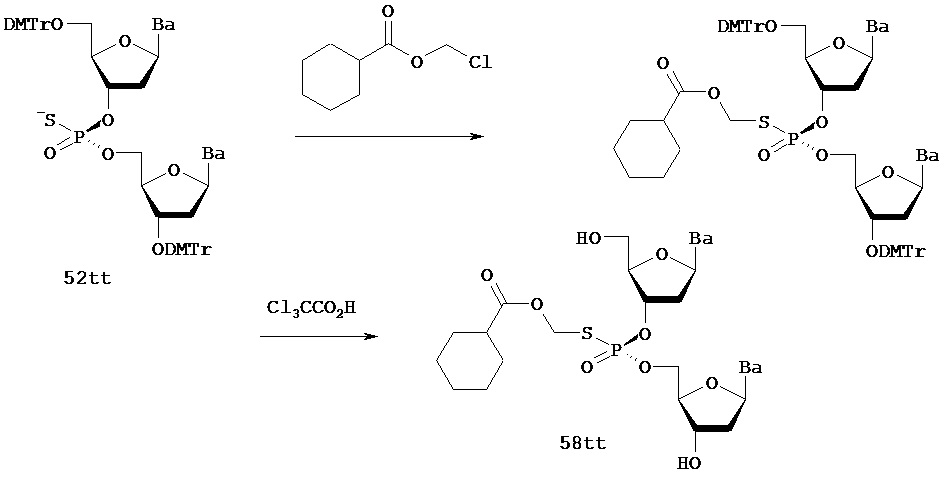
Пример 391. Синтез тио(циклогексил)ацилокси пронуклеотида (RP)-тимидин-3'-ил тимидин-5'-ил фосфортиоата [(RP)-58tt], как описано на Схеме Э.
Соединение (SP)-52tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом метиленхлориде (1 мл). Смесь обрабатывают хлорметилциклогексилацетоацетатом (100 мкмоль) в сухом метиленхлориде (100 мкмоль). Через 1 час смесь упаривают, затем растворяют в CH2Cl2 (1000 мкл) и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-58tt.
Схема АА: Синтез 2-карбоксиэтил пролекарств нуклеиновой кислоты.
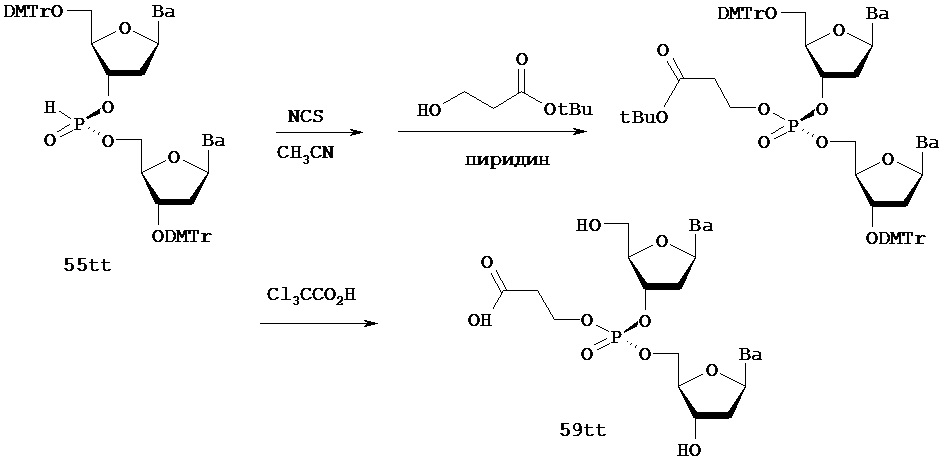
Пример 392. Синтез 2-карбоксиэтил пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-59tt], как описано на Схеме АА.
Соединение (RP)-55tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают трет-бутил-2-гидроксиэтилпропионатом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, затем растворяют в CH2Cl2 (1000 мкл) и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-59tt.
Схема ББ: Синтез 2-((2-гидроксиэтил)дисульфидом)этил пролекарств нуклеиновой кислоты.
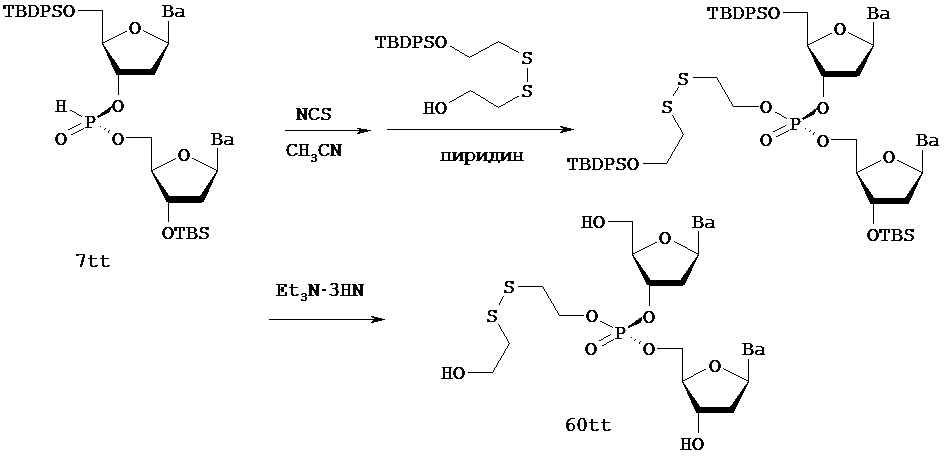
Пример 393. Синтез 2-((2-гидроксиэтил)дисульфидом)этил пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-60tt], как описано на Схеме ББ.
Соединение (RP)-7tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают 2-((2-(трет-бутилдифенилсилилокси)этил)дисульфанил)этанолом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, и затем растворяют в триэтиламина тригидрофториде (500 мкл). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствором аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением CRP)-60tt.
Схема ВВ: Синтез 2-(метансульфонотиоат)этил пролекарств нуклеиновой кислоты.
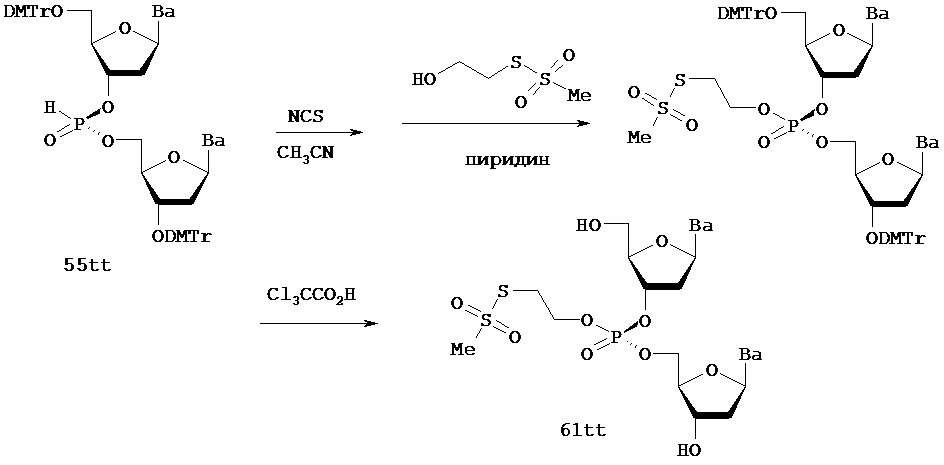
Пример 394. Синтез 2-(метансульфонотиоат)этил пролекарства нуклеиновой кислоты (RP)-тимидин-3'-ил тимидин-5'-ил фосфоната [(RP)-61tt], как описано на Схеме СС.
Соединение (RP)-55tt (100 мкмоль) сушат повторным соупариванием с сухим пиридином, и затем растворяют в сухом пиридине (1 мл). Добавляют N-хлорсукцинимид (0,1 ммоль), и смесь перемешивают в течение 2 час при 0°C. Смесь упаривают и растворяют в сухом пиридине (1 мл). Полученную выше смесь обрабатывают S-2-гидроксиэтилметансульфонотиоатом (100 мкмоль) в сухом пиридине (100 мкмоль). Через 1 час смесь упаривают, затем растворяют в СН2С12 (1000 мкл) и добавляют трихлоруксусную кислоту (50 мкмоль). Смесь перемешивают в течение 15 час при комнатной температуре. 0,1 М буферный раствор аммония ацетата (2,5 мл) затем добавляют к смеси, и смесь промывают Et2O (3×3 мл). Объединенные органические фракции снова экстрагируют 0,1 М буферным раствор аммония ацетата (3 мл). Объединенные водные фракции затем упаривают до сухого состояния при сниженном давлении, и остаток очищают обращенно-фазовой хроматографией на колонке [линейный градиент 0-10% ацетонитрила в 0,1 М буферном растворе аммония ацетата (рН 7,0)] с получением (RP)-61tt. Схема ДД: Синтез молекул пролекарств из димера Н-фосфоната тимидина
Хемоселективность и стереспецифичность опосредованного йодом окислительного сочетания с использованием отдельных диастереомеров динуклеозид Н-фосфоната и O-нуклеофилов для получения фосфотриэфиров известна в данной области (Nucleosides, Nucleotides & Nucleic Acids 2003 Vol.22, Nos. 5-8, 1467-1469). Продукты очищают хроматографией на силикагеле и характеризуют по данным 31Р и 1Н ЯМР спектроскопии. Продукты дополнительно очищают обращенно-фазовой ВЭЖХ в ходе кинетических стадий. Схема ГГ
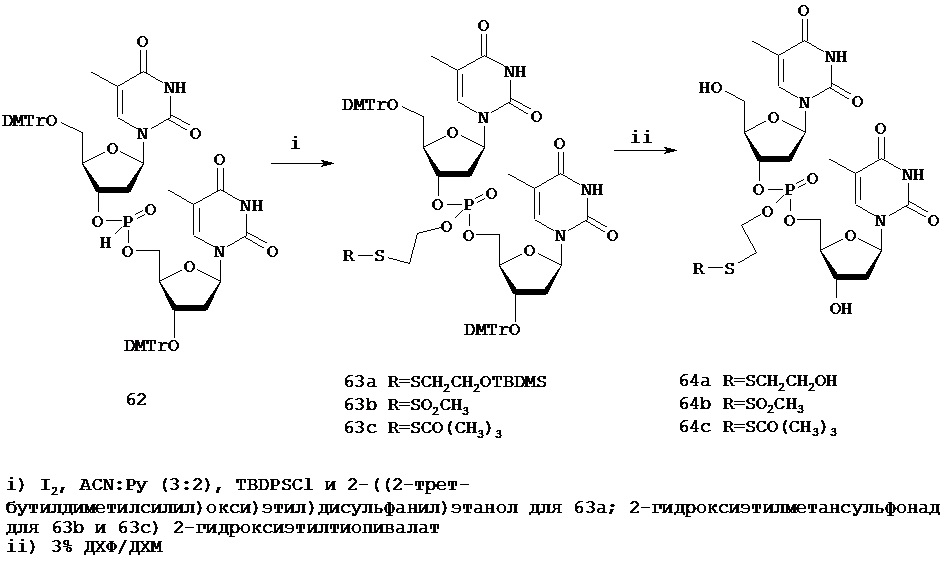
Пример 395. Общая методика синтеза 63а, 63b и 63с (Схема DD)
(RP,SP)-5'-O-(4,4'-Диметокситритил)тимидин-3'-ил 3'-O-(4,4'-диметокситритил)тимидин-5'-ил H-фосфонат (62) (113,5 мг, 100 мкмоль) сушат под высоким вакуумом в течение ночи и растворяют в смеси ACN (2 мл) и пиридина (2 мл). Добавляют трет-бутилдифенилсилилхлорид (52 мкл, 200 мкмоль) и 12 (76 мг, 300 мкмоль). Реакционную смесь охлаждают на льду, и соответствующий алкилирующий реагент (1 ммоль), в виде раствора в ACN (2 мл), добавляют по каплям к реакционной смеси. Смесь перемешивают в течение 10 мин в атмосфере аргона. Данные ТСХ неочищенной реакционной смеси показывают количественное превращение в продукт. Растворитель выпаривают, остаток растворяют в этилацетате и промывают 5% раствором Na2S2O3, солевым раствором и сушат над Na2SO4. Этилацетатную фракцию упаривают при сниженном давлении. Остаток очищают колоночной хроматографией на силикагеле с получением (RP,SP)-5'-O-(4,4'-диметокситритил)тимидин-3'-ил 3'-O-(4,4'-диметокситритил)тимидин-5'-ил фосфотриэфира 63а, 63b и 63с (выход 80-90%).
Общая методика синтеза 64а, 64b и 64с
3% ДХА/ДХМ медленно добавляют к защищенному ДМТр триэфиру, и реакционную смесь перемешивают при комнатной температуре в течение 30 мин. Реакцию гасят метанолом, растворитель выпаривают, и остаток очищают не колонке с кремния диоксидом. В случае соединения 63а, одновременно происходит удаление защитной группы ТБДМС. Соединения 64а, 64b и 64с получают с количественным выходом.
Соединение 63а: 1Н ЯМР (400 МГц, CDCl3) δ 7,58-7,18 (м, 20Н), 6,87-6,78 (м, 8Н), 6,49-6,27 (м, 2Н), 5,11-5,07 (м, 1Н), 4,2-4,05 (м, 3Н), 3,99-3,87 (м, 1Н), 3,85-3,73 (м, 13Н), 3,73-3,56 (м, 1Н), 3,54-3,26 (м, 2Н), 2,94-2,66 (м, 8Н), 1,97-1,78(м, 4Н), 1,76-1,54 (м, 1Н), 1,43-1,3 (м, 3Н), 0,94-0,78 (м, 9Н), 0,11-0,03 (м, 6Н). 31Р ЯМР (162 МГц, CDCl3) δ - 1,19, - 1,26 (два диастереомера).
Соединение 63b: 1Н ЯМР (400 МГц, CDCl3 + следовое количество Ру-D5) δ 9,72-9,45 (м, 2Н), 7,62-7,18 (м, 20Н), 6,90-6,81 (м, 8Н), 6,48-6,31 (м, 2Н), 5,18-5,10 (м, 1Н), 4,31-4,09 (м, 3Н), 4,03-3,91 (м, 1Н), 3,88-3,74 (м, 15Н), 3,74-3,62 (м, 1Н), 3,54-3,31 (м, 2Н), 2,89-2,76 (м, 4Н), 2,67-2,31 (м, 2Н), 1,98-1,89 (м, 1Н), 1,88, 1,85 (2s, 3Н, диастереомеры), 1,76-1,64 (м, 1Н), 1,39 (с, 3Н). 31P ЯМР (162 МГц, CDCl3) δ - 1,24, - 1,27 (два диастереомера).
Соединение 63c: 1Н ЯМР (400 МГц, CDCl3 + следовое количество Ру-D5) δ 7,6-7,16 (м, 20Н), 6,9-6,77 (м, 8Н), 6,49-6,27 (м, 2Н), 5,18-5,06 (м, 1Н), 4,32-4,04 (м, 2Н), 4,0-3,85 (м, 3Н), 3,82-3,71 (м, 12Н), 3,71-3,57 (м, 1Н), 3,55-3,27 (м, 2Н), 3,07-2,88 (м, 2Н), 2,62-2,24 (м, 2Н), 1,97-1,89 (м, 1Н), 1,89-1,81 (м, 3Н), 1,78-1,59 (м, 3Н), 1,45-1,32 (м, 3Н), 1,22-1,14 (м, 9Н). 31P ЯМР (162 МГц, CDCl3) δ - 1,23, - 1,27 (два диастереомера).
Соединение 64а: 1Н ЯМР (400 МГц, D2O) δ 7,52 (с, 1Н), 7,42 (с, 1Н), 6,28-6,07 (м, 2Н), 5,07-4,87 (м, 1Н), 4,54-4,38 (м, 1Н), 4,37-4,19 (м, 3Н), 4,19-3,95 (м, 2Н), 3,80-3,50 (м, 4Н), 2,99-2,62 (2m, 4Н), 2,60-2,17 (м, 4Н), 1,85-1,60 (м, 6Н). 3lP ЯМР (162 МГц, CD3OD) δ - 1,37, - 1,41 (два диастереомера). Вычисленная масса = 682,66. Зарегистрированная в режиме ИЭР-ve масса = 681,22.
Соединение 64b: 1Н ЯМР (400 МГц, CD3OD) δ 7,74, 7,49 (2s, 2H), 6,28-6,19 (м, 2H), 5,10-5,04 (м, 1Н), 4,41-4,23 (м, 4Н), 4,19-4,15 (м, 1Н), 4,04-3,98 (м, 1Н), 3,78-3,69 (м, 4Н), 3,00-2,77 (м, 4Н), 2,55-2,21 (м, 4Н), 1,86, 1,83 (2s, 6H). 31P ЯМР (162 МГц, CD3OD) δ - 1,37, - 1,41 (два диастереомера). Вычисленная масса = 684,63. Зарегистрированная в режиме ИЭР-ve масса = 683,14.
Соединение 64с: 1Н ЯМР (400 МГц, CD3OD) δ 7,799 (с, 1Н), 7,54 (с, 1Н), 6,32-6,24 (м, 2H), 5,17-5,07 (м, 1Н), 4,48-4,26 (м, 3Н), 4,26-4,12 (м, 3Н), 4,08-3,99 (м, 1Н), 3,21-3,15 (м, 2H), 2,61-2,48 (м, 1Н), 2,46-2,16 (м, 3Н), 1,9 (с, 3Н), 1,87 (с, 3Н), 1,27-1,19 (д, 9Н). 3lP ЯМР (162 МГц, CD3OD) δ - 1,53, - 1,60 (два диастереомера). Вычисленная масса = 690,66. Зарегистрированная в режиме ИЭР-ve масса = 689,53.
Очистка 64а, 64b и 64с методом ВЭЖХ
Очистку обращенно-фазовой ВЭЖХ осуществляют с использованием Waters 2525 BGM, оборудованного УФ-детектором 2487, колонкой Phenomenex Luna 5 мкм С 18 (2) 100Å, 250×10 мм, MassLynx v4,1. Используют градиент от воды до ацетонитрила со скоростью потока 5 мл/мин.
Градиент для соединений 64а и 64b: 10-50% Б в течение 30 мин.
Градиент для соединения 64с: 20-60% Б в течение 30 мин.
Пики продукта контролируют на длине волны 254 и 280 нм.
Условия аналитической ВЭЖХ
Количественный анализ осуществляют обращенно-фазовой ВЭЖХ с использованием автоматизированного прибора для ВЭЖХ Alliance Waters e2695 instrument с программным обеспечением Empower. Прибор оборудован колонкой XBridge С18 3,5 мкм, 4,6×150 мм, Waters №186003034A, и УФ-детектором (254 нм и 280 нм). Используется элюация с градиентом системы растворителей (табл.1), что позволяет разделить пролекарство, промежуточное соединение и высвобожденное лекарственное средство в пределах одной и той же хроматограммы; подвижная фаза А состоит из 20 мМ аммония ацетата в воде; подвижная фаза Б представляет собой ацетонитрил.
|
Пример 396. Высвобождение пролекарства при содействии глутатиона
Смешивают 20 мкл соединения 64 в воде (2 O.D.), 100 мкл 10Х ФБР и 630 мкл H2O. Смесь выдерживают на теплом планшете при температуре 37°C. К полученной выше смеси прибавляют 250 мкл свежеприготовленного 20 мМ восстановленного L-глутатиона (GSH) с получением концентрации GSH в реакционной смеси 5 мМ, что соответствует концентрации в цитозоле. Аликвоты по 100 мкл отбирают через 10 мин, 20 мин, 30 мин, 40 мин, 50 мин, 60 мин, 1,5 час, 2 час и 2,5 час. Каждую аликвоту немедленно гасят 400 мкл 100 мМ нитратного буферного раствора (рН 4) и анализируют обращенно-фазовой ВЭЖХ и РХ/МС.
Схема ДД: Механизм расщепления под действием глутатиона
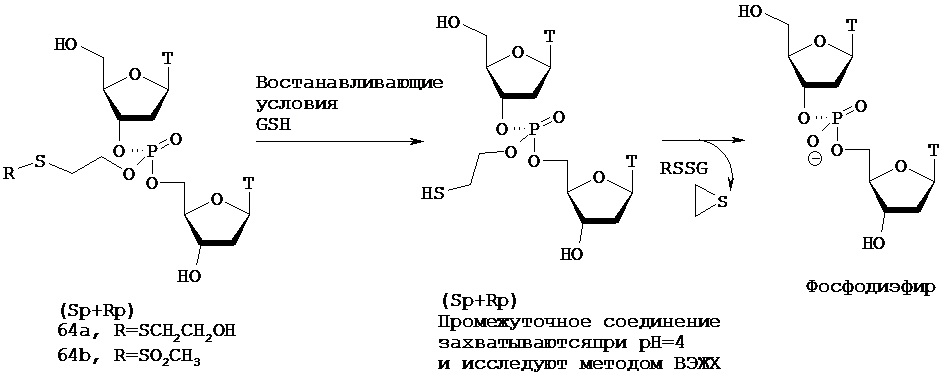
Анализ методом ЖХМС реакционной смеси соединения 64b + GSH в точке времени 20 мин
Waters Acquity UPLC и натрия лаурилсульфат используют для описания продуктов, которые образуются в ходе высвобождения пролекарства. Используют колонку XBridge c18 3,5 мкм, 4,6×150 мм, Waters №186003034 с системой растворителей А: 5 мМ аммония формиата в воде и Б: ацетонитрил, с линейным градиентом, как показано в табл.2.
|
На Фиг.1 представлен характерный ВЭЖХ профиль соединения 64а + GSH.
На Фиг.2 представлен характерный профиль ВЭЖХ соединения 64а, глутатионового аддукта и конечного продукта после высвобождения про-фрагмента.
На Фиг.3, соединения 64а и 64b демонстрируют кинетику псевдопервого порядка, поскольку концентрация глутатиона в существенной мере избыточна по сравнению с субстратом, и, таким образом, остается эффективно постоянной в ходе реакции. Кривые истощения исходного материала и образующегося продукта не являются зеркальными отображениями друг друга вследствие накопления промежуточного соединения, которое характеризуется как глутатионовый аддукт динуклеозидного триэфира (см. Фиг.2 и Фиг.4). Пример 397. Расщепление соединения 64 с при содействии карбоксиэстеразы
Схема ЕЕ
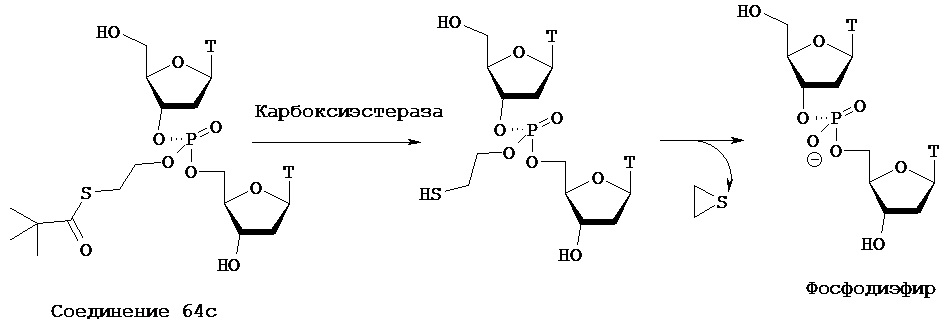
Эстеразу из свиной печени (ЭСП, Sigma Aldrich, продукт №Е2884) суспендируют в 3,2 М растворе аммония сульфата (рН=8,0), концентрация 36 мг белка/мл и 154 Ед/мг белка. В соответствии со спецификацией продукту, 1 Ед будет гидролизовать 1 мкМ этилбутирата до масляной кислоты и этанола за 1 мин при рН=8,0 и температуре 25°C. Соединение 64 с (0,1 O.D, 5,5 нмоль) в 10 мкл IX ФБР инкубируют при температуре 37°C в течение 10 мин. Серийные разведения ЭСП готовят в 10 флаконах с концентрацией (в Ед) 1, 10-1, 10-2, 10-3, 10-4, 10-5, 10-6, 10-7, 10-8, 10-9, в 10 мкл IX ФБР каждый. Раствор белка инкубируют при температуре 37°C в течение 10 мин, и затем прибавляют в каждый из 10 флаконов, содержащих соединение 64 с.Смеси хранят при температуре 37°C в течение 30 мин и анализируют методом аналитической ВЭЖХ и ЖХМС. Соединение 64 с полностью превращается в фосфодиэфир во флаконах с концентрацией белка от 1, 10-1 и 10-2. Побочных реакций не наблюдалось. Не наблюдалось реакции во флаконах с концентрацией белка от 10-6 до 10-9. Некоторое количество продукта наблюдалось во флаконах, содержащих концентрацию белка 10-3 и 10-4. Это наводит на мысль о том, что данные концентрации являются подходящими для изучения кинетики высвобождения пролекарства с использованием ЭСП. Зависимая от времени кинетика будет изучена с использованием концентраций в пределах интервала от 10-3 до 10-4/~6 нмоль соединения 64с.
Соединение 64с (5 O.D., 2,9 мкмоль) растворяют в 900 мкл 1X ФБР и инкубируют при температуре 37°C в течение 10 мин. Эстеразу свиной печени (1 Ед) в 100 мкл 1х ФБР прибавляют к полученной выше смеси и хранят при температуре 37°C. Аликвоты по 100 мкл отбирают через 0 мин, 15 мин и 45 мин, гасят с помощью 100 мкл ацетонитрила, и образцы охлаждают на ледяной бане. Образцы анализируют с помощью UPLC SQD на колонке XBridge С-18 3,5 мкм, 4,6×150 мм, используя систему растворителей А: 5 мМ аммония формиата в воде и Б: ацетонитрил, с линейным градиентом, как показано в табл.3. В точке 0 мин наблюдалось только соединение 64с, в точке 15 мин образуется приблизительно 50% продукта, и реакция завершается через 45 мин. Таким образом, ТрТ диэфир 64с высвобождается путем обработки карбоксиэстеразой без обнаружимого накопления любых полупродуктов.
Таблица 3
|
Пример 398. Лечение рака поджелудочной железы
Предусматривается способ лечения субъекта, страдающего раком поджелудочной железы, включающий введение субъекту терапевтически эффективного количества композиции, содержащей 2'-5'-A3 S-ацетил-2-тиоэтилпронуклеотид из Примера 242. Ожидается, что лечение будет давать усиленное торможение роста опухоли по сравнению с монотерапией гемцитабином или введения комбинации гемцитабина и эрлотиниба.
Пример 399. Анализ проникновения в клетки
Меченые Р32 лекарственные средства в форме нуклеиновых кислот
Готовят меченое пролекарство нуклеиновой кислоты и исходное лекарственное средство с использованием радионуклида [32P]dNTP (Fisher Scientific, Pittsburgh, PA) для синтеза молекул нуклеиновой кислоты, содержащих хиральные фосфорсодержащие фрагменты и соответствующие исходные лекарственные средства, как описано в данном описании.
Культура клеток и анализ проникновения
Выбирают культуру клеток HeLa (прикрепленные клетки рака поджелудочной железы), выращенную в модифицированной Дульбекко среде Игла-10% сыворотки телячьего эмбриона, или клетки ВхРС-3 (прикрепленные клетки аденокарциномы поджелудочной железы человека), выращенные в 90% RPMI 1640-10% сыворотки телячьего эмбриона. Для нанесения культур клеток на планшет, клетки трипсинизируют с помощью 0,05% трипсина-ЭДТА. Анализ жизнеспособности и подсчет клеток выполняют с помощью стандартного окрашивания трипановым голубым в фосфатном буферном растворе (ФБР). Клетки разбавляют и засевают с плотностью 1×105 клеток/ячейку в 6-луночном формате. Инкубируют при температуре 37°C в атмосфере, содержащей 5% CO2 в течение 16 час или до тех пор, пока клетки прикрепятся и достигнут слияния по меньшей мере 80%.
Добавляют смесь меченого пролекарства в экспериментальные лунки пролекарства до конечной концентрации в предварительно определенном интервале (например, 1 мкМ, 5 мкМ и 10 мкМ). Добавляют меченую смесь исходного лекарственного средства в лунки исходного лекарственного средства до конечной концентрации в предварительно определенном интервале (например, 1 мкМ, 5 мкМ и 10 мкМ). Резервируют необработанные лунки для отрицательного контроля. Инкубируют клетки с исследуемыми веществами в течение предварительно определенных интервалов времени (например, 15 мин, 1 час, 4 час и 8 час).
Обнаружение Р32 и определение проникновения пролекарства
Для сбора клеток, лунки промывают 3 раза бессывороточной средой и помещают неденатурирующий буфер для лизиса ТРИС-НС1, содержащий 1% Тритона Х100 (Cell Signaling Technology, Inc., Boston, MA), после чего обрабатывают ультразвуком в течение короткого времени. Собирают цитозольные и ядерные фракции с помощью стандартных методик сбора. Измерение проникновения лекарственного средства выполняют с использованием стандартных методов обнаружения излучения. Для обнаружения с помощью сцинтилляционного счетчика, добавляют 50 мкл образца к 5 мл сцинтилляционного коктейля и измеряют бета-эмиссию с помощью счетчика сцинтилляции жидкости. Аликвоты каждого образца анализируют с помощью колориметрических анализов Bradford для нормализации импульсов излучения на общую концентрацию белка.
Пример 400. Функциональный анализ проникновения в клетки с использованием репортерного гена
Сборка вектора гена слияния и трансфицирование клеточной линии
Если пролекарстваз нуклеиновых кислот применяют для ингибирования экспрессии конкретного гена, например, антисмысловые олигонуклеотиды или антигенные олигонуклеотиды, может быть желательным провести функциональный анализ проникновения. Используют культуру клеток HeLa (прикрепленные клетки рака шейки матки человека) в модифицированной Дульбекко среде Игла-10% ФБР. Целевой ген клонируют в коммерчески доступный вектор, такой как Living Colors® Fluorescent Protein Vector, Clontech, Mountain View, CA. Трансфекцию клеток конструкцией ДНК и селекцию стабильных трансфектантов выполняют с использованием стандартных методик. Результатом является конститутивная экспрессия целевого гена и флуоресцентного репортера (например, белка AcGFP1).
Лекарства в форме нуклеиновой кислоты ингибируют экспрессию конкретного гена
Готовят молекулы нуклеиновой кислоты, содержащие фрагменты, включающие хиральный атом фосфора, и соответствующие исходные лекарственные средства, как описано в данном описании, для разрушения промоторной последовательности гена в векторе.
Культура клеток и анализ проникновения
Готовят трансфицированную культуру путем трипсинизирования клеток с помощью 0,05% трипсин-ЭДТА для помещения на планшет. Анализ жизнеспособности и подсчет клеток выполняют с помощью стандартного окрашивания трипановым голубым в фосфатном буферном растворе (ФБР). Клетки разбавляют и засевают с плотностью 1×105 клеток/ячейку в 6-луночном формате. Инкубируют при температуре 37°C в атмосфере, содержащей 5% CO2 в течение 16 час или до тех пор, пока клетки прикрепятся и достигнут слияния по меньшей мере 80%.
Флуоресцентный сигнал сначала определяют через 8-12 час после трансфекции. Добавляют смесь пролекарства в экспериментальные лунки пролекарства до конечной концентрации в предварительно определенном интервале (например, 1 мкМ, 5 мкМ и 10 мкМ). Добавляют смесь исходного лекарственного средства в лунки исходного лекарственного средства до конечной концентрации в предварительно определенном интервале (например, 1 мкМ, 5 мкМ и 10 мкМ). Резервируют необработанные лунки для отрицательного контроля. Инкубируют клетки с исследуемыми веществами в течение предварительно определенных интервалов времени (например, 15 мин, 1 час, 4 час и 8 час).
Определение проникновения пролекарства с использованием экспрессии репортерного гена
Для сбора клеток, лунки промывают 3 раза бессывороточной средой и снова трипсинизируют. Измерение проникновения лекарственного средства выполняют с использованием стандартных методов обнаружения флуоресценции. Для количественного измерения флуоресценции с помощью микроскопии и количественного измерения проточной цитометрией используют длину волны, которая является возбуждающей для флуоресцентного репортера (например, 488 нм для AcGFP1).
Хотя предпочтительные варианты данного изобретения показаны и описаны в данном описании, для специалистов в данной области будет очевидно, что такие варианты предложены только для примера. Многочисленные вариации, изменения и замены будут осуществляться специалистами в данной области без отхода от изобретения. Следует понимать, что различные альтернативы вариантам изобретения, описанным в данном описании, могут применяться в практике изобретения. Предусматривается, что рамки изобретения определяются приведенной ниже формулы изобретения, и что охватываются способы и структуры, находящиеся в пределах указанной формулы изобретения, а также их эквиваленты.
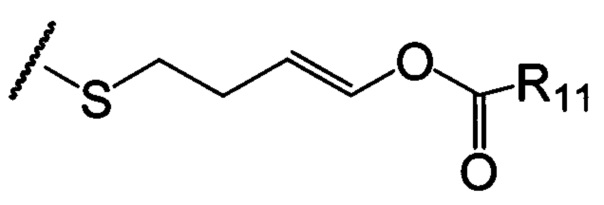
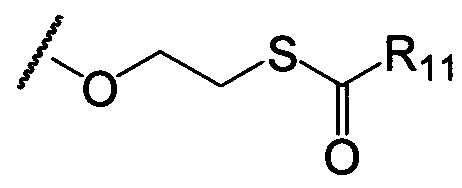
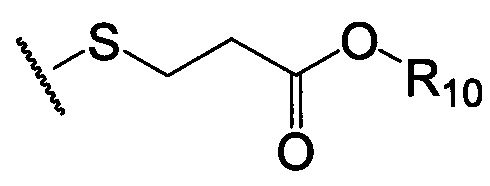
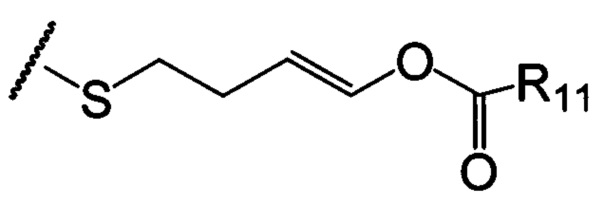
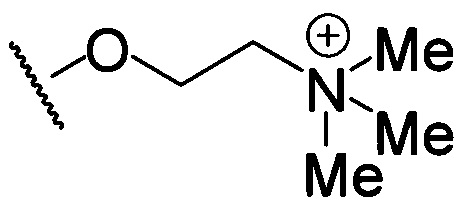
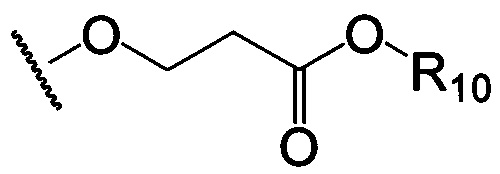
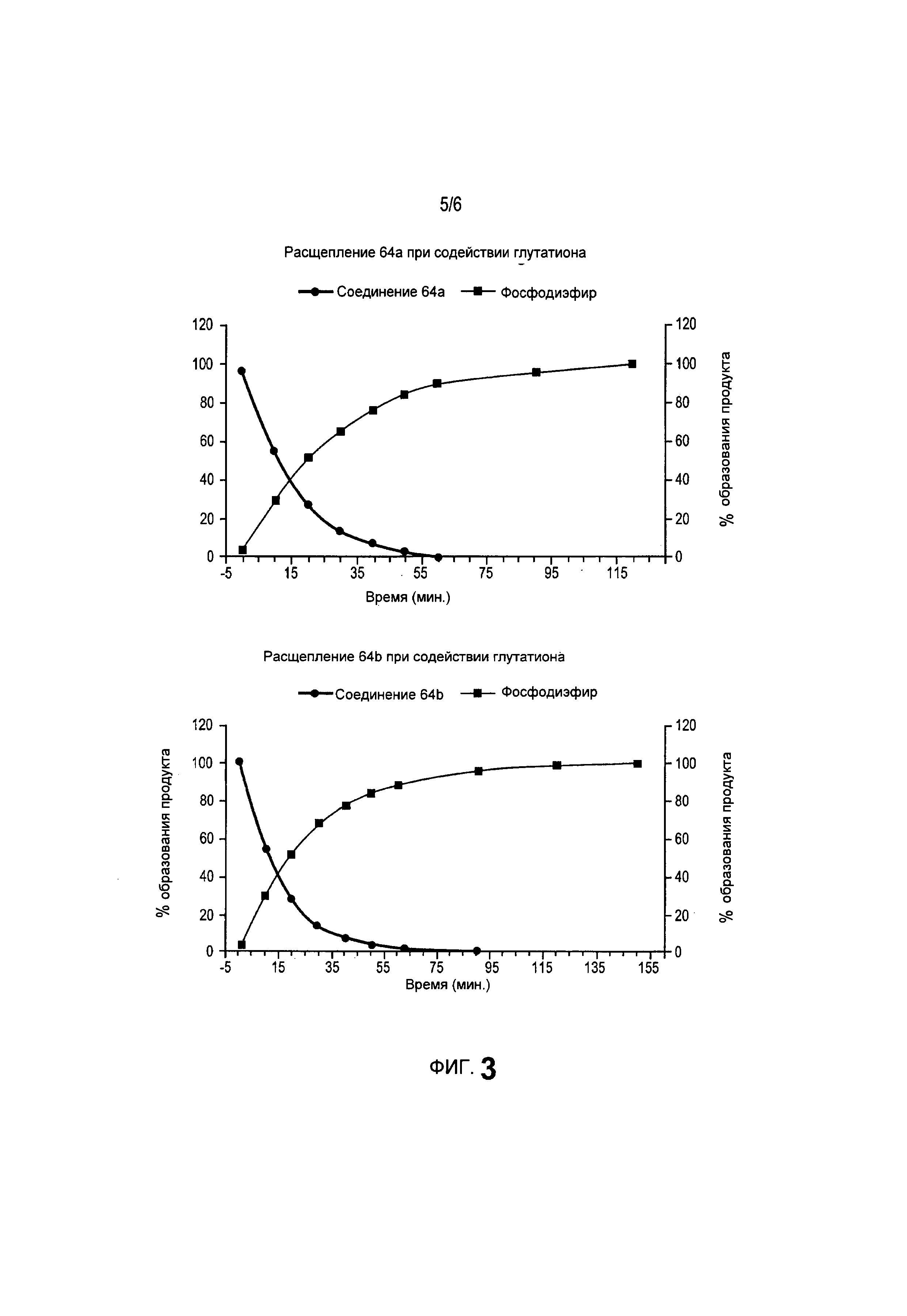
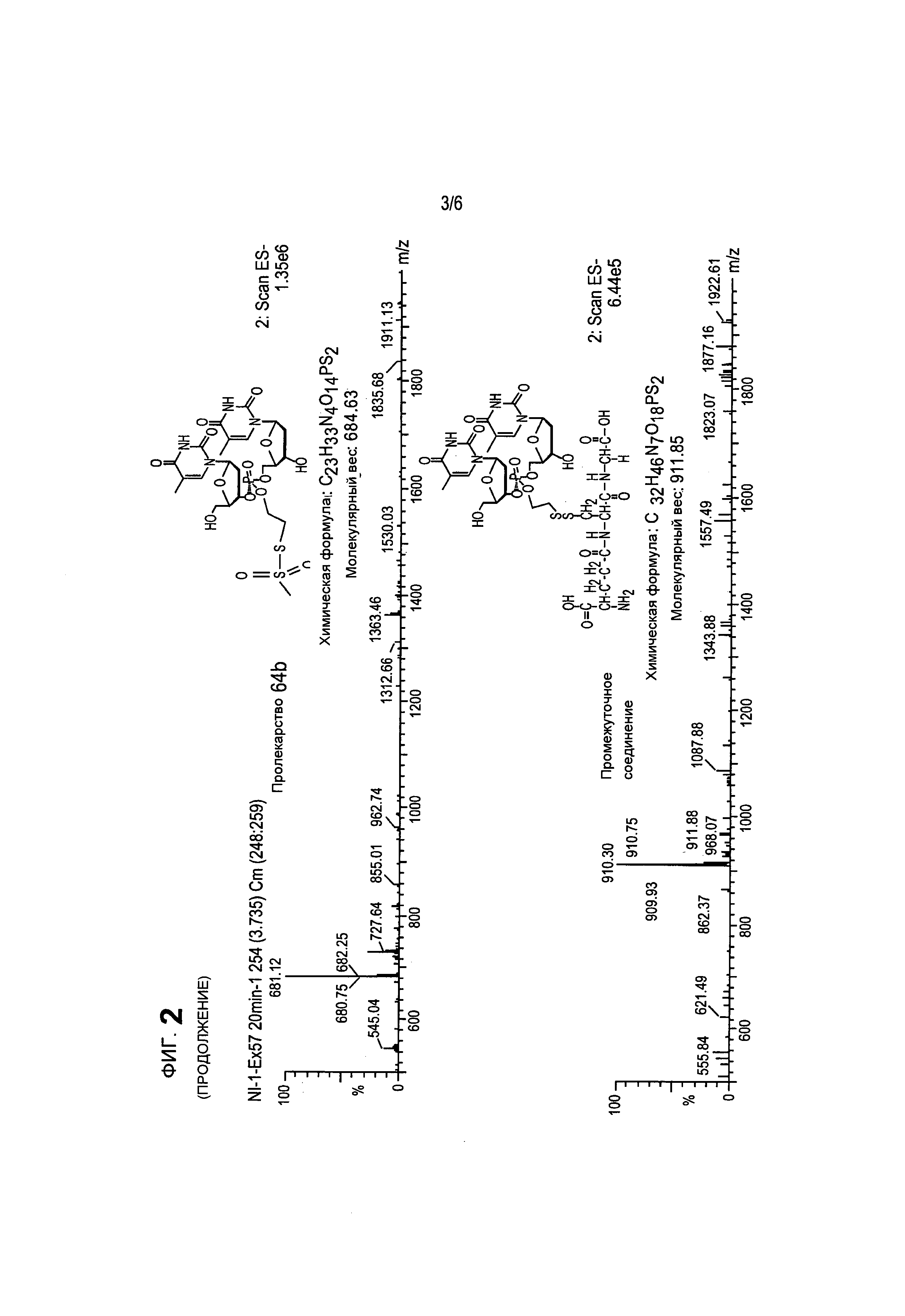
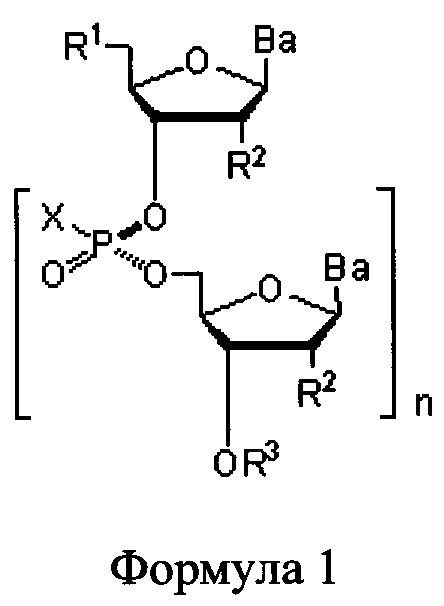
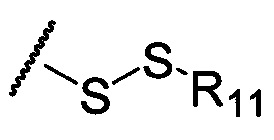
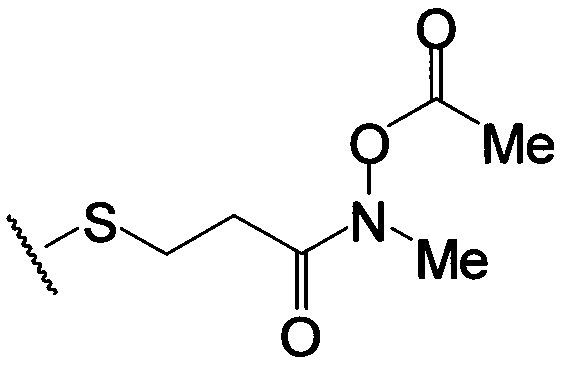
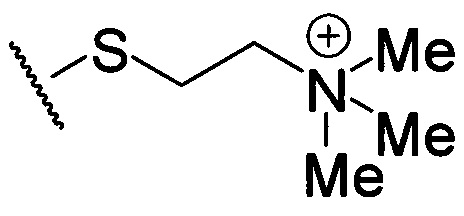
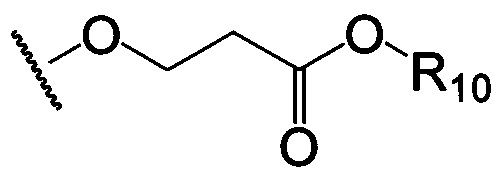
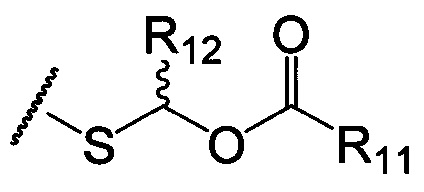
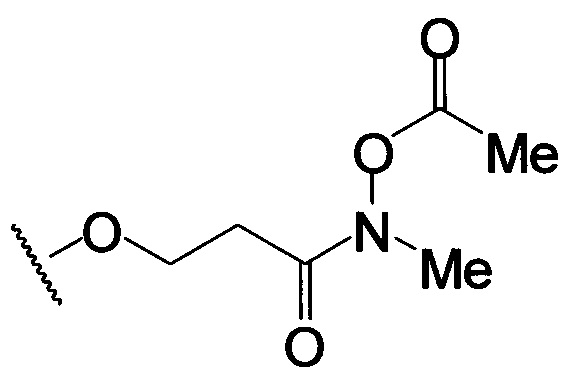
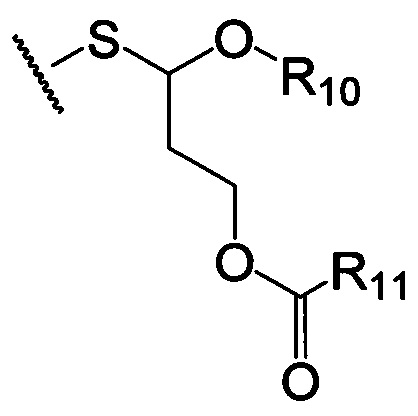
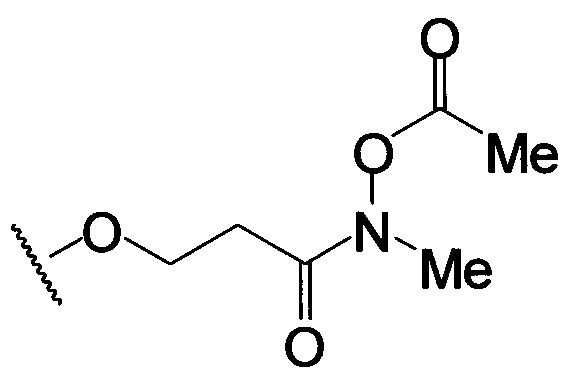
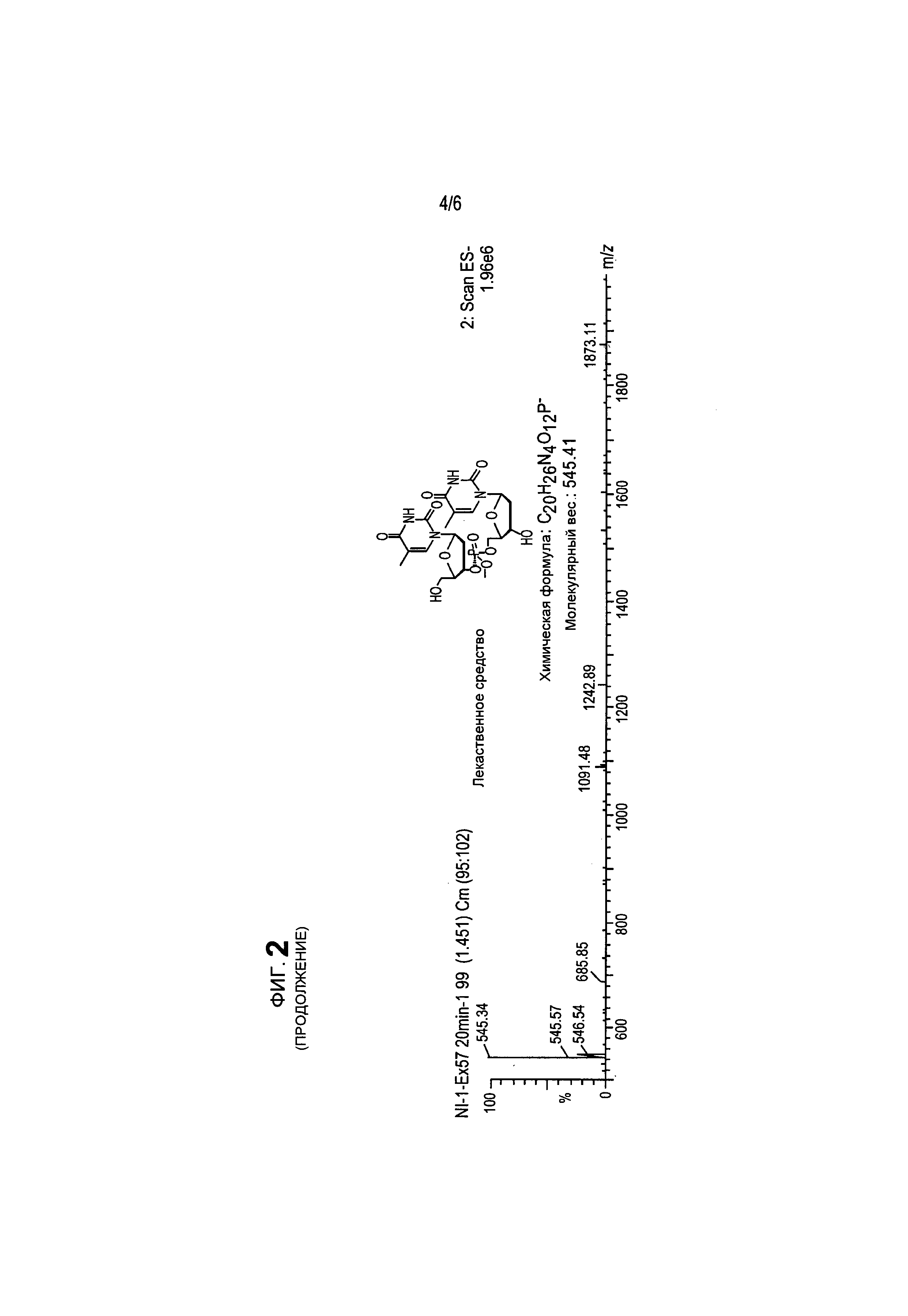
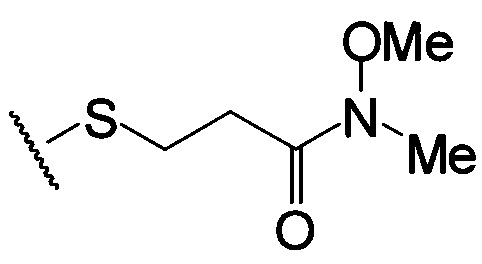
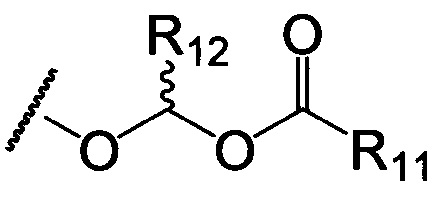
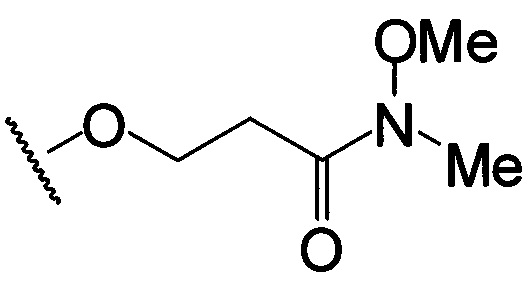
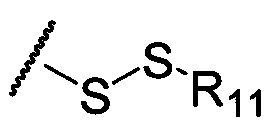
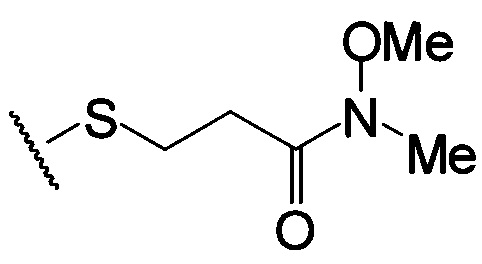
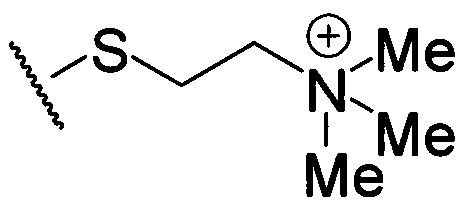
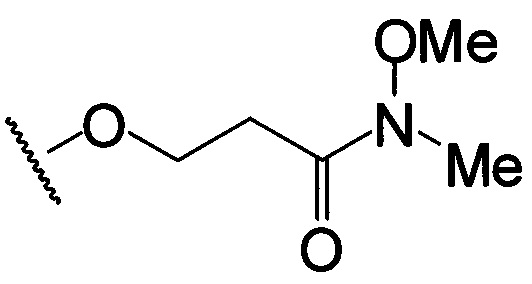
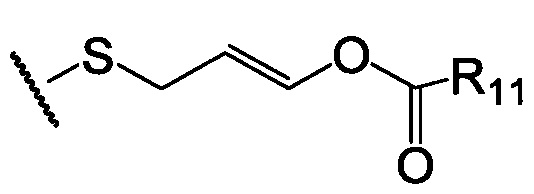
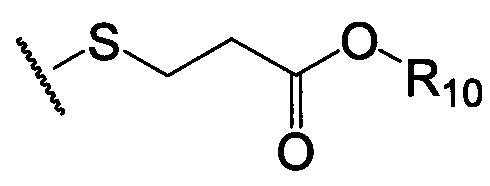
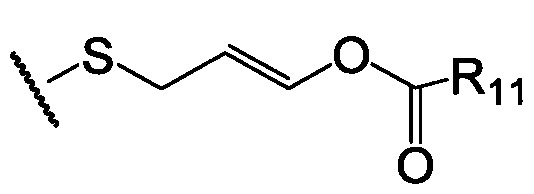
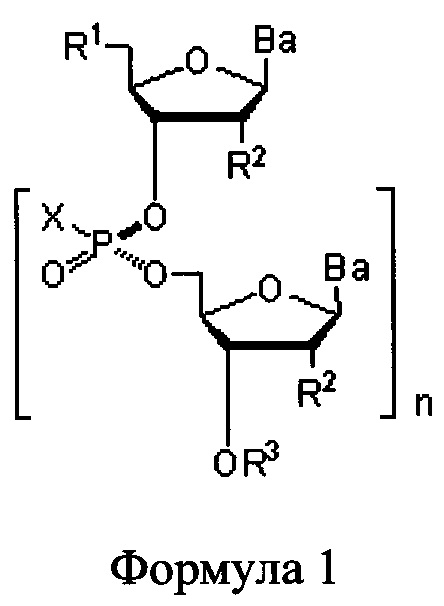
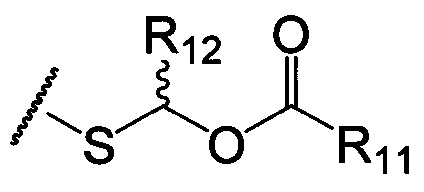
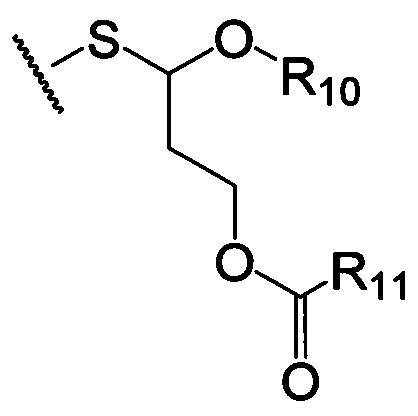
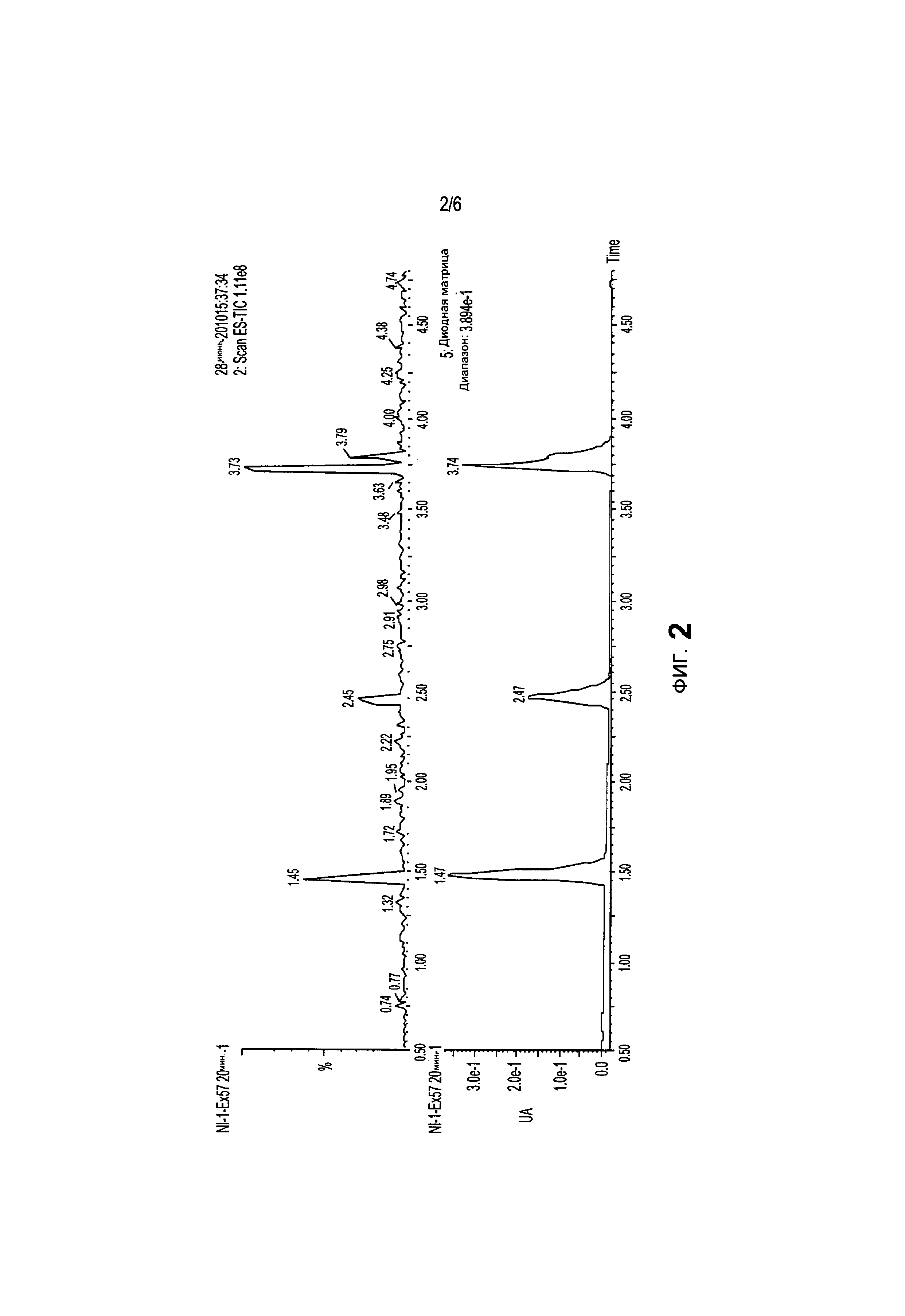
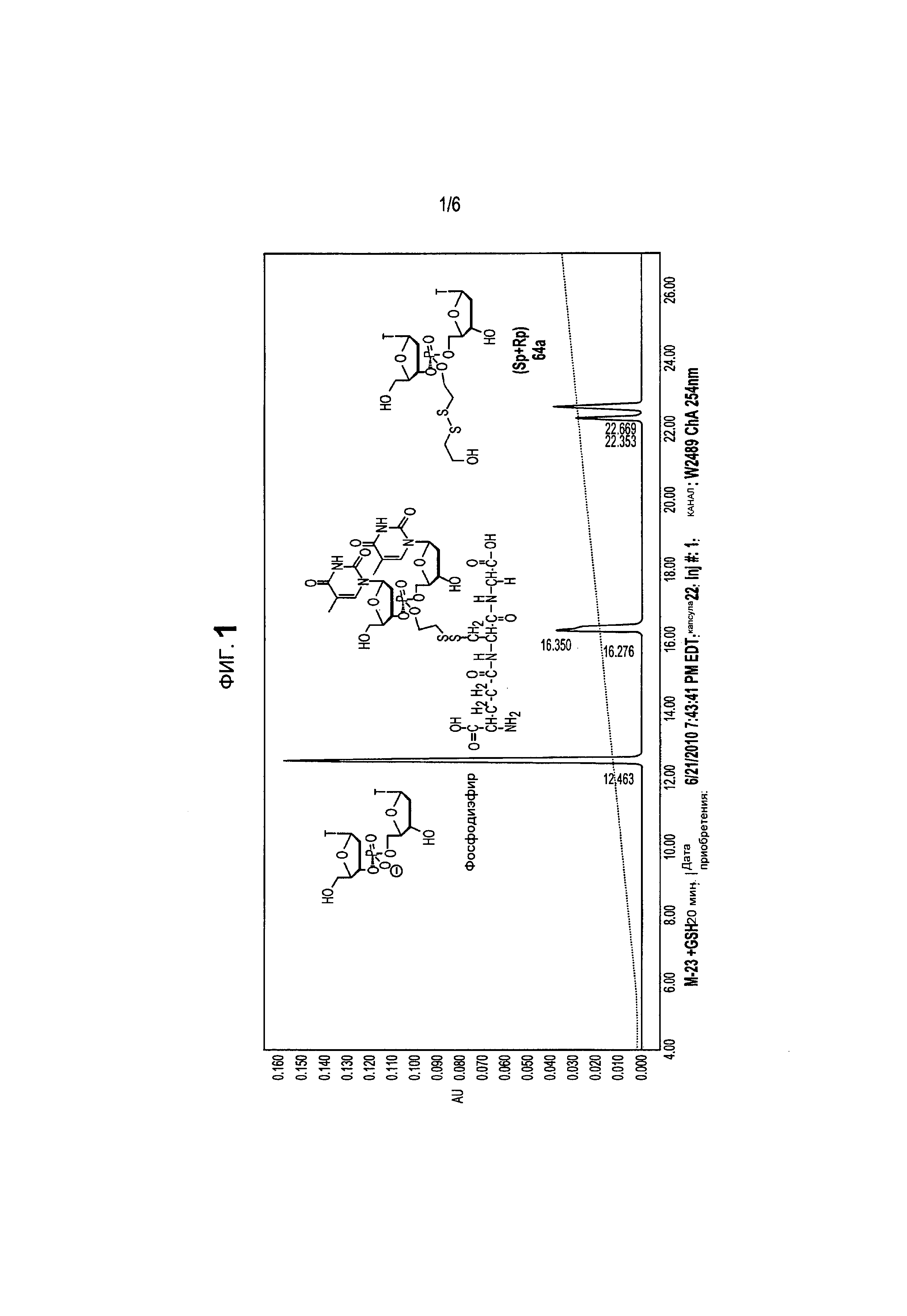
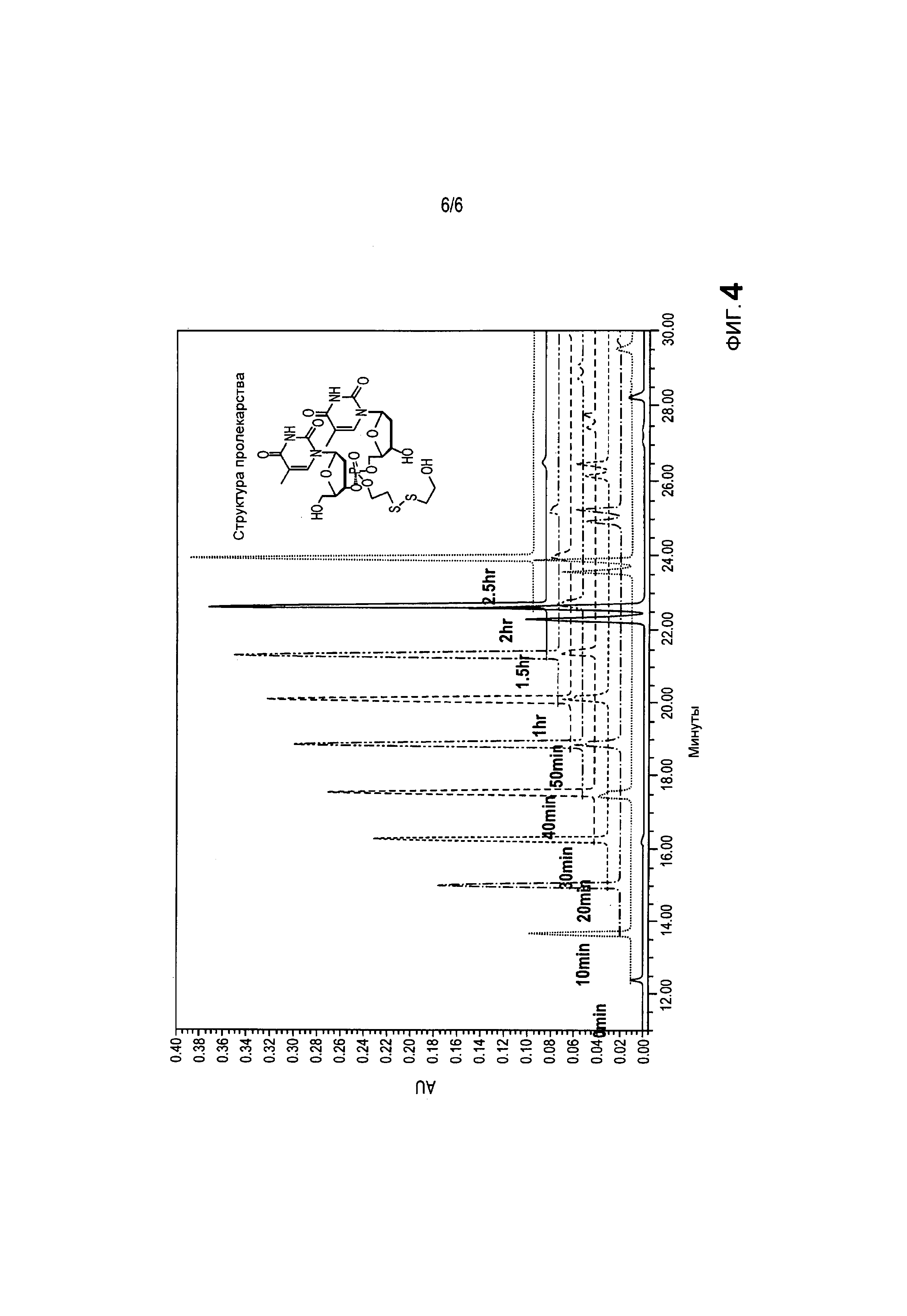
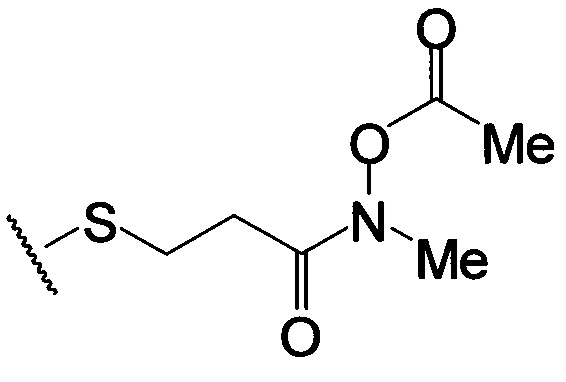
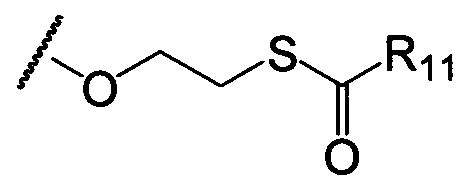
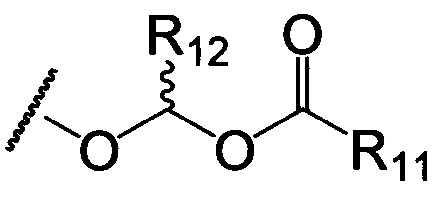
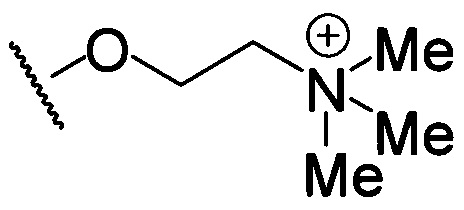
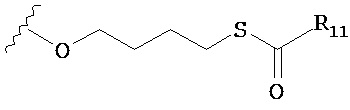 ,
,
