Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ С ПРОЛОНГИРОВАННЫМ ВЫСВОБОЖДЕНИЕМ ДЛЯ ЛЕЧЕНИЯ ЦЕРЕБРОВАСКУЛЯРНЫХ РАССТРОЙСТВ
Вид РИД
Изобретение
Изобретение относится к медицине, в частности к фармакологии и фармации, конкретно к лекарственному средству, содержащему 1-окси-4-адамантанон (кемантан), синтезированному в ФГБНУ «НИИ фармакологии имени В.В. Закусова», и предназначено для применения в качестве средства для лечения цереброваскулярных расстройств. Техническим результатом изобретения является повышение эффективности использования лекарственного средства 1-окси-4-адамантанон, повышение удобства применения лекарственной формы пациентом благодаря снижению кратности приема, получение композиции с пролонгированным высвобождением для терапии цереброваскулярных расстройств. Лидирующее место в структуре заболеваемости занимают поражения нервной системы. Ишемия головного мозга - распространенное и опасное заболевание, которое сопровождается опасными для человека последствиями, такими как хроническая дисциркуляторная энцефалопатия, в зависимости от локализации вызывающая двигательные нарушения, вплоть до паралича, изменения речи, изменения психики, поведения и восприятия. Ишемия головного мозга может протекать в двух формах - острой и хронической (хроническая ишемия головного мозга, в отечественной литературе чаще встречается термин - дисциркуляторная энцефалопатия).
Показано, что 1-окси-4-адамантанон вызывает увеличение локального кровотока в коре головного мозга крыс в условиях глобальной преходящей ишемии, не оказывая влияния на кровоснабжение мозга интактных животных. [Кемантан усиливает кровоснабжение ишемизированного мозга/ Р.С. Мирзоян, Т.С. Ганьшина, Д.В. Масленников, А.И. Турилова, Н.И. Авдюнина, Б.М. Пятин// экспериментальная и клиническая фармакология 2012. - n 6. - с. 27-30] 1-окси-4-адамантанон обладает коротким периодом полувыведения (менее часа), коррелирующим с его дозозависимыми показателями биодоступности. Кемантан полностью всасывается из ЖКТ в кровь, регистрируется уже на 5 минуте после перорального введения, в течение последующих 4 минут концентрация препарата быстро снижается, согласно кинетике первого порядка. Время достижения максимальной концентрации для перорально вводимой лекарственной формы в среднем составляет 4,5 минуты, период полувыведения кемантана колеблется от 7,7 до 8,8 минуты, константа элиминации составляет 0,0845 1/мин. [Литвин Е.А., Колыванов Г.Б., Жердев В.П. Биотрансформация и фармакокинетика производных адамантана // Фармакокинетика и фармакодинамика, 2012, Т. 4, №1, С. 18-24.]
Для фармакодинамической активности 1-окси-4-адамантанон выявлена куполообразная зависимость эффекта от дозы, поэтому его максимальное всасывание достигается при приеме внутрь нескольких разнесенных по времени в течение всего дня доз, а не при разовом приеме одной большой дозы. [Бойко С.С., Жердев В.П., Кисляк Н.А. Клиническая фармакокинетика кемантана. - Фармакология и Токсикология, 1991, т. 54, №1, с. 57-59.; Кисляк Н.А. Создание твердых дозированных лекарственных форм производных адамантана/диссертация на соискание ученой степени кандидата фарм. наук/М. - 1989. - с. 168]
При разработке таблетированных лекарственных форм пролонгированного действия одной из главнейших задач является обеспечение надлежащего времени высвобождения. Оптимальные значения данного параметра способствуют ряду преимуществ в применении: возможности уменьшения курсовой дозы, уменьшению стоимости лечения, сохранению системы гомеостаза вследствие отсутствия быстрого нарастания концентрации лекарственного вещества в плазме крови, поддержанию концентрации на терапевтическом уровне и снижению вероятности возникновения побочных эффектов, вызванных концентрационными колебаниями лекарственного средства
Константа скорости элиминации 1-го порядка (kel) веществ, к которым относится и 1-окси-4-адамантанон), показывает, какая часть вещества элиминируется из организма в единицу времени (размерность мин-1, ч-1).
Немногие лекарственные вещества (этанол, фенитоин) элиминируются в соответствии с кинетикой нулевого порядка. Скорость такой элиминации не зависит от концентрации вещества и является постоянной величиной, т.е. в единицу времени элиминируется определенное количество вещества (например, за 1 ч элиминируется 10 г. чистого этанола). Связано это с тем, что при терапевтических концентрациях названных веществ в крови происходит насыщение ферментов, метаболизирующих эти вещества. Поэтому при увеличении концентрации таких веществ в крови скорость их элиминации не повышается.
Ввиду средних показателей константы скорости элиминации 1-окси-4-адамантанона из организма (0,0845 1/мин у крыс и 0,311 1/ч у человека) необходима пролонгация высвобождения 1-окси-4-адамантанона для снижения кратности приема лекарственного средства при хронической форме ишемии головного мозга. [Литвин Е.А., Колыванов Г.Б., Жердев В.П. Биотрансформация и фармакокинетика производных адамантана //Фармакокинетика и фармакодинамика. -2012. - №1. - С. 18-24.] Близкие значения константы скорости элиминации для человека имеет метотрексат 0,380 1/ч (72%) и многие другие лекарственные средства. [Сингин А.С. Популярное моделирование фармакокинетики высоких доз метотрексата у пациентов с остеосаркомой/ А.С. Сингин, И.Б. Бондарева // Популяционная фармакокинетика. - 2005. - №1(2). - с. 18-22.] Более низким значением константы скорости элиминации обладает субстанция ГБ-115, при испытании на крысах она показала 0,0323 1/мин. [Жердев В.П. Доклиническое изучение фармакокинетики нового анксиолитика дипетидной структуры ГБ-115 / Жердев В.П. и соавт. // Исследования фармакокинетики. - 2015. - №1. - С. 52-59.]
Одним из надежных и наиболее доступных инструментов, для характеристики биофармацевтического качества лекарственного средства in vitro, является тест «Растворение». Данный тест позволяет определить скорость растворения (высвобождения) фармацевтической субстанции из лекарственной формы. Модельные системы in vitro, например применяемые для оценки всасывания из желудочно-кишечного тракта, являются ничем иным, как предпосылкой для осмысленной и эффективной экономии экспериментов in vivo. Модельные системы проведения оценки высвобождения фармацевтической субстанции стандартизованы, хорошо изучены и уже вошли в фармакопеи различных стран (USP (Фармакопея США), PH. Eur. (Европейская фармакопея), Государственная фармакопея XII и др) [А.Н. Мымриков In vitro - in vivo корреляция: от теории к практике/Провизор. - 2008. - №2; Ю.И. Кулинич Биофармацевтические свойства лекарственных веществ / Разработка и регистрация лекарственных средств. - 2014. - №1(6). - с. 26-29.]
Несмотря на расширяющийся поиск альтернативного пути введения и методов лекарственной доставки, пероральный способ введения остается к наиболее популярным. Около 70% всех лекарственных форм предназначены для перорального применения, так как данный способ введения является самым приемлемым и удобным для пациентов. Кроме того, это наиболее изученный и отработанный метод заводского производства, используемый для получения твердых дозированных лекарственных форм (таких как таблетки и капсулы). Твердые дозированные лекарственные формы отличаются оптимальным соотношением цена-качество. К преимуществам таблеток относятся: точное дозирование лекарственных веществ в условиях массового производства; длительное действие лекарственного вещества; последовательное всасывание лекарственных веществ; маскировка неприятных органолептических свойств (вкуса, запаха или красящих свойств) лекарственных веществ за счет нанесения полимерных пленочных оболочек; полная механизация процесса изготовления, обеспечивающая высокую производительность, чистоту и гигиеничность таблеток.
Твердые дозированные лекарственные формы можно подразделить на 2 основные категории: лекарственные формы с немедленным высвобождением, где распадаемость и последующее лекарственное растворение и высвобождение происходит в желудке, и лекарственные формы с модифицированным высвобождением, когда изменяются участок или время лекарственного высвобождения в ЖКТ.
Модифицированное высвобождение из лекарственной формы связана с такими параметрами как фармакокинетика и фармакодинамика субстанции. Эти параметры варьируются в зависимости от химической структуры и классовой принадлежности субстанции. Модификация времени высвобождения и выраженности действия обеспечивается, в первую очередь, за счет адекватных вспомогательных веществ, замедляющих растворение и всасывание лекарственного вещества. Для модификации применяются специальные технологии получения лекарственной формы, изменяющие его фармакокинетические свойства.
В зависимости от технологии получения твердых лекарственных форм с пролонгированным высвобождением различают два принципиальные типа: резервуарный и матричный. Формы резервуарного типа представляют собой ядро, содержащее субстанцию, и полимерную пленочную (мембранную) оболочку, которой определяется скорость высвобождения. Резервуаром может быть единичная лекарственная форма - таблетка или капсула. Под матричным типом лекарственной формы подразумевается наличие в ней полимерной матрицы, в которой распределена субстанция, в таких случаях лекарственные формы часто имеют вид обычной таблетки.
Наиболее распространены три технологические схемы получения таблеток: с применением влажного, сухого гранулирования или прямого прессования.
Одним из способов изготовления пролонгированных твердых лекарственных форм на основе предлагаемой композиции заключается в том, что лекарственное и вспомогательные вещества гранулируют водой и/или раствором связывающего вещества и полученные гранулы после этого сушат в сушильном шкафу. Остальные вспомогательные вещества, которые не использовали для включения в гранулы, затем смешивают с высушенными гранулами с получением в результате композиции, пригодной для капсулирования, таблетирования или др.
Обычно операции смешивания и равномерного увлажнения порошкообразной смеси различными гранулирующими растворами совмещают и проводят в одном смесителе. Иногда операции смешивания и гранулирования совмещаются в одном аппарате (высокоскоростные смесители - грануляторы). Смешивание обеспечивается за счет энергичного принудительного кругового перемешивания частиц и сталкивания их друг с другом. Другая конструкция аппарата для совмещения операций смешивания и гранулирования -центробежный смеситель - гранулятор.
По сравнению с сушкой в сушильных шкафах, которые являются малопроизводительными и в которых длительность сушки достигает 20-24 часа, более перспективной считается сушка гранул в кипящем (псевдоожиженом) слое. Основными ее преимуществами являются: высокая интенсивность процесса; уменьшение удельных энергетических затрат; возможность полной автоматизации процесса.
К наиболее перспективным установкам периодического действия, используемым в производстве, относятся аппараты псевдоожиженного слоя: сушилки-грануляторы (например, СГ-30, СГ-60, фирм Glatt и др.), совмещающие несколько операций: смешение, увлажнение, гранулирование, сушку, опудривание.
В некоторых случаях, если лекарственное вещество разлагается в присутствии воды, прибегают к сухому гранулированию. Для этого из порошка прессуют брикеты, которые затем размалывают, получая крупку. После отсеивания от пыли и опудривания скользящими вспомогательными веществами крупку таблетируют. В настоящее время под сухим гранулированием понимают метод, при котором порошкообразный материал подвергают первоначальному уплотнению (прессованию), получая гранулят, который затем таблетируют - вторичное уплотнение. При первоначальном уплотнении в массу вводят сухие склеивающие вещества, обеспечивающие под давлением сцепление частиц как гидрофильных, так и гидрофобных веществ. Доказана пригодность для сухого гранулирования полиэтиленоксида (ПЭО) в сочетании с крахмалом и тальком.
Технология прямого прессования таблеток заключается в смешении лекарственных препаратов с необходимым количеством вспомогательных веществ и прессовании на таблеточных прессах. Наиболее очевидное преимущество прямого прессования перед традиционной влажной грануляцией - экономичность - достигается благодаря уменьшению стоимости оборудования и производства. Однако применение данного метода возможно в силу физико-химических особенностей субстанций не для всех лекарственных веществ.
Полученные частицы затем смешиваются с другими вспомогательными веществами, например, связующим, скользящими веществами и т.д. Предлагаемые композиции, полученные любым из вышеуказанных методов, формуются в любую лекарственную форму при использовании общеизвестных в данной области технологий и методов, например таблетированием, включением в желатиновую капсулу и т.д. Из предлагаемых композиций изготавливаются лекарственные формы известными методами с обеспечением унифицированных доз заявляемого соединения для перорального приема, например 50 мг, 100 мг, 200 мг, 300 мг и т.д. в виде капсул, таблеток и тому подобное.
Полученные таблетированные или капсульные лекарственные формы должны быть защищены во время хранения от внешних факторов (действия тепла или света, а также и проникновения влаги). В целях обеспечения конкретного положительного эффекта на лекарственную форму может наноситься полимерная пленочная оболочка.
Полимерное пленочное покрытие лекарственных форм при использовании водного пленкообразующего состава следует осуществлять при температуре ядер таблеток от 30 до 50°C, температуре на входе 50-80°C и относительной влажности менее 50%.
Покрытие наносят на лекарственную форму с увеличением ее массы примерно на 1,0-15,0%, предпочтительно на 4,0-10,0 мас. %.
Полимерные пленочные покрытия можно наносить общеизвестными способами: погружением в раствор пленкообразующего вещества, наслаиванием в соответствующем перфорированном барабане, получением покрытия во взвешенном слое. Прекращают нанесение полимерного пленочного покрытия по достижении необходимой массы таблетки. Барабан с боковой вентиляцией обеспечивает высокую скорость испарения растворителя, благодаря чему покрытие таблеток применяемыми в фармацевтической технологии полимерными пленочными покрытиями осуществляется за достаточно короткое время. Подача в одном направлении распыляемой среды и подготовленного теплого воздуха, а также сведение турбулентности в барабане к минимуму уменьшают высушивание распыляемого материала, обеспечивая эффективность покрытия более 95,0%. Прирост массы таблетки, покрытой полимерной пленочной оболочкой, может находиться в интервале от 1,0 до 15,0%.
Покрытые с полимерной пленочной оболочкой таблетки или капсулы имеют время высвобождения примерно от 10 до 30 минут. Таблетки или капсулы с кишечнорастворимой полимерной пленочной оболочкой имеют время высвобождения обычно от 30 мин до 6 часов. Однако, полимерная пленочная оболочка может только отсрочить высвобождение фармацевтической субстанции, но не может обеспечить непрерывное высвобождение на протяжении всего времени. Подбор только матрикса способствует пролонгированию и обеспечению непрерывного высвобождения на протяжении нескольких часов.
Многие составы твердых лекарственных форм (70,0-80,0%) характеризуются содержанием большего количества вспомогательных ингредиентов, чем лекарственных веществ. Вследствие того, что значительная часть лекарственных веществ обладают низкими показателями сыпучести и неудовлетворительными физико-механическими характеристиками, в состав таблеточной и инкапсулируемой масс для получения необходимых реологических и технологических свойств вводятся различные вспомогательные вещества. Вспомогательные вещества не являются индифферентными формообразователями, а оказывают сложное, многогранное влияние на лекарственный препарат, на его фармакокинетику, а, в конечном итоге, на терапевтическую эффективность лекарственного препарата.
При производстве таблеток и капсул используется широкий ассортимент вспомогательных веществ. Для правильного выбора рецептуры необходимо знать свойства субстанции лекарственного вещества: сыпучесть, прессуемость, способность скольжения, способность электролизоваться, а также является ли материал ядовитым, раздражающим, взрывоопасным, как влияет на него влага, тепло, свет, воздух, давление, как он действует на пуансоны и матрицы.
На основании изложенного научно-обоснованный выбор вспомогательных веществ в каждом конкретном случае является одним из важных условий получения таблетированных или капсулированных препаратов с максимальной терапевтической активностью при наименьших дозировках и побочном действии.
пролонгированным высвобождением на основе 1-окси-4-адамантанона, отвечающих всем требованиям Государственной Фармакопеи XII издания.
Раскрытие изобретения
Фармацевтическая композиция, выполненные в твердых лекарственных формах содержат, в качестве действующего вещества - 1-окси-4-адамантанон в терапевтически эффективном количестве, а в качестве вспомогательных веществ - фармацевтически приемлемые вспомогательные вещества, пригодные для использования в твердых фармацевтических композициях пролонгированного действия.
В соответствии с настоящим изобретением фармацевтической композиции представлены в твердой форме, содержат следующие компоненты (мас. %):
|
Фармацевтическая композиция на основе 1-окси-4-адамантанона в качестве вспомогательных веществ, обеспечивающих достаточную массу таблетки (наполнителя), может содержать, по меньшей мере, одно вещество, выбранное из группы: микрокристаллическая целлюлоза, лактоза, лудипресс, кальция фосфат, кальция дигидрофосфат, кальция гидрофосфат дигидрат, кальция сульфат дигидрат, кальция карбонат основной, поливинилпирролидон; декстрин, амилопектин, ультра-амилпектин, сорбит, маннит, пектин, магния карбонат основной, магния окись, метилцеллюлоза (МЦ), прежелатинизированный крахмал, натриевая соль карбокси-метилцеллюлозы, картофельный и кукурузный крахмал, карбоксиметилцеллюлоза, гидроксипропилметилцеллюлоза, вспомогательные вещества с повышенной сорбционной способностью: коллоидный кремний (аэросил, Syloid®), алюмометосиликат магния (Neusilin®, Fuji, Япония);
В качестве связывающего вещества используется по меньшей мере, одно, выбранное из группы: вода очищенная, спирт этиловый, крахмальный клейстер, растворы: карбоксиметилцеллюлозы (КМЦ), оксиэтилцеллюлозы (ОЭЦ), оксипропилметилцеллюлозы (ОПМЦ); поливинилового спирта (ПВС), поливинилпирролидона (ПВП), альгиновой кислоты, натрия альгината, метилцеллюлозы, гидроксипропилметилцеллюлозы.
В качестве пролонгирующего полимера она может содержать, по меньшей мере, одно вещество, выбранное из группы: производные целлюлозы (этилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза), выпускаемые в промышленности под наименованиями: Methocel® K4M Premium CR, Methocel® K100M Premium CR, Methocel® A15 Premium LV, наименованиями: Methocel® K4M Premium CR, Methocel® K100M Premium CR, Methocel® A15 Premium LV, Methocel® E6 Premium LV, Methocel® K100 Premium LV (DOW Chemical, США); Walocel® HM 15PA, Walocel® HM 100000 PA (Wolff Cellulosics, концерн "Bayer AG") и акриловой кислоты (редкосшитые акриловые полимеры, метакриловая кислота, этилакрилат, триметиламмониоэтилметакрилат и их сополимеры), выпускаемые промышленностью под наименованиями: Eudragit® RS РО (Evonik, Германия), Carbopol® 71G (Noveon, США); полиэтиленгликоль, интерполимерный комплекс (выпускаемый в промышленности под наименованием КПН) полиметакриловой кислоты и полиэтиленгликоля эквимольного состава (1:40 мас. соответственно). [Фармацевтическая технология таблетки: учебное пособие/ под ред. С.А. Кедика. - М.: ЗАО ИФТ, 2015. - 672 с.].
В состав полимерных пленочных покрытий входит одно или смесь следующих вспомогательных веществ: поливинилпирролидон, поливиниловый спирт, гидроксипропилцеллюлоза, гидроксиметилцеллюлоза и гидроксипропилметилцеллюлоза (Opadry YellowT, Colorcon Corp.) оксипропилметилцеллюлозы фталат, ацетилцеллюлозы фталат, поливинилацетата фталат, метилцеллюлозы фталат, сополимер метакриловой кислота или сложные метиловые эфиры метакриловой кислоты (Eudragit R, Акрил-из), Колликут® МАЕ 100 П, Колликут® МАЕ 30D, Колликут® МАЕ 100 D, этилцеллюлоза, ацетилцеллюлоза, сополимеры поливинилового спирта и малеинового ангидрида, полиэтиленгликоль (полиэтиленгликоль 6000), триэтилцитрат, диэтилфталат, пропиленгликоль, глицерин, бутилфталат, двуокись титана и красители, окись железа, алюминиевые красители (Opadry II).
В качестве вспомогательных веществ, предотвращающих налипание и обеспечивающих выталкивание из матрицы, она может содержать, по меньшей мере, одно вещество, выбранное из группы скользящих: стеариновая кислота и/или ее соли, аэросил (диоксид кремния).
Следующие примеры иллюстрируют варианты получения фармацевтической композиции.
Пример 1. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (25,0 мас. %), 70,00 г лактозы (наполнитель) (35,0 мас. %) и 66,00 г пролонгирующих полимеров (Methocel® K4M - 11,0%, Methocel® K100 LV - 22,0%) смешивают в смесителе. Увлажняют массу клейстером крахмальным (связующее вещество) (массо-объемная концентрация крахмала в клейстере равна 8,0%). Масса крахмала в пересчете на чистое вещество составляет 12,00 г (6,0 мас. %). Увлажненная масса не должна иметь вкраплений от плохого распределения увлажнителя и должна хорошо комковаться. Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 45±5°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе с диаметром отверстий в сетке 1,0-1,5 мм. Массу сухого гранулята опудривают стеариновой кислотой (скользящее вещество), в количестве 2,00 г (1 мас. %). Сыпучесть полученной массы составляла 7,1 г/с.
Гранулят прессуют на таблеточном прессе или капсулируют в твердые желатиновые капсулы. Полученные таблетки имеют среднюю массу 0,20 г. Полученные таблетки и капсулы отвечают требованиям Государственной фармакопеи.
Пример 2. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (25,0 мас. %), 67,00 г кальция карбоната основного (наполнитель) (33,5 мас. %) и 66,00 г пролонгирующего полимера (Methocel® K4M - порошковую смесь просеивают для достижения однородности смешивания и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор поливинилпирролидона (связуюущее вещество) (Kollidon® 25) смешивают в смесителе. Масса Kollidon® 25 в пересчете на чистое вещество составляет 15,00 г (7,5 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают стеаратом кальция (скользящее вещество), в количестве 2,00 г (1,0 мас. %). Полученный гранулят можно капсулировать в твердые желатиновые капсулы. Полученные капсулы, с содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Пример 3. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (15,0 мас. %), 166,67 г метилцеллюлозы (наполнитель) (50,0 мас. %) перемешивают для достижения однородности смешивания и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор поливинилпирролидона (Kollidon® 25) (связующее вещество) смешивают в смесителе. Масса Kollidon® 25 в пересчете на чистое вещество составляет 16,67 г (5,0 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята смешивают с 66,67 г пролонгирующего полимера (Carbopol 71 G - 20,0%) и опудривают диоксидом кремния (скользящее вещество), в количестве 33,34 г (10,0 мас. %). Полученный гранулят таблетируют или капсулировать в твердые желатиновые капсулы. Содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Пример 4. Предварительно отвешенные 300,00 г 1-окси-4-адамантанона (50,0 мас. %), 144,00 г лактозы (24,0 мас. %) (наполнитель) и 120,00 г этилцеллюлоза (20,0 мас. %) (пролонгируюущий полимер) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор поливинилпирролидона (Kollidon® 30) (связуюущее вещество) смешивают в смесителе. Масса Kollidon® 30 в пересчете на чистое вещество составляет 12,00 г (2,0 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают диоксидом кремния (скользящее вещество), в количестве 12,00 г (4,0 мас. %). Полученный гранулят можно таблетировать или капсулировать. Получают таблетки по технологии или капсулы. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Опадрай 12,00 г (4,0 мас. % прирост массы таблетки после покрытия). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные таблетки или капсулы, с содержанием 1-окси-4-адамантанона 0,30 г, отвечают требованиям Государственной фармакопеи.
Пример 5. Предварительно просеянные и отвешенные 10,00 г 1-окси-4-адамантанона (5,0 мас. %), 154,00 г лудипресса (наполнитель) (77,0 мас. %), 34,00 г Carbopol® 71G (17,0 мас. %) (пролонгирующий полимер), тщательно перемешивают, после чего добавляют 2,00 г магния стеарата (скользящее вещество) (1,0 мас. %), повторно перемешивают. Получают таблетки по технологии прямого прессования или капсулы. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Колликут® оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные твердые лекарственные формы, с содержанием 1-окси-4-адамантанона 0,10 г, отвечают требованиям Государственной фармакопеи.
Пример 6. Предварительно просеянные и отвешенные 50,00 г 1-окси-4-адамантанона (25,0 мас. %), 46,00 г микрокристаллической целлюлозы (наполнитель) (23,0 мас. %) и 100,00 г КПН (50,0 мас. %) (пролонгирующий полимер) тщательно перемешивают, после чего увлажняют полученную смесь связующим: водой очищенной (1,0 мас. %), далее увлажненную массу гранулируют и сушат до остаточной влажности 2,0-3,0% (Под остаточной влажностью сырья понимают потерю в массе за счет гигроскопической влаги и летучих веществ, которую определяют в сырье при высушивании до постоянной массы. [ГФ XIII, Том 2, стр 413 ОФС 1.3.5.00007.15; ГФ XIII ОФС "Потеря в массе при высушивания" или "определение воды"]). Сушку проводят методом псевдоожиженного слоя. Высушенные гранулы размалывают в грануляторе фирмы Erweka (Германия). Сухие гранулы опудривают 2,00 г (1,0 мас. %) магния стеарата (скользящее вещество). Получают таблетки или капсулы с содержанием 1-окси-4-адамантанона 0,050 г. Полученные твердые лекарственные формы отвечают требованиям Государственной фармакопеи.
Пример 7. Получение фармацевтической композиции 1-окси-4-адамантанона осуществляют, смешивая 1000,00 г 1-окси-4-адамантанона (50,0 мас. %), 380,00 г лактозы (19,0 мас. %) (наполнитель), 600,00 г полиэтиленгликоля (30,0 мас. %) (пролонгирующий полимер) и 20,00 г кальция стеарата (скользящее вещество) (1,0 мас. %) в смесителе в течение 10-15 мин. Смесь порошков брикетируют на таблеточном или брикетировочном прессе (диаметр брикетов - от 12 мм до 50 мм). Полученные брикеты разламывают в грануляторе с размерами отверстий сетки 1,0-1,5 мм. Таблетирование производят на ротационном прессе фирмы «Киллиан». Диаметр пуансонов 8,0 мм, средняя масса таблеток 0,20 г. Получают таблетки с содержанием 1-окси-4-адамантанона 0,10 г, отвечающие всем нормативным требованиям.
Пример 8. Предварительно просеянные и отвешенные 100,00 г 1-окси-4-адамантанона (50,0 мас. %), 28,00 г лудипресса (наполнитель) (14,0 мас. %), 70,00 г редкосшитого акрилового полимера (пролонгирующий полимер) (35,0 мас. %) тщательно перемешивают, после чего добавляют 2,00 г магния стеарата (скользящее вещество) (1,0 мас. %), повторно перемешивают. Получают таблетки по технологии прямого прессования или капсулы с содержанием 1-окси-4-адамантанона 0,10 г. Полученные твердые лекарственные формы отвечают требованиям Государственной фармакопеи.
Пример 9. Получение фармацевтической композиции 1-окси-4-адамантанона осуществляют, смешивая 500,00 г 1-окси-4-адамантанона (33,3 мас. %), 285,00 г лудипресса (наполнитель) (19,0 мас. %), 700,00 г Eudragit® RS PO (пролонгирующий полимер) (46,7 мас. %) и 15,00 г кальция стеарата (скользящее вещество) (1,0 мас. %), в смесителе, в течение 10-15 мин. Смесь порошков брикетируют на таблеточном или брикетировочном прессе (диаметр брикетов - от 12 мм до 50 мм). Полученные брикеты разламывают в грануляторе с размерами отверстий 1,0-1,5 мм. Полученную крупку таблетируют или капсулируют. Получают таблетки или капсулы с содержанием 1-окси-4-адамантанона 0,05 г, отвечающие всем нормативным требованиям.
Пример 10. Предварительно просеянные и отвешенные 100,00 г 1-окси-4-адамантанона (46,3 мас. %), 28,00 г лудипресса (наполнитель) (13,0 мас. %), 81,00 г Carbopol® 71G (39,8 мас. %) (пролонгирующий полимер), тщательно перемешивают, после чего добавляют 2,00 г магния стеарата (скользящее вещество) (0,9 мас. %), повторно перемешивают. Получают таблетки по технологии прямого прессования или капсулы. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Опадрай II 16,00 г (7,4 мас. % прироста массы таблетки после покрытия) (гипромеллоза, лактозы моногидрат, полидекстроза, макрогол, титана диоксид, железа оксид желтый, железа оксид красный). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные твердые лекарственные формы, с содержанием 1-окси-4-адамантанона 0,10 г, отвечают требованиям Государственной фармакопеи.
Пример 11. Получение фармацевтической композиции 1-окси-4-адамантанона осуществляют, смешивая 1000,00 г 1-окси-4-адамантанона (26,0 мас. %), 230,00 г кальция фосфата (наполнитель) (6,0 мас. %), 1845,30 г микрокристаллической целлюлозы (наполнитель) (48,0 мас. %), 190,00 г Methocel® K100M (пролонгирующий полимер) (5,0 мас. %) и 580,00 г диоксида кремния (скользящее вещество) (15,0 мас. %) в смесителе в течение 10-15 мин. Смесь порошков брикетируют на таблеточном или брикетировочном прессе (диаметр брикетов - от 12 мм до 50 мм). Полученные брикеты разламывают в грануляторе с размерами отверстий сетки 1,0-1,5 мм. Таблетирование производят на ротационном прессе фирмы «Киллиан». Диаметр пуансонов 10,0 мм. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Колликут® МАЕ 100 D 120,00 г (3,0 мас. % прироста массы таблетки после покрытия). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные твердые лекарственные формы, с содержанием 1-окси-4-адамантанона 0,10 г, отвечают требованиям Государственной фармакопеи.
Пример 12. Предварительно просеянные и отвешенные 100,00 г 1-окси-4-адамантанона (5,0 мас. %), 1700,00 г лудипресса (наполнитель) (85,0 мас. %), 40,00 г Methocel® K100M (пролонгирующий полимер) (2,0 мас. %), 150,00 г микрокристаллической целлюлозы (7,5 мас. %) (наполнитель) тщательно перемешивают, после чего добавляют 5,00 г магния стеарата (скользящее вещество) (0,5 мас. %), повторно перемешивают. Получают таблетки по технологии прямого прессования или капсулы. Полученные таблетки ядра или капсулы отвечают требованиям Государственной фармакопеи.
Пример 13. Предварительно отвешенные 500,00 г 1-окси-4-адамантанона (10,47 мас. %), 750,00 г кальция дигидрофосфат (наполнитель) (15,7 мас. %) и 960,00 г гидроксипропилметилцеллюлоза (ГПМЦ) (наполнитель) (20,1 мас. %) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% спиртовым раствором ГПМЦ (связывающее вещество) смешивают в смесителе. Масса ГПМЦ в пересчете на чистое вещество составляет 40,00 г (0,84 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята смешивают с 2500,00 г Carbopol® 71G (пролонгирующий полимер) (52,36 мас. %), тщательно перемешивают, после чего добавляют 25,00 г диоксида кремния (0,53 мас. %), повторно перемешивают. Полученный гранулят можно таблетировать или капсулировать. Получают таблетки по технологии или капсулы, отвечающие требованиям Государственной фармакопеи, с содержанием 1-окси-4-адамантанона 0,05 г.
Пример 14. Предварительно отвешенные 1444,44 г 1-окси-4-адамантанона (39,0 мас. %), 74,00 г поливинилпирролидон (наполнитель) (2,0 мас. %) и 2050,00 г полиэтиленгликоля (пролонгирующий полимер) (55,3 мас. %) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве связывающего используем воду 111,00 г (3,0 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают диоксидом кремния (скользящее вещество), в количестве 25,90 г (0,7 мас. %). Полученный гранулят можно таблетировать или капсулировать. Получают таблетки по технологии или капсулы. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Опадрай 444,00 г (12,0 мас. % прирост массы таблетки после покрытия). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные таблетки или капсулы, с содержанием 1-окси-4-адамантанона 0,10 г, отвечают требованиям Государственной фармакопеи.
Пример 15. Предварительно отвешенные 150,00 г 1-окси-4-адамантанона (50,0 мас. %), 51,00 г картофельный крахмал (наполнитель) (17,0 мас. %) и 90,00 г этилакрилат (пролонгирующий полимер) (30,0 мас. %) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% спиртовым раствором ГПМЦ (связывающее вещество) смешивают в смесителе. Масса ГПМЦ в пересчете на чистое вещество составляет 6,00 г (2,0 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают диоксидом кремния (скользящее вещество), в количестве 3,0 г (1,0 мас. %). Полученный гранулят можно таблетировать или капсулировать. Полученные таблетки или капсулы, с содержанием 1-окси-4-адамантанона 0,15 г, отвечают требованиям Государственной фармакопеи.
Пример 16. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (20,0 мас %), 72,50 г декстрин (наполнитель) (29,0 мас %) и 90,00 г гидроксипропилцеллюлоза (пролонгирующий полимер) (36,0 мас %) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве смешивающего раствора выступает 15% водный раствор натрия альгината (связывающее вещество) смешивают в смесителе. Масса альгината натрия в пересчете на чистое вещество составляет 7,50 г (3,0 мас %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают магния стеаратом (скользящее вещество), в количестве 30,00 г (12,0 мас. %). Полученный гранулят можно таблетировать или капсулировать. Полученные таблетки или капсулы, с содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Пример 17. Предварительно отвешенные 1444,44 г 1-окси-4-адамантанона (39,0 мас. %), 74,00 г карбоксиметилцеллюлоза (наполнитель) (2,0 мас. %) и 2050,00 г гидроксиэтилцеллюлоза (пролонгирующий полимер) (55,3 мас. %) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве связывающего используем спирт этиловый 96% 111,00 г (3,0 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают диоксидом кремния (скользящее вещество), в количестве 25,90 г (0,7 мас. %). Полученный гранулят можно таблетировать или капсулировать. Получают таблетки по технологии или капсулы. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Опадрай 444,00 г (12,0 мас. % прирост массы таблетки после покрытия). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные таблетки или капсулы, с содержанием 1-окси-4-адамантанона 0,10 г, отвечают требованиям Государственной фармакопеи.
Пример 18. Получение фармацевтической композиции 1-окси-4-адамантанона осуществляют, смешивая 1000,00 г 1-окси-4-адамантанона (26,0 мас. %), 230,00 г кальция сульфат дигидрата (наполнитель) (6,0 мас. %), 1845,30 г кальция гидрофосфат дигидрата (наполнитель) (48,0 мас. %), 190,00 г метакриловой кислоты (пролонгирующий полимер) (5,0 мас. %) и 580,00 г диоксид кремния (скользящее вещество) (15,0 мас. %) в смесителе в течение 10-15 мин. Смесь порошков брикетируют на таблеточном или брикетировочном прессе (диаметр брикетов - от 12 мм до 50 мм). Полученные брикеты разламывают в грануляторе с размерами отверстий сетки 1,0-1,5 мм. Таблетирование производят на ротационном прессе фирмы «Киллиан». Диаметр пуансонов 10,0 мм. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Колликут® МАЕ 100 D 120,00 г (3,0 мас. % прироста массы таблетки после покрытия). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные твердые лекарственные формы, с содержанием 1-окси-4-адамантанона 0,10 г, отвечают требованиям Государственной фармакопеи.
Пример 19. Предварительно отвешенные 300,00 г 1-окси-4-адамантанона (50,0 мас. %), 144,00 г натриевая соль карбокси-метилцеллюлозы (наполнитель) (24,0 мас. %) и 120,00 г триметиламмониоэтилметакрилат (20,0 мас. %) (пролонгирующий полимер) перемешивают до получения однородной смеси и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор поливинилового спирта (связующее вещество) смешивают в смесителе. Масса поливинилового спирта в пересчете на чистое вещество составляет 12,00 г (2,0 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают диоксидом кремния (скользящее вещество), в количестве 12,0 г (4,0 мас. %). Полученный гранулят можно таблетировать или капсулировать. Получают таблетки по технологии или капсулы. Полученные таблетки ядра или капсулы покрывают полимерной пленочной оболочкой. В качестве пленкообразователя при производстве таблеток можно применять Опадрай 12,00 г (4,0 мас. % прирост массы таблетки после покрытия). Нанесение полимерной пленочной оболочки проводят в установке барабанного типа и прекращают по достижении необходимой массы. Полученные таблетки или капсулы, с содержанием 1-окси-4-адамантанона 0,30 г, отвечают требованиям Государственной фармакопеи.
Пример 20. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (25,0 мас. %), 67,00 г маннита (наполнитель) (33,5 мас. %) и 66,00 г пролонгирующего полимера (этилакрилат - 11,0 мас. %, гидроксиэтилцеллюлоза - 22,0 мас. %) до получения однородной смеси. Полученную порошковую смесь просеивают для достижения однородности смешивания и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор метилцеллюлозы и альгиновой кислоты (связывющее вещество) смешивают в смесителе. Масса в пересчете на чистое вещество составляет метилцеллюлозы 10,00 г (5 мас. %) и альгиновой кислоты 5,00 г (2,5 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают стеаратом магния (скользящее вещество), в количестве 2,00 г (1,0 мас. %). Полученный гранулят можно капсулировать в твердые желатиновые капсулы. Полученные капсулы, с содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Пример 21. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (25,0 мас. %), 67,00 г, редкосшитой полиакриловой кислоты (пролонгирующий полимер) (33,5 мас. %) и наполнителей 54,00 г (натриевой соли карбокси-метилцеллюлозы (11,0 мас. %) и сорбита (16,0 мас. %)) до получения однородной смеси. Полученную порошковую смесь просеивают для достижения однородности смешивания и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор карбоксиметилцеллюлозы (связывающее вещество) смешивают в смесителе. Масса карбоксиметилцеллюлозы в пересчете на чистое вещество составляет 15,00 г (7,5 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают диоксидом кремния (скользящее вещество), в количестве 14,00 г (7,0 мас. %). Полученный гранулят можно капсулировать в твердые желатиновые капсулы. Полученные капсулы, с содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Пример 22. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (26,0 мас. %), 67,00 г, гидроксиэтилцеллюлозы (пролонгирующий полимер) (34,8 мас. %) и наполнителей 66,00 г (гидроксипропилметилцеллюлозы (12,0 мас. %) и магния карбоната основного (22,3 мас. %)) до получения однородной смеси. Полученную порошковую смесь просеивают для достижения однородности смешивания и подвергают влажному гранулированию. В качестве связывающего раствора выступает 5% водный раствор оксипропилметилцеллюлозы (связывающее вество) смешивают в смесителе. Масса оксипропилметилцеллюлозы в пересчете на чистое вещество составляет 7,50 г (3,9 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают стеариновой кислотой (скользящее вещество), в количестве 2,00 г (1,0 мас. %). Полученный гранулят можно капсулировать в твердые желатиновые капсулы. Полученные капсулы, с содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Пример 23. Предварительно отвешенные 50,00 г 1-окси-4-адамантанона (25,0 мас. %), 67,00 г, редкосшитого акрилового полимера (пролонгирующий полимер) (33,5 мас. %) и наполнителей 66,00 г (амилопектина (11,0 мас. %) и алюмометосиликат магния (22,0 мас. %)) до получения однородной смеси. Полученную порошковую смесь просеивают для достижения однородности смешивания и подвергают влажному гранулированию. В качестве связывающего раствора выступает 10% водный раствор оксиэтилцеллюлозы (связующее вещество) смешивают в смесителе. Масса оксиэтилцеллюлозы в пересчете на чистое вещество составляет 15,00 г (7,5 мас. %). Увлажненную массу подвергают влажной грануляции. Влажный гранулят высушивают в сушильном шкафу в течение 2-3 часов при температуре 40-50°C или при комнатной температуре в течение 22-24 часов до остаточной влажности 2,0-3,0%. Высушенную массу гранул размалывают в грануляторе фирмы Erweka (Германия) с размером пор 1,0-1,5 мм. Массу сухого гранулята опудривают стеариновой кислотой (скользящее вещество), в количестве 2,00 г (1,0 мас. %). Полученный гранулят можно капсулировать в твердые желатиновые капсулы. Полученные капсулы, с содержанием 1-окси-4-адамантанона 0,05 г, отвечают требованиям Государственной фармакопеи.
Результаты теста «Растворение»
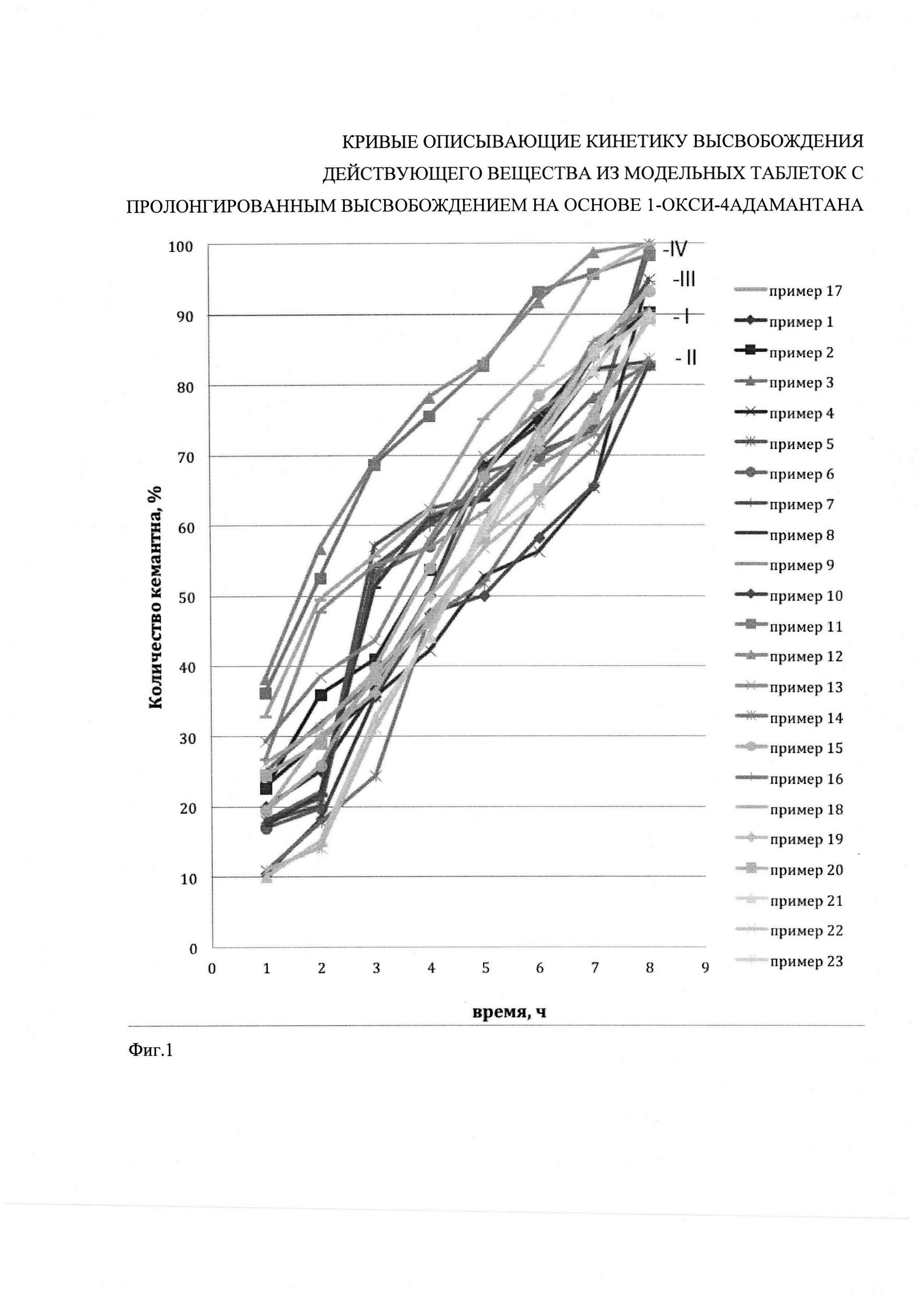
Одним из надежных и наиболее доступных инструментов, для характеристики биофармацевтического качества лекарственного средства in vitro, является тест «Растворение». Данный тест позволяет определить скорость растворения (высвобождения) фармацевтической субстанции из лекарственной формы. Таблетки с пролонгированным высвобождением - таблетки покрытые оболочкой или без оболочки, содержащие специальные вспомогательные вещества или полученные по особой технологии, что позволяет обеспечить замедленное непрерывное высвобождение фармацевтических субстанций. Соответственно, остальные критерии мы подбираем исходя из оптимальности их применения в индивидуальной терапевтической практике; 1-окси-4-адамантанон относится к лекарственному средству с небольшим периодом полувыведения и хорошо растворим/проницаем, следовательно необходим подбор матрикса (пролонгирующего полимера), так как при использовании других способов задержки высвобождения (оболочки и тд.) 1-окси-4-адамантанон быстро высвободит всю дозировку в начальных отделах кишечника и за счет высокой проницаемости вся эта дозировка сразу всосется. А это создает не столько пролонгированный сколько отсроченный (то есть вся доза, но через 2 часа, а не постепенно за 8). В данном случае, пролонгирование - способность обеспечить непрерывное высвобождение 1-окси-4-адамантанона за 8 часов, что подтверждается кривыми высвобождения (фиг. 1).
Тест «Растворение» заявленной фармацевтической композиции пролонгированного действия показал значения, представленные в таблицах 2-5. Результаты получены по примерам фармацевтической композиции, описанных выше, более наглядно отображены на фигуре 1 (кривые соответствуют примерам, указанным справа на чертеже). Как видно из кинетики высвобождения, 1-окси-4-адамантанон постепенно высвобождается из таблеток, на представленной фигуре 1 видны различные основные четыре группы, разница значения теста «Растворение» внутри каждой группы статистически незначимая, на основании разного количества высвободившегося 1-окси-4-адамантанона выделили четыре основные группы: I группа 89,72±1,02%; II группа 83,03±1,25%; III группа 94,99±1,66%;IV группа 99,34±1,03%, результаты представлены в таблице 2., таблице 3., таблице 4. и таблице 5. Наблюдается равномерное высвобождение 1-окси-4-адамантанона внутри каждой группы (таблицы 2, 3, 4, 5), а так как 1-окси-4-адамантанона обладает хорошей растворимостью и биодоступностью [Кисляк Н.А. Создание твердых дозированных лекарственных форм производных адамантана/диссертация на соискание ученой степени кандидата фарм. наук/М. - 1989. - с. 168], следовательно, и результаты тестов in vivo дадут примерно одинаковый результат, для экономии экспериментов in vivo взяли по одному примеру из каждой группы. [A.H. Мымриков In vitro - in vivo корреляция: от теории к практике/Провизор. - 2008. - №2]
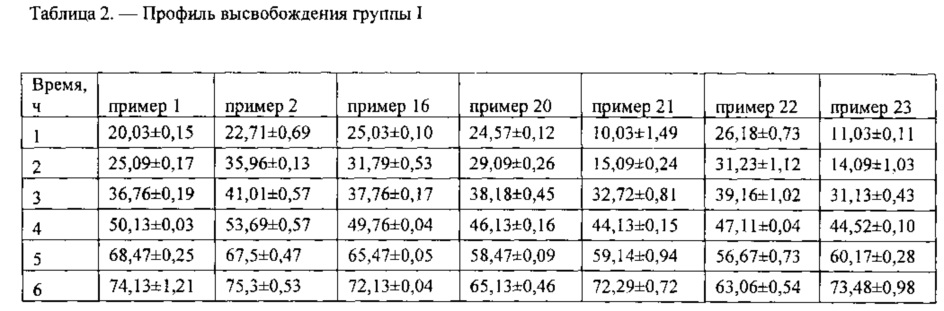

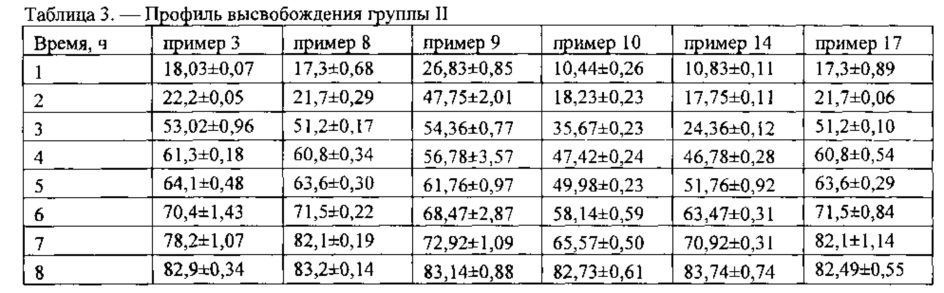
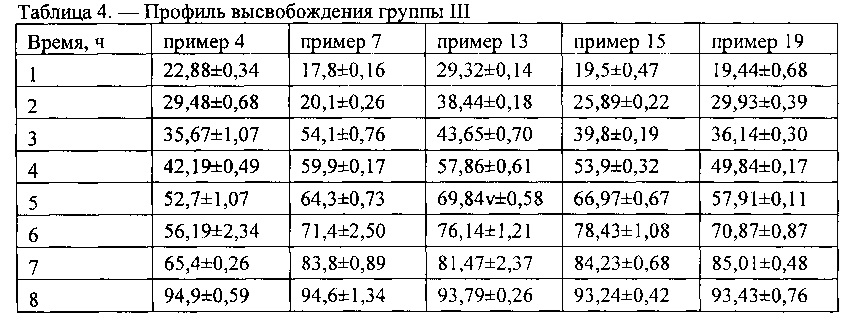
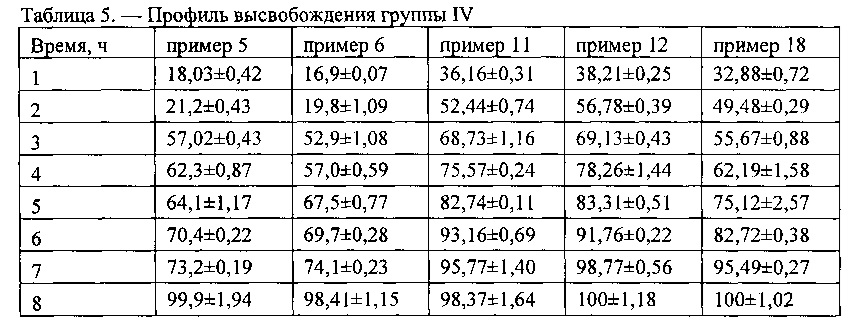
Все представленные составы фармацевтической композиции на основе 1-окси-4-адамантана соответствуют требованиям Государственной Фармакопеи XII к фармацевтическим композициям пролонгированного действия (табл. 1.), постепенно высвобождая фармацевтическую субстанцию, за первый час эксперимента значения превышающие 30,0% высвобождения фармацевтической субстанции показала только одна группа, содержащая рН-независимого пролонгирующего полимера менее 10%, однако результаты не превышали 40,0%. [Фармацевтическая технология таблетки: учебное пособие/ под ред. С.А. Кедика. - М.: ЗАО ИФТ, 2015. - 672 с.].
Проведенные исследования показали, что только определенные, показанные в примерах изготовления лекарственных форм, вспомогательные вещества в соответствующих соотношениях подходят для создания фармацевтической композиции на основе 1-окси-4-адамантанона с пролонгированным высвобождением, так как для каждая фармацевтическая субстанция обладает индивидуальным набором технологических и физико-химических параметров, которые необходимо учитывать при создании лекарственной формы для того, обеспечить оптимальное непрерывное пролонгированное высвобождение. Мы добились поддержания терапевтической концентрации 1-окси-4-адамантанона в крови животных и компенсации флуктуаций его концентрации благодаря оптимальному составу фармацевтической композиции с пролонгированным высвобождением, в состав которых входил хотя бы один из следующих пролонгирующих полимеров: этилцеллюлоза, гидроксипропилцеллюлоза, гидроксипропилметилцеллюлоза, гидроксиэтилцеллюлоза; редкосшитые акриловые полимеры, метакриловая кислота, этилакрилат, триметиламмониоэтилметакрилат и их сополимеры; полиэтиленгликоли, выполненных в твердых лекарственных формах, обеспечивающих профиль высвобождения, представленный на фигуре 1.
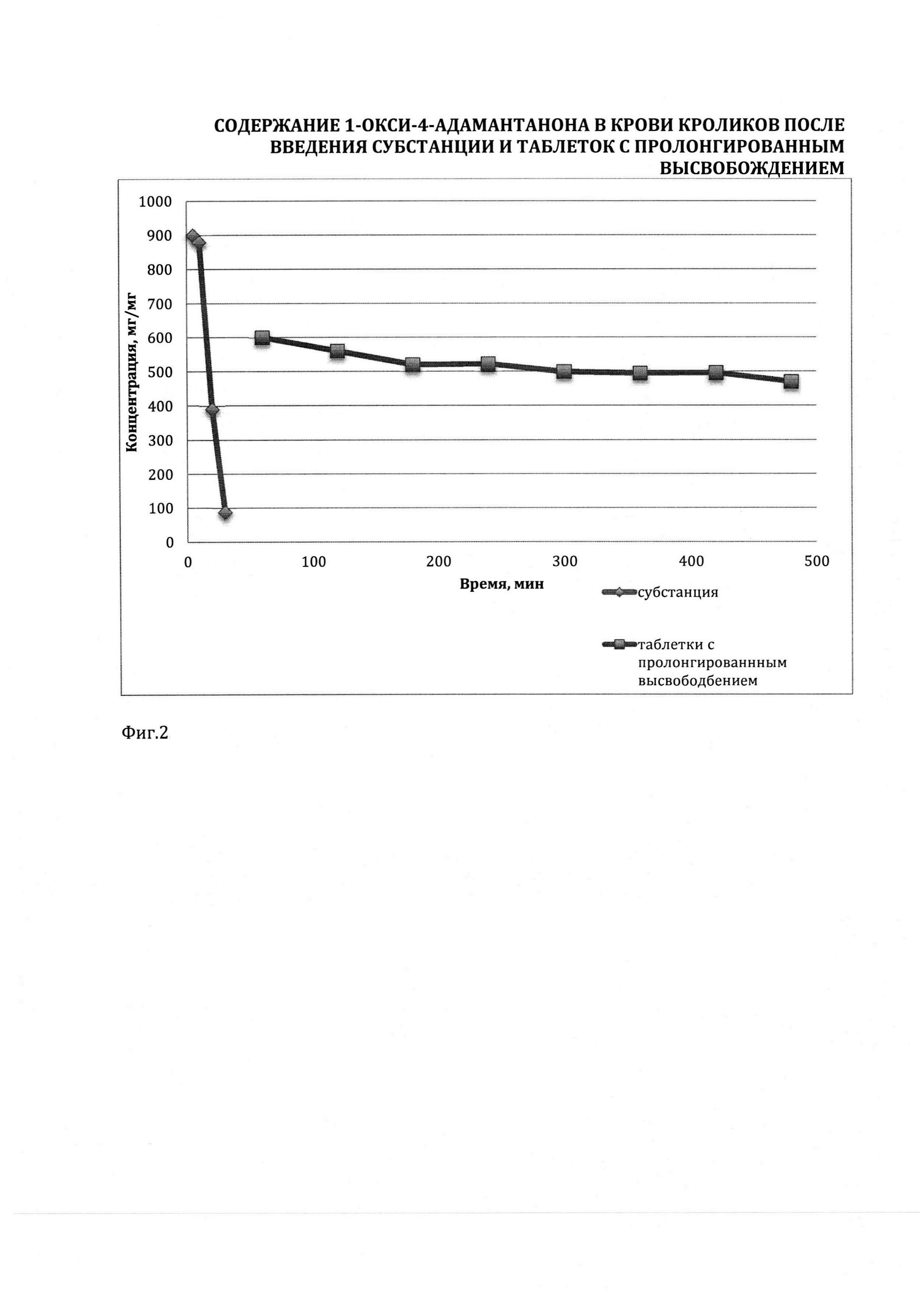
Изучив фармакокинетику мы получили результат, представленный на фигуре 2, позволяющий заключить, что время нахождения 1-окси-4-адамантанона и его действующего метаболита в организме значительно увеличивается при введении пролонгированной лекарственной формы, по сравнению со временем нахождения в организме введенной перорально в желатиновой капсуле непосредственно фармацевтической субстанции 1-окси-4-адамантанон.
Изучение эффективности фармацевтической композиции пролонгированного действия на основе 1-окси-4-адамантанона на модели глобальной ишемии мозга.
Известно, что при внутрибрюшинном введении 1-окси-4-адамантанона в дозах 50-100-150-200 мг/кг оказывает влияние на локальный кровоток ишемизированного мозга. [Мирзоян Р.С. Производное адамантона усиливает кровоснабжение ишемизированного мозга / Мирзоян Р.С. и др. // экспериментальная и клиническая фармакология. - 2012.- №75(6). - стр. 7-30.]
Фармакодинамическую активность изучали с использованием фармацевтической композиции пролонгированного действия на основе 1-окси-4-адамантанона, изготовленной по примерам 1, 7, 10 и 12 соответствующих всем приведенным показателям качества. Опыты выполнены на 160 наркотизированных (в дозе 250 мг/кг, перорально через зонд) нелинейных крысах-самцах массой 180-400 г, животные содержались в стандартных условиях и корме.
Состояние мозгового кровообращения у животных оценивали с помощью методики лазерной допплеровской флоуметрии. Для регистрации локального мозгового кровотока в теменной области коры головного мозга крыс использовали флоуметр ALF-21 фирмы "Transonic System Inc." (США). Игольчатый датчик флоуметра диаметром 0,8 мм устанавливали на теменной области коры большого мозга крысы с помощью микроманипулятора и коромысла. Одновременно регистрировали изменения артериального давления через предварительно введенный в бедренную артерию полиэтиленовый катетер. На основании данных датчиков кровотока и давления в реальном времени рассчитывал сопротивление сосудов. Запись показателей кровотока, артериального давления и сопротивления сосудов производили на полиграфе фирмы «BIOPAK» (США), соединенным с персональным компьютером. Исследуемое вещество вводили через полиэтиленовый катетер в бедренную вену животных.
Глобальную преходящую ишемию у крыс вызывали 10-минутной окклюзией обеих общих сонных артерий с одновременным снижением артериального давления до 40-50 мм рт.ст. методом кровопускания с последующей реинфузией. В работе также изучали влияние фармацевтической композиции с пролонгированным высвобождением на основе 1-окси-4-адамантанона на выживаемость животных в условиях гравитационных перегрузок. Для этого бодрствующих крыс помещали в специальные контейнеры центрифуги в краниокаудальном направлении относительно вектора ускорений. Скорость нарастания перегрузок составляла 40-50 с. При краниокаудальном векторе ускорений (9g в течение 12 мин) происходит перемещение крови в каудальном направлении, и в результате резкого и значительного снижения перфузионного давления во всех сосудах головы до нулевого уровня развивается ишемия мозга.
Статистическую обработку данных проводили с использованием пакета программ Statistika 8,0 (Statistika Inc., США). Нормальность распределения проверяли с помощью критерия Шапиро-Уилка. В основном нормальное распределение отсутствовало, поэтому для дальнейшей обработки данных использовали непараметрический метод Уилкоксона для связанных выборок. Данные по выживаемости животных в условиях циркуляторной ишемии оценивали с помощью критерия Фишера. Результаты рассматривали как значимые при р<0,05.
Далее было изучено влияние фармацевтической композиции пролонгированного действия на основе 1-окси-4-адамантанона на кровоснабжение мозга крыс после глобальной преходящей ишемии. Опыты показали, что фармацевтическая композиция пролонгированного действия на основе 1-окси-4-адамантанона в дозе 100 мг/кг при пероральном введении с применением зонда вызывает медленно развивающееся увеличение локального мозгового кровотока, которое достигает своих максимальных значений для композиции по примеру 1 - к 360 минуте достигает максимального (78,0%), для композиции по примеру 7 - к 376-ой минуте (79,0%), для композиции по примеру 10 - к 320-ой минуте (86,4%), для композиции по примеру 12 - к 280-ой минуте (89,4%). Кровоток сохраняется выше исходного уровня до конца эксперимента (480 минут). Уровень артериального давления под влиянием фармацевтической композиции пролонгированного действия на основе 1-окси-4-адамантанона у крыс в условиях ишемического поражения мозга снижается в среднем на 11%.
Таким образом, проведенное исследование позволило установить, что цереброваскулярный эффект фармацевтической композиции пролонгированного действия на основе 1-окси-4-адамантанона проявляется в условиях ишемического поражения мозга; следует отметить, что увеличение кровотока под влиянием препарата обусловлено понижением тонуса сосудов мозга, так как 1-окси-4-адамантанон наряду с увеличением мозгового кровотока понижает уровень артериального давления.
Изучение действия фармацевтической композиции на основе 1-окси-4-адамантанона в опытах на крысах в условиях гравитационных перегрузок
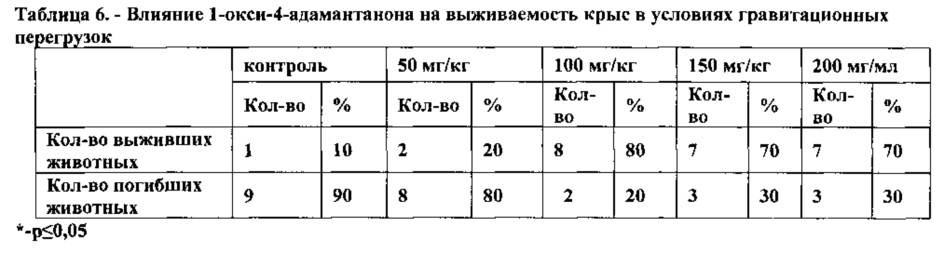
Противоишемические свойства фармацевтической композиции (примеры 1, 3, 11, 15) на основе 1-окси-4-адамантанон с пролонгированным высвобождением были изучены и в опытах на бодрствующих крысах в условиях гравитационных перегрузок при пероральном введении с помощью зонда. Опыты показали, что в контроле от гравитационных перегрузок погибает 90% животных, т.е. выживает 10%. После введения фармацевтической композиции с пролонгированным высвобождением на основе 1-окси-4-адамантанона в дозе 100 мг/кг (пример 3) выживаемость возрастает до 80% (табл. 6). В дозах 150-200 мг/кг (пример 15 и 1) выживаемость крыс составляет 70%, при отсутствии статистически значимых различий между контрольной и опытной группами. Следовательно, 1-окси-4-адамантанон при ишемическом поражении мозга вследствие гравитационных перегрузок проявляет свои противоишемические свойства, как и при глобальной преходящей ишемии.
Изучение фармакокинетики фармацевтической композиции с пролонгированным высвобождением на основе 1-окси-4-адамантанона, по полученным примерам 1, 3, 11, 15, проводили на 5 кроликах-самках массой 2-3 кг. Отбор крови у животных осуществляли через боковую вену через 5, 10, 20, 30, 45, 60, 120 и 180 минут после введения препарата. В качестве стандартной лекарственной формы использовали субстанцию, заключенную в желатиновую капсулу. Таблетки с пролонгированным высвобождением вводили животным с помощью зонда, время отбора проб 60, 120, 180, 240, 300, 360, 420, 480 минут после введения фармацевтической композиции. Введение полученных примеров 1, 3, 11, 15 фармацевтической композиции с пролонгированным высвобождением производили каждому животному последовательно с интервалом 2 недели.
При изучении полученных результатов концентраций 1-окси-4-адамантанона можно заключить, что он быстро всасывается и определяется в крови уже через 5 минут после введения субстанции. В течение последующих 30 минут его концентрация быстро снижается в соответствии с кинетикой первого порядка. Таким образом, время присутствия 1-окси-4-адамантанона в крови весьма ограничено. Начиная с 5 минут после введения субстанции, в крови определяется метаболит 1-окси-4-адамантанона-1,4-адамантандиол, концентрация которого достигает максимальных значений через 30-45 минут. Время определения 1,4-адамантандиола в крови животных - 3 часа после введения (Фиг. 2). Таблетки с пролонгированным высвобождением при отборе проб каждый час показывают, что концентрация 1-окси-4-адамантанона поддерживается на протяжении всего времени проведения эксперимента. На фигуре 2 показано, что фармацевтическая композиция с пролонгированным высвобождением обеспечивает непрерывное и равномерное высвобождение 1-окси-4-адамантанона на протяжении 8 часов.
Относительная биологическая доступность 1-окси-4-адамантанона в таблетках с пролонгированным высвобождением, выраженная процентным соотношением суммарных площадей под фармакокинетическими кривыми 1-окси-4-адамантанона и его активного метаболита равна 98,7%.
Описание чертежей.
Фиг. 1. Профиль высвобождения 1-окси-4-адамантанона из фармацевтической композиции с пролонгированным высвобождением, приготовленной по примерам 1-23, соответствующим представленным примерам справа. По оси абсцисс - часы теста «Растворение»; по оси ординат - количество 1-окси-4-адамантанона перешедшего в раствор из таблеток, выраженное в %. Кривые соответствуют примерам указанным справа на чертеже. Из кинетики высвобождения видно постепенное высвобождение 1-окси-4-адамантанона. На диаграмме видны различные основные четыре группы, разница значения теста «Растворение» внутри каждой группы статистически незначимая, результаты представлены в таблице 2., таблице 3., таблице 4. и таблице 5. В связи с этим для экономии экспериментов in vivo, все примеры разделены на четыре группы со статистически различными значениями. [A.H. Мымриков In vitro - in vivo корреляция: от теории к практике/Провизор. - 2008. - №2]
На фиг. 2 Содержание 1-окси-4-адамантанона в крови кроликов после введения таблеток с пролонгированнным высвобождением и субстанции, показано изменение содержания кемантана в крови кроликов после введения субстанции 1-окси-4-адамантанона и таблеток с пролонгированным высвобождением на основе 1-окси-4-адамантанона. Ось абсцисс - время, в течение которого проводилось количественное определение кемантана в крови кроликов (минуты); ось ординат - концентрация кемантана в крови кроликов (мг/мг). Время отборы проб для субстанции 5, 10, 20 и 30 минут; время отбора проб для таблеток 60, 120, 180, 240, 300, 360, 420, 480 минут. Изучив фармакокинетику мы получили результат, представленный на фигуре 2, позволяющий заключить, что время нахождения 1-окси-4-адамантанона и его действующего метаболита в организме значительно увеличивается при введении пролонгированной лекарственной формы, по сравнению со временем нахождения в организме введенной перорально в желатиновой капсуле непосредственно фармацевтической субстанции 1-окси-4-адамантанон.