ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА
Вид РИД
Изобретение
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Для получения формы твердого орально-доставляемого фармацевтического соединения требуется обеспечить целый ряд определенных характеристик. Хотя может быть создана аморфная форма фармацевтического соединения, в целом предпочтительны соединения, имеющие высокую степень кристалличности. Часто такие высоко кристаллические соединения - это соли.
Международная Публикация WO 2004/046092 описывает ряд соединений, которые определены как антагонисты CCR9 рецептора, и которые, как указано, используются при лечении CCR9-опосредованных нарушений. В частности, в этой заявке раскрыто соединение 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамид. Идентификация устойчивой кристаллической формы такого соединения с подходящими свойствами для орального введения была бы очень желательна для лечения CCR9-опосредованных заболеваний.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к новым полиморфным сольватированным или несольватированным формам натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (здесь и далее "Соединение А"). Соединение по изобретению представлено Структурой (I):
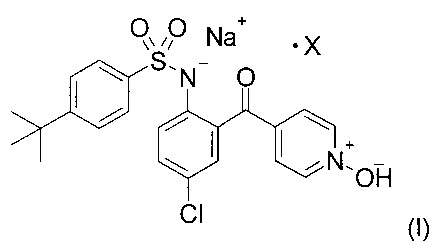
В частности, это соединения, в которых X - растворитель или смесь растворителей, такие как 1,4-диоксан/вода, формамид, диметилсульфоксид, или вода, или где X отсутствует.
Соединения этого изобретения используется для противодействия CCR9 рецептору и для лечения заболеваний, таких как воспалительные заболевания кишечника, включая заболевания Крона и язвенный колит.
КРАТКОЕ ОПИСАНИЕ РИСУНКОВ
Фиг. 1 показывает рентгеновскую порошковую дифракционную структуру Соединения А - сольвата 1,4-диоксан/вода.
Фиг. 2 показывает рентгеновскую порошковую дифракционную структуру Соединения А - сольвата диметилсульфоксида.
Фиг. 3 показывает рентгеновскую порошковую дифракционную структуру Соединения А - диметилсульфоксидного сольвата.
Фиг. 4 показывает рентгеновскую порошковую дифракционную структуру 10 Соединения А - несольватированной кристаллической формы.
Фиг. 5 показывает рентгеновскую порошковую дифракционную структуру Соединения А - гидрата.
Фиг. 6 показывает Спектр Рамана Соединения А сольвата 1,4-диоксан/вода.
Фиг. 7 показывает Спектр Рамана Соединения А - формамидного сольвата.
Фиг. 8 показывает Спектр Рамана Соединения А - диметилсульфоксидного сольвата.
Фиг. 9 показывает Спектр Рамана Соединения А - несольватированной кристаллической формы.
Фиг. 10 показывает след дифференциальной сканирующей калориметрии Соединения А - сольвата 1,4-диоксан/вода.
Фиг. 11 показывает след дифференциальной сканирующей калориметрии Соединения А - сольвата формамида.
Фиг. 12 показывает след дифференциальной сканирующей калориметрии Соединения А диметилсульфоксидного сольвата.
Фиг. 13 показывает след дифференциальной сканирующей калориметрии Соединения 25 А несольватированной кристаллической формы.
Фиг. 14 показывает след термогравиметрического анализа Соединения А - сольвата 1,4-диоксан/вода.
Фиг. 15 показывает след термогравиметрического анализа Соединения А - сольвата формамида.
Фиг. 16 показывает след термогравиметрического анализа Соединения А - диметилсульфоксидного сольвата.
Фиг. 17 показывает след термогравиметрического анализа Соединения А несольватированной кристаллической формы.
Фиг. 18 показывает след термогравиметрического анализа Соединения А - гидрата.
ДЕТАЛИЗИРОВАННОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
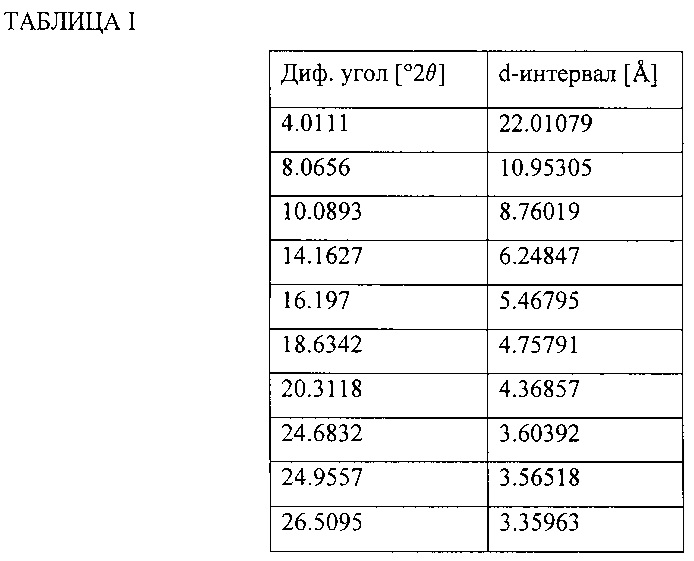
Настоящее изобретение направлено на новые полиморфные сольватированные и несольватированные формы натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида. Одно воплощение настоящего изобретения направлено на кристаллическую натриевую соль 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (в дальнейшем, "Соединение А - сольват 1,4-диоксан/вода"), в которой кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой, включающей углы дифракции (°2θ) при измерении с использованием CuKα излучения, в приблизительно 4.0, 8.1, 10.1, 14.2, 16.2, 18.6, 20.3, 24.7, 25.0 и 26.5.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват 1,4-диоксан/вода, в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой по существу в соответствии с Фиг. 1.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват 1,4-диоксан/вода, в котором кристаллическая форма обеспечивает Спектр Рамана, содержащий пики в приблизительно 668, 743, 804, 1125, 1154, 1162, 1286, 1544, 1587, 1597, 1611, 1657 и 1672 см-1.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват 1,4-диоксан/вода, в которой кристаллическая форма обеспечивает Спектр Рамана по существу в соответствии с Фиг. 6.
Другое воплощение настоящего изобретения направлено на Соединение сольват 1,4-диоксан/вода, в котором кристаллическая форма обеспечивает след дифференциальной сканирующей калориметрии по существу в соответствии с Фиг. 10 и/или след термогравиметрического анализа по существу в соответствии с Фиг. 14.
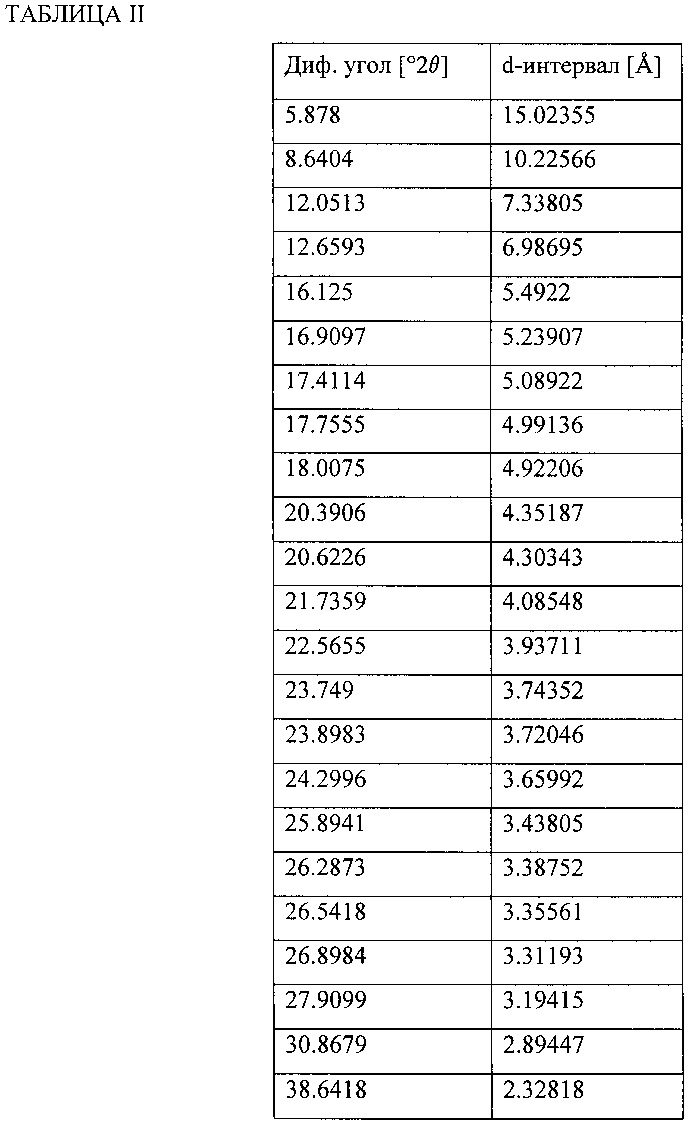
Другое воплощение настоящего изобретения направлено на кристаллическую натриевую соль 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (в дальнейшем, "Соединение А - сольват формамида"), в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой, включающей углы дифракции (°2θ) при измерении с использованием CuKα излучения в приблизительно 5.9, 8.6, 12.1, 12.7, 16.1, 16.9, 17.4, 17.8, 18.0, 20.4, 20.6, 21.7, 22.6, 23.7, 23.9, 24.3, 25.9, 26.3, 26.5, 26.9, 27.9, 30.9 и 38.6.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват формамида, в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой по существу в соответствии с Фиг. 2.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват формамида, в котором кристаллическая форма обеспечивает Спектр Рамана, содержащий пики в приблизительно 655, 668, 737, 804, 1079, 1099, 1123, 1161, 1229, 1303, 1465, 1537, 1595, 1611 и 1654 см-1.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват формамида, в котором кристаллическая форма обеспечивает Спектр Рамана по существу в соответствии с Фиг. 7.
Другое воплощение настоящего изобретения направлено на Соединение А - сольват формамида, в котором кристаллическая форма обеспечивает след дифференциальной сканирующей калориметрии по существу в соответствии с Фиг. 11 и/или след термогравиметрического анализа по существу в соответствии с Фиг. 15.
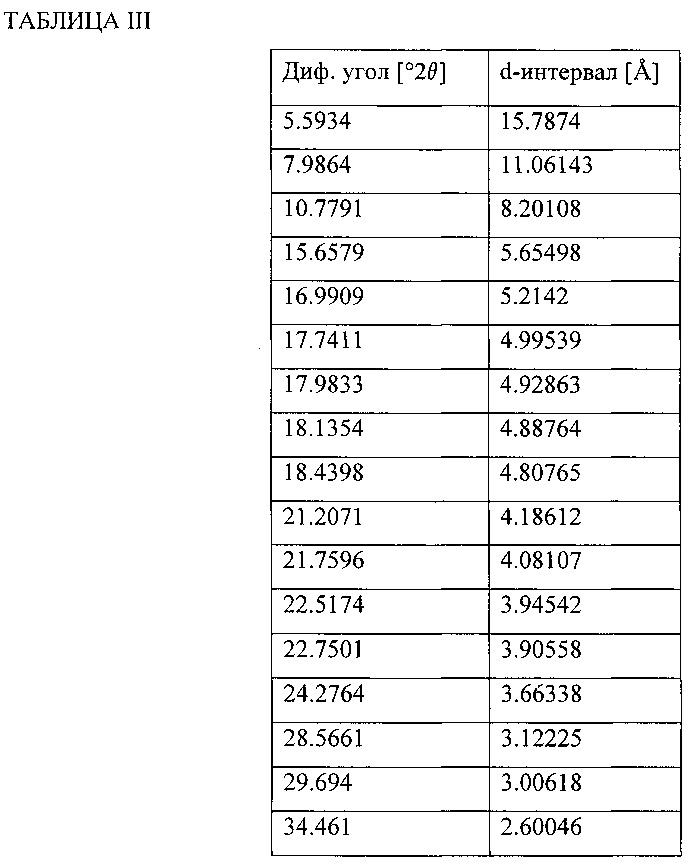
Другое воплощение настоящего изобретения направлено на кристаллическую натриевую соль 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (в дальнейшем, "Соединение А - диметилсульфоксид сольват"), в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой, включающей углы дифракции (°2θ), при измерении с использованием CuKα излучения, в приблизительно 5.6, 8.0, 10.8, 15.7, 17.0, 17.7, 18.0, 18.1, 18.4, 21.2, 21.8, 22.5, 22.8, 24.3, 28.6, 29.7 и 34.5.
Другое воплощение настоящего изобретения направлено на Соединение А - диметилсульфоксид сольват, в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой по существу в соответствии с Фиг. 3.
Другое воплощение настоящего изобретения направлено на Соединение А - диметилсульфоксид сольват, в котором кристаллическая форма обеспечивает Спектр Рамана, содержащий пики в приблизительно 662, 672, 718, 729, 750, 799, 1078, 1109, 1158, 1236, 1302, 1536, 1588, 1596 и 1636 см-1.
Другое воплощение настоящего изобретения направлено на Соединение А - диметилсульфоксид сольват, в котором кристаллическая форма обеспечивает Спектр Рамана по существу в соответствии с Фиг. 8.
Другое воплощение настоящего изобретения направлено на Соединение А - диметилсульфоксид сольват, в котором кристаллическая форма обеспечивает след дифференциальной сканирующей калориметрии по существу в соответствии с Фиг. 12 и/или след термогравиметрического анализа по существу в соответствии с Фиг. 16.
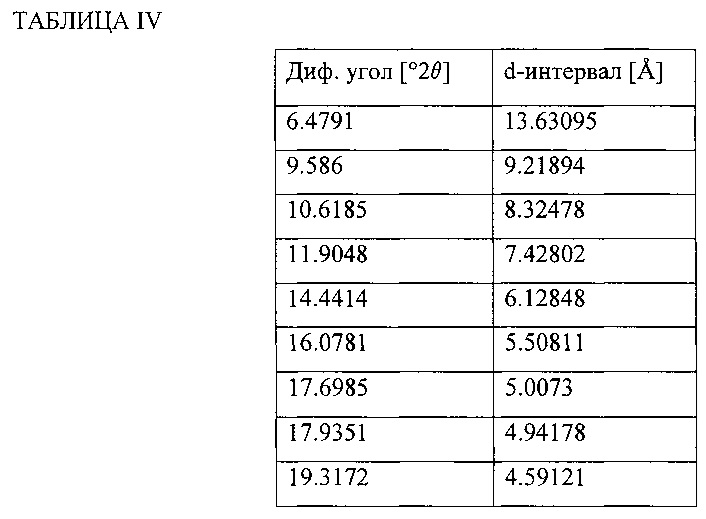
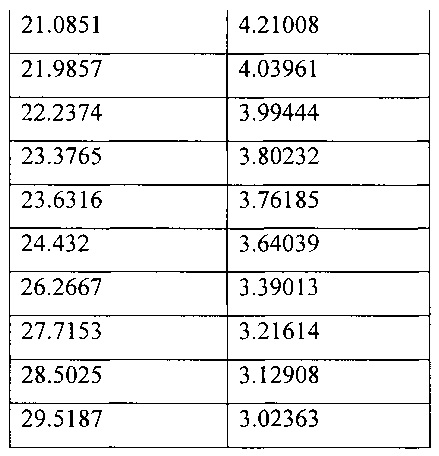
Другое воплощение настоящего изобретения направлено на кристаллическую натриевую соль 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (в дальнейшем, "Соединение А - несольватированная кристаллическая форма"), в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой, включающей углы дифракции (°2θ), при измерении с использованием CuKα излучения, в приблизительно 6.5, 9.6, 10.6, 11.9, 14.4, 16.1, 17.7, 17.9, 19.3, 21.1, 22.0, 22.2, 23.4, 23.6, 24.4, 26.3, 27.7, 28.5 и 29.5.
Другое воплощение настоящего изобретения направлено на Соединение А - несольватированная кристаллическая форма, в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой по существу в соответствии с Фиг. 4.
Другое воплощение настоящего изобретения направлено на Соединение А - несольватированная кристаллическая форма, в котором кристаллическая форма обеспечивает Спектр Рамана, содержащий пики в приблизительно 654, 667, 737, 803, 855, 1077, 1122, 1160, 1311, 1461, 1536, 1592, 1609 и 1648 см-1.
Другое воплощение настоящего изобретения направлено на Соединение А - несольватированная кристаллическая форма, в котором кристаллическая форма обеспечивает Спектр Рамана в основном по существу с Фиг. 9.
Другое воплощение настоящего изобретения направлено на Соединение А - несольватированная кристаллическая форма, в котором кристаллическая форма обеспечивает след дифференциальной сканирующей калориметрии по существу в соответствии с Фиг. 13 и/или след термогравиметрического анализа по существу в соответствии с Фиг. 17.
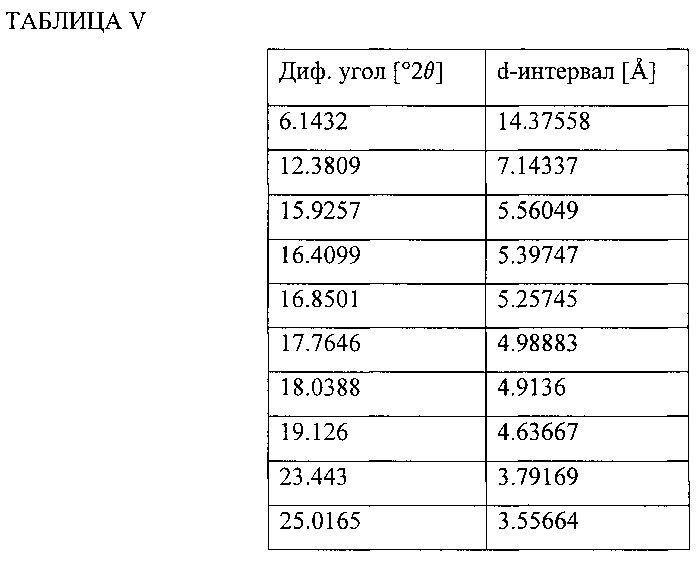
Другое воплощение настоящего изобретения направлено на кристаллическую натриевую соль 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (в дальнейшем, "Соединение А - гидрат"), в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой, включающей углы дифракции (°2θ), при измерении с использованием CuKα излучения, в приблизительно 6.1, 12.4, 15.9, 16.4, 16.9, 17.8, 18.0, 19.1, 23.4 и 25.0.
Другое воплощение настоящего изобретения направлено на Соединение А - гидрат, в котором кристаллическая форма характеризуется рентгеновской порошковой дифракционной структурой по существу в соответствии с Фиг. 5.
Другое воплощение настоящего изобретения направлено на Соединение А - гидрат, в котором кристаллическая форма обеспечивает след термогравиметрического анализа по существу в соответствии с Фиг. 18.
Известно и понятно специалистам в отрасли, что используемые приборы, влажность, температура, ориентация кристаллов порошка и другие параметры, имеющие место при получении рентгеновской порошковой дифракционной (XRPD) структуры, могут вызвать некоторую изменчивость во внешнем виде, интенсивностях и положениях линий в дифракционной структуре. Рентгеновская порошковая дифракционная структура, которая является, по существу, в соответствии с той, которая обеспечена здесь фигурами 1, 2, 3, 4 или 5, - это XRPD структура, которая, как полагают специалисты в данной области, представляет соединение, обладающее той же самой кристаллической формой, как соединение, которое обеспечила XRPD структура Фиг. 1, 2, 3, 4 или 5. Таким образом, XRPD структура может быть идентичной структуре из Фиг. 1, 2, 3, 4 или 5, или, более вероятно, она может быть несколько отличной. Такая XRPD структура не обязательно может показывать каждую из линий дифракционной структуры, представленной здесь, и/или может показывать небольшое изменение по внешности, интенсивности или сдвиге в положении упомянутых линий, следующих из различий в условиях, включаемых при получении данных. Специалист способен определить, имеет ли образец кристаллического соединения ту же самую форму или отличную от формы, раскрытой здесь, сравнением их XRPD структур. Например, специалист в данной области может совместить образец XRPD структуры натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида с Фиг. 1 и, используя экспертизу и знания в области техники, легко определить, является ли XRPD структура образца, по существу, в соответствии с XRPD структурой Соединения А - сольват 1,4 диоксан/вода. Если XRPD структура в основном соответствует Фиг. 1, форма образца может быть легко и точно идентифицирована как та же самая, что у Соединения А - сольват 1,4 диоксан/вода. Точно также специалист способен определить, находится ли данный угол дифракции (выраженный в °2θ), полученный из XRPD структуры, в приблизительно том же самом положении, как значение, представленное здесь.
"Соединение изобретения" означает натриевую соль 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида, в частности, кристаллические формы, определенные здесь как Соединение А - 1,4 диоксан/вода сольват, Соединение А - формамид сольват, Соединение А - несольватированная кристаллическая форма и Соединение А - гидрат.
Изобретение включает терапевтический метод лечения или улучшения CCR9-опосредованного нарушения в субъекте, который нуждается в этом, включающий введение нуждающемуся субъекту эффективного количества соединения изобретения или композиции, включающей эффективное количество соединения изобретения и дополнительно фармацевтически приемлемый носитель.
Как здесь используется, фраза "CCR9-опосредованное нарушение" и связанные фразы и термины относятся к состоянию или заболеванию, характеризующемуся несоответствующим, то есть, меньше чем или больше чем нормальная CCR9 функциональная активность. Несоответствующая CCR9 функциональная активность может возникнуть как результат CCR9 экспрессии в клетках, которые обычно не выражают CCR9, увеличения CCR9 экспрессии (приводящей к, например, воспалительным и иммунорегуляторным расстройствам и заболеваниям) или уменьшения CCR9 экспрессии. Несоответствующая CCR9 функциональная активность может также возникнуть как результат ТЕСК секреции клетками, которые обычно не секретируют ТЕСК, увеличенной ТЕСК секреции (приводящей, например, к воспалительным и иммунорегуляторным расстройствам и заболеваниям) или уменьшения ТЕСК экспрессии. CCR9-опосредованное нарушение может быть полностью или частично модулировано несоответствующей CCR9 функциональной активностью. Однако, CCR9-опосредованное нарушение - это то, в котором CCR9 модуляция приводит к некоторому влиянию на основное состояние или заболевание (например, CCR9 антагонист приводит к некоторому улучшению пациента, имеющему место, по крайней мере, у некоторых пациентов).
"Эффективное количество" означает то количество вещества препарата (то есть соединения настоящего изобретения), которое проявляет желательный биологический ответ в субъекте. Такой ответ включает облегчение признаков заболевания или нарушения, которые подвергаются лечению. Эффективное количество соединения изобретения в таком терапевтическом методе - приблизительно 0.001-100 мг на кг массы тела пациента в сутки, которое можно вводить в единственной или многократных дозах. Предпочтительно, уровень дозировки будет приблизительно 0.01 - приблизительно 25 мг/кг в сутки; более предпочтительно приблизительно 0.05 - приблизительно 10 мг/кг в сутки. Подходящий уровень дозировки может быть приблизительно 0.01-25 мг/кг в сутки, приблизительно 0.05-10 мг/кг в сутки или приблизительно 0.1-5 мг/кг в сутки. В пределах этого диапазона дозировка может составлять 0.005-0.05, 0.05-0.5, 0.5-5.0 или 5.0-50 мг/кг в сутки.
Для орального введения композиции предпочтительно обеспечиваются в форме таблеток, содержащих 1.0-1000 миллиграммов активного ингредиента, особенно 1.0, 5.0, 10.0, 15.0, 20.0, 25.0, 50.0, 75.0, 100.0, 150.0, 200.0, 250.0, 300.0, 400.0, 500.0, 600.0, 750.0, 800.0, 900.0 и 1000.0 мг активного ингредиента для симптоматического регулирования дозировки пациенту, которого лечат. Соединения можно вводить в режиме 1-4 раза в сутки, предпочтительно, несколько раз в сутки.
Должно быть понятно, однако, что определенный уровень дозы и частота дозировки для любого конкретного пациента могут быть различны и будут зависеть от разнообразия факторов, включая возраст, массу тела, наследственные особенности, общее здоровье, пол, диету, способ и время введения, скорости выделения, комбинации препаратов и характера и серьезности конкретного состояния, которое лечат.
Методы введения включают введение эффективного количества соединения или композиции изобретения в разное время в течение курса лечения или одновременно в комбинированной форме. Методы изобретения включают все известные терапевтические режимы лечения.
Заболевания и состояния, связанные с воспалением, иммунными нарушениями, инфекцией и раком, можно лечить или предотвращать настоящими соединениями, композициями и методами.
В одной группе воплощений заболевания или состояния, включая хронические заболевания людей или других разновидностей, можно лечить ингибитором CCR9 функции. Эти заболевания или состояния включают: (1) аллергические заболевания, такие как системная анафилаксия или реакции гиперчувствительности, аллергии на лекарства, аллергии на ужаливание насекомого и пищевые аллергии, (2) воспалительные заболевания кишечника, такие как заболевание Крона, язвенный колит, илеит и энтерит, (3) вагиниты, (4) псориаз и воспалительный дерматоз, такой как дерматит, экзема, атопический дерматит, аллергический контактный дерматит, крапивница и зуд, (5) васкулит, (6) спондилоартропатия, (7) склеродерма, (8) астма и дыхательные аллергические заболевания, такие как аллергическая астма, аллергический ринит, заболевания гиперчувствительности легких и т.п., (9) аутоиммунные заболевания, такие как фибромиалгия, склеродерма, анкилозный спондилит, юнвенильный РА, заболевание Стилла, полисуставной ювенильный РА, пауциартикулярный ювенильный РА, полимиалгия ревматическая, ревматоидный артрит, псориатический артрит, остеоартрит, полисуставной артрит, рассеянный склероз, системная волчанка, диабет типа I, диабет типа II, гломерулонефрит и т.п., (10) отторжение имплантата (включая отторжение аллотрансплантата), (11) заболевание протез - против - хозяина (включая и острое, и хроническое), (12) другие заболевания, в которых нежелательные воспалительные реакции должны замедляться, такие как атеросклероз, миозит, нейродегенеративные заболевания (например, болезнь Альцгеймера), энцефалит, менингит, гепатит, нефрит, сепсис, саркоидоз, аллергический конъюнктивит, отит, хроническое обструктивное заболевание легких, синусит, синдром Бехсета и подагра, (13) легочный фиброз и другие фиброзные заболевания и (14) синдром раздраженного кишечника.
Предпочтительно, настоящие методы направлены на лечение заболеваний или состояний, выбранных из воспалительных заболеваний кишечника, включая заболевание Крона и язвенный колит; аллергических заболеваний, типа псориаза, атопического дерматита и астмы; и аутоиммунных заболеваний, типа ревматоидного артрита.
Более предпочтительно, настоящие методы направлены на лечение воспалительного заболевания кишечника, включая заболевание Крона и язвенный колит.
Соединения и композиции настоящего изобретения могут быть объединены с другими соединениями и композициями, имеющими применения для предотвращения и лечения интересующего состояния или заболевания, типа воспалительных состояний и заболеваний, включая воспалительные заболевания кишечника, аллергические заболевания, псориаз, атопический дерматит и астму, и патологии, отмеченные выше. Выбор соответствующих агентов для использования в комбинированных терапиях может быть сделан специалистом в области. Комбинация терапевтических агентов может действовать синергетически для эффекта лечения или предотвращения различных нарушений. Используя этот подход, можно достигнуть терапевтическую эффективность с более низкими дозировками каждого агента, таким образом снижая возможность неблагоприятных побочных эффектов.
Весовое соотношение соединения настоящего изобретения ко второму активному ингредиенту может быть различно и будет зависеть от эффективной дозы каждого ингредиента. В целом, будет использоваться эффективная доза каждого.
Таким образом, например, когда соединение настоящего изобретения объединяется с NSAID, весовое соотношение соединения настоящего изобретения к NSAID будет в целом располагаться в интервале от приблизительно 1000:1 до приблизительно 1:1000, предпочтительно от 200:1 до приблизительно 1:200. Комбинации соединения настоящего изобретения и других активных ингредиентов в целом также будут в пределах вышеупомянутого диапазона, но в каждом случае должна использоваться эффективная доза каждого активного ингредиента.
Комбинированная терапия включает со-введение соединения изобретения и упомянутого другого агента, последовательное введение соединения изобретения и другого агента, введение композиции, содержащей соединение изобретения и другой агент, или одновременное введение отдельных композиций, содержащих соединение изобретения и другой агент.
Изобретение далее включает использование соединения изобретения как активного терапевтического вещества, в особенности при лечении CCR9-опосредованных нарушений. В частности, изобретение включает использование соединения изобретения в лечении воспалительного заболевания кишечника, включая заболевание Крона и язвенный колит.
В другом аспекте, изобретение включает использование соединений изобретения в производстве лекарства для использования в лечении вышеупомянутых нарушений.
"Фармацевтически приемлемый носитель" подразумевает любой один или более соединений и/или композиций, которые имеют достаточную чистоту и качество для использования в составе соединения изобретения, которые, когда соответственно вводятся человеку, не производят неблагоприятную реакцию, и используются как носитель для лекарственного препарата (то есть соединения настоящего изобретения). Изобретение далее включает процесс получения композиции, включающий смешивание соединения изобретения и дополнительного фармацевтически приемлемого носителя, и включает те композиции, следующие из такого процесса, которые включает обычный фармацевтический процесс.
Например, соединение изобретения может быть доведено до наноразмеров перед получением состава. Соединение изобретения может быть также получено размалыванием, микронизацией или другими методами уменьшения величины частиц, известными в технологии. Такие методы включают, но без ограничения, описанные в патентах США №№4826689, 5145684, 5298262, 5302401, 5336507, 5340564, 5346702, 5352459, 5354560, 5384124, 5429824, 5503723, 5510118, 5518187, 5518738, 5534270, 5536508, 5552160, 5560931, 5560932, 5565188, 5569448, 5571536, 5573783, 5580579, 5585108, 5587143, 5591456, 5622938, 5662883, 5665331, 5718919, 5747001, заявках WO 93/25190, WO 96/24336 и WO 98/35666, каждые из которых включены здесь ссылкой.
Фармацевтические композиции изобретения могут быть получены с использованием методик и методов, известных специалистам в технологии. Некоторые из методов, обычно используемых в технологии, описаны в Remington's Pharmaceutical Sciences (Издательство Макинтош), все содержание которого включено здесь ссылкой.
Композиции изобретения включают глазную, оральную, назальную, трансдермальную, местную с или без окклюзии, внутривенную (и болюсную, и инфузионную) и инъекционную (интраперитонеально, подкожно, внутримышечно, 30 внутриопухолево или парентерально).
Композиция может быть в единичной дозировке, типа таблетки, пилюли, капсулы, порошка, гранулы, липосомы, ионообменной смолы, стерильного глазного раствора или глазного средства доставки (типа контактной линзы, и т.п., облегчающей непосредственное высвобождение, продленное высвобождение или отложенное высвобождение), парентерального раствора или суспензии, порционного аэрозоля или жидкого распылителя, капель, ампулы, устройства автоинъекции или свечи; для введения окулярно, орально, внутриназально, сублингвально, парентерально, или ректально, или ингаляцией, или вдуванием.
Композиции изобретения, подходящие для орального введения, включают твердые формы, типа пилюль, таблеток, каплет, капсул (каждая включат составы немедленного высвобождения, продленного высвобождения и отложенного высвобождения), гранул и порошков.
Оральная композиция предпочтительно сформулирована как гомогенная композиция, в которой вещество препарата (то есть соединения настоящего изобретения) рассеяно равномерно по смеси, которая может быть легко подразделена на единицы дозировки, содержащие равные количества соединения изобретения. Предпочтительно, композиции получают, смешивая соединение изобретения с одним или более произвольно представленных фармацевтических носителей (типа крахмала, сахара, растворителя, гранулирующего агента, смазки, скользящего агента, связующего вещества и дезинтегрирующего агента), одного или более произвольно представленных фармацевтически инертных наполнителей (типа воды, гликолей, масел, спиртов, вкусовых агентов, консервирующих средств, пигментов и сиропа), одного или более произвольно представленных обычных таблетирующих ингредиентов (типа кукурузного крахмала, лактозы, сахарозы, сорбита, талька, стеариновой кислоты, стеарата магния, дикальция фосфата и любой разновидности смол) и дополнительного растворителя (такого как вода).
Связующие вещества включают крахмал, желатин, естественный сахар (например, глюкозу и бета-лактозу), зерновые подсластители и естественные и синтетические смолы (например, акацию и трагакант). Дезинтегрирующие агенты включают крахмал, метилцеллюлозу, агар-агар и бентонит.
Соединение изобретения можно также вводить посредством композиции отсроченного высвобождения, в которой композиция включает соединение изобретения и биоразлагаемый носитель медленного высвобождения (например, полимерный носитель) или фармацевтически приемлемый небиоразлагаемый носитель медленного высвобождения (например, ионообменный носитель).
Биоразлагаемые и небиоразлагаемые носители отсроченного высвобождения известны в технологии. Биоразлагаемые носители используются, чтобы сформировать частицы или матрицы, которые сохраняют вещество (а) препарата (то есть соединение настоящего изобретения) и которые медленно разлагаются/растворяются в подходящей окружающей среде (например, водной, кислой, основной и т.п.), чтобы высвободить вещество (а) препарата. Такие частицы разлагаются/растворяются в жидкостях тела, чтобы высвободить вещество (а) препарата (то есть соединения настоящего изобретения) в них.
Частицы - это предпочтительно наночастицы (например, в диапазоне приблизительно 1-500 нм в диаметре, предпочтительно приблизительно 50-200 нм в диаметре, и наиболее предпочтительно приблизительно 100 нм в диаметре).
В процессе получения композиции медленного высвобождения носитель медленного высвобождения и соединение изобретения сначала растворяют или диспергируют в органическом растворителе. Получающуюся смесь добавляют в водный раствор, содержащий дополнительный поверхностно-активный агент(ы), чтобы получить эмульсию. Органический растворитель затем испаряют из эмульсии, чтобы обеспечить коллоидную суспензию частиц, содержащих носитель медленного высвобождения и соединение изобретения.
Таблетки и капсулы представляют выгодную оральную форму единицы дозировки. Таблетки могут быть засахаренными или покрыты пленкой с использованием стандартных методик. Таблетки могут также быть покрыты или иначе составлены, чтобы обеспечить длительное контролирующее терапевтический эффект высвобождение. Форма дозировки может включать компоненты внутренней и внешней дозировки, в которой внешний компонент находится в форме снимающегося защитного покрытия над внутренним. Эти два компонента могут далее быть отделены слоем, который противодействует разложению в желудке (типа кишечного слоя) и допускает прохождение внутреннего компонента без повреждения в двенадцатиперстную кишку, или слоем, который задерживает или откладывает высвобождение. Различные кишечные и внекишечные слоистые или покрывающие материалы (типа полимерных кислот, шеллаков, ацетилалкоголя и ацетилцеллюлозы или их комбинаций) могут использоваться.
Без дальнейшей детализации очевидно, что специалист в технологии, используя предыдущее описание, может использовать настоящее изобретение до его самой полной степени. Следующие Примеры должны поэтому рассматриваться как просто иллюстративные, а не ограничивающие объем настоящего изобретения.
ПРИМЕР 1
Получение:
Безводной кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида
В реакционный сосуд загружены 300 г 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида, 4 737 мл промышленного метилового спирта (IMS) и 302.4 мл воды. 27.245 г гранул гидроокиси натрия добавлены к жидкому раствору при 25°C. Реакционная смесь перемешана при температуре окружающей среды в течение 50 минут с последующим нагревом до ~78°C, чтобы растворить все твердые частицы. Чистый раствор затем отфильтровали, поддерживая температуру выше 55°C в течение процесса фильтрации. После фильтрации отфильтрованный раствор повторно нагрет до 75°C и затем охлажден до 55°C и затравлен кристаллами 3.0 г Соединения В безводной кристаллической формы (полученной в соответствии с аналогичной процедурой) как суспензия в 15 мл IMS при температуре окружающей среды. Суспензию выдерживали при 55°C накануне и затем охладили до 45°C. Использовали перегонку в вакууме при нагреве реакторной рубашки до 65°C, и не позволяя температуре суспензии превысить 55°C, оставили ~1 500 мл суспензии в реакторе. Суспензию охладили до -10°C, выдержали при этой температуре, а затем перевели в фильтрационную сушилку и осаждали 10 минут. Температура рубашки фильтра была предварительно снижена до -10°C. Маточные растворы были удалены к проколу с использованием азота под давлением 0.5-1 бар. Кристаллизатор загружен сначала 1 200 мл предварительно охлажденного осадка IMS, охлажденного до -10°C. Осадок перенесен на фильтр, перемешан в течение 10 минут, осажден в течение 10 минут и удален под давлением азота 0.5-1 бар. Промывание фильтрованного сгустка повторили два дополнительных раза при тех же самых условиях. Температура рубашки фильтра увеличена до 20°C, и сгусток удален под давлением азота 0.5-1 бар, пока удаляемый растворитель не уменьшился до струйки. Влажный сгусток высушен при 70°C с перемешиванием под вакуумом, чтобы обеспечить 258.3 г названного соединения в виде желтого кристаллического твердого.
ПРИМЕР 2
Получение:
Кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - 1,4 диоксан/вода сольват)
200 мг безводной кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида отмерены в сосуд 1.8 мл, содержащий перемешивающий брусок. Вода (43.9 мкл), 1,4 диоксан (53.0 мкл) и 1 М гидроокиси натрия (4.3 мкл) добавлены, сосуд закупорен, и раствор размешивали в течение 5 часов при 25°C. Полученное твердое отделили, используя бюхнеровскую воронку, и отжатый осадок осушили воздухом в течение 1 часа, чтобы обеспечить названное соединение как желтое твердое.
Рентгеновская порошковая дифракционная (XRPD) структура этого материала показана на Фиг. 1, а дифракционные углы и d-интервалы сведены в Таблицу I. XRPD анализ проведен на Дифрактометре PANanalytical X'Pert Pro, модель PW3040/60, серийный номер DY2407, с использованием детектора X'Celerator.
Включенные условия: CuKα излучение (λ=1.54059 Å), напряжение генератора: 45 kV, ток генератора: 40 mA, начальный угол: 2.0°2θ, конечный угол: 50.0°2θ, размер шага: 0.0167°2θ, время на шаг: 40.005 секунды.
Образец был получен с использованием техники нулевого фона (фронт заполнения).
Спектр Рамана названного соединения зарегистрирован на Спектрометре Nicolet NXR 9650 FT-Raman, при 4 см-1 разрешении с возбуждением от Nd:YVO4 лазера (λ=1064 нм). Спектр Рамана этого материала показан на Фиг. 6 с главными пиками, наблюдаемыми в 668, 743, 804, 1125, 1154, 1162, 1286, 1544, 1587, 1597, 1611, 1657 и 1672 см-1.
Дифференциальная сканирующая калориметрическая (DSC) термограмма названного соединения зарегистрирована на дифференциальном сканирующем калориметре ТА Instruments Q1000 и показана на Фиг. 10. Образец взвешен в алюминиевый чаше, со сдвинутой крышкой, без герметизации чаши. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
Термограмма термогравиметрического анализа (TGA) названного соединения зарегистрирована на термогравиметрическом Анализаторе ТА Instruments Q5000 и показана на Фиг. 14. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
ПРИМЕР 3
Получение:
Кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - сольват формамида)
300 мг безводной кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида отмерено в сосуд на 4 мл, содержащий перемешивающий брусок. Дихлорметан (1.050 мкл), формамид (450 мкл) и 0.5 M гидроокиси натрия (38.4 мкл) добавлены последовательно. Суспензия нагрета до 40°C и размешана в течение 30 минут. Образец охлажден до 0°C при 1°C/мин и затем размешан в течение дополнительных 30 минут. Полученное твердое отделено с использованием бюхнеровской воронки, и отфильтрованный осадок промыт холодным дихлорметаном (4 мл, предварительно охлажденным до 1°C), и высушен при 50°C в течение 30 минут, чтобы обеспечить названное соединение как желтое твердое вещество.
Рентгеновская порошковая дифракционная (XRPD) структура этого материала показана на Фиг. 2 и дифракционные углы и d-интервалы сведены в Таблицу II.
XRPD анализ проведен на Дифрактометре PANanalytical X'Pert Pro, модель PW3040/60, серийный номер DY2407, с использованием детектора X'Celerator. Включенные условия сбора данных: CuKα излучение (λ=1.54059 Е), напряжение генератора: 45 kV, ток генератора: 40 mA, начальный угол: 2.0°2θ, конечный угол: 50.0°2θ, размер шага: 0.0167°2θ, время на шаг: 40.005 секунды.
Образец получен с использованием техники нулевого фона (фронт заполнения).
Спектр Рамана названного соединения зарегистрирован на Спектрометре Nicolet NXR 9650 FT-Raman, при 4 см-1 разрешении с возбуждением от Nd:YVO4 лазера (λ=1064 нм). Спектр Рамана этого материала показан на Фиг. 7 с главными пиками, наблюдаемыми в 655, 668, 737, 804, 1079, 1099, 1123, 1161, 1229, 1303, 1465, 1537, 1595, 1611, и 1654 см-1.
Дифференциальная сканирующая калориметрическая (DSC) термограмма названного соединения зарегистрирована на дифференциальном сканирующем калориметре ТА Instruments Q1000 и показана на Фиг. 11. Образец взвешен в алюминиевый чаше, со сдвинутой крышкой, без герметизации чаши. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
Термограмма термогравиметрического анализа (TGA) названного соединения зарегистрирована на термогравиметрическом Анализаторе ТА Instruments Q5000 и показана на Фиг. 15. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
ПРИМЕР 4
Получение:
Кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - диметилсульфоксид сольват)
100 мг безводной кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида отмерено в сосуд на 2 мл, содержащий перемешивающий брусок. Хлорбензол (350 мкл), диметилсульфоксид (150 мкл) и 0.5 M метоксида натрия (12.5 мкл) добавлены последовательно. Суспензию перемешивали при 25°C в течение 3 недель. Полученное твердое отделили с использованием фильтровальной бумаги, и отфильтрованный осадок высушен при 40°C в течение 2 часов, чтобы обеспечить названное соединение.
Рентгеновская порошковая дифракционная (XRPD) структура этого материала показана на Фиг. 3 и дифракционные углы и d-интервалы сведены в Таблицу III.
XRPD анализ проведен на Дифрактометре PANanalytical X'Pert Pro, модель PW3040/60, серийный номер DY2407, с использованием детектора X'Celerator. Включенные условия: CuKα излучение (λ=1.54059 Ε), напряжение генератора: 45 kV, ток генератора: 40 mA, начальный угол: 2.0°2θ, конечный угол: 50.0°2θ, размер шага: 0.0167°2θ, время на шаг: 40.005 секунды. Образец получен с использованием техники нулевого фона (фронт заполнения).
Спектр Рамана названного соединения зарегистрирован на Спектрометре Nicolet NXR 9650 FT-Raman при 4 см-1 разрешении с возбуждением от Nd:YVO4 лазера (λ=1064 нм). Спектр Рамана этого материала показан на Фиг. 8 с главными пиками, наблюдаемыми в 662, 672, 718, 729, 750, 799, 1078, 1109, 1158, 1236, 1302, 1536, 1588, 1596 и 1636 см-1.
Дифференциальная сканирующая калориметрическая (DSC) термограмма названного соединения зарегистрирована на дифференциальном сканирующем калориметре TA Instruments Q1000 и показана на Фиг. 12. Образец взвешен в алюминиевый чаше, со сдвинутой крышкой, без герметизации чаши. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
Термограмма термогравиметрического анализа(TGA) названного соединения зарегистрирована на термогравиметрическом Анализаторе ТА Instruments Q5000 и показана на Фиг. 16. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
ПРИМЕР 5
Получение:
Кристаллической натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - несольватированная кристаллическая форма)
100 мг кристаллического сольвата формамида натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - сольват формамида) помещено на алюминиевую TGA чашу и нагрето до 260°C при скорости 15°C/мин. с использованием термогравиметрического Анализатора TA Instruments Q6000 для обеспечения названного соединения.
Рентгеновская порошковая дифракционная (XRPD) структура этого материала показана на Фиг. 4 и дифракционные углы и d-интервалы сведены в Таблицу IV.
XRPD анализ проведен на Дифрактометре PANanalytical X'Pert Pro, модель PW3040/60, серийный номер DY2407, с использованием детектора X'Celerator. Включенные условия: CuKα излучение (λ=1.54059 Е), напряжение генератора: 45 kV, ток генератора: 40 mA, начальный угол: 2.0°2θ, конечный угол: 50.0°2θ, размер шага: 0.0167°2θ, время на шаг: 40.005 секунды. Образец получен с использованием техники нулевого фона (фронт заполнения).
Спектр Рамана названного соединения зарегистрирован на Спектрометре Nicolet NXR 9650 FT-Raman при 4 см-1 разрешении с возбуждением от Nd:YVO4 лазера (λ=1064 нм). Спектр Рамана этого материала показан на Фиг. 9 с главными пиками, наблюдаемыми в 654, 667, 737, 803, 855, 1077, 1122, 1160, 1311, 1461, 1536, 1592, 1609, и 1648 см-1.
Дифференциальная сканирующая калориметрическая (Б8С) термограмма названного соединения зарегистрирована на дифференциальном сканирующем калориметре TA Instruments Q1000 и показана на Фиг. 13. Образец взвешен в алюминиевый чаше со сдвинутой крышкой, без герметизации чаши. Эксперименты проводились с использованием скорости нагревания 15°C/мин.
Термограмма термогравиметрического анализа(TGA) названного соединения зарегистрирована на термогравиметрическом Анализаторе TA Instruments Q5000 и показана на Фиг. 17. Эксперименты проводились с использованием скорости нагрева 15°C/мин.
ПРИМЕР 6
Получение:
Кристаллической натриевой соли 4-трет-бутыл-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - гидрат)
Приблизительно 30 мг несольватированной кристаллической формы натриевой соли 4-трет-бутил-N-[4-хлор-2-(1-окси-пиридин-4-карбонил)-фенил]-бензолсульфонамида (Соединение А - несольватированная кристаллическая форма) поместили в плоский держатель ХКРЭ образцов и оставили стоять в вытяжном шкафу в течение 5 недель, чтобы обеспечить названное соединение, смешанное с частью исходного несольватированного материала.
Рентгеновская порошковая дифракционная (XRPD) структура этого материала показана на Фиг. 5 и дифракционные углы и d-интервалы сведены в Таблицу V.
XRPD анализ проведен на Дифрактометре PANanalytical X'Pert Pro, модель PW3040/60, серийный номер DY2407, с использованием детектора X'Celerator. Включенные условия: CuKα излучение (λ=1.54059 Е), напряжение генератора: 45 kV, ток генератора: 40 mA, начальный угол: 2.0°2θ, конечный угол: 50.0°2θ, размер шага: 0.0167°2θ, время на шаг: 40.005 секунды. Образец получен с использованием техники нулевого фона (фронт заполнения).
Термограмма термогравиметрического анализа (ТОА) названного соединения зарегистрирована на термогравиметрическом Анализаторе ТА 1пзиптеп15 05000 и показана на Фиг.18. Эксперименты проводились с использованием скорости нагрева 15°C/мин.
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/cd56d1b4366550e49279858886993ee7.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/86f37c29c7a858a5ebc3fd8e8c31e335.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/0812276aa19b9dbcbe83fbc420f6fec2.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/da16b421b5d879544c93912861778029.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/ab62b9405745cf969d7304d6f38365bc.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/f4640bda3d29950f30e1e7008f804c65.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/194d0bced3e64fa0c99623b9850e9f93.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/88a46a7a74c70fd54ba419a7d0ec6f13.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/faa3536a211927780b03348e2fd5cbff.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/016a18d2d07e18153be60a3cd70736ee.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/b29aaefdbc6368d9308dbfad7e3becb8.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/f52234172e581b562f621b19b50045ac.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/34664e135db6c012709acd1930d9e23c.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/fe27fcf6bb0e0d0d50f5e92d1d5b6599.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/d6583f6d4323578651451207ed75efdf.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/b145946a2f2faf30ce90573837eff35a.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/ff2ee31d8a196c0414a073277ce3a815.png)
![ПОЛИМОРФНЫЕ ФОРМЫ НАТРИЕВОЙ СОЛИ 4-ТРЕТ-БУТИЛ-N-[4-ХЛОР-2-(1-ОКСИ-ПИРИДИН-4-КАРБОНИЛ)-ФЕНИЛ]-БЕНЗОЛСУЛЬФОНАМИДА](https://fips.edrid.ru/images/rid/ce/4c/3b/49463850dfea590c933f316fa9f2d9b3.png)

