ПОЛУЧЕНИЕ N-ЗАЩИЩЕННОГО БИС-3,6-(4-АМИНОАЛКИЛ)-2,5-ДИКЕТОПИПЕРАЗИНА
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
[0001] Настоящая заявка испрашивает приоритет на основании предварительной заявки на патент США №61/441525, поданной 10 февраля 2011 года, содержание которой включено в настоящее описание посредством ссылки, как если бы было полностью приведено в настоящем описании.
ОБЛАСТЬ ТЕХНИКИ
[0002] Настоящее изобретение относится к композициям для доставки активных агентов и в частности биологически активных агентов. Описанные варианты реализации находятся в области химического синтеза и в частности относятся к улучшенным способам синтеза для получения и очистки 3,6-дизамещенных-2,5-дикетопиперазинов.
УРОВЕНЬ ТЕХНИКИ
[0003] Доставка лекарственных средств является постоянной проблемой, связанной с введением активных агентов пациентам. Традиционным способам доставки активных агентов зачастую присущи значительные ограничения биологического, химического и физического характера. Как правило, данные ограничения налагаются средой, через которую происходит доставка, средой мишени для доставки или самой мишенью.
[0004] Биологически активные вещества особенно чувствительны к таким барьерам. Например, при доставке фармакологических и терапевтических агентов людям барьеры установлены организмом. Примерами физических барьеров является кожа и различные мембраны органов, через которые необходимо пройти до достижения мишени. Химические барьеры включают, но не ограничиваются ими, изменения pH, липидные бислои и ферменты, способствующие распаду.
[0005] Данные барьеры имеют особое значение при создании систем для пероральной доставки. Пероральная доставка многих биологически активных агентов была бы предпочтительным путем введения у животных, если бы не биологические, химические и физические барьеры, такие как изменение pH в желудочно-кишечном (ЖК) тракте, активные пищеварительные ферменты и мембраны желудочно-кишечного тракта, непроницаемые для активных агентов. В число многочисленных агентов, которые, как правило, не подлежат пероральному введению, входят биологически активные пептиды, такие как кальцитонин и инсулин; полисахариды и, в частности, мукополисахариды, включая, но не ограничиваясь ими, гепарин; гепариноиды, антибиотики и другие органические вещества. Данные агенты быстро теряют эффективность или разрушаются в желудочно-кишечном тракте под действием кислотного гидролиза, ферментов и т.п.
[0006] Однако зачастую имеются препятствия для широкого использования систем доставки лекарственных средств, поскольку: (1) для указанных систем требуется применение токсичных количеств адъювантов или ингибиторов; (2) недоступны подходящие низкомолекулярные активные агенты; (3) системы демонстрируют низкую стабильность и недостаточный срок годности; (4) системы сложны в изготовлении; (5) системы не защищают активный агент; (6) системы неблагоприятным образом изменяют активный агент; или (7) системы не обеспечивают или не способствуют абсорбции активного агента.
[0007] В данной области техники по-прежнему существует необходимость в разработке простых недорогих систем доставки, которые легко получать и которые могут доставлять широкий диапазон активных агентов. Одним из классов системы доставки, оказавшимся перспективным в качестве наполнителей, являются дикетопиперазины (DKP). В частности, было показано, что 3,6-бис-замещенные-2,5-дикетопиперазины эффективно доставляют биологически активные агенты через выстилку легкого.
[0008] Традиционный синтез дикетопиперазинов протекает через циклоконденсацию двух молекул аминокислоты или дипептида. Один из типичных способов синтеза дикетопиперазинов включает нагревание аминокислоты (Cbz-L-лизина, например) в м-крезоле в течение 17-22 часов при 160-170°C и перекристаллизацию дикетопиперазина из уксусной кислоты с выходом примерно 48%.
[0009] В патенте США №7709639 Stevenson et al. подробно описаны способы синтеза бис-Cbz-N-защищенных дикетопиперазинов, при этом полное описание указанного патента включено в настоящее описание посредством ссылки, как если бы было полностью приведено в настоящем описании.
[0010] Другие авторы получали дикетопиперазины из выделенных дипептидов путем нагревания в соответствующем растворителе, при этом удаляя воду путем перегонки. Несмотря на то что данные способы позволяют получать желаемые дикетопиперазины, они обеспечивают недостаточные выходы и могут требовать применения длительной очистки. Таким образом, существует необходимость в разработке улучшенного способа синтеза дизамещенных 2,5-дикетопиперазинов, позволяющего получать N-защищенные дикетопиперазины с хорошим выходом при сохранении защитных групп и минимальной очистке.
КРАТКОЕ ОПИСАНИЕ
[0011] Эта и другие нереализованные потребности, существующие в данной области техники, решены путем обеспечения соединений и способов, более подробно описанных ниже. Использование N-замещенных 3,6-аминоалкил-2,5-дикетопиперазинов в качестве фармацевтических наполнителей оказалось в значительной степени перспективным. Как отмечено выше, данные соединения часто синтезируют путем циклоконденсации аминокислот. Если аминокислота содержит свободный азот в боковой цепи (как, например, в лизине или орнитине), часто необходимо блокировать данный азот перед проведением реакции циклизации. Поскольку возможно осуществление различных способов синтеза после циклизации, желательна совместимость с различными защитными группами. Таким образом, желательным является способ синтеза, для которого может быть предусмотрен ряд различных N-защитных групп и который может обеспечивать хороший выход N-защищенного дикетопиперазина.
[0012] Некоторые подходящие защитные группы включают трифторацетил, ацетил и другие амид-образующие защитные группы; карбаматные защитные группы, включая бензилоксикарбонил (Cbz) и трет-бутоксикарбонил (ВОС).
[0013] В одном из вариантов реализации 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазин получают путем нагревания ε-трифторацетил-L-лизина в смешивающемся с водой растворителе, таком как N-метил-2-пирролидон (NMP), в присутствии катализатора, выбранного из группы, включающей фосфорную кислоту, серную кислоту и пентоксид фосфора, до температуры примерно 150-175°C. Указанный дикетопиперазин выделяют путем гашения водой и фильтрации полученного твердого вещества.
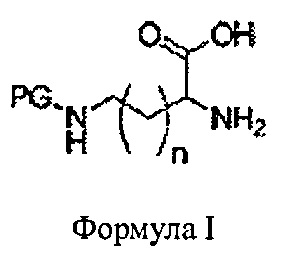
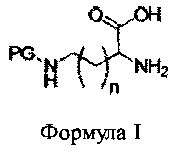
[0014] В предложенных вариантах реализации описаны способы синтеза 3,6-бис-[N-защищенного аминоалкил]-2,5-дикетопиперазина, включающие нагревание смеси аминокислоты общей формулы I в присутствии катализатора в органическом растворителе; при этом указанный катализатор выбран из группы, включающей в том числе серную кислоту, фосфорную кислоту, п-толуолсульфоновую кислоту, циклический ангидрид 1-пропилфосфоновой кислоты, трибутилфосфат, фенилфосфоновую кислоту и пентоксид фосфора; и при этом указанный растворитель выбран из группы, включающей в том числе: диметилацетамид, N-метил-2-пирролидон, диглим, этилглим, проглим, этилдиглим, м-крезол, п-крезол, о-крезол, ксилолы, этиленгликоль и фенол.
[0015] В предложенных вариантах реализации также описаны способы, в которых n составляет от 1 до 7, в которых n равно 3, в которых n равно 2, в которых PG представляет собой амид-образующую защитную группу, в которых указанная защитная группа представляет собой трифторацетил, в которых PG представляет собой карбамат-образующую защитную группу, в которых указанная защитная группа представляет собой Cbz, в которых растворитель, по существу, смешивается с водой, в которых указанный растворитель представляет собой N-метил-2-пирролидон, в которых аминокислота представляет собой ε-трифторацетил-L-лизин, в которых аминокислота представляет собой ε-Cbz-L-лизин, в которых аминокислота представляет собой γ-трифторацетилорнитин, в которых аминокислота представляет собой γ-Cbz-орнитин, в которых катализатор представляет собой пентоксид фосфора, при этом концентрация пентоксида фосфора составляет от 10% до примерно 50% концентрации аминокислоты, и варианты реализации, дополнительно включающие этап гашения смеси водой.
[0016] В предложенных вариантах реализации описаны способы синтеза 3,6-бис-[N-защищенного аминобутил]-2,5-дикетопиперазина, включающие: нагревание смеси N-защищенного лизина в присутствии катализатора в органическом растворителе до температуры от 110° до 175°C в течение 0,25-5 часов; при этом указанный катализатор выбран из группы, включающей серную кислоту, фосфорную кислоту и пентоксид фосфора, концентрация катализатора составляет от 5% до примерно 50% от концентрации лизина; и указанный растворитель выбран из группы, включающей диметилацетамид, N-метил-2-пирролидон, диглим, этилглим, проглим, этилдиглим, м-крезол, п-крезол, о-крезол, ксилолы, этиленгликоль и фенол.
[0017] В предложенных вариантах реализации описаны способы синтеза 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина, включающие: нагревание смеси ε-трифторацетил-L-лизина в присутствии пентоксида фосфора в N-метил-2-пирролидоне до температуры от 150° до 175°C в течение 0,25-5 часов; при этом концентрация пентоксида фосфора составляет от 10% до примерно 40% от концентрации лизина; и гашение указанной смеси вторым растворителем или, в качестве альтернативы, концентрация пентоксида фосфора относительно лизина составляет от 20% до 35% и смесь гасят водой.
[0018] Любая комбинация описанных выше элементов во всех их возможных вариантах включена в описанные варианты реализации, если в настоящем описании не указано иное или если это не противоречит явным образом контексту.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
[0019] Лучшее понимание типичных вариантов реализации настоящего изобретения будет достигнуто при ссылке на прилагаемые чертежи, на которых одинаковые части обозначены одинаковыми номерами позиций и где
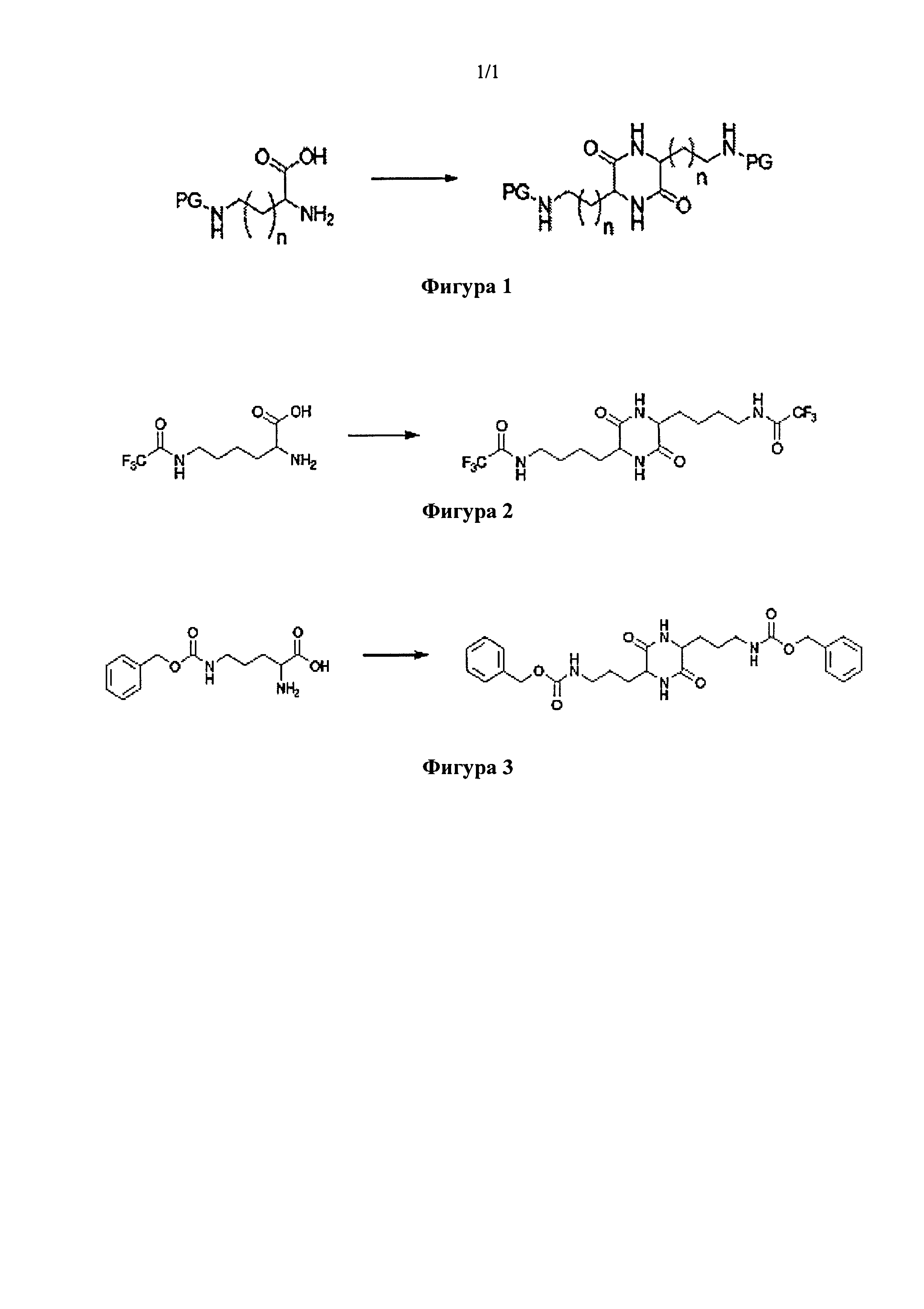
[0020] ФИГ.1 представляет собой схему, демонстрирующую циклоконденсацию N-защищенной аминокислоты с получением дикетопиперазина.
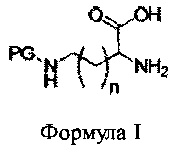
[0021] ФИГ.2 представляет собой схему, демонстрирующую циклоконденсацию ε-трифторацетиллизина.
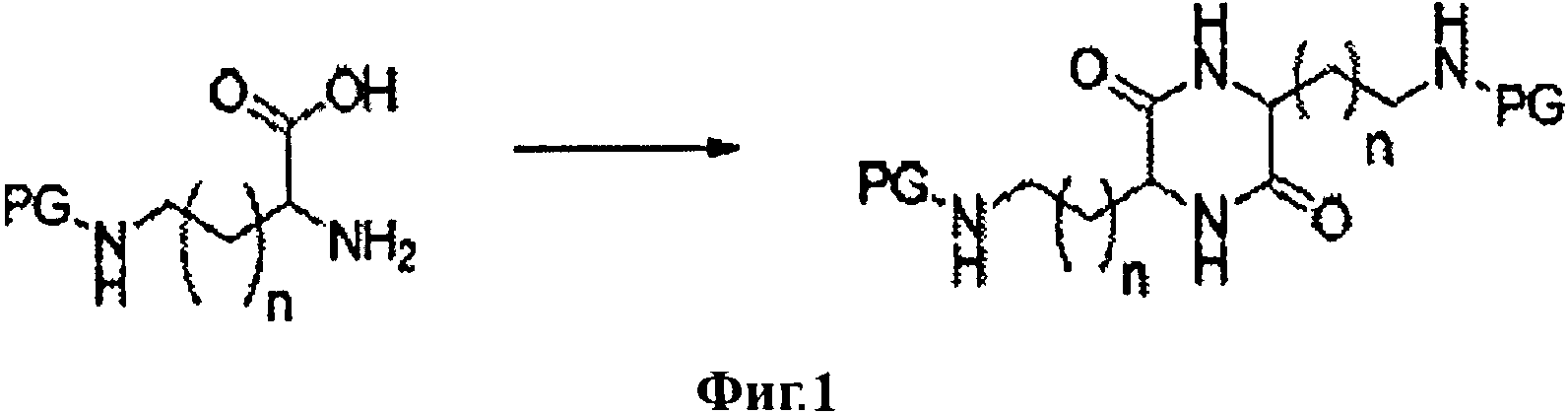
[0022] ФИГ.3 представляет собой схему, демонстрирующую циклоконденсацию γ-Cbz-орнитина.
ПОДРОБНОЕ ОПИСАНИЕ
[0023] В настоящем описании метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, гептил или октил и все изомеры по положению связи следует считать алкилом. Указанные группы могут быть моно- или полизамещены (C1-C8)-алкокси, (C1-C8)-галогеналкилом, OH, галогеном, NH2, NO2, SH, S-(C1-C8)алкилом. (C2-C8)-алкенил за исключением метила означает (C1-C8)-алкильную группу, показанную выше, содержащую по меньшей мере одну двойную связь.
[0024] Группа боковой цепи α-аминокислоты означает переменную группу при атоме α-С глицина в качестве основной аминокислоты. Природные аминокислоты представлены, например, в Bayer-Walter, Lehrbuch der organischen Chemie, S. Hirzel Verlag, Stuttgart, 22nd edition, страница 822ff. Предпочтительные синтетические аминокислоты и защищенные аминокислоты могут быть приобретены в компании Sigma-Aldrich. Группы боковой цепи могут быть получены из указанных там групп.
[0025] Указанные химические структуры относятся ко всем возможным стереоизомерам, которые могут быть получены путем изменения конфигурации индивидуальных хиральных центров, осей или поверхностей, другими словами, ко всем возможным диастереомерам, а также ко всем оптическим изомерам (энантиомерам), входящим в данную группу.
[0026] Обращаясь к чертежам для лучшего понимания, на ФИГ.1 показана общая схема синтеза дизамещенного дикетопиперазина. На данной схеме показана N-защищенная аминокислота, подвергающаяся циклоконденсации со второй молекулой аминокислоты. В данном варианте реализации PG представляет собой защитную группу для азота, и n может составлять от 0 до 7. Из схемы видно, что при получении дикетопиперазина с помощью амина в боковой цепи необходимо блокировать атом (атомы) азота перед проведением реакции циклизации или на выходы будут влиять нежелательные побочные конденсации. В зависимости от химических взаимодействий, которые будут осуществляться после образования кольца, желательны различные защитные группы и, таким образом, предпочтительным является способ, для которого предусмотрено множество групп. Некоторые подходящие защитные группы включают трифторацетил, ацетил и другие амид-образующие защитные группы; карбаматные защитные группы, включая бензилоксикарбонил (Cbz) и трет-бутоксикарбонил (ВОС).
[0027] В известных способах циклоконденсации аминокислот с образованием DKP использовали растворители, такие как н-бутанол (смешиваемость с водой примерно 7-8%), тогда как такие растворители, как NMP, больше смешиваются с водой, что позволяет просто гасить/промывать водой с удалением реакционного растворителя, и если катализатор обладает значительной растворимостью в воде, одновременно катализатора. В одном из вариантов реализации катализатор для циклоконденсации аминокислот растворим в воде, что обеспечивает гашение водой и последующее удаление путем фильтрации.
[0028] ФИГ.2 иллюстрирует вариант реализации, в котором PG представляет собой трифторацетил и n равно 3. Таким образом, исходная аминокислота представляет собой ε-трифторацетиллизин, и продукт представляет собой 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазин. Далее следует пример способа синтеза 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина:
ПРИМЕРЫ
[0029] Пример 1 и 2
[0030] 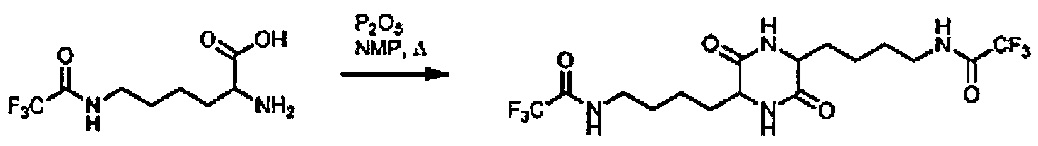
[0031] В 1-л трехгорлую круглодонную колбу, оснащенную устройством для продувки азотом, аппаратом для перегонки, механической мешалкой и термопарой с индикатором температуры, добавляли: NMP (256 мл), трифторуксусная кислота-Lys (ТФУ-Lys) (125 г, 0,52 моль) и Р205 (22 г, 0,15 моль). Реакционную смесь нагревали до 160°C и выдерживали при данной температуре в течение 1,5 часов. Затем смесь охлаждали до 100°C и вливали в деионизированную воду. Затем смесь охлаждали до менее 25°C и выделяли твердые вещества путем фильтрации, промывали деионизированной водой и сушили в вакууме при 50°C с получением 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина (65,28 г, 56,4%). 1H-ЯМР (ДМСО-d6): 1,3 (m, 4H), 1,5 (m, 4H), 1,7 (m, 4H), 3,2 (q, 4H), 3,8 (m, 2H), 8,1 (s, 2H), 9,4 (s, 2H). Элементный анализ, рассчитано C: 42,86; H: 4,95; N 12,50; F: 25,42. Обнаружено: C: 42,95; H: 4,91; N: 12,53; F: 24,99.
[0032] В футерованный стеклом реактор объемом 100 галлонов добавляли М-метил-2-пирролидон (200 л) и начинали перемешивание. К указанному растворителю добавляли ТФУ-лизин (100 кг, 413 моль) при температуре окружающей среды. К полученной суспензии добавляли пентоксид фосфора (15,2 кг, 107 моль). Затем смесь нагревали до 160°C течение 1 часа. Через 1 час при 160°C смесь охлаждали до 100°C и добавляли воду (500 л). Полученную смесь охлаждали до 25°C и выдерживали при данной температуре в течение 90 минут. Полученные твердые вещества дважды промывали водой (265 л каждый раз) и выделяли путем фильтрации с получением 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина с выходом 50%.
[0033] Исследовали различные катализаторы на предмет образования бис-замещенных дикетопиперазинов. Результаты исследования катализаторов приведены в Таблице 1. Далее следует общая схема и пример данного исследования:
[0034] Пример 3
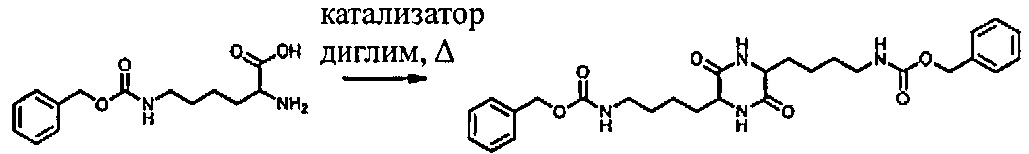
[0035] Cbz-лизин (10,0 г), диметиловый эфир диэтиленгликоля (диглим; 50 мл) и катализатор загружали в 250-мл круглодонную колбу. Смесь нагревали до 160-165°C в течение 2,5 часов. Реакционную смесь вливали в воду и охлаждали до температуры окружающей среды в течение ночи. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C.
[0036]
|
[0037] Далее исследовали применение серной кислоты и пентоксида фосфора (в двух концентрациях) для синтеза 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина в диглиме. Результаты приведены в Таблице 2.
[0038] Пример 4
[0039] 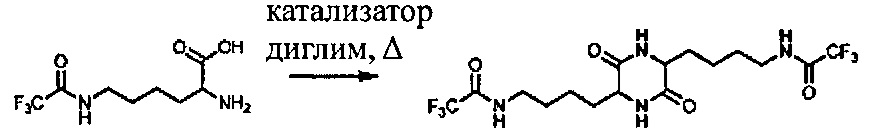
[0040] ТФУ-лизин (10,0 г), диметиловый эфир диэтиленгликоля (50 мл) и катализатор загружали в 250-мл круглодонную колбу. Смесь нагревали до 160-165°C в течение 2,5 часов. Реакционную смесь вливали в воду и охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C.
[0041]
|
[0042] Далее исследовали применение серной кислоты и пентоксида фосфора (в двух концентрациях) для синтеза 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина в диметилацетамиде (DMАс). Результаты приведены в Таблице 3.
[0043] Пример 5
[0044] 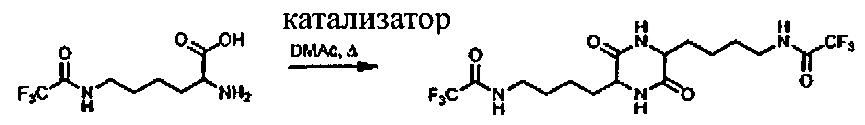
[0045] ТФУ-лизин (25,0 г), диметилацетамид (125 мл) и катализатор загружали в 250-мл круглодонную колбу. Смесь нагревали до 160-165°C в течение 2,5 часов. Реакционную смесь охлаждали до 100°C, вливали в воду, а затем охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C. Результаты приведены в Таблице 3.
|
[0046] Исследовали применение пентоксида фосфора для синтеза 3,6-бис-4-(N-трифторацетил)аминобутил-2,5-дикетопиперазина в N-метил-2-пирролидоне (NMP) при разном времени и температурах. Результаты приведены в Таблице 4.
[0047] Пример 6
[0048] 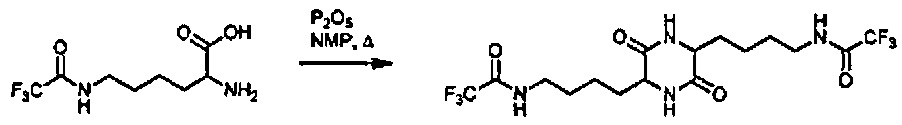
[0049] ТФУ-лизин (50 г), N-метилпирролидон (125 мл) и P2O5 (8,8 г, 0,3 экв.) загружали в круглодонную колбу. Смесь нагревали до температуры реакции в течение реакционного времени. Реакционную смесь охлаждали, вливали в воду, а затем охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C.
[0050]
|
[0051] Пример 7
[0052] 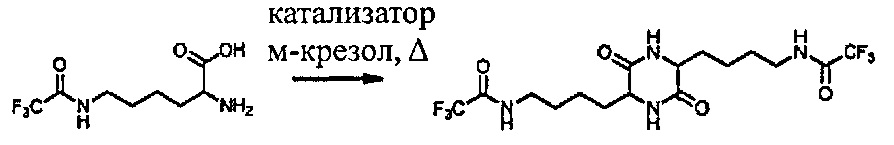
[0053] ТФУ-лизин (10,0 г), м-крезол (22 мл) и P2O5 загружали в 250-мл круглодонную колбу. Смесь нагревали до 160-165°C в течение 1 часа. Реакционную смесь охлаждали до 65°C, вливали в раствор 5% водного NaOH и метанола, а затем охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C. Выход продукта составил 12%.
[0054] Пример 8
[0055] 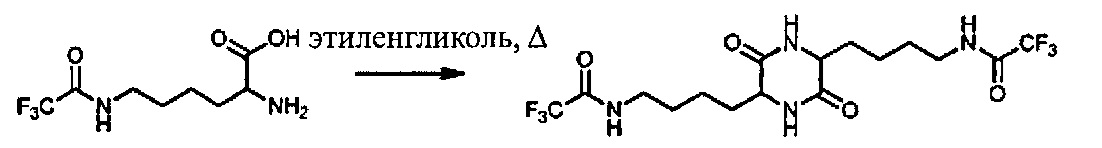
[0056] ТФУ-лизин (50,0 г) и этиленгликоль (150 мл) загружали в 500 мл круглодонную колбу. Смесь нагревали до 160-170°C в течение 2 часов. Реакционную смесь вливали в воду и охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C. Выход продукта составил 2%.
[0057] Пример 9
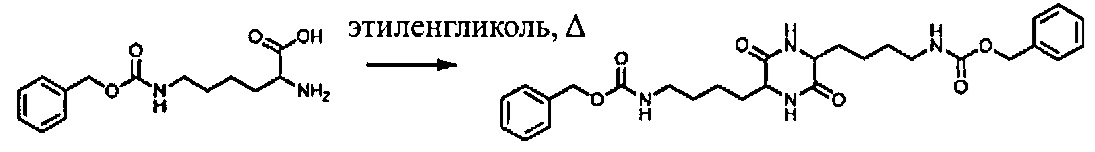
[0058] Cbz-лизин (100,0 г) и этиленгликоль (300 мл) загружали в 1000-мл круглодонную колбу. Смесь нагревали до 160-170°C в течение 6 часов. Реакционную смесь вливали в смесь воды и метанола и охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали водой и сушили в вакууме при 50°C. Выход продукта составил 64%.
[0059] На Фиг.3 показана общая схема циклоконденсации γ-Cbz-орнитина.
[0060] Пример 10
[0061] 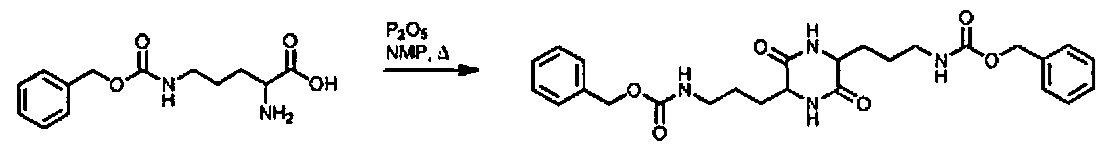
[0062] Cbz-орнитин (100 г), N-метилпирролидон (194 мл) и P2O5 (8 г) загружали в 1000-мл круглодонную колбу. Смесь нагревали до 160-165°C в течение 2 часов. Реакционную смесь вливали в воду и охлаждали до температуры окружающей среды. Выпавшее в осадок твердое вещество выделяли путем фильтрации, промывали метанолом и водой и сушили в вакууме при 50°C. Выход продукта составил 51%.
[0063] Если не указано иное, все числа, выражающие количества ингредиентов, свойства, такие как молекулярная масса, условия реакции и т.д., используемые в настоящем описании и формуле изобретения, следует понимать как модифицируемые во всех случаях термином «примерно». Соответственно, если не указано иное, числовые параметры, приведенные в следующем описании и прилагаемой формуле изобретения, представляют собой приблизительные значения, которые могут варьироваться в зависимости от желаемых свойств, которые пытались получить в описанных вариантах реализации. По меньшей мере, и не в качестве попытки ограничить применение доктрины эквивалентов объемом формулы изобретения, каждый числовой параметр следует рассматривать, по меньшей мере, с учетом количества приведенных значащих цифр и с применением обычных методик округления. Несмотря на то что числовые диапазоны и параметры, определяющие широкий объем описанных вариантов реализации, являются приблизительными значениями, численные значения, указанные в конкретных примерах, приведены настолько точно, насколько возможно. Однако любое численное значение, по существу, включает определенные ошибки, неизбежно являющиеся следствием стандартного отклонения, обнаруживаемые в соответствующих контрольных измерениях.
[0064] Термины в единственном числе и подобные обозначения, используемые в контексте описанных вариантов реализации (особенно в контексте следующей формулы изобретения), следует рассматривать как включающие и единственное, и множественное число, если в настоящем описании не указано иное или если это явным образом не противоречит контексту.
[0065] Перечисление диапазонов величин в настоящем описании предназначено только для краткости индивидуального указания каждой отдельной величины, входящей в указанный диапазон. Если в настоящем описании не указано иное, каждая отдельная величина включена в настоящее описание, как если бы она была отдельно указана в настоящем описании. Все способы, описанные в настоящем документе, могут быть осуществлены в любом подходящем порядке, если в настоящем описании не указано иное, или если это явным образом не противоречит контексту. Использование любого или всех примеров или использование типичных выражений (например, «такой как»), в настоящем описании предназначено только для более подробного пояснения описанных вариантов реализации и не ограничивает объем описанных вариантов реализации, если в формуле изобретения не указано иное. Выражения, употребляемые в настоящем описании, не следует рассматривать в том смысле, что какой-либо не указанный в формуле изобретения элемент является существенным для реализации описанных вариантов или любых их вариантов.
[0066] Группировки альтернативных элементов или вариантов реализации, описанных в настоящем документе, не следует рассматривать в качестве ограничений. Каждый элемент группы может быть упомянут и указан в формуле изобретения отдельно или в любой комбинации с другими элементами группы или другими элементами, встречающимися в настоящем описании. Ожидается, что один или более элементов группы могут быть включены в группу или исключены из группы, исходя из соображений удобства и/или патентоспособности. Когда происходит любое такое включение или исключение, считается, что в настоящем документе описание включает модифицированную группу, что, таким образом, соответствует письменному описанию любой и всех групп Маркуша, используемых в прилагаемой формуле изобретения.
[0067] В настоящем документе описаны предпочтительные варианты реализации настоящего изобретения, включая лучший вариант, известный авторам изобретения для осуществления настоящего изобретения (изобретений). Конечно, вариации описанных вариантов реализации будут очевидны специалисту в данной области техники после прочтения приведенного выше описания. Авторы настоящего изобретения ожидают, что специалист в данной области техники будет использовать такие вариации в случае необходимости, и авторы настоящего изобретения предполагают практически использовать изобретение (изобретения) иначе, чем, в частности, описано в настоящем документе. Соответственно, настоящее описание включает все модификации и эквиваленты объекта изобретения, изложенного в формуле изобретения, прилагаемой к настоящему документу, как это допускается действующим законом. Кроме того, любая комбинация описанных выше элементов во всех их возможных вариациях включена в описанные варианты реализации, если в настоящем описании не указано иное или если это явным образом не противоречит контексту.
[0068] Кроме того, на протяжении всего описания приведены ссылки на патенты и печатные публикации. Полное содержание каждого из указанных выше источников и печатных публикаций индивидуально включено в настоящее описание посредством ссылок.
[0069] После демонстрации и описания варианта реализации настоящего изобретения специалисту в данной области техники будет понятно, что могут быть осуществлены многочисленные вариации и модификации для того, чтобы повлиять на описанное изобретение, и указанные вариации и модификации по-прежнему будут входить в объем заявленного изобретения. Кроме того, многие элементы, указанные выше, могут быть изменены или заменены другими элементами, которые будут обеспечивать такой же результат и находиться в пределах сущности заявленного изобретения. Следовательно, настоящее изобретение ограничивается только объемом формулы изобретения.