Результат интеллектуальной деятельности: ПОРИСТЫЙ НЕОРГАНИЧЕСКИЙ КОМПОЗИТНЫЙ ОКСИД
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Данное изобретение относится к пористому неорганическому композитному оксиду, применимому для обработки выхлопных газов двигателей внутреннего сгорания.
Уровень техники
Продукты выхлопа двигателей внутреннего сгорания представляют известную опасность для здоровья и жизни людей, животных, а также растений. Загрязняющие вещества, в общем, представляют собой несгоревшие углеводороды, монооксид углерода, оксиды азота, а также остаточные количества серы и серосодержащих соединений. Катализаторы для выхлопных газов должны отвечать жестким требованиям относительно характеристик запуска, эффективности, длительной активности, механической стабильности, а также низкой стоимости, чтобы подходить для использования в транспортных средствах. Загрязняющие вещества, представляющие собой несгоревшие углеводороды, монооксиды углерода, а также оксиды азота, были успешно обработаны посредством контакта с многофункциональными катализаторами на основе благородных металлов, которые способны превратить загрязняющие вещества с высоким процентным содержанием в менее вредные продукты, представляющие собой диоксид углерода, воду (пар) и азот. Однако сера и соединения серы, присутствующие в топливе и, в свою очередь, в продуктах сгорания, как известно, отравляют благородные металлы, приводя к снижению их каталитической эффективности и срока службы.
«Каталитический нейтрализатор отработавших газов», используемый для превращения вредных загрязняющих веществ в безвредные газы, обычно состоит из трех компонентов, а именно, каталитически активного металла, носителя, на котором распределен активный металл, и подложки, на которую носитель наносят или осаждают в виде слоя пористого оксида.
Каталитические металлы, которые применяют, чтобы вызывать эффективную конверсию вредных загрязняющих веществ, таких как монооксид углерода, оксиды азота и несгоревшие углеводороды, при переменных встречающихся условиях, представляют собой благородные металлы, обычно металлы платиновой группы, такие как платина, палладий, родий и их смеси. Данные катализаторы на основе благородных металлов хорошо известны в уровне техники и более подробно описываются, например, в DE-053830318.
Благородный металл типично наносят на неорганические оксиды с высокой площадью поверхности, например, на частицы оксида алюминия с высокой площадью поверхности. Оксид алюминия с высокой площадью поверхности наносят или осаждают в виде слоя пористого оксида на керамическую или металлическую подложку, например, в форме ячеистого монолита или проволочной сетки или аналогичной конструкции. Также можно нанести благородные металлы на носитель после нанесения тонкого слоя материала носителя на монолит.
Патент США 6335305 описывает катализатор, который включает носитель на основе неорганического оксида и благородный металл, нанесенный на носитель, где носитель включает пористый оксид и композитный оксид формулы (Al2O3)a(CeO2)b(ZrO2)1-b, в которой a равно от 0,4 до 2,5, а b равно от 0,2 до 0,7.
EP 2036606 и EP 2036607 описывают неорганические оксиды, включающие оксид алюминия, металлический оксид, который не образует композитный оксид с оксидом алюминия и, по меньшей мере, один дополнительный элемент, выбранный из редкоземельных элементов и щелочноземельных элементов, применимые в качестве катализатора для обработки выхлопных газов, которые описываются как имеющие превосходную термостойкость.
Желательно сформировать пористый неорганический композитный оксид, который показывает улучшенную термостойкость и улучшенную устойчивость фаз при повышенной температуре.
Сущность изобретения
В первом аспекте настоящее изобретение нацелено на пористый неорганический композитный оксид, включающий оксиды алюминия и церия, или оксиды алюминия и циркония, или оксиды алюминия, церия и циркония, и необязательно оксиды одного или более допирующих элементов, выбранных из переходных металлов, редкоземельных металлов и их смесей, причем указанный неорганический композитный оксид имеет:
(a) удельную площадь поверхности после прокаливания при 1100°C в течение 5 часов, больше или равную площади, вычисленной согласно уравнению (2):
|
в котором:
SA представляет собой удельную площадь поверхности неорганического композитного оксида по БЭТ, в квадратных метрах на грамм, и
[Al] представляет собой количество оксидов алюминия в композитном оксиде, выраженное в виде массовых долей Al2O3 на 100 массовых долей композитного оксида, и
(b) общий объем пор после прокаливания при 900°C в течение 2 часов, больше или равный объему, вычисленному согласно уравнению (4.1):
|
в котором:
PV представляет собой объем пор неорганического композитного оксида, в кубических сантиметрах на грамм, и
[Al] является таким, как определено выше для уравнения (2).
Во втором аспекте настоящее изобретение нацелено на катализатор, включающий один или более благородных металлов, диспергированных на вышеописанном пористом неорганическом композитном оксиде.
В третьем аспекте настоящее изобретение нацелено на способ получения пористого неорганического композитного оксида, включающий:
(a) формирование (i) частиц, включающих гидрат алюминия, и (ii) частиц, включающих гидрат циркония, или частиц, включающих гидрат церия, или частиц, включающих гидрат циркония и гидрат церия, в водной среде:
(1) последовательно:
(1.1) формируя частицы гидрата алюминия в водной среде при температуре больше чем 50°C,
(1.2.) после стадии (a) (1.1) регулирование pH водной среды до pH от 4 до 6, и
(1.3) после стадии (a) (1.2) формирование частиц, включающих гидрат циркония, частиц, включающих гидрат церия, или частиц, включающих гидрат циркония и гидрат церия, в водной среде или
(2) одновременно формируя (i) частицы, включающие гидрат алюминия, и (ii) частицы, включающие гидрат циркония, или частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия, в водной среде при температуре больше чем 50°C,
(b) выделение частиц, полученных на стадии (a) из водной среды,
(c) сушку выделенных частиц, и
(d) прокаливание высушенных частиц,
с получением пористого неорганического композитного оксида.
В своих различных вариантах осуществления пористый неорганический композитный оксид по настоящему изобретению обеспечивает термическую стабильность, а также увеличенный объем пор, улучшенную фазовую чистоту, улучшенную устойчивость фаз и улучшенную локализацию областей смешанного циркониево-цериевого оксида.
Краткое описание чертежей
Фиг. 1 показывает рентгеновскую дифрактограмму композиции из примера 1 после прокаливания при 1200°C в течение 10 часов. В каждом случае предоставленная здесь рентгеновская дифрактограмма показывает график дифракционной интенсивности (в виде количества импульсов счета) относительно угла 2 тэта (в градусах в интервале от 20 до 90 градусов).
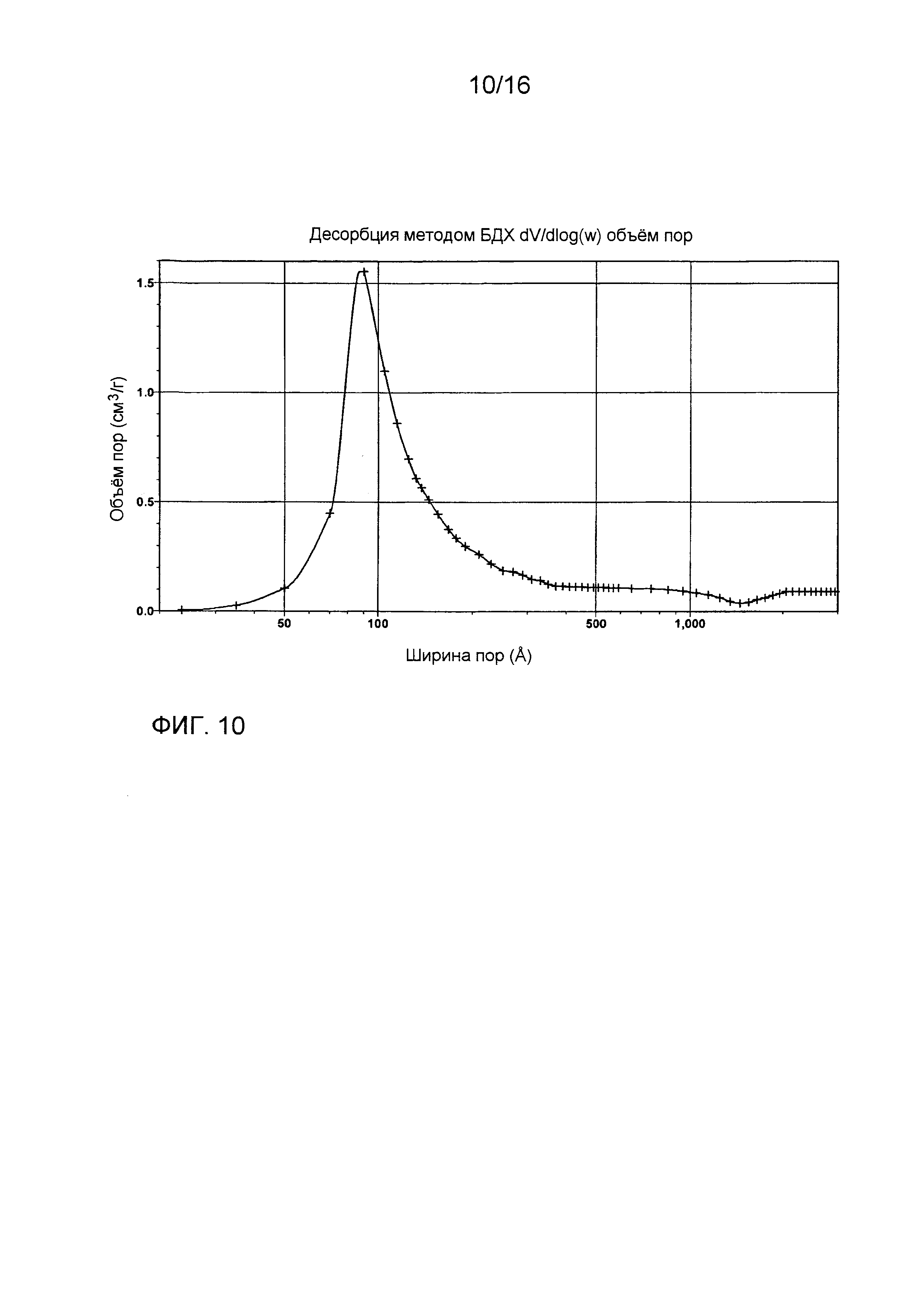
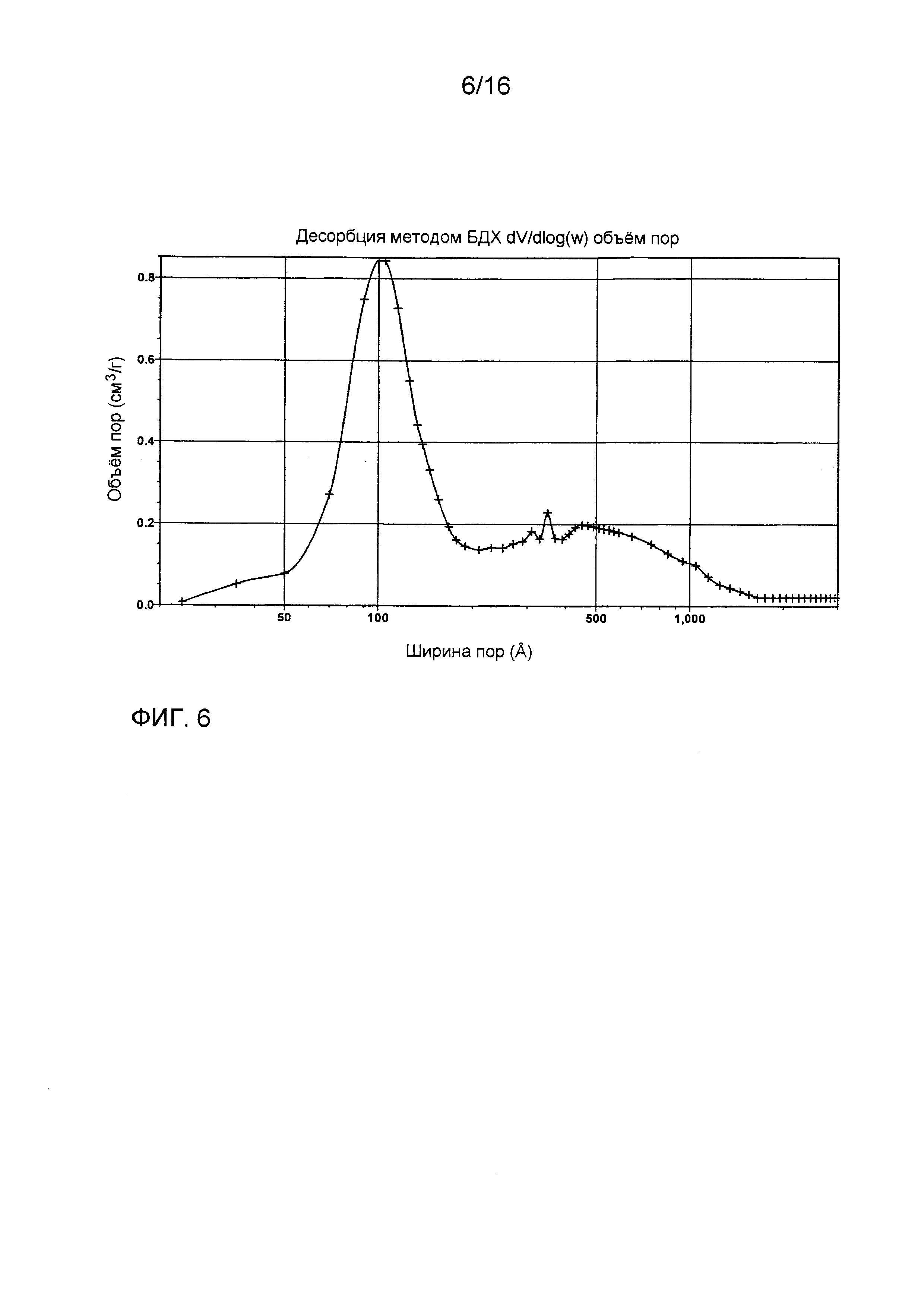
Фиг. 2 показывает производный логарифмический график распределения размера пор для композиции из примера 1 после прокаливания при 900°C в течение 2 часов. В каждом случае производный логарифмический график распределения размера пор, предоставленный здесь, показывает график dV/d(log w), где «V» представляет собой объем пор в сантиметрах на грамм (см3/г) и «w» представляет собой ширину пор (в Ангстремах (Å)).
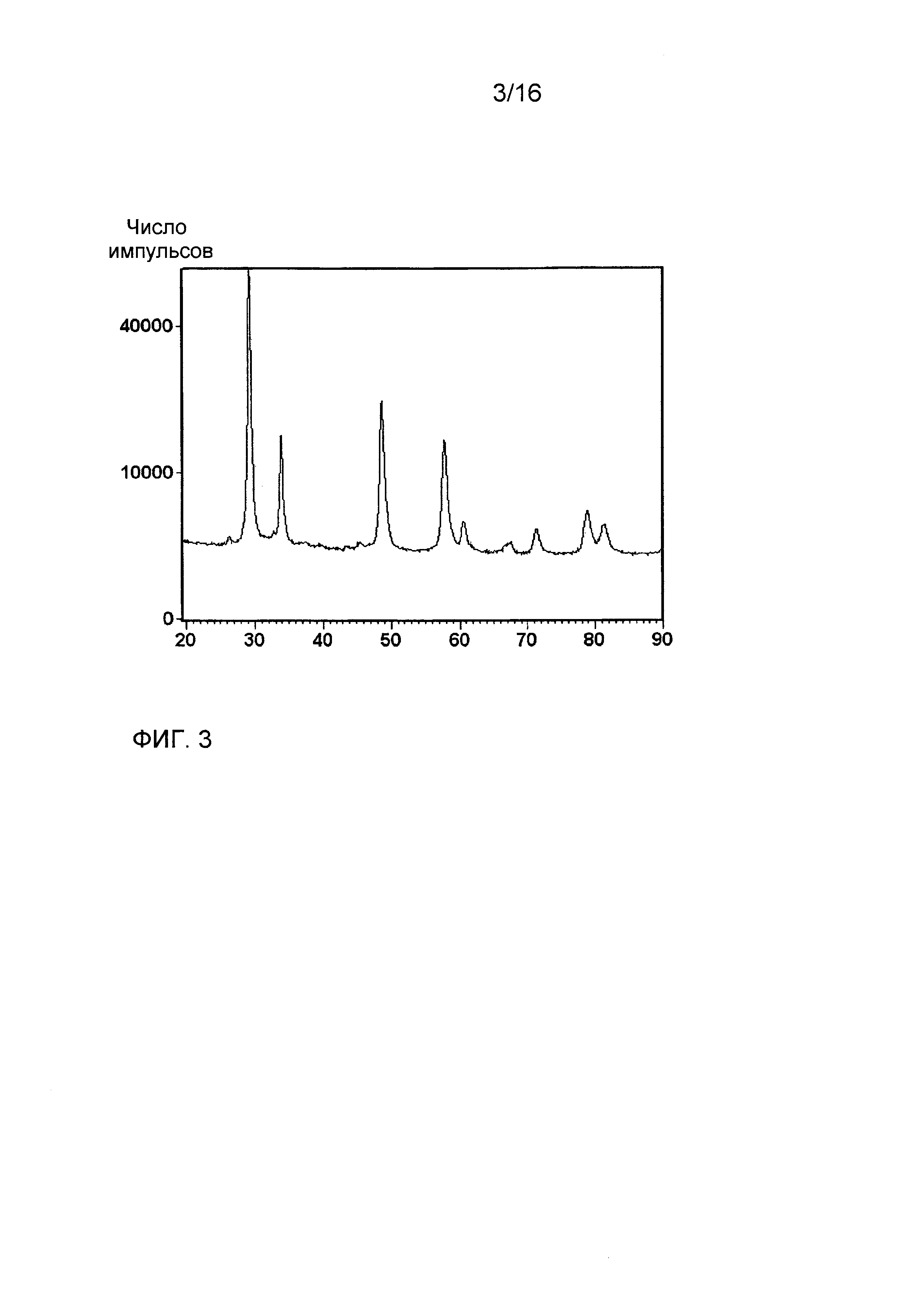
Фиг. 3 показывает рентгеновскую дифрактограмму композиции из примера сравнения 1 после прокаливания при 1200°C в течение 5 часов.
Фиг. 4 показывает производный логарифмический график распределения размера пор для композиции из примера сравнения 1 после прокаливания при 900°C в течение 2 часов.
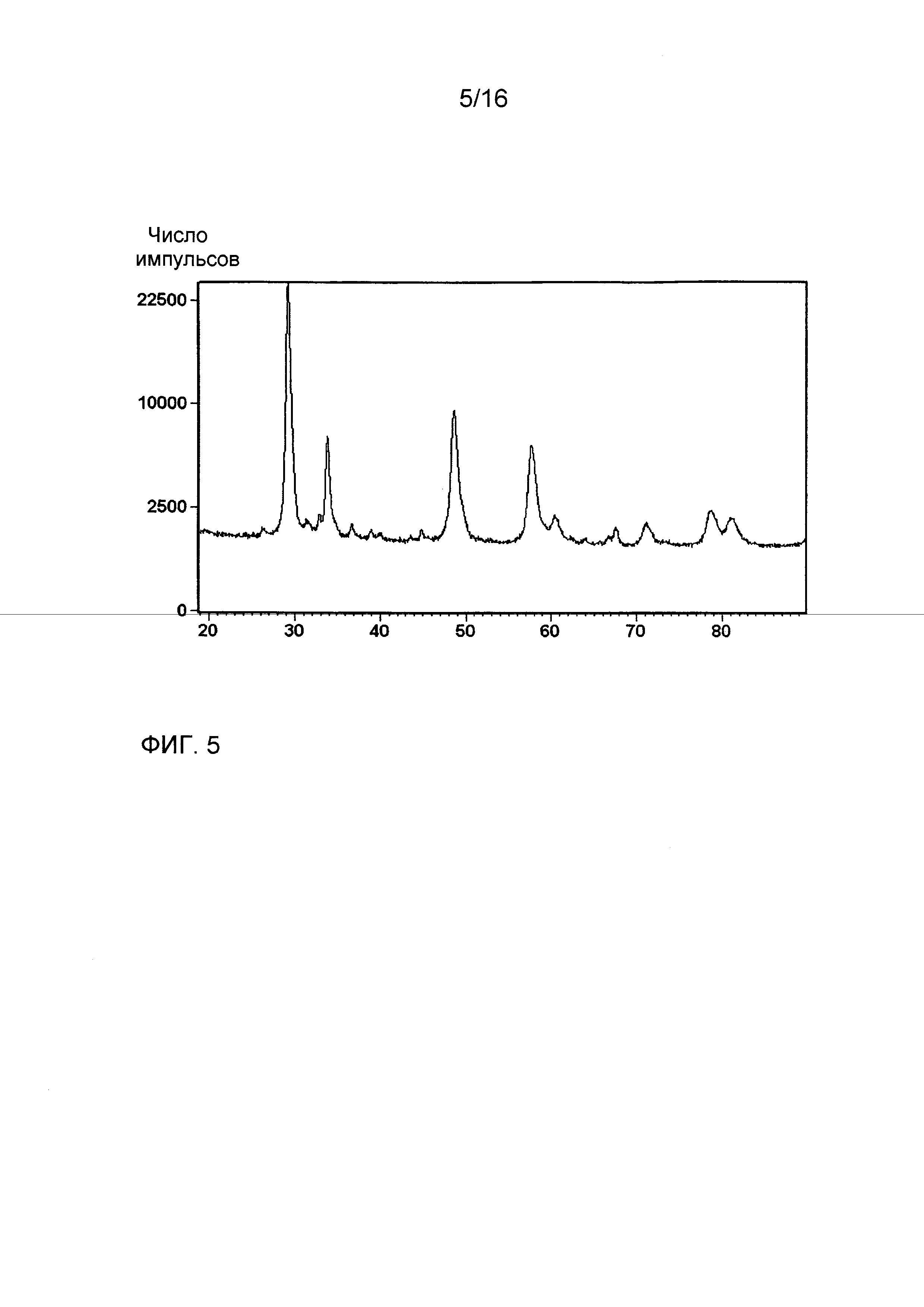
Фиг. 5 показывает рентгеновскую дифрактограмму композиции из примера 11 после прокаливания при 1200°C в течение 10 часов.
Фиг. 6 показывает производный логарифмический график распределения размера пор для композиции из примера 11 после прокаливания при 900°C в течение 2 часов.
Фиг. 7 показывает снимок, полученный методом просвечивающей электронной микроскопии, композиции из примера 11 при низком усилении (включая шкалу отсчета 2 микрометра (мкм)) после прокаливания при 900°C в течение 2 часов.
Фиг. 8 показывает снимок, полученный методом просвечивающей электронной микроскопии, композиции из примера 11 при высоком усилении (включая шкалу отсчета 500 нанометров (нм)) после прокаливания при 900°C в течение 2 часов.
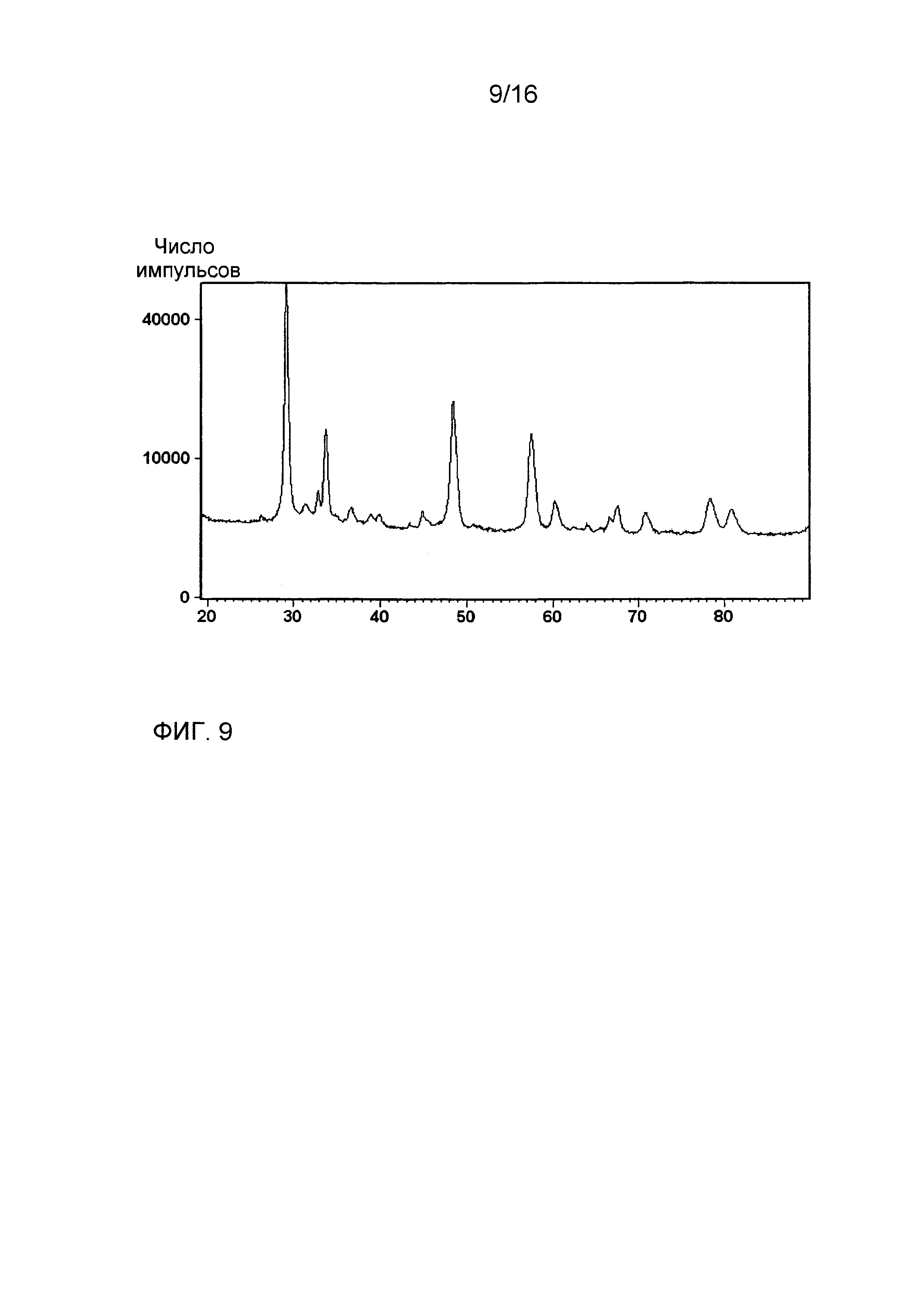
Фиг. 9 показывает рентгеновскую дифрактограмму композиции из примера 12 после прокаливания при 1200°C в течение 5 часов.
Фиг. 10 показывает производный логарифмический график распределения размера пор для композиции из примера 12 после прокаливания при 900°C в течение 2 часов.
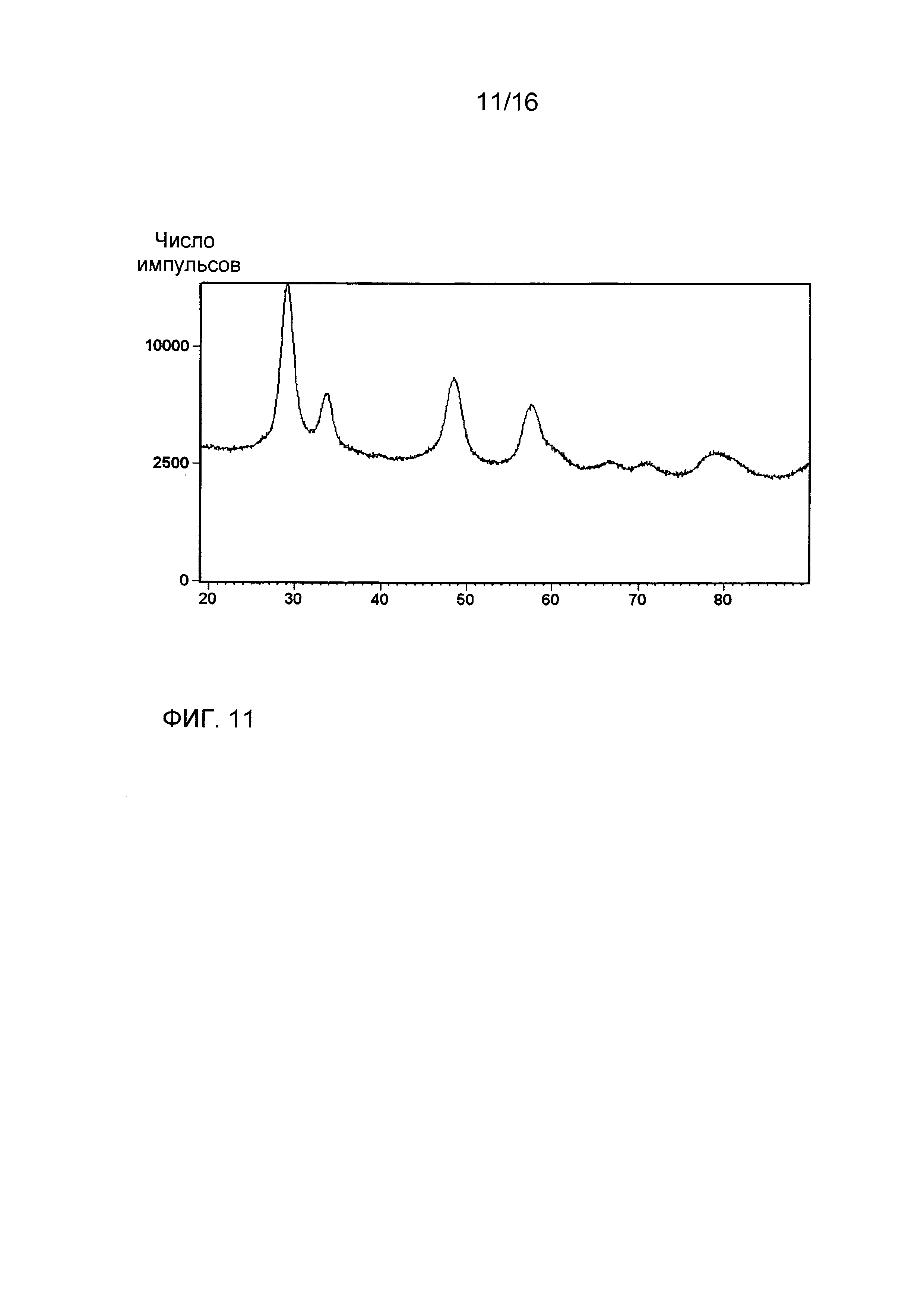
Фиг. 11 показывает рентгеновскую дифрактограмму композиции из примера 15 после прокаливания при 900°C в течение 2 часов.
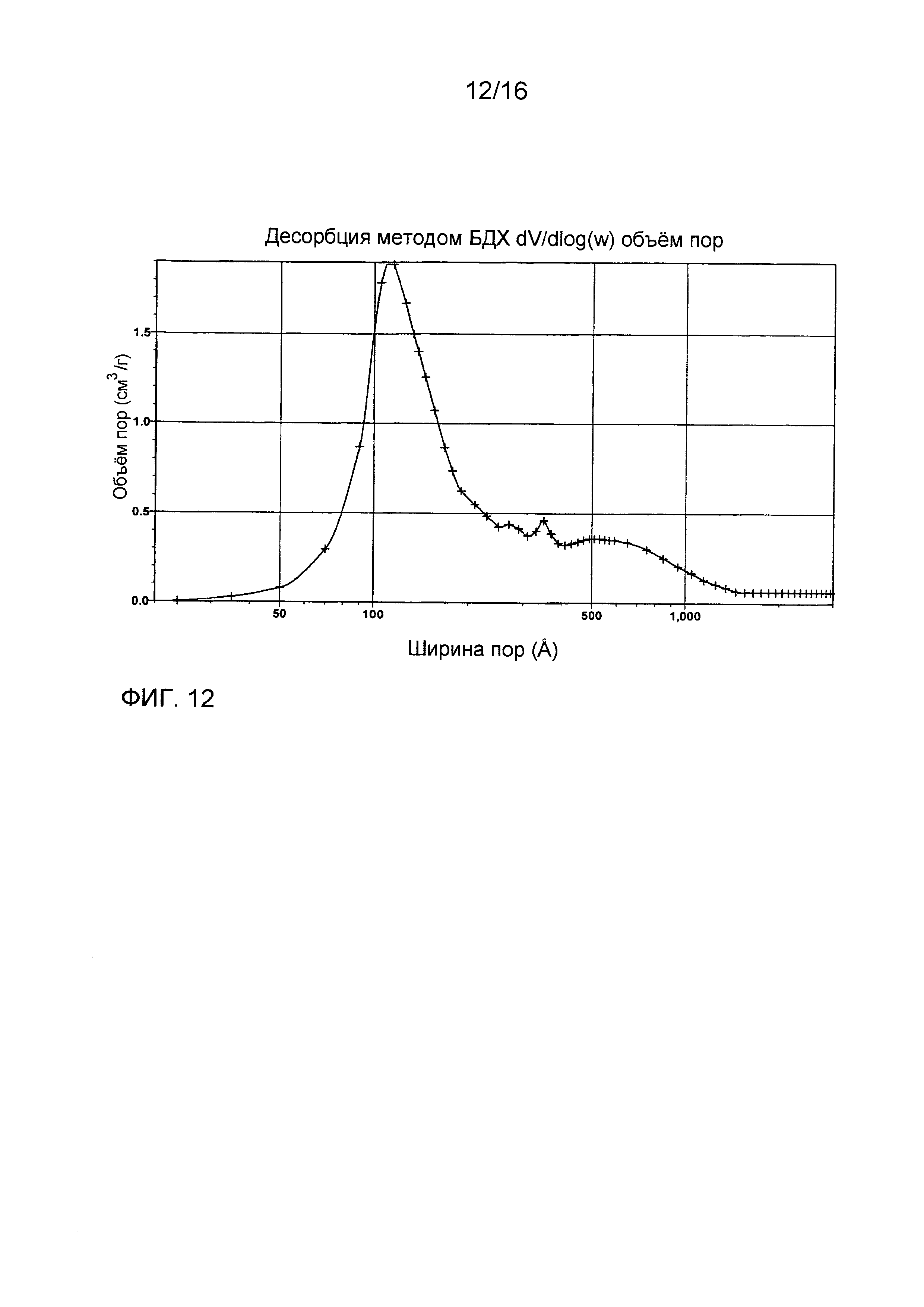
Фиг. 12 показывает производный логарифмический график распределения размера пор для композиции из примера 15 после прокаливания при 900°C в течение 2 часов.
Фиг. 13 показывает рентгеновскую дифрактограмму композиции из примера 16 после прокаливания при 1200°C в течение 5 часов.
Фиг. 14 показывает производный логарифмический график распределения размера пор для композиции из примера 16 после прокаливания при 900°C в течение 2 часов.
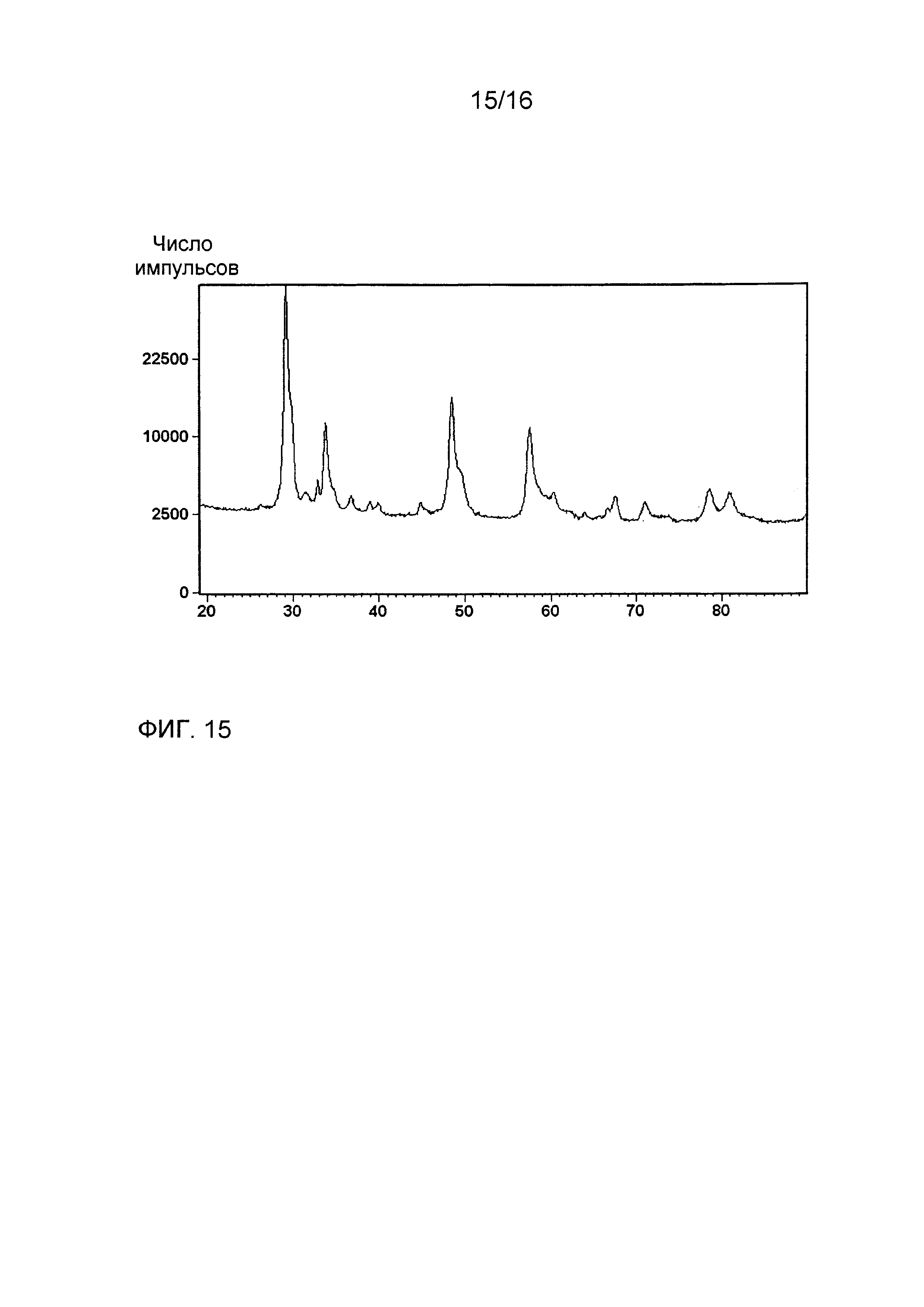
Фиг. 15 показывает рентгеновскую дифрактограмму композиции из примера 17 после прокаливания при 1200°C в течение 5 часов.
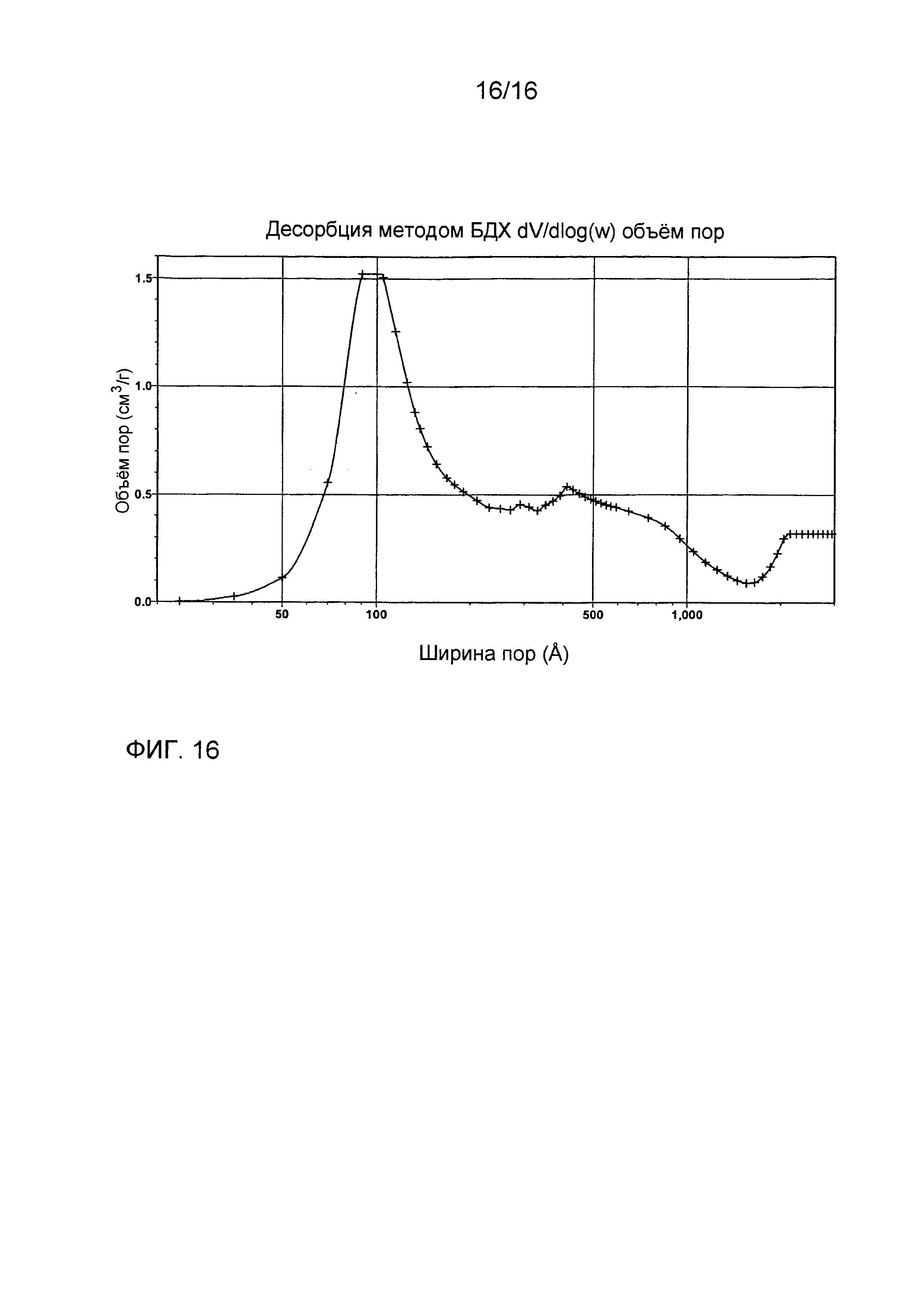
Фиг. 16 показывает производный логарифмический график распределения размера пор для композиции из примера 17 после прокаливания при 900°C в течение 2 часов.
Подробное описание изобретения
Следующие ниже термины, используемые в настоящем описании и прилагаемой формуле изобретения, имеют следующие значения:
Используемый здесь термин «дисперсный» относится к сформированным частицам в форме порошка, гранул, экструдата и аналогичной. В данном описании он используется со ссылкой к ядрам, носителям, а также к полученным в результате продуктам на основе нанесенных благородных металлов.
Используемый здесь термин «неорганический композитный оксид» обозначает неорганический оксидный материал, который включает, по меньшей мере, две отличные друг от друга кристаллографические фазы по результатам рентгеновской дифракции.
Используемый здесь термин «наночастицы» обозначает первичные частицы, имеющие диаметр частицы вплоть до примерно 500 нм, более типично примерно от 1 до 100 нм и еще более типично примерно от 1 до 50 нм. Соответствующие размеры частиц можно рассчитать, исходя из данных рентгеновской дифракции, или определить посредством наблюдения с использованием просвечивающего электронного микроскопа.
Используемая здесь терминология «первичная частица» обозначает одиночные отдельные частицы, а терминология «вторичная частица» обозначает агломерат из двух или более первичных частиц. Ссылка на «частицы», которая не конкретизирует «первичная» или «вторичная», обозначает первичные частицы, или вторичные частицы, или первичные частицы и вторичные частицы.
Используемый здесь термин «оксид алюминия» относится к любым формам оксида алюминия по отдельности или в виде смеси с другими металлами и/или оксидами металлов.
Используемый здесь термин «адсорбированный» или «адсорбция» следует коллективно относить к явлению адсорбции (способности удерживать или концентрировать газы, жидкости или растворенные вещества на поверхности адсорбента, например, оксида алюминия), и абсорбции (способности удерживать или концентрировать газы, жидкости или растворенные вещества по всему объему абсорбента, например, оксида алюминия); либо посредством химической реакции, которая может быть ионной, ковалентной или смешанной природы, либо посредством физических сил.
Используемая здесь для описания относительного количества данного компонента данной композиции терминология «массовые доли» компонента на основе 100 массовых долей данной композиции эквивалентна «массовому проценту» компонента на основе общей массы данной композиции. Например, ссылка на 10 массовых долей данного компонента на 100 массовых долей данной композиции эквивалентна по значению отнесению к 10% масс. компонента в композиции.
Если не указано иным образом, относительные количества соответствующих оксидов алюминия, церия, циркония и соответствующих допирующих элементов композиции композитного оксида по настоящему изобретению, каждое выражают, исходя из отдельного бинарного оксида соответствующего элемента (например, для алюминия как Al2O3, для циркония как ZrO2, для церия как CeO2, для иттрия как Y2O3, для лантана как La2O3, для неодима как Nd2O3, для празеодима как Pr6O11 и для гадолиния как Gd2O3).
Компонент оксида алюминия неорганического оксида по настоящему изобретению может быть аморфным или кристаллическим. В одном варианте осуществления композитный оксид по настоящему изобретению включает один или несколько оксидов алюминия в количестве, выраженном в виде массовых долей Al2O3 на 100 массовых долей композитного оксида, от примерно 20 до 90 массовых долей, более типично примерно 25 до 80 массовых долей и еще более типично примерно 30 до 70 массовых долей Al2O3.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению дополнительно включает оксиды циркония, оксиды церия или оксиды циркония и церия. В одном варианте осуществления неорганический композитный оксид по настоящему изобретению дополнительно включает один или более оксидов циркония, таких как ZrO2. В одном варианте осуществления неорганический композитный оксид по настоящему изобретению дополнительно включает один или более оксидов церия, таких как CeO2. В одном варианте осуществления неорганический композитный оксид по настоящему изобретению дополнительно включает один или более оксидов циркония и один или более оксидов церия.
В одном варианте осуществления композитный оксид по настоящему изобретению включает один или более оксидов циркония в количестве, выраженном в виде массовых долей ZrO2 на 100 массовых долей композитного оксида, составляющем от примерно 2 до 80 массовых долей, более типично от примерно 5 до 70 массовых долей и еще более типично от примерно 10 до 60 массовых долей ZrO2.
В одном варианте осуществления композитный оксид по настоящему изобретению включает один или более оксидов церия в количестве, выраженном в виде массовых долей CeO2 на 100 массовых долей композитного оксида, составляющем от примерно 2 до 80 массовых долей, более типично от примерно 5 до 70 массовых долей и еще более типично от примерно 10 до 60 массовых долей CeO2.
В одном варианте осуществления композитный оксид по настоящему изобретению включает один или более оксидов циркония и церия, каждый в количестве, выраженном в виде массовой доли ZrO2 или массовой доли CeO2 на 100 массовых долей композитного оксида:
от примерно 2 до 78 массовых долей, более типично от примерно 5 до 75 массовых долей, еще более типично от примерно 10 до 70 массовых долей и еще более типично от примерно 15 до 60 массовых долей ZrO2, и
от примерно 2 до 78 массовых долей, более типично от примерно 5 до 75 массовых долей, еще более типично от примерно 10 до 70 массовых долей и еще более типично от примерно 15 до 60 массовых долей CeO2,
при условии, что объединенное количество ZrO2 и CeO2 не превышает 80 массовых долей.
В одном варианте осуществления композитный оксид по настоящему изобретению включает оксиды алюминия и церия, или оксиды алюминия и циркония, или оксиды алюминия, церия и циркония, и необязательно оксиды одного или более допирующих элементов, выбранных из переходных металлов, редкоземельных металлов и их смесей, каждый в количестве, выраженном в виде массовой доли отдельного бинарного оксида соответствующего элемента на 100 массовых долей композитного оксида:
(a) примерно от 20 до 98 массовых долей, более типично примерно от 20 до 95 массовых долей Al2O3, и
(b)(i) примерно от 2 до 80 массовых долей, более типично примерно от 5 до 80 массовых долей ZrO2, или
(b)(ii) примерно от 2 до 80 массовых долей, более типично примерно от 5 до 80 массовых долей CeO2, или
(b)(iii) примерно от 2 до менее чем 78 массовых долей, более типично примерно от 5 до 75 массовых долей ZrO2 и от 2 до 78 массовых долей, более типично примерно от 5 до 75 массовых долей CeO2 при условии, что объединенное количество ZrO2 и CeO2 не превышает 80 массовых долей,
и
(c) необязательно вплоть до 15 массовых долей объединенного количества оксидов одного или более допирующих элементов, выбранных из переходных металлов, редкоземельных металлов и их смесей.
Каждый из оксидов допирующих элементов может независимо присутствовать в виде отдельного оксида соответствующего допирующего элемента, в виде компонентов в оксидах алюминия, циркония, церия и/или одного или нескольких других допирующих элементов. Подходящие допирующие элементы включают иттрий (Y), лантан (La), празеодим (Pr), неодим (Nd), самарий (Sa), европий (Eu), гадолиний (Gd), тербий (Tb), диспрозий (Dy), гольмий (Ho), эрбий (Er), тулий (Tm), иттербий (Yb), лютеций (Lu) и скандий (Sc). В одном варианте осуществления неорганические оксиды включают оксиды одного или более элементов, выбранных из Y, La, Pr, Nd и Gd.
В одном варианте осуществления композитный оксид по настоящему изобретению включает оксиды алюминия и лантана, где, когда каждое из количеств оксидов алюминия и лантана в композитном оксиде выражено в виде количества отдельного бинарного оксида соответствующего элемента, количество La2O3 больше или равно 2 массовым долям на 100 массовых долей Al2O3, и композитный оксид показывает улучшенную устойчивость фазы оксида алюминия.
В одном варианте осуществления композитный оксид по настоящему изобретению включает оксиды алюминия, циркония, церия и иттрия, где, когда каждое из количеств оксидов циркония, церия и иттрия выражено в виде количества отдельного бинарного оксида соответствующего элемента, количество Y2O3 больше или равно 2 массовым долям на 100 массовых долей объединенного количества ZrO2 и CeO2, и композитный оксид показывает улучшенную устойчивость фазы оксида циркония-оксида церия.
В одном варианте осуществления неорганический оксид по настоящему изобретению включает оксиды Y и La, оксиды Y и Pr, оксиды Y и Nd, оксиды Y и Gd, оксиды La и Pr, оксиды La и Nd, оксиды La и Gd, оксиды Pr и Nd, оксиды Pr и Gd или оксиды Nd и Gd.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению включает:
оксиды алюминия, циркония, церия, Y и La,
оксиды алюминия, циркония, церия, Y и Pr,
оксиды алюминия, циркония, церия, Y и Nd,
оксиды алюминия, циркония, церия, Y и Gd,
оксиды алюминия, циркония, церия, La и Pr,
оксиды алюминия, циркония, церия, La и Nd,
оксиды алюминия, циркония, церия, La и Gd,
оксиды алюминия, циркония, церия, Pr и Nd,
оксиды алюминия, циркония, церия, Pr и Gd, или
оксиды алюминия, циркония, церия, Nd и Gd.
В одном варианте осуществления неорганический оксид по настоящему изобретению включает оксиды Y, La и Pr, оксиды Y, La и Nd, оксиды Y, La и Gd, оксиды Y, Pr и Nd, оксиды Y, Pr и Gd, оксиды Y, Nd и Gd, оксиды La, Pr и Nd, оксиды La, Pr и Gd, оксиды La, Nd и Gd или оксиды Pr, Nd и Gd.
В одном варианте осуществления неорганический оксид по настоящему изобретению включает:
оксиды алюминия, циркония, церия, Y, La и Pr,
оксиды алюминия, циркония, церия, Y, La и Nd,
оксиды алюминия, циркония, церия, Y, La и Gd,
оксиды алюминия, циркония, церия, Y, Pr и Nd,
оксиды алюминия, циркония, церия, Y, Pr и Gd,
оксиды алюминия, циркония, церия, Y, Nd и Gd,
оксиды алюминия, циркония, церия, La, Pr и Nd,
оксиды алюминия, циркония, церия, La, Pr и Gd,
оксиды алюминия, циркония, церия, La, Nd и Gd, или
оксиды алюминия, циркония, церия, Pr, Nd и Gd.
В одном варианте осуществления композитный оксид по настоящему изобретению включает оксиды алюминия, циркония, церия и иттрия и лантана и/или неодима и/или празеодима, где, когда каждое из количеств оксидов циркония, церия и соответствующих допирующих элементов выражено в виде количества отдельного бинарного оксида соответствующего элемента:
объединенное количество La2O3, Nd2O3 и/или Pr6O11 больше или равно 2 массовым долям на 100 массовых долей Al2O3, и
количество Y2O3 больше или равно 2 массовым долям на 100 массовых долей объединенного количества ZrO2 и CeO2, и
композитный оксид показывает улучшенную устойчивость фазы оксида алюминия и улучшенную устойчивость фазы оксид циркония-оксид церия.
В одном варианте осуществления количество оксидов одного или нескольких допирующих элементов в неорганическом композитном оксиде по настоящему изобретению, выраженное в виде массовых долей объединенного количества отдельных бинарных оксидов соответствующих допирующих элементов на 100 массовых долей композитного оксида, составляет от более чем 0 до примерно 15 массовых долей, более типично от примерно 1 до 12 массовых долей и еще более типично от примерно 2 до 10 массовых долей оксидов одного или более допирующих элементов.
В одном варианте осуществления относительные количества компонентных элементов оксидов формулы неорганического композитного оксида, выраженных в виде бинарных оксидов соответствующих элементов, соответствуют структуре (1):
|
где:
каждый из MxOy, M’x’Oy’, M”x”Oy” представляет собой бинарный оксид, независимо выбранный из Y2O3, La2O3, Nd2O3, Pr6O11, Gd2O3:
коэффициенты a, b, c, d, e и f отражают соответствующие молярные количества соответствующих бинарных оксидов, где:
35≤a≤97,
0≤b≤50,
0≤c≤60,
0≤d≤14,
0≤e≤14 и
0≤f≤14,
при условии, что:
никакие два из M, M’ и M” не являются одним и тем же элементом, и
сумма d+e+f меньше или равна 14.
В одном варианте осуществления оксиды алюминия и необязательно одного или более допирующих элементов для первой одиночной кристаллографической фазы и оксиды одного или более элементов, выбранных из циркония и церия, и необязательно одного или более допирующих элементов формируют вторую кристаллографическую фазу.
В одном варианте осуществления неорганический оксид по настоящему изобретению включает пористую структуру оксида алюминия, включающую оксиды алюминия и необязательно оксиды одного или более соответствующих допирующих элементов и имеющую площадь поверхности и структуры, типично наночастицы, включающие оксид циркония, оксид церия или оксиды циркония и церия и необязательно оксиды одного или более соответствующих допирующих элементов, нанесенные на поверхность пористой структуры оксида алюминия.
В одном варианте осуществления неорганический оксид по настоящему изобретению включает пористую структуру оксида алюминия, включающую оксид алюминия и необязательно оксиды одного или более соответствующих допирующих элементов и имеющую площадь поверхности, которая включает площадь внешней поверхности и площадь внутренней поверхности, которая доступна посредством пор пористой структуры оксида алюминия, и дисперсные структуры, типично наночастицы, включающие оксид циркония, оксид церия или оксиды циркония и церия и необязательно оксиды одного или более соответствующих допирующих элементов, нанесенные на поверхность пористой структуры оксида алюминия, где дисперсные структуры, включающие оксид циркония, оксид церия или оксиды циркония и церия и необязательно оксиды одного или более соответствующих допирующих элементов, распределены по существу равномерно по всей площади внешней поверхности и доступной площади внутренней поверхности пористой структуры оксида алюминия.
В одном варианте осуществления неорганический оксид по настоящему изобретению включает пористую структуру оксида алюминия, включающую оксиды алюминия и необязательно оксиды одного или более соответствующих допирующих элементов и имеющую площадь поверхности, которая включает площадь внешней поверхности и площадь внутренней поверхности, и дисперсные структуры, типично наночастицы, включающие оксид циркония, оксид церия или оксиды циркония и церия и необязательно оксиды одного или более соответствующих допирующих элементов, нанесенные на поверхность пористой структуры оксида алюминия, где дисперсные структуры, включающие оксид циркония, оксид церия или оксиды циркония и церия и необязательно оксиды одного или более соответствующих допирующих элементов, распределены более плотно по всей площади внешней поверхности структуры носителя на основе оксида алюминия по сравнению с площадью внутренней поверхности структуры носителя на основе оксида алюминия.
В одном варианте осуществления структуры, включающие оксиды одного или более элементов, выбранных из циркония и церия, являются наночастицами, имеющими, после прокаливания при 1200°C в течение 5 часов, диаметр частиц или наиболее длинный характеристический размер примерно от 10 до 50 нм, более типично примерно от 15 до 35 нм.
В одном варианте осуществления неорганический оксид по настоящему изобретению находится в форме порошка, имеющего средний размер частиц от примерно 1 до 200 микрометров («мкм»), более типично от 10 до 100 мкм, или в форме гранул, имеющих средний размер частиц от 1 миллиметра («мм») до 10 мм. Альтернативно неорганический оксид может находиться в форме таблеток или экструдата (например, цилиндрической формы), причем размер и конкретная форма определяются рассматриваемым конкретным применением.
В одном варианте осуществления неорганический оксид по настоящему изобретению показывает высокую удельную площадь поверхности, имеющую хорошую термостойкость.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 900°C в течение 2 часов, больше или равную площади, вычисленной в соответствии с уравнением (1):
|
в котором:
SA представляет собой удельную площадь поверхности по БЭТ неорганического композитного оксида, в квадратных метрах на грамм (м2/г), и
[Al] представляет собой количество оксидов алюминия в композитном оксиде, выраженное в виде массовых долей Al2O3 на 100 массовых долей композитного оксида.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 1100°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (2):
|
в котором SA и Al, в каждом случае, является таким, как определено выше для уравнения 1.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 1200°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (3.1):
|
в котором SA и Al, в каждом случае, является таким, как определено выше для уравнения 1.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 1200°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (3.1), и для 50<[Al]≤90, больше или равную площади, вычисленной в соответствии с уравнением (3.2):
|
в котором SA и Al, в каждом случае, является таким, как определено выше для уравнения 1.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 900°C в течение 2 часов, больше или равную площади, вычисленной в соответствии с уравнением (1), и удельную площадь поверхности по БЭТ после прокаливания при 1100°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (2). В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 900°C в течение 2 часов, больше или равную площади, вычисленной в соответствии с уравнением (1), удельную площадь поверхности по БЭТ после прокаливания при 1100°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (2), и удельную площадь поверхности по БЭТ после прокаливания при 1200°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (3.1) или уравнением (3.1) и уравнением (3.2). В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает удельную площадь поверхности по БЭТ после прокаливания при 900°C в течение 2 часов, больше или равную площади, вычисленной в соответствии с уравнением (1), удельную площадь поверхности по БЭТ после прокаливания при 1100°C в течение 5 часов, больше или равную площади, вычисленной в соответствии с уравнением (2), и удельную площадь поверхности по БЭТ после прокаливания при 1200°C в течение 5 часов для 20≤[Al]≤50, больше или равную площади, вычисленной в соответствии с уравнением (3.1) и для 50<[Al]≤90, больше или равную площади, вычисленной в соответствии с уравнением (3.2).
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает объем пор, имеющий хорошую термическую устойчивость.
В одном варианте осуществления неорганический композитный оксид по настоящему изобретению показывает объем пор после прокаливания при 900°C в течение 2 часов, больше или равный объему, вычисленному в соответствии с уравнением (4.1):
|
в котором:
PV представляет собой объем пор неорганического композитного оксида, в кубических сантиметрах на грамм (см3/г), и
[Al] является таким, как определено выше для уравнения (1).
В предпочтительном варианте осуществления, в котором неорганический композитный оксид изготавливают последовательным способом, как описано более подробно ниже, осаждения гидратов алюминия при условиях кислотной реакции и затем осаждения гидратов циркония и/или церия, неорганический композитный оксид по настоящему изобретению показывает объем пор после прокаливания при 900°C в течение 2 часов, больше или равный объему, вычисленному в соответствии с уравнением (4.2):
|
в котором PV и Al, в каждом случае, является таким, как определено выше для уравнения 4.1. Поскольку уравнение 4.2 дает более высокое значение PV для любого данного [Al], объем пор таких неорганических композитных оксидов после прокаливания при 900°C в течение 2 часов неизбежно также будет больше или равен объему, вычисленному в соответствии с уравнением (4.1).
Неорганический оксид по настоящему изобретению показывает гомогенное перемешивание церия, циркония и любых необязательных допирующих элементов на молекулярном уровне и отличается тем, что оксиды церия и циркония формируют твердый раствор, а не смесь бинарных оксидов церия и оксидов циркония. Гомогенное перемешивание церия и циркония подтверждается методом рентгеноструктурного анализа существованием в дополнение к кристаллическим фазам, относящимся к оксиду алюминия, одной одиночной кристаллической фазы, относящейся к кристаллической структуре флуоритного типа, не соответствующей существующим нескольким кристаллическим фазам, относящимся к различным бинарным оксидам оксида церия, оксида циркония или, в конечном итоге, оксидам допирующих элементов.
Неорганический оксид по настоящему изобретению показывает улучшенную устойчивость фаз. В одном варианте осуществления неорганический композитный оксид показывает кристаллическую структуру до прокаливания и сохраняет по существу ту же самую кристаллическую структуру после прокаливания при 900°C в течение 2 часов. В частности, после прокаливания метод рентгеноструктурного анализа не дал доказательства значительного количества альфа-оксида алюминия или разделения фаз для кристаллической фазы оксид церия - оксид циркония. В одном варианте осуществления неорганический композитный оксид показывает кристаллическую структуру до прокаливания и сохраняет по существу ту же самую кристаллическую структуру после прокаливания при 900°C в течение 2 часов и после прокаливания при 1100°C в течение 5 часов. В одном варианте осуществления неорганический композитный оксид показывает кристаллическую структуру до прокаливания и сохраняет по существу ту же самую кристаллическую структуру после прокаливания при 900°C в течение 5 часов и после прокаливания при 1100°C в течение 5 часов. В одном варианте осуществления неорганический композитный оксид показывает кристаллическую структуру до прокаливания и сохраняет по существу ту же самую кристаллическую структуру после прокаливания при 900°C в течение 2 часов, после прокаливания при 1100°C в течение 5 часов и после прокаливания при 1200°C в течение 5 часов.
Пористый неорганический композитный оксид по настоящему изобретению изготавливают взаимодействием алюминийсодержащих прекурсорных материалов, цирконий- и/или церийсодержащих прекурсорных материалов и необязательных прекурсорных материалов допирующего элемента в водной среде. Используемая в настоящем изобретении водная среда представляет собой среду, включающую воду, и которая может дополнительно включать одну или более растворимых в воде органических жидкостей, таких как, например, низшие спирты, такие как метанол, этанол, пропанол и бутанол, низшие гликоли, такие как этиленгликоль и пропиленгликоль, и низшие кетоны, такие как ацетон и метилэтилкетон.
В одном варианте осуществления:
(i) частицы, включающие гидрат алюминия, и
(ii) частицы, включающие гидрат циркония, или частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия, формируют последовательно:
(1.1) формируя частицы гидрата алюминия в водной среде при температуре больше чем 50°C,
(1.2) после стадии (a) (1.1) регулируя pH водной среды до pH от 4 до 6, и
(1.3) после стадии (a) (1.2) формируя частицы, включающие гидрат циркония, частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия, в водной среде, содержащей частицы гидрата алюминия, типично при температуре больше чем 50°C.
Гидратированный оксид алюминия, такой как, например, Al(OH)3, боемит, гиббсит или байерит или их смесь, формируют в водной среде. Гидратированный оксид алюминия можно сформировать в водной среде из водорастворимых солей алюминия разнообразными известными методами, такими как, например, добавление гидроксида аммония к водному раствору галогенида алюминия, такого как хлорид алюминия, или взаимодействие сульфата алюминия с алюминатом щелочного металла, таким как алюминат натрия, в водной среде. Подходящие водорастворимые соли алюминия включают катион алюминия Al3+ и отрицательно заряженный противоион или алюминийсодержащий анион, такой как Al(OH)4- и положительно заряженный противоион. В одном варианте осуществления водорастворимые соли алюминия включают одну или более водорастворимых солей алюминия, каждая из которых независимо включает катион алюминия и отрицательно заряженный противоион, такие как, например, соли, представляющие собой галогенид алюминия, или соли, представляющие собой сульфат алюминия. В другом варианте осуществления водорастворимые соли алюминия включают одну или более водорастворимых солей алюминия, каждая из которых независимо включает анион алюминия и положительно заряженный противоион, такие как, например, водорастворимые алюминатные соли щелочного металла. В другом варианте осуществления водорастворимые соли алюминия включают одну или более водорастворимых солей алюминия, каждая из которых независимо включает катион алюминия и отрицательно заряженный противоион, и одну или более водорастворимых солей алюминия, каждая из которых независимо включает анион алюминия и положительно заряженный противоион.
В одном варианте осуществления водорастворимый алюминиевый прекурсор вводят в реактор в форме водного раствора водорастворимого алюминиевого прекурсора. Кислотность такого раствора алюминиевого прекурсора можно необязательно регулировать в широком диапазоне посредством добавления кислоты или основания. Например, можно добавить кислоту, такую как азотная кислота, хлористоводородная кислота, серная кислота или их смесь, чтобы увеличить кислотность раствора сульфата алюминия или хлорида алюминия, или можно добавить основание, такое как гидроксид натрия, гидроксид калия или их смесь, чтобы уменьшить кислотность раствора алюмината натрия. В одном варианте осуществления кислотность раствора алюминиевого прекурсора регулируют перед введением раствора прекурсора в реактор, добавляя кислоту к раствору алюминиевого прекурсора. В одном варианте осуществления кислотность раствора алюминиевого прекурсора регулируют перед введением раствора прекурсора в реактор, добавляя основание к раствору алюминиевого прекурсора.
В одном варианте осуществления затравочные кристаллы гидрата алюминия сначала формируют при кислотном pH в очень разбавленной водной системе и большее количество гидрата алюминия затем осаждают на затравочных кристаллах при pH примерно от 3 до 6.
В одном варианте осуществления затравочные кристаллы гидрата алюминия формируют взаимодействием сульфата алюминия и алюмината натрия в водной среде при pH примерно от 2 до 5 в реакционном сосуде и большее количество гидрата алюминия затем осаждают на затравочных кристаллах, одновременно подавая водные потоки сульфата алюминия и алюмината натрия в реакционный сосуд, в то же время давая возможность постепенно увеличивать pH водной среды до pH примерно от 3 до 6, более типично примерно от 5 до 6. Температура водной среды в течение формирования гидратированного оксида алюминия типично находится в диапазоне примерно от 30°C до 100°C, более типично примерно от 50°C до 100°C, еще более типично примерно от 55°C до 100°C и еще более типично от 60°C до менее чем 100°C.
В одном варианте осуществления затравочные кристаллы гидрата алюминия формируют взаимодействием сульфата алюминия и алюмината натрия в водной среде при pH примерно от 2 до 5 в реакционном сосуде и большее количество гидрата алюминия затем осаждают на затравочных кристаллах, одновременно подавая водные потоки сульфата алюминия и алюмината натрия в реакционный сосуд, в то же время давая возможность постепенно увеличивать pH водной среды до pH примерно от 3 до 6, более типично примерно от 4 до 5. Температура водной среды в течение формирования гидратированного оксида алюминия типично находится в диапазоне примерно от 30°C до 100°C, более типично примерно от 50°C до 100°C, еще более типично примерно от 55°C до 100°C и еще более типично от 60°C до менее чем 100°C. Было обнаружено, что частицы гидрата алюминия или контактирующие с кремнеземным прекурсором частицы оксида алюминия из альтернативного варианта осуществления имеют тенденцию демонстрировать, после прокаливания, особенно высокий удельный объем пор, где доля объема пор, вносимая порами с небольшим диаметром, является особенно низкой.
В одном варианте осуществления формирование затравочных кристаллов гидрата алюминия пропускают и гидрат алюминия формируют непосредственно, одновременно подавая водные потоки сульфата алюминия и алюмината натрия в реакционный сосуд, в то же время давая возможность постепенно увеличивать pH водной среды до pH примерно от 3 до 6, более типично примерно от 4 до 5. Температура водной среды в течение формирования гидратированного оксида алюминия типично находится в диапазоне примерно от 30°C до 100°C, более типично примерно от 50°C до 100°C, еще более типично примерно от 55°C до 100°C и еще более типично от 60°C до менее чем 100°C. Было обнаружено, что частицы гидрата алюминия или контактирующие с кремнеземным прекурсором частицы оксида алюминия из альтернативного варианта осуществления имеют тенденцию демонстрировать, после прокаливания, особенно высокий удельный объем пор, где доля объема пор, вносимая порами с небольшим диаметром, является особенно низкой.
В одном варианте осуществления осаждение частиц гидрата алюминия из водной среды продолжают, типично давая возможность увеличивать pH водной среды примерно от 8 до 10, более типично примерно от 8,5 до 9,5, чтобы сформировать суспензию частиц гидрата алюминия, суспендированных в водной среде. В одном варианте осуществления, в котором гидрат алюминия формируют одновременной подачей питающих потоков водного сульфата алюминия и водного алюмината натрия в реакционный сосуд, частицы гидрата алюминия можно осадить посредством прерывания подачи потока сульфата алюминия, в то же время продолжая подачу потока алюмината натрия и давая возможность расти pH реакционной смеси посредством продолжающегося добавления алюмината натрия в реакционный сосуд. Для увеличения pH раствора также можно использовать раствор гидроксида натрия или любой щелочи. Количество образующихся частиц гидрата алюминия типично находится в диапазоне примерно от 3 до 50 массовых долей (частей по массе) частиц гидратированного оксида алюминия на 100 массовых долей суспензии. Температура водной среды в течение осаждения гидратированного оксида алюминия типично находится в диапазоне примерно от 30°C до 100°C, более типично примерно от 50°C до 100°C, еще более типично примерно от 55°C до 100°C и еще более типично от 60°C до менее чем 100°C. Водная среда, в которой формируют гидрат алюминия, содержит противоионы водорастворимых солей алюминия, из которых изготавливают гидрат алюминия.
После осаждения частиц гидрата алюминия pH водной суспензии частиц гидрата алюминия регулируют до pH от 4 до 6 и затем в водной среде, содержащей частицы гидрата алюминия, формируют частицы, включающие гидрат циркония, частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия.
В одном варианте осуществления водорастворимый материал циркониевого прекурсора и/или цериевого прекурсора вводят в реактор в форме водного раствора материала-прекурсора. Подходящие водорастворимые циркониевые прекурсоры включают, например, нитрат циркония, оксихлорид циркония, сульфат циркония, ортосульфат циркония, ацетат циркония, лактат циркония и смешанный карбонат циркония-аммония, а также их смеси, такие как смеси нитрата циркония и сульфата циркония. Подходящие водорастворимые цериевые прекурсоры включают, например, нитрат трехвалентного церия, нитрат четырехвалентного церия, сульфат трехвалентного церия, сульфат четырехвалентного церия и смешанный карбонат четырехвалентного церия-аммония, а также их смеси, такие как смеси нитрата трехвалентного церия и нитрата четырехвалентного церия. Кислотность такого раствора прекурсора можно необязательно регулировать в широком диапазоне посредством добавления кислоты или основания. Например, можно добавить кислоту, такую как азотная кислота, хлористоводородная кислота, серная кислота или их смесь, чтобы увеличить кислотность раствора прекурсора, или можно добавить основание, такое как гидроксид натрия, гидроксид калия или их смесь, чтобы снизить кислотность раствора прекурсора. В одном варианте осуществления кислотность раствора прекурсора корректируют перед введением раствора прекурсора в реактор, добавляя кислоту в раствор прекурсора. В одном варианте осуществления кислотность раствора прекурсора корректируют перед введением раствора прекурсора в реактор, добавляя основание в раствор прекурсора. Альтернативно материалы-прекурсоры циркония и/или церия можно ввести в виде коллоидной дисперсии цирконийсодержащего или церийсодержащего материала, такого как соль циркония или соль церия, в органической жидкости, типично водорастворимой органической жидкости, такой как описана выше в качестве подходящих компонентов водной среды.
В одном варианте осуществления, когда нитрат трехвалентного церия используют в качестве цериевого прекурсора, предпочтительно, чтобы водная среда содержала пероксид водорода в течение осаждения частиц гидрата церия или гидрата церия-циркония. Пероксид водорода можно смешать, например, с раствором цериевого прекурсора перед добавлением раствора цериевого прекурсора в реактор. Молярное отношение молей пероксида водорода к молям церия типично составляет от примерно 1 до 6, более типично от примерно 3 до 6.
В одном варианте осуществления частицы гидрата алюминия формируют в водной среде, и затем формируют частицы гидрата циркония, вводя растворимый циркониевый прекурсор в водную среду вслед за формированием частиц гидрата алюминия. В одном варианте осуществления частицы гидрата алюминия формируют в водной среде, и затем формируют частицы гидрата церия, вводя растворимый цериевый прекурсор в водную среду вслед за формированием частиц гидрата алюминия. В одном варианте осуществления частицы гидрата алюминия формируют в водной среде, и затем формируют частицы гидрата циркония и гидрата церия, вводя циркониевый прекурсор и цериевый прекурсор в водную среду вслед за формированием частиц гидрата алюминия.
Материалы-прекурсоры циркония или церия типично добавляют в водную среду, содержащую гидрат алюминия, при температуре больше чем 50°C, более типично от более чем 50°C до примерно 100°C и еще более типично от примерно 55°C до 100°C и еще более типично от 60°C до менее чем 100°C, в то же время поддерживая pH водной среды в диапазоне от 4 до 6. После добавления всего количества материалов-прекурсоров циркония и церия pH регулируют до pH больше чем 7, более типично до pH от 8 до 9, чтобы осадить частицы, включающие гидрат циркония, частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия в жидкой среде, содержащей гидрат алюминия.
В другом варианте осуществления:
(i) частицы, включающие гидрат алюминия, и
(ii) частицы, включающие гидрат циркония, или частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия, формируют одновременно, формируя частицы, включающие гидрат алюминия, и частицы, включающие гидрат циркония, или частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия, в водной среде при температуре больше чем 50°C.
В одном варианте осуществления частицы гидрата алюминия и частицы гидрата циркония формируют одновременно, вводя алюминиевый прекурсор и циркониевый прекурсор в реактор до образования частиц гидрата алюминия. В одном варианте осуществления частицы гидрата алюминия и частицы гидрата церия формируют одновременно, вводя алюминиевый прекурсор и цериевый прекурсор в реактор до образования частиц гидрата алюминия. В одном варианте осуществления частицы гидрата алюминия, частицы гидрата циркония и частицы гидрата церия формируют одновременно, вводя алюминиевый прекурсор, циркониевый прекурсор и цериевый прекурсор в реактор до образования частиц гидрата алюминия.
В одном варианте осуществления алюминиевый материал-прекурсор, циркониевый и/или цериевый материалы-прекурсоры вводят в реактор, и частицы гидрата алюминия, гидрата циркония и/или гидрата церия формируют при условиях, описанных выше, в последовательном варианте осуществления способа по настоящему изобретению, в качестве подходящих для формирования частиц гидрата алюминия. В одном варианте осуществления алюминиевые материалы-прекурсоры, циркониевые и/или цериевые материалы-прекурсоры вводят в реактор при температуре, больше или равной 50°C, более типично при температуре от 55°C до 100°C и еще более типично от 60°C до менее чем 100°C. В одном варианте осуществления pH водной среды дают возможность расти до диапазона от примерно 8 до 10, более типично примерно от 8,5 до 9,5 в течение добавления алюминиевого материала-прекурсора, циркониевого материала-прекурсора и/или цериевого материала-прекурсора в реактор, и по мере того, как pH растет, формируются (i) частицы, включающие гидрат алюминия, и (ii) частицы, включающие гидрат циркония, или частицы, включающие гидрат церия, или частицы, включающие гидрат циркония и гидрат церия. В другом варианте осуществления pH водной среды поддерживают в диапазоне примерно от 4 до 6 в течение добавления алюминиевого материала-прекурсора, циркониевого материала-прекурсора и/или цериевого материала-прекурсора в реактор и затем увеличивают до pH больше 8, давая возможность формирования (i) частиц, включающих гидрат алюминия, и (ii) частиц, включающих гидрат циркония, или частиц, включающих гидрат церия, или частиц, включающих гидрат циркония и гидрат церия.
В каждом случае контакт гидрата алюминия с материалами циркониевого прекурсора и/или цериевого прекурсора типично проводят в водной среде и в присутствии противоионов одной или более водорастворимых солей алюминия. В одном варианте осуществления в водной среде присутствуют один или более отрицательно заряженных противоионов, таких как галогенид-анионы или сульфат-анионы. В одном варианте осуществления в водной среде присутствуют один или более положительно заряженных противоионов, таких как катионы щелочных металлов. В одном варианте осуществления в водной среде присутствуют один или более отрицательно заряженных противоионов и один или более положительно заряженных противоионов.
Заданные допирующие элементы типично вводят в пористый неорганический композитный оксид по настоящему изобретению, добавляя прекурсор допирующего элемента, типично водорастворимую соль желаемого допирующего элемента, в реакционный сосуд в течение вышеописанного формирования гидратированного оксида алюминия и/или в течение добавления материалов циркониевого прекурсора и/или цериевого прекурсора. Подходящие прекурсоры допирующих элементов включают водорастворимые соли соответствующего допирующего элемента, такие как, например, нитрат иттрия, хлорид иттрия, ацетат иттрия, нитрат лантана, хлорид лантана, ацетат лантана, нитрат празеодима, хлорид празеодима, ацетат празеодима, нитрат неодима, хлорид неодима, ацетат неодима, нитрат гадолиния, хлорид гадолиния, ацетат гадолиния и их смеси.
Цирконий, церий и/или допирующие элементы также можно ввести в виде коллоидной дисперсии элемента в растворителе, где растворитель может содержать дополнительные ионы для стабилизации дисперсии. Чтобы обеспечить хорошую стабильность коллоидной суспензии и получить высокую дисперсию элементов внутри пористого неорганического композитного оксида, размер коллоидных частиц предпочтительно составляет от 1 до 100 нм. Цирконий, церий и/или допирующие элементы можно ввести в реакционную смесь одновременно в виде элементов в форме коллоидных частиц элемента и в виде водного раствора ионных соединений данного элемента.
Материалы прекурсора оксида циркония и/или церия и необязательного допирующего элемента можно вводить в периодическом режиме или в непрерывном режиме. В одном варианте осуществления способа в периодическом режиме материалы прекурсоров вводят в реакционный сосуд, содержащий гидрат алюминия и водную среду, в то время как содержимое реакционного сосуда перемешивают. В другом варианте осуществления в периодическом режиме материалы прекурсоров вводят в реакционный сосуд одновременно с загрузкой водорастворимых солей алюминия и содержимое реакционного сосуда перемешивают. В одном варианте осуществления непрерывного способа потоки водной суспензии гидрата алюминия и водные растворы материалов циркониевого прекурсора, цериевого прекурсора и прекурсора допирующего элемента подают во встроенное в линию смешивающее устройство.
В одном варианте осуществления допирующий элемент вводят, добавляя прекурсор допирующего элемента, типично в форме водного раствора допирующего элемента, либо в виде отдельного потока поступающего материала, либо смешивая раствор прекурсора допирующего элемента с одним из исходных материалов, включающих в себя материалы алюминиевого прекурсора, в реакционный сосуд в течение образования частиц гидратированного гидрата алюминия.
В другом варианте осуществления допирующий элемент вводят, добавляя прекурсор допирующего элемента, типично в форме водного раствора допирующего элемента, в реакционный сосуд после образования частиц гидратированного оксида алюминия, либо в виде отдельного потока поступающего материала, либо смешивая раствор прекурсора допирующего элемента с одним из потоков поступающего материала, содержащих материал циркониевого прекурсора или материал цериевого прекурсора. В данном случае pH водной суспензии частиц гидратированного оксида алюминия типично регулируют до pH примерно от 4 до 9 кислотой, такой как азотная кислота, серная кислота или уксусная кислота, перед добавлением раствора прекурсора допирующего элемента. Раствор прекурсора допирующего элемента затем добавляют в реакционный сосуд при непрерывном энергичном перемешивании. После завершения данного добавления pH обычно регулируют до pH примерно от 6 до 10, добавляя основание, такое как гидроксид аммония или гидроксид натрия.
В одном варианте осуществления смесь частиц гидрата алюминия, материалов прекурсора оксида циркония и/или церия и материалов прекурсора необязательного допирующего элемента нагревают до температуры выше температуры окружающей среды, более типично до температуры примерно от 50°C до 200°C в течение периода времени примерно от 20 минут до 6 часов, более типично примерно от 20 минут до 1 часа. Для температур больше чем 100°C нагревание проводят в сосуде для работы под давлением при давлении, больше чем атмосферное давление.
Осажденные частицы, включающие гидраты алюминия, циркония, церия и/или допирующего элемента, затем отделяют от водной среды типично фильтрованием. В одном варианте осуществления перед отделением частиц от водной среды pH суспензии частиц гидрата алюминия, контактирующих с материалом прекурсора, в водной среде регулируют до pH примерно от 4 до 10, вводя в суспензию кислоту, типично кислоту, включающую азотную кислоту, серную кислоту или уксусную кислоту.
В одном варианте осуществления частицы гидрата алюминия, контактирующие с материалом прекурсора оксида циркония и/или церия, промывают для удаления остатков. В одном варианте осуществления перед отделением частиц от водной среды в суспензию частиц в водной среде добавляют одну или более водорастворимых солей, чтобы улучшить эффективность промывки. Подходящие водорастворимые соли включают, например, нитрат аммония, сульфат аммония, гидроксид аммония, карбонат аммония, карбонат калия, карбонат натрия, бикарбонат алюминия и их смеси.
Промывку можно провести, используя горячую воду и/или водный раствор водорастворимой соли аммония, такой как, например, нитрат аммония, сульфат аммония, гидроксид аммония, карбонат аммония, карбонат калия, карбонат натрия, бикарбонат алюминия и аналогичные или их смеси. В одном варианте осуществления стадии промывки суспензию частиц гидрата алюминия или частиц гидрата алюминия с оболочкой из оксида металла обезвоживают, затем промывают водным раствором водорастворимой соли аммония, затем обезвоживают, затем промывают водой и затем снова обезвоживают, формируя влажный осадок промытых частиц на фильтре.
В одном варианте осуществления влажный осадок на фильтре из промытых частиц гидрата алюминия, контактирующих с материалом прекурсора оксида циркония и/или церия, повторно диспергируют в воде, формируя вторую водную суспензию.
В одном варианте осуществления вторую водную суспензию затем подвергают распылительной сушке для получения частиц гидрата алюминия, контактирующих с материалом прекурсора оксида циркония и/или церия. В другом варианте осуществления, pH второй водной суспензии регулируют до pH примерно от 4 до 10, более типично примерно от 6 до 8,5, введением кислоты, такой как кислота, указанная выше относительно регулирования pH суспензии частиц гидрата алюминия, контактирующего с материалом прекурсора оксида циркония и/или церия, в водной среде, или основания, такого как гидроксид натрия, во вторую водную суспензию. В одном варианте осуществления вторую суспензию с отрегулированным pH затем нагревают до температуры выше температуры окружающей среды, более типично до температуры примерно от 50°C до 200°C, еще более типично до температуры примерно от 80°C до 200°C, в течение периода времени примерно от 20 минут до 6 часов, более типично примерно от 20 минут до 1 часа. Для температур больше чем 100°C нагревание проводят в сосуде для работы под давлением при давлении больше, чем атмосферное давление. Частицы гидрата алюминия, контактирующего с материалом прекурсора оксида циркония и/или церия, второй суспензии с отрегулированным pH затем отделяют от водной среды второй суспензии. В одном варианте осуществления частицы гидрата алюминия, контактирующего с материалом прекурсора оксида циркония и/или церия, отделенные от второй суспензии, повторно диспергируют в воде, формируя третью водную суспензию, и третью водную суспензию подвергают распылительной сушке.
Отделенные или отделенные, повторно диспергированные и подвергнутые распылительной сушке частицы гидрата алюминия, содержащие материал прекурсора оксида циркония и/или церия, затем прокаливают, получая желаемый оксид алюминия или продукт, представляющий собой оксид алюминия, покрытый оксидом металла. В одном варианте осуществления частицы гидрата алюминия, контактирующего с материалом прекурсора оксида циркония и/или церия, прокаливают при повышенной температуре типично от 400°C до 1100°C в течение периода времени, больше или равного примерно 30 минутам, более типично примерно от 1 до 5 часов, с получением пористого неорганического композитного оксидного продукта. Прокаливание можно провести на воздухе или в азоте, необязательно в присутствии вплоть до 20% водных паров.
В одном варианте осуществления частицы неорганического оксида прокаливают при температуре больше чем 400°C, более типично примерно от 600°C до 1100°C, в течение периода времени, больше или равного 1 часу, более типично примерно от 2 до 4 часов.
Пористый неорганический композитный оксид по настоящему изобретению, в особенности когда он в форме порошка с размером частиц от 1 до 200 мкм, более типично от 10 до 100 мкм, можно далее использовать в качестве каталитического покрытия на подложке с низкой площадью поверхности. Структуру подложки можно выбрать из разнообразных форм для конкретного использования. Такие структурные формы включают сплошную подложку, ячеистую структуру, проволочную сетку и аналогичные. Структуру подложки обычно формируют из огнеупорного материала, такого как, например, оксид алюминия, смешанный оксид кремния-алюминия, смешанный оксид кремния-магния-алюминия, оксид циркония, муллит, кордиерит, а также из проволочной сетки и аналогичного. Также можно использовать металлические ячеистые структуры. Порошок суспендируют в воде, переводят в состояние коллоидного раствора добавлением небольшого количества кислоты (типично минеральных кислот) и затем подвергают помолу, вызывая уменьшение размера частиц до размера, подходящего для нанесения покрытия из пористого оксида. Структура подложки контактирует с измельченной суспензией, например посредством погружения подложки в суспензию. Избыточный материал удаляют, например, используя обдув воздухом, после чего следует прокаливание покрытой структуры подложки, вызывая адгезию частиц оксида алюминия с высокой площадью поверхности, покрытых (пористым) диоксидом кремния, по настоящему изобретению к структуре подложки.
Благородные металлы, обычно металлы платиновой группы, такие как платина, палладий, родий и их смеси, можно наносить способами, хорошо известными специалистам в данной области, либо до нанесения покрытия частиц пористого оксида алюминия с кремнеземной оболочкой, используя подходящий традиционный прекурсор благородного металла (кислотный или основной), либо после нанесения покрытия из пористого оксида, погружая покрытую пористым оксидом подложку в раствор подходящего прекурсора благородного металла (кислотного или основного). Более типично формируют пористый неорганический композитный оксид, после чего следует нанесение на него благородного металла и, наконец, наносят материал катализатора с нанесенным пористым неорганическим композитным оксидом на подложку.
Пористый неорганический композитный оксид по настоящему изобретению можно смешать с другими оксидными носителями, аналогичными оксиду алюминия, оксиду магния, оксиду церия, смешанному оксиду церия-циркония, смесям оксид редкоземельного металла-оксид циркония и т.д., и затем нанести данные пористые продукты на подложку. Полученный в результате катализатор можно непосредственно загрузить в контейнеры и аналогичное либо по отдельности, либо в комбинации с другими материалами в качестве части системы выпуска выхлопных газов двигателя внутреннего сгорания. Таким образом, продукты выхлопа, которые обычно включают кислород, монооксид углерода, диоксид углерода, углеводороды, оксиды азота, серу, серосодержащие соединения и оксиды серы, пропускают через выхлопную систему, обеспечивая контакт с катализатором на основе нанесенного благородного металла. Результат обеспечивает превращение токсичных и вредных выхлопных продуктов в более приемлемые для окружающей среды материалы. При использовании катализатора, сформированного с носителем по настоящему изобретению, получают каталитическую систему, имеющую длительный срок службы и более высокую общую активность по сравнению с параметрами, достижимыми при использовании катализаторов, имеющих носитель либо без кремнезема, либо с кремнеземом-оксидом алюминия, сформированным традиционными методиками соосаждения или импрегнирования.
Следующие ниже примеры даны в качестве конкретной иллюстрации заявляемого изобретения. Однако следует понимать, что изобретение не ограничивается конкретными деталями, изложенными в примерах. Все доли и проценты в примерах и в оставшейся части описания являются массовыми, если не указано иное.
Далее подразумевается, что любые диапазоны чисел, перечисляемые в описании или формуле изобретения, такие как представляющие конкретный ряд свойств, единицы измерения, условия, физическое состояние или процентное содержание, ясно и точно включают здесь ссылкой или иным образом любое число, попадающее внутрь такого диапазона, включая любое подмножество чисел внутри любого диапазона, перечисленного таким образом.
Примеры 1-23 и сравнительный пример С1
Если не указано иным образом, состав каждого из композитных оксидов из примеров 1-23 и примера сравнения С1 дан в виде относительных количеств оксидов алюминия, циркония, церия и необязательных допирующих элементов в композитном оксиде, основанных на объединенном количестве оксидов алюминия, циркония, церия и необязательных допирующих элементов в композитном оксиде, каждое из которых выражено в виде количества отдельного бинарного оксида соответствующего элемента. Если не указано иным образом, прокаливание, на которое ссылаются в различных примерах, проводили на воздухе.
Аналитические результаты каждого из составов примеров 1-23 и примера сравнения С1 представлены в таблице 1 ниже в виде площади поверхности (SA (м2/г)), объема пор (PV (см3/г)), среднего диаметра пор (APD (нм)), площади поверхности после прокаливания при 1100°C в течение 5 часов (SA 1100/5ч (м2/г)), площади поверхности после прокаливания при 1200°C в течение 5 часов (SA 1200/5ч (м2/г)) и размера кристаллитов смешанного оксида церия-циркония после прокаливания при 1200°C в течение 5 часов (Fcryst 1200/5ч (нм)). Если не указано иным образом, распределения размеров пор, объем пор, диаметр пор и удельная площадь поверхности по БЭТ получены методом адсорбции азота с использованием прибора Micromeretics Tristar 3000. Данные по распределению размеров пор и объему пор собраны, используя 91 точку измерения между P/P0=0,01 и P/P0=0,998. Удельные площади поверхности (SA) сообщаются в квадратных метрах на грамм (м2/г)), объемы пор сообщаются в кубических сантиметрах на грамм (см3/г), средний диаметр пор сообщается в нанометрах (нм), температуры прокаливания сообщаются в градусах Цельсия (°C) и времена сообщаются в часах (час). Где это предоставлено, данные распределения размера пор по ртутной порометрии получены на Micromeretics Autopore Apparatus с 103 точками измерения между 0,5 фунт/кв. дюйм абс. (3,4 кПа) и 30000 фунт/кв. дюйм абс. (206,8 МПа). Анализ просвечивающей электронной микроскопией проводили на ультратонких срезах материала (от 20 до 100 нм по толщине).
Пример 1
Композитный оксид из примера 1 содержал, исходя из 100 массовых долей композитного оксида, 33 массовые доли Al2O3, 36 массовых долей CeO2, 27 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили, используя водные растворы следующих прекурсоров: сульфата алюминия (концентрация 8,3% масс. по Al2O3), нитрата церия (26,9% масс. по CeO2), ортосульфата циркония (17,2% масс. по ZrO2), нитрата иттрия (13,9% масс. по Y2O3), и раствор, содержащий смесь нитрата лантана и нитрата празеодима (общее содержание оксида 27% масс. по La2O3 и Pr6O11 с отношением La2O3/Pr6O11 90/10 по массе).
Кислый раствор (раствор A) готовили, смешивая вместе все растворы прекурсоров в пропорциях относительно конечного состава и на основе общего оксида, составляющего 50 граммов, для конечного материала. Температуру в реакторе поддерживали при 65°C от начала осаждения до фильтрования. Некоторое количество деионизированной воды добавляли в обогреваемый 1 литровый реактор, оборудованный перемешивающим устройством. Раствор A вводили при перемешивании в реактор в течение 60 минут. В ходе введения раствора A pH регулировали при значении 9, вводя в реактор раствор гидроксида натрия (концентрация 25% масс. по NaOH). После добавления всего раствора A поток раствора гидроксида натрия поддерживали, чтобы значение pH достигло величины 9,6 в течение 10 минут. Затем содержимое реактора фильтровали и промывали деионизированной водой при 60°C в воронке Бюхнера, получая влажный осадок на фильтре. Объем промывочной воды был эквивалентен объему водной среды в реакторе. Раствор готовили, растворяя 120 г бикарбоната аммония в литре воды и нагревая до 60°C. Влажный осадок на фильтре промывали объемом раствора бикарбоната аммония, соответствующим двукратному объему водной среды в реакторе, и затем промывали таким же объемом деионизированной воды при 60°C. Полученный в результате влажный осадок на фильтре затем диспергировали в деионизированной воде, получая суспензию, содержащую примерно 10% масс. твердого вещества. Затем суспензию подвергали распылительной сушке, получая высушенный порошок. Затем порошок, подвергнутый распылительной сушке, прокаливали при 900°C в течение 2 часов.
После прокаливания при 900°C в течение 2 часов композитный оксид примера 1 прокаливали при более высокой температуре.
Фиг. 1 показывает рентгеновскую дифрактограмму порошка, соответствующего композиции из примера 1, после прокаливания при 1200°C в течение 10 часов. Видны только две кристаллические фазы, соответствующие тэта-оксиду алюминия и кубической фазе, типичной для твердого раствора церия и циркония. Не было обнаружено никакого свидетельства бинарных оксидов, относящихся соответственно к лантану, иттрию и празеодиму. Это показывает, что данные допирующие элементы включены в кристаллическую матрицу, формируя твердый раствор с основными компонентами. Производный логарифмический график распределения размера пор для композиции из примера 1 после прокаливания при 900°C в течение 2 часов показан на фиг. 2.
Сравнительный пример 1
Композитный оксид из примера сравнения 1 содержал, исходя из 100 массовых долей композитного оксида, 33 массовые доли Al2O3, 36 массовых долей CeO2, 27 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 1, за исключением того, что температуру устанавливали при 45°C.
Фиг. 3 показывает рентгеновскую дифрактограмму порошка, соответствующего композиции из примера сравнения 1, после прокаливания при 1200°C в течение 5 часов. Видны только две кристаллические фазы, соответствующие тэта-оксиду алюминия и кубической фазе, типичной для твердого раствора церия и циркония.
Пример 2
Композитный оксид из примера 2 содержал, исходя из 100 массовых долей композитного оксида, 50 массовых долей Al2O3, 28 массовых долей CeO2, 18 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 1.
Пример 3
Композитный оксид из примера 3 содержал, исходя из 100 массовых долей композитного оксида, 50 массовых долей Al2O3, 28 массовых долей CeO2, 18 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 1 за исключением того, что прекурсоры распределяли между двумя растворами, причем данные два раствора вводили в реактор одновременно при перемешивании. Раствор A готовили, смешивая вместе сульфат алюминия и половину общего раствора, необходимого для лантана и празеодима. Раствор B готовили, смешивая вместе нитрат церия, ортосульфат циркония, нитрат иттрия, половину общего раствора, необходимого для лантана и празеодима, и 52 г воды. Растворы A и B водили в реактор одновременно вместе с гидроксидом натрия.
Пример 4
Композитный оксид из примера 4 содержал, исходя из 100 массовых долей композитного оксида, 67 массовых долей Al2O3, 16 массовых долей CeO2, 13 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному выше в примере 3 за исключением двух следующих отличий: раствор A содержал две трети общего раствора, необходимого для лантана и празеодима, и пероксид водорода (концентрация 35% масс. по H2O2) добавляли в раствор B, чтобы молярное отношение H2O2/CeO2 было равно 3.
Пример 5
Композитный оксид из примера 5 содержал, исходя из 100 массовых долей композитного оксида, 33 массовые доли Al2O3, 36 массовых долей CeO2, 27 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 1, за исключением того, что в кислый раствор перед осаждением добавляли пероксид водорода (концентрация 35% масс. по H2O2). Количество пероксида водорода устанавливали, чтобы молярное отношение H2O2/CeO2 было равно 3.
Пример 6
Композитный оксид из примера 6 содержал, исходя из 100 массовых долей композитного оксида, 47 массовых долей Al2O3, 30 массовых долей CeO2, 19 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили, используя водные растворы следующих прекурсоров: алюмината натрия (24,9% масс. по Al2O3), нитрата церия (26,9% масс. по CeO2), нитрата циркония (21,3% масс. по ZrO2), нитрата иттрия (13,9% масс. по Y2O3), и раствор, содержащий смесь нитрата лантана и нитрата празеодима (общее содержание оксида 27% масс. по La2O3 и Pr6O11, с отношением La2O3/Pr6O11 90/10 по массе).
Раствор A готовили, смешивая вместе нитрат церия, нитрат циркония, нитрат иттрия, раствор, содержащий смесь нитрата лантана и нитрата празеодима, 12,7 г концентрированной азотной кислоты (концентрация 69% масс. по HNO3), пероксид водорода (концентрация 35% масс. по H2O2) и 104 г деионизированной воды. Количество пероксида водорода устанавливали, чтобы молярное отношение H2O2/CeO2 было равно 3. Раствор B готовили, смешивая алюминат натрия с таким же количеством деионизированной воды. Температуру в реакторе поддерживали при 65°C от начала осаждения до фильтрования. Некоторое количество деионизированной воды добавляли в обогреваемый 1 литровый реактор, оборудованный перемешивающим устройством. Раствор A вводили при перемешивании в реактор в течение 50 минут. В ходе введения раствора A pH регулировали при значении 7,3, вводя в реактор раствор B. После добавления всего раствора A поток раствора B поддерживали, чтобы значение pH достигло величины 10 в течение 10 минут. Оставшуюся часть способа проводили, как описано выше в примере 1.
Пример 7
Композитный оксид из примера 7 содержал, исходя из 100 массовых долей композитного оксида, 67 массовых долей Al2O3, 16 массовых долей CeO2, 13 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 6, за исключением того, что количества азотной кислоты и воды в растворе A составляли соответственно 44 г и 60 г.
Пример 8
Композитный оксид из примера 8 содержал, исходя из 100 массовых долей композитного оксида, 33 массовые доли Al2O3, 36 массовых долей CeO2, 27 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 1, за исключением того, что вместо ортосульфата циркония использовали нитрат циркония (21,3% масс. по ZrO2).
Пример 9
Композитный оксид из примера 9 содержал, исходя из 100 массовых долей композитного оксида, 33 массовые доли Al2O3, 36 массовых долей CeO2, 27 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 8, за исключением того, что в кислый раствор перед осаждением добавляли пероксид водорода (концентрация 35% масс. по H2O2). Количество пероксида водорода устанавливали, чтобы молярное отношение H2O2/CeO2 было равно 3.
Пример 10
Композитный оксид из примера 10 содержал, исходя из 100 массовых долей композитного оксида, 67 массовых долей Al2O3, 16 массовых долей CeO2, 13 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 9.
Пример 11
Композитный оксид из примера 11 содержал, исходя из 100 массовых долей композитного оксида, 33 массовые доли Al2O3, 36 массовых долей CeO2, 27 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили, используя водные растворы следующих прекурсоров: сульфата алюминия (концентрация 8,3% масс. по Al2O3), алюмината натрия (24,9% масс. по Al2O3), нитрата церия (26,9% масс. по CeO2), ортосульфата циркония (17,2% масс. по ZrO2), нитрата иттрия (13,9% масс. по Y2O3), и раствор, содержащий смесь нитрата лантана и нитрата празеодима (общее содержание оксида 27% масс. по La2O3 и Pr6O11, с отношением La2O3/Pr6O11 90/10 по массе).
Раствор A готовили, смешивая сульфат алюминат и две трети раствора, содержащего смесь нитрата лантана и нитрата празеодима. Раствор B готовили, смешивая вместе нитрат церия, ортосульфат циркония, нитрат иттрия и одну треть раствора, содержащего смесь нитрата лантана и нитрата празеодима. Температуру в реакторе поддерживали при 65°C от начала осаждения до фильтрования. Некоторое количество деионизированной воды добавляли в обогреваемый 1 литровый реактор, оборудованный перемешивающим устройством. Раствор A вводили при перемешивании в реактор в течение 25 минут. В ходе введения раствора A pH регулировали при значении 7,3, вводя в реактор раствор алюмината натрия. После добавления всего раствора A поток раствора алюмината натрия поддерживали, чтобы значение pH достигло величины 9,3 в течение 10 минут. Затем pH снижали до pH 4 разбавленной азотной кислотой. Затем в реактор в течение 20 минут вводили раствор B. В течение введения раствора B pH регулировали при значении 4 посредством введения в реактор раствора аммиака (концентрация 10% масс. по NH4OH). После добавления всего раствора B поток раствора аммиака поддерживали, чтобы pH достигло значения 8,2 в течение 25 минут. Оставшуюся часть способа проводили, как описано выше в примере 1.
Фиг. 5 показывает рентгеновскую дифрактограмму порошка, соответствующего композиции из примера 11, после прокаливания при 1200°C в течение 10 часов. Видны только две кристаллические фазы, соответствующие тэта-оксиду алюминия и кубической фазе, типичной для твердого раствора церия и циркония. Производный логарифмический график распределения размера пор для композиции из примера 11 после прокаливания при 900°C в течение 2 часов показан на фиг. 6. Фиг. 7 и фиг. 8 представляют собой изображения, полученные из анализа прокаленного образца композиции из примера 11 методом просвечивающей электронной микроскопии, и показывают дисперсию наночастиц смешанного цериево-циркониевого оксида на агрегатах оксида алюминия.
Пример 12
Композитный оксид из примера 12 содержал, исходя из 100 массовых долей композитного оксида, 50 массовых долей Al2O3, 28 массовых долей CeO2, 18 массовых долей ZrO2, 1,8 массовой доли La2O3, 2 массовые доли Y2O3 и 0,2 массовой доли Pr6O11, и его готовили, используя водные растворы следующих прекурсоров: алюмината натрия (24,9% масс. по Al2O3), нитрата церия (26,9% масс. по CeO2), нитрата циркония (21,3% масс. по ZrO2), нитрата иттрия (13,9% масс. по Y2O3), и раствор, содержащий смесь нитрата лантана и нитрата празеодима (общее содержание оксида 27% масс. по La2O3 и Pr6O11 с отношением La2O3/Pr6O11 90/10 по массе).
Раствор A готовили, смешивая 53 г концентрированной азотной кислоты (концентрация 69% масс. по HNO3), 110 г деионизированной воды и половину раствора, содержащего смесь нитрата лантана и нитрата празеодима. Раствор B готовили, смешивая вместе нитрат церия, нитрат циркония, нитрат иттрия, пероксид водорода (концентрация 35% масс. по H2O2) и половину раствора, содержащего смесь нитрата лантана и нитрата празеодима. Количество пероксида водорода устанавливали, чтобы молярное отношение H2O2/CeO2 было равно 3. Температуру в реакторе поддерживали при 65°C от начала осаждения до фильтрования. Некоторое количество деионизированной воды добавляли в обогреваемый 1 литровый реактор, оборудованный перемешивающим устройством. Раствор A вводили в реактор при перемешивании в течение 25 минут. В ходе введения раствора A pH регулировали при значении 7,3, вводя в реактор раствор алюмината натрия. После добавления всего раствора A поток раствора алюмината натрия поддерживали, чтобы значение pH достигло величины 9,8 в течение 10 минут. Затем pH снижали до pH 4 разбавленной азотной кислотой. Затем в реактор в течение 20 минут вводили раствор B. В течение введения раствора B pH регулировали при значении 4 посредством введения в реактор раствора аммиака (концентрация 10% масс. по NH4OH). После добавления всего раствора B поток раствора аммиака поддерживали, чтобы pH достигло значения 8,2 в течение 25 минут. Оставшуюся часть способа проводили, как описано выше в примере 1.
Фиг. 9 показывает рентгеновскую дифрактограмму порошка, соответствующего композиции из примера 12, после прокаливания при 1200°C в течение 5 часов. Видны только две кристаллические фазы, соответствующие тэта-оксиду алюминия и кубической фазе, типичной для твердого раствора церия и циркония. Производный логарифмический график распределения размера пор после прокаливания при 900°C в течение 2 часов показан на фиг. 10.
Пример 13
Композитный оксид из примера 13 содержал, исходя из 100 массовых долей композитного оксида, 48 массовых долей Al2O3, 28 массовых долей CeO2, 18 массовых долей ZrO2, 3,6 массовых долей La2O3, 2 массовые доли Y2O3 и 0,4 массовой доли Pr6O11, и его готовили согласно методу, описанному в примере 12 за исключением следующих отличий: раствор A готовили, смешивая вместе 29 г сульфата алюминия (концентрация 8,3% масс. по Al2O3), 33 г концентрированной азотной кислоты, 131 г деионизированной воды и половину раствора, содержащего смесь нитрата лантана и нитрата празеодима. Раствор B готовили, смешивая вместе нитрат церия, нитрат циркония, нитрат иттрия, половину раствора, содержащего смесь нитрата лантана и нитрата празеодима, и пероксид водорода (концентрация 35% масс. по H2O2). Количество пероксида водорода устанавливали, чтобы молярное отношение H2O2/CeO2 было равно 3. Аналитические результаты представлены в таблице 1 ниже.
Пример 14
Композитный оксид из примера 14 содержал, исходя из 100 массовых долей композитного оксида, 50 массовых долей Al2O3, 10 массовых долей CeO2 и 40 массовых долей ZrO2, и его готовили в соответствии со способом, описанным выше в примере 15 за исключением следующей разницы: раствор A готовили, смешивая вместе 58 г сульфата алюминия, 30 г концентрированной азотной кислоты и 175 г деионизированной воды. Раствор B готовили, смешивая вместе нитрат церия, нитрат циркония и пероксид водорода (концентрация 35 массовых процентов по H2O2). Количество пероксида водорода устанавливали таким, чтобы мольное отношение H2O2/CeO2 было равным 6. В течение осаждения раствора A pH поддерживали при значении 5, затем повышали раствором алюмината натрия до значения 9,5. Промежуточное регулирование pH разбавленной азотной кислотой осуществляли при величине 5. В течение добавления раствора B pH поддерживали при значении 5. Температуру устанавливали при 70°C от осаждения раствора A до фильтрования. Прокаливание обработанного распылительной сушкой материала проводили при 930°C в течение 2 часов.
Пример 15
Композитный оксид из примера 15 содержал, исходя из 100 массовых долей композитного оксида, 50 массовых долей Al2O3, 29 массовых долей CeO2 и 21 массовую долю ZrO2, и его готовили в соответствии со способом, описанным выше в примере 16 за исключением следующей разницы: раствор A готовили, смешивая вместе 48 г сульфата алюминия, 25 г концентрированной азотной кислоты и 146 г деионизированной воды. Фиг. 11 показывает рентгеновскую дифрактограмму, полученную на порошке, соответствующем композиции из примера 15, после прокаливания при 900°C в течение 2 часов. Размер кристаллитов, измеренный после главного пика дифрактограммы, соответствующего смешанному оксиду церия-циркония, составлял 5,9 нм. Производный логарифмический график распределения размера пор композиции из примера 15 после прокаливания при 900°C в течение 2 часов показан на фиг. 12.
Пример 16
Композитный оксид из примера 16 содержал, исходя из 100 массовых долей композитного оксида, 30 массовых долей Al2O3, 31 массовую долю CeO2, 27,5 массовых долей ZrO2, 2,3 массовой доли La2O3, 5,5 массовых долей Y2O3, 3,4 массовых долей Nd2O3 и 0,3 массовой доли Pr6O11, и его готовили в соответствии со способом, описанным выше в примере 14, за исключением следующей разницы: раствор A готовили, смешивая вместе 28,9 г сульфата алюминия, 13,3 г концентрированной азотной кислоты, 89 г деионизированной воды и половину раствора, содержащего смесь нитрата лантана и нитрата празеодима (общее содержание оксида 27% масс. по La2O3 и Pr6O11 с соотношением La2O3/Pr6O11 90/10 по массе). Раствор B готовили, смешивая вместе нитрат церия, нитрат циркония, оставшуюся половину раствора, содержащего смесь нитрата лантана и нитрата празеодима, нитрат иттрия, нитрат неодима (концентрация 29,4% по Nd2O3) и пероксид водорода (концентрация 35% масс. по H2O2). После добавления всего раствора B поток раствора аммиака поддерживали, чтобы значение pH достигло величины 8,2 в течение 15 минут.
Фиг. 13 показывает рентгеновскую дифрактограмму, полученную на порошке, соответствующем композиции из примера 16, после прокаливания при 1200°C в течение 5 часов. Пики дифрактограммы, соответствующие смешанным оксидам церия-циркония, характеризуются существованием плеча, особенно видимого для пика при 2 тэта, равного 49,5°. Плечо является свидетельством фазового разделения смешанного оксида церия-циркония, являющегося результатом старения при высокой температуре. Производный логарифмический график распределения размера пор композиции из примера 16 после прокаливания при 900°C в течение 2 часов показан на фиг. 14.
Пример 17
Композитный оксид из примера 17 содержал, исходя из 100 массовых долей композитного оксида, 46,2 массовые доли Al2O3, 26,3 массовых долей CeO2, 24,2 массовых долей ZrO2 и 3,3 массовых долей Pr6O11, и его готовили в соответствии со способом, описанным выше в примере 16, за исключением следующей разницы: раствор A готовили, смешивая вместе 45 г сульфата алюминия, 22 г концентрированной азотной кислоты, 138 г деионизированной воды и одну треть от всего раствора нитрата празеодима (концентрация 27% масс. по Pr6O11). Температуру устанавливали при 65°C от начала осаждения раствора A до фильтрования. В течение осаждения раствора B pH поддерживали при значении 5,5. Прокаливание обработанного распылительной сушкой материала проводили при 850°C в течение 4 часов.
Фиг. 13 показывает рентгеновскую дифрактограмму порошка, соответствующего композиции из примера 17, после прокаливания при 1200°C в течение 5 часов. Видны только две кристаллические фазы, соответствующие тэта-оксиду алюминия и кубической фазе, типичной для твердого раствора церия и циркония. Производный логарифмический график распределения размера пор композиции из примера 17 после прокаливания при 900°C в течение 2 часов показан на фиг. 14.
Пример 18
Композитный оксид из примера 18 содержал, исходя из 100 массовых долей композитного оксида, 50 массовых долей Al2O3 и 50 массовых долей ZrO2, и его готовили, используя водные растворы следующих прекурсоров: алюмината натрия (24,9% масс. по Al2O3), сульфата алюминия (8,3% масс. по Al2O3) и нитрата циркония (21,3% масс. по ZrO2). Раствор A готовили, смешивая вместе нитрат циркония, 46 г сульфата алюминия и 46 г деионизированной воды. Температуру в реакторе поддерживали при 65°C от начала осаждения до фильтрования. Некоторое количество деионизированной воды добавляли в обогреваемый 1 литровый реактор, оборудованный перемешивающим устройством. Сначала в реактор в течение 5 минут добавляли 14 г раствора A. После 5 минут при перемешивании без дополнительного добавления реагентов раствор A вводили при перемешивании в реактор в течение 50 минут. В ходе введения раствора A pH регулировали при значении 9, вводя в реактор раствор алюмината натрия. После добавления всего раствора A поток раствора алюмината натрия поддерживали, чтобы значение pH достигло величины 9,8 в течение 8 минут. Оставшуюся часть способа проводили, как описано выше в примере 1. Фазовый анализ композиции из примера 18 методом рентгеновской дифракции после прокаливания при 1100°C в течение 5 часов показал только чистый тетрагональный оксид циркония и тэта-оксид алюминия.
Пример 19
Композитный оксид из примера 19 содержал, исходя из 100 массовых долей композитного оксида, 90 массовых долей Al2O3, 7,4 массовых долей ZrO2, 0,5 массовых долей La2O3, 1,4 массовых долей Y2O3 и 0,7 массовых долей Nd2O3, и его готовили, используя водные растворы следующих прекурсоров: алюмината натрия (24,9% масс. по Al2O3), сульфата алюминия (8,3% масс. по Al2O3), нитрата циркония (21,3% масс. по ZrO2), нитрата иттрия (13,9% масс. по Y2O3), нитрата неодима (21,3 % по Nd2O3) и нитрата лантана (27,2% масс. по La2O3).
Раствор A готовили, смешивая вместе 141 г сульфата алюминия, нитрата лантана, нитрата иттрия, нитрата неодима, нитрата циркония и 141 г деионизированной воды. Раствор B представлял собой раствор алюмината натрия. Температуру в реакторе поддерживали при 65°C от начала осаждения до фильтрования. Некоторое количество деионизированной воды добавляли в обогреваемый 1 литровый реактор, оборудованный перемешивающим устройством. Сначала в реактор в течение 5 минут добавляли 12 г раствора A. После 5 минут при перемешивании без дополнительного добавления реагентов раствор A вводили при перемешивании в реактор в течение 30 минут. В ходе введения раствора A pH регулировали при значении 5, вводя в реактор раствор B. После добавления всего раствора A поток раствора B поддерживали, чтобы значение pH достигло величины 9,8 в течение 25 минут. Затем pH корректировали до 9 разбавленной азотной кислотой. Оставшуюся часть способа проводили, как описано выше в примере 1. Фазовый анализ композиции из примера 19 методом рентгеновской дифракции после прокаливания при 1200°C в течение 5 часов показал только чистый кубический оксид циркония и тэта-оксид алюминия.
Пример 20
Композитный оксид из примера 20 содержал, исходя из 100 массовых долей композитного оксида, 75 массовых долей Al2O3, 18,5 массовых долей ZrO2, 1,3 массовой доли La2O3, 3,5 массовых доли Y2O3 и 1,8 массовой доли Nd2O3, и его готовили согласно методу, описанному в примере 21, за исключением того, что раствор A готовили, смешивая вместе 141 г сульфата алюминия, нитрата лантана, нитрата иттрия, нитрата неодима, нитрата циркония и 141 г деионизированной воды. Фазовый анализ композиции из примера 20 методом рентгеновской дифракции после прокаливания при 1200°C в течение 5 часов показал только чистый кубический оксид циркония и тэта-оксид алюминия.
|