СМЕСИ О-АЦИЛ-ИЗЕТИОНАТОВ И ПАВ НА ОСНОВЕ N-АЦИЛ-АМИНОКИСЛОТ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
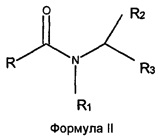
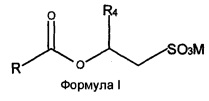
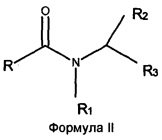
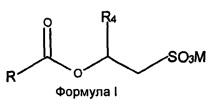
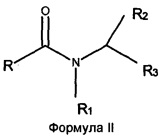
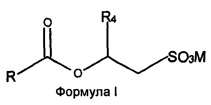
Настоящее изобретение относится к экономически эффективному способу производства гомогенных смесей O-ацил-изетионатов (соединений Формулы (I)) и ПАВ на основе N-ацил-аминокислот (соединений Формулы (II)), где заместитель R выбран из C5-C21 насыщенных или ненасыщенных алкильных групп, R1 означает H или алкильную цепь небольшой длины C1-C4, R2 означает H или любые группы, присутствующие у α-атома углерода природных аминокислот, R3 означает кислотную группу, например карбоксильную или сульфонильную, вместе с противоионом щелочного металла, как, например, COOX, CH2SO3X, где X=Li+, Na+ или K+, R4 означает H или Me, и M представляет собой катион, выбранный из Na+, K+, NH4+ или катиона четвертичного аммония, полученного из третичного амина, из хлорангидридов соответствующих жирных кислот с количественными выходами. Более конкретно настоящее изобретение относится к способу получения O-ацил-изетионатов взаимодействием гидроксиалкил сульфонатов щелочных металлов или аммония с хлорангидридами жирных кислот с последующим взаимодействием оставшегося хлорангидрида жирной кислоты с эквивалентным количеством водного раствора одной или нескольких аминокислот в присутствии основания в водной среде с получением смеси анионных ПАВ, а именно, O-ацил-изетионатов (Формула (I)) и N-ацил-аминокислот (Формула (II)) в любом желаемом соотношении:

ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Современные моющие композиции для личной гигиены предназначены для обеспечения хорошего моющего эффекта, а также других полезных эффектов, например увлажнения кожи. Для достижения превосходного моющего действия и увлажнения кожи традиционно применялись очень высокие уровни окклюзивных (образующих непроницаемую пленку) агентов, например воска. Например, в средствах для мытья тела Dove Cream Oil (Unilever) и Olay Ribbon (Proctor and Gamble) применяется вплоть до 30% мягчительных масел. Предпринимались постоянные усилия для придания моющим композициям способности ухаживать за кожей и волосами путем введения в их состав таких действующих компонентов, как силиконовое масло, вазелин и целый ряд триглицеридов. Сообщалось о применении в некоторых моющих композициях до 50% мягчительных компонентов. (Chambers et al., патент США 5612307 и Pavvada et al., патент США 5965500).
Недавно Tsaur et al. внесли революционные изменения в технологию моющих средств посредством разработки различных комбинаций мягких ПАВ. В патенте США №8263538 описана комбинация ПАВ из числа N-ацил-аминокислот, например N-кокоил-глицинатов натрия и N-кокоил-саркозинатов натрия, с амфотерными/цвиттерионными ПАВ для получения "сверхмягких" композиций личной гигиены, которые демонстрировали общий результат в тесте на раздражение по методике аппликационной пробы менее 75% относительно 0,5%-ного водного раствора додецилсульфата натрия.
В еще одном современном патенте, полученном той же группой (Tsaur et al., патент США №8268767), предложена комбинация моющих ПАВ, которая не только моет и доставляет для кожи полезные агенты, но и является "сверхмягкой" для кожи. Указанные композиции включают как O-ацил-изетионаты, так и ПАВ на основе N-ацил-аминокислот, и эти композиции представляют собой жидкие моющие средства как для кожи, так и для волос. Указано, что эти композиции являются "сверхмягкими" для кожи при тестировании по стандартной методике аппликационной пробы на добровольцах. В упомянутом патенте раскрыты также исключительно мягкие композиции, которые очень эффективно доставляют окклюзивные увлажнители. Аналогично в патенте США №8114824 раскрыты композиции, включающие ПАВ из числа O-ацил-изетионатов и N-ацил-аминокислот, которые могут содержать максимальное количество увлажняющего средства. Говоря вкратце, сообщается, что системы ПАВ, включающие в качестве основных ингредиентов O-ацил-изетионаты и N-ацил-глицинаты или N-ацил-саркозинаты, являются очень хорошими моющими системами, которые являются "сверхмягкими/щадящими" для кожи и представляют собой отличные носители для доставки действующих веществ (полезных агентов, таких как мягчители, силиконы, триглицериды и вазелин). В упомянутых выше патентах сообщается, что "сверхмягкость" и "способность доставлять полезные ингредиенты" возникает из-за дополнительной синергии, которую демонстрирует комбинация двух упомянутых классов мягких ПАВ, а именно O-ацил-изетионатов (Формула (I)) и N-ацил-аминокислот (Формула (II)).
Среди этих мягких ПАВ N-ацил-аминокислоты, а именно N-ацил-глицинаты, саркозинаты, таураты, глутаматы, аланаты и т.д. щелочных металлов или аммония, являются коммерчески доступными для производителей различных составов в форме твердых веществ, а также в форме водных растворов, поскольку они хорошо растворимы в воде. В противоположность этому соответствующие N-ацил-изетионаты демонстрируют практически полную нерастворимость в воде. Например, кокоил-изетионат натрия обладает растворимостью в воде 0,1% при 25°C. (Assessement Plan for Fatty acids, coco, sulfoethyl esters, sodium salts (sodium cocoyl isethionate prepared by Keller and Heckman LLP, Nov 2006)) (План исследования жирных кислот, натриевых солей кокосульфоэтиловых эфиров (кокоил-изетионат натрия получен Keller и Heckman LLP, Nov 2006)). Кроме того, O-ацил-изетионаты щелочных металлов имеют очень высокие температуры плавления, превышающие 200°C. Включение O-ацил-изетионатов с очень высокими температурами плавления в составы для личной гигиены (для мытья тела и мытья лица) предполагает обязательное нагревание состава, которое в некоторых случаях является нежелательным из-за термической чувствительности других ингредиентов, а также из-за затрат энергии на нагревание всей массы ингредиентов. Для преодоления проблемы с включением в составы O-ацил-изетионатов щелочных металлов в твердой форме исследователи разработали удобную для изготовителя состава "Liquid Delivery Systems" (LDS) ("Жидкую систему доставки"), в которой O-ацил-изетионаты щелочных металлов растворяют в водной среде с помощью других ПАВ, в результате чего продукт становится жидким и его легко вводить в составы для личной гигиены (холодное смешивание). В EP0964674 A2 и патенте США №5925603 (Rhodia, Paul D'Angelo) раскрываются концентрированные "Жидкие системы доставки", в которых O-ацил-изетионаты диспергированы с помощью алкилимидазолиновых амфотерных ПАВ и анионных ПАВ. В заявке на патент США №20090062406 и патенте США №5415810 (Clariant, Matthias Loeffler) описаны концентрированные водные смеси, в которых доставка O-ацил-изетионатов облегчается с помощью N-ацил-таурата и бетаинов. В патенте США №7879780 описаны устойчивые моющие композиции, включающие O-ацил-изетионаты в комбинации с бетаинами и сульфосукцинатами. В недавней заявке на патент, поданной Galaxy Surfactants, предложены жидкие системы доставки O-ацил-изетионатов, в которых применяются N-ацил-глицинаты и алкилбетаины (заявка на патент США №13/749458, A Jawale et al.). Примерами коммерчески доступных "жидких систем доставки" для кокоил-изетионата натрия являются 1) Chemoryl™ SFB, Lubrizol (кокоил-изетионат натрия, лаурет-сульфосукцинат и кокоимидопропил-бетаин), 2) Hostapon SCB, Clariant (кокоил-изетионат натрия, кокобетаин) и 3) Miracare Plaisant, Rhodia (кокоил-изетионат натрия, кокоамфоацетат и кокоил-таурат натрия).
Во всех жидких системах доставки (LDS), о которых сообщалось до сих пор, для придания твердым O-ацил-изетионатам щелочных металлов способность растворяться или диспергироваться в водной среде, главным образом, применялись другие анионные или амфотерные/цвиттерионные ПАВ ("Solubilization sodium cocoyl isethionate", J.Z. Sun, M.C.E. Erickson and J.W. Paar, J. Cosmetic Science 54, 559-568, 2003). Самый значительный недостаток таких "жидких систем доставки" заключается в том, что они основаны на твердых формах солей O-ацил-изетионатов, которые могут иметь форму игл, пластинок, порошка или гранул. Получение самих твердых форм O-ацил-изетионатов включает проведение реакции при 225°C и обработку расплавленной массы для превращения ее в твердое вещество желаемой физической формы. Упомянутые жидкие системы доставки O-ацил-изетионатов разработаны, чтобы облегчить получение композиций для личной гигиены. Однако производители жидких систем доставки должны обеспечить растворение твердых, практически нерастворимых в воде, высокоплавких (выше 200°C) O-ацил-изетионатов. Это достигается нагреванием и смешиванием твердых O-ацил-изетионатов с другими ПАВ, либо анионными, либо амфотерными, либо ПАВ обоих этих типов. Промышленный способ получения O-ацил-изетионатов включает применение очень высоких температур от 200 до 240°C при взаимодействии жирной кислоты с солями - гидроксиэтилсульфонатами щелочных металлов (Friedman, M. 2004, Chapter 5: Chemistry, Formulation and Performance of Syndet and Combo Bars. In, Spitz, L.(ed), SODEOPEC Soaps, Detergents, Oleo-chemicals and Personal Care Products, AOCS Press, Champaign, II). Типовая промышленная методика этерификации, катализируемой кислотой, включает применение как минимум 1,4-2,0 мольных эквивалентов жирных кислот по отношению к изетионату щелочного металла (избыток жирной кислоты от 40 до 100%). После достижения желаемой степени этерификации избыток жирной кислоты выделяют из реакционной смеси. Этот способ известен в литературе как DEFI (жирный ацил-изетионат, полученный прямой этерификацией). Этерификацию с участием гидроксиэтилсульфоната и жирной кислоты проводят при температуре выше 200-225°C, и избыток жирной кислоты, как правило, выделяют при температуре выше 200°C в глубоком вакууме. Выделение жирной кислоты никогда не проходит полностью и поэтому коммерчески доступные алканоил изетионаты (O-ацил-изетионаты) имеют чистоту примерно 65-85%. Для того чтобы реакционная масса, содержащая 65-85% O-ацил-изетионата оставалась текучей при 200-240°C, в реакционной смеси следует оставить некоторое количество (10-15% масс./масс. от массы полученного состава) жирной кислоты. Это облегчает перемещение расплавленной массы и ее превращение в иглы или гранулы с помощью комплексной технологии, которая гарантирует отсутствие разложения основной массы расплава при очень высокой температуре. Для каждой формы полученного твердого O-ацил-изетионата (гранулы, порошок или кусочки) характерна определенная степень сопутствующего пылеобразования, требующая специальных мер безопасности, поскольку вдыхание этой пыли несет серьезную угрозу для здоровья. Поскольку O-ацил-изетионаты являются довольно высокоплавкими соединениями и практически не растворяются в воде, эти анионные ПАВ нелегко вводить в составы для личной гигиены. Поэтому в жидких системах доставки применяют коммерчески доступную твердую форму O-ацил-изетионатов, которую превращают в жидкую/текучую форму, которую можно ввести в композицию, с применением других ПАВ. Другой основной недостаток жидких систем доставки O-ацил-изетионатов заключается в том, что коммерчески доступные и запатентованные LDS поставляются со значительным количеством определенных ПАВ. Это ограничивает применение т.н. "жидких систем доставки", поскольку изготовителю состава может быть нежелательно наличие этих дополнительных ПАВ, которые применяются для получения жидких систем доставки O-ацил-изетионата. Имеющиеся на рынке "жидкие системы доставки" поставляются с имидазолиновыми амфотерными ПАВ или алкил бетаинами, или даже анионными ПАВ, например жирный спирт- эфир сульфатами, и количество этих ПАВ является слишком высоким относительно количества O-ацил-изетионатов, которые растворяют или диспергируют в воде. Кроме того, такие ПАВ, как (жирный алкил)бетаины (применяемые Galaxy Surfactant и Clariant), являются очень дорогими, поскольку их получают из дорогого сырья, которое представляет собой жирный третичный амин с одной длинной цепью и двумя короткими алкильными цепями у третичного атома азота. Наконец, до сих пор не сообщалось о жидких системах доставки, включающих только комбинации "сверхмягких" ПАВ из числа O-ацил-изетионатов и N-ацил-аминокислот. Очевидная причина этого заключается в том, что в случае применения твердой формы O-ацил-изетионатов нельзя получить текучие и стабильные системы. Например, из коммерчески доступной твердой формы кокоил-изетионата натрия невозможно получить гомогенный водный раствор кокоил-изетионата натрия и кокоил-глицината натрия в мольном соотношении 1:1.
Поскольку ПАВ из числа O-ацил-изетионатов и N-ацил-аминокислот являются основой "сверхмягких" моющих систем для личной гигиены, в технике существует потребность 1) получения композиции, включающей только эти два "сверхмягких" ПАВ, которую легко вводить в состав продуктов для личной гигиены и 2) разработки простого и эффективного способа получения такой композиции, который мог бы обеспечить гибкое изменение соотношения между O-ацил-изетионатами и N-ацил-аминокислотами.
Цель настоящего изобретения
i) Соответственно, цель настоящего изобретения заключалась в разработке простого, удобного, энергоэффективного способа, который позволял бы получать смеси двух типов ПАВ, известных как "сверхмягкие" в своей комбинации, а именно O-ацил-изетионатов (Формула (I)) и N-ацил-аминокислот (Формула (II)), из распространенного сырья, а именно хлорангидридов жирных кислот, без добавления третьего ПАВ.
ii) Другой целью настоящего изобретения являлась разработка способа, который мог бы обеспечить гибкость получения "сверхмягких" смесей ПАВ с точки зрения изменения отношения O-ацил-изетионатов и N-ацил-аминокислот.
iii) Следующей целью настоящего изобретения являлась разработка "жидкой системы доставки" для O-ацил-изетионата щелочного металла, который без такой системы является нерастворимым и с трудом включается в состав продукта.
iv) Еще одной целью настоящего изобретения являлось получение указанных смесей в твердой форме для определенных применений, в которых необходимо избегать присутствия воды.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
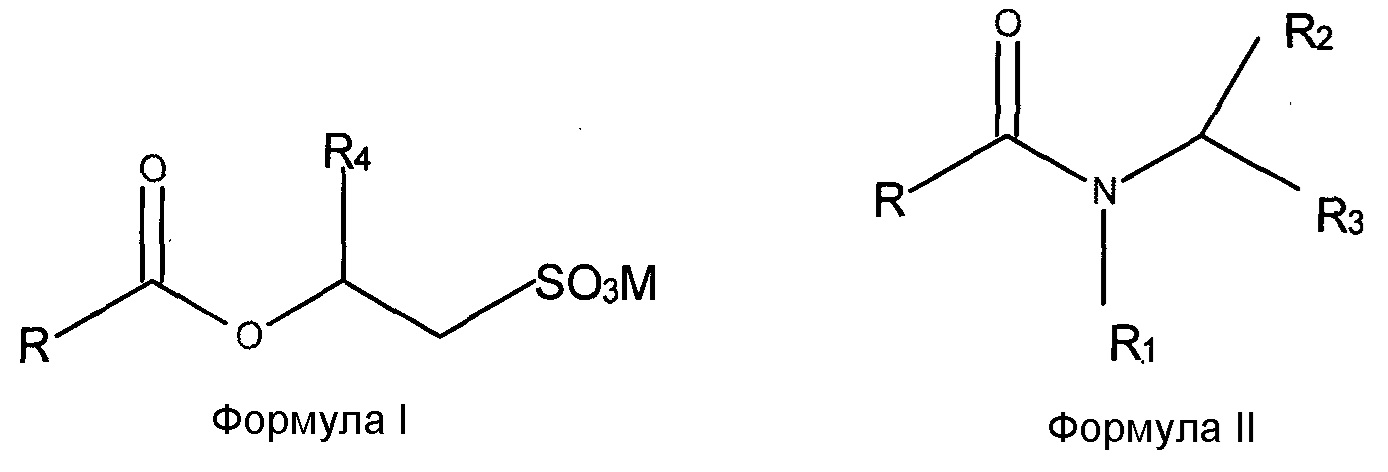
В настоящем изобретении раскрыт способ получения смесей O-ацил-изетионатов формулы (I) и ПАВ на основе и N-ацил-аминокислот формулы (II):
 ,
,
где заместитель R выбран из насыщенных или ненасыщенных алкильных групп C5-C21, заместитель R1 выбран из H, C1-C4 алкила, заместитель R2 выбран из H или любых групп, присутствующих у α-атома углерода природных аминокислот, заместитель R3 выбран из COOX, CH2SO3X, где X выбран из NH4+, Li+, Na+ или K+, R4 означает H или метил, и M означает катион, выбранный из Na+, K+, NH4+ или катиона четвертичного аммония, полученного из третичного амина,
где указанный способ включает стадии:и
A) взаимодействия более чем одного эквивалента хлорангидрида жирной кислоты с гидроксиалкилсульфонатом щелочного металла или аммония при 50-70°C с получением соединения формулы (I) и
B) взаимодействия продукта стадии (A) (содержащего остаток не вступившего в реакцию хлорангидрида жирной кислоты) с эквивалентным количеством водного раствора одной или нескольких аминокислот и водного раствора основания в типовых условиях реакции Шоттена-Баумана в водной среде при pH от 9 до 10,5 и температуре ниже 50°C с получением соединения формулы (II).
Таким образом, в настоящем изобретении предложен новый способ получения водной смеси, включающей O-ацил-изетионаты и ПАВ на основе N-ацил-аминокислот, из одного хлорангидрида жирной кислоты путем последовательного взаимодействия с изетионатом щелочного металла на первой стадии, и затем с одной или несколькими аминокислотами. Настоящее изобретение дает возможность легко получать смеси ПАВ, состоящие из O-ацил-изетионатов и N-ацил-аминокислот. Способ по настоящему изобретению позволяет получать "жидкие системы доставки" O-ацил-изетионатов в комбинации с N-ацил-аминокислотами в любом соотношении без посредничества третьего ПАВ, которое применялось в технике известного уровня.
Сообщалось, что O-ацил-изетионаты формулы (I) и N-ацил-аминокислоты формулы (II) при смешивании друг с другом образуют "сверхмягкие" композиции для личной гигиены. В настоящем изобретении предложен экономически эффективный и очень легкий в реализации способ получения смесей указанных "сверхмягких" ПАВ с различными соотношениями компонентов.
Специалист в данной области техники сможет понять и оценить описанные выше особенности и преимущества настоящего изобретения, обратившись к приведенному ниже подробному описанию и формуле изобретения.
ОПИСАНИЕ ИЛЛЮСТРАТИВНОГО МАТЕРИАЛА
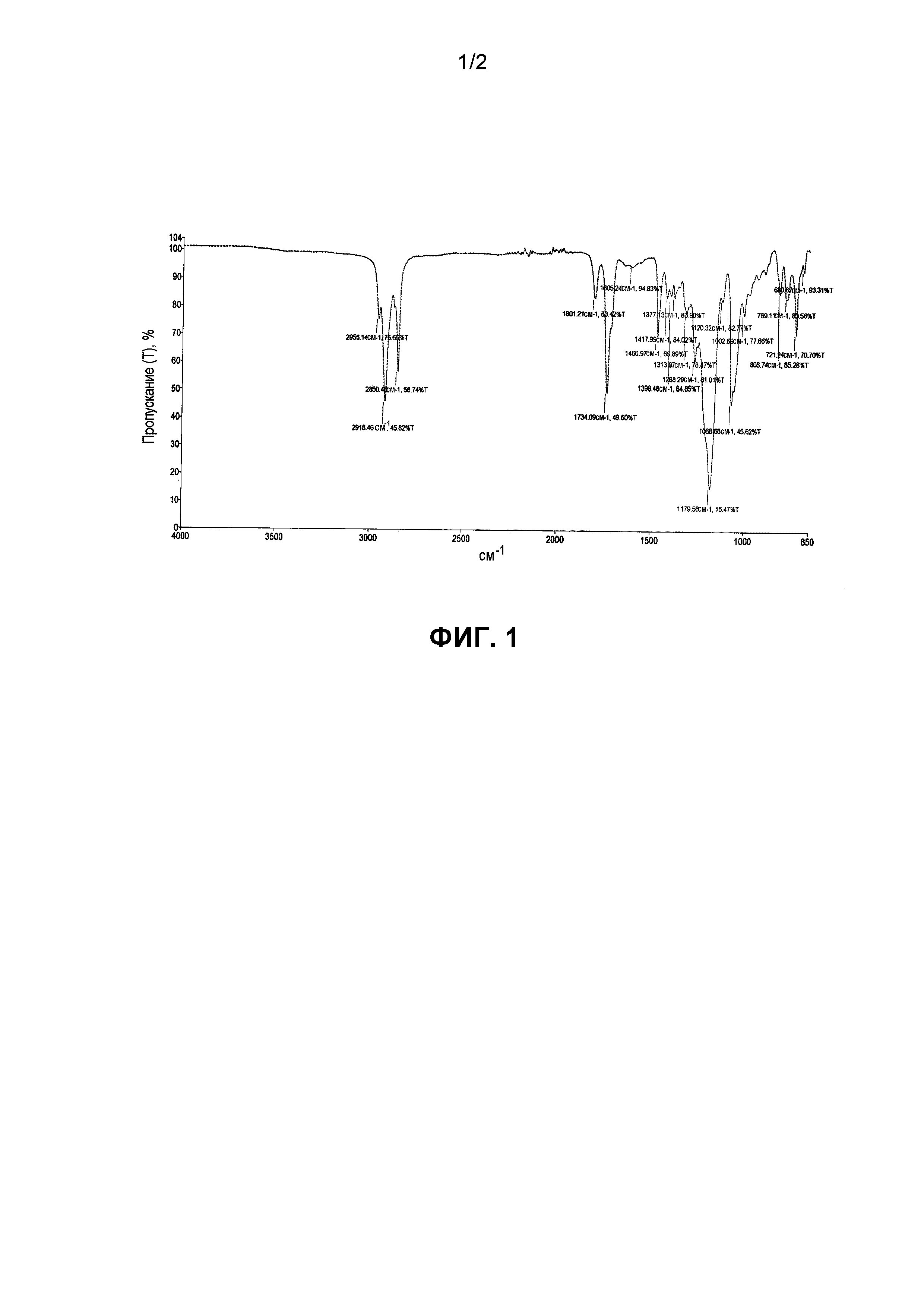
На Фиг. 1 показан FTIR (ИК-спектр с преобразованием Фурье) реакционной смеси первой стадии реакции, на котором можно видеть исчезновение сигнала валентных колебаний гидроксильной группы гидроксиэтилизетионата при 3400 см-1 и одновременное появление сигнала валентных колебаний сложноэфирной группы (O-ацил-изетионата) при 1734 см-1, а также присутствие избытка хлорангидрида жирной кислоты, на который указывают валентные колебания карбонильной группы в области 1800 см-1.
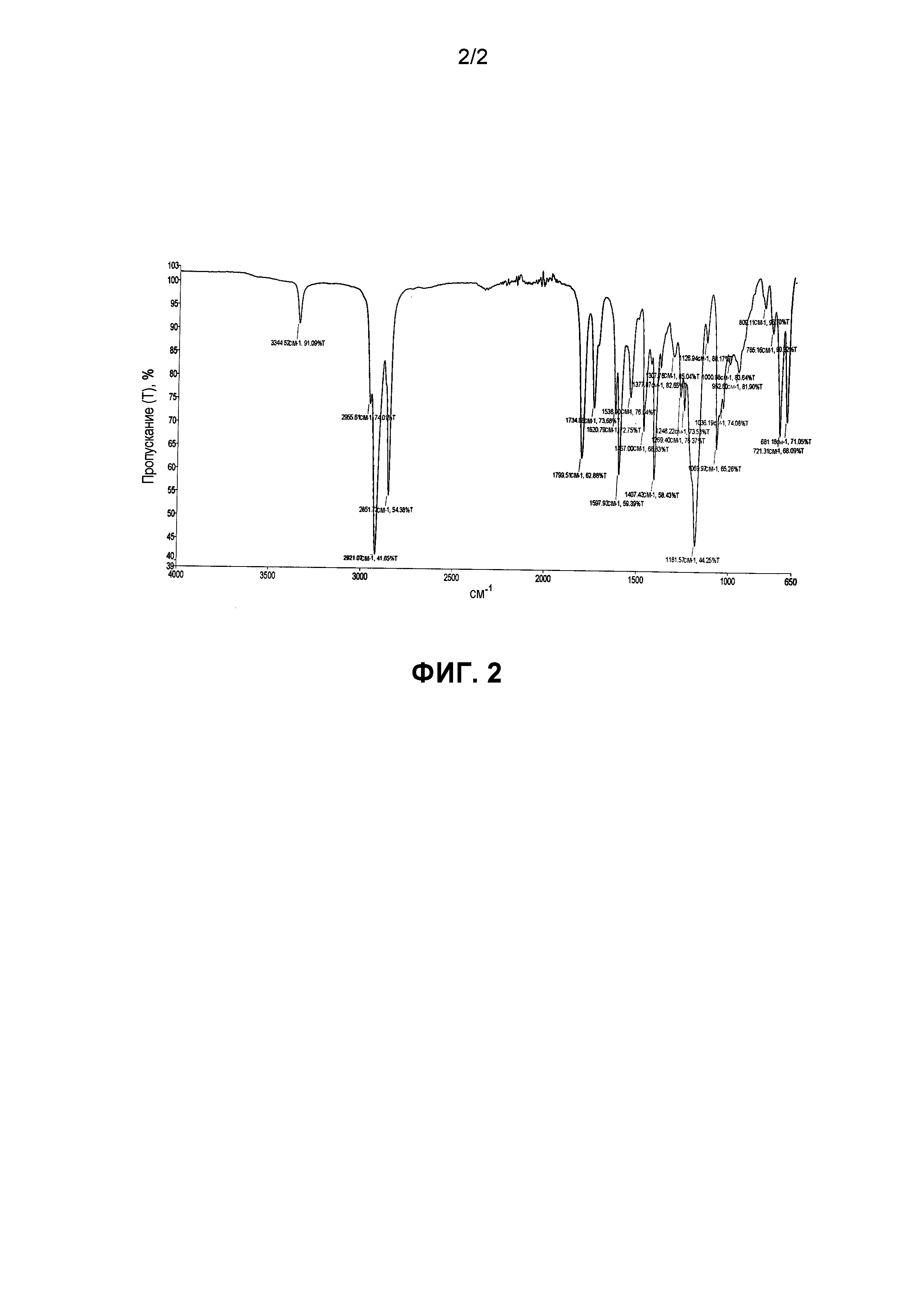
На Фиг. 2 показан инфракрасный спектр высушенного образца примера 1, представляющего собой смесь SCI:SCG в соотношении 1:2, который демонстрирует валентные колебания карбонила и группы NH амидной связи N-ацил-глицината при 1605 см-1, 1620 см-1 и 3344 см-1 соответственно.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В настоящем изобретении описан экологически безопасный и экономический эффективный способ производства смесей мягких ПАВ, а именно O-ацил-изетионатов формулы (I) и N-ацил-аминокислот формулы (II) в различных соотношениях. Эти две категории мягких моющих средств при смешивании друг с другом позволяют получить "сверхмягкие" моющие композиции (патенты США №8268767; 8114824; и 8263538).
 .
.
Способ получения по настоящему изобретению подходит для получения "сверхмягких" смесей с использованием одного исходного вещества, а именно хлорангидрида жирной кислоты, для синтеза мягких ПАВ обоих типов по двухстадийной методике. Описанный в заявке способ является весьма энергоэффективным и позволяет гибко регулировать соотношение между O-ацил-изетионатами и N-ацил-аминокислотами. Выходы продуктов являются количественными, и в описанном способе не образуются какие-либо отходы. Наконец, помимо получения смесей хорошо известных "сверхмягких" ПАВ, т.е. O-ацил-изетионатов и N-ацил-аминокислот, для композиций личной гигиены, способ по настоящему изобретению позволяет получать O-ацил-изетионаты щелочных металлов в жидкой форме для легкого введения в составы продуктов личной гигиены, тогда как коммерчески доступные твердые формы этого продукта включаются в составы подобных композиций с очень большим трудом (твердые формы O-ацил-изетионатов превращают в "жидкие системы доставки", как описано в патентах США №5925603, 5415810 и 7879780). Важно отметить, что в отличие от всех "жидких систем доставки" O-ацил-изетионатов, описанных в литературе до настоящего времени (запатентованных и коммерчески доступных, см. раздел "Предпосылки изобретения"), LDS по настоящему изобретению состоит только их двух компонентов, а именно O-ацил-изетионатов и N-ацил-аминокислот. Два этих класса компонентов составляют основу "сверхмягких" моющих систем для личной гигиены (патент США №8268767).
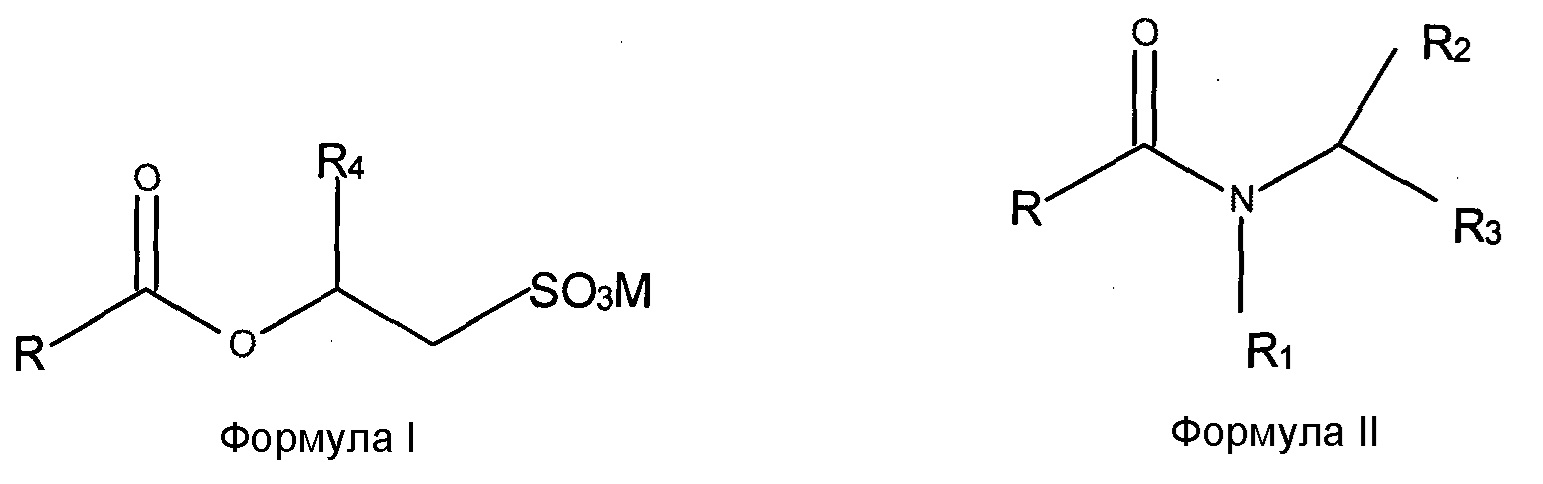
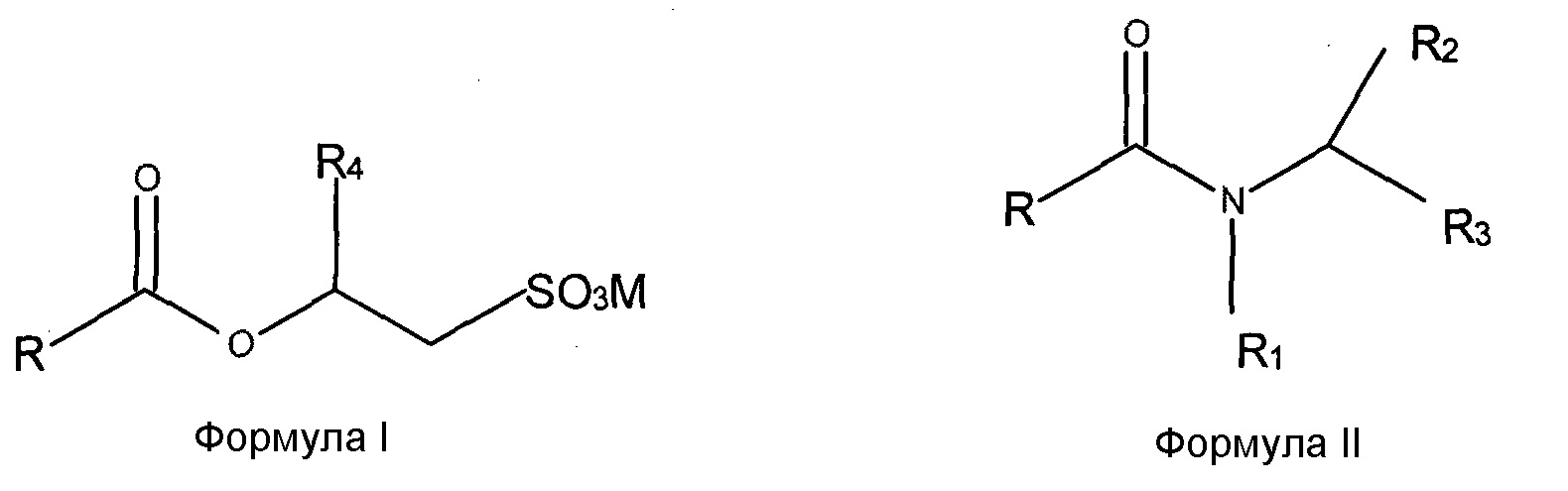
Таким образом, настоящее изобретение относится к получению "сверхмягких" смесей O-ацил-изетионатов Формулы (I) и ПАВ на основе N-ацил-аминокислот формулы (II):
 ,
,
где заместитель R представляет собой насыщенную или ненасыщенную алкильную цепь с числом атомов углерода в пределах от C5 до C21, R1 означает H или алкильную цепь небольшой длины в пределах от C1 до C4, R2 означает H или любые группы, присутствующие у α-атома углерода природных аминокислот, R3 означает кислотную группу, например карбоксильную или сульфонильную, вместе с противоионом щелочного металла, как, например, COOX, CH2SO3X, где X=Li+, Na+ или K+, R4 выбран из H или метила, и M представляет собой катион, выбранный из Na+, K+, NH4+ или катиона четвертичного аммония, полученного из третичного амина.
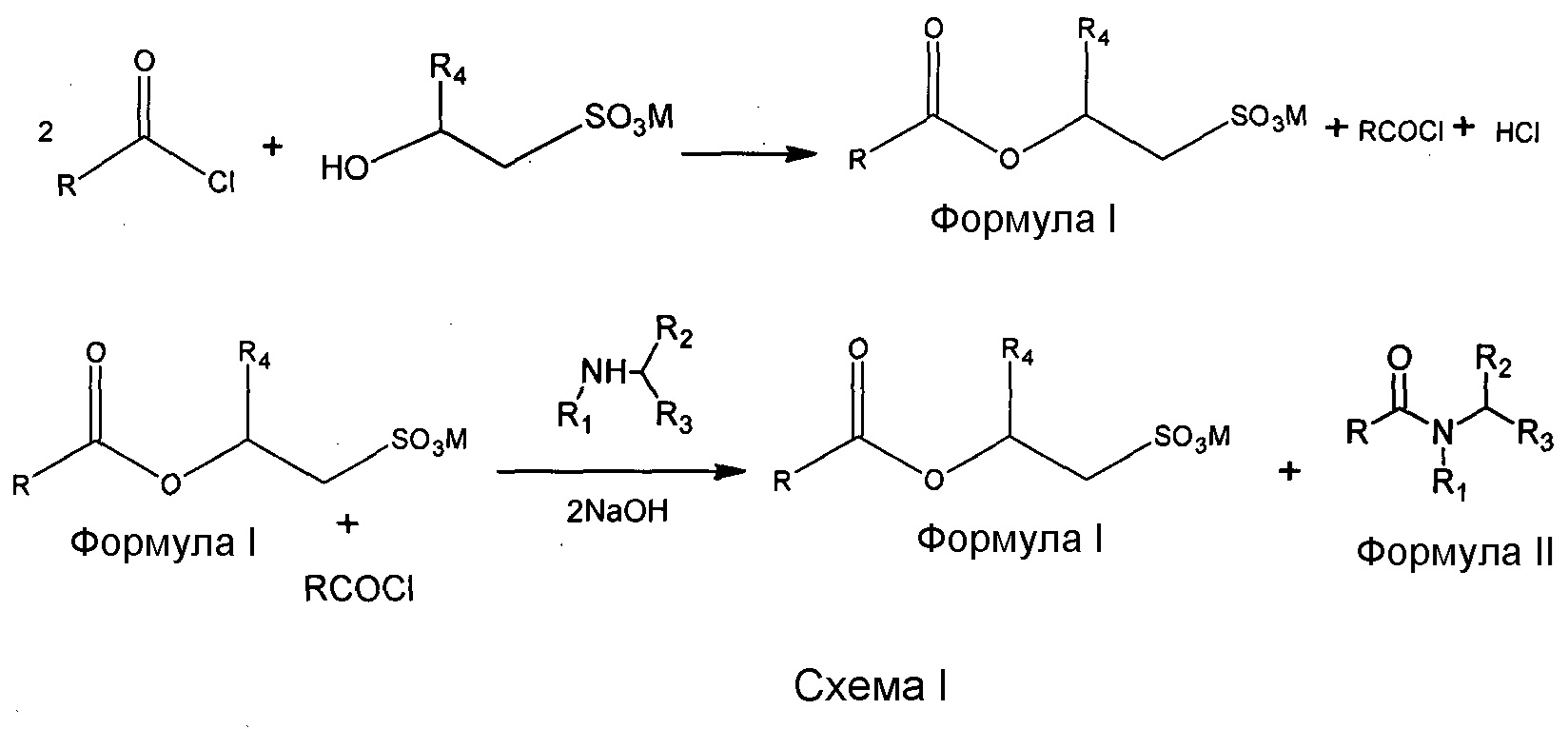
Способ по настоящей заявке включает двухстадийный синтез указанных смесей, где стадии осуществляются последовательно. Смесь порошкообразного гидроксиалкилсульфоната щелочного металла или аммония (один эквивалент) и хлорангидрида жирной кислоты (более одного эквивалента) перемешивают при медленном пропускании азота при температуре 50-70°C в течение примерно 3-4 часов (схема 1). Газообразный хлористый водород, который вытесняется из смеси медленным током азота, поглощают щелочной ловушкой. За ходом реакции следят по исчезновению линии валентных колебаний гидроксильной группы гидроксиэтилизетионата при 3400 см-1 и одновременному появлению линии валентных колебаний карбонила сложноэфирной группы при 1734 см-1 в спектре FTIR. Избыток хлорангидрида жирной кислоты проявляется в спектре FTIR полосой валентных колебаний карбонила в окрестности 1800 см-1 (как показано на фиг. 1).
В течение примерно 3-4 часов эквивалент хлорангидрида жирной кислоты вступает во взаимодействие с гидроксиалкилсульфонатом щелочного металла или аммония, и реакционную массу охлаждают до комнатной температуры. При этом текучая слегка пастообразная реакционная смесь, полученная на этой стадии (стадия 1 схемы 1), содержит O-ацил-изетионат и избыток не вступившего в реакцию хлорангидрида кислоты (один эквивалент, более одного эквивалента или менее одного эквивалента, в зависимости от стехиометрии исходной смеси). Этот стехиометрический избыток хлорангидрида жирной кислоты на первой стадии играет роль реакционной среды, так что взаимодействие с твердым гидроксиалкилсульфонатом щелочного металла можно проводить при температурах менее 70°C с количественным выходом. Как правило, первая стадия этерификации (схема 1) завершается в течение 3-4 часов при 50-70°C по данным FT инфракрасной спектроскопии. Избыток хлорангидрида жирной кислоты на первой стадии является реагентом для второй стадии, которая представляет собой реакцию Шоттена-Баумана с аминокислотой в присутствии основания (стадия 2 схемы 1):
 .
.
Избыточное количество хлорангидрида жирной кислоты делает реакционную смесь, содержащую стехиометрическое количество O-ацил-изетионата, достаточно текучей для проведения следующей стадии. Для проведения N-ацилирования аминокислоты на второй стадии, текучую пастообразную реакционную массу, полученную на первой стадии добавляют при перемешивании к необходимому количеству аминокислоты (эквивалентное количество аминокислоты зависит от избытка хлорангидрида жирной кислоты, который в свою очередь зависит от исходной стехиометрии первой стадии) в воде (количество воды зависит от желаемого конечного содержания твердого вещества), в атмосфере азота при температуре примерно 30-35°C, поддерживая pH реакционной смеси в пределах от 9,0 до 10,5 одновременным добавлением щелочи (двух эквивалентов по отношению к аминокислоте или хлорангидриду жирной кислоты), как правило, в виде 25%-ного или 48%-ного водного раствора (например, гидроксида калия или натрия), как показано на схеме 1. Взаимодействие непрореагировавшего хлорангидрида жирной кислоты, оставшегося в текучей пастообразной массе продукта стадии 1 схемы 1, проводят в типовых условиях реакции Шоттена-Баумана (патент США №2527657). Реакцию Шоттена-Баумана проводят при температурах в диапазоне от 20 до 50°C. Предпочтительный температурный диапазон составляет от 20 до 35°C. Для достижения максимального выхода в конденсации Шоттена-Баумана важную роль играет диапазон pH. Как правило, N-ацилирование аминокислот может очень легко проходить в диапазоне pH от 9,0 до 10,5. Однако предпочтительный диапазон pH для N-ацилирования аминокислот составляет от 10,0 до 10,5. После одновременного добавления текучей пасты продукта стадии 1 (содержащей избыток хлорангидрида жирной кислоты и O-ацил-изетионат) и двух эквивалентов раствора щелочи реакционную смесь перемешивают в течение еще 3-4 часов. После этого pH реакционной смеси доводят до значения в диапазоне от 7,0 до 8,0 добавлением небольшого количества минеральной кислоты (хлористоводородной кислоты), при содержании твердого вещества от 30 до 40%. Содержание твердого вещества в смеси мягких ПАВ доводят до желаемого уровня. Предпочтительный диапазон содержания твердого вещества для хорошей текучести конечного продукта составляет от 30 до 40% (примеры 10 и 11). Однако возможно и получение смесей с более высоким содержанием твердого вещества (>40%). При более высоком содержании твердого вещества вместо прозрачного раствора, как правило, получается пастообразный продукт (с высокой вязкостью от 1000 сП до 10 сП, еще текучий при комнатной температуре), и его свойства зависят от компонентов смеси и соотношения O-ацил-изетионата и N-ацил-аминокислоты.
Мольное соотношение не вступившего в реакцию на первой стадии O-ацилирования хлорангидрида жирной кислоты к аминокислоте, используемой на второй стадии N-ацилирования, может меняться в пределах от 1:1 до 1:1,10. Предпочтительный избыток аминокислоты составляет примерно 3,0-5,0 мол.%. В примере 1 описан синтез смеси "сверхмягких" ПАВ в соотношении 1:2 (кокоил-изетионат натрия (SCI):кокоил-глицинат натрия (SCG)), в то время как в примере 7 показан синтез смеси тех же "сверхмягких" ПАВ в соотношении 1:1.
Инфракрасный спектр (Фиг. 2) высушенного образца, полученного в примере 1, представляющего собой смесь SCI:SCG в соотношении 1:2 включает валентные колебания карбонильной группы и группы NH амидной связи N-ацил-глицината при 1605 см-1, 1620 см-1 и 3344 см-1 соответственно. Карбонильная группа O-ацил-изетионата (карбонил сложноэфирной группы) дает сигнал при 1734 см-1, и валентные колебания групп CH алкильных цепей обоих мягких ПАВ проявляются сигналами при 2850, 2920 и 2956 см-1.
Хлорангидриды жирных кислот, применяемые в настоящем изобретении, получены экологически безопасным каталитическим способом, описанным Koshti и соавторами в недавно поданной заявке на патент (PCT/IB2012/055197).
Примеры 1-10 иллюстрируют получение смеси ПАВ, включающей O-ацил-изетионат и N-ацил-аминокислоту, с применением различных хлорангидридов жирных кислот.
Алкильная цепь хлорангидрида жирной кислоты, представленная символом R на схеме 1, может включать четное или нечетное количество атомов углерода и являться линейной или разветвленной цепью. Хлорангидрид может представлять собой чистое вещество, все молекулы которого включают один и тот же алкильный заместитель, или являться смесью веществ, включающих различные алкильные цепи от C5 до C21. Алкильная цепь может быть полностью насыщенной или ненасыщенной, с одной или несколькими двойными связями. Такие алкильные цепи входят в структуру природных жирных кислот, которые обычно являются компонентами животных жиров или растительных масел. Ненасыщенные алкильные цепи могут содержаться в олеиновой кислоте, рицинолевой кислоте, линолевой кислоте, линоленовой кислоте, элеостеариновой кислоте, эйкозеновой кислоте, эруковой кислоте, докозодиеновой кислоте и ундециленовой кислоте. Насыщенные жирные кислоты обычно выделяют из пальмового/пальмоядрового масла или кокосового масла, причем все эти кислоты имеют четное число атомов углерода в диапазоне от октановой кислоты (C8) до стеариновой кислоты (C18). Жирные кислоты с большим числом атомов углерода (C18-C22) получают из горчичного масла, тунгового масла и рапсового масла. Типовой состав кокоил-хлорида, который применяется для иллюстрации настоящего изобретения (примеры 1, 3, 5, 6, 7 и 9), показан в приведенной ниже таблице 1. В примере 4 применяется кокоил-хлорид другого сорта, который имеет более высокое процентное содержание стеароил-хлорида.
|
Состав лауроил-хлорида (примеры 2 и 8), который применялся для иллюстрации данного изобретения, приведен в таблице 2.
|
В соответствии с настоящим изобретением типы аминокислоты, которые применяются в синтезе соединений формулы (II) на второй стадии способа, включают природные α-аминокислоты (глицин, аланин, валин, лейцин, изолейцин, метионин, пролин, цистеин, фенилаланин, тирозин, триптофан, аргинин, лизин, гистидин, аспарагиновую кислоту, глутаминовую кислоту серин, треонин, аспарагин, глутамин), не встречающиеся в природе аминокислоты (энантиомеры, имеющие противоположную D-конфигурацию), смеси стереоизомеров, аминокислоты искусственного происхождения (аминопропионовую кислоту, N-метил-таурин, саркозин). Вкратце, для синтеза соединений формулы (II) необходимо, чтобы аминокислота, с одной стороны, содержала первичную или вторичную аминогруппу и, с другой стороны. кислотную группу, например карбоксил или сульфоновую группу. Настоящее изобретение проиллюстрировано применением таких кислот, как глицин (первичная аминокислота, содержащая карбоксильную группу, примеры 1-4, 7 и 8), N-метил-таурин (вторичная аминокислота, содержащая сульфоновую кислотную группу, пример 5) и саркозин (содержащий вторичную аминогруппу и карбоксильную группу, пример 6). Пример 9 демонстрирует, что все три указанные аминокислоты могут применяться совместно с получением смеси всех трех N-ацил-аминокислотных ПАВ с O-ацил-изетионатом.
Основание, применяемое на второй стадии в реакции Шоттена-Баумана, можно выбрать из гидроксидов или карбонатов калия или натрия, или гидроксида аммония. При получении ПАВ на основе N-ацил-аминокислот формулы (II) также могут применяться водорастворимые третичные амины, например триметил- или триэтиламин, или триэтаноламин, в форме водного раствора. В примере 3 показано применение в качестве основания гидроксида калия, тогда как во всех остальных примерах в качестве основания для N-ацилирования аминокислот по Шоттену-Бауману применялся гидроксид натрия.
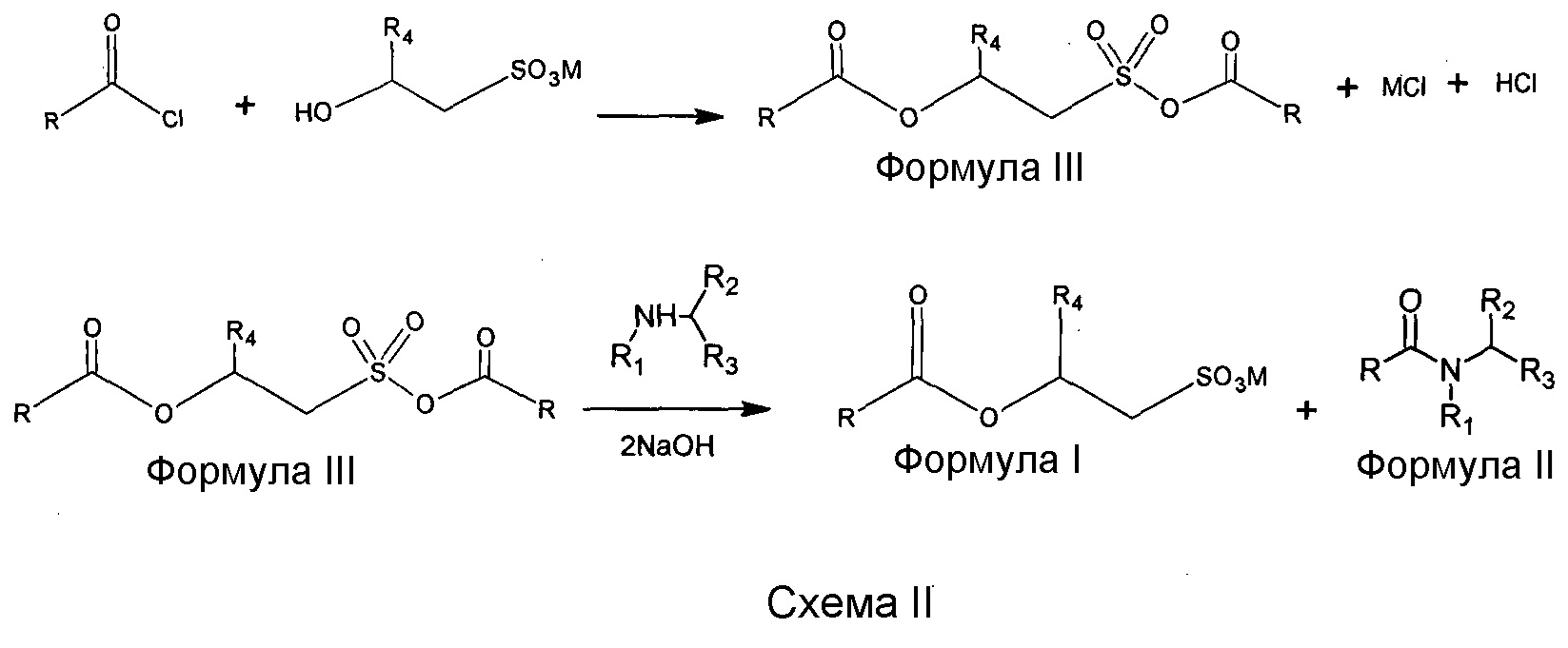
На первой стадии способа по настоящему изобретению, когда хлорангидрид жирной кислоты вводят в реакцию с гидроксиэтилсульфонатом для получения соединения формулы (I), существует вероятность образования определенного количества молекул смешанного сложного эфира-ангидрида (соединения формулы (III)), как показано на схеме II. Образование смешанного сложного эфира-ангидрида может происходить в значительных количествах из-за слишком глубокого протекания взаимодействия хлорангидрида кислоты с изетионатом щелочного металла на первой стадии. Однако на второй стадии, когда полученную текучую пастообразную массу вводят во взаимодействие с водным раствором аминокислоты, нуклеофильная первичная или вторичная аминогруппа преимущественно реагирует с сильноактивированной ангидридной группой соединения формулы (III), приводя к получению изначально намеченного соотношения соединений формулы (I) и соединений формулы (II), как показано на схеме II:
 .
.
Таким образом, примеры 1-11 иллюстрируют образование смесей ПАВ, содержащих O-ацил-изетионат и N-ацил-аминокислоту в различных мольных соотношениях с применением хлорангидридов жирных кислот различных типов и целого ряда различных аминокислот и оснований. Смеси чистых O-ацил-изетионатов и N-ацил-аминокислот можно высушить распылительной сушкой с получением гомогенного порошка. При растворении этого высушенного порошка, включающего два указанных типа ПАВ, в воде до исходного содержания твердых веществ образуется чистый раствор того же химического состава. Поэтому смесь сверхмягких ПАВ в сухой форме можно легко получить обычным способом распылительной сушки. Смеси сверхмягких ПАВ в твердой форме могут оказаться желательными в некоторых приложениях, если необходимо избегать присутствия воды. Например, в отличие от средств для мытья лица и тела, в которые можно легко включать водные растворы сверхмягких ПАВ, в случае бруска синтетического мыла, добавление водного раствора сверхмягких ПАВ потребовало бы обязательного удаления воды из массы готового продукта перед формованием, и эту операцию невозможно было бы выполнить в сигма-смеси с применением нагревания и вакуума. В таких случаях могла бы потребоваться сухая форма мягкого ПАВ в виде порошка, гранул или комочков.
Пример 12 демонстрирует, что водные смеси ПАВ по настоящей заявке, включающие O-ацил-изетионат и N-аминокислоту, можно высушить и традиционным способом превратить в сухую форму.
Преимущества настоящего изобретения
1) В изобретении предложен недорогой и эффективный способ получения "сверхмягкой системы ПАВ", состоящей из O-ацил-изетионатов и N-ацил-аминокислот.
2) Описанный в настоящей заявке способ позволяет обойти большое число недостатков, связанных с традиционным энергозатратным способом этерификации DEFI (при высокой температуре >200°C) жирных кислот действием гидроксиэтилсульфонатов щелочных металлов, который применяется для получения O-ацил-изетионатов. Способ прямой этерификации жирной кислоты при очень высокой температуре требует не только сильного нагревания, но и применения избытка жирной кислоты относительно стехиометрического количества. Этот значительный избыток относительно стехиометрического количества необходимо удалить в конце реакции, что увеличивает время реакционного цикла и потребление энергии. Другой наиболее существенный недостаток указанного способа, проводимого при высокой температуре, заключается в том, что при выделении жирной кислоты удаляются низшие жирные кислоты из-за частично проходящей реакции переэтерификации, и поэтому в случае смеси жирных кислот конечный состав продукта, т.е. O-ацил-изетионата, отличается от распределения алкильных цепей в исходном веществе. Способ, описанный в настоящей заявке, позволяет также исключить еще одну операцию, которая требует применения сложного оборудования, а именно превращения расплавленного O-ацил-изетионата щелочного металла (продукта) в порошок, гранулы/комки или иглы.
3) O-ацилирование и N-ацилирование гидроксиалкилсульфонатов щелочных металлов или аммония и аминокислот,соответственно хлорангидридом жирной кислоты проводят в течение 4-5 часов при температуре, которая никогда не превышает 70°C.
4) Получение "сверхмягкой" системы ПАВ, включающей O-ацил-изетионат (Формула (I)) и N-ацил-аминокислоту (Формула (II)) в мольном соотношении от 1,0:0,5 до 1,0:10, исходя из одного исходного вещества, представляющего собой хлорангидрид жирной кислоты.
5) Получение "сверхмягкой" системы ПАВ, включающей O-ацил-изетионат и N-ацил-аминокислоту в мольном соотношении от 1,0:0,5 до 1,0:10, причем в систему может входить одна или более чем одна N-ацил-аминокислота. Кроме того, можно получить дополнительную выгоду от синергии ацил-изетионата и смеси соответствующих N-ацил-аминокислот, таких как глицинаты, таураты или саркозинаты и т.д.
6) O-ацил-изетионаты коммерчески доступны в твердой форме и N-ацил-аминокислоты доступны как в твердой, так и в водной форме. Твердая форма O-ацил-изетионатов плохо растворима в присутствии только аминокислотных ПАВ, и поэтому существует несколько описанных в литературе систем и коммерческих продуктов, известных как "жидкие системы носителей" O-ацил-изетионатов, в которых применяются другие ПАВ, такие как бетаины, амфоацетаты и сульфосукцинаты. Однако с применением способов по настоящей патентной заявке можно создать жидкую систему доставки O-ацил-изетионатов, включающую только N-ацил-аминокислотные ПАВ, без помощи какого-либо третьего ПАВ. Следует отметить, что O-ацил-изетионаты (Формулы (I)) и N-ацил-аминокислоты (Формулы (II)) составляют основу "сверхмягких" моющих систем.
7) Смеси "сверхмягких" ПАВ, включающие O-ацил-изетионаты и N-ацил-аминокислоты в форме сухого вещества можно получать из водных растворов этих веществ, описанных в данной патентной заявке. Твердые сухие формы "сверхмягких" ПАВ необходимы для получения некоторых продуктов для ухода за кожей, например брусков синтетического мыла или любых других продуктов/применений, в которых может оказаться необходимой твердая смесь веществ двух указанных типов, если необходимо избежать применения воды или применять ее в минимальных количествах (неводная среда).
ПРИМЕРЫ
Ниже по тексту настоящее изобретение описано с привлечением неограничивающих иллюстративных примеров. Детали настоящего изобретения, приведенные в нижеследующих примерах, даны только в качестве иллюстрации и их не следует понимать как ограничение объема настоящего изобретения.
Жирные кислоты приобретали у компании Natural Oleo-chemicals, Malaysia, а тионилхлорид - у компании Transpek Industries, Vadodara, India. Глицин, саркозин и N-метил-таурин приобретали у компании Sigma-Aldrich.
Хлорангидриды жирных кислот получали по методике, описанной в заявке на патент (PCT/IB2012/055197) Koshti et al., (Method to produce N-acyl amino acid surfactants using N-acyl amino acid surfactants or corresponding anhydrides as catalyst) (Способ получения N-ацил-аминокислотных ПАВ с применением N-ацил-аминокислотных ПАВ или соответствующих ангидридов в качестве катализатора).
Анионную активность смесей по настоящему изобретению определяли способом двухфазного титрования, описанным в литературе (Introduction to Surfactant Analysis автор D.C. Cullum, 59-61 1994, издатель Blackie Academic & Professional (Chapman&Hall)).
Пример 1: Синтез смеси кокоил-изетионата натрия и кокоил-глицината натрия (1:2)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 55-60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (270 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (53,55 г, 0,71 г-моль) в воде (730 г) вместе с раствором гидроксида натрия (48,8%, 116 г, 1,41 г-моль), поддерживая pH реакционной смеси в диапазоне от 10,2 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение двух часов и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH до 7,5, добавляя HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1169 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
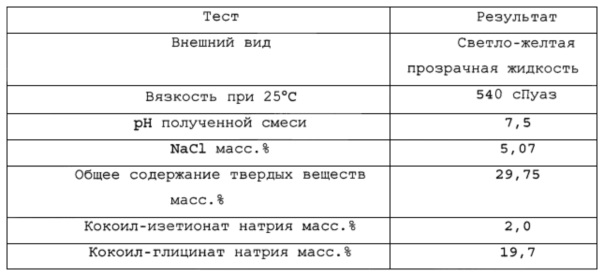
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 2: Синтез смеси лауроил-изетионата натрия и лауроил-глицината натрия (1:2)
Лауроил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 5,0%
C12: 90%
К лауроил-хлориду (228 г, 1,04 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52,0 г, 0,35 г-моль) и перемешивали суспензию при 65-70°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию лауроил-хлорида (валентные колебания карбонила при 1800 см-1), лауроил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (260 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (53,5 г, 0,71 г-моль) в воде (709 г) вместе с раствором гидроксида натрия (48,8%, 116 г, 1,41 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при комнатной температуре, составлявшей 30°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества до 30%, получая 1138 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) лауроил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 3: Синтез смеси кокоил-изетионата калия и кокоил-глицината калия (1:2)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234,5 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат калия (57,4 г, 0,35 г-моль) и перемешивали полученную суспензию при 50-55°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата калия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата калия.
Текучую вязкую реакционную массу (270 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (53,55 г, 0,71 г-моль) в воде (757 г) вместе с раствором гидроксида калия (50%, 160 г, 1,41 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 30°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1239 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 4: Синтез смеси кокоил-изетионата натрия и кокоил-глицината натрия (1:2)
Кокоил-хлорид, который применялся в этом эксперименте, имел более высокое содержание хлорангидридов жирных кислот с длинной цепью, а именно пальмитоил-хлорида и стеароил-хлорида, и характеризовался следующим распределением длины алкильных цепей:
C8: 6,1%
C10: 6,2%
C12: 58,5%
C14: 19,5%
C16: 6,5%
C18: 3,2%
К кокоил-хлориду (236 г, 1,05 г-моль (м.масса 221)) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 55-60°C в течение 3,5 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (265 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (53,55 г, 0,71 г-моль) в воде (720 г) вместе с раствором гидроксида натрия (48%, 116 г, 1,41 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1154 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 5: Синтез смеси кокоил-изетионата натрия и N-кокоил, N-метил-таурата натрия (1:2)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Пастообразную реакционную массу (260 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору N-метилтаурина (99,246 г, 0,714 г-моль) в воде (805 г) вместе с раствором гидроксида натрия (48,8%, 116 г, 1,414 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1280 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 6: Синтез смеси кокоил-изетионата натрия и N-кокоил-саркозината натрия (1:2)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Пастообразную реакционную массу (260 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору натрий саркозина (198 г 40%-ного водного раствора, 0,71 г-моль) в воде (670 г) вместе с раствором гидроксида натрия (48,8%, 57,4 г, 0,7 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1185 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 7: Синтез смеси кокоил-изетионата натрия и кокоил-глицината натрия (1:1)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (223 г, 1,0 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (74,05 г, 0,5 г-моль) и перемешивали полученную суспензию при 55-60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Пастообразную реакционную массу (265 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (38,25 г, 0,51 г-моль) в воде (671 г) вместе с раствором гидроксида натрия (48,8%, 83 г, 1,01 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 30°C. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1057 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 8: Синтез смеси лауроил-изетионата натрия и лауроил-глицината натрия (1:1)
Лауроил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 5,0%
C12: 90%
К лауроил-хлориду (217,47 г, 1,00 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (74,05 г, 0,5 г-моль) и перемешивали суспензию при 65-70°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию лауроил-хлорида (валентные колебания карбонила при 1800 см-1), лауроил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (265 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (38,25 г, 0,71 г-моль) в воде (671 г) вместе с раствором гидроксида натрия (48,8%, 82,78 г, 1,01 г-моль), поддерживая pH реакционной смеси в диапазоне от 10,0 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 30°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества до 30%, получая 1057 г продукта в форме водного раствора.
ИК спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) лауроил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 9: Синтез смеси ПАВ, включающей кокоил-изетионат натрия и натриевые соли кокоил-аминокислот: изетионат натрия:(кокоил-глицинат натрия, кокоил-саркозинат натрия и кокоил-таурат натрия)=(1:2)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 55-60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (260 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (17,5 г, 0,23 г-моль), N-метилтаурина (32,5 г, 0,23 г-моль) и саркозина (65 г 40%-ного водного раствора, 0,23 г-моль) в воде (706 г) вместе с раствором гидроксида натрия (48,5%, 95,63 г, 1,16 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение двух часов и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH реакционной смеси до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1176 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоилизетионата, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 10: Синтез смеси кокоил-изетионата натрия и N-кокоил, N-метил-таурата натрия (1:2) с содержанием твердых веществ 35 масс. %
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Полученную пастообразную реакционную массу (260 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору N-метилтаурина (99,246 г, 0,714 г-моль) в воде (696 г) вместе с раствором гидроксида натрия (48,8%, 116 г, 1,414 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение 3 ч и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 35%, получая 1171 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 11: Синтез смеси кокоил-изетионата натрия и N-кокоил, N-метил-таурата натрия (1:2) с содержанием твердых веществ 40 масс. %
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
C8: 5,0%
C10: 6,0%
C12: 63%
C14: 20%
C16: 6%
C18: 0,4%
К кокоил-хлориду (234 г, 1,05 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (52 г, 0,35 г-моль) и перемешивали полученную суспензию при 60°C в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Полученную пастообразную реакционную массу (260 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору N-метилтаурина (99,246 г, 0,714 г-моль) в воде (560 г) вместе с раствором гидроксида натрия (48,8%, 116 г, 1,414 г-моль), поддерживая pH реакционной смеси в диапазоне от 10 до 10,5 и температуру в пределах от 20 до 30°C. Добавление осуществляли в течение трех часов и перемешивали реакционную смесь в течение еще 4 ч при 25°C. Доводили pH до 7,5, добавляя несколько капель HCl. Доводили содержание твердого вещества в реакционной смеси до 40%, получая 1034 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента, при этом полностью исчез сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
Результаты исследования полученной водной смеси ПАВ были следующими:
|
Пример 12: Превращение водной смеси Примера 1 (кокоил-изетионат натрия и N-кокоил-глицинат натрия (1:2)) в порошок
Водный раствор примера 1 распыляли в токе азота и распыленные частицы высушивали током горячего воздуха с температурой 180°C (температура входящего воздуха) и 100°C (температура выходящего воздуха) в лабораторном аппарате для распылительной сушки при расходе потока 200 мл/ч.
В полученном мелкодисперсном порошке наблюдалось следующее распределение размеров частиц: 80% в диапазоне размеров 60-200 меш, 10% более 200 меш и 10 менее 60 меш.
Полученный порошок подвергали повторному растворению, получая водный раствор с содержанием твердого вещества 30%.
Дополнительный пример 1: Синтез смеси кокоил-изетионата натрия и кокоил-глицината натрия (1:5)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
С8: 5,0%
С10: 6,0%
С12: 63%
С14: 20%
С16: 6%
С18: 0,4%
К кокоил-хлориду (200 г, 0,897 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (22,15 г, 0,1495 г-моль) и перемешивали полученную суспензию при 55-60°С в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (216,5 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (57,22 г, 0,7629 г-моль) в воде (628 г) вместе с раствором гидроксида натрия (48,8%, 124,6 г, 1,511 г-моль), поддерживая рН реакционной смеси в диапазоне от 10,2 до 10,5 и температуру в пределах от 20 до 30°С. Добавление осуществляли в течение двух часов и перемешивали реакционную смесь в течение еще 4 ч при 25°С. Доводили рН до 7,5, добавляя HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1026 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 3344 см-1. Другой значимый сигнал при частоте 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчезал сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
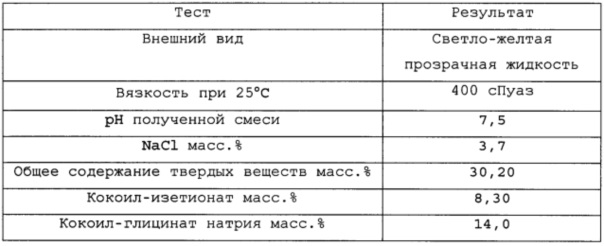
Результаты исследования полученной водной смеси ПАВ были следующими:
Дополнительный пример 2: Синтез смеси кокоил-изетионата натрия и кокоил-глицината натрия (1:5)
Кокоил-хлорид, который применялся в этом эксперименте, имел следующее распределение длины алкильных цепей:
С8: 5,0%
С10: 6,0%
С12: 63%
С14: 20%
С16: 6%
С18: 0,4%
К кокоил-хлориду (200 г, 0,897 г-моль) при перемешивании в слабом токе азота при комнатной температуре добавляли изетионат натрия (12,07 г, 0,0815 г-моль) и перемешивали полученную суспензию при 55-60°С в течение 4 ч. Образующийся газообразный HCl поглощали раствором щелочи, и за ходом реакции наблюдали с помощью ИК-спектроскопии. Спектр FTIR промежуточно полученной реакционной смеси показал наличие не вступившего в реакцию кокоил-хлорида (валентные колебания карбонила при 1800 см-1), кокоил-изетионата натрия (карбонил сложноэфирной группы при 1734 см-1) и исчезновение сигнала гидроксила (3323 см-1) изетионата натрия.
Текучую вязкую реакционную массу (209 г) охлаждали до комнатной температуры и затем медленно при перемешивании добавляли к раствору глицина (62,38 г, 0,8318 г-моль) в воде (629 г) вместе с раствором гидроксида натрия (48,8%, 135,86 г, 1,6473 г-моль), поддерживая рН реакционной смеси в диапазоне от 10,2 до 10,5 и температуру в пределах от 20 до 30°С. Добавление осуществляли в течение двух часов и перемешивали реакционную смесь в течение еще 4 ч при 25°С. Доводили рН до 7,5, добавляя HCl. Доводили содержание твердого вещества в реакционной смеси до 30%, получая 1037 г продукта в форме водного раствора.
ИК-спектр высушенного образца продемонстрировал валентные колебания карбонила амидной группы при 1600-1620 см-1 и сигнал NH при 334 4 см-1. Другой значимый сигнал при частоте 1734 см-1 соответствовал карбонилу сложноэфирного фрагмента алканоил изетионата, при этом полностью исчезал сигнал валентных колебаний карбонила (1800 см-1) кокоил-хлорида.
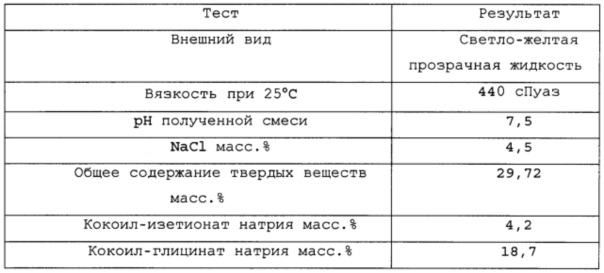
Результаты исследования полученной водной смеси ПАВ были следующими: