Результат интеллектуальной деятельности: ЭКСПРЕССИОННЫЕ СИСТЕМЫ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение касается экспрессионных систем, включающих полинуклеотиды, кодирующие белки, причем экспрессионная система содержит первый полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует Т-клеточный ответ, и второй полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует В-клеточный ответ против патогена. Изобретение также касается смесей белков, кодируемых экспрессионной системой, и клеток, содержащих экспрессионную систему или смесь белков, и фармацевтических композиций, содержащих экспрессионную систему или смесь белков. Экспрессионная система, полинуклеотиды, белки, клетки и фармацевтические композиции применимы при профилактике или лечении инфекций. Изобретение также касается нуклеотидных конструкций и экспрессионных систем, кодирующих модифицированный гемагглютинин (НА) вируса гриппа.
Уровень техники
Инфекционные заболевания все еще представляют большую угрозу для человечества. Одним из способов предотвращения или лечения инфекционных заболеваний является искусственное индуцирование иммунного ответа путем вакцинации, которая представляет собой введение антигенного материала индивиду с тем, чтобы возникал адаптивный иммунный ответ против соответствующего антигена. Антигенным материалом могут быть такие патогены (например, микроорганизмы или вирусы), которые интактны по структуре, но инактивированы (т.е. не инфекционны) или ослаблены (т.е. с пониженной инфекционностью), либо очищенные компоненты патогена, которые оказались сильно иммуногенными. Другой подход к индуцированию иммунного ответа против патогена состоит в обеспечении экспрессионных систем, содержащих один или несколько векторов, кодирующих иммуногенные белки или пептиды патогена. Такой вектор может иметь вид голой плазмидной ДНК, или же иммуногенные белки или пептиды вводятся с помощью вирусных векторов, к примеру, на основе модифицированных вирусов осповакцины (например, модифицированного вируса осповакцины Ankara; MVA) или аденовирусных векторов. Такие системы экспрессии обладают тем преимуществом, что они содержат хорошо изученные компоненты, обладающие слабой чувствительностью к условиям окружающей среды.
Конкретная задача при разработке экспрессионных систем на основе векторов состоит в том, чтобы применение таких экспрессионных систем на пациентах вызывало такой иммунный ответ, который будет защищать от инфекции соответствующим патогеном. Однако, несмотря на то что они индуцируют иммунногенный ответ против патогена, некоторые экспрессионные системы неспособны вызвать достаточно сильный иммунный ответ, который бы полностью защищал от инфекций, вызванных патогеном. Соответственно, все еще существует потребность в таких экспрессионных системах, которые способны индуцировать защитный иммунный ответ против патогенов, например, таких возбудителей инфекций, как вирусы.
Вирусы
Вирусы составляют группу таких патогенов/возбудителей инфекций, которые не обладают собственным метаболизмом и могут считаться облигатными эндопаразитами соответствующих клеток хозяев, использующими по меньшей мере часть аппарата клеток хозяев для осуществления экспрессии вирусных белков и репликации вируса. Вирусы можно классифицировать на основании типа (ДНК/РНК), количества нитей (одноцепочечная или двухцепочная), полярности (отрицательная или положительная) нуклеиновой кислоты, составляющей их геном, и их репликации (классификация Baltimore). Соответственно, вирусы обычно относятся к ДНК- или РНК-вирусам. Вирусы также могут относиться к одноцепочечным (оц) или двухцепочным (дц) ДНК- или РНК-вирусам, геном которых представлен одноцепочечной или двухцепочной нуклеиновой кислотой. У некоторых вирусов геном является частично двухцепочным и частично одноцепочечным (например, гепаднавирусы). Ориентация или направление генома и/или при изготовлении медикаментов для применения при профилактике или лечении от патогена и/или для применения в способах профилактики или лечения от патогена, причем патогенность играет важную роль в жизненном цикле вирусов, в частности, в жизненном цикле оцРНК-вирусов или оцДНК-вирусов. Геном из оцРНК плюс нити имеет такую же ориентацию, как и клеточная РНК, и может прямо транслироваться в вирусные белки. В жизненном цикле вирусов с геномом из одноцепочечной РНК минус нити((-)оцРНК) необходимо, чтобы геномные последовательности транскрибировались в мРНК плюс нити, которая может транслироваться в вирусные белки в клетках хозяевах. Одноцепочечной геном, содержащий и плюс, и минус нити, называется "амбисмысловым" (например, (+/-)оцРНК, (+/-)оцДНК)).
Несмотря на то что геном вирусов может быть весьма большим (например, в случае ДНК-вирусов), особенно небольшие РНК-вирусы эволюционно выработали стратегии для экспрессии своих генных продуктов (например, белков и пептидов) очень эффективным образом. Одной из таких стратегий является экспрессия одного или нескольких полибелков, кодируемых вирусным геномом, которые при ко- или посттрансляционном процессинге дают отдельные белки и/или пептиды. Эта стратегия принята, к примеру, у некоторых двухцепочечных (дц) РНК-вирусов или одноцепочечных (оц) РНК-вирусов с геномом из плюс нити. "Оболочечные вирусы", как-то ортомиксовирусы, парамиксовирусы, ретровирусы, флавивирусы, рабдовирусы и альфавирусы, окружены липидным бислоем, происходящим из плазматической мембраны хозяина (1).
У всех оболочечных вирусов встречаются соединительные гликопротеины, которые обеспечивают исходное взаимодействие между оболочкой вируса и плазматической мембраной клетки хозяина посредством связывания с углеводными группировками или доменами клеточной адгезии белков или другими молекулами на плазматической мембране клетки хозяина. Тем самым соединительные гликопротеины образуют мостик между вирусом и мембраной клетки хозяина. Соединительные гликопротеины, обозначаемые как "Н", обладают активностью гемагглютинина, а гликопротеины, обозначаемые как "HN", обладают активностями гемагглютинина и нейраминидазы. Соединительные гликопротеины обозначаются как "G", если они не обладают ни активностью гемагглютинина, ни активностью нейраминидазы.
Парамиксовирусы
Парамиксовирусы составляют семейство таких вирусов животных, которые содержат одноцепочечную несегментированную минус нить РНК. Парамиксовирусы ответственны за ряд заболеваний у животных и человека. РНК-геном парамиксовирусов имеет длину в 15-19 тысяч оснований (т.о.) и кодирует 6-10 генов. Каждый ген содержит старт/стоп-сигналы транскрипции в начале и в конце, которые транскрибируются в составе гена. Последовательности генов консервативны у всех парамиксовирусов вследствие феномена, известного как транскрипционная полярность, при которой гены, ближайшие к 3'-концу генома, транскрибируются в большем количестве, чем те, что расположены ближе к 5'-концу. После транскрипции каждого гена РНК-зависимая РНК-полимераза останавливается для высвобождения новой мРНК, когда она встречает межгенную последовательность. Когда РНК-полимераза останавливается, то есть вероятность, что она диссоциирует от РНК генома. Если она диссоциирует, то должна будет повторно войти в репликативный комплекс в области лидерной последовательности, а не продолжить транскрипцию оставшейся части генома. В результате этого, чем дальше будут находиться нижележащие гены от лидерной последовательности, тем меньше они будут транскрибироваться РНК-полимеразой. Гены парамиксовирусов располагаются в относительном порядке белков, необходимых для успешной инфекции. Консервативная последовательность генов такова: нуклеокапсид - фосфопротеин - матриксные - слияния - прикрепительный - большая субъединица (полимеразы).
Геномы многих парамиксовирусов следуют так называемому "правилу шести". Согласно этому правилу, общая длина генома почти всегда кратна шести. Однако члены подсемейства Pneumovirinae, содержащего респираторный синцитиальный вирус (RSV), не подчиняются этому правилу.
Респираторный синцитиальный вирус (RSV)
Оболочечный вирус, обозначаемый как респираторный синцитиальный вирус (RSV), является наиболее важной причиной вирусных заболеваний нижних дыхательных путей (LRTI) у младенцев и детей по всему миру (2). В Соединенных Штатах, по оценкам, каждый год подвергаются госпитализации 70000-126000 младенцев с пневмонией или бронхиолитом RSV, причем уровень госпитализации при бронхиолите все возрастает с 1980 г. (3). Дети заражаются к 2-летнему возрасту, а по оценкам ВОЗ вирус RSV вызывает заболевания примерно у 64 миллионов детей каждый год и 160000 смертей. В промышленно развитых странах RSV ответственен по меньшей мере за 50% случаев госпитализации при респираторных заболеваниях у детей, причем до 6% всех заражений RSV у детей заканчиваются госпитализацией (4). Заражение RSV не вызывает длительного иммунитета, так что организм человека испытывает пожизненные циклы инфицирования и повторного инфицирования. Несмотря на то, что RSV по традиции считается педиатрическим патогеном, он также вызывает тяжелое заболевание у пожилых и лиц с ослабленным иммунитетом (5). Бремя заболевания RSV у пожилых сравнимо с сезонным гриппом, а экономические последствия связанных с RSV заболеваний у взрослых по оценкам даже больше, чем у гриппа в отношении количества потерянных для работы дней (6, 7). Профилактика моноклональными антителами эффективно снижает госпитализацию при RSV на 50% у детей с повышенным риском тяжелого заболевания (8). Однако в настоящее время не существует эффективной вакцины или антивирусной терапии против RSV.
Катастрофический эффект вакцины из инактивированного формалином (FI) RSV у детей в 1960 г.г. помешал разработке вакцины. Вакцина не защищала от заражения RSV и усугубляла респираторное заболевание (9), что объясняли индуцированием высокого титра слабо нейтрализующих антител с низким сродством, отсутствием прайминга Т-клеток CD8+ и смещением иммунного ответа в сторону Th2 (10, 11 и 12). Существуют данные о том, что RSV нарушает возникновение адекватного адаптивного Т-клеточного иммунного ответа (13).
Таким образом, имеется явная потребность в эффективной вакцине не только для защиты детей, но также для повышения иммунитета у пожилых людей и уменьшения циркуляции RSV у братьев и сестер и у тех взрослых, которые являются основным источником заражения RSV для детей. Особенно желательно, чтобы вакцина против RSV была способна индуцировать нейтрализующие антитела и мощный и широкий Т-клеточный ответ для прайминга Т-клеточного ответа у тех лиц, которые еще не были инфицированы RSV (дети), или для усиления уже существующего Т-клеточного ответа у тех лиц, которым необходимо "перенастроить" реакцию памяти на более высокий уровень (пожилых).
Ортомиксовирусы
Ортомиксовирусы составляют семейство РНК-вирусов, которое включает пять родов: Influenzavirus A, Influenzavirus В, Influenzavirus С, Isavirus и Thogotovirus. Недавно был описан шестой род. Первые три рода включают вирусы, которые вызывают грипп у позвоночных, включая птиц, людей и других млекопитающих. Три рода вирусов гриппа имеют антигенные различия по нуклеопротеинам и матриксным белкам. Influenzavirus А инфицирует людей, других млекопитающих и птиц и вызывает все пандемии гриппа. Influenzavirus В инфицирует людей и тюленей. Influenzavirus С инфицирует людей и свиней.
Вирусы семейства Orthomyxovirus содержат от 6 до 8 сегментов линейной одноцепочечной РНК минус нити. Общая длина генома составляет 12000-15000 нуклеотидов (нт): наибольший сегмент - 2300-2500 нт; второй по величине - 2300-2500 нт; третий - 2200-2300 нт; четвертый - 1700-1800 нт; пятый - 1500-1600 нт; шестой -1400-1500 нт; седьмой - 1000-1100 нт; восьмой - 800-900 нт. Последовательность генома содержит концевые повторы, которые повторяются на обоих концах. Концевые повторы на 5'-конце имеют длину в 12-13 нуклеотидов. Нуклеотидные последовательности с 3'-конца идентичны таковым у родов того же семейства; у большинства (сегментов) РНК либо у всех разновидностей РНК. Концевые повторы на 3'-конце имеют длину в 9-11 нуклеотидов.
Вирус гриппа является одним из наиболее важных дыхательных патогенов. Только в США заражение гриппом ответственно за 20000-40000 смертей и более 100000 случаев госпитализации в год (1). Младенцы, пожилые люди и лица с ослабленной сердечной, легочной или иммунной системой подвергаются большому риску серьезных осложнений после заражения гриппом.
Иммунизация оказалась наиболее эффективной мерой при профилактике заболевания. Одной из общих черт у всех современных вакцин против гриппа является индукция главным образом нейтрализующих антител, направленных против главного белка вирусной оболочки - гемагглютинина (НА).
Сущность изобретения
В первом аспекте изобретением предусмотрена экспрессионная система, содержащая первый полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует Т-клеточный ответ, и второй полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует В-клеточный ответ против патогена.
Во втором аспекте изобретением предусмотрена выделенная смесь белков, кодируемых экспрессионной системой из первого аспекта.
В третьем аспекте изобретением предусмотрены выделенные клетки хозяева, содержащие экспрессионную систему из первого аспекта и/или смесь белков из второго аспекта.
В четвертом аспекте настоящим изобретением предусмотрена композиция, содержащая экспрессионную систему из первого аспекта и/или смесь белков из второго аспекта и фармацевтически приемлемый носитель и/или наполнитель.
В пятом аспекте настоящим изобретением предусмотрена экспрессионная система из первого аспекта, смесь белков из второго аспекта, клетки из третьего аспекта и композицию из четвертого аспекта для применения в медицине, в частности, при лечении или профилактике инфекционных заболеваний, предпочтительно вирусных заболеваний.
В шестом аспекте настоящим изобретением предусмотрен способ лечения или профилактики вирусных заболеваний, включающий введение эффективного количества экспрессионной системы из первого аспекта, смеси белков из второго аспекта, клеток из третьего аспекта и композиции из четвертого аспекта.
В седьмом аспекте настоящим изобретением предусмотрен способ усиления иммунного ответа, включающий введение эффективного количество экспрессионной системы из первого аспекта, смеси белков из второго аспекта, клеток из третьего аспекта и композиции из четвертого аспекта.
В восьмом аспекте настоящим изобретением предусмотрены нуклеотидные конструкции, кодирующие гемагтлютинин (НА) вируса гриппа, экспрессионная система, содержащая эти нуклеотидные конструкции, и белки или полипротеины, кодируемые нуклеотидными конструкциями или экспрессионной системой, при этом сайт расщепления НАО имеет многоосновную последовательность.
В девятом аспекте настоящим изобретением предусмотрено применение многоосновного сайта расщепления НАО для конструирования систем экспрессии, способных экспрессировать гемагглютинин (НА) вируса гриппа in vitro и/или in vivo.
В десятом аспекте изобретением предусмотрена выделенная смесь белков, кодируемых экспрессионной системой из восьмого аспекта.
В одиннадцатом аспекте изобретением предусмотрены выделенные клетки хозяева, содержащие нуклеотидные конструкции, экспрессионную систему либо белки или полипротеины из восьмого аспекта и/или смесь белков из десятого аспекта.
В двенадцатом аспекте настоящим изобретением предусмотрена композиция, содержащая нуклеотидные конструкции, экспрессионную систему либо белки или полипротеины из восьмого аспекта или смесь белков из десятого аспекта и фармацевтически приемлемый носитель и/или наполнитель.
В тринадцатом аспекте настоящим изобретением предусмотрены нуклеотидные конструкции, экспрессионная система либо белки или полипротеины из восьмого аспекта, смесь белков из десятого аспекта, клетки из одиннадцатого аспекта и композиция из двенадцатого аспекта для применения в медицине, в частности, при лечении или профилактике инфекций, вызванных вирусом гриппа.
В четырнадцатом аспекте настоящим изобретением предусмотрен способ лечения или профилактики инфекций, вызванных вирусом гриппа, включающий введение эффективного количества нуклеотидных конструкций, экспрессионной системы либо белков или полипротеинов из восьмого аспекта, смеси белков из десятого аспекта, клеток из одиннадцатого аспекта и композиции из двенадцатого аспекта.
В пятнадцатом аспекте настоящим изобретением предусмотрен способ усиления иммунного ответа, включающий введение эффективного количества нуклеотидных конструкций, экспрессионной системы либо белков или полипротеинов из восьмого аспекта, смеси белков из десятого аспекта, клеток из одиннадцатого аспекта и композиции из двенадцатого аспекта.
В вышеприведенном кратком изложении не обязательно описаны все аспекты настоящего изобретения.
Краткое описание фигур
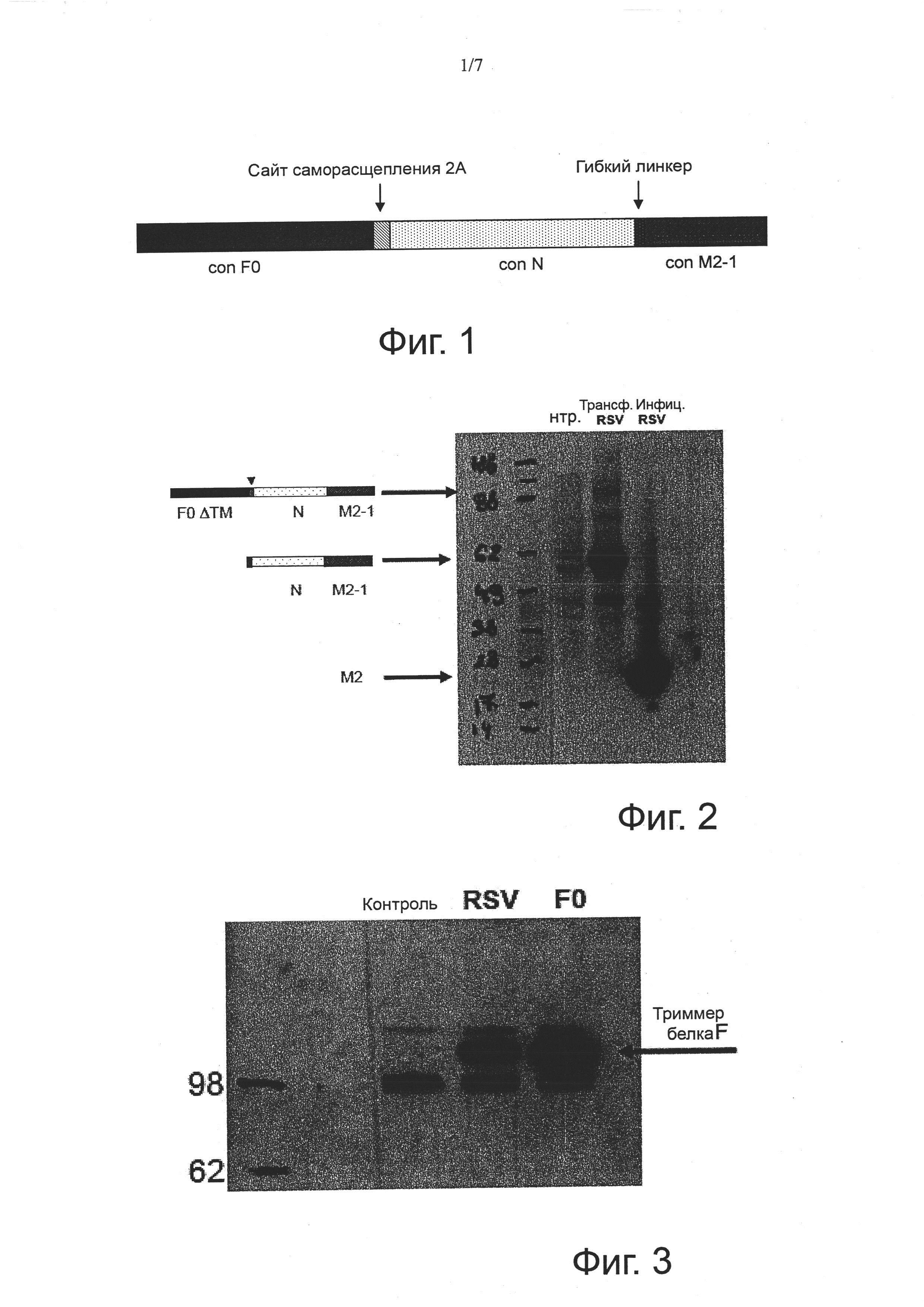
Фиг. 1. Схематическое изображение вакцинного полипротеина RSV. conF0 = консенсусная последовательность белка F; 2А = трансляционный сайт расщепления вируса ящура; conN = консенсусная последовательность белка N; conM2-1 = консенсусная последовательность белка М2-1.
Фиг. 2. Вакцинный антиген F0ΔTM-N-M2-1 подвергается эффективному процессингу в клетках млекопитающих. Анализ методом Вестерн-блот лизатов клеток HeLa. нтр.: нетрансфецированные клетки Hela; трансф. RSV: клетки HeLa, трансфецированные F0ΔTM-N-M2-1; инфиц. RSV: клетки Нер2, инфицированные RSV штамма А.
Фиг. 3. Секретируемый белок F образует гомотример. Анализ методом Вестерн-блот супернатантов из трансфецированных клеток HeLa. RSV: клетки трансфецированы F0ΔTM-N-M2-1; F0: клетки трансфецированы F0ΔTM; Ctrl: клетки трансфецированы пустой плазмидой.
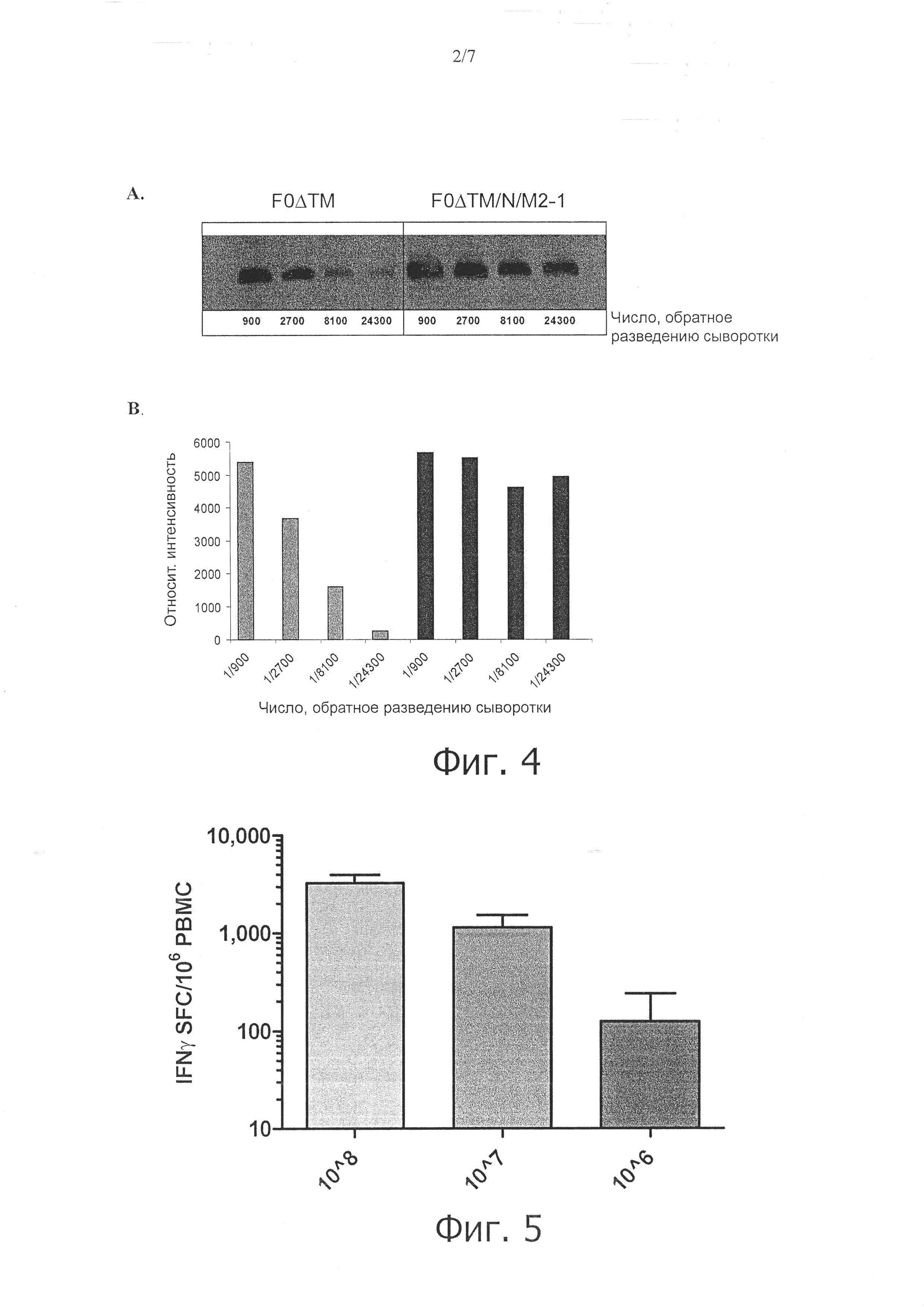
Фиг. 4. Белок F, экспрессируемый из вакцинного полипротеина, является лучшим иммуногеном, чем сам белок F. А. Анализ методом Вестерн-блот супернатанта из клеток HeLa, инфицированных PanAd3/F0ΔTM-N-M2-1, который зондировали различными разведениями сыворотки от мышей, иммунизированных F0ΔTM или F0ΔTM-N-M2-1. В. Денситометрическое сканирование Вестерн-блота из панели А. Данные выражены в виде относительной интенсивности зоны, соответствующей полосе белка.
Фиг. 5. Вакцина против RSV индуцирует сильный системный Т-клеточный иммунитет у мышей при однократном внутримышечном введении. Анализ методом IFNg-Elispot спленоцитов мышей Balb/C, иммунизированных PanAd3/F0ΔTM-N-M2-1, с помощью картированных иммунодоминантных пептидов из белков F и M RSV.
Фиг. 6. Схематическое изображение вакцинного полипротеина вируса гриппа. NP = консенсусная последовательность белка NP, М1 = консенсусная последовательность белка M1, 2А = трансляционный сайт расщепления вируса ящура, H1p = консенсусная последовательность белка НА из H1N12009.
Фиг. 7. Анализ методом Вестерн-блот экспрессии H1p в трансфецированных клетках HeLa. Полные лизаты клеток HeLa, трансфецированных PVJ-H1p (дорожка 1), PVJ-H1 (дорожка 2) и не трансфецированных CTR (дорожка 3). Стрелками показаны полосы, соответствующие нерасщепленной форме (70 кД) НА0 и расщепленному (28 кД) НА2. Поликлональная сыворотка против НА распознает эпитопы у фрагмента белка НА2. Видно, что белок H1p полностью подвергается процессингу.
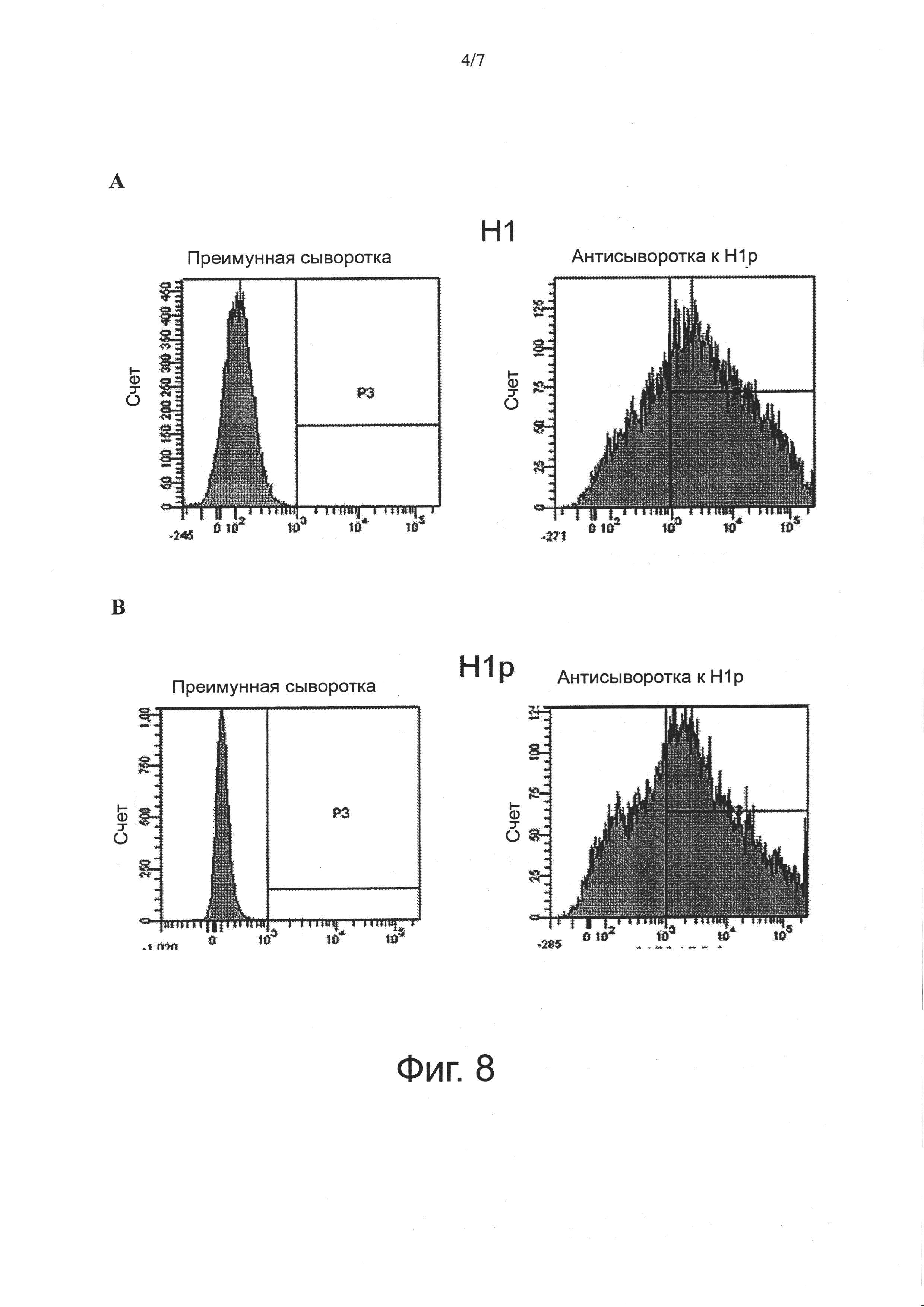
Фиг. 8. Анализ методом FACS на целых клетках экспонированных на мембране белков НА. На гистограммах представлена медиана флуоресценции клеток HeLa, трансфецированных НА дикого типа (справа сверху) и H1 (справа снизу). Клетки инкубировали с гипериммунной поликлональной сывороткой мышей против H1p, а затем с конъюгированным с РЕ вторичным антителом против мыши. Слева сверху и снизу клетки инкубировали с преиммунной сывороткой мышей, чтобы установить базальный уровень флуоресценции.
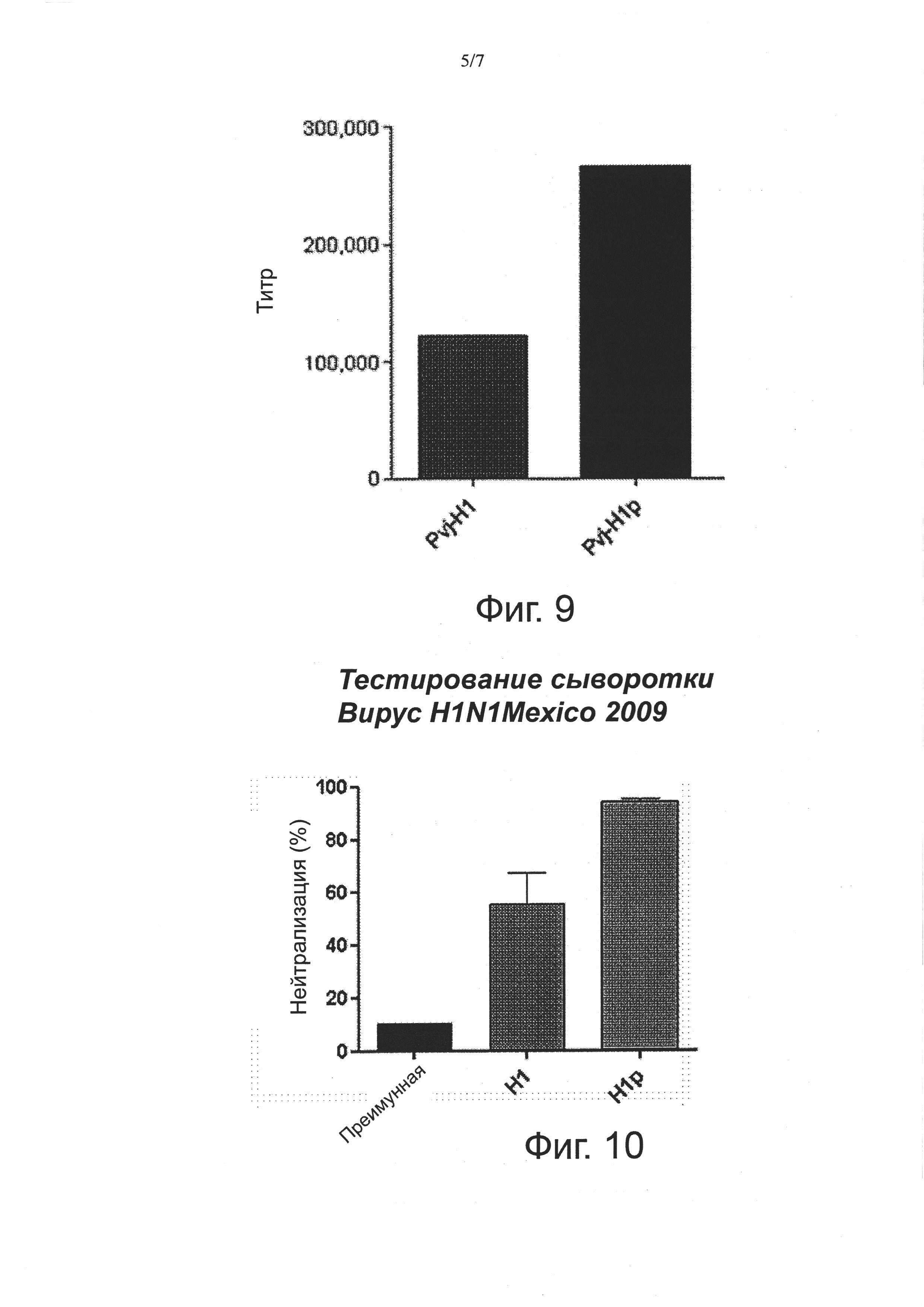
Фиг. 9. H1p способен индуцировать высокий титр антител. Анализ методом ELISA на фиксированном рекомбинантном НА (H1N1California 2009). Титры антител измеряли на сыворотке животных, иммунизированных H1 и H1p. Титры рассчитывали по серийным разведениям сыворотки и они представляют разведения, дающие значения OD, в три раза превышающие уровень фона.
Фиг. 10. Заражение клеток MDCK псевдотипированным по НА (H1N1Mexico 2009) вирусом сильнее нейтрализуется сывороткой от животных, иммунизированных H1p. Результаты анализа методом ELISA на фиксированном рекомбинантном НА (H1N1California 2009) с использованием сыворотки от животных, иммунизированных H1p и NPM1H1p.
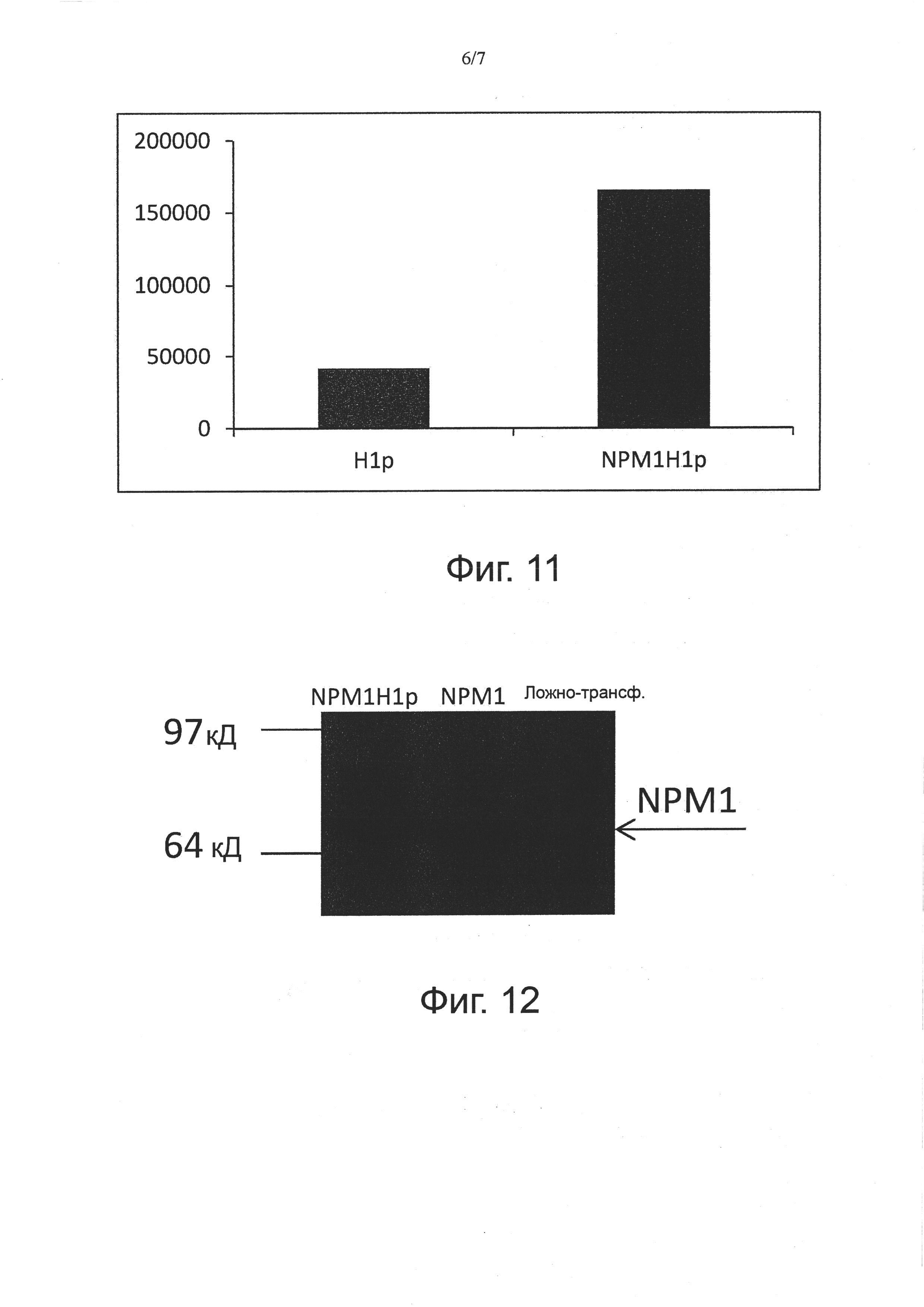
Фиг. 11. Экспрессия H1p на фоне тройного антигена способна индуцировать высокий титр антител. Анализ методом ELISA на фиксированном рекомбинантном НА (H1N1 California 2009). Титры антител измеряли на сыворотке от животных, иммунизированных H1p и NPM1H1p. Титры рассчитывали по серийным разведениям сыворотки и они представляют разведения, дающие значения OD, в три раза превышающие уровень фона.
Фиг. 12. Анализ методом Вестерн-блот экспрессии антигена NPM1H1p в трансфецированных клетках HeLa показывает, что белок полностью подвергается процессингу. Полные лизаты клеток HeLa, трансфецированных pNEB-NPM1H1p (дорожка 1), pNEB-NPM1 (дорожка 2) и ложно-трансфецированных (дорожка 3). Стрелкой показана полоса, соответствующая слитому белку NPM1 (70 кД). Для выявления внутриклеточного белка использовали моноклональное антитело против NP.
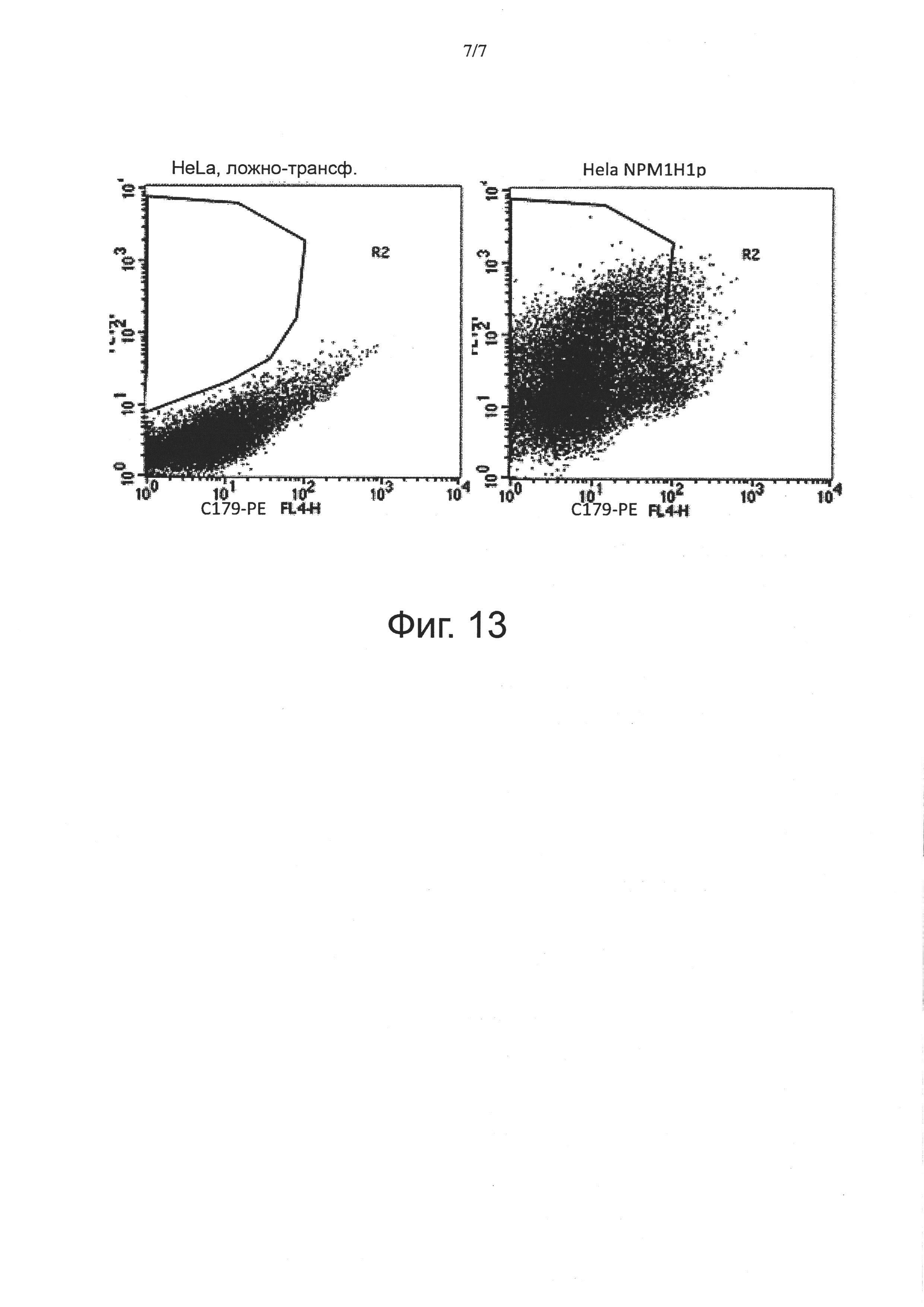
Фиг. 13. H1p, полученный при процессинге NPM1H1p, экспонирован на клеточной мембране и имеет правильную укладку. Анализ методом FACS на целых клетках ложно-трансфецированных (слева) или трансфецированных NPM1H1p (справа) клеток HeLa. Клетки инкубировали с мышиным mAb С179, которое связывается с конформационным эпитопом на стволовом участке НА, а затем с вторичным конъюгированным с РЕ антителом против мыши.
Раскрытие сущности изобретения
Перед тем, как перейти к подробному описанию настоящего изобретения, следует иметь в виду, что настоящее изобретение не ограничивается конкретной методологией, методиками и реагентами, описанными здесь, поскольку они могут меняться. Также следует иметь в виду, что используемая здесь терминология предназначена только для описания определенных воплощений и не должна ограничивать объем настоящего изобретения, который должен ограничиваться лишь прилагаемой формулой изобретения. Если не указано иначе, все используемые здесь технические и научные термины имеют те же значения, которые обычно понимаются рядовыми специалистами в данной области.
Предпочтительно используемые здесь термины определяются так, как описано в "А multilingual glossary of biotechnological terms: (IUPAC Recommendations)", Leuenberger H.G.W., Nagel В. and Kölbl H., eds. (1995) Helvetica Chimica Acta, CH-4010 Basel, Switzerland).
По всему тексту настоящего описания приводятся некоторые документы. Каждый из процитированных здесь документов (включая все патенты, патентные заявки, научные публикации, спецификации производителя, инструкции, номера доступа в GenBank поданных последовательностей и т.д.), независимо от того, приведен он выше или ниже, включен сюда путем ссылки во всей полноте. Ничто в нем не должно восприниматься как допущение того, что изобретение не может датироваться задним числом по факту более раннего создания настоящего изобретения (antedate).
Определения
По всему описанию и в прилагаемой формуле изобретения, если контекстом не требуется иначе, слово "включать" и такие его варианты, как "включает" и "включающий", следует понимать, как включение приведенного числа или стадии, но не исключение любого другого числа или стадии или группы чисел или стадий.
Сокращения "F" или "F0" здесь применяются взаимозаменяемым образом и относятся к белку слияния парамиксовирусов, предпочтительно вируса RSV.
Сокращение "G" относится к гликопротеину парамиксовирусов, предпочтительно пневмовирусов, более предпочтительно вируса RSV.
Сокращение "Н" относится к белку гемагглютинину парамиксовирусов, предпочтительно морбилливирусов.
Сокращение "HN" относится к белку гемагглютинину-нейраминидазе парамиксовирусов, в частности респировируса, авулавируса и рубулавируса.
Сокращение "N" относится к нуклеокапсидному белку парамиксовирусов, предпочтительно вируса RSV.
Сокращение "М" относится к гликозилированному матриксному белку парамиксовирусов, предпочтительно вируса RSV.
Что касается парамиксовирусов, то сокращение "М2" or "М2-1" относится к негликозилированному матриксному белку парамиксовирусов, предпочтительно вируса RSV.
Сокращение "Ρ" относится к фосфопротеину парамиксовирусов, предпочтительно вируса RSV.
Что касается парамиксовирусов, то сокращения "NS1" и "NS2" относятся к неструктурным белкам 1 и 2 парамиксовирусов, предпочтительно вируса RSV.
Сокращение "L" относится к каталитической субъединице полимеразы парамиксовирусов, предпочтительно вируса RSV.
Сокращение "НА" относится к гемагглютинину ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "НАО" относится к белку-предшественнику субъединиц НА1 и НА2 гемагглютинина ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "H1p" относится к модифицированному гемагглютинину ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "NA" относится к нейраминидазе ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "NP" относится к нуклеопротеину ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "M1" относится к матриксному белку 1 ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Что касается ортомиксовирусов, то сокращение "М2" относится к матриксному белку М2 ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Что касается ортомиксовирусов, то сокращение "NS1" относится к неструктурному белку 1 ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "NS2/NEP" относится к неструктурному белку 2 (также называется NEP, ядерный экспортный белок) ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "РА" относится к белку субъединицы полимеразы ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "РВ1" относится к белку субъединицы полимеразы ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "РВ2" относится к белку субъединицы полимеразы ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Сокращение "PB1-F2" или "PB1F2" относится к белку, кодируемому альтернативной рамкой считывания у сегмента гена РВ1 ортомиксовирусов, предпочтительно вирусов гриппа, более предпочтительно вируса гриппа А.
Термином "экспрессионная система" в настоящем изобретении обозначается система, предназначенная для получения одного или нескольких представляющих интерес генных продуктов. Как правило, такая система разрабатывается "искусственно", т.е. посредством генных технологий, применимых для получения представляющего интерес генного продукта как в бесклеточных системах in vitro, так и в клеточных системах in vivo. Понятно, что естественные экспрессионные систем, такие, к примеру, как нативные вирусы, не охватываются экспрессионной системой настоящего изобретения.
Термин "представляющий интерес генный продукт", как правило, относится к таким макромолекулам, без ограничения, как РНК, пептиды, полипептиды или белки либо их сегменты, эпитопы или фрагменты.
В экспрессионной системе определенный генный продукт кодируется одной или несколькими молекулами нуклеиновой кислоты. Молекулы нуклеиновой кислоты понимаются как полимерные макромолекулы, состоящие из мономеров. Нуклеотиды-мономеры состоят из нуклеотидного основания, пятиуглеродного сахара (типа рибозы или 2'-дезоксирибозы, но не ограничиваясь этим) и от одной до трех фосфатных групп. Как правило, полинуклеотид образуется посредством фосфодиэфирных связей между отдельными нуклеотидами-мономерами. В контексте настоящего изобретения к молекулам нуклеиновой кислоты относятся, без ограничения, рибонуклеиновая кислота (РНК) и дезоксирибонуклеиновая кислота (ДНК). Термины "полинуклеотид" и "нуклеиновая кислота" применяются здесь взаимозаменяемым образом.
В бесклеточных системах экспрессии в качестве матрицы для реакций трансляции in vitro используются выделенные полинуклеотиды. В клеточных системах экспрессии полинуклеотиды содержатся в одном или нескольких векторах. В настоящем изобретении термин "вектор" относится к белкам или полинуклеотидам либо их смесям, которые могут вводиться или вводить содержащиеся в них белки и/или нуклеиновые кислоты в клетки. В контексте настоящего изобретения предпочтительно, чтобы гены, кодируемые введенным полинуклеотидом, экспрессировались внутри клетки после введения вектора или векторов. Примеры подходящих векторов включают, без ограничения, плазмиды, космиды, фаги, вирусы или искусственные хромосомы.
Фраза "индукция Т-клеточного ответа" относится к образованию или повторной стимуляции специфичных к вирусу Т-клеток CD4+или CD8+. Экспрессионная система изобретения может индуцировать или повторно стимулировать опосредованный Т-клетками адаптивный ответ, направленный на эпитопы МНС класса I или класса II, присутствующие в вирусных белках, экспрессируемых полинуклеотидом. Такой Т-клеточный ответ можно измерить известными методами, предпочтительно посредством повторной стимуляции Т-клеток ex vivo синтетическими пептидами, охватывающими все вирусные белки, и анализа пролиферации или продукции γ-интерферона.
Фраза "индукция В-клеточного ответа" относится к образованию или повторной стимуляции специфичных к вирусу В-клеток, вырабатывающих иммуноглобулины класса IgG или IgA. Экспрессионная система изобретения может индуцировать или повторно стимулировать В-клетки, вырабатывающие антитела, специфичные к патогенным, например, вирусным антигенам, экспрессируемым полинуклеотидом. Такой В-клеточный ответ можно измерить методом ELISA (ферментного иммуносорбентного анализа) с помощью синтетического антигена из сыворотки или иммуноглобулина из слизистой. С другой стороны, титр индуцированных антител можно измерить методами нейтрализации вируса.
Фраза "индукция В-клеточного ответа против патогена" относится к образованию или повторному стимулированию специфичных к вирусу В-клеток, вырабатывающих иммуноглобулины класса IgG или IgA, которые инактивируют, блокируют и/или нейтрализируют соответствующий патоген таким образом, что вызванное патогеном заболевание не возникает и/или его симптомы ослабляются. Это также называется "защитным иммунным ответом" против патогена. Экспрессионные системы настоящего изобретения могут индуцировать или повторно стимулировать В-клетки, вырабатывающие антитела, специфичные к патогенным, например, вирусным антигенам, экспрессируемым полинуклеотидом. Такой В-клеточный ответ можно измерить методом ELISA (ферментного иммуносорбентного анализа) с помощью синтетического антигена из сыворотки или иммуноглобулина из слизистой. С другой стороны, титр индуцированных антител можно измерить методами нейтрализации вируса.
Фраза "усиление иммунного ответа" относится к усилению или интенсификации гуморального и/или клеточного иммунного ответа против иммуногена, предпочтительно патогена, более предпочтительно вируса. Усиление иммунного ответа можно измерить путем сравнения иммунного ответа, вызванного экспрессионной системой изобретения, с иммунным ответом от экспрессионной системы, экспрессирующей тот же самый антиген/иммуноген сам по себе, с помощью описанных здесь тестов и/или тестов, хорошо известных в данной области техники.
В экспрессирующей системе определенный ген может кодироваться одним полинуклеотидом или несколькими отдельными полинуклеотидами. В клеточных системах экспрессии один или несколько полинуклеотидов могут содержаться в одном или нескольких отдельных векторах. Каждый из этих полинуклеотидов может кодировать весь генный продукт или его часть.
Кроме того, экспрессионные системы могут включать и "контролирующие экспрессию последовательности", регулирующие экспрессию данного гена. Как правило, контролирующие экспрессию последовательности представлены полипептидами или полинуклеотидами, такими, без ограничения, как промоторы, энхансеры, сайленсеры, инсуляторы или репрессоры.
Соответственно, вектор, содержащий один или несколько полинуклеотидов, кодирующих один или несколько генных продуктов, может содержать дополнительные контролирующие экспрессию последовательности. У вектора, содержащего один или несколько полинуклеотидов, кодирующих один или несколько генных продуктов, экспрессия может контролироваться вместе или по отдельности одной или несколькими контролирующими экспрессию последовательностями. В частности, каждый полинуклеотид, содержащийся в векторе, может контролироваться отдельной контролирующей экспрессию последовательностью, или же все полинуклеотиды в векторе могут контролироваться одной контролирующей экспрессию последовательностью. Полинуклеотиды, содержащиеся в одном векторе контролем одной контролирующей экспрессию последовательности, предпочтительно образуют открытую рамку считывания.
Термин "экспрессионная система" также охватывает экспрессию определенного генного продукта, включая транскрипцию полинуклеотидов, сплайсинг РНК, трансляцию в полипептид и посттрансляционную модификацию полипептида или белка.
Термин "открытая рамка считывания" (ORF) относится к последовательности нуклеотидов, которая может транслироваться в аминокислоты. Как правило, такие ORF содержат стартовый кодон, а последующие участки обычно имеют длину, кратную 3 нуклеотидам, но не содержат стоп-кодон (TAG, ТАА, TGA, UAG, UAA или UGA) в данной рамке считывания. Как правило, ORFs встречаются в природе или конструируются искусственно, т.е. средствами генной технологии. ORF кодирует белок, причем аминокислоты, в которые он может транслироваться, образуют соединенную пептидными связями цепь.
Термины "белок", "полипептид" и "пептид" применяются здесь взаимозаменяемым образом и относятся к любой соединенной пептидными связями цепи аминокислот, независимо от длины или посттрансляционной модификации.
Термин "посттрансляционные" в настоящем изобретении относится к событиям, происходящим после трансляции триплета нуклеотидов в аминокислоту и образования пептидной связи со следующей аминокислотой в последовательности. Такие посттрансляционные события могут происходить после того, как образуется полипептид, или же в процессе трансляции в тех частях полипептида, которые уже подверглись трансляции. Посттрансляционные события, как правило, изменяют или модифицируют химические или структурные свойства образующегося полипептида. Примеры посттрансляционных событий включают, без ограничения, такие события, как гликозилирование или фосфорилирование аминокислот либо расщепление пептидной цепи, например, эндопептидазой.
Термин "котрансляционные" в настоящем изобретении относится к событиям, происходящим во время процесса трансляции триплета нуклеотидов в аминокислотную цепь. Эти события, как правило, изменяют или модифицируют химические или структурные свойства образующейся аминокислотной цепи. Примеры котрансляционных событий включают, без ограничения, события, которые могут полностью остановить процесс трансляции или прервать образование пептидной связи, приводя к образованию двух отдельных продуктов трансляции.
Термины "полипротеин" или "искусственный полипротеин" в настоящем изобретении относятся к такой аминокислотной цепи, которая содержит или в основном состоит или состоит из двух аминокислотных цепей, которые не соединяются в природе друг с другом. Полипротеин может содержать одну или несколько дополнительных аминокислотных цепей. Каждая аминокислотная цепь предпочтительно составляет полный белок, т.е. охватывает весь ORF, или же его фрагмент, домен или эпитоп. Отдельные части полипротеина могут постоянно либо временно соединяться друг с другом. Те части полипротеина, которые соединены постоянно, транслируются с одного ORF и после этого не отделятся ко- или посттрансляционно. Те части полипротеина, которые соединены временно, тоже могут происходить из одного ORF, но они отделяются котрансляционно вследствие разделения в процессе трансляции или посттрансляционно вследствие расщепления пептидной цепи, например, эндопептидазой. С другой стороны, части полипротеина также могут происходить из двух различных ORF и соединяться посттрансляционно, к примеру, посредством ковалентных связей.
Белки или полипротеины, применимые в настоящем изобретении (включая производные белков, варианты белков, фрагменты белков, сегменты белков, эпитопы белков и домены белков) могут быть дополнительно модифицированы посредством химической модификации. Это означает, что такой химически модифицированный полипептид содержит и другие химические группы, чем 20 природных аминокислот. Примеры таких других химических групп включают, без ограничения, гликозилированные аминокислоты и фосфорилированные аминокислоты. Химические модификации полипептида могут обеспечить предпочтительные свойства по сравнению с исходным полипептидом, например, повышение стабильности и/или увеличение времени полужизни и/или повышение растворимости в воде. Химические модификации, применимые к вариантам, использующимся в настоящем изобретении, включают, без ограничения: ПЭГилирование, гликозилирование негликозилированных исходных полипептидов или модифицирование профиля гликозилирования негликозилированных исходных полипептидов. Такие химические модификации, применимые к вариантам, использующимся в настоящем изобретении, могут происходить ко- или посттрансляционно.
Термин "сегмент" относится к любой части макромолекулы (например, полипептида, белка или полипротеина), на которые эта макромолекула может разделяться. Макромолекула может состоять из одного или нескольких сегментов. Такая сегментация может иметь место вследствие функциональных (например, иммунореактивных свойств или функции связывания с мембраной) или структурных (например, нуклеотидной или аминокислотной последовательности либо вторичной или третичной структуры) свойств макромолекулы и/или отдельного сегмента. В контексте настоящего изобретения термин "сегмент" предпочтительно относится к части белка или полипротеина. Особенно предпочтительно, чтобы такой сегмент сворачивался и/или функционировал независимо от остальной части белка или полипротеина.
"Эпитоп", также известный как антигенная детерминанта, представляет собой такой сегмент макромолекулы, который распознается иммунной системой, в частности антителами, В-клетками или Т-клетками. Эпитопами являются те части или сегменты макромолекулы, которые способны связываться с антителами или их антигенсвязывающими фрагментами. При этом термин "связывание" предпочтительно относится к специфическому связыванию. В контексте настоящего изобретения термин "эпитоп" предпочтительно относится к такому сегменту белка или полипротеина, который распознается иммунной системой. Эпитопы обычно состоят из химически активных поверхностных группировок молекул, как-то боковых цепей аминокислот или сахаров, и обычно имеют специфические трехмерные структурные характеристики, равно как и специфические характеристики заряда. Конформационные и не конформационные эпитопы отличаются тем, что связывание с первыми, но не последними, утрачивается в присутствии денатурирующих растворителей.
Термин "домен" в настоящем изобретении относится к таким сегментам последовательности или структуры белка или полипротеина (или соответствующей последовательности нуклеотидов), которая может эволюционировать, функционировать и/или существовать независимо от остальной части белковой цепи. Как правило, белок состоит из одного или нескольких доменов, каждый из которых имеет трехмерную структуру, которая стабильна и сворачивается независимо от остальной части белковой цепи. Такие домен обычно образуют независимые функциональные единицы внутри белка (например, трансмембранные домена, иммуноглобулиновые домены или ДНК-связывающие домены).
Термин "вариант" белка или сегмента в настоящем изобретении следует понимать как полипептид (или сегмент), который в сравнении с тем полипептидом (либо сегментом, эпитопом или доменом), из которого он происходит, отличается одним или несколькими изменениями в аминокислотной последовательности. Полипептид, из которого происходит вариант белка, также известен как исходный полипептид. Точно так же сегмент, из которого происходит вариант сегмента, также известен как исходный сегмент. Как правило, вариант конструируется искусственно, предпочтительно средствами генной технологии. Как правило, исходный полипептид является белком дикого типа или доменом белка дикого типа. В контексте настоящего изобретения также исходный белок (или исходный сегмент) предпочтительно имеет консенсусную последовательность двух или нескольких полипептидов дикого типа (или сегментов дикого типа). Кроме того, варианты, применимые в настоящем изобретении, могут происходить и из гомологов, ортологов или паралогов исходного полипептида либо из искусственно сконструированных вариантов, при условии, что вариант обладает по меньшей мере одной биологической активностью исходного полипептида. Изменения в аминокислотной последовательности могут представлять собой замены, вставки, делеции аминокислот, N-концевые усечения или С-концевые усечения или же любые комбинации таких изменений, которые могут происходить по одному или нескольким сайтам. В предпочтительных воплощениях применимые в настоящем изобретении варианты проявляют в общей сложности до 200 (до 1,2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20,25, 30, 35, 40,45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95, 100, ПО, 120, 130, 140, 150, 160, 170, 180, 190 или 200) изменений в аминокислотной последовательности (т.е. замен, вставок, делеций, N-концевых усечений и/или С-концевых усечений). Замены аминокислот могут быть консервативными и/или не консервативными. В предпочтительных воплощениях применимые в настоящем изобретении варианты отличаются от тех белков или доменов, из которых они происходят, заменой до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 100 аминокислот, предпочтительно консервативной заменой аминокислот.
С другой стороны, в настоящем изобретении "вариант" может характеризоваться определенной степенью идентичности последовательности с исходным полипептидом или исходным полинуклеотидом, из которого он происходит. В частности, вариант белка в контексте настоящего изобретения проявляет по меньшей мере 80%-ную идентичность последовательности со своим исходным полипептидом. А вариант полинуклеотида в контексте настоящего изобретения проявляет по меньшей мере 80%-ную идентичность последовательности со своим исходным полинуклеотидом. Предпочтительно идентичность последовательности у вариантов белка наблюдается на непрерывном отрезке из 20, 30, 40, 45, 50, 60, 70, 80, 90,100 или больше аминокислот. Предпочтительно идентичность последовательности у вариантов полинуклеотида наблюдается на непрерывном отрезке из 60, 90, 120, 135, 150, 180, 210, 240, 270, 300 или больше нуклеотидов.
Термин "идентичность последовательности по меньшей мере на 80%" применяется по всему описанию в отношении сравнения последовательностей полипептидов или полинуклеотидов. Это выражение предпочтительно означает идентичность последовательности по меньшей мере на 80%, на 81%, на 82%, на 83%, на 84%, на 85%, на 86%, на 87%, на 88%, на 89%, на 90%, на 91%, на 92%, на 93%, на 94%, на 95%, на 96%, на 97%), на 98%) или по меньшей мере на 99% соответствующему контрольному полипептиду или соответствующему контрольному полинуклеотиду. Предпочтительно данный полипептид и контрольный полипептид проявляют указанную идентичность последовательности на непрерывном участке из 20, 30, 40, 45, 50, 60, 70, 80, 90, 100 или больше аминокислот или же по всей длине контрольного полипептида. Предпочтительно данный полинуклеотид и контрольный полинуклеотид проявляют указанную идентичность последовательности на непрерывном участке из 60, 90, 120, 135, 150, 180, 210, 240, 270, 300 или больше нуклеотидов или же по всей длине контрольного полинуклеотида.
Варианты могут дополнительно или альтернативно включать делеции аминокислот, которые могут представлять собой N-концевые усечения, С-концевые усечения или внутренние делеции или же любые комбинации из них. Такие варианты, содержащие N-концевые усечения, С-концевые усечения и/или внутренние делеции, в контексте настоящей заявки называются "делеционными вариантами" или "фрагментами". Термины "делеционный вариант" и "фрагмент" используются здесь взаимозаменяемо. Фрагмент может быть природным (например, сплайс-варианты) или же он может быть сконструирован искусственно, предпочтительно средствами генной технологии. Предпочтительно фрагмент (или делеционный вариант) содержит делецию до 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 15, 20, 25, 30, 35, 40, 45, 50, 55, 60, 65, 70, 75, 80, 85, 90, 95 или 100 аминокислот на N-конце и/или С-конце и/или внутри по сравнению с исходным полипептидом, предпочтительно на N-конце, на N- и С-концах или на С-конце. В том случае, когда при сравнении двух последовательностей не указана эталонная последовательность, относительно которой нужно рассчитывать степень идентичности последовательности, то она рассчитывается по более длинной из двух сравниваемых последовательностей, если специально не указано иначе. Если указана эталонная последовательность, то идентичность последовательности определяется по полной длине эталонной последовательности, приведенной в SEQ ID, если специально не указано иначе. Например, при сравнении последовательности пептида, состоящего из 50 аминокислот, с аминокислотной последовательностью белка F согласно SEQ ID NO: 1 максимальная степень идентичности последовательности может составлять 10.04% (50/498), тогда как у последовательности длиной в 249 аминокислот максимальная степень идентичности последовательности может составлять 50.00% (249/498).
Сходство нуклеотидных и аминокислотных последовательностей, т.е. степень идентичности последовательностей, можно определить посредством выравнивания последовательностей. Такое выравнивание можно проводить с помощью нескольких известных алгоритмов, предпочтительно с помощью математического алгоритма Карлина и Альтшуля (Karlin & Altschul (1993) Proc. Natl. Acad. Sci. USA 90: 5873-5877), с помощью пакета HMMAlign (HMMER package, http://hmmer.wustl.edu/) или алгоритма CLUSTAL (Thompson J.D., Higgins D.G. & Gibson T.J. (1994) Nucleic Acids Res. 22, 4673-80), который доступен, например, на http://www.ebi.ac.uk/Tools/clustalw/ или на http://www.ebi.ac.uk /Tools/clustalw2/index.html или на http://npsa-pbil.ibcp.fr/cgibin/npsa_automat.pl?page=/NPSA/npsa_clustalw.html. Предпочтительно используются параметры по умолчанию в том виде, как они приведены на http://www.ebi.ac.uk/Tools/clustalw/ или на http://www.ebi.ac.uk/Tools/clustalw2/index.html. Степень идентичности последовательностей (совпадения последовательностей) можно рассчитать, например, с помощью BLAST, BLAT или BlastZ (или BlastX). Сходный алгоритм встроен в программы BLASTN и BLASTP по Altschul et al. (1990) J. Mol. Biol. 215: 403-410. Поиск полинуклеотидов по BLAST проводится с помощью программы BLASTN, счет = 100, длина слова = 12, чтобы получить последовательности полинуклеотидов, гомологичных тем нуклеиновым кислотам, которые кодируют F, N или М2-1. Поиск белков по BLAST проводится с помощью программы BLASTP, счет =50, длина слова=3, чтобы получить аминокислотные последовательности, гомологичные полипептиду F, полипептиду N или полипептиду М2-1. Для того, чтобы получить выравнивание с пробелами для сравнительных целей, применяется Gapped BLAST, как описано в Altschul et al. (1997) Nucleic Acids Res. 25: 3389-3402. При использовании программ BLAST и Gapped BLAST используются параметры по умолчанию соответствующих программ. Анализ совпадения последовательностей может дополняться признанными методами картирования гомологичности типа Shuffle-LAGAN (Brudno M., Bioinformatics 2003b, 19 Suppl 1:154-162) или случайных полей Маркова. Когда в настоящем изобретении приводится степень идентичности последовательностей, то она рассчитывается относительно полной длины более длинной последовательности, если специально не указано иначе.
Полинуклеотиды по изобретению кодируют белки, пептиды либо их варианты, содержащие аминокислоты, которые обозначаются по стандартным одно- или трехбуквенным кодам в соответствии со стандартом WIPO ST.25, если не указано иначе. Если не указано иначе, одно- или трехбуквенные коды обозначают встречающиеся в природе L-аминокислоты, а аминокислотные последовательности приводятся в направлении от N-конца к С-концу соответствующего белка, пептида либо их варианта.
В качестве меры идентичности последовательностей или гомологии между двумя последовательностями нуклеиновых кислот также может использоваться "гибридизация". Последовательность нуклеиновой кислоты, кодирующей белок изобретения, или любая ее часть может использоваться в качестве гибридизационного зонда в соответствии со стандартными методами гибридизации. Гибридизация соответствующего зонда с ДНК или РНК из тестируемого источника является показателем присутствия в нем ДНК или РНК мишени, соответственно. Условия гибридизации известны специалистам и приведены, к примеру, в Current Protocols in Molecular Biology, John Wiley & Sons, N.Y., 6.3.1-6.3.6, 1991. "Умеренные условия гибридизации" определяются как эквивалентные гибридизации в 2х растворе хлорида натрия/цитрата натрия (SSC) при 30°С с последующей отмывкой в 1×SSC, 0.1% SDS при 50°С. "Очень жесткие условия" определяются как эквивалентные гибридизации в 6×растворе хлорида натрия/цитрата натрия (SSC) при 45°С с последующей отмывкой в 0.2×SSC, 0.1% SDS при 65°С.
С другой стороны, делеционные варианты могут возникать не вследствие структурных делеций соответствующих аминокислот, как описано выше, а из-за того, что эти аминокислоты заингибированы либо иным образом не могут выполнять свою биологическую функцию. Как правило, такая функциональная делеция происходит вследствие вставок или замен в аминокислотной последовательности, изменяющих функциональные свойства образующегося белка, такие, без ограничения, как изменения химических свойств образующегося белка (например, замена гидрофобных аминокислот на гидрофильные аминокислоты), изменения постгрансляционных модификаций образующегося белка (например, посттрансляционного расщепления или профиля гликозилирования) либо изменения вторичной или третичной структуры белка. Кроме того, функциональная делеция также может возникнуть в результате транскрипционного или посттрансляционного сайленсинга гена (например, посредством siRNA) либо присутствия или отсутствия ингибиторных молекул, таких, без ограничения, как белковые ингибиторы или ингибиторные антитела.
В контексте настоящего изобретения предпочтительно то, что белок (либо сегмент или домен или эпитоп) "функционально делегирован" означает, что аминокислоты или нуклеотиды соответствующей последовательности либо подверглись делеции, либо присутствуют, но не выполняют свою биологическую функцию.
Термин "консенсусная" в настоящем изобретении относится к таким аминокислотным или нуклеотидным последовательностям, которые являются результатом множественного выравнивания последовательностей при сравнении друг с другом родственных последовательностей. Такая консенсусная последовательность состоит из аминокислот или нуклеотидов, наиболее часто встречающихся в каждом положении. В контексте настоящего изобретения предпочтительно последовательности, используемые при выравнивании последовательностей для получения консенсусной последовательности, представляют собой последовательности различных подтипов/серотипов вирусных штаммов, выделенных при самых разных вспышках заболевания по всему миру. Каждая индивидуальная последовательность, используемая при выравнивании, считается последовательностью определенного "изолята" вируса. Более подробное описание математических методов для получения такого консенсуса приводится в разделе Примеры. В том случае, когда для данного положения невозможно определить "консенсусный нуклеотид" или "консенсусную аминокислоту", например, потому что сравнивались только два изолята, то предпочтительно используются аминокислоты каждого изолята. Полученный белок проверяется на его способность индуцировать В-клетки и/или Т-клетки, соответственно.
"Пептидный линкер" (или просто "линкер") в контексте настоящего изобретения означает аминокислотную последовательность длиной от 1 до 100 аминокислот. В предпочтительных воплощениях пептидный линкер по настоящему изобретению имеет минимальную длину по меньшей мере в 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29 или 30 аминокислот. В других предпочтительных воплощениях пептидный линкер по настоящему изобретению имеет максимальную длину в 100, 95, 90, 85, 80, 75, 70, 65, 60, 55, 50,45,40, 35, 34,33, 32, 31, 30, 29, 28, 27, 26, 25, 24, 23, 22, 21, 20, 19, 18, 17, 16 или 15 аминокислот или меньше. Предпочтительно пептидный линкер обеспечивает гибкость между аминокислотами из двух белков, фрагментов, сегментов, эпитопов и/или доменов, соединенных друг с другом. Такая гибкость обычно возрастает, если аминокислоты небольшие. Так, предпочтительно пептидный линкер настоящего изобретения имеет повышенное содержание небольших аминокислот, в частности глицина, аланина, серина, треонина, лейцина и изолейцина. Предпочтительно более 20%, 30%, 40%, 50%, 60% или больше аминокислот пептидного линкера представлены небольшими аминокислотами. В предпочтительном воплощении аминокислоты линкера выбирают из глицина и серина. В особенно предпочтительных воплощениях приведенная выше предпочтительная минимальная и максимальная длина пептидного линкера по настоящему изобретению могут комбинироваться, если такое комбинирование имеет математический смысл. В других предпочтительных воплощениях пептидный линкер настоящего изобретения не является иммуногенным, а в особенно предпочтительных воплощениях пептидный линкер не является иммуногенным для человека.
Термин "сайт расщепления" в настоящем изобретении относится к такой аминокислотной последовательности или нуклеотидной последовательности, которая направляет разделение, например, потому что она распознается расщепляющим ферментом, и/или может разделяться. Как правило, полипептидная цепь расщепляется посредством гидролиза одной или нескольких пептидных связей, соединяющих аминокислоты, а полинуклеотидная цепь расщепляется посредством гидролиза одной или нескольких фосфодиэфирных связей между нуклеотидами. Расщепление пептидных или фосфодиэфирных связей могут происходить вследствие химического или ферментативного расщепления. Ферментативное расщепление означает такое расщепление, которое происходит под действием протеолитических ферментов, включая, без ограничения, рестрикционные эндонуклеазы (например, рестрикционные ферменты I типа, II типа, III типа, IV типа либо искусственные) и эндо- или экзопептидазы или -протеазы (например, сериновые протеазы, цистеиновые протеазы, металлопротеазы, треониновые протеазы, аспартатные протеазы, глутаматные протеазы). Как правило, ферментативное расщепление происходит посредством саморасщепления или же осуществляется независимым протеолитическим ферментом. Ферментативное расщепление белка или полипептида может происходить как ко-, так и посттрансляционно. Соответственно, термин "сайт расщепления эндопептидазами" в настоящем изобретении относится к сайтам расщепления внутри аминокислотной или нуклеотидной последовательности, причем эта последовательность расщепляется эндопептидазой (например, трипсином, пепсином, эластазой, тромбином, коллагеназой, фурином, термолизином, эндопептидазой V8, катепсинами). С другой стороны, полипротеин настоящего изобретения может расщепляться аутопротеазой, т.е. такой протеазой, которая расщепляет пептидные связи в той же белковой молекуле, в которой содержится и сама протеаза. Примерами таких аутопротеаз являются протеаза NS2 у флавивирусов или протеаза VP4 у бирнавирусов.
С другой стороны, термин "сайт расщепления" относится к такой аминокислотной последовательности или нуклеотидной последовательности, которая предотвращает образование пептидных или фосфодиэфирных связей между аминокислотами или нуклеотидами, соответственно. Например, образование связи может предотвращаться вследствие котрансляционного аутопроцессинга полипептида или полипротеина, при этом образуются два отдельных продукта трансляции, происходящие от одного эпизода трансляции открытой рамки считывания. Как правило, такой аутопроцессинг осуществляется путем "рибосомного перескока", вызванного последовательностью псевдостоп-кодона, которая индуцирует передвижение трансляционного комплекса от одного кодона к следующему без образования пептидной связи. Примеры последовательностей, индуцирующих рибосомный перескок, включают, без ограничения, вирусные пептиды 2А или им подобные пептиды (здесь они все собирательно именуются "пептидами 2А" или же "сайтами 2А" или "сайтами расщепления 2А"), которые используются некоторыми семействами вирусов, включая пикорнавирусы, вирусы насекомых, Aphtoviridae, ротавирусы и трипаносомы. Наиболее известны сайты 2А риновирусов и вируса ящура из семейства Picornaviridae, которые обычно используются для получения нескольких полипептидов из одного ORF.
Соответственно, термин "сайт саморасщепления" в настоящем изобретении означает сайт расщепления внутри аминокислотной или нуклеотидной последовательности, причем она расщепляется и без участия какой-либо другой молекулы или же образование пептидной или фосфодиэфирной связи в ней предотвращается в первую очередь (например, посредством котрансляционного аутопроцессинга, как описано выше).
Понятно, что сайты расщепления обычно включают несколько аминокислот или кодируются несколькими кодонами (например, в тех случаях, когда "сайт расщепления" не транслируется в белок, а приводит к прерыванию трансляции). Таким образом, сайт расщепления также может служить цели пептидного линкера, т.е. стерически разделяет два пептида. Так, в некоторых воплощениях "сайт расщепления" является и пептидным линкером, и выполняет описанную выше функцию расщепления. В таких воплощениях сайт расщепления может включать дополнительные N- и/или С-концевые аминокислоты.
Термин "клетки хозяева" в настоящем изобретении относится к таким клеткам, которые содержат вектор (например, плазмиду или вирус). Такие клетки хозяева могут быть как прокариотическими (например, бактериальные клетки), так и эукариотическими (например, клетки грибов, растений или животных).
"Фармацевтически приемлемый" означает одобренный регулирующим агентством федерального правительства или правительства штата либо представленный в Фармакопее США или другой общепризнанной фармакопее для применения на животных, в частности на людях.
Термин "носитель" в настоящем изобретении относится к фармакологически неактивным веществам, таким, без ограничения, как разбавители, наполнители или носители, вместе с которыми вводится терапевтически активный ингредиент. Такие фармацевтические носители могут быть жидкими или твердыми. К жидким носителям относятся, без ограничения, стерильные жидкости, как-то солевые растворы в воде и маслах, включая масла из нефти, животного, растительного или синтетического происхождения, такие как арахисовое масло, соевое масло, минеральное масло, кунжутное масло и др. Солевые растворы и водные растворы декстрозы и глицерина также могут использоваться в качестве жидких носителей, предпочтительно растворов для инъекций. Солевой раствор является предпочтительным носителем при внутривенном введении фармацевтических композиций или интраназальном с помощью распылителя.
Подходящими фармацевтическими наполнителями являются крахмал, глюкоза, лактоза, сахароза, желатин, солод, рис, мука, мел, силикагель, стеарат натрия, моностеарат глицерина, тальк, хлорид натрия, сухое обезжиренное молоко, глицерин, пропиленгликоль, вода, этанол и др.
Примеры подходящих фармацевтических носителей описаны в "Remington's Pharmaceutical Sciences" by Ε.W. Martin.
Термин "композиция" служит для обозначения лекарственной формы активного соединения с инкапсулирующим материалом в качестве носителя, образующим капсулу, в которой активный компонент, вместе с другими носителями или без них, окружен носителем, который таким образом с ним связан.
Термин "адъювант" относится к веществам, которые увеличивают, стимулируют, активируют, усиливают или модулируют иммунный ответ на активный ингредиент композиции либо на клеточном, либо на гуморальном уровне, например, иммунологические адъюванты стимулируют реакцию иммунной системы на фактический антиген, но сами по себе не обладают иммунологическим действием. Примеры таких адъювантов включают, без ограничения, неорганические адъюванты (например, неорганические соли металлов, как-то фосфат алюминия или гидроокись алюминия), органические адъюванты (например, сапонины или сквалены), масляные адъюванты (например, полный адъювант Фрейнда и неполный адъювант Фрейнда), цитокины (например, IL-1β, IL-2, IL-7, IL-12, IL-18, GM-CFS и INF-γ), корпускулярные адъюванты (например, иммуностимулирующие комплексы (ISCOMS), липосомы или биоразлагаемые микросферы), виросомы, бактериальные адъюванты (например, монофосфорил-липид А или мурамиловые пептиды), синтетические адъюванты (например, неионные блок-сополимеры, аналоги мурамиловых пептидов или синтетический липид А) или синтетические полинуклеотидные адъюванты (например, полиаргинин или полилизин).
Термин "активный ингредиент" относится к такому веществу в фармацевтической композиции или препарате, которое является биологически активным, т.е. обеспечивает фармацевтическую ценность. Фармацевтическая композиция может содержать один или несколько активных ингредиентов, которые могут действовать совместно или независимо друг от друга.
Активный ингредиент может входить в состав в виде нейтральной формы или соли. Фармацевтически приемлемые соли включают соли, образованные со свободными аминогруппами типа тех, что образованы из хлористоводородной, фосфорной, уксусной, щавелевой, винной кислоты и др., и соли, образованные со свободными карбоксильными группами, такими, без ограничения, как те, что получены из гидроокиси натрия, калия, аммония, кальция, железа, изопропиламина, триэтиламина, 2-этиламиноэтанола, гистидина, прокаина и др.
"Пациент" в настоящем изобретении означает любое млекопитающее, пресмыкающееся или птицу, которые могут получить пользу от лечения описанной здесь противораковой вакциной. Предпочтительно "пациент" выбирается из группы, состоящей из лабораторных животных (например, мыши или крысы), домашних животных (в том числе, например, морские свинки, кролики, лошади, ослы, коровы, овцы, козы, свиньи, куры, верблюды, кошки, собаки, морские черепахи, сухопутные черепахи, змеи или ящерицы) и приматов, в том числе шимпанзе, карликовый шимпанзе, горилла и человек. Особенно предпочтительно "пациентом" является человек.
В настоящем изобретении термин "лечить", "лечащий" или "лечение" заболевания означает выполнение одного или нескольких из следующего: (а) снижение тяжести заболевания; (b) ограничение или предотвращение развития симптомов, характерных для данного заболевания; (с) подавление ухудшения симптомов, характерных для данного заболевания; (d) ограничение или предотвращение рецидива заболевания у тех пациентов, у которых ранее было это заболевание; и (е) ограничение или предотвращение рецидива симптомов у тех пациентов, у которых ранее были симптомы заболевания.
В настоящем изобретении "предотвращать", "предотвращающий", "предотвращение" или "профилактика" заболевания означает предупреждение возникновения такого заболевания у пациента.
Термин "введение" в настоящем изобретении включает введение in vivo, а также введение непосредственно в ткань ex vivo, как-то при пересадке вен.
"Эффективное количество" есть такое количество терапевтического средства, которое достаточно для достижения своего предназначения. Эффективное количество данного терапевтического средства зависит от таких факторов, как природа этого средства, способ введения, размер и вид животного, получающего это терапевтическое средство, и цель введения. Эффективное количество в каждом отдельном случае должно определяться эмпирически специалистом в соответствии с известными в данной области способами.
Воплощения изобретения
Теперь настоящее изобретение будет описано подробно. В следующих записях будут более подробно определены различные аспекты изобретения. Каждый аспект, определенный таким образом, может комбинироваться с любым другим аспектом или аспектами, если явно не указано обратное. В частности, любой признак, указанный как предпочтительный или преимущественный, может комбинироваться с любым другим признаком или признаками, указанными как предпочтительные или преимущественные.
В первом аспекте настоящим изобретением предусмотрена экспрессионная система, включающая первый полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует Т-клеточный ответ, и второй полинуклеотид, кодирующий по меньшей мере один белок, который индуцирует В-клеточный ответ против патогена. Одним из преимуществ, обеспечиваемых настоящим изобретением, является то, что В-клеточный ответ на белок, пептид или их вариант, индуцирующий В-клеточный ответ против патогена, может быть усилен, если в то же самое время ввести белок, индуцирующий Т-клеточный ответ.
В контексте настоящего изобретения термин "экспрессионная система" предпочтительно относится к последовательностям одного или нескольких полинуклеотидов, содержащим наряду с первым и вторым полинуклеотидом элементы, направляющие транскрипцию и трансляцию белков, кодируемых первым и вторым или любым другим полинуклеотидом, которые могут быть включены в предпочтительные воплощения, изложенные ниже. Такие элементы включают промоторы и энхансеры, направляющие транскрипцию мРНК в бесклеточной или клеточной системе, предпочтительно клеточной системе. В другом воплощении, в котором полинуклеотиды представлены в виде транслируемой РНК, предусматривается, что экспрессирующая система содержит те элементы, которые необходимы для трансляции и/или стабилизации РНК, кодирующей белок, индуцирующий Т-клетки и В-клетки, например, хвост поли-А, 1RES, кэп-структуры и др.
В соответствии с предпочтительным воплощением первого аспекта, первый полинуклеотид кодирует белок, который индуцирует реакцию иммунной системы (т.е. иммунный ответ) у хозяина, опосредованный Т-клетками. Т-клеточный ответ включает активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (Тн-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). Т-клеточный ответ против белка индуцируется, если пептиды белка подвергаются процессингу внутри клетки и презентируются Т-клеткам на поверхности клетки через путь МНС I или МНС II. Так, в контексте настоящего изобретения для индуцирования Т-клеточного ответа предпочтительно используются те белки или их части, которые обычно не выходят на поверхность, например, неструктурные или внутренние белки либо части структурных или внутренних белков вируса, недоступные для В-клеток.
Второй полинуклеотид кодирует белок, пептид или их вариант, который индуцирует В-клеточный ответ против патогена. В-клеточный ответ представляет собой иммунный ответ, основанный на активации В-лимфоцитов, которые вырабатывают и секретируют антиген-специфичные антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1. Так, в контексте настоящего изобретения для индуцирования В-клеточного ответа предпочтительно используются те белки или их части от патогена, например, вируса, которые выходят на поверхность вируса, например, структурные белки или по крайней мере те части структурных белков, которые доступны для В-клеток на наружной поверхности патогена (вируса).
В воплощениях первого аспекта настоящего изобретения первый и второй полинуклеотиды содержатся в отдельных векторах или в одном и том же векторе. Соответственно, первый полинуклеотид может содержаться в одном векторе, а второй полинуклеотид может содержаться в другом векторе. С другой стороны, первый и второй полинуклеотиды могут содержаться в одном и том же векторе. Предпочтительно и первый, и второй полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно первый и второй полинуклеотиды, содержащиеся в одном и том же векторе, соединяются таким образом, чтобы они экспрессировались в виде полипротеина. Предпочтительно первый и второй полинуклеотид образуют открытую рамку считывания.
Предпочтительно первый и второй полинуклеотид экспрессируются в виде искусственного полипротеина. В контексте настоящего изобретения термин "искусственный полипротеин" обозначает такие полипротеины, которые не встречаются в природе, например, полученные методами рекомбинантной ДНК. Соответственно, белки, пептиды или их варианты, кодируемые в этом искусственном полипротеине, предпочтительно происходят из таких патогенов, геном которых не кодирует полипротеин, включающий белки, пептиды или их варианты, кодируемые первым и вторым полинуклеотидом (необязательно также и третьим полинуклеотидом) настоящего изобретения. Предпочтительно первый и второй полинуклеотиды происходят из вирусов, не кодирующих полипротеин или кодирующих такой полипротеин, у которого соответствующие полинуклеотиды имеют другой порядок и/или последовательность. Более предпочтительно первый и второй полинуклеотид происходят из вируса, который выбран из группы, состоящей из ДНК-вирусов, одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)) или амбисмысловых РНК-вирусов. Еще более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)). А еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов.
В предпочтительных воплощениях первого аспекта белок, который индуцирует Т-клеточный ответ, является неструктурным и/или внутренним белком вируса, а/или белок, который индуцирует В-клеточный ответ против патогена, является структурным и/или поверхностным белком патогена, предпочтительно вируса, причем вирус предпочтительно выбран из группы, состоящей из ДНК-вирусов, РНК-вирусов с минус нитью или амбисмысловых РНК-вирусов. Еще более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью. А еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов.
Предпочтительно аминокислотная последовательность структурного (поверхностного) и/или неструктурного (внутреннего) белка содержит последовательные сегменты или консенсусную последовательность одного или нескольких различных изолятов вируса.
В контексте настоящего изобретения термин "сегмент" предпочтительно относится к части белка или полипротеина. Особенно предпочтительно, чтобы такой сегмент сворачивался и/или функционировал независимо от остальной части белка или полипротеина, как-то, без ограничения, его домен, эпитоп или фрагмент. Следует иметь в виду, что вариант белка в контексте настоящего изобретения отличается от исходного полипептида изменениями в аминокислотной последовательности, такими как аминокислотные замены, вставки, делеции, N-концевые усечения или С-концевые усечения или же любые комбинации этих изменений, которые могут происходить по одному или нескольким сайтам, при этом вариант по меньшей мере на 80% идентичен по последовательности своему исходному полипептиду.
В предпочтительных воплощениях структурный белок, пептид или их вариант представлен белком или пептидом, экспонированным на поверхности нативного патогена, например, вируса. Предпочтительно структурный и/или поверхностный белок запускает независимый от Т-клеток иммунный ответ, такой, без ограничения, как опосредованный антителами иммунный ответ или активация системы комплемента. В особенно предпочтительном воплощении структурный и/или поверхностный белок индуцирует опосредованный антителами иммунный ответ. Такой опосредованный антителами иммунный ответ основан на активации В-клеток, которые вырабатывают и секретируют специфичные к антигену антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1.
В соответствии с предпочтительным воплощением первого аспекта, второй полинуклеотид кодирует белок или его вариант, который индуцирует В-клеточный ответ против патогена. В-клеточный ответ представляет собой иммунный ответ, основанный на активации В-лимфоцитов, которые вырабатывают и секретируют антиген-специфичные антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1. Так, в контексте настоящего изобретения для индуцирования В-клеточного ответа предпочтительно используются те белки или их части, которые выходят на поверхность вируса, например, структурные и/или поверхностные белки или по крайней мере те части структурных и/или поверхностных белков, которые доступны для В-клеток на наружной поверхности вируса. В-клеточный ответ против патогена является В клеточным ответом, направленным против патогена, который инактивирует, устраняет, блокирует и/или нейтрализирует соответствующий патоген таким образом, что заболевание, вызываемое возбудителем, не возникает и/или его симптомы ослабляются. В предпочтительных воплощениях изобретения В-клеточный ответ против патогена осуществляют антитела, которые связываются с поверхностью патогенного организма и с помощью своего Fc-участка привлекают первый компонент каскада комплемента и запускают активацию "классической" системы комплемента. Это приводит к элиминации патогена по двум механизмам. Во-первых, при связывании антитела и молекул комплемента патоген помечается на переваривание фагоцитами в процессе, называемом опсонизацией. Во-вторых, некоторые компоненты системы комплемента образуют мембраноатакующий комплекс, который помогает антителам непосредственно разрушить патоген. С другой стороны, В-клеточный ответ против патогена осуществляют антитела, которые связываются со структурными белками патогена, блокируя прикрепление к клеточным рецепторам. Таким образом, антитела могут нейтрализовать заражение. А еще с одной стороны В-клеточный ответ против патогена осуществляют антитела, которые связываются со специализированным участком поверхностного белка патогена -пептидом слияния, который необходим для проникновения патогена в клетку хозяина. Связывание антитела приводит к фиксации белка в состоянии перед слиянием и блокирует заражение. Способность белка или варианта индуцировать В-клеточный ответ против патогена может определить специалист при помощи тестов и/или анализов, хорошо известных в данной области.
В другом предпочтительном воплощении у белка, экспонированного на поверхности нативного вируса, или его варианта домен прикрепления к мембране подвергается функциональной делеции, то есть он либо структурно делегирован, либо структурно присутствует, но не выполняет свою биологическую функцию. В особенно предпочтительном воплощении подвергается делеции аминокислотная последовательность, соответствующая домену прикрепления к мембране. Удаление участка прикрепления к мембране служит гарантией того, что белок, индуцирующий В-клеточный ответ против патогена, будет секретироваться из клетки, в которую была введена экспрессионная система изобретения.
В следующем предпочтительном воплощении изобретения белок, индуцирующий В-клеточный ответ против патогена, содержит сигнал секреции, который направляет белок в эндоплазматический ретикулум (ER). Такие сигналы секреции предпочтительно присутствуют в контексте удаления домена прикрепления к мембране. Специалистам хорошо известны многие такие сигналы секреции, которые могут использоваться в качестве гетерологичных сигналов секреции, например, при добавлении их к N-концу белка, индуцирующего В-клеточный ответ против патогена. С другой стороны, можно использовать природный сигнал секреции, например, который присутствует у большинства структурных и/или поверхностных белков вируса. Так, если у соответствующего белка сигнал секреции присутствует от природы, то предпочтительно он сохраняется и в модифицированной версии структурного и/или поверхностного белка.
В воплощениях первого аспекта неструктурный белок является консервативным внутренним белком, подходящим для индукции опосредованного Т-клетками иммунного ответа против патогена, предпочтительно вируса, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). При этом предпочтительно индуцирующий Т-клетки белок патогена (вируса) не содержит сигнала секреции.
В контексте настоящего изобретения белок, пептид или их вариант, кодируемый первым полинуклеотидом, располагается с N-конца или С-конца относительно белка, пептида или варианта, кодируемого вторым полинуклеотидом. В предпочтительном воплощении белок, пептид или их вариант, кодируемый вторым полинуклеотидом, располагается с С-конца относительно белка, пептида или варианта, кодируемого первым полинуклеотидом.
Соответственно, воплощения настоящего изобретения имеют формулу X-Y или Y-X, где "X" означает белок, индуцирующий Т-клеточный ответ, "Y" означает белок, индуцирующий В-клеточный ответ против патогена, а "тире" означает пептидную связь.
В предпочтительных воплощениях первого аспекта между первым полинуклеотидом и вторым полинуклеотидом располагается полинуклеотид, кодирующий сайт расщепления. В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком и любые два белка могут или не могут соединяться через сайт расщепления.
Предпочтительно этот сайт расщепления является либо сайтом саморасщепления (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется и без участия какой-либо дополнительной молекулы или же образование пептидной связи в ней предотвращается в первую очередь), либо сайтом расщепления эндопептидазами (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется эндопептидазой, например, трипсином, пепсином, эластазой, тромбином, коллагеназой, фурином, термолизином, эндопептидазой V8, катепсинами). Более предпочтительно сайт саморасщепления представлен сайтом расщепления 2А, выбранным из группы, состоящей из вирусного пептида 2А или 2А-подобных пептидов пикорнавирусов, вирусов насекомых, Aphtoviridae, ротавирусов и трипаносом, при этом предпочтительно сайт расщепления 2А представлен пептидом 2А вируса ящура. С другой стороны, полипротеин настоящего изобретения может расщепляться аутопротеазой, т.е. такой протеазой, которая расщепляет пептидные связи в той же белковой молекуле, в которой содержится и сама протеаза. Примерами таких аутопротеаз являются протеаза NS2 у флавивирусов или протеаза VP4 у бирнавирусов.
В контексте настоящего изобретения сайт расщепления может располагаться с N-конца относительно белка, пептида или варианта, кодируемого первым полинуклеотидом, и с С-конца относительно белка, пептида или их варианта, кодируемого вторым полинуклеотидом. С другой стороны, сайт расщепления может располагаться с С-конца относительно белка, пептида или их варианта, кодируемого первым полинуклеотидом, и с N-конца относительно белка, пептида или их варианта, кодируемого вторым полинуклеотидом.
Соответственно, воплощения настоящего изобретения имеют формулу X-C-Y или Y-C-X, где X" означает белок, индуцирующий Т-клеточный ответ, "Y" означает белок, индуцирующий В-клеточный ответ против патогена, "С" означает сайт расщепления, а "тире" означает пептидную связь.
В предпочтительном воплощении первого аспекта экспрессионная система дополнительно содержит третий полинуклеотид, кодирующий белок, пептид или их вариант от патогена.
Предпочтительно белок, пептид или их вариант, кодируемый третьим полинуклеотидом, является белком, пептидом или вариантом, индуцирующим Т-клеточный ответ, предпочтительно он представлен белком, пептидом или вариантом, который является неструктурным или внутренним белком, пептидом или вариантом, индуцирующим Т-клеточный ответ.
Предпочтительно белок, пептид или их вариант, кодируемый третьим полинуклеотидом, отличается от белка, пептида или их варианта, кодируемого первым полинуклеотидом или вторым полинуклеотидом. Предпочтительно белки, пептиды или их варианты, кодируемые первым, вторым и третьим полинуклеотидом, отличаются друг от друга тем, что они содержат аминокислотные последовательности различных белков.
В предпочтительных воплощениях между вторым полинуклеотидом и третьим полинуклеотидом располагается полинуклеотид, кодирующий линкер. Предпочтительно линкер представляет собой гибкий линкер, предпочтительно гибкий линкер, включающий аминокислотную последовательность согласно SEQ ID NO: 6 (Gly-Gly-Gly-Ser-Gly-Gly-Gly).
В предпочтительных воплощениях третий полинуклеотид содержится в отдельном либо в том же самом векторе, что и первый полинуклеотид и/или второй полинуклеотид. Соответственно, первый полинуклеотид содержится в одном векторе, а второй полинуклеотид содержится во втором векторе, а третий полинуклеотид содержится в третьем векторе. По другой версии, первый и второй полинуклеотид содержатся в одном и том же векторе, а третий полинуклеотид содержится в отдельном векторе, или же первый и третий полинуклеотид содержатся в одном и том же векторе, а второй полинуклеотид содержится в отдельном векторе, или же второй и третий полинуклеотид содержатся в одном и том же векторе, а первый полинуклеотид содержится в отдельном векторе. По другой версии, первый, второй и третий полинуклеотид содержатся в одном и том же векторе. Предпочтительно первый, второй и третий полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно первый, второй и третий полинуклеотид, содержащиеся в одном и том же векторе, соединяются таким образом, чтобы они экспрессировались в виде полипротеина. Предпочтительно первый, второй и третий полинуклеотид, содержащиеся в одном и том же векторе, образуют открытую рамку считывания и предпочтительно экспрессируются в виде полипротеина.
В предпочтительных воплощениях этого аспекта белок, кодируемый вторым полинуклеотидом, располагается с N-конца относительно белка, кодируемого первым полинуклеотидом, и/или белок необязательного третьего полинуклеотида либо белок, кодируемый вторым полинуклеотидом, располагается с С-конца относительно белка, кодируемого первым полинуклеотидом и/или белка необязательного третьего полинуклеотида.
В еще более предпочтительных воплощениях этого аспекта первый полинуклеотид располагается с N-конца относительно белка, кодируемого вторым полинуклеотидом, и/или белок необязательного третьего полинуклеотида располагается с N-конца относительно белка, кодируемого первым полинуклеотидом, или между белком, кодируемым вторым полинуклеотидом, и белком, кодируемым первым полинуклеотидом; или же белок, кодируемый первым полинуклеотидом, располагается с С-конца относительно белка, кодируемого вторым полинуклеотидом, и/или белок необязательного третьего полинуклеотида располагается с С-конца относительно белка, кодируемого первым полинуклеотидом, или между белком, кодируемым вторым полинуклеотидом, и белком, кодируемым первым полинуклеотидом.
Предпочтительные воплощения настоящего изобретения имеют формулу X-K-Y, Υ-Κ-Χ, Χ-Κ-Υ-Υ, Υ-Υ-Κ-Χ, Χ-Υ-Κ-Υ, Υ-Κ-Υ-Χ, Χ-Κ-Υ-Κ-Υ, Y-K-Y-K-X, X-C-Y, Y-C-X, X-C-Y-Y, Y-Y-C-X, X-Y-C-Y, Y-C-Y-X, X-C-Y-C-Y, Y-C-Y-C-X, X-K-Y-C-Y, Y-C-Y-K-X, X-C-Y-K-Y или Y-K-Y-C-X, где "X" означает второй полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует В-клеточный ответ против патогена, "Y" означает первый полинуклеотид, кодирующий по меньшей мере один белок, пептид или их вариант, который индуцирует Т-клеточный ответ, "К" означает, что в этом положении находится один или несколько пептидных линкеров, "С" означает, что в этом положении находится один или несколько сайтов расщепления, а "тире" означает пептидную связь. Предпочтительным является сочетание Y-K-Y-C-X или X-C-Y-K-Y.
Также предпочтительно неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, является консервативным внутренним белком, подходящим для индуцирования Т-клеточного иммунного ответа против вируса, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки).
В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком и любые два белка могут или не могут соединяться через сайт расщепления или линкерный пептид.
В предпочтительных воплощениях вектор или векторы, содержащие первый, второй и/или третий полинуклеотид, выбираются из группы, состоящей из плазмид, космид, фагов, вирусов и искусственных хромосом. Более предпочтительно вектор, подходящий для воплощения настоящего изобретения, выбирается из группы, состоящей из плазмидных векторов, космидных векторов, фаговых векторов, предпочтительно векторов из фага лямбда и нитчатых фагов, вирусных векторов, аденовирусных векторов (например, не реплицирующихся векторов Ad5, Ad11, Ad26, Ad35, Ad49, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, CbAd55, ChAd63, CbAd73, ChAd82, CbAd83, ChAd146, CbAd147, PanAd1, PanAd2 и PanAd3 или компетентных к репликации векторов Ad4 и Ad7), аденоассоциированных вирусных (AAV) векторов (например, AAV типа 5 и типа 2), альфавирусных векторов (например, вируса венесуэльского энцефалита лошадей (VEE), вируса Синдбис (SIN), вируса леса Семлики (SFV) и химеры VEE-SIN), герпесвирусных векторов (например, векторов, полученных из цитомегаловирусов типа цитомегаловируса резус (RhCMV) (14)), аренавирусных векторов (например, векторов из вируса лимфоцитарного хориоменингита (LCMV) (15)), векторов из вируса кори, поксвирусных векторов (например, вируса осповакцины, модифицированного вируса осповакцины Анкара (MVA), NYVAC (из вируса осповакцины штамма Копенгаген), авипоксвирусных векторов: вирусов оспы канареек (ALVAC) и оспы домашних птиц (FPV)), векторов из вируса везикулярного стоматита, ретровирусов, лентивирусов, вирусоподобных частиц и бактериальных спор. Векторы ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, CbAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd63 и ChAd82 подробно описаны в WO 2005/071093. Векторы PanAd1, PanAd2, PanAd3, ChAd55, ChAd73, ChAd83, ChAd146 и ChAd147 подробно описаны в WO 2010/086189. Особенно предпочтительно вектор выбирается из группы, состоящей из MVA, ChAd63 и PanAd3.
В предпочтительных воплощениях экспрессионная система предназначается для применения в медицине. В более предпочтительных воплощениях экспрессионная система предназначается для применения при профилактике или лечении инфекций и/или при изготовлении лекарственных средств для применения при профилактике или лечении инфекций и/или для применения в способах профилактики или лечения инфекций, при этом инфекция предпочтительно представлена вирусной инфекцией, особенно предпочтительно для применения при профилактике или лечении от патогена и/или при изготовлении лекарственных средств для применения при профилактике или лечении от патогена и/или для применения в способах профилактики или лечения от патогена, при этом патоген предпочтительно представлен вирусом. Предпочтительно экспрессионная система предназначается для применения при профилактике или лечении вирусных инфекций и/или при изготовлении лекарственных средств для применения при профилактике или лечении от вирусов и/или для применения в способах профилактики или лечения от вирусов, при этом патоген выбирается из группы, состоящей из ДНК-вирусов, одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)) или амбисмысловых РНК-вирусов. Более предпочтительно экспрессионная система предназначается для применения при профилактике или лечении и/или при изготовлении лекарственных средств для применения при профилактике или лечении от вирусов и/или для применения в способах профилактики или лечения инфекций, вызванных одноцепочечными РНК-вирусами с минус нитью (ssRNA(-)). Еще более предпочтительно экспрессионная система предназначается для применения при профилактике или лечении и/или при изготовлении лекарственных средств для применения при профилактике или лечении от вирусов и/или для применения в способах профилактики или лечения инфекций, вызванных вирусами из числа оболочечных ssRNA(-) вирусов, более предпочтительно из числа парамиксовирусов и ортомиксовирусов.
В предпочтительных воплощениях экспрессионная система предназначается для усиления иммунного ответа. В более предпочтительных воплощениях экспрессионная система предназначается для усиления В-клеточного иммунного ответа против иммуногена, предпочтительно патогена, более предпочтительно вируса, как определено выше.
В соответствии с предпочтительным воплощением первого аспекта, первый полинуклеотид кодирует вирусный белок парамиксовируса или его вариант, который индуцирует реакцию иммунной системы (т.е. иммунный ответ) у хозяина, опосредованную Т-клетками, а второй полинуклеотид кодирует вирусный белок парамиксовируса или его вариант, который индуцирует В-клеточный антипатогенный ответ против парамиксовируса. Предпочтительно парамиксовирус, вирусные белки которого кодируются первым и вторым полинуклеотидом, выбирается из подсемейства Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama. В еще более предпочтительных воплощениях Pneumovirinae выбирают из группы, состоящей из пневмовирусов, предпочтительно респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз, вируса ринотрахеита индюков, и метапневмовирусов, предпочтительно метапневмовируса человека (hMPV) и метапневмовируса птиц. В еще более предпочтительных воплощениях Paramyxovirinae выбирают из группы, состоящей из респировирусов, предпочтительно вирусов парагриппа 1 и 3 человека, и рубулавирусов, предпочтительно вирусов парагриппа 2 и 4 человека.
В воплощениях первого аспекта настоящего изобретения первый и второй полинуклеотид содержатся в отдельных векторах или в одном и том же векторе. Соответственно, первый полинуклеотид может находиться в одном векторе, а второй полинуклеотид может находиться во втором векторе. По другой версии, первый и второй полинуклеотид могут находиться в одном и том же векторе. Предпочтительно первый и второй полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно первый и второй полинуклеотид, содержащиеся в одном и том же векторе, соединяются таким образом, чтобы они экспрессировались в виде полипротеина. Предпочтительно первый и второй полинуклеотид образуют открытую рамку считывания.
В соответствии с предпочтительными воплощениями первого аспекта, первый полинуклеотид кодирует вирусный белок парамиксовируса или его вариант, который индуцирует реакцию иммунной системы (т.е. иммунный ответ) у хозяина, опосредованный Т-клетками. Т-клеточный ответ включает активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). Т-клеточный ответ против белка индуцируется в том случае, если пептиды белка подвергаются процессингу внутри клетки и презентируются Т-клеткам на поверхности клетки через путь МНС I или МНС II. Так, в контексте настоящего изобретения для индукции Т-клеточного ответа предпочтительно используются те вирусные белки или их части, которые обычно не выходят на поверхность вируса, например, неструктурные или внутренние белки или части структурных или поверхностных белков, недоступные для В-клеток на внешней поверхности вируса.
Второй полинуклеотид кодирует вирусный белок парамиксовируса или его вариант, который индуцирует В-клеточный антипатогенный ответ против парамиксовируса. В-клеточный ответ представляет собой иммунный ответ, основанный на активации В-лимфоцитов, которые вырабатывают и секретируют антиген-специфичные антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1. Так, в контексте настоящего изобретения для индуцирования В-клеточного ответа предпочтительно используются те вирусные белки или их части, которые выходят на поверхность вируса, например, структурные белки или по крайней мере те части структурных белков, которые доступны для В-клеток на внешней поверхности вируса.
В соответствии с предпочтительным воплощением первого аспекта, второй полинуклеотид кодирует вирусный белок парамиксовируса или его вариант, который индуцирует В-клеточный антипатогенный ответ. В-клеточный ответ представляет собой иммунный ответ, основанный на активации В-лимфоцитов, которые вырабатывают и секретируют антиген-специфичные антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1. Так, в контексте настоящего изобретения для индуцирования В-клеточного ответа против патогена предпочтительно используются те вирусные белки или их части, которые выходят на поверхность вируса, например, структурные белки и/или поверхностные белки или по крайней мере те части структурных и/или поверхностных белков, которые доступны для В-клеток на внешней поверхности вируса.
В предпочтительных воплощениях первого аспекта вирусный белок парамиксовируса, который вызывает Т-клеточный ответ, является неструктурным и/или внутренним белком парамиксовируса, а/или вирусный белок парамиксовируса, который вызывает В-клеточный ответ против патогена, является структурным и/или поверхностным белком парамиксовируса.
Предпочтительно аминокислотная последовательность структурного (поверхностного) и/или неструктурного (внутреннего) белка содержит последовательные сегменты или консенсусную последовательность одного или нескольких различных изолятов парамиксовируса.
В предпочтительных воплощениях структурный белок представлен белком, экспонированным на поверхности нативного парамиксовируса, или его вариантом. Предпочтительно структурный белок запускает независимый от Т-клеток иммунный ответ, такой, без ограничения, как опосредованный антителами иммунный ответ или активация системы комплемента. В особенно предпочтительном воплощении структурный и/или поверхностный белок индуцирует опосредованный антителами иммунный ответ. Такой опосредованный антителами иммунный ответ основан на активации В-клеток, которые вырабатывают и секретируют специфичные к антигену антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1.
В другом предпочтительном воплощении у белка, экспонированного на поверхности нативного парамиксовируса, или его варианта домен прикрепления к мембране подвергается функциональной делеции, то есть он либо структурно делегирован, либо структурно присутствует, но не выполняет свою биологическую функцию. В особенно предпочтительном воплощении подвергается делеции аминокислотная последовательность, соответствующая домену прикрепления к мембране. Удаление участка прикрепления к мембране служит гарантией того, что белок, индуцирующий В-клеточный ответ против патогена, будет секретироваться из клетки, в которую была введена экспрессионная система изобретения.
В следующем предпочтительном воплощении изобретения белок, индуцирующий В-клеточный ответ против патогена, содержит сигнал секреции, который направляет белок в эндоплазматический ретикулум (ER). Так, если у соответствующего структурного или поверхностного белка сигнал секреции присутствует от природы, то предпочтительно он сохраняется и в модифицированной версии структурного или поверхностного белка.
Также предпочтительно структурный и/или поверхностный белок нативного парамиксовируса выбирается из группы, состоящей из белка слияния (F) и прикрепительных гликопротеинов G, H и HN.
У всех оболочечных вирусов встречаются прикрепительные гликопротеины, которые обеспечивают исходное взаимодействие между оболочкой вируса и плазматической мембраной клетки хозяина посредством связывания с углеводными группировками или доменами клеточной адгезии белков или с другими молекулами на плазматической мембране клетки хозяина. Тем самым прикрепительные гликопротеины образуют мостик между вирусом и мембраной клетки хозяина. Прикрепительные гликопротеины, обозначаемые как "Н", обладают активностью гемагглютинина и встречаются у морбилливирусов и генипавирусов, а гликопротеины, обозначаемые как "HN", обладают активностями гемагглютинина и нейраминидазы и встречаются у респировирусов, рубулавирусов и авулавирусов. Прикрепительные гликопротеины обозначаются как "G", если они не обладают ни активностью гемагглютинина, ни активностью нейраминидазы. Прикрепительные гликопротеины G встречаются у всех представителей Pneumovirinae.
Белок слияния "F" встречается у всех оболочечных вирусов и опосредует слияние оболочки вируса с плазматической мембраной клетки хозяина. Белок F является гликопротеином I типа, который распознает рецепторы, находящиеся на поверхности клетки хозяина, с которой он связывается. Белок F состоит из пептида слияния, рядом с которым располагаются трансмембранные домены, за которыми следуют участки двух гептадных повторов (HR) HR1 и HR2, соответственно. При внедрении пептида слияния в плазматическую мембрану клетки хозяина участок HR1 образует трехмерную структуру суперспирали, в гидрофобные канавки которой встраиваются участки HR2. При этом образуется шпилькообразная структура, которая подтягивает липидный бислой вируса еще ближе к плазматической мембране клетки и обеспечивает образование поры слияния, а затем и полное слияние двух липидных бислоев, что дает возможность вирусному капсиду проникнуть в цитоплазму клетки хозяина. Эти особенности присущи всем белкам оболочечных вирусов, опосредующим слияние.
В предпочтительном воплощении первого аспекта белок F включает в себя, в основном состоит или состоит из аминокислотной последовательности белка F одного из изолятов RSV или консенсусной аминокислотной последовательности двух или нескольких различных изолятов RSV, предпочтительно согласно SEQ ID NO: 1, более предпочтительно согласно SEQ ID NO: 2, или его варианта.
В предпочтительных воплощениях первого аспекта неструктурный белок является консервативным внутренним белком парамиксовирусов, подходящим для индуцирования опосредованного Т-клетками иммунного ответа против парамиксовируса, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). При этом индуцирующий Т-клетки белок парамиксовируса предпочтительно не содержит сигнала секреции.
Предпочтительно неструктурный белок и/или внутренний белок выбирается из группы, состоящей из нуклеопротеина N, матриксных белков M и М2, фосфопротеина Р, неструктурных белков NS1 и NS2 и каталитической субъединицы полимеразы (L).
Нуклеопротеин N выполняет несколько функций, в числе которых инкапсуляция РНК генома в устойчивый к РНКазе нуклеокапсид. Белок N также взаимодействует с белком M в процессе сборки вируса и взаимодействует с полимеразой P-L во время транскрипции и репликации генома.
Матриксный белок M является самым распространенным белком у парамиксовирусов и считается главным организатором морфологии вируса путем взаимодействия с цитоплазматическим хвостом интегральных мембранных белков и нуклеокапсида. Белок М2 является вторым ассоциированным с мембраной белком, который не подвергается гликозилированию и в основном встречается у пневмовирусов.
Фосфопротеин Ρ связывается с белками N и L и входит в состав РНК-полимеразного комплекса у всех парамиксовирусов. Большой белок L является каталитической субъединицей РНК-зависимой РНК-полимеразы.
Функция неструктурных белков NS1 и NS2 пока еще не установлена; однако есть признаки того, что они участвуют в цикле репликации вируса.
В предпочтительных воплощениях белок N включает аминокислотную последовательность N одного из изолятов RSV или консенсусную аминокислотную последовательность двух или нескольких различных изолятов RSV, предпочтительно согласно SEQ ID NO: 3, при этом белок М2 включает аминокислотную последовательность М2 одного из изолятов RSV или консенсусную аминокислотную последовательность двух или нескольких различных изолятов RSV, предпочтительно согласно SEQ ID NO: 5. Еще более предпочтительно белок N включает аминокислотную последовательность согласно SEQ ID NO: 4, а белок М2 включает аминокислотную последовательность согласно SEQ ID NO: 5.
В контексте настоящего изобретения структурный и/или поверхностный белок, кодируемый первым полинуклеотидом, располагается с N-конца либо с С-конца относительно неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В предпочтительном воплощении неструктурный и/или внутренний белок, кодируемый вторым полинуклеотидом, располагается с С-конца относительно структурного и/или поверхностного белка, кодируемого первым полинуклеотидом.
В частности, белок Ν, M, М2, Р, NSI, NS2 или L может располагаться с N-конца либо с С-конца F, G, H или HN. Предпочтительно белок Ν, M, М2, Р, NS1, NS2 или L располагается с С-конца F, G, H или HN. В более предпочтительном воплощении N или М2 располагается с С-конца F. В особенно предпочтительном воплощении белок N располагается с С-конца F.
Соответственно, воплощения настоящего изобретения имеют формулу X-Y или Y-X, где "X" означает F, G, H или ΗΝ, "Y" означает Ν, M, М2, Р, NS1, NS2 или L, а "тире" означает пептидную связь. Предпочтительными являются следующие сочетания:
F-N, G-N, H-N, HN-N, F-M, G-M, Н-М, HN-M, F-M2, G-M2, Н-М2, HN-M2, F-P, G-Р, Н-Р, HN-P, F-NS1, G-NS1, H-NS1, HN-NS1, F-NS2, G-NS2, H-NS2, HN-NS2, F-L, G-L, H-L, HN-L, N-F, N-G, N-H, N-HN, M-F, M-G, М-Н, M-HN, M2-F, M2-G, М2-Н, M2-HN, Р-F, P-G, Р-Н, P-HN, NS1-FF, NS1-G, NS1-H, NS1-HN, NS2-F, NS2-G, NS2-H, NS2-HN, L-F, L-G, L-H или L-HN.
В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком.
В предпочтительных воплощениях первого аспекта между первым полинуклеотидом и вторым полинуклеотидом располагается полинуклеотид, кодирующий сайт расщепления.
Предпочтительно этот сайт расщепления является либо сайтом саморасщепления (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется и без участия какой-либо дополнительной молекулы или же образование пептидной связи в ней предотвращается в первую очередь), либо сайтом расщепления эндопептидазами (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется эндопептидазой, например, трипсином, пепсином, эластазой, тромбином, коллагеназой, фурином, термолизином, эндопептидазой V8, катепсинами). Более предпочтительно сайт саморасщепления представлен сайтом расщепления 2А, выбранным из группы, состоящей из вирусного пептида 2А или 2А-подобных пептидов пикорнавирусов, вирусов насекомых, Aphtoviridae, ротавирусов и трипаносом, при этом предпочтительно сайт расщепления 2А представлен пептидом 2А вируса ящура.
В контексте настоящего изобретения сайт расщепления может располагаться с N-конца относительно структурного и/или поверхностного белка, кодируемого первым полинуклеотидом, и с С-конца относительно неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. С другой стороны, сайт расщепления может располагаться с С-конца относительно структурного и/или поверхностного белка, кодируемого первым полинуклеотидом, и с N-конца относительно неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В частности, сайт расщепления может располагаться с С-конца или с N-конца относительно F, G, H или HN, и с С-конца или с N-конца относительно Ν, M, М2, Р, NS1, NS2 или L. В предпочтительном воплощении сайт расщепления располагается с N-конца относительно Ν, M, М2, Р, NS1, NS2 или L и с С-конца относительно F, G, H или HN. Особенно предпочтительно сайт расщепления располагается с N-конца относительно N и с С-конца относительно F.
Соответственно, воплощения настоящего изобретения имеют формулу X-C-Y или Y-C-X, где "X" означает F, G, H или ΗΝ, "Y" означает Ν, M, М2, Р, NSI, NS2 или L, "С" означает сайт расщепления, а "тире" означает пептидную связь. Предпочтительными являются следующие сочетания:
F-C-N, G-C-N, H-C-N, HN-C-N, F-C-M, G-C-M, Н-С-М, HN-C-M, F-C-M2, G-C-M2, Н-С-М2, HN-C-M2, F-C-P, G-C-P, Н-С-Р, HN-C-P, F-C-NS1, G-C-NS1, H-C-NS1, HN-C-NS1, F-C-NS2, G-C-NS2, H-C-NS2, HN-C-NS2, F-C-L, G-C-L, H-C-L, HN-C-L, N-C-F, N-C-G, N-C-H, N-C-HN, M-C-F, M-C-G, М-С-Н, M-C-HN, M2-C-F, M2-C-G, М2-С-Н, M2-C-HN, P-C-F, P-C-G, Р-С-Н, P-C-HN, NS1-C-FF, NS1-C-G, NS1-C-H, NS1-C-HN, NS2-C-F, NS2-C-G, NS2-C-H, NS2-C-HN, L-C-F, L-C-G, L-C-H, or L-C-HN. Особенно предпочтительным является сочетание F-C-N.
В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком и любые два белка могут или не могут соединяться через сайт расщепления.
В предпочтительном воплощении первого аспекта экспрессионная система дополнительно включает третий полинуклеотид, кодирующий неструктурный и/или внутренний белок парамиксовируса или его вариант. Предпочтительно неструктурный и/или внутренний белок парамиксовируса выбирается из группы, состоящей из Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama, более предпочтительно Pneumovirinae выбирают из группы, состоящей из пневмовирусов, предпочтительно респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз, вируса ринотрахеита индюков, и метапневмовирусов, предпочтительно метапневмовируса человека и метапневмовируса птиц, еще более предпочтительно Paramyxovirinae выбирают из группы, состоящей из респировирусов, предпочтительно вирусов парагриппа 1 и 3 человека, и рубулавирусов, предпочтительно вирусов парагриппа 2 и 4 человека.
В предпочтительных воплощениях третий полинуклеотид содержится в отдельном либо в том же самом векторе, что и первый полинуклеотид и/или второй полинуклеотид.
Соответственно, первый полинуклеотид содержится в одном векторе, а второй полинуклеотид содержится во втором векторе, а третий полинуклеотид содержится в третьем векторе. По другой версии, первый и второй полинуклеотид содержатся в одном и том же векторе, а третий полинуклеотид содержится в отдельном векторе, или же первый и третий полинуклеотид содержатся в одном и том же векторе, а второй полинуклеотид содержится в отдельном векторе, или же второй и третий полинуклеотид содержатся в одном и том же векторе, а первый полинуклеотид содержится в отдельном векторе. По другой версии, первый, второй и третий полинуклеотид содержатся в одном и том же векторе. Предпочтительно первый, второй и третий полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно первый, второй и третий полинуклеотид, содержащиеся в одном и том же векторе, соединяются таким образом, чтобы они экспрессировались в виде вирусного полипротеина. Предпочтительно первый, второй и третий полинуклеотид, содержащиеся в одном и том же векторе, образуют открытую рамку считывания.
Также предпочтительно неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, является консервативным внутренним белком, подходящим для индуцирования Т-клеточного иммунного ответа против вируса, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки).
Предпочтительно неструктурный и/или внутренний белок выбирается из группы, состоящей из нуклеопротеина N, матриксных белков M и М2, фосфопротеина Р, неструктурных белков NS1 и NS2 и каталитической субъединицы полимеразы (L).
В предпочтительных воплощениях белок N включает аминокислотную последовательность N одного из изолятов RSV или консенсусную аминокислотную последовательность двух или нескольких различных изолятов RSV, предпочтительно согласно SEQ ID NO: 3, при этом белок М2 включает аминокислотную последовательность М2 одного из изолятов RSV или консенсусную аминокислотную последовательность двух или нескольких различных изолятов RSV, предпочтительно согласно SEQ ID NO: 5. Также предпочтительно, если белок N включает аминокислотную последовательность согласно SEQ ID NO: 4, а белок М2 включает аминокислотную последовательность согласно SEQ ID NO: 5.
Предпочтительно неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, отличается от неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом.
Неструктурные и/или внутренние белки, кодируемые вторым и третьим полинуклеотидом, отличаются друг от друга тем, что они включают аминокислотные последовательности разных вирусных белков. Например, это значит, что неструктурный и/или внутренний белок, кодируемый вторым полинуклеотидом, включает аминокислотную последовательность белка N, а неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, включает аминокислотную последовательность белка М2, и наоборот.
Неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, располагается с N-конца или с С-конца неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В предпочтительном воплощении первого аспекта неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, располагается с С-конца неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В частности, белок N или М2 может располагаться с N-конца или с С-конца N или М2, предпочтительно белок N располагается с С-конца М2.
В предпочтительных воплощениях между вторым полинуклеотидом и третьим полинуклеотидом располагается полинуклеотид, кодирующий линкер. Предпочтительно линкер представляет собой гибкий линкер, предпочтительно гибкий линкер, включающий аминокислотную последовательность согласно SEQ ID NO: 6.
В воплощениях первого аспекта белок, кодируемый вторым полинуклеотидом, располагается с N-конца относительно белка, кодируемого первым полинуклеотидом, и/или белок необязательного третьего полинуклеотида либо белок, кодируемый вторым полинуклеотидом, располагается с С-конца относительно белка, кодируемого первым полинуклеотидом и/или белка необязательного третьего полинуклеотида.
В еще более предпочтительных воплощениях этого аспекта первый полинуклеотид располагается с N-конца относительно белка, кодируемого вторым полинуклеотидом, и/или белок необязательного третьего полинуклеотида располагается с N-конца относительно белка, кодируемого первым полинуклеотидом, или между белком, кодируемым вторым полинуклеотидом, и белком, кодируемым первым полинуклеотидом; или же белок, кодируемый первым полинуклеотидом, располагается с С-конца относительно белка, кодируемого вторым полинуклеотидом, и/или белок необязательного третьего полинуклеотида располагается с С-конца относительно белка, кодируемого первым полинуклеотидом, или между белком, кодируемым вторым полинуклеотидом, и белком, кодируемым первым полинуклеотидом. В частности, белок F, G, H или HN располагается с С-конца либо с N-конца относительно Ν, M, М2, Р, NS1, NS2 или L, а белок Ν, M, М2, Р, NSI, NS2 или L располагается с С-конца либо с N-конца относительно N или М2. В предпочтительном воплощении белок F располагается с N-конца относительно N, а М2 располагается с С-конца относительно N.
Соответственно, предпочтительные воплощения настоящего изобретения имеют формулу Χ-Κ-Υ, Υ-Κ-Χ, Χ-Κ-Υ-Υ, Υ-Υ-Κ-Χ, Χ-Υ-Κ-Υ, Υ-Κ-Υ-Χ, Χ-Κ-Υ-Κ-Υ, Υ-Κ-Υ-Κ-Χ, X-C-Y, Y-C-X, X-C-Y-Y, Y-Y-C-X, X-Y-C-Y, Y-C-Y-X, X-C-Y-C-Y, Y-C-Y-C-X, X-K-Y-C-Υ, Y-C-Y-K-X, X-C-Y-K-Y или Υ-Κ-Y-C-X, где "Χ" означает F, G, Η или ΗΝ, "Υ" означает Ν, M, M2, Ρ, NS1, NS2 или L, "К" означает, что в этом положении находится один или несколько пептидных линкеров, "С" означает, что в этом положении находится один или несколько сайтов расщепления, а "тире" означает пептидную связь. Предпочтительным является сочетание X-C-Y-K-Y. Еще более предпочтительными являются следующие сочетания:
F-K-N, G-K-N, H-K-N, HN-K-N, F-K-M, G-K-M, Н-К-М, HN-K-M, F-K-M2, G-K-M2, Н-К-М2, HN-K-M2, F-K-P, G-K-P, Н-К-Р, HN-K-P, F-K-NS1, G-K-NS1, H-K-NS1, HN-K-NS1, F-K-NS2, G-K-NS2, H-K-NS2, HN-K-NS2, F-K-L, G-K-L, H-K-L, HN-K-L, N-K-F, N-K-G, N-K-H, N-K-HN, M-K-F, M-K-G, М-К-Н, M-K-HN, M2-K-F, M2-K-G, М2-К-Н, М2-К-HN, P-K-F, P-K-G, Р-К-Н, P-K-HN, NS1-K-FF, NS1-K-G, NS1-K-H, NS1-K-HN, NS2-K-F, NS2-K-G, NS2-K-H, NS2-K-HN, L-K-F, L-K-G, L-K-H, L-K-HN, F-C-N, G-C-N, H-C-N, HN-C-N, F-C-M, G-C-M, Н-С-М, HN-C-M, F-C-M2, G-C-M2, Н-С-М2, HN-C-M2, F-C-P, G-C-P, Н-С-Р, HN-C-P, F-C-NS1, G-C-NS1, H-C-NS1, HN-C-NS1, F-C-NS2, G-C-NS2, H-C-NS2, HN-C-NS2, F-C-L, G-C-L, H-C-L, HN-C-L, N-C-F, N-C-G, N-C-H, N-C-HN, M-C-F, M-C-G, М-С-Н, M-C-HN, M2-C-F, M2-C-G, М2-С-Н, M2-C-HN, P-C-F, P-C-G, Р-С-Н, P-C-HN, NS1-C-FF, NS1-C-G, NS1-C-H, NS1-C-HN, NS2-C-F, NS2-C-G, NS2-C-H, NS2-C-HN, L-C-F, L-C-G, L-C-H, or L-C-HN, F-N-M, G-N-M, H-N-M, HN-N-M, F-N-M2, G-N-M2, H-N-M2, HN-N-M2, F-N-P, G-N-P, H-N-P, HN-N-P, F-N-NS1, G-N-NS1, H-N-NS1, HN-N-NS1, F-N-NS2, G-N-NS2, H-N-NS2, HN-N-NS2, F-N-L, G-N-L, H-N-L, HN-N-L, F-M-N, G-M-N, Н-М-N, HN-M-N, F-M-P, G-M-P, Η-М-Р, HN-M-P, F-M-NS1, G-M-NS1, H-M-NS1, HN-M-NS1, F-M-NS2, G-M-NS2, H-M-NS2, HN-M-NS2, F-M-L, G-M-L, H-M-L, HN-M-L, F-M2-N, G-M2-N, H-M2-N, HN-M2-N, F-M2-P, G-M2-P, Н-М2-Р, HN-M2-P, F-M2-NS1, G-M2-NS1, Н-M2-NS1, HN-M2-NS1, F-M2-NS2, G-M2-NS2, H-M2-NS2, HN-M2-NS2, F-M2-L, G-M2-L, H-M2-L, HN-M2-L, F-P-N, G-P-N, H-P-N, HN-P-N, F-P-M, G-P-M, Н-Р-М, HN-P-M, F-P-М2, G-P-M2, Н-Р-М2, HN-P-M2, F-P-NS1, G-P-NS1, H-P-NS1, HN-P-NS1, F-P-NS2, G-P-NS2, H-P-NS2, HN-P-NS2, F-P-L, G-P-L, H-P-L, HN-P-L, F-NS1-N, G-NS1-N, H-NS1-N, HN-NS1-N, F-NS1-M, G-NS1-M, H-NS1-M, HN-NS1-M, F-NS1-M2, G-NS1-M2, H-NS1-M2, HN-NS1-M2, F-NS1-P, G-NS1-P, H-NS1-P, HN-NS1-P, F-NS1-NS2, G-NS1-NS2, H-NS1-NS2, HN-NS1-NS2, F-NS1-L, G-NS1-L, H-NS1-L, HN-NS1-L, F-NS2-N, G-NS2-N, H-NS2-N, HN-NS2-N, F-NS2-M, G-NS2-M, H-NS2-M, HN-NS2-M, F-NS2-M2, G-NS2-M2, H-NS2-M2, HN-NS2-M2, F-NS2-P, G-NS2-P, H-NS2-P, HN-NS2-P, F-NS2-NS1, G-NS2-NS1, H-NS2-NS1, HN-NS2-NS1, F-NS2-L, G-NS2-L, H-NS2-L, HN-NS2-L, F-L-N, G-L-N, H-L-N, HN-L-Ν, F-L-M2, G-L-M2, H-L-M2, HN-L-M2, F-L-P, G-L-P, H-L-P, HN-L-P, F-L-NS1, G-L-NS1, H-L-NS1, HN-L-NS1, F-L-NS2, G-L-NS2, H-L-NS2, HN-L-NS2, M-N-F, M-N-G, M-N-H, M-N-HN, M2-N-F, M2-N-G, M2-N-H, M2-N-HN, P-N-F, P-N-G, P-N-H, P-N-HN, NS1-N-F, NS1-N-G, NS1-N-H, NS1-N-HN, NS2-N-F, NS2-N-G, NS2-N-H, NS2-N-HN, L-N-F, L-N-G, L-N-H, L-N-HN, N-M-F, N-M-G, N-M-H, N-M-HN, P-M-F, P-M-G, P-M-H, P-M-HN, NS1-M-F, NS1-M-G, NS1-M-H, NS1-M-HN, NS2-M-F, NS2-M-G, NS2-M-H, NS2-M-HN, L-M-F, L-M-G, L-M-H, L-M-HN, N-M2-F, N-M2-G, N-M2-H, N-M2-HN, P-M2-F, P-M2-G, P-M2-H, P-M2-HN, NS1-M2-F, NS1-M2-G, NS1-M2-H, NS1-M2-HN, NS2-M2-F, NS2-M2-G, NS2-M2-H, NS2-M2-HN, L-M2-F, L-M2-G, L-M2-H, L-M2-HN, N-P-F, N-P-G, N-P-H, N-P-HN, M-P-F, M-P-G, М-Р-Η, M-P-HN, M2-P-F, M2-P-G, M2-P-H, M2-P-HN, NS1-P-F, NS1-P-G, NS1-P-H, NS1-P-HN, NS2-P-F, NS2-P-G, NS2-P-H, NS2-P-HN, L-P-F, L-P-G, L-P-H, L-P-HN, N-NS1-F, N-NS1-G, N-NS1-H, N-NS1-HN, M-NS1-F, M-NS1-G, M-NS1-H, M-NS1-HN, M2-NS1-F, M2-NS1-G, M2-NS1-H, M2-NS1-HN, P-NS1-F, P-NS1-G, P-NS1-H, P-NS1-HN, NS2-NS1-F, NS2-NS1-G, NS2-NS1-H, NS2-NS1-HN, L-NS1-F, L-NS1-G, L-NS1-H, L-NS1-HN, N-NS2-F, N-NS2-G, N-NS2-H, N-NS2-HN, M-NS2-F, M-NS2-G, M-NS2-H, M-NS2-HN, M2-NS2-F, M2-NS2-G, M2-NS2-H, M2-NS2-HN, P-NS2-F, P-NS2-G, P-NS2-H, P-NS2-HN, NS1-NS2-F, NS1-NS2-G, NS1-NS2-H, NS1-NS2-HN, L-NS2-F, L-NS2-G, L-NS2-H, L-NS2-HN, N-L-F, N-L-G, N-L-H, N-L-HN, M-L-F, M-L-G, M-L-H, M-L-HN, M2-L-F, M2-L-G, M2-L-H, M2-L-HN, P-L-F, P-L-G, P-L-H, P-L-HN, NS1-L-F, NS1-L-G, NS1-L-H, NS1-L-HN, NS2-L-F, NS2-L-G, NS2-L-H, NS2-L-HN, F-K-N-N, G-K-N-N, H-K-N-N, HN-K-N-N, F-K-N-M, G-K-N-M, H-K-N-M, HN-K-N-M, F-K-N-M2, G-K-N-M2, H-K-N-M2, HN-K-N-M2, F-K-N-P, G-K-N-P, H-K-N-P, HN-K-N-P, F-K-N-NS1, G-K-N-NS1, H-K-N-NS1, HN-K-N-NS1, F-K-N-NS2, G-K-N-NS2, H-K-N-NS2, HN-K-N-NS2, F-K-N-L, G-K-N-L, H-K-N-L, HN-K-N-L, F-C-N-N, G-C-N-N, H-C-N-N, HN-C-N-N, F-C-N-M, G-C-N-M, H-C-N-M, HN-C-N-M, F-C-N-M2, G-C-N-M2, H-C-N-M2, HN-C-N-M2, F-C-N-P, G-C-N-P, H-C-N-P, HN-C-N-P, F-C-N-NS1, G-C-N-NS1, H-C-N-NS1, HN-C-N-NS1, F-C-N-NS2, G-C-N-NS2, H-C-N-NS2, HN-C-N-NS2, F-C-N-L, G-C-N-L, H-C-N-L, HN-C-N-L, F-K-M-M, G-K-M-M, H-K-M-M, HN-K-M-M, F-K-M-M2, G-K-M-M2, H-K-M-M2, HN-K-M-M2, F-K-M-N, G-K-M-N, H-K-M-N, HN-K-M-N, F-K-M-P, G-K-M-P, H-K-M-P, HN-K-M-P, F-K-M-NS1, G-K-M-NS1, H-K-M-NS1, HN-K-M-NS1, F-K-M-NS2, G-K-M-NS2, H-K-M-NS2, HN-K-M-NS2, F-K-M-L, G-K-M-L, H-K-M-L, HN-K-M-L, F-K-M2-M, G-K-M2-M, H-K-M2-M, HN-K-M2-M, F-K-M2-N, G-K-M2-N, H-K-M2-N, HN-K-M2-N, F-K-M2-P, G-K-M2-P, H-K-M2-P, HN-K-M2-P, F-K-M2-NS1, G-K-M2-NS1, H-K-M2-NS1, HN-K-M2-NS1, F-K-M2-NS2, G-K-M2-NS2, H-K-M2-NS2, HN-K-M2-NS2, F-K-M2-L, G-K-M2-L, H-K-M2-L, HN-K-M2-L, F-K-P-N, G-K-P-N, H-K-P-N, HN-K-P-N, F-K-P-M, G-K-P-M, H-K-P-M, HN-K-P-M, F-K-P-M2, G-K-P-M2, H-K-P-М2, HN-K-P-M2, F-K-P-P, G-K-P-P, H-K-P-P, HN-K-P-P, F-K-P-NS1, G-K-P-NS1, H-K-P-NS1, HN-K-P-NS1, F-K-P-NS2, G-K-P-NS2, H-K-P-NS2, HN-K-P-NS2, F-K-P-L, G-K-P-L, H-K-P-L, HN-K-P-L, F-K-NS1-N, G-K-NS1-N, H-K-NS1-N, HN-K-NS1-N, F-K-NS1-M, G-K-NS1-M, H-K-NS1-M, HN-K-NS1-M, F-K-NS1-M2, G-K-NS1-M2, H-K-NS1-M2, HN-K-NS1-M2, F-K-NS1-P, G-K-NS1-P, H-K-NS1-P, HN-K-NS1-P, F-K-NS1-NS1, G-K-NS1-NS1, H-K-NS1-NS1, HN-K-NS1-NS1, F-K-NS1-NS2, G-K-NS1-NS2, H-K-NS1-NS2, HN-K-NS1-NS2, F-K-NS1-L, G-K-NS1-L, H-K-NS1-L, HN-K-NS1-L, F-K-NS2-N, G-K-NS2-N, H-K-NS2-N, HN-K-NS2-N, F-K-NS2-M, G-K-NS2-M, H-K-NS2-M, HN-K-NS2-M, F-K-NS2-M2, G-K-NS2-M2, H-K-NS2-M2, HN-K-NS2-M2, F-K-NS2-P, G-K-NS2-P, H-K-NS2-P, HN-K-NS2-P, F-K-NS2-NS1, G-K-NS2-NS1, H-K-NS2-NS1, HN-K-NS2-NS1, F-K-NS2-NS2, G-K-NS2-NS2, H-K-NS2-NS2, HN-K-NS2-NS2, F-K-NS2-L, G-K-NS2-L, H-K-NS2-L, HN-K-NS2-L, F-K-L-N, G-K-L-N, H-K-L-N, HN-K-L-N, F-K-L-M, G-K-L-M, H-K-L-M, HN-K-L-M, F-K-L-M2, G-K-L-M2, H-K-L-M2, HN-K-L-M2, F-K-L-P, G-K-L-P, H-K-L-P, HN-K-L-P, F-K-L-NS1, G-K-L-NS1, H-K-L-NS1, HN-K-L-NS1, F-K-L-NS2, G-K-L-NS2, H-K-L-NS2, HN-K-L-NS2, F-K-L-L, G-K-L-L, H-K-L-L, HN-K-L-L, F-N-K-N, G-N-K-N, H-N-K-N, HN-N-K-N, F-N-K-M, G-N-K-M, H-N-K-M, HN-N-K-M, F-N-K-M2, G-N-K-M2, H-N-K-M2, HN-N-K-M2, F-N-K-P, G-N-K-P, H-N-K-P, HN-N-K-P, F-N-K-NS1, G-N-K-NS1, H-N-K-NS1, HN-N-K-NS1, F-N-K-NS2, G-N-K-NS2, H-N-K-NS2, HN-N-K-NS2, F-N-K-L, G-N-K-L, H-N-K-L, HN-N-K-L, F-M-K-N, G-M-K-N, H-M-K-N, HN-M-K-N, F-M-K-M, G-M-K-M, H-M-K-M, HN-M-K-M, F-M-K-M2, G-M-K-M2, H-M-K-M2, HN-M-K-M2, F-M-K-P, G-M-K-P, H-M-K-P HN-M-K-P, F-M-K-NS1, G-M-K-NS1, H-M-K-NS1, HN-M-K-NS1, F-M-K-NS2, G-M-K-NS2, H-M-K-NS2, HN-M-K-NS2, F-M-K-L, G-M-K-L, H-M-K-L, HN-M-K-L, F-M2-K-N, G-M2-K-N, H-M2-K-N, HN-M2-K-N, F-M2-K-M, G-M2-K-M, H-M2-K-M, FÍN-M2-K-M, F-M2-K-M2, G-M2-K-M2, H-M2-K-M2, HN-M2-K-M2, F-M2-K-P, G-M2-K-P, H-M2-K-P HN-M2-K-P, F-M2-K-NS1, G-M2-K-NS1, H-M2-K-NS1, HN-M2-K-NS1, F-M2-K-NS2, G-M2-K-NS2, H-M2-K-NS2, HN-M2-K-NS2, F-M2-K-L, G-M2-K-L, H-M2-K-L, HN-M2-K-L, F-P-K-N, G-P-K-N, H-P-K-N, HN-P-K-N, F-P-K-M, G-P-K-M, H-P-K-M, HN-P-K-M, F-P-K-M2, G-P-K-M2, H-P-K-M2; HN-P-K-M2, F-P-K-P, G-P-K-P, H-P-K-P, HN-P-K-P, F-P-K-NS1, G-P-K-NS1, H-P-K-NS1, HN-P-K-NS1, F-P-K-NS2, G-P-K-NS2, H-P-K-NS2, HN-P-K-NS2, F-P-K-L, G-P-K-L, H-P-K-L, FIN-P-K-L, F-NS1-K-N, G-NS1-K-N, H-NS1-K-N, HN-NS1-K-N, F-NS1-K-M, G-NS1-K-M, H-NS1-K-M; HN-NS1-K-M, F-NS1-K-M2, G-NS1-K-M2, H-NS1-K-M2; HN-NS1-K-M2, F-NS1-K-P, G-NS1-K-P, H-NS1-K-P, HN-NS1-K-P, F-NS1-K-NS1, G-NS1-K-NS1, H-NS1-K-NS1, HN-NS1-K-NS1, F-NS1-K-NS2, G-NS1-K-NS2, H-NS1-K-NS2, FINNS 1-K-NS2, F-NS1-K-L, G-NS1-K-L, H-NS1-K-L, HN-NS1-K-L, F-NS2-K-N, G-NS2-K-N, H-NS2-K-N, HN-NS2-K-N, F-NS2-K-M, G-NS2-K-M, H-NS2-K-M, HN-NS2-K-M, F-NS2-K-М2, G-NS2-K-M2, H-NS2-K-M2, HN-NS2-K-M2, F-NS2-K-P, G-NS2-K-P, H-NS2-K-P, HN-NS2-K-P, F-NS2-K-NS1, G-NS2-K-NS1, H-NS2-K-NS1, HN-NS2-K-NS1, F-NS2-K-NS2, G-NS2-K-NS2, H-NS2-K-NS2, HN-NS2-K-NS2, F-NS2-K-L, G-NS2-K-L, H-NS2-K-L, HN-NS2-K-L, F-C-M-M, G-C-M-M, H-C-M-M, HN-C-M-M, F-C-M-M2, G-C-M-M2, H-C-M-M2, HN-C-M-M2, F-C-M-N, G-C-M-N, H-C-M-N, HN-C-M-N, F-C-M-P, G-C-M-P, H-C-M-P, HN-C-M-P, F-C-M-NS1, G-C-M-NS1, H-C-M-NS1, HN-C-M-NS1, F-C-M-NS2, G-C-M-NS2, H-C-M-NS2, HN-C-M-NS2, F-C-M-L, G-C-M-L, H-C-M-L, HN-C-M-L, F-C-M2-M, G-C-M2-M, H-C-M2-M, HN-C-M2-M, F-C-M2-N, G-C-M2-N, H-C-M2-N, HN-C-M2-N, F-C-M2-P, G-C-M2-P, H-C-M2-P, HN-C-M2-P, F-C-M2-NS1, G-C-M2-NS1, H-C-M2-NS1, HN-C-M2-NS1, F-C-M2-NS2, G-C-M2-NS2, H-C-M2-NS2, HN-C-M2-NS2, F-C-M2-L, G-C-M2-L, H-C-M2-L, HN-C-M2-L, F-C-P-N, G-C-P-N, H-C-P-N, HN-C-P-N, F-C-P-M, G-C-P-M, H-C-P-M, HN-C-P-M, F-C-P-M2, G-C-P-M2, H-C-P-M2, HN-C-P-M2, F-C-P-P, G-C-P-P, H-C-P-P, HN-C-P-P, F-C-P-NS1, G-C-P-NS1, H-C-P-NS1, HN-C-P-NS1, F-C-P-NS2, G-C-P-NS2, H-C-P-NS2, HN-C-P-NS2, F-C-P-L, G-C-P-L, H-C-P-L, HN-C-P-L, F-C-NS1-N, G-C-NS1-N, H-C-NS1-N, HN-C-NS1-N, F-C-NS1-M, G-C-NS1-M, H-C-NS1-M, HN-C-NS1-M, F-C-NS1-M2, G-C-NS1-M2, H-C-NS1-M2, HN-C-NS1-M2, F-C-NS1-P, G-C-NS1-P, H-C-NS1-P, HN-C-NS1-P, F-C-NS1-NS1, G-C-NS1-NS1, H-C-NS1-NS1, HN-C-NS1-NS1, F-C-NS1-NS2, G-C-NS1-NS2, H-C-NS1-NS2, HN-C-NS1-NS2, F-C-NS1-L, G-C-NS1-L, H-C-NS1-L, HN-C-NS1-L, F-C-NS2-N, G-C-NS2-N, H-C-NS2-N, HN-C-NS2-N, F-C-NS2-M, G-C-NS2-M, H-C-NS2-M, HN-C-NS2-M, F-C-NS2-M2, G-C-NS2-M2, H-C-NS2-M2, FIN-C-NS2-M2, F-C-NS2-P, G-C-NS2-P, H-C-NS2-P, HN-C-NS2-P, F-C-NS2-NS1, G-C-NS2-NS1, H-C-NS2-NS1, HN-C-NS2-NS1, F-C-NS2-NS2, G-C-NS2-NS2, H-C-NS2-NS2, HN-C-NS2-NS2, F-C-NS2-L, G-C-NS2-L, H-C-NS2-L, HN-C-NS2-L, F-C-L-N, G-C-L-N, H-C-L-N, HN-C-L-N, F-C-L-M, G-C-L-M, H-C-L-M, HN-C-L-M, F-C-L-M2, G-C-L-M2, H-C-L-M2, HN-C-L-M2, F-C-L-P, G-C-L-P, H-C-L-P, HN-C-L-P, F-C-L-NS1, G-C-L-NS1, H-C-L-NS1, HN-C-L-NS1, F-C-L-NS2, G-C-L-NS2, H-C-L-NS2, FTN-C-L-NS2, F-C-L-L, G-C-L-L, H-C-L-L, HN-C-L-L, F-N-C-N, G-N-C-N, H-N-C-N, HN-N-C-N, F-N-C-M, G-N-C-M, H-N-C-M, HN-N-C-M, F-N-C-M2, G-N-C-M2, H-N-C-M2, HN-N-C-M2, F-N-C-P, G-N-C-P, H-N-C-P, HN-N-C-P, F-N-C-NS1, G-N-C-NS1, H-N-C-NS1, HN-N-C-NS1, F-N-C-NS2, G-N-C-NS2, H-N-C-NS2, HN-N-C-NS2, F-N-C-L, G-N-C-L, H-N-C-L, HN-N-C-L, F-M-C-N, G-M-C-N, H-M-C-N, HN-M-C-N, F-M-C-M, G-M-C-M, H-M-C-M, HN-M-C-M, F-M-C-M2, G-M-C-M2, H-M-C-M2, HN-M-C-M2, F-M-C-P, G-M-C-P, H-M-C-P HN-M-C-P, F-M-C-NS1, G-M-C-NS1, H-M-C-NS1, HN-M-C-NS1, F-M-C-NS2, G-M-C-NS2, H-M-C-NS2, HN-M-C-NS2, F-M-C-L, G-M-C-L, H-M-C-L, HN-M-C-L, F-M2-C-N, G-M2-C-N, H-M2-C-N, HN-M2-C-N, F-M2-C-M, G-M2-C-M, H-M2-C-M, HN-M2-C-M, F-M2-C-M2, G-M2-C-M2, H-M2-C-M2, FIN-M2-C-M2, F-M2-C-P, G-M2-C-P, H-M2-C-P HN-M2-C-P, F-M2-C-NS1, G-M2-C-NS1, H-M2-C-NS1, HN-M2-C-NS1, F-M2-C-NS2, G-M2-C-NS2, H-M2-C-NS2, HN-M2-C-NS2, F-M2-C-L, G-M2-C-L, H-M2-C-L, HN-M2-C-L, F-P-C-N, G-P-C-N, H-P-C-N, HN-P-C-N, F-P-C-M, G-P-C-M, H-P-C-M, HN-P-C-M, F-P-C-M2, G-P-C-M2, H-P-C-M2; HN-P-C-M2, F-P-C-P, G-P-C-P, H-P-C-P, HN-P-C-P, F-P-C-NS1, G-P-C-NS1, H-P-C-NS1, HN-P-C-NS1, F-P-C-NS2, G-P-C-NS2, H-P-C-NS2, HN-P-C-NS2, F-P-C-L, G-P-C-L, H-P-C-L, HN-P-C-L, F-NS1-C-N, G-NS1-C-N, H-NS1-C-N, HN-NS1-C-N, F-NS1-C-M, G-NS1-C-M, H-NS1-C-M; HN-NS1-C-M, F-NS1-C-M2, G-NS1-C-M2, H-NS1-C-M2; HN-NS1-C-M2, F-NS1-C-P, G-NS1-C-P, H-NS1-C-P, HN-NS1-C-P, F-NS1-C-NS1, G-NS1-C-NS1, H-NS1-C-NS1, HN-NS1-C-NS1, F-NS1-C-NS2, G-NS1-C-NS2, H-NS1-C-NS2, HN-NS1-C-NS2, F-NS1-C-L, G-NS1-C-L, H-NS1-C-L, HN-NS1-C-L, F-NS2-C-N, G-NS2-C-N, H-NS2-C-N, HN-NS2-C-N, F-NS2-C-M, G-NS2-C-M, H-NS2-C-M, HN-NS2-C-M, F-NS2-C-M2, G-NS2-C-M2, H-NS2-C-M2, HN-NS2-C-M2, F-NS2-C-P, G-NS2-C-P, H-NS2-C-P, HN-NS2-C-P, F-NS2-C-NS1, G-NS2-C-NS1, H-NS2-C-NS1, HN-NS2-C-NS1, F-NS2-C-NS2, G-NS2-C-NS2, H-NS2-C-NS2, HN-NS2-C-NS2, F-NS2-C-L, G-NS2-C-L, H-NS2-C-L, HN-NS2-C-L, F-L-K-N, G-L-K-N, H-L-K-N, HN-L-K-N, F-L-K-M, G-L-K-M, H-L-K-M, HN-L-K-M, F-L-K-M2, G-L-K-M2, H-L-K-M2, HN-L-K-M2, F-L-K-P, G-L-K-P, H-L-K-P, HN-L-K-P, F-L-K-NS1, G-L-K-NS1, H-L-K-NS1, HN-L-K-NS1, F-L-K-NS2, G-L-K-NS2, H-L-K-NS2, HN-L-K-NS2, F-L-K-L, G-L-K-L, H-L-K-L, HN-L-K-L, F-L-C-N, G-L-C-N, H-L-C-N, HN-L-C-N, F-L-C-M, G-L-C-M, H-L-C-M, HN-L-C-M, F-L-C-M2, G-L-C-M2, H-L-C-M2, HN-L-C-M2, F-L-C-P, G-L-C-P, H-L-C-P, HN-L-C-P, F-L-C-NS1, G-L-C-NS1, H-L-C-NS1, HN-L-C-NS1, F-L-C-NS2, G-L-C-NS2, H-L-C-NS2, HN-L-C-NS2, F-L-C-L, G-L-C-L, H-L-C-L, HN-L-C-L, F-K-N-K-N, G-K-N-K-N, H-K-N-K-N, HN-K-N-K-N, F-K-M-K-N, G-K-M-K-N, H-K-M-K-N, HN-K-M-K-N, F-K-M2-K-N, G-K-M2-K-N, H-K-M2-K-N, HN-K-M2-K-N, F-K-P-K-N, G-K-P-K-N, H-K-P-K-N, HN-K-P-K-N, F-K-NS1-K-N, G-K-NS1-K-N, H-K-NS1-K-N, HN-K-NS1-K-N, F-K-NS2-K-N, G-K-NS2-K-N, H-K-NS2-K-N, HN-K-NS2-K-N, F-K-L-K-N, G-K-L-K-N, H-K-L-K-N, HN-K-L-K-N, F-K-N-K-M, G-K-N-K-M, H-K-N-K-M, HN-K-N-K-M, F-K-M-K-M, G-K-M-K-M, H-K-M-K-M, HN-K-M-K-M, F-K-M2-K-M, G-K-M2-K-M, H-K-M2-K-M, HN-K-M2-K-M, F-K-P-K-M, G-K-P-K-M, H-K-P-K-M, HN-K-P-K-M, F-K-NS1-K-M, G-K-NS1-K-M, H-K-NS1-K-M, HN-K-NS1-K-M, F-K-NS2-K-M, G-K-NS2-K-M, H-K-NS2-K-M, HN-K-NS2-K-M, F-K-L-K-M, G-K-L-K-M, H-K-L-K-M, HN-K-L-K-M, F-K-N-K-M2, G-K-N-K-M2, H-K-N-K-M2, HN-K-N-K-M2, F-K-M-K-M2, G-K-M-K-M2, H-K-M-K-M2, HN-K-M-K-M2, F-K-M2-K-M2, G-K-M2-K-M2, H-K-M2-K-M2, HN-K-M2-K-M2, F-K-P-K-M2, G-K-P-K-M2, H-K-P-K-M2, HN-K-P-K-M2, F-K-NS1-K-M2, G-K-NS1-K-M2, H-K-NS1-K-M2, HN-K-NS1-K-M2, F-K-NS2-K-M2, G-K-NS2-K-M2, H-K-NS2-K-M2, HN-K-NS2-K-M2, F-K-L-K-M2, G-K-L-K-M2, H-K-L-K-M2, HN-K-L-K-M2, F-K-N-K-P, G-K-N-K-P, H-K-N-K-P, HN-K-N-K-P, F-K-M-K-P, G-K-M-K-P, H-K-M-K-P, HN-K-M-K-P, F-K-M2-K-P, G-K-M2-K-P, H-K-M2-K-P, HN-K-M2-K-P, F-K-P-K-P, G-K-P-K-P, H-K-P-K-P, HN-K-P-K-P, F-K-NS1-K-P, G-K-NS1-K-P, H-K-NS1-K-P, HN-K-NS1-K-P, F-K-NS2-K-P, G-K-NS2-K-P, H-K-NS2-K-P, HN-K-NS2-K-P, F-K-L-K-P, G-K-L-K-P, H-K-L-K-P, HN-K-L-K-P, F-K-N-K-NS1, G-K-N-K-NS1, H-K-N-K-NS1, HN-K-N-K-NS1, F-K-M-K-NS1, G-K-M-K-NS1, H-K-M-K-NS1, HN-K-M-K-NS1, F-K-M2-K-NS1, G-K-M2-K-NS1, H-K-M2-K-NS1, HN-K-M2-K-NS1, F-K-P-K-NS1, G-K-P-K-NS1, H-K-P-K-NS1, HN-K-P-K-NS1, F-K-NS1-K-NS1, G-K-NS1-K-NS1, H-K-NS1-K-NS1, HN-K-NS1-K-NS1, F-K-NS2-K-NS1, G-K-NS2-K-NS1, H-K-NS2-K-NS1, HN-K-NS2-K-NS1, F-K-L-K-NS1, G-K-L-K-NS1, H-K-L-K-NS1, HN-K-L-K-NS1, F-K-N-K-NS2, G-K-N-K-NS2, H-K-N-K-NS2, HN-K-N-K-NS2, F-K-M-K-NS2, G-K-M-K-NS2, H-K-M-K-NS2, HN-K-M-K-NS2, F-K-M2-K-NS2, G-K-M2-K-NS2, H-K-M2-K-NS2, HN-K-M2-K-NS2, F-K-P-K-NS2, G-K-P-K-NS2, H-K-P-K-NS2, HN-K-P-K-NS2, F-K-NS1-K-NS2 G-K-NS1-K-NS2, H-K-NS1-K-NS2, HN-K-NS1-K-NS2, F-K-NS2-K-NS2 G-K-NS2-K-NS2, H-K-NS2-K-NS2, HN-K-NS2-K-NS2, F-K-L-K-NS2, G-K-L-K-NS2, H-K-L-K-NS2, HN-K-L-K-NS2, F-K-N-K-L, G-K-N-K-L, H-K-N-K-L, HN-K-N-K-K, F-K-M-K-L, G-K-M-K-L, H-K-M-K-L, HN-K-M-K-L, F-K-M2-K-L, G-K-M2-K-L, H-K-M2-K-L, HN-K-M2-K-L, F-K-P-K-L, G-K-P-K-L, H-K-P-K-L, HN-K-P-K-L, F-K-NS1-K-L, G-K-NS1-K-L, H-K-NS1-K-L, HN-K-NS 1-K-L, F-K-NS2-K-L, G-K-NS2-K-L, H-K-NS2-K-L, HN-K-NS2-K-L, F-K-L-K-L, G-K-L-K-L, H-K-L-K-L, HN-K-L-K-L, N-K-N-F, N-K-N-G, N-K-N-H, N-K-N-HN, M-K-N-F, M-K-N-G, M-K-N-H, M-K-N-HN, M2-K-N-F, M2-K-N-G, M2-K-N-H, M2-K-N-HN, P-K-N-F, P-K-N-G, P-K-N-H, P-K-N-HN, NS1-K-N-F, NS1-K-N-G, NS1-K-N-H, NS1-K-N-HN, NS2-K-N-F, NS2-K-N-G, NS2-K-N-H, NS2-K-N-HN, L-K-N-F, L-K-N-G, L-K-N-H, L-K-N-HN, N-K-M-F, N-K-M-G, N-K-M-H, N-K-M-HN, M-K-M-F, M-K-M-G, M-K-M-H, M-K-M-HN, M2-K-M-F, M2-K-M-G, M2-K-M-H, M2-K-M-HN, P-K-M-F, P-K-M-G, P-K-M-H, P-K-M-HN, NS1-K-M-F, NS1-K-M-G, NS1-K-M-H, NS1-K-M-HN, NS2-K-M-F, NS2-K-M-G, NS2-K-M-H, NS2-K-M-HN, L-K-M-F, L-K-M-G, L-K-M-H, L-K-M-HN, N-K-M2-F, N-K-M2-G, N-K-M2-H, N-K-M2-HN, M-K-M2-F, M-K-M2-G, M-K-M2-H, M-K-M2-HN, M2-K-M2-F, M2-K-M2-G, M2-K-M2-H, M2-K-M2-HN, P-K-M2-F, P-K-M2-G, P-K-M2-H, P-K-M2-HN, NS1-K-M2-F, NS1-K-M2-G, NS1-K-M2-H, NS1-K-M2-HN, NS2-K-M2-F, NS2-K-M2-G, NS2-K-M2-H, NS2-K-M2-HN, L-K-M2-F, L-K-M2-G, L-K-M2-H, L-K-M2-HN, N-K-P-F, N-K-P-G, N-K-P-H, N-K-P-HN, M-K-P-F, M-K-P-G, M-K-P-H, M-K-P-HN, M2-K-P-F, M2-K-P-G, M2-K-P-H, M2-K-P-HN, P-K-P-F, P-K-P-G, P-K-P-H, P-K-P-HN, NS1-K-P-F, NS1-K-P-G, NS1-K-P-H, NS1-K-P-HN, NS2-K-P-F, NS2-K-P-G, NS2-K-P-H, NS2-K-P-HN, L-K-P-F, L-K-P-G, L-K-P-H, L-K-P-HN, N-K-NS1-F, N-K-NS1-G, N-K-NS1-H, N-K-NS1-HN, M-K-NS1-F, M-K-NS1-G, M-K-NS1-H, M-K-NS1-HN, M2-K-NS1-F, M2-K-NS1-G, M2-K-NS1-H, M2-K-NS1-HN, P-K-NS1-P-K-NS1-G, P-K-NS1-H, P-K-NS1-HN, NS1-K-NS1-F, NS1-K-NS1-G, NS1-K-NS1-H, NS1-K-NS1-HN, NS2-K-NS1-F, NS2-K-NS1-G, NS2-K-NS1-H, NS2-K-NS1-HN, L-K-NS1-F, L-K-NS1-G, L-K-NS1-H, L-K-NS1-HN,N-K-NS2-F, N-K-NS2-G, N-K-NS2-H, N-K-NS2-HN, M-K-NS2-F, M-K-NS2-G, M-K-NS2-H, M-K-NS2-HN, M2-K-NS2-F, M2-K-NS2-G, M2-K-NS2-H, M2-K-NS2-HN, P-K-NS2-F, P-K-NS2-G, P-K-NS2-H, P-K-NS2-HN, NS1-K-NS2-F, NS1-K-NS2-G, NS1-K-NS2-H, NS1-K-NS2-HN, NS2-K-NS2-F, NS2-K-NS2-G, NS2-K-NS2-H, NS2-K-NS2-HN, L-K-NS2-F, L-K-NS2-G, L-K-NS2-H, L-K-NS2-HN, N-K-L-F, N-K-L-G, N-K-L-H, N-K-L-HN, M-K-L-F, M-K-L-G, M-K-L2-H, M-K-L-HN, M2-K-L-F, M2-K-L-G, M2-K-L-H, M2-K-L-HN, P-K-L-F, P-K-L-G, P-K-L-H, P-K-L-HN, NS1-K-L-F, NS1-K-L-G, NS1-K-L-H, NS1-K-L-HN, NS2-K-L-F, NS2-K-L-G, NS2-K-L-H, NS2-K-L-HN, L-K-L-F, L-K-L-G, L-K-L-H, L-K-L-HN, N-N-K-F, N-N-K-G, N-N-K-H, N-N-K-HN, N-M-K-F, N-M-K-N-M-K-H, N-M-K-HN, N-M2-K-F, N-M2-K-G, N-M2-K-H, N-M2-K-HN, N-P-K-F, N-P-K-G, N-P-K-H, N-P-K-HN, N-NS1-K-F, N-NS1-K-G, N-NS1-K-H, N-NS1-K-HN, N-NS2-K-F, N-NS2-K-G, N-NS2-K-H, N-NS2-K-HN, N-L-K-F, N-L-K-G, N-L-K-H, N-L-K-HN, M-N-K-F, M-N-K-G, M-N-K-H, M-N-K-HN, M-M-K-F, M-M-K-G, M-M-K-H, M-M-K-HN, M-M2-K-F, M-M2-K-G, M-M2-K-H, M-M2-K-HN, M-P-K-F, M-P-K-G, M-P-K-H, M-P-K-HN, M-NS1-K-F, M-NS1-K-G, M-NS1-K-H, M-NS1-K-HN, M-NS2-K-F, M-NS2-K-G, M-NS2-K-H, M-NS2-K-HN, M-L-K-F, M-L-K-G, M-L-K-H, M-L-K-HN, M2-N-K-F, M2-N-K-G, M2-N-K-H, M2-N-K-HN, M2-M-K-F, M2-M-K-G, M2-M-K-H, M2-M-K-HN, M2-M2-K-F, M2-M2-K-G, M2-M2-K-H, M2-M2-K-HN, M2-P-K-F, M2-P-K-G, M2-P-K-H, M2-P-K-HN, M2-NS1-K-F, M2-NS1-K-G, M2-NS1-K-H, M2-NS1-K-HN, M2-NS2-K-F, M2-NS2-K-G, M2-NS2-K-H, M2-NS2-K-HN, M2-L-K-F, M2-L-K-G, M2-L-K-H, M2-L-K-HN, P-N-K-F, P-N-K-G, P-N-K-H, P-N-K-HN, P-M-K-F, P-M-K-G, P-M-K-H, P-M-K-HN, P-M2-K-F, P-M2-K-G, P-M2-K-H, P-M2-K-HN, P-P-K-F, P-P-K-G, P-P-K-H, P-P-K-HN, P-NS1-K-F, P-NS1-K-G, P-NS1-K-H, P-NS1-K-HN, P-NS2-K-F, P-NS2-K-G, P-NS2-K-H, P-NS2-K-HN, P-L-K-F, P-L-K-G, P-L-K-H, P-L-K-HN, NS1-N-K-F, NS1-N-K-G, NS1-N-K-H, NS1-N-K-HN, NS1-M-K-F, NS1-M-K-G, NS1-M-K-H, NS1-M-K-HN, NS1-M2-K-F, NS1-M2-K-G, NS1-M2-K-H, NS1-M2-K-HN, NS1-P-K-F, NS1-P-K-G, NS1-P-K-H, NS1-P-K-HN, NS1-NS1-K-F, NS1-NS1-K-G, NS1-NS1-K-H, NS1-NS1-K-HN, NS1-NS2-K-F, NS1-NS2-K-G, NS1-NS2-K-H, NS1-NS2-K-HN, NS1-L-K-F, NS1-L-K-G, NS1-L-K-H, NS1-L-K-HN, NS2-N-K-F, NS2-N-K-G, NS2-N-K-H, NS2-N-K-HN, NS2-M-K-F, NS2-M-K-G, NS2-M-K-H, NS2-M-K-HN, NS2-M2-K-F, NS2-M2-K-G, NS2-M2-K-H, NS2-M2-K-HN, NS2-P-K-F, NS2-P-K-G, NS2-P-K-H, NS2-P-K-HN, NS2-NS1-K-F, NS2-NS1-K-G, NS2-NS1-K-H, NS2-NS1-K-HN, NS2-NS2-K-F, NS2-NS2-K-G, NS2-NS2-K-H, NS2-NS2-K-HN, NS2-L-K-F, NS2-L-K-G, NS2-L-K-H, NS2-L-K-HN, L-N-K-F, L-N-K-G, L-N-K-H, L-N-K-HN, L-M-K-F, L-M-K-G, L-M-K-H, L-M-K-HN, L-M2-K-F, L-M2-K-G, L-M2-K-H, L-M2-K-HN, L-L-K-F, L-P-K-G, L-P-K-H, L-P-K-HN, L-NS1-K-F, L-NS1-K-G, L-NS1-K-H, L-NS1-K-HN, L-NS2-K-F, L-NS2-K-G, L-NS2-K-H, L-NS2-K-HN, L-L-K-F, L-L-K-G, L-L-K-H, L-L-K-HN, N-K-N-K-F, N-K-N-K-G, N-K-N-K-H, N-K-N-K-HN, N-K-M-K-F, N-K-M-K-G, N-K-M-K-H, N-K-M-K-HN, N-K-M2-K-F, N-K-M2-K-G, N-K-M2-K-H, N-K-M2-K-HN, N-K-P-K-F, N-K-P-K-G, N-K-P-K-H, N-K-P-K-HN, N-K-NS1-K-F, N-K-NS1-K-G, N-K-NS1-K-H, N-K-NS1-K-HN, N-K-NS2-K-F, N-K-NS2-K-G, N-K-NS2-K-H, N-K-NS2-K-HN, N-K-L-K-F, N-K-L-K-G, N-K-L-K-H, N-K-L-K-HN, M-K-N-K-F, M-K-N-K-G, M-K-N-K-H, M-K-N-K-HN, M-K-M-K-F, M-K-M-K-G, M-K-M-K-H, M-K-M-K-HN, M-K-M2-K-F, M-K-M2-K-G, M-K-M2-K-H, M-K-M2-K-HN, M-K-P-K-F, M-K-P-K-G, M-K-P-K-H, M-K-P-K-HN, M-K-NS1-K-F, M-K-NS1-K-G, M-K-NS1-K-H, M-K-NS1-K-HN, M-K-NS2-K-F, M-K-NS2-K-G, M-K-NS2-K-H, M-K-NS2-K-HN, M-K-L-K-F, M-K-L-K-G, M-K-L-K-H, M-K-L-K-HN, M2-K-N-K-F, M2-K-N-K-G, M2-K-N-K-H, M2-K-N-K-HN, M2-K-M-K-F, M2-K-M-K-G, M2-K-M-K-H, M2-K-M-K-HN, M2-K-M2-K-F, M2-K-M2-K-G, M2-K-M2-K-H, M2-K-M2-K-HN, M2-K-P-K-F, M2-K-P-K-G, M2-K-P-K-H, M2-K-P-K-HN, M2-K-NS1-K-F, M2-K-NS1-K-G, M2-K-NS1-K-H, M2-K-NS1 -K-HN, M2-K-NS2-K-F, M2-K-NS2-K-G, M2-K-NS2-K-H, M2-K-NS2-K-HN, M2-K-L-K-F, M2-K-L-K-G, M2-K-L-K-H, M2-K-L-K-HN, P-K-N-K-F, P-K-N-K-G, P-K-N-K-H, P-K-N-K-HN, P-K-M-K-F, P-K-M-K-G, P-K-M-K-H, P-K-M-K-HN, P-K-M2-K-F, P-K-M2-K-G, P-K-M2-K-H, P-K-M2-K-HN, P-K-P-K-F, P-K-P-K-G, P-K-P-K-H, P-K-P-K-HN, P-K-NS1-K-F, P-K-NS1-K-G, P-K-NS1-K-H, P-K-NS1-K-HN, P-K-NS2-K-F, P-K-NS2-K-G, P-K-NS2-K-H, P-K-NS2-K-HN, P-K-L-K-F, P-K-L-K-G, P-K-L-K-H, P-K-L-K-HN, NS1-K-N-K-F, NS1-K-N-K-G, NS1-K-N-K-H, NS1-K-N-K-HN, NS1-K-M-K-F, NS1-K-M-K-G, NS1-K-M-K-H, NS1-K-M-K-HN, NS1-K-M2-K-F, NS1-K-M2-K-G, NS1-K-M2-K-H, NS1-K-M2-K-HN, NS1-K-P-K-F, NS1-K-P-K-G, NS1-K-P-K-H, NS1-K-P-K-HN, NS1-K-NS1-K-F, NS1-K-NS1-K-G, NS1-K-NS1-K-H, NS1-K-NS1-K-HN, NS1-K-NS2-K-F, NS1-K-NS2-K-G, NS1-K-NS2-K-H, NS 1-K-NS2-K-HN, NS1-K-L-K-F, NS1-K-L-K-G, NS1-K-L-K-H, NS1-K-L-K-HN, NS2-K-N-K-F, NS2-K-N-K-G, NS2-K-N-K-H, NS2-K-N-K-HN, NS2-K-M-K-F, NS2-K-M-K-G, NS2-K-M-K-H, NS2-K-M-K-HN, NS2-K-M2-K-F, NS2-K-M2-K-G, NS2-K-M2-K-H, NS2-K-M2-K-HN, NS2-K-P-K-F, NS2-K-P-K-G, NS2-K-P-K-H, NS2-K-P-K-HN, NS2-K-NS1-K-F, NS2-K-NS1-K-G, NS2-K-NS1-K-H, NS2-K-NS1-K-HN, NS2-K-NS2-K-F, NS2-K-NS2-K-G, NS2-K-NS2-K-H, NS2-K-NS2-K-HN, NS2-K-L-K-F, NS2-K-L-K-G, NS2-K-L-K-H, NS2-K-L-K-HN, L-K-N-K-F, L-K-N-K-G, L-K-N-K-H, L-K-N-K-HN, L-K-M-K-F, L-K-M-K-G, L-K-M-K-H, L-K-M-K-HN, L-K-M2-K-F, L-K-M2-K-G, L-K-M2-K-H, L-K-M2-K-HN, L-K-P-K-F, L-K-P-K-G, L-K-P-K-H, L-K-P-K-HN, L-K-NS1-K-F, L-K-NS1-K-G, L-K-NS1-K-H, L-K-NS1-K-HN, L-K-NS2-K-F, L-K-NS2-K-G, L-K-NS2-K-H, L-K-NS2-K-HN, L-K-L-K-F, L-K-L-K-G, L-K-L-K-H, or L-K-L-K-HN, F-C-N-K-N, G-C-N-K-N, H-C-N-K-N, HN-C-N-K-N, F-C-M-K-N, G-C-M-K-N, H-C-M-K-N, HN-C-M-K-N, F-C-M2-K-N, G-C-M2-K-N, H-C-M2-K-N, HN-C-M2-K-N, F-C-P-K-N, G-C-P-K-N, H-C-P-K-N, HN-C-P-K-N, F-C-NS1-K-N, G-C-NS1-K-N, H-C-NS1-K-N, HN-C-NS1-K-N, F-C-NS2-K-N, G-C-NS2-K-N, H-C-NS2-K-N, HN-C-NS2-K-N, F-C-L-K-N, G-C-L-K-N, H-C-L-K-N, HN-C-L-K-N, F-C-N-K-M, G-C-N-K-M, H-C-N-K-M, HN-C-N-K-M, F-C-M-K-M, G-C-M-K-M, H-C-M-K-M, HN-C-M-K-M, F-C-M2-K-M, G-C-M2-K-M, H-C-M2-K-M, HN-C-M2-K-M, F-C-P-K-M, G-C-P-K-M, H-C-P-K-M, HN-C-P-K-M, F-C-NS1-K-M, G-C-NS1-K-M, H-C-NS1-K-M, HN-C-NS1-K-M, F-C-NS2-K-M, G-C-NS2-K-M, H-C-NS2-K-M, HN-C-NS2-K-M, F-C-L-K-M, G-C-L-K-M, H-C-L-K-M, FIN-C-L-K-M, F-C-N-K-M2, G-C-N-K-M2, H-C-N-K-M^ HN-C-N-K-M2, F-C-M-K-M2, G-C-M-K-M2, H-C-M-K-M2, HN-C-M-K-M2, F-C-M2-K-M2, G-C-M2-K-M2, H-C-M2-K-M2, HN-C-M2-K-M2, F-C-P-K-M2, G-C-P-K-M2, H-C-P-K-M2, HN-C-P-K-M2, F-C-NS1-K-M2, G-C-NS1-K-M2, H-C-NS1-K-M2, HN-C-NS1-K-M2, F-C-NS2-K-M2, G-C-NS2-K-M2, H-C-NS2-K-M2, HN-C-NS2-K-M2, F-C-L-K-M2, G-C-L-K-M2, H-C-L-K-M2, HN-C-L-K-M2, F-C-N-K-P, G-C-N-K-P, H-C-N-K-P, HN-C-N-K-P, F-C-M-K-P, G-C-M-K-P, H-C-M-K-P, HN-C-M-K-P, F-C-M2-K-P, G-C-M2-K-P, H-C-M2-K-P, HN-C-M2-K-P, F-C-P-K-P, G-C-P-K-P, H-C-P-K-P, HN-C-P-K-P, F-C-NS1-K-P, G-C-NS1-K-P, H-C-NS1-K-P, HN-C-NS1-K-P, F-C-NS2-K-P, G-C-NS2-K-P, H-C-NS2-K-P, HN-C-NS2-K-P, F-C-L-K-P, G-C-L-K-P, H-C-L-K-P, HN-C-L-K-P, F-C-N-K-NS1, G-C-N-K-NS1, H-C-N-K-NS1, HN-C-N-K-NS1, F-C-M-K-NS1, G-C-M-K-NS1, H-C-M-K-NS1, HN-C-M-K-NS1, F-C-M2-K-NS1, G-C-M2-K-NS1, H-C-M2-K-NS1, HN-C-M2-K-NS1, F-C-P-K-NS1, G-C-P-K-NS1, H-C-P-K-NS1, HN-C-P-K-NS1, F-C-NS1-K-NS1, G-C-NS1-K-NS1, H-C-NS1-K-NS1, HN-C-NS1-K-NS1, F-C-NS2-K-NS1, G-C-NS2-K-NS1, H-C-NS2-K-NS1, HN-C-NS2-K-NS1, F-C-L-K-NS1, G-C-L-K-NS1, H-C-L-K-NS1, HN-C-L-K-NS1, F-C-N-K-NS2, G-C-N-K-NS2, H-C-N-K-NS2, HN-C-N-K-NS2, F-C-M-K-NS2, G-C-M-K-NS2, H-C-M-K-NS2, HN-C-M-K-NS2, F-C-M2-K-NS2, G-C-M2-K-NS2, H-C-M2-K-NS2, HN-C-M2-K-NS2, F-C-P-K-NS2, G-C-P-K-NS2, H-C-P-K-NS2, HN-C-P-K-NS2, F-C-NS1-K-NS2 G-C-NS1-K-NS2, H-C-NS1-K-NS2, HN-C-NS1-K-NS2, F-C-NS2-K-NS2 G-C-NS2-K-NS2, H-C-NS2-K-NS2, HN-C-NS2-K-NS2, F-C-L-K-NS2, G-C-L-K-NS2, H-C-L-K-NS2, HN-C-L-K-NS2, F-C-N-K-L, G-C-N-K-L, H-C-N-K-L, HN-C-N-K-L, F-C-M-K-L, G-C-M-K-L, H-C-M-K-L, HN-C-M-K-L, F-C-M2-K-L, G-C-M2-K-L, H-C-M2-K-L, HN-C-M2-K-L, F-C-P-K-L, G-C-P-K-L, H-C-P-K-L, HN-C-P-K-L, F-C-NS1-K-L, G-C-NS1-K-L, H-C-NS1-K-L, HN-C-NS1-K-L, F-C-NS2-K-L, G-C-NS2-K-L, H-C-NS2-K-L, HN-C-NS2-K-L, F-C-L-K-L, G-C-L-K-L, H-C-L-K-L, HN-C-L-K-L, N-C-N-F, N-C-N-G, N-C-N-H, N-C-N-HN, M-C-N-F, M-C-N-G, M-C-N-H, M-C-N-HN, M2-C-N-F, M2-C-N-G, M2-C-N-H, M2-C-N-HN, P-C-N-F, P-C-N-G, P-C-N-H, P-C-N-HN, NS1-C-N-F, NS1-C-N-G, NS1-C-N-H, NS1-C-N-HN, NS2-C-N-F, NS2-C-N-G, NS2-C-N-H, NS2-C-N-HN, L-C-N-F, L-C-N-G, L-C-N-H, L-C-N-HN, N-C-M-F, N-C-M-G, N-C-M-H, N-C-M-HN, M-C-M-F, M-C-M-G, M-C-M-H, M-C-M-HN, M2-C-M-F, M2-C-M-G, M2-C-M-H, M2-C-M-HN, P-C-M-F, P-C-M-G, P-C-M-H, P-C-M-HN, NS1-C-M-F, NS1-C-M-G, NS1-C-M-H, NS1-C-M-HN, NS2-C-M-F, NS2-C-M-G, NS2-C-M-H, NS2-C-M-HN, L-C-M-F, L-C-M-G, L-C-M-H, L-C-M-HN, N-C-M2-F, N-C-M2-G, N-C-M2-H, N-C-M2-HN, M-C-M2-F, M-C-M2-G, M-C-M2-H, M-C-M2-HN, M2-C-M2-F, M2-C-M2-G, M2-C-M2-H, M2-C-M2-HN, P-C-M2-F, P-C-M2-P-C-M2-H, P-C-M2-HN, NS1-C-M2-F, NS1-C-M2-G, NS1-C-M2-H, NS1-C-M2-HN, NS2-C-M2-F, NS2-C-M2-G, NS2-C-M2-H, NS2-C-M2-HN, L-C-M2-F, L-C-M2-G, L-C-M2-H, L-C-M2-HN, N-C-P-F, N-C-P-G, N-C-P-H, N-C-P-HN, M-C-P-F, M-C-P-G, M-C-P-H, M-C-P-HN, M2-C-P-F, M2-C-P-G, M2-C-P-H, M2-C-P-HN, P-C-P-F, P-C-P-G, P-C-P-H, P-C-P-HN, NS1-C-P-F, NS1-C-P-G, NS1-C-P-H, NS1-C-P-HN, NS2-C-P-F, NS2-C-P-G, NS2-C-P-H, NS2-C-P-HN, L-C-P-F, L-C-P-G, L-C-P-H, L-C-P-HN, N-C-NS1-F, N-C-NS1-G, N-C-NS1-H, N-C-NS1-HN, M-C-NS1-F, M-C-NS1-G, M-C-NS1-H, M-C-NS1-HN, M2-C-NS1-F, M2-C-NS1-G, M2-C-NS1-H, M2-C-NS1-HN, P-C-NS1-F, P-C-NS1-G, P-C-NS1-H, P-C-NS1-HN, NS1-C-NS1-F, NS1-C-NS1-G, NS1-C-NS1-H, NS1-C-NS1-HN, NS2-C-NS1-F, NS2-C-NS1-G, NS2-C-NS1-H, NS2-C-NS1-HN, L-C-NS1-F, L-C-NS1-G, L-C-NS1-H, L-C-NS1-HN, N-C-NS2-F, N-C-NS2-G, N-C-NS2-H, N-C-NS2-HN, M-C-NS2-F, M-C-NS2-G, M-C-NS2-H, M-C-NS2-HN, M2-C-NS2-F, M2-C-NS2-G, M2-C-NS2-H, M2-C-NS2-HN, P-C-NS2-F, P-C-NS2-G, P-C-NS2-H, P-C-NS2-HN, NS1-C-NS2-F, NS1-C-NS2-G, NS1-C-NS2-H, NS1-C-NS2-HN, NS2-C-NS2-F, NS2-C-NS2-G, NS2-C-NS2-H, NS2-C-NS2-HN, L-C-NS2-F, L-C-NS2-G, L-C-NS2-H, L-C-NS2-HN, N-C-L-F, N-C-L-G, N-C-L-H, N-C-L-HN, M-C-L-F, M-C-L-G, M-C-L2-H, M-C-L-HN, M2-C-L-F, M2-C-L-G, M2-C-L-H, M2-C-L-HN, P-C-L-F, P-C-L-G, P-C-L-P-C-L-HN, NS1-C-L-F, NS1-C-L-G, NS1-C-L-H, NS1-C-L-HN, NS2-C-L-F, NS2-C-L-G, NS2-C-L-H, NS2-C-L-HN, L-C-L-F, L-C-L-G, L-C-L-H, L-C-L-HN, N-N-C-F, N-N-C-G, N-N-C-H, N-N-C-HN, N-M-C-F, N-M-C-G, N-M-C-H, N-M-C-HN, N-M2-C-F, N-M2-C-G, N-M2-C-H, N-M2-C-HN, N-P-C-F, N-P-C-G, N-P-C-H, N-P-C-HN, N-NS1-C-F, N-NS1-C-G, N-NS1-C-H, N-NS1-C-HN, N-NS2-C-F, N-NS2-C-G, N-NS2-C-H, N-NS2-C-HN, N-L-C-F, N-L-C-G, N-L-C-H, N-L-C-HN, M-N-C-F, M-N-C-G, M-N-C-H, M-N-C-HN, M-M-C-F, M-M-C-G, M-M-C-H, M-M-C-HN, M-M2-C-F, M-M2-C-G, M-M2-C-H, M-M2-C-HN, M-P-C-F, M-P-C-G, M-P-C-H, M-P-C-HN, M-NS1-C-F, M-NS1-C-G, M-NS1-C-H, M-NS1-C-HN, M-NS2-C-F, M-NS2-C-G, M-NS2-C-H, M-NS2-C-HN, M-L-C-F, M-L-C-G, M-L-C-H, M-L-C-HN, M2-N-C-F, M2-N-C-G, M2-N-C-H, M2-N-C-HN, M2-M-C-F, M2-M-C-G, M2-M-C-H, M2-M-C-HN, M2-M2-C-F, M2-M2-C-G, M2-M2-C-H, M2-M2-C-HN, M2-P-C-F, M2-P-C-G, M2-P-C-H, M2-P-C-HN, M2-NS1-C-F, M2-NS1-C-G, M2-NS1-C-H, M2-NS1-C-HN, M2-NS2-C-F, M2-NS2-C-G, M2-NS2-C-H, M2-NS2-C-HN, M2-L-C-F, M2-L-C-G, M2-L-C-H, M2-L-C-HN, P-N-C-F, P-N-C-G, P-N-C-H, P-N-C-HN, P-M-C-F, P-M-C-G, P-M-C-H, P-M-C-HN, P-M2-C-F, P-M2-C-G, P-M2-C-H, P-M2-C-HN, P-P-C-F, P-P-C-G, P-P-C-H, P-P-C-HN, P-NS1-C-F, P-NS1-C-P-NS1-C-H, P-NS1-C-HN, P-NS2-C-F, P-NS2-C-G, P-NS2-C-H, P-NS2-C-HN, P-L-C-F, P-L-C-G, P-L-C-H, P-L-C-HN, NS1-N-C-F, NS1-N-C-G, NS1-N-C-H, NS1-N-C-HN, NS1-M-C-F, NS1-M-C-G, NS1-M-C-H, NS1-M-C-HN, NS1-M2-C-F, NS1-M2-C-G, NS1-M2-C-H, NS1-M2-C-HN, NS1-P-C-F, NS1-P-C-G, NS1-P-C-H, NS1-P-C-HN, NS1-NS1-C-F, NS1-NS1-C-G, NS1-NS1-C-H, NS1-NS1-C-HN, NS1-NS2-C-F, NS1-NS2-C-G, NS1-NS2-C-H, NS1-NS2-C-HN, NS1-L-C-F, NS1-L-C-G, NS1-L-C-H, NS1-L-C-HN, NS2-N-C-F, NS2-N-C-G, NS2-N-C-NS2-N-C-HN, NS2-M-C-F, NS2-M-C-G, NS2-M-C-H, NS2-M-C-HN, NS2-M2-C-F, NS2-M2-C-G, NS2-M2-C-H, NS2-M2-C-HN, NS2-P-C-F, NS2-P-C-G, NS2-P-C-H, NS2-P-C-HN, NS2-NS1-C-F, NS2-NS1-C-G, NS2-NS1-C-H, NS2-NS1-C-FÍN, NS2-NS2-C-F, NS2-NS2-C-G, NS2-NS2-C-H, NS2-NS2-C-HN, NS2-L-C-F, NS2-L-C-G, NS2-L-C-H, NS2-L-C-HN, L-N-C-F, L-N-C-G, L-N-C-H, L-N-C-HN, L-M-C-F, L-M-C-G, L-M-C-H, L-M-C-HN, L-M2-C-F, L-M2-C-G, L-M2-C-H, L-M2-C-HN, L-L-C-F, L-P-C-G, L-P-C-H, L-P-C-HN, L-NS1-C-F, L-NS1-C-G, L-NS1-C-H, L-NS1-C-HN, L-NS2-C-F, L-NS2-C-G, L-NS2-C-H, L-NS2-C-HN, L-L-C-F, L-L-C-G, L-L-C-H, L-L-C-HN, N-C-N-K-F, N-C-N-K-G, N-C-N-K-H, N-C-N-K-HN, N-C-M-K-F, N-C-M-K-G, N-C-M-K-H, N-C-M-K-HN, N-C-M2-K-F, N-C-M2-K-G, N-C-M2-K-H, N-C-M2-K-HN, N-C-P-K-F, N-C-P-K-G, N-C-P-K-H, N-C-P-K-Ш, N-C-NS1-K-F, N-C-NS1-K-G, N-C-NS1-K-H, N-C-NS1-K-HN, N-C-NS2-K-F, N-C-NS2-K-G, N-C-NS2-K-H, N-C-NS2-K-HN, N-C-L-K-F, N-C-L-K-G, N-C-L-K-H, N-C-L-K-HN, M-C-N-K-F, M-C-N-K-G, M-C-N-K-H, M-C-N-K-HN, M-C-M-K-F, M-C-M-K-G, M-C-M-K-H, M-C-M-K-HN, M-C-M2-K-F, M-C-M2-K-G, M-C-M2-K-H, M-C-M2-K-HN, M-C-P-K-F, M-C-P-K-G, M-C-P-K-H, M-C-P-K-HN, M-C-NS1-K-F, M-C-NS1-K-G, M-C-NS1-K-H, M-C-NS1-K-HN, M-C-NS2-K-F, M-C-NS2-K-G, M-C-NS2-K-H, M-C-NS2-K-HN, M-C-L-K-F, M-C-L-K-G, M-C-L-K-H, M-C-L-K-HN, M2-C-N-K-F, M2-C-N-K-G, M2-C-N-K-H, M2-C-N-K-HN, M2-C-M-K-F, M2-C-M-K-G, M2-C-M-K-H, M2-C-M-K-HN, M2-C-M2-K-F, M2-C-M2-K-G, M2-C-M2-K-H, M2-C-M2-K-HN, M2-C-P-K-F, M2-C-P-K-G, M2-C-P-K-H, M2-C-P-K-HN, M2-C-NS1-K-F, M2-C-NS1-K-G, M2-C-NS1-K-H, M2-C-NS1 -K-HN, M2-C-NS2-K-F, M2-C-NS2-K-G, M2-C-NS2-K-H, M2-C-NS2-K-HN, M2-C-L-K-F, M2-C-L-K-G, M2-C-L-K-H, M2-C-L-K-HN, P-C-N-K-F, P-C-N-K-G, P-C-N-K-H, P-C-N-K-FÍN, P-C-M-K-F, P-C-M-K-G, P-C-M-K-H, P-C-M-K-HN, P-C-M2-K-F, P-C-M2-K-G, P-C-M2-K-H, P-C-M2-K-HN, P-C-P-K-F, P-C-P-K-G, P-C-P-K-H, P-C-P-K-HN, P-C-NS1-K-F, P-C-NS1-K-G, P-C-NS1-K-H, P-C-NS1-K-HN, P-C-NS2-K-F, P-C-NS2-K-G, P-C-NS2-K-H, P-C-NS2-K-HN, P-C-L-K-F, P-C-L-K-G, P-C-L-K-H, P-C-L-K-HN, NS1-C-N-K-F, NS1-C-N-K-G, NS1-C-N-K-H, NS1-C-N-K-HN, NS1-C-M-K-F, NS1-C-M-K-G, NS1-C-M-K-H, NS1-C-M-K-HN, NS1-C-M2-K-F, NS1-C-M2-K-G, NS1-C-M2-K-H, NS1-C-M2-K-HN, NS1-C-P-K-F, NS1-C-P-K-G, NS1-C-P-K-H, NS1-C-P-K-HN, NS1-C-NS1-K-F, NS1-C-NS1-K-G, NS1-C-NS1-K-H, NS1-C-NS1-K-HN, NS1-C-NS2-K-F, NS1-C-NS2-K-G, NS1-C-NS2-K-H, NS1-C-NS2-K-HN, NS1-C-L-K-F, NS1-C-L-K-G, NS1-C-L-K-H, NS1-C-L-K-HN, NS2-C-N-K-F, NS2-C-N-K-G, NS2-C-N-K-H, NS2-C-N-K-HN, NS2-C-M-K-F, NS2-C-M-K-G, NS2-C-M-K-H, NS2-C-M-K-HN, NS2-C-M2-K-F, NS2-C-M2-K-G, NS2-C-M2-K-H, NS2-C-M2-K-HN, NS2-C-P-K-F, NS2-C-P-K-G, NS2-C-P-K-H, NS2-C-P-K-HN, NS2-C-NS1-K-F, NS2-C-NS1-K-G, NS2-C-NS1-K-H, NS2-C-NS1 -K-HN, NS2-C-NS2-K-F, NS2-C-NS2-K-G, NS2-C-NS2-K-H, NS2-C-NS2-K-HN, NS2-C-L-K-F, NS2-C-L-K-G, NS2-C-L-K-H, NS2-C-L-K-HN, L-C-N-K-F, L-C-N-K-G, L-C-N-K-H, L-C-N-K-HN, L-C-M-K-F, L-C-M-K-G, L-C-M-K-H, L-C-M-K-HN, L-C-M2-K-F, L-C-M2-K-G, L-C-M2-K-H, L-C-M2-K-HN, L-C-P-K-F, L-C-P-K-G, L-C-P-K-H, L-C-P-K-HN, L-C-NS1-K-F, L-C-NS1-K-G, L-C-NS1-K-H, L-C-NS1-K-HN, L-C-NS2-K-F, L-C-NS2-K-G, L-C-NS2-K-H, L-C-NS2-K-HN, L-C-L-K-F, L-C-L-K-G, L-C-L-K-H, or L-C-L-K-HN. Наиболее предпочтительным является сочетание F-C-N-K-M2.
В предпочтительных воплощениях экспрессионная система предназначается для применения при профилактике или лечении вирусных инфекций, особенно предпочтительно для применения при профилактике или лечении парамиксовирусных инфекций, предпочтительно инфекций RSV, и/или при изготовлении лекарственных средств для профилактики или лечения парамиксовирусных инфекций, предпочтительно инфекций RSV, и/или для применения в способах профилактики или лечения парамиксовирусных инфекций, предпочтительно инфекций RSV.
В предпочтительных воплощениях экспрессионная система предназначается для усиления иммунного ответа, предпочтительно В-клеточного иммунного ответа против парамиксовирусных инфекций, предпочтительно инфекций RSV.
В соответствии с предпочтительным воплощением первого аспекта, первый полинуклеотид кодирует вирусный белок ортомиксовируса или его вариант, который индуцирует реакцию иммунной системы (т.е. иммунный ответ) у хозяина, опосредованную Т-клетками, а второй полинуклеотид кодирует вирусный белок ортомиксовируса или его вариант, который индуцирует В-клеточный антипатогенный ответ против ортомиксовируса. Предпочтительно ортомиксовирус, вирусные белки которого кодируются первым и вторым полинуклеотидом, выбирается из числа вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях вирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7. В соответствии с предпочтительным воплощением первого аспекта, второй полинуклеотид кодирует вирусный белок ортомиксовируса или его вариант, который вызывает антипатогенный В-клеточный ответ против ортомиксовируса.
В соответствии с предпочтительными воплощениями первого аспекта, первый полинуклеотид кодирует вирусный белок ортомиксовируса или его вариант, который индуцирует реакцию иммунной системы (т.е. иммунный ответ) у хозяина, опосредованный Т-клетками. Т-клеточный ответ включает активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). Т-клеточный ответ против белка индуцируется в том случае, если пептиды белка подвергаются процессингу внутри клетки и презентируются Т-клеткам на поверхности клетки через путь МНС I или МНС II. Так, в контексте настоящего изобретения для индукции Т-клеточного ответа предпочтительно используются те вирусные белки или их части, которые обычно не выходят на поверхность вируса, например, неструктурные или внутренние белки или части структурных или поверхностных белков, недоступные для В-клеток на внешней поверхности вируса.
В соответствии с предпочтительным воплощением первого аспекта, второй полинуклеотид кодирует вирусный белок ортомиксовируса или его вариант, который индуцирует антипатогенный В-клеточный ответ. В-клеточный ответ представляет собой иммунный ответ, основанный на активации В-лимфоцитов, которые вырабатывают и секретируют антиген-специфичные антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1. Так, в контексте настоящего изобретения для индуцирования В-клеточного ответа предпочтительно используются те вирусные белки или их части, которые выходят на поверхность вируса, например, структурные и/или поверхностные белки или по крайней мере те части структурных и/или поверхностных белков, которые доступны для В-клеток на внешней поверхности вируса.
В предпочтительном воплощении первого аспекта вирусный белок ортомиксовируса, который вызывает Т-клеточный ответ, является неструктурным и/или внутренним белком ортомиксовируса, а/или вирусный белок ортомиксовируса, который вызывает В-клеточный ответ против патогена, является структурным и/или поверхностным белком ортомиксовируса.
Предпочтительно аминокислотная последовательность структурного (поверхностного) и/или неструктурного (внутреннего) белка содержит последовательные сегменты или консенсусную последовательность одного или нескольких различных изолятов ортомиксовируса.
В предпочтительных воплощениях структурный белок представлен белком, экспонированным на поверхности нативного ортомиксовируса, или его вариантом. Предпочтительно структурный и/или поверхностный белок запускает независимый от Т-клеток иммунный ответ, такой, без ограничения, как опосредованный антителами иммунный ответ или активация системы комплемента. В особенно предпочтительном воплощении структурный и/или поверхностный белок индуцирует опосредованный антителами иммунный ответ. Такой опосредованный антителами иммунный ответ основан на активации В-клеток, которые вырабатывают и секретируют специфичные к антигену антитела. В-клетки, участвующие в таком иммунном ответе, включают, без ограничения, плазматические В-клетки, В-клетки памяти и клетки В-1.
В другом предпочтительном воплощении у белка, экспонированного на поверхности нативного ортомиксовируса, или его варианта домен прикрепления к мембране подвергается функциональной делеции, то есть он либо структурно делетирован, либо структурно присутствует, но не выполняет свою биологическую функцию. В особенно предпочтительном воплощении подвергается делеции аминокислотная последовательность, соответствующая домену прикрепления к мембране. Удаление участка прикрепления к мембране служит гарантией того, что белок, индуцирующий В-клеточный ответ против патогена, будет секретироваться из клетки, в которую была введена экспрессионная система изобретения.
Также предпочтительно вирусный поверхностный белок нативного ортомиксовируса выбирается из группы, состоящей из гемагглютинина (НА) и нейраминидазы (NA). Более предпочтительно вирусный поверхностный белок нативного ортомиксовируса представлен гемагглютинином (НА).
В предпочтительном воплощении первого аспекта НА включает, в основном состоит или состоит из аминокислотной последовательности НА одного из изолятов вируса гриппа А или консенсусной аминокислотной последовательности двух или нескольких различных изолятов вируса А, предпочтительно согласно SEQ ID NO: 8 или SEQ ID NO: 20, более предпочтительно согласно SEQ ID NO: 9, SEQ ID NO: 10, SEQ ID NO: 21 или варианта одной из этих последовательностей.
В предпочтительных воплощениях первого аспекта неструктурный белок является консервативным внутренним белком ортомиксовирусов, подходящим для индуцирования опосредованного Т-клетками иммунного ответа против ортомиксовируса, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). При этом индуцирующий Т-клетки белок ортомиксовируса предпочтительно не содержит сигнала секреции.
Предпочтительно неструктурный и/или внутренний белок выбирается из группы, состоящей из нуклеопротеина NP, матриксных белков Ml и М2, неструктурных белков NS1 и NS2/NEP, РНК-полимераз PA, РВ1, РВ2 и белка PB1-F2 (PB1F2).
Нуклеопротеин NP является структурным белком, инкапсулирующим минус нить РНК вирусов. NP является одним из главных детерминантов видовой специфичности.
Белок M1 является матриксным белком вируса гриппа. Он образует покрытие внутри вирусной оболочки. Белок M1 связывается с вирусной РНК. Он также выполняет несколько регуляторных функций, взаимодействуя с различными компонентами клетки хозяина. Эти механизмы регуляции включают роль в экспорте вирусных рибонуклеопротеинов из ядра клетки хозяина, ингибирование транскрипции вируса и роль в сборке вируса и почковании. Белок Ml образует слой под теми участками мембраны клетки хозяина, которые богаты гемагглютинином, нейраминидазой и трансмембранными белками М2, что способствует почкованию зрелых частиц вируса.
Неструктурный белок NS1 создается кодирующим внутренний белок, линейным сегментом гена NS из одноцепочечной РНК минус нити, который также кодирует белок ядерного экспорта NEP, ранее называвшийся белком NS2, который опосредует экспорт vRNPs. NS1 также связывается с дцРНК. В результате связывания с дцРНК белок NS1 блокирует активацию дцРНК-активируемой протеинкиназы (PKR) in vitro. Эта киназа фосфорилирует α-субъединицу эукариотического фактора инициации трансляции 2 (elF-2 альфа), что приводит к снижению скорости инициации трансляции. В отсутствие NS1 этот путь ингибируется при антивирусном ответе, останавливая трансляцию всех белков - при этом прекращается синтез вирусных белков. Однако белок NS1 вируса гриппа обходит защитные механизмы хозяина, способствуя транскрипции вирусных генов.
В предпочтительных воплощениях НА включает аминокислотную последовательность НА одного из изолятов вируса гриппа А или консенсусную аминокислотную последовательность двух или нескольких изолятов вируса гриппа А, предпочтительно согласно SEQ ID NO: 9 или SEQ ID NO: 21; NP включает аминокислотную последовательность NP одного из изолятов вируса гриппа А или консенсусную аминокислотную последовательность двух или нескольких изолятов вируса гриппа А, предпочтительно согласно SEQ ID NO: 11; а/или M1 включает аминокислотную последовательность M1 одного из изолятов вируса гриппа А или консенсусную аминокислотную последовательность двух или нескольких изолятов вируса гриппа А, предпочтительно согласно SEQ ID NO: 12. Еще более предпочтительно NP включает аминокислотную последовательность согласно SEQ ID NO: 11, a M1 включает аминокислотную последовательность согласно SEQ ID NO: 12.
В контексте настоящего изобретения структурный и/или поверхностный белок, кодируемый первым полинуклеотидом, располагается с N-конца либо с С-конца относительно неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В предпочтительном воплощении неструктурный и/или внутренний белок, кодируемый вторым полинуклеотидом, располагается с С-конца относительно структурного и/или поверхностного белка, кодируемого первым полинуклеотидом.
В частности, белок НА или NA может располагаться с N-конца либо с С-конца от NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или PB1-F2 (PB1F2). В предпочтительном воплощении белок M1 располагается с N-конца от НА.
Соответственно, воплощения настоящего изобретения имеют формулу X-Y или Y-X, где "X" означает НА или NA, предпочтительно НА, "Y" означает NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или PB1-F2 (PB1F2), предпочтительно NP или M1, а "тире" означает пептидную связь. Предпочтительными являются следующие сочетания:
HA-NP, HA-M1, НА-М2, HA-NS1, HA-NS2/NEP, НА-РА, НА-РВ1, НА-РВ2, НА-PB1F2, NP-HA, M1-НА, М2-НА, NS1-HA, NS2/NEP-HA, ΡΑ-HA, РВ1-НА, РВ2-НА, PB1F2-HA, NA-NP, NA-M1, NA-M2, NA-NS1, NA-NS2/NEP, NA-PA, NA-PB1, NA-PB2, NA-PB1F2, NP-NA, M1-NA, M2-NA, NS1-NA, NS2/NEP-NA, PA-NA, PB1-NA, PB2-NA или PB1F2-NA. Особенно предпочтительным является сочетание M1-НА.
В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком.
В предпочтительных воплощениях первого аспекта между первым полинуклеотидом и вторым полинуклеотидом располагается полинуклеотид, кодирующий сайт расщепления.
Предпочтительно этот сайт расщепления является либо сайтом саморасщепления (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется и без участия какой-либо дополнительной молекулы или же образование пептидной связи в ней предотвращается в первую очередь), либо сайтом расщепления эндопептидазами (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется эндопептидазой, например, трипсином, пепсином, эластазой, тромбином, коллагеназой, фурином, термолизином, эндопептидазой V8, катепсинами). Более предпочтительно сайт саморасщепления представлен сайтом расщепления 2А, выбранным из группы, состоящей из вирусного пептида 2А или 2А-подобных пептидов пикорнавирусов, вирусов насекомых, Aphtoviridae, ротавирусов и трипаносом, при этом предпочтительно сайт расщепления 2А представлен пептидом 2А вируса ящура. С другой стороны, полипротеин настоящего изобретения может расщепляться аутопротеазой, т.е. такой протеазой, которая расщепляет пептидные связи в той же белковой молекуле, в которой содержится и сама протеаза. Примерами таких аутопротеаз являются протеаза NS2 у флавивирусов или протеаза VP4 у бирнавирусов.
В контексте настоящего изобретения сайт расщепления может располагаться с N-конца относительно структурного и/или поверхностного белка, кодируемого первым полинуклеотидом, и с С-конца относительно неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. С другой стороны, сайт расщепления может располагаться с С-конца относительно структурного и/или поверхностного белка, кодируемого первым полинуклеотидом, и с N-конца относительно неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В частности, сайт расщепления может располагаться с С-конца или с N-конца относительно НА или NA и с С-конца или с N-конца относительно NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или РВ1-F2 (PB1F2). В предпочтительном воплощении сайт расщепления располагается с С-конца относительно NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или PB1-F2 (PB1F2) и с N-конца относительно НА или NA. Особенно предпочтительно сайт расщепления располагается с N-конца относительно НА и с С-конца относительно M1.
Соответственно, воплощения настоящего изобретения имеют формулу X-C-Y или Y-C-X, где "X" означает НА или NA, предпочтительно НА, "Y" означает NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или PB1-F2 (PB1F2), предпочтительно NP или M1, "С" означает сайт расщепления, а "тире" означает пептидную связь.
Предпочтительными являются следующие сочетания:
HA-C-NP, НА-С-М1, НА-С-М2, HA-C-NS1, HA-C-NS2/NEP, НА-С-РА, НА-С-РВ1, НА-С-РВ2, HA-C-PB1F2, NP-C-HA, М1-С-НА, М2-С-НА, NS1-C-HA, NS2/NEP-C-HA, РА-С-НА, РВ1-С-НА, РВ2-С-НА, PB1F2-C-HA, NA-C-NP, NA-C-M1, NA-C-M2, NA-C-NS1, NA-C-NS2/NEP, NA-C-PA, NA-C-PB1, NA-C-PB2, NA-C-PB1F2, NP-C-NA, M1-C-NA, М2-C-NA, NS1-C-NA, NS2/NEP-C-NA, PA-C-NA, PB1-C-NA, PB2-C-NA или PB1F2-C-NA. Особенно предпочтительным является сочетание М1-С-НА.
В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком и любые два белка могут или не могут соединяться через сайт расщепления.
В предпочтительном воплощении первого аспекта экспрессионная система дополнительно включает третий полинуклеотид, кодирующий неструктурный и/или внутренний белок ортомиксовируса или его вариант. Предпочтительно неструктурный и/или внутренний белок ортомиксовируса выбирается из группы, состоящей из родов вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях ортомиксовирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно вирусом гриппа А подтипа H1N1.
В предпочтительных воплощениях третий полинуклеотид содержится в отдельном либо в том же самом векторе, что и первый полинуклеотид и/или второй полинуклеотид.
Соответственно, первый полинуклеотид содержится в одном векторе, а второй полинуклеотид содержится во втором векторе, а третий полинуклеотид содержится в третьем векторе. По другой версии, первый и второй полинуклеотид содержатся в одном и том же векторе, а третий полинуклеотид содержится в отдельном векторе, или же первый и третий полинуклеотид содержатся в одном и том же векторе, а второй полинуклеотид содержится в отдельном векторе, или же второй и третий полинуклеотид содержатся в одном и том же векторе, а первый полинуклеотид содержится в отдельном векторе. По другой версии, первый, второй и третий полинуклеотид содержатся в одном и том же векторе. Предпочтительно первый, второй и третий полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно первый, второй и третий полинуклеотид, содержащиеся в одном и том же векторе, соединяются таким образом, чтобы они экспрессировались в виде вирусного полипротеина. Предпочтительно первый, второй и третий полинуклеотид, содержащиеся в одном и том же векторе, образуют открытую рамку считывания.
Также предпочтительно неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, является консервативным внутренним белком, подходящим для индуцирования Т-клеточного иммунного ответа против вируса, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки).
Предпочтительно неструктурный и/или внутренний белок выбирается из группы, состоящей из NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или PB1-F2 (PB1F2), более предпочтительно NP или M1.
Предпочтительно неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, отличается от неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом.
Неструктурные и/или внутренние белки, кодируемые вторым и третьим полинуклеотидом, отличаются друг от друга тем, что они включают аминокислотные последовательности разных вирусных белков. Например, это значит, что неструктурный и/или внутренний белок, кодируемый вторым полинуклеотидом, включает аминокислотную последовательность белка M1, а неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, включает аминокислотную последовательность белка NP, и наоборот.
Неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, располагается с N-конца или с С-конца неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом. В предпочтительном воплощении первого аспекта неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, располагается с С-конца неструктурного и/или внутреннего белка, кодируемого вторым полинуклеотидом.
В предпочтительных воплощениях между вторым полинуклеотидом и третьим полинуклеотидом располагается полинуклеотид, кодирующий линкер. Предпочтительно линкер представляет собой гибкий линкер, предпочтительно гибкий линкер, включающий аминокислотную последовательность согласно SEQ ID NO: 6.
В воплощениях первого аспекта белок, кодируемый вторым полинуклеотидом, располагается с N-конца относительно белка, кодируемого первым полинуклеотидом, и/или белок необязательного третьего полинуклеотида либо белок, кодируемый вторым полинуклеотидом, располагается с С-конца относительно белка, кодируемого первым полинуклеотидом и/или белка необязательного третьего полинуклеотида.
В еще более предпочтительных воплощениях этого аспекта первый полинуклеотид располагается с N-конца относительно белка, кодируемого вторым полинуклеотидом, а/или белок необязательного третьего полинуклеотида располагается с N-конца относительно белка, кодируемого первым полинуклеотидом, или между белком, кодируемым вторым полинуклеотидом, и белком, кодируемым первым полинуклеотидом; или же белок, кодируемый первым полинуклеотидом, располагается с С-конца относительно белка, кодируемого вторым полинуклеотидом, а/или белок необязательного третьего полинуклеотида располагается с С-конца относительно белка, кодируемого первым полинуклеотидом, или между белком, кодируемым вторым полинуклеотидом, и белком, кодируемым первым полинуклеотидом. В частности, белок НА или NA располагается с С-конца либо с N-конца относительно NP, M1, М2, NS1, NS2/NEP, РА, РВ1, PB2 или PB1-F2 (PB1F2).
В предпочтительном воплощении белок HA располагается с С-конца относительно M1, a NP располагается с N-конца относительно M1.
Соответственно, предпочтительные воплощения настоящего изобретения имеют формулу Χ-Κ-Υ, Υ-Κ-Χ, Χ-Κ-Υ-Υ, Υ-Υ-Κ-Χ, Χ-Υ-Κ-Υ, Υ-Κ-Υ-Χ, Χ-Κ-Υ-Κ-Υ, Y-K-Y-K-X, X-C-Y, Y-C-X, X-C-Y-Y, Y-Y-C-X, X-Y-C-Y, Y-C-Y-X, X-C-Y-C-Y, Y-C-Y-C-X, X-K-Y-C-Y, Y-C-Y-K-X, X-C-Y-K-Y или Y-K-Y-C-X, где "X" означает НА или NA, предпочтительно НА, "Y" означает NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или PB1-F2 (PB1F2), предпочтительно NP или M1, "К" означает, что в этом положении находится один или несколько пептидных линкеров, "С" означает, что в этом положении находится один или несколько сайтов расщепления, а "тире" означает пептидную связь. Предпочтительным является сочетание Y-K-Y-C-X. Еще более предпочтительными являются следующие сочетания:
HA-K-NP, NP-K-HA, HA-K-NP-NP, NP-NP-K-HA, HA-NP-K-NP, NP-K-NP-HA, НА-K-NP-K-NP, NP-K-NP-K-HA, HA-C-NP, NP-C-HA, HA-C-NP-NP, NP-NP-C-HA, HA-NP-C-NP, NP-C-NP-HA, HA-C-NP-C-NP, NP-C-NP-C-HA, HA-K-NP-C-NP, NP-C-NP-K-HA, НА-C-NP-K-NP, NP-K-NP-C-HA, HA-K-NP-M1, HA-K-M1-NP, NP-M1-K-HA, M1-NP-K-HA, HA-NP-K-M1, HA-M1-K-NP, NP-K-M1-HA, M1-K-NP-HA, HA-K-NP-K-M1, НА-К-М1-К-NP, NP-K-M1-K-HA, M1-K-NP-K-HA, HA-C-NP-M1, HA-C-M1-NP, NP-M1-C-HA, M1-NP-С-НА, HA-NP-C-M1, HA-M1-C-NP, NP-C-M1-HA, M1-C-NP-HA, HA-C-NP-C-M1, НА-С-M1-C-NP, NP-C-M1-C-HA, M1-C-NP-C-HA, HA-K-NP-C-M1, HA-K-M1-C-NP, NP-C-M1-К-НА, M1-C-NP-K-HA, HA-C-NP-K-M1, HA-C-M1-K-NP, NP-K-M1-C-HA, M1-K-NP-C-НА, HA-K-NP-M2, HA-K-M2-NP, NP-M2-K-HA, M2-NP-K-HA, HA-NP-K-M2, НА-М2-К-NP, NP-K-M2-HA, M2-K-NP-HA, HA-K-NP-K-M2, HA-K-M2-K-NP, NP-K-M2-K-HA, М2-K-NP-K-HA, HA-C-NP-M2, HA-C-M2-NP, NP-M2-C-HA, M2-NP-C-HA, HA-NP-C-M2, НА-M2-C-NP, NP-C-M2-HA, M2-C-NP-HA, HA-C-NP-C-M2, HA-C-M2-C-NP, NP-C-M2-C-HA, M2-C-NP-C-HA, HA-K-NP-C-M2, HA-K-M2-C-NP, NP-C-M2-K-HA, M2-C-NP-K-HA, НА-C-NP-K-M2, HA-C-M2-K-NP, NP-K-M2-C-HA, M2-K-NP-C-HA, HA-K-NP-NS1, НА-К-NS1-NP, NP-NS1-K-HA, NS1-NP-K-HA, HA-NP-K-NS1, HA-NS1-K-NP, NP-K-NS1-HA, NS1-K-NP-HA, HA-K-NP-K-NS1, HA-K-NS1-K-NP, NP-K-NS1 -К-НА, NS 1-K-NP-K-HA, HA-C-NP-NS1, HA-C-NS1-NP, NP-NS1-C-HA, NS1-NP-C-HA, HA-NP-C-NS1, HA-NS1-C-NP, NP-C-NS1-HA, NS1-C-NP-HA, HA-C-NP-C-NS1, HA-C-NS1-C-NP, NP-C-NS1-C-HA, NS1-C-NP-C-HA, HA-K-NP-C-NS1, HA-K-NS 1-C-NP, NP-C-NS1 -К-НА, NS1-C-NP-K-HA, HA-C-NP-K-NS1, HA-C-NS1-K-NP, NP-K-NS1-C-HA, NS1-K-NP-C-HA, HA-K-NP-NS2/NEP, HA-K-NS2/NEP-NP, NP-NS2/NEP-K-HA, NS2/NEP-NP-K-HA, HA-NP-K-NS2/NEP, HA-NS2/NEP-K-NP, NP-K-NS2/NEP-HA, NS2/NEP-K-NP-HA, HA-K-NP-K-NS2/NEP, HA-K-NS2/NEP-K-NP, NP-K-NS2/NEP-K-HA, NS2/NEP-K-NP-K-HA, HA-C-NP-NS2/NEP, HA-C-NS2/NEP-NP, NP-NS2/NEP-C-HA, NS2/NEP-NP-C-HA, HA-NP-C-NS2/NEP, HA-NS2/NEP-C-NP, NP-C-NS2/NEP-HA, NS2/NEP-C-NP-HA, HA-C-NP-C-NS2/NEP, HA-C-NS2/NEP-C-NP, NP-C-NS2/NEP-C-HA, NS2/NEP-C-NP-C-HA, HA-K-NP-C-NS2/NEP, HA-K-NS2/NEP-C-NP, NP-C-NS2/NEP-K-HA, NS2/NEP-C-NP-K-HA, HA-C-NP-K-NS2/NEP, HA-C-NS2/NEP-K-NP, NP-K-NS2/NEP-C-HA, NS2/NEP-K-NP-C-HA, HA-K-NP-PA, HA-K-PA-NP, NP-PA-K-HA, PA-NP-K-HA, HA-NP-K-PA, HA-PA-K-NP, NP-K-PA-HA, PA-K-NP-HA, HA-K-NP-K-PA, HA-K-PA-K-NP, NP-K-PA-K-HA, PA-K-NP-K-HA, HA-C-NP-PA, HA-C-PA-NP, NP-PA-C-HA, PA-NP-C-HA, HA-NP-C-PA, HA-PA-C-NP, NP-C-PA-HA, PA-C-NP-HA, HA-C-NP-C-PA, HA-C-PA-C-NP, NP-C-PA-C-HA, PA-C-NP-C-HA, HA-K-NP-C-PA, HA-K-PA-C-NP, NP-C-PA-K-HA, PA-C-NP-K-HA, HA-C-NP-K-PA, HA-C-PA-K-NP, NP-K-PA-C-HA, PA-K-NP-C-HA, HA-K-NP-PB1, HA-K-PB1-NP, NP-PB1-K-FÍA, PB1-NP-K-HA, HA-NP-K-PB1, HA-PB 1-K-NP, NP-K-PB1-HA, PB1-K-NP-HA, HA-K-NP-K-PB1, HA-K-PB1-K-NP, NP-K-PB1-K-HA, PB1-K-NP-K-HA, HA-C-NP-PB1, HA-C-PB1-NP, NP-PB1-C-HA, PB1-NP-C-HA, HA-NP-C-PB1, HA-PB1-C-NP, NP-C-PB1-HA, PB1-C-NP-HA, HA-C-NP-C-PB1, HA-C-PB1-C-NP, NP-C-PB1-C-HA, PB1-C-NP-C-HA, HA-K-NP-C-PB1, HA-K-PB1-C-NP, NP-C-PB1-K-HA, PB1-C-NP-K-HA, HA-C-NP-K-PB1, HA-C-PB1-K-NP, NP-K-PB1-C-HA, PB1-K-NP-C-HA, HA-K-NP-PB2, HA-K-PB2-NP, NP-PB2-K-HA, PB2-NP-K-HA, HA-NP-K-PB2, HA-PB2-K-NP, NP-K-PB2-HA, PB2-K-NP-HA, HA-K-NP-K-PB2, HA-K-PB2-K-NP, NP-K-PB2-K-HA, PB2-K-NP-K-HA, HA-C-NP-PB2, HA-C-PB2-NP, NP-PB2-C-HA, PB2-NP-C-HA, HA-NP-C-PB2, HA-PB2-C-NP, NP-C-PB2-HA, PB2-C-NP-HA, HA-C-NP-C-PB2, HA-C-PB2-C-NP, NP-C-PB2-C-HA, PB2-C-NP-C-FÍA, HA-K-NP-C-PB2, HA-K-PB2-C-NP, NP-C-PB2-K-HA, PB2-C-NP-K-HA, HA-C-NP-K-PB2, HA-C-PB2-K-NP, NP-K-PB2-C-HA, PB2-K-NP-C-HA, HA-K-NP-PB1F2, HA-K-PB1F2-NP, NP-PB1F2-K-HA, PB 1F2-NP-K-HA, HA-NP-K-PB1F2, HA-PB1F2-K-NP, NP-K-PB1F2-HA, PB 1F2-K-NP-HA, HA-K-NP-K-PB1F2, HA-K-PB 1F2-K-NP, NP-K-PB 1F2-K-HA, PB1F2-K-NP-K-HA, HA-C-NP-PB1F2, HA-C-PB1F2-NP, NP-PB1F2-C-HA, PB1F2-NP-C-HA, HA-NP-C-PB1F2, HA-PB 1F2-C-NP, NP-C-PB1F2-HA, PB 1F2-C-NP-HA, HA-C-NP-C-PB1F2, HA-C-PB 1F2-C-NP, NP-C-PB1F2-C-HA, PB 1F2-C-NP-C-HA, HA-K-NP-C-PB1F2, HA-K-PB 1F2-C-NP, NP-C-PB 1F2-K-HA, PB 1F2-C-NP-K-HA, HA-C-NP-K-PB1F2, HA-C-PB 1F2-K-NP, NP-K-PB1F2-C-HA, PB 1F2-K-NP-C-HA, HA-K-M1, M1-K-HA, HA-K-M1-M1, M1-M1-K-HA, HA-M1-K-M1, M1-K-M1-HA, HA-K-M1-K-M1, M1-K-M1-K-HA, HA-C-M1, M1-C-HA, HA-C-M1-M1, M1-M1-C-HA, HA-M1-C-M1, M1-C-M1-HA, HA-C-M1-C-M1, M1-C-M1-C-HA, HA-K-M1-C-M1, M1-C-M1-K-HA, HA-C-M1-K-M1, M1-K-M1-C-HA, HA-K-M1-M2, НА-К-М2-М1, М1-М2-К-НА, М2-М1-К-НА, НА-М1-К-М2, НА-М2-К-М1, М1-К-М2-НА, М2-К-М1-НА, НА-К-М1-К-М2, НА-К-М2-К-М1, М1-К-М2-К-НА, М2-К-М1-К-НА, НА-С-М1-М2, НА-С-М2-М1, М1-М2-С-НА, М2-М1-С-НА, НА-М1-С-М2, НА-М2-С-М1, Ml-С-М2-НА, М2-С-М1-НА, НА-С-М1-С-М2, НА-С-М2-С-М1, М1-С-М2-С-НА, М2-С-М1-С-НА, НА-К-М1-С-М2, НА-К-М2-С-М1, М1-С-М2-К-НА, М2-С-М1-К-НА, НА-С-М1-К-М2, НА-С-М2-К-М1, М1-К-М2-С-НА, М2-К-М1-С-НА, HA-K-M1-NS1, HA-K-NS1-M1, Ml-NS1-K-HA, NS1-M1-K-HA, HA-M1-K-NS1, HA-NS1-K-M1, M1-K-NS1-HA, NS1-K-M1-HA, HA-K-M1-K-NS1, HA-K-NS1-K-M1, M1-K-NS1-K-HA, NS1-K-M1-K-HA, HA-C-M1-NS1, HA-C-NS1-M1, M1-NS1-C-HA, NS1-M1-C-HA, HA-M1-C-NS1, HA-NS1-C-M1, Ml-C-NS1-HA, NS1-C-M1-HA, HA-C-M 1-C-NS1, HA-C-NS1-C-M1, M1-C-NS1-C-HA, NS1-C-Ml-C-HA, HA-K-M1-C-NS1, HA-K-NS1-C-M1, M1-C-NS1-K-HA, NS1-C-M1-K-HA, HA-C-M1-K-NS1, HA-C-NS1-K-M1, M1-K-NS1-C-HA, NS1-K-M1-C-HA, HA-K-M1-NS2/NEP, HA-K-NS2/NEP-M1, M1-NS2/NEP-K-HA, NS2/NEP-M1-K-HA, HA-M1-K-NS2/NEP, HA-NS2/NEP-K-M1, M1-K-NS2/NEP-HA, NS2/NEP-K-M1 -HA, HA-K-M 1-K-NS2/NEP, HA-K-NS2/NEP-K-M1, M1-K-NS2/NEP-K-HA, NS2/NEP-K-M1 -K-HA, HA-C-M1-NS2/NEP, HA-C-NS2/NEP-M1, M1-NS2/NEP-C-HA, NS2/NEP-M1 -C-HA, HA-M 1-C-NS2/NEP, HA-NS2/NEP-C-M1, M1-C-NS2/NEP-HA, NS2/NEP-C-M1 -HA, HA-C-M 1-C-NS2/NEP, HA-C-NS2/NEP-C-M1, M1-C-NS2/NEP-C-HA, NS2/NEP-C-M1 -C-HA, HA-K-M 1-C-NS2/NEP, HA-K-NS2/NEP-C-M1, M1-C-NS2/NEP-K-HA, NS2/NEP-C-M1 -K-HA, HA-C-M 1-K-NS2/NEP, HA-C-NS2/NEP-K-M1, M1-K-NS2/NEP-C-HA, NS2/NEP-K-M1 -C-HA, HA-K-M1-PA, HA-K-PA-M1, M1-PA-K-HA, PA-M1-K-HA, HA-M1-K-PA, HA-PA-K-M1, M1-K-PA-HA, PA-K-M1-HA, HA-K-M1-K-PA, HA-K-PA-K-M1, M1-K-PA-K-HA, PA-K-M1-K-HA, HA-C-M1-PA, HA-C-PA-M1, M1-PA-C-HA, PA-M1-C-HA, HA-M1-C-PA, HA-PA-C-M1, M1-C-PA-HA, PA-C-M1-HA, HA-C-M1-C-PA, HA-C-PA-C-M1, M1-C-PA-C-HA, PA-C-M1-C-HA, HA-K-M1-C-PA, HA-K-PA-C-M1, M1-C-PA-K-HA, PA-C-M1-K-HA, HA-C-M 1-K-PA, HA-C-PA-K-M1, M1-K-PA-C-HA, PA-K-M1-C-HA, HA-K-M1-PB1, HA-K-PB1-M1, M1-PB1-K-HA, PB1-M1-K-HA, HA-M1-K-PB1, HA-PB1-K-M1, M1-K-PB1-HA, PB1-K-M1-HA, HA-K-M1-K-PB1, HA-K-PB1-K-M1, M1-K-PB1-K-HA, PB1-K-M1-K-HA, HA-C-M1-PB1, HA-C-PB1-M1, M1-PB1-C-HA, PB1-M1-C-HA, HA-M1-C-PB1, HA-PB1-C-M1, M1-C-PB1-HA, PB1-C-M1-HA, HA-C-M1-C-PB1, HA-C-PB1-C-M1, M1-C-PB1-C-HA, PB1-C-M1-C-HA, HA-K-M1-C-PB1, HA-K-PB1-C-M1, M1-C-PB1-K-HA, PB1-C-M1-K-HA, HA-C-M 1-K-PB1, HA-C-PB1-K-M1, M1-K-PB1-C-HA, PB1-K-M1-C-HA, HA-K-M 1-PB2, HA-K-PB2-M1, Ml-PB2-K-HA, PB2-M1-K-HA, HA-M1-K-PB2, HA-PB2-K-M1, M1-K-PB2-HA, PB2-K-M1-HA, HA-K-M 1-K-PB2, HA-K-PB2-K-M1, M1-K-PB2-K-HA, PB2-K-M1 -K-HA, HA-C-M 1-PB2, HA-C-PB2-M1, M1-PB2-C-HA, PB2-M1-C-HA, HA-M1-C-PB2, HA-PB2-C-M1, M1-C-PB2-НА, РВ2-С-М1-НА, НА-С-М1-С-РВ2, НА-С-РВ2-С-М1, М1-С-РВ2-С-НА, РВ2-С-М1-С-НА, НА-К-М1-С-РВ2, НА-К-РВ2-С-М1, М1-С-РВ2-К-НА, РВ2-С-М1-К-НА, НА-С-М1-К-РВ2, НА-С-РВ2-К-М1, М1-К-РВ2-С-НА, РВ2-К-М1-С-НА, НА-К-М1 -PB 1F2, НА-К-PB1F2-M1, M1-PB1F2-K-HA, PB1F2-M1-K-HA, HA-M1-K-PB1F2, НА-PB1F2-K-M1, М1-K-PB1F2-HA, PB1F2-K-M1-HA, НА-К-М 1 -К-PB1F2, НА-К-PB1F2-K-M1, M1-K-PB1F2-K-НА, PB 1F2-K-M1 -К-НА, HA-C-M1-PB1F2, HA-C-PB1F2-M1, M1-PB1F2-C-HA, PB1F2-М1-С-НА, HA-M1-C-PB1F2, НА-РВ 1F2-C-M1, M1-C-PB1F2-HA, PB 1F2-C-M1 -НА, НА-С-M1-C-PB1F2, НА-С-PB1F2-C-M1, M1 -С-PB1F2-C-HA, PB 1F2-C-M1 -С-НА, НА-К-М 1-С-PB1F2, НА-К-РВ 1F2-C-M1, M1 -С-РВ 1F2-K-HA, PB 1F2-C-M1 -К-НА, НА-С-М1 -К-РВ 1F2, НА-С-РВ 1F2-K-M1, M1 -К-РВ 1F2-C-HA, PB 1F2-K-M1 -С-НА, НА-К-М2, М2-К-НА, НА-К-М2-М2, М2-М2-К-НА, НА-М2-К-М2, М2-К-М2-НА, НА-К-М2-К-М2, М2-К-М2-К-НА, НА-С-М2, М2-С-НА, НА-С-М2-М2, М2-М2-С-НА, НА-М2-С-М2, М2-С-М2-НА, НА-С-М2-С-М2, М2-С-М2-С-НА, НА-К-М2-С-М2, М2-С-М2-К-НА, НА-С-М2-К-М2, М2-К-М2-С-НА, HA-K-M2-NS1, HA-K-NS1-M2, M2-NS1-K-HA, NS1-M2-K-HA, HA-M2-K-NS1, HANS 1-К-М2, M2-K-NS1-HA, NS1-K-M2-HA, HA-K-M2-K-NS1, HA-K-NS1-К-М2, М2-К-NS1-K-HA, NS1-К-М2-К-НА, HA-C-M2-NS1, HA-C-NS1-M2, M2-NS1-C-HA, NS1-M2-C-НА, HA-M2-C-NS1, HA-NS1-C-M2, M2-C-NS1-HA, NS1-C-M2-HA, HA-C-M2-C-NS1, НА-C-NS1-C-M2, M2-C-NS1-C-HA, NS 1-С-М2-С-НА, HA-K-M2-C-NS1, HA-K-NS 1-С-М2, М2-C-NS1-K-HA, NS 1-С-М2-К-НА, HA-C-M2-K-NS1, HA-C-NS1-К-М2, M2-K-NS1-C-HA, NS1-K-M2-C-HA, HA-K-M2-NS2/NEP, HA-K-NS2/NEP-M2, M2-NS2/NEP-K-HA, NS2/NEP-M2-K-HA, HA-M2-K-NS2/NEP, HA-NS2/NEP-K-M2, M2-K-NS2/NEP-HA, NS2/NEP-K-M2-HA, HA-K-M2-K-NS2/NEP, HA-K-NS2/NEP-K-M2, M2-K-NS2/NEP-K-HA, NS2/NEP-K-M2-K-HA, HA-C-M2-NS2/NEP, HA-C-NS2/NEP-M2, M2-NS2/NEP-C-HA, NS2/NEP-M2-C-HA, HA-M2-C-NS2/NEP, HA-NS2/NEP-C-M2, M2-C-NS2/NEP-HA, NS2/NEP-C-M2-HA, HA-C-M2-C-NS2/NEP, HA-C-NS2/NEP-C-M2, M2-C-NS2/NEP-C-HA, NS2/NEP-C-M2-C-HA, HA-K-M2-C-NS2/NEP, HA-K-NS2/NEP-C-M2, M2-C-NS2/NEP-K-НА, NS2/NEP-C-M2-K-HA, HA-C-M2-K-NS2/NEP, HA-C-NS2/NEP-K-M2, М2-К-NS2/NEP-C-HA, NS2/NEP-K-M2-C-HA, НА-К-М2-РА, НА-К-РА-М2, М2-РА-К-НА, РА-М2-К-НА, НА-М2-К-РА, НА-РА-К-М2, М2-К-РА-НА, РА-К-М2-НА, НА-К-М2-К-РА, НА-К-РА-К-М2, М2-К-РА-К-НА, РА-К-М2-К-НА, НА-С-М2-РА, НА-С-РА-М2, М2-РА-С-НА, РА-М2-С-НА, НА-М2-С-РА, НА-РА-С-М2, М2-С-РА-НА, РА-С-М2-НА, НА-С-М2-С-РА, НА-С-РА-С-М2, М2-С-РА-С-НА, РА-С-М2-С-НА, НА-К-М2-С-РА, НА-К-РА-С-М2, М2-С-РА-К-НА, РА-С-М2-К-НА, НА-С-М2-К-РА, НА-С-РА-К-М2, М2-К-РА-С-НА, РА-К-М2-С-НА, НА-К-М2-РВ1, НА-К-РВ 1-М2, М2-РВ1-К-НА, РВ1-М2-К-НА, НА-М2-К-РВ1, НА-РВ 1-К-М2, М2-К-РВ1-НА, РВ1-К-М2-НА, НА-К-М2-К-РВ1, НА-К-РВ 1-К-М2, М2-К-РВ1 -К-НА, PB 1-К-М2-К-НА, НА-С-М2-РВ1, НА-С-РВ1-М2, М2-РВ1-С-НА, РВ1-М2-С-НА, НА-М2-С-РВ1, НА-РВ1-С-М2, М2-С-РВ1-НА, РВ1-С-М2-НА, НА-С-М2-С-РВ1, НА-С-РВ1-С-М2, М2-С-РВ1-С-НА, РВ1-С-М2-С-НА, НА-К-М2-С-РВ1, НА-К-РВ 1-С-М2, М2-С-РВ1 -К-НА, РВ1-С-М2-К-НА, НА-С-М2-К-РВ1, НА-С-РВ1-К-М2, М2-К-РВ1-С-НА, PB 1-К-М2-С-НА, НА-К-М2-РВ2, НА-К-РВ2-М2, М2-РВ2-К-НА, РВ2-М2-К-НА, НА-М2-К-РВ2, НА-РВ2-К-М2, М2-К-РВ2-НА, РВ2-К-М2-НА, НА-К-М2-К-РВ2, НА-К-РВ2-К-М2, М2-К-РВ2-К-НА, РВ2-К-М2-К-НА, НА-С-М2-РВ2, НА-С-РВ2-М2, М2-РВ2-С-НА, РВ2-М2-С-НА, НА-М2-С-РВ2, НА-РВ2-С-М2, М2-С-РВ2-НА, РВ2-С-М2-НА, НА-С-М2-С-РВ2, НА-С-РВ2-С-М2, М2-С-РВ2-С-НА, РВ2-С-М2-С-НА, НА-К-М2-С-РВ2, НА-К-РВ2-С-М2, М2-С-РВ2-К-НА, РВ2-С-М2-К-НА, НА-С-М2-К-РВ2, НА-С-РВ2-К-М2, М2-К-РВ2-С-НА, РВ2-К-М2-С-НА, НА-К-М2-PB1F2, НА-К-PB1F2-M2, М2-PB1F2-K-HA, PB 1F2-M2-K-HA, HA-M2-K-PB1F2, HA-PB1F2-K-M2, M2-K-PB1F2-HA, PB 1F2-K-M2-HA, НА-К-М2-К-PB1F2, НА-К-РВ 1F2-K-M2, М2-К-PB1F2-K-HA, PB 1F2-K-M2-K-HA, НА-С-M2-PB1F2, НА-С-РВ 1F2-M2, М2-PB1F2-C-HA, PB1F2-M2-C-HA, HA-M2-C-PB1F2, НА-PB1F2-C-M2, М2-С-PB1F2-HA, PB 1F2-C-M2-HA, НА-С-М2-С-PB1F2, НА-С-РВ 1F2-C-M2, М2-С-PB1F2-C-HA, PB 1F2-C-M2-C-HA, НА-К-М2-С-PB1F2, НА-К-РВ 1F2-C-M2, М2-С-PB1F2-K-HA, PB 1F2-C-M2-K-HA, НА-С-М2-К-PB1F2, НА-С-РВ 1F2-K-M2, M2-K-PB1F2-С-НА, PB 1F2-K-M2-C-HA, HA-K-NS1, NS1-K-HA, HA-K-NS1-NS1, NS1-NS1-K-HA, HANS 1-K-NSl, NS1-K-NS1-HA, HA-K-NS1-K-NS1, NS1-K-NS1-K-HA, HA-C-NS1, NS1-C-HA, HA-C-NS1-NS1, NS1-NS1-C-HA, HA-NS1-C-NS1, NS1-C-NS1-HA, HA-C-NS1-C-NS1, NS1-C-NS1-C-HA, HA-K-NS1-C-NS1, NS1-C-NS1-K-HA, HA-C-NS1-K-NS1, NS1-K-NS1-C-HA, HA-K-NS1-NS2/NEP, HA-K-NS2/NEP-NS1, NS1-NS2/NEP-K-HA, NS2/NEP-NS1 -K-HA, HA-NS1-K-NS2/NEP, HA-NS2/NEP-K-NS1, NS 1-K-NS2/NEP-HA, NS2/NEP-K-NS1-HA, HA-K-NS 1-K-NS2/NEP, HA-K-NS2/NEP-K-NS1, NS 1-K-NS2/NEP-K-HA, NS2/NEP-K-NS1-K-HA, HA-C-NS1-NS2/NEP, HA-C-NS2/NEP-NS1, NS 1-NS2/NEP-C-HA, NS2/NEP-NS1-C-HA, HA-NS 1-C-NS2/NEP, HA-NS2/NEP-C-NS1, NS 1-C-NS2/NEP-HA, NS2/NEP-C-NS1-HA, HA-C-NS 1-C-NS2/NEP, HA-C-NS2/NEP-C-NS1, NS 1-C-NS2/NEP-C-HA, NS2/NEP-C-NS1 -C-HA, HA-K-NS 1-C-NS2/NEP, HA-K-NS2/NEP-C-NS1, NS 1-C-NS2/NEP-K-HA, NS2/NEP-C-NS1 -K-HA, HA-C-NS 1-K-NS2/NEP, HA-C-NS2/NEP-K-NS1, NS1-K-NS2/NEP-C-HA, NS2/NEP-K-NS1 -C-HA, HA-K-NS 1-PA, HA-K-PA-NS1, NS1-PA-K-HA, PA-NS1-K-HA, HA-NS 1-K-PA, HA-PA-K-NS1, NS1-K-PA-HA, PA-K-NS1-HA, HA-K-NS 1-K-PA, HA-K-PA-K-NS1, NS1-K-PA-K-HA, PA-K-NS1-K-HA, HA-C-NS1-PA, HA-C-PA-NS1, NS1-PA-C-HA, PA-NS1-C-HA, HA-NS1-C-PA, HA-PA-C-NS1, NS1-C-PA-HA, PA-C-NS1-HA, HA-C-NS 1-C-PA, HA-C-PA-C-NS1, NS1-C-PA-C-HA, PA-C-NS1-C-HA, HA-K-NS 1-C-P A, HA-K-PA-C-NS1, NS1-C-PA-K-HA, PA-C-NS1-K-HA, HA-C-NS 1-K-PA, HA-C-PA-K-NS1, NS1-K-PA-C-HA, PA-K-NS1-C-HA, HA-K-NS1-PB1, HA-K-PB1-NS1, NS1-PB1-K-HA, PB1-NS1-K-HA, HA-NS1-K-PB1, HA-PB1-K-NS1, NS1-K-PB1-HA, PB1-K-NS1-HA, HA-K-NS1-K-PB1, HA-K-PB1-K-NS1, NS1-K-PB1-K-HA, PB1-K-NS1-K-HA, HA-C-NS1-PB1, HA-C-PB1-NS1, NS1-PB1-C-HA, PB1-NS1-C-HA, HA-NS1-C-PB1, HA-PB1-C-NS1, NS1-C-PB1-HA, PB1-C-NS1-HA, HA-C-NS1-C-PB1, HA-C-PB1-C-NS1, NS1-C-PB1-C-HA, PB1-C-NS1-C-HA, HA-K-NS1-C-PB1, HA-K-PB1-C-NS1, NS1-C-PB 1-K-HA, PB1-C-NS1-K-HA, HA-C-NS 1-K-PB 1, HA-C-PB1-K-NS1, NS1-K-PB1-C-HA, PB1-K-NS1-C-HA, HA-K-NS1-PB2, HA-K-PB2-NS1, NS1-PB2-K-HA, PB2-NS1-K-HA, HA-NS1-K-PB2, HA-PB2-K-NS1, NS1-K-PB2-HA, PB2-K-NS1-HA, HA-K-NS 1-K-PB2, HA-K-PB2-K-NS1, NS1-K-PB2-K-HA, PB2-K-NS1 -K-HA, HA-C-NS1-PB2, HA-C-PB2-NS1, NS1-PB2-C-HA, PB2-NS1-C-HA, HA-NS1-C-PB2, HA-PB2-C-NS1, NS1-C-PB2-HA, PB2-C-NS1-HA, HA-C-NS1-C-PB2, HA-C-PB2-C-NS1, NS1-C-PB2-C-HA, PB2-C-NS1-C-HA, HA-K-NS1-C-PB2, HA-K-PB2-C-NS1, NS 1-C-PB2-K-HA, PB2-C-NS1 -K-HA, HA-C-NS 1-K-PB2, HA-C-PB2-K-NS1, NS1-K-PB2-C-HA, PB2-K-NS1 -C-HA, HA-K-NS 1-PB 1F2, HA-K-PB1F2-NS1, NS1-PB1F2-K-HA, PB 1F2-NS1 -K-HA, HA-NS1-K-PB1F2, HA-PB1F2-K-NS1, NS 1 -K-PB1F2-HA, PB1F2-K-NS1-HA, HA-K-NS 1 -K-PB 1F2, HA-K-PB1F2-K-NS1, NS 1 -K-PB 1F2-K-HA, PB1F2-K-NS1-K-HA, HA-C-NS 1 -PB 1F2, HA-C-PB1F2-NS1, NS 1 -PB 1F2-C-HA, PB 1F2-NS1 -C-HA, HA-NS1-C-PB1F2, HA-PB 1F2-C-NS1, NS 1 -C-PB1F2-HA, PB1F2-C-NS1-HA, HA-C-NS1-C-PB1F2, HA-C-PB 1F2-C-NS1, NS 1 -C-PB 1F2-C-HA, PB 1F2-C-NS1 -C-HA, HA-K-NS1-C-PB1F2, HA-K-PB 1F2-C-NS1, NS 1 -C-PB 1F2-K-HA, PB 1F2-C-NS1 -K-HA, HA-C-NS1-K-PB1F2, HA-C-PB 1F2-K-NS1, NS 1 -K-PB 1F2-C-HA, PB 1F2-K-NS1 -C-HA, HA-K-NS2/NEP, NS2/NEP-K-HA, HA-K-NS2/NEP-NS2/NEP, NS2/NEP-NS2/NEP-K-HA, HA-NS2/NEP-K-NS2/NEP, NS2/NEP-K-NS2/NEP-HA, HA-K-NS2/NEP-K-NS2/NEP, NS2/NEP-K-NS2/NEP-K-HA, HA-C-NS2/NEP, NS2/NEP-C-HA, HA-C-NS2/NEP-NS2/NEP, NS2/NEP-NS2/NEP-C-HA, HA-NS2/NEP-C-NS2/NEP, NS2/NEP-C-NS2/NEP-HA, HA-C-NS2/NEP-C-NS2/NEP, NS2/NEP-C-NS2/NEP-C-HA, HA-K-NS2/NEP-C-NS2/NEP, NS2/NEP-C-NS2/NEP-K-HA, HA-C-NS2/NEP-K-NS2/NEP, NS2/NEP-K-NS2/NEP-C-HA, HA-K-NS2/NEP-PA, HA-K-PA-NS2/NEP, NS2/NEP-PA-K-HA, PA-NS2/NEP-K-HA, HA-NS2/NEP-K-PA, HA-PA-K-NS2/NEP, NS2/NEP-K-PA-HA, PA-K-NS2/NEP-HA, HA-K-NS2/NEP-K-PA, HA-K-PA-K-NS2/NEP, NS2/NEP-K-PA-K-HA, PA-K-NS2/NEP-K-HA, HA-C-NS2/NEP-PA, HA-C-PA-NS2/NEP, NS2/NEP-PA-C-HA, PA-NS2/NEP-C-HA, HA-NS2/NEP-C-PA, HA-PA-C-NS2/NEP, NS2/NEP-C-PA-HA, PA-C-NS2/NEP-HA, HA-C-NS2/NEP-C-PA, HA-C-PA-C-NS2/NEP, NS2/NEP-C-PA-C-HA, PA-C-NS2/NEP-C-HA, HA-K-NS2/NEP-C-PA, HA-K-PA-C-NS2/NEP, NS2/NEP-C-PA-K-HA, PA-C-NS2/NEP-K-HA, HA-C-NS2/NEP-K-PA, HA-C-PA-K-NS2/NEP, NS2/NEP-K-PA-C-HA, PA-K-NS2/NEP-C-HA, HA-K-NS2/NEP-PB1, HA-K-PB1-NS2/NEP, NS2/NEP-PB1 -K-HA, PB 1-NS2/NEP-K-HA, HA-NS2/NEP-K-PB1, ΗΑ-PB1-K-NS2/NEP, NS2/NEP-K-PB1 -HA, PB 1-K-NS2/NEP-HA, HA-K-NS2/NEP-K-PB1, ΗΑ-Κ-ΡΒ1-K-NS2/NEP, NS2/NEP-K-PB1 -K-HA, PB 1-K-NS2/NEP-K-HA, HA-C-NS2/NEP-PB1, HA-C-PB1-NS2/NEP, NS2/NEP-PB1-C-HA, PB 1-NS2/NEP-C-HA, HA-NS2/NEP-C-PB1, ΗΑ-PB1-C-NS2/NEP, NS2/NEP-C-PB1 -HA, PB 1-C-NS2/NEP-HA, HA-C-NS2/NEP-C-PB1, HA-C-PB 1-C-NS2/NEP, NS2/NEP-C-PB1 -C-HA, PB 1-C-NS2/NEP-C-HA, HA-K-NS2/NEP-C-PB1, HA-K-PB1-C-NS2/NEP, NS2/NEP-C-PB1 -K-HA, PB 1-C-NS2/NEP-K-HA, HA-C-NS2/NEP-K-PB1, HA-C-PB 1-K-NS2/NEP, NS2/NEP-K-PB1 -C-HA, PB 1-K-NS2/NEP-C-HA, HA-K-NS2/NEP-PB2, HA-K-PB2-NS2/NEP, NS2/NEP-PB2-K-HA, PB2-NS2/NEP-K-HA, HA-NS2/NEP-K-PB2, HA-PB2-K-NS2/NEP, NS2/NEP-K-PB2-HA, PB2-K-NS2/NEP-HA, HA-K-NS2/NEP-K-PB2, HA-K-PB2-K-NS2/NEP, NS2/NEP-K-PB2-K-HA, PB2-K-NS2/NEP-K-HA, HA-C-NS2/NEP-PB2, HA-C-PB2-NS2/NEP, NS2/NEP-PB2-C-HA, PB2-NS2/NEP-C-HA, HA-NS2/NEP-C-PB2, HA-PB2-C-NS2/NEP, NS2/NEP-C-PB2-HA, PB2-C-NS2/NEP-HA, HA-C-NS2/NEP-C-PB2, HA-C-PB2-C-NS2/NEP, NS2/NEP-C-PB2-C-HA, PB2-C-NS2/NEP-C-HA, HA-K-NS2/NEP-C-PB2, HA-K-PB2-C-NS2/NEP, NS2/NEP-C-PB2-K-HA, PB2-C-NS2/NEP-K-HA, HA-C-NS2/NEP-K-PB2, HA-C-PB2-K-NS2/NEP, NS2/NEP-K-PB2-C-HA, PB2-K-NS2/NEP-C-HA, HA-K-NS2/NEP-PB1F2, HA-K-PB 1F2-NS2/NEP, NS2/NEP-PB1F2-K-HA, PB 1F2-NS2/NEP-K-HA, HA-NS2/NEP-K-PB1F2, HA-PB1F2-K-NS2/NEP, NS2/NEP-K-PB1F2-HA, PB 1F2-K-NS2/NEP-HA, HA-K-NS2/NEP-K-PB1F2, HA-K-PB 1F2-K-NS2/NEP, NS2/NEP-K-PB1F2-K-HA, PB 1F2-K-NS2/NEP-K-HA, HA-C-NS2/NEP-PB1F2, HA-C-PB 1F2-NS2/NEP, NS2/NEP-PB1F2-C-HA, PB 1F2-NS2/NEP-C-HA, HA-NS2/NEP-C-PB1F2, HA-PB 1F2-C-NS2/NEP, NS2/NEP-C-PB1F2-HA, PB 1F2-C-NS2/NEP-HA, HA-C-NS2/NEP-C-PB1F2, HA-C-PB 1F2-C-NS2/NEP, NS2/NEP-C-PB1F2-C-H A, PB1F2-C-NS2/NEP-C-HA, HA-K-NS2/NEP-C-PB1F2, HA-K-PB 1F2-C-NS2/NEP, NS2/NEP-C-PB1F2-K-HA, PB 1F2-C-NS2/NEP-K-HA, HA-C-NS2/NEP-K-PB1F2, HA-C-PB 1F2-K-NS2/NEP, NS2/NEP-K-PB1F2-C-HA, PB 1F2-K-NS2/NEP-C-HA, HA-K-PA, PA-K-HA, HA-K-PA-PA, PA-PA-K-HA, HA-PA-K-PA, PA-K-PA-HA, HA-K-PA-K-PA, PA-K-PA-K-HA, HA-C-PA, PA-C-HA, HA-C-PA-PA, PA-PA-C-HA, HA-PA-C-PA, PA-C-PA-HA, HA-C-PA-C-PA, PA-C-PA-C-HA, HA-K-PA-C-PA, PA-C-PA-K-HA, HA-C-PA-K-PA, PA-K-PA-C-HA, HA-K-PA-PB1, HA-K-PB1-PA, PA-PB1-K-HA, PB1-PA-K-HA, HA-PA-K-PB1, HA-PB1-K-PA, PA-K-PB1-HA, PB1-K-PA-HA, HA-K-PA-K-PB1, HA-K-PB 1-K-PA, PA-K-PB1-K-HA, PB 1-K-P A-K-HA, HA-C-PA-PB1, HA-C-PB1-PA, PA-PB1-C-HA, PB1-PA-C-HA, HA-PA-C-PB1, HA-PB 1-C-PA, PA-C-PB1-HA, PB1-C-PA-HA, HA-C-PA-C-PB1, HA-C-PB 1-C-PA, PA-C-PB1-C-HA, PB1-C-PA-C-HA, HA-K-PA-C-PB1, HA-K-PB 1-C-PA, PA-C-PB1-K-HA, PB1-C-PA-K-HA, HA-C-PA-K-PB1, HA-C-PB 1-K-PA, PA-K-PB1-C-HA, PB 1-K-PA-C-HA, HA-K-PA-РВ2, НА-К-РВ2-РА, РА-РВ2-К-НА, РВ2-РА-К-НА, НА-РА-К-РВ2, НА-РВ2-К-РА, РА-К-РВ2-НА, РВ2-К-РА-НА, НА-К-РА-К-РВ2, НА-К-РВ2-К-РА, РА-К-РВ2-К-НА, РВ2-К-РА-К-НА, НА-С-РА-РВ2, НА-С-РВ2-РА, РА-РВ2-С-НА, РВ2-РА-С-НА, НА-РА-С-РВ2, НА-РВ2-С-РА, РА-С-РВ2-НА, РВ2-С-РА-НА, НА-С-РА-С-РВ2, НА-С-РВ2-С-РА, РА-С-РВ2-С-НА, РВ2-С-РА-С-НА, НА-К-РА-С-РВ2, НА-К-РВ2-С-РА, РА-С-РВ2-К-НА, РВ2-С-РА-К-НА, НА-С-РА-К-РВ2, НА-С-РВ2-К-РА, РА-К-РВ2-С-НА, РВ2-К-РА-С-НА, НА-К-РА-PB1F2, HA-K-PB 1F2-PA, ΡΑ-PB 1F2-K-HA, PB 1F2-PA-K-HA, НА-РА-К-PB1F2, НА-PB1F2-K-PA, РА-К-PB1F2-HA, PB 1F2-K-PA-HA, НА-К-РА-К-PB1F2, HA-K-PB 1F2-K-PA, ΡА-К-PB1F2-K-FÍA, PB 1F2-K-PA-К-НА, НА-С-РА-PB1F2, HA-C-PB1F2-PA, PA-PB1F2-C-НА, PB1F2-PA-C-HA, HA-PA-C-PB1F2, HA-PB1F2-C-PA, РА-С-PB1F2-HA, PB1F2-C-PA-НА, НА-С-РА-С-PB1F2, HA-C-PB 1F2-C-PA, РА-С-РВ 1F2-C-HA, PB 1F2-C-PA-C-HA, НА-K-PA-C-PB1F2, HA-K-PB 1F2-C-PA, РА-С-РВ 1F2-K-HA, PB 1F2-C-PA-К-НА, НА-С-РА-К-PB1F2, HA-C-PB 1F2-K-PA, РА-К-РВ 1F2-C-HA, PB 1F2-K-PA-С-НА, НА-К-РВ1, РВ1-К-НА, НА-К-РВ1-РВ1, РВ1-РВ1-К-НА, НА-РВ1-К-РВ1, РВ1-К-РВ1-НА, H А-К-РВ 1 -К-РВ1, PB 1 -К-РВ1 -К-НА, НА-С-РВ1, РВ1-С-НА, НА-С-РВ1-РВ1, РВ1-РВ1-С-НА, НА-РВ1-С-РВ1, PB 1-С-РВ 1-НА, HA-C-PB 1 -С-РВ1, PB 1 -С-РВ1 -С-НА, НА-К-РВ1 -С-РВ1, РВ1-С-РВ1-К-НА, HA-C-PB 1 -К-РВ 1, PB 1-К-РВ 1-С-НА, HA-K-PB 1-РВ2, НА-К-РВ2-РВ1, РВ1-РВ2-К-НА, РВ2-РВ1-К-НА, НА-РВ1-К-РВ2, НА-РВ2-К-РВ1, РВ1-К-РВ2-НА, РВ2-К-РВ1-НА, HA-K-PB 1-К-РВ2, НА-К-РВ2-К-РВ1, PB 1-К-РВ2-К-НА, РВ2-К-РВ1 -К-НА, НА-С-РВ1-РВ2, НА-С-РВ2-РВ1, РВ1-РВ2-С-НА, РВ2-РВ1-С-НА, НА-РВ1-С-РВ2, НА-РВ2-С-РВ1, РВ1-С-РВ2-НА, РВ2-С-РВ1-НА, HA-C-PB 1-С-РВ2, НА-С-РВ2-С-РВ1, РВ1-С-РВ2-С-НА, РВ2-С-РВ1 -С-НА, HA-K-PB 1-С-РВ2, НА-К-РВ2-С-РВ1, PB 1-С-РВ2-К-НА, РВ2-С-РВ1-К-НА, HA-C-PB 1-К-РВ2, НА-С-РВ2-К-РВ1, PB 1-К-РВ2-С-НА, РВ2-К-РВ1 -С-НА, НА-К-PB1-PB1F2, HA-K-PB 1F2-PB1, PB 1 -PB 1F2-K-HA, PB 1F2-PB1 -К-НА, HA-PB 1-К-РВ 1F2, HA-PB 1F2-K-PB1, PB 1 -К-РВ 1F2-HA, PB 1F2-K-PB1 -НА, HA-K-PB 1-К-РВ 1F2, НА-К-PB1F2-K-PB1, PB 1 -К-РВ 1F2-K-HA, PB 1F2-K-PB1 -К-НА, HA-C-PB 1 -PB 1F2, HA-C-PB1F2-РВ1, PB1-PB1F2-C-HA, PB1F2-PB1-C-HA, HA-PB 1-С-РВ 1F2, HA-PB 1F2-C-PB1, РВ1-С-PB1F2-HA, PB 1F2-C-PB1 -HA, HA-C-PB 1-C-PB1F2, HA-C-PB 1F2-C-PB1, PB1-C-PB1F2-C-HA, PB 1F2-C-PB1 -C-HA, HA-K-PB 1-C-PB 1F2, HA-K-PB 1F2-C-PB1, PB 1 -C-PB 1F2-K-HA, PB 1F2-C-PB1-K-HA, HA-C-PB 1-K-PB1F2, HA-C-PB 1F2-K-PB1, PB 1 -K-PB1F2-C-HA, PB 1F2-K-PB1 -С-НА, HA-K-PB2, PB2-K-HA, HA-K-PB2-PB2, PB2-PB2-K-HA, HA-PB2-K-PB2, PB2-K-PB2-HA, HA-K-PB2-K-PB2, PB2-K-PB2-K-HA, HA-C-PB2, PB2-C-HA, HA-C-PB2-PB2, PB2-PB2-C-HA, HA-PB2-C-PB2, PB2-C-PB2-HA, HA-C-PB2-C-PB2, PB2-C-PB2-C-HA, HA-K-PB2-C-PB2, PB2-C-PB2-K-HA, HA-C-PB2-K-PB2, PB2-K-PB2-C-HA, HA-K-PB2-PB1F2, HA-K-PB 1F2-PB2, PB2-PB1F2-K-HA, PB 1F2-PB2-K-HA, HA-PB2-K-PB1F2, НА-РВ 1F2-K-PB2, РВ2-К-PB1F2-HA, PB 1F2-K-PB2-HA, НА-К-РВ2-К-PB1F2, НА-К-РВ 1F2-K-PB2, РВ2-К-PB1F2-K-HA, PB 1F2-K-PB2-K-HA, НА-С-РВ2-PB1F2, НА-С-РВ 1F2-РВ2, РВ2-PB1F2-C-HA, PB 1F2-PB2-C-HA, НА-РВ2-С-PB1F2, НА-РВ 1F2-C-PB2, РВ2-С-PB1F2-HA, PB 1F2-C-PB2-HA, НА-С-РВ2-С-PB1F2, НА-С-РВ 1F2-C-PB2, PB2-C-PB1F2-C-НА, PB 1F2-C-PB2-C-HA, НА-К-РВ2-С-PB1F2, НА-К-РВ 1F2-C-PB2, РВ2-С-PB1F2-K-HA, PB 1F2-C-PB2-K-HA, НА-С-РВ2-К-PB1F2, НА-С-РВ 1F2-K-PB2, РВ2-К-PB1F2-C-HA, PB 1F2-K-PB2-C-HA, НА-К-РВ 1F2, PB1F2-K-HA, НА-К-РВ 1F2-PB1F2, PB1F2-PB1F2-K-НА, НА-РВ 1F2-K-PB1F2, PB 1F2-K-PB1F2-HA, НА-К-РВ 1F2-K-PB1F2, PB1F2-K-PB1F2-К-НА, НА-С-РВ 1F2, PB1F2-C-HA, НА-С-РВ 1F2-PB1F2, PB 1F2-PB1F2-C-HA, НА-РВ 1F2-C-PB1F2, PB 1F2-C-PB1F2-HA, HA-C-PB1F2-C-PB1F2, PB 1F2-C-PB1F2-C-HA, НА-К-РВ 1F2-C-PB1F2, PB 1F2-C-PB1F2-K-HA, НА-С-РВ 1F2-K-PB1F2, PB 1F2-K-PB1F2-C-HA, NA-K-NP, NP-K-NA, NA-K-NP-NP, NP-NP-K-NA, NA-NP-K-NP, NP-K-NP-NA, NA-K-NP-K-NP, NP-K-NP-K-NA, NA-C-NP, NP-C-NA, NA-C-NP-NP, NP-NP-C-NA, NA-NP-C-NP, NP-C-NP-NA, NA-C-NP-C-NP, NP-C-NP-C-NA, NA-K-NP-C-NP, NP-C-NP-K-NA, NA-C-NP-K-NP, NP-K-NP-C-NA, NA-K-NP-M1, NA-K-M1-NP, NP-M1-K-NA, M1-NP-K-NA, NA-NP-K-M1, NA-M1-K-NP, NP-K-M1-NA, M1-K-NP-NA, NA-K-NP-K-M1, NA-K-M1-K-NP, NP-K-M1-K-NA, M1-K-NP-K-NA, NA-C-NP-M1, NA-C-M1-NP, NP-M1-C-NA, M1-NP-C-NA, NA-NP-C-M1, NA-M1-C-NP, NP-C-M1-NA, M1-C-NP-NA, NA-C-NP-C-M1, NA-C-M1-C-NP, NP-C-M1-C-NA, M1-C-NP-C-NA, NA-K-NP-C-M1, NA-K-M1-C-NP, NP-C-M1-K-NA, M1-C-NP-K-NA, NA-C-NP-K-M1, NA-C-M1-K-NP, NP-K-M1-C-NA, M1-K-NP-C-NA, NA-K-NP-M2, NA-K-M2-NP, NP-M2-K-NA, M2-NP-K-NA, NA-NP-K-M2, NA-M2-K-NP, NP-K-M2-NA, M2-K-NP-NA, NA-K-NP-K-M2, NA-K-M2-K-NP, NP-K-M2-K-NA, M2-K-NP-K-NA, NA-C-NP-M2, NA-C-M2-NP, NP-M2-C-NA, M2-NP-C-NA, NA-NP-C-M2, NA-M2-C-NP, NP-C-M2-NA, M2-C-NP-NA, NA-C-NP-C-M2, NA-C-M2-C-NP, NP-C-M2-C-NA, M2-C-NP-C-NA, NA-K-NP-C-M2, NA-K-M2-C-NP, NP-C-M2-K-NA, M2-C-NP-K-NA, NA-C-NP-K-M2, NA-C-M2-K-NP, NP-K-M2-C-NA, M2-K-NP-C-NA, NA-K-NP-NS1, NA-K-NS1-NP, NP-NS1-K-NA, NS1-NP-K-NA, NA-NP-K-NS1, NA-NS1-K-NP, NP-K-NS1-NA, NS1-K-NP-NA, NA-K-NP-K-NS1, NA-K-NS1-K-NP, NP-K-NS1-K-NA, NS1-K-NP-K-NA, NA-C-NP-NS1, NA-C-NS1-NP, NP-NS1-C-NA, NSI-NP-C-NA, NA-NP-C-NS1, NA-NS1-C-NP, NP-C-NS1-NA, NS1-C-NP-NA, NA-C-NP-C-NS1, NA-C-NS1-C-NP, NP-C-NS1-C-NA, NS1-C-NP-C-NA, NA-K-NP-C-NS1, NA-K-NS1-C-NP, NP-C-NS1-K-NA, NS1-C-NP-K-NA, NA-C-NP-K-NS1, NA-C-NS1-K-NP, NP-K-NS1-C-NA, NS1-K-NP-C-NA, NA-K-NP-NS2/NEP, NA-K-NS2/NEP-NP, NP-NS2/NEP-K-NA, NS2/NEP-NP-K-NA, NA-NP-K-NS2/NEP, NA-NS2/NEP-K-NP, NP-K-NS2/NEP-NA, NS2/NEP-K-NP-NA, NA-K-NP-K-NS2/NEP, NA-K-NS2/NEP-K-NP, NP-K-NS2/NEP-K-NA, NS2/NEP-K-NP-K-NA, NA-C-NP-NS2/NEP, NA-C-NS2/NEP-NP, NP-NS2/NEP-C-NA, NS2/NEP-NP-C-NA, NA-NP-C-NS2/NEP, NA-NS2/NEP-C-NP, NP-C-NS2/NEP-NA, NS2/NEP-C-NP-NA, NA-C-NP-C-NS2/NEP, NA-C-NS2/NEP-C-NP, NP-C-NS2/NEP-C-NA, NS2/NEP-C-NP-C-NA, NA-K-NP-C-NS2/NEP, NA-K-NS2/NEP-C-NP, NP-C-NS2/NEP-K-NA, NS2/NEP-C-NP-K-NA, NA-C-NP-K-NS2/NEP, NA-C-NS2/NEP-K-NP, NP-K-NS2/NEP-C-NA, NS2/NEP-K-NP-C-NA, NA-K-NP-PA, NA-K-PA-NP, NP-PA-K-NA, PA-NP-K-NA, NA-NP-K-PA, NA-PA-K-NP, NP-K-PA-NA, PA-K-NP-NA, NA-K-NP-K-PA, NA-K-PA-K-NP, NP-K-PA-K-NA, PA-K-NP-K-NA, NA-C-NP-PA, NA-C-PA-NP, NP-PA-C-NA, PA-NP-C-NA, NA-NP-C-PA, NA-PA-C-NP, NP-C-PA-NA, PA-C-NP-NA, NA-C-NP-C-PA, NA-C-PA-C-NP, NP-C-PA-C-NA, PA-C-NP-C-NA, NA-K-NP-C-PA, NA-K-PA-C-NP, NP-C-PA-K-NA, PA-C-NP-K-NA, NA-C-NP-K-PA, NA-C-PA-K-NP, NP-K-PA-C-NA, PA-K-NP-C-NA, NA-K-NP-PB1, NA-K-PB1-NP, NP-PB1-K-NA, PB1-NP-K-NA, NA-NP-K-PB1, NA-PB 1-K-NP, NP-K-PB1-NA, PB1-K-NP-NA, NA-K-NP-K-PB1, NA-K-PB1-K-NP, NP-K-PB1-K-NA, PB1-K-NP-K-NA, NA-C-NP-PB1, NA-C-PB1-NP, NP-PB1-C-NA, PB1-NP-C-NA, NA-NP-C-PB1, NA-PB1-C-NP, NP-C-PB1-NA, PB1-C-NP-NA, NA-C-NP-C-PB1, NA-C-PB1-C-NP, NP-C-PB1-C-NA, PB1-C-NP-C-NA, NA-K-NP-C-PB1, NA-K-PB1-C-NP, NP-C-PB1-K-NA, PB1-C-NP-K-NA, NA-C-NP-K-PB1, NA-C-PB1-K-NP, NP-K-PB1-C-NA, PB1-K-NP-C-NA, NA-K-NP-PB2, NA-K-PB2-NP, NP-PB2-K-NA, PB2-NP-K-NA, NA-NP-K-PB2, NA-PB2-K-NP, NP-K-PB2-NA, PB2-K-NP-NA, NA-K-NP-K-PB2, NA-K-PB2-K-NP, NP-K-PB2-K-NA, PB2-K-NP-K-NA, NA-C-NP-PB2, NA-C-PB2-NP, NP-PB2-C-NA, PB2-NP-C-NA, NA-NP-C-PB2, NA-PB2-C-NP, NP-C-PB2-NA, PB2-C-NP-NA, NA-C-NP-C-PB2, NA-C-PB2-C-NP, NP-C-PB2-C-NA, PB2-C-NP-C-NA, NA-K-NP-C-PB2, NA-K-PB2-C-NP, NP-C-PB2-K-NA, PB2-C-NP-K-NA, NA-C-NP-K-PB2, NA-C-PB2-K-NP, NP-K-PB2-C-NA, PB2-K-NP-C-NA, NA-K-NP-PB1F2, NA-K-PB1F2-NP, NP-PB1F2-K-NA, PB 1F2-NP-K-NA, NA-NP-K-PB1F2, NA-PB1F2-K-NP, NP-K-PB1F2-NA, PB 1F2-K-NP-NA, NA-K-NP-K-PB1F2, NA-K-PB1F2-K-NP, NP-K-PB1F2-K-NA, PB1F2-K-NP-K-NA, NA-C-NP-PB1F2, NA-C-PB1F2-NP, NP-PB1F2-C-NA, PB1F2-NP-C-NA, NA-NP-C-PB1F2, NA-PB 1F2-C-NP, NP-C-PB1F2-NA, PB1F2-C-NP-NA, NA-C-NP-C-PB1F2, NA-C-PB 1F2-C-NP, NP-C-PB1F2-C-NA, PB 1F2-C-NP-C-NA, NA-K-NP-C-PB1F2, NA-K-PB 1F2-C-NP, NP-C-PB 1F2-K-NA, PB 1F2-C-NP-K-NA, NA-C-NP-K-PB1F2, NA-C-PB 1F2-K-NP, NP-K-PB1F2-C-NA, PB 1F2-K-NP-C-NA, NA-K-M1, M1-K-NA, NA-K-M1-M1, M1-M1-K-NA, NA-M1-K-M1, M1-K-M1-NA, NA-K-M1-K-M1, M1-K-M1-K-NA, NA-C-M1, M1-C-NA, NA-C-M1-M1, M1-M1-C-NA, NA-M1-C-M1, M1-C-M1-NA, NA-C-M1-C-M1, M1-C-Ml-C-NA, NA-K-M1-C-M1, M1-C-M1-K-NA, NA-C-M1-K-M1, M1-K-M1-C-NA, NA-K-M1-M2, NA-K-M2-M1, M1-M2-K-NA, M2-M1-K-NA, NA-M1-K-M2, NA-M2-K-M1, M1-K-M2-NA, M2-K-M1-NA, NA-K-M1-K-M2, NA-K-M2-K-M1, M1-K-M2-K-NA, M2-K-M1-K-NA, NA-С-М1-М2, NA-C-M2-M1, M1-M2-C-NA, M2-M1-C-NA, NA-M1-C-M2, NA-M2-C-M1, Ml-C-M2-NA, M2-C-M1-NA, NA-C-M1-C-M2, NA-C-M2-C-M1, M1-C-M2-C-NA, M2-C-M1-C-NA, NA-K-M1-C-M2, NA-K-M2-C-M1, M1-C-M2-K-NA, M2-C-M1-K-NA, NA-C-M1-K-M2, NA-C-M2-K-M1, M1-K-M2-C-NA, M2-K-M1-C-NA, NA-K-M1-NS1, NA-K-NS1-M1, Ml-NS1-K-NA, NS1-M1-K-NA, NA-M1-K-NS1, NA-NS1-K-M1, M1-K-NS1-NA, NS1-K-M1-NA, NA-K-M1-K-NS1, NA-K-NS1-K-M1, M1-K-NS1-K-NA, NS1-K-M1-K-NA, NA-C-M1-NS1, NA-C-NS1-M1, M1-NS1-C-NA, NS1-M1-C-NA, NA-M1-C-NS1, NA-NS1-C-M1, Ml-C-NS1-NA, NS1-C-M1-NA, NA-C-M1-C-NS1, NA-C-NS1-C-M1, M1-C-NS1-C-NA, NS1-C-Ml-C-NA, NA-K-M 1-C-NS1, NA-K-NS1-C-M1, M1-C-NS1-K-NA, NS1-C-M1-K-NA, NA-C-M1-K-NS1, NA-C-NS1-K-M1, M1-K-NS1-C-NA, NS1-K-M1-C-NA, NA-K-M1-NS2/NEP, NA-K-NS2/NEP-M1, M1-NS2/NEP-K-NA, NS2/NEP-M1 -K-NA, NA-M1-K-NS2/NEP, NA-NS2/NEP-K-M1, M1-K-NS2/NEP-NA, NS2/NEP-K-M1 -NA, NA-K-M 1-K-NS2/NEP, NA-K-NS2/NEP-K-M1, M1-K-NS2/NEP-K-NA, NS2/NEP-K-M1 -K-NA, NA-C-M1-NS2/NEP, NA-C-NS2/NEP-M1, M1-NS2/NEP-C-NA, NS2/NEP-M1 -C-N A, NA-M 1-C-NS2/NEP, NA-NS2/NEP-C-M1, M1-C-NS2/NEP-NA, NS2/NEP-C-M1 -NA, NA-C-M1-C-NS2/NEP, NA-C-NS2/NEP-C-M1, M1-C-NS2/NEP-C-NA, NS2/NEP-C-M1 -C-NA, NA-K-M 1-C-NS2/NEP, NA-K-NS2/NEP-C-M1, M1-C-NS2/NEP-K-NA, NS2/NEP-C-M1 -K-NA, NA-C-M1-K-NS2/NEP, NA-C-NS2/NEP-K-M1, M1-K-NS2/NEP-C-NA, NS2/NEP-K-M1 -C-NA, NA-K-M1-PA, NA-K-PA-M1, M1-PA-K-NA, PA-M1-K-NA, NA-M1-K-PA, NA-PA-K-M1, M1-K-PA-NA, PA-K-M1-NA, NA-K-M1-K-PA, NA-K-PA-K-M1, M1-K-PA-K-NA, PA-K-M1-K-NA, NA-C-M1-PA, NA-C-PA-M1, M1-PA-C-NA, PA-M1-C-NA, NA-M1-C-PA, NA-PA-C-M1, M1-C-PA-NA, PA-C-M1-NA, NA-C-M1-C-PA, NA-C-PA-C-M1, M1-C-PA-C-NA, PA-C-M1-C-NA, NA-K-M1-C-PA, NA-K-PA-C-M1, M1-C-PA-K-NA, PA-C-M1-K-NA, NA-C-M1-K-PA, NA-C-PA-K-M1, M1-K-PA-C-NA, PA-K-M1-C-NA, NA-K-M1-PB1, NA-K-PB1-M1, M1-PB1-K-NA, PB1-M1-K-NA, NA-M1-K-PB1, NA-PB1-K-M1, M1-K-PB1-NA, PB1-K-M1-NA, NA-K-M1-K-PB1, NA-K-PB1-K-M1, M1-K-PB1-K-NA, PB1-K-M1-K-NA, NA-C-M1-PB1, NA-C-PB1-M1, M1-PB1-C-NA, PB1-M1-C-NA, NA-M1-C-PB1, NA-PB1-C-M1, M1-C-PB1-NA, PB1-C-M1-NA, NA-C-M1-C-PB1, NA-C-PB1-C-M1, M1-C-PB1-C-NA, PB1-C-M1-C-NA, NA-K-M 1-C-PB1, NA-K-PB1-C-M1, M1-C-PB1-K-NA, PB1-C-M1-K-NA, NA-C-M 1-K-PB1, NA-C-PB1-K-M1, M1-K-PB1-C-NA, PB1-K-M1-C-NA, NA-K-M 1-PB2, NA-K-PB2-M1, Ml-PB2-K-NA, PB2-M1-K-NA, NA-M1-K-PB2, NA-PB2-K-M1, M1-K-PB2-NA, PB2-K-M1-NA, NA-K-M 1-K-PB2, NA-K-PB2-K-M1, M1-K-PB2-K-NA, PB2-K-M1 -K-NA, NA-C-M 1-PB2, NA-C-PB2-M1, M1-PB2-C-NA, PB2-M1-C-NA, NA-M1-C-PB2, NA-PB2-C-M1, M1-C-PB2-NA, PB2-C-M1-NA, NA-C-M 1-C-PB2, NA-C-PB2-C-M1, M1-C-PB2-C-NA, PB2-C-M1-C-NA, NA-K-M 1-C-PB2, NA-K-PB2-C-M1, M1-C-PB2-K-NA, PB2-C-M1-K-NA, NA-C-M1-K-РВ2, NA-С-РВ2-К-М1, Μ1-K-PB2-C-NA, PB2-K-M1-C-NA, NA-K-M1-PB1F2, ΝΑ-Κ-PB1F2-M1, M1-PB1F2-K-NA, PB 1F2-M1 -Κ-ΝΑ, NA-M1-K-PB1F2, NA-PB1F2-K-M1, Μ1-K-PB1F2-NA, PB1F2-K-M1-NA, ΝΑ-Κ-Μ1 -K-PB 1F2, ΝΑ-Κ-ΡΒ1F2-K-M1, M1-K-PB1F2-K-ΝΑ, PB 1F2-K-M1 -Κ-ΝΑ, NA-C-M1-PB1F2, NA-C-PB1F2-M1, M1-PB1F2-C-NA, PB1F2-Ml-C-NA, NA-M1-C-PB1F2, NA-PB1F2-C-M1, M1-C-PB1F2-NA, PB1F2-C-M1-NA, NA-C-M1-C-PB1F2, NA-C-PB1F2-C-M1, Μ1 -C-PB 1F2-C-NA, PB 1F2-C-M1-C-NA, ΝΑ-Κ-Μ 1-C-PB1F2, ΝΑ-Κ-ΡΒ 1F2-C-M1, Μ1 -C-PB 1F2-K-NA, PB 1F2-C-M1 -Κ-ΝΑ, NA-C-M1 -K-PB 1F2, ΝA-C-PB1F2-K-M1, Μ1-Κ-ΡΒ1F2-C-NA, PB 1F2-K-M1-C-NA, ΝΑ-Κ-Μ2, Μ2-Κ-ΝΑ, ΝΑ-Κ-Μ2-Μ2, Μ2-Μ2-Κ-ΝΑ, ΝΑ-Μ2-Κ-Μ2, Μ2-Κ-Μ2-ΝΑ, ΝΑ-Κ-Μ2-Κ-Μ2, Μ2-Κ-Μ2-Κ-ΝΑ, NA-C-M2, M2-C-NA, NA-C-M2-M2, M2-M2-C-NA, NA-M2-C-M2, M2-C-M2-NA, NA-C-M2-C-M2, M2-C-M2-C-NA, NA-K-M2-C-M2, M2-C-M2-K-NA, NA-C-M2-K-M2, Μ2-Κ-Μ2-C-NA, NA-K-M2-NS1, NA-K-NS1-M2, M2-NS1-K-NA, NS1-M2-K-NA, NA-M2-K-NS1, NANS 1-Κ-Μ2, M2-K-NS1-NA, NS1-K-M2-NA, NA-K-M2-K-NS1, NA-K-NS1-Κ-Μ2, Μ2-Κ-NS1-K-NA, NS1-K-M2-K-NA, NA-C-M2-NS1, NA-C-NS1-M2, M2-NS1-C-NA, NS1-M2-C-ΝΑ, NA-M2-C-NS1, NA-NS1-C-M2, M2-C-NS1-NA, NS1-C-M2-NA, NA-C-M2-C-NS1, ΝΑ-C-NS1-C-M2, M2-C-NS1-C-NA, NS1-C-M2-C-NA, NA-K-M2-C-NS1, NA-K-NS 1-C-M2, Μ2-C-NS1-K-NA, NS1-C-M2-K-NA, NA-C-M2-K-NS1, NA-C-NS1-Κ-Μ2, M2-K-NS1-C-NA, NS 1-K-M2-C-NA, NA-K-M2-NS2/NEP, NA-K-NS2/NEP-M2, M2-NS2/NEP-K-NA, NS2/NEP-M2-K-NA, NA-M2-K-NS2/NEP, NA-NS2/NEP-K-M2, M2-K-NS2/NEP-NA, NS2/NEP-K-M2-NA, NA-K-M2-K-NS2/NEP, NA-K-NS2/NEP-K-M2, M2-K-NS2/NEP-K-NA, NS2/NEP-K-M2-K-NA, NA-C-M2-NS2/NEP, NA-C-NS2/NEP-M2, M2-NS2/NEP-C-NA, NS2/NEP-M2-C-NA, NA-M2-C-NS2/NEP, NA-NS2/NEP-C-M2, M2-C-NS2/NEP-NA, NS2/NEP-C-M2-NA, NA-C-M2-C-NS2/NEP, NA-C-NS2/NEP-C-M2, M2-C-NS2/NEP-C-NA, NS2/NEP-C-M2-C-NA, NA-K-M2-C-NS2/NEP, NA-K-NS2/NEP-C-M2, M2-C-NS2/NEP-K-ΝΑ, NS2/NEP-C-M2-K-NA, NA-C-M2-K-NS2/NEP, NA-C-NS2/NEP-K-M2, Μ2-Κ-NS2/NEP-C-NA, NS2/NEP-K-M2-C-NA, ΝΑ-Κ-Μ2-ΡΑ, ΝΑ-Κ-ΡΑ-Μ2, Μ2-ΡΑ-Κ-ΝΑ, ΡΑ-Μ2-Κ-ΝΑ, ΝΑ-Μ2-Κ-ΡΑ, ΝΑ-ΡΑ-Κ-Μ2, Μ2-Κ-ΡΑ-ΝΑ, ΡΑ-Κ-Μ2-ΝΑ, ΝΑ-Κ-Μ2-Κ-ΡΑ, ΝΑ-Κ-ΡΑ-Κ-Μ2, Μ2-Κ-ΡΑ-Κ-ΝΑ, ΡΑ-Κ-Μ2-Κ-ΝΑ, NA-C-M2-PA, NA-C-PA-M2, Μ2-ΡΑ-C-NA, PA-M2-C-NA, NA-M2-C-PA, NA-PA-C-M2, M2-C-PA-NA, PA-C-M2-NA, NA-C-M2-C-PA, NA-C-PA-C-M2, M2-C-PA-C-NA, PA-C-M2-C-NA, NA-K-M2-C-PA, NA-K-PA-C-Μ2, M2-C-PA-K-NA, PA-C-M2-K-NA, NA-C-M2-K-PA, NA-C-PA-K-M2, M2-K-PA-C-NA, PA-K-M2-C-NA, ΝΑ-Κ-Μ2-ΡΒ1, ΝΑ-Κ-ΡΒ 1-Μ2, Μ2-ΡΒ1-Κ-ΝΑ, ΡΒ1-Μ2-Κ-ΝΑ, ΝΑ-Μ2-Κ-ΡΒ1, ΝΑ-ΡΒ1-Κ-Μ2, Μ2-Κ-ΡΒ1-ΝΑ, ΡΒ1-Κ-Μ2-ΝΑ, ΝΑ-Κ-Μ2-Κ-ΡΒ1, ΝΑ-Κ-ΡΒ 1-Κ-Μ2, Μ2-Κ-ΡΒ1 -Κ-ΝΑ, PB 1-Κ-Μ2-Κ-ΝΑ, NA-C-M2-PB1, NA-C-PB 1-Μ2, M2-PB1-C-NA, PB1-M2-C-NA, NA-M2-C-PB1, NA-PB1-C-M2, M2-C-PB1-NA, PB1-C-M2-NA, NA-C-M2-С-РВ1, NA-C-PB1-C-M2, M2-C-PB1-C-NA, PB1-C-M2-C-NA, NA-K-M2-C-PB1, NA-K-PB1-C-M2, M2-C-PB1-K-NA, PB 1-C-M2-K-NA, NA-C-M2-K-PB1, NA-C-PB1-K-M2, M2-K-PB1-C-NA, PB1-K-M2-C-NA, NA-K-M2-PB2, NA-K-PB2-M2, M2-PB2-K-NA, PB2-M2-K-NA, NA-M2-K-PB2, NA-PB2-K-M2, M2-K-PB2-NA, PB2-K-M2-NA, NA-K-M2-K-PB2, NA-K-PB2-K-M2, M2-K-PB2-K-NA, PB2-K-M2-K-NA, NA-C-M2-PB2, NA-C-PB2-M2, M2-PB2-C-NA, PB2-M2-C-NA, NA-M2-C-PB2, NA-PB2-C-M2, M2-C-PB2-NA, PB2-C-M2-NA, NA-C-M2-C-PB2, NA-C-PB2-C-M2, M2-C-PB2-C-NA, PB2-C-M2-C-NA, NA-K-M2-C-PB2, NA-K-PB2-C-M2, M2-C-PB2-K-NA, PB2-C-M2-K-NA, NA-C-M2-K-PB2, NA-C-PB2-K-M2, M2-K-PB2-C-NA, PB2-K-M2-C-NA, NA-K-M2-PB1F2, NA-K-PB1F2-M2, M2-PB1F2-K-NA, PB 1F2-M2-K-NA, NA-M2-K-PB1F2, NA-PB1F2-K-M2, M2-K-PB1F2-NA, PB 1F2-K-M2-N A, NA-K-M2-K-PB1F2, NA-K-PB 1F2-K-M2, M2-K-PB1F2-K-NA, PB 1F2-K-M2-K-NA, NA-C-M2-PB1F2, NA-C-PB1F2-M2, M2-PB1F2-C-NA, PB1F2-M2-C-NA, NA-M2-C-PB1F2, NA-PB1F2-C-M2, M2-C-PB1F2-NA, PB1F2-C-M2-NA, NA-C-M2-C-PB1F2, NA-C-PB1F2-C-M2, M2-C-PB1F2-C-NA, PB 1F2-C-M2-C-NA, NA-K-M2-C-PB1F2, NA-K-PB 1F2-C-M2, M2-C-PB1F2-K-NA, PB 1F2-C-M2-K-NA, NA-C-M2-K-PB1F2, NA-C-PB 1F2-K-M2, M2-K-PB1F2-C-NA, PB1F2-K-M2-C-NA, NA-K-NS1, NS1-K-NA, NA-K-NS1-NS1, NS1-NS1-K-NA, NA-NS1-K-NS1, NS1-K-NS1-NA, NA-K-NS 1-K-NS1, NS1-K-NS 1-K-NA, NA-C-NS1, NS1-C-NA, NA-C-NS1-NS1, NS1-NS1-C-NA, NA-NS1-C-NS1, NS1-C-NS1-NA, NA-C-NS1-C-NS1, NS1-C-NS1-C-NA, NA-K-NS1-C-NS1, NS1-C-NS 1-K-NA, NA-C-NS1-K-NS1, NS1-K-NS1-C-NA, NA-K-NS1-NS2/NEP, NA-K-NS2/NEP-NS1, NS 1-NS2/NEP-K-NA, NS2/NEP-NS 1-K-NA, NA-NS1-K-NS2/NEP, NA-NS2/NEP-K-NS1, NS 1-K-NS2/NEP-NA, NS2/NEP-K-NSΙΝΑ, NA-K-NS 1-K-NS2/NEP, NA-K-NS2/NEP-K-NS1, NS 1-K-NS2/NEP-K-NA, NS2/NEP-K-NS1-K-NA, NA-C-NS1-NS2/NEP, NA-C-NS2/NEP-NS1, NS 1-NS2/NEP-C-NA, NS2/NEP-NS1-C-NA, NA-NS 1-C-NS2/NEP, NA-NS2/NEP-C-NS1, NS 1-C-NS2/NEP-NA, NS2/NEP-C-NS1-NA, NA-C-NS 1-C-NS2/NEP, NA-C-NS2/NEP-C-NS1, NS 1-C-NS2/NEP-C-NA, NS2/NEP-C-NS1 -C-NA, NA-K-NS 1-C-NS2/NEP, NA-K-NS2/NEP-C-NS1, NS 1-C-NS2/NEP-K-NA, NS2/NEP-C-NS 1-K-NA, NA-C-NS 1-K-NS2/NEP, NA-C-NS2/NEP-K-NS1, NS1-K-NS2/NEP-C-NA, NS2/NEP-K-NS1 -C-NA, NA-K-NS 1-PA, NA-K-PA-NS1, NS1-PA-K-NA, PA-NS1-K-NA, NA-NS1-K-PA, NA-PA-K-NS1, NS1-K-PA-NA, PA-K-NS1-NA, NA-K-NS1-K-PA, NA-K-PA-K-NS1, NS 1-K-PA-K-NA, ΡA-K-NS 1-K-NA, NA-C-NS1-PA, NA-C-PA-NS1, NS1-PA-C-NA, PA-NS1-C-NA, NA-NS1-C-PA, NA-PA-C-NS1, NS1-C-PA-NA, PA-C-NS1-NA, NA-C-NS 1-C-PA, NA-C-PA-C-NS1, NS1-C-PA-C-NA, PA-C-NS1-C-NA, NA-K-NS 1-C-PA, NA-K-PA-C-NS1, NS1-C-PA-K-NA, PA-C-NS 1-K-NA, NA-C-NS 1-K-PA, NA-C-PA-K-NS1, NS1-K-PA-C-NA, PA-K-NS1-C-NA, NA-K-NS1-PB1, NA-K-PB1-NS1, NS1-PB1-K-NA, PB 1-NS 1-K-NA, NA-NS 1-K-PB1, NA-PB 1-K-NS1, NS1-K-PB1-NA, PB1-K-NS1-NA, NA-K-NS1-K-PB1, NA-K-PB1-K-NS1, NS1-K-PB1-K-NA, PB1-K-NS1-K-NA, NA-C-NS1-PB1, NA-C-PB 1-NS1, NS1-PB1-C-NA, PB1-NS1-C-NA, NA-NS1-C-PB1, NA-PB1-C-NS1, NS1-C-PB1-NA, PB1-C-NS1-NA, NA-C-NS1-C-PB1, NA-C-PB1-C-NS1, NS1-C-PB1-C-NA, PB1-C-NS1-C-NA, NA-K-NS1-C-PB1, NA-K-PB 1-C-NS1, NS1-C-PB1-K-NA, PB1-C-NS1-K-NA, NA-C-NS 1-K-PB 1, NA-C-PB1-K-NS1, NS1-K-PB1-C-NA, PB1-K-NS1-C-NA, NA-K-NS 1-PB2, NA-K-PB2-NS1, NS1-PB2-K-NA, PB2-NS1-K-NA, NA-NS1-K-PB2, NA-PB2-K-NS1, NS1-K-PB2-NA, PB2-K-NS1-NA, NA-K-NS1-K-PB2, NA-K-PB2-K-NS1, NS1-K-PB2-K-NA, PB2-K-NS1 -K-NA, NA-C-NS 1-PB2, NA-C-PB2-NS1, NS1-PB2-C-NA, PB2-NS1-C-NA, NA-NS1-C-PB2, NA-PB2-C-NS1, NS1-C-PB2-NA, PB2-C-NS1-NA, NA-C-NS1-C-PB2, NA-C-PB2-C-NS1, NS 1-C-PB2-C-NA, PB2-C-NS1 -C-NA, NA-K-NS 1-C-PB2, NA-K-PB2-C-NS1, NS 1-C-PB2-K-NA, PB2-C-NS1 -K-NA, NA-C-NS 1-K-PB2, NA-C-PB2-K-NS1, NS1-K-PB2-C-NA, PB2-K-NS1 -C-NA, NA-K-NS 1-PB 1F2, NA-K-PB1F2-NS1, NS 1 -PB 1F2-K-NA, PB 1F2-NS1 -K-NA, NA-NS1 -K-PB1F2, NA-PB1F2-K-NS1, NS 1 -K-PB1F2-NA, PB1F2-K-NS1-NA, NA-K-NS 1-K-PB1F2, N A-K-PB 1F2-K-NS1, NS 1 -K-PB 1F2-K-NA, PB1F2-K-NS1-K-NA, NA-C-NS 1-PB 1F2, NA-C-PB1F2-NS1, NS 1 -PB 1F2-C-NA, PB 1F2-NS1 -C-NA, NA-NS1-C-PB1F2, NA-PB 1F2-C-NS1, NS 1 -C-PB1F2-NA, PB 1F2-C-NS1 -NA, NA-C-NS1-C-PB1F2, NA-C-PB 1F2-C-NS1, NS 1 -C-PB 1F2-C-NA, PB1F2-C-NS1-C-NA, NA-K-NS1-C-PB1F2, NA-K-PB1F2-C-NS1, NS 1 -C-PB 1F2-K-NA, PB 1F2-C-NS1 -K-NA, NA-C-NS1-K-PB1F2, NA-C-PB 1F2-K-NS1, NS 1 -K-PB 1F2-C-NA, PB 1F2-K-NS1 -C-NA, NA-K-NS2/NEP, NS2/NEP-K-NA, NA-K-NS2/NEP-NS2/NEP, NS2/NEP-NS2/NEP-K-NA, NA-NS2/NEP-K-NS2/NEP, NS2/NEP-K-NS2/NEP-NA, NA-K-NS2/NEP-K-NS2/NEP, NS2/NEP-K-NS2/NEP-K-NA, NA-C-NS2/NEP, NS2/NEP-C-NA, NA-C-NS2/NEP-NS2/NEP, NS2/NEP-NS2/NEP-C-NA, NA-NS2/NEP-C-NS2/NEP, NS2/NEP-C-NS2/NEP-NA, NA-C-NS2/NEP-C-NS2/NEP, NS2/NEP-C-NS2/NEP-C-NA, NA-K-NS2/NEP-C-NS2/NEP, NS2/NEP-C-NS2/NEP-K-NA, NA-C-NS2/NEP-K-NS2/NEP, NS2/NEP-K-NS2/NEP-C-NA, NA-K-NS2/NEP-PA, NA-K-PA-NS2/NEP, NS2/NEP-PA-K-NA, PA-NS2/NEP-K-NA, NA-NS2/NEP-K-PA, NA-PA-K-NS2/NEP, NS2/NEP-K-PA-NA, PA-K-NS2/NEP-NA, NA-K-NS2/NEP-K-PA, NA-K-PA-K-NS2/NEP, NS2/NEP-K-PA-K-NA, PA-K-NS2/NEP-K-NA, NA-C-NS2/NEP-PA, NA-C-PA-NS2/NEP, NS2/NEP-PA-C-NA, PA-NS2/NEP-C-NA, NA-NS2/NEP-C-PA, NA-PA-C-NS2/NEP, NS2/NEP-C-PA-NA, PA-C-NS2/NEP-NA, NA-C-NS2/NEP-C-PA, NA-C-PA-C-NS2/NEP, NS2/NEP-C-PA-C-NA, PA-C-NS2/NEP-C-NA, NA-K-NS2/NEP-C-PA, NA-K-PA-C-NS2/NEP, NS2/NEP-C-PA-K-NA, PA-C-NS2/NEP-K-NA, NA-C-NS2/NEP-K-PA, NA-C-PA-K-NS2/NEP, NS2/NEP-K-PA-C-NA, PA-K-NS2/NEP-C-NA, NA-K-NS2/NEP-PB1, NA-K-PB 1-NS2/NEP, NS2/NEP-PB1 -K-NA, PB 1-NS2/NEP-K-NA, NA-NS2/NEP-K-PB1, NA-PB 1-K-NS2/NEP, NS2/NEP-K-PB1 -NA, PB 1-K-NS2/NEP-NA, NA-K-NS2/NEP-K-PB1, NA-К-РВ 1-K-NS2/NEP, NS2/NEP-K-PB1 -K-NA, PB 1-K-NS2/NEP-K-NA, NA-C-NS2/NEP-PB1, NA-C-PB1-NS2/NEP, NS2/NEP-PB1 -C-NA, PB 1-NS2/NEP-C-NA, NA-NS2/NEP-C-PB1, NA-PB1-C-NS2/NEP, NS2/NEP-C-PB1 -NA, PB 1-C-NS2/NEP-NA, NA-C-NS2/NEP-C-PB1, NA-C-PB 1-C-NS2/NEP, NS2/NEP-C-PB1 -C-NA, PB 1-C-NS2/NEP-C-NA, NA-K-NS2/NEP-C-PB1, NA-K-PB1-C-NS2/NEP, NS2/NEP-C-PB1 -K-NA, PB 1-C-NS2/NEP-K-NA, NA-C-NS2/NEP-K-PB1, NA-C-PB 1-K-NS2/NEP, NS2/NEP-K-PB1 -C-NA, PB 1-K-NS2/NEP-C-NA, NA-K-NS2/NEP-PB2, NA-K-PB2-NS2/NEP, NS2/NEP-PB2-K-NA, PB2-NS2/NEP-K-NA, NA-NS2/NEP-K-PB2, NA-PB2-K-NS2/NEP, NS2/NEP-K-PB2-NA, PB2-K-NS2/NEP-NA, NA-K-NS2/NEP-K-PB2, NA-K-PB2-K-NS2/NEP, NS2/NEP-K-PB2-K-NA, PB2-K-NS2/NEP-K-NA, NA-C-NS2/NEP-PB2, NA-C-PB2-NS2/NEP, NS2/NEP-PB2-C-NA, PB2-NS2/NEP-C-NA, NA-NS2/NEP-C-PB2, NA-PB2-C-NS2/NEP, NS2/NEP-C-PB2-NA, PB2-C-NS2/NEP-NA, NA-C-NS2/NEP-C-PB2, NA-C-PB2-C-NS2/NEP, NS2/NEP-C-PB2-C-NA, PB2-C-NS2/NEP-C-NA, NA-K-NS2/NEP-C-PB2, NA-K-PB2-C-NS2/NEP, NS2/NEP-C-PB2-K-NA, PB2-C-NS2/NEP-K-NA, NA-C-NS2/NEP-K-PB2, NA-C-PB2-K-NS2/NEP, NS2/NEP-K-PB2-C-NA, PB2-K-NS2/NEP-C-NA, NA-K-NS2/NEP-PB1F2, NA-K-PB 1F2-NS2/NEP, NS2/NEP-PB1F2-K-NA, PB 1F2-NS2/NEP-K-NA, NA-NS2/NEP-K-PB1F2, NA-PB1F2-K-NS2/NEP, NS2/NEP-K-PB1F2-NA, PB 1F2-K-NS2/NEP-NA, NA-K-NS2/NEP-K-PB1F2, NA-K-PB 1F2-K-NS2/NEP, NS2/NEP-K-PB1F2-K-NA, PB 1F2-K-NS2/NEP-K-NA, NA-C-NS2/NEP-PB1F2, NA-C-PB 1F2-NS2/NEP, NS2/NEP-PB1F2-C-NA, PB 1F2-NS2/NEP-C-NA, NA-NS2/NEP-C-PB1F2, NA-PB 1F2-C-NS2/NEP, NS2/NEP-C-PB1F2-NA, PB 1F2-C-NS2/NEP-NA, NA-C-NS2/NEP-C-PB1F2, NA-C-PB 1F2-C-NS2/NEP, NS2/NEP-C-PB1F2-C-NA, PB1F2-C-NS2/NEP-C-NA, NA-K-NS2/NEP-C-PB1F2, NA-K-PB 1F2-C-NS2/NEP, NS2/NEP-C-PB1F2-K-NA, PB 1F2-C-NS2/NEP-K-NA, NA-C-NS2/NEP-K-PB1F2, NA-C-PB 1F2-K-NS2/NEP, NS2/NEP-K-PB1F2-C-NA, PB 1F2-K-NS2/NEP-C-NA, NA-K-PA, PA-K-NA, NA-K-PA-PA, PA-PA-K-NA, NA-PA-K-PA, PA-K-PA-NA, NA-K-PA-K-PA, PA-K-PA-K-NA, NA-C-PA, PA-C-NA, NA-C-PA-PA, PA-PA-C-NA, NA-PA-C-PA, PA-C-PA-NA, NA-C-PA-C-PA, PA-C-PA-C-NA, NA-K-PA-C-PA, PA-C-PA-K-NA, NA-C-PA-K-PA, PA-K-PA-C-NA, NA-K-PA-PB1, NA-K-PB 1-PA, PA-PB1-K-NA, PB 1-PA-K-NA, NA-PA-K-PB1, NA-PB1-K-PA, PA-K-PB1-NA, PB1-K-PA-NA, NA-K-PA-K-PB1, NA-K-PB 1-K-PA, PA-K-PB1-K-NA, PB1-K-PA-K-NA, NA-C-PA-PB1, NA-C-PB1-PA, PA-PB1-C-NA, PB1-PA-C-NA, NA-PA-C-PB1, NA-PB1-C-PA, PA-C-PB1-NA, PB1-C-PA-NA, NA-C-PA-C-PB1, NA-C-PB 1-C-P A, PA-C-PB1-C-NA, PB1-C-PA-C-NA, NA-K-PA-C-PB1, NA-K-PB 1-C-PA, PA-C-PB1-K-NA, PB1-C-PA-K-NA, NA-C-PA-K-PB1, NA-C-PB 1-K-P A, PA-K-PB1-C-NA, PB 1-K-P A-C-NA, NA-K-PA-PB2, NA-K-PB2-PA, PA-PB2-K-NA, PB2-PA-K-NA, NA-PA-K-PB2, NA-PB2-K-PA, PA-K-PB2-NA, PB2-K-PA-NA, NA-K-PA-K-PB2, NA-K-PB2-K-PA, PA-K-PB2-K-NA, PB2-K-PA-K-NA, NA-C-PA-PB2, NA-C-PB2-PA, PA-PB2-C-NA, PB2-PA-C-NA, NA-PA-C-PB2, NA-PB2-C-PA, PA-C-PB2-NA, PB2-C-PA-NA, NA-C-PA-C-PB2, NA-C-PB2-C-PA, PA-C-PB2-C-NA, PB2-C-PA-C-NA, NA-K-PA-C-PB2, NA-K-PB2-C-PA, PA-C-PB2-K-NA, PB2-C-PA-K-NA, NA-C-PA-K-PB2, NA-C-PB2-K-PA, PA-K-PB2-C-NA, PB2-K-PA-C-NA, NA-K-PA-PB1F2, NA-K-PB 1F2-PA, ΡΑ-PB 1F2-K-NA, PB 1F2-PA-K-NA, NA-PA-K-PB1F2, NA-PB1F2-K-PA, PA-K-PB1F2-NA, PB 1F2-K-PA-NA, NA-K-PA-K-PB1F2, NA-K-PB 1F2-K-PA, ΡA-K-PB1F2-K-NA, PB 1F2-K-PA-K-NA, NA-C-PA-PB1F2, NA-C-PB 1F2-PA, PA-PB1F2-C-NA, PB1F2-PA-C-NA, NA-PA-C-PB1F2, NA-PB1F2-C-PA, PA-C-PB1F2-NA, PB 1F2-C-PΑΝΑ, NA-C-PA-C-PB1F2, NA-C-PB 1F2-C-PA, PA-C-PB 1F2-C-NA, PB 1F2-C-PA-C-NA, NA-K-PA-C-PB1F2, NA-K-PB 1F2-C-PA, PA-C-PB 1F2-K-NA, PB 1F2-C-PA-K-NA, NA-C-PA-K-PB1F2, NA-C-PB 1F2-K-P A, Ρ A-K-PB 1F2-C-NA, PB 1F2-K-P A-C-NA, NA-K-PB1, PB1-K-NA, NA-K-PB1-PB1, PB1-PB1-K-NA, NA-PB1-K-PB1, PB1-K-PB1-NA, NA-K-PB 1-K-PB1, PB1-K-PB1-K-NA, NA-C-PB 1, PB1-C-NA, NA-C-PB 1-PB 1, PB1-PB1-C-NA, NA-PB 1-C-PB1, PB1-C-PB1-NA, NA-C-PB 1-C-PB1, PB1-C-PB1-C-NA, NA-K-PB 1-C-PB1, PB1-C-PB1-K-NA, NA-C-PB 1-K-PB1, PB1-K-PB1-C-NA, NA-K-PB 1-PB2, NA-K-PB2-PB1, PB1-PB2-K-NA, PB2-PB1-K-NA, NA-PB 1-K-PB2, NA-PB2-K-PB1, PB1-K-PB2-NA, PB2-K-PB1-NA, NA-K-PB 1-K-PB2, NA-K-PB2-K-PB1, PB 1-K-PB2-K-NA, PB2-K-PB1 -K-NA, NA-C-PB1-PB2, NA-C-PB2-PB1, PB1-PB2-C-NA, PB2-PB1-C-NA, NA-PB 1-C-PB2, NA-PB2-C-PB1, PB1-C-PB2-NA, PB2-C-PB1-NA, NA-C-PB 1-C-PB2, NA-C-PB2-C-PB1, PB 1-C-PB2-C-NA, PB2-C-PB1 -C-NA, NA-K-PB 1-C-PB2, NA-K-PB2-C-PB1, PB 1-C-PB2-K-NA, PB2-C-PB1-K-NA, NA-C-PB 1-K-PB2, NA-C-PB2-K-PB1, PB 1-K-PB2-C-NA, PB2-K-PB1 -C-NA, NA-K-PB1-PB1F2, NA-K-PB 1F2-PB1, PB 1 -PB 1F2-K-NA, PB 1F2-PB1 -K-NA, NA-PB 1-K-PB1F2, NA-PB 1F2-K-PB1, PB 1 -K-PB1F2-NA, PB1F2-K-PB1-NA, NA-K-PB 1-K-PB1F2, NA-K-PB1F2-K-PB1, PB 1 -K-PB 1F2-K-NA, PB 1F2-K-PB1 -K-NA, NA-C-PB 1-PB 1F2, NA-C-PB 1F2-PB1, PB 1 -PB 1F2-C-NA, PB 1F2-PB1 -C-NA, NA-PB 1-C-PB1F2, NA-PB 1F2-C-PB1, PB1-C-PB1F2-NA, PB 1F2-C-PB1 -NA, NA-C-PB 1-C-PB1F2, NA-C-PB 1F2-C-PB1, PB1-C-PB1F2-C-NA, PB 1F2-C-PB1 -C-NA, NA-K-PB 1-C-PB1F2, NA-K-PB 1F2-C-PB1, PB 1 -C-PB1F2-K-NA, PB 1F2-C-PB1 -K-NA, NA-C-PB 1-K-PB 1F2, NA-C-PB 1F2-K-PB1, PB 1 -K-PB 1F2-C-NA, PB 1F2-K-PB1 -C-NA, NA-K-PB2, PB2-K-NA, NA-K-PB2-PB2, PB2-PB2-K-NA, NA-PB2-K-PB2, PB2-K-PB2-NA, NA-K-PB2-K-PB2, PB2-K-PB2-K-NA, NA-C-PB2, PB2-C-NA, NA-C-PB2-PB2, PB2-PB2-C-NA, NA-PB2-C-PB2, PB2-C-PB2-NA, NA-C-PB2-C-PB2, PB2-C-PB2-C-NA, NA-K-PB2-C-PB2, PB2-C-PB2-K-NA, NA-C-PB2-K-PB2, PB2-K-PB2-C-NA, NA-K-PB2-PB1F2, NA-K-PB 1F2-PB2, PB2-PB1F2-K-NA, PB 1F2-PB2-K-NA, NA-PB2-K-PB1F2, NA-PB 1F2-K-PB2, PB2-K-PB1F2-NA, PB 1F2-K-PB2-NA, NA-K-PB2-K-PB1F2, NA-K-PB 1F2-K-PB2, PB2-K-PB1F2-K-NA, PB 1F2-K-PB2-K-NA, NA-C-PB2-PB1F2, NA-C-PB 1F2-РВ2, РВ2-PB1F2-C-NA, PB1F2-PB2-C-NA, NA-PB2-C-PB1F2, NA-PB1F2-C-PB2, PB2-C-PB1F2-NA, PB 1F2-C-PB2-NA, NA-C-PB2-C-PB1F2, NA-C-PB1F2-C-PB2, PB2-C-PB1F2-C-NA, PB 1F2-C-PB2-C-NA, NA-K-PB2-C-PB1F2, NA-K-PB1F2-C-PB2, PB2-C-PB1F2-K-NA, PB 1F2-C-PB2-K-NA, NA-C-PB2-K-PB1F2, NA-C-PB 1F2-K-PB2, PB2-K-PB1F2-C-NA, PB 1F2-K-PB2-C-NA, NA-K-PB 1F2, PB1F2-K-NA, NA-K-PB 1F2-PB1F2, PB1F2-PB1F2-K-NA, NA-PB 1F2-K-PB1F2, PB 1F2-K-PB1F2-NA, NA-K-PB 1F2-K-PB1F2, PB1F2-K-PB1F2-K-NA, NA-C-PB 1F2, PB1F2-C-NA, NA-C-PB 1F2-PB1F2, PB 1F2-PB1F2-C-NA, NA-PB 1F2-C-PB1F2, PB 1F2-C-PB1F2-NA, NA-C-PB 1F2-C-PB1F2, PB 1F2-C-PB1F2-C-NA, NA-K-PB 1F2-C-PB1F2, PB 1F2-C-PB1F2-K-NA, NA-C-PB 1F2-K-PB1F2 или PB 1F2-K-PB1F2-C-NA. Наиболее предпочтительным является сочетание NP-K-M1-C-HA.
В рамках настоящего изобретения каждый белок может комбинироваться с любым другим белком и любые два белка могут или не могут соединяться через сайт расщепления или линкерный пептид.
В предпочтительных воплощениях экспрессионная система предназначается для применения при профилактике или лечении вирусных инфекций, особенно предпочтительно при профилактике или лечении ортомиксовирусных инфекций, предпочтительно инфекций вирусом гриппа, более предпочтительно инфекций вирусом гриппа А, и/или при изготовлении лекарственных средств для применения при профилактике или лечении ортомиксовирусных инфекций, предпочтительно инфекций вирусом гриппа, более предпочтительно инфекций вирусом гриппа А, и/или для применения в способах профилактики или лечения ортомиксовирусных инфекций, предпочтительно инфекций вирусом гриппа, более предпочтительно инфекций вирусом гриппа А.
В предпочтительных воплощениях экспрессионная система предназначается для усиления иммунного ответа, предпочтительно В-клеточного иммунного ответа против ортомиксовирусных инфекций, предпочтительно инфекций вирусом гриппа, более предпочтительно инфекций вирусом гриппа А.
В предпочтительном воплощении этого аспекта НА определяется в соответствии с восьмым аспектом.
Особенно предпочтительно, чтобы вирусный полипротеин, кодируемый первым, вторым и третьим полинуклеотидом, имел аминокислотную последовательность согласно SEQ ID NO: 13 или ее варианта и/или кодировался полинуклеотидом, имеющим аминокислотную последовательность согласно SEQ ID NO: 14 или ее варианта. Предпочтительно кодируемый тройной антигенный белок NP-M1-H1p подвергается процессингу в цитоплазматический слитый белок NP-M1 и трансмембранный белок H1p под действием последовательности 2А.
В предпочтительных воплощениях экспрессионная система предназначается для применения при профилактике или лечении ортомиксовирусных инфекций, предпочтительно инфекций вирусом гриппа А.
В более предпочтительных воплощениях экспрессионная система предназначается для усиления иммунного ответа, предпочтительно В-клеточного иммунного ответа против ортомиксовирусных белков, предпочтительно белка вируса гриппа А.
В предпочтительных воплощениях вектор или векторы, содержащие первый, второй и/или третий полинуклеотид, выбираются из группы, состоящей из плазмид, космид, фагов, вирусов и искусственных хромосом. Более предпочтительно вектор, подходящий для воплощения настоящего изобретения, выбирается из группы, состоящей из плазмидных векторов, космидных векторов, фаговых векторов, предпочтительно векторов из фага лямбда и нитчатых фагов, вирусных векторов, аденовирусных векторов (например, не реплицирующихся векторов Ad5, Ad11, Ad26, Ad35, Ad49, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAdlO, ChAdll, ChAdl6, ChAdl7, ChAdl9, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAdl46, ChAdl47, PanAd1, PanAd2 и PanAd3 или компетентных к репликации векторов Ad4 и Ad7), аденоассоциированных вирусных (AAV) векторов (например, AAV типа 5 и типа 2), альфавирусных векторов (например, вируса венесуэльского энцефалита лошадей (VEE), вируса Синдбис (SIN), вируса леса Семлики (SFV) и химеры VEE-SIN), герпесвирусных векторов (например, векторов, полученных из цитомегаловирусов типа цитомегаловируса резус (RhCMV) (14)), аренавирусных векторов (например, векторов из вируса лимфоцитарного хориоменингита (LCMV) (15)), векторов из вируса кори, поксвирусных векторов (например, вируса осповакцины, модифицированного вируса осповакцины Анкара (MVA), NYVAC (из вируса осповакцины штамма Копенгаген), авипоксвирусных векторов: вирусов оспы канареек (ALVAC) и оспы домашних птиц (FPV)), векторов из вируса везикулярного стоматита, ретровирусов, лентивирусов, вирусоподобных частиц и бактериальных спор. Векторы ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd63 и ChAd82 подробно описаны в WO 2005/071093. Векторы PanAd1, PanAd2, PanAd3, ChAd55, ChAd73, ChAd83, ChAd146 и ChAd147 подробно описаны в WO 2010/086189. Особенно предпочтительно вектор выбирается из группы, состоящей из MVA, ChAd63 и PanAd3.
В предпочтительных воплощениях экспрессионная система предназначается для применения в медицине. В более предпочтительных воплощениях экспрессионная система предназначается для применения при профилактике или лечении вирусных инфекций, особенно предпочтительно при профилактике или лечении инфекций RSV.
Во втором аспекте настоящим изобретением предусмотрена выделенная смесь белков, кодируемых экспрессирующей системой из первого аспекта. Предпочтительно выделенная смесь белков содержит, в основном содержит или включает один или несколько вирусных белков, кодируемых экспрессирующей системой из первого аспекта.
В предпочтительных воплощениях выделенная смесь белков предназначается для применения в медицине. В особенно предпочтительных воплощениях выделенная смесь белков предназначается для применения при профилактике или лечении вирусных инфекций, особенно предпочтительно при профилактике или лечении инфекций RSV либо при профилактике или лечении инфекций вирусом гриппа А.
В третьем аспекте настоящим изобретением предусмотрены выделенные клетки хозяева, содержащие экспрессирующую систему из первого аспекта и/или смесь белков из второго аспекта. Предусматривается, что такие клетки хозяева включают, без ограничения, прокариотические (например, бактериальные клетки) или эукариотические клетки (например, клетки грибов, растений или животных).
В предпочтительных воплощениях клетки хозяева предназначаются для применения в медицине. В особенно предпочтительных воплощениях клетки хозяева предназначаются для применения при профилактике или лечении вирусных инфекций, особенно предпочтительно при профилактике или лечении инфекций RSV либо при профилактике или лечении инфекций вирусом гриппа А.
В четвертом аспекте настоящим изобретением предусмотрены композиции, содержащие экспрессионную систему из первого аспекта и/или смесь белков из второго аспекта и фармацевтически приемлемый носитель и/или наполнитель. Предпочтительно такие композиции являются фармацевтическими композициями.
Композиции из четвертого аспекта содержат терапевтически эффективное количество соединения, предпочтительно в очищенном виде, вместе с подходящим количеством носителя, обеспечивающим надлежащую форму для введения пациентам. Лекарственная форма должна соответствовать способу введения.
Композиции могут иметь вид растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, форм для замедленного высвобождения и т.п.Композиции могут быть составлены в виде свечей, с традиционными связующими веществами и носителями типа триглицеридов.
Для приготовления фармацевтических композиций настоящего изобретения фармацевтически приемлемые носители могут быть либо твердыми, либо жидкими.
Композиции в твердом виде включают порошки, таблетки, пилюли, капсулы, пастилки, облатки, свечи и диспергируемые гранулы. Твердым наполнителем может быть одно или несколько веществ, которые также могут действовать в качестве разбавителей, ароматизаторов, связующих веществ, консервантов, разрыхлителей таблеток или инкапсулирующих материалов. В порошках наполнителем предпочтительно является мелкоизмельченное твердое вещество, которое образует смесь с мелкоизмельченным ингибитором настоящего изобретения. В таблетках активный ингредиент смешан в соответствующей пропорции с носителем, обладающим необходимыми связывающими свойствами, и запрессован в требуемую форму и размер. Подходящими наполнителями являются карбонат магния, стеарат магния, тальк, сахар, лактоза, пектин, декстрин, крахмал, желатин, трагакант, метилцеллюлоза, натриевая карбоксиметилцеллюлоза, легкоплавкий воск, масло какао и др. Для приготовления свечей сначала расплавляют легкоплавкий воск типа смеси глицеридов жирных кислот или масло какао и в нем гомогенно диспергируют активный компонент, например, путем перемешивания. Затем расплавленную однородную смесь разливают в формы удобного размера, оставляют остывать и при этом затвердеть. Таблетки, порошки, капсулы, пилюли, облатки и пастилки могут применяться в виде твердых дозовых форм, удобных для перорального введения.
Композиции в жидком виде включают растворы, суспензии и эмульсии, к примеру, водные, солевые растворы, водные растворы декстрозы, глицерина или растворы типа вода/пропиленгликоль. Солевой раствор является предпочтительным носителем при введении фармацевтической композиции внутривенно или интраназально при помощи распылителя. Для парентеральных инъекций жидкие препараты могут быть составлены в виде раствора, например, в водном растворе полиэтиленгликоля.
В особенно предпочтительном воплощении этого аспекта фармацевтическая композиция имеет вид раствора, суспензии или эмульсии и вводится интраназально при помощи распылителя.
Предпочтительно фармацевтическая композиция имеет вид стандартной дозовой формы. В такой форме композиция может разделяться на стандартные дозы, содержащие надлежащее количество активного компонента. Стандартная дозовая форма может представлять собой расфасованную композицию, при этом упаковка содержит дискретные дозы композиции, как-то упаковки таблеток, капсул и порошки во флаконах или ампулах. Стандартной дозовой формой также может служить сама капсула, флакон для инъекций, таблетка, облатка или пастилка или же она может представлять собой соответствующее количество любого из них в виде упаковки.
Композиция, если это нужно, также может содержать небольшие количества смачивающих или эмульгирующих веществ либо рН-буферных веществ.
Кроме того, такая композиция может содержать и другие фармакологически активные вещества, такие, без ограничения, как адъюванты и/или дополнительные активные ингредиенты.
Адъюванты в контексте настоящего изобретения включают, без ограничения, неорганические адъюванты, органические адъюванты, масляные адъюванты, цитокины, корпускулярные адъюванты, виросомы, бактериальные адъюванты, синтетические адъюванты или синтетические полинуклеотидные адъюванты.
Дополнительные активные ингредиенты включают, без ограничения, другие вакцинные соединения или композиции. Предпочтительно дополнительным активным ингредиентом является другая вирусная вакцина, более предпочтительно вакцина против ДНК-вируса, одноцепочечного РНК-вируса с минус нитью (ssRNA(-)) или амбисмыслового РНК-вируса. Более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)). Еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов. Предпочтительно дополнительным активным ингредиентом является вакцина против парамиксовируса, предпочтительно выбранного из группы, состоящей из Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama. Особенно предпочтительно Pneumovirinae выбирают из группы, состоящей из пневмовирусов (например, респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз) и метапневмовирусов (например, метапневмовируса человека, метапневмовируса птиц). Особенно предпочтительно Paramyxovirinae выбирают из группы, состоящей из респировирусов (например, вирусов парагриппа 1 и 3 человека) и рубулавирусов (например, вирусов парагриппа 2 и 4 человека). В качестве альтернативы дополнительным активным ингредиентом предпочтительно является другая вирусная вакцина против ортомиксовируса, более предпочтительно выбранного из числа вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях ортомиксовирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно вирусом гриппа А подтипа H1N1.
В пятом аспекте настоящим изобретением предусмотрена экспрессионная система из первого аспекта, выделенная смесь белков из второго аспекта, выделенные клетки хозяева из третьего аспекта или композиция из четвертого аспекта, предназначенная для применения при лечении или предупреждении вирусных заболеваний.
В предпочтительных воплощениях этого аспекта вирусное заболевание вызвано ДНК-вирусом, одноцепочечным РНК-вирусом с минус нитью (ssRNA(-)) или амбисмысловым РНК-вирусом. Более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)). Еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов. Парамиксовирус предпочтительно выбирают из группы, состоящей из Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama. Особенно предпочтительно Pneumovirinae выбирают из группы, состоящей из пневмовирусов (например, респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз) и метапневмовирусов (например, метапневмовируса человека, метапневмовируса птиц). Особенно предпочтительно Paramyxovirinae выбирают из группы, состоящей из респировирусов (например, вирусов парагриппа 1 и 3 человека) и рубулавирусов (например, вирусов парагриппа 2 и 4 человека). В качестве альтернативы вирусное заболевание вызвано ортомиксовирусом, более предпочтительно выбранным из числа вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях ортомиксовирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно вирусом гриппа А подтипа H1N1.
В шестом аспекте настоящим изобретением предусмотрен способ лечения или профилактики вирусных заболеваний, включающий введение эффективного количества экспрессионной системы из первого аспекта, выделенной смеси белков из второго аспекта, выделенных клеток хозяев из третьего аспекта или композиции из четвертого аспекта для применения при лечении или профилактике вирусного заболевания.
В предпочтительных воплощениях этого аспекта вирусное заболевание вызвано ДНК-вирусом, одноцепочечным РНК-вирусом с минус нитью (ssRNA(-)) или амбисмысловым РНК-вирусом. Более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)). Еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов. Парамиксовирус предпочтительно выбирают из группы, состоящей из Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama. Особенно предпочтительно Pneumovirinae выбирают из группы, состоящей из пневмовирусов (например, респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз) и метапневмовирусов (например, метапневмовируса человека, метапневмовируса птиц). Особенно предпочтительно Paramyxovirinae выбирают из группы, состоящей из респировирусов (например, вирусов парагриппа 1 и 3 человека) и рубулавирусов (например, вирусов парагриппа 2 и 4 человека). В качестве альтернативы вирусное заболевание вызвано ортомиксовирусом, более предпочтительно выбранным из числа вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях ортомиксовирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно вирусом гриппа А подтипа H1N1.
В седьмом аспекте настоящим изобретением предусмотрен способ усиления иммунного ответа против иммуногена, включающий введение эффективного количества экспрессионной системы из первого аспекта, смеси белков из второго аспекта, клеток хозяев из третьего аспекта или композиции из четвертого аспекта.
В предпочтительных воплощениях этого аспекта иммуногеном является патоген, более предпочтительно иммуногеном является вирус. Предпочтительно вирус выбирается из группы, состоящей из ДНК-вирусов, одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)) или амбисмысловых РНК-вирусов. Более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)). Еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов. Парамиксовирус предпочтительно выбирают из группы, состоящей из Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama. Особенно предпочтительно Pneumovirinae выбирают из группы, состоящей из пневмовирусов (например, респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз) и метапневмовирусов (например, метапневмовируса человека, метапневмовируса птиц). Особенно предпочтительно Paramyxovirinae выбирают из группы, состоящей из респировирусов (например, вирусов парагриппа 1 и 3 человека) и рубулавирусов (например, вирусов парагриппа 2 и 4 человека). В качестве альтернативы вирусное заболевание вызвано ортомиксовирусом, более предпочтительно выбранным из числа вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях ортомиксовирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно вирусом гриппа А подтипа H1N1.
В восьмом аспекте настоящим изобретением предусмотрены нуклеотидные конструкции, кодирующие гематтлютинин (НА), экспрессионные системы, содержащие эти нуклеотидные конструкции, и белки или полипротеины, кодируемые нуклеотидными конструкциями, при этом сайт расщепления НАО имеет многоосновную последовательность.
Конструкция из нуклеиновой кислоты из данного аспекта включает в себя, в основном состоит или состоит из полинуклеотида, кодирующего модифицированный гемагглютитин вируса гриппа (НА), при этом сайт расщепления НА0 модифицирован путем введения одной или нескольких основных аминокислот. Предпочтительно у модифицированного НА сайт расщепления НА0 из консенсусного гена НА заменен на многоосновный сайт расщепления H5N1, который расщепляется распространенными протеазами с образованием полностью процессированного НА (H1p).
Гематтлютинин гриппа (НА) представляет собой белок, принадлежащий к группе вирусных гемагтлютининов, находящихся на поверхности вирусов гриппа. Это антигенный гликопротеин, который отвечает за связывание вируса с заражаемой клеткой. Белки НА типа гемагглютинина гриппа связываются с сиаловой кислотой на мембранах таких клеток, как клетки верхних дыхательных путей или эритроциты. Существует по меньшей мере 16 различных антигенов НА. Эти серотипы или подтипы поименованы от HI до Н16.
НА обладает двумя функциями:
1) распознавание клеток мишени путем связывания с рецепторами, содержащими сиаловую кислоту,
2) опосредование проникновения вирусного генома в клетки мишени путем слияния эндосомной мембраны хозяина с вирусной мембраной (оболочкой).
В частности, НА связывается с моносахаридами сиаловой кислоты, которая присутствует на поверхности клеток мишени. Затем клеточная мембрана охватывает вирус и часть мембраны, покрывающей вирус, образует эндосому. Затем эндосома подкисляется и превращается в лизосому. Как только рН внутри эндосомы упадет примерно до 6.0, исходная свернутая структура молекулы НА становится нестабильной, вызывая частичное разворачивание ее с высвобождением гидрофобной части пептидной цепи. Этот пептид слияния встраивается в мембрану эндосом. Затем остальная часть молекулы НА повторно укладывается в новую структуру и вызывает слияние вирусной мембраны с эндосомной мембраной таким образом, что содержимое вируса, включая его РНК-геном, высвобождается в цитоплазму клетки.
Чтобы приобрести способность вызывать слияние мембран, НАО должен быть расщеплен на НА1 и НА2 протеазами клеток хозяев. Расщепление происходит по последовательности линкера, соединяющего субъединицы НА1 и НА2, которая располагается на частично выходящей на поверхность петли. Сайт расщепления Н0 у НА вируса гриппа располагается примерно на уровне а.к. 340 у подтипа H1N1 (от а.к. 339 до 344 в SEQ ID NO: 8), подтипа H5N1 (от а.к. 337 до 346 в SEQ ID NO: 10) и H3N2 (от а.к. 340 до 350 в SEQ ID NO: 20). Специалисты могут определить положение сайта расщепления Н0 у НА из других подтипов вируса гриппа путем сопоставления последовательностей и анализа гомологичности последовательностей хорошо известными в данной области техники методами. Чтобы перейти в компетентное к слиянию состояние, НА вируса гриппа А подтипа H1N1 и H3N2 требует расщепления протеазами клетки хозяев. Протеолитическая активации вирусов гриппа может происходить в аппарате Гольджи или на плазматической мембране инфицируемых клеток, а также во внеклеточном пространстве и в везикулах клеток мишени, поэтому природа сайта расщепления и соответствующие активирующие протеазы имеют важное значение для биологических свойств вируса гриппа и для терапевтического вмешательства. Было показано, что НА подтипа H5N1 содержит несколько остатков аргинина и лизина в сайте расщепления, причем для эффективного расщепления необходима консенсусная последовательность R-X-R/K-R. Кроме того, получены данные о том, что расщепление НА может происходить в сети транс-Гольджи (TGN). Было показано, что эти вирусы активируются фурином.
Аминокислотная последовательность SEQ ID NO: 8 - это консенсусная последовательность, полученная при выравнивании 829 последовательностей подтипа H1N1, аннотированного в базе данных Ресурса по вирусам гриппа NCBI и циркулировавшего по всему миру с апреля по сентябрь 2009 г. Аминокислотная последовательность SEQ ID NO: 9 идентична SEQ ID NO: 8 за исключением того, что естественный сайт расщепления Н0 протеазами был заменен на многоосновный сайт, происходящий из H5N1. Аминокислотная последовательность SEQ ID NO: 10 - это консенсусная последовательность, полученная при выравнивании 259 последовательностей подтипа H5N1, аннотированного в базе данных Ресурса по вирусам гриппа NCBI и заражавшего людей по всему миру с 1990 по 2009 г. Аминокислотная последовательность SEQ ID NO: 20 - это последовательность НА вируса гриппа А подтипа H3N2, штамма A/Wellington/01/2004(H3N2). Аминокислотная последовательность SEQ ID NO: 21 основана на SEQ ID NO: 20, при этом естественный сайт расщепления Н0 протеазами был заменен на многоосновный сайт, происходящий из H5N1.
Аминокислотная последовательность SEQ ID NO: 11 - это консенсусная последовательность NP, которая была разработана на основании выравнивания консенсусных последовательностей различных подтипов вируса гриппа. Кроме того, в последовательности NP по SEQ ID NO: 11 отсутствует сигнал ядерной локализации, который располагается на а.к. 6-8 (от TRK до AAA) и усиливает экспрессию в цитоплазме.
Аминокислотная последовательность SEQ ID NO: 12 - это консенсусная последовательность M1, которая была получена при выравнивании различных консенсусных последовательностей, при сопоставлении которых выбирали самые распространенные аминокислоты в каждом положении.
В предпочтительном воплощении этого аспекта конструкция из нуклеиновой кислоты и/или экспрессионная система, содержащая конструкцию из нуклеиновой кислоты, включает элементы для прямой транскрипции и трансляции НА и необязательно дополнительные белки, кодируемые конструкцией из нуклеиновой кислоты и/или экспрессирующей системой, которые могут быть включены в предпочтительные воплощения, изложенные ниже. Такие элементы включают промоторные и энхансерные элементы, направляющие транскрипцию мРНК в бесклеточной или клеточной системе, предпочтительно в клеточной системе. В другом воплощении, в котором в качестве транслируемой РНК представлены полинуклеотиды, предусматривается, что экспрессионная система включает все те элементы, которые необходимы для трансляции и/или стабилизации РНК, кодирующей НА и/или белки, индуцирующие Т-клетки белок, например, хвост полиА, IRES, кэп-структуры и др.
В предпочтительном воплощении этого аспекта конструкция из нуклеиновой кислоты кодирует белок НА, пептид или их вариант, содержащий модифицированный сайт расщепления Н0, причем НА выбирается из группы подтипов НА, состоящей из H1, Н2, Н3, Н4, Н6, Н7, Н8, Н9, Н10, Н11, Н12, Н13, Н14, Н15, Н16 либо их вариантов или консенсусных последовательностей, либо вариантов или консенсусных последовательностей одного или нескольких подтипов НА, выбранных из группы подтипов НА, состоящей из H1, Н2, Н3, Н4, Н5, Н6, Н7, Н8, Н9, Н10, H11, Н12, Н13, Н14, Н15, Н16. Предпочтительно подтипы НА выбираются из группы, состоящей из H1, Н2, Н3, Н7, Н9, НЮ либо их вариантов или консенсусных последовательностей, либо вариантов или консенсусных последовательностей одного или нескольких подтипов НА, выбранных из группы подтипов НА, состоящей из H1, Н2, Н3, Н5, Н7, Н9, Н10. Более предпочтительно белок НА, пептид или их вариант, содержащий модифицированный сайт расщепления Н0, представлен НА из подтипа H1 или его вариантом. Наиболее предпочтительно полинуклеотид, кодирующий НА из нуклеотидной конструкции, имеет последовательность SEQ ID NO: 9.
В предпочтительном воплощении этого аспекта конструкция из нуклеиновой кислоты кодирует белок НА, пептид или их вариант, у которого сайт расщепления НО модифицирован путем замены по меньшей мере одной неосновной аминокислоты на основную аминокислоту и/или введения по меньшей мере одной основной аминокислоты в последовательность сайта расщепления НО. Предпочтительно основная аминокислота выбирается из группы, состоящей из аргинина (Arg; R), лизина (Lys; К) и гистидина (His, H). Более предпочтительно основная аминокислота выбирается из группы, состоящей из аргинина (Arg; R) и лизина (Lys; К).
Предпочтительно сайт расщепления содержит последовательность от 6 до 12 аминокислот, более предпочтительно 10-12 аминокислот.
Предпочтительно по меньшей мере 20%, по меньшей мере 30%, по меньшей мере 40%, по меньшей мере 50%, по меньшей мере 60%, по меньшей мере 70%, по меньшей мере 80%, по меньшей мере 90% или 100% аминокислот полипептида, составляющих сайт расщепления НО, являются основными аминокислотами.
Предпочтительно сайт расщепления НА0 имеет последовательность, выбранную из группы, состоящей из PQRERRRKKR (SEQ ID NO: 15), PQRESRRKKR (SEQ ID NO: 16), PQGERRRKKR (SEQ ID NO: 17), PLRERRRKR (SEQ ID NO: 18) и PQRETR (SEQ ID NO: 19). Наиболее предпочтительно сайт расщепления НАО имеет последовательность PQRERRRKKR (SEQ ID NO: 15).
В таблице 1 представлено сравнение последовательностей сайта расщепления Н0 у штамма H1N1 и последовательностей сайта расщепления Н0 у штамма H5N1 по их соответствующему контексту аминокислотной цепи НА. В первой строке приведена консенсусная последовательность многоосновного сайта расщепления у сильно патогенного подтипа H5N1. Во второй строке приведена аминокислотная последовательность сайта расщепления Н0 у НА из штамма дикого типа H1N1. В третьей строке приведена сконструированная последовательность полиосновного сайта расщепления у белка H1p, заменяющая природную последовательность.

В воплощениях восьмого аспекта настоящего изобретения конструкция из нуклеиновой кислоты является частью экспрессионной системы, кодирующей модифицированный НА и второй полинуклеотид. В этой экспрессионной системе полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид содержатся в отдельных векторах или в одном и том же векторе. Соответственно, полинуклеотид, кодирующий модифицированный НА, может содержаться в одном векторе, а второй полинуклеотид может содержаться во втором векторе. С другой стороны, полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид могут содержаться в одном и том же векторе. Предпочтительно полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид, содержащийся в том же векторе, соединяются таким образом, чтобы они экспрессировались в виде полипротеина. Предпочтительно полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид образуют открытую рамку считывания.
Предпочтительно полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид экспрессируются в виде искусственного полипротеина. В контексте настоящего изобретения термин "искусственный полипротеин" обозначает такие полипротеины, которые не встречаются в природе, например, полученные методами рекомбинантной ДНК. Соответственно, белки, пептиды или их варианты, кодируемые в этом искусственном полипротеине, предпочтительно происходят из таких патогенов, геном которых не кодирует полипротеин, включающий белки, пептиды или их варианты, кодируемые полинуклеотидом, кодирующим модифицированный НА, и вторым полинуклеотидом изобретения. Предпочтительно полинуклеотид, кодирующий модифицированный НА, и второй полинуклеотид оба происходят из вирусов гриппа А.
В предпочтительных воплощениях восьмого аспекта второй полинуклеотид кодирует белок или его вариант, который индуцирует Т-клеточный ответ и который предпочтительно является неструктурным и/или внутренним белком вируса гриппа А. Предпочтительно неструктурный и/или внутренний белок, кодируемый вторым полинуклеотидом, выбран из группы, состоящей из NP, M1, М2, NS1, NS2/NEP, PA, РВ1, РВ2 или РВ1-F2 (PB1F2).
Предпочтительно аминокислотная последовательность модифицированного НА и/или неструктурного (внутреннего) белка, кодируемого вторым полинуклеотидом, включает последовательные сегменты или консенсусную последовательность одного или нескольких различных изолятов вируса.
В контексте настоящего изобретения термин "сегмент" предпочтительно относится к части белка или полипротеина. Особенно предпочтительно, чтобы такой сегмент сворачивался и/или функционировал независимо от остальной части белка или полипротеина, как-то, без ограничения, его домен, эпитоп или фрагмент. Предусматривается, что вариант белка в контексте настоящего изобретения отличается в сравнении со своим исходным полипептидом изменениями в аминокислотной последовательности, такими как аминокислотные замены, вставки, делеции, N-концевые усечения или С-концевые усечения или комбинации этих изменений, которые могут происходить по одному или нескольким сайтам, при этом вариант по меньшей мере на 80% идентичен по последовательности своему исходному полипептиду.
В другом предпочтительном воплощении у модифицированного НА или его варианта домен прикрепления к мембране подвергается функциональной делеции, то есть он либо структурно делетирован, либо структурно присутствует, но не выполняет свою биологическую функцию. В особенно предпочтительном воплощении подвергается делеции аминокислотная последовательность, соответствующая домену прикрепления к мембране. Удаление участка прикрепления к мембране служит гарантией того, что белок, индуцирующий В-клеточный ответ против патогена, будет секретироваться из клетки, в которую была введена экспрессионная система изобретения.
В следующем предпочтительном воплощении этого аспекта модифицированный НА содержит сигнал секреции, который направляет белок в эндоплазматический ретикулум (ER). Такие сигналы секреции предпочтительно присутствуют в контексте удаления домена прикрепления к мембране. Специалистам хорошо известны многие такие сигналы секреции, которые могут использоваться в качестве гетерологичных сигналов секреции, например, при добавлении их к N-концу модифицированного НА. С другой стороны, можно использовать природный сигнал секреции, например, который присутствует у большинства структурных и/или поверхностных белков вируса. Так, если у соответствующего белка сигнал секреции присутствует от природы, то предпочтительно он сохраняется и в модифицированной версии структурного и/или поверхностного белка.
В воплощениях восьмого аспекта неструктурный белок является консервативным внутренним белком, подходящим для индукции опосредованного Т-клетками иммунного ответа против патогена, включающего активацию антиген-специфичных Т-лимфоцитов, таких, без ограничения, как цитотоксические Т-клетки (CTLs), хелперные Т-клетки (TH-клетки), центральные Т-клетки памяти (клетки ТСМ), эффекторные Т-клетки памяти (клетки ТЕМ) и регуляторные Т-клетки (Treg-клетки). При этом предпочтительно индуцирующий Т-клетки белок патогена не содержит сигнала секреции.
В контексте настоящего изобретения модифицированный НА или его вариант располагается с N-конца или с С-конца относительно белка, пептида или их варианта, кодируемого вторым полинуклеотидом. В предпочтительном воплощении белок, пептид или их вариант, кодируемый вторым полинуклеотидом, располагается с N-конца относительно модифицированного НА или его варианта.
В предпочтительных воплощениях восьмого аспекта между модифицированным НА или его вариантом и вторым полинуклеотидом располагается полинуклеотид, кодирующий сайт расщепления. В рамках настоящего изобретения любые два белка могут или не могут соединяться через сайт расщепления.
Предпочтительно этот сайт расщепления является либо сайтом саморасщепления (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется и без участия какой-либо дополнительной молекулы или же образование пептидной связи в ней предотвращается в первую очередь), либо сайтом расщепления эндопептидазами (т.е. сайтом расщепления внутри аминокислотной последовательности, причем она расщепляется эндопептидазой, например, трипсином, пепсином, эластазой, тромбином, коллагеназой, фурином, термолизином, эндопептидазой V8, катепсинами). Более предпочтительно сайт саморасщепления представлен сайтом расщепления 2А, выбранным из группы, состоящей из вирусного пептида 2А или 2А-подобных пептидов пикорнавирусов, вирусов насекомых, Aphtoviridae, ротавирусов и трипаносом, при этом предпочтительно сайт расщепления 2А представлен пептидом 2А вируса ящура. С другой стороны, полипротеин настоящего изобретения может расщепляться аутопротеазой, т.е. такой протеазой, которая расщепляет пептидные связи в той же белковой молекуле, в которой содержится и сама протеаза. Примерами таких аутопротеаз являются протеаза NS2 у флавивирусов или протеаза VP4 у бирнавирусов.
В контексте настоящего изобретения сайт расщепления может располагаться с N-конца относительно модифицированного НА или его варианта и с С-конца относительно белка, пептида или их варианта, кодируемого вторым полинуклеотидом. С другой стороны, сайт расщепления может располагаться с С-конца относительно модифицированного НА или его варианта и с N-конца относительно белка, пептида или их варианта, кодируемого вторым полинуклеотидом.
В предпочтительном воплощении восьмого аспекта экспрессионная система дополнительно содержит третий полинуклеотид, кодирующий белок, пептид или их вариант от патогена.
Предпочтительно белок, пептид или их вариант, кодируемый третьим полинуклеотидом, отличается от модифицированного НА или его варианта или от белка, пептида или их варианта, кодируемого вторым полинуклеотидом. Предпочтительно белки, пептиды или их варианты, кодируемые первым, вторым и третьим полинуклеотидом, отличаются друг от друга тем, что они содержат аминокислотные последовательности различных белков.
В предпочтительных воплощениях восьмого аспекта третий полинуклеотид кодирует белок или его вариант, который индуцирует Т-клеточный ответ и который предпочтительно является неструктурным и/или внутренним белком вируса гриппа А. Предпочтительно неструктурный и/или внутренний белок, кодируемый третьим полинуклеотидом, выбран из группы, состоящей из NP, M1, М2, NS1, NS2/NEP, PA, РВ1, PB2 или PB1-F2 (PB1F2).
В предпочтительных воплощениях между вторым полинуклеотидом и третьим полинуклеотидом располагается полинуклеотид, кодирующий линкер. Предпочтительно линкер представляет собой гибкий линкер, включающий аминокислотную последовательность согласно SEQ ID NO: 6 (Gly-Gly-Gly-Ser-Gly-Gly-Gly).
В предпочтительных воплощениях третий полинуклеотид содержится в отдельном или в том же самом векторе, что и полинуклеотид, кодирующий модифицированный НА или его вариант и/или второй полинуклеотид.
Соответственно, полинуклеотид, кодирующий модифицированный НА или его вариант, содержится в одном векторе, а второй полинуклеотид содержится во втором векторе и третий полинуклеотид содержится в третьем векторе. По другой версии, полинуклеотид, кодирующий модифицированный НА или его вариант, и второй полинуклеотид содержатся в одном и том же векторе, а третий полинуклеотид содержится в отдельном векторе, или же полинуклеотид, кодирующий модифицированный НА или его вариант, и третий полинуклеотид содержатся в одном и том же векторе, а второй полинуклеотид содержится в отдельном векторе, или же второй и третий полинуклеотид содержатся в одном и том же векторе, а полинуклеотид, кодирующий модифицированный НА или его вариант, содержится в отдельном векторе. По другой версии, полинуклеотид, кодирующий модифицированный НА или его вариант, и второй и третий полинуклеотид содержатся в одном и том же векторе. Предпочтительно полинуклеотид, кодирующий модифицированный НА или его вариант, и второй и третий полинуклеотид содержатся в одном и том же векторе. Особенно предпочтительно полинуклеотид, кодирующий модифицированный НА или его вариант, и второй и третий полинуклеотид, содержащиеся в одном и том же векторе, соединяются таким образом, чтобы они экспрессировались в виде полипротеина. Предпочтительно полинуклеотид, кодирующий модифицированный НА или его вариант, и второй и третий полинуклеотид, содержащиеся в одном и том же векторе, образуют открытую рамку считывания.
В предпочтительных воплощениях этого аспекта вектор или векторы, содержащие полинуклеотид, кодирующий модифицированный НА или его вариант, и второй и/или третий полинуклеотид, выбираются из группы, состоящей из плазмид, космид, фагов, вирусов и искусственных хромосом. Более предпочтительно вектор, подходящий для воплощения настоящего изобретения, выбирается из группы, состоящей из плазмидных векторов, космидных векторов, фаговых векторов, предпочтительно векторов из фага лямбда и нитчатых фагов, вирусных векторов, аденовирусных векторов (например, не реплицирующихся векторов Ad5, Ad11, Ad26, Ad35, Ad49, ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd55, ChAd63, ChAd73, ChAd82, ChAd83, ChAd146, ChAd147, PanAd1, PanAd2 и PanAd3 или компетентных к репликации векторов Ad4 и Ad7), аденоассоциированных вирусных (AAV) векторов (например, AAV типа 5 и типа 2), альфавирусных векторов (например, вируса венесуэльского энцефалита лошадей (VEE), вируса Синдбис (SIN), вируса леса Семлики (SFV) и химеры VEE-SIN), герпесвирусных векторов (например, векторов, полученных из цитомегаловирусов типа цитомегаловируса резус (RhCMV) (14)), аренавирусных векторов (например, векторов из вируса лимфоцитарного хориоменингита (LCMV) (15)), векторов из вируса кори, поксвирусных векторов (например, вируса осповакцины, модифицированного вируса осповакцины Анкара (MVA), NYVAC (из вируса осповакцины штамма Копенгаген), авипоксвирусных векторов: вирусов оспы канареек (ALVAC) и оспы домашних птиц (FPV)), векторов из вируса везикулярного стоматита, ретровирусов, лентивирусов, вирусоподобных частиц и бактериальных спор. Векторы ChAd3, ChAd4, ChAd5, ChAd6, ChAd7, ChAd8, ChAd9, ChAd10, ChAd11, ChAd16, ChAd17, ChAd19, ChAd20, ChAd22, ChAd24, ChAd26, ChAd30, ChAd31, ChAd37, ChAd38, ChAd44, ChAd63 и ChAd82 подробно описаны в WO 2005/071093. Векторы PanAd1, PanAd2, PanAd3, ChAd55, ChAd73, ChAd83, ChAd146 и ChAdl47 подробно описаны в WO 2010/086189. Особенно предпочтительно вектор выбирается из группы, состоящей из MVA, ChAd63 и PanAd3.
В предпочтительных воплощениях этого аспекта нуклеотидная конструкция или экспрессионная система либо вектор или векторы, содержащие полинуклеотид из нуклеотидной конструкции или экспрессионной системы, могут включать "контролирующие экспрессию последовательности", регулирующие экспрессию данного гена. Как правило, контролирующие экспрессию последовательности представлены полипептидами или полинуклеотидами, такими, без ограничения, как промоторы, энхансеры, сайленсеры, инсуляторы или репрессоры.
В особенно предпочтительном воплощении этого аспекта экспрессионная система определяется в соответствии с воплощениями первого аспекта настоящего изобретения, направленными на экспрессионные системы, содержащие полинуклеотиды, кодирующие белки, пептиды или их варианты из ортомиксовирусов, предпочтительно белки, пептиды или варианты из вирусов гриппа А.
В предпочтительных воплощениях конструкция из нуклеиновой кислоты и/или экспрессионная система из восьмого аспекта предназначается для применения в медицине. В более предпочтительных воплощениях конструкции из нуклеиновой кислоты, экспрессионные системы или белки из этого аспекта предназначаются для применения при профилактике или лечения инфекций вирусом гриппа и/или при изготовлении лекарственных средств для применения при профилактике или лечении инфекций вирусом гриппа и/или для применения в способах профилактики или лечения инфекций вирусом гриппа А.
В предпочтительных воплощениях экспрессионная система предназначается для усиления иммунного ответа. В более предпочтительных воплощениях экспрессионная система предназначается для усиления антипатогенного В-клеточного иммунного ответа против инфекций вирусом гриппа А, более предпочтительно вирусом гриппа А, определенным в первом аспекте изобретения.
В девятом аспекте настоящим изобретением предусмотрено применение многоосновного сайта расщепления НА0, определенного в восьмом аспекте, для получения конструкции из нуклеиновой кислоты или экспрессионной системы, способной экспрессировать модифицированный гемагтлютинин вируса гриппа (НА) из восьмого аспекта in vitro и/или in vivo. Кроме того, этим аспектом предусматривается выделенная белковая смесь, белок и/или полипротеин, кодируемые конструкцией из нуклеиновой кислоты или экспрессионной системой, сконструированной согласно этому аспекту.
В десятом аспекте изобретением предусмотрена выделенная смесь белков, кодируемых экспрессионной системой из восьмого аспекта. Предпочтительно выделенная смесь белков содержит, в основном содержит или состоит из одного или нескольких белков или полипротеинов, кодируемых конструкцией из нуклеиновой кислоты или экспрессионной системой из восьмого аспекта. В предпочтительных воплощениях выделенная смесь белков предназначается для применения в медицине. В особо предпочтительных воплощениях выделенная смесь белков предназначается для применения при профилактике или лечения инфекций вирусом гриппа и/или при изготовлении лекарственных средств для применения при профилактике или лечении инфекций вирусом гриппа и/или для применения в способах профилактики или лечения инфекций вирусом гриппа А.
В одиннадцатом аспекте изобретением предусмотрены выделенные клетки хозяева, содержащие нуклеотидные конструкции, экспрессионные системы либо белки или полипротеины из восьмого аспекта и/или смесь белков из десятого аспекта. Предусматривается, что такие клетки хозяева включают, без ограничения, прокариотические (например, бактериальные клетки) или эукариотические клетки (например, клетки грибов, растений или животных). В предпочтительных воплощениях этого аспекта клетки хозяева предназначаются для применения в медицине. В особо предпочтительных воплощениях клетки хозяева предназначаются для применения при профилактике или лечения инфекций вирусом гриппа и/или при изготовлении лекарственных средств для применения при профилактике или лечении инфекций вирусом гриппа и/или для применения в способах профилактики или лечения инфекций вирусом гриппа А.
В двенадцатом аспекте настоящим изобретением предусмотрены композиции, содержащие нуклеотидные конструкции, экспрессионные системы либо белки или полипротеины из восьмого аспекта или смесь белков из десятого аспекта и фармацевтически приемлемый носитель и/или наполнитель. Предпочтительно такие композиции являются фармацевтическими композициями.
Композиции из двенадцатого аспекта содержат терапевтически эффективное количество соединения, предпочтительно в очищенном виде, вместе с подходящим количеством носителя, обеспечивающим надлежащую форму для введения пациентам. Лекарственная форма должна соответствовать способу введения.
Композиции могут иметь вид растворов, суспензий, эмульсий, таблеток, пилюль, капсул, порошков, форм для замедленного высвобождения и т.п. Композиции могут быть составлены в виде свечей, с традиционными связующими веществами и носителями типа триглицеридов.
Для приготовления фармацевтических композиций настоящего изобретения фармацевтически приемлемые носители могут быть либо твердыми, либо жидкими.
Композиции в твердом виде включают порошки, таблетки, пилюли, капсулы, пастилки, облатки, свечи и диспергируемые гранулы. Твердым наполнителем может быть одно или несколько веществ, которые также могут действовать в качестве разбавителей, ароматизаторов, связующих веществ, консервантов, разрыхлителей таблеток или инкапсулирующих материалов. В порошках наполнителем предпочтительно является мелкоизмельченное твердое вещество, которое образует смесь с мелкоизмельченным ингибитором настоящего изобретения. В таблетках активный ингредиент смешан в соответствующей пропорции с носителем, обладающим необходимыми связывающими свойствами, и запрессован в требуемую форму и размер. Подходящими наполнителями являются карбонат магния, стеарат магния, тальк, сахар, лактоза, пектин, декстрин, крахмал, желатин, трагакант, метилцеллюлоза, натриевая карбоксиметилцеллюлоза, легкоплавкий воск, масло какао и др. Для приготовления свечей сначала расплавляют легкоплавкий воск типа смеси глицеридов жирных кислот или масло какао и в нем гомогенно диспергируют активный компонент, например, путем перемешивания. Затем расплавленную однородную смесь разливают в формы удобного размера, оставляют остывать и при этом затвердеть. Таблетки, порошки, капсулы, пилюли, облатки и пастилки могут применяться в виде твердых дозовых форм, удобных для перорального введения.
Композиции в жидком виде включают растворы, суспензии и эмульсии, к примеру, водные, солевые растворы, водные растворы декстрозы, глицерина или растворы типа вода/пропиленгликоль. Солевой раствор является предпочтительным носителем при введении фармацевтической композиции внутривенно или интраназально при помощи распылителя. Для парентеральных инъекций жидкие препараты могут быть составлены в виде раствора, например, в водном растворе полиэтиленгликоля.
В особенно предпочтительном воплощении этого аспекта фармацевтическая композиция имеет вид раствора, суспензии или эмульсии и вводится интраназально при помощи распылителя.
Предпочтительно фармацевтическая композиция имеет вид стандартной дозовой формы. В такой форме композиция может разделяться на стандартные дозы, содержащие надлежащее количество активного компонента. Стандартная дозовая форма может представлять собой расфасованную композицию, при этом упаковка содержит дискретные дозы композиции, как-то упаковки таблеток, капсул и порошки во флаконах или ампулах. Стандартной дозовой формой также может служить сама капсула, флакон для инъекций, таблетка, облатка или пастилка или же она может представлять собой соответствующее количество любого из них в виде упаковки.
Композиция, если это нужно, также может содержать небольшие количества смачивающих или эмульгирующих веществ либо рН-буферных веществ.
Кроме того, такая композиция может содержать и другие фармакологически активные вещества, такие, без ограничения, как адъюванты и/или дополнительные активные ингредиенты.
Адъюванты в контексте настоящего изобретения включают, без ограничения, неорганические адъюванты, органические адъюванты, масляные адъюванты, цитокины, корпускулярные адъюванты, виросомы, бактериальные адъюванты, синтетические адъюванты или синтетические полинуклеотидные адъюванты.
Дополнительные активные ингредиенты включают, без ограничения, другие вакцинные соединения или композиции. Предпочтительно дополнительным активным ингредиентом является другая вирусная вакцина, более предпочтительно вакцина против ДНК-вируса, одноцепочечного РНК-вируса с минус нитью (ssRNA(-)) или амбисмыслового РНК-вируса. Более предпочтительно вирус выбирается из одноцепочечных РНК-вирусов с минус нитью (ssRNA(-)). Еще более предпочтительно вирус выбирается из оболочечных вирусов ssRNA(-), более предпочтительно из группы, состоящей из парамиксовирусов и ортомиксовирусов. Предпочтительно дополнительным активным ингредиентом является вакцина против парамиксовируса, предпочтительно выбранного из группы, состоящей из Pneumovirinae, Paramyxovirinae, вируса Fer-de-Lance, вируса Nariva, вируса Salem, парамиксовируса Tupaia, вируса Beilong, вируса J, вируса Menangle, вируса Mossmann и вируса Murayama. Особенно предпочтительно Pneumovirinae выбирают из группы, состоящей из пневмовирусов (например, респираторного синцитиального вируса человека (RSV), вируса пневмонии мышей, бычьего RSV, RSV овец, RSV коз) и метапневмовирусов (например, метапневмовируса человека, метапневмовируса птиц). Особенно предпочтительно Paramyxovirinae выбирают из группы, состоящей из респировирусов (например, вирусов парагриппа 1 и 3 человека) и рубулавирусов (например, вирусов парагриппа 2 и 4 человека). В качестве альтернативы дополнительным активным ингредиентом предпочтительно является другая вирусная вакцина против ортомиксовируса, более предпочтительно выбранного из числа вируса гриппа А, вируса гриппа В, вируса гриппа С, тоготовирусов и исавирусов. В еще более предпочтительных воплощениях ортомиксовирус представлен вирусом гриппа А, предпочтительно выбранным из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно вирусом гриппа А подтипа H1N1.
В тринадцатом аспекте настоящим изобретением предусмотрены нуклеотидные конструкции, экспрессионные системы либо белки или полипротеины из восьмого аспекта, смесь белков из десятого аспекта, клетки из одиннадцатого аспекта и композиции из двенадцатого аспекта, предназначенные для применения в медицине, в частности, при лечении или профилактике инфекций вирусом гриппа А. Вирус гриппа А предпочтительно выбирают из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно подтипа H1N1 вируса гриппа А.
В четырнадцатом аспекте настоящим изобретением предусмотрен способ лечения или профилактики инфекций вирусом гриппа А, включающий введение эффективного количества нуклеотидных конструкций, экспрессионной системы либо белков или полипротеинов из восьмого аспекта, смеси белков из десятого аспекта, клеток из одиннадцатого аспекта или композиции из двенадцатого аспекта. Вирус гриппа А предпочтительно выбирают из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно подтипа H1N1 вируса гриппа А.
В пятнадцатом аспекте настоящим изобретением предусмотрен способ усиления иммунного ответа, включающий введение нуклеотидных конструкций, экспрессионной системы либо белков или полипротеинов из восьмого аспекта, смеси белков из десятого аспекта, клеток из одиннадцатого аспекта или композиции из двенадцатого аспекта. В предпочтительном воплощении этого аспекта способ вызывает усиление иммунного ответа против вируса гриппа А. Вирус гриппа А предпочтительно выбирают из подтипов H1N1, H1N2, H2N2, H3N1, H3N2, H3N8, H5N1, H5N2, H5N3, H5N8, H5N9, H7N1, H7N2, H7N3, H7N4, H7N7, H9N2, H10N7 вируса гриппа А, более предпочтительно подтипа H1N1 вируса гриппа А.
Следующие примеры только раскрывают настоящее изобретение и не должны никоим образом рассматриваться как ограничивающие объем изобретения, которое раскрыто в прилагаемой формуле изобретения.
Примеры
Пример 1. Разработка и синтез ДНК, кодирующей оптимизированный антиген RSV
Консенсусная вакцина
Существует несколько вычислительных альтернатив разработке вакцин на основе изолятов. Один подход заключается в реконструкции последовательности последнего общего предка (MRCA) (9). В этом методе предковое состояние является оценкой фактической последовательности, существовавшей в прошлом (т.е. оно вытекает напрямую из реконструированной истории). Другим типом вычислительного анализа является метод центральной точки дерева (СОТ). В методе СОТ идентифицируют точку на некорневом дереве, в которой сводится к минимуму среднее эволюционное расстояние от этой точки до каждой верхушки филогенетического дерева. Сторонники этого подхода утверждают, что поскольку точка СОТ находится на филогенетическом дереве, то оценка последовательности по методу СОТ будет обладать такими же преимуществами, как и оценка предковой последовательности. К примеру, см. U.S. Application 2005/0137387 A1. Однако метод СОТ является настолько сложным, что применение его на практике к большим и неоднородным массивам данных типа базы данных по последовательности вируса гриппа будет непрактичным по технологии. В целом методы MRCA и СОТ не подходят для применения на комплексной базе данных по последовательности вируса гриппа.
Третьим типом вычислительного анализа является метод консенсусной последовательности. Поскольку консенсусная последовательность состоит из аминокислот, наиболее часто встречающихся в каждом положении, то она, вероятно, представляет наиболее приспособленное состояние вируса. Так, эффективное уклонение от иммунного ответа путем отбора последовательностей, отходящих от консенсуса, может привести к меньшей приспособленности вируса с точки зрения размножения. Метод консенсусной последовательности благоприятствует сильно представленным в выборке линиям и не придает значения выбросам. Используемые нами методы значительно проще, чем другие типы вычислительного анализа. Более того, в них можно использовать весь массив данных по RSV. Одним из преимуществ консенсусной последовательности является то, что она сводит к минимуму генетические различия между вакцинными штаммами и современными изолятами, эффективно уменьшает наполовину степень разнообразия и поэтому может обладать большим потенциалом для выработки перекрестных реакций.
Разработка вакцины
Для разработки антигена для вакцины настоящего изобретения извлекали последовательности белков F0, N и М2-1 вируса RSV из базы данных Ресурса по RSV Национального центра информации по биотехнологии (NCBI) (http://www.ncbi.nlm.nih.gov). Последовательности белков брали от различных штаммов RSV подтипа А.
Консенсусную последовательность F0 получали путем выравнивания всех неидентичных последовательностей белка F с помощью MUSCLE версии 3.6 с применением правила большинства. Консенсусную последовательность F0 для вакцины разрабатывали на основании выравнивания различных последовательностей RSV. Степень сходства для консенсусной последовательности F0 для вакцины измеряли методом BLAST, что означает Базовый поисковый инструмент для локального выравнивания, который общедоступен через NCBI. Наибольшее среднее сходство консенсусной последовательности при расчете исходя из сравнения всех последовательностей RSV в базе данных составляло 100% относительно штамма А2 респираторного синцитиального вируса человека.
Кроме того, в последовательности F0 для вакцины отсутствует трансмембранный участок, состоящий из а.к. 525-574, что способствует секреции F0ΔTM.
Наконец, последовательность F0ΔTM для вакцины подвергали оптимизации кодонов для экспрессии в эукариотических клетках.
Консенсусную последовательность белка N для вакцины получали путем выравнивания всех неидентичных последовательностей белка N с помощью MUSCLE версии 3.6 и применения правила большинства. Анализ консенсусной последовательности белка N с помощью BLAST дал наилучшее совпадение со штаммом А2 респираторного синцитиального вируса человека. Затем последовательность белка N для вакцины подвергали оптимизации кодонов для экспрессии в эукариотических клетках.
Консенсусную последовательность белка М2-1 для вакцины получали путем выравнивания всех неидентичных последовательностей белка М2-1 с помощью MUSCLE версии 3.6 и применения правила большинства. Анализ консенсусной последовательности белка М2-1 с помощью BLAST дал наилучшее совпадение со штаммом А2 респираторного синцитиального вируса человека. Затем последовательность белка М2-1 для вакцины подвергали оптимизации кодонов для экспрессии в эукариотических клетках.
Последовательности F0ΔTM и белка N для вакцины соединяли через последовательность расщепления 2А вируса ящура. Последовательности белка N и белка М2-1 для вакцины разделяли гибким линкером (GGGSGGG; SEQ ID NO: 6).
Наконец, оптимизированные по кодонам вирусные гены клонировали в виде единой рамки считывания F0ΔTM-N-M2-1. Схематическое изображение состава антигена приведено на фиг. 1.
Создание ДНК-плазмид, кодирующих F0ΔTM и F0ΔTM-N-M2-1
Консенсусные последовательности F0ΔTM, N и М2-1 подвергали оптимизации для экспрессии у млекопитающих, включая добавление последовательности Козака и оптимизацию кодонов. Последовательность ДНК, кодирующей мультиантигенную вакцину, синтезировали химическим путем, а затем субклонировали с помощью подходящих рестрикционных ферментов EcoRV и NotI в челночный вектор pVJTetOCMV под контролем промотора CMV.
Создание вакцины от RSV в вирусном векторе PanAd3
Была создана вакцина PanAd3/F0ΔTM-N-M2-1 от RSV в вирусном векторе, которая содержит полипротеин в 809 а.к., кодирующий консенсусные белки F0ΔTM, N и М2-1, слитые с помощью гибкого линкера.
Аденовирус шимпанзе 3-го типа (PanAd3) - это новый штамм аденовируса с улучшенной серопревалентностью, который был описан ранее.
Клонирование F0ΔTM-N-M2-1 из плазмидного вектора pVJTetOCMV/F0ΔTM-N-М2-1 в вектор pre-Adeno из PanAd3 проводили путем вырезания антигенных последовательностей с гомологичными участками по бокам и энзиматической рекомбинации in vitro.
Анализ экспрессии антигена в клетках млекопитающих
Для проверки того, что такая уникальная комбинация вирусных антигенов эффективно экспрессируется и правильно процессируется в клетках млекопитающих, клетки Hela трансфецировали с помощью 10 мкг ДНК плазмиды, кодирующей антиген F0ΔTM-N-M2-1. Клетки культивировали в течение 36 часов, а затем отбирали супернатант и готовили клеточные лизаты. Белки разделяли методом электрофореза в SDS-PAGE и переносили на нейлоновые фильтры. Для выявления экспрессируемых белков использовали мышиное моноклональное антитело (mAb8) против вирусного белка M (подарок от Dr. Geraldine Taylor).
Как видно из фиг. 2 и 3, слитый вирусный белок N-M2-1 весьма эффективно высвобождается из полипротеина по сайту расщепления 2А и распознается антителом mAb8 в виде основной полосы. В стационарном состоянии в клетках находится очень мало высокомолекулярных предшественников. В качестве контроля использовали лизаты клеток Нер2, инфицированных штаммом А вируса RSV.
Анализ культуральной среды клеток методами невосстановительного SDS-PAGE и Вестерн-блота показал, что белок F, удаленный из трансмембранного участка, секретируется в супернатант (см. фиг. 3, дорожка RSV). Молекулярная масса белка F в супернатанте соответствует гомотримеру белка F, который составляет его естественную конфигурацию.
Пример 2. Иммуногенность вакцины у мышей
Антитела против белка F при иммунизации с помощью ДНК
Для иммунизации мышей использовали ДНК плазмид, кодирующих F0ΔTM-N-M2-1 или только F0ΔTM, путем инъекции плазмидной ДНК и электропорации (GET) с режимом прайминга и бустинга через 3 недели после прайминга. Через две недели после бустинга отбирали сыворотку иммунизированных мышей и объединяли.
Супернатанты из клеток Hela, инфицированных PanAd3/F0ΔTM-N-M2-1 при MOI 250, разделяли методом невосстановительного SDS-PAGE, переносили на нейлоновые фильтры и гибридизовали с различными разведениями сыворотки от мышей, иммунизированных F0ΔTM или F0ΔTM-N-M2-1.
Как видно из фиг. 4А и В, титры антител, индуцированных белком F, экспрессируемым в составе вакцинного антигена, были по меньшей мере в 30 раз выше, чем индуцированные самим белком F. Таким образом, антиген F0ΔTM-N-M2-1 обладает превосходными иммуногенными свойствами при индуцировании В-клеточного ответа у мышей.
Т-клеточный ответ
Иммунологический потенциал вектора из аденовируса шимпанзе PanAd3, несущего антиген F0ΔTM-N-M2-1 вакцины от RSV, оценивали на мышах.
Группы мышей Balb/C иммунизировали посредством внутримышечной инъекции в четырехглавую мышцу возрастающими дозами PanAd3/F0ΔTM-N-M2-1. Через 4 недели после вакцинации мышей забивали, а спленоциты подвергали анализу на IFNγ методом Elispot с помощью картированных иммунодоминантных пептидов из белков F и M вируса RSV (пептид GWYTSVITIELSNIKE: а.к. 51-66 из F, пептид KYKNAVTEL: а.к. 85-93 из F и пептид SYIGSINNI: а.к. 282-290 из М).
Как видно из фиг. 5, наблюдался сильный Т-клеточный ответ по известным иммунодоминантным эпитопам Balb/C против белков F и M вируса RSV.
Пример 3. Индукция нейтрализующих антител под действием H1p
Новый химерный белок H1p, сконструированный так, чтобы он содержал многоосновный сайт расщепления НА0 из H5N1, эффективно экспрессировался и полностью расщеплялся в трансфецированных клетках HeLa. Эквивалентный белок с сайтом расщепления дикого типа - H1 не расщеплялся в клетках HeLa, как видно из фиг. 7.
Для того чтобы проверить, что химерный белок H1p корректно представлен на клеточной мембране, проводили анализ связывания методом FACS на целых клетках, используя для выявления трансфецированного белка на клеточной поверхности поликлональную антисыворотку против НА. Как видно из фиг. 8, H1p представлен на клеточной мембране столь же эффективно, как и соответствующий белок НА дикого типа.
Для измерения иммунологического потенциала H1p мышей Balb/C иммунизировали плазмидными ДНК-векторами, кодирующими модифицированный H1p и немодифицированный H1 (PVJ-H1p и PVJ-H1, соответственно). Сыворотки от иммунизированных животных анализировали методом ELISA на очищенном рекомбинантном белке НА (H1N1California2009). Титры антител к НА, вызванные сконструированным белком H1p, оказались значительно более высокими, чем вызванные белком НА, несущим сайт протеазного расщепления дикого типа (фиг. 9).
Для того, чтобы проверить и расширить эти результаты, сыворотки от животных, иммунизированных H1 и H1p, тестировали на их способность нейтрализировать инфицирование ретровирусными векторами, псевдотипированными по белку НА Flu на основе анализа клеточной культуры. Псевдовирионы инфекционны только в течение одного цикла заражения, при котором они экспрессируют ген-репортер люциферазы. На фиг. 10 представлена нейтрализующая способность сыворотки при анализе инфицирования частицами псевдотипированного по НА (H1N1Mexico2009) вируса на клетках MDCK. Результаты подтверждают, что антитела, индуцированные H1p, обладают большей нейтрализующей активностью, чем антитела, индуцированные белком H1.
Пример 4. Повышение титра антител полипротеином, содержащим NP, M1 и H1p
Непосредственное сравнение иммунологического потенциала H1p и NPM1H1p показало, что белок НА, экспрессируемый в контексте тройного антигена, индуцирует более высокий титр антител по сравнению с одним только НА. На фиг. 11 представлены результаты анализа методом ELISA, в котором рекомбинантный НА (H1N1California 2009) фиксировали на дне 96-луночного планшета. Серийные разведения сыворотки животных, иммунизированных H1p и NPM1H1p, наносили на планшет и выявляли связанный IgG с помощью вторичных антител против IgG мыши. Как это наблюдалось уже для антигена RSV, совместное экспрессирование внутренних антигенов (NP и M1) с экспонированным на поверхности антигеном (НА) повышает гуморальный ответ, направленный на последний белок.
Пример 5. Процессинг нового антигена FLU, состоящего из NP, M1 и H1p
Для проверки экспрессии и процессинга белков антигена вакцины, клетки HeLa трансфецировали экспрессионной плазмидой, содержащей NPM1H1p под контролем промотора CMV. Клетки собирали через 48 часов после трансфекции. Половину клеток подвергали лизису для анализа методом Вестерн-блот (фиг. 12), а другую половину инкубировали с коммерческим антителом С179 (Okuno Y, JVI 1994), которое связывается со стволовым участком белка НА (фиг. 13), и анализировали методом FACS. Анализ полного лизата клеток методом Вестерн-блот показал уникальную полосу в 70 кДа, которая соответствует слитому белку NP-M1 (фиг. 12). Это означает, что антиген полностью и правильно процессируется по сайту расщепления 2А. Из фиг. 13 видно, что высвобождаемый белок H1p затем экспонируется на клеточной мембране и правильно сворачивается, как это видно при использовании конформационно-зависимого антитела С179, которое связывается со стволовым участком НА. Соответственно, новый антиген FLU, состоящий из NP, M1 и H1p, правильно процессируется, а высвобождаемый белок НА экспонируется на клеточной поверхности и распознается конформационным антителом.
БИБЛИОГРАФИЯ
1. Ono and Freed (2005) Adv. Virus Res., 273:5419-5442.
2. Collins Ρ et al. (1996) Parainfluenza viruses, 1205-1241. In Fields et al. (ed.), Fields Virology. Lippincot-Raven Publishers, Philadelphia (PA) USA.
3. Shay DK et al. (1999) Bronchiolitis-associated hospitalizations among US children, 1980-1996. JAMA 282:1440-1446.
4. Simoes EA & Carbonell-Estrany X (2003) Pediatr Infect Dis J 22:S13-8; discussion S18-20.
5. Collins PL and Graham BS (2008) J Virol 82:2040-55.
6. Falsey AR et al. (2005) N Engl J Med 352:1749-59.
7. Fleming DM and Elliot AJ (2007) Eur Respir J 30:1029-31.
8. Cardenas S et al. (2005) Expert Rev Anti Infect Ther 3:719-26.
9. Kim HW et al. (1969) Amer J Epidemiol 89:422-434.
10. Delgado MF et al. (2009) Nat Med 15:34-41.
11. Graham BS et al. (1993) J Immunol 151:2032-2040.
12. Polack FP et al. (2002) J Exp Med 196:859-865.
13. Castilow EM and Varga SM (2008) Future Virol 3:445-454.
14. Hansen S et al. (2011) Nature 473:523-527.
15. Flatz L et al. (2010) Nature Med 16:339-345.
Перечень последовательностей - информация в свободной форме
|
|