Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ОКСИДОВ УРАНА
Вид РИД
Изобретение
Изобретение относится к радиохимической технологии и может быть использовано для получения порошка диоксида урана, идущего на изготовление керамических таблеток уранового и смешанного уран-плутониевого оксидного ядерного топлива для сборки тепловыделяющих элементов ядерных реакторов атомных электростанций, в том числе реакторных установок на быстрых нейтронах.
Известен способ получения диоксида урана [RU 2158971 C1, МПК G21C 3/62, опубл. 10.11.2000], по которому проводят гидролиз гексафторида урана, экстракцию урана из азотнокислого раствора 30% раствором трибутилфосфата в органическом разбавителе, его реэкстракцию в водный кислый раствор, осаждения полиураната аммония гидроксидом аммония при рН 6,6-8,0 с последующей фильтрацией, сушкой-прокалкой при 450-600°С и восстановлением в токе водорода при 680-720°С.
По другому способу [RU 2296106, МПК C01G 43/025, опубл. 27.03.2007] диоксид урана получают обработкой 25%-ным раствором аммиака, предварительно приготовленного водного раствора уранилнитрата с содержанием урана 50-100 г/дм3 с поддержанием значения рН не менее 6,6 при осаждении полиураната аммония. Далее следуют промежуточные стадии (фильтрация, сушка) с получением порошка полиураната аммония, его термическим разложением при 500°С и последующим восстановлением при 670-730°С, что приводит к получению диоксида урана.
Известен способ получения диоксида урана [Заявка ФРГ, N 2693977, МПК С01С 43/02, 1978], пригодного для изготовления таблетированного ядерного топлива, методом осаждения пероксида урана. Для получения пероксида урана через раствор уранилнитрата (~100 г/л по урану) пропускают смесь аммиака и воздуха для нейтрализации избыточной кислотности до рН среды ~2, затем в раствор добавляют до ~20 масс. % водного раствора перекиси водорода и молярного соотношение уран : перекись водорода = 1 : 1,5-3. Пероксид урана после отделения от маточного раствора прокаливают при температуре 500-800°С с последующим восстановлением до диоксида урана при 550-750°С.
Известен способ получения диоксида урана [RU 2415084, МПК C01G 43/025, опубл. 27.03.2011], согласно которому при добавлении к азотнокислому раствору уранилнитрата восстановителя - хлорида гидроксиламина и аммиачной воды до рН 7 получают, в зависимости от температурных условий, малорастворимые соединения: моногидрат диаквадигидроксиламинат уранила [UO2(Н2О)2(NH2O)2]·Н2О или безводный дигидроксиламинат уранила UO2(NH2O)2, термическое разложение которых приводит к образованию UO2 в инертной атмосфере в температурном интервале 200-400°С. Восстановителем U(VI) до U(IV) при термическом разложении указанного соединения служит координированный с ионом уранила лиганд гидроксиламина.
Во всех перечисленных способах исходным веществом является раствор уранилнитрата, из которого, добавляя соответствующие реагенты и используя многоступенчатых процессы, получают диоксид урана. По своей сути все описанные выше способы переработки раствора уранилнитрата являются способами многостадийной термической реагентной денитрации, осуществляемой в растворах и приводящей к образованию маточных растворов, подлежащих дальнейшей утилизации тем или иным способом. Это является их главным недостатком.
Известен способ [RU 2404925 С2, МПК C01G 43/01, опубл. 27.11.2010], при котором оксиды урана получают нагреванием смеси раствора уранилнитрата и аминоуксусной кислоты (глицин) при температуре 180-220°С в автоклавном режиме. Глицин берут в количестве 90-140% от стехиометрии. При этом в зависимости от соотношения уранилнитрат : аминокислота, могут образовываться UO3, U3O8 или UO2.
Недостатком и этого метода также является использование для термической денитрации водного раствора уранилнитрата с вытекающими отсюда последствиями по переработке остающегося маточного раствора, являющимся жидким радиоактивным отходом.
Наиболее близким к предлагаемому способу и выбранным в качестве прототипа является способ [US 4364859 G21F 9/08, опубл. 21.12.82], при котором оксиды урана получают денитрацией раствора нитрата уранила до 500 г/л по урану в две стадии: выпаривание раствора под действием СВЧ-излучения с последующей денитрацией полученного продукта в другом устройстве в атмосфере водорода с получением оксидов. Недостаток метода - необходимость использования двух стадий при получении диоксида урана, первая из которых связана с упариванием раствора.
Задачей, на решение которой направлено предлагаемое изобретение, является разработка технологичного способа получения порошков оксидов урана в одну стадию, что сокращает время проведения процесса.
Техническим результатом является упрощение способа получения оксидов урана за счет использования твердого уранилнитрата в виде соли гексагидрата нитрата уранила (ГНУ), в процессе микроволновой термической денитрации при взаимодействии с гидразингидратом с исключением образования водных растворов-отходов при проведении процесса, уменьшение времени проведения процесса.
Технический результат достигается в способе получения оксидов урана под действием микроволнового излучения путем нагревания уранилнитрата, причем используют твердый уранилнитрат, предварительно обработанный гидразингидратом, причем процесс проводят при температуре 600-1000°С в течение 10-30 минут.
Процесс осуществляют в восстановительной атмосфере смеси водорода с аргоном при содержании до 10 объемных % водорода с получением диоксида урана или процесс осуществляют в атмосфере воздуха с получением октооксидатриурана.
Способ осуществляется следующим способом.
Порошок оксида урана получают при микроволновом воздействии на твердый уранилнитрат, находящийся в кварцевом сосуде, через горловину которого проходит трубка для подачи в объем сосуда требуемой атмосферы. На поверхность порошка уранилнитрата вносится гидразингидрат при мольном соотношении ГНУ к N2H4, равном 1:0,05-0,15. Гидразингидрат является инициатором процесса поглощения СВЧ-излучения, и разогрев всей массы уранилнитрата происходит лавинообразно от точки внесения гидразингидрата. Процесс проводят в диапазоне 600-1000°С в течение 10-30 мин.
В этих условиях при подаче микроволнового излучения гидразингидрат выступает в роли инициатора процесса поглощения СВЧ-излучения и разогрев всей массы уранилнитрата происходит лавинообразно от точки внесения гидразингидрата. При этом уранилнитрат подвергается процессу денитрации с образованием оксидов урана.
При подаче в колбу восстановительной атмосферы смеси водорода с аргоном в процессе денитрации уранилнитрата сразу образуется диоксид урана.
Если процесс проводится при контакте с атмосферой воздуха, образуется триуранооктооксид.
Сущность заявляемого изобретения поясняется следующими таблицами и прилагаемыми иллюстрациями.
В табл. 1. приведены данные гравиметрических определений исследуемых образцов и расчетные величины потери веса при микроволновом термическом разложении ГНУ (1000°С) в восстановительной атмосфере.
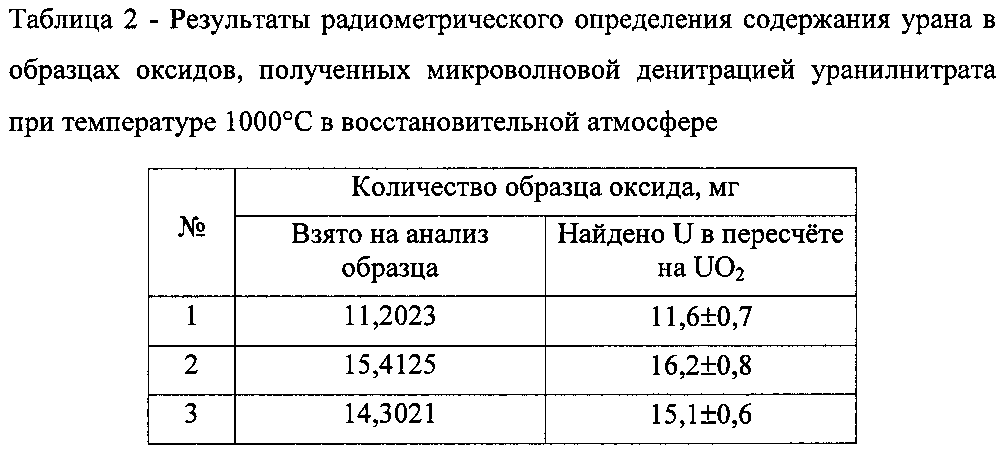
В табл. 2 даны результаты радиометрического определения содержания урана в образцах оксидов, полученных при микроволновой денитрации уранилнитрата при температуре 1000°С в восстановительной атмосфере.
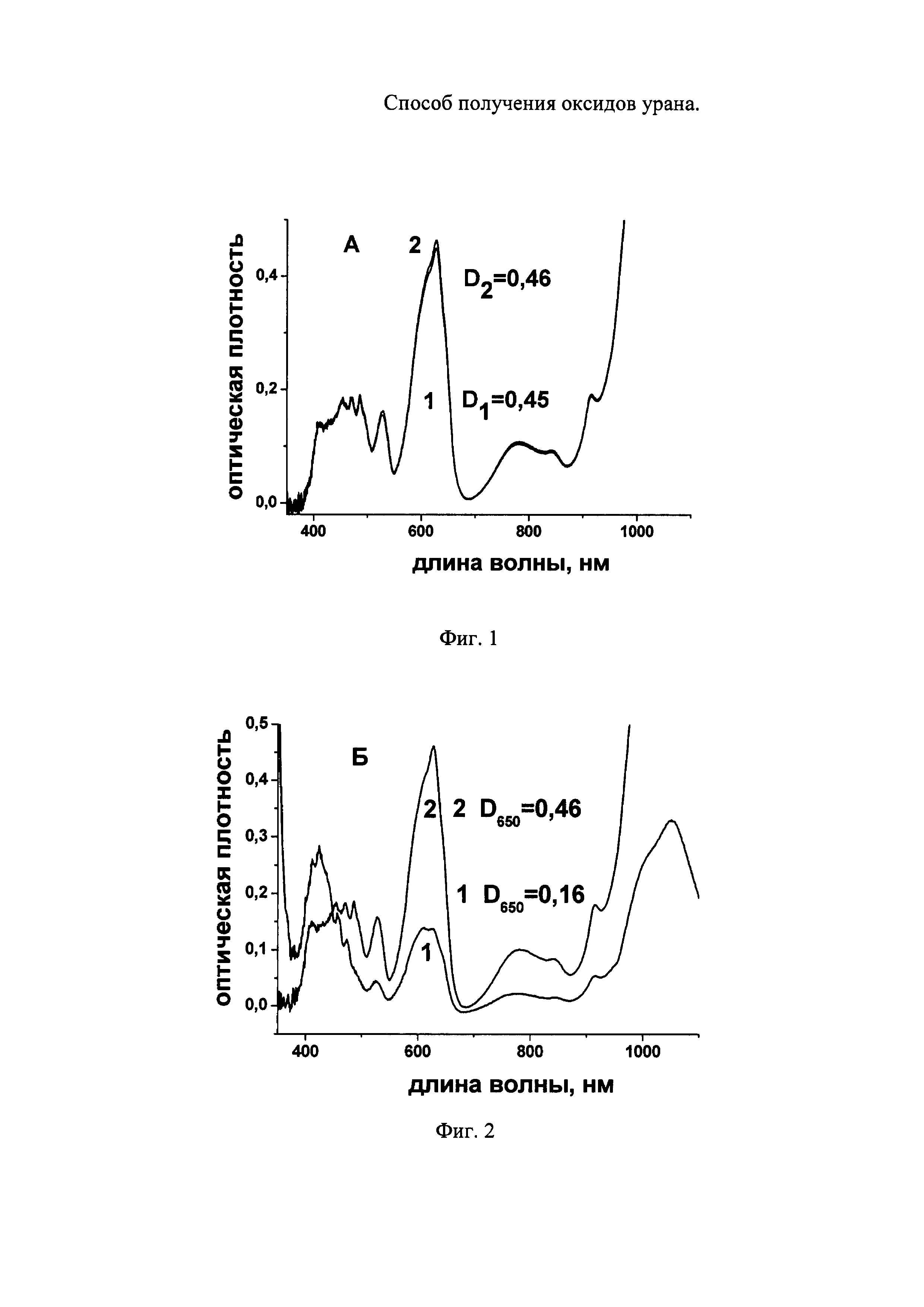
Для определения содержания валентных форм урана в полученных оксидах проводили их растворение в смеси 4 моль/л HCl с 0,05 моль/л HF.
После чего записывали спектр поглощения полученного раствора. Содержание U(IV) в растворе определяли при длине волны 650 нм. Для определения U(VI) в образце этот же раствор контактировали с амальгамой цинка, при этом ионы уранила восстанавливаются до U(IV). После этого повторно записывали спектр раствора и по разнице оптической плотности при длине волны 650 нм двух спектров определяли содержание U(VI) в анализируемом образце.
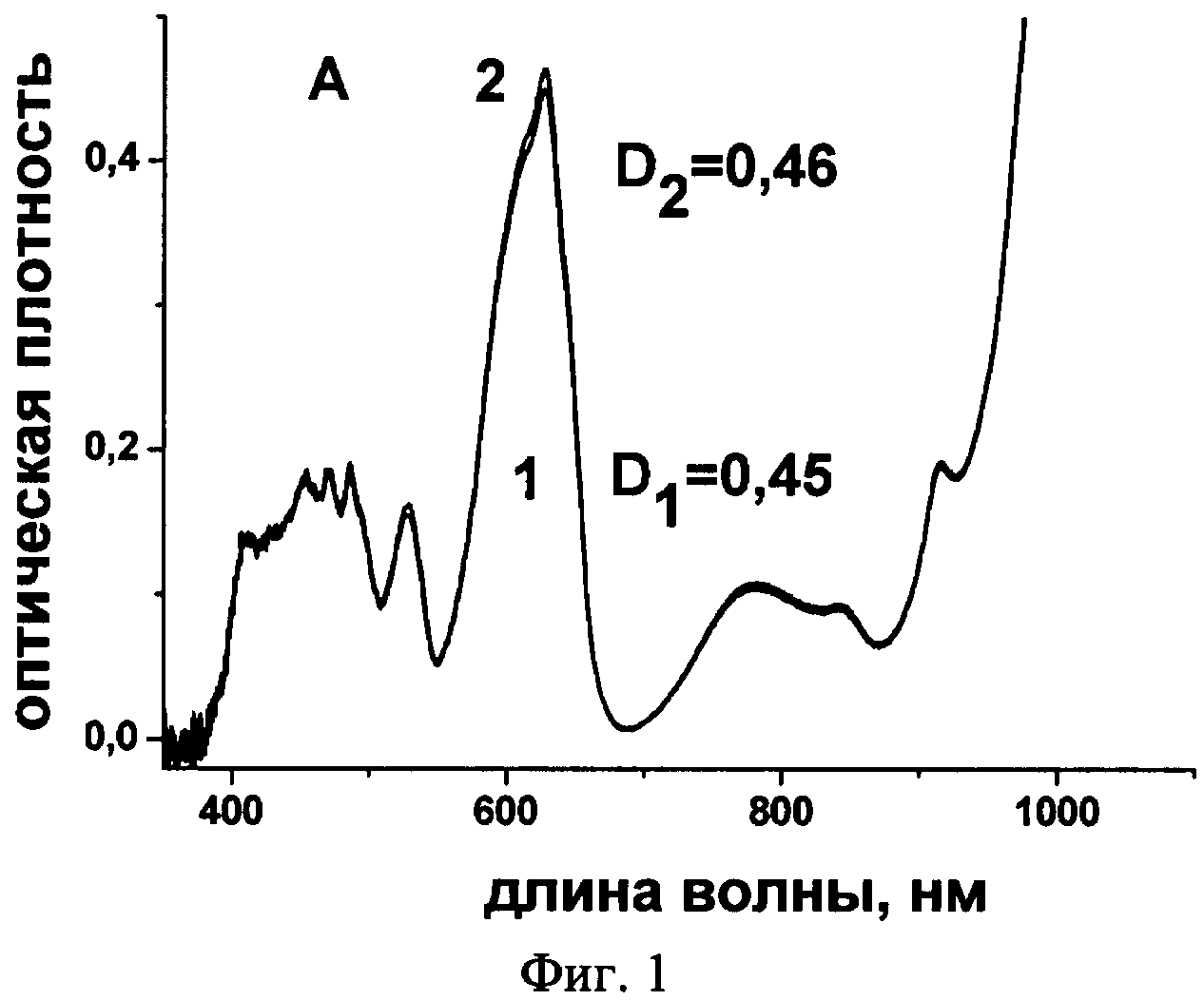
На фиг. 1 показаны спектры 1 и 2 раствора оксида, полученного при термическом разложении соли гексагидрата нитрата уранила (ГНУ) в восстановительной атмосфере до (1) и после контакта этого же раствора (2) с амальгамой цинка.
На фиг. 2 - спектры 1 и 2 раствора оксида, полученного при термическом разложении ГНУ в атмосфере воздуха до (1) и после контакта раствора (2) с амальгамой цинка.
Примеры реализации способов
Пример 1
Порошок соли гексагидрата нитрата уранила (ГНУ) 12 г помещали в реакционный кварцевый сосуд. Поверхность смачивали 0,1 мл гидразингидрата (мольное соотношение ГНУ к N2H4 составляет 1:0,1) и помещали в МВ-печь «SAMSUNG, модель MW83UR» с частотой излучения 2450 МГц и мощностью 800 Вт. Через тефлоновую трубку, проходящую через горловину колбы, во внутренний объем печи подавали смесь водорода с аргоном, содержащую до 10 объемных % Н2 для создания восстановительной атмосферы. Процесс микроволновой денитрации начинали кратковременной ~2-минутной подачей излучения при мощности 800 Вт, после чего переходили на 10-минутный режим излучения при мощности 300 Вт, при котором температура образующегося продукта достигала 1000°С. В этом режиме магнетрон включался на 12 сек, затем отключался на 18 сек, в течение которых продукт остывал. В общей сложности процесс длился 10 мин.
Образовавшийся в денитрационном процессе продукт анализировали методами гравиметрии, спектрофотометрии и радиометрии. Полученные данные приведены в табл. 1 и 2 и на фиг. 1. Как видно из таблицы 1, найденная потеря веса всех обработанных образцов соответствует теоритическому значению перехода UO2(NO3)2·6H2O в UO2. Общее содержание урана в полученных образцах также соответствует химической форме UO2. Спектр раствора (фиг. 1 кривая А) незначительно изменился после обработки раствора с амальгамой цинка. Все выполненные аналитические измерения однозначно свидетельствуют о получении диоксида урана в процессе денитрационного термолиза в восстановительной атмосфере.

Пример 2
Способ осуществляли как в примере 1 в том же микроволновом режиме термической денитрации образца, однако процесс проводили в условиях доступа атмосферы воздуха в реакционный объем колбы. Из разницы оптических плотностей раствора (кривая А фиг. 2) полученного образца и его контакта с амальгамой цинка (кривая Б фиг. 2) определено, что содержание U(VI) близко к теоретическому содержанию U(VI) в оксиде U3O8.
Пример 3
Порошок соли гексагидрата нитрата уранила (ГНУ) 67 г помещали в реакционный кварцевый сосуд. Поверхность смачивали 0,25 мл гидразингидрата (мольное соотношение ГНУ к N2H4 составляет 1:0,05) и помещали в МВ-печь. Через тефлоновую трубку, проходящую через горловину колбы, во внутренний объем печи подавали смесь водорода с аргоном, содержащую до 10 объемных % Н2 для создания восстановительной атмосферы. Процесс микроволновой денитрации проводили при мощности 300 Вт при котором температура образующегося продукта достигала 600°С. В ходе процесса денитрации через каждые 10 минут проводили остановку и перемешивание полученного продукта. Общее время СВЧ-обработки составило 30 минут. По результатам анализа полученный продукт состоял на 99% из диоксида урана.
Пример 4.
Способ осуществляли как в примере 3, но время СВЧ-обработки составляло 15 минут, перемешивание не осуществлялось. По результатам анализа полученный порошок содержал 85% UO2.
При проведении процесса при температуре менее 600°С происходит неполное разложение уранилнитрата и восстановление до диоксида урана. Уменьшение температуры менее 10 минут приводит к замедлению скорости восстановления.
Увеличение времени денитрации выше 30 минут и температуры более 1000°С нецелесообразно в связи с экономически необоснованными затратами энергии и расхода восстановительной атмосферы водорода с аргоном.
Таким образом, заявляемый способ приводит к быстрому образованию целевого продукта без каких-либо промежуточных стадий и без возникновения растворов-отходов, за исключением образования газовой фазы с парами воды, аммиака и окислов азота.