Результат интеллектуальной деятельности: ПОЛИПЕПТИДЫ, ОБЛАДАЮЩИЕ ЦЕЛЛЮЛАЗНОЙ АКТИВНОСТЬЮ
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Данная заявка претендует на приоритет согласно 35 U.S.C. §119 в отношении предварительной заявки США серийный №61/166993, поданной 6 апреля 2009, и 61/177882, поданной 13 мая 2009, описания которых включены в данную заявку посредством ссылки.
УКАЗАНИЕ ОТНОСИТЕЛЬНО ИССЛЕДОВАНИЯ, ФИНАНСИРУЕМОГО ИЗ ФЕДЕРАЛЬНОГО БЮДЖЕТА
Правительство США обладает определенными правами на данное изобретение в соответствии с Грантом № GM 068664, предоставленным Национальным институтом здравоохранения, и Грантом № DAAD 19-03-0D-0004, предоставленным ARO - US Army Robert Morris Acquisition Center (Центром материально-технического обеспечения армии США Роберта Морриса).
ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к биомолекулярной инженерии и конструированию, и к белкам и нуклеиновым кислотам, полученным методами биоинженерии.
ПРЕДШЕСТВУЮЩИЙ УРОВЕНЬ ТЕХНИКИ
Качество целлюлазных смесей в процессах переработки биомассы зависит от многих свойств фермента, включая стабильность, ингибирование продуктом, синергизм среди различных целлюлазных ингредиентов, продуктивное связывание по сравнению с непродуктивной адсорбцией и рН зависимость, в дополнение к физическому состоянию и композиции целлюлозного субстрата. С учетом многовариантной природы гидролиза целлюлозы желательно иметь разнообразные целлюлазы для выбора из них с целью оптимизации ферментных препаратов для различных областей применения и исходного сырья.
КРАТКОЕ ИЗЛОЖЕНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
В изобретении предложены рекомбинантные полипептиды, обладающие целлюлазной активностью и повышенной термостойкостью и активностью по сравнению с белком дикого типа. В изобретении предложено и продемонстрировано, что химеры и нативные ферменты CBHII, имеющие мутацию Cys на Ser на С-конце (например, примерно в аминокислоте 310-315 в зависимости от нативной последовательности белка, см., например, SEQ ID NO:2 и 4), гидролизуют более твердую целлюлозу, чем нативный фермент, в анализах на долгосрочный гидролиз.
В изобретении предложен рекомбинантный полипептид, содержащий замену C→S в С-концевой области в мотиве, включающем последовательность GECDG (SEQ ID NO:2 от 312-316), где вариант включает повышенную термостойкость и целлюлазную активность по сравнению с целлобиогидролазой дикого типа. Например, в изобретении предложены полипептиды, обладающие повышенной термостойкостью и целлюлазной активностью, включающие последовательность, которая по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:2, содержащей C314S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:4, содержащей C311S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:12, содержащей C310S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:13, содержащей C312S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:14, содержащей C314S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:15, содержащей C315S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:16, содержащей C313S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:17, содержащей C311S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:19, содержащей C313S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:21, содержащей C312S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:22, содержащей C311S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:64, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:65, содержащей C407S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:66, содержащей C394S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:67, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:68, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:69, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:70, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:71, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:72, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:73, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:74, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:75, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:76, содержащей C407S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:77, содержащей C394S; или по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:78, содержащей C412S, где вышеуказанные полипептиды обладают целлюлазной активностью и улучшенной термостойкостью по сравнению с соответствующим исходным белком дикого типа, в котором отсутствует мутация Cys→Ser.
В изобретении также предложены по существу очищенные полипептиды, которые либо продуцированы рекомбинантным путем, либо получены синтетическим путем или созданы иным неприродным путем, где полипептид содержит последовательность, как изложено ниже, имеющую 1-10, 10-20 или 20-30 консервативных аминокислотных замен за исключением положения, идентифицированного ниже, где присутствует замена C→S: SEQ ID NO:2, содержащую C314S; SEQ ID NO:4, содержащую C311S; SEQ ID NO:12, содержащую C310S; SEQ ID NO:13, содержащую C312S; SEQ ID NO:14, содержащую C314S; SEQ ID NO:15, содержащую C315S; SEQ ID NO:16, содержащую C313S; SEQ ID NO:17, содержащую C311S; SEQ ID NO:19, содержащую C313S; SEQ ID NO:21, содержащую C312S; SEQ ID NO:22, содержащую C311S; SEQ ID NO:64, содержащую C400S; SEQ ID NO:65, содержащую C407S; SEQ ID NO:66, содержащую C394S; SEQ ID NO:67, содержащую C400S; SEQ ID NO:68, содержащую C400S; SEQ ID NO:69, содержащую C400S; SEQ ID NO:70, содержащую C400S; SEQ ID NO:71, содержащую C400S; SEQ ID NO:72, содержащую C400S; SEQ ID NO:73, содержащую C400S; SEQ ID NO:74, содержащую C400S; SEQ ID NO:75, содержащую C400S; SEQ ID NO:76, содержащую C407S; SEQ ID NO:77, содержащую C394S; или SEQ ID NO:78, содержащую C412S.
В изобретении предложен рекомбинантный полипептид, содержащий последовательность, выбранную из группы, состоящей из: (а) полипептида, обладающего по меньшей мере 85% или большей идентичностью SEQ ID NO:2, имеющей Ser в положении 314, где этот полипептид обладает целлюлазной активностью; (b) полипептида, обладающего по меньшей мере 70% или большей идентичностью SEQ ID NO:4, имеющей Ser в положении 311, где этот полипептид обладает целлюлазной активностью; (с) полипептида, обладающего 70% или большей идентичностью последовательности, выбранной из группы, состоящей из: (i) SEQ ID NO:12 и имеющей Ser в положении 310, (ii) SEQ ID NO:13 и имеющей Ser в положении 312, (iii) SEQ ID NO:14 и имеющей Ser в положении 314, (iv) SEQ ID NO:15 и имеющей Ser в положении 315, (v) SEQ ID NO:16 и имеющей Ser в положении 313, (vi) SEQ ID NO:17 и имеющей Ser в положении 311, (vii) SEQ ID NO:19 и имеющей Ser в положении 313, (viii) SEQ ID NO:21 и имеющей Ser в положении 312, и (ix) SEQ ID NO:22 и имеющей Ser в положении и имеющей Ser в положении 311, и где каждый из вышеуказанных полипептидов обладает целлюлазной активностью; и (d) химерного полипептида, содержащего по меньшей мере два домена от двух различных исходных целлобиогидролазных полипептидов, где эти домены содержат от N- к С-концу: (сегмент 1)-(сегмент 2)-(сегмент 3)-(сегмент 4)-(сегмент 5)-(сегмент 6)-(сегмент 7)-(сегмент 8); где: сегмент 1 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка примерно 1 до примерно x1 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 2 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка x1 до примерно x2 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 3 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка x2 до примерно x3 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 4 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка x3 до примерно x4 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 5 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка примерно x4 до примерно x5 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 6 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка x5 до примерно x6 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 7 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка x6 до примерно х7 SEQ ID NO:2 (″1″) или SEQ ID NO:4 (″2″); и сегмент 8 содержит последовательность, по меньшей мере на 50-100% идентичную от аминокислотного остатка x7 до примерно x8 SEQ ID NO:2 (″1″) или SEQ ID NO:4 (″2″); где x1 представляет собой остаток 43, 44, 45, 46 или 47 SEQ ID NO:2, либо остаток 42, 43, 44, 45 или 46 SEQ ID NO:4 или SEQ ID NO:6; x2 представляет собой остаток 70, 71, 72, 73 или 74 SEQ ID NO:2, либо остаток 68, 69, 70, 71, 72, 73 или 74 SEQ ID NO:4 или SEQ ID NO:6; x3 представляет собой остаток 113, 114, 115, 116, 117 или 118 SEQ ID NO:2, либо остаток 110, 111, 112, 113, 114, 115 или 116 SEQ ID NO:4 или SEQ ID NO:6; x4 представляет собой остаток 153, 154, 155, 156 или 157 SEQ ID NO:2, либо остаток 149, 150, 151, 152, 153, 154, 155 или 156 SEQ ID NO:4 или SEQ ID NO:6; x5 представляет собой остаток 220, 221, 222, 223 или 224 SEQ ID NO:2, либо остаток 216, 217, 218, 219, 220, 221, 222 или 223 SEQ ID NO:4 или SEQ ID NO:6; x6 представляет собой остаток 256, 257, 258, 259, 260 или 261 SEQ ID NO:2, либо остаток 253, 254, 255, 256, 257, 258, 259 или 260 SEQ ID NO:4 или SEQ ID NO:6; x7 представляет собой остаток 312, 313, 314, 315 или 316 SEQ ID NO:2, либо остаток 309, 310, 311, 312, 313, 314, 315 или 318 SEQ ID NO:4; и х8 представляет собой аминокислотный остаток, соответствующий С-концу полипептида, имеющего последовательность SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO:6, где химерный полипептид содержит Ser в положении 314 SEQ ID NO:2 или в положении 311 SEQ ID NO:4, и где химерный полипептид обладает целлюлазной активностью и улучшенной термостойкостью и/или рН стабильностью по сравнению с полипептидом СВН II, содержащим SEQ ID NO:2, 4 или 6. В одной форме осуществления рекомбинантного полипептида сегмент 1 содержит аминокислотные остатки от примерно 1 до примерно x1 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″) и имеет 1-10 консервативных аминокислотных замен; сегмент 2 составляют аминокислотные остатки от примерно x1 до примерно x2 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 3 составляют аминокислотные остатки от примерно x2 до примерно x3 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 4 составляют аминокислотные остатки от примерно x3 до примерно x4 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 5 составляют аминокислотные остатки от примерно x4 до примерно x5 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 6 составляют аминокислотные остатки от примерно x5 до примерно x6 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 7 составляют аминокислотные остатки от примерно х6 до примерно x7 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; и сегмент 8 составляют аминокислотные остатки от примерно x7 до примерно x8 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен за исключением положения 314 SEQ ID NO:2, положения 311 SEQ ID NO:4 или 313 SEQ ID NO:6. Еще в одной другой форме осуществления химерный полипептид содержит последовательность, которая по меньшей мере на 80%, 90%, 95%, 98% или 99% идентична последовательности, выбранной из группы, состоящей из SEQ ID NO:12-62 и 63.
В изобретении также предложен рекомбинантный полипептид, состоящий из последовательности, как представлено в SEQ ID NO:12-62 или 63.
В изобретении также предложен полинуклеотид, кодирующий любой из полипептидов, как описано выше, векторы, содержащие полинуклеотид, и клетки-хозяева, содержащие полинуклеотид или вектор.
В изобретении также предложен ферментный препарат, содержащий полипептид по изобретению по существу в очищенной форме или в виде части клеточного лизата.
В изобретении также предложен способ обработки биомассы, содержащей целлюлозу, включающий приведение биомассы в контакт с полипептидом или ферментным препаратом по изобретению.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
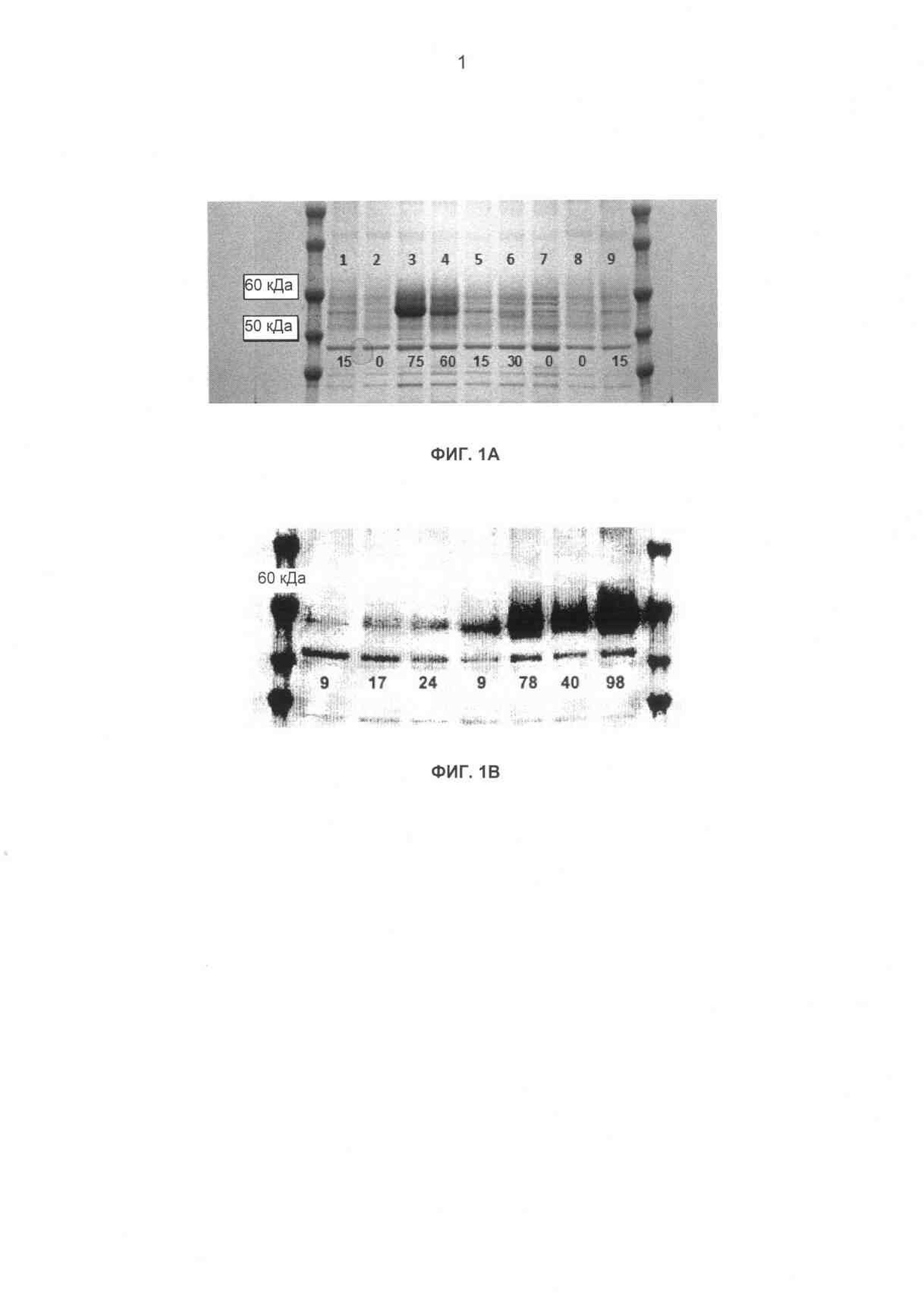
Фиг.1А-В Электрофорез в ДСН-ПААГ супернатантов дрожжевой экспрессионной культуры родительского гена-кандидата СВН II. (А) Дорожки геля (слева направо): 1 - Н. jecorina, 2 - пустой вектор, 3 - H. insolens, 4 - С. thermophilum, 5 - Н. jecorina (второй повтор), 6 - Р. chrysosporium, 7 - Т. emersonii, 8 - пустой вектор (второй повтор), 9 - Н. jecorina (третий повтор). Цифрами внизу геля представлена концентрация восстанавливающего сахара (мкг/мл), присутствующего в реакционной смеси анализа гидролиза PASC после 2 ч при 50°С. Последующее сравнение ДСН-ПААГ со стандартом БСА дало возможность оценки уровня экспрессии Н. insolens как 5-10 мг/л. (В) Показан анализ с помощью электрофореза в ДСН-ПААГ супернатантов экспрессионной культуры S. cerevisiae СВН II. Полосы СВН II видны непосредственно ниже стандарта молекулярной массы 60 кДа. Дорожки, слева направо, 1 - дикий тип Н. jeco, 2 - Н. jeco B7P3, 3 - Н. jeco C311S, 4 - дикий тип С. ther, 5 - дикий тип Н. inso, 6 - Н. inso B7P3, 7 - Н. inso C314S. Цифрами обозначены мкг эквиваленты глюкозы/мл объема реакционной смеси на мл эквивалент супернатанта экспрессионной культуры в ДСН-ПААГ, продуцированной в течение 100-минутной инкубации с PASC (1 мг/мл) при 50°С в 50 мМ ацетате натрия, рН 4,8. Значения для дорожек 1-4 разделены на 2 для коррекции на двукратный объем нанесенного концентрированного супернатанта культуры, где отсутствие этой коррекции сделало бы значения удельной активности ферментов Н. insolens искусственно низкими.
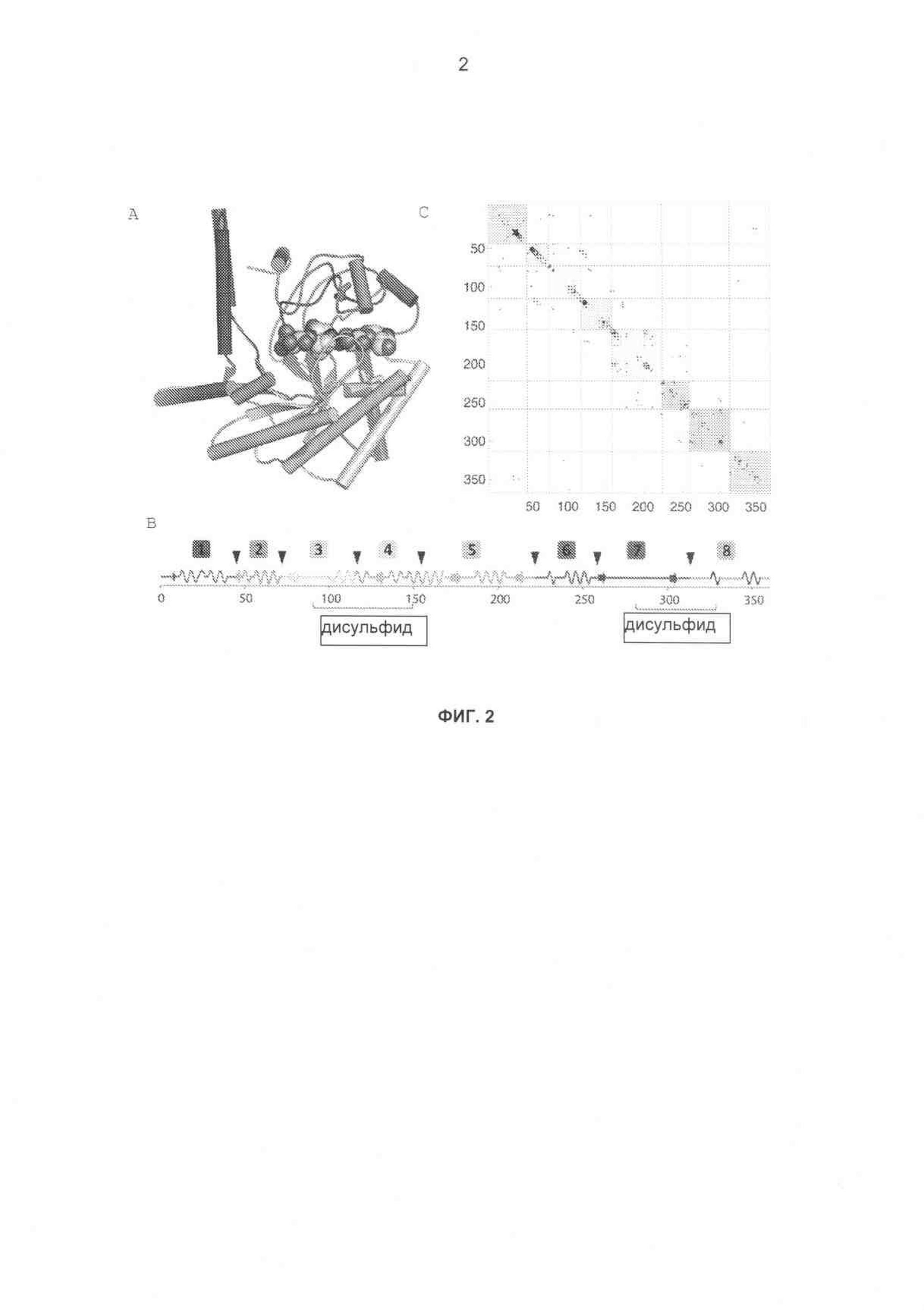
На фиг.2А-С показаны иллюстрации границ блоков библиотеки химер СВН II. (А) ленточная диаграмма каталитического домена Н. insolens СВН II с блоками, различающимися по цвету. Фермент СВН II образует комплекс с ингибитором гликозидазы изофагомином целлобиозного происхождения. (В) Линейное представление каталитического домена Н. insolens, показывающее элементы вторичной структуры, дисульфидные связи и деления на блоки, обозначенные черными стрелками. (С) Карта контактов боковых цепей, обозначающая контакты (тяжелые атомы боковых цепей в пределах 4,5 Å), которые могут быть разрушены посредством рекомбинации. Большинство разрушенных контактов возникает между блоками, следующими друг за другом.
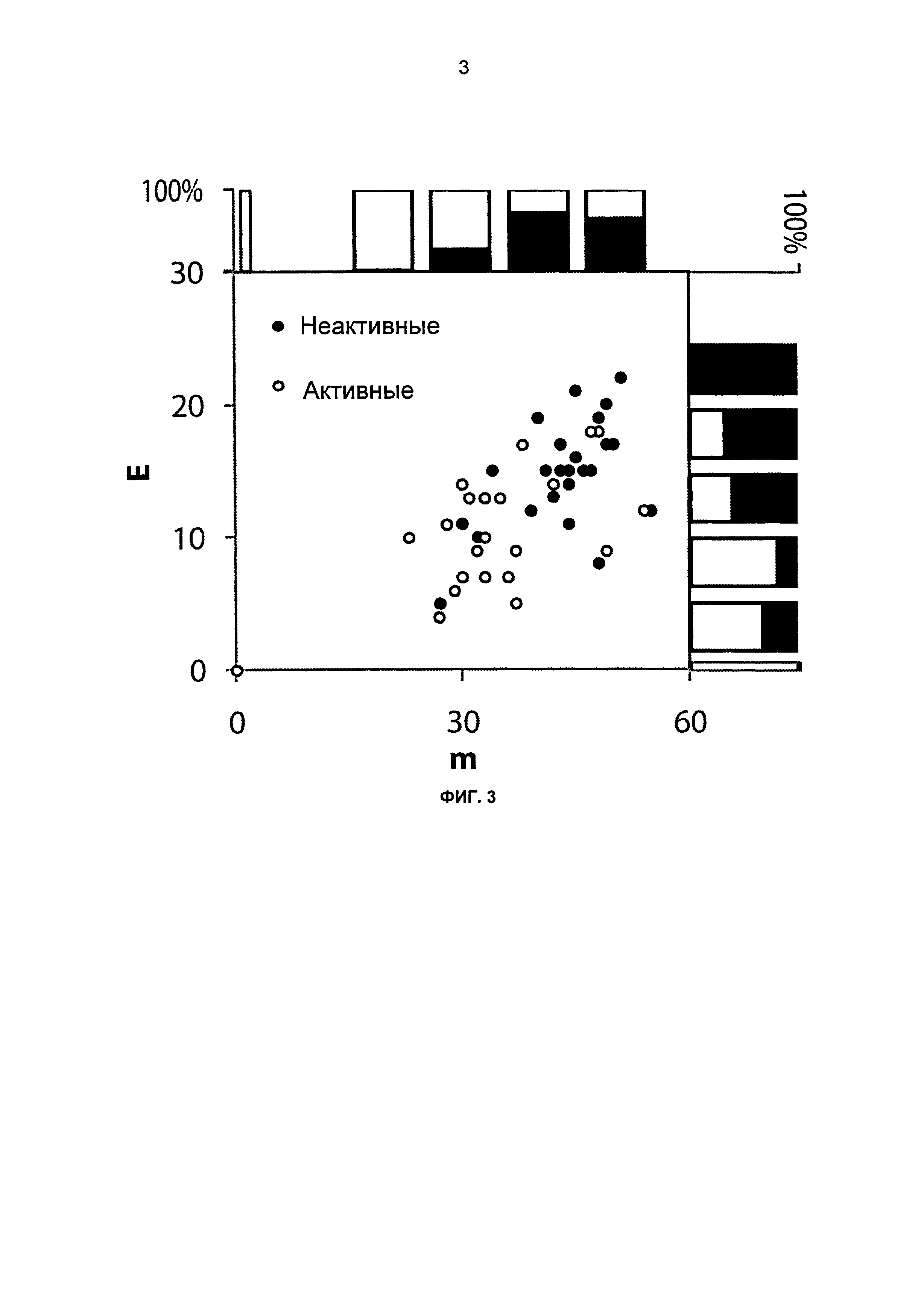
На фиг.3 показано число разрушенных контактов (Е) и число мутаций по отношению к ближайшему родителю (m) для 23 секретированных/активных и 15 несекретированных/неактивных химер серии образцов.
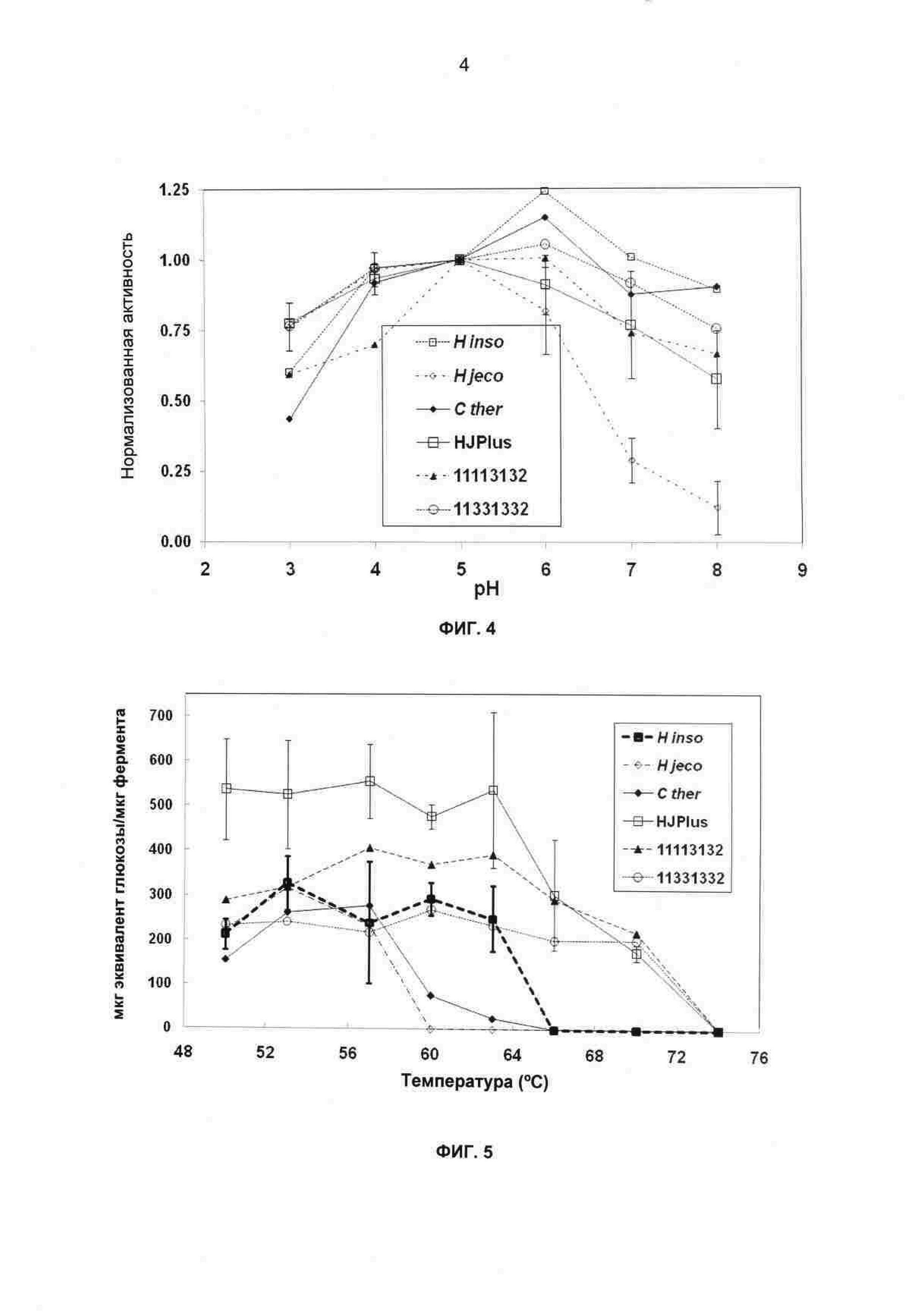
На фиг.4 показана удельная активность, нормализованная на рН 5,0, как функция рН для родительских ферментов СВН II и трех термостойких химер. Представленные данные представляют собой средние для двух повторов, где ″усы″ для значений HJPlus и Н. jeco обозначают исследования для двух независимых испытаний. 16-часовая реакция, 300 мкг фермента/г PASC, 50°С, буфер 12,5 мМ цитрат натрия/12,5 мМ фосфат натрия при рН, как показано.
На фиг.5 показаны результаты анализа долговременного гидролиза целлюлозы (мкг эквиваленты восстанавливающего сахара глюкозы/мкг фермента СВН II) для родителей и термостойких химер на протяжении диапазона температур. ″Усы″ указывают стандартные ошибки для трех повторов ферментов СВН II HJPlus и Н. insolens. 40-часовая реакция, 100 мкг фермента/г PASC, 50 мМ ацетат натрия, рН 4,8.
На фиг.6 показаны нормализованные остаточные активности для оценки серии химер после 12-часовой инкубации при 63°С. Остаточные активности для ферментов СВН II в концентрированных супернатантах культуры определены в 2-часовом анализе с PASC в качестве субстрата, 50°С, буфер 25 мМ ацетат натрия, рН 4,8.
Фиг.7 Карта родительского и химерного экспрессионного вектора для фермента СВН II Yep352/PGK91-1-ss. Изображенный вектор содержит ген дикого типа Н. jecorina ceI6a (фермент СВН II). Как для химерного, так и для родительского фермента СВН II аминокислотная последовательность CBD/линкера, следующая за сайтом ss Lys-Arg Kex2, представляет собой:
ASCSSVWGQCGGQNWSGPTCCASGSTCVYSNDYYSQCLPGAASSSSSTRAA
STTSRVSPTTSRSSSATPPPGSTTTRVPPVGSGTATYS (SEQ ID NO:8).
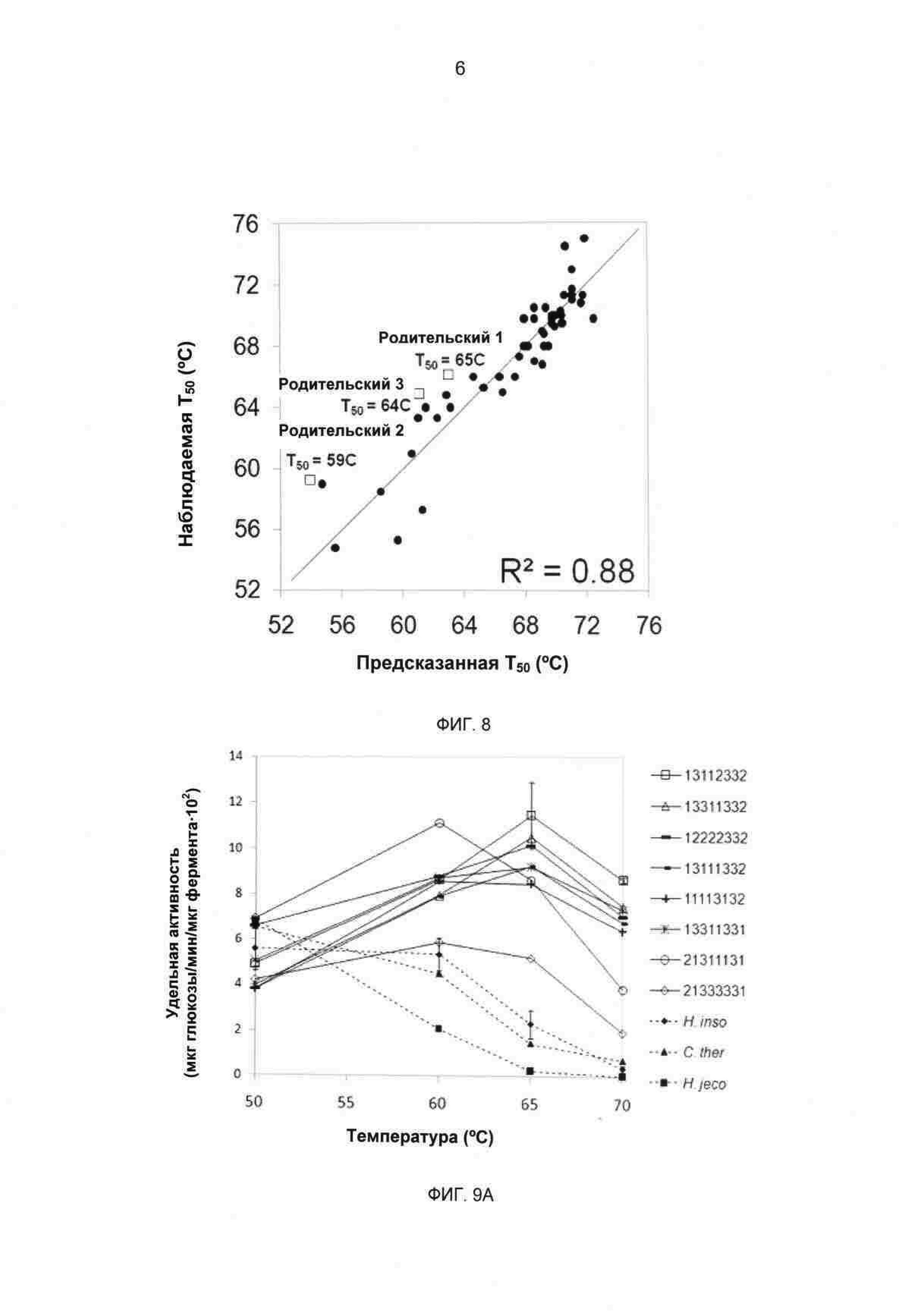
На фиг.8 показаны наблюдаемые и предсказанные значения T50 для родительских СВН II и 51 химерного СВН II. Кривая обозначает уравнение модели линейной регрессии (параметры в таблице 7). Значения Т50 родительского СВН II обозначены в виде квадратов.
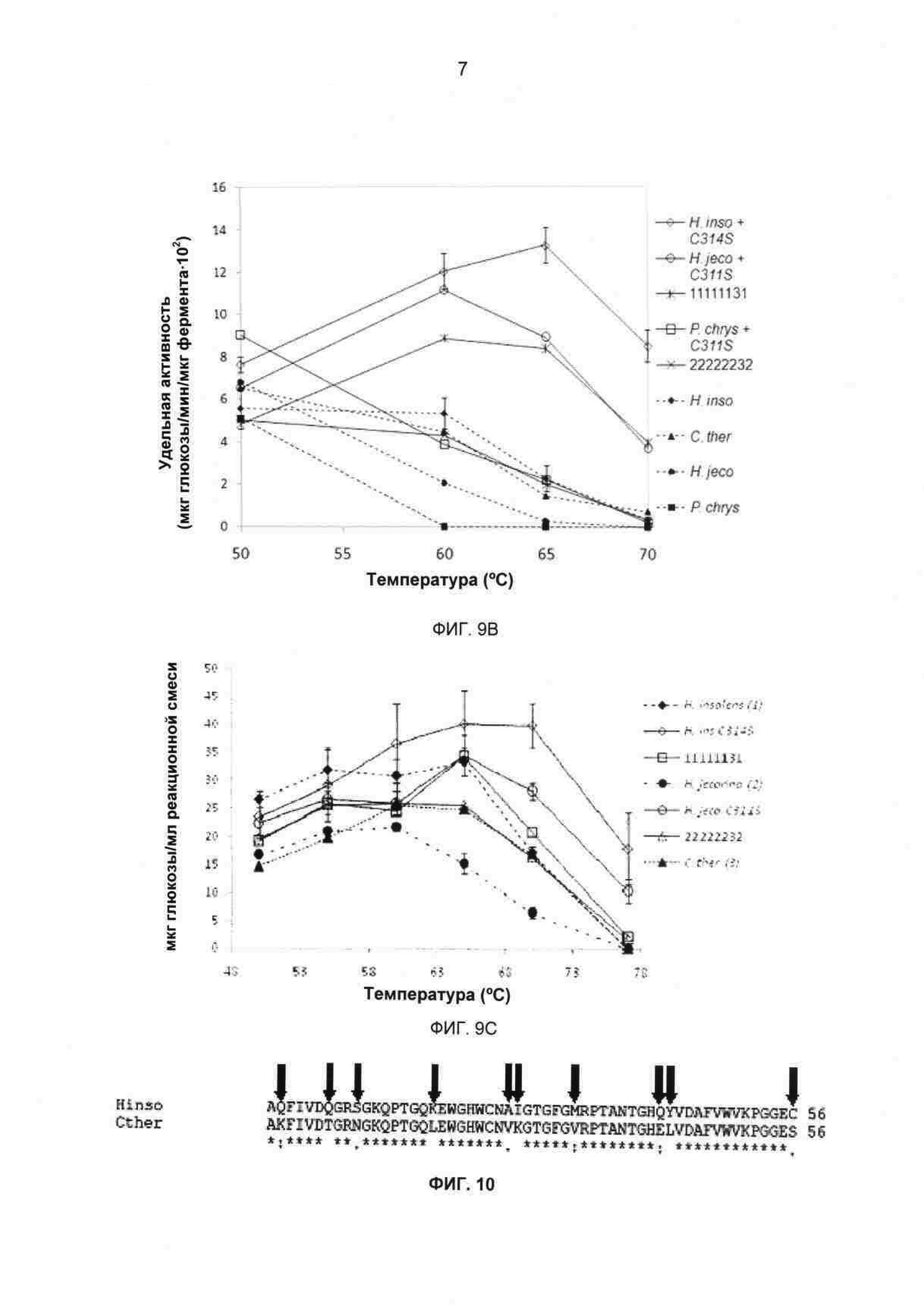
На фиг.9А-С показаны удельные активности СВН II в отношении Avicel в зависимости от температуры, (а) удельные активности родительского и химерного СВН II. (b) удельные активности родительского СВН II, мутанта C311S химеры В7Р3 с заменой одного блока. Реакции проводили в течение 16 часов в 50 мМ ацетате натрия, рН 4,8, при концентрации Avicel 15 мг/мл. (с) активности родительского СВН II, одиночного точечного мутанта химеры с заменой одного блока (мкг/глюкоза/мл реакционной смеси) в отношении Avicel в зависимости от температуры. Реакции проводили в течение 150 минут в 50 мМ ацетате натрия, рН 4,8, при концентрации Avicel 15 мг/мл. Супернатанты дрожжевой культуры СВН II дозировали до достижения приблизительно эквивалентных концентраций продукта восстанавливающего сахара при 55°С. Представленные данные представляют собой средние двух независимых повторов, где усы указывают значения активности двух повторов для каждой температурной точки.
На фиг.10 показано множественное выравнивание последовательностей ClustalW для блока 7 от родителя 1, Н. insolens, и родителя 3, C.thermophilum. Стрелками обозначены остатки, измененные в реверсионных мутантах.
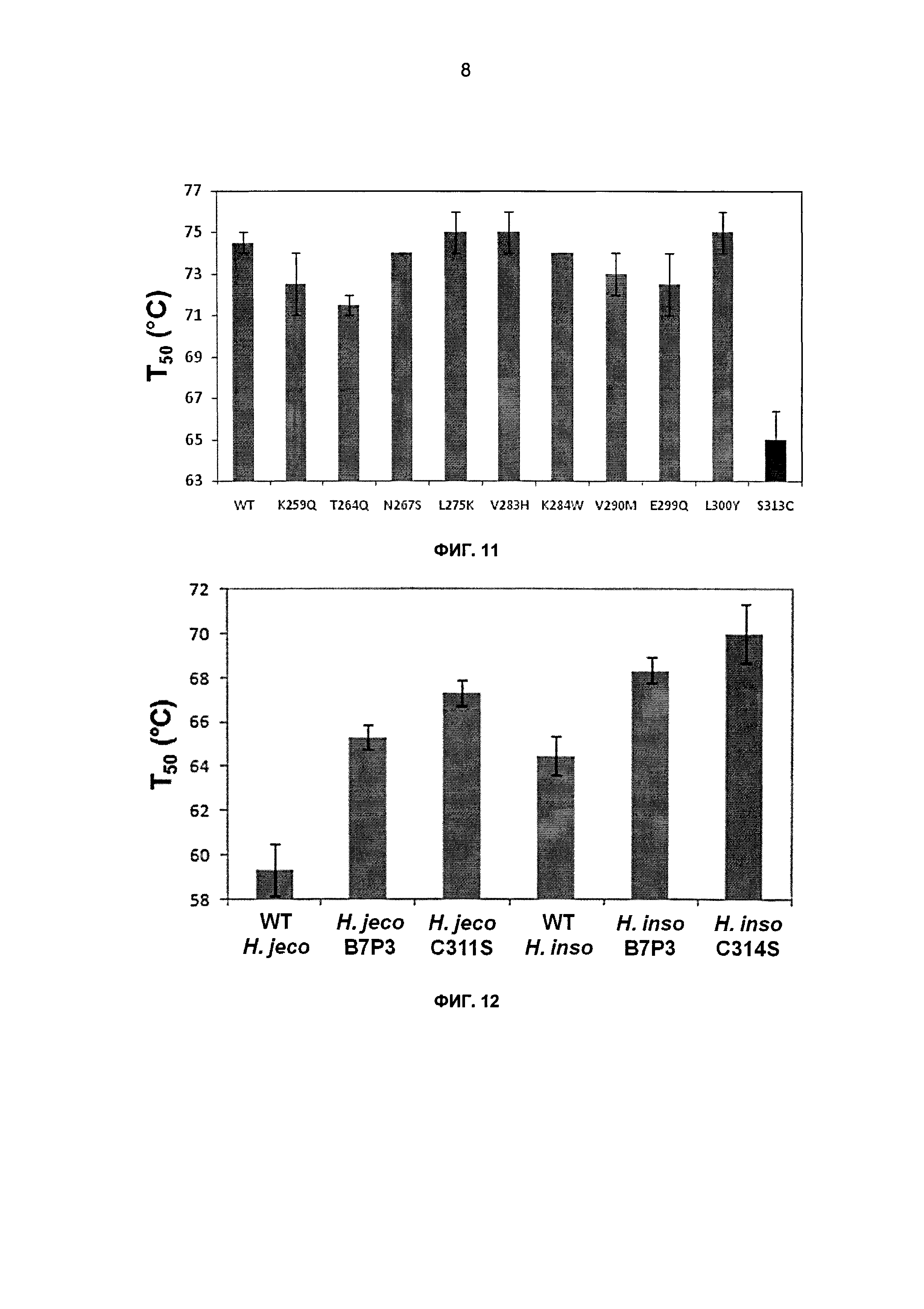
На фиг.11 показаны значения Т50 для точечных мутантов химеры 21111331. Значения показаны в виде среднего двух независимых повторов, усы указывают значения Т50 двух повторов для каждого точечного мутанта. Инактивацию осуществляли в течение 10 минут при тестируемой температуре в 50 мМ натрийацетатном буфере, рН 4,8. Остаточную активность определяли путем инкубации с 1 г/л целлюлозы, набухшей в фосфорной кислоте (PASC), в вышеуказанном буфере в течение 100 минут при 50°С.
На фиг.12 показаны значения Т50 для родительских СВН II Н. insolens и Н. jecorina, одиночных точечных мутантов Ser химер с заменой блока В7Р3. Значения показаны в виде среднего трех независимых повторов, усы указывают одно стандартное отклонение для каждого СВН II. Инактивацию осуществляли в течение 10 минут при тестируемой температуре в 50 мМ натрийацетатном буфере, рН 4,8. Остаточную активность определяли путем инкубации с 1 г/л целлюлозы, набухшей в фосфорной кислоте (PASC), в вышеуказанном буфере в течение 100 минут при 50°С.
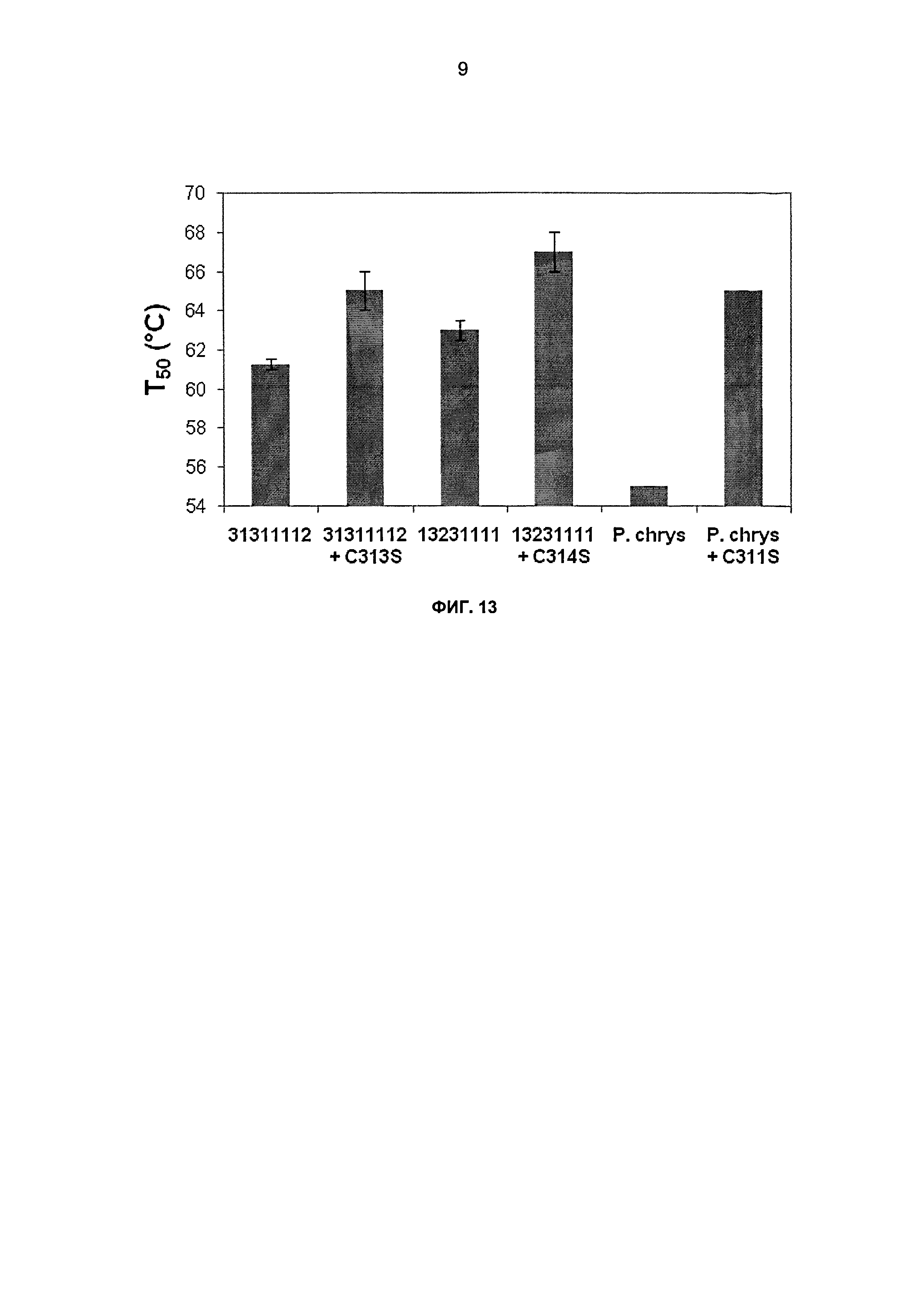
На фиг.13 показаны значения Т50 для химер СВН II 31311112, 13231111 и каталитического домена СВН II дикого типа из Р. chrysosporium (слитого с Н. jecorina CBM), гетерологично секретированных из S. cerevisiae. Значения показаны в виде двух независимых повторов, где усы показывают значения для каждого испытания. Инактивацию осуществляли в течение 10 минут при тестируемой температуре в 50 мМ натрийацетатном буфере, рН 4,8. Остаточную активность определяли путем инкубации с 1 г/л целлюлозы, набухшей в фосфорной кислоте (PASC), в вышеуказанном буфере в течение 100 минут при 50°С.
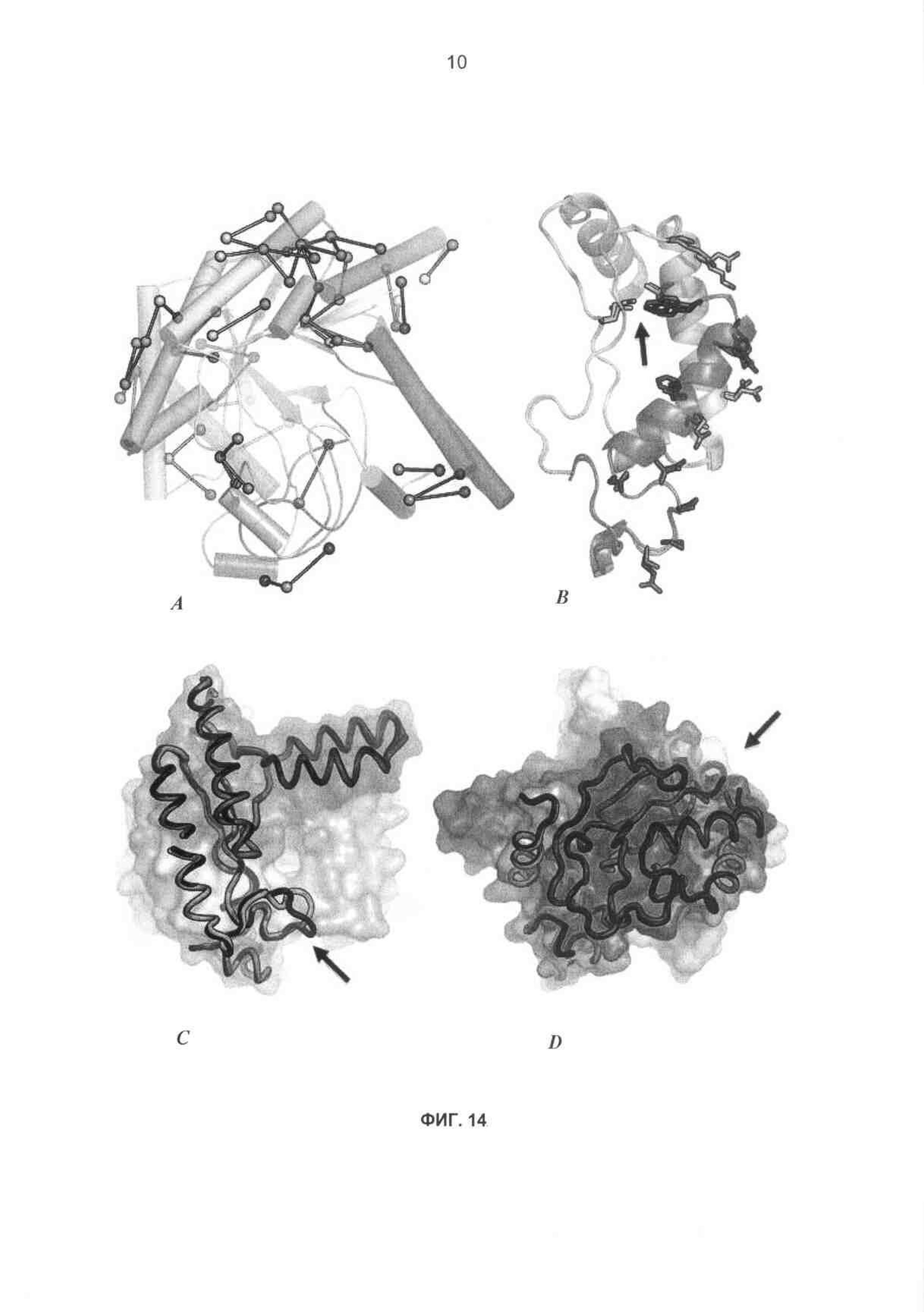
На фиг.14A-D показаны границы раздела блоков рекомбинации СВН II. (а) сайты между блоками, где возможны новые неродительские пары остатков (соединенные круги), обычно экспонированы на поверхности, потенциально давая возможность растворителю экранировать взаимодействия. (b) Примерная граница раздела (В5-В6) иллюстрирует консервативность каркаса (изображения выровненных Н. jecorina и Н. insolens), вариабельные остатки на поверхности и сравнительно редкую возможность новой углубленной пары при остатках 173 и 253 (стрелка), (с) блоки 1-4 от Н. jecorina (черный рисунок) совпадают с родственными блоками Н.insolens (рисунок с цветовой маркировкой) без больших отклонений, хотя наблюдается перемещение, обусловленное связыванием субстрата (стрелка), в участке ВЗ (желтый), (d) родственные блоки 5-8 также являются сходными, хотя вставка-делеция на стыке В6, В7 (стрелка) потребует конформационного изменения.
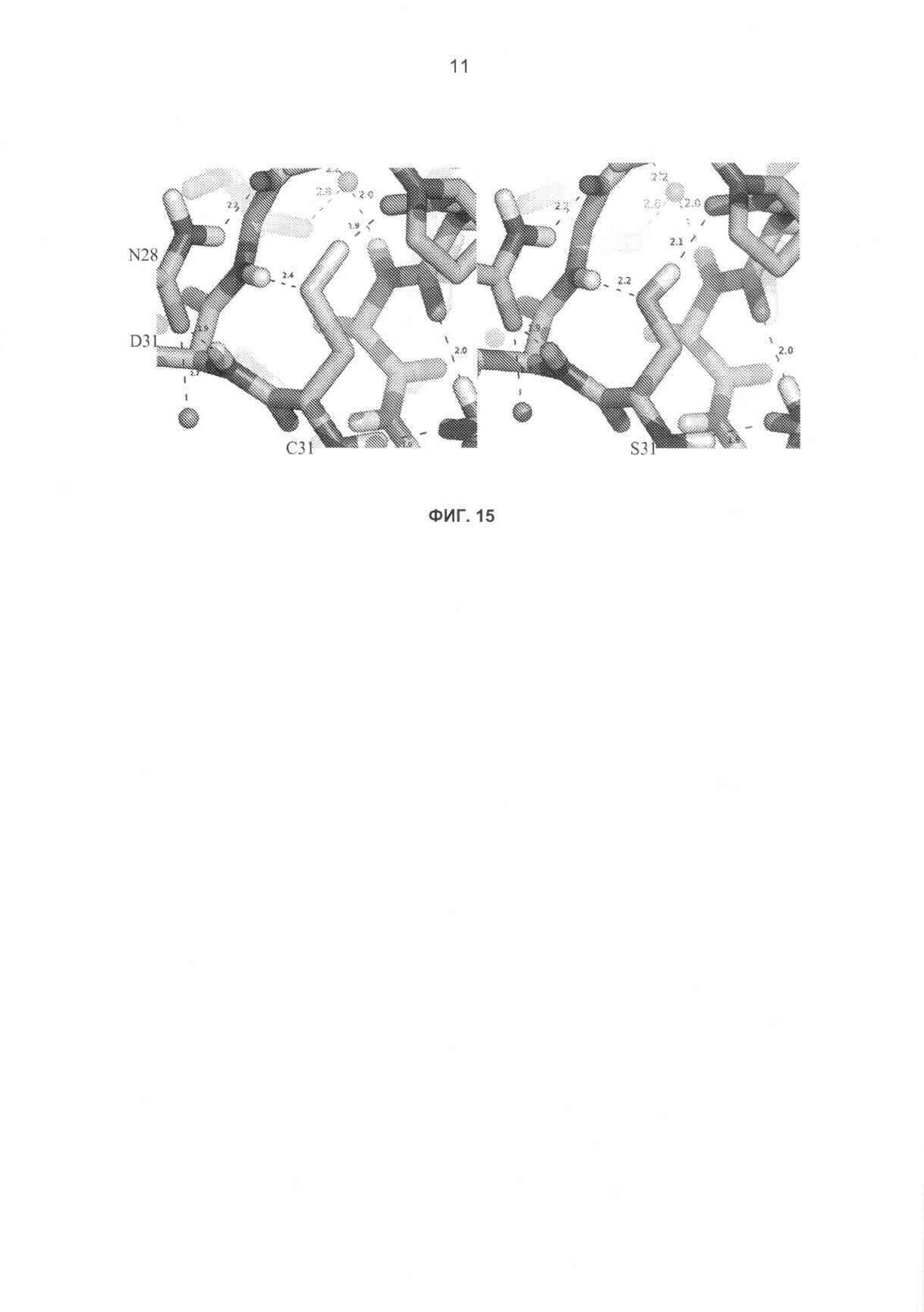
На фиг.15 показан структурный анализ мутации C314S и ее стабилизирующий эффект, (а) Положения водорода для структуры высокого разрешения H.insolens (1ocn) были добавлены с помощью REDUCE.1 (b) Реконструкция геометрии аналогичной сериновой структуры было смоделировано с помощью PyMOL (http:(//)www.pymol.org). Оптимизация боковых цепей в платформе моделирования SHARPEN2 (с функцией энергии всех атомов Rosetta) также позволила предположить, что, как Cys314, так и Ser314 будут донорами водородной связи для карбонила Pro339 и акцепторами водородной связи от амида Gly316. Наилучшая способность серина к водородному связыванию может играть роль в более высокой стабильности серинсодержащих вариантов. Другим возможным объяснением является геометрическая комплементарность. Конкретно, положение Cys из 1ocn проявляет данные о конформационном напряжении, при котором боковая цепь заметно согнута (то есть неправильный угол между двумя плоскостями от N-C-Cα-Cβ составляет 6° от стандартного положения), увеличивая расстояние до карбонила Pro. Цифры на фиг., которым не предшествуют буквы, обозначают расстояния водородных связей (Å).
ПОДРОБНОЕ ОПИСАНИЕ
Как используют в описании и в прилагаемой формуле изобретения, формы единственного числа включают ссылки на множественное число, если контекст четко не диктует иное. Так, например, ссылка на ″домен″ включает множество таких доменов, и ссылка на ″белок″ включает ссылку на один или более чем один белок, и т.д.
Также использование ″или″ означает ″и/или″, Если не указано иное. Подобным образом, ″содержат″, ″содержит″, ″содержащий″, ″включают″, ″включает″ и ″включающий″ являются взаимозаменяемыми и не предназначены для ограничения.
Кроме того, должно быть понятно, что, где в описаниях различных форм осуществления используют термин ″содержащий″, специалистам в данной области техники должно быть понятно, что в некоторых конкретных случаях форма осуществления может быть описана альтернативно, используя выражение ″состоящий по существу из″ или ″состоящий из″.
Хотя методы и материалы, подобные или эквивалентные описанным в данной заявке, можно использовать в практике раскрытых способов и композиций, в данной заявке описаны примерные способы, устройства и материалы.
Если не определено иное, все технические и научные термины, используемые в данной заявке, имеют такое же значение, как общепринято понимают обычные специалисты в области техники, к которой принадлежит данное изобретение. Таким образом, как используют на протяжении всей настоящей заявки, приведенные ниже термины имеют следующие значения.
В недавних исследованиях документированы превосходные характеристики целлюлаз из термофильных грибов относительно их мезофильных аналогов в процессах преобразования биомассы в лабораторном масштабе, где усиленная стабильность приводит к сохранению активности в течение более длительных периодов времени как при умеренных, так и при повышенных температурах. Целлюлазы грибов привлекательны, поскольку обладают высокой активностью и могут экспрессироваться в хозяевах-грибах, таких как Hypocrea jecorina (анаморф Trichoderma reesei), на уровнях вплоть до 40 г/л в супернатанте. К сожалению, набор документированных термостойких целлюлаз грибов мал. В случае процессивных ферментов целлобиогидролаз класса II (СВН II) менее 10 последовательностей природных термостойких генов аннотировано в базе данных CAZy.
Как более полно описано в данной заявке, с использованием рекурсивного создания химерных полипептидов и анализа конкретных стабилизированных доменов, наконец, были идентифицированы конкретные аминокислоты, придающие термостойкость и улучшенную активность.
Как более подробно описано ниже, изобретение основано, по меньшей мере частично, на создании и экспрессии новых ферментов, которые катализируют гидролиз целлюлозы. В одной форме осуществления предложены новые полипептиды, которые сконструированы для гидролиза целлюлозы при повышенных температурах. Такие полипептиды включают варианты целлобиогидролаз, которые изменены таким образом, что включают аминокислотные замены в указанных остатках. Хотя эти варианты описаны более подробно ниже, понятно, что полипептиды по изобретению могут содержать одну или более чем одну модифицированную аминокислоту. Присутствие модифицированных аминокислот может обладать преимуществом, например, при (а) увеличении периода полураспада полипептида, (b) термостойкости и (с) повышенному круговороту субстрата. Аминокислота(ы) модифицирована, например, котрансляционно или посттрансляционно во время рекомбинантного продуцирования (например, N-сцепленное гликозилирование при мотивах N-X-S/T во время экспрессии в клетках млекопитающих), либо модифицирована синтетическими способами. Соответственно, ″мутант″, ″вариант″ или ″модифицированный″ белок, фермент, полинуклеотид, ген или клетка означают белок, фермент, полинуклеотид, ген или клетку, которые изменены или преобразованы, либо являются каким-либо образом отличными или измененными по сравнению с родительским белком, фермент, полинуклеотид, ген или клеткой. Мутант или модифицированный белок или фермент обычно, хотя необязательно, экспрессирован с мутантного полинуклеотида или гена.
″Мутация″ означает любой процесс или механизм, результатом которого является мутантный белок, фермент, полинуклеотид, ген или клетка. Это включает любую мутацию, при которой белок, фермент, полинуклеотид или последовательность гена изменены, и любое обнаружимое изменение в клетке, возникающее в результате такой мутации. Типично мутация происходит в полинуклеотиде или последовательности гена в результате точечных мутаций, делеций или инсерций одного или множественных нуклеотидных остатков. Мутация включает как изменения полинуклеотида, возникающие в пределах кодирующей белок области гена, так и изменения в областях вне последовательности, кодирующей белок, таких как, но не ограниченных ими, регуляторные или промоторные последовательности. Мутация в гене может быть ″молчащей″, то есть не отражающейся в изменении аминокислоты при экспрессии, приводя к варианту гена ″консервативной последовательности″. Обычно это происходит, когда одна аминокислота соответствует более чем одному кодону.
Не ограничивающие примеры модифицированной аминокислоты включают гликозилированную аминокислоту, сульфатированную аминокислоту, пренилированную (например, фарнезилированную, геранилгеранилированную) аминокислоту, ацетилированную аминокислоту, ацилированную аминокислоту, пегилированную аминокислоту, биотинилированную аминокислоту, карбоксилированную аминокислоту, фосфорилированную аминокислоту и тому подобное. В литературе в изобилии имеются ссылки, адекватные для руководства специалиста в данной области техники по модификации аминокислот. Примерные протоколы находятся в Walker (1998) Protein Protocols on CD-ROM (Humana Press, Towata, N.J.).
Рекомбинантные способы продуцирования и выделения модифицированных полипептидов целлобиогидролаз по изобретению описаны в данной заявке. В дополнение к рекомбинантному продуцированию, полипептиды могут быть получены путем прямого синтеза пептидов с использованием твердофазных методов (например, Stewart et al. (1969) Solid-Phase Peptide Synthesis (WH Freeman Co, San Francisco); и Merrifield (1963) J. Am. Chem. Soc. 85: 2149-2154). Пептидный синтез можно осуществлять, используя ручные методы, или путем автоматизации. Автоматизированный синтез может быть достигнут, например, с использованием пептидного синтезатора Applied Biosystems 431A (Perkin Elmer, Foster City, Calif.) в соответствии с инструкциями, предоставленными изготовителем.
″Целлобиогидролаза II″ или ″фермент СВН II″ означает фермент из семейства целлюлаз из 6 белков, который широко распространен в бактериях и грибах. Эти ферменты вовлечены в гидролиз целлюлозы.
Под ″целлюлазной активностью″ подразумевают фермент, который способен к гидролизу целлюлозы. Целлюлаза относится к классу ферментов, продуцируемых грибами, бактериями и простейшими, которые катализируют гидролиз целлюлозы. Однако также существуют целлюлазы, продуцируемые другими типами организмов, такими как растения и животные. Номером ЕС для данной группы ферментов является ЕС 3.2.1.4. Существует пять общих типов целлюлаз, основанных на типе катализируемой реакции: эндоцеллюлаза; экзоцеллюлаза, где в пределах этой категории имеется два основных типа экзоцеллюлаз (или целлобиогидролаз, сокращенно СВН) - один тип работает процессивно с восстанавливающего конца, и один тип работает процессивно с нередуцирующего конца целлюлозы; гидролитические целлобиаза или бета-глюкозидаза; окислительные целлюлазы и целлюлозофосфорилазы, которые деполимеризуют целлюлозу, используя фосфаты вместо воды. Большинство грибных целлюлаз имеет два домена: каталитический домен и целлюлозосвязывающий домен, которые соединены гибким линкером. В конкретных формах осуществления изобретения целлюлазной активностью является активность СВН. Последовательности, описанные в данной заявке, включают в некоторых случаях и целлюлозосвязывающий домен, и каталитический домен, или только каталитический домен. В тех случаях, где предложена последовательность только каталитического домена, понятно, что целлюлозосвязывающий домен (CBD), такой как представлено в SEQ ID NO:8, может быть функционально сцеплен (либо как часть кодирующей последовательности, либо слит позже) с каталитическим доменом, непосредственно или посредством линкера.
″Белок″ или ″полипептид″, где эти термины используют в данной заявке взаимозаменяемо, включает одну или более чем одну цепь химических строительных блоков, называемых аминокислотами, которые связаны вместе химическими связями, называемыми пептидными связями. ″Фермент″ означает любое вещество, предпочтительно полностью или большей частью состоящее из белка, которое катализирует или стимулирует, более или менее специфично, одну или более чем одну химическую или биохимическую реакцию. ″Нативный″ или ″дикого типа″ белок, фермент, полинуклеотид, ген или клетка означает белок, фермент, полинуклеотид, ген или клетку, которые встречаются в природе.
″Аминокислотная последовательность″ представляет собой полимер из аминокислот (белок, полипептид и т.д.) или последовательность символов, представляющую аминокислотный полимер, в зависимости от контекста. Термины ″белок″, ″полипептид″ и ″пептид″ используют в данной заявке взаимозаменяемо. ″Аминокислота″ представляет собой молекулу, имеющую структуру, где центральный атом углерода связан с атомом водорода, группой карбоновой кислоты (атом углерода которой называют в данной заявке ″карбоксильным атомом углерода″), аминогруппой (атом азота которой называют в данной заявке ″амино-атомом азота″) и группой боковой цепи, R. Когда она включена в пептид, полипептид или белок, аминокислота теряет один или более чем один атом ее карбоксильных групп аминокислоты в реакции дегидрирования, которая связывает одну аминокислоту с другой. В результате, когда аминокислота включена в белок, ее называют ″аминокислотным остатком″.
Конкретная аминокислотная последовательность данного белка (то есть ″первичная структура″ полипептида, записанная от амино-конца к карбокси-концу) определяется нуклеотидной последовательностью кодирующего участка мРНК, который, в свою очередь, определен генетической информацией, типично геномной ДНК (включая ДНК органелл, например, митохондриальную или хлоропластную ДНК). Таким образом, определение последовательности гена помогает при предсказании первичной последовательности соответствующего полипептида и более конкретно роли или активности полипептидов или белков, кодируемых этим геном или полинуклеотидной последовательностью.
″Консервативная аминокислотная замена″ или просто ″консервативные вариации″ конкретной последовательности относятся к замене одной аминокислоты или группы аминокислот по существу идентичными аминокислотными последовательностями. Специалисту в данной области техники понятно, что результатом индивидуальных замен, делеций или добавлений, которые изменяют, добавляют или делегируют одну аминокислоту или процентную долю аминокислот в кодируемой последовательности, являются ″консервативные вариации″, где эти изменения приводят в результате к делеций аминокислоты, добавлению аминокислоты или замене аминокислоты химически подобной аминокислотой.
Таблицы консервативных замен, в которых приведены функционально подобные аминокислоты, хорошо известны в данной области техники. Например, одна группа консервативных замен включает аланин (А), серин (S) и треонин (Т). Другая группа консервативных замен включает аспарагиновую кислоту (D) и глутаминовую кислоту (Е). Другая группа консервативных замен включает аспарагин (N) и глутамин (Q). Еще одна другая группа консервативных замен включает аргинин (R) и лизин (К). Другая группа консервативных замен включает изолейцин (I), лейцин (L), метионин (М) и валин (V). Другая группа консервативных замен включает фенилаланин (F), тирозин (Y) и триптофан (W).
Таким образом, ″консервативные аминокислотные замены″ перечисленных полипептидных последовательностей (например, SEQ ID NO:2, 4, 6 и 12-78) включают замены процентной доли, типично менее 10%, аминокислот полипептидной последовательности консервативно подобранной аминокислотой той же группы консервативных замен. Соответственно, консервативно замененная вариация полипептида по изобретению может содержать 100, 75, 50, 25 или 10 замен консервативно замененной вариацией одной и той же группы консервативных замен.
Понятно, что добавление последовательностей, которое не изменяет кодируемую активность молекулы нуклеиновой кислоты, такое как добавление нефункциональной или некодирующей последовательности, является консервативной вариацией базовой нуклеиновой кислоты. ″Активность″ фермента является мерой его активность катализа реакции, то есть ″функции″, и может быть выражена как скорость, с которой образуется продукт реакции. Например, активность фермента может быть представлена как количество продукта, образующегося в единицу времени или на единицу фермента (например, концентрации или массы), либо в отношении констант сродства или диссоциации. Как взаимозаменяемо используют в данной заявке, ″целлобиогидролазная активность или целлюлазная активность″, ″биологическая активность целлобиогидролазы или целлюлазьГ или ″функциональная активность целлобиогидролазы или целлюлазы″ относится к активности, проявляемой белком, полипептидом, обладающим целлюлазной активностью, и в конкретных формах осуществления к целлобиогидролазной активности на целлюлозном субстрате, которая определена in vivo или in vitro в соответствии со стандартными методами.
Специалисту в данной области техники понятно, что многие консервативные вариации нуклеиново-кислотных конструкций, которые раскрыты, дают функционально идентичную конструкцию. Например, как описано выше, благодаря вырожденности генетического кода, ″молчащие замены″ (то есть замены в нуклеиново-кислотной последовательности, которые не приводят в результате к изменению кодируемого полипептида) являются подразумеваемым признаком каждой нуклеиново-кислотной последовательности, которая кодирует аминокислоту. Подобным образом, ″консервативные аминокислотные замены″ в одной или в нескольких аминокислотах в аминокислотной последовательности, замененные другими аминокислотами с высоко подобными свойствами, также легко идентифицируют как высоко подобные раскрытой конструкции. Такие консервативные вариации каждой раскрытой конструкции являются признаком полипептидов, предложенных в данной заявке.
″Консервативные варианты″ представляют собой белки или ферменты, в которых данный аминокислотный остаток изменен без изменения общей конформации и функции белка или фермента, включая, но не ограничиваясь ими, замену аминокислоты другой, обладающей подобными свойствами, включающими полярный или неполярный характер, размер, форму и заряд. Аминокислоты, иные, чем те, которые указаны как консервативные, могут отличаться в белке или ферменте таким образом, что процент подобия белковой или аминокислотной последовательности между двумя белками подобной функции может варьировать и может составлять, например, по меньшей мере 30%, по меньшей мере 50%, по меньшей мере 70%, по меньшей мере 80% или по меньшей мере 90%, как определено в соответствии со схемой выравнивания. В отношении данной заявки ″подобие последовательностей″ означает степень, до которой нуклеотидные или белковые последовательности являются родственными. Степень подобия между двумя последовательностями может быть основана на проценте идентичности и/или консервативности последовательности. ″Идентичность последовательности″ в данной заявке означает степень, до которой две нуклеотидные или аминокислотные последовательности являются инвариантными. ″Выравнивание последовательностей″ означает процесс построения двух или более чем двух последовательностей в одну колонку до достижения максимальных уровней идентичности (и, в случае аминокислотных последовательностей, консервативности) с целью оценки степени подобия. В данной области техники известны многочисленные способы выравнивания последовательностей и оценки подобия/идентичности, такие как, например, кластерный метод, где подобие основано на алгоритме MEGALIGN, а также BLASTN, BLASTP и FASTA (Lipman and Pearson, 1985; Pearson and Lipman, 1988). При использовании всех этих программ предпочтительными установками являются те, которые приводят в результате к самой высокой степени подобия.
Неконсервативными модификациями конкретного полипептида являются те, которые заменяют любую аминокислоту, не характеризующуюся как консервативная замена, например, любая замена, которая выходит за границы шести групп, изложенных выше. Они включают замены основных или кислых аминокислот на нейтральные аминокислоты (например, Asp, Glu, Asn или Gin на Val, lie, Leu или Met), ароматической аминокислоты на основные или кислые аминокислоты (например, Phe, Tyr или Trp на Asp, Asn, Glu или Gin) или любую другую замену, не заменяющую аминокислоту подобной аминокислотой. Основные боковые цепи включают лизин (К), аргинин (R), гистидин (Н); кислые боковые цепи включают аспарагиновую кислоту (D), глутаминовую кислоту (Е); незаряженные полярные боковые цепи включают глицин (G), аспарагин (N), глутамин (Q), серин (S), треонин (Т), тирозин (Y), цистеин (С); неполярные боковые цепи включают аланин (А), валин (V), лейцин (L), изолейцин (I), пролин (Р), фенилаланин (F), метионин (М), триптофан (W); бета-разветвленные боковые цепи включают треонин (Т), валин (V), изолейцин (I); ароматические боковые цепи включают тирозин (Y), фенилаланин (F), триптофан (W), гистидин (Н).
″Родительским″ белком, ферментом, полипептидом, геном или клеткой является любой белок, фермент, полипептид, ген или любая клетка, от которых имеют происхождение или получены другой белок, фермент, полипептид, ген или другая клетка с использованием любых способов, инструментов или методов, независимо от того, является ли сам родитель нативным или мутантным. Родительский полинуклеотид или ген кодирует родительский белок или фермент.
В дополнение к предложенным вариантам полипептидов СВН II предложены химерные полипептиды, которые содержат: 1) вариант домена, изолированного из первой родительской цепи и модифицированного таким образом, что включает аминокислотную замену; и 2) домен, изолированный из второй родительской цепи, либо немодифицированный, либо модифицированный таким образом, что включает новую активность или активность, которая комплементирует этот домен. Способы конструирования химерного полипептида по изобретению раскрыты в данной заявке.
В изобретении предложены варианты, мутанты и химеры целлюлазы и целлобиогидролазы (СВН) II, обладающие повышенной термостойкостью по сравнению с диким типом или родительским белком, где белок дикого типа состоит из SEQ ID NO:2, 4 или 6. Вариант содержит серин в С-концевой области в мотиве, включающем последовательность GEXDG, где Х представляет собой С, А или G (SEQ ID NO:107), где Х заменен серином, где этот вариант включает целлюлазную активность, и где полипептид обладает повышенной термостойкостью по сравнению с целлюлазой дикого типа, в которой отсутствует серин в последовательности GEXDG (SEQ ID NO:107). В одной форме осуществления варианты содержат по меньшей мере мутацию Cys→Ser в мотиве GECDG (см., например, SEQ ID NO:2, аминокислоты 312-316), обнаруженном в большинстве белков целлюлазы и целлобиогидролазы II (как более полно описано ниже), и могут содержать дополнительные мутации, которые улучшают термостойкость или активность. Идентичность между целлюлазами может быть достаточно низкой. Замена на серин, как описано выше, применима к любой целлюлазе, имеющей мотив SEQ ID NO:107 (например, где полипептид обладает по меньшей мере 60% или более высокой идентичностью SEQ ID NO:2 или 4).
Например, в изобретении предложены полипептиды, обладающие повышенной термостойкостью и целлюлазной активностью, включающие последовательность, которая по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:2, содержащей C314S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:4, содержащей C311S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:12, содержащей C310S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:13, содержащей C312S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:14, содержащей C314S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:15, содержащей C315S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:16, содержащей C313S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:17, содержащей C311S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:19, содержащей C313S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:21, содержащей C312S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:22, содержащей C311S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:64, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:65, содержащей C407S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:66, содержащей C394S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:67, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:68, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:69, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:70, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:71, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:72, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:73, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:74, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:75, содержащей C400S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:76, содержащей C407S; по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:77, содержащей C394S; или по меньшей мере на 85%, 90%, 95%, 98%, 99% идентична SEQ ID NO:78, содержащей C412S, где вышеуказанные полипептиды обладают целлюлазной активностью и улучшенной термостойкостью по сравнению с их соответствующим родительским (дикого типа) белком, в котором отсутствует мутация Cys→Ser.
Еще в одной другой форме осуществления в изобретении предложены полипептиды, как описано выше, однако, они дополнительно содержат по меньшей мере одну дополнительную мутацию, которая может быть определена путем выравнивания с SEQ ID NO:64, где SEQ ID NO:64 содержит Pro в положении 413, либо Ser или Thr в положении 231, либо Ser или Thr в положении 305, либо Gin или Asn в положении 410, либо Glu в положении 82, либо любую комбинацию вышеописанного. Подобные замены могут быть идентифицированы путем выравнивания последовательностей аминокислотной последовательности SEQ ID NO:64 с последовательностями SEQ ID NO:2, 4, 6, 12-63 и 65-78.
В изобретении также предложены по существу очищенные полипептиды, которые либо продуцированы рекомбинантным путем, либо получены синтетическим путем, либо образованы иным неприродным путем, где полипептид включает последовательность, как изложено ниже, имеющую 1-10, 10-20 или 20-30 консервативных аминокислотных замен за исключением положения, идентифицированного ниже, где присутствует замена C→S:
SEQ ID NO:2 содержащую C314S;
SEQ ID NO:4 содержащую C311S;
SEQ ID NO:12 содержащую C310S;
SEQ ID NO:13 содержащую C312S;
SEQ ID NO:14 содержащую C314S;
SEQ ID NO:15 содержащую C315S;
SEQ ID NO:16 содержащую C313S;
SEQ ID NO:17 содержащую C311S;
SEQ ID NO:19 содержащую C313S;
SEQ ID NO:21 содержащую C312S;
SEQ ID NO:22 содержащую C311S;
SEQ ID NO:64 содержащую C400S;
SEQ ID NO:65 содержащую C407S;
SEQ ID NO:66 содержащую C394S;
SEQ ID NO:67 содержащую C400S;
SEQ ID NO:68 содержащую C400S;
SEQ ID NO:69 содержащую C400S;
SEQ ID NO:70 содержащую C400S;
SEQ ID NO:71 содержащую C400S;
SEQ ID NO:72 содержащую C400S;
SEQ ID NO:73 содержащую C400S;
SEQ ID NO:74 содержащую C400S;
SEQ ID NO:75 содержащую C400S;
SEQ ID NO:76 содержащую C407S;
SEQ ID NO:77 содержащую C394S; или
SEQ ID NO:78 содержащую C412S.
″Изолированный полипептид″ относится к полипептиду, который отделен от других примесей, которые естественно сопровождают его, например, белков, липидов и полинуклеотидов. Этот термин охватывает полипептиды, которые извлечены или очищены из их естественной окружающей среды или экспрессионной системы (например, клетки-хозяина или синтеза in vitro).
″По существу чистый полипептид″ относится к композиции, в которой the полипептидное соединение является преобладающим присутствующим соединением (то есть на молярной или массовой основе он является более представленным, чем любые другие индивидуальные макромолекулярные соединения в композиции), и обычно представляет собой по существу очищенную композицию, где целевое соединение составляет по меньшей мере примерно 50 процентов моль/моль или % масс/масс присутствующих макромолекулярных соединений. Как правило, по существу чистая полипептидная композиция будет содержать примерно 60% или более, примерно 70% или более, примерно 80% или более, примерно 90% или более, примерно 95% или более и примерно 98% или более моль/моль или % масс/масс всех макромолекулярных соединений, присутствующих в композиции. В некоторых формах осуществления целевое соединение очищают по существу до гомогенности (то есть примесные соединения невозможно обнаружить в композиции общепринятыми способами обнаружения), где композиция состоит по существу из единственного макромолекулярного соединения. Соединение-растворитель, малые молекулы (<500 Дальтон) и элементарные ионные соединения не считают макромолекулярные соединениями.
″Референсная последовательность″ относится к определенной последовательности, используемой в качестве основы для сравнения последовательностей. Референсная последовательность может представлять собой подмножество большей последовательности, например, сегмент полноразмерного гена или полипептидной последовательности. Как правило, референсная последовательность может составлять по меньшей мере 20 нуклеотидов или аминокислотных остатков в длину, по меньшей мере 25 нуклеотидов или остатков в длину, по меньшей мере 50 нуклеотидов или остатков в длину или полную длину нуклеиновой кислоты или полипептида. Поскольку два полинуклеотида или полипептида могут каждый (1) включать последовательность (то есть участок полноразмерной последовательности), которая является подобной между двумя последовательностями, и (2) может дополнительно включать последовательность, которая является различающейся между двумя последовательностями, сравнения последовательности между двумя (или более) полинуклеотидами или полипептидами типично проводят путем сравнения последовательностей двух полинуклеотидов или полипептидов на протяжении ″окна сравнения″, чтобы идентифицировать и сравнить локальные области подобия последовательностей.
″Идентичность последовательности″ означает, что две аминокислотных последовательности по существу идентичны (то есть на основе последовательных аминокислот) на протяжении окна сравнения. Термин ″подобие последовательности″ относится к подобным аминокислотам, которые имеют общие биофизические характеристики. Термин ″процент идентичности последовательности″ или ″процент подобия последовательности″ вычисляют путем сравнения двух оптимально выровненных последовательностей на протяжении окна сравнения, определяя число положений, в которых идентичные остатки (или подобные остатки) встречаются в обеих полипептидных последовательностях, с получением числа совпадающих положений, деления числа совпадающих положений на общее число положений в окне сравнения (то есть на размер окна) и умножения результата на 100 с получением процента идентичности последовательности (или процента подобия последовательности). В отношении полинуклеотидных последовательностей термины идентичность последовательности и подобие последовательности имеют значение, сравнимое с описанным для белковых последовательностей, где термин ″процент идентичности последовательности″ указывает на то, что две полинуклеотидных последовательности идентичны (на основе последовательных нуклеотидов) на протяжении окна сравнения. Как таковой, процент идентичности полинуклеотидной последовательности (или процент подобия полинуклеотидной последовательности, например, для молчащих замен или других замен, на основании алгоритма анализа) может быть также вычислен. Максимальное соответствие можно определить путем использования одного из алгоритмов последовательности, описанных в данной заявке (или других алгоритмов, доступных обычным специалистам в данной области техники), или путем визуальной проверки.
Применительно к полипептидам термин существенная идентичность или существенное подобие означает, что две пептидные последовательности при оптимальном выравнивании, например, с помощью программ BLAST, GAP или BESTFIT с использованием массы гэпов по умолчанию или путем визуальной проверки, обладают идентичностью последовательности или подобием последовательности. Подобным образом, применительно к контексту двух нуклеиновых кислот термин существенная идентичность или существенное подобие означает, что две нуклеиново-кислотные последовательности при оптимальном выравнивании, например, с помощью программ BLAST, GAP или BESTFIT с использованием массы гэпов по умолчанию (описанной в данной заявке в другом месте) или путем визуальной проверки, обладают идентичностью последовательности или подобием последовательности.
Одним из примеров алгоритма, который пригоден для определения процента идентичности последовательности или подобия последовательности, является алгоритм FASTA, который описан в Pearson, W. R. & Lipman, D. J., (1988) Proc. Natl. Acad. Sci. USA 85:2444. См. также W. R. Pearson, (1996) Methods Enzymology 266:227-258. Предпочтительные параметры, используемые при выравнивании последовательностей ДНК FASTA для вычисления процента идентичности или процента подобия, оптимизированы, BL50 Matrix 15: -5, k-tuple = 2; штраф на соединение = 40, оптимизация = 28; штраф на гэп -12, штраф на длину гэпа = -2; и ширина = 16.
Другим примером полезного алгоритма является PILEUP. PILEUP создает множественное выравнивание последовательностей из группы родственных последовательностей с использованием прогрессивных попарных выравниваний, чтобы показать отношение и процент идентичности последовательностей или процент подобия последовательностей. Он также строит дерево или дендрограмму, показывающую кластерные отношения, используемые для создания выравнивания. PILEUP использует упрощение прогрессивного способа выравнивания Feng & Doolittle, (1987) J. Mol. Evol. 35:351-360. Используемый способ подобен способу, описанному Higgins & Sharp, CABIOS 5:151-153, 1989. Эта программа может выравнивать вплоть до 300 последовательностей, каждая максимальной длины 5000 нуклеотидов или аминокислот. Операция множественного выравнивания начинается с попарного выравнивания двух наиболее подобных последовательностей, создавая кластер двух выровненных последовательностей. Затем этот кластер выравнивают со следующей наиболее родственной последовательностью или кластером выровненных последовательностей. Два кластера последовательностей выравнивают путем простого распространения попарного выравнивания двух индивидуальных последовательностей. Конечное выравнивание достигается серией прогрессивных попарных выравниваний. Программа осуществляется путем определения конкретных последовательностей и их координат аминокислот или нуклеотидов для областей сравнения последовательности и путем определения параметров программы. Используя PILEUP, референсную последовательность сравнивают с другими тестируемыми последовательностями для определения отношения процента идентичности последовательностей (или процента подобия последовательностей) с использованием следующих параметров: взвешенные гэпы по умолчанию (3.00), взвешенная длина гэпов по умолчанию (0.10) и взвешенные концы гэпов. PILEUP может быть получена из пакета программ анализа последовательностей GCG, например, версии 7.0 (Devereaux et al., (1984) Nuc. Acids Res. 12:387-395).
Другим примером алгоритма, который пригоден для множественных выравниваний ДНК и аминокислотных последовательностей, является программа CLUSTALW (Thompson, J. D. et al., (1994) Nuc. Acids Res. 22:4673-4680). CLUSTALW проводит множественные попарные сравнения между группами последовательностей и собирает их в множественное выравнивание, основанное на идентичности последовательностей. Штрафы на открытие гэпа и удлинение гэпа составляют 10 и 0,05 соответственно. Для аминокислотных выравниваний можно использовать алгоритм BLOSUM в качестве весовой матрицы белков (Henikoff and Henikoff, (1992) Proc. Natl. Acad. Sci. USA 89:10915-10919).
Как упомянуто выше, члены семейств целлобиогидролаз и целлюлаз могут быть идентифицированы с помощью выравнивания последовательностей, и получена замена в мотиве GECDG (см., например, SEQ ID NO:2, аминокислоты 312-316). Затем модифицированный полипептид можно анализировать на активность, как описано ниже, при различных температурах и условиях, чтобы идентифицировать те модификации, которые вводят благоприятную активность. Примерные последовательности можно найти в приведенных ниже номерах по каталогу GenBank, которые включены в данную заявку посредством ссылки.
Еще в одних других формах осуществления семейство вариантов целлюлазных полипептидов, обладающих улучшенной термостойкостью, включает приведенные в нижеследующей таблице, имеющие замену C→S, G→S или A→S. Кроме того, полипептиды, обладающие 85%, 90%, 95%, 98% или 99% идентичностью последовательности с любой из приведенных ниже последовательностей, имеющих идентифицированные замены, в нижеследующей таблице, обладающие целлюлазной активностью и термостойкостью, также охвачены изобретением.
|
|
Еще в одних других формах осуществления семейство вариантов целлюлазных полипептидов, обладающих улучшенной термостойкостью, включает приведенные в нижеследующей таблице, имеющие замену C→S, G→S или A→S. Кроме того, полипептиды, обладающие 85%, 90%, 95%, 98% или 99% идентичностью последовательности с любой из приведенных ниже последовательностей, имеющих замены, идентифицированные в нижеследующей таблице, и обладающие целлюлазной активностью и термостойкостью, также охвачены изобретением.
Выравнивание группирования аминокислотного каркаса Н. jecorina CBH II Cys311 на белковые последовательности, обладающие самой высокой идентичностью Н. jecorina CBH II. Показаны остатки в положении, эквивалентном 311, полужирным шрифтом и подчеркиванием. Последовательности рекомбинантных Н. insolens и Р. chrys CBH II, исследованных в данной работе, обозначены как Н. inso и Р. chrys. Пятьдесят четыре из 250 наиболее идентичных последовательностей было исключено вследствие избыточности (то есть точечных мутантов для структурных исследований или >95% идентичных изоформ). Идентифицирован номер по каталогу для целлюлазы, и соответствующая последовательность включена в данную заявку посредством ссылки в виде прямого копирования из номера по каталогу базы данных. Последовательности, соответствующие номерам по каталогу, указаны как SEQ ID NO:79-106. Остаток, подчеркнутый жирным шрифтом (например, С, А или G), заменен S. Номер в скобках, следующий за идентифицированной последовательностью, соответствует SEQ ID NO:)


Для целей изобретения полипептид по изобретению проявляет улучшенную термостойкость по сравнению с соответствующим родительским полипептидом, если он имеет T50, которое по меньшей мере примерно на 4°С или по меньшей мере примерно на 9°С выше, чем для родительской целлюлазы, или целлобиогидролаза имеет Т50 от примерно 4°С до примерно 30°С или на любое количество между ними выше, или Т50 от примерно 9°С до примерно 30°С или на любое количество между ними выше по сравнению с родительской целлобиогидролазой. Т50 представляет собой температуру, при которой модифицированный или природный фермент сохраняет 50% его остаточной активности после предварительной инкубации в течение 15 минут, и определенной с помощью анализа, подробно описанного в приведенных ниже Примерах, или как известно в данной области техники.
Модифицированные целлобиогидролазы или целлюлазы по изобретению могут иметь T50, которое от примерно 4°С до примерно 30°С или на любой интервал между ними выше, чем для соответствующей родительской целлобиогидролазы (например, SEQ ID NO:2, 4 или 6), от примерно 5°С до примерно 20°С или на любой интервал между ними выше, от примерно 8°С до примерно 15°С или на любой интервал между ними выше или от примерно 9°С до примерно 15°С или на любой интервал между ними выше. Например, модифицированная целлюлаза может иметь Т50, которое по меньшей мере примерно на 4, 5, 6, 7, 8, 9, 10, 12, 14, 16, 18, 20, 22, 24, 26, 28 или 30°С выше, чем для соответствующей родительской целлобиогидролазы.
Варианты, идентифицированные в данной заявке, можно также использовать для создания химерных целлобиогидролаз. Например, SCHEMA использована ранее для создания семейств сотен активных химер ферментов β-лактамазы и цитохрома Р450. SCHEMA использует данные белковой структуры для определения границ непрерывных аминокислотных ″блоков″, которые минимизируют <Е>, библиотечное среднее число контактов боковых цепей аминокислот, когда блоки обмениваются между различными родителями. Показано, что вероятность того, что химера β-лактамазы является уложенной и активной, связана обратной связью со значением Е для этой последовательности. Алгоритм RASPP (Recombination as Shortest Path Problem, рекомбинация как кратчайший путь к решению проблемы) использовали, чтобы идентифицировать границы блоков, которые минимизируют <E> относительно библиотечного среднего числа мутаций, <m>. Более 20% ~500 уникальных химер, охарактеризованных из коллекции β-лактамаз, состоящих из 8 блоков от 3 родителей (38=6561 возможных последовательностей), были каталитически активными. С помощью подобного подхода было получено семейство химер от 3 родителей, 8 блоков цитохрома Р450, содержащее более чем 2300 новых каталитически активных ферментов. Химеры из этих коллекций характеризовались высоким числом мутаций, 66 и 72 аминокислоты в среднем от ближайшего родителя, соответственно. Таким образом, программа SCHEMA/RASPP обеспечила разработку семейств химер, обладающих значительным разнообразием последовательностей и заметной долей функциональных членов.
Также показано, что термостойкости химер SCHEMA могут быть предсказаны на основании данных стабильности последовательности из малой выборки последовательностей. Моделированные данных термической инактивации методом линейной регрессии для 184 химер цитохрома Р450 показало, что блоки SCHEMA вносили аддитивный вклад в термостойкость. С помощью этой модели более 300 химер было предсказано как термостойкие, и все 44, которые были протестированы, были более стабильны, чем наиболее стабильный родитель. Было установлено, что всего лишь 35 измерений термостойкости можно использовать для предсказания наиболее термостойких химер. Кроме того, термостойкие химеры Р450 проявляли уникальные профили активности и специфичности, демонстрируя, что химерогенез может привести к дополнительным полезным свойствам ферментов. В данной заявке рекомбинация ферментов СВН II по SCHEMA может создать химерные целлюлазы, которые активны на целлюлозе, набухающей в фосфорной кислоте (PASC), при высоких температурах, в течение пролонгированных периодов времени и в широких диапазонах рН.
Используя способы, раскрытые в данной заявке, был создан ряд химерных полипептидов, обладающих целлобиогидролазной активностью, обладающих улучшенными характеристиками по сравнению с родительскими белками СВН II дикого типа.
Разнообразное семейство новых ферментов СВН II был сконструировано путем обмена блоков последовательности из трех грибных ферментов СВН II. Двадцать три из 48 химерных последовательностей, отобранных из данной серии, секретировались в активной форме S. cerevisiae, и пять имели период полураспада при 63°С, который был выше, чем у самого стабильного родителя. Учитывая, что данная 48-членная серия образцов составляет менее 1% возможных суммарно 6561 последовательностей, авторы изобретения предсказывают, что данная коллекция химер уже содержит сотни активных термостойких ферментов СВН II, число, которое значительно превышает примерно двадцать грибных ферментов СВН II в базе данных CAZy.
Подход использования данных по стабильности последовательности серии образцов для идентификации блоков, которые вносят положительный вклад в термостойкость химеры, оценивали в результате обнаружения того, что все 10 каталитически активных химер во второй серии оценивания СВН II были более термостойкими, чем наиболее термостойкий родитель, естественно термостойкий СВН II из термостойких грибов, Н. insolens. Это открытие, таким образом, дополнительно позволило создать суммарно 33 новых фермента СВН II, которые экспрессируются в каталитически активной форме в S. cerevisiae, 15 из которых являются более термостойкими, чем наиболее стабильный родитель, из которого они были сконструированы. Эти 15 термостойких ферментов являются различными по последовательности, отличающимися друг от друга и от их ближайших природных гомологов более чем по 94 и 58 положениям аминокислот, соответственно.
Анализ термостойкости химер СВН II в комбинированном образце и в серии оценок показывает, что четыре идентифицированных термостабилизирующих блока, В1Р1, В6Р3, В7Р3 и В8Р2, вносят кумулятивный вклад в термостойкость, когда присутствуют в одной и той же химере. Четыре из пяти химер из серии образцов, которые являются более термостойкими, чем Н. insolens СВН II, содержат два или три из этих термостабилизирующих блоков (Таблица 1). Десять дополнительных членов этой серии оценок, два из которых более стабильны, чем фермент Н. insolens, содержат по меньшей мере два стабилизирующих блока, где пять или шесть термостойких химер в этой группе содержат либо три, либо четыре стабилизирующих блока.
Изобретение демонстрирует, что стабилизирующие блоки можно перекомбинировать, чтобы создать новые высоко стабильные, активные целлюлазы. Регрессионная модель стабильности предсказывает, что библиотека СВН II программы SCHEMA содержит 2026 химер, которые более стабильны, чем наиболее стабильный родительский фермент. Эти химеры являются разнообразными и отличными от нативных целлюлаз: они отличаются о т родителей примерно на 8 и 72 мутации (в среднем на 50) и друг от друга в среднем на 63 мутации. Суммарно 33 гена из этой серии было синтезировано и экспрессировано в S. cerevisiae: было обнаружено, что каждый из этих СВН II более стабилен, чем наиболее стабильная родительская целлюлаза из термофильного гриба Н. insolens, как измерено либо на основании ее полураспада, либо на основании ее инактивации при 63°С или Т50. Уменьшение сложности последовательности путем создания химер только из восьми блоков дало возможность создания модели стабильности последовательности и идентификации одного высоко стабилизирующего блока последовательности. За счет тестирования только десяти аминокислотных замен в этом блоке была идентифицирована единственная высоко стабилизирующая замена. Очень большой стабилизирующий эффект замены C313S (в отношении последовательности SEQ ID NO:6; C314S, SEQ ID NO:2 и 0311S, SEQ ID NO:4), наблюдаемый во всех химерах и в нативных ферментах СВН II Р. chrysosporium, Н. insolens и Н. Jecorina, позволил предположить, что мутация любого остатка в данном положении на Ser может стабилизировать любое семейство 6 целлюлаз, в которое она введена.
Минимизация числа разрушенных контактов при рекомбинации (Фиг.2С) дает возможность аппроксимировать блоки как несвязанные единицы, которые вносят независимый вклад в стабильность всего белка, приводя, таким образом, к кумулятивным или даже аддитивным вкладам в термостойкость химеры. Для рекомбинации данного фермента СВН II алгоритм SCHEMA был эффективен при минимизации таких разрушенных контактов: если в кристаллической структуре родительского СВН II Н. insolens определено суммарно 303 межблочных контакта, дизайн СВН II библиотеки SCHEMA приводит в результате только к 33 потенциальным разрушенным контактам. С учетом того, что фермент СВН II родителей не характеризуется очевидными структурными субдоменами, и только четыре из восьми блоков (1, 5, 7 и 8) напоминают компактные структурные единицы или модули, низкое число разрушенных контактов демонстрирует, что алгоритм SCHEMA/RASPP эффективен для случаев, в которых число блоков оказывается более высоким, чем число структурных подразделений. Как наблюдали ранее для химер β-лактамазы и цитохрома Р450, низкие значения Е были предсказательными для укладки и активности химер. Хотя это не использовано в данной заявке, данное отношение должно быть значимым для конструирования серий химерных образцов, которые содержат высокую долю активных членов.
В изобретении также использована химера, чтобы определить, можно ли улучшить стабильность рН в ферментах СВН II. Если удельная активность Н. jecorina СВН II резко снижается, когда рН повышается выше оптимального значения 5, HJPlus, созданный путем замещения стабилизирующих блоков на наиболее промышленно релевантном ферменте Н. jecorina СВН II, сохраняет значительно более высокую активность при этих более высоких рН (Фиг.4). Термостойкие химеры 11113132 и 13311332, а также родительские целлюлазы Н. insolens и С. thermophilum СВН II имеют даже более широкие профили рН/активности, чем HJPlus. Узкий профиль рН/активности Н. jecorina СВН II считают связанным с депротонированием нескольких пар карбоксил-карбоксилат, которое дестабилизирует белок выше рН ~6. Замещение родителя 3 в блоке 7 в HJPlus изменяет аспартат 277 на гистидин, элиминируя пару карбоксил-карбоксилат между D277 и D316 (блока 8). Замещение D277 положительно заряженным гистидином может предотвратить дестабилизирующее отталкивание зарядом при некислом рН, давая возможность HJPlus сохранять активность при более высоком рН, чем Н. jecorina СВН II. Даже более широкие профили рН/активности двух остальных термостойких химер и родительских ферментов СВН II Н. insolens и С.thermophilum может быть следствием отсутствия кислых остатков в положениях, соответствующих паре карбоксил-карбоксилат Е57-Е119 HJPlus и Н. jecorina СВН II.
HJPlus проявляет как относительно высокую удельную активность, так и высокую термостойкость. На фиг.5 показано, что эти свойства приводят к хорошим характеристикам в экспериментах по долговременному гидролизу: HJPlus гидролизовал целлюлозу при температурах на 7-15°С выше, чем родительские ферменты СВН II, а также обладал значительно повышенной долговременной активностью относительно всех родителей при их температурном оптимуме, улучшая Н. jecorina CBH II в 1,7 раза. С учетом того, что удельная активность химеры HJPlus меньше, чем у родителя Н. jecorina CBH II, эту повышенную долговременную активность можно считать следствием способности термостойкой HJPlus к сохранению активности при оптимальных температурах гидролиза в течение более длительного времени реакции.
Две другие термостойкие химеры имели общий с HJPlus широкий температурный диапазон. Это наблюдение подтверждает положительную корреляцию между t1/2 при повышенной температуре и максимумом рабочей температуры, и позволяет предположить, что многие термостойкие химеры среди 6561 последовательностей химер CBH II будут также способны к расщеплению целлюлозы при повышенных температурах. Хотя эта способность к гидролизу аморфного субстрата PASC при повышенных температурах хорошо предсказывает потенциальную пользу термостойких химер грибного CBH II, исследования с более проблемными кристаллическими субстратами и субстратами, содержащими лигнин, обеспечат более полную оценку релевантности этих новых семейств фермента CBH II для применений при расщеплении биомассы.
В большинстве процессов преобразования биомассы используют смеси грибных целлюлаз (прежде всего CBH II, целлобиогидролазы класса I (CBH I), эндоглюканаз и β-глюкозидазы) для достижения высоких уровней гидролиза целлюлозы. Создание разнообразной группы термостойких химер фермента CBH II является первой стадией в построении материального запаса стабильных, высокоактивных целлюлаз, из которых можно готовить смеси ферментов и оптимизировать для конкретных применений и исходного сырья.
″Пептидный сегмент″ относится к участку или фрагменту большего полипептида или белка. Пептидный сегмент необязательно сам обладает собственной функциональной активностью, хотя в некоторых случаях пептидный сегмент может соответствовать домену полипептида, где этот домен обладает своей собственной биологической активностью. Пептидным сегментом, обусловливающим стабильность, является пептидный сегмент, находящийся в полипептиде, который стимулирует стабильность, функцию и укладку по сравнению с родственным полипептидом, в котором отсутствует этот пептидный сегмент. Пептидным сегментом, обусловливающим дестабилизацию, является пептидный сегмент, который идентифицирован как вызывающий утрату стабильности, функции или укладки, когда он присутствует в полипептиде.
″Слитый″, ″оперативно сцепленный″ и ″оперативно связанный″ используют в данной заявке взаимозаменяемо для широкой ссылки на химическое или физическое сочетание двух доменов или пептидных сегментов, отличающихся во всем остальном, где каждый домен или пептидный сегмент при оперативном сцеплении может обеспечить функциональный полипептид, обладающий желаемой активностью. Домены или пептидные сегменты могут быть соединены посредством пептидных линкеров таким образом, что они являются функциональными, или могут быть слиты посредством других промежуточных соединений или химических связей. Например, два домена могут составлять часть одной и той же кодирующей последовательности, где полинуклеотиды находятся в одной рамке считывания, так что этот полинуклеотид при транскрипции кодирует единую мРНК, которая при трансляции включает оба домена в виде единого полипептида. Альтернативно оба домена могут экспрессироваться по отдельности в виде индивидуальных полипептидов, и их сливают друг с другом, используя химические способы. Типично кодирующие домены сцеплены ″в рамке″ либо непосредственно, либо разделены пептидным линкером, и кодируются в виде единого полипептида. Различные кодирующие последовательности для пептидных линкеров и пептида известны в данной области техники.
″Полинуклеотид″ или ″нуклеиново-кислотная последовательность″ относится к полимерной форме нуклеотидов. В некоторых случаях полинуклеотид относится к последовательности, которая не является непосредственно примыкающей к любой из кодирующих последовательностей, к которой она непосредственно примыкает (либо на 5′ конце, либо на 3′ конце) в природном геноме организма, от которого она имеет происхождение. Этот термин, таким образом, включает, например, рекомбинантную ДНК, которую встраивают в вектор; в автономно реплицирующуюся Плазмиду или вирус; либо в геномную ДНК прокариота или эукариота, либо которая существует в виде отдельной молекулы (например, кДНК) независимо от других последовательностей. Нуклеотиды по изобретению могут представлять собой рибонуклеотиды, дезоксирибонуклеотиды или модифицированные формы любого нуклеотида. Полинуклеотиды, как используют в данной заявке, относятся среди прочего к одно- и двунитевой ДНК, ДНК, которая представляет собой смесь одно- и двунитевых участков, одно- и двунитевой РНК и РНК, которая представляет собой смесь одно- и двунитевых участков, к гибридным молекулам, содержащим ДНК и РНК, которые могут быть однонитевыми или, более типично, двунитевыми или представлять собой смесь одно- и двунитевых участков. Термин полинуклеотид охватывает как геномную ДНК или РНК (в зависимости от организма, то есть РНК геном вирусов), так и мРНК, кодируемую геномной ДНК, и кДНК.
″Нуклеиново-кислотный сегмент,″ ″олигонуклеотидный сегмент″ или ″полинуклеотидный сегмент″ относится к участку большей полинуклеотидной молекулы. Полинуклеотидный сегмент необязательно должен соответствовать кодируемому функциональному домену белка; однако, в некоторых случаях сегмент кодирует функциональный домен белка. Полинуклеотидный сегмент может составлять примерно 6 нуклеотидов или более в длину (например, 6-20, 20-50, 50-100, 100-200, 200-300, 300-400 или более нуклеотидов в длину). Пептидный сегмент, обусловливающий стабильность, может кодироваться полинуклеотидным сегментом, обусловливающим стабильность, где этот пептидный сегмент стимулирует стабильность, функцию или укладку по сравнению с полипептидом, в котором отсутствует этот пептидный сегмент.
″Химера″ относится к комбинации по меньшей мере двух сегментов по меньшей мере двух различных родительских белков. Как понятно специалисту в данной области техники, сегменты необязательно действительно происходят от каждого из родителей, то есть представляют собой конкретную последовательность, которая является релевантной, а не сами по себе физические нуклеиновые кислоты. Например, химерные грибные целлобиогидролазы класса II (целлюлазы СВН II) будут иметь по меньшей мере два сегмента от двух различных родительских полипептидов СВН II. Эти два сегмента соединены таким образом, что приводят в результате к новому полипептиду, обладающему целлюлазной активностью. Иными словами, белок не будет химерой, если он имеет идентичную последовательность любому из полноразмерных родителей. Химерный полипептид может содержать более чем два сегмента от двух различных родительских белков. Например, для каждой конечной химеры или библиотеки химер может быть 2, 3, 4, 5-10, 10-20 или более родителей. Сегмент каждого родительского полипептида может быть очень коротким или очень длинным, где сегменты могут иметь диапазон длины непрерывных аминокислот от 1 до 90%, 95%, 98% или 99% всей длины белка. В одной форме осуществления минимальная длина составляет 10 аминокислот. В одной форме осуществления единый кроссоверный сайт определен для двух родителей. Положение кроссовера определяет, где останавливается аминокислотный сегмент одного родителя и где начинается аминокислотный сегмент следующего родителя. Таким образом, простая химера будет иметь только одно положение кроссовера, где сегмент перед этим положением кроссовера будет принадлежать одному родителю, а сегмент после этого положения кроссовера будет принадлежать второму родителю. В одной форме осуществления химера имеет более чем одно положение кроссовера, например, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11-30 положений кроссовера или более. Ниже обсуждается, как эти положения кроссовера называют и определяют. В форме осуществления, где имеется два положения кроссовера и два родителя, будет первый непрерывный сегмент от первого родителя, за которым следует второй непрерывный сегмент от второго родителя, за которым следует третий непрерывный сегмент от первого родителя. Непрерывный подразумевают как означающий, что прерывание сегментов не происходит. Эти непрерывные сегменты соединены с образованием непрерывной аминокислотной последовательности. Например, химера СВН II от Humicola insolens (далее в данной заявке ″1″) и Н. jecori (далее в данной заявке ″2″) с двумя кроссоверами в положениях 100 и 150 может иметь первые 100 аминокислот от 1, за которыми следуют следующие 50 от 2, за которыми следуют остальные аминокислоты от 1, где все они соединены в одну непрерывную цепь аминокислот. Альтернативно химера СВН II может иметь первые 100 аминокислот от 2, за которыми следуют следующие 50 от 1, за которыми следуют остальные от 2. Как понятно специалисту в данной области техники, существуют как варианты, так и точные последовательности химер. Таким образом, не 100% каждого сегмента обязательно должно присутствовать в конечной химере, если она является вариантом химеры. Количество, которое может быть изменено, либо посредством дополнительных остатков, либо удаления или изменения остатков, будет определяться так, как определено термином вариант. Конечно, как понятно специалисту в данной области техники, приведенное выше обсуждение применимо не только к аминокислотам, но также к нуклеиновым кислотам, которые кодируют аминокислоты.
Кроме конкретных вариантов, в изобретении описаны варианты, которые можно использовать для создания химер СВН II. Библиотеку направленной рекомбинации SCHEMA использовали для создания ферментов целлобиогидролаз на основе особенно хорошо изученного члена этого семейства разнообразных ферментов, и более конкретно ферментов целлобиогидролаз II: Н. insolens является родителем ″1″ (SEQ ID NO:2), H. jecorina является родителем ″2″ (SEQ ID NO:4), и С. thermophilum является родителем ″3″ (SEQ ID NO:6). SCHEMA представляет собой способ на компьютерной основе для предсказания того, какие фрагменты гомологичных белков могут рекомбинировать, не влияя на структурную целостность белка (см., например, Meyer et al., (2003) Protein Sci., 12:1686-1693). С помощью этого компьютерного подхода идентифицировали семь точек рекомбинации в родительских белках СВН II, что дало возможность создания библиотеки химерных полипептидов СВН II, где каждый полипептид содержит восемь сегментов. Химеры с более высокой стабильностью являются идентифицируемыми путем определения аддитивного вклада каждого сегмента в общую стабильность, либо путем использования линейной регрессии данных по стабильности, либо основываясь на консенсусном анализе MSA уложенных белков по сравнению с развернутыми. Рекомбинация SCHEMA гарантирует, что химеры сохраняют биологическую функцию и проявляют высокое разнообразие последовательности за счет сохранения важных функциональных остатков при обмене толерантных остатков.
Таким образом, как проиллюстрировано различными формами осуществления данной заявки, в изобретении предложены полипептиды СВН II, содержащие химеры родительских доменов, из которых родительская цепь полученной в результате химерной кодирующей последовательности может быть модифицирована таким образом, что содержит замену C→S, как описано выше. В некоторых формах осуществления полипептид содержит химеру, имеющую множество доменов от N- до С-конца из различных родительских белков СВН II: (сегмент 1)-(сегмент 2)-(сегмент 3)-(сегмент 4)-(сегмент 5)-(сегмент 6)-(сегмент 7)-(сегмент 8);
где сегмент 1 включает аминокислотные остатки от примерно 1 до примерно x1 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 2 составляют аминокислотные остатки от примерно x1 до примерно x2 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 3 составляют аминокислотные остатки от примерно x2 до примерно x3 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 4 составляют аминокислотные остатки от примерно x3 до примерно x4 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 5 составляют аминокислотные остатки от примерно x4 до примерно x5 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 6 составляют аминокислотные остатки от примерно x5 до примерно x6 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 7 составляют аминокислотные остатки от примерно х6 до примерно х7 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); и сегмент 8 составляют аминокислотные остатки от примерно х7 до примерно х8 SEQ ID NO:2 (″1″), SEQ ID NQ:4 (″2″) или SEQ ID NO:6 (″3″);
где: x1 представляет собой остаток 43, 44, 45, 46 или 47 SEQ ID NO:2, или остаток 42, 43, 44, 45 или 46 SEQ ID NO:4 или SEQ ID NO:6; x2 представляет собой остаток 70, 71, 72, 73 или 74 SEQ ID NO:2, или остаток 68, 69, 70, 71, 72, 73 или 74 SEQ ID NO:4 или SEQ ID NO:6; x3 представляет собой остаток 113, 114, 115, 116, 117 или 118 SEQ ID NO:2, или остаток 110, 111, 112, 113, 114, 115 или 116 SEQ ID NO:4 или SEQ ID NO:6; x4 представляет собой остаток 153, 154, 155, 156 или 157 SEQ ID NO:2, или остаток 149, 150, 151, 152, 153, 154, 155 или 156 SEQ ID NO:4 или SEQ ID NO:6; x5 представляет собой остаток 220, 221, 222, 223 или 224 SEQ ID NO:2, или остаток 216, 217, 218, 219, 220, 221, 222 или 223 SEQ ID NO:4 или SEQ ID NO:6; x6 представляет собой остаток 256, 257, 258, 259, 260 или 261 SEQ ID NO:2, или остаток 253, 254, 255, 256, 257, 258, 259 или 260 SEQ ID NO:4 или SEQ ID NO:6; x7 представляет собой остаток 312, 313, 314, 315 или 316 SEQ ID NO:2, или остаток 309, 310, 311, 312, 313, 314, 315 или 318 SEQ ID NO:4 или SEQ ID NO:6; и x8 представляет собой аминокислотный остаток, соответствующий С-концу полипептида, имеющего последовательность SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO:6.
Используя приведенные выше соотношения доменов, был создан ряд химерных структур, которые приведены в таблице 1.
1588 последовательностей химер СВН II, для которых предсказаны более высокие значения T50, чем измеренное значение Т50 64,8°С для родительского СВН II Н. insolens
|
|
|
|
|
Ссылаясь на приведенную выше таблицу, каждая цифра относится к домену химерного полипептида СВН II. Номер обозначает родительскую цепь, от которой этот домен имеет происхождение. Например, химерный полипептид СВН II, имеющий последовательность 12111131, указывает на то, что этот полипептид включает последовательность от N-конца к С-концу: аминокислоты от примерно 1 до x1 SEQ ID NO:2 (″1″), сцепленные с аминокислотами от примерно x1 до x2 SEQ ID NO:4 (″2″), сцепленными с аминокислотами от примерно x2 до примерно x3 SEQ ID NO:2, сцепленными с аминокислотами от примерно x3 до примерно x4 SEQ ID NO:2, сцепленными с аминокислотами от примерно x4 до примерно x5 SEQ ID NO:2, сцепленными с аминокислотами от примерно x5 до примерно x6 SEQ ID NO:2, сцепленными с аминокислотами от примерно х6 до x7 SEQ ID NO:6 (″3″), сцепленными с аминокислотами от примерно х7 до x8 (например, с С-концом) SEQ ID NO:2.
В некоторых формах осуществления полипептид СВН II имеет химерную сегментную структуру, выбранную из группы, состоящей из: 11113132, 21333331, 21311131, 22232132, 33133132, 33213332, 13333232, 12133333, 13231111, 11313121. 11332333, 12213111, 23311333, 13111313, 31311112, 23231222, 33123313, 22212231, 21223122, 21131311, 23233133, 31212111 и 32333113.
В некоторых формах осуществления полипептид обладает улучшенной термостойкостью по сравнению с полипептидом дикого типа SEQ ID NO:2, 4 или 6. Активность полипептида может быть измерена с любым из субстратов или их комбинацией, как описано в примерах. Как очевидно специалисту в данной области техники, другие соединения в пределах класса соединений, примеры которых приведены и обсуждены в примерах, можно тестировать и использовать.
В некоторых формах осуществления полипептид может иметь различные изменения аминокислотной последовательности по отношению к референсной последовательности. Эти изменения могут представлять собой замену, делецию или инсерцию одной или более чем одной аминокислоты. Где изменение представляет собой замену, эта замена может представлять собой консервативную, неконсервативную замену или комбинацию консервативных и неконсервативных замен. Например, химера может содержать замену C→S в С314 SEQ ID NO:2 или С311 SEQ ID NO:4.
Таким образом, в некоторых формах осуществления полипептиды могут включать общую структуру от N-конца к С-концу: (сегмент 1)-(сегмент 2)-(сегмент 3)-(сегмент 4)-(сегмент 5)-(сегмент 6)-(сегмент 7)-(сегмент 8),
где сегмент 1 содержит аминокислотный остаток от примерно 1 до примерно x1 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″) и имеет 1-10 консервативных аминокислотных замен; сегмент 2 составляют аминокислотные остатки от примерно x1 до примерно x2 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 3 составляют аминокислотные остатки от примерно x2 до примерно x3 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 4 составляют аминокислотные остатки от примерно x3 до примерно x4 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 5 составляют аминокислотные остатки от примерно x4 до примерно x5 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 6 составляют аминокислотные остатки от примерно x5 до примерно х6 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; сегмент 7 составляют аминокислотные остатки от примерно x6 до примерно x7 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен; и сегмент 8 составляют аминокислотные остатки от примерно x7 до примерно x8 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″), и он имеет примерно 1-10 консервативных аминокислотных замен;
где x1 представляет собой остаток 43, 44, 45, 46 или 47 SEQ ID NO:2, или остаток 42, 43, 44, 45 или 46 SEQ ID NO:4 или SEQ ID NO:6; x2 представляет собой остаток 70, 71, 72, 73 или 74 SEQ ID NO:2, или остаток 68, 69, 70, 71, 72, 73 или 74 SEQ ID NO:4 или SEQ ID NO:6; x3 представляет собой остаток 113, 114, 115, 116, 117 или 118 SEQ ID NO:2, или остаток 110, 111, 112, 113, 114, 115 или 116 SEQ ID NO:4 или SEQ ID NO:6; x4 представляет собой остаток 153, 154, 155, 156 или 157 SEQ ID NO:2, или остаток 149, 150, 151, 152, 153, 154, 155 или 156 SEQ ID NO:4 или SEQ ID NO:6; x5 представляет собой остаток 220, 221, 222, 223 или 224 SEQ ID NO:2, или остаток 216, 217, 218, 219, 220, 221, 222 или 223 SEQ ID NO:4 или SEQ ID NO:6; x6 представляет собой остаток 256, 257, 258, 259, 260 или 261 SEQ ID NO:2, или остаток 253, 254, 255, 256, 257, 258, 259 или 260 SEQ ID NO:4 или SEQ ID NO:6; x7 представляет собой остаток 312, 313, 314, 315 или 316 SEQ ID NO:2, или остаток 309, 310, 311, 312, 313, 314, 315 или 318 SEQ ID NO:4 или SEQ ID NO:6; и x8 представляет собой аминокислотный остаток, соответствующий С-концу полипептида, имеющего последовательность SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO:6, и где химера имеет алгоритм, представленный в таблице 1, и где химера содержит замену C→S, соответствующую С314 SEQ ID NO:2 или 0311 SEQ ID NO:4.
В некоторых формах осуществления число замен может составлять 2, 3, 4, 5, 6, 8, 9 или 10, или большее число аминокислотных замен (например, 10-20, 21-30, 31-40 и тому подобное число аминокислотных замен).
В некоторых формах осуществления функциональные полипептиды СВН II могут обладать целлюлазной активностью параллельно с повышенной термостойкостью, как, например, для определенного субстрата, обсуждаемого в примерах, а также обладает уровнем идентичности аминокислотной последовательности с референсной целлобиогидролазой или ее сегментами. Референсный фермент или сегмент может быть дикого типа (например, встречающийся в природе) или представлять собой сконструированный фермент. Таким образом, в некоторых формах осуществления полипептиды по изобретению могут содержать общую структуру от N-конца к С-концу:
где сегмент 1 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от примерно 1 до примерно x1 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 2 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от x1 до примерно x2 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 3 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от x2 до примерно x3 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 4 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от x3 до примерно x4 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 5 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от примерно x4 до примерно x5 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 6 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от x5 до примерно x6 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); сегмент 7 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от x6 до примерно x7 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″); и сегмент 8 содержит последовательность, которая по меньшей мере на 50-100% идентична аминокислотным остаткам от х7 до примерно x8 SEQ ID NO:2 (″1″), SEQ ID NO:4 (″2″) или SEQ ID NO:6 (″3″);
где x1 представляет собой остаток 43, 44, 45, 46 или 47 SEQ ID NO:2, или остаток 42, 43, 44, 45 или 46 SEQ ID NO:4 или SEQ ID NO:6; x2 представляет собой остаток 70, 71, 72, 73 или 74 SEQ ID NO:2, или остаток 68, 69, 70, 71, 72, 73 или 74 SEQ ID NO:4 или SEQ ID NO:6; x3 представляет собой остаток 113, 114, 115, 116, 117 или 118 SEQ ID NO:2, или остаток 110, 111, 112, 113, 114, 115 или 116 SEQ ID NO:4 или SEQ ID NO:6; x4 представляет собой остаток 153, 154, 155, 156 или 157 SEQ ID NO:2, или остаток 149, 150, 151, 152, 153, 154, 155 или 156 SEQ ID NO:4 или SEQ ID NO:6; x5 представляет собой остаток 220, 221, 222, 223 или 224 SEQ ID NO:2, или остаток 216, 217, 218, 219, 220, 221, 222 или 223 SEQ ID NO:4 или SEQ ID NO:6; x6 представляет собой остаток 256, 257, 258, 259, 260 или 261 SEQ ID NO:2, или остаток 253, 254, 255, 256, 257, 258, 259 или 260 SEQ ID NO:4 или SEQ ID NO:6; x7 представляет собой остаток 312, 313, 314, 315 или 316 SEQ ID NO:2, или остаток 309, 310, 311, 312, 313, 314, 315 или 318 SEQ ID NO:4 или SEQ ID NO:6; и x8 представляет собой аминокислотный остаток, соответствующий С-концу полипептида, имеющего последовательность SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO:6, и где химера имеет алгоритм, представленный в таблице 1, и где химера содержит замену C→S, соответствующую С314 SEQ ID NO:2 или С311 SEQ ID NO:4.
В некоторых формах осуществления каждый сегмент химерного полипептида может обладать по меньшей мере 60%, 70%, 80%, 90%, 95%, 96%, 97%, 98% или 99% или большей идентичностью последовательности по сравнению с референсным сегментом, указанным для каждого из (сегмент 1), (сегмент 2), (сегмент 3), (сегмент 4), (сегмент 5), (сегмент 6), (сегмент 7) и (сегмент 8) SEQ ID NO:2, SEQ ID NO:4 или SEQ ID NO:6.
В некоторых формах осуществления варианты полипептидов могут обладать улучшенной термостойкостью по сравнению с ферментативной активностью полипептида дикого типа SEQ ID NO:2, 4 или 6, и где содержит замену C→S, соответствующую С314 SEQ ID NO:2 или С311 SEQ ID NO:4.
Химерные ферменты, описанные в данной заявке, могут быть получены в различных формах, таких как лизаты, грубые экстракты или изолированные препараты. Полипептиды можно растворять в подходящих растворах; готовить в виде порошков, таких как ацетоновый порошок (со стабилизаторами или без стабилизаторов); либо готовить в виде лиофилизатов. В некоторых формах осуществления полипептид может представлять собой изолированный полипептид.
В некоторых формах осуществления полипептиды могут находиться в форме наборов. Ферменты могут находиться в растворимой форме, например, в виде растворов в лунках микротитрационных планшетов, либо иммобилизованы на субстрате. Субстрат может представлять собой твердый субстрат или пористый субстрат (например, мембрану), который может состоять из органических полимеров, таких как полистирол, полиэтилен, полипропилен, полифторэтилен, полиэтиленокси и полиакриламид, а также из их сополимеров и привитых сополимеров. Твердый носитель может быть также неорганическим, таким как стекло, кремнезем, стекло с контролируемым размером пор (CPG), обращенно-фазовый кремнезем или металл, такой как золото или платина. Конфигурация субстрата может представлять собой форму шариков, сфер, частиц, гранул, геля, мембраны или поверхности. Поверхности могут быть плоскими, по существу плоскими или не плоскими. Твердые носители могут быть пористыми или непористыми, и могут обладать набухающими или не набухающими свойствами. Твердый носитель может иметь конфигурацию лунки, выемки или другого контейнера, сосуда, оборудования или положения. Множество носителей может иметь конфигурацию на матрице различных положений с электронной адресацией для робототехнической доставки реагентов или способов обнаружения и/или инструментов.
В изобретении также предложены полинуклеотиды, кодирующие сконструированные полипептиды СВН II, раскрытые в данной заявке. Полинуклеотиды могут быть оперативно сцеплены с одной или более чем одной гетерологичной регуляторной или контролирующей последовательностью, которая контролирует экспрессию гена, чтобы создать рекомбинантный полинуклеотид, способный к экспрессии экспрессируемого полипептида. Экспрессионные конструкции, содержащие гетерологичный полинуклеотид, кодирующий химеру СВН II, можно вводить в соответствующие клетки-хозяева для экспрессии полипептида.
С учетом знания конкретных последовательностей химерных ферментов СВН II (например, сегментной структуры химерного СВН II) полинуклеотидные последовательности будут очевидны специалисту в данной области техники на основании аминокислотной последовательности сконструированных химерных ферментов СВН II. Знание кодонов, соответствующих различным аминокислотам, в сочетании со знанием аминокислотной последовательности полипептидов дает возможность специалистам в данной области техники получать различные полинуклеотиды, кодирующие полипептиды по изобретению, таким образом, в изобретении рассмотрены все до единой возможные вариации полинуклеотидов, которые могут быть получены путем подбора комбинаций на основании возможных выборов кодонов, и все такие вариации следует считать конкретно раскрытыми для любого из полипептидов, описанных в данной заявке.
В некоторых формах осуществления полинуклеотиды кодируют полипептиды, описанные в данной заявке, но обладают примерно 80% или большей идентичностью последовательности, примерно 85% или большей идентичностью последовательности, примерно 90% или большей идентичностью последовательности, примерно 91% или большей идентичностью последовательности, примерно 92% или большей идентичностью последовательности, примерно 93% или большей идентичностью последовательности, примерно 94% или большей идентичностью последовательности, примерно 95% или большей идентичностью последовательности, примерно 96% или большей идентичностью последовательности, примерно 97% или большей идентичностью последовательности, примерно 98% или большей идентичностью последовательности или примерно 99% или большей идентичностью последовательности на нуклеотидном уровне с референсным полинуклеотидом, кодирующим варианты полипептидов или химерные полипептиды СВН II, имеющие замену C→S, как описано выше (например, где полипептид или химера содержит замену C→S, соответствующую С314 SEQ ID NO:2 или С311 SEQ ID NO:4).
В некоторых формах осуществления изолированные полинуклеотиды, кодирующие полипептиды, можно подвергать разнообразным манипуляциям, чтобы обеспечить экспрессию полипептида. Манипуляции с изолированным полинуклеотидом перед его вставкой в вектор могут быть желательными или необходимыми в зависимости от экспрессионного вектора. Способы модификации полинуклеотидов и нуклеиново-кислотных последовательностей с использованием методов рекомбинантных ДНК хорошо известны в данной области техники. Руководство приведено в Sambrook et al., 2001, Molecular Cloning: A Laboratory Manual, 3rd Ed., Cold Spring Harbor Laboratory Press; и в Current Protocols in Molecular Biology, Ausubel. F. ed., Greene Pub. Associates, 1998, обновления до 2007.
В некоторых формах осуществления полинуклеотиды оперативно сцеплены с контролирующими последовательностями для экспрессии полинуклеотидов и/или полипептидов. В некоторых формах осуществления контролирующая последовательность может представлять собой соответствующую промоторную последовательность, которая может быть получена из генов, кодирующих внеклеточные или внутриклеточные полипептиды, либо гомологичные, либо гетерологичные для клетки-хозяина. Для бактериальных клеток-хозяев подходящие промоторы для направления транскрипции нуклеиново-кислотных конструкций по настоящему изобретению включают промоторы, полученные из lac оперона Е. соli, генов xylA и xylB Bacillus subtilis, генов утилизации ксилозы Bacillus megatarium (например, Rygus et al. (1991) Appl. Microbiol. Biotechnol. 35:594-599; Meinhardt et al., (1989) Appl. Microbiol. Biotechnol. 30:343-350), прокариотического гена бета-лактамазы (Villa-Kamaroff et al., (1978) Proc. Natl Acad. Sci. USA 75: 3727-3731), а также промотор tac (DeBoer et al., (1983) Proc. Natl Acad. Sci. USA 80:21-25). Различные подходящие промоторы описаны в ″Useful proteins from recombinant bacteria″ в Scientific American, 1980, 242:74-94; и в Sambrook et al., см. выше.
В некоторых формах осуществления контролирующая последовательность может также представлять собой соответствующую последовательность терминации транскрипции, последовательность, распознаваемую клеткой-хозяином для терминации транскрипции. Терминаторная последовательность оперативно сцеплена с 3′ концом нуклеиново-кислотной последовательности, кодирующей полипептид. Можно использовать любой терминатор, который является функциональным в выбранной клетке-хозяине.
В некоторых формах осуществления контролирующая последовательность может также представлять собой соответствующую лидерную последовательность, нетранслируемый участок мРНК, который важен для трансляции клеткой-хозяином. Эта лидерная последовательность оперативно сцеплена с 5′ концом нуклеиново-кислотной последовательности, кодирующей полипептид. Можно использовать любую лидерную последовательность, которая является функциональной в выбранной клетке-хозяине.
В некоторых формах осуществления контролирующая последовательность может также представлять собой участок, кодирующий сигнальный пептид, который кодирует аминокислотную последовательность, сцепленную с амино-концом полипептида, и направляет кодируемый полипептид в секреторный биохимический путь клетки. 5′ конец кодирующей последовательности нуклеиново-кислотной последовательности может естественно содержать участок, кодирующий сигнальный пептид, естественно сцепленный в рамке считывания трансляции с сегментом кодирующей области, который кодирует секретируемый полипептид. Альтернативно 5′ конец кодирующей последовательности может содержать участок, кодирующий сигнальный пептид, который является чужеродным для кодирующей последовательности. Чужеродный участок, кодирующий сигнальный пептид, может требоваться, где кодирующая последовательность естественно не содержит участок, кодирующий сигнальный пептид. Эффективными участками, кодирующими сигнальный пептид, для бактериальных клеток-хозяев могут быть участки, кодирующие сигнальный пептид, полученные из генов для мальтогенной амилазы Bacillus NCIB 11837, альфа-амилазы Bacillus stearothermophilus, субтилизина Bacillus licheniformis, бета-лактамазы Bacillus licheniformis, нейтральных протеаз Bacillus stearothermophilus (nprT, nprS, nprM) и prsA Bacillus subtilis. Дополнительные сигнальные пептиды описаны Simonen and Palva, (1993) Microbiol Rev 57:109-137.
Далее изобретение направлено на рекомбинантный экспрессионный вектор, содержащий полинуклеотид, кодирующий сконструированный вариант полипептида или химерный полипептид СВН II, и один или более чем один участок регуляции экспрессии, такой как промотор и терминатор, точка начала репликации и т.д., в зависимости от типа хозяев, в которых их вводят. При создании экспрессионного вектора кодирующую последовательность располагают в векторе таким образом, что кодирующая последовательность оперативно сцеплена с соответствующими контролирующими последовательностями для экспрессии.
Рекомбинантный экспрессионный вектор может представлять собой любой вектор (например, плазмиду или вирус), который можно удобно подвергать методам рекомбинантных ДНК, и который может вызывать экспрессию полинуклеотидной последовательности. Выбор вектора типично зависит от совместимости вектора с клеткой-хозяином, в которую нужно вводить этот вектор. Векторы могут представлять собой линейные или замкнутые кольцевые плазмиды.
Экспрессионный вектор может представлять собой автономно реплицирующийся вектор, то есть вектор, который существует в виде экстрахромосомной молекулы, репликация которой независима от хромосомной репликации, например, плазмиду, экстрахромосомный элемент, минихромосому или искусственную хромосому. Вектор может содержать любые средства для обеспечения саморепликации. Предпочтительно вектор может быть таким, который при введении в клетку-хозяина интегрирует в геном и реплицируется вместе с хромосомой(ами), в которую он интегрирован. Кроме того, можно использовать один вектор или плазмиду, либо два или более чем два вектора или две плазмиды, которые вместе содержат суммарную ДНК для введения в геном клетки-хозяина, либо транспозон.
В некоторых формах осуществления экспрессионный вектор по изобретению содержит один или более чем один селективный маркер, который дает возможность легко обнаружить трансформированные клетки. Селективный маркер представляет собой ген, продукт которого обеспечивает устойчивость к биоциду или вирусу, устойчивость к тяжелым металлам, прототрофность для ауксотрофов и тому подобное. Примерами бактериальных селективных маркеров являются гены dal от Bacillus subtilis или Bacillus licheniformis, или маркеры, которые придают устойчивость к антибиотикам, таким как ампициллин, канамицин, хлорамфеникол (пример 1) или устойчивость к тетрациклину. Другие полезные маркеры очевидны специалисту в данной области техники.
В другой форме осуществления в изобретении предложена клетка-хозяин, содержащая полинуклеотид, кодирующий вариант полипептида или химерный полипептид СВН II, где полинуклеотид оперативно сцеплен с одной или более чем одной контролирующей последовательностью для экспрессии полипептида в клетке-хозяине. Клетки-хозяева для использования при экспрессии полипептидов, кодируемых экспрессионными векторами по изобретению, хорошо известны в данной области техники и включают, но не ограничены ими, бактериальные клетки, такие как Е. coli и Bacillus megaterium; эукариотические клетки, такие как клетки дрожжей, клетки СНО и тому подобное, клетки насекомых, такие как клетки Drosophila S2 и Spodoptera Sf9; клетки животных, такие как СНО, COS, BHK, 293 и клетки меланомы Боуэса; а также клетки растений. Другие подходящие клетки-хозяева будут очевидны специалистам в данной области техники. Соответствующие культуральные среды и условия выращивания для вышеописанных клеток-хозяев хорошо известны в данной области техники.
Варианты полипептидов или химерные полипептиды СВН II по изобретению могут быть получены путем использования способов, хорошо известных в данной области техники. Полинуклеотиды можно синтезировать с помощью рекомбинантных методов, таких как предложено в Sambrook et al., 2001, Molecular Cloning: A Laboratory Manual, 3rd Ed., Cold Spring Harbor Laboratory Press; и Current Protocols in Molecular Biology, Ausubel. F. ed., Greene Pub. Associates, 1998, обновления до 2007. Полинуклеотиды, кодирующие ферменты, или праймеры для амплификации могут быть также получены стандартными твердофазными способами в соответствии с известными способами синтеза, например, используя фосфорамидитный метод, описанный Beaucage et al., (1981) Tet Lett 22:1859-69, или метод, описанный Matthes et al., (1984) EMBO J. 3:801-05, например, как типично практикуют при автоматизированных способах синтеза. Кроме того, по существу любая нуклеиновая кислота может быть получена из любого из разнообразных коммерческих источников, таких как The Midland Certified Reagent Company, Midland, TX, The Great American Gene Company, Ramona, CA, ExpressGen Inc. Chicago, IL, Operon Technologies Inc., Alameda, CA, и многих других.
Сконструированные ферменты, экспрессированные в клетках-хозяевах, можно выделить из клеток или из культуральной среды, используя любой один или более чем один из хорошо известных методов очистки белка, включая среди прочего обработку лизоцимом, соникацию, фильтрование, высаливание, ультрацентрифугирование, хроматографию и аффинное разделение (например, антитела, связанные с субстратом). Подходящие растворы для лизиса и высокоэффективной экстракции белков из бактерий, таких как Е. coli, имеются в продаже под торговым названием CelLytic BTM от Sigma-Aldrich St. Louis МО.
Хроматографические методы выделения полипептидов включают среди прочего хроматографию с обращенной фазой, высокоэффективную жидкостную хроматографию, ионообменную хроматографию, гель-электрофорез и аффинную хроматографию. Условия очистки конкретного фермента будут зависеть отчасти от таких факторов, как суммарный заряд, гидрофобность, гидрофильность, молекулярная масса, молекулярная форма и т.д., и будут очевидны специалистам в данной области техники.
Описания направленной рекомбинации SCHEMA и синтеза химерных полипептидов приведены в примерах данной заявки, а также в Otey et al., (2006), PLoS Biol. 4(5):e112; Meyer et al., (2003) Protein Sci., 12:1686-1693; заявке на патент США №12/024515, поданной 1 февраля 2008; и заявке на патент США №12/027885, поданной 7 февраля 2008; такие ссылки полностью включены в данную заявку посредством ссылки.
Как обсуждено выше, полипептид можно использовать в ряде областей применения, таких как среди прочего создание биотоплива, расщепление целлюлозы и тому подобное.
Приведенные ниже примеры подразумевают дополнительное объяснение, но не ограничение приведенного выше описания или прилагаемой формулы изобретения.
ПРИМЕРЫ
Конструирование экспрессионной плазмиды СВН II. Родительские и химерные гены, кодирующие ферменты СВН II, клонировали в дрожжевом экспрессионном векторе YEp352/PGK91-1-αss (Фиг.6). Последовательности ДНК, кодирующие родительские и химерные каталитические домены СВН II, конструировали со сдвигом кодонов для S. cerevisiae, используя программное обеспечение GeneDesigner (DNA2.0), и синтезировали с помощью DNA2.0. Гены каталитического домена СВН II расщепляли Xhol и Kpnl, лигировали в векторе между сайтами Xhol и Kpnl и трансформировали в E. coli XL-1 Blue (Stratagene). Гены СВН II секвенировали, используя праймеры: CBH2L (5′-GCTGAACGTGTCATCGGTTAC-3′ (SEQ ID NO:9) и RSQ3080 (5′-GCAACACCTGGCAATTCCTTACC-3′ (SEQ ID NO:10)). Родительские и химерные конструкции СВН II с С-концевым His6 были получены путем амплификации гена СВН II с прямым праймером CBH2LPCR (5′-GCTGAACGTGTCATCGTTACTTAG-3′ (SEQ ID NO:11)) и обратными праймерами, комплементарными соответствующему гену СВН II с выступающим концом Hise и стоп-кодонами. Продукты ПЦР лигировали, трансформировали и секвенировали, как описано выше.
Экспрессия фермента СВН II в S. cerevisiae. Штамм S. cerevisiae YDR483W BY4742 (Mata his3Δ1 leu2Δ0 lys2Δ0 ura3Δ0 ΔKRE2, ATCC No. 4014317) делали компетентным, используя набор для трансформации дрожжей EZ Yeast II (Zymo Research), трансформировали плазмидной ДНК и высевали на синтетический агар без урацила. Колонии собирали в 5 мл ночные культуры синтетической среды с декстрозой и казаминовыми кислотами (SDCAA) (20 г/л декстрозы, 6,7 г/л дрожжевых азотистых оснований Difco, 5 г/л казаминовых кислот Bacto, 5,4 г/л Na2HPO4, 8,56 г/л NaH2PO4·H2O) с добавлением 20 мкг/мл триптофана и выращивали в течение ночи при 30°С, 250 об/мин. 5 мл культуры наращивали в 40 мл SDCAA в 250 мл колбах Tunair (Shelton Scientific) и встряхивали при 30°С, 250 об/мин в течение 48 часов. Культуры центрифугировали, и супернатанты концентрировали до 500 мкл, используя ячейку для ультрафильтрации Amicon, оборудованную мембраной 30-кДа ПЭС (полиэфирсульфон), для использования в анализах t1/2. Концентрированные супернатанты доводили до 1 мМ фенилметилсульфонилфторида и 0,02% NaN3. HiS6-меченые белки СВН II очищали, используя спин-колонки Ni-NTA (Qiagen) согласно протоколу изготовителя, и белки обменивали в 50 мМ ацетате натрия, рН 4,8, используя обессоливающие колонки Zeba-Spin (Pierce). Концентрацию белка определяли, используя реагент для белков Кумасси-плюс Pierce, с БСА в качестве стандарта. Анализ с помощью электрофореза в ДСН-ПААГ проводили путем нанесения либо 20 мкл концентрированного супернатанта культуры, либо примерно 5 мкг очищенного фермента СВН II на гель с 7,5% Трис-HCl (Biorad) и окрашивания безопасным красителем SimplyBlue (Invitrogen). Супернатанты или очищенные белки СВН II обрабатывали EndoH (New England Biolabs) в течение 1 ч при 37°С в соответствии с инструкциями изготовителя. Активность фермента СВН II в концентрированных супернатантах дрожжевой культуры измеряли путем добавления 37,5 мкл концентрированного супернатанта культуры к 37,5 мкл PASC и инкубации в течение 2 ч при 50°С. Образовавшиеся эквиваленты восстанавливающего сахара определяли с помощью анализа Шомоди-Нельсона, как описано ниже.
Измерения периода полураспада, удельной активности, рН-активности и долговременного гидролиза целлюлозы. Готовили целлюлозу, набухшую в фосфорной кислоте (PASC). Для усиления активности фермента СВН II на субстрате PASC предварительно инкубировали при концентрации 10 г/л с 10 мг/мл эндоглюканазы A. niger (Sigma) в 50 мМ ацетате натрия, рН 4,8 в течение 1 ч при 37°С. Эндоглюканазу инактивировали нагреванием при 95°С в течение 15 минут, PASC дважды промывали 50 мМ ацетатным буфером и ресуспендировали при 10 г/л в деионизованной воде.
Значения t1/2 фермента СВН II измеряли путем добавления концентрированного супернатанта экспрессионной культуры СВН II к 50 мМ ацетату натрия, рН 4,8 при концентрации, дающей А520 0,5, как измерено в анализе восстанавливающего сахара Шомоди-Нельсона после инкубации с обработанной PASC, как описано выше. 37,5 мкл смесей фермент СВН II/буфер инактивировали в водяной бане при 63°С. После инактивации добавляли 37,5 мкл PASC, обработанной эндоглюканазой, и проводили гидролиз в течение 2 ч при 50°С. Реакционные супернатанты фильтровали через планшеты Multiscreen HTS (Millipore). Значения анализа Шомоди-Нельсона log(A520), полученные с использованием считывающего устройства для планшетов SpectraMax (Molecular Devices), скорректированные на фоновое поглощение, наносили на график против времени, и периоды полураспада фермента СВН II получали на основании линейной регрессии, используя Microsoft Excel.
Для измерений удельной активности очищенный фермент СВН II добавляли к PASC до получения конечного объема реакции 75 мкл 25 мМ ацетат натрия, рН 4,8, с 5 г/л PASC и концентрации фермента СВН II 3 мг фермента/г PASC. Инкубация происходила в течение 2 ч в 50°С водяной бане, и определяли концентрацию восстанавливающего сахара. Для измерений профиля рН/активности очищенный фермент СВН II добавляли при концентрации 300 мкг/г PASC в объеме реакции 75 мкл. Реакционные смеси забуферивали 12,5 мМ цитратом натрия/12,5 мМ фосфатом натрия, проводили в течение 16 ч при 50°С и определяли восстанавливающий сахар. Измерения долговременного гидролиза целлюлозы проводили с объемами 300 мкл 1 г/л обработанной PASC в 100 мМ ацетате натрия, рН 4,8, 20 мМ NaCl. Очищенный фермент СВН II добавляли при 100 мкг/г PASC, и реакции проводили в водяных банях в течение 40 ч перед определением восстанавливающего сахара.
Пять родительских генов-кандидатов, кодирующих ферменты СВН II, были синтезированы со сдвигом кодонов для S. cerevisiae. Все пять содержали идентичные N-концевые кодирующие последовательности, где остатки 1-89 соответствуют целлюлозосвязывающему модулю (СВМ), гибкий линкерный участок и пять N-концевых остатков каталитического домена Н. jecorina. Два из ферментов-кандидатов СВН II от Humicola insolens и Chaetomium thermophilum секретировались из S. cerevisiae при значительно более высоких уровнях, чем три другие от Hypocrea jecorina, Phanerochaete chrysosporium и Talaromyces emersonii (Фиг.1). Поскольку полосы в ДСН-ПААГ геле для трех слабо экспрессирующихся родителей-кандидатов был трудно увидеть, проводили анализы активности, в которых концентрированные супернатанты культуры инкубировали с целлюлозой, набухшей в фосфорной кислоте (PASC), чтобы подтвердить присутствие активной целлюлазы. Значения для образовавшегося восстанавливающего сахара, представленные на Фиг.1, подтвердили присутствие активного СВН II в концентрированных супернатантах культуры S. cerevisiae для всех ферментов за исключением СВН II Т. emersonii. Последовательности Н. insolens и С. thermophilum были выбраны для рекомбинации с наиболее промышленно релевантным ферментом грибов СВН II из Н. jecorina. Идентичности соответствующих последовательностей каталитических доменов составляют 64% (1:2), 66% (2:3) и 82% (1:3), где Н. insolens является родителем 1, Н. jecorina является родителем 2 и С. thermophilum является родителем 3. Эти соответствующие каталитические домены содержат 360, 358 и 359 аминокислотных остатков.
Экспрессию гетерологичного белка в мицелиальном грибе Н. jecorina, организме, чаще всего используемом для продуцирования целлюлаз для промышленных применений, значительно более труднодоступна, чем в Saccharomyces cerevisiae. Наблюдаемая секреция СВН II Н. jecorina из S. cerevisiae мотивировала выбор гетерологичного хозяина. Чтобы минимизировать избыточное гликозилирование, которое, как сообщили, снижает активность рекомбинантных целлюлаз, рекомбинантные гены СВН II экспрессировали в штамме dKRE2 S. cerevisiae с дефицитом гликозилирования. Ожидают, что данный штамм присоединяет олигомеры маннозы меньшего размера к обоим сайтам N-связанного и O-связанного гликозилирования, чем штаммы дикого типа, что ближе всего напоминает гликозилирование нативно продуцируемого фермента СВН II Н. jecorina. Анализ белков СВН II в электрофорезе ДСН-ПААГ, как с обработкой, так и без обработки EndoH для удаления структур с высоким содержанием маннозы, показал, что обработка EndoH не увеличивает электрофоретическую подвижность ферментов, секретируемых из этого штамма, что подтверждает отсутствие разветвленных маннозных группировок, которые штаммы S. cerevisiae дикого типа присоединяют к сайтам гликозилирования в рекомбинантных белках.
Высокое разрешение структуры Н. insolens (pdb entry 1ocn) использовали в качестве матрицы для SCHEMA, чтобы идентифицировать контакты, которые могли бы быть разрушены при рекомбинации. Алгоритм RASPP выдал четыре библиотеки-кандидата, где для каждой значение <E> было ниже 15. Все библиотеки-кандидаты имели более низкое значение <Е>, чем ранее сконструированные библиотеки химер, что позволяет предположить, что приемлемая доля уложенных, активных химер может быть получена для относительно высокого значения <m>. Разнообразие химерных последовательностей было увеличено до максимума за счет выбора границ блоков, приводящего к самому высокому значению <m> = 50. Блоки для данного дизайна проиллюстрированы на Фиг.2В и подробно описаны в таблице 2.
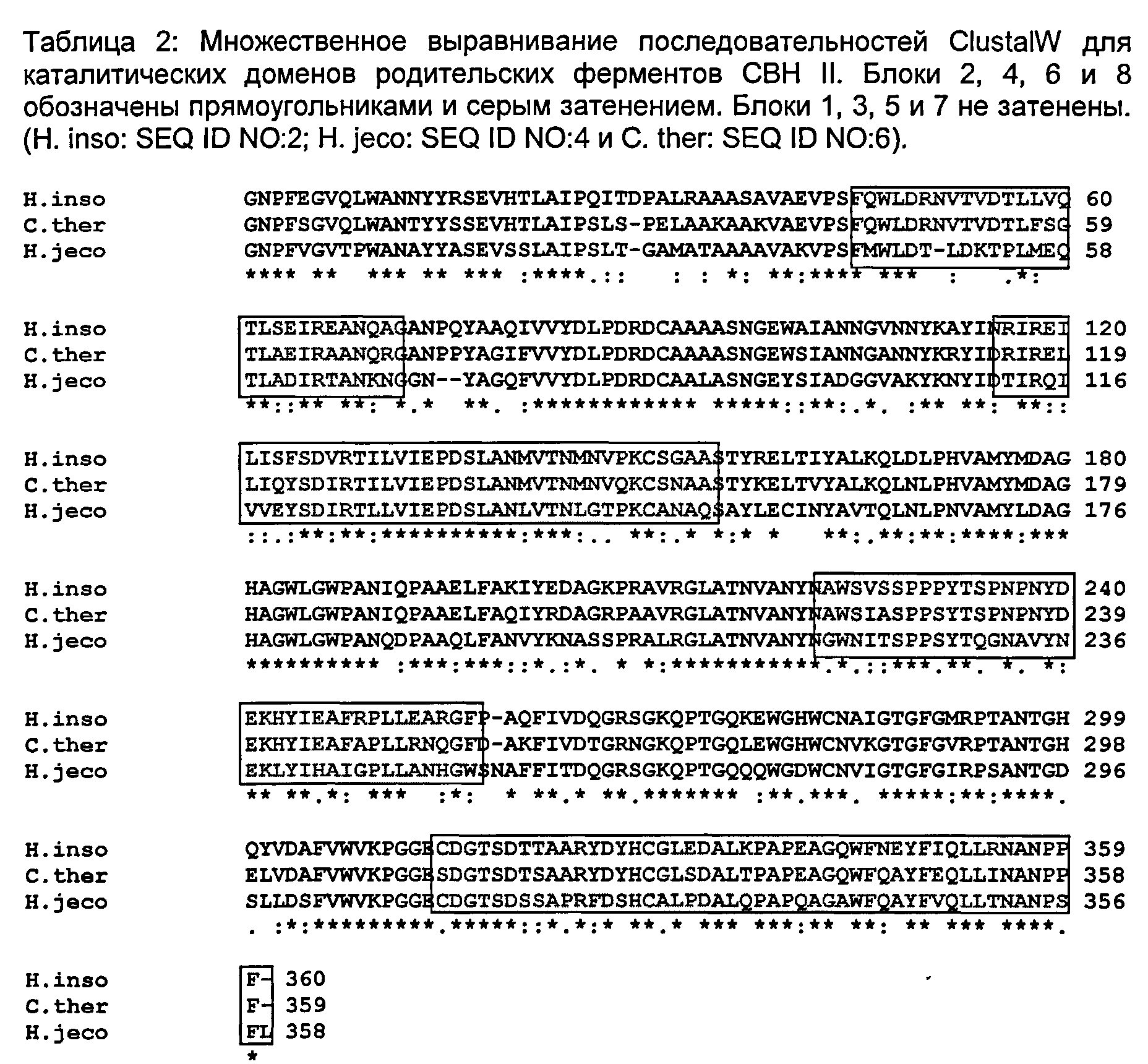
Каталитический домен СВН II Н. insolens имеет α/β бочковидную структуру, в которой восемь спиралей определяют периметр бочонка, а семь параллельных β-складок образуют активный центр (Фиг.2А). Две протяженные петли образуют крышу над активным центром, создавая туннель, через который проходят целлюлозные цепи субстрата в процессе гидролиза. Пять из семи границ блоков попадают между элементами вторичной структуры, тогда как блок 4 начинается и заканчивается в середине следующих друг за другом α-спиралей (Фиг.2А, 2В). Большинство межблочных контактов боковых цепей встречается между блоками, которые являются примыкающими в первичной структуре (Фиг.2С).
Серия образцов из 48 химерных генов была сконструирована в виде трех групп по 16 химер, имеющих пять блоков от одного родителя и три блока либо от одного, либо от обоих остальных двух родителей (таблица 3); последовательности были выбраны так, чтобы выровнять присутствие каждого родителя в положении каждого блока. Соответствующие гены были синтезированы и экспрессированы.
|
Двадцать три из серии 48 образцов концентрированных супернатантов культуры S. cerevisiae проявляли гидролитическую активность в отношении PASC. Эти результаты позволяют предположить, что тысячи из 6561 возможных химерных последовательностей СВН II (см., например, таблицу 1) кодируют активные ферменты. 23 активные химеры СВН II серии образцов проявляют значительное разнообразие последовательностей, отличающихся от ближайшей родительской последовательности и друг от друга по меньшей мере 23 и 36 аминокислотными заменами, и не менее 54 и 123, соответственно. Их средний уровень мутаций <m> составляет 36.
Поскольку авторами Meyer et аl. обнаружены корреляции между Е, m и вероятностью того, что химера является уложенной и активной, был проведен анализ, существуют ли подобные корреляции для серии образцов химер СВН II. Количество активности фермента СВН II в концентрированных супернатантах экспрессионных культур, измеренное путем количественного определения активности на PASC, коррелировало с интенсивностью полос СВН II в ДСН-ПААГ гелях (Фиг.1). Как для родительского СВН II Н. jecorina, активность можно было обнаружить для некоторых химер СВН II с необнаружимыми полосами в геле. Химер СВН II, представленных полосами в геле, но с отсутствием активности, не наблюдали. Вероятность того, что химера СВН II секретируется в активной форме, была связана обратной связью как с Е, так и с m (Фиг.3).
Периоды полураспада термической инактивации (t1/2) измеряли при 63°С для концентрированных супернатантов культур родительского и активных химерных ферментов СВН II. Периоды полураспада для СВН II родителей Н. insolens, Н. jecorina и С.thermophilum составляли 95, 2 и 25 минут соответственно (таблица 1). Активные химеры серии образцов проявляли более широкий диапазон периодов полураспада, от менее 1 минуты до более 3000. Пять из 23 активных химер имели периоды полураспада выше, чем наиболее термостойкий родительский СВН II Н. insolens.
При попытке конструирования предсказательной количественной модели для периода полураспада химеры СВН II было использовано пять различных алгоритмов, моделирующих данные линейной регрессии (таблица 4). Каждый алгоритм использовали для конструирования модели, связывающей составы блоков каждой химеры серии образцов СВН II и родителей с log(t1/2). С помощью этих моделей получили взвешенные значения термостойкости, которые количественно определяли вклад блока в log(t1/2). Для всех пять алгоритмов моделирования этот процесс повторяли 1000 раз с двумя случайно выбранными последовательностями, исключенными из каждого вычисления, так что каждый алгоритм давал 1000 взвешенных значений для каждого из 24 блоков. Среднее и стандартное отклонение (SD) вычисляли для взвешенной термостойкости каждого блока. Предсказательную точность каждого алгоритма модели оценивали путем измерения, насколько хорошо каждая модель предсказывала значения t1/2 двух исключенных последовательностей. Корреляция между измеренными и предсказанными значениями для 1000 итераций алгоритма является баллом перекрестной проверки достоверности модели для алгоритма. Для всех пяти моделей баллы перекрестной проверки достоверности (X-val) были меньшими или равными 0,57 (таблица 4), что показывает, что моделирование линейной регрессии неприменимо для данной малой серии данных t1/2 23 химер для количественного предсказания периода полураспада химеры СВН II.
|
Моделирование линейной регрессии использовали для качественной классификации блоков как стабилизирующих, дестабилизирующих или нейтральных. Влияние каждого блока на термостойкость химеры характеризовали, используя балльную систему, которая основана на вкладе в термостойкость, определенном с помощью каждого из алгоритмов регрессии. Для каждого алгоритма блоки с взвешенным значением термостойкости более 1 SD выше нейтрального оценивали ″+1″, блоки в пределах 1 SD нейтрального оценивали как ноль, и блоки на 1 или более SD ниже нейтрального оценивали как ″-1″. ″Балл стабильности″ для каждого блока получали путем суммирования баллов стабильности 1, 0, -1 от каждой из пяти моделей. В таблице 5 суммированы баллы для каждого блока. Блок 1/родитель 1 (В1Р1), В6РЗ, В7РЗ и В8Р2 были идентифицированы как обладающие самыми высокими стабилизирующими эффектами, тогда как было обнаружено, что В1РЗ, В2Р1, ВЗР2, В6Р2, В7Р1, В7Р2 и В8РЗ являются наиболее сильно дестабилизирующими блоками.
|
Вторую серию генов, кодирующих химеры фермента СВН II, синтезировали с целью проверки достоверности предсказанных стабилизирующих блоков и идентификации целлюлаз, более термостойких, чем наиболее термостойкий родитель. В 24 химерах, включенных в данную серию проверки (таблица 6), отсутствовало семь блоков, предсказанных как наиболее дестабилизирующие, и они были обогащены четырьмя наиболее стабилизирующими блоками, где присутствие было смещено в направлении баллов более высокой стабильности.
Кроме того, была сконструирована химера ″HJPlus″ 12222332 путем замены предсказанных наиболее стабилизирующих блоков в ферменте СВН II Н. jecorina (родитель 2).
|
Концентрированные супернатанты экспрессионных культур S. cerevisiae для девяти из 24 химер серии проверки достоверности, а также химеры HJPlus, проявляли активность в отношении PASC (таблица 6). Из 15 химер, для которых активность не была обнаружена, девять содержали блок В4Р2. Из 16 химер, содержащих В4Р2 в первоначальной серии образцов, только одна проявляла активность в отношении PASC. Суммируя обе серии химер и HJPlus, только две из 26 химер, характеризующихся В4Р2, были активными, что указывает на то, что данный конкретный блок является в высокой степени разрушительным для экспрессии активной целлюлазы в S. cerevisiae.
Были проверены стабильности 10 функциональных химерных ферментов СВН II из серии проверки достоверности. Поскольку стабильные ферменты уже имели периоды полураспада более 50 часов, остаточную гидролитическую активность в отношении PASC после 12-часовой термической инактивации при 63°С использовали как меру для предварительной проверки. Эта 12-часовая инкубация приводила к измеримому снижению активности наиболее термостойкой химеры серии образцов, 11113132, и полностью инактивировала наиболее термостойкий родительский СВН II Н. insolens. Все десять функциональных химер серии проверки достоверности сохранили более высокую долю своей активности, чем наиболее стабильный родительский СВН II Н. insolens.
Проанализировали активности отобранных термостойких химер с использованием очищенных ферментов. Родительские ферменты СВН II и три термостойкие химеры, наиболее термостойкую химеру серии образцов 11113132, наиболее термостойкую химеру серии проверки достоверности 13311332 и химеру HJPlus 12222332 экспрессировали с С-концевыми метками Hiss для очистки и очищали. Для минимизации термической инактивации ферментов СВН II во время теста на активность авторы изобретения использовали более кратковременную двухчасовую инкубацию с субстратом PASC при 50°С, рН 4,8. Как показано в таблице 3, удельные активности родительских и химерных СВН II находились в пределах коэффициента четыре наиболее активного родительского фермента СВН II от Н. jecorina. Удельная активность HJPlus была выше, чем у всех других протестированных ферментов СВН II за исключением СВН II Н. jecorina.
Зависимость от рН целлюлазной активности также важна, поскольку широкий профиль рН/активности дал бы возможность использовать химеру СВН II при более широком диапазоне потенциальных условий гидролиза целлюлозы. Наблюдали, что СВН II Н. jecorina обладает оптимальной активностью в диапазоне рН от 4 до 6, причем вне этих значений активность заметно снижается. 16 На Фиг.4 показано, что ферменты СВН II Н. insolens и С. thermophilum и все три очищенные термостойкие химеры СВН II имели профили рН/активности, которые являются значительно более широкими, чем у СВН II Н. jecorina. Хотя Liu et al. сообщают оптимальный рН 4 для СВН II С. thermophilum, оптимальный рН рекомбинантного фермента в данной заявке составлял около 7. Нативный СВН II Н. insolens имел широкий профиль рН/активности при максимальной активности около рН 9 и примерно 60% этой максимальной активности при рН 4. Подобно широкий профиль наблюдали для рекомбинантного фермента. Химера HJPlus имела значительно более широкий профиль рН/активности, чем СВН II Н. jecorina, проявляя зависимость от рН, подобную двум другим родительским ферментам СВН II.
Достижение активности при повышенной температуре и сохранение активности в течение пролонгированных интервалов времени являются двумя основными мотивациями для конструирования высоко стабильных ферментов СВН II. Характеристики термостойких химер СВН II при гидролизе целлюлозы тестировали на протяжении диапазона температур в течение 40-часового интервала времени. Как показано на Фиг.5, все три термостойкие химеры проявляли активность на PASC при более высоких температурах, чем родительские ферменты СВН II. Химеры сохраняли активность при 70°С, тогда как СВН II Н. jecorina не гидролизовал PASC выше 57°С, и стабильный фермент Н. insolens не проявлял гидролиза при 63°С. Активность HJPlus в анализе долговременного гидролиза целлюлозы превышала активность всех родителей при их соответствующих оптимальных температурах.
Библиотека СВН II имела меньшие потенциальные прерывания по нескольким причинам. В дополнение к более высокой идентичности родительских последовательностей СВН II, бочковидная топология укладки СВН II ограничивает число контактов большого радиуса действия, которые могут быть разрушены рекомбинацией. Межблочные контакты (тяжелые атомы в пределах 4,5 Å) составляют только 27% (503/1831) всех контактов на карте контактов структуры Н.insolens 1ocn. Когда только учтенные контакты, для которых новые пары остатков возможны в химерах, суммарные межблочные контакты снижены до 23% (68/294). Кроме того, большинство этих взаимодействий происходит между остатками на поверхности белка, и возможность улавливания растворителя дополнительно снижает шансы резко деструктивных взаимодействий между остатками (Фиг.14а). Одно исключение, углубленное взаимодействие между положениями 176 и 256, проиллюстрировано на Фиг.14b. В этом сайте химеры с В6Р2 и либо В5Р1, либо В5Р3 спаривают Met173:Trp253 (большей аминокислотой, чем родительская пара Met176:Phe256 или Leu173:Trp253). Тем не менее, при исследовании родительских кристаллографических моделей стерическое столкновение в данном положении считали невероятным вследствие движения в участке белкового каркаса, которое располагает Trp253, и собственной гибкости боковых цепей Met. Примечательно, что одна охарактеризованная химера соответствует данному паттерну (13333232) и является более стабильной, чем родители (67°С), при приведении в соответствие с регрессионной моделью (68°С).
Другой механизм, посредством которого может происходить спаривание, структурная дивергенция блоков, не зависит от присутствия новых пар остатков на границах блоков, вместо этого, по мере того как дивергируют родительские последовательности, могут дивергировать внутренние структуры блоков, затрудняя модульные пересадки блоков. В случае библиотеки СВН II высокие значения идентичности родительских пар (82%, 66% и 64%) предполагают, что вероятны только минорные отклонения структуры (среднее квадратичное отклонение, RMSD,<1 Å). Эту возможность можно оценить путем сравнения кристаллографических структур для СВН II H.insolens и H.jecorina (у СВН II C. therinophilum отсутствует кристаллическая структура, но он на 82% идентичен Н. insolens). Выравнивания блоков из структур для каждого родителя (1ocn и 1cb2) создает низкие значения RMSD альфа-углерода (RMSD 0.5, 0.5, 0.6, 0.5, 0.3, 0.7, 0.3 и 0.4 Å). Блоки Н. jecorina, наложенные на Н. insolens, проиллюстрированы в дополнении к Фиг.5 с.Для проверки контекст-зависимых эффектов была проведена структурная рекомбинация in silico со сплайсингом каждого выровненного блока на структуре противоположного хозяина. Возможно сконструировать структурные модели без столкновений (альфа-атомы углерода на расстоянии более 3 Å) для всех химер с заменой одного блока (например, 11112111 или 22122222), за исключением минорного столкновения (2,65 Å) при использовании В7Р2 (11111121) вследствие инсерции Asn между блоками 6 и 7 (Фиг.14D).
Следующие эксперименты были проведены, чтобы определить вклады различных блоков/сегментов в стабильность химеры и улучшенную термостойкость и/или рН стабильность. Родительские и химерные гены, кодирующие ферменты СВН II, клонировали в дрожжевом экспрессионном векторе YEp352/PGK91-1-αss и экспрессировали в синтетической среде с декстрозой и казаминовыми кислотами (SDCAA). Для анализов активности на Avicel супернатанты дрожжевых культур на среде с пептоном и декстрозой (YPD) доводили до 1 мМ фенилметилсульфонилфторида и 0,02% NaN3 и использовали без концентрирования. Ферментативную активность СВН II в концентрированных супернатантах дрожжевых культур на SDCAA измеряли путем добавления разведении концентрированного супернатанта культуры в 37,5 мкл PASC и 225 мкл 50 мМ ацетата натрия, рН 4,8 и инкубации в течение 2 ч при 50°С. Эквиваленты образовавшегося восстанавливающего сахара определяли с помощью анализа Шомоди-Нельсона.
Значения T50 фермента СВН II измеряли путем добавления концентрированного супернатанта экспрессионной культуры в SDCAA к 50 мМ ацетату натрия, рН 4,8, при концентрации, дающей А520 0,5 при измерении в анализе на восстанавливающий сахар Шомоди-Нельсона после инкубации с PASC, обработанной эндоглюканазой. Смеси 200 мкл фермента СВН II/буфера инкубировали в водяной бане при интересующей температуре в течение 10 минут. После инкубации добавляли 37,5 мкл PASC, обработанной эндоглюканазой, и 62,5 мкл 50 мМ ацетата натрия, и гидролиз проводили в течение 2 ч при 50°С. температуру инкубации, при которой фермент терял половину своей активности, определяли путем линейной интерполяции значений А520 анализа Шомоди-Нельсона, нанесенных на график против температуры.
Для измерений долговременного гидролиза Avicel PH101 (Fluka) 0,3 мкг очищенного СВН II инкубировали с 3 мг Avicel в 270 мкл 50 мМ ацетата натрия, рН 4,8, в пробирках для ПЦР, помещенных в водяную баню, в течение 16 часов. Пробирки охлаждали в водяной бане комнатной температуры в течение 10 минут, центрифугировали при 1000 g в течение 10 минут, и супернатанты отбирали на анализ восстанавливающего сахара.
Для оценки активности СВН II в супернатантах экспрессионных культур в YPD объемы супернатантов в диапазоне от 2 мл до 40 мл добавляли к 800 мкл 33 мг/мл Avicel, суспендированного в 50 мМ ацетате натрия, рН 4,8, в конических пробирках. Ферментам СВН II давали возможность связаться с Avicel при 4°С в течение одного часа, центрифугировали при 2000 g в течение 2 минут и дважды промывали 50 мМ ацетатом натрия, рН 4,8. После второй промывки СВН II-связанный Avicel ресуспендировали в 2,75 мл натрийацетатного буфера, делили на аликвоты по 270 мкл и инкубировали при 50°С в течение 2,5 часов. Центрифугирование и анализ восстанавливающего сахара проводили, как описано выше.
Пакет программ линейной регрессии в Mathematica использовали для приведения в соответствие данных Т50 химер СВН II с 17-параметрической аддитивной моделью блока и также использовали для анализа перекрестной проверки достоверности. Эффекты блока сообщают относительно референсного состояния родителя 1 (Н. insolens СВН II) с 16 параметрами, представляющими замену каждого из 8 блоков блоками от родителей 2 и 3.
Значения T50, определенные в данной заявке как температура, при которой фермент теряет 50% его активности во время десятиминутной инкубации, были определены для трех родительских целлобиогидролаз, 33 активных химер СВН II из предшествующих экспериментов и 18 дополнительных химер, предсказанных качественным моделированием стабильности как находящиеся среди наиболее термостойких, то есть не содержащие ни одного из 7 предсказанных дестабилизирующих блоков и содержащие либо 3, либо 4 из 4 предсказанных стабилизирующих блоков. Последовательности всех химер в количестве 51 приведены в таблице 8. Повторное культивирование и повторное концентрирование всех предсказанных термостойких химер, ранее классифицированных как несекретируемые, дало возможность получения достаточных количеств СВН II 12112132, 13111132 и 13322332 для определения Тбо. Полная серия значений Т50 для химер и родительских СВН II приведена в таблице 8. Аминокислотные последовательности для всех этих СВН II показаны в таблице 7. Все предсказанные протестированные термостойкие химеры в количестве 31 имели значения Т50 более чем на два градуса выше, чем наиболее термостойкий родительский фермент (64,8°С). В таблице также идентифицирован остаток Cys в блоке/домене 7, который может быть мутирован на Ser для получения повышенной термостойкости. Соответственно, в изобретении предложен полипептид любой из нижеследующих последовательностей, где подчеркнутый/выделенный курсивом/выделенный полужирным шрифтом Cys заменен остатком Ser, и где полученный в результате полипептид обладает улучшенной термостойкостью по сравнению с ферментом дикого типа.
|










|
|
Применение линейной регрессии к данным последовательности - стабильности привело в результате к десятипараметрической модели, которая соответствует наблюдаемым значениям Т50 с R2=0,88 (Фиг.8). Чтобы лучше оценить предсказательную способность регрессионной модели вне испытательной серии, была проведена одиннадцатикратная проверка достоверности, которая привела в результате к R2 0,57, где удаление двух резко отклоняющихся значений (11313121 и 22222222) повышает достоверность перекрестной проверки R2 до 0,76. В регрессионной модели использован наиболее стабильный родитель 1 (Н. insolens) в качестве референсного значения Т50, и она включает девять дополнительных элементов, имеющих значение р ≤ 0,1. Параметры модели (таблица 9) показывают, что единственный блок, блок 7 от родителя 3 (В7Р3), вне всяких сомнений вносит самый сильный вклад в термостойкость химер относительно СВН II Н. insolens. Этот блок от СВН II С. thermophilum вносит вклад примерно 8,5°С в стабильность химер, которые его содержат. Было обнаружено, что два из 8 остальных блоков со значениями р ≤ 0,1 вносят меньшие вклады в стабильность, 1,2°С и 2,7°С, тогда как другие шесть снижают стабильность.
|
Выравнивание последовательностей В7Р1 и В7Р3 (Фиг.10) показывает, что блок 7 различается на 10 из 56 положений аминокислот в ферментах Н. insolens и С. thermophilum. В генетическом фоне химеры с самым высоким значением T50, 21311131, каждый остаток в В7Р3 (сегмент 7 родителя 3 (SEQ ID NO:6)) был индивидуально мутирован до соответствующего остатка в В7Р1 (сегмент 7 родителя 1 (SEQ ID NO:2)), и определены значения Т50 для каждого из полученных точечных мутантов. Мутация, S313C, значительно изменяла термостойкость химеры: данная одиночная мутация снижала Т50 21311131 примерно на 10°С (Фиг. 11).
Для изучения эффекта обратной мутации в различных генетических фонах гены для родительских СВН II Н. insolens и H. jecorina, кодирующие замену C313S (C314S в Н. insolens и C311S в Н. jecorina) были сконструированы, экспрессированы, и определены значения Т50 ферментов. Также количественно определяли стабильности химер 11111131 и 22222232, в которых стабилизирующий блок В7Р3 заменен с образованием ферментов дикого типа Н. insolens и Н. jecorina. Как замена блока В7Р3, так и точечная мутация Cys-Ser значительно стабилизировала родительские СВН II; самым высоким эффектом было ~8°С повышение Т50 для СВН II H. jecorina, содержащего замену C311S (Фиг.12). Мутацию Cys-Ser также тестировали в двух химерах, 31311112 и 13231111, которые не содержат В7Р3, а также в гомологичном СВН II (от Phanerochaete chrysosporium), который отсутствовал в рекомбинантной серии родителей. Каталитический домен СВН II Р. chrysosporium только на 55-56% идентичен каталитическим доменам родительских СВН II. Все эти ферменты стабилизировались в результате замены Cys-Ser; СВН II Р. chrysosporium был значительно стабилизирован на 10°С (Фиг.13).
Восемь из термостойких химер СВН II и родительских ферментов, содержащих эквивалентную мутацию C313S, были мечены His6-меткой и очищены таким образом, чтобы можно было определить их удельные активности. Как показано в таблице 10А, удельные активности, которые измеряли на аморфной целлюлозе (PASC) при 50°С, для этих химер и нативных ферментов, содержащих мутацию Cys-Ser, сходны с таковыми для родителей дикого типа. Таким образом, повышенная термостойкость осуществляется не за счет удельной активности.
|
|
Затем те же восемь термостойких химер (Т50 на 2-10°С выше, чем для наиболее стабильного родителя) тестировали на активность на кристаллической целлюлозе в течение 16-часовой инкубации на протяжении диапазона температур, включающего температуры, где родительские ферменты проявляют малую активность или не проявляют никакой активности. На Фиг.9а показано, что 7 из 8 протестированных термостойких химер обладали максимальной активностью в отношении Avicel при 60-65°С, причем все 8 химер сохраняли активность при 70°С, самой высокой тестируемой температуре. Напротив, три родительские СВН II проявляют максимальную активность при 50°С и полностью или почти полностью неактивны при 70°С. Кроме того, семь химер с повышенными оптимальными температурами активности гидролизуют значительно большее количество Avicel, чем любой из родительских ферментов СВН II. Как показано на Фиг.9b, подобное поведение наблюдают для родителей Н. insolens и Н. jecorina, содержащих точечную мутацию Cys-Ser. Точечная мутация Cys-Ser также повышала гидролиз Avicel и максимальную рабочую температуру для СВН II Р. chrysosporium. Замена блока РЗВ7, которую осуществляли в родителях Н. insolens и Н. jecorina, повышала как рабочую температуру, так и гидролиз СВН II Н. insolens, но, несмотря на повышение максимальной рабочей температуры, не улучшала общий гидролиз целлюлозы ферментом Н. jecorina.
Низкую (менее 1 мг/л) секрецию СВН II Н. jecorina дикого типа из гетерологичного хозяина экспрессии S. cerevisiae. Мутация C311S в ферменте СВН II Н. jecorina дикого типа значительно повышает суммарную секретируемую активность СВН II (таблица 11). В синтетической среде (SDCAA) замены C311S и В7Р3 повышают суммарную секретируемую активность СВН II Н. jecorina в два раза, тогда как в богатой среде (YPD) повышение активности является десятикратным. Для родительского СВН II Н. insolens, который экспрессируется на значительно более высоких уровнях, чем два других родительских СВН II, мутация C314S повышала секретируемую активность примерно в 1,5 раза, тогда как замена блока В7Р3 снижала ее. Поскольку дикий тип и мутанты Cys-Ser Н. insolens и Н. jecorina все обладают сходными удельными активностями (таблица 10), увеличение суммарной секретируемой целлюлазной активности является результатом улучшенной секреции функционального фермента. Наблюдается корреляция между секрецией гетерологичного белка S. cerevisiae и стабильностью белка, что позволяет предположить, что повышенная секреция мутанта Cys-Ser СВН II может отражать его более высокие стабильности.
|
|
Для моделирования мутации Cys-Ser использовали высокое разрешение кристаллической структуры СВН II Н. insolens 1ocn. Сначала оптимизировали сеть водородных связей с помощью REDUCE. Было предсказано, что Cys314 образует водородную связь с карбонилом Pro 339. Для подтверждения этого предсказания укладку боковых цепей оптимизировали, используя платформу моделирования SHARPEN. Предсказано, что Ser314 осуществляет взаимодействия, подобные Cys314, приводящие в результате к более сильному водородному связыванию и более благоприятной геометрии (Фиг.14).
Ряд эффектов может объяснить, почему мутация Cys-Ser стабилизирует широкий ряд СВН II, включая нативные СВН II и химеры. Cys и Ser являются подобными (хотя не изостерическими), и эти две аминокислоты доминируют в выравниваниях последовательностей в этом положении по сравнению с другими альтернативами. Схемы водородного связывания для этого остатка являются структурными элементами (амид Gly316 и карбонил Pro339), и поэтому менее вероятно зависят от вариаций третьесторонних аминокислот. Кроме того, непосредственно примыкающие боковые цепи для этого кармана (Asn283, Pro339, Phe345) являются консервативными среди всех четырех исследованных нативных целлюлаз СВН II.
Высокое разрешение (1.3 Å) кристаллической структуры Н. insolens (pdb entry 1ocn6) показывает, что Cys314 составляет часть сети водородных связей (Фиг.15). Повышенная способность к водородному связыванию Ser относительно Cys может позволить предположить роль более сильных взаимодействий водородного связывания в стабилизации. Кристаллическая структура также позволяет предположить, что Ser может быть предпочтительным по стерическим причинам. Конкретно, когда боковая цепь Cys заново строится с каноническими углами связей, наклон 6° исчезает, и Cys проталкивается ближе к карбонилу Pro339, создавая неблагоприятное стерическое взаимодействие.
Выравнивание 196 белковых последовательностей, обладающих самой высокой идентичностью с СВН II Н. jecorina. Пятьдесят четыре из 250 наиболее идентичных последовательностей было исключено из выравнивания вследствие избыточности (то есть точечных мутаций для структурных исследований или более 95% идентичных изоформ). Существует предпочтительный сдвиг в направлении Ser311: 158 последовательностей имеет Ser, 20 имеет Ala, 10 имеет Cys, 5 имеет делецию, и 3 имеет Gly. Однако существует 42 других положения, где наиболее частый выбор осуществляется более чем с двукратной частотой аминокислоты Н. jecorina.
Большой стабилизирующий эффект мутации Cys-Ser создает возможность, что Ser в данном положении является глобальным показателем термостойкости нативной целлюлазы. Однако Т50 64,8°С для СВН II Н. insolens, который характеризуется Cys в данном положении, является более высокой, чем для СВН II С.thermophilum (64,0°C), указывая на то, что Ser является не единственной детерминантой стабильности.
Термостойкость является не единственным свойством, представляющим интерес для промышленных целлюлаз. Важны также удельная активность, изменения в связывании целлюлозы и эффекты на экспрессию и ингибирование продуктом. Представленные в данной заявке химеры и данные демонстрируют, что рекомбинация образует химеры СВН II, улучшенная термостойкость которых происходит не за счет удельной активности, измеренной в анализах кратковременного (например, 2-часового) гидролиза целлюлозы. Подобные наблюдения были сделаны для СВН II, содержащих термостабилизирующую мутацию Cys-Ser. В анализах долговременного гидролиза несколько из химер СВН II и все три протестированных мутанта Cys-Ser СВН II гидролизовали большее количество целлюлозы, чем нативные СВН II. Данное лучшее качество, вероятно, является результатом обладания удельной активностью, сравнимой с родительскими СВН II, параллельно с более высокой термостойкостью, которая позволяет ферменту продолжать функционировать в течение более длительного времени при повышенных температурах, поскольку эти анализы проводили с равными количествами очищенного родительских ферментов, химерных ферментов и мутантов Cys-Ser, наблюдаемые улучшения высокотемпературного гидролиза не являются результатом повышенной секреции из хозяина экспрессии S. cerevisiae. Следовательно, доказано, что термостойкие химеры и мутанты Cys-Ser могут быть полезными компонентами препаратов ферментов для расщепления целлюлозы.
Хотя проиллюстрированы и описаны различные конкретные формы осуществления, понятно, что можно произвести различные изменения без отклонения от сущности и объема изобретения.