Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ЖИДКОЙ СТАБИЛЬНОЙ СЫВОРОТКИ
Вид РИД
Изобретение
Изобретение относится к биотехнологии, медицине и ветеринарии, а именно к получению жидкой стабильной сыворотки, которая может быть использована для постановки реакции пассивной гемагглютинации (РПГА), а также в реакции агглютинации (РА). Изобретение может быть также использовано для получения набора для выявления специфических антител к различным видам сальмонелл в сыворотке крови человека в реакции пассивной гемагглютинации (РПГА).
Сальмонеллы (лат. Salmonella) - род неспороносных бактерий, имеющих форму палочек. Род назван в честь американского ветеринара Д.Э. Салмона (англ. Daniel Elmer Salmon; 1850-1914). Сальмонеллы являются грамотрицательными подвижными факультативно анаэробными палочками, которые, как правило, не ферментируют лактозу и патогенны для людей и животных при пероральном введении. Одно из опаснейших заболеваний, которое вызывается серотипами бактерий сальмонеллы, это сальмонеллез. Это заболевание характеризуется разными клиническими симптомами, от совершенно бессимптомного проявления, до тяжелых септических форм. Особенно часто заболевание протекает с сильным поражением органов пищеварения. Другим заболеванием, вызываемым сальмонеллой, является брюшной тиф - острая циклически протекающая кишечная антропонозная инфекция, вызываемая бактериями Salmonella typhi (Salmonella enterica серотип typhi), с алиментарным путем передачи. Заболевание характеризуется лихорадкой, явлениями общей интоксикации с развитием тифозного статуса, розеолезными высыпаниями на коже, гепато- и спленомегалией и специфическим поражением лимфатической системы нижнего отдела тонкой кишки.
При заболевании сальмонеллой можно выделить следующие формы, это субклиническая форма, когда диагностируется заболевание по выделениям сальмонеллы из фекалий, и при этом добавляется титр противосальмонеллезных антител в серологических реакциях. Еще одной формой определения наличия сальмонелл является бактерионосительство, когда отсутствуют клинические симптомы, а сальмонелла выявляется при серологических и бактериологических исследованиях.
Существует и реализуется на настоящий момент множество диагностикумов, позволяющих определить в крови специфические антитела к антигенам сальмонелл. Для выявления антител к сальмонеллам используется реакция пассивной гемагглютинации (РПГА) (Каральник Б.В. Эритроцитарные диагностикумы, М.: Медицина, 1976). Агглютинация подразделяется на прямую (активную) и непрямую (пассивную). Феномен прямой (активной) агглютинации реализуется при специфическом взаимодействии узнающих антител с собственными структурными антигенами мембран эритроцитов или бактериальных клеток.
Действующим началом диагностикумов, используемых в реакции РПГА, являются антигены сальмонелл, находящиеся на поверхности эритроцитов. При взаимодействии с сыворотками, содержащими антитела к сальмонеллам, наблюдается феномен агглютинации эритроцитов.
В настоящее время выпускается для РПГА несколько видов эритроцитарных диагностикумов (комплексный, групповой и т.д.). Реакцию ставят с парными сыворотками в соответствии с рекомендациями к указанным диагностическим препаратам. Диагностически достоверным показателем, подтверждающим заболевание, является увеличение титра антител не менее чем в 8 раз.
В патентной литературе также описаны эритроцитарные диагностикумы для выявления антител к антигенам сальмонелл (см., например, RU 2257581, 27.07.2005, 95117746, 10.10.1997 и т.д.).
В настоящее время для постановки реакции РПГА, также как и для постановки реакции агглютинации (РА) сухая лиофильно высушенная сальмонеллезная сыворотка требует разведения, например, раствором хлорида натрия. Однако полученный разведенный раствор имеет маленький срок хранения. В лабораториях обычно используется лишь малая часть сыворотки из вскрытой ампулы. Большую часть приходится утилизировать, поскольку в разведенном состоянии сыворотка быстро теряет свою специфическую активность. Таким образом, на настоящий момент существует задача сохранения функциональной активности антител сывороток, т.е. способности к специфическому взаимодействию с соответствующим антигеном при длительном их нахождении в водных растворах.
Ранее были предприняты попытки по увеличению срока годности сывороток. Так, в автореферате Михайловой В.А. «Разработка технологии получения кроличьей холерной агглютинизирующей О-сыворотки», Иркутск, 1998, был изложен способ стабилизации кроличьей холерной О-сыворотки с целью повышения срока ее годности. При поиске стабилизатора диагностических сывороток были исследованы вещества, известные своим стабилизирующим действием на молекулы иммуноглобулинов, прежде всего многоатомные спирты (сорбит), углеводы (сахароза) и аминокислоты (цистеин, глутамин). В качестве стабилизатора испытаны также тиосульфат натрия и глутатион - исходя из предположения, что эти вещества как антиоксиданты могут предотвратить свободнорадикальное окисление.
В результате сравнительных исследований установлено, что наилучший стабилизирующий эффект оказывает смесь сахарозы (в концентрации от 2.2 до 3.0%) и тиосульфата натрия (от 0.75 до 1.0%). Оба компонента стабилизатора растворяют в 0.9% растворе хлористого натрия и вносят в сыворотку в соотношении, зависящем от специфической активности сыворотки. Сыворотку с титром антител 1:3200 и выше разводят 3:1 стабилизатором, содержащим 9% сахарозы и 3% тиосульфата натрия, с титром антител не ниже 1:1600 - 12:1 раствором, содержащим 30% сахарозы и 10% тиосульфата натрия. Конечное содержание стабилизирующих веществ в сыворотке в обоих случаях было одинаково: 3% - сахарозы и 1% - тиосульфата натрия. В результате стабильность экспериментальной сыворотки была выше, чем у контрольной, в 5 и более раз. Кроме того, сахароза и тиосульфат натрия значительно улучшали растворимость препарата. На специфическую активность и растворимость оказывала влияние остаточная влажность препарата: наиболее стабильными были холерные агглютинирующие О-сыворотки с остаточной влажностью не более 2.0-2.2%.
Авторами же настоящего изобретения было обнаружено, что можно получить жидкую сыворотку с длительным сроком хранения вплоть до 3 лет с сохранением ее функциональной активности. Таким образом, получение такой сыворотки позволяет в любой момент времени иметь уже готовую к использованию сыворотку, сократить расход используемых материалов, исключить из стадии получения трудоемкую и энергозатратную стадию лиофильной сушки, что значительно упрощает и удешевляет процесс получения сыворотки.
Это также приводит к упрощению проведения реакции агглютинации, поскольку жидкие сыворотки не требуют стадии разведения сухой сыворотки раствором для разведения.
Таким образом, технический результат заключается в сохранении функциональной активности антител сыворотки при длительном нахождении в водном растворе, что приводит также и к упрощению способа получения сыворотки, а также к упрощению проведения реакции агглютинации.
Технический результат достигается тем, что в качестве основного разводящего и стабилизирующего раствора исходной жидкой адсорбированной сыворотки использовали растворы, содержащие полиглюкин (ПГ) - международное непатентованное название - декстран (ср. мол. масса 50000-70000)(крупномолекулярный стабилизатор антител) - 60 г; натрия хлорид - 9 г, вода для инъекций - до 1 л; прозрачная бесцветная или слегка желтоватая жидкость, азид натрия в конечной концентрации 0.2% и 0,2% сорбит в конечной концентрации.
Известно, что полиглюкин используют в качестве криопротектра при лиофильном высушивании препаратов, поскольку он оказывает защитное действие на белковые молекулы (см., например, RU 2326655, 20.06.2008, RU 2214836, 27.10.2003, RU 2236866,27.09.2004).
При этом в уровне техники не описана возможность использования полиглюкина для придания сохранения свойств, входящих в состав сывороток антител при нахождении их в водном растворе.
Таким образом, изобретение представляет собой:
1. Набор для выявления специфических антител к различным видам сальмонелл в сыворотке крови, включающий:
- диагностикум эритроцитарный сальмонеллезный, представляющий собой взвесь формалинзированных эритроцитов барана, сенсибилизированных липополисахаридными антигенами из сальмонелл в буферном растворе,
- стабильную жидкую сыворотку диагностическую сальмонеллезную, полученную путем разведения жидкой адсорбированной сыворотки 6% полиглюкином, содержащим 0.2% азида натрия в конечной концентрации и 0,2% сорбит в конечной концентрации,
- взвесь формалинизированных несенсибилизированных эритроцитов барана,
- планшет для иммунологических реакций;
2. Способ получения стабильной жидкой сыворотки диагностической сальмонеллезной, менингококковой, коклюшной или паракоклюшной, включающий разведение соответствующей жидкой адсорбированной сыворотки 6% полиглюкином, содержащим 0.2% азида натрия в конечной концентрации и 0,2% сорбит в конечной концентрации;
3. Сыворотку диагностическую сальмонеллезную, полученную способом, включающим разведение жидкой адсорбированной сыворотки 6% полиглюкином, содержащим 0.2% азида натрия в конечной концентрации и 0,2% сорбит в конечной концентрации;
4. Применение стабильной жидкой сыворотки, полученной способом по п. 2, в реакции агглютинации (РА);
5. Применение стабильной жидкой сыворотки, полученной способом по п. 2, в реакции пассивной гемагглютинации (РПГА).
Изобретение осуществляется следующим способом.
В качестве неограничивающего примера осуществления показано получение сальмонеллезной сыворотки и ее использование в реакциях РА и РПГА. Аналогичным образом были протестированы менингококковые, коклюшные и паракоклюшные сыворотки. Полученные результаты показывают, что во всех случаях для всех указанных сывороток применение в качестве разбавляющего именно раствора полиглюкина с азидом натрия и сорбитом позволяет сохранить стабильность сывороток в жидком виде в течение трех лет.
Были приготовлены разводящие растворы для сыворотки.
В 6%-ный полиглюкин был внесен азид натрия в конечной концентрации 0.2% и сорбит в конечной концентрации 0,2%
Исходную жидкую адсорбированную сальмонеллезную сыворотку разбавляют раствором, полученным внесением в полиглюкин 0.2% азида натрия и 0,2% сорбита.
В качестве дополнительных стабилизаторов были использованы - лс-18 - 0,2%, сорбит 2%, глицин 0,2%, глютатион 0,2%, тиосульфат натрия 0,2 и 0,4% (в дальнейшем от использования тиосульфата натрия отказались в связи с резким снижением активности сывороток), красгемодез 8000 (ГД).
Степень разведения сывороток зависит от того, какая сыворотка используется в качестве исходной и для какой реакции (РА или РПГА). Однако вне зависимости от степени разведения сыворотки использование в качестве стабилизирующего и разводящего раствора полиглюкина с 0.2%-ным азидом натрия или раствора красгемодеза 8000 с 0.2%-ным сорбитом и 0.2%-ным азидом натрия позволяет получить жидкую стабильную в течение трех лет диагностическую сыворотку.
Полученные сыворотки были проверены по показателю специфическая активность в реакции РПГА с использованием сальмонеллезных диагностикумов, производимых ООО «Био-Диагностика» - 1,2,12; 1,4,12; 6,7;6,8;1,9,12;3,10; Ви; комплексный в разведении 1/10 и 1/100 и в реакции РА без разведения с использованием тест штаммов- Salmonella paratyphi А №392, S.typhimurium №415, S.enteritidis (gertneri) №921, S.cholerae suis №92, S. newport, S.anatum №61, S. typhi Vi
Были исследованы сыворотки в различных вариантах, а именно:
|
В процессе хранения все сыворотки проверялись в реакциях РПГА и РА. В РПГА все сыворотки использовались в разведении 1/10. В РА сыворотки использовали без разведения.
Реакция РА.
Когда бактериальная культура смешивается с антисывороткой, специфичной строго к компонентам поверхности клеток бактерий, клетки скрепляются вместе благодаря взаимодействию антиген-антитело и формируют агрегаты (происходит агглютинация). Обычно данную реакцию можно наблюдать невооруженным глазом в виде хлопьев в суспензии. Благодаря смешиванию специфичной антисыворотки с культурой микроорганизмов (например, Salmonella), происходит идентификация определяемых антигенов (например, О и Н). На основе наблюдаемой агглютинации образца серотип определяется по схеме Кауффманна-Уайта.
Реакция протекает следующим образом:
1. Готовят клетки микроорганизмов для постановки реакции. Суспензию обезвреженных клеток микроорганизмов разводят физиологическим раствором (0.9% NaCl, рН=6.5-7.2) до концентрации 20-40 МЕ/мл (используя стандарт мутности МакФарланда). Либо исследуемую культуру берут бактериологической петлей, добавляют в лунку планшета к раствору для разведения и растирают ее до получения однородной суспензии бежево-белого цвета мутностью от 20 до 40 МЕ/мл;
2. Используют сыворотку для реакции, учитывая титр антител (если известен). Исходная сыворотка разводится таким образом, чтобы минимальный титр составлял не менее 1/80. То есть при использовании исходной сыворотки с титром 1/320, развести необходимо будет в 4 раза:
k=t/80, где k - коэффициент разведения, t - титр исходной сыворотки.
Исходную жидкую адсорбированную сальмонеллезную сыворотку разбавляют раствором, полученным внесением в полиглюкин 0.2% азида натрия и 0,2» сорбита;
3. В центр лунки 8-луночного планшета для реакции агглютинации вносится 50 мкл исследуемой культуры и рядом 50 мкл разведенной сыворотки. Капли соединяют, наклоняя планшет. Реакцию определяют визуально в течение 2-6 минут. При развитии реакции агглютинации происходит выпадение агрегатов клеток с антителами, при этом раствор становится более прозрачным.
Учет реакции проводится по четырехкрестной системе:
(4+) - отчетливый агглютинат при полном просветлении жидкости;
(3+) - отчетливый агглютинат на фоне мутноватой жидкости;
(2+) - незначительный агглютинат на фоне мутной жидкости;
(1+) - незначительное количество агглютината на фоне мутной жидкости;
(-) - признаков агглютинации нет. Однородная мутная жидкость.
Положительной считается реакция агглютинации интенсивностью не менее чем на (3+).
Реакция РПГА.
Принцип РПГА заключается в том, что при специфическом взаимодействии антител к различным видам сальмонелл исследуемой сыворотки крови с антигенами, фиксированными на поверхности индикаторных эритроцитов, наблюдается их характерная агглютинация.
Реакция РПГА проводится в соответствии с рекомендациями используемого диагностикума. В состав набора для диагностики входят:
- диагностикум эритроцитарный сальмонеллезный, представляющий собой взвесь формалинзированных эритроцитов барана, сенсибилизированных липополисахаридными антигенами из сальмонелл в буферном растворе,
- стабильная жидкая сыворотка диагностическая сальмонеллезная, полученная путем разведения жидкой адсорбированной сыворотки 6% полиглюкином, содержащим 0.2% азида натрия в конечной концентрации и 0,2% сорбит в конечной концентрации;
- взвесь формалинизированных несенсибилизированных эритроцитов барана,
- планшет для иммунологических реакций.
Учет РПГА проводится по четырехкрестной системе:
(4+) - все эритроциты агглютинированы и равномерно покрывают дно лунки в виде "зонтика";
(3+) - агглютинированы почти все эритроциты, на фоне их имеется малозаметное кольцо из осевших неагглютинированных эритроцитов;
(2+) - наряду с равномерным агглютинатом на дне лунки имеется осадок в виде маленького " колечка " или "пуговки";
(1+) - большинство эритроцитов не агглютинировано и осело в виде маленького "колечка" в центре дна лунки;
(-) - признаков агглютинации нет. Эритроциты осели в виде "пуговки" или "колечка".
Результаты исследований представлены в таблице 1.
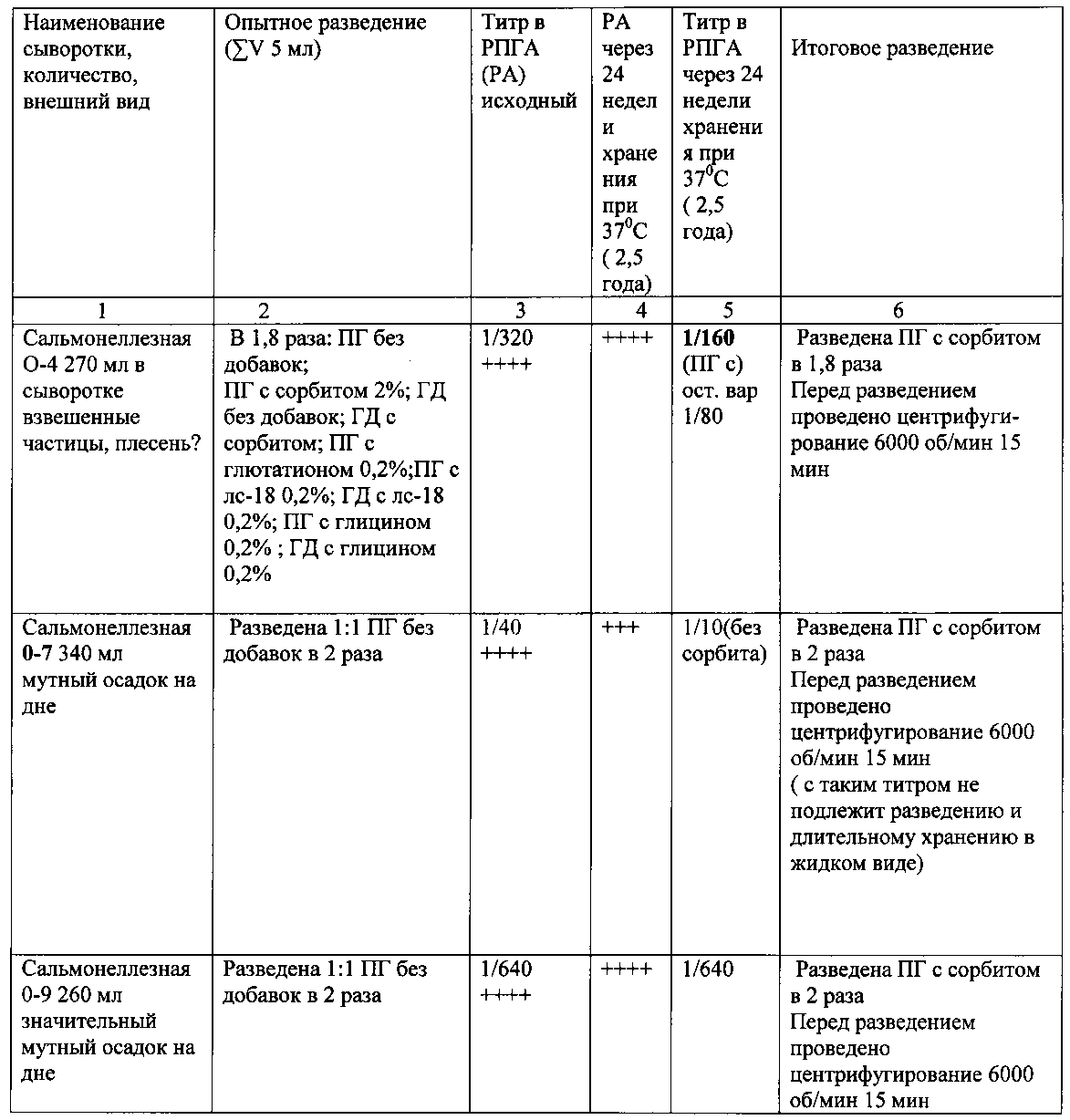
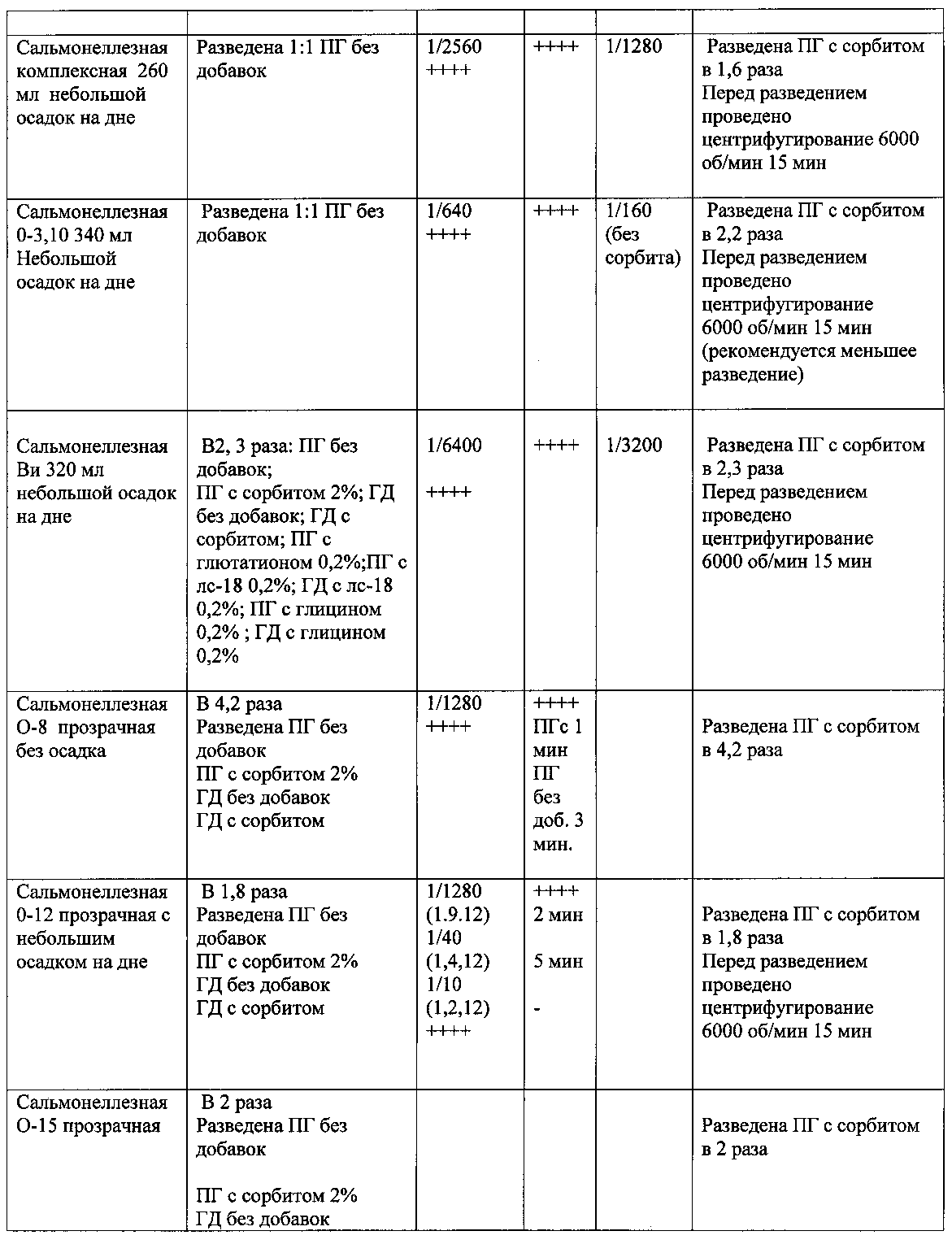

На основании полученных данных можно сделать вывод, что все сальмонеллезные сыворотки рекомендовано разбавлять полиглюкином с натрия азидом 0,2% и с сорбитом 0.2%. Это позволяет сделать сыворотку в жидком виде стабильной в течение длительного времени (до трех лет).
Аналогичным образом были получены и протестированы жидкие диагностические менингокковые, коклюшные и паракоклюшные сыворотки. В результате проведенных опытов было установлено, что менингокковые, коклюшные и паракоклюшные сыворотки для придания им стабильности в жидком виде, также как и сальмонеллезные сыворотки, следует разбавлять полиглюкином с натрия азидом 0,2% и с сорбитом 0.2%. Такие сыворотки также сохраняют свою стабильность в течение трех лет.
Таким образом, в результате осуществления изобретения было подтверждено, что можно получить жидкую сыворотку с длительным сроком хранения вплоть до 3 лет с сохранением ее функциональной активности.

