Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ЗАМЕЩЕННЫХ ХИНОНОВ
Вид РИД
Изобретение
Изобретение относится к области тонкого органического синтеза, а именно к усовершенствованному способу получения замещенных хинонов, в том числе, 2,3,6-триметил-1,4-бензохинона (ТМБХ) и 2-метил-1,4-нафтохинона (МНХ) - ключевых интермедиатов в синтезе витаминов Ε и K, соответственно, широко применяемых в медицинской практике и животноводстве.
Хиноны получают путем окисления доступного сырья - соответствующих алкилароматических соединений (алкилфенолов) экологически чистым и дешевым окислителем - водным пероксидом водорода.
Существуют несколько способов получения алкилзамещенных хинонов из соответствующих алкилфенолов: 1) стехиометрическое окисление неорганическими окислителями (оксидами марганца(IV) и хрома(VI), перманганатом и бихроматом, азотной кислотой и др.); 2) гомогенное каталитическое окисление в присутствии комплексов переходных металлов и 3) гетерогенное каталитическое окисление в присутствии твердофазных катализаторов, содержащих переходные металлы. Поскольку при стехиометрическом окислении используются большие количества дорогих и часто токсичных окислительных агентов, неизбежно возникают проблемы, связанные с утилизацией большого количества токсичных отходов. Поэтому каталитические способы окисления гораздо более приемлемы как с точки зрения экологии, так и с точки зрения экономики.
Наибольший интерес представляют каталитические способы получения хинонов из замещенных фенолов, основанные на использовании экологически безопасных окислителей - молекулярного кислорода и пероксида водорода, которые в качестве единственного побочного продукта дают воду. Хотя стоимость пероксида водорода выше, чем стоимость кислорода, в малотоннажных процессах тонкого органического синтеза использование первого часто оказывается предпочтительным, поскольку стоимость технологического оборудования для окисления пероксидом водорода ниже, чем для окисления кислородом [R.A. Sheldon, J. Dakka. Heterogeneous catalytic oxidations in the manufacture of fine chemicals. Catalysis Today 19 (1994) 215].
При окислении замещенных фенолов кислородом используют два основных типа гомогенных катализаторов: 1) галогениды меди [ЕР 0093540, С07С 50/04, 1983; ЕР 0127888 В1, С07С 46/08, 1987] и 2) фосформолибдованадиевые гетерополикислоты H3+nPMo12-nVnO40 (ΓΠΚ-n, n=2-6) [SU 1719392, С07С 50/04, 1991; PCT/FR 96/01689, С07С 46/08; RU 2022958, С07С 50/12, 1994; WO 2004/014832]. Недостатками каталитических способов, основанных на использовании галогенидов меди, являются высокие (практически стехиометрические) количества катализатора и загрязнение продукта токсичными переходными металлами, а также коррозия аппаратуры. Кроме того, в случае использования хлоридов меди имеет место побочное образование токсичных хлорорганических соединений. В способах, основанных на применении ГПК-n, также используют близкие к стехиометрическим количества катализатора, и продукт загрязняется переходным металлом.
Для окисления замещенных фенолов пероксидом водорода известны системы, основанные на использовании в качестве гомогенного катализатора комплексов кобальта с основаниями Шиффа [DE 2460665 and 2517870, 1975], соединений рутения и железа [Ito S., Aihara K., Matsumoto Μ. Tetr. Lett. Ruthenium-catalyzed oxidation of phenols with hydrogen peroxide. 24 (1983) 5249; Wienhcfer G., Schrcder K., Mcller K., Jungc K., Beller M. Adv. Synth. Catal. 2010, 352, 1615; Moller, K., Wienhcfer, G., Schrcder, K., Join, В., Junge, K., Beller, M. Chem. Eur. J. 2010, 16, 10300], а также гетерополикислот структуры Кеггина (HnXM12O40, X=Si (n=4), Ρ (n=3); Μ=Μο, W) [US 5245059, C07C 50/04, 1993]. В качестве гетерогенных катализаторов могут быть использованы мезопористые титан-силикатные материалы [US 5712402, С07С 50/02, 1998; RU 2164510, 2000; 2196764, 2001]. Недостатками перечисленных выше каталитических систем является, как правило, недостаточно высокий выход целевого продукта и, соответственно, необходимость затрат на очистку от побочных продуктов, а также низкая эффективность использования окислителя (селективность по пероксиду водорода) вследствие побочного процесса его разложения на катализаторе.
Наиболее близким к данному изобретению является способ окисления замещенных фенолов в хиноны пероксидом водорода в присутствии гетерополикислот структуры Кеггина (ΗnΧΜ12O40, X=Si (n=4), Ρ (n=3); Μ=Μο, W) [US 5245059, C07C 50/04, 1993]. Недостатками данного способа являются относительно большое время реакции (3-12 ч), недостаточно высокий выход целевого продукта (максимальный выход ТМБХ - 78% при использовании 60%-ного пероксида водорода и 61% - при использовании 30%-ного Н2О2) и низкая эффективность использования окислителя, а также проведение реакции в инертной атмосфере.
Задачей изобретения является создание экологически безопасного высокоэффективного каталитического способа окисления замещенных фенолов в хиноны с использованием экологически чистого и атомно-эффективного окислителя - пероксида водорода.
Решение задачи должно привести к существенному упрощению и удешевлению технологии существующих процессов получения хинонов, увеличению выхода целевых продуктов и повышению эффективности использования окислителя. Предлагаемый способ исключает образование ядовитых хлорсодержащих побочных продуктов и коррозию аппаратуры.
Технический результат - высокий выход целевого продукта (как на исходный субстрат, так и на окислитель) при использовании небольших количеств катализатора.
Задача достигается тем, что в способе получения замещенных хинонов путем окисления алкилароматических соединений пероксидом водорода в присутствии катализатора в среде органического растворителя в качестве катализатора используют кислые алкиламмониевые соли ванадийсодержащих полиоксовольфраматов (Alkm-nHn)[γ-XV2W10O40], где: в качестве центрального атома полиоксометаллата X может быть Si или Р, предпочтительно, Р; в качестве алкиламмонийного катиона полиоксовольфрамата Alk=(CkH2k+1)4N, k=4-6; число протонов η в катионной части полиоксовольфрамата (Alkm-nHn)[γ-XV2W10O40] варьируется от 0 до 2).
Синтез соединений данного типа описан в [K. Kamata, K. Sugahara, K. Yonehara, R. Ishimoto, N. Mizuno, Chcm. Eur. J. 2011, 17, 7549].
В качестве алкилароматических соединений берут алкилзамещенные фенолы (2,3,6-тиметилфенол, 2,3,5-триметилфенол, 2,6-диметилфенол, 2,6-ди-трет-бутилфенол) и нафтолы (2-метил-1-нафтол).
В качестве окислителя используют водный раствор пероксида водорода с содержанием пероксида не менее 30 мас.%.
Процесс ведут при температуре не ниже 25°С.
В качестве органического растворителя используют ацетонитрил или его смесь со спиртами.
Используют концентрацию субстрата не выше 0,4 М.
Используют мольное отношение пероксид водорода/субстрат не ниже 2/1.
Мольное отношение субстрат/катализатор не ниже 66.
Сущность изобретения иллюстрируется нижеследующими примерами.
Пример 1.
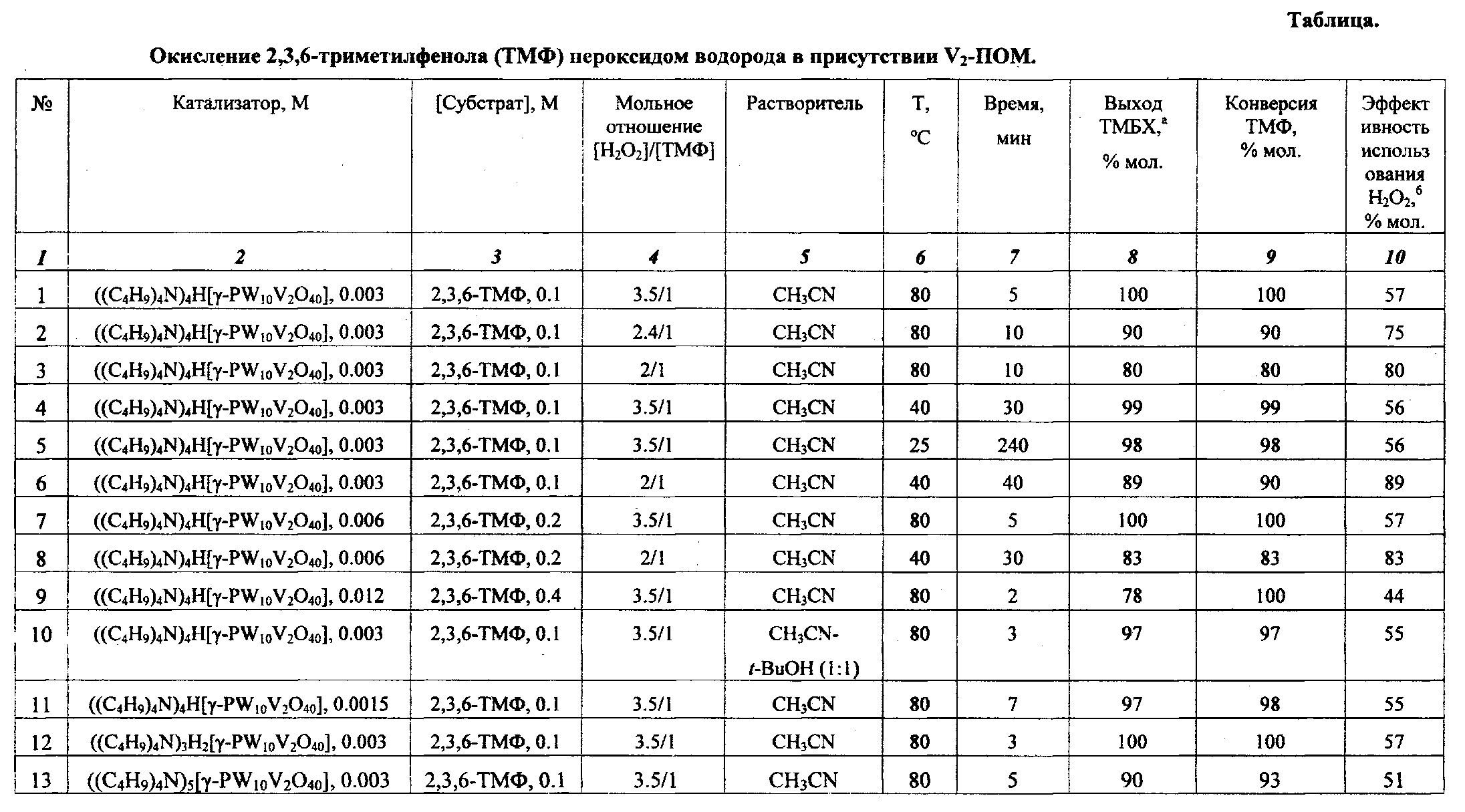
В термостатируемый при 80°С стеклянный реактор, снабженный магнитной мешалкой и конденсором, помещают 14 мг (0,1 ммоль) 2,3,6-триметилфенола (ТМФ), 11 мг (0.003 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] и 1 мл ацетонитрила. Затем при перемешивании добавляют 35 µл (0.35 ммоль) 30%-ной Н2О2 (мольное отношение [H2O2]/[ТМФ]=3.5/1). Смесь перемешивают при 80°С. Через 5 мин конверсия ТМФ и выход 2,3,5-триметил-1,4-бензохинона (ТМБХ) в расчете на исходный ТМФ, определенные методом ГЖХ, составляют 100%. Эффективность использования окислителя (выход в расчете на Н2О2) составляет 57%.
Пример 2.
Процесс проводят, как в примере 1, но вместо мольного отношения [H2O2]/[ТМФ]=3.5/1 используют мольное отношение [H2O2]/[ТМФ]=2.4/1. Через 10 мин конверсия ТМФ - 90%, выход ТМБХ - 90, эффективность использования окислителя - 75%.
Пример 3.
Процесс проводят, как в примере 1, но вместо мольного отношения [H2O2]/[ТМФ]=3.5/1 используют мольное отношение [H2O2]/[ТМФ]=2/1. Через 10 мин конверсия ТМФ - 80%, выход ТМБХ - 80%, эффективность использования окислителя - 80%.
Примеры 2 и 3 демонстрируют, что уменьшение мольного отношение [H2O2]/[ТМФ] при сохранении остальных параметров приводит к уменьшению конверсии субстрата и выхода продукта, увеличению времени реакции, но позволяет увеличить эффективность использования окислителя.
Пример 4.
Процесс проводят, как в примере 1, но при температуре 40°С. Через 30 мин конверсия ТМФ - 99%, выход ТМБХ - 99, эффективность использования окислителя - 56%.
Пример 5.
Процесс проводят, как в примере 1, но при температуре 25°С. Через 240 мин конверсия ТМФ - 98%, выход ТМБХ - 98, эффективность использования окислителя - 56%.
Примеры 4 и 5 демонстрируют, что снижение температуры реакции при мольном отношении [H2O2]/[ТМФ]=3.5/1 приводит к увеличению времени реакции и незначительному снижению конверсии субстрата, выхода продукта и эффективности использования окислителя.
Пример 6.
Процесс проводят, как в примере 3, но при 40°С. Через 40 мин конверсия ТМФ составляет 90%, выход ТМБХ - 89%, эффективность использования H2Ο2 - 89%.
Данный пример показывает, что снижение температуры реакции при мольном отношении [H2O2]/[ТМФ]=2/1 приводит к увеличению времени реакции, но позволяет увеличить конверсию субстрата, выход продукта и эффективность использования окислителя.
Пример 7.
Процесс проводят, как в примере 1, но концентрации всех реагентов увеличивают в 2 раза: вместо 14 мг (1 ммоль) ТМФ, 35 µл (0.35 ммоль) 30%-ной H2O2 и 11 мг (0.003 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] берут 28 мг (0.2 ммоль) ТМФ, 70 μл (0.70 ммоль) 30%-ной Н2О2 и 22 мг (0.006 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] (мольные отношения реагентов не меняются). Через 5 мин конверсия ТМФ - 100%, выход ТМБХ - 100%, эффективность использования окислителя - 57%.
Данный пример показывает, что при 80°С увеличение концентраций реагентов в 2 раза не влияет на параметры процесса.
Пример 8.
Процесс проводят, как в примере 6, но концентрации реагентов увеличивают в 2 раза: вместо 14 мг (1 ммоль) ТМФ, 20 μл (0.20 ммоль) 30%-ной H2Ο2 (мольное отношение [H2O2]/|ТМФ]=2/1) и 11 мг (0.003 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] берут 28 мг (0.2 ммоль) ТМФ, 40 μл (0.40 ммоль) 30%-ной H2O2 и 22 мг (0.006 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40]. Через 30 мин конверсия ТМФ - 83%, выход ТМБХ - 83%, эффективность использования окислителя - 83%.
Данный пример показывает, что увеличение концентраций реагентов при 40°С приводит к некоторому сокращению времени реакции, но при этом уменьшаются конверсия ТМР, выход продукта и эффективность использования окислителя.
Пример 9.
Процесс проводят, как в примере 7, но концентрации реагентов увеличивают еще в 2 раза: вместо 28 мг (0.2 ммоль) ТМФ, 70 μл (0.70 ммоль) 30%-ной Н2О2 и 22 мг (0.006 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] берут 56 мг (0.4 ммоль) ТМФ, 140 μл(1.40 ммоль) 30%-ной Н2О2 и 44 мг (0.012 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] (мольные отношения реагентов не меняются). Через 2 мин конверсия ТМФ - 100%, выход ТМБХ - 78%, эффективность использования окислителя - 44%.
Данный пример демонстрирует, что увеличение концентраций реагентов в 4 раза относительно примера 1 приводит к уменьшению выхода целевого продукта (за счет снижения селективности образования ТМБХ при полной конверсии субстрата).
Пример 10.
Процесс проводят, как в примере 1, но в качестве растворителя вместо ацетонитрила используют смесь ацетонитрил - трет-бутанол в соотношении 1:1. Через 3 мин конверсия ТМФ - 97%, выход ТМБХ - 97%, эффективность использования окислителя - 55%.
Данный пример демонстрирует, что частичная замена ацетонитрила трет-бутанолом приводит к незначительному уменьшению параметров процесса.
Пример 11.
Процесс проводят, как в примере 1, но вместо 11 мг (0.003 ммоль) катализатора ((C4H9)4N)4H[γ-PW10V2O40] его берут в количестве 5.5 мг (0.0015 ммоль). Через 7 мин конверсия ТМФ - 98%, выход ТМБХ - 97%, эффективность использования окислителя - 55%.
Данный пример показывает, что уменьшение количества катализатора в 2 раза (увеличение мольного отношения субстрат/катализатор в 2 раза - с 33 до 66) незначительно влияет на параметры процесса.
Пример 12.
Процесс проводят, как в примере 1, но вместо ((C4H9)4N)4H[γ-PW10V2O40] используют катализатор ((C4H9)4N)4H2[γ-PW10V2O40]. Через 3 мин конверсия ТМФ -100%, выход ТМБХ - 100%, эффективность использования окислителя - 57%.
Данный пример показывает, что замена одного трет-бутиламмонийного катиона на протон в катионной части катализатора ускоряет реакцию и не влияет на другие параметры реакции.
Пример 13.
Процесс проводят, как в примере 1, но вместо катализатора ((C4H9)4N)4H[γ-PW10V2O40] используют катализатор ((C4H9)4N)5[γ-PW10V2O40]. Через 3 мин конверсия ТМФ - 93%, выход ТМБХ - 90%, эффективность использования окислителя - 51%.
Данный пример демонстрирует, что отсутствие в катионной части катализатора протона приводит к ухудшению всех параметров процесса (уменьшению конверсии ТМФ, выхода ТМБХ и эффективности использования окислителя).
Пример 14.
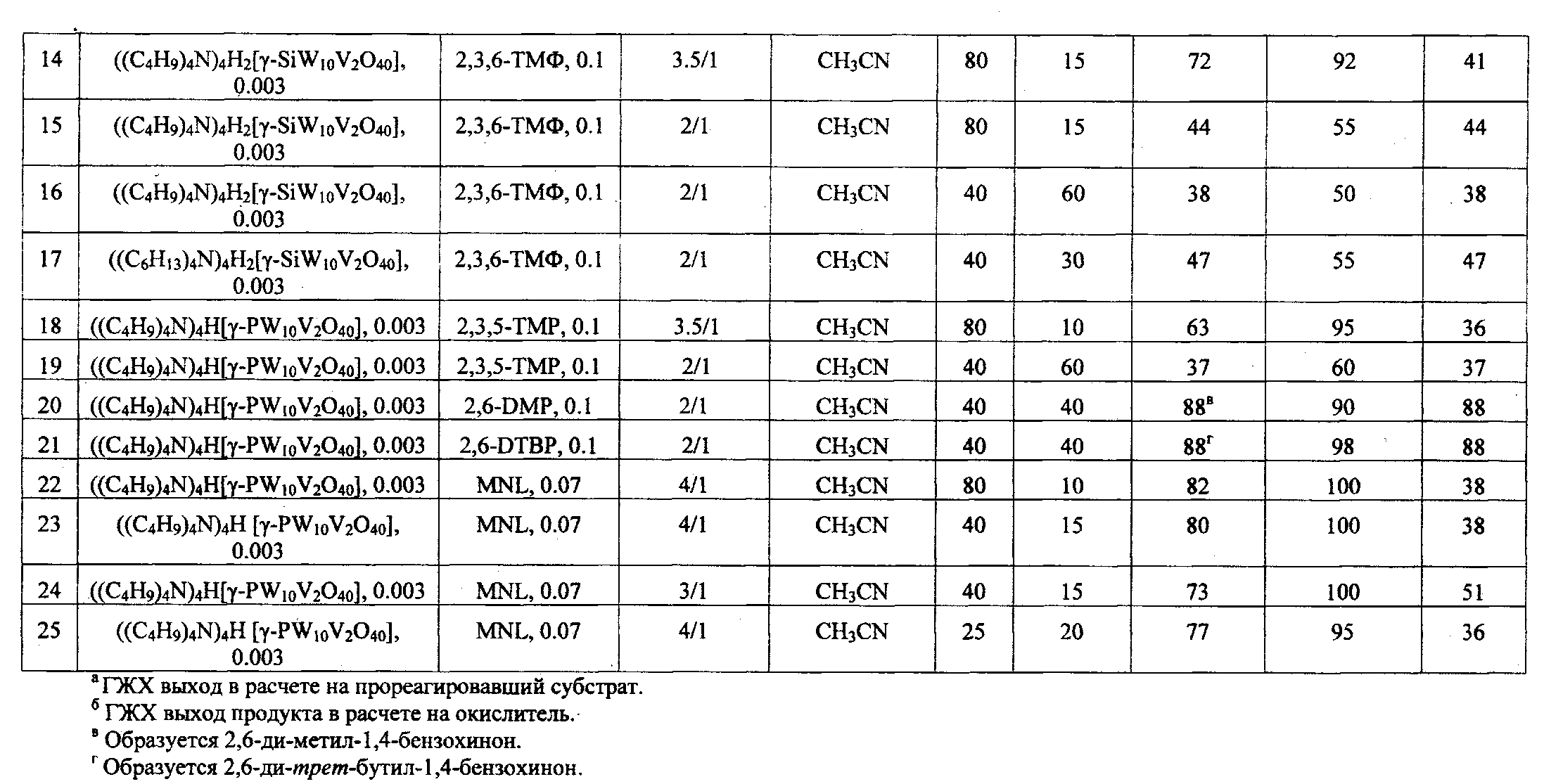
Процесс проводят, как в примере 1, но вместо катализатора ((C4H9)4N)4H[γ-PW10V2O40] с центральным атомом фосфора берут катализатор ((C4H9)4N)4H2[γ-SiW10V2O40] с центральным атомом кремния. Через 15 мин конверсия ТМФ - 92%, выход ТМБХ - 72%, эффективность использования окислителя - 41%.
Пример 15.
Процесс проводят, как в примере 3, но вместо катализатора ((C4H9)4N)4H[γ-PW10V2O40] берут катализатор ((C4H9)4N)4H2[γ-SiW10V2O40]. Через 15 мин конверсия ТМФ - 55%, выход ТМБХ - 44%, эффективность использования окислителя - 44%.
Пример 16.
Процесс проводят, как в примере 6, но вместо катализатора ((C4H9)4N)4H[γ-PW10V2O40] берут катализатор ((C4H9)4N)4H2[γ-SiW10V2O40]. Через 60 мин конверсия ТМФ - 50%, выход ТМБХ - 38%, эффективность использования окислителя - 38%.
Примеры 12-14 демонстрируют, что катализатор, имеющий центральный атом кремния, является менее эффективным по всем параметрам, чем катализатор с центральным атомом фосфора.
Пример 17.
Процесс проводят, как в примере 16, но вместо катализатора ((C4H9)4N)4H2[γ-SiW10V2O40] используют катализатор ((C6H13)4N)5[γ-SiW10V2O40]. Через 30 мин конверсия ТМФ - 55%, выход ТМБХ - 47%, эффективность использования окислителя - 47%.
Этот пример показывает, что замена в катализаторе тетра-бутиламмонийного катиона (C4H9)4N+ на тетра-гексиламмонийный (С6Н13)4N+ позволяет сократить время реакции и увеличить конверсию ТМФ, выход ТМБХ и эффективность использования окислителя.
Пример 18.
Процесс проводят, как в примере 1, но в качестве субстрата вместо 2,3,6-триметилфенола берут 2,3,5-триметилфенол. Через 10 мин конверсия субстрата достигает 95%, выход целевого ТМБХ - 63%, эффективность использования окислителя - 36%.
Пример 19.
Процесс проводят, как в примере 6, но в качестве субстрата вместо 2,3,6-триметилфенола берут 2,3,5-триметилфенол. Через 60 мин конверсия субстрата достигает 60%, выход ТМБХ - 37%, эффективность использования окислителя - 37%.
Примеры 18-19 показывает, что при использовании в качестве окисляемого субстрата 2,3,5-триметилфенола выход ТМБХ и эффективность использования окислителя ниже, чем в случае изомерного 2,3,6-триметилфенола.
Пример 20.
Процесс проводят, как в примере 6, но в качестве субстрата вместо 2,3,6-триметилфенола берут 2,6-диметилфенол (ДМФ). Через 40 мин конверсия ДМФ достигает 90%, выход 2,6-диметил-1,4-бензохинона - 88%, эффективность использования H2O2 - 88%.
Пример 21.
Процесс проводят, как в примере 6, но в качестве субстрата вместо 2,3,6-триметилфенола берут 2,6-ди-трет-бутил-фенол (ДТБФ). Через 40 мин конверсия ДТБФ - 98%, выход 2,6-ди-трет-бутил-хинона - 88%, эффективность использования H2O2 - 88%.
Примеры 20-21 показывают, что предложенный способ может быть использован для получения алкилзамещенных бензохинонов разного строения.
Пример 22.
Процесс проводят, как в примере 1, но в качестве субстрата берут 11 мг (0.07 ммоль) 2-метил-1-нафтола (МНЛ) и добавляют 28 μл (0.28 ммоль) 30%-ной H2O2 (мольное отношение [H2O2]/[МНЛ]=4/1). Через 10 мин конверсия МНЛ - 100%, выход 2-метил-1,4-нафтохинона (МНХ, менадиона, витамина K3) достигает 82% при эффективности использования окислителя - 38%.
Пример 23.
Процесс проводят, как в примере 22, но при 40°С. Через 15 мин конверсия МНЛ - 100%, выход МНХ - 80%, эффективность использования окислителя - 38%.
Пример 24.
Процесс проводят, как в примере 23, но вместо мольного отношения [H2O2]/[МНЛ]=4/1 берут отношение [H2O2]/[МНЛ]=3/1. Через 15 мин конверсия МНЛ - 100%, выход МНХ - 73%, эффективность использования окислителя - 51%.
Пример 25.
Процесс проводят, как в примере 22, но при 25°С. Через 20 мин конверсия МНЛ - 95%, выход МНХ - 77%, эффективность использования окислителя - 36%.
Примеры 22-25 показывают, что предложенный способ может быть использован для получения 2-метил-1,4-нафтохинона (менадиона или витамина K3).
Обобщенные результаты проведения процесса по примерам 1-25 приведены в таблице.
Приведенные примеры показывают, что предлагаемый настоящим изобретением способ получения хинонов является достаточно дешевым, простым в реализации и экологически чистым и позволяет получить целевой продукт с высоким выходом (как на исходный субстрат, так и на окислитель) при использовании небольших количеств катализатора.