Результат интеллектуальной деятельности: 8-АЛКИЛ-2-(ТИОФЕН-2-ИЛ)-8H-ТИОФЕН[2,3-b]ИНДОЛ ЗАМЕЩЕННЫЕ2-ЦИАНОАКРИЛОВЫЕ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИСПОЛЬЗУЕМЫЕ ДЛЯ ЭТОГО НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ
Вид РИД
Изобретение
1. Область техники, к которой относится изобретение
Изобретение относится к области органической химии - синтезу гетероциклических соединений - 8-алкил-2-(тиофен-2-ил)-8H-тиофен[2,3-b]индол замещенных 2-цианоакриловых кислот, представляющих интерес в качестве новых материалов для органической электроники, в частности органических солнечных батарей.
2. Уровень техники
Среди возобновляемых источников энергии особое место занимает Солнце, для трансформации энергии которого активно используют различные подходы, основанные на термодинамических (тепловых), фотоэлектрических и химических методах. Энергия, получаемая таким образом, является экологически чистой и процесс ее получения не сопряжен со значительным загрязнением окружающей среды вредными отходами. Таким образом, солнечная энергетика является одним из крупнейших и наиболее активно развивающихся сегментов рынка альтернативной энергетики.
В настоящее время более 90% мирового рынка солнечной энергетики составляют солнечные элементы на основе моно- или поликристаллических кремниевых пластин. Однако производственные процессы кристаллизации и очистки кремния лимитируют данную технологию, так как она требует значительных энергозатрат.
Альтернативой кремниевым солнечным батареям являются органические полимерные и цветосенсибилизированные солнечные батареи. В 1991 году Рейган и Гретцель в своей работе доказали возможность использования фотоэлектрохимических батарей, в которых используют сенсибилизированные фотоактивным органическим красителем мезопористые неорганические полупроводники с широкой запрещенной зоной, такие как TiO2, ZnO, SnO2 (ячейки Гретцеля) [O′Regan, В.; Grätzel, Μ. Nature, 1991, 353, 737].
Анализ известных в мире технических решений показал, что красители на платформе гетероциклической системы карбазола успешно используют для изготовления стабильных фотоэлектрических преобразователей (солнечных батарей) с высоким КПД [Wu, Y.; Zhu, W. Chem. Soc. Rev., 2013, 42, 2039]. В свою очередь, гетероциклическая система 8H-тиено[2,3-b]индола является изоэлектронной по своей структуре с системой карбазола. Таким образом, использование донорного трициклического фрагмента 8H-тиено[2,3-b]индола в создании новых эффективных красителей-сенсибилизаторов для солнечных батарей является перспективным направлением.
Гетероциклическая система 8H-тиено[2,3-b]индола плохо изучена, в литературе описано малое количество методов синтеза этого гетероцикла.
К известным способам получения относятся:
1) Восстановительная циклизация производных 3-(2′-нитрофенил)тиофена, кислотно-катализируемая рециклизация производных 2-фенилфурана [Smitrovich, J.Η.; Davies, I.V. Org. Lett. 2004, 4, 533; Appukkuttan, P.; Van der Eycken, E.; Dehaen, W. Synlett 2005, 127; Butin, Α.V.; Tsiunchik, F.Α.; Abaev, V.Т.; Zavodnik, V.E. Synlett 2008, 8, 1145]. В частности, производные 8H-тиено[2,3-b]индола получены при длительном кипячении 3-(2′-нитрофенил)тиофенов в избытке триэтилфосфита либо при нагревании производных 2-фенилфурана с хлоридом алюминия в растворе 1,2-дихлорэтана.
2) Формирование конденсированного тиофенового ядра в различных производных индола и индолина [Levy, J.; Royer, D.; Guilhem, J.; Cesario, M.; Pascard, C. Bull. Soc. Chim. France 1987, 193; Olesen, P.H.; Hansen, J.В.; Engelstoft, M.J. Heterocyclic Chem. 1995, 32, 1641; Engqvist, R.; Javaid, Α.; Bergman, J. Eur. J. Org. Chem. 2004; 2589.; Majumdar, К.C; Alam, S.J. Chem. Res. Synop. 2006, 289; Boeini, Η.Z. Helvetica Chimica Acta, 2009, 92, 7, 1268; Singh, P. P.; Yadav, А.К.; Ila, H.; Junjappa, H. European Journal of Organic Chemistry, 2011, 20-21, 4001]. В частности, производные 8H-тиено[2,3-b]индола получены в результате реакции 2-хлоро-1-алкил-1H-индол-3-альдегидов с производными 2-меркаптоуксусной кислоты в растворе метанола в присутствии метилата натрия при длительном нагревании. Ни один из выше перечисленных методов не позволяет получить 8-алкил-2-(тиофен-2-ил)-8H-тиофен[2,3-b]индол замещенные 2-цианоакриловые кислоты, а также используемые в их синтезе промежуточные соединения.
Задача изобретения: найти новые эффективные фото- и электроактивные вещества на основе 8H-тиено[2,3-b]индола для материалов органической электроники, в частности для органических солнечных батарей, и разработать оптимальный способ их получения.
3. Сущность изобретения
Поставленная задача решается новыми 8-алкил-2-(тиофен-2-ил)-8H-тиофен[2,3-b]индол замещенными 2-цианоакриловыми кислотами формулы I, способом их получения, а также новыми промежуточными соединениями для их синтеза общих формул II и III. Предлагаемые соединения и способы их получения в литературе не описаны.
1. Соединения общей формулы I
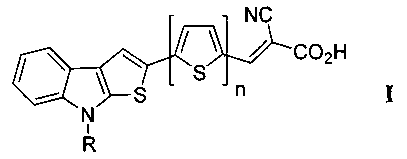
где R=С2Н5 или н-С4Н9; n=1,2,3
2. Способ получения соединений общей формулы I.
Стадия 1.
Синтез промежуточного соединения общей формулы II.
В способе получения производных 2-(тиофен-2-ил)-8H-тиено[2,3-b]индола IIa-г исходные (E)-1-алкил-3-(2-оксо-2-(тиофен-2-ил)этилиден)индолин-2-оны перемешивают с 2,4-бис(4-метоксифенил)-1,3,2,4-дитиадифосфетан-2,4-дисульфидом (реагентом Лавессона) при соотношении реагентов 1:1.1 и кипятят в толуоле в течение 2-8 часов.
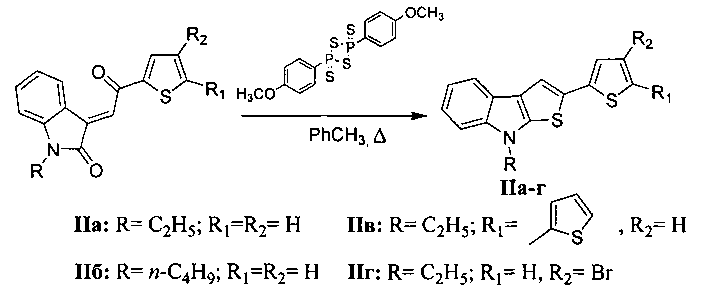
В результате данного процесса последовательно происходят тионирование и последующая циклизация (E)-1-алкил-3-(2-оксо-2-(тиофен-2-ил)этилиден)индолин-2-онов, с одновременным восстановлением этилиденового фрагмента молекулы, в производные 2-(тиофен-2-ил)-8H-тиено[2,3-b]индола II. Исходные (E)-1-алкил-3-(2-оксо-2-(тиофен-2-ил)этилиден)индолин-2-оны синтезированы по известной методике из 1-алкилизатинов [Metwally, S.Α.; Younes, Μ.I.; Abbas, Η.Η. Acta Chimica Hungarica, 1989, 126, 591].
Стадия 2.
а) Синтез промежуточного соединения общей формулы IIIa.
В способе получения промежуточных соединений IIIa производные 2-(тиофен-2-ил)-8H-тиено[2,3-b]индола IIa, б перемешивают со смесью N-метилформанилида и оксохлорида фосфора (POCl3) в мольном соотношении реагентов 1:3:3 в растворе 1,2-дихлорэтана при комнатной температуре и выдерживают в течение 96-120 часов.
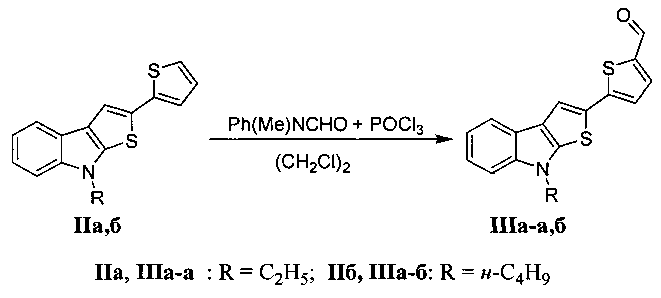
В результате данного процесса происходит формилирование С(2) атома тиофенового фрагмента в соединениях IIa, б и образование альдегидов IIIa.
б) Синтез промежуточного соединения общей формулы IIIб.
В способе получения промежуточных соединений производные 2-(тиофен-2-ил)-8H-тиено[2,3-b]индола IIa, в обрабатывают последовательно н-бутиллитием и хлоридом три(н-бутил)олова в растворе сухого 1,2-диметоксиэтана в атмосфере аргона, и далее образующиеся промежуточные оловоорганические соединения, без выделения их из реакционной массы, обрабатывают 5-бромтиофенкарбоксальдегидом в присутствии каталитических количеств органического комплекса палладия при мольном соотношении реагентов 1:2:2:1.1:0.08 при температуре 0-85°C.
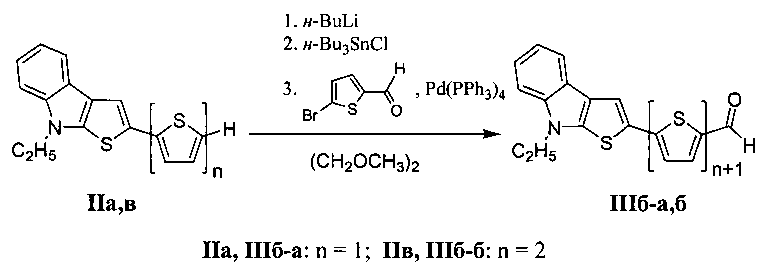
В результате данного процесса происходит литирование С(2) атома терминального тиофенового фрагмента в производных 2-(тиофен-2-ил)-8H-тиено[2,3-b]индолов IIa, в, образование промежуточных оловоорганических производных и их последующая палладий катализируемая реакция кросс-сочетания с 5-бромтиофенкарбоксальдегидом, что приводит к образованию соединений IIIб-а, б.
Стадия 3.
Синтез соединений общей формулы I.
В способе получения целевых соединений I производные 2-(тиофен-2-ил)-8H-тиено[2,3-b]индола IIIa, б перемешивают с 2-цианоуксусной кислотой в присутствии катализатора - пиперидина, при кипячении в растворе ледяной уксусной кислоты в соотношении 1:2:0.05 в течение 5-8 часов.
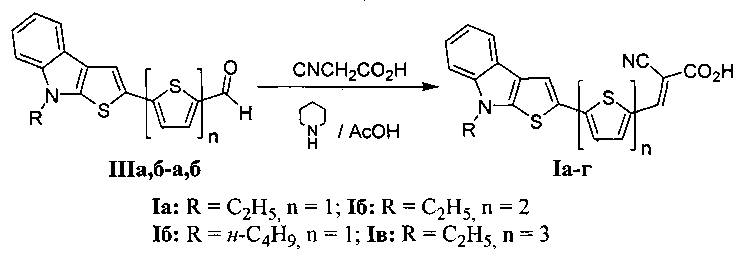
В результате данного процесса происходит конденсация альдегидной группы соединений IIa и IIб с метилен-активным фрагментом 2-циануксусной кислоты и образование искомых красителей общей формулы I.
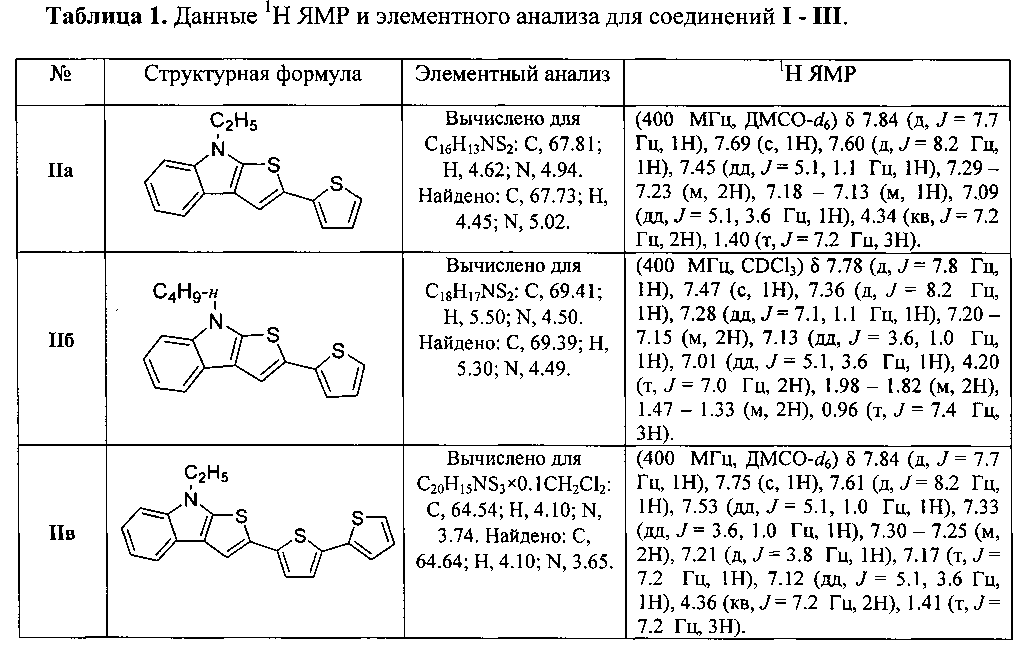
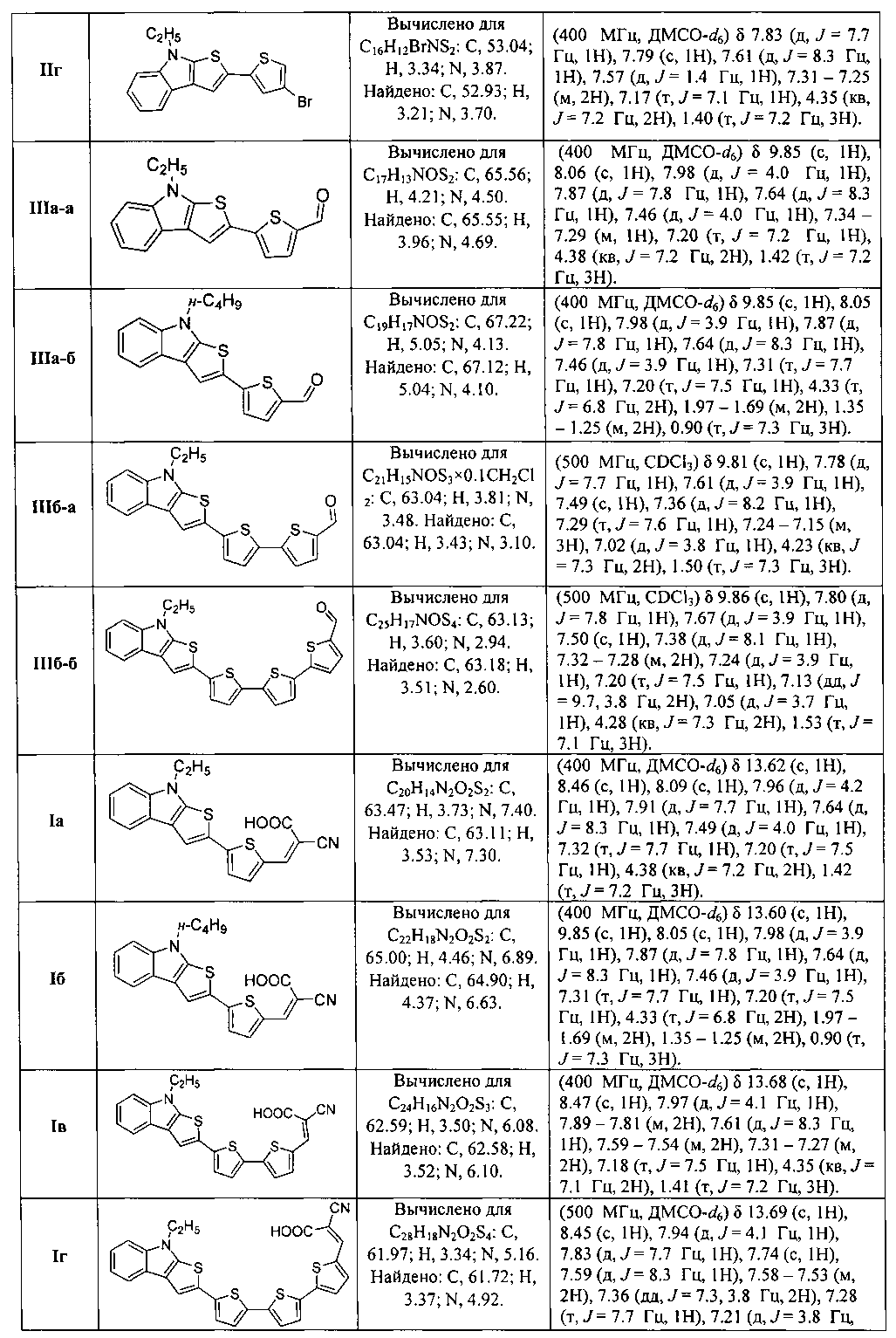
Строение всех новых впервые полученных соединений подтверждено данными ЯМР спектроскопии и элементного анализа.
4. Сведения, подтверждающие сущность изобретения
ПРИМЕР 1. Способ получения 8-этил-2-(тиофен-2-ил)-8H-тиено[2,3-b]индол IIa.
Смесь (E)-1-этил-3-(2-оксо-2-(тиофен-2-ил)этилиден)индолин-2-она (2.83 г, 10 ммоль) и 2,4-бис(4-метоксифенил)-1,3,2,4-дитиадифосфетан-2,4-дисульфида (4.45 г, 11 ммоль) кипятят (110-111°C) в толуоле (25 мл) при перемешивании в течение 2 часов. При этом мольное соотношение реагентов составляет 1:1.1. Растворитель отгоняют при пониженном давлении, остаток после отгонки очищают посредством хроматографии на силикагеле, используя смесь дихлорметана и гексана (2:3 по объему) в качестве элюента. Получают 8-этил-2-(тиофен-2-ил)-8H-тиено[2,3-b]индол IIa с выходом 1.84 г (65%); т.пл.=85-86°C.
Аналогично со способом, описанным в ПРИМЕРЕ 1, получают:
8-Бутил-2-(тиофен-2-ил)-8H-тиено[2,3-b]индол IIб, выход 75%; т.пл.=83-84°C.
2-([2,2′-Битиофен]-5-ил)-8-этил-8H-тиено[2,3-b]индол IIв, выход 57%; т.пл.=133-135°C.
2-(4-Бромтиофен-2-ил)-8-этил-8H-тиено[2,3-b]индол IIг, выход 51%; т.пл.=120-121°C.
Соединения IIa-г представляют собой слабо-желтые порошки, данные 1H ЯМР спектроскопии и элементного анализа для соединений IIa-г приведены в Таблице 1.
ПРИМЕР 2. Способ получения 5-(8-этил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-карбальдегида IIIa-а.
К раствору N-метилформанилида (0.37 мл, 3 ммоль) в безводном 1,2-дихлорэтане (15 мл) добавляют оксохлорид фосфора (0.28 мл, 3 ммоль) и перемешивают 0.5 часа. К полученному раствору добавляют 8-этил-2-(тиофен-2-ил)-8H-тиено[2,3-b]индол IIa (0.28 г, 1 ммоль) и перемешивают при комнатной температуре 96 часов. При этом мольное соотношение соединения IIa, N-метилформанилида и оксохлорид фосфора составляет 1:3:3. Затем реакционную смесь обрабатывают 5% раствором гидрокарбоната натрия (20 мл) и перемешивают в течение 3 часов, после чего отделяют органический слой. Растворитель отгоняют при пониженном давлении, остаток после отгонки очищают посредством хроматографии на силикагеле, используя дихлорметан в качестве элюента. Получают 5-(8-этил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-карбальдегид IIIa-а с выходом 0.25 г (80%); т.пл.=131-132°C.
Аналогично со способом, описанным в ПРИМЕРЕ 2, получают:
5-(8-Бутил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-карбальдегид IIIa-б, выход 73%, т.пл.=105-106°C.
Соединения IIIa-а, б представляют собой желтые порошки, данные 1Ή ЯМР спектроскопии и элементного анализа для соединений IIIa-а, б приведены в Таблице 1.
ПРИМЕР 3. Способ получения 5′-(8-этил-8H-тиено[2,3-b]индол-2-ил)-[2,2′-битиофен]-5-карбальдегида IIIб-а.
К раствору 8-этил-2-(тиофен-2-ил)-8H-тиено[2,3-b]индола IIа (0.56 г, 2 ммоль) в безводном 1,2-диметоксиэтане (15 мл), в атмосфере аргона при 0°C, прикапывают 1,6М раствор н-бутиллития в гексане (2,5 мл, 4 ммоль) и смесь перемешивают 1 час при этой температуре, а затем 0.25 часа при комнатной температуре. После этого реакционную массу охлаждают до 0°C и прикапывают хлорид три(н-бутил)олова (1.08 мл, 4 ммоль), перемешивают 24 часа при комнатной температуре. Затем к реакционной массе добавляют 5-бромтиофенкарбоксальдегид (0.26 мл, 2.2 ммоль) и тетракис(трифенилфосфин)палладий (0.18 г, 0.16 ммоль) и перемешивают при нагревании до температуры кипения 1,2-диметоксиэтана (85°C) в течение 9 часов. При этом мольное соотношение соединения IIa, н-бутиллития, хлорид три(н-бутил)олова, 5-бромтиофенкарбоксальдегид и тетракис(трифенилфосфин)палладий составляет 1:2:2:1.1:0.08. После охлаждения реакционную массу выливают в 10% раствор фторида калия (100 мл) и перемешивают 4 часа, после чего экстрагируют этилацетатом (100 мл). Растворитель отгоняют при пониженном давлении, а остаток после отгонки очищают посредством хроматографии на силикагеле, используя дихлорметан в качестве элюента. Получают 5′-(8-этил-8H-тиено[2,3-b]индол-2-ил)-[2,2′-битиофен]-5-карбальдегид IIIб-а с выходом 0.40 г (51%); т.пл.=144-145°C.
Аналогично со способом, описанным в ПРИМЕРЕ 3, получают:
5″-(8-Этил-8H-тиено[2,3-b]индол-2-ил)-[2,2′:5′,2″-терттиофен]-5-карбальдегид IIIб-б, выход 30%, т.пл.=202-203°C.
Соединения IIIб-а, б представляют собой красные порошки, данные 1H ЯМР спектроскопии и элементного анализа для соединений IIIб-а, б приведены в Таблице 1.
ПРИМЕР 4. Способ получения (E)-2-циан-3-(5-(8-этил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-ил)акриловой кислоты Ia.
К раствору 5-(8-этил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-карбальдегида IIIa-а (1 ммоль) в ледяной уксусной кислоте (15 мл) добавляют 2-циануксусную кислоту (0.17 г, 2 ммоль) и пиперидин (0.0042 г, 0.05 ммоль) и кипятят в течение 8 часов. При этом мольное соотношение альдегида IIIa-а, 2-циануксусной кислоты и пиперидина составляет 1:2:0.05. После охлаждения фильтруют осадок и промывают этанолом (15 мл), получают (E)-2-циан-3-(5-(8-этил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-ил)акриловую кислоту Ia c выходом 0.29 г (77%); т.разл.>300°C.
Аналогично со способом, описанным в ПРИМЕРЕ 4, получают:
(E)-3-(5-(8-бутил-8H-тиено[2,3-b]индол-2-ил)тиофен-2-ил)-2-цианакриловую кислоту Iб, выход 79%, т.разл.>300°C.
(E)-2-циан-3-(5′-(8-этил-8H-тиено[2,3-b]индол-2-ил)-[2,2′-битиофен]-5-ил)акриловую кислоту Iв, выход 87%; т.разл.>300°C.
(E)-2-циан-3-(5″-(8-этил-8H-тиено[2,3-0]индол-2-ил)-[2,2′:5′,2″-терттиофен]-5-ил)акриловую кислоту Iг, выход 69%; т.разл.>300°C.
Соединения Ia-г представляют собой черные порошки, данные 1H ЯМР спектроскопии и элементного анализа для соединений Ia-г приведены в Таблице 1.

Впервые синтезированные 8-алкил-2-(тиофен-2-ил)-8H-тиофен[2,3-b]индол замещенные 2-цианоакриловые кислоты могут быть использованы как перспективные красители для сенсибилизации неорганических полупроводников в составе цветосенсибилизированных солнечных батарей, так как обладают всеми необходимыми структурными характеристиками, предъявляемыми к красителям-сенсибилизаторам. Промежуточные соединения, используемые для синтеза данных целых продуктов, являются 8H-тиофен[2,3-b]индол содержащими синтонами и могут быть использованы при получении различных новых фото- и электрочувствительных производных 8H-тиофен[2,3-b]индола для нужд органической электроники.
![8-АЛКИЛ-2-(ТИОФЕН-2-ИЛ)-8H-ТИОФЕН[2,3-b]ИНДОЛ ЗАМЕЩЕННЫЕ2-ЦИАНОАКРИЛОВЫЕ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИСПОЛЬЗУЕМЫЕ ДЛЯ ЭТОГО НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ](https://fips.edrid.ru/images/rid/54/18/78/6420d2a3d04355dfb70fbdc4bac160de.png)
![8-АЛКИЛ-2-(ТИОФЕН-2-ИЛ)-8H-ТИОФЕН[2,3-b]ИНДОЛ ЗАМЕЩЕННЫЕ2-ЦИАНОАКРИЛОВЫЕ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИСПОЛЬЗУЕМЫЕ ДЛЯ ЭТОГО НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ](https://fips.edrid.ru/images/rid/54/18/78/9809deb21420a145f620fafe128967a2.png)
![8-АЛКИЛ-2-(ТИОФЕН-2-ИЛ)-8H-ТИОФЕН[2,3-b]ИНДОЛ ЗАМЕЩЕННЫЕ2-ЦИАНОАКРИЛОВЫЕ КИСЛОТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ И ИСПОЛЬЗУЕМЫЕ ДЛЯ ЭТОГО НОВЫЕ ПРОМЕЖУТОЧНЫЕ СОЕДИНЕНИЯ](https://fips.edrid.ru/images/rid/54/18/78/d46632054335ee661a3e59520b6c0ba2.png)

