Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ НЕЙТРАЛИЗУЮЩЕЙ АКТИВНОСТИ АНТИТЕЛ К ИММУНОГЛОБУЛИНУ Е
Вид РИД
Изобретение
Изобретение относится к иммунологии, в частности к способам определения нейтрализующей активности антител к иммуноглобулину Е человека, и может использоваться в биотехнологии, фармацевтике и медицине, например, при диагностике и лечении аллергических заболеваний, в частности бронхиальной астмы.
Бронхиальная астма - тяжелое хроническое заболевание дыхательных путей - наиболее распространенная патология среди аллергических и бронхолегочных заболеваний [Аллергические болезни: диагностика и лечение. Под редакцией Р. Паттерсона, Л.К. Греммера, П.А. Гринберга, Москва, Медицина, 2000]. В России, по разным источникам, бронхиальной астмой страдает от 2,2 до 5-7% населения, т.е. от 3 до 9,8 млн человек, значительная часть которых болеет в тяжелой форме, при которой малоэффективно лечение кортикостероидами.
Проявление бронхиальной астмы является аллергической реакцией, опосредуемой иммуноглобулином Е (IgE). Когда антиген, такой как пыльца, домашняя пыль или иной аллерген, попадает в организм, в крови появляются IgE, специфичные к такому антигену, которые связываются с рецепторами, расположенными на поверхности базофилов и тучных клеток. При дальнейшем контакте с антигеном данный антиген связывается с IgE с образованием комплекса антиген-IgE-рецептор, что приводит к немедленной активации рецептора и проведению в клетку сигнала, вызывающего дегрануляцию клеток, в ходе которой химические медиаторы (главным образом гистамин и лейкотриены) освобождаются из клеточных гранул и попадают в кровоток с последующим развитием аллергических симптомов.
Общепринятые подходы к лечению аллергии, в частности бронхиальной астмы, заключаются в системной терапии антагонистами химических медиаторов, такими как антигистамины и стероиды. Применение данных антагонистов направлено на десенсибилизацию пациентов и на уменьшение воспаления, однако оно обеспечивает только симптоматическую терапию, поскольку не направлено на вмешательство во взаимодействие IgE с клеточным рецептором, запускающее аллергическую реакцию. Кроме того, применение стероидов приводит к ингибированию общего иммунного ответа, что выражается в ряде нежелательных побочных эффектов.
В настоящее время разработан способ лечения, основанный на применении полипептидов, блокирующих связывание IgE с Fc-рецепторами на поверхности клеток, а также способных вытеснить IgE из комплекса с рецептором, если IgE с ним уже связан. Наиболее перспективным является применение для данной цели антител к IgE. Молекула IgE состоит из двух легких и двух тяжелых цепей, сшитых вместе дисульфидными связями. Каждая цепь состоит из вариабельной и константной областей, первая из которых отвечает за связывание антигена, а вторая - за взаимодействие с рецепторами. При этом константная область тяжелой цепи IgE состоит из четырех участков, обозначаемых Ch1, Ch2, Ch3, Ch4. Высокоаффинное связывание IgE с рецептором FcεRI происходит в результате сложного взаимодействия участка Ch3 IgE с α-субъединицей рецептора. Для предотвращения такого связывания предложены антитела, в частности омализумаб [RU 2242515], TES-C21 [WO 2004070011], BSW17 [RU 2193413]. На основе гуманизированного антитела Е25 (омализумаб) выпускается препарат «Ксолар», который представляет собой IgG1kappa антитело, содержащее человеческую структурную основу с определяющими комплементарность участками мышиного антитела, связывающими IgE [health.mail.ru/drug/xolair/].
В настоящее время разрабатываются другие гуманизированные и человеческие моноклональные антитела, однако для выбора оптимальной технологии лечения, позволяющей осуществить быструю и надежную нейтрализацию биологической активности иммуноглобулинов Е человека антителами необходимо разработать методы, позволяющие сравнить их эффективность.
В настоящее время для определения биологической активности иммуноглобулинов Е человека предлагаются, как правило, способы, основанные на использовании клеточных линий животных, стабильно экспрессирующих рецептор FcεRI человека или его субъединицу альфа [Hakimi J, Seals С, Kondas JA, Pettine L, Danho W, Kochan J. The alpha subunit of the human IgE receptor (FcERI) is sufficient for high affinity IgE binding. J Biol Chem. 1990; 265(36): 22079-81]. Связывание IgE клетками таких линий с последующим взаимодействием связанного IgE с антителами к IgE, обладающими анафилогенной активностью, приводит к дегрануляции клеток, которая может быть зарегистрирована, в частности, по мобилизации клетками кальция [WO 2008099188]. Недостатком вышеуказанных способов является их громоздкость и длительность.
Также известны способы, основанные на использовании базофилов человека. При этом выделенные базофилы человека либо гепаринизированную кровь инкубируют с IgE, после чего индуцируют дегрануляцию клеток обработкой антителами к IgE, обладающими анафилогенной активностью. Далее клетки осаждают, в супернатанте и в клеточных лизатах, полученных путем многократного замораживания-оттаивания ацетилируют гистамин, количество которого определяют с помощью иммуноферментного анализа (RU 2242515). Нейтрализацию биологической активности иммуноглобулинов Е антителами определяют по концентрации антител, вызывающей 50% ингибирование биологической активности IgE в стандартных условиях эксперимента.
Так, в патенте WO 2008123999 клетки RBL-2H3(FcεRI) инкубируют с IgE человека и исследуемыми антителами в течение 48 часов, после чего отмывают от IGE-анти-IgE комплексов, оставляя на поверхности клеток только IgE, связанные с рецептором FcεRI. Эти IgE связывают поликлональными антителами, вызывая дегрануляцию клеток, уровень которой определяют по выходу гистамина, определяемого с помощью ИФА. Недостатком данного способа является его длительность и трудоемкость
Наиболее близким к заявляемому по технической сущности является способ определения нейтрализующей активности антител с использованием клеток базофильной клеточной линии крыс RBL-2H3, трансфецированных ДНК, экспрессирующей рецептор FcεRI человека(WO 2008099188). После выделения клона, стабильно экспрессирующего FcεRI, клетки культивируют в присутствии антибиотика, поддерживающего экспрессию рецептора. Для определения нейтрализующей активности антител 5×104 клеток высевают в ячейки планшета для культивирования клеток и подращивают при 37°C в среде, содержащей 5% CO2, с добавлением 400 мкг/мл антибиотика G418 в течение 18-24 часов, после чего клетки многократно промывают и к ним добавляют IgE человека вместе с разведениями исследуемых антител. О степени дегрануляции судят по мобилизации клетками кальция, кинетику которой (80 измерений с интервалом 1 сек и 40 измерений с интервалом 8 сек) регистрируют быстродействующим фотометром).
Недостатком данного способа является его длительность и трудоемкость.
Задачей, решаемой авторами, являлось создание более быстрого и простого способа определения нейтрализующей активности антител к IgE.
Техническая задача состояла в исключении из процесса наиболее трудоемких стадий за счет использования поверхностного маркера CD63, который объединяет группу белков, являющихся компонентами лизосомальных мембран и переносимых на клеточную поверхность при активации базофилов и ряда других клеток.
Предлагаемое решение задачи основано на связывании с рецептором FcεRI базофилов свободного (ненейтрализованного) IgE. После отмывки клеток от IgE, исследуемых антител и комплексов антитела-IgE связывание избытка известных антител к IgE (поликлональные антитела козы к IgE человека) с комплексом IgE-FcεRI вызывает дегрануляцию базофилов и позволяет оценить нейтрализующую способность антител.
Технический результат достигается за счет того, что содержащий базофилы препарат - гепаринизированную кровь донора - инкубируют не менее чем с тремя смесями исследуемых антител с IgE человека, содержащих различные соотношения антител при 37±1°C, отмывают центифугированием, затем добавляют поликлональные антитела козы к иммуноглобулину Е человека и вновь инкубируют при 37±1°C в течение 30-40 мин. Реакцию прекращают введением этилендиаминотетраацетата (ЭДТА), добавляют меченные разными флуоресцентными метками антитела к CD63, CD 123 и HLA-DR, выдерживают при комнатной температуре в темноте в течение 30-35 минут, затем лизируют эритроциты, отмывают смесь центрифугированием и анализируют в проточном цитофлуориметре с последующим подсчетом процента активированных клеток с фенотипом CD63high из пула клеток с фенотипом CD123highHLA-DR-. В качестве положительного контроля используют формил-метионин-лейцин-фенилаланин, а в качестве отрицательного контроля - показатель клеток, инкубированных в отсутствие иммуноглобулина Е, а также показатель клеток, инкубированных с иммуноглобулином Е, предварительно связанным с избытком нейтрализующих антител к иммуноглобулину Е, и констатируют в случае обнаружения дозозависимого увеличения доли клеток CD63high в популяции клеток с фенотипом CD123+HLA-DR-, что исследуемые антитела относят к анафилогенным, а при обнаружении дозозависимого снижения доли клеток CD63high в исследуемой популяции считают, что исследуемые антитела относят к нейтрализующим с вычислением концентрации антител по формуле:
% нейтр = 100×(1-(%АБоп-%АБа-IgE)/(%АБК IgE-%АБа-IgE)),
где % нейтр - процент нейтрализации;
%АБоп - процент активированных базофилов в присутствии соответствующей концентрации исследуемых антител;
%ABa-IgE - процент активированных базофилов в образце контроля анти-IgE;
%АБК IgE - процент активированных базофилов в образце контроля IgE без исследуемого препарата.
Анализ осуществляют следующим образом.
Исследуемые антитела предварительно раститровывают и инкубируют в течение 1 часа с раствором IgE человека с постоянным перемешиванием на орбитальном шейкере при комнатной температуре (по 50 мкл каждого разведения антитела и 50 мкл раствора IgE человека с концентрацией 20 мкг/мл), после чего смесь добавляют к 100 мкл донорской гепаринизированной крови человека и инкубируют при 37°C в течение 1 часа. Клетки дважды отмывают низкоскоростным центрифугированием, добавляют поликлональные антитела козы к IgE человека (50 мкг/мл) в объеме 10 мкл и вновь инкубируют в течение 30 минут при 37°C. Реакцию останавливают добавлением 10 мкл раствора ЭДТА (20 мМ) с последующей инкубацией при комнатной температуре в течение 15 минут. Далее к образцам добавляют 20 мкл смеси меченных разными флуоресцентными метками антител к CD63, CD 123 и HLA-DR (коммерческий набор BD FastImmune CD63 FITC/CD123 PE/Anti-HLA-DR PerCP). После инкубации при комнатной температуре в темноте в течение 30 минут производят лизис эритроцитов внесением 2 мл лизирующего раствора (0/75% раствор хлорида аммония) с последующей трехкратной отмывкой центрифугированием. Далее образцы анализируют в проточном цитофлуориметре с последующим подсчетом процента активированных клеток с фенотипом CD63high из пула клеток с фенотипом CD123highHLA-DR-. В качестве положительного контроля используют формил-метионин-лейцин-фенилаланин (fMLP) (Sigma), в качестве отрицательного контроля определяют показатель клеток, инкубированных в отсутствие IgE, а также показатель клеток, инкубированных с IgE, предварительно связанным с избытком нейтрализующих антител к IgE.
Изобретение иллюстрируется следующими диаграммами.
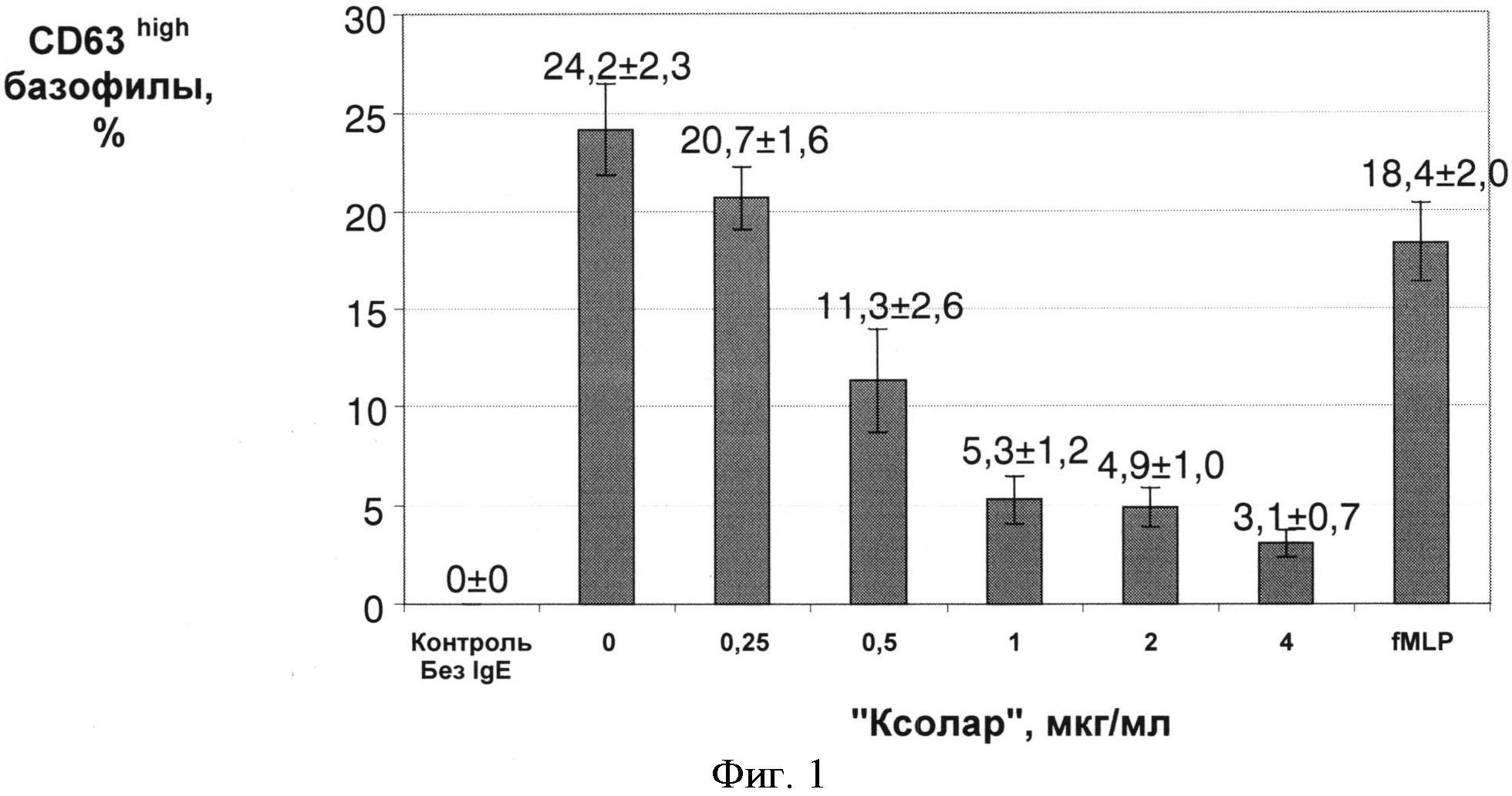
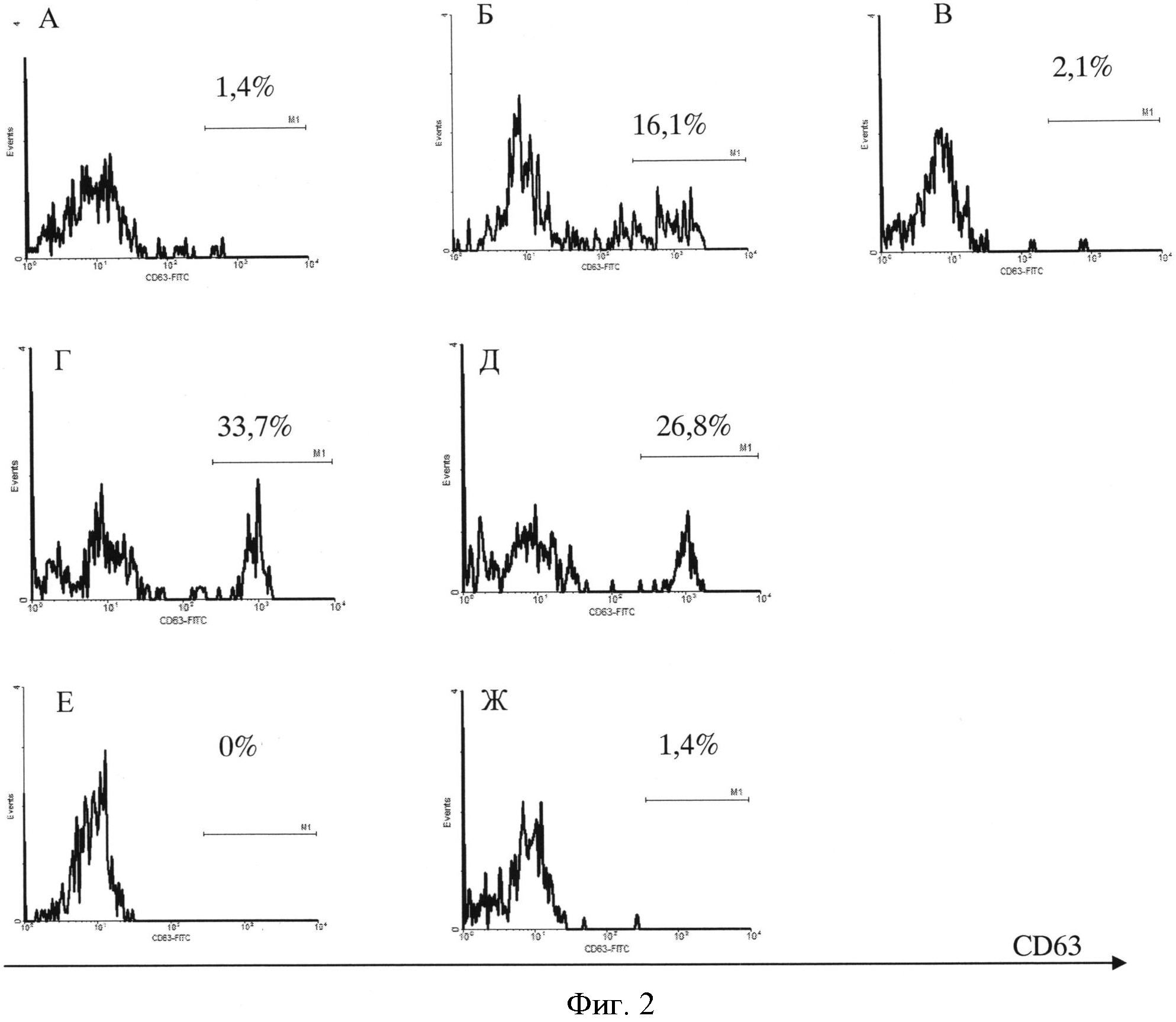
На фиг.1 представлены результаты нейтрализации биологической активности иммуноглобулинов Е известными антителами против IgE человека «Ксолар». На фиг.2 представлена оценка нейтрализующей активности мышиных антител против IgE человека, данные проточной цитофлюориметрии, анализ CD123+HLA-DR- базофилов. Цифры на гистограммах указывают процент клеток, высокоэкспрессирующих CD63. А - контроль поликлональных анти-IgE антител; Б - положительный контроль (fMLP); В - контроль известных нейтрализующих антител («Ксолар», 5 мкг/мл); Г и Д - 5 мкг/мл и 1 мкг/мл антител клона 1С2; Е и Ж - 5 мкг/мл и 1 мкг/мл антител клона 3В5 соответственно.
Промышленная применимость изобретения поясняется следующими примерами.
Пример 1. Определяли нейтрализацию биологической активности иммуноглобулинов Е человека рекомбинантными гуманизированными антителами к IgE человека (коммерческий препарат «Ксолар»).
Выявление активированных базофилов проводили с помощью набора BD FastImmune CD63 по инструкции изготовителя. В качестве положительного контроля использовали формил-метионин-лейцин-фенилаланин (fMLP) (Sigma) в конечной концентрации 2 мкг/мл. Учет результатов проводили с помощью проточного цитофлюориметра EPICS XL (Beckman Coulter) в трехцветном режиме. Базофилы при анализе выделяли как CD123+HLA-DR- клетки и далее определяли процент базофилов, высокоэкспрессирующих CD63 (CD63high).
Результаты анализа приведены на фиг. 1.
Из фиг. 1 видно, что антитела «Ксолар» дозозависимо снижают процент базофилов, активированных в результате инкубации с IgE человека и последующей обработкой поликлональными антителами к IgE. IC50 в эксперименте составил 0,515 мкг/мл.
Пример 2. Определяли нейтрализующую активность мышиных моноклональных антител клонов 1С2 и 3В5 против иммуноглобулинов Е человека.
Мышиные моноклональные антитела (клоны 1С2 и 3В5) против IgE человека были получены с помощью гибридомной технологии. Нейтрализующую активность антител изучали, как описано выше, используя в тесте конечные концентрации антител 5 мкг/мл и 1 мкг/мл. В качестве положительного контроля нейтрализации использовали препарат «Ксолар» в концентрации 5 мкг/мл. Результаты проточной цитофлюориметрии показаны на фиг. 2. Из фиг. 2 видно, что при увеличении концентрации антител 1С2 наблюдается увеличение процента CD63high активированных базофилов, что указывает на то, что данный клон антител является анафилактогенным. При этом в присутствии антител клона 3В5 имеет место полное подавление активации базофилов, что указывает на нейтрализующие свойства антител данного клона.
Сопоставление заявляемого способа с аналогами показало, что при его использовании время анализа сокращается с 20-30 до 4 часов, при этом достигается существенное снижение трудозатрат.
Способ определения нейтрализующей активности антител к иммуноглобулину Е, включающий в себя взаимодействие базофилов с антителами и иммуноглобулином Е человека, отмывание клеток от излишков иммуноглобулина, анализ физико-химических параметров полученной смеси и определение значимого параметра, отличающийся тем, что предварительно готовят не менее трех смесей антител с иммуноглобулином Е человека, которые потом инкубируют с гепаринизированной кровью донора при 37±1°C, а после отмывки излишков иммуноглобулина добавляют поликлональные антитела козы к иммуноглобулину Е человека и вновь инкубируют при 37±1°C в течение 30-40 мин, после чего реакцию прекращают введением этилендиаминотетраацетата, добавляют меченные разными флуоресцентными метками антитела к CD63, CD123 и HLA-DR, выдерживают при комнатной температуре в темноте в течение 30-35 минут, затем лизируют эритроциты, отмывают смесь центрифугированием и анализируют в проточном цитофлуориметре с последующим подсчетом процента активированных клеток с фенотипом CD63 из пула клеток с фенотипом CD123HLA-DR, используя в качестве положительного контроля формил-метионин-лейцин-фенилаланин, а в качестве отрицательного контроля - показатель клеток, инкубированных в отсутствие иммуноглобулина Е, а также показатель клеток, инкубированных с иммуноглобулином Е, предварительно связанным с избытком нейтрализующих антител к иммуноглобулину Е, и в случае, если в опытных образцах при увеличении дозы исследуемых антител не отмечается дозозависимых изменений процента активированных базофилов, соответствующие антитела признаются не нейтрализующими, в случае обнаружения дозозависимого увеличения доли клеток CD63 в популяции клеток с фенотипом CD123HLA-DR исследуемые антитела относят к анафилогенным, а при обнаружении дозозависимого снижения доли клеток CD63 в исследуемой популяции считают, что исследуемые антитела относят к нейтрализующим с вычислением концентрации антител по формуле:% нейтр = 100×(1-(%АБ-%АБ)/(%АБ-%АБ)),где % нейтр - процент нейтрализации; %АБ - процент активированных базофилов в присутствии соответствующей концентрации исследуемых антител; %АБ - процент активированных базофилов в образце контроля анти-IgE; %АБ - процент активированных базофилов в образце контроля IgE без исследуемого препарата.