ПОЛУЧЕНИЕ КАРБОНАТА КАЛЬЦИЯ
Вид РИД
Изобретение
Данное изобретение относится к способу получения карбоната кальция из извести, которая используется для получения раствора с ионами кальция, к которому добавляется диоксид углерода, чтобы осадить карбонат кальция.
Карбонат кальция имеет широкий диапазон областей применения. Например, он широко используется в качестве функционального наполнителя в материалах, таких как краски, бумага, покрытия, пластики, герметики и чернила. Другими областями применения карбоната кальция являются пищевая, косметическая и фармацевтическая отрасли промышленности.
Карбонат кальция является природным минералом, который после измельчения используется в большом числе видов применения. Вместе с тем, морфология, размер частиц и распределение частиц по размерам измельченного продукта, а также его чистота не подходят для определенных видов применения и не являются оптимальными для других видов применения.
Карбонат кальция может также быть получен «химическим путем», при этом диоксид углерода добавляется в раствор с ионами кальция, что приводит к осаждению карбоната кальция. Исходным материалом для такого процесса является обычно известь (CaO) или гидратированная известь (Ca(OH)2). «Классический» процесс использует CaO в качестве исходного материала. Первоначально эта известь гидратируется водой, чтобы получить водную суспензию гидратированной извести («гашеную известь»):
CaO+H2O=Ca(OH)2,
к которой добавляется диоксид углерода, чтобы получить карбонат кальция в соответствии со следующим уравнением:
Ca(OH)2+CO2=CaCO3+H2O.
Имеет место, однако, недостаток, связанный с «классическим» процессом, заключающийся в том, что Ca(OH)2 обладает весьма ограниченной растворимостью в воде, так что процесс в целом является сравнительно медленным.
В развитие вышеуказанного процесса, раствор с ионами кальция получают растворением извести или гидратированной извести в водном растворе, включающим полигидроксисоединение, которое способствует растворению ионов кальция. В результате процесс карбонизации ускоряется. Различные полигидроксисоединения могут быть использованы для этой цели. Например, WO-A-0034182 (Kemgas Ltd) раскрывает применение полигидроксисоединений формулы HOCH2(CHOH)nCH2OH, где n составляет от 1 до 6, при предпочтительном примере, являющемся сорбитолом. Другие полигидроксисоединения, которые могут быть использованы, чтобы способствовать растворению извести или гидратированной извести (чтобы получить раствор с ионами кальция, к которому добавляется диоксид углерода для осаждения диоксида углерода), включают сахарозу.
Получение карбоната кальция с применением процесса, описанного в WO-A-0034182, имеет особое преимущество, заключающееся в том, что известь или гидратированная известь может быть отходами, побочным продуктом от другого химического процесса, так что ее преобразование в карбонат кальция предоставляет возможность получения полезного материала, тогда как в противном случае она была бы направлена в отходы. Соответственно, например, известковые отходы могут быть карбидной известью, которая является побочным продуктом при получении ацетилена посредством реакционного взаимодействия карбида кальция и воды в соответствии с уравнением
CaC2+2H2O→Ca(OH)2+C2H2.
Карбидная известь также известна как карбидный шлам, шлам от генератора, известковый шлам, гашеная известь и гидратированная карбидная известь. Она представляет собой черно-серое вещество, обычно состоящее из примерно 90 масс.% гидроксида кальция (в расчете на сухой остаток карбидной извести), остальное - примеси, которые зависят от способа, применявшегося для получения ацетилена и также от исходных материалов, использованных для производства карбида кальция (обычно получаемого обжигом оксида кальция и угля). Основными примесями являются оксиды кремния, железа, алюминия, магния и марганца, вступившие в соединение с углеродом, ферросилиций и сульфат кальция. Кроме того, если карбидная известь хранится вне помещения, то в качестве примеси может присутствовать карбонат кальция, образованный реакционным взаимодействием гидроксида кальция с диоксидом углерода. Преобразование карбидной извести в карбонат кальция описано в WO-A-0034182 (Kemgas Ltd).
Диоксид углерода, требующийся для осаждения карбоната кальция из раствора с ионами кальция, может также быть отходами, выпуск которых должен контролироваться из экологических соображений (он является хорошо известным «парниковым газом»), так что он может быть эффективно уловлен посредством преобразования в карбонат кальция.
Получение карбоната кальция из известковых отходов или гидратированной извести и диоксида углерода поэтому представляет собой процесс, привлекательный с точки зрения охраны окружающей среды.
Имеют место несколько недостатков, связанных с получением карбоната кальция карбонизацией раствора с ионами кальция, полученного из извести или ее гидроксида с применением «классического» процесса. Они описаны ниже при конкретных ссылках на известь, хотя будет очевидно, что такие же недостатки имеют место при использовании гидратированной извести в качестве исходного материала.
Во-первых, карбонат кальция, полученный из извести, может включать неприемлемо высокие уровни содержания примесей, производных от последней. Имеются по меньшей мере два источника таких примесей в извести. Один источник является «природным» и обусловлен тем, что известь сама будет (обычно) произведена из минерального исходного карбоната кальция (например, известняка, доломита и т.п.) и такие минералы будут включать примеси, которые остаются в извести. Другой (возможный) источник примесей в извести относится особенно к случаю гидратированной извести и возникает из химической реакции, посредством которой была произведена гидратированная известь (например, карбидная известь может включать примеси из углерода, использованного при получении карбида кальция). Независимо от источника примеры примесей, присутствующих в карбонате кальция, являющемся продуктом, полученным карбонизацией раствора с ионами кальция, производного от извести или гидратированной извести, могут включать алюминий, мышьяк, свинец, железо, ртуть, хром, никель, медь и/или цинк. Некоторые из этих примесей делают карбонат кальция непригодным для определенных видов применения (например, для пищевой и фармацевтической отраслей промышленности) вследствие их токсичности. Другие примеси (например, железо), которые не обязательно являются токсичными, могут оказывать влияние на свойства, такие как «белизна» карбоната кальция, так что он может не подходить, например, для применения в качестве покрытия в высококачественных бумагах.
Во-вторых, карбонат кальция, полученный посредством классического процесса, включающего добавление диоксида углерода к суспензии гашеной извести, может иметь нерегулярные размеры и формы частиц, и частицы могут образовывать агломераты, а не поддерживаться в виде дискретных частиц. Нерегулярные размеры частиц вызывают проблемы в таких видах применения, как полимеры, герметики, художественные краски, промышленные покрытия, чернила и меловое покрытие бумаги.
В-третьих, для определенных видов применения обычный процесс, вследствие нерегулярных размеров частиц, требует последующего измельчения продукта. Измельчение является энергоемким и всегда создает определенное количество тонких частиц, которые могут быть вредными и являются трудноудаляемыми.
Поэтому целью данного изобретения является устранение или смягчение вышеуказанных недостатков.
В соответствии с данным изобретением предоставляется способ получения карбоната кальция из извести, включающий следующие стадии:
(i) получение водного раствора, содержащего от 10 масс.% до 35 масс.% растворенного полигидроксисоединения и от 1 масс.% до 5 масс.% растворенного гидроксида кальция (в пересчете на Ca(OH)2) и имеющего pH по меньшей мере 11,5;
(ii) обработка раствора, полученного на стадии (i), для удаления твердотельных веществ, включая суспендированные твердотельные частицы;
(iii) диспергирование диоксида углерода внутри раствора, таким образом, для образования карбоната кальция с последовательным уменьшением pH реакционной смеси;
(iv) в течение периода времени, начиная от внезапного, кратковременного увеличения pH и заканчивая последующим снижением pH, однако перед тем, как pH достигнет 9,5, завершение диспергирования диоксида углерода и добавление щелочного реагента для поддержания pH результирующей смеси по меньшей мере при 9,5; и
(v) извлечение осажденного карбоната кальция.
Авторами было установлено, что реакция карбонизации с включением диспергирования диоксида углерода внутри водного раствора извести, растворенной с помощью полигидроксисоединения, протекает в несколько этапов.
На первом этапе («этапе 1») вязкость остается стабильной, диоксид углерода может быть абсорбирован при сравнительно высоком расходе, и имеет место постепенное снижение pH. По прохождении определенного времени, в зависимости от условий реакции, имеет место переход от первого этапа ко второму этапу («этапу 2»), на котором максимальный расход, при котором диоксид углерода может быть абсорбирован реакционной смесью, меньше, чем на этапе 1 процесса. Переход от этапа 1 к этапу 2 может быть распознан посредством увеличения количества диоксида углерода, выходящего из реактора, в котором выполняется реакция карбонизации (при условии, что диоксид углерода подается в реактор при таком же расходе, что и на этапе 1). В зависимости от условий реакции может иметь место то, что вязкость увеличивается при переходе от этапа 1 к этапу 2, и может наблюдаться студенистый осадок на протяжении последнего. Величина pH продолжает постепенно уменьшаться на протяжении этапа 2, хотя обычно она будет оставаться выше 10.
Неожиданно было обнаружено внезапное, кратковременное увеличение pH с последующим уменьшением, которое, если остается нерегулируемым, приводит к тому, что pH результирующей смеси продолжает уменьшаться. Авторы идентифицировали начало этого кратковременного резкого увеличения pH как начало третьего этапа («этапа 3») реакции. Во время этапа 3 частицы карбоната кальция осаждаются, и обычно имеет место увеличение мутности, вызываемой осаждаемыми частицами карбоната кальция. Увеличение мутности заметно посредством видимого осветления реакционной смеси при разрушении любого геля.
На основании исследований реакции (как подробно указано выше) авторы установили, что карбонат кальция высокой чистоты и с небольшим, одинаковым размером частиц может быть получен с помощью регулирования реакции на этапе 3 посредством:
(a) завершения диспергирования диоксида углерода в реакционной смеси после начала этапа 3 (подтверждаемое внезапным, кратковременным увеличением pH), однако перед тем, как pH уменьшается ниже 9,5; и
(b) обеспечение того, что pH результирующей смеси поддерживается при величине по меньшей мере 9,5, посредством добавления щелочного реагента.
Посредством адаптации этих двух признаков регулирования авторы установили, что образуется карбонат кальция с небольшим, одинаковым размером частиц и высокой чистоты.
В предпочтительном варианте осуществления способа по данному изобретению расход, при котором диоксид углерода диспергируется в реакционной смеси во время этапа 1 способа, является максимальным расходом, при котором диоксид углерода может быть абсорбирован таким образом, что диоксид углерода почти не выделяется из реакционной смеси. Это минимизирует время, необходимое для завершения этапа 1, что повышает производительность процесса.
Сходным образом этап 2 также предпочтительно выполняется при использовании расхода диспергированного диоксида углерода, являющегося максимальным расходом, который может быть абсорбирован реакционной смесью. Однако обычно данный расход (для этапа 2) меньше, чем для этапа 1.
Предпочтительно добавление диоксида углерода прекращается после начала внезапного, кратковременного увеличения pH и перед добавлением щелочного реагента. Это обеспечивает то, что диоксид углерода не вносит вклад в уменьшение pH после добавления щелочного реагента.
Карбонат кальция, полученный способом по данному изобретению, имеет очень узкое распределение частиц по размерам. Это может быть выражено посредством соотношения d90/d10, где d90 представляет собой размер, величину меньше которого имеют 90% частиц, и d10 представляет собой размер, величину меньше которого имеют 10% частиц. Это соотношение типично составляет менее 4,0. Обычно способ по данному изобретению предоставляет возможность получения карбоната кальция со средними размерами частиц от 0,3 до 3,0 микрон. В типичном примере частицы, полученные в соответствии со способом по данному изобретению, имеют размер примерно 0,9 микрона при распределении частиц по размерам, соответствующим d90 примерно 1,3 микрона и d10 примерно 0,5 микрона, так что соотношение d90/d10 составляет 2,6. Размеры частиц измерялись с помощью анализатора размера частиц по дифракции лазерного излучения Beckman Coulter.
Как видно при большом увеличении, частицы карбоната кальция, полученные в соответствии с данным изобретением, имели внешний вид «рисовых зерен», поскольку они были вытянутыми с закругленными концами. Соотношение размеров (длина, деленная на диаметр) находится в интервале между 1,5 и 5,0 и типично составляет 3,0.
Карбонат кальция, полученный в соответствии с предпочтительными вариантами осуществления данного изобретения, может иметь такие уровни содержания примесей, которые указаны в следующей таблице:
|
|
Карбонат кальция, полученный в соответствии с изобретением, имеет ряд преимуществ. Например, он обладает высокими величинами яркости, рассеяния света и глянца поверхности, а также низкой абразивностью, что делает его особенно подходящим для применения для мелования бумаги и в индустрии полимеров, в частности, с точки зрения очень регулярной морфологии кристаллов в виде «рисовых зерен», которая приводит к превосходным реологическим свойствам. В дополнение к этому, чистота продукта и отсутствие в нем крупных частиц обеспечивают очень низкую абразивность. Карбонат кальция, полученный в соответствии с изобретением, также имеет широкую применимость помимо применения для мелования бумаги и в индустрии полимеров. Например, низкий уровень содержания в нем примесей (в частности, низкий уровень содержания свинца) делает его подходящим для пищевой, косметической и фармацевтической отраслей промышленности.
Яркость карбоната кальция дает хорошее представление о его чистоте. Карбонат кальция, полученный в соответствии с изобретением, будет обычно иметь яркость R 457, равную или превосходящую 96,0.
Источники извести или гидратированной извести, которые могут быть использованы для получения карбоната кальция в соответствии со способом по данному изобретению, включают, например, негашеную известь, полученную обжигом известняка, карбидной извести и других известковых отходов или гидратированных известей. Дополнительные источники оксида или гидроксида кальция могут включать золу от бумажного шлама, продукт от прокаливания ила бумажных отходов, в частности, потока ила от очистки пульпы, полученной при изготовлении бумаги из бумажных отходов. Прокаливание ила бумажных отходов приводит к образованию оксида кальция. Компонент оксида кальция предоставляет источник ионов кальция, вводимых в раствор, содержащий полигидроксид.
Стадия (i) способа по данному изобретению включает получение раствора с ионами кальция (производного от исходной извести или гидратированной извести) в полигидроксисоединении, которое промотирует растворение кальция. Конечный полученный раствор содержит от 10 масс.% до 35 масс.% растворенного полигидроксисоединения и от 1 масс.% до 5 масс.% растворенной гидратированной извести (в пересчете на Ca (OH)2). Раствор имеет pH по меньшей мере 11,5, однако обычно по меньшей мере 12. Если исходным материалом является известь (CaO), то обычно предпочтительно первоначально получить суспензию гидратированной извести («гашеную известь») и смешивать эту суспензию с раствором полигидроксисоединения таким образом, чтобы получить конечный раствор, содержащий от 10 масс.% до 35 масс.% растворенного полигидроксисоединения и от 1 масс.% до 5 масс.% растворенной гидратированной извести (в пересчете на Ca(OH)2). Если исходным материалом является гидратированная известь, то она может быть смешана непосредственно с раствором полигидроксисоединения.
Как правило, чем больше количество растворенного полигидроксисоединения, тем больше количество ионов кальция, которое может быть введено в раствор. Соответственно, например, если раствор содержит примерно 12% полигидроксисоединения, то количество гидроксида кальция (в пересчете на Ca(OH)2), которое может быть растворено в нем, будет составлять максимум примерно 2%. В качестве другого примера, раствор, содержащий примерно 25 масс.% полигидроксисоединения, может содержать максимум примерно 4% растворенного гидроксида кальция.
Хотя способ по данному изобретению является эффективным при использовании растворенного полигидроксисоединения в количестве от 10 масс.% до 35 масс.% и растворенного гидроксида кальция от 1 масс.% до 5 масс.%, авторами найдено, что предпочтительное количество полигидроксисоединения находится в интервале от 20% до 30%, и количество растворенного гидроксида кальция составляет от 2 до 4,5%. Более предпочтительно, как было найдено авторами, количество полигидроксисоединения находится в интервале от 23% до 27%, и количество растворенного гидроксида кальция находится в интервале от 3 до 4,0%. Особенно хорошие результаты получаются при использовании примерно 25 масс.% растворенного полигидроксисоединения и примерно от 3,4 масс.% до 3,9 масс.% растворенного гидроксида кальция.
Примеры полигидроксисоединений, которые могут быть использованы для способа по данному изобретению, раскрыты в WO-A-0034182 (Kemgas Ltd) и включают соединения формулы:
HOCH2(CHOH)nCH2OH,
где n составляет от 1 до 6. Соответственно, например, полигидроксисоединение может быть глицерином (n=1). Однако более предпочтительно, если n составляет от 2 до 6 и особенно предпочтительно, если полигидроксисоединение является сахарным спиртом («гидрированным моносахаридом»). Примеры сахарных спиртов включают сорбитол, маннитол, ксилитол, треитол и эритритол.
Также применимыми в качестве полигидроксисоединений, которые могут быть использованы в данном изобретении, являются те, что имеют неразветвленную цепь из n атомов углерода, где n составляет от 4 до 8 и (n-1) атомов углерода имеют связанную с ними гидроксильную группу. Другой атом углерода (т.е. атом углерода без гидроксильной группы) может иметь связанный с ним остаток сахарида. Такими соединениями являются гидрированные дисахаридные спирты, и их примеры включают мальтитол и лактитол.
Особенно предпочтительными для применения в данном изобретении являются гидрированный моносахарид (например, сорбитол) и дисахаридные спирты, по причине их термической стабильности, которая может быть важна для последующей обработки раствора с ионами кальция (см. ниже).
Могут быть использованы смеси указанных выше многоатомных спиртов. Соответственно, возможно применение промышленного сорбитола, который в состоянии в виде сухого вещества содержит примерно 80% сорбитола вместе с другими полигидроксисоединениями, такими как маннитол и дисахаридные спирты. Примеры промышленного сорбитола включают Sorbidex NC 16205 от Cerestar и Meritol 160 от Syral.
В дополнение к этому, однако, полигидроксисоединением может быть сахарид (например, моно- или дисахарид).
Раствор, приготовленный для стадии (i) процесса, затем обрабатывается на стадии (ii), чтобы удалить нерастворимый материал, включающий суспендированные твердотельные частицы, которые будут содержать металлические примеси, которая является стадией, обеспечивающей чистоту карбоната кальция, являющегося продуктом, полученным способом по данному изобретению. Особенно предпочтительно, чтобы суспендированные твердотельные частицы удалялись посредством стадии флокуляции. Используемый флокулирующий агент может быть, например, катионным полимером (таким как Nalco 9908), который добавляется к раствору при перемешивании. Хлопья и твердотельные частицы могут быть отделены от раствора обычными методами. Соответственно, например, раствор может быть направлен в «отстойник», который предоставляет возможность накапливания хлопьев в нижней части и удаления их из нее. Раствор может затем быть профильтрован через песчаную колонну или любой другой подходящий узел, чтобы удалить остающийся твердотельный материал.
Раствор, полученный от стадии (ii), затем подвергается реакции карбонизации (стадии iii), на которой диоксид углерода, либо чистый, либо разбавленный (если, например, используются дымовые газы), барботируется через раствор.
Предпочтительно данная реакция выполняется в реакторе периодического действия с мешалкой для распределения газа с приложением высоких сдвиговых напряжений. Однако также возможно выполнение реакции непрерывным образом либо в последовательности реакторов с мешалками с приложением высоких сдвиговых напряжений, либо в проточной линии, с добавлением газа посредством эжекторов на одной или нескольких стадиях. Количество добавляемого диоксида углерода должно быть по меньшей мере стехиометрическим количеством, требующимся для преобразования всех ионов кальция в растворе в карбонат кальция.
Раствор, подлежащий карбонизации, будет обычно находиться при контролируемой температуре в начале реакции карбонизации. Начальная температура будет предпочтительно находиться в интервале от 10 до 40°C и в идеальном случае в интервале от 25 до 32°C.
В течение типичной реакции величина pH (которая составляет первоначально по меньшей мере 11,5, чаще по меньшей мере 12) постепенно уменьшается. В определенный момент протекания реакции имеет место заметное увеличение вязкости раствора. Авторы называют это этапом 2. В зависимости от конкретных концентраций полигидроксисоединения и гидроксида кальция в исходном растворе это увеличение вязкости может быть вызвано образованием геля. Исследования авторов установили, что постепенное уменьшение pH реакционной смеси обычно резко прерывается при величине примерно 10,2-10,8 в виде внезапного резкого увеличения обычно на 0,5-1 единиц pH перед тем, как продолжает снова уменьшаться.
Начало кратковременного резкого увеличения pH указывает на окончание этапа 2, и в течение данного периода увеличения происходит быстрое осаждение частиц карбоната кальция. Как указано выше, количество диоксида углерода, добавляемого во время реакции, должно быть по меньшей мере стехиометрическим количеством, требующимся для преобразования всех ионов кальция в растворе в карбонат кальция. При условиях, описанных в данном документе, чтобы получить частицы размером 0,8 микрона, количество диоксида углерода, инжектированного во время этапа 1, находится между 70 и 85% от общего количества, при остатке, инжектируемом на этапе 2. Расходы обычно являются такими высокими, насколько это позволяют условия процесса. Расходы на этапе 1 обычно гораздо выше, чем на этапе 2. Типично реакция занимает от 15 до 30 минут.
Важной особенностью данного изобретения является то, что, как только величина pH результирующей смеси начинает уменьшаться после ее кратковременного резкого увеличения, не допускается ее уменьшение ниже 9,5, предпочтительно ниже чем 10, и в идеальном случае она поддерживается по меньшей мере при 10,5.
Авторы установили, что этот жесткий контроль pH результирующей смеси (а не просто предоставление возможности уменьшения pH до более низких величин) важен для обеспечения получения карбоната кальция с небольшим одинаковым размером частиц и чистоты конечного карбоната кальция, являющегося продуктом. Более конкретно, авторы нашли, что некоторые металлические примеси, присутствующие в извести, переходят в раствор на стадии (i) способа (например, посредством хелатообразования с полигидроксисоединением) и поэтому не удаляются на стадии (ii) отделения твердотельных частиц. Посредством обеспечения того, что pH результирующей смеси не уменьшается ниже 9,5, большинство этих металлических примесей остаются в растворе и поэтому не загрязняют конечный осажденный карбонат кальция.
Задержка уменьшения pH может быть достигнута посредством добавления к результирующей смеси щелочного реагента. Наиболее предпочтительно щелочной реагент добавляется к результирующей смеси так быстро, насколько это практически возможно, как только величина pH начинает уменьшаться после ее кратковременного увеличения и независимо от времени, чтобы обеспечить то, что pH не уменьшается ниже 9,5. Щелочной реагент должен быть таким, который не приводит к введению примесей в осажденный карбонат кальция, являющийся продуктом. По этой причине весьма предпочтительно применение в качестве щелочного реагента раствора, такого как тот, что получен от стадии (ii), как указано выше, поскольку растворенные металлические примеси, содержащиеся в нем, не осаждаются в каком-либо существенном количестве при условиях pH, превалирующих в результирующей смеси. Обычно используемое количество этого раствора будет составлять от 3 до 8% от объема результирующей смеси с тем, чтобы достигнуть требуемой задержки в уменьшении pH.
Твердотельный карбонат кальция может быть отделен от результирующей смеси посредством любого обычного метода отделения. Соответственно, например, может быть использован фильтр-пресс.
Жидкость, отделенная от результирующей смеси, содержит полигидроксисоединение, которое, в идеальном случае, повторно используется в целях получения раствора, требующегося на стадии (i) способа. Это способствует общей экономичности процесса. Для этой цели отделенную жидкость очищают и концентрируют перед возвращением на стадию (i). Очистка служит для удаления примесей, которые могут, в противном случае, загрязнять карбонат кальция, полученный из использованного повторно раствора полигидроксисоединения. Очистка наиболее обычно выполняется посредством уменьшения рН жидкости до величины менее чем 8 (предпочтительно до 7-8) посредством добавления диоксида углерода. Затем раствор подвергается испарению для увеличения его концентрации до величины, подходящей для использования на стадии (i) способа. Испарение должно выполняться при условиях, которые не вызывают какого-либо значительного разложения полигидроксисоединения. Предпочтительным является испарение в вакууме. После стадии испарения оставшиеся твердотельные загрязняющие вещества удаляются из раствора, например, посредством второй стадии флокуляции и фильтрации или седиментации, как описано выше для стадии (ii), однако не обязательно с ними обеими.
Данное изобретение будет далее описано со ссылками на неограничивающие примеры ниже и также на сопроводительные чертежи, среди которых:
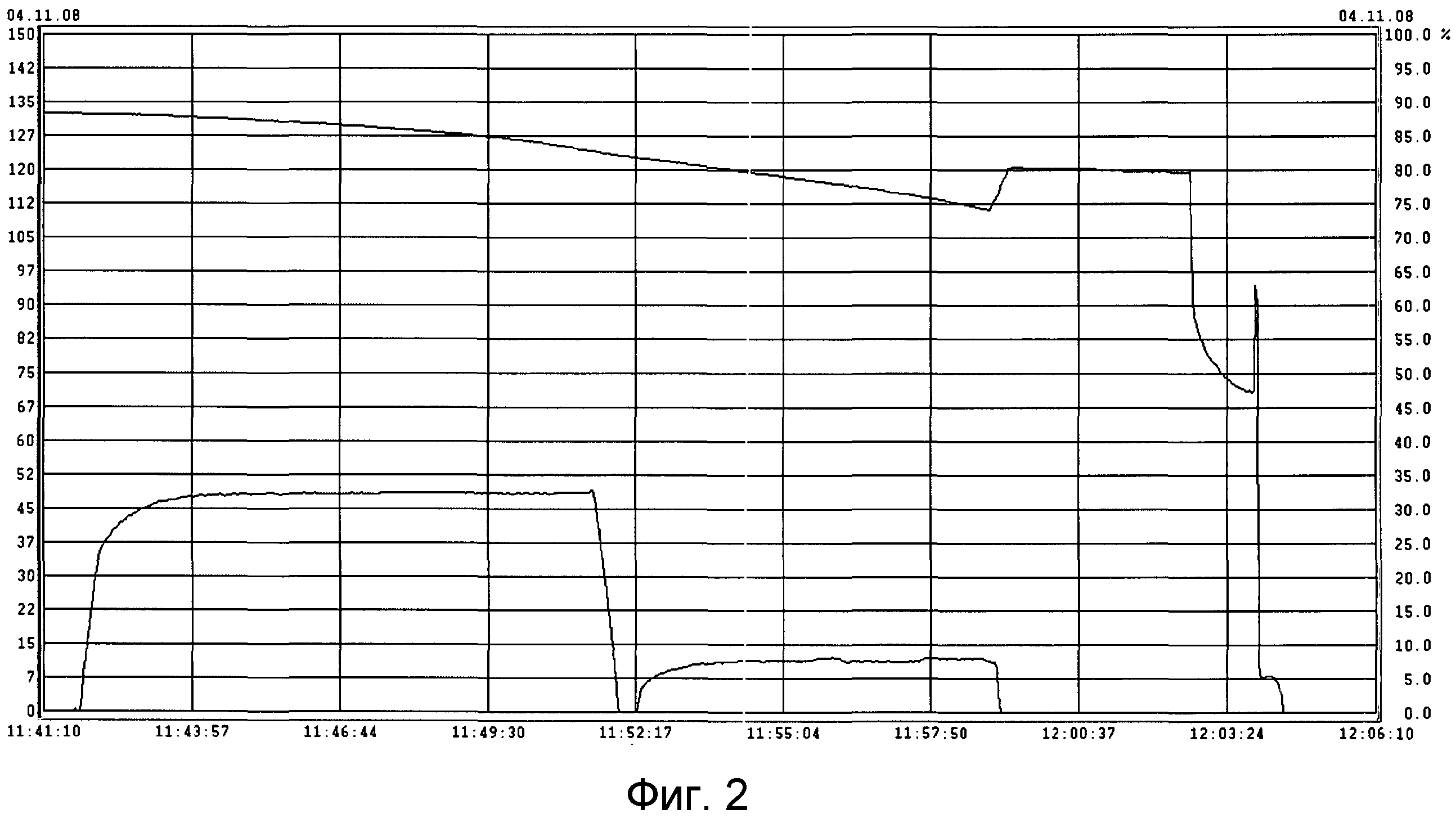
Фиг. 1 представляет собой график изменения рН в зависимости от времени для процедуры, описанной в Примере 1 ниже;
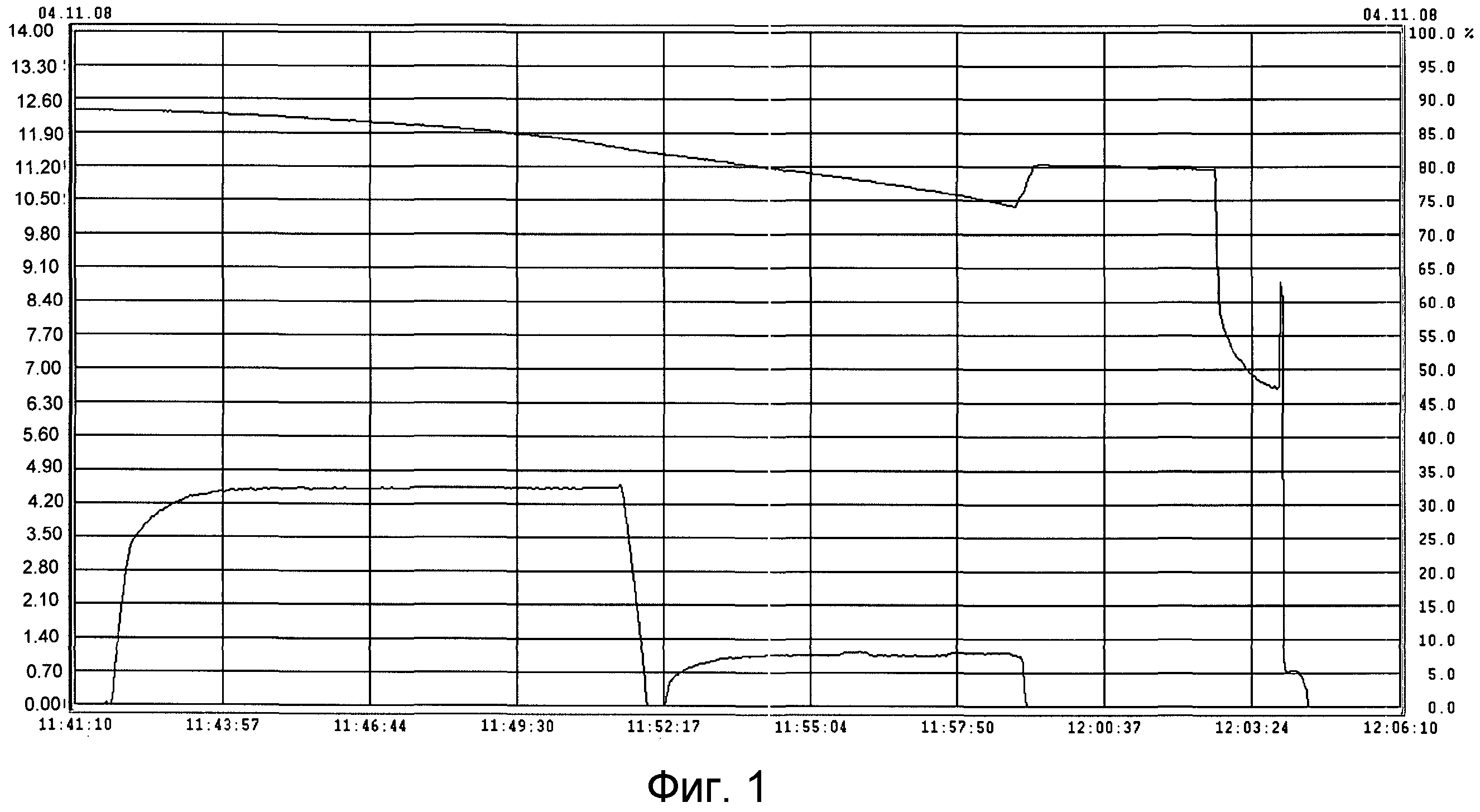
Фиг. 2 представляет собой график расходов диоксида углерода при его распределении в зависимости от времени для процедуры Примера 1;
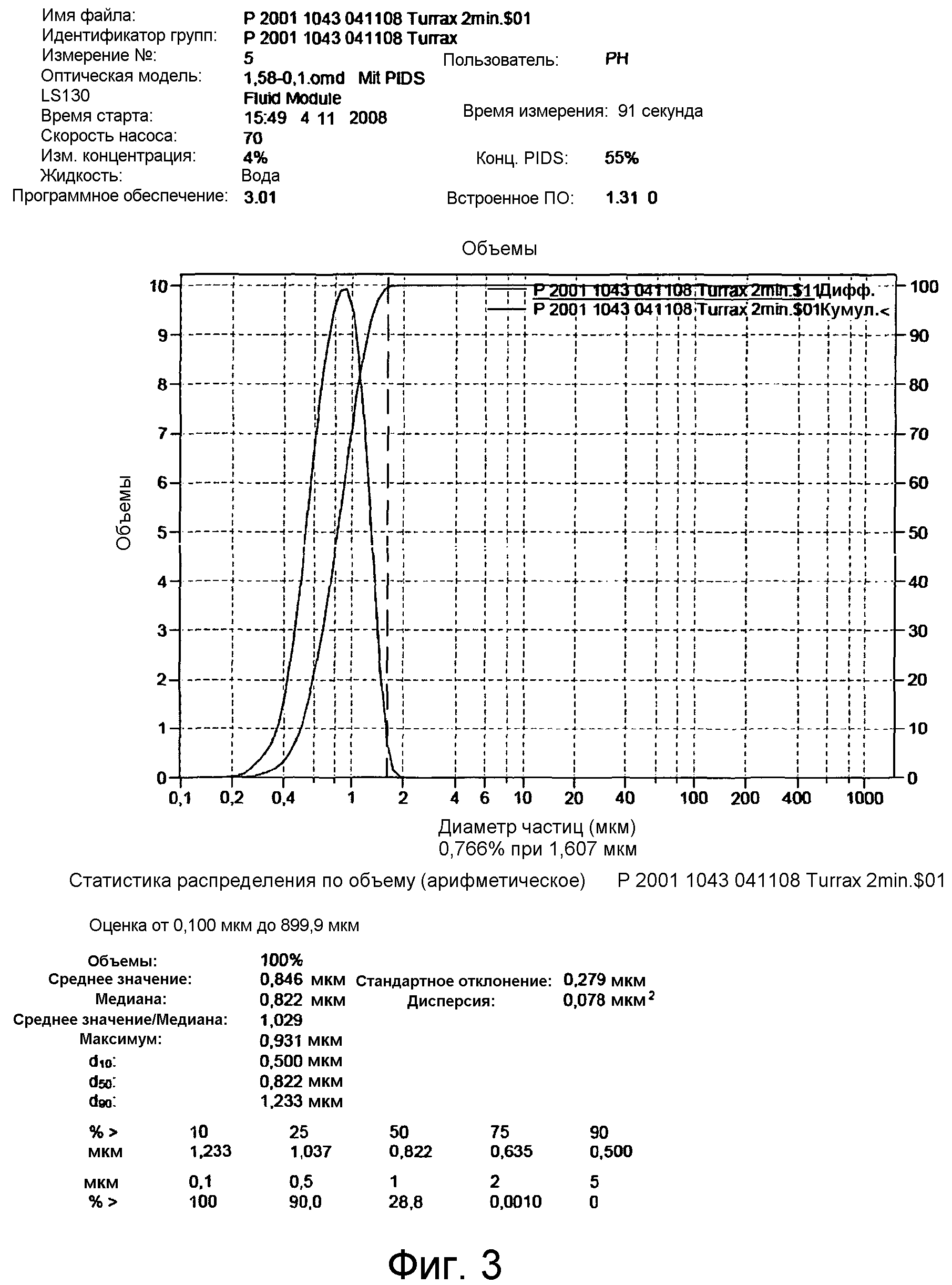
Фиг. 3 показывает распределение частиц по размерам продукта, полученного в соответствии с Примером 1; и
Фиг. 4 представляет собой фотографию при 5000-кратном
увеличении продукта, полученного в соответствии с Примером 1.
Пример 1
Этот пример описывает получение чистого карбоната кальция, содержащего дискретные частицы в форме «рисовых зерен», с использованием извести, полученной из обожженного известняка из карьера в Чешской республике. Известь имела уровни содержания примесей, представленные ниже в Таблице 1 в разделе «Результаты».
Процедура
1. Гашение негашеной извести
Суспензию гашеной извести получали смешиванием негашеной извести в качестве исходного материала с водой, чтобы получить конечную консистенцию с 46 масс.% для гашеной извести. В конце реакции гашения суспензия имела температуру примерно 85°C. Суспензию оставляли охлаждаться до температуры окружающей среды перед использованием на следующей стадии процесса, хотя это не является необходимым.
2. Растворение гашеной извести
88 кг гашеной извести (46 масс.%) смешивали с 940 кг раствора сорбитола 26,4 масс.%. Раствор сорбитола по существу не содержал примесей, и смешивание выполнялось при температуре окружающей среды с применением мешалки со спиральными лопастями, функционирующей при 80 об/мин.
Результирующий раствор содержал 25 масс.% сорбитола и 3,46 масс.% гашеной извести (в пересчете на Ca(OH)2).
3. Флокуляция/осаждение раствора гашеной извести
Катионный полимер добавляли к раствору при перемешивании, чтобы флокулировать загрязняющие вещества, присутствующие в растворе. Добавляли 6 млн-1 продукта Nalco 9908. Взаимно связанные хлопья затем образовывали при регулируемом перемешивании в течение примерно 20 минут. Эти хлопья затем отделяли от раствора посредством пропускания через пластинчатый отстойник. Хлопья, содержащие примеси, удаляли из нижней части отстойника. Анализ состава хлопьев представлен ниже в Таблице 1 в разделе «Результаты».
Результирующий раствор из отстойника затем профильтровывали через песчаную колонну, получая очень прозрачный раствор.
4. Карбонизация
Прозрачный раствор, полученный на стадии (iii), вводили в бак реактора на 1,2 м3 и примерно 20 кг CO2 инжектировали при температуре 23,1°C в нижнюю часть бака. Можно видеть из Фиг. 1, что имеют место три этапа, а именно:
(a) Первый этап, во время которого реакционная смесь была жидкостью, и чистый CO2 инжектировали при расходе 48,5 норм. м3/ч в течение 10 минут (1 норм. м3 представляет собой количество газа, которое занимает объем в 1 кубический метр при температуре 0°C и давлении 1,013 бар (101,3 кПа) абсолютного давления). Инжекция CO2 показана на Фиг. 2. Во время этого первого эапа величина pH монотонно уменьшалась от 12,35 до примерно 11,55 (см. Фиг. 1). Для удобства кривая растворения диоксида углерода, показанная на Фиг. 2, наложена на кривую pH по Фиг. 1. Аналогичным образом на Фиг. 2 кривая pH по Фиг. 1 наложена на кривую расхода диоксида углерода при растворении.
(b) Второй этап, на котором реакционная смесь была в форме геля, и чистый CO2 инжектировали при расходе 11,5 норм. м3/ч в течение 7 минут. Во время этого второго этапа величина pH продолжала падать до 10,4 (см. Фиг. 1).
(c) Третий этап осаждения, на котором частицы карбоната кальция достигали своей конечной величины. Суспензия становилась белой, и происходило значительное снижение вязкости. Как только начинался третий этап, инжектирование CO2 прекращали. В начале этого этапа величина pH быстро возрастала. Для обеспечения того, что pH не будет затем уменьшаться снова, добавляли 40 кг раствора, полученного на стадии (3) выше. Величина pH затем поддерживалась постоянной при примерно 11,2 (см. Фиг. 1).
5. Отделение карбоната кальция
Суспензию, полученную при окончании стадии (4), концентрировали при применении фильтр-пресса до консистенции с примерно 70-72%.
6. Повторное использование раствора сорбитола
Фильтрат от фильтр-пресса (стадия (5)) имел концентрацию сорбитола 26 масс.%. Этот раствор нейтрализовали с помощью CO2 до pH от 7 до 8 и затем испаряли под вакуумом при температуре примерно 65°C для увеличения концентрации сорбитола до 29 масс.%.
Результирующий раствор был применим для повторного использования на стадии (2) процесса.
Результаты
Продукт, полученный на стадии (4), имел распределение частиц по размерам, показанное на Фиг. 3. Видно, что частицы имели средний размер 0,82 мкм и узкое распределение по размерам, величины d10 и d90 составляли 0,50 мкм и 1,23 мкм соответственно или соотношение d90/d10, равное 2,46. Фиг. 4 представляет собой фотографию продукта стадии (4), сделанную при примерно 5000-кратном увеличении. Из Фиг. 4 можно видеть, что частицы имели внешний вид «рисовых зерен».
Полученный карбонат кальция имел яркость R 457, равную 97,1.
Таблица 1 ниже показывает уровни содержания примесей в карбонате кальция, являющемся продуктом, вместе с уровнями их содержания в исходном известковом материале и также в хлопьях, отделенных в конце стадии (3), при этом все количества указаны в мг/кг.
|
В вышеприведенной таблице «н/о» означает, что данная конкретная примесь имеет содержание ниже пределов обнаружения и поэтому «не обнаружена».
Пример 2
Этот пример описывает получение частиц карбоната кальция меньшего размера, чем те, что получены в Примере 1.
Процедуры, описанные для стадий 1-3 Примера 1, использовали для получения 773 кг раствора, содержащего 25 масс.% сорбитола и 3,9 масс.% гашеной извести (в пересчете на Ca(OH)2).
Раствор вводили в реактор с начальной температурой 22,5°C. Во время первого этапа CO2 инжектировали при 44 норм. м3/ч в течение 9,3 минуты. Во время второго этапа CO2 инжектировали при 9 норм. м3/ч в течение 8,3 минуты. Величина pH в начале реакции составляла 12,5. Величина pH постепенно уменьшалась до 10,5, и в этой точке она внезапно возрастала до 11,2. Как только величина pH начинала возрастать, инжекцию CO2 прекращали и добавляли 25 кг раствора, идентичного тому, что вводился в реактор в начале процесса. Это поддерживало pH при 11,2.
Карбонат кальция, полученный таким образом, имел средний размер частиц 0,5 микрона. Распределение частиц по размерам, выраженное соотношением d90/d10, составляло 3,6. Карбонат кальция имел яркость R 457, равную 96,9.
Пример 3
Этот пример описывает получение частиц карбоната кальция большего размера, чем те, что получены в Примере 1.
Процедуры, описанные для стадий 1-3 Примера 1, использовали для получения 606 кг раствора, содержащего 25 масс.% сорбитола и 1,8 масс.% гашеной извести (в пересчете на Ca(OH)2).
Раствор вводили в реактор с начальной температурой 17,0°C. Во время первого этапа CO2 инжектировали при 34 норм. м3/ч в течение 7,6 минуты. Во время второго этапа CO2 инжектировали при 10,9 норм. м3/ч в течение 0,7 минуты. Величина pH в начале реакции составляла 13,0. Величина pH постепенно уменьшалась до 10,1, и в этой точке она внезапно возрастала до 11,2. Как только величина pH начинала возрастать, инжекцию CO2 прекращали и добавляли 25 кг раствора, идентичного тому, что вводился в реактор в начале процесса. Это поддерживало pH выше 11,2.
Частицы карбоната кальция, полученного таким образом, имели средний размер 1,42 микрона. Распределение частиц по размерам, выраженное соотношением d90/d10, составляло 3,25. Карбонат кальция имел яркость R 457, равную 96,2.
Пример 4
Этот пример демонстрирует влияние pH на чистоту продукта.
Лабораторный эксперимент выполняли на 2000 граммах раствора, содержащего 25 масс.% сорбитола и 3,4 масс.% гашеной извести. Раствор разделяли на две равные порции. Каждую порцию размещали в небольшом реакторе на 3 литра и инжектировали CO2 в раствор, при 96 литрах/час на этапе 1 и при 25,5 литрах/час на этапе 2. Начальная величина pH составляла 12,7 для обеих порций. Инжекцию CO2 прекращали для обеих порций, когда происходило внезапное увеличение pH.
Характеристики реакции для каждой из порций и подробности обработки соответственно описаны ниже.
Порция 1: Внезапное, кратковременное увеличение pH происходило при pH 10,9. Тотчас же добавляли 11 граммов исходного раствора, и это поддерживало pH выше 11,2.
Порция 2: Внезапное, кратковременное увеличение pH происходило при 11,1. После увеличения до 11,5 величина pH затем быстро уменьшалась до 7,4. Раствор не добавляли, и величина pH продолжала уменьшаться до 7,0 в течение последующих 15 минут.
Карбонат кальция, полученный в каждой из двух порций, анализировали в отношении яркости R 457 и содержания железа. Результаты представлены в приведенной ниже таблице.
|
Можно видеть из представленной выше таблицы, что регулирование pH в соответствии с данным изобретением (порция 1) приводит к получению чистого продукта с низким содержанием железа, как это отражено посредством величины яркости R457 (97,7). В противоположность этому, порция 2 (которая обрабатывалась без регулирования pH) предоставляла продукт, имеющий содержание железа 200 млн-1 и величину яркости R457 95,3.