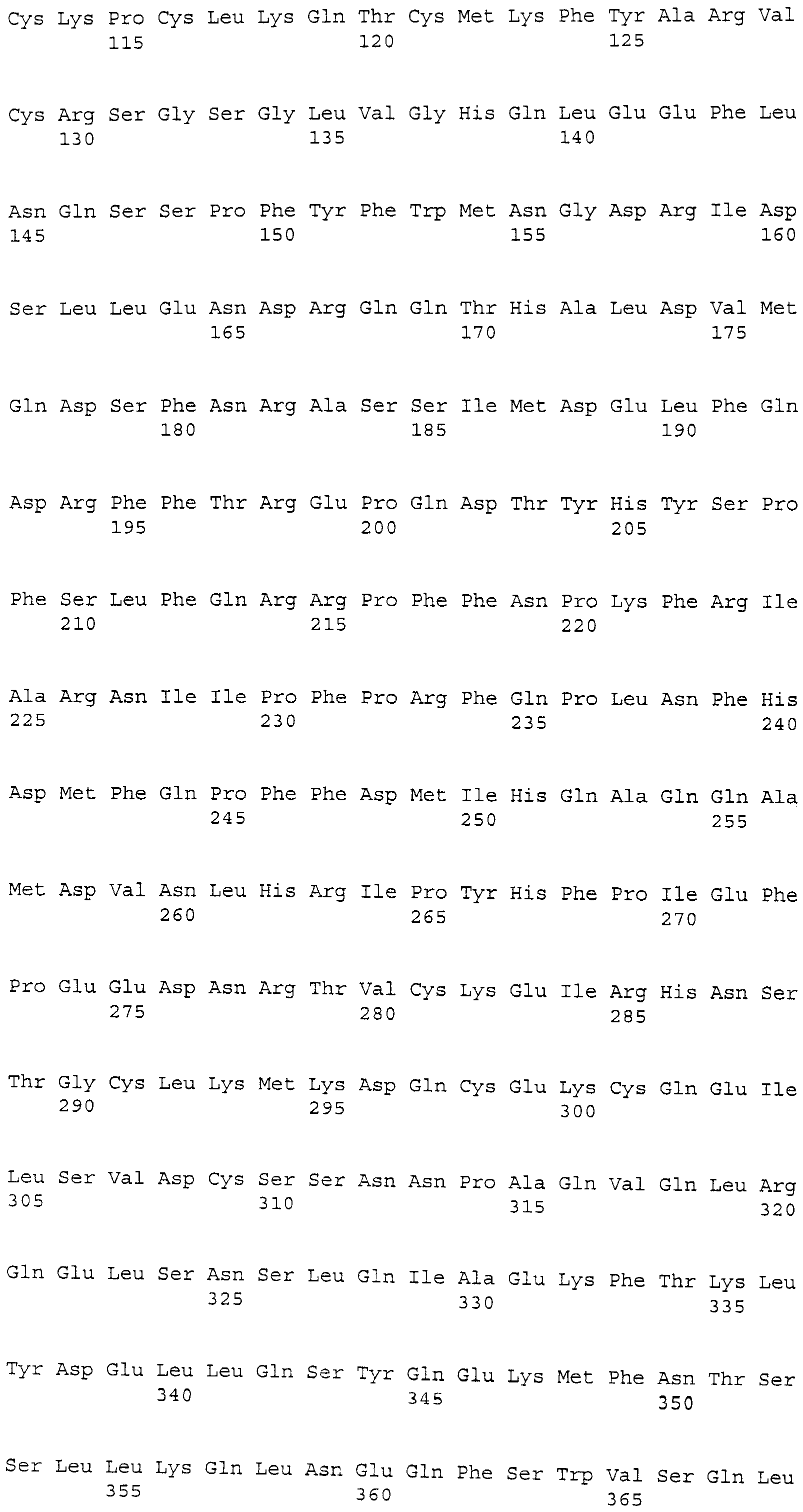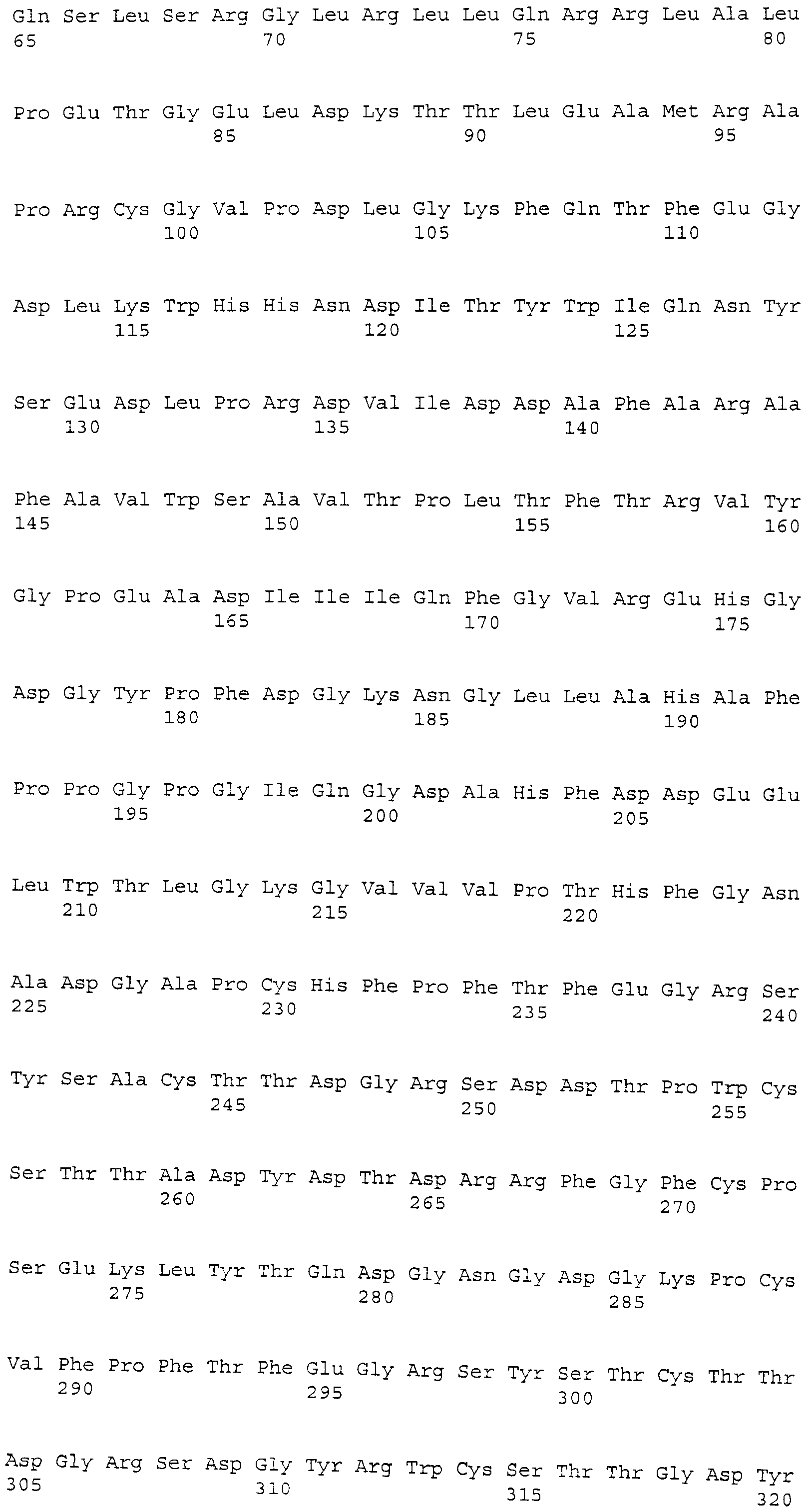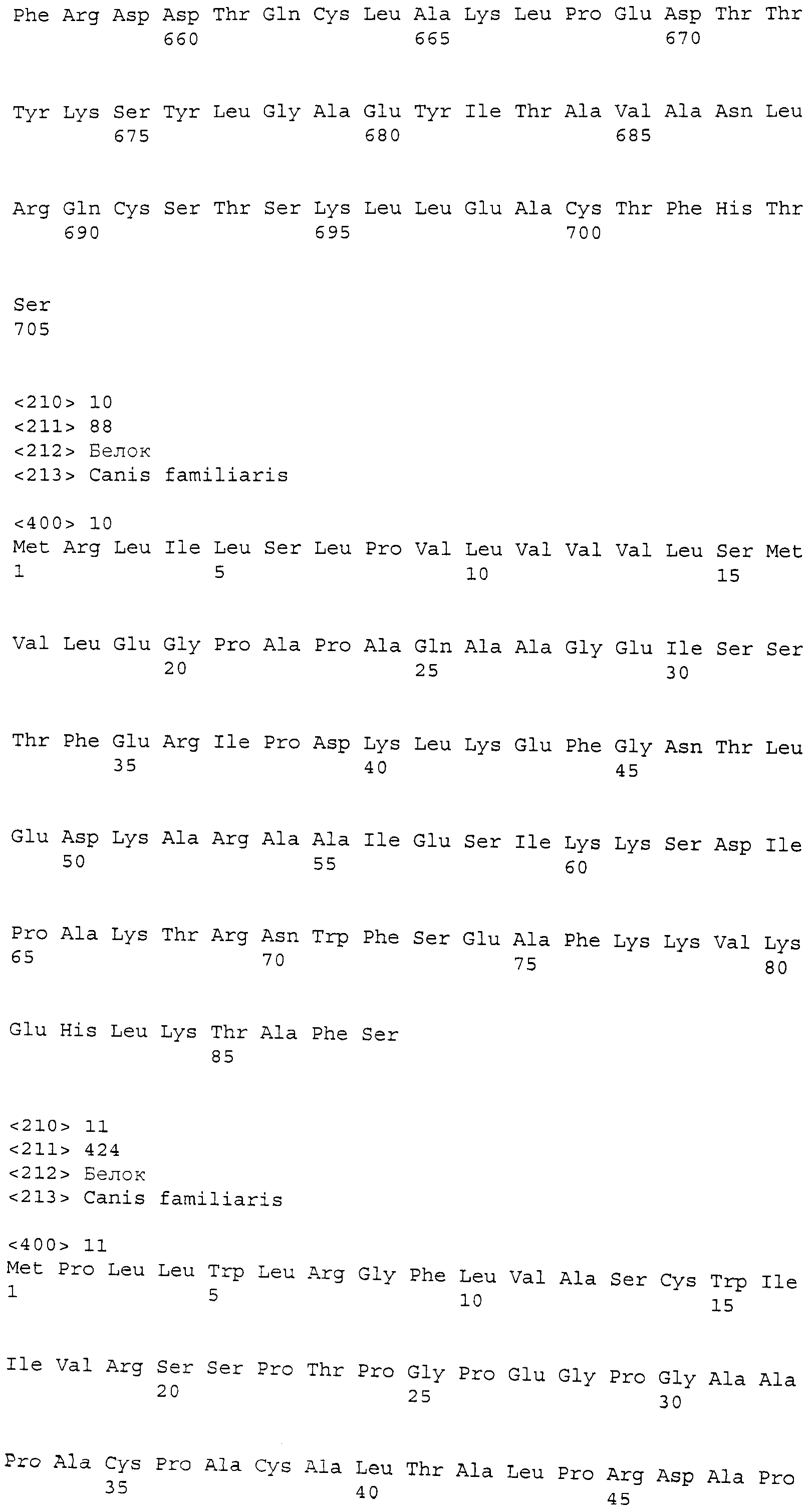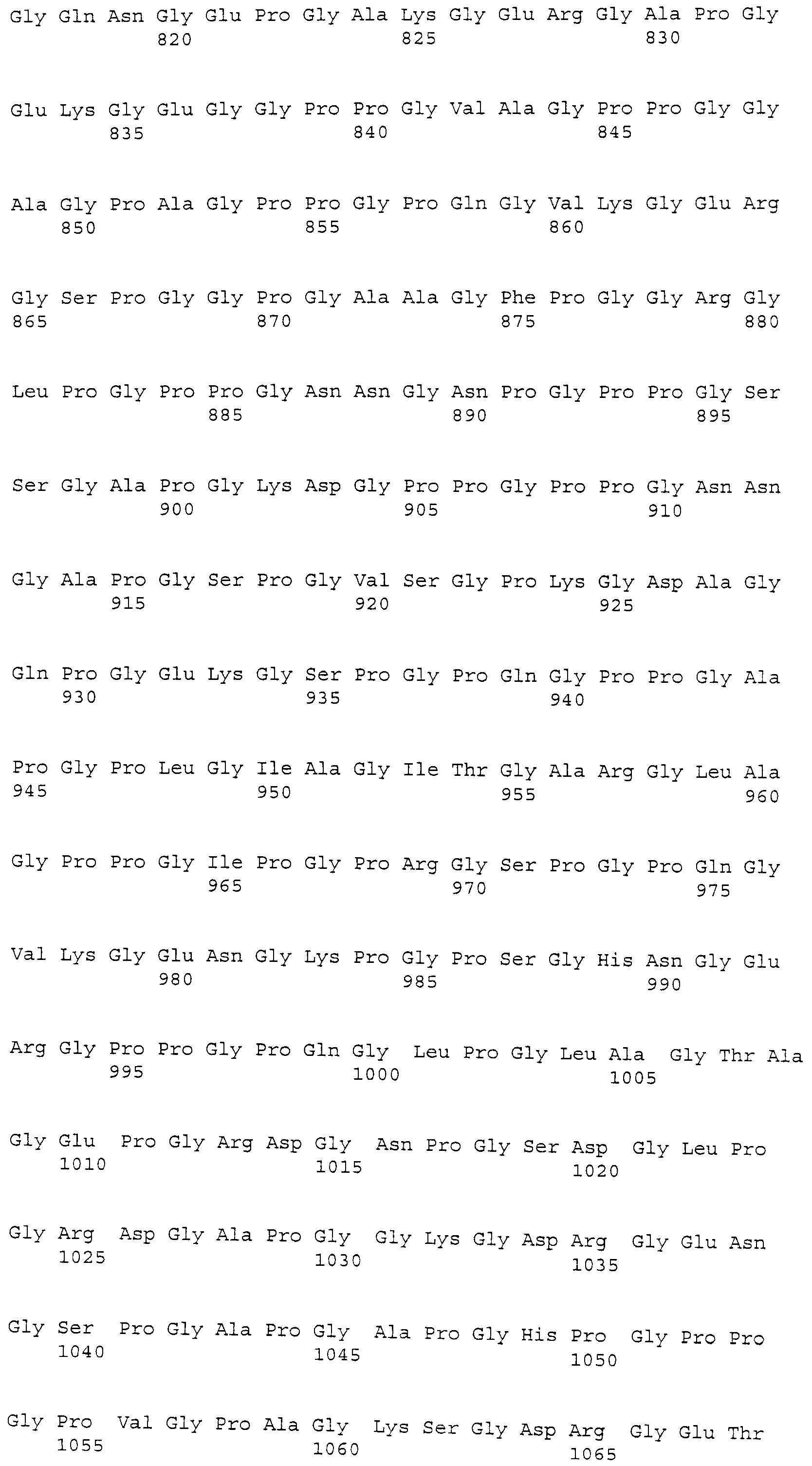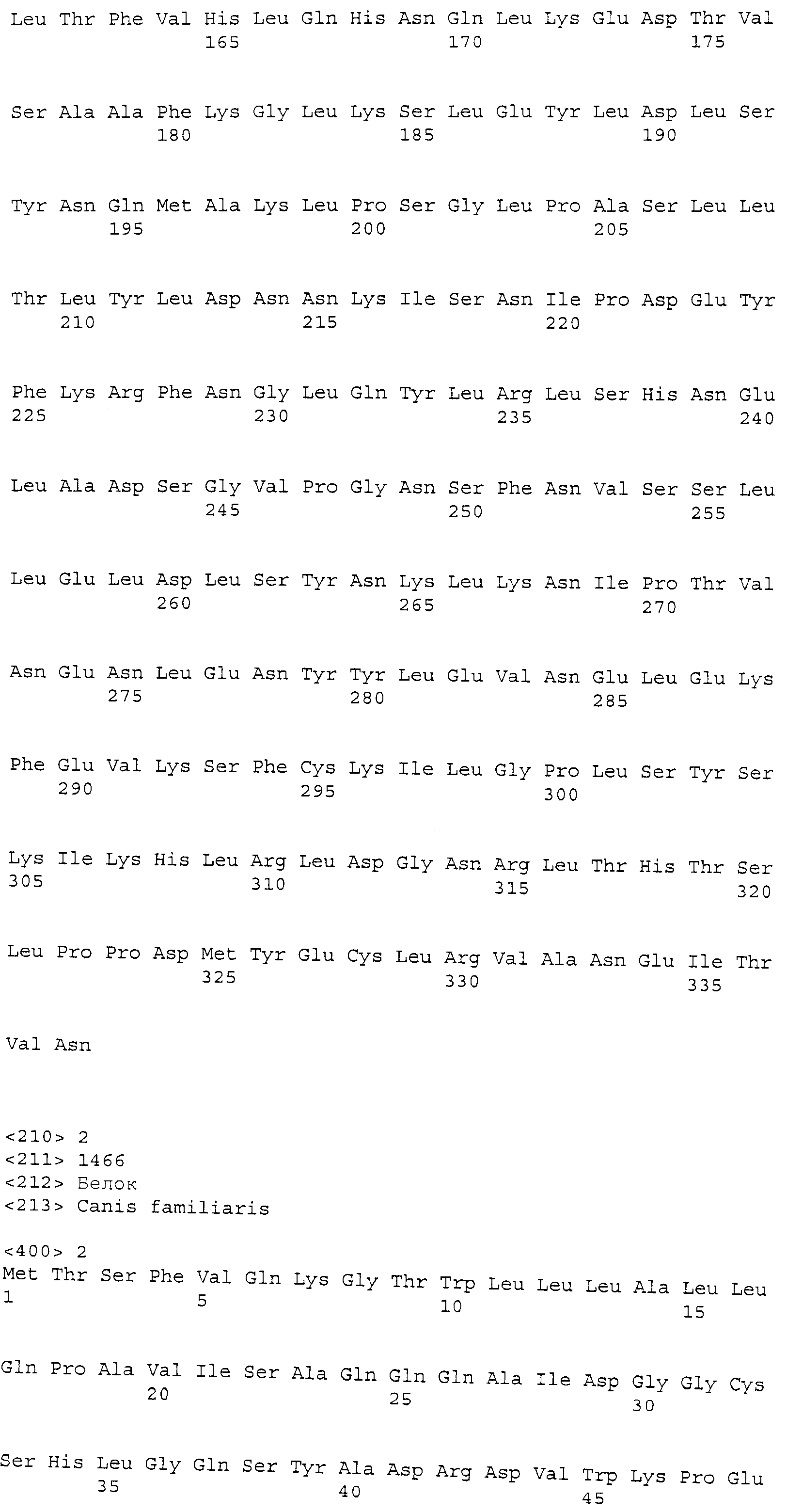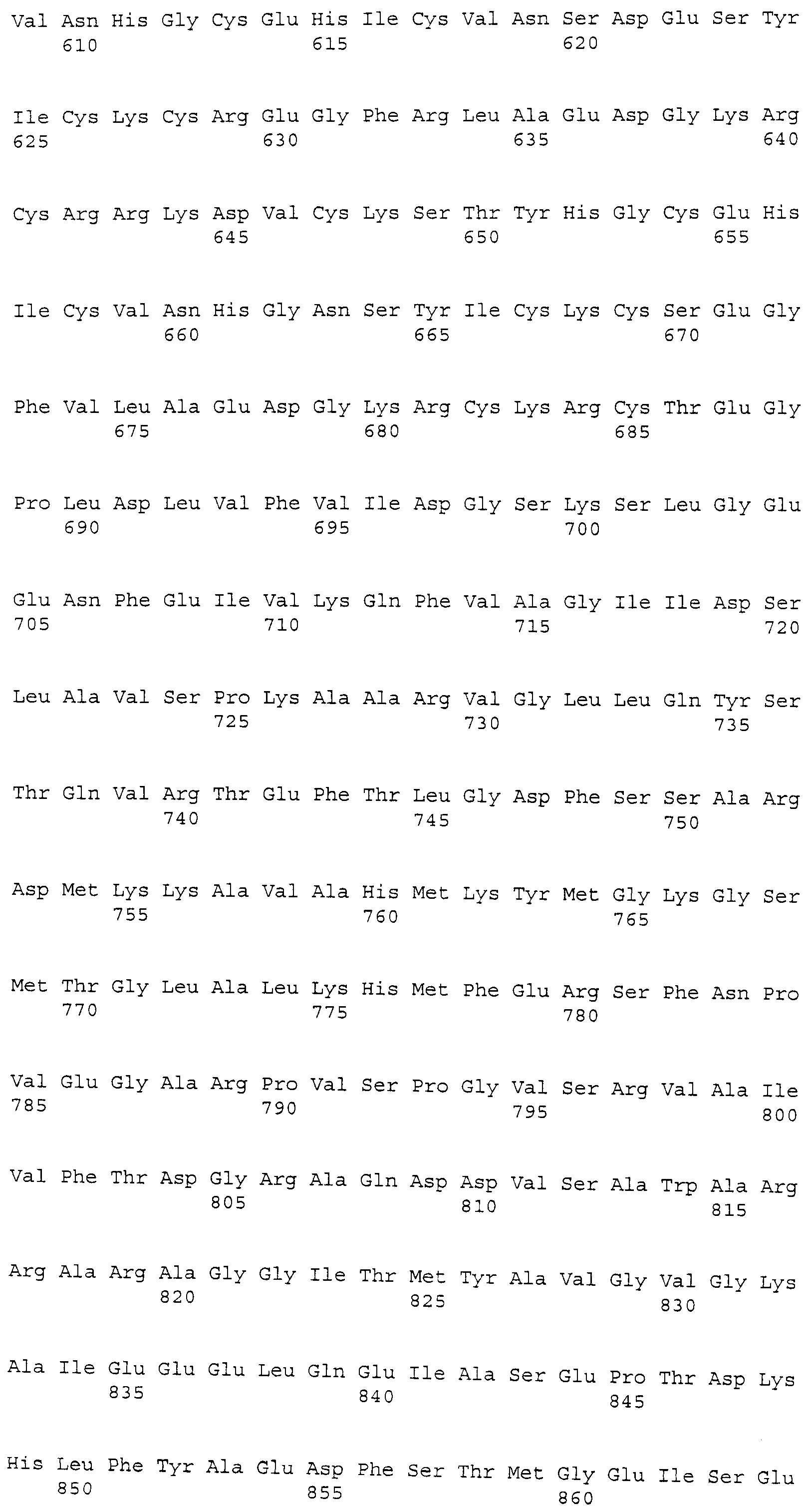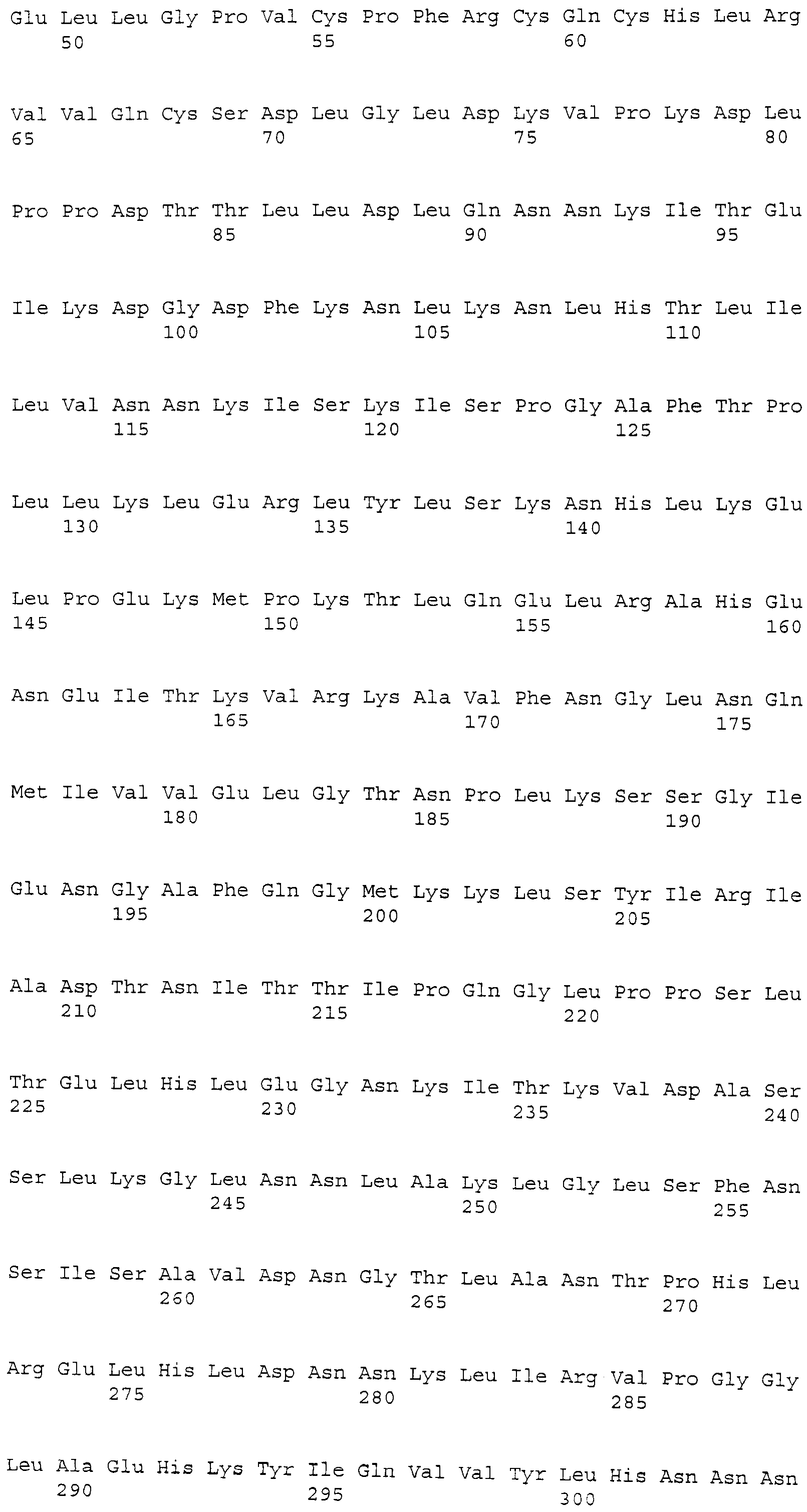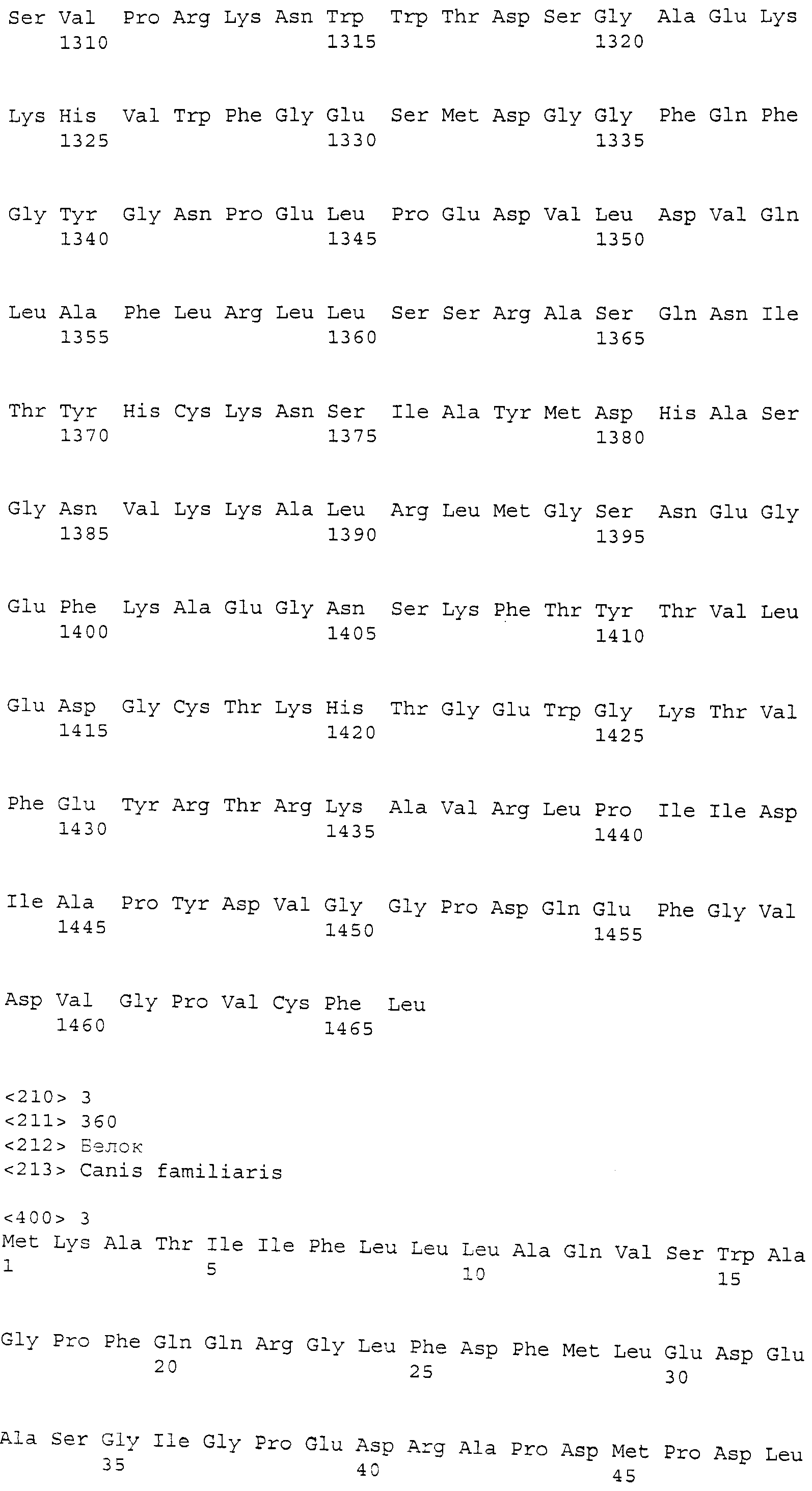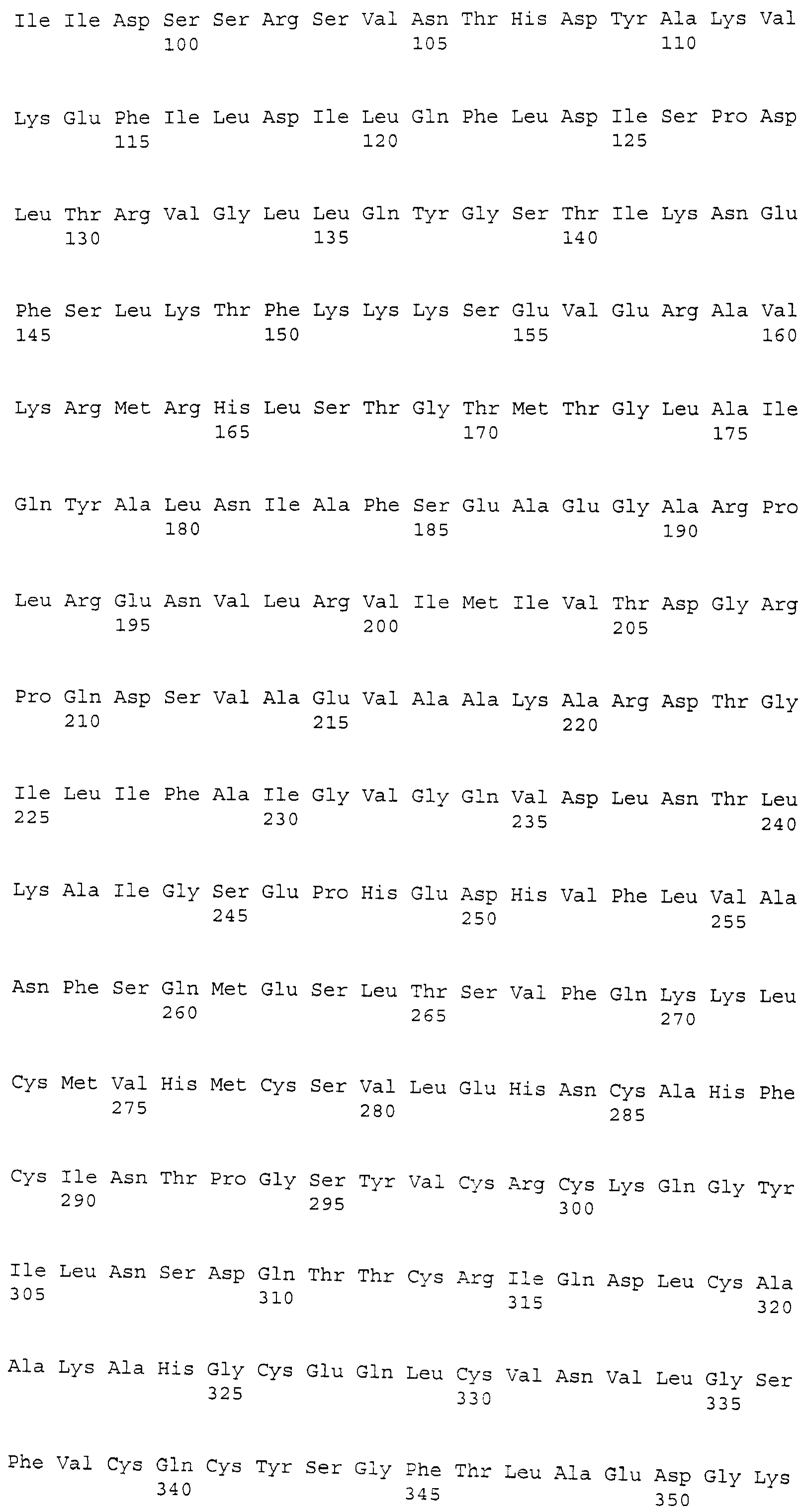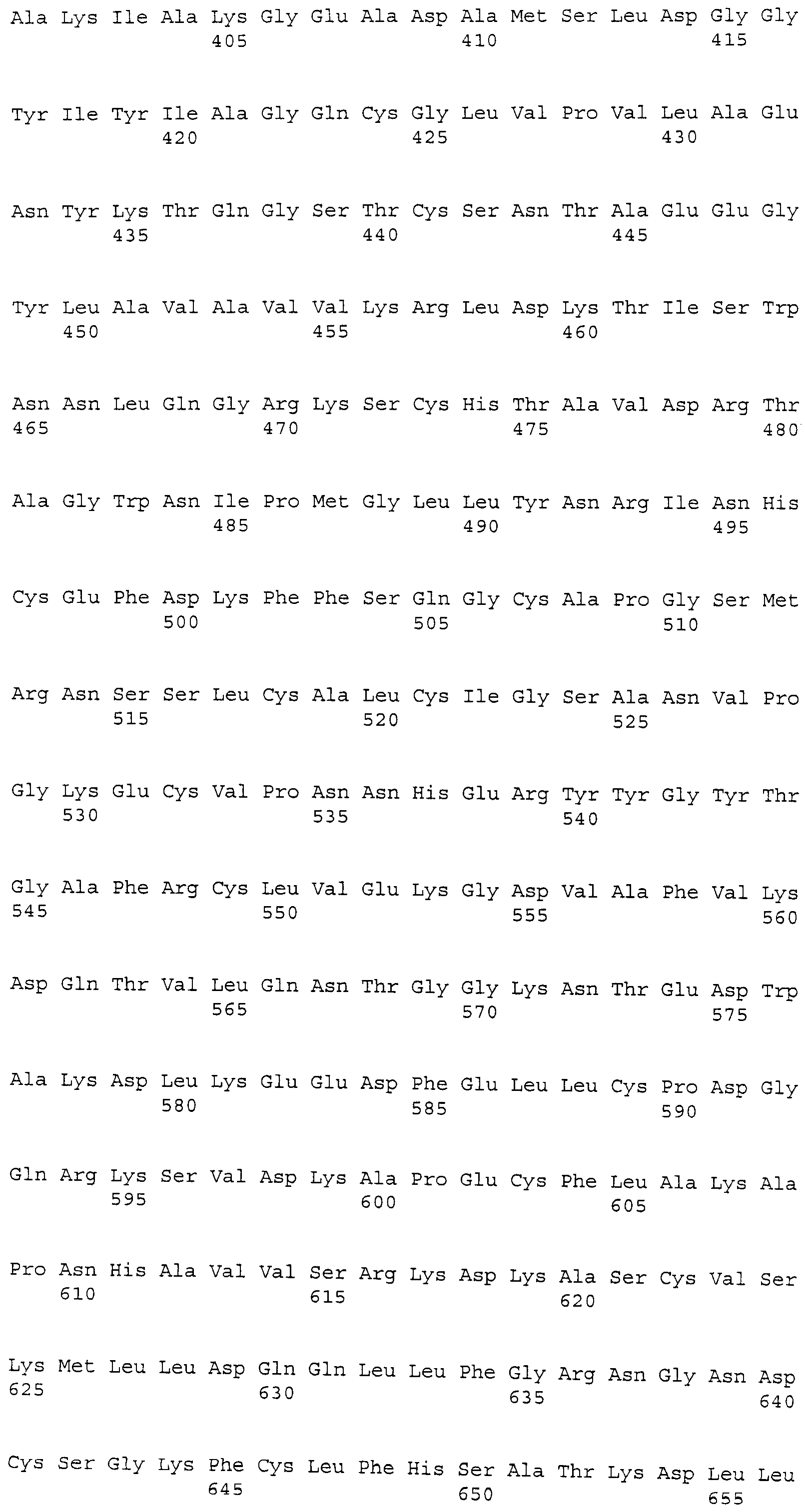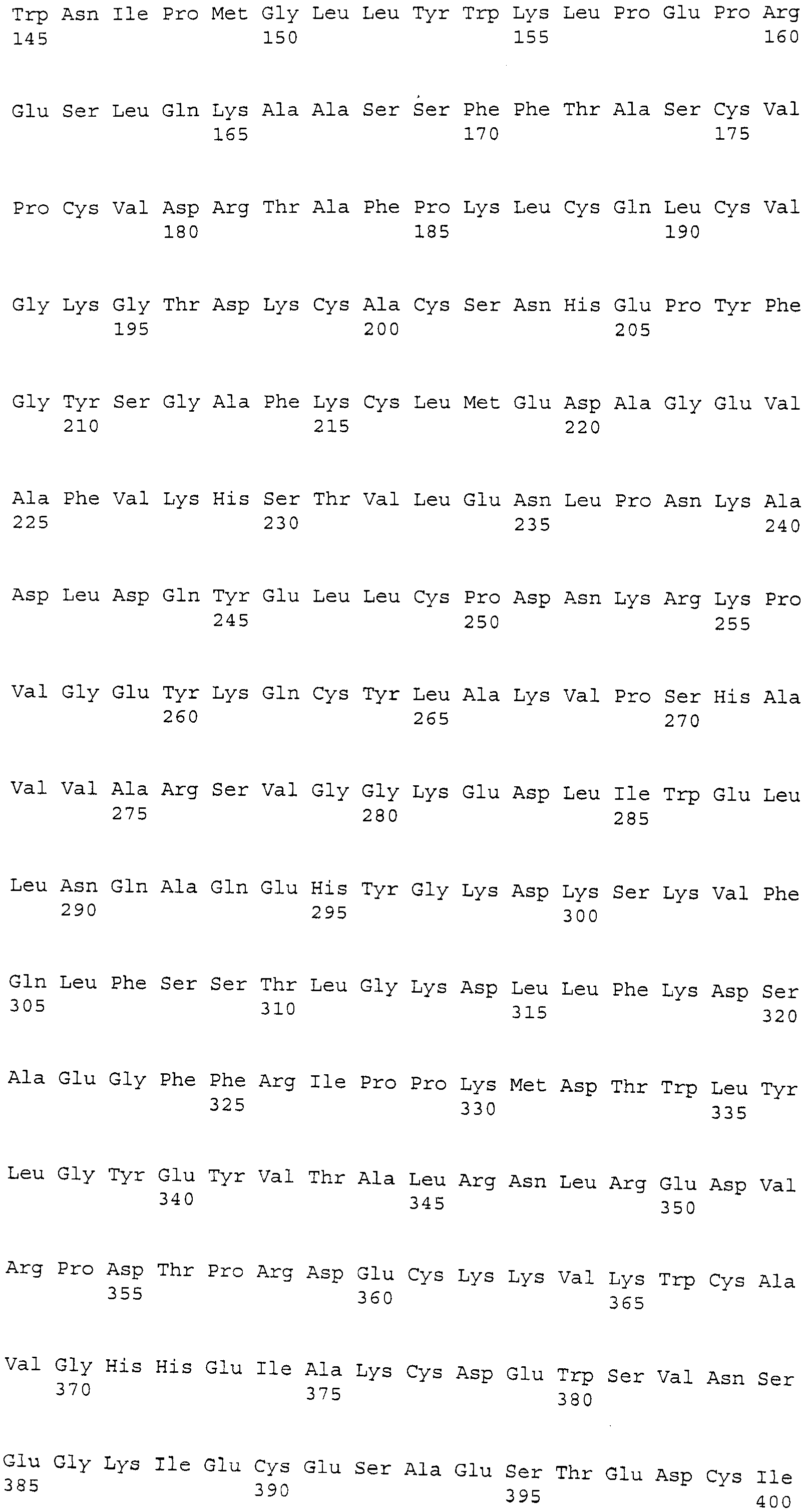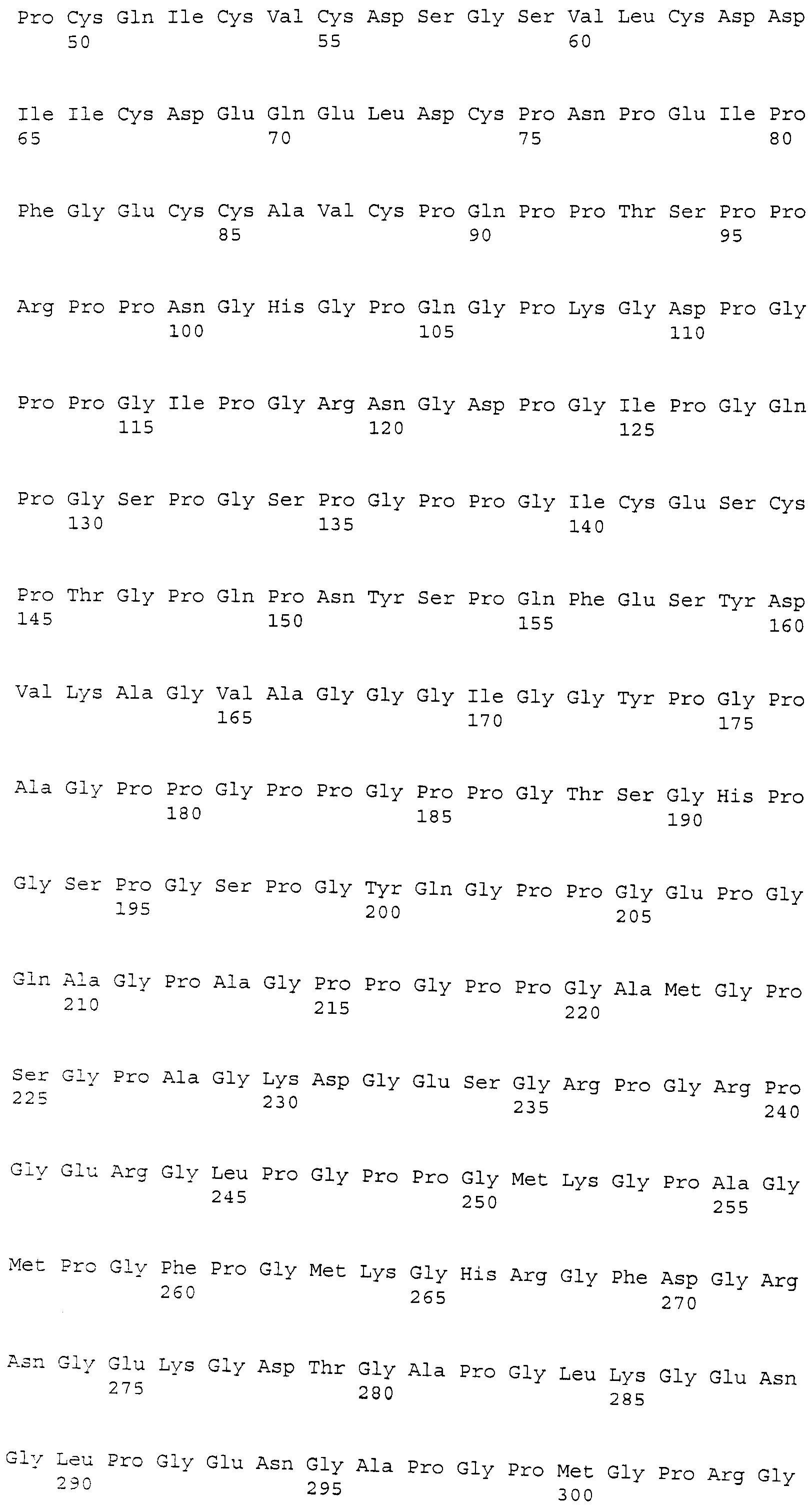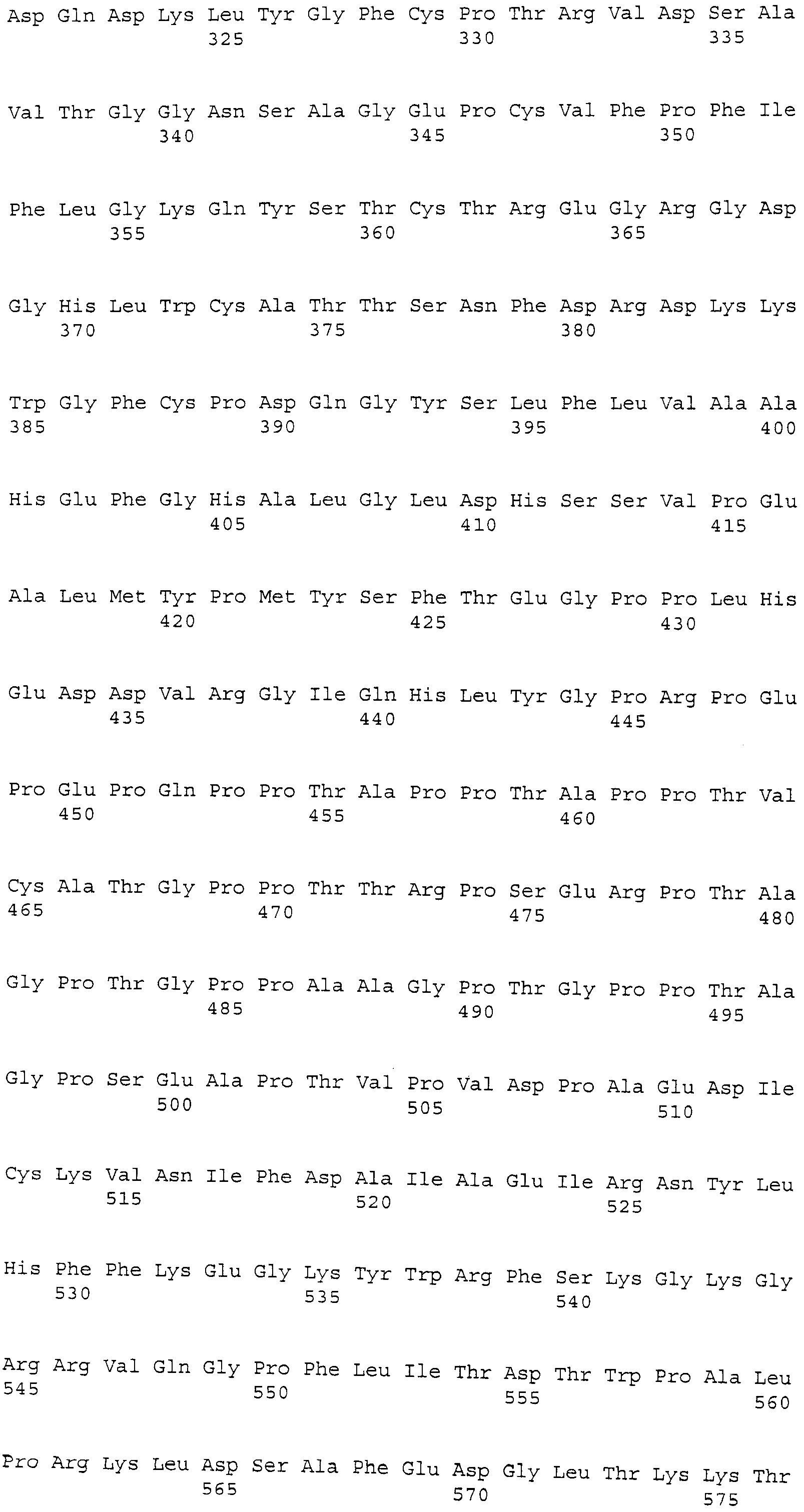Результат интеллектуальной деятельности: КОМПОЗИЦИИ И СПОСОБЫ ДЛЯ ДИАГНОСТИКИ И ЛЕЧЕНИЯ НАРУШЕНИЙ ПОЧЕК У СОБАК
Вид РИД
Изобретение
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
По данной заявке испрашивается приоритет предварительной патентной заявки США № 61/289773, поданной 23 декабря 2009 года, которая включена в настоящее описание в качестве ссылки.
Настоящее изобретение относится к композициям и способам для: диагностики, разработки и мониторинга плана лечения, и мониторинга статуса нарушения почек, характеризующегося аномальной утратой почечной функции, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, у собак, где нарушение почек поддается детекции с использованием по меньшей мере одного характерного биомаркера, выделенного из биологического тестируемого образца, взятого от собаки, и измеренного в нем. Значимый биомаркер для применения на практике композиций и способов по настоящему изобретению включает РНК-транскрипт или его продукт трансляции, взятый из такого биологического тестируемого образца такой собаки. Биологический тестируемый образец для применения на практике способа по изобретению включает образец ткани почки такой собаки или образец биологической жидкости, взятый от такой собаки.
Настоящее изобретение также относится к идентификации комбинаций новых биомаркеров для применения в диагностике, разработке и мониторинге плана лечения, и мониторинге статуста нарушения почки, характеризующегося аномальной утратой почечной функции, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, у собак.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Гломерулонефрит или гломерулярный нефрит ("GN") представляет собой заболевание почек, характеризующееся воспалением гломерул или капиллярных петель почки. Он представляет собой патологический процесс, ассоциированный с рядом разнообразных лежащих в его основе заболеваний. Это состояние возникает в острой, подострой и хронической формах, а также вторично после инфекции. В первом случае состояния, когда сопутствующее заболевание не может быть найдено, обычно называют идиопатическим гломерулонефритом. Во втором случае состояния обычно называют вторичным GN. Независимо от первопричины, образуются иммунные комплексы и приводят к серии событий, ведущих к повреждению гломерул и утрате почечной функции, протеинурии и, в конечном итоге, в некоторых случаях, к почечной недостаточности.
Нефрит представляет собой воспаление почки, которое может быть очаговым или диффузным, пролиферативным или деструктивным заболеванием, вовлекающим гломерулы, почечные канальцы или интерстициальную (или соединительную) ткань почек. Наиболее распространенной формой нефрита является гломерулонефрит. Нефрит может прогрессировать через ряд стадий, оканчивающихся заболеванием почек конечной стадии или почечной недостаточностью конечной стадии.
Почечная недостаточность возникает вследствие неспособности почки поддерживать ее нормальные функции. В результате метаболические продукты жизнедеятельности и метаболиты накапливаются в крови. Эти продукты жизнедеятельности и метаболиты могут неблагоприятно влиять на большинство систем организма. Характеристиками почечной недостаточности являются нарушения поддержания баланса жидкостей и электролитов.
Острая почечная недостаточность может возникать неожиданно вследствие травмы, инфекции, воспаления или воздействия нефротоксических веществ. Это состояние может приводить к дегидратации, гипотензии и сосудистому коллапсу. Острую почечную недостаточность часто подразделяют на три категории: (1) предпочечная недостаточность, которая ассоциирована со сниженным почечным кровотоком; (2) внутрипочечная недостаточность, которая связана с ишемией и токсинами; и (3) постпочечная недостаточность, которая является результатом затруднения потока мочи.
Хроническая почечная недостаточность вовлекает прогрессирующую утрату почечной функции, которая в конечном итоге может прогрессировать в конечное заболевание почек или почечную недостаточность. В начале, хроническая почечная недостаточность начинается как уменьшение почечной функции без поддающегося оценке накопления метаболических продуктов жизнедеятельности в крови. По мере замедления скорости гломерулярной фильтрации вследствие воспаления начинают накапливаться продукты жизнедеятельности. Заболевание прогрессирует в уремию вследствие низкой функции почек, и высокие уровни белковых конечных продуктов начинают накапливаться и нарушать функции организма. Частые причины хронической почечной недостаточности включают: воспаление, инфекцию, обструкцию мочевых путей и определенные системные заболевания и токсичность, включая гиперкальциемию, красную волчанку, сахарный диабет и гипертензию.
Заболевание почек конечной стадии характеризуется необратимой хронической почечной недостаточностью. Уровни креатинина в сыворотке и азота мочевины в крови продолжают расти, и возникшая в результате уремия повреждает все системы организма. Почка может претерпевать постоянную и практически полную утрату функции до порядка 10% или менее нормальной функции почек. Одной из причин заболевания почек конечной стадии является гломерулонефрит. Другие причины включают причины, упомянутые для хронической почечной недостаточности.
Гломерулонефрит может возникать в результате биологического повреждения иммунной системы. Чужеродные вещества могут прикрепляться к базальной мембране и вызывать иммунный ответ, приводящий к продуцированию антител. Эти антитела в комбинации с чужеродными веществами могут приводить к отложению иммунных комплексов на стенках мелких гломерулярных капилляров, вызывая повреждение нефрона. Альтернативно, у некоторых индивидуумов иммунная система может вырабатывать аутоантитела, которые представляют собой иммуноглобулины, которые могут атаковать клетки почки, что приводит к так называемому аутомиммунному ответу. Если белки в организме изменены, может возникнуть аутоантительный ответ, поскольку аутоантитела распознают измененные белки как чужое. Эти комплексы аутоантитело-белок могут аналогично откладываться на базальной мембране гломерул, вызывая нарушение функционирования нефрона.
Гломерулонефрит является частой причиной протеинурии у собак и может представлять собой либо идиопатическую, либо вторичную форму состояния. В последнем случае состояние может развиваться вторично после новообразования, воспалительных заболеваний, нарушения эндокринных функций, инфекций или семейных нефропатий. Как и у человека, GN у собак опосредуется иммунологически, вовлекая иммуноглобулины и факторы комплемента в организме животного. Повреждение возникает в гломерулах почки, что приводит к морфологическим изменениям гломерул. В результате повреждение является необратимым и приводит к нарушению функции нефронов.
В научном сообществе общепризнано, что регуляция экспрессии генов играет ключевую роль в развитии некоторых заболеваний или состояний, которые влияют на здоровье и благополучие животного. Аналогично, дифференциальная экспрессия генов является одним из факторов развития таких заболеваний и состояний и оценка профилей экспрессии генов стала широко признанной в качестве важной для понимания развития и контроля таких заболеваний и состояний на молекулярном уровне. Для продвижения в понимании генов и их взаимосвязи с заболеванием был разработан ряд способов исследования дифференциальной экспрессии генов, например ДНК-микрочипы, секвенирование маркерных экспрессированных последователностей (EST), серийный анализ экспрессии генов (SAGE), вычитательная гибридизация, вычитательное клонирование и дифференциальный дисплей (DD) для мРНК, ПЦР с произвольной затравкой РНК (RAP-ПЦР), ПЦР в реальном времени (RT-ПЦР), репрезентативный анализ отличий (RDA), двумерный гель-электрофорез, масс-спектрометрия и белковый микрочип на основе связывания антител для белков.
Вследствие сложности биологических каскадов, вовлеченных в заболевание почек, и присущих им молекулярных взаимодействий и процессов внутриклеточной передачи сигнала очень желательно понимать происходящие взаимодействия на генетическом уровне. Детекция генов с нарушенной регуляцией на ранних стадиях утраты функции почек у собак полезна для понимания биологии заболевания почек, особенно гломерулонефрита, исходя из генома в целом. Тот факт, что нарушение регуляции генов может быть выявлено на ранней стадии развития заболевания у животных, подвергаемых повторяющемуся ишемическому повреждению, полезен для создания способов диагностики и разработки и мониторинга плана лечения аномальной утраты функции почек, почечной недостаточности, сниженной скорости гломерулярной фильтрации или гломерулонефрита у собак.
Более детальное понимание вовлекаемых биологических путей посредством определения профиля экспрессии генов может способствовать разработке диагностических способов, реагентов и тестовых наборов, а также полезных фармацевтических, нутрицевтических и пищевых (диетологических) вмешательств в связанные с заболеванием каскады. Эти подходы могут обеспечить раннюю детекцию и, возможно, профилактику или лечение связанного с ними заболевания почек, в частности гломерулонефрита, а также мониторинг прогноза почечной недостаточности и гломерулонефрита ранней стадии, особенно у собак. Гены с нарушенной регуляцией, вовлеченные в патологию таких нарушений, могут служить в качестве важных биомаркеров для диагностики и потенциально предупреждения или лечения нарушения и для оптимизации выбора подходящих фармацевтических, нутрицевтических и пищевых (диетологических) вмешательств.
Уровень экспрессии генов и/или определение уровня функционирования экспрессированного продукта гена у собак можно использовать для выбора подходящего средства для терапевтического или профилактического применения. Эти данные может использовать квалифицированный специалист при выборе подходящих лекарственных средств в качестве средств для профилактики или лечения заболеваний почек у собак путем определения профиля экспрессии генов. Данные и анализ экспрессии генов также можно использовать для выбора пищевых композиций, добавок в рацион и нутрицевтических средств, имеющих полезный эффект на работу почек, с использованием биомаркеров, указывающих на состояние здоровья с точки зрения функционирования почки.
Только очень ограниченная работа была проведена к настоящему времени для скрининга генома собак в отношении профилей экспрессии генов применительно к диагностике заболевания у собак. В определенной работе с использованием моделей на животных использовали технологии кДНК-чипов для скрининга экспрессии генов в тканях почек, ассоциированных с заболеванием почек.
Тщательных исследований в здоровых популяциях собак против популяций с заболеванием, таким как заболевание почек и утрата функции почек, как описано в настоящем описании, не проводили. Доступно мало данных в отношении профиля экспрессии генома собак, особенно в отношении развития заболеваний почек у собак с течением времени. Данные об экспрессии генов, содержащиеся в этом описании, идентифицируют гены, ассоциированные с функцией почек у собак. Такие данные об экспрессии генов обеспечивают разработку композиций и способов для диагностики, разработки и мониторинга плана лечения, и мониторинга статуса нарушения почек, характеризующегося аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, у собак, где нарушение почек поддается детекции с использованием по меньшей мере одного характерного биомаркера, выделенного и измеренного в биологическом тестируемом образце, взятом от такой собаки.
Данные об экспрессии генов, представленные в описании и примерах, обеспечивают различные желательные изобретения на основе профилей экспрессии генов, описанных в описании и примерах этой патентной заявки. Эти данные позволяют идентификацию и количественное определение продуктов экспрессии генов в качестве биомаркеров для предупреждения, идентификации и лечения связанного с ними заболевания почек. Данные об экспрессии генов, полученные в результате применения на практике способов по изобретению, также позволяют мониторинг прогрессирования такого заболевания почек. Эти изобретения, кроме того, включают генетическое тестирование для идентификации предпрасположенных субпопуляций животных, которые вероятно будут страдать таким заболеванием почек, для идентификации оптимального рациона для профилактики или лечения таких заболеваний почек, для идентификации фармацевтических, нутрицевтических и пищевых (диетологических) вмешательств на основе данных, указанных в этом описании, для лечения исходного заболевания. Изобретения также включают биомаркеры для ранней детекции заболевания, направленных лекарственных средств, диагностических реагентов и наборов для анализа образцов тканей и крови от собак, предрасположенных к такому заболеванию почек или имеющих его.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к композициям и способам для: диагностики, разработки и мониторинга плана лечения, и мониторинга статуса нарушения почек, характеризующегося аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, у собак, где нарушение почек поддается детекции с использованием по меньшей мере одного характерного биомаркера, выделенного из биологического тестируемого образца, взятого от такой собаки, и измеренного в нем.
Характерный биомаркер для применения на практике композиций и способов по настоящему изобретению включает РНК-транскрипт или его продукт трансляции, взятый из такого биологического тестируемого образца такой собаки. Биологический тестируемый образец для применения на практике способа по изобретению включает образец ткани почки такой собаки или образец биологической жидкости, взятый от такой собаки.
В частности, это изобретение относится к способам для: диагностики, разработки и мониторинга плана лечения, и мониторинга статуса нарушения почек, характеризующегося аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, у собак, с использованием анализа экспрессии генов.
Настоящее изобретение также относится к идентификации комбинаций новых биомаркеров для применения при определении, диагностике, разработке и мониторинге плана лечения и мониторинге статуса нарушения почек, характеризующегося аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, у собак.
Кроме того, изобретение относится к композициям, реагентам и набором для осуществления указанных способов.
Изобретение основано, частично, на открытии, что конкретные профили экспрессии генов у собак коррелируют с изменением у такого животного нормального биологического процесса в почках на ненормальный, что может приводить к снижению функции почек с течением времени. Корреляцию конкретного профиля экспрессии с риском снижения функции почек можно предсказать, выявить и диагностировать у собак без проведения общепринятой клинической диагностики, основанной на признанных в данной области клинических признаках и симптомах заболевания почек. Таким образом, измененный профиль экспрессии генов у собак прогнозирует снижение функции почек, что может быть иным образом диагностировано позднее с использованием признанных в данной области показателей функции почек. Такие признанные в данной области показатели функции почек, как правило, могут включать, например, один из следующих показателей: скорость гломерулярной фильтрации, скорость выведения креатинина, уровни белка в моче, уровни креатинина в сыворотке, уровни креатинина в моче, уровни азота мочевины в крови (BUN), радиоизотопное метаболическое мечение, визуализацию мягких тканей, включая сонографию, магнитно-резонансную томографию и/или компьютерную томографию. Неинвазивные анализы, такие как уровни креатинина в сыворотке и BUN, как правило, демонстрируют слабую корреляцию с гистопатологией почек и, как правило, не прогнозируют последующие изменения в почке.
Способы оценки собаки для диагностики нарушения почек вовлекают оценку уровня экспрессии генов или активности одного или нескольких из следующих генов или продуктов экспрессии (трансляции) таких генов у собак, выбранных из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); декорина (DCN); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
Способы оценки собаки для диагностики нарушения почек вовлекают оценку уровня экспрессии генов или активности одного или нескольких из следующих генов или продуктов экспрессии таких генов у собак, выбранных из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2) или матрилина-2 (Matn2); и необязательно, второй группы, состоящей из: лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
Биомаркеры, пригодные для применения этого изобретения на практике, представляют собой: лумикан (LUM); альфа 1 (III) цепь коллагена, вариант 12 (COL3A1); декорин (DCN); секретируемый связанный с frizzle белок 2 (sFRP2); матрилин-2 (Matn2); ретинол-связывающий белок 4 (rbp4); MMP-9; кластерин (CLU); трансферрин (TF); Apo-C-1 (ApoC1); и ингибин-бета A (INHBA), как более подробно описано ниже и в списке последовательностей, прилагаемом к этому описанию.
Лумикан собаки. Зонд Affymetrix CfaAFFx.10198.1.S1_s_at соответствует эталонной последовательности NCBI: XP_539716.1, регистрационный номер XP_539716, который, как предсказано, является сходным с предшественником лумикана (кератинсульфатный протеогликан лумикан [KSPG лумикан]) [Canis familiaris]. Лумикан собаки представляет собой белок с лейцин-богатым повтором из 338 аминокислот, кодируемый XM_539716.2 с GeneID:482599 [SEQ. ID. NO: 1].
Термины "лумикан", "LUM" и "Lum" обозначают белок, по существу имеющий аминокислотную последовательность, представленную в SEQ. ID. NO: 1. Предпочтительно, лумикан представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 1. Лумикан также включает белковые варианты последовательности, представленной в SEQ. ID. NO: 1, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин лумикан также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует XM_539716.2 и прилагаемой SEQ. ID. NO: 12. Лумикан также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 12 и с фрагментами SEQ. ID. NO: 12.
Коллаген альфа 1 (III), вариант 12 (COL3A1) собаки. Зонд Affymetrix CfaAffx.22804.1S1_s_at соответствует эталонной последовательности NCBI: XP_863148.1, регистрационный номер XP_863148, которая, как предсказано, является сходной с предшественником альфа (III) цепи коллагена изоформы 12. COL3A1 собаки представляет собой белок из 1446 аминокислот, кодируемый XM_863148.1 с GeneID: 478835 [SEQ. ID. NO: 2].
Термины "предшественник альфа (III) цепи коллагена изоформа 12," "Col3a1" и "COL3A1" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 2. Предпочтительно, COL3A1 представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 2. COL3A1 также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 2, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин COL3A1 также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует XM_863148.1 и прилагаемой SEQ. ID. NO: 13. COL3A1 также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 13 и к фрагментам SEQ. ID. NO: 13.
Декорин (DCN) собаки. Зонд Affymetrix Cfa.6065.1.A1_s_at соответствует эталонной последовательности NCBI: NP_001003228.1, регистрационный номер NP_001003228, декорин [Canis lupus familiaris]. Декорин собаки представляет собой белок с лейцин-богатым повтором из 360 аминокислот, кодируемый NM_001003228.1 с GeneID: 403904 [SEQ.ID. NO: 3].
Термины "декорин," "Den" и "DCN" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 3. Предпочтительно, декорин представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 3. Декорин также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 3, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин "декорин" также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует NM_001003228.1 и прилагаемой SEQ. ID. NO: 14. Декорин также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 14 и с фрагментами SEQ. ID. NO: 14.
Секретируемый связанный с frizzle белок 2 (sFRP2) собаки. Зонд Affymetrix Cfa.l200.1.S1_s_at соответствует эталонной последовательности NCBI: NP_001002987.1, регистрационный номер NP_001002987 XP_532695, секретируемый связанный с frizzle белок 2 (sFRP2) [Canis lupus familiaris]. Секретируемый связанный с frizzle белок 2 (sFRP2) собаки представляет собой белок из 294 аминокислот, кодируемый NM_001002987.1 с GeneID: 475471 [SEQ.ID. NO: 4].
Термины "секретируемый связанный с frizzle белок 2", "SFRP2" и "sFRP2" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 4. Предпочтительно, sFRP2 представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 4. sFRP2 также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 4, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин "sFRP2" также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует NM_001002987.1 и прилагаемой SEQ. ID. NO: 15. sFRP2 также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 15 и с фрагментами SEQ. ID. NO: 15.
Матрилин-2 (Matn2) собаки. Зонд Affymetrix Cfa.9487.1A1_at соответствует эталонной последовательности NCBI: XP_5485552.2, регистрационный номер NP_5485552, сходный с предшественником матрилином 2 изоформы a [Canis lupus familiaris]. Матрилин-2 собаки представляет собой белок из 978 аминокислот, кодируемый XM_5485552.2, с GeneID: 491431 [SEQ.ID. NO: 5].
Термины "предшественник матрилина-2 изоформы a", "матрилин-2" и "Matn2" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 5. Предпочтительно, Matn2 представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 5. Matn2 также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 5, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин Matn2 также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует XM_5485552.2 и прилагаемой SEQ. ID. NO: 16. Matn2 также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 16 и с фрагментами SEQ. ID. NO: 16.
Ретинол-связывающий белок 4 (rbp4) собаки. Зонд Affymetrix Cfa.15489.1.S1_at соответствует эталонной последовательности NCBI: XP_534969.2, регистрационный номер NP_534969, сходный с плазматическим предшественником ретинол-связывающего белка 4, (rbp4) [Canis lupus familiaris]. Ретинол-связывающий белок 4 (rbp4) собаки представляет собой белок из 267 аминокислот, кодируемый XM_534969.2, с GeneID: 477775 [SEQ.ID. NO: 6].
Термины "ретинол-связывающий белок 4", "плазматический предшественник", "ретинол" и "Rbp4" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 6. Предпочтительно, Rbp4 представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 6. Rbp4 также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 6, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин Rbp4 также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует XM_534969.2 и прилагаемой SEQ. ID. NO: 17. Rbp4 также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 17, и к фрагментам SEQ. ID. NO: 17.
Матриксная металлопротеиназа 9 (MMP-9) собак. Зонд Affymetrix Cfa.3470.1S1_at соответствует эталонной последовательности NCBI: NP_001003219.1, регистрационный номер NP_001003219, матриксная металлопротеиназа 9 [Canis lupus familiaris]. Матриксная металлопротеиназа 9 (MMP9) собак представляет собой белок из 704 аминокислот, кодируемый NM_001003219.1, с GeneID: 403885 [SEQ.ID. NO: 7].
Термины "матриксная металлопротеиназа 9" и "MMP9" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 7. Предпочтительно, MMP9 представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 7. MMP9 также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 7, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин MMP9 также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует NM_001003219.1 и прилагаемой SEQ. ID. NO: 18. MMP9 также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 18, и к фрагментам SEQ. ID. NO: 18.
Кластерин (CLU) собаки. Зонд Affymetrix Cfa1254.S1_s_at соответствует эталонной последовательности NCBI: NM_001003370.1, регистрационный номер NM_001003370, кластерин собаки. Кластерин собаки представляет собой белок из 445 аминокислот, кодируемый NM_001003370.1, с GeneID: 442971 [SEQ.ID. NO: 8].
Термины "кластерин" и "Clu" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 8. Предпочтительно, кластерин представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 8. Кластерин также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 8, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин "кластерин" также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует NM_001003370.1 и прилагаемой SEQ. ID. NO: 19 Кластерин также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 19, и к фрагментам SEQ. ID. NO: 19.
Трансферрин (TF) собаки. Зонд Affymetrix Cfa2217.1.A1_at соответствует эталонной последовательности NCBI: XP_534268.2, регистрационный номер XP_534268, сходной с предшественником серотрансферрина собаки (трансферрин) изоформы 1. Трансферрин собаки представляет собой белок из 705 аминокислот, кодируемый XM_534268.2, с GeneID: 477072 [SEQ.ID. NO: 9].
Термины "предшественник серотрансферрина собаки (трансферрин) изоформы 1", "трансферрин" и "TF" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 9. Предпочтительно, трансферрин представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 9. Трансферрин также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 9, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин "трансферрин" также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует XM_534268.2 и прилагаемой SEQ. ID. NO: 20 Трансферрин также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 20 и к фрагментам SEQ. ID. NO: 20.
Аполипопротеин C-1 (ApoC1) собаки. Зонд Affymetrix Cfa1254.S1_s_at соответствует эталонной последовательности NCBI: XP 533643.2, регистрационный номер XP_533643, сходной с предшественником аполипопротеина C-1 (ApoC1) собаки. Аполипопротеин C-1 (ApoC1) собаки представляет собой белок из 88 аминокислот, кодируемый NM_533643.2, с GeneID: 113459 [SEQ.ID. NO: 10].
Термины "аполипопротеин C-1" и "ApoC1" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 10. Предпочтительно, трансферрин представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 10. ApoC1 также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 10, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин "ApoC1" также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует NM_533643.2 и прилагаемой SEQ. ID. NO: 21 ApoC1 также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 21, и к фрагментам SEQ. ID. NO: 21.
Ингибин-бета A (INHBA). Зонд Affymetrix Cfa596.1A1_at соответствует эталонной последовательности NCBI: XP_540364, регистрационный номер XP_540364, сходный с предшественником A-цепи ингибина-бета (INHBA) (A-цепь активина-бета) (белок эритроидной дифференцировки; EDF). Предшественник A-цепи ингибина-бета (INHBA) собаки представляет собой белок из 424 аминокислот, кодируемый XM_540364.2, с GeneID: 483245 [SEQ.ID. NO: 11].
Термины "предшественник A-цепи ингибина-бета" и "INHBA" обозначают белок, по существу имеющий аминокислотную последовательность, как представлено в SEQ. ID. NO: 11. Предпочтительно, ингибин представляет собой белок, по существу состоящий из аминокислотной последовательности, как представлено в SEQ. ID. NO: 11. Ингибин также включает варианты белка с последовательностью, представленной в SEQ. ID. NO: 11, такие как аллельные варианты и другие мутации, такие как замены, вставки и/или делеции. Термин ингибин также относится к последовательности нуклеиновой кислоты, кодирующей белок. Последовательность соответствует XM_540364.2 и прилагаемой SEQ. ID. NO: 22. Трансферрин также относится к последовательностям нуклеиновых кислот, которые гибридизуются с SEQ. ID. NO: 22, и к фрагментам SEQ. ID. NO: 22.
В предпочтительном варианте осуществления настоящего изобретения, способ диагностики нарушения почек у собак включает стадии: (a) измерения уровня экспрессии по меньшей мере одного биомаркера в биологическом образце собаки, где по меньшей мере один биомаркер выбран из секретируемого связанного с frizzle белка 2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA); и (b) идентификации собаки как имеющей нарушение почек, где отличия в экспрессии одного или нескольких биомаркеров в образце относительно контрольной величины экспрессии в образце от нормального животного указывают на существование нарушения почек.
В другом предпочтительном варианте осуществления настоящего изобретения собака имеет нормальную функцию почки при определении с помощью общепринятых клинических показателей, например скорости гломерулярной фильтрации, выведения креатинина, уровней белка в моче, уровней креатинина в крови, уровней креатинина в моче и/или уровней азота мочевины в крови, и способы по изобретению можно использовать для детекции и диагностики у такой собаки изменения нормального состояния в ненормальное состояние, приводящее к нарушению почек, характеризующемуся сниженной функцией почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации и гломерулонефритом.
В другом предпочтительном варианте осуществления повышенный уровень активности или экспрессии одного или нескольких генов у собак, выбранных из группы, состоящей из: лумикана (LUM); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); декорина (DCN); секретируемого связанного с frizzle белка 2 (sFRP2); и матрилина-2 (Matn2), коррелирует с нарушением почек, характеризующимся аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом. Уровень активности или экспрессии одного или нескольких генов можно определять путем изменения продукта экспрессии таких генов, который может представлять собой полинуклеотид, или полипептид, или белок, как правило, транскрипт РНК или его продукт трансляции.
В другом предпочтительном варианте осуществления дифференциальная экспрессия одного или нескольких генов у собак, выбранных из по меньшей мере одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA), коррелирует с аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом.
В другом предпочтительном варианте осуществления дифференциальная экспрессия одного или нескольких генов у собак, выбранных из первой группы по меньшей мере из одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2) или матрилина-2 (Matn2); и необязательно, второй группы из по меньшей мере одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA) коррелирует с аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом. Следует понимать, что настоящее изобретение предусматривает комбинацию биомаркеров, включающих гены и их продукты экспрессии, которые (i) выбраны из первой группы по меньшей мере из одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2) или матрилина-2 (Matn2); и необязательно, второй группы по меньшей мере из одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA); а также (ii) выбраны из первой группы из по меньшей мере одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2) или матрилина-2 (Matn2); и второй группы по меньшей мере из одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA). Варианты осуществления изобретения предусматривают конструирование панелей биомаркеров из различных комбинацией двух групп генов и их продуктов экспрессии.
В другом предпочтительном вариант осуществления изобретение относится к измерению и коррелированию дифференциальной экспрессии у собак одного или нескольких генов, выбранных из по меньшей мере одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA), с ускоренной или ранней утратой функцией почек у собак, на что указывает аномальный процесс, приводящий к нарушению почек, характеризующемуся сниженной функцией почек, сниженной скоростью гломерулярной фильтрации, гломерулонефритом или почечной недостаточностью.
В одном аспекте изобретение включает контактирование образца ткани или образца жидкости организма с агентом, который осуществляет детекцию у собак одного или нескольких генов или продуктов экспрессии таких одного или нескольких генов, выбранных по меньшей мере из одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA). Средство может представлять собой антитело или зонд на основе нуклеиновой кислоты, используемые с общепринятыми средствами анализа, такими как иммобилизация на твердой фазе, лунки микропланшетов для титрования, пробирки, измерители уровня жидкостей или другие общепринятые средства.
Другой вариант осуществления способа по изобретению охватывает применение общепринятых средств для анализа в целях определения экспрессии генов у собак либо отдельно, либо с данными чипов, для определения экспрессии генов с использованием полипептидов и/или полинуклеотидов, таких как общепринятые средства анализа, включающие один или несколько из ELISA, RIA, иммуноблоттинга, гибридизации in situ, нозерн-блоттинга, вестерн-блоттинга и анализа Luminex X-Map®.
Другой вариант осуществления изобретения охватывает диагностику нарушения почек, характеризующегося аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, с течением времени путем определения профилей экспрессии генов для одного или нескольких генов или продуктов их экспрессии, выбранных из по меньшей мере одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA) совместно с одним или несколькими общепринятыми диагностическими показателями, выбранными из группы, состоящей из: определения уровней альбумина, сывороточного цистатина C, креатинина в крови, креатинина в моче, выведения креатинина, белка в моче, азота мочевины в крови и скорости гломерулярной фильтрации, для выбора курса лечения для такой собаки.
В другом варианте осуществления изобретение относится к набору для диагностики и/или мониторинга нарушения почек у собак с течением времени, причем набор содержит одно или несколько средств, способных осуществлять детекции профилей одного или нескольких генов или их продуктов экспрессии, выбранных по меньшей мере из одного РНК-транскрипта или его продукта трансляции выбранный из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA), и инструкции по применению одного или нескольких средств для оценки риска развития у такой собаки нарушения почек, характеризующегося аномальной утратой функции почек, почечной недостаточностью, сниженной скоростью гломерулярной фильтрации или гломерулонефритом, с течением времени.
В другом аспекте изобретение включает контактирование образца ткани или образца жидкости организма со средством, которое осуществляет детекцию одного или нескольких генов или их продуктов экспрессии, выбранных по меньшей мере из одного РНК-транскрипта или его продукта трансляции, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (IHBA). Средство может представлять собой антитело или зонд нуклеиновой кислоты, используемый совестно с общепринятыми средствами для анализа, такими как иммобилизация на твердой фазе, лунки микропланшета для титрования, пробирки, измерители уровней жидкости или другие общепринятые средства.
Особенно предпочтительные варианты осуществления настоящего изобретения представлены ниже. В каждом из следующих вариантов осуществления настоящее изобретение предусматривает тестируемый образец, содержащий либо образцы солидной ткани почки, либо образцы биологических жидкостей от собаки. Дифференциальная экспрессия указанных генов предусматривает значимые отличия в абсолютных значениях. В предпочтительных вариантах осуществления дифференциальная экспрессия может быть более, чем приблизительно 1,1-, 1,2-, 1,3-, 1,4-, 1,5-, 1,6-, 1,7-, 1,8-, 1,9-, 2,0-, 2,1-, 2,2-, 2,3-, 2,4-, 2,5- или 3,0-кратной или более. Особенно предпочтительные величины дифференциальной экспрессии являются более, чем 2-кратными или в пределах одного стандартного отклонения от среднего значения. Также в вариантах осуществления изобретения может использоваться множество известных в данной области средств для детекции, включая чип с одним или несколькими гибридизационными зондами, панели с одним или несколькими антителами и комбинации этих технологий. Когда являются желательными иммуноанализы, квалифицированный специалист может выбрать их среди многих известных в данной области способов, включая иммуноанализы, выбранные из группы, состоящей из конкурентного анализа связывания, неконкурентного анализа связывания, радиоиммунного анализа, твердофазного иммуноферментного анализа (ELISA), сэндвич-анализа, реакции преципитации, анализа иммунодиффузии в геле, анализа агглютинации, флуоресцентного иммуноанализа, хемилюминесцентного иммуноанализа, иммуноанализа иммуно-ПЦР, иммуноанализа с белком A или белком G и анализа способом иммуноэлектрофореза. Когда указаны общепринятые диагностические показатели, они могут быть выбраны из группы, состоящей из: определения уровней альбумина, сывороточного цистатина C, креатинина в крови, креатинина в моче, выведения креатинина, белка в моче, азота мочевины в крови и скорости гломерулярной фильтрации.
Кроме того, способы и композиции по изобретению предусматривают использование по меньшей мере одного РНК-транскрипта или его продукта трансляции, который может представлять собой измененную форму гена или его продукта трансляции.
Следующий вариант осуществления изобретения включает способ диагностики нарушения почек у собак, включающий стадии: (a) измерения уровня экспрессии по меньшей мере одного биомаркера в биологическом образце от собаки, где по меньшей мере один биомаркер выбран по меньшей мере из одного гена или продукта трансляции такого гена, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA); и (b) идентификации собаки как имеющей нарушение почек, где отличия в экспрессии одного или нескольких биомаркеров в образце относительно контрольной величины для экспрессии в образце от нормального животного указывает на существование нарушения почек.
Другой вариант осуществления включает набор для диагностики, прогнозирования или мониторинга нарушения почек у собак, включающий по меньшей мере одно или несколько средств, способных осуществлять детекцию по меньшей мере одного или нескольких РНК-транскриптов или их продуктов трансляции, выбранных из первой группы по меньшей мере из одного гена или продукта трансляции такого гена, выбранного из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM), декорина (DCN), альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA); и инструкции по применению такого по меньшей мере одного или нескольких средств для измерения экспрессии одного или нескольких биомаркеров и для диагностики заболевания почек у такой собаки.
В следующем аспекте изобретение относится к композициям, содержащим один или несколько зондов на основе нуклеиновой кислоты, которые специфично гибридизуются с нуклеиновой кислотой, или ее фрагментом, кодирующим биомаркер по настоящему изобретению, выбранный из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
В дополнительном аспекте изобретение относится к композициям, содержащим антитела, которые специфично связываются с полипептидом, кодируемым геном, экспрессирующим биомаркер по настоящему изобретению, выбранный из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
Кроме того, в настоящем документе предусматривается, что способы по настоящему изобретению можно использовать в комбинации с традиционными способами диагностики, которые способны осуществлять детекцию физических или морфологических характеристик нарушений почек. Таким образом, например, охарактеризацию дифференциальной экспрессии генов для почки в клетках, полученных из образцов тканей или образцов жидкостей организма собаки, можно комбинировать с общепринятыми диагностическими (например, радиологическими) способами для подтверждения диагноза нарушения почек у собак, включая, например, гломерулонефрит.
Также изобретение относится к наборам для диагностики аномального нарушения почек у собак, содержащим компоненты, которые можно использовать для детекции экспрессии биомаркеров по настоящему изобретению, включая, но не ограничиваясь ими, композиции и микрочипы, описанные в настоящем описании.
Следующим аспектом изобретения является способ диагностики и/или прогнозирования нарушения почек у собак, где способ включает стадии: получения по меньшей мере одного образца ткани или образца жидкости организма от животного; определения количества одного или нескольких биомаркеров, выбранных из таблицы 3, в указанном по меньшей мере одном образце или образце, полученном от животного, где указанным биомаркером является полипептид, белок, РНК, ДНК, полинуклеотид или их метаболит.
Другой вариант осуществления изобретения представляет собой набор для диагностики и/или прогнозирования нарушения почек у собак, в частности для осуществления способа диагностики и/или прогнозирования гломерулонефрита у собак, где способ включает стадии: получения по меньшей мере одного образца ткани или образца жидкости организма от животного; определения количества одного или нескольких биомаркеров, выбранных из таблицы 3, в указанном по меньшей мере одном образце или образце, полученном от животного, где указанным биомаркером является полипептид, белок, РНК, ДНК, полинуклеотид или их метаболит, и, необязательно, дополнительно содержащим поддающийся детекции агент, связанный с указанным биомаркером.
Следующим вариантом осуществления изобретения является реагент для диагностики и/или прогнозирования гломерулонефрита у собак, в частности для осуществления способа диагностики и/или прогнозирования гломерулонефрита у собак, где способ включает стадии: получения по меньшей мере одного образца ткани или образца жидкости организма от животного; определения количества одного или нескольких биомаркеров, выбранных из таблицы 3, в указанном по меньшей мере одном образце или образце жидкости, полученном от собаки, где указанный биомаркер представляет собой полипептид, белок, РНК, ДНК, полинуклеотид или их метаболит, и, необязательно, дополнительно содержащем поддающийся детекции агент, связанный с указанным биомаркером.
Следующим аспектом изобретения является способ диагностики и/или прогнозирования нарушения почек у собак, где способ включает стадии: получения по меньшей мере одного образца ткани или образца жидкости организма от животного; определения количества одного или нескольких биомаркеров, выбранных из таблиц 3 и 4, в указанном по меньшей мере одном образце или образце жидкости, полученном от животного, где указанный маркер представляет собой полипептид, белок, РНК, ДНК, полинуклеотид или его метаболит.
Другой вариант осуществления изобретения представляет собой применение одного или нескольких полипептидов, белков, РНК, ДНК, полинуклеотидов или их метаболитов, выбранных из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA) в качестве биомаркера для диагностики и/или прогнозирования нарушения почек, в частности для получения набора для диагностики или прогнозирования нарушения почек у собак.
Другой вариант осуществления изобретения представляет собой применение одного или нескольких полипептидов, белков, РНК, ДНК, полинуклеотидов или их метаболитов, выбранных из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C- 1 (ApoC1); и ингибина бета A (INHBA) в качестве биомаркера для диагностсики и/или прогнозирования нарушения почек, в частности для получения набора для диагностики или прогнозирования нарушения почек у собак.
Другой вариант осуществления представляет собой такой набор, где реагенты и оборудование включают материалы для анализа ДНК-микрочипов, включая олигонуклеотидный микрочип, кДНК-микрочип и сфокусированный генный чип, или их комбинацию.
Другой вариант осуществления изобретения представляет собой способ оценки прогрессирования курса лечебного питания для собаки, страдающей нарушением почек, причем способ включает (a) измерение первого уровня одного или нескольких биомаркерных полипептидов, белков, РНК, ДНК, полинуклеотидов или их метаболитов, выбранных из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA), в образце ткани или образце жидкости организма от такой собаки в первый момент времени в ходе лечения, (b) измерение второго уровня указанного биомаркера в указанном образце или образце жидкости от указанной собаки во второй момент времени в ходе лечения и (c) сравнение показателей биомаркера в указанный первый момент времени и указанный второй момент времени; где экспрессия генов является по меньшей мере приблизительно 1,0-, 1,1-, 1,2-, 1,3-, 1,4-, 1,5-, 1,6-, 1,7-, 1,8-, 1,9-, 2,0-, 2,5- или 3,0-кратно дифференциальной или имеет большее отличие в экспрессии гена по сравнению с экспрессией в клетке контрольного животного.
Другой вариант осуществления изобретения представляет собой способ идентификации множества генов, которые дифференциально экспрессируются между образцами тканей и образцами жидкостей организма для применения в информативном чипе, включающий: предоставление первого набора гетерогенных зондов на основе нуклеиновых кислот, полученных из первого образца ткани; предоставление набора гетерогенных зондов нуклеиновых кислот, полученных из второго образца ткани; гибридизацию чипа нуклеиновых кислот, содержащего множество последовательностей, происходящих из генов биологического процесса, с первым набором зондов и определение первого уровня экспрессии последовательностей на чипе; гибридизацию чипа с указанным вторым набором зондов и определение второго уровня экспрессии для последовательностей чипа; идентификацию множества генов, которые дифференциально экспрессируются в указанном биологическом процессе путем сравнения первого уровня экспрессии с указанным вторым уровнем экспрессии для гибридизованных последовательностей; и ранжирование идентифицированных генов с помощью стадии, выбранной из группы стадий, состоящей из: определения абсолютной величины отличий между первым уровнем экспрессии и вторым уровнем экспрессии и ранжирования генов, имеющих более высокие отличия относительно генов, имеющих более низкие отличия; и определения стандартного отклонения для отличий между первым уровнем экспрессии и вторым уровнем экспрессии и ранжирования генов, имеющих более высокое стандартное отклонение, относительно генов, имеющих более низкое стандартное отклонение, где гены выбраны из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
Другой вариант осуществления изобретения относится к способу преобразования чипа с нуклеиновыми кислотами в информативный чип, включающий: предоставление первого набора гетерогенных зондов на основе нуклеиновой кислоты, полученных из первого образца ткани; предоставление отличающегося второго набора гетерогенных зондов на основе нуклеиновой кислоты, полученных из второго образца ткани; гибридизацию чипа с нуклеиновыми кислотами, содержащего множество последовательностей, с первым набором зондов и определение первого уровня экспрессии для последовательностей на чипе; гибридизацию чипа с указанным вторым набором зондов и определение второго уровня экспрессии для последовательностей на чипе; идентификацию множества генов, которые дифференциально экспрессируются в указанном биологическом процессе, исходя из отличий между указанным первым уровнем экспрессии и вторым уровнем экспрессии для идентифицированных генов, с помощью стадии, выбранной из группы стадий, состоящей из: определения абсолютной величины отличий между первым уровнем экспрессии и вторым уровнем экспрессии и ранжирования генов, имеющих более высокие отличия относительно генов, имеющих более низкие отличия; и определения стандартного отклонения для отличий между первым уровнем экспрессии и вторым уровнем экспрессии и ранжирования генов, имеющих более высокое стандартное отклонение, относительно генов, имеющих более низкое стандартное отклонение; и выбор генов из множества идентифицированных дифференциально экспрессируемых генов для включения в информативный чип, где указанные гены выбраны из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2); матрилина-2 (Matn2); лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
Другой вариант осуществления изобретения представляет собой способ определения эффективности лечения нарушения почек, включающий стадии: (a) представления биологического образца от собаки, страдающей нарушением почек, которую подвергали указанному лечению, (b) определение уровня в указанном образце одного или нескольких биомаркеров гломерулонефрита для получения профиля экспрессии для указанной собаки, и (c) сравнение указанного профиля экспрессии c: i) сравнимым профилем экспрессии, полученным для указанной тестируемой собаки до начала указанного лечения, и/или ii) сравнимым профилем экспрессии, полученным для указанной тестируемой собаки на более ранней стадии лечения, и/или iii) сравнимым профилем экспрессии, характерным для индивидуума, который не страдает нарушением почек, где один или несколько биомаркеров нарушения почек включают продукты экспрессии одного или нескольких генов, выбранных из группы, состоящей из: секретируемого связанного с frizzle белка-2 (SFRP2) и матрилина-2 (Matn2); и, необязательно, одного или нескольких генов, выбранных из группы, состоящей из: лумикана (LUM); декорина (DCN); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); ретинол-связывающего белка 4 (rbp4); матриксной металлопротеиназы 9 (MMP9); кластерина (CLU); трансферрина (TF); Apo-C-1 (ApoC1); и ингибина-бета A (INHBA).
Другие и дополнительные задачи, признаки и преимущества настоящего изобретения будут хорошо понятны специалистам в данной области.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как используют в рамках изобретения, ненормальная собака представляет собой собаку, которая имеет риск развития, предрасположенность к или аномальную утрату функции почек, почечную недостаточность, сниженную скорость гломерулярной фильтрации или гломерулонефрит, где ненормальность поддается детекции с использованием по меньшей мере одного характерного биомаркера, выбранного из биологического образца, взятого от такой собаки, и измеренного в нем.
На протяжении этого описания различные аспекты этого изобретения могут быть представлены в формате диапазона. Следует понимать, что описание в диапазоне формата представлено только для удобства и краткости, и его не следует истолковывать как жесткое ограничение объема изобретения. Таким образом, описание диапазона следует рассматривать как конкретное описание всех возможных поддиапазонов, а также всех отдельных числовых величин в этом диапазоне. Например, описание диапазона, такого как от 1 до 5, следует рассматривать как конкретно описанные поддиапазоны, такие как от 1 до 3, от 1 до 4, от 2 до 4, от 2 до 5, от 3 до 5 и т.д., а также отдельные числа в этом диапазоне, например 1, 2, 3, 4 и 5. Это применимо, независимо от ширины диапазона.
На практике этого изобретения могут использоваться, если нет иных указаний, общепринятые способы и описания органической химии, технологии полимеров, молекулярной биологии (включая рекомбинантные способы), клеточной биологии, биохимии и иммунологии, которые находятся в пределах квалификации в данной области. Такие общепринятые способы включают синтез полимерных чипов, гибридизацию, лигирование и детекцию гибридизации с использованием метки.
Также настоящее изобретение предусматривает множество применений для полимеров, связанных с твердыми подложками. Эти применения включают мониторинг экспрессии генов, определение профилей, скрининг библиотек, генотипирование и диагностику.
Специалистам в данной области будет понятно, что продукты и способы, осуществленные в настоящем изобретении, можно применять для различных систем, включая коммерчески доступные системы для мониторинга экспрессии генов, включающие чипы с зондами на основе нуклеиновых кислот, мембранные блоты, лунки микропланшетов, гранулы и пробирки для образцов, изготовленные с помощью различных материалов с использованием различных способов, известных в данной области. Таким образом, настоящее изобретение не ограничивается какими-либо конкретными условиями, и представленное ниже описание конкретных вариантов осуществления настоящего изобретения представлено только для иллюстративных целей.
Система мониторинга экспрессии генов, в предпочтительном варианте осуществления, может включать чип с зондами на основе нуклеиновой кислоты (включая олигонуклеотидный чип, кДНК-чип, точечный чип и т.п.), мембранный блот (такой как используется в анализе гибридизации, таком как нозерн-блоттинг, саузерн-блоттинг, дот-блоттинг и т.п.), или лунки микропланшетов для титрования, пробирки для образца, гранулы или волокна (или любая твердая подложка, содержащая связанные с ней нуклеиновые кислоты). Система мониторинга экспрессии генов также может включать зонды нуклеиновых кислот в растворе.
Настоящее изобретение также предусматривает получение образца, вовлекающее амплификацию. Геномный образец можно амплифицировать с помощью различных механизмов, в некоторых из которых может использоваться ПЦР. Образец можно амплифицировать на чипе.
Другие пригодные способы амплификации включают лигазную цепную реакцию (LCR) (например, Wu and Wallace, Genomics 4, 560 (1989), Landegren et al, Science 241, 1077 (1988) и Barringer et al. Gene 89:1 17 (1990)), транскрипционную амплификацию (Kwoh et al., Proc. Natl. Acad. Sci. USA 86, 1173 (1989) и WO88/10315), самоподдерживающуюся репликацию последовательности (Guatelli et al., Proc. Nat. Acad. Sci. USA, 87, 1874 (1990) и WO90/06995), селективную амплификацию последовательностей полинуклеотидов-мишеней (патент США № 6410276), полимеразную цепную реакцию с затравкой в виде консенсусной последовательности (CP-ПЦР) (патент США № 4437975), полимеразную цепную реакцию с произвольной затравкой (AP-ПЦР) (патенты США № 5413909, 5861245) и амплификацию на основе нуклеиновой кислоты (NABSA).
Систему мониторинга в соответствии с настоящим изобретением можно использовать для упрощения сравнительного анализа экспрессии в различных клетках или тканях, различных субпопуляциях одних и тех же клеток или тканей, различных физиологических состояний одних и тех же клеток или тканей, различных стадий развития одних и тех же клеток или тканей, или различных популяций клеток одной и той же ткани. В предпочтительном варианте осуществления способы пропорциональной амплификации по настоящему изобретению могут обеспечивать воспроизводимые результаты (т.е. в статистически значимых пределах ошибки или степени доверительности), достаточные для упрощения измерения количественных, а также качественных отличий в протестированных образцах.
Термин "антитело" означает любой иммуноглобулин, который связывается со специфическим антигеном, включая антитела IgG, IgM, IgA, IgD и IgE. Термин включает поликлональные, моноклональные, одновалентные, гуманизированные, гетероконъюгатные антитела, композиции антител с полиэпитопной специфичностью, химерные, биспецифические антитела, диантитела, одноцепочечные антитела и фрагменты антител, такие как Fab, Fab', F(ab')2 и Fv, или другие антигенсвязывающие фрагменты.
Термин "чип" означает упорядоченное расположение по меньшей мере двух зондов на субстрате. По меньшей мере один из зондов является контрольным или стандартным, и по меньшей мере один из зондов представляет собой диагностический зонд. Расположение от приблизительно двух до приблизительно 40000 зондов на субстрате обеспечивает, чтобы размер и интенсивность сигнала для каждого меченого комплекса, образованного между зондом и полинуклеотидом или полипептидом образца, был индивидуально отличимым. Коллекцию молекул, нанесенных на чип, можно получать либо синтетическими, либо биосинтетическими путями. Чип может иметь различные формы, включая библиотеки растворимых молекул, библиотеки соединений, связанных с резиновыми гранулами, чипы на основе кремнизема или другие твердые положки. Чип с нуклеиновыми кислотами может включать библиотеки нуклеиновых кислот, которые можно получать нанесением точками нуклеиновых кислот по существу любой длины (например, от 1 до приблизительно 1000 нуклеотидов в длину) на субстрат. Чип с зондами на основе нуклеиновых кислот предпочтительно содержит нуклеиновые кислоты, связанные с субстратом, в известных областях. В других вариантах осуществления система может включать твердую подложку или субстрат, такие как мембрана, фильтр, предметное стекло для микроскопа, лунка микропланшета, пробирка для образца, гранула, чип с гранулами или сходные с ними. Твердую подложку можно получать из различных материалов, включая бумагу, целлюлозу, нейлон, полистирол, поликарбонат, пластмассу, стекло, керамику, нержавеющую сталь или сходные с ними. Твердая подложка предпочтительно может иметь жесткую или полужесткую поверхность, и предпочтительно она может быть сферической (например, гранулы) или по существу плоской (например, плоская поверхность) с подходящими лунками, приподнятыми областями, вытравленными углублениями или сходными с ними. Твердая подложка также может включать гель или матрицу, в которые нуклеиновые кислоты могут быть погружены.
Термин "биомаркер" относится к генам и продуктам генов, кодируемым геном по изобретению, т.е. где определено, что ген дифференциально регулируется в результате нарушения почек. Кроме того, термин можно широко использовать для обозначения любой части такого гена или белка, которая может идентифицировать или коррелировать с полноразмерным геном или белком, например, в анализе или другом способе по изобретению.
Экспрессию биомаркеров также можно идентифицировать путем детекции трансляции биомаркера (т.е. детекции биомаркерного белка в образце). Способы, пригодные для детекции биомаркерного белка, включают любой пригодный способ детекции и/или измерения белков из клетки или клеточного экстракта. Такие способы включают, но не ограничиваются ими, иммуноблоттинг (например, вестерн-блоттинг), твердофазный иммуноферментный анализ (ELISA), радиоиммунный анализ (RIA), иммунопреципитацию, иммуногистохимию и иммунофлуоресценцию. Особенно предпочтительные способы детекции белков включают любой анализ отдельных клеток, включая иммуногистохимию и иммунофлуоресцентные анализы. Такие способы хорошо известны в данной области. Более того, антитела против определенных биомаркеров, описанных в настоящем описании, известны в данной области и описаны в общедоступной литературе, и способы их получения хорошо известны квалифицированному специалисту.
Термин "дифференциальная экспрессия" или "дифференциально экспрессируемый" означает увеличенную или активированную экспрессию генов или означает сниженную или ингибированную экспрессию генов, что выявляют по отсутствию, присутствию или по меньшей мере двукратному, или по меньшей мере 2,0-, 1,9-, 1,8-, 1,7-, 1,6-, 1,5-, 1,4-, 1,3-, 1,2-, 1,1- или 1,0-кратному изменению количества транскрибированной матричной РНК или транслированного белка в образце.
Термин "кратный", при использовании в качестве меры дифференциальной экспрессии генов, означает величину экспрессии гена у собаки, т.е. многократную или дробную величину экспрессии генов по сравнению с контрольной величиной экспрессии генов. Например, ген, который экспрессируется в 2 раза больше у животного по сравнению с контрольной величиной, имеет 2-кратную дифференциальную экспрессию генов, и ген, который экспрессируется у животного на уровне одной трети по сравнению с контрольной величиной, также имеет 2-кратную дифференциальную экспрессию гена.
Термин "фрагмент" означает (1) олигонуклеотидную или полинуклеотидную последовательность, которая является частью полной последовательности и которая имеет ту же или сходную активность для конкретного применения, что и полная полинуклеотидная последовательность, или (2) пептидную или полипептидную последовательность, которая является частью полной последовательности и которая имеет ту же или сходную активность для конкретного применения, что и полная полипептидная последовательность. Такие фрагменты могут включать любое число нуклеотидов или аминокислот, считающихся пригодными для конкретного применения. Как правило, олигонуклеотидные или полинуклеотидные фрагменты содержат по меньшей мере приблизительно 10, 50, 100 или 1000 нуклеотидов, и полипептидные фрагменты содержат по меньшей мере приблизительно 4, 10, 20 или 50 последовательно расположенных аминокислот из полной последовательности. Термин охватывает полинуклеотидные и полипептидные варианты фрагментов. Полинуклеотид, например, может быть разрушен или фрагментирован на множество сегментов.
Различные способы фрагментирования нуклеиновых кислот хорошо известны в данной области. Эти способы могут быть, например, либо химическими, либо физическими. Химическая фрагментация может включать частичную деградацию ДНКазой; частичную дупуринизацию кислотой; применение ферментов рестрикции; кодируемые интроном эндонуклеазы; основанные на ДНК способы расщепления, такие как способы образования триплекса и гибрида, которые основаны на специфической гибридизации сегмента нуклеиновой кислоты для локализации расщепляющего агента в конкретной области молекулы нуклеиновой кислоты; или другие ферменты или соединения, которые расщепляют ДНК в известной или неизвестной областях. Физические способы фрагментации могут вовлекать воздействие на ДНК высоких сдвиговых усилий. Высокие сдвиговые усилия могут быть обеспечены, например, путем продвижения ДНК через камеру или канал с углублениями или выступами, или пропускания образца ДНК через проточный канал ограниченного размера, например отверстие, имеющее поперечный размер микронного или субмикронного порядка. Другие физические способы включают обработку ультразвуком и распыление. Аналогично можно использовать комбинации физической и химической фрагментации, такие как фрагментация нагреванием и опосредуемый ионами гидролиз. Эти способы можно оптимизировать для расщепления нуклеиновой кислоты на фрагменты выбранного диапазона размеров. Пригодные диапазоны размеров могут составлять от 100, 200, 400, 700 или 1000 до 500, 800, 1500, 2000, 4000 или 10000 пар оснований. Однако также могут быть пригодные более высокие диапазоны размеров, такие как от 4000, 10000 или 20000 до 10000, 20000 или 500000 пар оснований.
Термин "ген" или "гены" означает полный или неполный сегмент ДНК, вовлеченный в продуцирование полипептида, включая области, предшествующие и следующие после кодирующей области (лидерные и концевые) и встроенные последовательности (интроны) между отдельными кодирующими сегментами (экзонами). Термин охватывает любую последовательность ДНК, которая гибридизуется с последовательностью, комплементарной для кодирующих гены последовательностей.
Термин "гомолог" означает (1) полинуклеотид, включающий полинуклеотиды из того же или другого вида животных, имеющие более чем 30%, 50%, 70%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% сходство последовательности с полинуклеотидом и имеющие те же или по существу те же свойства и выполняющие ту же или по существу ту же функцию, что и полный полинуклеотид, или обладающие способностью специфично гибридизоваться с полинуклеотидом в строгих условиях, или (2) полипептид, включающий полипептиды из того же или отличающегося вида животных, имеющие более чем 30%, 50%, 70%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% сходство последовательности с полипептидом, идентифицированным по экспрессии полинуклеотидов, и имеющие те же или по существу те же свойства, выполняющие ту же или по существу ту же функцию, что и полный полипептид, или обладающие способностью специфично связываться с полипептидом, идентифицированным по экспрессии полинуклеотидов. Сходство последовательностей для двух полипептидных последовательностей или двух полинуклеотидных последовательностей определяют с использованием способов, известных квалифицированным специалистам, например алгоритма Karlin and Altschul (Proc. Natl. Acad. Sci. USA 87:2264-2268 (1990)). Такой алгоритм включен в программы NBLAST и XBLAST Altschul et al. (J. Mol. Biol. 215:403-410 (1990)). Для проведения выравниваний с пропусками для целей сравнения можно использовать Gapped Blast, как описано в Altschul et al. (Nucl. Acids Res. 25: 3389-3402 (1997)). При использовании программ BLAST и Gapped BLAST используют параметры по умолчанию и соответствующие программы (например, XBLAST и NBLAST). См. http://www.ncbi.nlm.nih.gov.
Термин "гибридизация" относится к процессу, при котором два одноцепочечных полинуклеотида нековалентно связываются с образованием стабильного двухцепочечного полинуклеотида. Термин "гибридизация" также может относиться к трехцепочечной гибридизации. Полученный (обычно) двухцепочечный полинуклеотид представляет собой "гибрид". Долю совокупности полинуклеотидов, которые образуют стабильные связи, называют в настоящем описании "степенью гибридизации".
Реакции гибридизации можно проводить в форматах абсолютной или дифференциальной гибридизации. В формате абсолютной гибридизации полинуклеотиды, происходящие из одного образца, гибридизуются с зондами на чипе с нуклеиновыми кислотами. Сигналы, выявленные после образования комплексов гибридизации, коррелируют с уровнями полинуклеотида в образце. В формате дифференциальной гибридизации полинуклеотиды, происходящие из двух образцов, метят различными группами для мечения. Смесь эти дифференциально меченных полинуклеотидов добавляют к чипу с нуклеиновыми кислотами. Затем чип с нуклеиновыми кислотами исследуют в условиях, при которых испускание двух различных меток является индивидуально поддающимся детекции. В одном варианте осуществления в качестве частей для мечения для формата дифференциальной гибридизации используют флуорофоры Cy3 и Cy5 (Amersham Pharmacia Biotech, Piscataway, N.J.).
Сигналы, полученные с чипов с нуклеиновыми кислотами, можно анализировать с использованием коммерчески доступного программного обеспечения, такого как программное обеспечение, предоставляемое Affymetrix или Agilent Technologies. Предпочтительно в эксперименты по гибридизации включают контроли, например для чувствительности сканирования, мечения зондов и дискретизации кДНК или кРНК. Сигналы гибридизации можно масштабировать или нормализовать перед проведением дальнейшего их анализа. Например, сигналы гибридизации для каждого отдельного зонда можно нормализовать для учета варьирования интенсивности гибридизации, когда используют более одного чипа в сходных условиях тестирования. Сигналы гибридизации также можно нормализовать с использованием интенсивностей, полученных для внутренних контролей для нормализации, содержащихся на каждом чипе. Кроме того, можно использовать гены с относительно постоянными уровнями экспрессии в образцах для нормализации уровней экспрессии других генов. В одном варианте осуществления в чип с нуклеиновыми кислотами по настоящему изобретению включены зонды для определенных поддерживающих генов. Эти гены выбирают, поскольку они демонстрируют стабильные уровни экспрессии среди различных групп тканей. Сигналы гибридизации можно нормализовать и/или масштабировать, исходя из уровней экспрессии этих поддерживающих генов.
Термин "гибридизационный комплекс" означает комплекс, который образован между полинуклеотидами образца, когда пурины одного полинуклеотида образуют водородные связи с пиримидинами комплементарного полинуклеотида, например 5'-A-G-T-C-3' образует пары оснований с 3'-T-C-A-G-5'. Степень комплементарности и использование нуклеотидных аналогов влияют на эффективность и строгость реакций гибридизации.
Термин "зонды для гибридизации" включает нуклеиновые кислоты (такие как олигонуклеотиды), способные связываться специфичным для оснований образом с комплементарной цепью нуклеиновой кислоты.
Термин "заболевание почек" или "нарушение почек" или аналогично "почечное заболевание" или "почечное нарушение" охватывает острую или хроническую аномальную утрату функции почек, такую как почечная недостаточность, сниженная скорость гломерулярной фильтрации и гломерулонефрит. Гломерулонефрит может иметь форму мембранозного гломерулонефрита, который вовлекает утолщение гломерулярной базальной мембраны. Альтернативно гломерулонефрит может иметь форму пролиферативного или мезангиопролиферативного гломерулонефрита, который характеризуется пролиферацией клеток в мезангиальном матриксе. Кроме того, гломерулонефрит может иметь форму мембранопролиферативного гломерулонефрита, который вовлекает комбинацию указанных выше изменений. Гломерулосклероз представляет собой тяжелую форму гломерулонефрита. Заболевания почек или нарушения почек также включают нефрит, нефропатию, гиперфильтрацию, мягкую микроальбуминурию, клиническую альбуминурию, развернутую клиническую нефропатию, хроническую почечную недостаточность, повреждения почечных сосочков, канальцевый некроз и диабетическую нефропатию, все из них согласно дифференциальной диагностике, проведенной ветеринарами, являющимися специалистами в данной области. Термин не охватывает поликистоз почек генетического происхождения.
Термин "полинуклеотид" или "олигонуклеотид" означает полимер нуклеотидов. Термин охватывает молекулы ДНК и РНК (включая кДНК и мРНК), либо одноцепочечные, либо двухцепочечные и, в случае одноцепочечных, комплементарную им последовательность либо в линейной, либо в замкнутой форме. Также термин охватывает фрагменты, варианты, гомологи и аллели, в соответствующих случаях, последовательностей, которые имеют те же или по существу те же свойства и выполняют ту же или по существу ту же функцию, что и исходная последовательность. Последовательности могут быть полностью комплементарными (без несовпадений) при выравнивании, или они могут иметь вплоть до 30% несовпадений в последовательности. Предпочтительно, для полинуклеотидов, цепь содержит приблизительно от 50 до 10000 нуклеотидов, более предпочтительно приблизительно от 150 до 3500 нуклеотидов. Предпочтительно, для олигонуклеотидов, цепь содержит приблизительно от 2 до 100 нуклеотидов, более предпочтительно приблизительно от 6 до 30 нуклеотидов. Точный размер полинуклеотида или олигонуклеотида зависит от различных факторов и от конкретного применения и использования полинуклеотида или олигонуклеотида. Термин включает нуклеотидные полимеры, которые синтезированы и которые выделены и очищены из природных источников. Термин "полинуклеотид" включает термин "олигонуклеотид".
Термин "полипептид", "пептид" или "белок" означает полимер аминокислот. Термин охватывает встречающиеся в природе и не встречающиеся в природе (синтетические) полимеры и полимеры, в которых искусственные химические миметики заменяют одну или несколько аминокислот. Также термин охватывает фрагменты, варианты и гомологи, которые обладают теми же или по существу теми же свойствами и выполняют ту же или по существу ту же функцию, что и исходная последовательность. Термин охватывает полимеры любой длины, предпочтительно полимеры, содержащие приблизительно от 2 до 1000 аминокислот, более предпочтительно приблизительно от 5 до 500 аминокислот. Термин включает полимеры аминокислот, которые являются синтезированными и которые являются выделенными и очищенными из природных источников.
Термин "зонд" означает (1) олигонуклеотид или полинуклеотид, либо РНК, либо ДНК, как встречающийся в природе, например, в очищенном продукте расщепления ферментом рестрикции, так и продуцированный синтетически, который способен подвергаться отжигу или специфично гибридизоваться с полинуклеотидом с последовательностями, комплементарными зонду, или (2) пептид или полипептид, способный специфично связывать конкретный белок или фрагмент белка по существу для исключения других белков или фрагментов белков. Олигонуклеотидный или полинуклеотидный зонд может быть либо одноцепочечным, либо двухцепочечным. Точная длина зонда зависит от многих факторов, включая температуру, источник и применение. Например, для диагностических применений, в зависимости от комплексности последовательности-мишени, олигонуклеотидный зонд, как правило, содержит приблизительно от 10 до 100, от 15 до 50 или от 15 до 25 нуклеотидов. В определенных диагностических применениях полинуклеотидный зонд содержит приблизительно 100-1000, 300-600, нуклеотидов, предпочтительно приблизительно 300 нуклеотидов. Зонды, описанные в настоящем описании, выбирают так, чтобы они были "по существу" комплементарными различным цепям конкретной последовательности-мишени. Это означает, что зонды должны быть достаточно комплементарными для специфической гибридизации или отжига с их соответствующими последовательностями-мишенями в наборе заданных условий. Таким образом, последовательность зонда не должна отражать точную комплементарную последовательность мишени. Например, некомплементарный нуклеотидный фрагмент может связываться с 5'- или 3'-концом зонда, а остальная последовательность зонда может являться комплементарной последовательности-мишени. Альтернативно некомплементарные основания или более длинные последовательности могут быть вставлены в зонд, при условии что последовательность зонда имеет достаточную комплементарность с последовательностью полинуклеотида-мишени, чтобы подвергаться специфическому отжигу с полинуклеотидом-мишенью. Пептидный или полипептидный зонд может представлять собой любую молекулу, с которой белок или пептид специфично связывается, включая ДНК (для связывающих ДНК белков), антитела, рецепторы клеточной мембраны, пептиды, кофакторы, лектины, сахара, полисахариды, клетки, клеточные мембраны, органеллы и мембраны органелл.
Термины "образец" и "жидкий образец" означает любую ткань животного или жидкость, содержащую, например, полинуклеотиды, полипептиды, антитела, метаболиты и т.п., включая клетки и другие ткани, содержащие ДНК и РНК. Примеры включают: кровь, хрящ, соединительную ткань, мышечную ткань, нервную ткань, мокроту и т.п. Образец может быть твердым или жидким или он может представлять собой ДНК, РНК, кДНК, жидкости организма, такие как кровь или моча, клетки, клеточные препараты или растворимые фракции или их аликвоты среды, хромосомы, органеллы и т.п.
Термин "единая упаковка" означает, что компоненты набора физически объединены в или с одним или несколькими контейнерами и рассматриваются как единица для изготовления, распространения, продажи или применения. Контейнеры включают, но не ограничиваются ими, мешки, коробки, бутылки, упаковки из целлофановой пленки, пришитые скобками или иным образом присоединенные компоненты или их комбинации. Единая упаковка может представлять собой контейнеры отдельных пищевых композиций, физически объединенные так, что их рассматривают как единицу для изготовления, распространения, продажи или применения.
Термин "специфически связывать" означает обособленное и точное взаимодействие между двумя молекулами, которое зависит от их структуры, в частности от их молекулярных боковых групп, например встраивание регуляторного белка в большую бороздку молекулы ДНК, образование водородных связей вдоль основной цепи между двумя одноцепочечными нуклеиновыми кислотами или связывание между эпитопом белка и агонистом, антагонистом или антителом.
Термин "специфически гибридизоваться" означает ассоциацию двух одноцепочечных полинуклеотидов с достаточно комплементарной последовательностью, чтобы позволить такую гибридизацию в заданных условиях, обычно используемых в данной области (иногда называемых "по существу комплементарными"). Например, термин может относится к гибридизации полинуклеотидного зонда по существу с комплементарной последовательностью, содержащейся в одноцепочечной молекуле ДНК или РНК согласно одному аспекту изобретения, по существу исключая гибридизацию полинуклеотидного зонда с одноцепочечными полинуклеотидами с некомплементарной последовательностью.
Термин "жесткие условия" означает (1) гибридизацию в 50% (об./об.) формамиде 0,1% бычьим сывороточным альбумином, 0,1% Ficoll, 0,1% поливинилпирролидоном, 50 мМ натрий-фосфатном буфере при pH 6,5 с 750 мМ NaCl, 75 мМ цитратом натрия при 42°C, (2) гибридизацию в 50% формамиде, 5x SSC (0,75 M NaCl, 0,075M цитрате натрия), 50 мМ фосфате натрия (pH 6,8), 0,1% пирофосфате натрия, 5x растворе Денхардта, обработанной ультразвуком ДНК спермы лосося (50 мкг/мл), 0,1% SDS и 10% сульфате декстран при 42°C; с промыванием при 42°C в 0,2x SSC и 0,1% SDS или промыванием 0,015M NaCl, 0,0015 M цитратом натрия, 0,1% Na2SO4 при 50°C, или сходные методики с использованием сходной низкой ионной силы и средств для промывания при высокой температуре и сходных денатурирующих средств.
Термин "вещество" означает элемент, соединение, молекулу, или их смесь, или любой другой материал, который потенциально может быть пригоден для диагностики, прогнозирования или модулирования возникновения или тяжести нарушения почек у животного, включая любое лекарственное средство, химическую структуру или биологическую структуру.
Термин "приемлемое варьирование" означает (1) для полинуклеотида: комплементарные последовательности полинуклеотида; гомологи полинуклеотида и комлементарные им последовательности; варианты полинуклеотида, комплементарные им последовательности и их гомологи; и фрагменты полинуклеотида, комплементарные им последовательности, их гомологи и их варианты, и (2) для полипептида: гомологи полипептида; варианты полипептида и их гомологи; и фрагменты полинуклеотида, их гомологи и их варианты.
Термин "вариант" означает (1) полинуклеотидную последовательность, содержащую любую замену, варьирование, модификацию, замену, делецию или вставку одного или нескольких нуклеотидов из полинуклеотидной последовательность или в полинуклеотидную последовательность и которая имеет те же или по существу те же свойства и выполняет ту же или по существу ту же функцию, что и исходная последовательность, и (2) полипептидную последовательность, содержащую любую замену, варьирование, модификацию, замену, делецию или вставку одной или нескольких аминокислоты из полипептидной последовательности или в полипептидную последовательность и которая имеет те же или по существу те же свойства и выполняет ту же или по существу ту же функцию, что и исходная последовательность. Таким образом, термин включает однонуклеотидные полиморфизмы (SNP) и аллельные варианты и включает консервативные и неконсервативные аминокислотные замены в полипептидах. Также термин охватывает химическое преобразование в производное полинуклеотида или полипептида и замену нуклеотидов или аминокислот нуклеотидами или аминокислотами, которые не встречаются в природе, в соответствующих случаях.
Термин "виртуальная упаковка" означает, что компоненты набора взаимосвязаны указаниями на одном или нескольких физических или виртуальных компонентах набора, инструктирующих пользователя о том, как получить другие компоненты, например, в мешке, содержащем один компонент и указания, инструктирующие обратиться к web-сайту, обратиться к записанной информации, просмотреть зрительное обращение, или обратиться к лицу, осуществляющему уход, или инструктору для получения инструкций о том, как использовать набор.
Изобретение не ограничивается конкретной методологией, протоколами и реагентами, описанными в настоящем описании, поскольку они могут отличаться. Кроме того, терминология, используемая в настоящем описании, предназначена только для описания конкретных вариантов осуществления и не предназначена для ограничения объема настоящего изобретения. Как используют в рамках изобретения и в прилагаемой формуле изобретения, формы единственного числа включают множество указываемых объектов, если контекст не указывает на иное, например указание на "вариант" включает множество вариантов. Кроме того, определенные термины включают варианты терминов, используемые в надлежащем грамматическом контексте, например термин "специфично связывает" включает "специфическое связывание" и другие формы этого термина. Аналогично, слова "содержать", "содержит" и "содержащий" следует интерпретировать включительно, а не исключительно.
Если нет иных указаний, все технические и научные термины и любые сокращения, используемые в настоящем описании, имеют те же значения, как обычно понимает специалист в данной области изобретения. Хотя для применения на практике этого изобретения можно использовать любые композиции, способы, изделия или другие средства или материалы, сходные или эквивалентные композициям, способам, изделиям или другим средствам или материалам, описанным в настоящем описании, предпочтительные композиции, способы, изделия или другие средства или материалы описаны в настоящем описании.
Все патенты, патентные заявки, публикации и другие источники литературы, цитированные или упоминаемые в настоящем описании, включены в настоящее описание в качестве ссылок в степени, допускаемой законом. Обсуждение этих ссылок предназначено только для обобщения утверждений, сделанных в них. Не допускается, что какие-либо из таких патентов, патентных заявок, публикаций или источников литературы, или любая их часть, являются соответствующим уровнем техники для настоящего изобретения, и, в частности, сохраняется право на оспаривание точности и значимости таких патентов, патентных заявок, публикаций и других источников литературы.
В одном варианте осуществления настоящее изобретение относится к одному или нескольким генам или сегментам генов ("гены", как определено в настоящем описании), которые дифференциально экспрессируются у не являющихся нормальными животных по сравнению с контрольной величиной, полученной от одного или нескольких нормальных животных. Изобретение основано на открытии полинуклеотидов, которые дифференциально экспрессируются у не являющихся нормальными животных по сравнению с нормальными животными. Эти гены были идентифицированы путем сравнения экспрессии генов в образцах ткани, взятых от животных, диагностированных как не являющихся нормальными, с генами в образцах тканей от животных, диагностированных как нормальные, с использованием технологии Affymetrix GeneChip®.
Полинуклеотиды и гены идентифицируют путем измерения отличий в экспрессии генов из образцов тканей, взятых от собак, диагностированных как не являющиеся нормальными и имеющих нарушение почек, против контрольной величины, где контрольную величину получают из образца для одного или нескольких нормальных животных. Изменение экспрессии гена можно определять любым способом, известным квалифицированным специалистам. Как правило, изменение экспрессии генов определяют путем измерения транскрипции (определения количества мРНК, продуцируемой геном) или измерения трансляции (определения количества белка, продуцируемого геном). Количество РНК или белка, продуцируемых геном, можно определять с использованием любого известного квалифицированным специалистам способа количественного определения полинуклеотидов и белков.
Как правило, экспрессию мРНК определяют с использованием полимеразной цепной реакции (ПЦР) (включая, но не ограничиваясь ими, ПЦР с обратной транскрипцией (RT-ПЦР) и количественную ПЦР в реальном времени (q-ПЦР)), чипы с короткими или длинными олигонуклеотидами, кДНК-чипы, секвенирование EST, нозерн-блоттинг, SAGE, MPSS, MS, чипы с гранулами и другие способы гибридизации. Измеренная РНК, как правило, имеет форму мРНК или обратно транскрибированной мРНК.
Экспрессию белка или полипептида определяют с использованием различных колориметрических и спектроскопических анализов и способов, таких как количественный вестерн-блоттинг, ELISA, 2D-гели, газовая или жидкостная хроматография, масс-спектрометрия, анализ Лоури, биуретовый анализ, флуоресцентные анализы, турбодиметрические способы, анализ с бицинхолиновой кислотой, технология белковых чипов, поглощение инфракрасного излучения, способ с нингидрином, анализ Брэдфорд и поглощение ультрафиолетовых лучей.
В предпочтительном способе изменение экспрессии гена определяют с использованием генных чипов Affymetrix Canine-1 и Canine-2, доступных от Affymetrix, Inc., и инструкций по применению таких чипов для определения экспрессии генов. Генные чипы позволяют крупномасштабное исследование биологических процессов и измерение активности в клетке в определенный момент времени. Анализ микрочипов позволяет учитывать различия в фенотипах на крупномасштабной генетической основе. Фактическое изменение продуктов экспрессии генов является более точным индикатором функции гена, чем определение самих последовательностей. Анализ микрочипов основан на количественном определении концентрации мРНК-транскрипта гена в клетке в данный момент времени. ДНК иммобилизуют на носителе и меченую мРНК-мишень гибридизуют с зондами на чипе. Связывание меченой мРНК с зондами измеряют с помощью лазерного анализа. Показателем является количество испускаемых фотонов. Весь чип сканируют и получают его цифровое изображение. Изображение обрабатывают для определения положения зондов и для присвоения показателей интенсивности каждому зонду. Таким путем можно определять активированные и ингибированные гены. Этот анализ позволяет квалифицированному специалисту найти группы генов со сходными профилями экспрессии и определить ткани со сходными профилями экспрессии. Таким образом, можно идентифицировать гены, которые объясняют наблюдаемые отличия в образцах тканей.
Для генных чипов Affymetrix, как правило, используются зонды размером 25 п.о. и наборы зондов из от 11 до 20 зондов, соответствующих конкретному гену или EST. Чип конструируют с зондом с абсолютным соответствием и с зондом с несоответствием по 25 п.о. каждый, причем первый из них является полностью комплементарным конкретной области гена, а второй имеет замененную 13-ую п.о. для внесения несоответствия. Алгоритм суммирования зондов используют для определения коррекции по фону, нормализации и суммирования зондов, которое представляет собой преобразование величин для зондов в величины экспрессии по набору зондов. RMA представляет собой один из алгоритмов, которые можно использовать для этой цели. Алгоритм выполняет последние две стадии анализа - нормализацию и суммирование показателей интенсивности на уровне зондов. Таким образом, величины абсолютного соответствия являются скорректированными по фону, нормализованными и суммированными в набор показателей экспрессии.
Необработанные данные анализируют с использованием программного обеспечения GeneSpring версии 7.0 (GS) (Agilent Corporation) и проверяют с использованием свободно распространяемого программного обеспечения R-Bioconductor (RB). Оба пакета программ используют для вычисления интенсивности зондов из файлов CEL, создаваемых Affymetrix Instrument. Сигналы присутствия/отсутствия/предела на зонд и величины P вычисляют с использованием программного обеспечения R-Bioconductor и GeneSpring по отдельности.
Как правило, дифференциальную экспрессию генов определяют путем измерения экспрессии по меньшей мере одного гена. Предпочтительно, для получения паттерна экспрессии генов или профиля экспрессии генов измеряют экспрессию двух или более диффененциально экспрессируемых генов. Более предпочтительно, измеряют экспрессию множества дифференциально экспрессируемых генов для получения дополнительной информации для более показательного паттерна или профиля экспрессии генов.
Настоящее изобретение относится ко множеству маркеров, которые вместе или по отдельности используют или можно использовать в качестве маркеров заболевания почек. В особенно пригодных вариантах осуществления изобретения можно выбирать множество из этих маркеров и их экспрессию мРНК можно одновременно измерять для получения профилей экспрессии для применения в различных аспектах изобретения, описанных в этой заявке. В предпочтительном варианте осуществления настоящих способов и композиций, по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10 или 11 маркеров выбраны из лумикана (LUM); альфа 1 (III) цепи коллагена, варианта 12 (COL3A1); декорина (DCN); секретируемого связанного с frizzle белка 2 (sFRP2); матрилина-2 (Matn2); ретинол-связывающего белка 4 (rbp4); MMP-9; кластерина (CLU); трансферрина (TF), Apo-C-1 (ApoC1); и ингибина-бета A (INHBA), и их можно использовать для определения профилей экспрессии генов при осуществлении на практике способов по изобретению. Каждый маркер, в частности, может быть связан с определенными аспектами заболевания почек.
В другом варианте осуществления изобретения уровень экспрессии генов альтернативно можно определять путем детекции белка, соответствующего продукту экспрессии гена. Предпочтительными являются секретируемые белки названных генов.
В другом аспекте изобретение относится к устройству, пригодному для детекции экспрессии множества генов, дифференциально экспрессируемых у не являющихся нормальными животных по сравнению с контрольными величинами. Устройство содержит подложку, имеющую множество олигонуклеотидных или полинуклеотидных зондов по настоящему изобретению, связанных с подложкой в известных положениях. Устройство по существу представляет собой иммобилизованную версию олигонуклеотидных или полинуклеотидных зондов, описанных в настоящем описании. Устройство пригодно для быстрой и специфической детекции генов и полинуклеотидов и их паттернов и профилей экспрессии. Как правило, такие зонды связывают с субстратом или сходной твердой подложкой и образец, содержащий один или несколько полинуклеотидов (например, ген, продукт ПЦР, продукт лигазной цепной реакции (LCR), последовательность ДНК, синтезированная с использованием способов амплификации, или их смесь) подвергают воздействию зондов, так чтобы полинуклеотид(ы) образца могли гибридизоваться с зондами. Либо зонды, либо полинуклеотид(ы), образца, или и зонды и полинуклеотид(ы) образца, можно метить, как правило, флуорофором или другой меткой, такой как стрептавидин, и подвергать детекции с использованием способов, известных квалифицированным специалистам. Если полинуклеотид(ы) образца является меченным, детекцию гибридизации можно проводить путем детекции флуоресценции при связывании. Если зонды являются мечеными, детекцию гибридизации, как правило, проводят по тушению метки. Если и зонд, и полинуклеотид(ы) образца являются мечеными, детекцию гибридизации, как правило, проводят путем мониторинга изменения цвета в результате сближения двух связанных меток. Специалистам в данной области известны различные стратегии мечения и метки, в частности, для флуоресцентных меток. Предпочтительно, зонды иммобилизуют на подложках, пригодных для формирования чипа (известного под различными названиями, включая ДНК-микрочип, генный чип, биочип, ДНК-чип и генная матрица), сравнимого с чипами, известными в данной области.
Полипептидные зонды можно получать общепринятыми способами, например, с использованием данных о нуклеотидной последовательности, предоставленных для полинуклеотидов по настоящему изобретению, и способов, известных в данной области. Такие способы включают, но не ограничиваются ими, выделение полипептида непосредственно из клеток, выделение или синтез ДНК или РНК, кодирующей полипептиды, и использование ДНК или РНК для получения рекомбинантных продуктов, химического синтеза полипептидов из отдельных аминокислот и продуцирования фрагментов полипептидов химическим расщеплением существующих полипептидов.
В другом аспекте изобретение относится к устройству, пригодному для детекции экспрессии множества генов, дифференциально экспрессируемых у не являющихся нормальными животных, по сравнению с контрольной величиной. Устройство содержит подложку, имеющую множество пептидных или полипептидных зондов по настоящему изобретению, связанных с подложкой в известных положениях. Устройство представляет собой по существу иммобилизованную версию пептидных или полипептидных зондов, описанных в настоящем описании. Устройство пригодно для быстрой и специфической детекции белков и их паттернов экспрессии. Как правило, такие зонды связаны с подложкой, и образец, содержащий один или несколько белков, подвергают взаимодействию с зондами, так чтобы белки образцов могли гибридизоваться с зондами. В определенных вариантах осуществления зонды, белки образцов или и зонды, и белки образцов метят и подвергают детекции, как правило, с помощью флуорофора или другого средства, известного квалифицированным специалистам. Как правило, для белковых матриц применимы те же способы и оборудование, которые используются для считывания полинуклеотидных микрочипов. Предпочтительно, зонды иммобилизуют на подложке, пригодной для формирования матрицы.
Способы определения количества или концентрации белка в образце известны квалифицированным специалистам. Такие способы включают радиоиммунные анализы, конкурентные анализы связывания, вестерн-блоттинг и анализы ELISA. Для способов, в которых используют антитела, пригодны поликлональные и моноклональные антитела. Такие антитела могут быть иммунологически специфичными к белку, эпитопу белка или белковому фрагменту.
В некоторых вариантах осуществления изобретения используются антитела для детекции и количественного определения белков, продуцируемых экспрессией полинуклеотидов по настоящему изобретению. Хотя детекцию белков можно осуществлять путем иммунопреципитации, аффинного разделения, вестерн-блоттинга, белковых чипов и т.п., в предпочтительном способе используется технология ELISA, где антитело иммобилизуют на твердой подложке и белок-мишень или пептид-мишень подвергают воздействию иммобилизованного антитела. Либо зонд, либо мишень, или и зонд, и мишень можно метить с использованием известных способов.
В некоторых вариантах осуществления паттерны или профили экспрессии множества генов, дифференциально экспрессируемых у не являющихся нормальными животных, выявляют с использованием чипа с зондами для детекции полинуклеотидов или полипептидов. В одном варианте осуществления можно использовать чипы с олигонуклеотидными или полинуклеотидными зондами, в то время как в другом варианте осуществления можно использовать чипы с антителами или другими белками, которые специфично связываются с дифференциально экспрессируемыми продуктами генов по настоящему изобретению. Такие чипы могут быть коммерчески доступными, или они могут быть изготовлены на заказ с использованием способов, известных квалифицированным специалистам, например синтеза in situ на твердой подложке или связывания предварительно синтезированных зондов с твердой подложкой способами микропечати. В различных вариантах осуществления чипы полинуклеотидных или полипептидных зондов изготавливают на заказ для специфической детекции транскриптов или белков, продуцируемых дифференциально экспрессируемыми генами по настоящему изобретению.
В одном варианте осуществления чипы с полинуклеотидными или полипептидными зондами делают на заказ для специфической детекции транскриптов или белков, продуцируемых двумя или более полинуклеотидами или генами, идентифицированными в таблице 2. Эти зонды предназначены для детекции генов, ассоциированных с каскадами метаболизма липидов и глюкозы у животных. В другом варианте осуществления чипы полинуклеотидных или полипептидных зондов изготавливают на заказ, чтобы они осуществляли специфическую детекцию транскриптов или белков, продуцируемых двумя или более полинуклеотидами или генами, указанными в таблицах 3-5. Эти зонды предназначены для детекции генов, которые имеют особое значение для не являющихся нормальными собак по сравнению с нормальными собаками.
Эти зонды подвергают взаимодействию с образцом для образования комплексов гибридизации, которые подвергают детекции и сравнивают со стандартными комплексами гибридизации. Отличия между комплексами гибридизации из образца и стандартом указывают на дифференциальную экспрессию полинуклеотидов и, таким образом, на гены, дифференциально экспрессируемые у не являющихся нормальными собак по сравнению с контрольной величиной в образце. В предпочтительном варианте осуществления зонды изготавливают для специфической детекции полинуклеотидов или их фрагментов, продуцируемых одним или несколькими генами или фрагментами генов, идентифицированных согласно настоящему изобретению. Способы детекции комплексов гибридизации известны квалифицированным специалистам.
В другом аспекте изобретение относится к способу детекции дифференциальной экспрессии генов, дифференциально экспрессируемых у не являющихся нормальными собак по сравнению с нормальными собаками в образце. Способ включает (a) реакцию комбинации, содержащей множество полипептидных зондов, с белками в образце в условиях, которые позволяют специфическое связывание между зондами и белками, где белки, связанные зондами, дифференциально экспрессируются у не являющихся нормальными собак по сравнению с нормальной собакой; (b) необязательно, реакцию комбинации, содержащей множество полипептидных зондов, с белками в стандарте в условиях, которые позволяют специфическое связывание между зондами и белками, где белки, связанные зондами, дифференциально экспрессируются у не являющейся нормальной собаки по сравнению с нормальной собакой; (c) детекцию специфического связывания в образце и, необязательно, стандарте стадии (b); и (d) сравнение специфического связывания в образце со связыванием стандарта, где отличия между специфическим связыванием в стандарте и образце указывают на дифференциальную экспрессию генов, дифференциально экспрессируемых у не являющихся нормальными собак по сравнению с нормальными собаками, в образце.
Эти зонды подвергают взаимодействию с образцом с получением специфического связывания, которое выявляют и сравнивают со специфическим связыванием стандарта. Отличия между специфическим связыванием образца и стандарта указывают на дифференциальную экспрессию белков и, таким образом, генов, дифференциально экспрессируемых у не являющихся нормальными собак по сравнению с нормальными собаками, в частности генов, ассоциированных с ненормальным состоянием, в образце. В предпочтительном варианте осуществления зонды изготавливают для специфической детекции белков или их фрагментов, продуцируемых одним или несколькими генами или фрагментами генов, идентифицированных согласно настоящему изобретению.
В одном варианте осуществления способ дополнительно включает воздействие на собаку или образец тестируемого вещества перед реакцией полипептидов с белками. Затем сравнение указывает на то, изменяет ли тестируемое вещество экспрессию генов, дифференциально экспрессируемых у не являющихся нормальными собак по сравнению с нормальными собаками, в частности генов, ассоциированных с ненормальным состоянием, в образце.
Пример 1: Классификация собак с хроническим заболеванием почек согласно руководству International Renal Interest Society.
В примерах, представленных ниже, собак, проявляющих клинические признаки хронического заболевания почек, тестировали против животных, не проявляющих признаков или симптомов хронического заболевания почек. Патологические диагнозы хронического заболевания почек ставили, исходя из критериев, указанных в таблицах 1 и 2 ниже, и согласно принципам International Renal Interest Society (IRIS).
Определение стадии хронического заболевания почек (CKD) проводят после постановки диагноза CKD для облегчения соответствующего лечения и мониторинга рассматриваемого животного. Определение стадии основано первоначально на уровне креатинина в плазме натощак, оцениваемом по меньшей мере два раза у стабильного животного. Собаки, демонстрирующие нормальную функцию почек и отсутствие клинических признаков или симптомов CKD, определялись в группу не имеющих заболевания собак. Стадия 1 у собак соответствует предшествующим классификациям раннего заболевания почек от отсутствия биохимических признаков CKD вплоть до почечной недостаточности, где азотемия не выявляется, но где уровень гломерулярной фильтрации (GFR) может быть снижен и концентрирующая способность почек может быть ухудшена. Стадия 2 соответствует предшествующей классификации ранней почечной недостаточности. На стадии 2 отмечается мягкая азотемия. Стадия 3 соответствует предшествующей классификации уремической почечной недостаточности, где выявляется умеренная азотемия. Могут присутствовать системные признаки уремической почечной недостаточности, такие как боль в костях, уремический гастрит, анемия и метаболический ацидоз. Стадия 4 соответствует почечной недостаточности конечной стадии, которая характеризуется тяжелой азотемией и нарастающими клиническими признаками уремического криза.
В таблице 1 представлены пять категорий исследованных собак соответственно. Исследовали всего 42 собаки, диагностированные как не имеющие CKD. Всего 14 собак 1 стадии проявляли минимальный гломерулонефрит (GN). Число исследованных собак, проявляющих развернутые стадии CKD, представляло собой: мягкий GN стадии 2=24; умеренный GN стадии 3=8 и выраженный GN стадии 4=13. Уровни креатинина в плазме для каждой из групп собак представлены в таблице 2 в качестве средних и медианных уровней креатинина в плазме для каждой группы собак.
|
|
Пример 2: Критерии выбора кандидатов
Необработанные данные анализируют с использованием программного обеспечения GeneSpring версии 7.0 (GS) (Agilent Corporation) и проверяют с использованием свободно распространяемого программного обеспечения R-Bioconductor (RB). Оба пакета программ используют для вычисления интенсивности зондов из файлов CEL, создаваемых Affymetrix Instrument. Сигналы присутствия/отсутствия/предела на зонд и величины P вычисляют с использованием программного обеспечения R-Bioconductor и GeneSpring по отдельности.
Данные об экспрессии генов определяют либо как "активированная", либо как "ингибированная" для всего приведенного анализа. Решение о том, является ли ген "активированным" или "ингибированным" основано на кратности изменения, которую вычисляют в качестве отношения интенсивность при лечении/контрольная интенсивность для каждого отдельного зонда. Кратность изменения считают сниженной, если ее величина составляет <1/2, и увеличенной, если она составляет >2,0. Также зонд считается представляющим интерес для последующего исследования, если он генерирует сигнал присутствия только при одном из сравниваемых состояний (лечение или контроль) и "отсутствия" или "предела" при других и кратное изменение является существенным согласно используемому программному обеспечению.
Пример 3: Способы выделения РНК
Материалы и способы. Следующие общие методики можно использовать для выделения РНК из образцов тканей собак и кошек для определения профиля экспрессии генов с использованием генных чипов, как дополнительно описано в примерах настоящего описания. Специалисту в данной области очевидно, что эти методики или их модификации, общепризнанные в данной области, можно применять для выделения РНК из образцов ткани или жидкости организма для дальнейшего анализа экспрессии генов с использованием различных аналитических методик, доступных специалисту в данной области, в частности технологий микрочипов.
Выделение рибонуклеиновой кислоты (РНК) из ткани. Образцы тканей можно собирать, замораживать в жидком азоте, размораживать, а затем растирать с помощью ступки и пестика, гомогенизировать и переносить в 50-мл коническую колбу. Затем гомогенизированный образец ткани перерабатывают с использованием способа экстракции РНК TRIzol® согласно инструкциям изготовителя (Invitrogen) для получения высококачественной РНК, которую затем подвергают дальнейшему геномному анализу.
Материалы: лед, жидкий азот, замороженная ткань собаки, реагент для анализа TRIzol®, хлороформ минимум 99%, изопропиловый спирт, 70% этанол (полученный из этанола, абсолютного и деионизированного, не содержащей РНКаз воды), РНКаза Zap®, деионизированная вода, раствор для хранения РНК RNA Storage Solution®, от Ambion.
Оборудование: гомогенизатор Ultra-Turrax T25 Power, центрифуга Beckman Coulter Allegra 25R, центрифуга Eppendorf, щипцы, скальпель, твердая поверхность для нарезания, т.е. разделочная доска, 1,5-мл не содержащие ДНКаз и РНКаз/стерильные микроцентрифужные пробирки, 50-мл не содержащие ДНКаз и РНКаз/стерильные одноразовые полипропиленовые пробирки, пипетки P1000, P200, P20, P10 и P2 Rainin Pipetman, наконечники с фильтрами для пипеток P1000, P200, P20, P10 и P2, не содержащие ДНКаз и РНКаз/стерильные и не содержащие нитей полотенца.
Приготовление: подготовить 50-мл полипропиленовые пробирки с 4 мл TRIzol® (одна пробирка для каждой ткани, выбранной для выделения РНК).
Гомогенизация тканей: заполнить контейнер, который пригоден для содержания жидкого азота, содержимым 3-4 совков жидкого азота. Поместить фрагмент замороженной ткани непосредственно в упомянутый выше контейнер (ткань должна иметь размер приблизительно с горошину) и поместить ткань в подходящую обозначенную 50-мл полипропиленовую пробирку (которая уже содержит 4 мл TRIzol®). Сразу начать гомогенизацию с использованием гомогенизатора Ultra-Turrax T25 Power. Гомогенизировать при наиболее высоком режиме (6) в течение 10-15 секунд. Охладить образец на льду в течение других 10-15 секунд, а затем повторить. Продолжать до тех пор, пока ткань полностью не гомогенизируется и раствор не станет мутным. После завершения гомогенизации закрыть 50-мл пробирку и обратно поместить на лед. Инкубировать гомогенизированные ткани при комнатной температуре в течение 5 минут перед продолжением процесса выделения.
Пример 4: Методики получения РНК
Выделение РНК: Главным образом, следуют методикам, приведенным в инструкциях Invitrogen, предоставляемых вместе с реагентом TRIzol®. Разделить гомогенизированный образец на четыре аликвоты объемом 1 мл в четыре 1,5-мл микроцентрифужные пробирки. Добавить 200 мкл хлороформа к каждой 1-мл аликвоте. Закрыть пробирки, встряхивать в течение 15 секунд, а затем встряхивать вверх и вниз. В результате должна образоваться розовая мутная жидкость. Инкубировать пробирки при комнатной температуре в течение 2-3 минут. Центрифугировать пробирки в течение 15 минут при 14000 об/мин и 4°C. Перенести водную фазу (верхний слой) в стерильную 1,5-мл микроцентрифужную пробирку. Типичный объем водной фазы, которую следует переносить в новую пробирку, составляет приблизительно 500 мкл. Следует убедиться в том, что не переносится ни промежуточная, ни нижняя фазы. Осадить РНК из раствора добавлением 500 мкл изопропилового спирта в каждую микроцентрифужную пробирку, содержащую водный слой. Встряхивать пробирки вверх и вниз в течение по меньшей мере 20 секунд. Инкубировать образцы при комнатной температуре в течение 10 минут. Центрифугировать образцы в течение 10 минут, 14000 об/мин, при 4°C. Удалить супернатант осторожно путем аспирирования жидкости, следя за тем, чтобы не потерять осадок. Добавить 1 мл 70% этанола, чтобы промыть осадок. Удалить осадок постукиванием по пробирке (или постукиванием пробирки по поверхности стола) и встряхнуть для перемешивания. Центрифугировать в течение 5 минут при 8200 об/мин при 4°C. Осторожно удалить супернатант аспирированием жидкости, следя за тем, чтобы не потерять осадок. Использовать полотенце без ниток для тщательного впитывания избытка этанола, убедившись, что осадок является сухим. Ресуспензировать каждый осадок в 30 мкл раствора для хранения РНК RNA Storage Solution РНК. Перемешать осторожно пипетированием до тех пор, пока РНК не перейдет обратно в раствор, а затем хранить при -80°C. Может быть необходимым встряхнуть образец в течение нескольких секунд при низкой скорости для способствования ресуспендированию РНК. Если это необходимо, центрифугировать образцы с использованием микроцентрифуги перед замораживанием.
Очистка РНК: Следуют методике, приведенной в RNeasy® Mini Handbook.
Выделение РНК из клеток, культивированных в камерах OptiCell Chambers с использованием набора RNeasy Mini Kit. Для выделения высококачественной РНК, которую затем используют для последующего геномного анализа, используют культивированные клетки из клеточных линий млекопитающих. Все операции, связанные с культивированием клеток, следует проводить в строгих асептических условиях.
Реагенты: 10X PBS, деионизированная H2O, абсолютный этанол, раствор для хранения РНК RNA Storage Solution, β-меркаптоэтанол, РНКаза Zap®, буфер RLT и буфер RW1 и буфер RPE (предоставленные в наборе RNeasy Mini Kit).
Оборудование/материалы: Набор RNeasy Mini Kit, центрифугируемые колонки QIAshredder, нож OptiCell, 20-мл стерильный шприц, наконечники OptiCell, скребок для клеток, пипетка P1000 Pipetman, Rainin, пипетка P200 Pipetman, Rainin, 100-100 мкл наконечники для пипетки с фильтрами, 1-200 мкл наконечники для пипетки с фильтрами, стерильные пипетки для переноса, 55 мл емкость со стерильным раствором, 1,5 мл стерильные микроцентрифужные пробирки и микроцентрифуга Eppendorf.
Растворы: буфер RLT (исходный раствор, предоставленный в наборе RNeasy Mini Kit); добавить 100 мкл β-меркаптоэтанола на 10 мл буфера RLT перед началом протокола. 70% этанол: получить 50 мл 70% этанола добавлением 35 мл абсолютного этанола к 15 мл деионизированной не содержащей РНКаз воды. 1X PBS: не содержащая РНКаз вода. Фильтровать с использованием 0,22-мкм фильтра.
Методика: Удалить клетки из камеры OptiCell (использовать одну OptiCell за один раз). Проверить клетки под микроскопом, чтобы убедиться, что клетки являются живыми перед выделением РНК. Удалить и отбросить среду для культивирования клеток. С использованием ножа OptiCell вырезать верхнюю мембрану, открывая клетки на нижней мембране. Промыть мембрану, к которой клетки прикреплены, три раза посредством 1X PBS. Накапать пипеткой 600 мкл раствора буфера RLT (содержащего β-меркаптоэтанол) на центр мембраны, к которой прикреплены клетки. С использованием скребка для клеток осторожно распределить буфер RLT по всей поверхности мембраны, а затем собрать жидкость в одном углу. Отсосать пипеткой полный объем буфера RLT и поместить в центрифугируемую колонку QIAshredder.
Выделение РНК: центрифугировать центрифугируемые колонки QIAshredder при 14000 об/мин в течение 2 минут. Выбросить центрифугируемую колонку, но сохранить пробирку для сбора и ее содержимое. Добавить 600 мкл 70% этанола в пробирку для сбора и хорошо перемешать пипетированием (после этого общий объем=1,2 мл). Перенести 600 мкл клеточного лизата в колонку RNeasy и центрифугировать в течение 15 секунд при 14000 об/мин. Выбросить пропускаемую жидкость, но сохранить пробирку для сбора и центрифугируемую колонку. Перенести оставшийся объем клеточного лизата (~600 мкл) в центрифугируемую колонку и повторить центрифугирование. Выбросить пропускаемую жидкость, но сохранить пробирку для сбора и центрифугируемую колонку. Добавить 700 мкл буфера RW1 к центрифугируемой колонке. Центрифугировать в течение 15 секунд при 14000 об/мин для промывания колонки. Выбросить пропускаемую жидкость и пробирку для сбора. Перенести центрифугируемую колонку в новую 2-мл пробирку для сбора и в колонку добавить 500 мкл буфера RPE. Центрифугировать в течение 15 секунд при 14000 об/мин. Выбросить пропускаемую жидкость, сохранить пробирку для сбора/колонку. Добавить в колонку другие 500 мкл буфера RPE. Центрифугировать в течение 2 минут при 14000 об/мин. Перенести центрифугируемую колонку в 1,5-мл пробирку для сбора. Добавить 30 мкл раствора для хранения РНК RNA Storage Solution непосредственно к мембране с силикагелем и центрифугировать в течение 1 минуты при 14000 об/мин для элюирования РНК. Хранить конечную РНК при -70°C.
Анализ RNA 6000 Nano Assay. С использованием Agilent 2100 Bioanalyzer и анализа РНК 6000 Nano Assay, анализировать РНК, выделенную из культивированных клеток млекопитающих, лимфоцитов или тканей в отношении качества.
Реагенты: гелеобразная матрица RNA 6000 Nano, концентрат красителя RNA 6000 Nano, маркер РНК 6000 Nano (все из указанных выше реагентов содержатся в наборе RNA 6000 Nano Assay kit, Agilent), лестничный маркер RNA 6000 ladder, РНКаза Zap и не содержащая РНКазу вода от Ambion.
Оборудование/другие материалы: Agilent Chip Priming Station, Agilent, чип RNA 6000, Agilent, очистители электродов, пипетки P2, P10, P200 и P1000 Rainin Pipetman, стерильные, не содержащие ДНКаз/РНКаз наконечники для пипеток с фильтрами, 1,5-мл микроцентрифужные пробирки, стерильные, устройство для встряхивания, вихревой смеситель 1A, микроцентрифуга и нагревающий блок.
Методика: Методика приведена в Reagent Kit Guide, RNA 6000 Nano Assay, Edition November 2003, от Agilent Technologies. Следуют методике, приведенной в руководстве, со следующими модификациями: приготовление геля, стр. 17, - вместо разделения отфильтрованного геля на аликвоты по 65 мкл каждая хранить исходный фильтрованный гель в исходной микроцентрифужной пробирке и разделить на аликвоты объемом 65 мкл при необходимости. Нанесение маркера RNA 6000 Nano Marker, стр. 22, - добавить 1 мкл не содержащей РНКаз воды (вместо маркера РНК 6000 Nano Marker) в каждую лунку для образца, которая не будет содержать образец. Это не только экономит некоторое количество используемого маркера, но также служит в качестве отрицательного контроля, чтобы видеть, что ни один из реагентов не загрязнен, включая не содержащую РНКаз воду. Нанесение лестничного маркера и образцов, стр. 23, - денатурировать нагреванием образцы и лестничный маркер РНК RNA 6000 Ladder в течение дополнительных 30 секунд (всего 2,5 минуты) при 71°C. Начало анализа чипа, стр. 26, - выбрать опцию "Eukaryote Total RNA Nano" из меню анализа.
Пример 5: Анализ экспрессии Affymetrix GeneChip Expression Analysis
Экспрессию генов анализируют с использованием чипов Affymetrix Canine 1 и Canine 2 GeneChip®, которые являются коммерчески доступными от Affymetrix, Inc., Santa Clara, CA 95051. Тотальную РНК подвергают обратной транскрипции в кДНК. кДНК используют для получения кРНК, которую фрагментируют и используют в качестве зондов для гибридизации GeneChip. Генный чип промывают и сигнал гибридизации измеряют с помощью лазерного сканера Affymetrix. Затем данные гибридизации подтверждают и нормализуют для дальнейшего анализа согласно инструкциям изготовителя.
Материалы: Affymetrix предоставляет большинство реагентов и набор. Другие реагенты, указанные в Affymetrix Manual, но не предоставленные в наборе, можно получить отдельно (для подробного описания см. GeneChip Expression Analysis Technical Manual (701021 Rev.4)), РНКазу Zap® и деонизированную воду.
Оборудование: микроцентрифуга Eppendorf, 1,5-мл не содержащие ДНКаз и РНКаз/стерильные микроцентрифужные пробирки, 50-мл не содержащие ДНКаз и РНКаз/стерильные одноразовые полипропиленовые пробирки, пипетки P1000, P200, P20, P10 и P2 Rainin Pipetman, наконечники пипеток с фильтрами для пипеток P1000, P200, P20, P10 и P2, не содержащие ДНКаз и РНКаз/стерильные, и термоблок Пельтье PTC-200.
Методика: следовать всем методикам точно, как описано в GeneChip Expression Analysis Technical Manual (Affymetrix Copyright 1999-2003). Использовать 5 микрограмм тотальной РНК для синтеза первой цепи кДНК. Использовать либо термоблок Пельтье PTC-200, либо нагревательный блок для контроля температуры реакций и денатурации зондов. Контроль качества проводят с использованием чипов RNA NanoDrop в BioAnalyer 2100. Использовать формат 100 (Midi Array) для генного чипа собаки.
Пример 6: Экспресссия генов у собак с хроническим заболеванием почек
Исследования проводили в соответствии с предшествующими примерами 1-5 с использованием собак, имеющих различные стадии хронического заболевания почек, для определения лежащих в его основе отличий в экспрессии генов, между собаками с нормальной функцией почек и собаками, имеющими минимальный, мягкий, умеренный и выраженный гломерулонефрит, соответствующий стадиям 1-4, как представлено в таблице 1. Для подготовки образцов тканей и жидкостей организма от 42 собак, имеющих нормальную функцию, 14 собак, имеющих минимальный гломерулонефрит, 24 собак, имеющих мягкий гломерулонефрит, 8 собак, имеющих умеренный гломерулонефрит, и 13 собак, имеющих выраженный гломерулонефрит, определяемый по уровням креатинина в плазме, представленным в таблице 2 и с помощью клинического наблюдения, использовали методики, описанные в примерах настоящей заявки.
Исходя из данных об экспрессии генов, сравнивающих собак с нормальной функцией почек с собаками, имеющими гломерулонефрит, как определено в предшествующих примерах, было идентифицировано пять генов, приведенных в таблице 3, удовлетворяющих критериям селекции примера 2 в качестве потенциальных биомаркеров хронических нарушений почек у собак. Эти гены включают лумикан (LUM); альфа 1 (III) цепь коллагена, вариант 12 (COL3A1); декорин (DCN); секретируемый связанный с frizzle белок 2 (SFRP2); и матрилин-2 (Matn2). Аналогичные синонимы человека и регистрационные номера для мРНК и белков приведены в таблице 3 для каждого гена. Каждый из белков является секретируемым белком.
|
|
|