Результат интеллектуальной деятельности: ВЯЗКОЭЛАСТИЧНЫЕ ГЕЛИ В КАЧЕСТВЕ НОВЫХ НАПОЛНИТЕЛЕЙ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Гиалуроновая кислота (HA) представляет собой гетерополисахарид, состоящий из чередующихся остатков D-глюкуроновой кислоты и N-ацетил-D-глюкозамина.
HA представляет собой прямоцепочечный полимер с молекулярной массой в диапазоне от 50000 до 13×106 Да, в зависимости от источника, из которого она получена, и используемого способа получения.
HA присутствует в природе в околоклеточных гелях, в основном веществе соединительной ткани позвоночных (одним из основных компонентов которого она является), в стекловидном теле и в пупочном канатике.
HA играет важную роль в биологическом организме в качестве структурной и механической опоры для тканей и в качестве активного компонента в клеточной физиологии тканей, таких как кожа, сухожилия, мышцы и хрящ.
Она представляет собой одну из основных молекул в хрящевой матрице, а также представляет основной не белковый составляющий компонент синовиальной жидкости. Поскольку она представляет собой сильно гидрофильную вязкоэластичную молекулу, то она придает синовиальной жидкости смазывающие свойства; поэтому HA использовалась при остеоартрите в течение более чем 30 лет, главным образом, для лечения связанной с остеоартритом боли.
HA также играет ключевую роль в процессе репарации ткани со структурной точки зрения (в организации внеклеточной матрицы и регуляции ее гидратации) и в качестве стимулирующего/регулирующего вещества широкого диапазона физиологических процессов, где указанный полисахарид действует непосредственно и/или опосредованно (образование кровяного сгустка, фагоцитарная активность, пролиферация фибробластов, неоваскуляризация, повторная эпителизация и т.д.) (Weigel P. et al., J Theoretical Biol, 1986:219-234; Abatangelo G. et al., J Surg Res, 1983, 35:410-416; Goa K. et al., Drugs, 1994, 47:536-566). Поскольку указанные свойства были известны в течение длительного времени, HA также используется для получения перевязочных материалов для лечения ран, язв и повреждений кожи различного происхождения.
Гиалуроновая кислота также используется в качестве заполнителя для морщин, складок и небольших вдавленных зон на коже лица и для увеличения объема губ и щек, потому что она иммунологически инертна, нетоксична, биологически разлагаема и биологически рассасываема.
Лечение средствами на основе гиалуроновой кислоты показано для коррекции:
объема и контуров губ,
кожных складок (например, носогубных складок),
коррекции контуров лица (например, щек и подбородка),
морщин (например, складок надпереносья и ротовых спаек),
морщин вокруг глаз,
фиброзных рубцов после угрей,
фиброзных посттравматических рубцов,
дефектов мягких тканей,
рубцов после ринопластики.
Гиалуроновая кислота не является долговременным наполнителем. Это означает, что после инъекции продукт постепенно метаболизируется и поглощается организмом за периоды времени, изменяющиеся в соответствии с обрабатываемой областью и использованным типом препарата. Эффект заполнения и увеличенного объема (или уменьшения морщин) проявляется немедленно и длится только несколько недель. Основные продукты, присутствующие на рынке, могут быть классифицированы на следующие категории на основании различных периодов времени их рассасывания:
быстро рассасываемые наполнители (2-3 месяца),
наполнители со среднесрочным рассасыванием (5-6 месяцев),
наполнители медленного рассасывания (1 год), такие как Restylane Sub Q (QMed, EP0839159).
В дерме HA выполняет гидратирующие функции благодаря ее высокой способности связывать воду и структурные функции в качестве «каркаса», поскольку путем связывания с другими веществами она образует макромолекулярные комплексы, которые придают коже плотность.
Поэтому механизм действия состоит в немедленном объемном заполнении вследствие вязкоэластичных свойств продукта и синтезе нового коллагена вследствие стимуляции кожных фибробластов.
Однако HA представляет собой природный полисахарид, который быстро разрушается ферментами гиалуронидазы, присутствующими в соединительной ткани; для того, чтобы получить наполнители, эффект которых продолжается в течение нескольких месяцев, HA поэтому подвергают процессам поперечной сшивки, которые улучшают ее вязкоэластичные свойства и увеличивают время ее пребывания в ткани. Образованные таким образом наполнители являются поперечносшитыми, например, посредством BDDE (простого диглицидилового эфира 1,4-бутандиола, Restylane®, BELOTERO® и Regenyal Idea) или DVS (дивинилсульфона, Hylaform®), которые создают мостиковые связи между молекулами полимера. Однако увеличение степени поперечной сшивки вызывает прогрессирующую денатурацию HA до степени глубокой модификации ее химических, физических и биологических свойств. Матрицы из излишне поперечносшитой HA присутствуют в виде твердых веществ в форме частиц, которые больше не распознаются клетками (и, в частности, иммунной системой) как HA; поэтому полисахарид воспринимается как инородное тело, которое запускает воспалительные реакции с образованием вокруг него фибротической капсулы. Кроме того, избыточно поперечносшитая HA не способна стимулировать регенерацию дермы/кожной ткани, вызванную, как известно по хорошо установленным научным результатам, фрагментами HA (особенно фрагментами с низкой молекулярной массой), которые оказывают эффект стимуляции синтеза коллагена кожными фибробластами.
Наполнители также классифицируются как рассасываемые или долговременные. Наполнители рассасываемого типа являются наиболее биологически совместимыми; они состоят из гиалуроновой кислоты или коллагена, или модифицированных, или присутствующих в их природной форме, и в последующем рассасываются в пределах самое большее года. Долговременный тип состоит из синтетических полимеров, таких как полиакриламиды, особые поперечносшитые молекулы которых образуют стабильный гель при объединении с водой. Наполнители долговременного типа всегда остаются in situ и очень полезны для наполнения губ, но их применение не рекомендуется, потому что их введение в кожу все чаще вызывает острые воспалительные реакции, приводя к образованию фибротических капсул вокруг наполнителя, которые воспринимаются как инородное тело, и поэтому являются токсичными.
Автор усовершенствовал новый тип биоматериала в качестве нового наполнителя и/или в качестве нового продукта для профилирования тела, образуемого смешиванием двух поперечносшитых производных HA различными, но дополняющими путями для получения заместителя кожи/ткани, который обеспечивает возможность немедленной гидратации (и следовательно, немедленного заполнения) обработанной кожи/ткани, в то же время, способствуя очень длительным периодам разрушения in vivo для устранения необходимости в повторных инъекциях и, таким образом, уменьшая побочные эффекты.
Новые биоматериалы, к которым относится настоящее изобретение, обладают особыми характеристиками биологической совместимости, идентичными характеристикам гиалуроновой кислоты как таковой, но их биоразлагаемость отличается; при имплантации in vivo время их нахождения в организме гораздо дольше, чем у немодифицированной HA, таким образом обеспечивая возможность немедленной регенерации/восстановления дермальной/кожной ткани, которая утратила свою первоначальную плотность.
Подробное описание изобретения
Автор усовершенствовал новый тип биоматериала в качестве нового наполнителя и/или в качестве нового продукта для профилирования тела на основе смешивания двух производных HA с различными, но дополняющими характеристиками. Для получения нового продукта для инъекции при лечении дефектов кожи, в дерматологии, в дерматокосметологии и/или эстетической хирургии, который вызывает:
1)немедленную гидратацию дермы/кожи,
2) немедленное заполнение обрабатываемой ткани,
3) очень длительные периоды времени разрушения in vivo,
4) сниженные побочные эффекты.
Новые биоматериалы состоят из:
автопоперечносшитой гиалуроновой кислоты (ACP) или гексадециламида HA (HYADD), смешанного с
гиалуроновой кислотой, поперечносшитой с BDDE (HBC).
ACP, используемая в настоящем изобретении, полученная как описано в EP 0341745, обладает средней степенью поперечной сшивки от 4 до 5% и предпочтительно получена с использованием HA со средней молекулярной массой (ММ) 200 кДа. При гидратации она присутствует в виде автопоперечносшитого геля без молекул, инородных для нативного полисахарида, потому что она возникает из сложноэфирной связи между карбоксильной и гидроксильной группами одной и той же полисахаридной цепи и/или соседних цепей. Она поэтому лишена иммунотоксичности, также биологически совместима как нативная HA, обладает высокой увлажняющей способностью и легко разрушается гиалуронидазами, высвобождая молекулы с низкой молекулярной массой, способные стимулировать синтез коллагена, для улучшения тонуса и эластичности кожной ткани.
Гексадециламид HA (HYADD) получают, как описано в EP 1095064 и EP 1853279, предпочтительно, используя HA с молекулярной массой (ММ) 500-730 кДа, со средней степенью конечного амидирования/замещения от 1 до 3% моль.
ACP и HYADD представляют собой производные HA, ответственные за немедленную гидратацию (приводящую к мгновенному заполнению дермы), вызываемую внутридермальной инъекцией наполнителя, к которому относится настоящее изобретение.
HA, поперечносшитая с BDDE (молекулой, содержащей эпоксидную группу для образования простых эфиров на первичных гидроксилах HA), содержит поперечносшивающую молекулу и поэтому более устойчива к ферментативному разрушению, поскольку она имеет эфирные связи, которые стабилизируют полисахарид, обеспечивая полученному продукту длительное время пребывания в организме.
Смешивание двух видов поперечносшитой HA приводит к образованию нового биоматериала, который имеет характеристики биологической совместимости, идентичные характеристикам нативной гиалуроновой кислоты, но другую биоразрушаемость, так что при имплантации in vivo, время его пребывания в организме гораздо длительнее, чем время пребывания немодифицированной HA, таким образом, обеспечивая возможность регенерации/восстановления дермальной ткани, которая утратила свою первоначальную плотность. Автор также продемонстрировал, что их объединение совершенно неожиданно приводит к гораздо более длительному времени разрушения in vivo, чем время разрушения коммерческих контрольных наполнителей, образованных таким же типом HA, поперечносшитой с BDDE, с последующим увеличением времени пребывания в организме. Наконец, автор претендует на приоритет применения новых биоматериалов в качестве наполнителей и/или в качестве новых продуктов для профилирования тела при лечении дефектов кожи, в дерматологии, в дерматокосметологии и/или эстетической хирургии.
Химически неоднородная природа нового биоматериала обеспечивает возможность модуляции свойств конечного продукта путем подходящего варьирования соотношения массы между компонентами. Две HA могут быть смешаны в соотношении ACP (или HYADD):HBC от 10:90 до 90:10; массовое соотношение будет выбираться на основании желательной конечной вязкости, которая будет зависеть от обрабатываемого участка. Если предстоит обработка участков, требующих имплантации большого количества биоматериала, как в случае заполнения молочных желез, ягодиц, щек или подбородка, или глубоких морщин, то используемый биоматериал должен предпочтительно обеспечивать хорошую плотность и, следовательно, вязкость, подходящую для получения геля с превосходной консистенцией и низкой скоростью биоразрушаемости; в данном случае, смесь ACP (или HYADD):HBC будет составлять от 10:90 до 50:50, и предпочтительно, 25:75, потому что продукт, полученный путем увеличенная массовой фракции HBC, больше подходит для оказания более длительно продолжающегося увеличивающего объем эффекта. Однако если предстоит обрабатывать губные борозды или мелкие лобные морщины, то соотношение ACP (или HYADD):HBC предпочтительно будет составлять от 90:10 до 50:50, поскольку более высокая фракция ACP в наполнителе обеспечивает получение материала, более подходящего для биоревитализации кожи и коррекции мелких морщин, небольших мимических морщин и тому подобное. Кроме того, игла должна иметь очень высокий калибр; поэтому гель должен быть легко выдавливаемым и менее вязким, чем гель, описанный выше. Реологические свойства продукта, следовательно, могут корригироваться на основании выбранного соотношения ACP:HBC.
Свойства биоматериала, составленного композицией из равных количеств ACP (или HYADD)/HBC, также могут подходящим образом модулироваться путем целевого выбора носителя, в котором он получен: например, смесь в массовом соотношении ACP:HBC 50:50, диспергированная в солевом растворе (0,9% NaCl), будет более вязкой, чем если бы она была диспергирована в фосфатном буфере при pH=6,95; следовательно, для данной определенной смеси, солевой раствор является более подходящей средой для составления продуктов с ограниченной скоростью диспергирования in situ. Материалы, состоящие из преобладающего количества HBC, проявляют противоположный профиль. Следовательно, вязкоэластичные свойства материала воздействуют на эксплуатационные качества продукта.
Настоящее изобретение также относится к двум способам получения описанных выше биоматериалов: способу A и способу B.
Новые способы A и B делятся на две стадии:
1) способ получения производного HBC и
2) способ смешивания его с производным ACP или HYADD.
Данные две стадии приводят к получению продуктов с очень высокой степенью чистоты. При способах, обычно используемых для получения HA, поперечносшитой с BDDE, очистку выполняют промыванием массы полученного геля или диализом. В обоих случаях оптимальная эффективность очистки может не быть достигнута вследствие природы матрицы геля, которая в связи с ее тенденцией к набуханию, включает большое количество растворителя. Эти гели имеют низкую подвижность и транспортную способность и склонны к осаждению в виде желатинозных смол. Полученный таким образом осадок, выделенный в виде твердого вещества, обладает свойствами растворимости и реологии при регидратации, в частности способностью к набуханию, эластичностью и однородностью (существенные характеристики для наполнителя), отличные от свойств геля перед очисткой.
Однако в способе, описываемом ниже в виде способа A, продукт осаждается в форме мелко измельченного порошка, который впоследствии легко промываем. Кроме того, тщательный выбор условий реакции дает после выделения осаждением и промыванием продукт со способностью восстановления геля гидратацией и стерилизацией, что обеспечивает получение биоматериала, имеющего воспроизводимые, достаточно стандартизированные характеристики эластичности и однородности.
Способ B не включает стадию осаждения продукта HBC в виде порошка; очистку и гомогенизацию геля (полученного после смешивания HBC с ACP или HYADD) осуществляют на стадии дробления, которая включает пропускание его через фильтр с коэффициентом удерживания вещества в форме частиц от 25 до 150 мкм. На данной стадии происходит очистка конечного геля, что делает его в высшей степени однородным.
HA, используемая в настоящем изобретении для получения описанных выше производных (HBC, ACP и HYADD), может происходить из любого источника, такого как экстракция из петушиных гребней или ферментация, и иметь среднюю молекулярную массу от 400 до 3×106 Да, предпочтительно, от 1×105 Да до 1×106 Да, и еще предпочтительнее, от 200000 до 1×106 Да.
Новый способ получения A включает следующие стадии:
Синтез поперечносшитой HBC
1) Растворение в щелочном растворе (предпочтительно, 0,15M-0,35M NaOH) диэпоксидного BDDE в стехиометрическом соотношении от 2,5 до 25% моль, предпочтительно, от 5 до 15% моль (в зависимости от предполагаемого применения продукта; чем выше процентная доля BDDE, тем дольше время пребывания в организме) повторяющихся звеньев гиалуроновой кислоты с последующим
2) диспергированием HA в растворе, описанном в предыдущем абзаце, при комнатной температуре. Концентрация HA должна составлять от 80 до 300 мг/мл, и время гомогенизации от 30 до 300 минут.
3) Запуск реакции тепловой активацией, причем указанный раствор нагревают при температуре от 35 до 55°C в течение от 2 до 36 часов.
4) Экструзия полученной массы через металлическое сито для уменьшения ее частиц до размера приблизительно 600 мкм.
5) Гидратация геля разбавлением его водой фактором 3 к 25 в течение времени от 4 до 48 часов при температуре от 4 до 24°C.
6) Доведение pH до нейтрального значения водным раствором HCl, имеющим концентрацию от 0,5 до 5 моль/л, предпочтительно, от 1 до 2 моль/л.
7) Добавление 2,5 объемов растворимого в воде органического растворителя, такого как этанол, метанол, изопропанол, н-пропанол, диоксан, ацетонитрил, ацетон и/или их смеси (предпочтительно, этанола и ацетона), до тех пор, пока не будет получен продукт в форме осажденного порошка.
8) Промывание органическими растворителями, такими как этанол, метанол, изопропанол, н-пропанол, диоксан, ацетонитрил, ацетон и/или их смеси (предпочтительно, этанола и ацетона), содержащими водную фракцию ниже 35%.
9) Сушка в вакууме при температуре от 30 до 45°C в течение от 2 до 7 дней, и в любом случае до удаления остаточных растворителей ниже уровня 400 ч./млн. с получением белого порошка HBC.
Смешивание ACP (или HYADD) с HBC
10) Смешивание порошка HBC с порошком ACP (или HYADD) при соотношении ACP:HBC от 10:90 до 90:10 (в зависимости от выбранного применения, как описано ранее).
11) Гидратация солевым раствором или фосфатным буфером, предпочтительно, солевым раствором (который может содержать другие эксципиенты, такие как лидокаин), приводящая к общей концентрации HA от 12 до 27 мг/мл, предпочтительно, от 20 до 25 мг/мл, при температуре от 0 до 26°C.
12) Экструзия через сито с размером ячеек от 50 до 500 мкм, предпочтительно, от 100 до 250 мкм. Указанную фильтрацию выполняют при комнатной температуре или при температуре от 25 до 65°C, предпочтительно, от 40 до 60°C.
13) Заполнение шприцев, предпочтительно, изготовленных из стекла или полимерного материала, полученным продуктом.
14) Тепловая стерилизация насыщенным паром при температуре от 120 до 124°C (предпочтительно, 121,5±1°C) в течение по меньшей мере 10 мин.
Новый способ получения B включает следующие стадии:
Синтез поперечносшитой HBC
1) Растворение в щелочном растворе (предпочтительно, 0,15M-0,35M NaOH) диэпоксидного BDDE в стехиометрическом соотношении от 2,5 до 25% моль, предпочтительно, от 5 до 15% моль (в зависимости от предполагаемого применения продукта) повторяющихся звеньев гиалуроновой кислоты, с последующим
2) диспергированием HA в растворе, описанном в предыдущем абзаце, при комнатной температуре. Концентрация HA должна составлять от 80 до 300 мг/мл, и время гомогенизации от 30 до 300 минут.
3) Запуск реакции тепловой активацией, причем указанный раствор нагревают при температуре от 35 до 55°C в течение от 2 до 36 часов.
4) Доведение pH до нейтрального водным раствором HCl, имеющим концентрацию от 0,05 до 1 моль/л, предпочтительно, 0,1 моль/л.
5) Гидратация геля разведением его водой фактором 3 к 20 в течение периода времени от 4 до 48 часов при температуре от 4 до 24°C. Этот раствор может содержать другие эксципиенты, такие как NaCl, натриевая и калиевая соль фосфорной кислоты и лидокаин, предпочтительно, в форме гидрохлорида. Натриевые соли (хлорид и фосфат) выполняют функцию поддержания соответствующей осмолярности продукта и поддержания pH на уровне величины, сравнимой с pH тканей. В предпочтительном варианте осуществления изобретения NaCl добавляют в таком количестве, чтобы конечный раствор содержал его в концентрации от 0,8 до 1,0%, предпочтительно, 0,9%; гидрохлорид лидокаина, в случае его присутствия, добавляют в таком количестве, чтобы конечный состав содержал его в количестве от 2,2 до 3,2 мг/мл, предпочтительно, 2,7 мг/мл.
Смешивание ACP (или HYADD) с HBC
6) Смешивание геля HBC с порошком ACP (или HYADD) при соотношении ACP:HBC от 10:90 до 90:10 (по массе активного ингредиента) в зависимости от выбранного применения нового наполнителя, как описано выше. Альтернативно, ACP или HYADD могут быть смешаны с HBC, начиная с обоих компонентов в форме геля, с использованием подходящего перемешивающего устройства (предпочтительно, орбитальной лопаточной мешалки) в течение периода времени от 30 минут до 24 часов при температуре от 0 до 26°C.
7) Дробление и гомогенизация пропусканием через фильтр с коэффициентом удерживания вещества в виде частиц от 25 до 150 мкм, предпочтительно, от 40 до 110 мкм. Если вязкость избыточна, то операция может быть выполнена при высокой температуре от 25 до 65°C.
8) Заполнение шприцев, изготовленных для стекла или полимерного материала, полученным продуктом.
9) Стерилизация нагреванием от насыщенного пара при температуре от 120 до 124°C (предпочтительно, 121,5±1°C) в течение по меньшей мере 10 мин.
Некоторые примеры получения нового наполнителя в соответствии с изобретением описаны ниже в качестве примера, но не ограничения.
Пример 1: Синтез HBC 500 (HA 500-730 кДа)
Способ A
0,075 моля HA с молекулярной массой 500-730 кДа, полученного ферментацией диспергируют в 215 мл раствора 0,25M NaOH, содержащего 1,41 мл BDDE. Затем смесь нагревают до 42°C и подвергают взаимодействию в течение 3 часов. Затем смесь гидратируют в течение 24 ч 300 мл раствора, содержащего стехиомтерическое количество HCl, для доведения pH до нейтрального. Общий объем доводят до 750 мл и осаждают 2,5 объемами этанола с получением фильтруемого удаляемого осадка. Смесь промывают 75% этанолом до полного осаждения, верифицированного измерением удельной проводимости промывающих растворителей, которая должна составлять менее 30 мкСм/см, и сушат в вакууме при 40°C в течение 5 дней. Продукт HBC получают с массовым выходом 87%.
Пример 2: Синтез HBC 1000 (HA 1 мДа)
Способ A
1,60 г HA со средней молекулярной массой 1 мДа, полученную ферментацией, диспергируют в 20 мл 0,25M раствора NaOH, содержащего 75 мкл BDDE. Затем смесь нагревают до 42°C и подвергают взаимодействию в течение 2 часов. Затем смесь гидролизируют в течение 24 ч 20 мл раствора, содержащего стехимометрическое количество HCl, для доведения pH до нейтрального. Общий объем доводят до 75 мл и HBC осаждают 2,5 объемами этанола с получением фильтруемого удаляемого осадка. Смесь промывают 75% этанолом до полной очистки, верифицированной измерением удельной проводимости промывающих растворителей, которая должна быть ниже 30 мкСм/см, и сушат в вакууме при 40°C в течение 5 дней. Продукт HBC 1000 получают с массовым выходом 90%.
Пример 3: Синтез HBC 200 (HA 200 кДа)
Способ A
2,55 г HA со средней молекулярной массой 200 кДа, полученной ферментацией, диспергируют в 20 мл 0,25M раствора NaOH, содержащего 63 мкл BDDE. Затем смесь нагревают до 42°C и подвергают взаимодействию в течение 150 минут. Затем смесь гидратируют в течение 24 ч 20 мл раствора, содержащего стехиометрическое количество HCl. Общий объем доводят до 75 мл и осаждают 2,5 объемами этанола с получением фильтруемого удаляемого осадка. Смесь промывают 75% этанолом до достижения полной очистки, верифицированной измерением удельной проводимости промывающих растворителей, которая должна составлять менее 30 мкСм/см, и сушат в вакууме при 40°C в течение 5 дней. Продукт HBC 200 получают с массовым выходом 85%.
Пример 4: получение геля ACP:HBC 500 в соотношении 50:50
Способ A
1,00 г HBC 500, полученной, как описано в примере 1, смешивают с 1,00 г внутреннего сложного эфира HA ACP. Порошок гидратируют 100 мл 0,9% мас./об. стерильного солевого раствора при температуре 8°C в течение 16 часов. Полученный гель нагревают до 48°C, фильтруют через металлическое сито с размером ячеек 0,17 мм и затем распределяют между стеклянными шприцами емкостью 1 мл, которые впоследствии подвергают циклу стерилизации насыщенным паром при температуре 121°C в течение 10 минут. Получают однородный стерильный гель, подходящий для местного введения.
Пример 5: получение геля ACP:HBC 1000 в соотношении 30:70
Способ A
1,40 г HBC 1000, полученной, как описано в примере 2, смешивают с 0,60 г внутреннего сложного эфира HA ACP. Порошок гидратируют 100 мл 0,9% мас./об. стерильного солевого раствора при температуре 8°C в течение 16 часов. Полученный гель нагревают до 48°C, фильтруют через металлическое сито с размером ячеек 0,17 мм и затем распределяют по стеклянным шприцам емкостью 1 мл, которые впоследствии подвергают циклу стерилизации насыщенным паром при температуре 121°C в течение 10 минут. Получают однородный стерильный гель, подходящий для местного введения.
Пример 6: получение геля ACP:HBC 500 в соотношении 25:75
Способ A
1,875 г HBC 500, полученной, как описано в примере 1, смешивают с 0,625 г внутреннего сложного эфира HA ACP. Порошок гидратируют 100 мл 0,9% мас./об. стерильного солевого раствора при температуре 8°C в течение 16 часов. Полученный гель нагревают до 48°C, фильтруют через металлическое сито с размером ячеек 0,19 мм и затем разливают в стеклянные шприцы емкостью 1 мл, которые впоследствии подвергают циклу стерилизации насыщенным паром при температуре 121°C в течение 12 минут. Получают однородный стерильный гель, подходящий для местного введения.
Пример 7: получение геля ACP:HBC 1000 в соотношении 75:25
Способ A
0,50 г HBC 1000, полученной, как описано в примере 2, смешивают с 1,50 г внутреннего сложного эфира HA ACP. Порошок гидратируют 100 мл 0,9% мас./об. стерильного солевого раствора при температуре 8°C в течение 24 часов. Полученный гель нагревают до 42°C, фильтруют через металлическое сито с размером ячеек 0,17 мм и затем разливают в стеклянные шприцы емкостью 2 мл, которые впоследствии подвергают циклу стерилизации насыщенным паром при температуре 121°C в течение 12 минут. Получают однородный стерильный гель, подходящий для местного введения.
Пример 8: получение геля HYADD:HBC, в соотношении 60:40
Способ A
1,20 г HBC 500, полученной, как описано в примере 1, смешивают с 0,80 г гексадециламида HA (HYADD). Порошок гидратируют 100 мл 0,9% мас./об. стерильного солевого раствора при температуре 8°C в течение 24 часов. Полученный гель нагревают до 52°C, фильтруют через металлическое сито с размером ячеек 0,17 мм и затем разливают в стеклянные шприцы емкостью 1 мл, которые впоследствии подвергают циклу стерилизации насыщенным паром при температуре 121°C в течение 11 минут. Получают однородный стерильный гель, подходящий для местного введения.
Пример 9: получение геля HYADD:HBC 500 в соотношении 40:60
Способ A
8,0 г натриевой соли HA со средней молекулярной массой 500-730 кДа, полученной ферментацией, диспергируют в 40 мл 0,25M раствора NaOH, содержащего 0,44 мл BDDE. Смесь нагревают при 41,5°C в течение 2 часов 40 минут. Затем ее гидратируют в течение ночи 100 мл 0,1M раствора HCl и 200 мл воды. Добавляют 50 мл насыщенного раствора NaCl, и смесь оставляют для набухания в течение ночи. На следующий день добавляют 170 мл ацетона и 30 мл насыщенного раствора NaCl, и смесь осаждают медленным добавлением одного литра этанола. Осадок промывают таким же растворителем до устранения остатков NaCl, затем сушат в печи при 35°C в вакууме до тех пор, пока не удаляются остаточные растворители. Полученный таким образом порошок HBC смешивают в соотношении 5:3 с HYADD, полученным, как описано в патенте EP 1853279. Смешанные порошки гидратируют солевым раствором, приводя к общей концентрации 20 мг/мл (соответствующей 12,5 мг/мл HBC и 7,5 мг/мл HYADD4). Продукт оставляют для набухания при 5°C и на следующий день фильтруют через плоскую мембрану с номинальной степенью удерживания 100 мкм. Стеклянные шприцы емкостью 1 мл заполняют полученным таким образом продуктом и стерилизуют в цикле с F0=13 при 121,5°C.
Пример 10: Наполнение кожи и переносимость геля HYADD:HBC на модели внутридермального введения кроликам
Целью эксперимента была оценка наполнения кожи, выявление начала любых макроскопических побочных эффектов и тканевой реакции, вызванной гелем HYADD:HBC (полученным, как описано в примере 9), инъецированным во внутридермальную ткань кролика, путем сравнения с коммерческим наполнителем BELOTERO®.
Для указанной оценки, тестируемые гели вводили внутридермально самцам кроликов NZW-KBL с массой тела 1,8-2,3 кг.
Структура эксперимента:
Животных анестезировали внутривенным введением кетамина и ксилазина. Для каждого тестируемого наполнителя использовали 3 животных.
День 0: T0
инъекция образцов (1 мл гидрогеля на образец) после бритья спины кроликов;
измерение набухания на кроликах и макроскопическое наблюдение для выявления побочных явлений.
День 7: T7
Измерение объема набухания и макроскопическое наблюдение для выявления побочных явлений.
Объем набухания рассчитывали по формуле:
(2/3×π)×(r1)×(r2)×(r3)
где: (r1), (r2) и (r3) представляют соответственно ширину, длину и высоту набухания, измеренные циркулем.
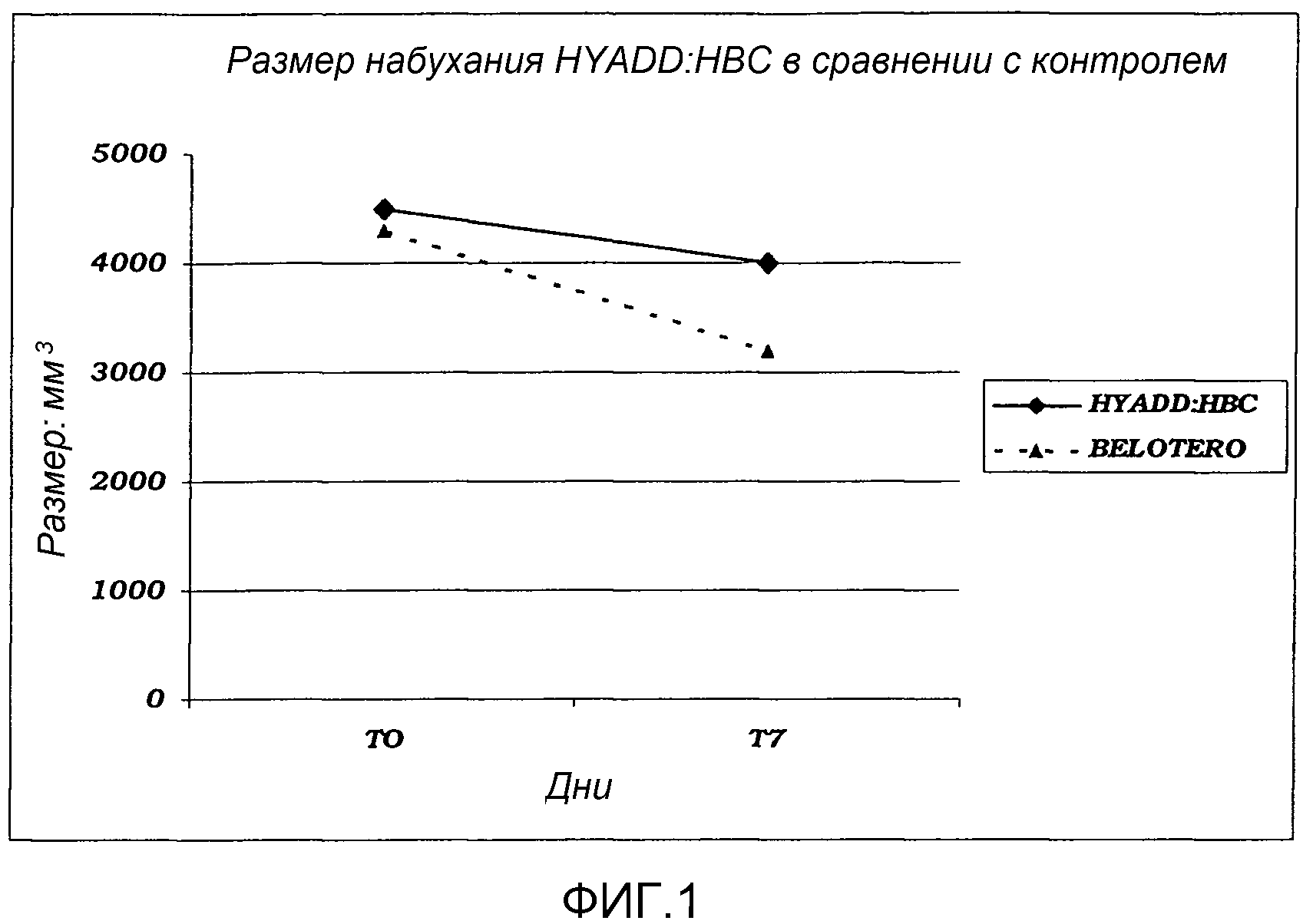
Результаты:
Новый наполнитель не вызывал каких-либо воспалительных явлений в обработанной дерме.
Результаты, полученные для времени пребывания в ткани, показаны на фиг.1: количественная оценка набухания, оцененная в первую неделю обработки (выраженная в виде мм3) продемонстрировала, что гель согласно изобретению способен вызывать больший, чем в контроле, объем набухания кожи, который оставался высоким даже через 7 дней, тоже в гораздо большей степени, чем коммерческий наполнитель, используемый в качестве сравнения. Эти данные ясно подтверждают, что новые наполнители немедленно вызывают значительную гидратацию дермы, и данный эффект можно отнести на счет присутствия производного HYADD, которое ввиду его химических/реологических характеристик оказалось существенным для содействия немедленному наполнению кожи, которое остается стабильным с течением времени.
Пример 11: Синтез HBC 500 (HA 500-730 кДа)
Способ B
18,75 г натриевой соли HA с молекулярной массой 500-730 кДа, полученной ферментацией, диспергируют в 133 мл 0,25M растворе NaOH, содержащем 885 мкл BDDE. Затем смесь нагревают при 45°C в течение 2,5 часов. Смесь гидратируют в течение ночи 0,62 л раствора, содержащего стехиометрическое количество HCl, 2,65 г NaCl и 2,7 г гидрохлорида лидокаина, при медленном перемешивании.
Пример 12: получение геля ACP:HBC 500 в соотношении 25:75
Способ B
6,25 г внутреннего эфира гиалуроновой кислоты ACP 200 солюбилизируют в 250 мл раствора, содержащего 4,4 г NaCl, при медленном перемешивании. Когда гидратация завершена, гель объединяют с гелем, полученным в соответствии с примером 11, в миксере, оборудованном устройством для смешивания полутвердых веществ до гомогенности. Полученный гель подвергают экструзии через плоский мембранный фильтр с номинальной степенью удерживания вещества в виде частиц 70 мкм. Полученный таким образом продукт вводят в стеклянные шприцы и стерилизуют в цикле с F0=13 при 121,5°C.
Пример 13: получение геля HYADD:HBC 500 в соотношении 25:75
Способ B
6,25 г гексадециламида HYADD солюбилизируют в 250 мл раствора, содержащего 4,4 г NaCl, при медленном перемешивании. Когда гидратация завершена, гель объединяют с гелем, полученным в соответствии с примером 11, в миксере, оборудованном орбитальным смешивающим устройством, до однородности. Полученный гель подвергают экструзии через плоский мембранный фильтр с номинальной степенью удерживания материала в виде частиц 70 мкм. Полученный таким образом продукт вводят в стеклянные шприцы и стерилизуют в цикле с FO=13 при 121,5°C.
Пример 14: Синтез HBC 500 (HA 500-730 кДа)
Способ B
125 г натриевой соли HA с молекулярной массой 500-730 кДа, полученной ферментацией, диспергируют в 1,33 л 0,25M раствора NaOH, содержащего 9,4 мл BDDE. Смесь нагревают при 45°C в течение 2,5 часов. Смесь гидратируют в течение ночи 6,2 л раствора, содержащего стехиометрическое количество HCl, 26,5 г NaCl и 27 г гидрохлорида лидокаина, при медленном перемешивании.
Пример 15: осаждение геля ACP:HBC 500 в соотношении 50:50
Способ B
125 г внутреннего эфира гиалуроновой кислоты ACP200 солюбилизируют в 2,5 л раствора, содержащего 44 г NaCl, при медленном перемешивании. Когда гидратация завершена, гель объединяют с гелем, полученным в соответствии с примером 14, в миксере, оборудованном орбитальным смешивающим устройством с отражательной перегородкой и скребком. Полученный гель подвергают экструзии через плоский мембранный фильтр с номинальной степенью удерживания материала в виде частиц 45 мкм. Полученный таким образом продукт вводят в стеклянные шприцы и стерилизуют в цикле с FO=13 при 121,5°C.
Пример 16: Наполнение кожи и переносимость геля ACP:HBC на модели внутридермального введения кроликам
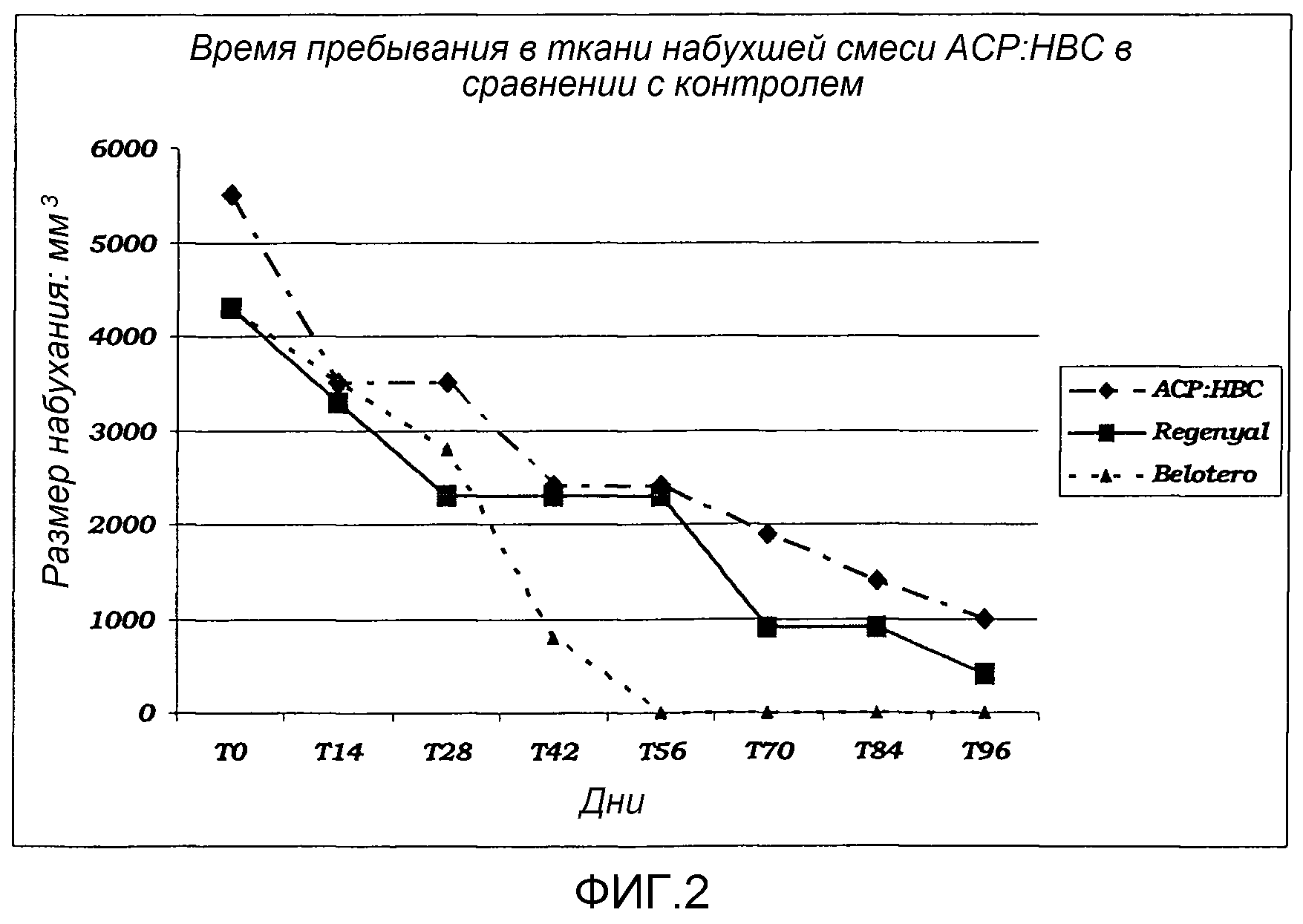
Эксперимент выполняли, как описано в примере 10, с использованием геля, полученного, как описано в примерах 11-12, и сравнением его с контролем Belotero® и со вторым коммерческим наполнителем, Regenyal Idea.
Для данного эксперимента, автор не только определил объем набухания кожи, вызванного обработкой, но также оценил общее время пребывания в ткани геля/наполнителя согласно изобретению путем сравнения с двумя хорошо известными коммерческими наполнителями, которые представляют собой конечный сравнительный образец, потому что они оба состоят из HA, поперечносшитой с BDDE.
Набухание кожи у кроликов после обработки измеряли раз в две недели (с макроскопическим наблюдением для выявления побочных явлений) в течение максимум 96 дней.
Результаты:
На фиг.2 показаны полученные результаты: были подтверждены описанные выше данные, а именно немедленная гидратация обработанной дермы (главным образом, в течение первых 7 дней) в удивительно большей степени, чем у контролей; кроме того, размер набухания кожи был более очевиден, и время пребывания в ткани более длительное, чем данные показатели у двух коммерческих образцов сравнения. В конце эксперимента новый наполнитель согласно изобретению еще присутствовал, в то время как оба контрольных образца почти исчезли.
Следует понимать, что способы, описанные в данном описании, могут быть модифицированы различными путями. Такие модификации не должны рассматриваться как отходящие от сущности и перспектив изобретения, и все модификации, которые могли бы показаться очевидными для специалиста в данной области, включены в объем следующей формулы изобретения.