Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ ГРАМОТРИЦАТЕЛЬНЫХ ПАТОГЕННЫХ БАКТЕРИЙ В АНАЛИЗИРУЕМОЙ СРЕДЕ
Вид РИД
Изобретение
Изобретение относится к электрохимическим методам анализа, а именно к иммуноанализу, в частности к определению содержания патогенных микроорганизмов в различных объектах и средах. Изобретение может быть использовано в микробиологии, медицине, экологии для мониторинга содержания патогенных микроорганизмов в природных объектах и дифференциальной диагностики инфекционных заболеваний.
Недостатками используемых в настоящее время методов являются: низкая чувствительность (реакции агглютинации), высокая стоимость используемых реагентов и оборудования (иммуноферментный анализ), необходимость создания специальных условий (метод анализа, основанный на полимеразной цепной реакции) и длительность проведения анализа (бактериальный посев).
Для мониторинга колиформных бактерий, продуцирующих в результате своей жизнедеятельности фенол, предлагают использовать амперометрический тирозиназный сенсор и аминомодифицированный магнетит, осажденный на углеродных нанотрубках. Эту систему используют для детектирования фенола. Тирозиназа катализирует окисление фенольных соединений в присутствии кислорода с получением о-хинонов, которые могут быть восстановлены электрохимически при низких потенциалах без медиаторов. Однако в данном методе требуется ≈4 часа для предварительной активации β-D-галактрозидазы и другие длительные подготовительные процедуры. Отсутствие специфичности реакции также является недостатком данного метода (Amperometric tyrosinase biosensor based on Fe3O4 nanoparticles-coated carbon nanotubes nanocomposite for rapid detection of coliforms/Yuxiao Cheng, Yajun Liu, Jingjing Huang et all//Electrochimica Acta, 2009, V.54, P.2588-2594).
Предложен метод обнаружения бактерий E.Coli при помощи кварцевого сенсора с использованием наночастиц магнетита, покрытых декстраном, и наночастиц золота, покрытых стрептавидином. Данный метод до момента непосредственного детектирования включает в себя 7 предварительных стадий (таких как инкубирование, сепарирование, декантирование). Помимо значительного увеличения продолжительности анализа, все эти стадии вносят огромный вклад в погрешность измерения (QCM immunosensor detection of Escherichia coli O157:H7 based on beacon immunomagnetic nanoparticles and catalytic growth of colloidal gold/Zhi-Qiang Shen, Jing-Feng Wang, Zhi-Gang Qiu et all/Biosensors and Bioelectronics, 2011, V.26, P.3376-3381).
Также для детектирования бактерий E.Coli предложено использовать магнитоэластичный сенсор, модифицированный полиуретаном и наночастицы магнетита модифицированные хитозаном. Подготовленный сенсор помещается в кювету с суспензией магнетита, модифицированного хитозаном, и E.Coli. Затем вся система помещается в катушку соленоида, от которой получают сигнал. Измеряется резонансная частота сенсора. При pH 5-6.5 бактерии электростатически притягиваются к наночастицам, затем наночастицы примагничиваются к сенсору, уменьшая его резонансную частоту. Однако данный метод также лишен специфичности (Detection of pathogen Escherichia coli O157:H7 with a wireless magnetoelastic-sensing device amplified by using chitosan-modified magnetic Fe3O4 nanoparticles/Hailan Lin, Qingzhu Lu, Shutian Ge, Qingyun Cai et all//Sensors and Actuators B, 2010, V.147, P.343-349).
Наиболее близким техническим решением, выбранным в качестве прототипа, служит способ определения патогенных микроорганизмов, включающий конъюгацию патогенного микроорганизма с магнитными наночастицами в анализируемой среде с последующим концентрированием конъюгатов и определением наличия и концентрации патогенных микроорганизмов с помощью электроактивной сигналообразующей метки. В качестве магнитных наночастиц и, одновременно, электроактивной сигналообразующей метки авторы использовали наночастицы переходного металла. Перед концентрированием меченых конъюгатов наночастицы, несвязанные с патогенными микроорганизмами, выводили из анализируемой среды. Концентрирование меченого конъюгата осуществляли путем формирования на электроде иммунокомлекса «меченный магнитной меткой патогенный микроорганизм - антитело» с последующим изъятием иммунокомплекса из среды на электроде. Далее проводили кислотную обработку электрода, содержащего меченый иммунокомплекс. Определение наличия и концентрации патогенных микроорганизмов осуществляли по сигналу, генерируемому ионами переходного металла, получаемых путем кислотного разрушения иммунокомплекса (Патент РФ №2397243 от 20.08.2010).
К недостаткам данного способа следует отнести многостадийность процесса анализа, низкий предел обнаружения, высокую трудоемкость процесса, большие временные затраты, а также высокие требования к квалификации операторов.
Предлагаемое техническое решение направлено на упрощение анализа, увеличение чувствительности, экспрессности, воспроизводимости, а также на расширение круга электрохимически активных меток.
Указанный технический эффект достигается тем? что предлагаемый способ электрохимического иммуноанализа включает в себя конъюгацию патогенных микроорганизмов с электроактивными магнитными нанокомпозитными частицами, магнитную сепарацию с последующим концентрированием конъюгатов и определением наличия и концентрации патогенных микроорганизмов с помощью сигналобразующей метки, локализованной путем образования иммунокомплекса на поверхности электрода, в качестве которой выступают электроактивные магнитные нанокомпозитные частицы. Концентрацию патогенных микроорганизмов определяют путем получения прямого электрохимического отклика от электроактивных магнитных нанокомпозитных частиц, регистрируемого в результате электрохимического превращения электроактивного полимерного покрытия (полимерного покрытия, модифицированного электроактивными соединениями) наночастиц.
Указанные отличительные признаки существенны. Получение электрохимического отклика от метки в результате разряда непосредственно электроактивного полимерного покрытия (полимерного покрытия, модифицированного электроактивными соединениями) электроактивных магнитных нанокомпозитных частиц позволит исключить из процедуры иммуноанализа стадию кислотного разложения иммунокомплекса и увеличить экспрессность и чувствительность способа определения патогенных микроорганизмов.
Кроме того, создание на поверхности магнитных наночастиц электроактивного полимерного покрытия (полимерного покрытия, модифицированного электроактивными соединениями) приводит к уменьшению поверхностной энергии наночастиц и позволит предотвратить их агрегацию, в результате чего размер частиц не изменяется в течение эксперимента. Таким образом, использование полимерного покрытия позволит добиться высокой чувствительности и воспроизводимости анализа.
Использование магнитных нанокомпозитных частиц с электроактивным полимерным покрытием (полимерным покрытием, модифицированным электроактивными соединениями) позволит расширить круг потенциальных электрохимически активных меток
Предложенный способ иммуноанализа позволит существенно снизить материало- и трудозатраты на проведение анализа, увеличить производительность и уменьшить себестоимость определения.
Таким образом, из патентной и научно-технической литературы не известен способ определения патогенных микроорганизмов заявляемой совокупности признаков.
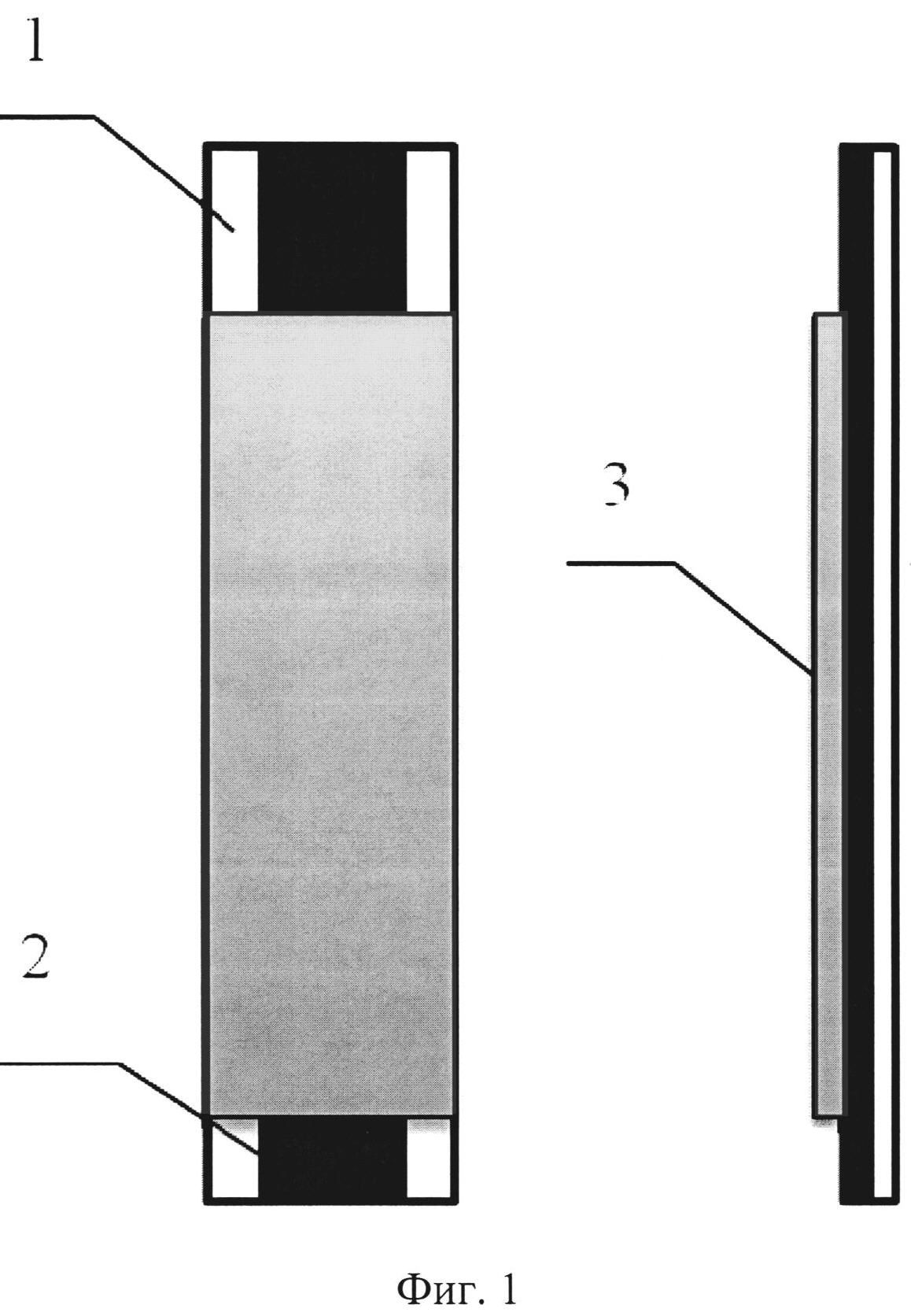
На фигуре 1 изображен общий вид рабочего электрода, где 1 - подложка из стеклотекстолита, 2 - дорожка из токопроводящего материала (графитовая композиция, углеродные чернила), 3 - слой изолятора или цементита.
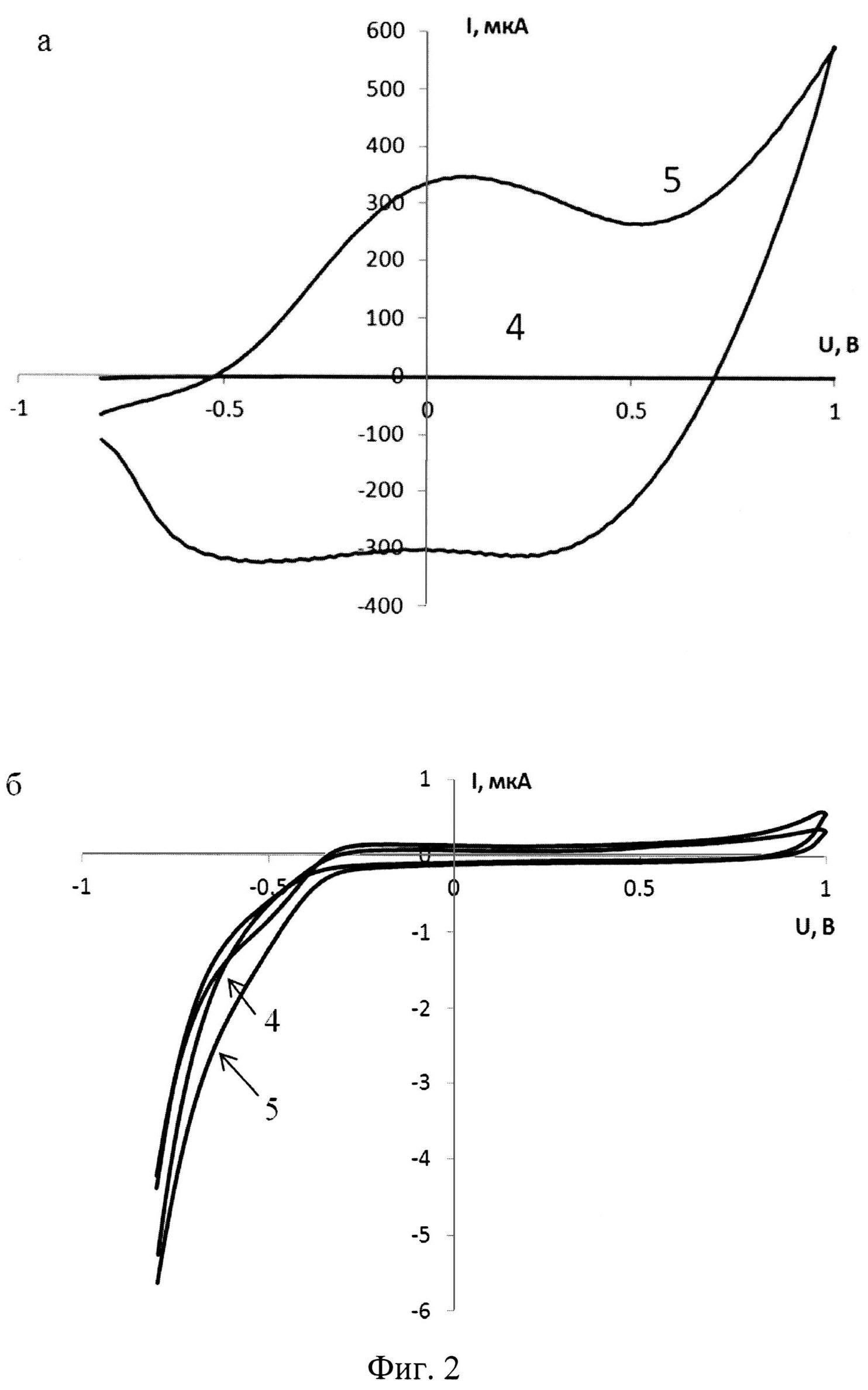
На фигуре 2 представлены циклические вольтамперограммы, зарегистрированные в модельных растворах, содержащих (а, 4-5) и не содержащих (б, 4-5) микроорганизмы Е.Coli (штамм O-12).
4 - вольтамперограмма фонового электролита, 5 - вольтамперограмма модельного раствора.
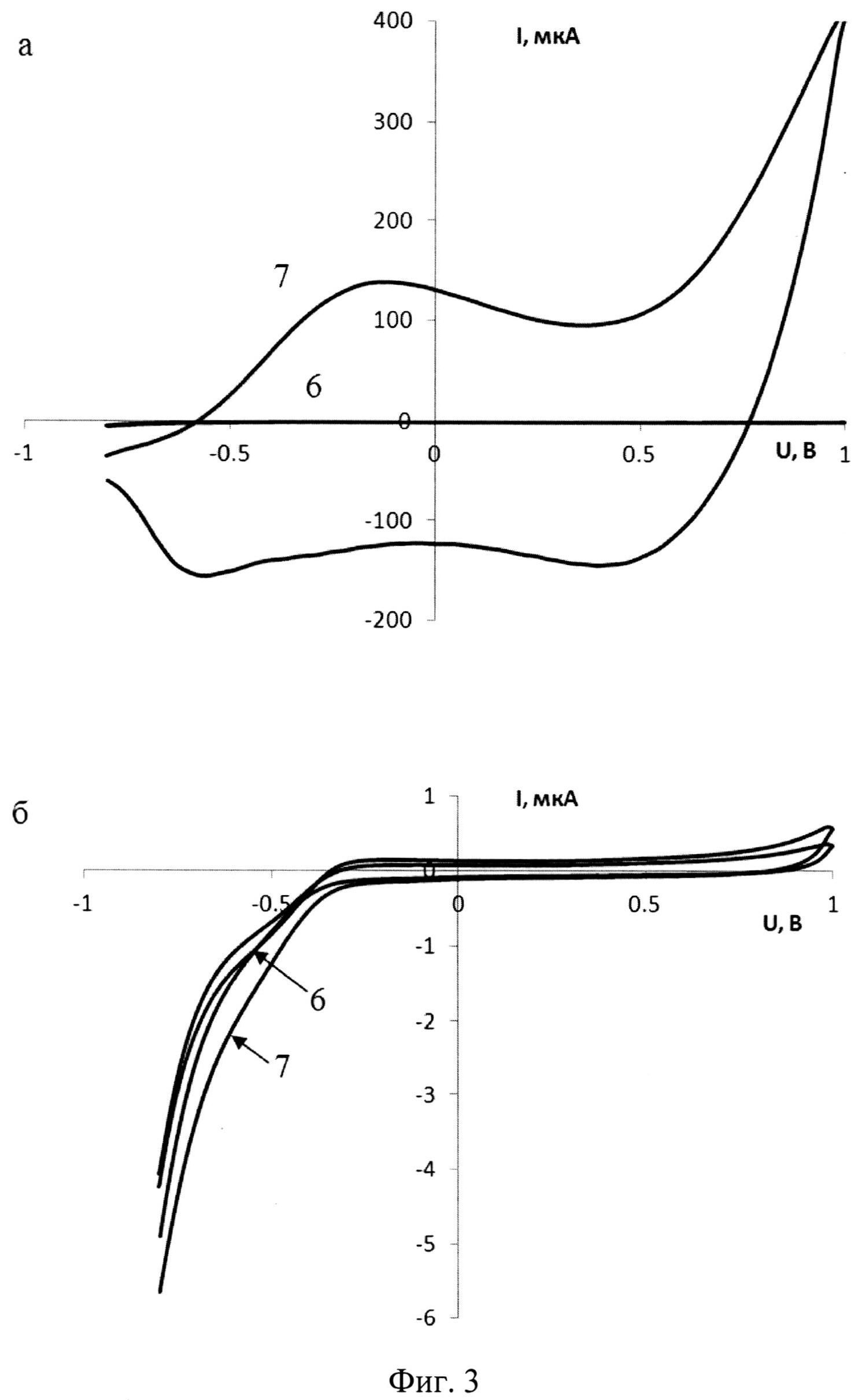
На фигуре 3 представлены циклические вольтамперограммы, зарегистрированные в пробах, содержащих (а, 6-7) и не содержащих (б, 6-7) микроорганизмы Е.Coli (штамм O-12).
6 - вольтамперограмма фонового электролита, 7 - вольтамперограмма пробы.
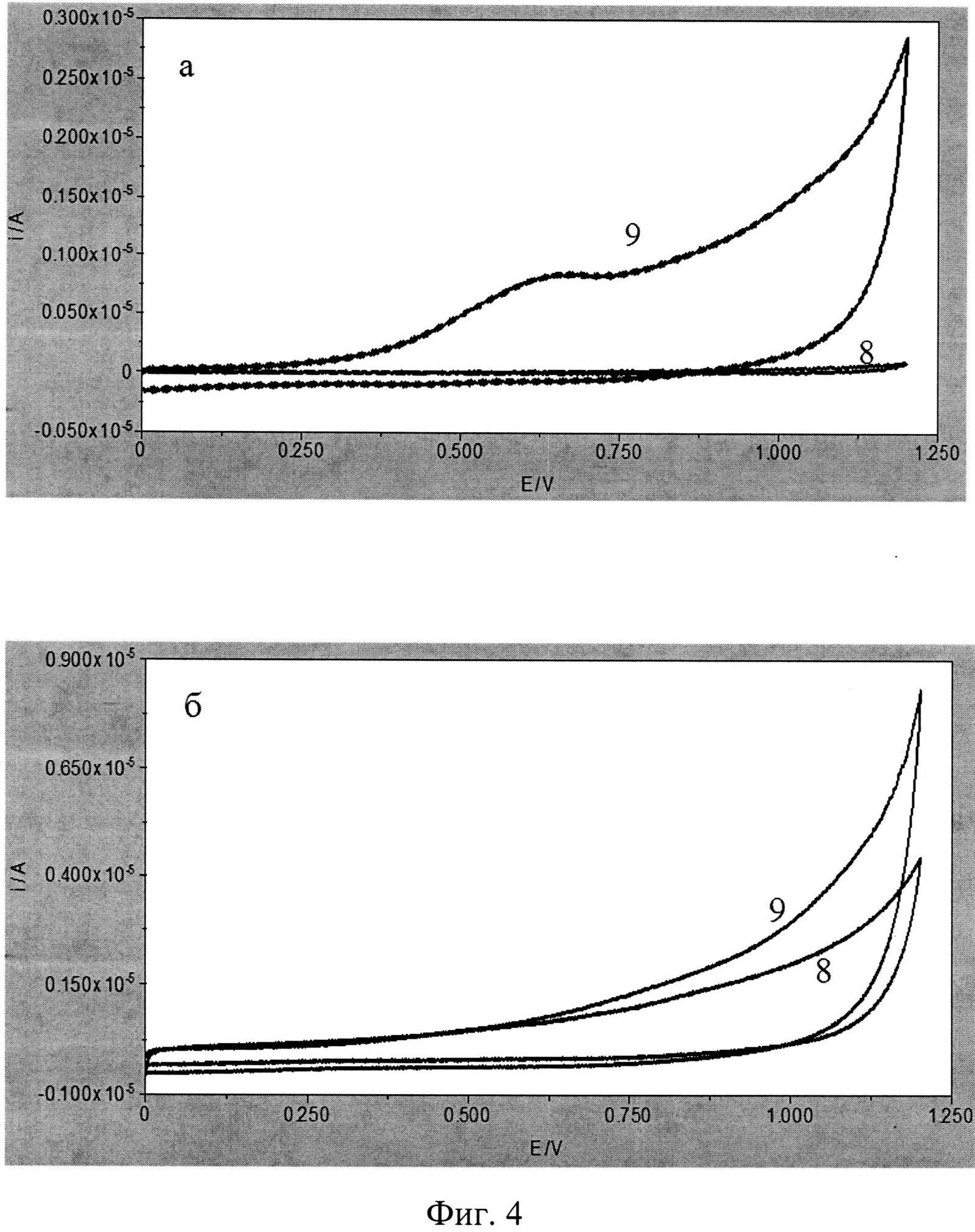
На фигуре 4 представлены циклические вольтамперограммы, зарегистрированные в пробах, содержащих (а, 8-9) и не содержащих (б, 8-9) микроорганизмы Е.Coli (штамм O-12).
8 - вольтамперограмма фонового электролита, 9 - вольтамперограмма пробы.
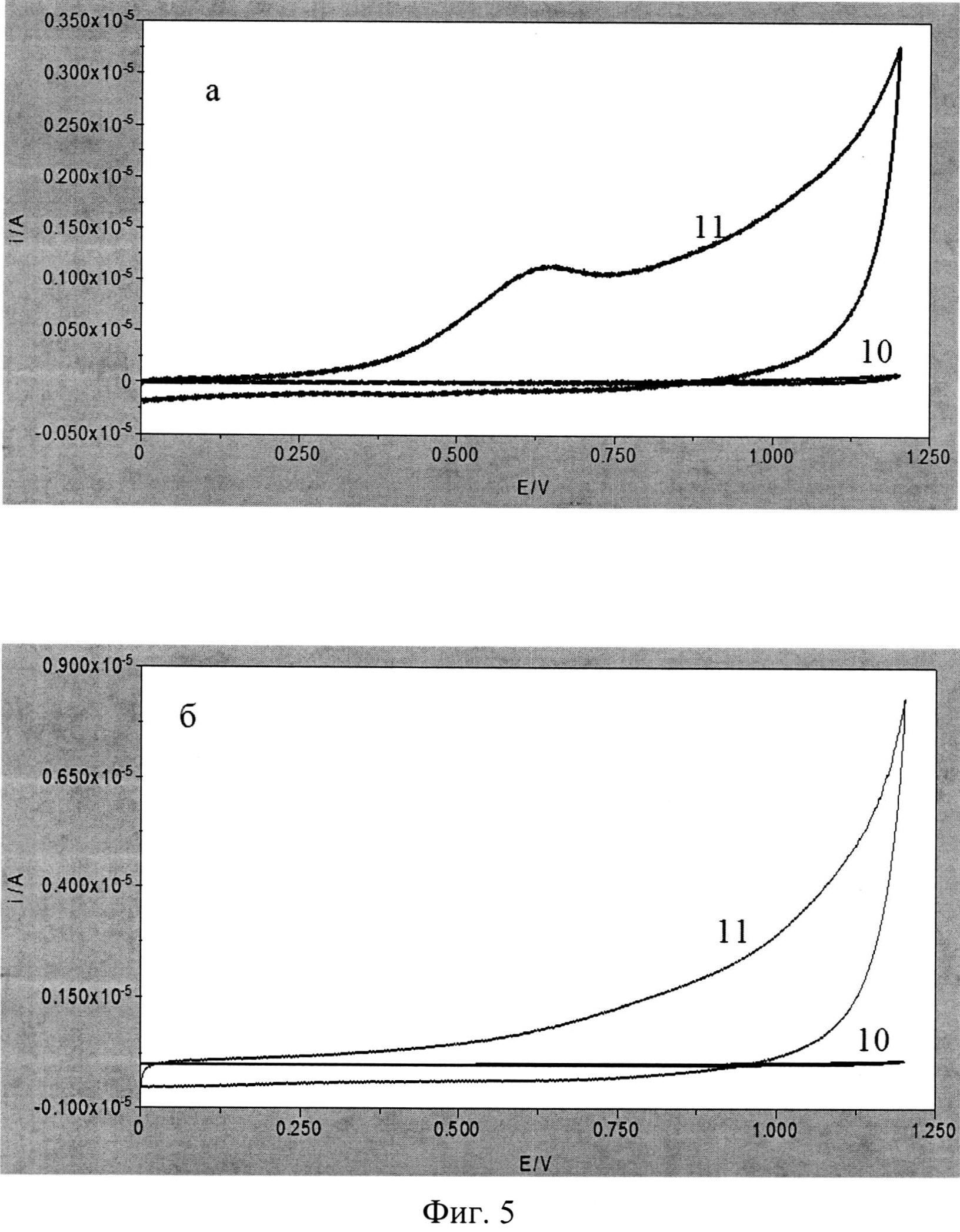
На фигуре 5 представлены циклические вольтамперограммы, зарегистрированные в пробах, содержащих (а, 10-11) и не содержащих (б, 10-11) микроорганизмы Е.Coli (штамм O-12).
10 - вольтамперограмма фонового электролита, 11 - вольтамперограмма пробы.
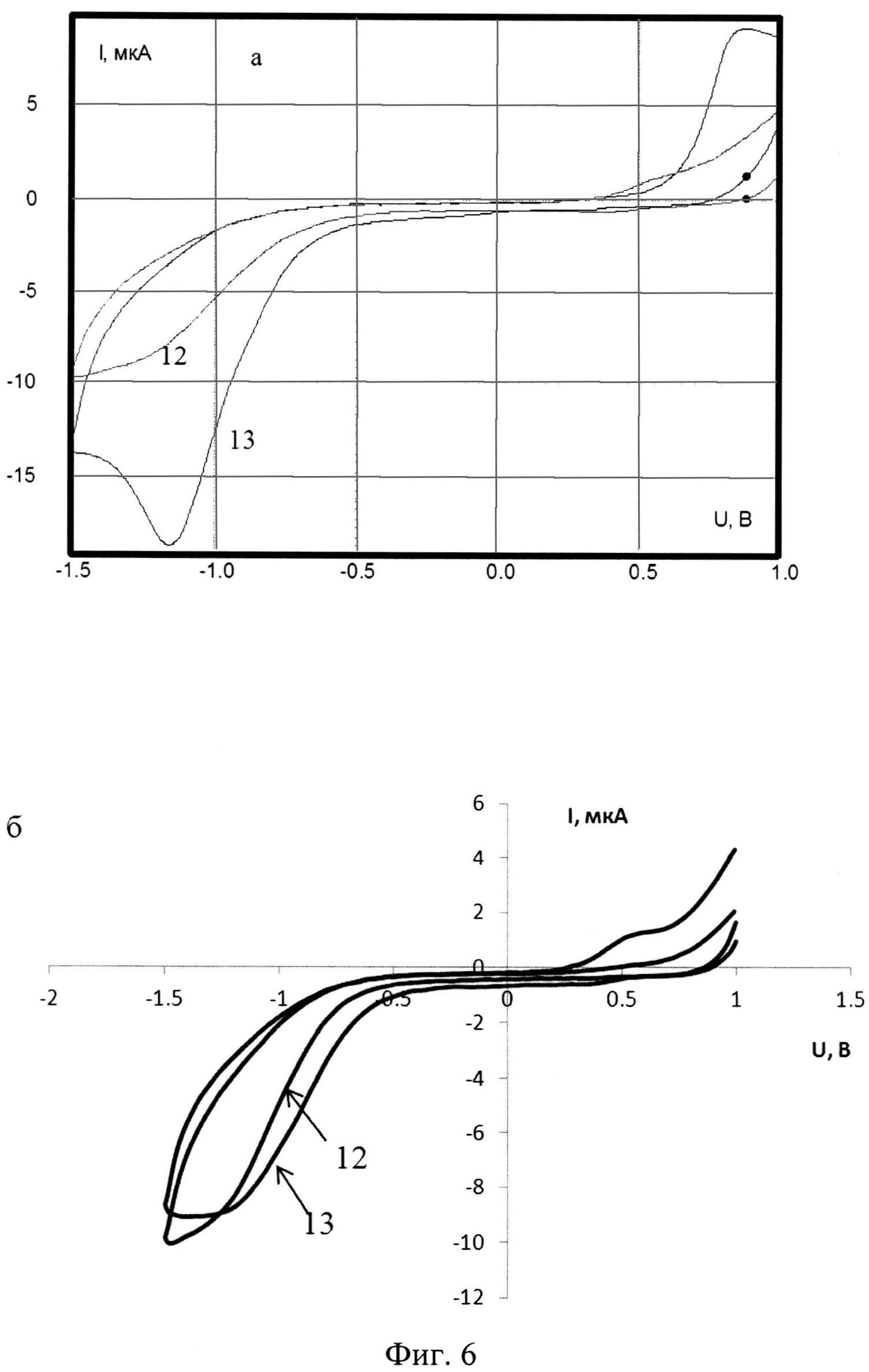
На фигуре 6 представлены циклические вольтамперограммы, зарегистрированные в модельных растворах, содержащих (а, 12-13) и не содержащих (б, 12-13) микроорганизмы Salmonella typhimurium (штамм SL 7207).
12 - вольтамперограмма фонового электролита, 13 - вольтамперограмма модельного раствора.
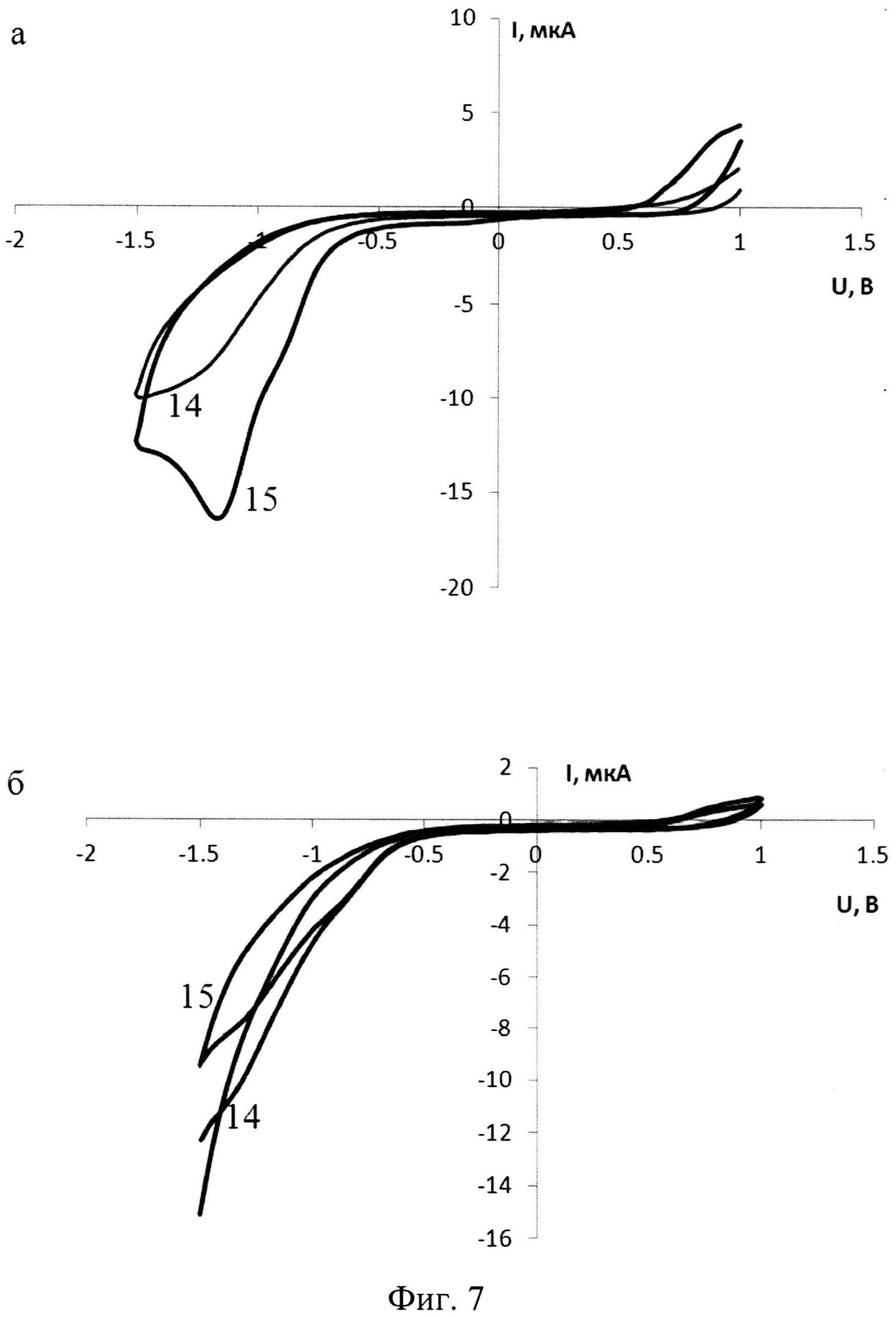
На фигуре 7 представлены циклические вольтамперограммы, зарегистрированные в пробах, содержащих (а, 14-15) и не содержащих (б, 14-15) микроорганизмы Salmonella typhimurium (штамм SL 7207).
14 - вольтамперограмма фонового электролита, 15 - вольтамперограмма пробы.
Способ иллюстрируется следующими примерами.
Пример 1.
Вытяжку анализируемой среды (модельного раствора) инкубируют в течение 30 минут с электроактивными магнитными нанокомпозитными частицами Fe3O4-полипиррол при температуре 37°С. После инкубации несвязавшиеся электроактивные магнитные нанокомпозитные частицы отделяют с использованием магнитного поля. В подготовленную таким образом вытяжку помещают ТГЭ (фиг.1), модифицированный антителами против Е.Coli (штамм O-12), и выдерживают в течение 20 минут при температуре 37°С. Для ускорения доставки меченых микроорганизмов к поверхности сенсора используют магнитное поле. Затем электрод промывают буферным раствором, содержащим нормальную лошадиную сыворотку (НЛС) и твин-20. Извлеченный из анализируемого раствора электрод помещают в электрохимическую ячейку. В качестве фонового электролита используют раствор KNO3 в воде. В качестве аналитического сигнала используют электрохимический отклик окисления полипиррольного покрытия электроактивных магнитных нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности ТГЭ. Для проведения холостого опыта используют раствор, не содержащий микроорганизмы Е.Coli (штамм O-12) (фиг.2). В модельном растворе обнаружили 5×103 клеток/мл микроорганизма Е.Coli (штамм O-12).
Пример 2.
Вытяжку анализируемой среды инкубируют в течение 30 минут с электроактивными магнитными нанокомпозитными частицами Fe-полипиррол при температуре 37°С. После инкубации несвязавшиеся электроактивные магнитные нанокомпозитные частицы отделяют с использованием магнитного поля. В подготовленную таким образом вытяжку помещают ТУЭ (фиг.1), модифицированный антителами против Е.Coli (штамм O-12), и выдерживают в течение 20 минут при температуре 37°С. Для ускорения доставки меченых микроорганизмов к поверхности сенсора используют магнитное поле. Затем электрод промывают буферным раствором, содержащим нормальную лошадиную сыворотку (НЛС) и твин-20. Извлеченный из анализируемого раствора электрод помещают в электрохимическую ячейку. В качестве фонового электролита используют 0,1 М раствор KNO3 в воде. В качестве аналитического сигнала используют электрохимический отклик окисления полипиррольного покрытия электроактивных магнитных нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности ТУЭ. Для проведения холостого опыта используют раствор, не содержащий микроорганизмы Е.Coli (штамм O-12) (фиг.3). В пробе, взятой у пациента, обнаружили 2×104 клеток/мл микроорганизма Е.Coli (штамм O-12).
Пример 3.
Вытяжку анализируемой среды инкубируют в течение 30 минут с электроактивными магнитными нанокомпозитными частицами Fe3O4-модифицированный ферроценом оксид кремния при температуре 37°С. После инкубации несвязавшиеся электроактивные магнитные нанокомпозитные частицы отделяют с использованием магнитного поля. В подготовленную таким образом вытяжку помещают ТГЭ (фиг.1), модифицированный антителами против Е.Coli (штамм O-12), и выдерживают в течение 20 минут при температуре 37°С. Для ускорения доставки меченых микроорганизмов к поверхности сенсора используют магнитное поле. Затем электрод промывают буферным раствором, содержащим нормальную лошадиную сыворотку (НЛС) и твин-20. Извлеченный из анализируемого раствора электрод помещают в электрохимическую ячейку. В качестве фонового электролита используют раствор KNO3 в воде. В качестве аналитического сигнала используют электрохимический отклик окисления ферроценовых групп полимерного покрытия электроактивных магнитных нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности ТГЭ. Для проведения холостого опыта используют раствор, не содержащий микроорганизмы Е.Coli (штамм O-12) (фиг.2). В пробе, взятой у пациента, обнаружили 1,5×103 клеток/мл микроорганизма Е.Coli (штамм O-12).
Пример 4.
Пробу воды инкубируют в течение 30 минут с электроактивными магнитными нанокомпозитными частицами Fe3O4-модифицированный ферроценом оксид кремния при температуре 37°С. После инкубации несвязавшиеся электроактивные магнитные нанокомпозитные частицы отделяют с использованием магнитного поля. В подготовленную таким образом вытяжку помещают ТУЭ (фиг.1), модифицированный антителами против Е.Coli (штамм O-12), и выдерживают в течение 20 минут при температуре 37°С. Для ускорения доставки меченых микроорганизмов к поверхности сенсора используют магнитное поле. Затем электрод промывают буферным раствором, содержащим нормальную лошадиную сыворотку (НЛС) и твин-20. Извлеченный из анализируемого раствора электрод помещают в электрохимическую ячейку. В качестве фонового электролита используют 0,1 М раствор KNO3 в воде. В качестве аналитического сигнала используют электрохимический отклик окисления ферроценовых групп полимерного покрытия электроактивных магнитных нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности ТУЭ. Для проведения холостого опыта используют раствор, не содержащий микроорганизмы Е.Coli (штамм O-12) (фиг.3). В пробе обнаружили 2,3×102 клеток/мл микроорганизма Е.Coli (штамм O-12).
Пример 5.
Вытяжку анализируемой среды (модельный раствор) инкубируют в течение 30 минут с электроактивными магнитными нанокомпозитными частицами Fe-модифицированный хинолином поливинилбензилхлорид при температуре 37°С. После инкубации несвязавшиеся электроактивные магнитные нанокомпозитные частицы отделяют с использованием магнитного поля. В подготовленную таким образом вытяжку помещают ТГЭ (фиг.1), модифицированный антителами против Salmonella typhimurium (штамм SL 7207), и выдерживают в течение 20 минут при температуре 37°С. Для ускорения доставки меченых микроорганизмов к поверхности сенсора используют магнитное поле. Затем электрод промывают буферным раствором, содержащим нормальную лошадиную сыворотку (НЛС) и твин-20. Извлеченный из анализируемого раствора электрод помещают в электрохимическую ячейку. В качестве фонового электролита используют раствор KNO3 в воде. В качестве аналитического сигнала используют электрохимический отклик восстановления хинолиновых групп полимерного покрытия электроактивных магнитных нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности ТГЭ. Для проведения холостого опыта используют раствор, не содержащий микроорганизмы Salmonella typhimurium (штамм SL 7207) (фиг.2). В модельном растворе обнаружили 6×103 клеток/мл микроорганизма Salmonella typhimurium (штамм SL 7207).
Пример 6.
Вытяжку анализируемой среды инкубируют в течение 30 минут с электроактивными магнитными нанокомпозитными частицами Fe3O4-модифицированный хинолином поливинилбензилхлорид при температуре 37°С. После инкубации несвязавшиеся электроактивные магнитные нанокомпозитные частицы отделяют с использованием магнитного поля. В подготовленную таким образом вытяжку помещают ТУЭ (фиг.1), модифицированный антителами против Salmonella typhimurium (штамм SL 7207), и выдерживают в течение 20 минут при температуре 37°С. Для ускорения доставки меченых микроорганизмов к поверхности сенсора используют магнитное поле. Затем электрод промывают буферным раствором, содержащим нормальную лошадиную сыворотку (НЛС) и твин-20. Извлеченный из анализируемого раствора электрод помещают в электрохимическую ячейку. В качестве фонового электролита используют раствор KNO3 в воде. В качестве аналитического сигнала используют электрохимический отклик восстановления хинолиновых групп полимерного покрытия электроактивных магнитных нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности ТУЭ. Для проведения холостого опыта используют раствор, не содержащий микроорганизмы Salmonella typhimurium (штамм SL 7207) (фиг.2). В пробе, взятой у пациента, обнаружили 3,7×102 клеток/мл микроорганизма Salmonella typhimurium (штамм SL 7207).
Способ определения содержания грамотрицательных патогенных бактерий в анализируемой среде, характеризующийся конъюгированием бактерий с электрохимической меткой, в качестве которой используют магнитные нанокомпозитные частицы на основе Fe, FeO с электроактивным полимерным покрытием из полипиррола, модифицированного хинолином поливинилбензилхлорида либо модифицированного ферроценом оксида кремния, осуществляемым в водной среде в течение 30 минут при температуре 37С, отделением несвязавшихся нанокомпозитных частиц с использованием магнитного поля, помещением в среду рабочего электрода, изготовленного из графитсодержащих материалов, поверхность которого предварительно модифицируют антителами, специфичными к определяемому штамму бактерий, образованием иммунокомплекса на поверхности электрода в течение 20 минут при температуре 37С с использованием магнитного поля, промыванием электрода буферным раствором, содержащим нормальную лошадиную сыворотку и твин-20, помещением извлеченного из анализируемой среды рабочего электрода в электрохимическую ячейку, содержащую фоновый электролит KNO, растворенный в воде, и определением содержания определяемых бактерий по величине аналитического сигнала, в качестве которого используют электрохимический отклик окисления/восстановления нанокомпозитных частиц, локализованных в иммунокомплексе на поверхности рабочего электрода.