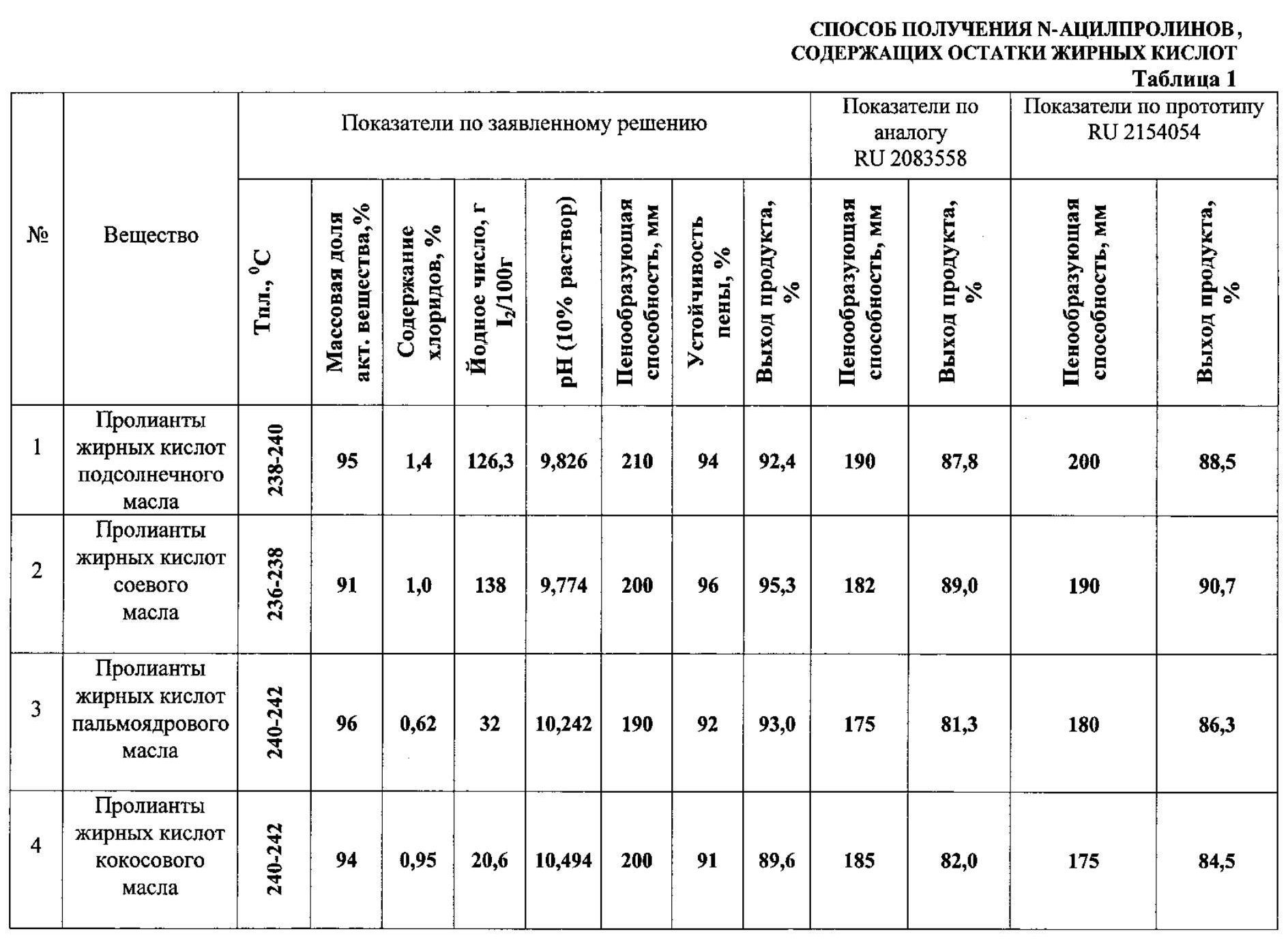
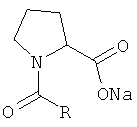
Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ N-АЦИЛПРОЛИНОВ, СОДЕРЖАЩИХ ОСТАТКИ ЖИРНЫХ КИСЛОТ
Вид РИД
Изобретение
Изобретение относится к области органической химии и химии поверхностно-активных веществ, а именно к способу получения N-ацилпролинов, которые проявляют свойства пенообразователей и могут найти применение в косметических и моющих композициях.
N-Ациламинокислоты в течение многих лет используются в косметических средствах для ухода за полостью рта, кожей и волосами. Эти соединения способствуют снижению проникновения потенциально раздражающих веществ через кожу человека, проявляют низкую токсичность, крайне быстро разлагаются. Уникальные комбинации свойств этих поверхностно-активных веществ привели к их широкому промышленному применению, в том числе в качестве ингибиторов коррозии металлов [Crudden J J. Industrial Applications of Surfactants / J.J. Crudden [et al.] // The Royal Society of Chemistry. - 1992. - №1. - Р.95-119]. Реализация получения N-ациламинокислот в промышленных условиях связана с серьезными осложнениями при ведении технологического процесса, обусловленными обильным пенообразованием реакционной массы при подаче водных растворов солей аминокислот к высшим карбоновым кислотам. Данных трудностей удается избежать при использовании эфиров высших карбоновых кислот. Чаще всего в подобные превращения вводятся α-аминокислоты.
Такой подход использовался авторами патента [WO 9507881, МПК С07С 231/02; С07С 233/47; С07С 233/49; C11D 1/04, опубл. 1995-03-23]. В качестве исходных соединений выступают эфиры жирных кислот (насыщенных и ненасыщенных) и низших спиртов (метилового, этилового, пропилового и бутилового), которые вводили в реакцию с солью саркозина и щелочного металла (натрия или калия). Таким образом, получают производные N-ацилсаркозина. К недостаткам данного метода можно отнести: использование катализаторов - алкоксидов натрия или калия, проведение реакции в абсолютированных растворителях. Известен способ получения N-ациламинокислот, обладающих поверхностно-активными и флотационными свойствами [RU 2083558, МПК С07С 233/47, С07С 233/49, С07С 231/02, опубл. 10.07.1997], непосредственным взаимодействием эфиров карбоновых кислот с солями аминокислот. Способ основан на взаимодействии эфиров олеиновой кислоты, или эфиров жирных таловых кислот, или синтетических жирных кислот С10-С18 с водным раствором соли щелочного металла и низших алифатических аминокислот или белковых гидролизатов. К недостаткам данного метода можно отнести невысокую конверсию метиловых эфиров олеиновой кислоты и жирных таловых кислот, а также время проведения реакции 150-180 минут.
Ряд способов получения N-ацилпроизводных пролина формулы
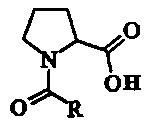
описан авторами международной заявки WO 2013149022 [МПК A23L 1/227; C07D 207/16, опубл. 2013-10-03], где R - остаток алкила, содержащий от 6 до 20 атомов углерода, или остаток алкена, содержащий от 9 до 25 атомов углерода и от 1 до 6 двойных связей. Предлагается три варианта проведения процесса:
- взаимодействием аминокислоты с галогенангидридом карбоновой кислоты. К недостаткам данного метода можно отнести дополнительную стадию получения хлорангидридов жирных кислот с использованием токсичных реагентов (хлориды фосфора, сульфурилхлорид);
- из жирных кислот и О-метилированных аминокислот. К недостаткам данного метода можно отнести необходимость проведения дополнительной стадии гидролиза;
- реакцией жирных кислот с аминокислотой в растворе бикарбоната натрия. К недостаткам данного метода можно отнести использование дорогостоящих дополнительных реагентов: дициклогексилкарбодиимида и 1-гидроксипирролидин-2,5-диона.
Наиболее близким является способ получения соли щелочного металла и N-ацил-аминокислоты по патенту RU 2154054 [МПК С07С 231/02, С07С 233/47, опубл. 10.08.2000], основанный на взаимодействии свободных кислот, содержащих от 1 до 20 атомов углерода, и соли аминокислоты со щелочным металлом (натрий, калий). Жирную кислоту выбирают из олеиновой, лауриновой, миристиновой, кокосовой, стеариновой, нонановой, декановой и ундекановой кислот. Дополнительно предусматривает постоянное удаление воды из реакционной среды по мере ее образования барботированием инертным газом. Реакцию проводят при 170-190°С. Аминокислоту добавляют в количестве одного или двух эквивалентных избытков из расчета на жирную кислоту. Соль аминокислоты с щелочным металлом выбирают из группы, состоящей из соли щелочного металла с саркозином, глицином, иминодиуксусной кислотой, аланином, N-метилаланином, бета-аланином, N-метил-бета-аланином, аспарагиновой кислотой, валином, лейцином, изолейцином, цистином, метионином, фенилаланином, глутаминовой кислотой, пролином и лизином. К недостаткам данного способа можно отнести необходимость постоянного удаления воды из реакционной среды по мере ее образования, проведение синтеза в инертной атмосфере, использование двукратного избытка аминокислоты, что приводит к существенному увеличению затрат.
Задачей настоящего изобретения является разработка способа получения N-ацилпролинов, позволяющего избежать использование инертной атмосферы и удаления воды из реакционной среды, а также снизить количество используемой в реакции дорогостоящей натриевой соли пролина.
Технический результат заключается в получении N-ацилпролинов формулы
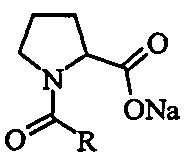
где R - остатки жирных кислот растительных масел (подсолнечного, соевого, пальмоядрового и кокосового), обладающих высокой пенообразующей способностью, простым и экономичным способом, без использования катализатора и инертной атмосферы, а также в повышении выхода и конверсии.
Технический результат достигается тем, что в способе получения N-ацилпролинов, содержащих остатки жирных кислот, включающем взаимодействие исходных соединений и соли щелочного металла - натрия с пролином, выдерживание реакционной массы при 190°С в течение 2 часов, очистку путем перевода натриевых солей N-ацилпролина в соответствующие нерастворимые кислоты, согласно изобретению в качестве исходных соединений используются метиловые эфиры жирных кислот растительных масел (подсолнечного, соевого, пальмоядрового и кокосового), причем мольное соотношение реагентов натриевая соль пролина:метиловые эфиры жирных кислот растительных масел = 1,1:1.
Ниже представлены примеры осуществления предлагаемого изобретения.
ПРИМЕР 1.
Синтез N-ацилпролинов, содержащих остатки жирных кислот подсолнечного масла, происходит в результате следующей реакции:
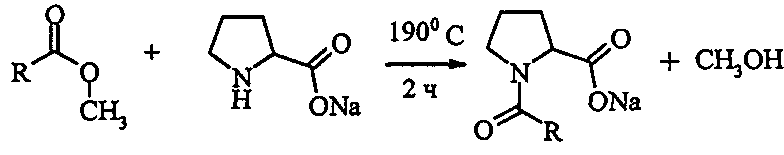
где R - углеводородные фрагменты жирных кислот (С16-С22) подсолнечного масла.
100 г метиловых эфиров жирных кислот подсолнечного масла поместили в плоскодонную колбу на 500 мл, нагрели при перемешивании до 160°С. Медленно, в течение 2.0-2.5 ч прикапывали водный раствор пролината натрия (приготовленный из 15 г гидроксида натрия, 42.7 г пролина в 60 мл воды) так, чтобы температура смеси держалась в диапазоне 150-165°С. Затем смесь выдержали 2 часа при 190°С (при интенсивном перемешивании) и горячей перенесли в фарфоровую ступку (предварительно нагретую) и растерли.
В стакан на 500 мл поместили растертый N-ацилпролин и добавили 200 мл смеси петролейного и диэтилового эфиров (2:1). К полученному раствору добавили при перемешивании 10% раствор соляной кислоты до рН=1. Эфирный слой отделили на делительной воронке и добавили к нему безводный сульфат натрия (40 г) для удаления остатков воды. Раствор декантировали, осушитель ополаскивали 30 мл смеси петролейного и диэтилового эфиров (2:1) и после декантации объединили с первым раствором. Петролейный и диэтиловый эфир удалили на роторном испарителе в вакууме водоструйного насоса. Остаток взвесили, растворили в 300 мл этилового спирта и добавили эквимольное количество гидроксида натрия (~11 г), растворенного в 200 мл этанола. Выпавший осадок N-ацилпролинов, содержащих остатки жирных кислот подсолнечного масла, отфильтровали, промыли 300 мл спирта и высушили.
Результаты приведены в таблице 1.
ПРИМЕР 2.
Синтез N-ацилпролинов, содержащих остатки жирных кислот соевого масла, проводят согласно способу, описанному в примере 1, где R - углеводородные фрагменты жирных кислот (С8-С18) соевого масла, а водный раствор пролината натрия готовят из 15 г гидроксида натрия, 43.3 г пролина в 60 мл воды.
Результаты приведены в таблице 1.
ПРИМЕР 3.
Синтез N-ацилпролинов, содержащих остатки жирных кислот пальмоядрового масла, проводят согласно способу, описанному в примере 1, где R - углеводородные фрагменты жирных кислот пальмоядрового масла (С8-С18), а водный раствор пролината натрия готовят из 18 г гидроксида натрия, 51.4 г пролина в 70 мл воды.
Результаты приведены в таблице 1.
ПРИМЕР 4.
Синтез N-ацилпролинов, содержащих остатки жирных кислот кокосового масла, проводят согласно способу, описанному в примере 1, где R - углеводородные фрагменты жирных кислот (С6-С18) кокосового масла, а водный раствор пролината натрия готовят из 19.6 г гидроксида натрия, 56.2 г пролина в 76 мл воды.
Результаты анализа физико-химических свойств смесей N-ацилпролинов, полученных в примерах 1-4, приведены в таблице 1. Независимо от особенностей жирно-кислотного состава (длины углеводородного радикала, степени ненасыщенности остатков жирных кислот) соединения обладают высокой пенообразующей способностью.