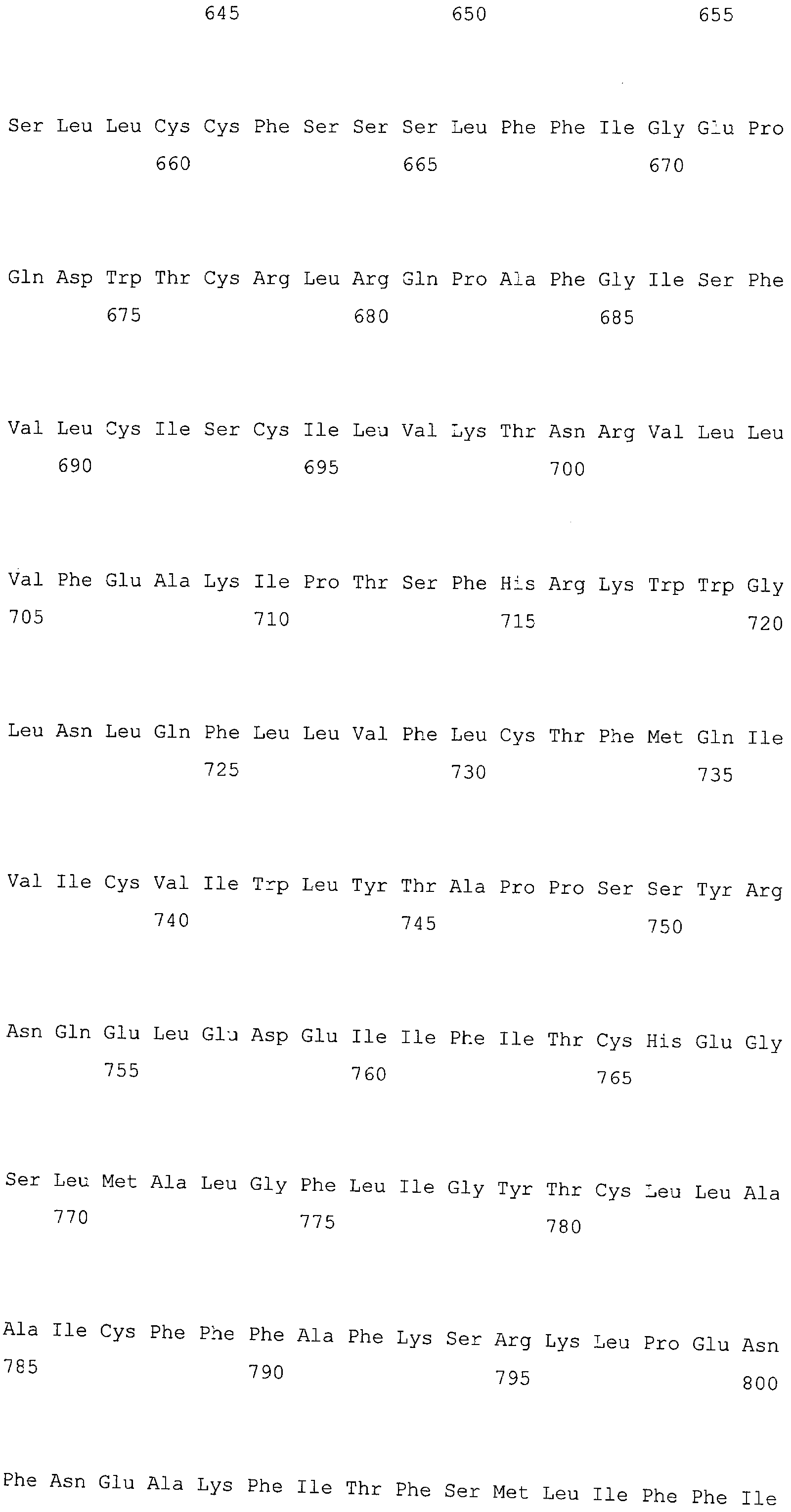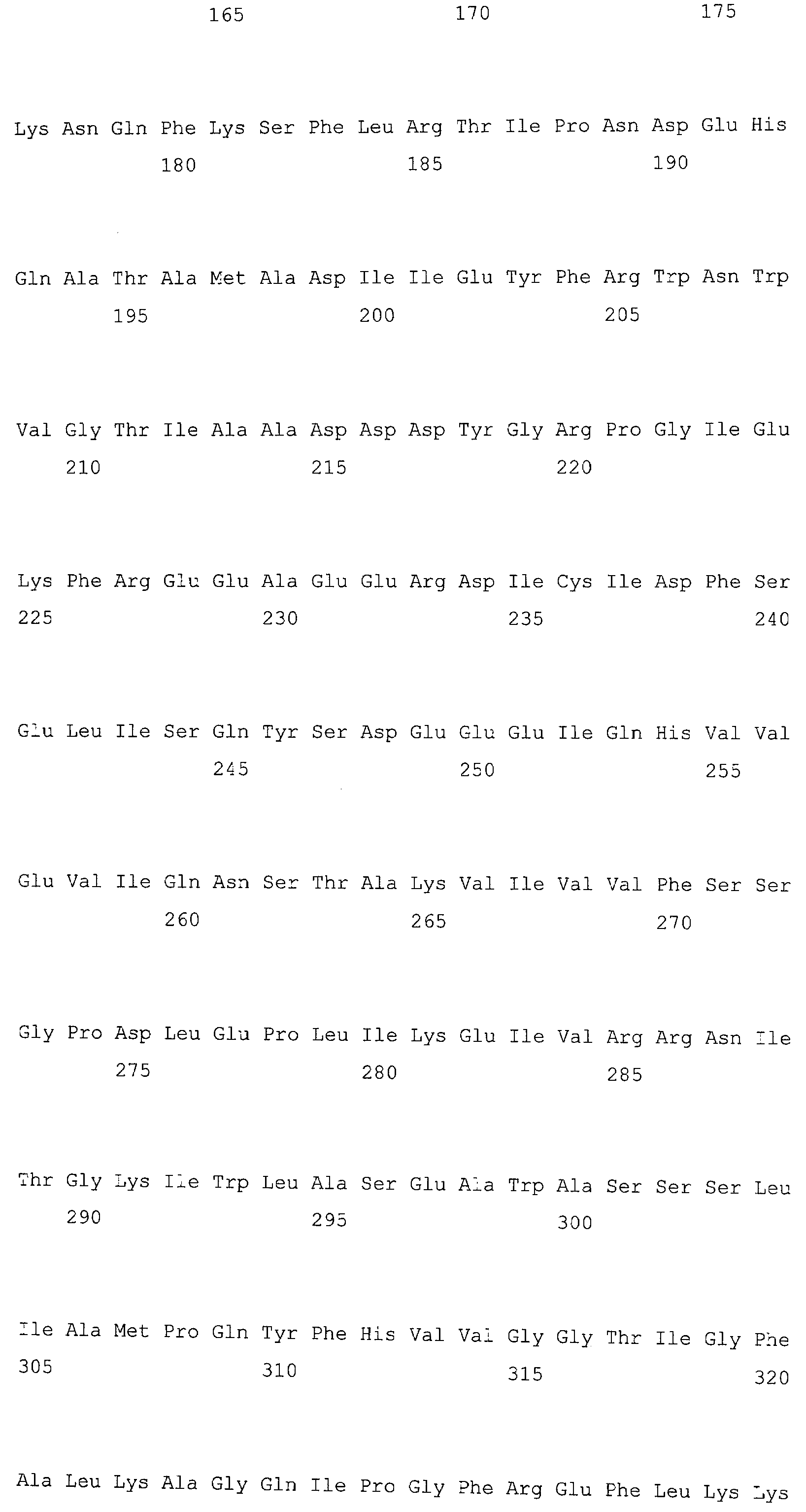Результат интеллектуальной деятельности: ПРИМЕНЕНИЕ ПЕПТИДОВ ДЛЯ ПРИДАНИЯ КОКУМИ
Вид РИД
Изобретение
Область техники
Изобретение относится к агенту, придающему кокуми, и комплексному агенту, придающему кокуми, состоящему из пептида, проявляющего активность агониста CaSR. Дополнительно настоящее изобретение также относится к композиции приправы, включающей пептид в концентрации не менее заданного уровня, проявляющий активность агониста CaSR.
Предшествующий уровень техники
В последнее время возросли требования потребителей к вкусу и вкусовой привлекательности пищевых продуктов в виду, например, различия во вкусовых привычках людей. Вкус и вкусовая привлекательность пищевого продукта условно выражается пятью основными вкусами, другими словами, сладким вкусом, соленым вкусом, кислым вкусом, горьким вкусом и умами (изысканный), соответственно, возросла необходимость в разработке превосходного агента, придающего кокуми пищевым продуктам, «кокуми» может придать пищевому продукту дополнительно улучшенный вкус и даже интенсифицированный вкус, например плотность, нарастание (ощущение заполненности во рту при потреблении), продолжительность и гармоничность указанных выше пяти основных вкусов, как пограничных вкусов, которые не могут быть выражены только этими пятью основными вкусами.
С другой стороны, сигналы, исходящие от чувствительных к кальцию рецепторов (CaSR), также известных как кальциевые рецепторы, могут контролировать множество биологических функций у живого организма, и вещества, обладающие активностью агониста CaSR, могут быть использованы в качестве агента, придающего кокуми (см., патентные документы 1, 3 и непатентный документ 4, как приведено ниже).
Может существовать множество моделей развития вкуса указанного выше «кокуми». В связи с этим существует настоятельная потребность в получении агента, способного придать кокуми пищевым продуктам и запускающего такую модель развития вкуса, которая может развить или придать начальному вкусу кокуми. Дополнительно вещество для придания кокуми может быть использовано, главным образом, например, в пищевых продуктах и, соответственно, оно должно иметь превосходную стабильность. Дополнительно вещество для придания кокуми должно быть легко получаемым и иметь низкую стоимость с точки зрения промышленного производства.
Следовательно, желательно провести исследование множества соединений, обладающих заданной активностью агониста CaSR, для того, чтобы найти вещество, способное придать кокуми другим веществам (пищевым продуктам или напиткам), которое демонстрирует более сильно выраженный эффект придания кокуми, в частности эффект придания кокуми начальному вкусу, которое обладает превосходной стабильностью и которое может быть легко получено при низкой стоимости, чтобы таким образом обеспечить агент, придающий кокуми, состоящий из такого вещества, наряду с комплексным агентом кокуми, включающим вещество и другие вещества, обладающие в комбинации активностью агониста CaSR.
С другой стороны, известен синтез некоторых γ-глутамил пептидов, каждый из которых несет остаток γ-глутамина на N-конце, в качестве субстратов, например, в исследованиях по ферментативной активности (см. патентный документ 2 и непатентные документы 1-3, как приведено ниже), но до настоящего времени не известно использование γ-Glu-Abu в качестве агента, придающего кокуми, или приправы, или также в качестве ингредиента пищевого продукта. В этом отношении содержание Патентных документов 1-3 введено здесь ссылками в полном объеме, как если бы они были описаны в описании настоящей патентной заявки.
Документы предшествующего уровня техники
ПАТЕНТНЫЕ ДОКУМЕНТЫ:
Патентный документ 1: опубликованная международная заявка № 2007/055393, описание;
Патентный документ 2: опубликованная международная патентная заявка № 2007/066430, описание;
Патентный документ 3: опубликованная международная патентная заявка № 2008/139945, описание.
НЕПАТЕНТНЫЕ ДОКУМЕНТЫ:
Непатентный документ 1: Molecular Pharmacology (1982), 21(3), 629-36;
Непатентный документ 2: Agricultural and Biological Chemistry (1981), 45(12), 2839-45;
Непатентный документ 3: Journal of Biological Chemistry (1979), 254(12), 5184-90;
Непатентный документ 4: Journal of Biological Chemistry, (2010), 285 (2), 1016-22.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
ЗАДАЧИ, РЕШАЕМЫЕ НАСТОЯЩИМ ИЗОБРЕТЕНИЕМ
Объектом настоящего изобретения является исследование множества соединений, обладающих заданной активностью агониста CaSR, для обнаружения, таким образом, вещества, способного придавать кокуми, которое демонстрирует более выраженный эффект придания кокуми, в частности эффект придания кокуми начальному вкусу, которое обладает превосходной стабильностью и которое может быть легко получено при низкой стоимости, и обеспечение таким образом агента, придающего кокуми, состоящего из такого вещества, наряду с комплексным агентом, придающим кокуми, включающим вещество и другие вещества, обладающие в комбинации активностью агониста CaSR. Дополнительно объект настоящего изобретения обеспечивает композицию приправы, включающую указанное выше вещество в концентрации не менее заданного уровня.
СРЕДСТВА ДЛЯ РЕШЕНИЯ ЗАДАЧ
В результате исследования множества соединений авторы настоящего изобретения неожиданно установили, что γ-Glu-Abu (L-γ-глутамил-L-2-аминомолочная кислота) обладает высокой активностью агониста CaSR и оказывает довольно сильно выраженный эффект кокуми, и, в частности, его модель развития вкуса позволяет придавать кокуми начальному вкусу у субъекта. Дополнительно авторы настоящего изобретения обнаружили, что исследованный γ-Glu-Abu, таким образом, обладает превосходной стабильностью и подходящей моделью развития вкуса, которая оказывает более сильное воздействие на начальный вкус по сравнению с таковой наблюдаемой у γ-Glu-Cys - дипептида, аналогичного первому. Дополнительно, исследованный γ-Glu-Abu, таким образом, может служить как таковой в качестве полезного агента, придающего кокуми, и комплексного агента, придающего кокуми, за счет комбинирования вещества с другими веществами, каждое из которых демонстрирует активность агониста CaSR, и за счет этого решается задача настоящего изобретения.
В частности, настоящее изобретение относится к агенту, придающему кокуми, состоящему из γ-Glu-Abu. Дополнительно настоящее изобретение относится к комплексному агенту, придающему кокуми, включающему комбинацию (a) γ-Glu-Abu и (b) по меньшей мере одной или двух аминокислот или пептидов, выбранных из группы, состоящей из γ-Glu-X-Gly, где X представляет аминокислоту или производное аминокислоты, γ-Glu-Val-Y, где Y представляет аминокислоту или производное аминокислоты, γ-Glu-Ala, γ-Glu-Gly, γ-Glu-Cys, γ-Glu-Met, γ-Glu-Thr, γ-Glu-Val, γ-Glu-Orn, Asp-Gly, Cys-Gly, Cys-Met, Glu-Cys, Gly-Cys, Leu-Asp, D-Cys, γ-Glu-Met (O), γ-Glu-γ-Glu-Val, γ-Glu-Val-NH2, γ-Glu-Val-ол, γ-Glu-Ser, γ-Glu-Tau, γ-Glu-Cys (S-Me) (O), γ-Glu-Leu, γ-Glu-Ile, γ-Glu-t-Leu и γ-Glu-Cys (S-Me).
Также настоящее изобретение относится к комплексному агенту, придающему кокуми, включающему комбинацию (a) γ-Glu-Abu и (b) по меньшей мере одного или двух пептидов, выбранных из группы, состоящей из представленных следующей общей формулой: γ-Glu-X-OCH-(Z)-CO2H (где X представляет аминокислоту или производное аминокислоты и Z представляет H (атом водорода) или CH3 группу (метильную группу)); и представленных указанной выше общей формулой: γ-Glu-Val-Y (где Y представляет GlyA или LacA).
Дополнительно настоящее изобретение относится к композиции приправы (здесь и далее указанной как «композиция приправы по настоящему изобретению»), включающей γ-Glu-Abu в количестве не менее чем 1000 частей на миллион по массе, предпочтительно не менее чем 2000 частей на миллион по массе и более предпочтительно не менее 2500 частей на миллион по массе.
В дополнительном аспекте настоящее изобретение также относится к способу получения пищевого продукта или напитка, включающему стадии добавления ингредиента пищевого продукта или напитка, содержащего γ-Glu-Abu в количестве не менее чем 1000 частей на миллион по массе, предпочтительно не менее чем 2000 частей на миллион по массе и более предпочтительно не менее чем 2500 частей на миллион по массе к другим ингредиентам пищевых продуктов и напитков и необязательно обработку или тепловую обработку полученной в результате смеси ингредиентов. Также настоящее изобретение относится к пищевому продукту или напитку или промежуточному продукту, используемому для получения пищевого продукта или напитка, полученного способом по настоящему изобретению.
Дополнительно, настоящее изобретение относится к пищевому продукту или напитку или промежуточному продукту для получения пищевого продукта или напитка, включающему γ-Glu-Abu в пределах от 20 до 200 частей на миллион по массе; по меньшей мере одну органическую кислоту или ее соль, выбранную из группы, состоящей из молочной кислоты, лимонной кислоты, яблочной кислоты и янтарной кислоты и их солей в пределах от 0,005 до 0,1% по массе; и поваренную соль в пределах от 0,01 до 0,5% по массе наряду с носителем, приемлемым для пищевых продуктов и напитков, и/или по меньшей мере одним или двумя ингредиентами для приправы.
В другом аспекте настоящее изобретение относится к способу усиления вкуса и аромата и/или вкуса пищевого продукта или напитка, включающему стадию введения в продукт или напиток композиции, содержащей γ-Glu-Abu в количестве не менее чем 400 частей на миллион по массе, предпочтительно не менее чем 1000 частей на миллион по массе, более предпочтительно не менее чем 2000 частей на миллион по массе и еще более предпочтительно не менее чем 2500 частей на миллион по массе.
ПОЛЕЗНЫЕ ЭФФЕКТЫ ИЗОБРЕТЕНИЯ
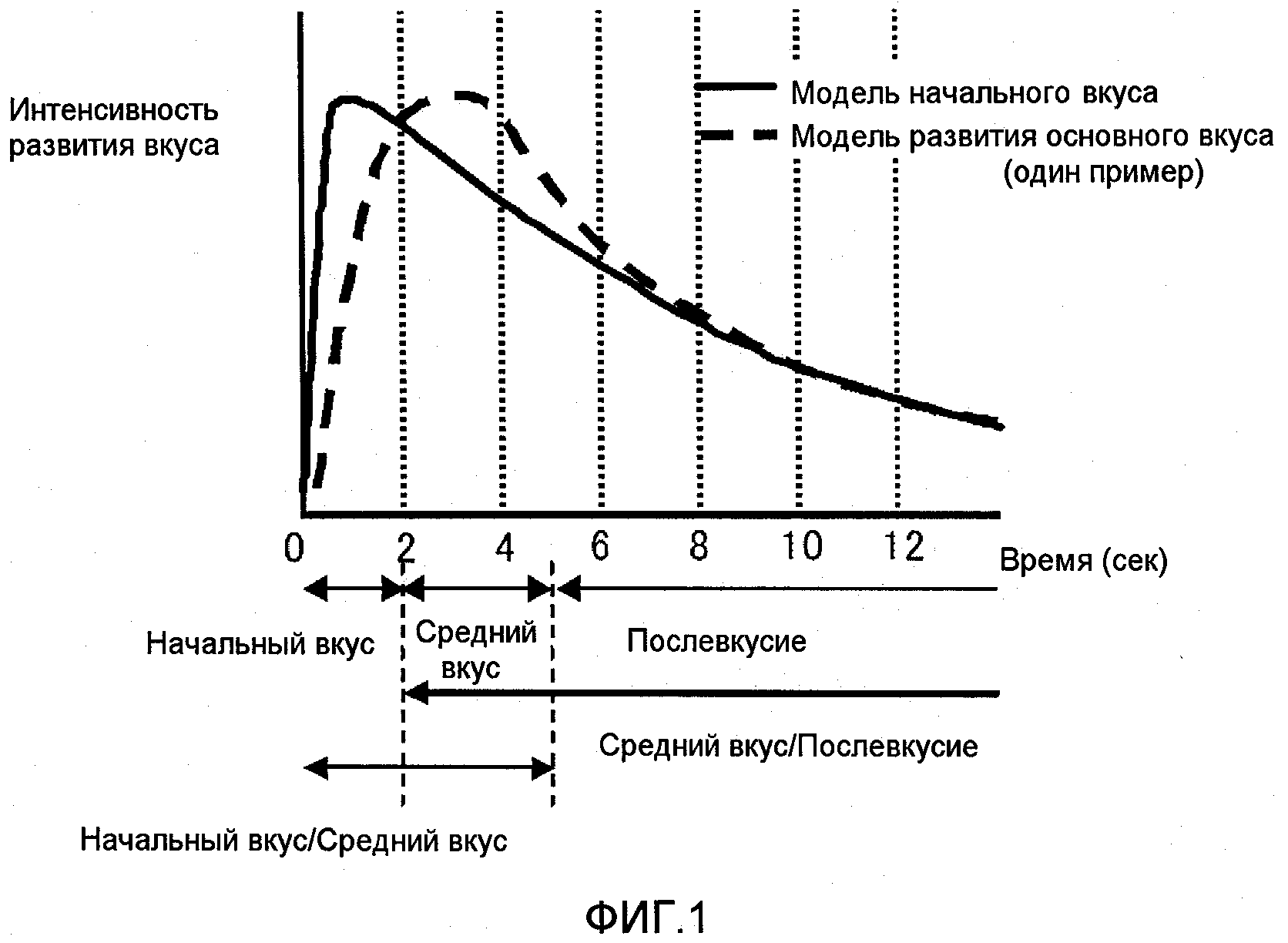
Настоящее изобретение относится к агенту, придающему кокуми, который оказывает довольно сильно выраженный эффект придания кокуми и, в частности, оказывает превосходный и уникальный эффект придания кокуми начальному вкусу, представленному, например, такой моделью развития вкуса, как, например, с профилем, приведенным на Фигуре 1, который обладает также превосходной стабильностью и который может быть легко получен при низкой стоимости, наряду с комплексным агентом, придающим кокуми, содержащим тоже самое. Дополнительно настоящее изобретение также относится к превосходной композиции приправы, включающей вещество, придающее выраженный эффект кокуми в концентрации не менее заданного уровня.
Агент, придающий кокуми, по настоящему изобретению демонстрирует модель развития вкуса и аромата и/или вкуса, очень похожую на таковую, наблюдаемую для поваренной соли и, следовательно, при использовании агента, придающего кокуми, последний может придать продукту с низким содержанием соли или аналогичному ему более сильное ощущение соленого вкуса и выраженность начального вкуса (или воздействие). Следовательно, полученный в результате продукт, содержащий агент по настоящему изобретению, может поддерживать ощущение соленого вкуса, аналогичное таковому перед снижением содержания соли, даже когда содержание соли в продукте понижено и, следовательно, агент по настоящему изобретению позволяет получить очень полезный для здоровья пищевой продукт. Примеры таких пищевых продуктов включают различные супы и соусы. В частности, при потреблении пищевого продукта, содержащего агент, придающий кокуми по настоящему изобретению, потребитель может воспринимать более сильное ощущение соленого вкуса и выраженность начального вкуса (или воздействие) сразу же после его потребления.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
Фиг. 1 - профиль вкуса и вкусовой привлекательности (модель развития вкуса), наблюдаемые для агента, придающего кокуми начальному вкусу.
ВАРИАНТЫ ВОПЛОЩЕНИЯ ИЗОРЕТЕНИЯ
Агент, придающий кокуми, по настоящему изобретению состоит из γ-Glu-Abu и с точки зрения вкуса этого достаточно, что агент состоит по существу из γ-Glu-Abu, и при этом агент может дополнительно включать другие компоненты в количестве, по существу не оказывающем воздействие на вкус агента по настоящему изобретению.
Агент, придающий кокуми, по настоящему изобретению или γ-Glu-Abu также может быть использован в комбинации по меньшей мере с одним дополнительным ингредиентом для приправы, выбранным из группы, состоящей из аминокислот, таких как глутамат натрия (MSG), нуклеиновых кислот, таких как инозин монофосфат (IMP), неорганических солей, таких как хлорид натрия, органических кислот, таких как лимонная кислота, и различных видов дрожжевых экстрактов с получением, таким образом, подходящей композиции приправы, улучшенной по кокуми по сравнению с таковым, полученным при использовании по отдельности таких дополнительных ингредиентов для приправы. При использовании γ-Glu-Abu в комбинации с указанными выше дополнительными ингредиентами для приправ концентрация последнего может быть легко или в установленном порядке определена или установлена специалистом в области техники, к которой относится настоящее изобретение, после проведения исследований, например проведения сенсорного теста.
Композиция приправы по настоящему изобретению или композиция, содержащая не менее 1000 частей на миллион по массе γ-Glu-Abu, аналогично может быть скомбинирована с другими ингредиентами для приправ с получением, таким образом, более подходящих отдельных приправ.
Используемый в описании настоящей патентной заявки термин «кокуми» относится к вкусу, который не может быть выражен пятью основными вкусами или сладким вкусом, соленым вкусом, кислым вкусом, горьким вкусом и умами и, в частности, относится к вкусу, в котором пограничные вкусы основных вкусов: плотность, нарастание (ощущение заполненности во рту при потреблении), продолжительность и гармоничность усиливаются дополнительно к основным вкусам. Дополнительно используемый в описании настоящей патентной заявки термин «придание кокуми» означает, что пять основных вкусов, выраженных сладким вкусом, соленым вкусом, кислым вкусом, горьким вкусом и умами, усиливаются, при этом у субъекта одновременно вызываются пограничные вкусы основных вкусов, такие как плотность, нарастание (ощущение заполненности во рту при потреблении), продолжительность и гармоничность, ассоциированные с первым. Кроме того, это также может быть указанно, как усиление вкуса и аромата. Следовательно, γ-Glu-Abu служит в качестве агента, придающего кокуми по настоящему изобретению, и аналогично может быть указан как «усилитель вкуса и аромата». Агент, придающий кокуми, по настоящему изобретению или γ-Glu-Abu также может быть использован в качестве усилителя сладкого вкуса, усилителя соленого вкуса, усилителя кислого вкуса, усилителя горького вкуса или усилителя умами. Дополнительно вкус пищевого продукта может варьировать с течением времени после его потребления и вкус пищевого продукта после его потребления, как правило, указан как начальный вкус, средний вкус и послевкусие, возникающее непосредственно после потребления пищевого продукта. Хотя, конечно, они являются относительным понятием, но начальный вкус, средний вкус и послевкусие у субъекта составляют целое, определяемое как вкус, наблюдаемый в течение от 0 до 2 секунд, от 2 до 5 секунд и не менее чем 5 секунд после его потребления соответственно. Вкус, наблюдаемый в течение от 0 до 5 секунд, указан как «начальный/средний вкус», а вкус, наблюдаемый в течение от 2 до около 30 секунд указан, как «средний/послевкусие» (см. данные, приведенные на Фиг. 1). Для оценки вкуса в случае, когда вкус подразделяется на три части, для дегустаторов (лиц, потребляющих и оценивающих пищевой продукт) трудно сконцентрировать внимание на оценке, и традиционно используемый тест включает оценку вкуса, разделяя при этом на две части.
Воздействие вещества, демонстрирующего активность CaSR на кокуми и модель развития вкуса, может быть подтверждено, например, способом проведения сенсорного теста для оценки вкуса при участии человека. Пример такого сенсорного теста для оценки вкуса при участии человека приведен в Примерах настоящей патентной заявки, но сенсорный тест для оценки вкуса, используемый здесь, не ограничивается одним конкретным.
Используемый в описании настоящей патентной заявки термин «CaSR» относится к чувствительным к кальцию рецепторам, которые принадлежат к классу C 7-трансмембранного рецептора, который также указан как «кальциевый рецептор». Используемый в описании настоящей патентной заявки термин «агонист CaSR» относится к веществу, связывающемуся с указанным выше CaSR для активации рецептора. Дополнительно используемый в описании настоящей патентной заявки термин «активизировать CaSR» означает, что лиганд связывается с CaSR для активации таким образом гуанин-связывающего белка, и передачи сигналов, исходящих от него. Дополнительно способность вещества образовывать связь с CaSR для активации таким образом также указана как «активность агониста CaSR».
Далее приведен способ отбора соединения, обладающего активностью агониста CaSR, но стадии отбора соединения не ограничиваются приведенными ниже.
1) Стадия добавления тестируемого на активность CaSR вещества в систему, используемую для определения активности CaSR, и стадия определения активности CaSR;
2) Стадия сравнения активности CaSR, наблюдаемой при добавлении тестируемого вещества в систему, измеряющую активность, с таковой, наблюдаемой перед добавлением вещества; и
3) Стадия отбора вещества, которое демонстрирует активность агониста CaSR при добавлении в систему, измеряющую активность CaSR.
Определение активности CaSR также может быть проведено при использовании, например, системы измерений, в которой используются клетки, способные экспрессировать CaSR. Указанные выше клетки могут представлять таковые, эндогенно экспрессирующие CaSR или генетически рекомбинантные клетки, в которых ген, экспрессирующий CaSR, введен экзогенно. Указанная выше система измерения активности CaSR не ограничивается только одной конкретной, поскольку это позволяет определить связь (или реакцию) между веществом, активирующим CaSR, и CaSR, или могут испускать или продуцировать детектируемый сигнал в ответ на образование связи (или реакцию) между веществом, активирующим CaSR, и CaSR в клетках при добавлении внеклеточного лиганда (активирующее вещество), специфичного к CaSR, к указанным выше клеткам, способным экспрессировать CaSR. Если активность CaSR определяют через реакцию с тестируемым веществом, то можно судить, что тестируемое вещество демонстрирует заданную стимулирующую активность CaSR.
Приведенный в качества примера, указанный выше CaSR, предпочтительно используемый здесь CaSR человека, кодируемый человеческим геном CaSR, зарегистрированным в GenBank под инвентарным номером NM_000388. Однако CaSR не ограничивается белком, кодируемым геном с указанной выше последовательностью зарегистрированного CaSR, и может быть любым белком, кодируемым геном не менее чем 60%, предпочтительно не менее чем 80% и более предпочтительно не менее чем 90% гомологией последовательности с указанной выше последовательностью гена, поскольку белок, кодируемый таким геном, обладает функцией CaSR. В этой связи функция CaSR может быть исследована при использовании клеток, экспрессирующих эти гены, и последующем определении изменения электропроводимости и/или заряда ионов кальция в клетках, наблюдаемого при добавлении кальция в систему, содержащую клетки.
Что касается CaSR, то его источник не ограничивается каким-либо одним конкретным и может быть получен ото всех видов животных, включая мышей, крыс и собак, в дополнение к указанному выше CaSR человека.
Как указано выше, активность CaSR может быть подтверждена при использовании живых клеток, способных экспрессировать CaSR или его фрагмент, клеточных мембран, способных экспрессировать CaSR или его фрагмент, или в in vitro системе, включая CaSR или его белковый фрагмент.
Пример, в котором используют живые клетки, приведен ниже, но настоящее изобретение не ограничивается этим примером.
CaSR экспрессируется в культивируемых клетках, таких как ооциты лягушек, овариальные клетки, полученные от хомячков, и фетальные клетки почек человека. Эта экспрессия CaSR может быть проведена введением в плазмиду, способную нести экзогенный ген, гена CaSR, который клонирован в виде плазмиды или кРНК, полученной при использовании того же гена. Для определения такой реакции могут быть использованы электрофизиологические средства или флюоресцентный индикатор для определения какого-либо повышения концентрации кальция в клетках.
Экспрессия CaSR изначально подтверждена наличием какого-либо ответа, наблюдаемого при добавлении кальция или активатора со специфичностью к нему. В частности, используемыми здесь заданными клетками являются те, в которых внутриклеточная электропроводность определяется при добавлении кальция в концентрации около 5 мМ, или те, в которых при добавлении флюоресцентного индикатора наблюдается флюоресцентное излучение. В этой связи концентрация кальция, добавленная в клетки, по-разному варьируется при определении зависимости интенсивности внутриклеточной электропроводности от концентрации кальция. Затем тестируемое вещество разводят в пределах от около 1мкМ до 1 мМ, в полученную в результате дисперсию добавляют ооциты или культивируемые клетки и впоследствии в присутствии указанного выше тестируемого вещества измеряют активность CaSR, определяя, таким образом, активность агониста CaSR тестируемого вещества.
В частности, здесь используется тест для определения активности агониста CaSR, например, тест, приведенный в Тестовых примерах, приведенных ниже в описании настоящей патентной заявки, но тест не ограничивается приведенным тестом на определение активности.
Аминокислоты или пептиды, используемые в агенте, придающем кокуми, по настоящему изобретению в комбинации с γ-Glu-Abu, включают, например, по меньшей мере одну или две аминокислоты или пептида, выбранных из группы, состоящей из γ-Glu-Abu и γ-Glu-X-Gly (где X представляет аминокислоту или производное аминокислоты), γ-Glu-Val-Y (где Y представляет аминокислоту или производное аминокислоты), γ-Glu-Ala, γ-Glu-Gly, γ-Glu-Cys, γ-Glu-Met, γ-Glu-Thr, γ-Glu-Val, γ-Glu-Orn, Asp-Gly, Cys-Gly, Cys-Met, Glu-Cys, Gly-Cys, Leu-Asp, D-Cys, γ-Glu-Met (O), γ-Glu- γ-Glu-Val, γ-Glu-Val-NH2, γ-Glu-Val-ол, γ-Glu-Ser, γ-Glu-Tau, γ-Glu-Cys (S-Me) (O), γ-Glu-Leu, γ-Glu-Ile, γ-Glu-t-Leu и γ-Glu-Cys (S-Me). В этом отношении аминокислоты аналогично могут включать нейтральные аминокислоты, такие как Gly, Ala, Val, Leu, Ile, Ser, Thr, Cys, Met, Asn, Gln, Pro, Hyp, t-Leu; кислые аминокислоты, такие как Asp, Glu; основные аминокислоты, такие как Lys, Arg, His; ароматические аминокислоты, такие как Phe, Tyr, Trp; наряду с гомосерином, цитрулином, орнитином и α-аминомасляной кислотой, норвалином, норлейцином и таурином. Дополнительно аминокислоты, используемые в настоящем изобретении, также могут быть искусственными аминокислотами (имеющие не белковую конструкцию), такими как трет-лейцин, цикло-лейцин, α-амино-изомасляная кислота, L-пеницилламин, аллотреонин и алло-изолейцин. В этой связи в пептиде γ-Glu-X-Gly X может представлять указанную выше аминокислоту или производное аминокислоты, но предпочтительно использовать в настоящем изобретении аминокислоты или их производные иные, чем Cys.
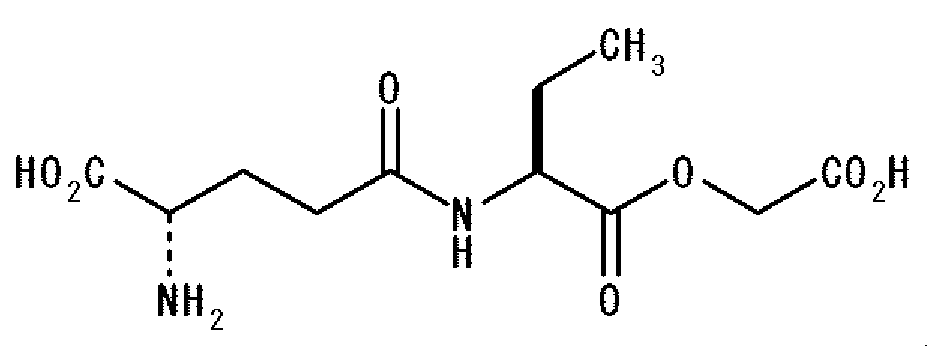
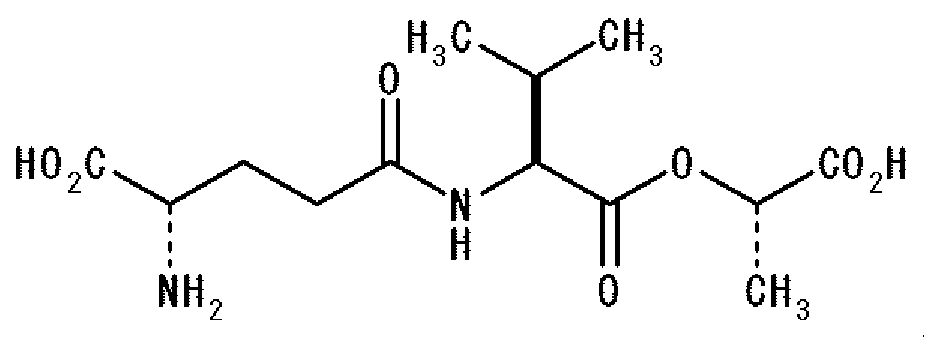
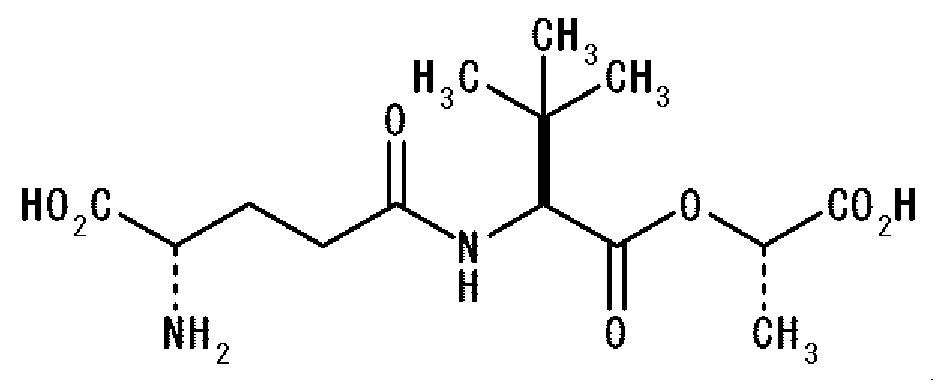
Дополнительно аминокислоты или пептиды, используемые в комбинации с γ-Glu-Abu, в агенте, придающем кокуми, по настоящему изобретению могут представлять производные пептида, каждый со структурой, представленной формулой: γ-Glu-X-OCH- (Z)CO2H, где X представляет аминокислоту или производное аминокислоты, и Z представляет H (атом водорода) или CH3 группу (метильную группу). Дополнительно аминокислоты или пептиды, используемые в настоящем изобретении, аналогично могут представлять соединения, представленные указанной выше общей формулой: γ-Glu-Val-Y, где Y представляет GlyA или LacA. Конкретными примерами предпочтительно используемых в настоящем изобретении аминокислот и пептидов являются γ-Glu-Val-GlyA, γ-Glu-tLeu-GlyA, γ-Glu-Abu-GlyA, γ-Glu-Val-LacA, γ-Glu-tLeu-LacA и γ-Glu-Abu-LacA. Используемый в описании настоящей патентной заявки термин «GlyA» относится к гликолевой кислоте, а LacA относится к масляной кислоте. Масляная кислота может быть как S-изомером, так и R-изомером, но предпочтительно она является S-изомером. Далее приведены структурные формулы этих соединений:
[Химическая формула 1]
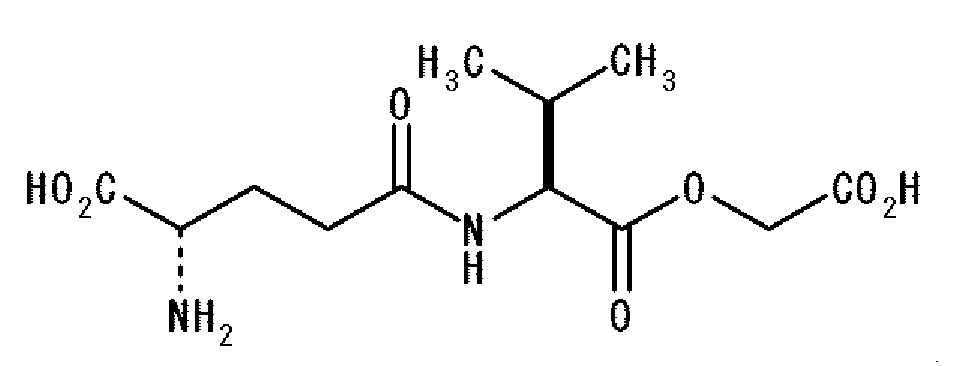
[Химическая формула 2]
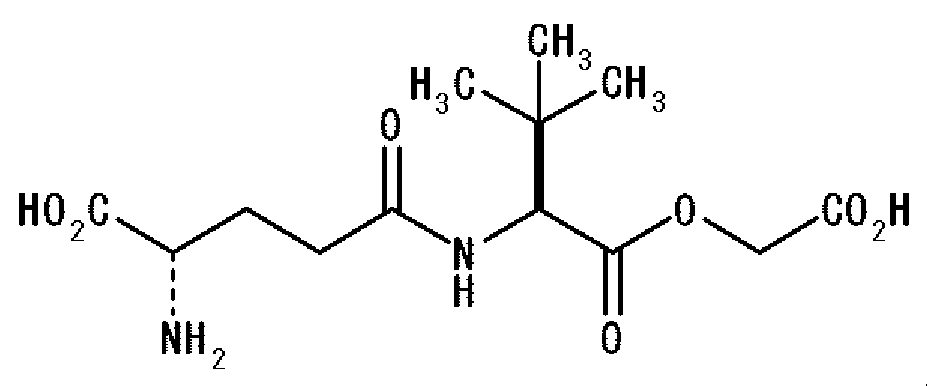
[Химическая формула 3]
[Химическая формула 4]
[Химическая формула 5]
[Химическая формула 6]
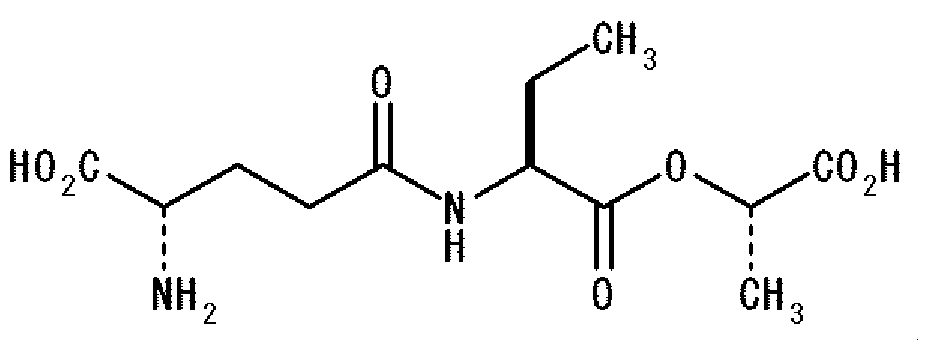
В частности, агент, придающий кокуми, по настоящему изобретению состоит из γ-Glu-Abu, и этот агент имеет уникальный и превосходный эффект придания кокуми начальному вкусу и эффект развития профиля вкуса, как приведено на Фиг. 1. Следовательно, предпочтительно, чтобы γ-Glu-Abu использовался в комбинации с таким пептидом, как γ-Glu-Val-Gly, который демонстрирует развитие профиля вкуса, отличное от первого.
В описании настоящей патентной заявки каждая аминокислота (остаток) приведена следующим сокращением:
(1) Gly: глицин;
(2) Ala: аланин;
(3) Val: валин;
(4) Leu: лейцин;
(5) Ile: изолейцин;
(6) Met: метионин;
(7) Phe: фенилаланин;
(8) Tyr: тирозин;
(9) Trp: триптофан;
(10) His: гистидин;
(11) Lys: лизин;
(12) Arg: аргинин;
(13) Ser: серин;
(14) Thr: треонин;
(15) Asp: аспарагиновая кислота;
(16) Glu: глутаминовая кислота;
(17) Asn: аспарагин;
(18) Gln: глутамин;
(19) Cys: цистеин;
(20) Pro: пролин;
(21) Orn: орнитин;
(22) Sar: саркозин;
(23) Cit: цитруллин;
(24) N-Val: (или Nva): норвалин (2-аминовалериановая кислота);
(25) N-Leu (или Nle): норлейцин;
(26) Abu: α-аминомасляная кислота;
(27) Tau: таурин;
(28) Hyp: гидроксипролин;
(29) t-Leu: трет-лейцин;
(30) Cle: цикло-лейцин;
(31) Aib: α-амино-изомасляная кислота (2-метил-аланин);
(32) Pen: L-пеницилламин;
(33) allo-Thr: аллотреонин;
(34) allo-Ile: алло-изолейцин.
Дополнительно используемый в описании настоящей патентной заявки термин «производное аминокислоты» относится к различным производным указанных выше аминокислот, и конкретные примеры включают специальные аминокислоты и искусственные аминокислоты, аминоспирты или аминокислоты, боковые цепочки которых, такие как концевые карбоксильные группы, аминогруппы и/или тиольная группа цистеина заменены множеством заместителей. Примеры таких заместителей включают алкильную группу, ацильную группу, гидроксильную группу, аминогруппу, алкиламино группу, нитрогруппу, сульфонильную группу или различные защитные группы. Следовательно, примеры таких производных аминокислот включают Arg (NO2): N-γ-нитро-алгинин, Cys (SNO): S-нитро-цистеин, Cys (S-Me): S-метил цистеин, Cys (S-allyl): S-аллил цистеин, Val-NH2: валин-амид, и Val-ол: валинол (2-амино-3-метил-1-бутанол). В тоже время пептид: γ-Glu-Cys(SNO)-Gly, используемый в настоящей патентной заявке, представляет таковой, представленный следующей структурной формулой, и символ: «(O)», появляющийся в приведенных выше формулах: γ-Glu-Met (O) и γ-Glu-Cys (S-Me) (O), относится к этим пептидам, каждый из которых имеет сульфоксидную структуру. Символ «(γ)» γ-Glu относится к другой аминокислоте, связанной с глутаминовой кислотой через карбоксильную группу, расположенную в γ-позиции последней.
[Химическая формула 7]
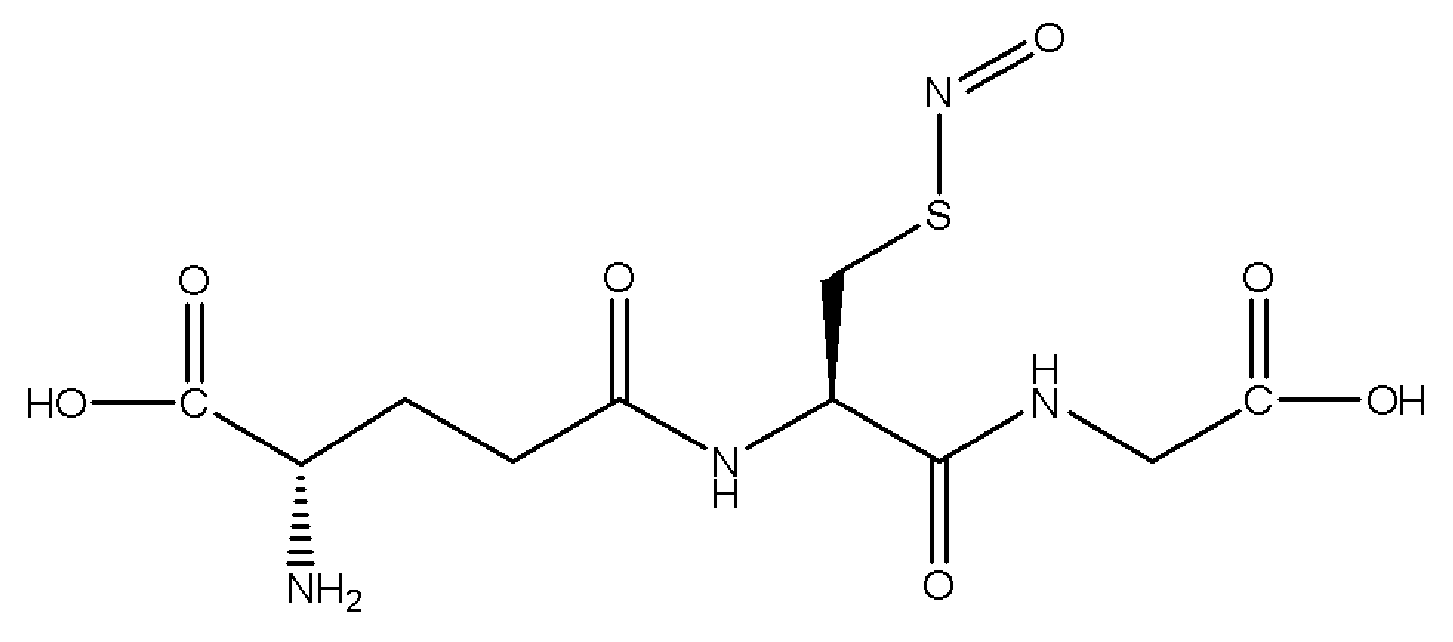
S-нитрозоглутатион (GNSO)
γ-Glu-Abu, используемая в описании настоящей патентной заявки, относится к L-γ-глутамил-L-2-аминомасляной кислоте. γ-Glu-Abu и аминокислоты и пептиды, используемые в комбинации в настоящем изобретении, могут быть коммерчески доступны, если они могут быть закуплены на рынке или могут быть получены при использовании любой известной технологии, такой как (1) химический синтез или (2) использование ферментативной реакции, но удобнее было бы использовать химический синтез. γ-Glu-Abu, используемая в настоящем изобретении, очень короткая в длину, поскольку включает только два аминокислотных остатка и, следовательно, удобнее применить технологию химического синтеза. В частности, она может быть получена простым и дешевым способом по сравнению с любым трипептидом, включающим три аминокислотных остатка, и, соответственно, применение этого дипептида является достаточно выгодным с точки зрения промышленного производства. Дополнительно при химическом синтезе γ-Glu-Abu, используемой в настоящем изобретении, и аминокислот и пептидов, используемых в комбинации с ней, при ее получении могут быть получены синтезом или полусинтезом этих олигопептидов при использовании при этом устройства для синтеза пептидов. Таким химическим синтезом этих пептидов, подходящим для использования в настоящем изобретении, является, например, технология твердофазного пептидного синтеза. Затем полученный таким образом пептид может быть очищен согласно традиционно используемым для этого технологиям, таким как ионообменная хроматография, высокоэффективная жидкостная хроматография с обращенными фазами или аффинная хроматография. Такой твердофазный пептидный синтез и последующая очистка используемых пептидов хорошо известны специалисту в области техники, к которой относится настоящее изобретение.
В качестве альтернативы при получении γ-Glu-Abu, используемой в настоящем изобретении, и аминокислот и пептидов, используемых в комбинации с ней, при использовании ферментативной реакции ее получение может быть проведено при использовании способа, описанного в описании находящейся на рассмотрении патентной заявки WO 2004/011653. В частности, они могут быть получены реакцией аминокислоты или пептида, в которой одна из концевых карбоксильных групп этерифицируется или аминируется другой аминокислотой, аминогруппа которой находится в свободном состоянии (например, аминокислота, карбоксильная группа которой защищена) в присутствии пептидообразующего фермента, и затем очищают с получением в результате дипептида или трипептида. Примерами таких пептидобразующих ферментов являются культуры микроорганизмов, демонстрирующих способность продуцировать пептиды; клетки микроорганизмов, выделенные из культур; или продукт, полученный обработкой клеток микроорганизмов, или пептидообразующий фермент, полученный из микроорганизмов. В тоже время здесь это истолковано, как в описании WO 2004/011653, введенной здесь ссылкой.
Дополнительно к указанным выше способам ферментативного получения и синтеза в настоящем изобретении часто используют пептиды натурального происхождения, например из растений, таких как овощи и фрукты, микроорганизмов, таких как дрожжи, и из других натуральных источников. В случае, когда они присутствуют в веществах натурального происхождения, они могут быть выделены из них, и полученные выделенные продукты аналогично могут быть использованы в настоящем изобретении.
Агент, придающий кокуми, или комплексный агент, придающий кокуми, по настоящему изобретению может быть использован в качестве приправы без какой-либо постобработки или может быть смешан с носителями, приемлемыми для пищевых продуктов и напитков, или другими ингредиентами для приправ с получением, таким образом, различных приправ. Примеры таких других ингредиентов для приправ включают специи, сахариды, подсластители, пищевые волокна, витамины, аминокислоты, такие как глутамат натрия (MSG), нуклеиновые кислоты, такие как инозин монофосфат (IMP), неорганические соли, такие как хлорид натрия, и органические кислоты, такие как лимонная кислота или ее соли, наряду с различными видами дрожжевых экстрактов.
В частности, предпочтительными композициями пищевых продуктов являются пищевые продукты с низким содержанием соли, включающие агент, придающий кокуми, или комплексный агент, придающий кокуми по настоящему изобретению, и они представляют таковые, изначально содержащие поваренную соль и, в частности, пищевые продукты с пониженным содержанием поваренной соли. Пищевые продукты с низким содержанием соли включают не только таковые в твердой форме, а также таковые в жидкой форме, и используемый в описании настоящей патентной заявки термин «пищевой продукт с низким содержанием соли» является синонимом «пищевого продукта и напитка с низким содержанием соли».
Примерами таких пищевых продуктов с низким содержанием соли являются такие продукты, как сливочное масло и сыр; пищевые продукты, содержащие животные масла и жиры, и/или пищевые продукты, содержащие растительные масла или жиры, такие как маргарин, соусы и ру; эмульгированные пищевые продукты, такие как дрессинги и майонез; различные виды карри и тушеного мяса; различные виды снэковых продуктов; и различные супы, содержащие экстракты мяса, или мясные эссенции и/или сливки. Дополнительно такие пищевые продукты с низким содержанием соли аналогично включают, например, ферментированные пищевые продукты или сброженные пищевые продукты, такие как мисо и соевый соус; супы или бульоны и соусы, получаемые при использовании таких ферментированных или сброженных пищевых продуктов; прошедшие технологическую обработку овощи, такие как соленые овощи и соленые огурцы; прошедшие технологическую обработку мясные продукты, такие как ветчина и колбасные изделия; прошедшие технологическую обработку морепродукты, такие как паста из вареной рыбы, сухие морепродукты и пищевые продукты, уваренные с соей; прошедшие тепловую обработку мясные шарики, котлеты из рубленого фарша; жареные продукты и куры-гриль. Среди этого предпочтительными пищевыми продуктами с низким содержанием соли являются таковые с содержанием поваренной соли при потреблении в концентрации в пределах от 0,01 до 0,5% по массе. Дополнительно также предпочтительно использование по меньшей мере одного члена, выбранного из группы, состоящей из органических кислот, таких как молочная кислота, лимонная кислота, яблочная кислота и янтарная кислота и их соли, в комбинации с поваренной солью в пределах от 0,005 до 0,1% по массе. Применение этих ингредиентов в комбинации позволяет дополнительно улучшить эффект усиления соленого вкуса агентом, придающим кокуми, или γ-Glu-Abu по настоящему изобретению.
Также настоящее изобретение относится к пищевому продукту или напитку, включающему в пределах от 20 до 200 частей на миллион по массе γ-Glu-Abu и в пределах от 0,01 до 0,5% по массе поваренной соли. Предпочтительно пищевой продукт или напиток дополнительно включает по меньшей мере один член, выбранный из группы, состоящей из органической кислоты, такой как молочная кислота, лимонная кислота, яблочная кислота и янтарная кислота и их соли в концентрации в пределах от 0,005 до 0,1% по массе.
В случае, когда агент, придающий кокуми, по настоящему изобретению вводят в указанные выше пищевые продукты с низким содержанием соли, пищевые продукты будут способны вызвать более сильное ощущение соленого вкуса и выраженность начального вкуса (или воздействие) на начальной стадии при потреблении ими пищевых продуктов с низким содержанием соли.
γ-Glu-Abu, используемая в настоящем изобретении, и аминокислоты или пептиды, используемые в комбинации с ней, также могут аналогично включать их в форме соли. В случае, когда γ-Glu-Abu, используемая в настоящем изобретении, и аминокислоты или пептиды, используемые в комбинации с ней, находятся в форме соли, соли не ограничиваются конкретными солями исходя из их фармакологической приемлемости, и конкретные примеры включают соли аммония, соли с щелочными металлами, такие как натрия и калия, соли с щелочно-земельными металлами, такие как кальция и магния, соли алюминия, соли цинка, соли с органическими аминами, такие как триэтиламин, этаноламин, морфолин, пирролидин, пиперидин, пиперазин и дицикло-гексиламин, и соли с основными аминокислотами, такими как аргинин и лизин, для кислых групп, таких как карбоксильные группы. Дополнительно примеры указанных выше соединений аналогично включают соли с неорганическими кислотами, такими как хлористоводородная кислота, серная кислота, фосфорная кислота, азотная кислота и бромистоводородная кислота; соли с органическими кислотами, такими как уксусная кислота, лимонная кислота, бензойная кислота, малеиновая кислота, фумаровая кислота, винная кислота, янтарная кислота, дубильная кислота, масляная кислота, хибензойная кислота, памовая кислота, энантовая кислота, декановая кислота, 8-хлортеофиллиновая кислота, салициловая кислота, молочная кислота, щавелевая кислота, миндальная кислота и яблочная кислота; и соли с органическими сульфоновыми кислотами, такими как метансульфоновая кислота, бензолсульфоновая кислота и п-толуолсульфоновая кислота, для основных групп соединений.
Агент, придающий кокуми, или комплексный агент, придающий кокуми, по настоящему изобретению может быть использован в любой форме, такой как сухие порошки, пасты и растворы без ограничения по физическим свойствам.
Агент, придающий кокуми, или комплексный агент, придающий кокуми, по настоящему изобретению может быть использован, например, для введения в пищевые продукты, напитки и приправы.
В случае, когда агент, придающий кокуми, или комплексный агент, придающий кокуми, по настоящему изобретению используют, например, для ведения в пищевые продукты, напитки и приправы, окончательное количество γ-Glu-Abu и аминокислоты или пептида, используемых в комбинации с ней, не ограничивается каким-либо конкретным, поскольку они могут гарантировать достижение заданного эффекта по настоящему изобретению, но количество γ-Glu-Abu и/или аминокислоты или пептида, каждого составляет в пределах от 1 частей на миллиард по массе до 99,9% по массе и предпочтительно в пределах от около 10 частей на миллиард по массе до 10% по массе и более предпочтительно в пределах от около 1 частей на миллион по массе до 1% по массе от общей массы каждого пищевого продукта, напитка, приправы или аналогичного им соответственно.
В другом аспекте настоящее изобретение также относится к способу получения композиции приправы, включающему стадию смешивания агента, придающего кокуми, с носителем, приемлемым для других ингредиентов для приправ или пищевых продуктов и напитков. Концентрация γ-Glu-Abu в композиции приправы, полученной таким образом, по существу предпочтительно составляет в пределах от 400 до 500000 частей на миллион по массе. В частности, способ получения композиции приправы по настоящему изобретению предпочтительно включает стадии смешивания агента, придающего кокуми, с другими ингредиентами приправы, и концентрация γ-Glu-Abu в композиции приправы, полученной таким образом, составляет в пределах от 400 до 500000 частей на миллион по массе.
Дополнительно настоящее изобретение относится к способу получения пищевого продукта или напитка, включающему стадию введения агента, придающего кокуми, по настоящему изобретению с другими ингредиентами пищевых продуктов или напитков. Концентрация γ-Glu-Abu в пищевом продукте или напитке, полученном таким образом, по существу предпочтительно составляет в пределах от 20 до 200 частей на миллион по массе. Следовательно, по настоящему изобретению предпочтительно, чтобы стадия введения агента, придающего кокуми, по настоящему изобретению в пищевой продукт или напиток, включающая стадию регулирования концентрации γ-Glu-Abu в пищевом продукте или напитке, полученном таким образом, проводилась до уровня в пределах от 20 до 200 частей на миллион по массе.
Пищевой продукт, напиток, приправа или аналогичное им, включающее введенный агент, придающий кокуми, или комплексный агент, придающий кокуми, по настоящему изобретению дополнительно может включать, например, твердый или жидкий носитель и/или подходящие ингредиенты приправы, приемлемые для пищевых продуктов и напитков.
Указанные выше носители могут представлять, например, глюкозу, лактозу, сахарозу, крахмал, маннит, декстрин, глицериды жирных кислот, полиэтиленгликоль, гидроксиэтилированный крахмал, этиленгликоль, полиоксиэтиленовый эфир сорбитана жирных кислот, желатин, альбумин, аминокислоты, воду и физиологический раствор.
Указанные выше ингредиенты для приправы не ограничиваются каким-либо конкретным и могут представлять любой, используемый в этой области ингредиент, конкретные примеры таковых приведены выше.
Указанные выше носители, другие ингредиенты приправы или аналогичное им не ограничиваются конкретными из них.
Композиция приправы по настоящему изобретению включает γ-Glu-Abu не менее чем 1000 частей на миллион по массе, предпочтительно 2000 частей на миллион по массе и более предпочтительно 2500 частей на миллион по массе. Эти приправы по существу продемонстрировали эффект придания γ-Glu-Abu. Соотношение γ-Glu-Abu в композиции приправы по настоящему изобретению предпочтительно составляет не менее чем 3000 частей на миллион по массе, более предпочтительно 5000 частей на миллион по массе, еще более предпочтительно не менее чем 1% по массе, по существу предпочтительно не менее чем 3% по массе. Дополнительно предпочтительно включает таковые с содержанием γ-Glu-Abu не более чем 99,9% по массе. Компоненты композиции приправы по настоящему изобретению иные, чем γ-Glu-Abu, не ограничиваются какими-либо конкретными и их конкретные примеры включают носители и ингредиенты приправы, приемлемые для пищевых продуктов и напитков.
Более конкретными примерами приправ по настоящему изобретению являются дрожжевые экстракты, содержащие γ-Glu-Abu в количестве не менее чем 2500 частей на миллион по массе. Дрожжевой экстракт по существу не ограничивается клетками какого-либо микроорганизма, из которых получен экстракт, условиями культивирования микроорганизмов и способами экстракции, и, следовательно, любой дрожжевой экстракт может быть использован в композиции приправы по настоящему изобретению. Дополнительно эти дрожжевые экстракты могут представлять таковые, прошедшие обработку, например тепловую обработку, обработку ферментами, концентрирование и/или обработку для превращения в порошкообразную форму. Способ получения такого дрожжевого экстракта, содержащего не менее чем 2500 частей на миллион по массе γ-Glu-Abu, не ограничивается каким-либо конкретным, но такой дрожжевой экстракт может быть получен, например, добавлением γ-Glu-Abu в дрожжевой экстракт таким образом, что концентрация первого составляет таковую в указанных выше пределах.
Композиция приправы по настоящему изобретению может быть использована в любой форме и может быть, например, в форме сухого порошка, пасты и раствора без какого-либо ограничения по физическим свойствам.
Композиция приправы по настоящему изобретению может быть использована для ее введения, например, в пищевые продукты и напитки.
Дополнительно настоящее изобретение относится к способу получения другого типа композиции приправы, включающему стадию добавления приправы по настоящему изобретению в другие ингредиенты приправы или носитель, приемлемый для пищевых продуктов и напитков. Концентрация γ-Glu-Abu в композиции приправы, полученной этим способом, по существу предпочтительно составляет в пределах от 400 до 500000 частей на миллион по массе. В частности, способ получения этого типа композиции приправы по настоящему изобретению предпочтительно включает стадии смешивания композиции приправы по настоящему изобретению с другими ингредиентами приправы и контроль концентрации γ-Glu-Abu в таком типе композиции приправы, полученной таким образом, в пределах от 400 до 500000 частей на миллион по массе.
Дополнительно настоящее изобретение относится к способу получения пищевого продукта или напитка, включающему стадию введения композиции приправы по настоящему изобретению в другие ингредиенты, используемые для получения пищевого продукта или напитка. Концентрация γ-Glu-Abu в пищевом продукте или напитке, полученном таким образом, по существу предпочтительно составляет в пределах от 20 до 200 частей на миллион по массе. В частности, в настоящем изобретении предпочтительно стадия введения композиции приправы по настоящему изобретению в другие ингредиенты, используемые для получения пищевого продукта или напитка, включает стадию регулирования концентрации γ-Glu-Abu в пищевом продукте или напитке, полученном таким образом, в пределах от 20 до 200 частей на миллион по массе.
Также настоящее изобретение относится к способу получения, например, пищевого продукта, напитка или приправы, включающему добавление в промежуточный продукт, используемый для получения, например, пищевого продукта, напитка или приправы, γ-Glu-Abu таким образом, что полученный в результате пищевой продукт, напиток или приправа содержит γ-Glu-Abu в пределах от 1 частей на миллиард по массе до 99,9% по массе. Предпочтительно пищевой продукт, напиток, приправа или аналогичное им представляет пищевой продукт с низким содержанием соли.
Также настоящее изобретение относится к способу получения пищевого продукта или напитка, включающему стадию введения композиции приправы по настоящему изобретению в промежуточный продукт, используемый для получения такого пищевого продукта или напитка. Предпочтительно пищевой продукт или напиток представляет пищевой продукт или напиток с низким содержанием соли.
В способе получения пищевого продукта или напитка или промежуточного продукта, используемого для получения пищевого продукта или напитка по настоящему изобретению, также может быть использован, например, указанный выше дрожжевой экстракт, содержащий γ-Glu-Abu в высокой концентрации, в качестве ингредиента, используемого для получения пищевого продукта или напитка, включающего γ-Glu-Abu не менее чем 1000 частей на миллион по массе, и использован для получения другого пищевого продукта или напитка. Дополнительно в настоящем изобретении могут быть аналогично использованы такие ингредиенты, включающие, например, продукты γ-Glu-Abu, полученные при использовании химического синтеза или ферментативного синтеза, и затем выделенные; или разведенные и/или диспергированные продукты из продуктов γ-Glu-Abu, выделенных таким образом. Примеры таких разведенных и/или диспергированных продуктов, содержащих γ-Glu-Abu, включают таковые, полученные разведением порошкообразного продукта γ-Glu-Abu любыми твердыми или жидкими носителями, приемлемыми для пищевых продуктов и напитков, которые уже приведены здесь выше.
Используемая в описании настоящей патентной заявки фраза «другие ингредиенты, используемые для получения пищевых продуктов и напитков» включают все типы ингредиентов для пищевых продуктов и напитков, используемые в настоящее время в качестве сырьевых материалов для пищевых продуктов и напитков, за исключением «ингредиентов для пищевых продуктов и напитков, содержащих не менее чем 1000 частей на миллион по массе γ-Glu-Abu», и их конкретные примеры включают таковые, приведенные ниже в качестве пищевых продуктов и напитков и промежуточных продуктов для их получения, дополнительно к указанным выше носителям и ингредиентам для приправ, приемлемых для пищевых продуктов и напитков.
Способ получения пищевого продукта или напитка или промежуточного продукта, используемого для их получения, по настоящему изобретению может включать стадию дополнительной технологической обработки или тепловой обработки смеси ингредиентов для пищевых продуктов и напитков, полученной на стадии введения ингредиента для пищевого продукта и напитка, содержащего менее чем 1000 частей на миллион по массе γ-Glu-Abu, в другие ингредиенты для пищевых продуктов и напитков. Используемый в описании настоящей патентной заявки термин «технологическая обработка или тепловая обработка» включает любую стадию тепловой обработки, традиционно используемую в этой области. Примеры таких стадий тепловой обработки включают обжарку, выпекание или жарку на открытом огне, варку, жарку, обработку паром, резку, грубое измельчение или дробление, измельчение с использованием терки, измельчение с использованием терки и сита, мелкое дробление, мелкое дробление и помол, рубку, смешивание, стадии просеивания и толчения, но настоящее изобретение не ограничивается этими конкретными стадиями тепловой обработки.
Примеры пищевых продуктов и напитков или промежуточных продуктов, используемых для их получения, которые могут быть получены при использовании способа по настоящему изобретению, включают приведенные выше, то есть молочные продукты, такие как сливочное масло и сыр, пищевые продукты, содержащие животные масла и жиры, и/или пищевые продукты, содержащие растительные масла или жиры, такие как маргарин, соусы и ру; эмульгированные пищевые продукты, такие как дрессинги и майонез; различные виды карри и тушеного мяса; различные виды снэковых продуктов; и различные супы, содержащие экстракты мяса, или мясные эссенции и/или сливки. Дополнительно такие пищевые продукты и напитки или промежуточные продукты, используемые для их получения, аналогично включают, например, ферментированные пищевые продукты или сброженные пищевые продукты, такие как мисо и соевый соус; супы или бульоны и соусы, получаемые при использовании ферментированных или сброженных пищевых продуктов; прошедшие технологическую обработку овощи, такие как соленые овощи и соленые огурцы; прошедшие технологическую обработку мясные продукты, такие как ветчина и колбасные изделия; прошедшие технологическую обработку морепродукты, такие как паста из вареной рыбы, сухие морепродукты и пищевые продукты, уваренные с соей; прошедшие тепловую обработку мясные шарики, котлеты из рубленого фарша; жареные продукты и куры-гриль.
Пищевые продукты и напитки по настоящему изобретению также включают пищевые продукты или напитки, представляющие готовые продукты в таких формах, которые в настоящее время представлены на рынке и могут быть употреблены в пищу, и используемый в описании настоящей патентной заявки термин «промежуточные продукты, используемые для получения пищевых продуктов и напитков» относится ко всем, имеющим любую форму перед технологической обработкой их в готовые продукты. В случае, когда используют промежуточный продукт, используемый для получения пищевого продукта или напитка, в качестве ингредиента приправы, содержащего γ-Glu-Abu, предпочтительно, чтобы промежуточный продукт включал γ-Glu-Abu в количестве от около 400 до 500000 частей на миллион по массе, и предпочтительно в пределах от около 4000 до 40000 частей на миллион по массе, и такой промежуточный продукт может быть получен добавлением ингредиента для пищевых продуктов и напитков, содержащего, например, не менее чем 1000 частей на миллион по массе γ-Glu-Abu, таким образом, что полученный в результате промежуточный продукт имеет ее концентрацию, составляющую в указанных выше пределах. В качестве альтернативы конечный или готовый продукт предпочтительно включает в пределах от около 20 до 200 частей на миллион по массе γ-Glu-Abu, что является концентрацией ее во время потребления, или ее в пищевом продукте или напитке, представляющем готовый продукт, и такой готовый продукт может быть получен добавлением ингредиента для пищевых продуктов и напитков, содержащего, например, не менее чем 1000 частей на миллион по массе γ-Glu-Abu, таким образом, что полученный в результате готовый продукт имеет ее концентрацию, составляющую в указанных выше пределах.
В способе получения пищевого продукта или напитка, или промежуточного продукта, используемого для их получения, по настоящему изобретению стадия добавления в ингредиент для получения других пищевых продуктов или напитков ингредиента, используемого для получения пищевого продукта или напитка, включающего γ-Glu-Abu, предпочтительно включает стадию контроля концентрации γ-Glu-Abu в полученном в результате промежуточном продукте в пределах от 400 до 500000 частей на миллион по массе, и способ по настоящему изобретению более предпочтительно включает дополнительную стадию добавления промежуточного продукта, используемого для получения пищевых продуктов или напитков, в ингредиент, используемый для получения других пищевых продуктов и напитков, регулируя таким образом концентрацию γ-Glu-Abu в полученном в результате пищевом продукте или напитке в пределах от 20 до 200 частей на миллион по массе.
В способе получения пищевого продукта или напитка по настоящему изобретению стадия добавления ингредиента, используемого для получения пищевого продукта или напитка, включающего γ-Glu-Abu, в ингредиент для получения других пищевых продуктов или напитков, предпочтительно включает стадию контроля концентрации γ-Glu-Abu в полученном в результате пищевом продукте или напитке в пределах от 20 до 200 частей на миллион по массе.
Способ получения пищевого продукта или напитка по настоящему изобретению подходит для случаев, в которых пищевой продукт или напиток представляет таковой с низким содержанием соли. В этом случае предпочтительно, чтобы способ включал дополнительную стадию добавления в ингредиент для пищевых продуктов или напитков по меньшей мере одного члена, выбранного из группы, состоящей из органических кислот, таких как молочная кислота, лимонная кислота, яблочная кислота и янтарная кислота и их солей, и предпочтительно молочной кислоты и яблочной кислоты, таким образом, что ее концентрация в полученном в результате пищевом продукте или напитке составляет в пределах от 0,005 до 0,1% по массе, аналогично предпочтительно, чтобы способ дополнительно включал добавление поваренной соли в ингредиент для пищевых продуктов или напитков в количестве меньшем, чем используемое при получении пищевого продукта или напитка в предшествующем уровне техники соответственно. Используемый в описании настоящей патентной заявки термин «малое количество поваренной соли в пищевом продукте с низким содержанием соли» относится, например, к концентрации поваренной соли в пищевом продукте с низким содержанием соли по меньшей мере на 5% и предпочтительно по меньшей мере на 10% меньше, чем количество, используемое при получении пищевого продукта или напитка в предшествующем уровне техники.
Пищевой продукт и напиток по настоящему изобретению может иметь любою форму, традиционно используемую в области получения пищевых продуктов и напитков, например продукты, упакованные в контейнеры для автоклавирования, консервированные и бутилированные формы или в форме сухих продуктов.
Далее настоящее изобретение будет описано более детально со ссылкой на следующие иллюстрирующие и не ограничивающие его Примеры.
ПРИМЕРЫ
Получение различных образцов:
На рынке закупают следующие четыре вещества: γ-L-Glu-L-Abu (Abu: α-аминомасляная кислота; доступная от Bachem Feinchemikalien AG); γ-L-Glu-L-Ala (доступно от Bachem Feinchemikalien AG); γ-L-Glu-L-Cys (доступно от Sigma Aldrich Japan Co., Ltd.); и γ-L-Glu-L-Thr (доступно от KOKUSAN Chemical Co., Ltd).
Синтез L-Glu-L-Val:
(Стадия 1): Растворенный в метилен хлориде (100 мл) Z-L-Glu-OBzl (α-бензиловый эфир N-α-карбобензилокси-L-глутаминовой кислоты, 7,619 г, 20,51 мМ) и Val-OBzl・HCl (гидрохлорид бензилового эфира L-валина, 5 г, 20,51 мМ), и полученный в результате раствор выдерживали при температуре 0°C. Затем в раствор добавляют триэтиламин (3,2 мл, 22,57 мМ), HOBt (1-гидроксибензотриазол, 3,053 г, 22,57 мМ) и WSC・HCl (1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид, 4,326 г, 22,57 мМ) и полученную в результате смесь перемешивали при комнатной температуре в течение ночи. Затем реакционную жидкость концентрируют при пониженном давлении и полученный в результате остаток разбавляли этилацетатом (220 мл). Раствор фракционировали при использовании 5% водного раствора лимонной кислоты (100 мл) и полученную таким образом водную фазу дополнительно экстрагируют этилацетатом (60 мл). Органическую фазу комбинируют и затем промывают насыщенным раствором поваренной соли (80 мл), 5% водным раствором гидрокарбоната натрия (80 мл) и насыщенным раствором поваренной соли (80 мл). Полученную таким образом органическую фазу сушат безводным сульфатом магния, последний затем удаляют фильтрацией и полученный фильтрат концентрируют при пониженном давлении. Остаток промывают смесью этилацетата/н-гексана (1:1) при поддержании первого в виде суспензии и затем фильтруют с получением Z-L-Glu-L-Val-OBzl (10,0273 г). Дополнительно кристаллы, осажденные из фракции этилацетата/н-гексана добавлением н-гексана, собирают и затем перекристаллизовывают из этилацетата/н-гексана для извлечения Z-L-Glu-L-Val-OBzl (1,0399 г).
Выход: 94,25%.
(Стадия 2) В этанол (160 мл) добавляют Z-L-Glu-L-Val-OBzl (11,71 г, 20,86 мМ) с последующим добавлением в смесь 10% палладия на угле (2,3 г) и затем воды (10 мл) и полученную в результате реакционную систему перемешивают при комнатной температуре в течение ночи в атмосфере газообразного водорода. Во время реакции в систему маленькими порциями добавляют воду (100 мл). Палладий на угле удаляют фильтрацией, полученный в результате фильтрат концентрируют при пониженном давлении, полученный таким образом остаток перекристаллизовывают из малого количества воды и этанола с получением таким образом γ-L-Glu-L-Val (5,0 г).
Выход: 97,23%.
Полученный продукт имеет следующие характеристики:
ESI-MS: m/z 247,2 (M+H)+
1H-ЯМР (400 мГц D2O): δ (частей на миллион): 0,86 (3H, д, J=6,8 Гц), 0,88 (3H, д, J=6,8 Гц), 2,04-2,13 (3H, м), 2,42-2,46 (2H, м), 3,74 (1H, т, J=6,3 Гц), 4,13 (1H, д, J=5,8 Гц).
Получение γ-L-Glu-L-Ser:
Применяют процедуры, использованные выше для получения препарата γ-L-Glu-L-Val, γ-L-Glu-L-Ser, синтезируемого при использовании Z-L-Glu-OBzl и L-Ser- OBzl, в качестве исходных веществ. Полученный продукт имеет следующие характеристики:
ESI-MS: m/z 235,1 (M+H)+
1H-ЯМР (400 мГц, D2O): δ (частей на миллион): 1,98-2,09 (2H, м), 2,40 (2H, т, J=8,0 Гц), 3,71-3,81 (3H, м), 4,33 (1H, т, J=8,0 Гц).
Получение γ-L-Glu-L-t-Leu:
Применяют процедуры, использованные выше, для получения препарата γ-L-Glu-L-Val, γ-L-Glu-L-t-Leu, синтезируемого при использовании Z-L-Glu-OBzl и L-t-Leu-OBzl, в качестве исходных веществ. Полученный продукт имеет следующие характеристики:
ESI-MS: m/z 261,3 (M+H)+
Получение γ-L-Glu-Aib:
Применяют процедуры, использованные выше, для получения препарата γ-L-Glu-L-Val, γ-L-Glu-Aib, синтезируемого при использовании Z-L-Glu-OBzl и Aib-Ot-Bu, в качестве исходных веществ. Полученный продукт имеет следующие характеристики:
ESI-MS: m/z 233,3 (M+H)+
1H-NMR (400 мГц, D2O): δ (частей на миллион): 1,36 (6H, с), 2,00-2,06 (2H, м), 2,30-2,34 (2H, м), 3,69 (1H, т, J=6,2 Гц).
(Тестовый пример 1): Получение плазмиды, экспрессирующей CaSR
Плазмиду, экспрессирующую CaSR, получают согласно следующим процедурам:
Для ПЦР используют синтезированную синтетическую олиго ДНК (то есть прямой праймер (Последовательность № 3: ACTAATACGACTCACTATAGGGACCATGGCA-TTTTATAGCTGCTGCTGG) и обратный праймер (Последовательность № 4: TTATGAATT-CACTACGTTTTCTGTAACAG) на основе последовательности ДНК, зарегистрированной в NCBI (CaSR (кальциевый рецептор): NM_000388, последовательность № 1 и 2).
ПЦР проводят при условиях, описанных ниже, при использовании кДНК (доступно от Clontech Company), полученной из почек человека, в качестве материала, при использовании указанных выше праймеров и ДНК полимеразы Pfu Ultra (доступной от Stratagene Company): Реакционную систему обрабатывают при температуре 94°C в течение 3 минут и затем при температуре 94°C в течение 30 секунд, при температуре 55°C в течение 30 секунд и при температуре 72°C в течение 2 минут, при этом стадии повторяют 35 раз и, наконец, реакцию в системе проводят при температуре 72°C в течение 7 минут. Затем реакционную систему подвергают электрофорезу на агарозе, агарозу окрашивают ДНК-окрашивающим веществом и затем облучают УФ светом для определения наличия амплификации кДНК в результате ПЦР. В то же самое время электрофорезную картину сравнивают с ДНК маркером, чья электрофорезная подвижность известна, для подтверждения таким образом наличия длинноцепочечных продуктов ПЦР.
Плазмидный вектор pBR322 расщепляют рестрикционным ферментом EcoRV (доступен от Takara Co., Ltd) и амплифицированный с помощью ПЦР фрагмент гена сшивают с плазмидным вектором по сайту расщепления при использовании набора Ligation Kit (доступно от Promega Company). Клетки штамма Escherichia coli DH5α перемещают в этот реакционный раствор с последующим отбором трансформантов, содержащих плазмиду, в которой ПЦР амплифицированный продукт клонирован и дополнительно ПЦР амплифицированный продукт подтверждают при использовании анализа ДНК последовательностей.
Эту рекомбинантную плазмиду используют для установления экспрессии CaSR человека плазмидой hCaSR/pcDNA3.1.
(Тестовый пример 2): Оценка активности агониста CaSR
Клетки 293E (EBNA1-экспрессия HEK293 клетки, ATCC № CRL-10852) культивируют в DMEN/Ham's-F12 (3,15/мл глюкозосодержащей модифицированной Eagle среды Дульбекко, доступной от Nakaraitesk Company), добавляя 10% фетальной телячьей сыворотки, в присутствии 200 мкг/мл G418 (доступно от Genetisin). Культивированные клетки инокулируют в колбу F25 при плотности 3×106 клеток/10 мл, колбы выдерживают в течение 24 часов в CO2 инкубаторе (5% CO2, 37°C) и затем трансформируют или трансфицируют плазмидами hCaSR/pcDNA3.1, экспрессирующими CaSR человека с реагентом для трансфекции Fugene6 (доступно от Roche Company). Трансфицирующие плазмиды выдерживают в CO2 инкубаторе в течение от 6 до 7 часов, затем клетки восстанавливают при использовании DMEM/ Ham's-F12, содержащей 10% фетальную телячью сыворотку, и инокулируют в каждую лунку 96-луночной пластины с покрытием из поли-D-лизина (BD-Biocoat) при плотности 70000 клеток/лунка.
96-луночную пластину выдерживают в течение 24 часов в CO2 инкубаторе, затем удаляют культуральную среду из каждой лунки 96-луночной пластины, в которые инокулировали клетки, с последующим добавлением в каждую лунку Ca2+ флюоресцентного индикатора Calcium 4 Assay Kit (доступно от Molecular Devices Company), растворенного в буфере (содержащем 146 мМ NaCl, 5 мМ KCl, 1 мМ MgSO4, 1 мг/мл глюкозы, 20 мМ HEPES (pH 7,2) и в пределах от 0,75 до 1,25 мМ CaCl2) в количестве 200 мкл/лунка, с последующей выдержкой 96-луночной пластины при температуре 37°C в течение одного часа и затем при комнатной температуре в течение 10 минут для включения индикатора в клетки.
В каждую лунку 96-луночной пластины добавляют каждое тестируемое соединение, растворенное в буфере 0,1% BSA-содержащем Assay Buffer, в количестве 50 мкл/лунку и затем отслеживают любое изменение интенсивности флюоресценции в течение 3 минут при использовании FLEX Station (доступно от Molecular Devices Company).
(Способ определения EC 50 ):
Разницу (RFU (Max-Min)) между максимальной и минимальной интенсивностью флюоресценции отслеживают для каждой лунки перед и после добавления каждого тестируемого соединения и определяют, используя автоматические вычисления при использовании FLEX Station. Показатель активности рассчитывают исходя из того, что показатель RFU (Max-Min) принимают как 100% при добавлении соединения в максимальной концентрации, и показатель RFU (Max-Min) принимают как 0% при использовании 0,1% BSA-содержащего Assay Buffer, свободного от тестируемого соединения, затем обрабатывают полученные в результате данные для построения кривой при использовании программного обеспечения для обработки крупноформатных таблиц Xfit или Graph-Pad-Prism для определения EC50, которая является концентрацией соединения при показателе активности 50%. Полученные результаты приведены в Таблице 1 ниже.
|
|
При сравнении γ-Glu-Abu с другими дипептидами было установлено, что она обладает сильной активностью агониста CaSR по сравнению с таковой у γ-Glu-Cys. Известно использование в качестве агента, придающего кокуми, пептида с низкой молекулярной массой, обладающего активностью агониста CaSR (см. Патентный документ 1, как указанно выше), и это позволяет предположить, что γ-Glu-Abu может быть по существу превосходным агентом, придающим кокуми.
Пример 1: Оценка активности придания кокуми
В этом примере исследуют γ-Glu-Abu на интенсивность придания кокуми при проведении количественной сенсорной оценки.
Количественную сенсорную оценку проводят согласно следующим процедурам: Интенсивность придания кокуми отслеживается для каждого тестируемого соединения и определяется как показатель, наблюдаемый при смешивании в пределах от 0,001 до 0,5 г/дл соответствующего тестируемого соединения с дистиллированной водой, содержащей глутамат натрия (0,05 г/дл), инозин монофосфат (0,05 г/дл) и хлорид натрия (0,05 г/дл). В случае, когда образец демонстрирует кислую природу при разбавлении тестируемого соединения по сравнению с контролем, свободным от тестируемого соединения, показатель pH образца регулируют при использовании NaOH до показателя pH (контрольный) ±0,2 перед практической оценкой образца. Используют следующие критерии оценки: контроль: 0 баллов; сильный: 3 балла; очень сильный: 5 баллов, тест проводят при участии дегустационной комиссии из n (количества дегустаторов)=4. Дополнительно для большей ясности критерия начальный вкус и средний вкус/послевкусие γ-Glu-Val-Gly в концентрации 0,001 г/дл оценивают как 3,0 балла соответственно. Используемый в описании настоящей патентной заявки термин «средний вкус/послевкусие» относится к вкусу, ощущаемому в течение комбинированного периода времени, длящемуся с момента ощущения среднего вкуса и в течение периода ощущения послевкусия. Оценку проводят при использовании метода линейной шкалы, в частности, проводят, записывая каждую соответствующую оценку в прямую линию, на которой указаны соответствующие баллы -5~0~5. Дегустаторов, участвующих в этом тесте, выбирают из лиц, участвующих в разработке приправ для пищевых продуктов не менее одного года по совокупности и которые могут определить разницу в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly, добавленным в раствор со вкусом умами/соленым вкусом около 10 раз (подтверждая способность этих лиц на регулярной основе). Агент, придающий кокуми, по настоящему изобретению достойно продемонстрировал активность придания кокуми при добавлении в указанной выше концентрации. Результаты, полученные при типовых концентрациях, приведены в Таблице 2 ниже.
Дополнительно аналогично исследуют γ-Glu-Ala на эффект придания кокуми при использовании тех же процедур, и результаты также приведены в Таблице 2 ниже. Оба эти агента, придающие кокуми, демонстрируют высокие оценки в отношении начального вкуса, но было установлено, что γ-Glu-Abu является дипептидом, обладающим среди других очень высоким титром.
|
В качестве альтернативы γ-Glu-Cys и другие дипептид также оценивают на интенсивность придания кокуми при использовании той же количественной сенсорной оценки, как указано выше. Полученные результаты приведены в Таблице 3 ниже.
|
Таким образом, установлено, что γ-Glu-Abu обладает превосходным приданием кокуми, также было установлено, что он превосходно усиливает начальный вкус в отношение модели развития вкуса или модели развития вкуса приправы. Такое превосходное усиление начального вкуса, наблюдаемое у γ-Glu-Abu, является одним из преимуществ по сравнению с γ-Glu-Cys. Также γ-Glu-Abu обладает превосходной стабильностью, что также является преимуществом по сравнению γ-Glu-Cys. Дополнительно γ-Glu-Abu имеет короткую длину цепочки, поскольку включает только два аминокислотных остатка. Следовательно, можно относительно легко и при низкой стоимости, с точки зрения промышленного получения, получить агент по настоящему изобретению по сравнению с получением трипептида, включающего 3 аминокислотных остатка.
Пример 2: Определение интенсивности активности придания кокуми
Исследование интенсивности γ-Glu-Abu проводят методом тестирования с определением точки субъективного равенства (Point of Subjective Equality) (PSE) согласно технике определения пределов (“Statistical Sensory Examination techniques”, written by SATO Shin, опубликованной Japan Federation of Science and Technology).
В этом Примере сенсорную оценку проводят следующим образом: в качестве раствора для сенсорной оценки используют дистиллированную воду, содержащую глутамат натрия (0,05 г/дл), инозин монофосфат (0,05 г/дл) и хлорид натрия (0,5 г/дл). В качестве существующего дипептида, обладающего эффектом придания кокуми, используют γ-Glu-Val. Такой же уровень такого эффекта также можно наблюдать для γ-Glu-Cys и γ-Glu-Val, но они не демонстрируют по существу интенсивного начального вкуса и демонстрируют качество вкуса, отличающееся от такового γ-Glu-Abu. γ-Glu-Ala демонстрирует интенсивность эффекта придания кокуми, более слабую по сравнению с γ-Glu-Val, и обладает более сильным кислым вкусом, что создает трудности для манипулирования, поскольку требуется контроль pH. Аналогично γ-Glu-Ser демонстрирует интенсивность эффекта придания кокуми, более слабую по сравнению с γ-Glu-Val, аналогично придает посторонний вкус и, соответственно, создает трудности для манипулирования.
Для определения концентрации γ-Glu-Val, демонстрирующей развитие вкуса или эффект приправы, интенсивность которой идентична таковой для указанного выше раствора, используемого для сенсорной оценки, в него добавляют 0,005 г/дл γ-Glu-Abu, полученные таким образом растворы γ-Glu-Val имеют концентрации, варьирующие по 50% логарифмической шкале при использовании ее в качестве стандарта, в раствор, используемый для сенсорной оценки, добавляют 0,01 г/дл γ-Glu-Val. Концентрацию γ-Glu-Val изменяют на 7 стадиях в пределах от 0,0030 до 0,0337 г/дл. Когда образец демонстрирует кислую природу после каждого тестируемого соединения, растворенного в растворе для сенсорной оценки по сравнению с показателем pH контроля, свободного от тестируемого соединения, pH образца регулируют при использовании NaOH до показателя pH ( контрольный) ± 0,2 перед практической оценкой образца. Представленные восемнадцати дегустаторам эти растворы повышают концентрацию γ-Glu-Val, и тест проводят до тех пор, пока каждый дегустатор не оценит тестируемый раствор, имеющий конкретную концентрацию, демонстрирующую более сильный эффект придания кокуми по сравнению с таковым наблюдаемым для раствора, содержащего 0,005 г/дл γ-Glu-Abu. После паузы эти же восемнадцать дегустаторов оценивают указанные выше растворы на снижение концентрации γ-Glu-Val, проводят оценку до тех пор, пока каждый дегустатор не оценит тестируемый раствор, имеющий конкретную концентрацию, демонстрирующую более слабый эффект придания кокуми по сравнению с наблюдаемым у раствора, содержащего 0,005 г/дл γ-Glu-Abu.
В этом тесте на сенсорную оценку участвуют дегустаторы, обладающие достаточным опытом в области разработки пищевых продуктов. Результаты, полученные при проведении оценки, суммированы и приведены в Таблице 4 ниже.
|
|
1) Случаи, в которых верхнее и нижнее пороговые значения идентичны друг другу, соответствуют случаям, в которых оценка разницы между «сильнее» и «слабее» не определима, или в которых любая концентрация γ-Glu-Val не была четко указана. Например, дегустатор № 1 оценил, что эффект у γ-Glu-Val слабее по сравнению с γ-Glu-Abu при концентрации γ-Glu-Val 44 частей на миллион (0,0044 г/дл), в то время как он же оценил эффект γ-Glu-Abu более сильным при концентрации γ-Glu-Val 67 частей на миллион (0,0067 г/дл) и соответственно более низкое пороговое значение (55,5 частей на миллион) и более высокое пороговое значение (55,5 частей на миллион) идентичны друг другу.
2) «Доверительная область (или уровень доверия)» определяется как среднее низкого порогового значения и высокого порогового значения.
Точка субъективного равенства (PSE) γ-Glu-Val относительно 50 частей на миллион (0,0050 г/дл) γ-Glu-Abu определена, как следующее: (Сумма уровня доверия низкого порогового значения и высокого порогового значения)÷2.
Концентрация γ-Glu-Val (PSE) демонстрирует заданный эффект, интенсивность, которого идентична наблюдаемой для 0,0050 г/дл γ-Glu-Abu и может приниматься как около 0,0100 г/дл согласно оценке дегустаторов, приведенной в Таблице 4. При расчете PSE на основе верхнего и нижнего пороговых значений γ-Glu-Val, каждый из дегустаторов оценил эффекты, наблюдаемые для этих двух дипептидов, эквивалентными друг другу, и он установлен как 0,0122 г/дл. В этой связи интенсивность заданного придания эффекта кокуми γ-Glu-Abu установлена в около 2,4 раза по сравнению с γ-Glu-Val, и, следовательно, можно заключить, что первый дипептид обладает очень высокой интенсивностью эффекта. Таким образом, можно говорить о том, что γ-Glu-Abu является очень ценным дипептидом, который может быть легко получен по сравнению с традиционными известными веществами, и он продемонстрировал кокуми даже на стадии начального вкуса при использовании его в широком ряде пищевых продуктов.
Пример 3: Оценка эффективности γ-Glu-Abu на усиление соленого вкуса
В этом Примере исследуют эффект усиления γ-Glu-Abu соленого вкуса при проведении количественной сенсорной оценки.
Сенсорную оценку проводят следующим образом: тестируемое соединение в количестве, считающемся оптимальным, растворяют в дистиллированной воде, содержащей хлорид натрия (0,5 г/дл), и определяют интенсивность эффекта усиления соленого вкуса. Когда образец демонстрирует кислую природу после каждого тестируемого соединения, растворенного в растворе для сенсорной оценки, по сравнению с показателем pH контроля, свободного от тестируемого соединения, pH образца регулируют при использовании NaOH до показателя pH (контрольный) ±0,2 перед практической оценкой образца.
Сенсорную оценку эффекта проводят, используя следующие критерии от -5 до 0 до 5, при этом контроль, свободный от какого-либо соединения, или водный раствор хлорида натрия с концентрацией 0,5 г/дл оценивают как 0, а водный раствор хлорида натрия с концентрацией 0,75 г/дл оценивают как 5, тест проводят при участии дегустационной комиссии (n), состоящей из 5 дегустаторов. Используемый в описании настоящей патентной заявки термин «начальный вкус» относится к ощущению вкуса, определяемому каждым дегустатором во времени с момента потребления каждого образца до 2 секунд после этого, при этом термин «средний вкус/послевкусие» относится к вкусу, ощущаемому каждым дегустатором с момента 2 секунд после потребления образца или в течение, термин комбинирует период ощущения среднего вкуса и период ощущения послевкусия. Оценку проводят при использовании стандартной линейной техники, в частности, проводят, записывая каждую соответствующую оценку в прямую линию, на которой указаны соответствующие баллы -5~0~5. Дегустаторов, участвующих в этом тесте, выбирают из лиц, участвующих в разработке приправ для пищевых продуктов не менее одного года по совокупности и которые могут определить разницу в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly около 10 раз (подтверждая способность этих лиц на регулярной основе). Полученные результаты суммированы и приведены в Таблице 6 ниже.
|
В этом примере сравнивают способность придания кокуми трипетидом γ-Glu-Val-Gly с высоким титром с соответствующей способностью дипептида γ-Glu-Abu по настоящему изобретению. Результаты показывают, что γ-Glu-Val-Gly демонстрирует более высокую интенсивность активности придания кокуми по сравнению с таковой у γ-Glu-Abu, при этом следует принять во внимание концентрацию, используемую для оценки, и полученные в результате оценки. Такие же результаты получены при проведении сенсорной оценки профиля, однако баланс соленого вкуса значительно ниже в случае γ-Glu-Val-Gly. С другой стороны, γ-Glu-Abu может усиливать соленый вкус гораздо более сбалансированно и, следовательно, γ-Glu-Abu по существу подходит в качестве пептида, усиливающего соленый вкус.
Пример 4: Оценка воздействия органической кислоты, используемой в комбинации:
В этом примере исследуют воздействие использования органической кислоты на эффект усиления соленого вкуса в комбинации с γ-Glu-Abu при проведении количественной сенсорной оценки.
Тесты на сенсорную оценку проводят согласно следующим процедурам. С низким содержанием соли «Whole Chicken Stock» («цельный куриный бульон»), доступный от Ajinomoto Co., Ltd., растворяют в горячей воде, таким образом, что полученный в результате раствор имеет концентрацию поваренной соли 0,48 г/дл, затем растворяют подходящее количество каждого тестируемого соединения и определяют интенсивность соленого вкуса. Показатель pH образца, полученного раствора каждого тестируемого соединения, не отличается от такового у контроля, свободного от добавленного соединения и, следовательно, не требуется какого-либо регулирования показателя pH. При проведении сенсорной оценки не было обнаружено какого-либо воздействия, например кислый вкус. Для большей ясности критериев проведения сенсорной оценки используют следующие критерии оценки соленого вкуса: контроль: 3 балла; соленый вкус, наблюдаемый у супа, полученный при повышении концентрации соли в 1,25 раза по сравнению с контролем: 4 балла; и соленый вкус, наблюдаемый у супа, полученный при повышении концентрации соли в 1,5 раза по сравнению с контролем: 5 баллов, при этом тест проводят при участии дегустационной комиссии n (количество дегустаторов) = 6. Оценку проводят при использовании стандартной линейной техники, в частности, проводят, записывая каждую соответствующую оценку в прямую линию, на которой указаны соответствующие баллы 1~3~5. Дегустаторов, участвующих в этом тесте, выбирают из лиц, участвующих в разработке приправ для пищевых продуктов не менее одного года в совокупности и которые могут определить разницу в титре между γ-Glu-Cys-Gly и γ-Glu-Val-Gly около 10 раз (подтверждая способность этих лиц на регулярной основе). Полученные результаты суммированы и приведены в Таблице 7 ниже.
|
Следовательно, установлено, что молочная кислота и яблочная кислота в качестве органических кислот вполне подходят к γ-Glu-Abu и что использование молочной кислоты и яблочной кислоты в качестве органических кислот дополнительно улучшает эффект усиления соленого вкуса γ-Glu-Abu в комбинации с первым.
Другими словами, оказывается такое воздействие γ-Glu-Abu, что усиление соленого вкуса происходит в хорошо сбалансированной манере и может быть дополнительно улучшено при использовании органической кислоты в комбинации с дипептидом. При этом γ-Glu-Abu может быть получен из дешевых и широко доступных в настоящее время материалов, и соединение может дополнительно улучшить эффекты придания вкуса традиционных известных веществ.