Результат интеллектуальной деятельности: СПОСОБ ОБРАБОТКИ РАДИАКТИВНОГО РАСТВОРА
Вид РИД
Изобретение
Изобретение относится к технологии очистки растворов от радионуклидов и может быть использовано для дезактивации жидких радиоактивных отходов, содержащих радионуклиды кобальта, цезия и органические комплексообразователи в виде щавелевой кислоты, лимонной кислоты, этилендиаминтетрауксусной кислоты и др.
Дезактивация жидких радиоактивных отходов (ЖРО) сложного солевого состава на атомных электростанциях и предприятиях по переработке ЖРО является важной технологической и экологической задачей. Основная активность таких ЖРО определяется наличием радионуклидов кобальта, цезия, стронция. В составе ЖРО наряду с высокими концентрациями солей нерадиоактивных элементов присутствуют органические комплексообразователи, например этилендиаминтетрауксусная (ЭДТА), щавелевая, лимонная кислоты и др. Лиганды указанных органических кислот образуют с кобальтом(II) устойчивые в широком диапазоне рН комплексы, что препятствует извлечению радионуклидов кобальта(II) из раствора. Переработка ЖРО становится еще более сложной с появлением в растворе кобальта(III), который образует с органическими лигандами более устойчивые, чем кобальт(II), комплексы. На практике для переработки таких растворов предложено использовать различные варианты окислительного разрушения содержащихся в ЖРО органических соединений, после чего удаление кобальта становится возможным. Однако известные способы сложны, малопроизводительны, энерго- и реагентнозатратны и недостаточно эффективны, что определяет необходимость разработки более эффективных технических решений.
Известен способ обработки радиоактивного раствора (см. пат. 2321909 РФ, МПК G21F 9/16 (2006.01), 2008), согласно которому иммобилизируемые долгоживущие радионуклиды, преимущественно кобальт, стронций и марганец, конвертируют в нерастворимые соединения в гидротермальных условиях, пропуская поток перерабатываемого раствора и необходимые реагенты через слой нерастворимых частиц оксидов металлов: железа, и/или марганца, и/или кобальта, и/или циркония или соли в виде гидроксилапатита со скоростью, обеспечивающей кристаллизацию синтезируемых соединений, содержащих радионуклиды, на поверхности частиц слоя. Процесс ведут в автоклаве в присутствии хлорида марганца(II) и реагентов-окислителей: пероксида водорода и перманганата калия при температуре 180-250°С и давлении 20-150 атм. После очистки 1 л раствора от радиоактивных кобальта и цезия активность раствора составляет, Бк/л 60Co - 410, l37Cs - 2000.
Недостатком данного способа является необходимость проведения процесса в автоклаве при высоких температуре и давлении, что обусловливает низкую производительность, большие энергозатраты и повышенную опасность при переработке радиоактивных растворов. Все это снижает технологичность способа.
Наиболее близким к предлагаемому является способ обработки радиоактивного раствора (см. пат. 4340499 США, МПК3 G21F 9/10, 9/12, 9/16, 1982), содержащего органические комплексообразователи в виде щавелевой, муравьиной, лимонной и этилендиаминтетрауксусной кислот и радионуклиды кобальта и цезия. Согласно способу в радиоактивном растворе создают величину рН около 5 добавлением серной кислоты или натриевой щелочи, окисляют комплексообразователи в течение не менее 10 часов путем введения окисляющего реагента в виде перманганата калия, который берут с избытком, восстанавливают избыток иона MnO4 - до MnO2 добавлением сульфата марганца MnSO4 и отделяют образовавшийся осадок от маточного раствора. Затем рН раствора повышают до 9,0-10,5 введением, например, гидроксида натрия, растворяют в воде и добавляют сначала K4Fe(CN)6, а затем NiSO4 с образованием и осаждением Ni2Fe(CN)6, который одновременно осаждает радионуклиды цезия с коэффициентом очистки от 700 до 1000. Этот осадок отделяют от раствора, содержащего радионуклиды кобальта в форме соединений Co3+, добавляют к раствору [Co(NH3)6]Cl3 или другую соль Co3+ в щелочной среде, поддерживая рН добавлением, например, NH3, и восстанавливают Co3+ до Co2+ введением восстанавливающего реагента, например FeSO4, Na2S2O4 или SnCl2. Затем в раствор вводят декомплексующие агенты Са2+, Sr2+, с которыми соосаждают путем добавления NH4HS радионуклиды кобальта в виде CoS с отделением кобальтсодержащего осадка от маточного раствора. Коэффициент очистки от кобальта составляет ≥ 2000. Для предотвращения повторного окисления Co2+ в Co3+ отделение радионуклидов кобальта проводят в атмосфере инертного газа.
Известный способ обеспечивает хорошую очистку радиоактивного раствора от радионуклидов кобальта и цезия, однако нетехнологичен по причине использования значительного количества реагентов, в том числе дорогих и дефицитных солей кобальта, длительности окисления, образования и отделения 3-х осадков разного состава с раздельной очисткой от радионуклидов кобальта и цезия, использования защитной атмосферы инертного газа.
Настоящее изобретение направлено на достижение технического результата, заключающегося в повышении технологичности способа при обработке сложных по составу радиоактивных растворов, за счет снижения количества и стоимости используемых реагентов, длительности способа и уменьшения массы подлежащего захоронению радиоактивного осадка при обеспечении высокой степени очистки раствора от радионуклидов кобальта и цезия.
Технический результат достигается тем, что в способе обработки радиоактивного раствора, содержащего радионуклиды кобальта совместно с органическим комплексообразователем и радионуклиды цезия, включающем введение в исходный радиоактивный раствор окисляющего реагента при обеспечении заданной величины рН раствора и содержащего железо(II) восстанавливающего реагента с восстановлением кобальта(III) до кобальта(II) и декомплексацией последнего, введение осадителя с переводом радионуклидов кобальта и цезия в осадок и его отделение от маточного раствора, содержащего органический комплексообразователь и остаточное количество радионуклидов кобальта и цезия, согласно изобретению в качестве окисляющего реагента используют азотную кислоту, содержащий железо(II) реагент вводят в количестве 0,5-2,0 г/л Fe(II) при рН 3,0-3,5 с декомплексацией кобальта образующимися в растворе соединениями железа(III), полученный раствор выдерживают в течение 2-6 часов, в качестве осадителя берут сульфид натрия Na2S в количестве, стехиометрически необходимом для образования при величине рН 4-6 основного коллективного осадка сульфида железа FeS, содержащего радионуклиды кобальта и цезия, при этом маточный раствор подвергают циклу доочистки.
Технический результат достигается также тем, что в качестве органического комплексообразователя радиоактивный раствор содержит щавелевую, лимонную и этилендиаминтетрауксусную кислоту.
Технический результат достигается также и тем, что используют азотную кислоту при ее расходе 0,18-0,24 г-экв/л.
Технический результат достигается и тем, что в качестве реагента, содержащего железо(II), используют хлорид или сульфат.
На достижение технического результата направлено то, что перед введением реагента, содержащего железо(II), в раствор дополнительно вводят серную или соляную кислоту.
На достижение технического результата направлено также то, что обработку радиоактивного раствора ведут при 70-100°С.
Достижению технического результата способствует то, что цикл доочистки маточного раствора ведут путем добавления в раствор азотной, серной или соляной кислоты до обеспечения рН 3,0-3,5, соединений железа(II) и железа(III) в суммарном количестве 0,01-0,04 моль/л в пересчете на железо, выдержки маточного раствора в течение 2-6 часов, введения в него сульфида натрия Na2S в количестве, стехиометрически необходимом для образования при величине рН 4-6 дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия, и отделения осадка от доочищенного маточного раствора.
Достижению технического результата способствует также то, что осуществляют несколько циклов доочистки маточного раствора.
Сущность заявленного изобретения заключается в следующем. Из присутствующих в жидких радиоактивных отходах органических комплексообразователей в виде лимонной, щавелевой и этилендиаминтетрауксусной кислоты наиболее прочные комплексы образует ЭДТА с катионами кобальта. Цезий не образует комплексов с присутствующими в радиоактивном растворе органическими комплексообразователями. Логарифм константы устойчивости комплексов катионов Fe3+ с ЭДТА равен 25,1, в то время как комплексов катионов Co2+ - 16,31 при ионной силе раствора µ=0,1 и температуре 20°С (см. Г.Шварценбах. Комплексометрическое титрование // В сб.: Комплексометрия. Теоретические основы и практическое применение. Пер.с нем. М.: Госхимиздат, 1958. С.22), а катионов Со3+ - 36 (см. Лурье Ю.Ю. Справочник по аналитической химии. - М: Химия, 1967. С.260). То есть комплексы ЭДТА3- с Fe3+ значительно более устойчивы, чем комплексы ЭДТА2- с Co2+, но менее устойчивы, чем комплексы ЭДТА2- с Co3+. Сходные зависимости имеют место для комплексов Fe3+, Co2+ и Co3+ с лимонной и щавелевой кислотами. Хотя промышленные ЖРО имеют значительно более высокую ионную силу, нами экспериментально установлено, что и в таких ЖРО возможно катионное замещение согласно обменной реакции:
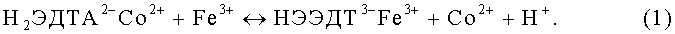
Для успешного проведения замещения всех катионов кобальта на катионы железа в органических комплексах необходимо обеспечить переход кобальта(III) в кобальт(II) и преобладающее присутствие в радиоактивном растворе вводимого железа (III) в катионной форме, поскольку при повышении кислотности оно может переходить в анионную форму, например, в виде FeCl4 -. Для этого требуется введение агента, восстанавливающего кобальт(III) до кобальта(II), и точное регулирование кислотности раствора. Однако промышленные радиоактивные растворы содержат высокие концентрации нерадиоактивных солей, в том числе боратов, нитратов, хлоридов и сульфатов натрия и калия в присутствии небольших количеств окислителей, например соединений xpoMa(VI), содержащих ионы Cr2O7 2- или CrO4 2-. Согласно изобретению наиболее эффективное восстановление кобальта(III) до кобальта(II) в органических комплексах промышленных ЖРО может быть осуществлено введением такого восстановителя, как соединение железа(II), после предварительной азотнокислотной обработки раствора. В результате азотнокислотной обработки при расходе 0,18-0,24 г-экв/л кислоты наблюдается реакция окисления наиболее окисляемой части органики, сопровождаемая пенообразованием и уменьшением кислотности раствора. После этого, при необходимости, вводят серную или соляную кислоту до рН 3,0-3,5, создавая оптимальную для проведения реакции (1) кислотность. Из-за высокой устойчивости органических комплексов, содержащих кобальт, реакция (1) протекает медленно, что определяет необходимость выдержки раствора в течение 2-6 часов после кислотной обработки. Повышение температуры радиоактивного раствора до 70-100°С ускоряет протекание реакции (1).
После установления равновесия согласно реакции (1) в радиоактивный раствор вводят сульфид натрия Na2S, при этом в условиях слабокислой среды при рН 4-6 протекают реакции:
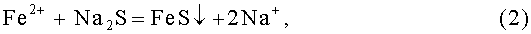
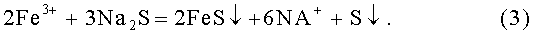
Образующийся коллективный осадок, содержащий сульфид железа FeS, захватывает радионуклиды кобальта и цезия. После отделения осадка получают в значительной мере очищенный от радионуклидов кобальта и цезия маточный раствор. За одну ступень обработки степень очистки от радионуклидов кобальта составляет 77-86%, а от радионуклидов цезия - 98,2-98,5%. Доочистка маточного раствора позволяет повысить степень очистки от радионуклидов кобальта и цезия до требуемых санитарных норм (см. Нормы радиационной безопасности (НРБ-99). СП.2.6.1.758-99. М.: Минздрав России, 1999. 130 с.).
Существенные признаки заявленного изобретения, определяющие объем правовой охраны и достаточные для получения вышеуказанного технического результата, выполняют функции и соотносятся с результатом следующим образом.
Использование в качестве окисляющего реагента азотной кислоты обеспечивает окисление части органики с уменьшением кислотности раствора до рН 3,0-3,5. Кроме того, при обработке сложных по составу радиоактивных растворов, содержащих значительное количество нитратов натрия и калия, их присутствие будет усиливать окисляющее воздействие азотной кислоты.
Введение недорогого содержащего железо(II) восстанавливающего реагента в количестве 0,5-2,0 г/л Fe(II) при рН 3,0-3,5 обеспечивает эффективное восстановление кобальта(III) до кобальта(II) в комплексе с органическим лигандом и замещение кобальта(II) на железо(III) по реакции (1) с декомплексацией кобальта образующимися в растворе соединениями железами), что обеспечивает более высокую степень извлечения радионуклидов кобальта из раствора. Концентрации железа(II) менее 0,5 г/л не обеспечивают полного восстановления всех присутствующих в растворе окисленных форм. При этом снижается степень замещения в органических комплексах катионов радиоактивного кобальта(II) на катионы Fe3+. Концентрация железа(II) более 2 г/л приводит к излишнему расходу реагентов в виде солей железа и сульфида натрия, не оказывая заметного влияния на степень замещения в комплексах катионов радиоактивного кобальта(II) на катионы Fe3+.
Выдержка очищаемого радиоактивного раствора в течение 2-6 часов необходима для обеспечения наиболее полного прохождения реакции замещения катионов радиоактивного кобальта(II) на катионы Fe3+. Выдержка раствора в течение менее 2 часов не обеспечивает полноты восстановления кобальта(III) до кобальта(II) и замещения кобальта(II) железом(III). Выдержка более 6 часов не приводит к существенному повышению полноты замещения.
Использование в качестве сульфидного осадителя сульфида натрия Na2S в количестве, стехиометрически необходимом для образования при величине рН 4-6 основного коллективного осадка сульфида железа FeS, содержащего радионуклиды кобальта и цезия, позволяет достичь наиболее полное извлечение радионуклидов согласно реакциям (2, 3) при обеспечении хорошей фильтруемости осадка. При количестве сульфида натрия, меньшем стехиометрического, снижается полнота образования сульфида железа и, как следствие, полнота осаждения радионуклидов кобальта и цезия. Введение сульфида натрия в количестве, большем, чем стехиометрическое, приводит к нерациональному с технологической точки зрения расходу сульфида натрия. В результате потребуется повышенный расход соединений железа(III) при доочистке маточного раствора и возрастет масса по отношению к очищаемому раствору подлежащих захоронению коллективных осадков, содержащих сульфид железа наряду с радионуклидами кобальта и цезия.
Доочистка маточного раствора необходима для обеспечения более высокой степени извлечения радионуклидов кобальта и цезия из ЖРО сложного солевого состава.
Совокупность вышеуказанных признаков необходима и достаточна для достижения технического результата изобретения, заключающегося в снижении количества и стоимости используемых реагентов, длительности способа, уменьшении массы подлежащего захоронению радиоактивного осадка при обеспечении высокой степени очистки раствора от радионуклидов кобальта и цезия. Все это повышает технологичность способа при обработке сложных по составу радиоактивных растворов.
В частных случаях осуществления изобретения предпочтительны следующие конкретные операции и режимные параметры.
Присутствие в радиоактивном растворе в качестве комплексообразователя щавелевой, лимонной и этилендиаминтетрауксусной кислоты обусловлено тем, что эти кислоты являются основными используемыми комплекосообразователями при эксплуатации и профилактике атомных реакторов. Они могут присутствовать в ЖРО как совместно, так в различном сочетании в зависимости от конкретного состава ЖРО.
Использование в качестве окисляющего реагента азотной кислоты при ее расходе 0,18-0,24 г-экв/л обеспечивает необходимую кислотность раствора, при которой происходит окисление части органики с уменьшением концентрации ионов водорода. Введение кислоты в количестве более 0,24 г-экв/л приводит к избыточному расходу реагента, расход менее 0,18 г-экв/л не обеспечивает интенсивного протекания окисления.
Использование хлорида или сульфата железа в качестве реагента, содержащего железо(II), обусловлено высокой растворимостью этих соединений в водных средах и возможностью создания значительных концентраций железа(II), что обеспечивает при относительной дешевизне реагентов эффективное восстановление кобальта(III) до кобальта(II).
Введение в радиоактивный раствор серной или соляной кислоты в дополнение к азотной кислоте перед введением реагента, содержащего железо(II), обеспечивает поддерживание требуемого диапазона значений рН 3,0-3,5 с использованием эффективных и более дешевых реагентов.
Проведение обработки радиоактивного раствора при 70-100°С обусловлено тем, что из-за высокой устойчивости органических комплексов, содержащих кобальт, реакция замещения (1) протекает медленно, а повышение температуры раствора ускоряет ее.
При доочистке маточного раствора от остаточного количества радионуклидов кобальта и цезия добавление в раствор азотной, серной или соляной кислоты до обеспечения рН 3,0-3,5 позволяет создать оптимальные условия для проведения реакции (1).
Введение в маточный раствор соединений железа(II) и железа(III) в суммарном количестве 0,01-0,04 моль/л в пересчете на железо обусловлено тем, чтобы, с одной стороны, в присутствии железа(II) предотвратить неконтролируемое окисление кобальта(II) в кобальт(III), а с другой стороны, чтобы в присутствии железа(III) обеспечить более полное замещение кобальта(II) железом(III) из органического комплекса согласно реакции (1). Мольное соотношение соединений железа(II) и железа(III) в пересчете на железо предпочтительно в диапазоне 1:1-4.
Выдержка маточного раствора в течение 2-6 часов обусловлена полнотой протекания реакций восстановления кобальта(III) до кобальта(II) и замещения кобальта(II) железом(III). Выдержка раствора в течение менее 2 часов не обеспечивает полноты восстановления кобальта(III) до кобальта(II) и замещения кобальта(II) железом(III). Выдержка более 6 часов приводит к неоправданным затратам времени на переработку маточного раствора.
Введение в доочищаемый маточный раствор сульфида натрия Na2S в количестве, стехиометрически необходимом для образования при величине рН 4-6 дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия, как и при очистке исходного радиоактивного раствора, обеспечивает наиболее полное извлечение радионуклидов при хорошей фильтруемости осадка от доочищенного маточного раствора. Основной и дополнительный коллективные осадки, содержащие радионуклиды кобальта и цезия, перед захоронением, как правило, объединяют.
Вышеуказанные частные признаки изобретения позволяют осуществить способ в оптимальном режиме с точки зрения повышения технологичности способа при обеспечении высокой степени очистки раствора от радионуклидов кобальта и цезия.
Указанные выше особенности и преимущества заявляемого изобретения могут быть более наглядно пояснены нижеследующими Примерами.
Пример 1. Берут 1 л радиоактивного раствора плотностью 1,37 кг/дм3, содержащего, Бк/л: 60Co - 7·103 и Σ134Cs и 137Cs - 8,6·104 и 640 г солей в виде боратов, нитратов, хлоридов и сульфатов натрия и калия в присутствии микроколичеств соединений хрома(VI), а также органические комплексообразователи в виде смеси щавелевой, лимонной и этилендиаминтетрауксусной кислот. В раствор, имеющий рН 8, вводят окисляющий реагент в виде азотной кислоты при ее расходе 0,2 г-экв/л (12,6 г/л) до прекращения пенообразования и обеспечения рН 3,2. Затем вводят 5,44 г восстанавливающего реагента в виде сульфата железа FeSO4 (2,0 г/л в пересчете на Fe(II)) с восстановлением кобальта(III) до кобальта(II) и декомплексацией последнего образующимися в растворе соединениями железа(III). Раствор выдерживают в течение 3 часов. После этого в раствор вводят 2,8 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 3,14 г основного коллективного осадка сульфида железа FeS, содержащего радионуклиды кобальта и цезия. Величина рН раствора составляет 5. Осадок отделяют фильтрованием от маточного раствора, содержащего органический комплексообразователь и остаточное количество радионуклидов кобальта и цезия. Состав маточного раствора, Бк/л: 60Co - 9,8·102 и Σl34Cs и 137Cs - 1,3·103. Степень очистки составила по 60Co - 86%, по Σ134Cs и 137Cs - 98,49%.
Проводят цикл доочистки маточного раствора. В маточный раствор вводят раствор серной кислоты до обеспечения рН 3,1, добавляют 3 г сульфата железа(II) FeSO4 и 3,25 г хлорида железа(III) FeCl3 в суммарном количестве 2,2 г (0,04 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 4 часа, после чего в него добавляют 3,9 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 3,84 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 6. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного маточного раствора по радионуклидам, Бк/л: 60Co - 210 и Σl34Cs и l37Cs - 37. Степень очистки составила по 60Co - 78,6%, по Σl34Cs и l37Cs - 97,2%. Доочищенный маточный раствор по радиоактивности соответствует установленным нормам. Общая масса высушенных основного и дополнительного радиоактивных осадков равна 6,98 г. Итоговая степень очистки за одну ступень обработки и один цикл доочистки маточного раствора составила 97% для кобальта и 99,96% для цезия. Соответственно, коэффициент очистки раствора, характеризующий распределение активности между раствором и образующимся радиоактивным осадком, составляет по кобальту - 6,3·103 и по цезию - 4,56·105.
Пример 2. Берут 1 л радиоактивного раствора плотностью 1,32 кг/дм3, содержащего, Бк/л: 60Co - 1,2·104 и Σ134Cs и 137Cs - 1,6·105 и 540 г солей в виде боратов, нитратов, хлоридов и сульфатов натрия и калия в присутствии микроколичеств соединений хрома(VI), а также органические комплексообразователи в виде смеси щавелевой, лимонной и этилендиаминтетрауксусной кислот. В раствор, имеющий рН 7, при температуре 70°С вводят окисляющий реагент в виде азотной кислоты при ее расходе 0,24 г-экв/л (15,12 г/л) до прекращения пенообразования и обеспечения рН 3. Затем вводят 2,72 г восстанавливающего реагента в виде сульфата железа FeSO4 (1 г/л в пересчете на Fe(II)) с восстановлением кобальта(III) до кобальта(II) и декомплексацией последнего образующимися в растворе соединениями железа(III). Раствор выдерживают в течение 6 часов. После этого в раствор вводят 1,4 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 1,57 г основного коллективного осадка сульфида железа FeS, содержащего радионуклиды кобальта и цезия. Величина рН раствора составляет 4. Осадок отделяют фильтрованием от маточного раствора, содержащего органический комплексообразователь и остаточное количество радионуклидов кобальта и цезия. Состав маточного раствора, Бк/л: 60Co - 2,76·103 и Σl34Cs и l37Cs - 2,88·103. Степень очистки составила по 60Co - 77%, по Σ134Cs и 137Cs - 98,2%.
Проводят первый цикл доочистки маточного раствора. В маточный раствор вводят раствор соляной кислоты до обеспечения рН 3, добавляют 1,9 г хлорида железа(II) FeCl2 и 2,43 г хлорида железа(III) FeCl3 в суммарном количестве 1,7 г (0,03 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 2 часа при температуре 70°С, после чего в него добавляют 2,93 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 2,88 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 5. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после первого цикла маточного раствора по радионуклидам, Бк/л: 60Co - 654 и Σ134Cs и 137Cs - 115. Степень очистки в 1 цикле доочистки составила по 60Co - 76,3%, по Σ134Cs и 137Cs - 96%. За одну ступень обработки и один цикл доочистки маточного раствора степень очистки составила: Co - 94,55%, Cs - 99,93%.
Проводят второй цикл доочистки маточного раствора. В маточный раствор вводят раствор соляной кислоты до обеспечения рН 3, добавляют 1,9 г хлорида железа(II) FeCl2 и 2,43 г хлорида железа(III) FeCl3 в суммарном количестве 1,7 г (0,03 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 2 часа при температуре 70°С, после чего в него добавляют 2,93 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 2,88 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 5. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после второго цикла маточного раствора по радионуклидам, Бк/л: 60Co - 158 и Σl34Cs и l37Cs - 23. Степень очистки во 2 цикле доочистки составила по 60Co - 75,84%, по Σ134Cs и l37Cs - 80%.
Доочищенный маточный раствор по радиоактивности соответствует установленным нормам. Общая масса высушенных основного и двух дополнительных радиоактивных осадков равна 7,33 г. С учетом 2 циклов доочистки маточного раствора итоговая степень очистки составила 98,68% для кобальта и 99,99% для цезия. Соответственно, коэффициент очистки раствора составляет по кобальту - 1,3·104 и по цезию - 1,25·106.
Пример 3. Берут 1 л радиоактивного раствора плотностью 1,29 кг/дм3, содержащего, Бк/л: 60Co - 1,94·104 и Σ134Cs и l37Cs - 1,54·106 и 480 г солей в виде боратов, нитратов, хлоридов и сульфатов натрия и калия в присутствии микроколичеств соединений хрома(VI), а также органические комплексообразователи в виде смеси щавелевой, лимонной и этилендиаминтетрауксусной кислот. В раствор, имеющий рН 8, при температуре 80°С вводят окисляющий реагент в виде азотной кислоты при ее расходе 0,18 г-экв/л (11,34 г/л) до прекращения пенообразования и обеспечения рН 3,5. Затем вводят 4,1 г восстанавливающего реагента в виде сульфата железа FeSO4 (1,5 г/л в пересчете на Fe(II)) с восстановлением кобальта(III) до кобальта(II) и декомплексацией последнего образующимися в растворе соединениями железа(III). Раствор выдерживают в течение 2 часов. После этого в раствор вводят 2,1 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 2,36 г основного коллективного осадка сульфида железа FeS, содержащего радионуклиды кобальта и цезия. Величина рН раствора составляет 6. Осадок отделяют фильтрованием от маточного раствора, содержащего органический комплексообразователь и остаточное количество радионуклидов кобальта и цезия. Состав маточного раствора, Бк/л: 60Co - 4,2·103 и Σl34Cs и l37Cs - 2,31·104. Степень очистки составила по 60Co - 78,35%, по Σ134Cs и l37Cs - 98,5%.
Проводят первый цикл доочистки маточного раствора. В маточный раствор вводят раствор азотной кислоты до обеспечения рН 3,5, добавляют 0,76 г сульфата железа(Н) FeSO4 и 3 г сульфата железа(III) Fe2(SO4)3 в суммарном количестве 1,11 г (0,02 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 6 часов при температуре 80°С, после чего в него добавляют 2,15 сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 2 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 6. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после первого цикла маточного раствора по радионуклидам, Бк/л: 60Co -994 и Σl34Cs и 137Cs - 970. Степень очистки в 1 цикле составила по 60Co - 76,3%, по Σl34Cs и l37Cs - 95,8%. За одну ступень обработки и один цикл доочистки маточного раствора степень очистки составила: Со - 94,77%, Cs - 99,37%.
Проводят второй цикл доочистки маточного раствора. В маточный раствор вводят раствор азотной кислоты до обеспечения рН 3,5, добавляют 0,76 г сульфата железа(II) FeSO4 и 3 г сульфата железа(III) Fe2(SO4)3 в суммарном количестве 1,11 г (0,02 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 6 часов при температуре 80°С, после чего в него добавляют 2,15 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 2 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 6. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после второго цикла маточного раствора по радионуклидам, Бк/л: 60Co - 220 и Σl34Cs и 137Cs - 32. Степень очистки во 2 цикле составила по 60Co - 76,7%, по Σ134Cs и 137Cs - 96,7%.
Доочищенный маточный раствор по радиоактивности соответствует установленным нормам. Общая масса высушенных основного и двух дополнительных радиоактивных осадков равна 6,36 г. С учетом 2 циклов доочистки маточного раствора итоговая степень очистки составила 98,87% для кобальта и 99,98% для цезия. Соответственно, коэффициент очистки раствора составляет по кобальту - 1,77·104 и по цезию - 9,76·106.
Пример 4. Берут 1 л радиоактивного раствора плотностью 1,36 кг/дм3, содержащего, Бк/л: 60Co - 1,06·105 и Σ134Cs и 137Cs - 5,4·107 и 610 г солей в виде боратов, нитратов, хлоридов и сульфатов натрия и калия в присутствии микроколичеств соединений хрома(VI), а также органические комплексообразователи в виде смеси щавелевой, лимонной и этилендиаминтетрауксусной кислот. В раствор, имеющий рН 6, при температуре 100°С вводят окисляющий реагент в виде азотной кислоты при ее расходе 0,21 г-экв/л (13,33 г/л) до прекращения пенообразования и обеспечения рН 3,2. Затем вводят 1,37 г восстанавливающего реагента в виде сульфата железа FeSO4 (0,5 г/л в пересчете на Fe(II)) с восстановлением кобальта(III) до кобальта(II) и декомплексацией последнего образующимися в растворе соединениями железа(III). Раствор выдерживают в течение 4 часов. После этого в раствор вводят 0,7 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 0,79 г основного коллективного осадка сульфида железа FeS, содержащего радионуклиды кобальта и цезия. Величина рН раствора составляет 6. Осадок отделяют фильтрованием от маточного раствора, содержащего органический комплексообразователь и остаточное количество радионуклидов кобальта и цезия. Состав маточного раствора, Бк/л: 60Co - 2,3·104 и Σl34Cs и l37Cs - 9,2·105. Степень очистки составила по 60Co - 78,3%, по Σ134Cs и l37Cs - 98,3%.
Проводят первый цикл доочистки маточного раствора. В маточный раствор вводят раствор серной кислоты до обеспечения рН 3,3, добавляют 0,76 г сульфата железа(II) FeSO4 и 0,81 г хлорида железа(III) FeCl3 в суммарном количестве 0,56 г (0,01 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 5 часов при температуре 100°С, после чего в него добавляют 0,98 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 0,96 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 4. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после первого цикла маточного раствора по радионуклидам, Бк/л: 60Co - 5,1·103 и Σ134Cs и 137Cs - 2,4·104. Степень очистки в 1 цикле составила по 60Co 77,8%, по Σl34Cs и 137Cs - 97,4%. За одну ступень обработки и один цикл доочистки маточного раствора степень очистки составила: Co - 95,19%, Cs - 99,96%.
Проводят второй цикл доочистки маточного раствора. В маточный раствор вводят раствор серной кислоты до обеспечения рН 3,3, добавляют 0,76 г сульфата железа(II) FeSO4 и 0,81 г хлорида железа(III) FeCl3 в суммарном количестве 0,56 г (0,01 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 5 часов при температуре 100°С, после чего в него добавляют 0,98 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 0,96 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 4. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после второго цикла маточного раствора по радионуклидам, Бк/л: 60Co - 1,16·103 и Σ134Cs и 137Cs - 745. Степень очистки во 2 цикле составила по 60Co - 77,25%, по Σ134Cs и 137Cs - 96,9%.
Проводят третий цикл доочистки маточного раствора. В маточный раствор вводят раствор серной кислоты до обеспечения рН 3,3, добавляют 0,76 г сульфата железа(II) FeSO4 и 0,81 г хлорида железа(III) FeCl3 в суммарном количестве 0,56 г (0,01 моль/л) в пересчете на железо. Маточный радиоактивный раствор выдерживают 5 часов при температуре 100°С, после чего в него добавляют 0,98 г сульфида натрия Na2S, что соответствует стехиометрически необходимому количеству для образования 0,96 г дополнительного коллективного осадка сульфида железа FeS, содержащего остаточные радионуклиды кобальта и цезия. Величина рН раствора составляет 4. Полученный осадок отделяют фильтрованием от маточного раствора. Состав доочищенного после третьего цикла маточного раствора по радионуклидам, Бк/л: 60Co - 270 и Σ134Cs и 137Cs - 35. Степень очистки в 3 цикле составила по 60Со - 76,7%, по Σ134Cs и l37Cs - 95,3%.
Доочищенный маточный раствор по радиоактивности соответствует установленным нормам. Общая масса высушенных основного и трех дополнительных радиоактивных осадков равна 3,67 г. С учетом 3 циклов доочистки маточного раствора итоговая степень очистки составила 99,75% для кобальта и 99,999% для цезия. Соответственно, коэффициент очистки раствора составляет по кобальту - 1,45·105 и по цезию - 5,72·108.
Из данных, приведенных в Примерах 1-4, видно, что предлагаемый способ обработки радиоактивного раствора при снижении количества и стоимости используемых реагентов и незначительной массе подлежащего захоронению радиоактивного осадка позволяет за одну ступень обработки и один цикл доочистки маточного раствора обеспечить степень очистки от радионуклидов кобальта 94,55-97,0% (коэффициент очистки - не менее 5,1·103), а от радионуклидов цезия - 99,37-99,96% (коэффициент очистки - не менее 4,69·103). За 3 цикла доочистки маточного раствора итоговая степень очистки возрастает до 99,75% для кобальта (коэффициент очистки 1,45·105) и до 99,999% для цезия (коэффициент очистки 5,72·108). Все это свидетельствует о высокой технологичности заявленного способа обработки радиоактивного раствора. Кроме того, способ относительно прост и может быть реализован с привлечением стандартного технологического оборудования.

