Результат интеллектуальной деятельности: ТЕСТ-СИСТЕМА ДЛЯ ПОЛУКОЛИЧЕСТВЕННОГО ИММУНОХРОМАТОГРАФИЧЕСКОГО АНАЛИЗА
Вид РИД
Изобретение
Изобретение относится к устройствам для иммунохроматографического определения с использованием в качестве маркера золотых наночастиц и может быть использовано в биотехнологии и медицинской диагностики для полуколичественного визуального определения поливалентных антигенов, в том числе белков, с чувствительностью, достигаемой известными методами твердофазного иммуноферментного анализа (ИФА).
В течение последнего десятилетия получили развитие так называемые «быстрые методы» проведения анализа различных соединений с визуальной регистрацией результатов, которые уже нашли широкое использование в медицинской диагностике, фармацевтической и пищевой промышленности, охране окружающей среды, ветеринарии и других областях (R.C. Wang, H.Y. Tse, Eds., Lateral Flow Immunoassay, Springer, 2009). Методы основаны на использовании специальных мембранных носителей с заранее импрегнированными в них реакционными компонентами, позволяющими определять анализируемое соединение по окрашиванию линии в тестовой зоне устройства. Наиболее распространенным вариантом является иммунохроматографический метод, основанный на связывании определяемого антигена специфическими антителами в тестовой области аналитической мембраны с использованием в качестве визуальной метки образующегося иммунокомплекса окрашенных в розовый цвет частиц коллоидного золота (Posthuma-Trumpie G.A., Jakob Korf J, Amerongen A. Lateral flow (immuno)assay: its strengths, weaknesses, opportunities and threats. A literature survey. Anal Bioanal Chem, 2009, vol.393, pp.569-582)
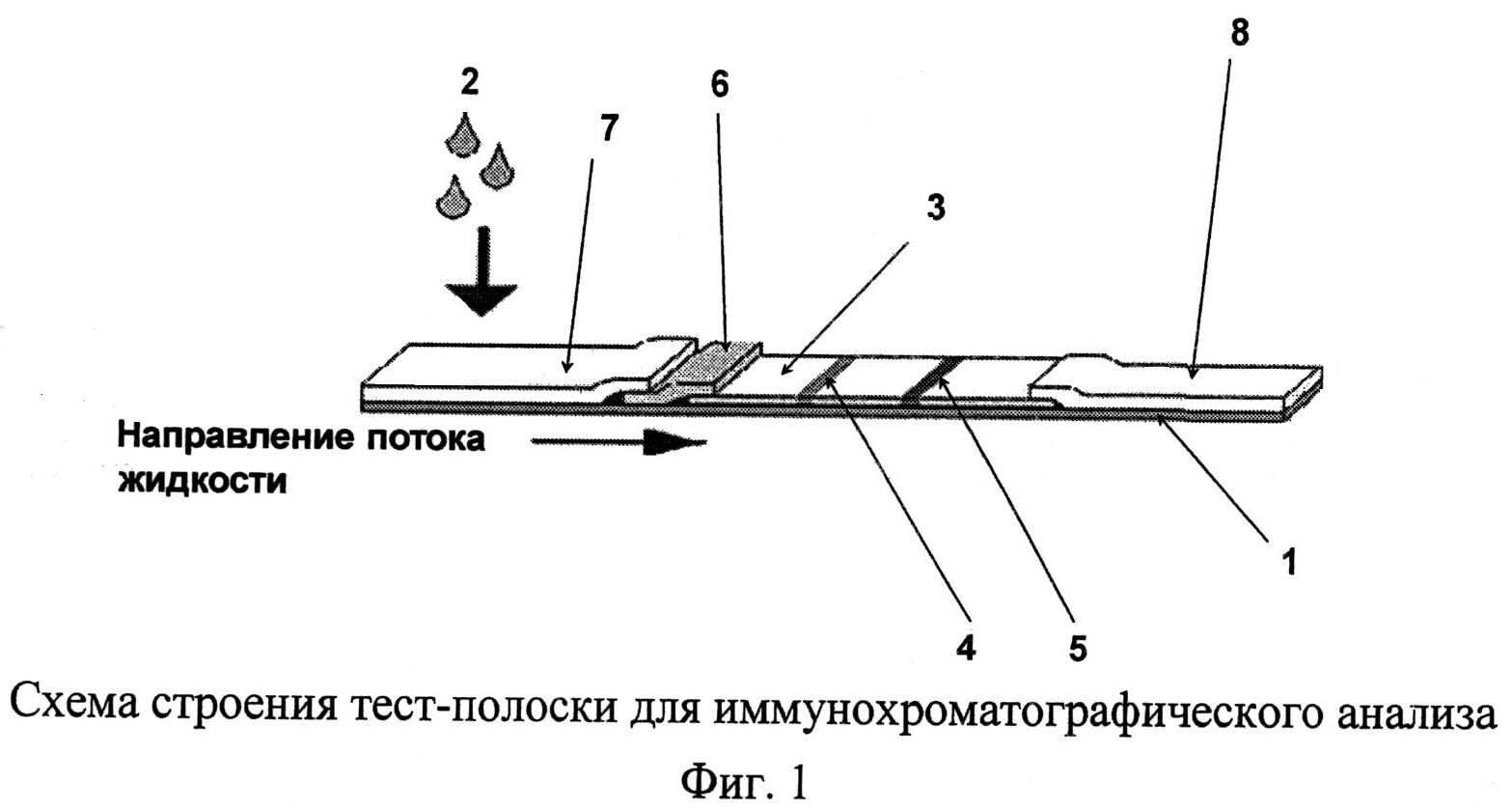
На фиг.1. приведена схема тест-системы для иммунохроматографического определения антигенов по сэндвич-схеме иммуноанализа (см., например, патент США №5712172, МПК G01N/533, опубл. 27.12.1997 - прототип).
Основой устройства является тест-полоска, состоящая из нескольких ламинированных на пластиковой подложке 1 примыкающих друг к другу мембран, по которым движется поток жидкости, содержащей анализируемый образец 2. На стекловолоконной мембране 6 содержится конъюгат наночастиц золота со специфическими первыми моноклональными антителами к определяемому антигену. На аналитической мембране 3 в виде узкой линии в тестовой зоне 4 нанесены вторые специфические моноклональные антитела к определяемому антигену и в аналогичной контрольной зоне 5 - вторичные (антивидовые) антитела против первых специфических моноклональных антител. При нанесении образца 2 на специальную мембрану 7 для образца, расположенную у начала тест - полоски, начинается его движение вдоль полоски под действием капиллярных сил. В присутствии определяемого антигена в образце, по мере продвижения вдоль мембраны происходит его взаимодействие с конъюгатом меченых золотом первых моноклональных антител и образование комплекса антигена с сорбированными на поверхности коллоидных частиц золота специфическими первыми моноклональными антителами. В тестовой зоне 3 происходит связывание иммунокомплекса иммобилизованными специфическими вторыми моноклональными антителами и наблюдается появление окрашенной линии, интенсивность окраски которой пропорциональна содержанию анализируемого вещества в образце. Избыток несвязавшихся меченых антител проходит далее к контрольной зоне 8, где образуется вторая окрашенная линия. При отсутствии в исследуемом образце определяемого антигена, меченные золотом антитела задерживаются лишь вторичными антителами в области контрольной линии 8. Таким образом, наличие видимой окраски в контрольной зоне в обоих случаях свидетельствует о работоспособности теста. Расположение дополнительной впитывающей мембраны 9 на конце тест - полоски позволяет осуществлять более равномерное и продолжительное движение образца вдоль полоски.
В этой связи рассмотренное в прототипе устройство и метод визуального анализа является качественным, позволяющим на основании появления или отсутствия тестовой полосы по принципу «да-нет» говорить о наличии или отсутствии определяемого соединения в анализируемом растворе. Появление окрашенной линии в тестовой зоне свидетельствует о превышении некоторого порогового уровня концентрации антигена в анализируемом растворе. Наилучшие достоверные результаты получают для тех антигенов, для которых наблюдается значительное превышение некоторой пороговой концентрации (например, в медицинской практике, при определении хорионического гонадотропина человека для ранней диагностики беременности).
Интенсивность окраски тестовой линии зависит от концентрации определяемого в образце антигена, однако определение интенсивности окраски тестовой линии визуальным методом для получения полуколичественных результатов сопряжено с большими ошибками ввиду трудности визуальной сравнительной оценки интенсивности окраски линии со стандартными шаблонами. Количественная оценка может быть достигнута только с использованием специальных фотометрических методик, основанных на отражении или отражательных фотометров, например (патент РФ №2217755, МПК7 G01N 33/53, G01N 21/01, опубликовано: 27.11.2003), что значительно усложняет и удорожает стоимость проводимого анализа.
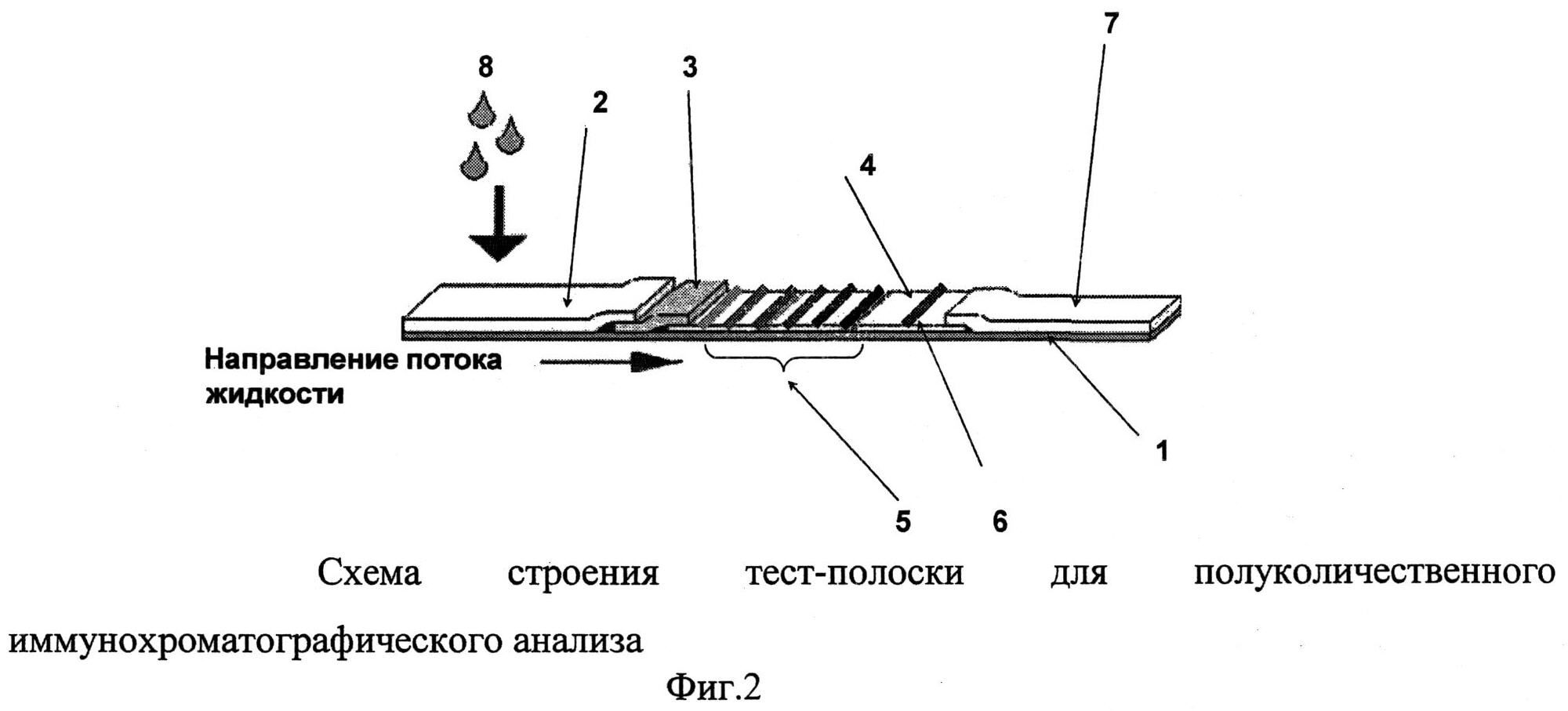
Задачей настоящего изобретения является создание тест-системы (устройства) для осуществления полуколичественного визуального иммунохроматографического анализа и бесприборной оценки результатов, основанной не на определении интенсивности окрашивания тестовой полосы, а на подсчете числа окрашенных тестовых линий. Схема предлагаемой тест - системы представлена на фиг.2. Задача решается тем, что используют тест-систему для иммунохроматографического анализа, включающую пластиковую подложку 1 с ламинированными на ее поверхности внахлестку (соприкасающимися по концам) мембранами (мембрана для образца 2, мембрана для конъюгата золотых наночастиц с первыми специфическими моноклональными антителами 3, аналитическая мембрана 4 с тестовой 5 и контрольной 6 зонами, отсасывающая мембрана 7), причем на аналитической мембране 4 в тестовой зоне 5 расположено от 2 до 10 поперечных параллельных тестовых линий, образованных путем нанесения на мембрану растворов вторых специфических моноклональных антител против определяемого соединения с концентрацией антител, последовательно увеличивающейся в направлении движения образца жидкости. В конечном участке аналитической мембраны иммобилизуют в виде поперечной контрольной линии 6 антивидовые антитела, которые связывают избыток конъюгата золотых частиц в ходе проведения анализа с образованием окрашенной контрольной линии.
Принцип работы заявляемой тест-системы заключается в следующем. При нанесении образца 8, содержащего определяемый антиген, на мембрану для нанесения образца 2 под действием капиллярных сил раствор анализируемого соединений движется вдоль полоски, взаимодействует с конъюгатом специфических антител с золотыми наночастицами, иммобилизованном в мембране для конъюгата 2, и образующийся иммунокомплекс далее распространяется вдоль аналитической мембраны 4, на которой иммобилизованы вторые специфические антитела в тестовой зоне 5 в виде нескольких линий с последовательно увеличивающейся концентрацией антител. В зависимости от концентрации анализируемого антигена, образующийся иммунокомплекс будет задерживаться различными участками тестовой зоны 5 аналитической мембраны 4: при относительно небольших концентрациях антигена в образце, удерживание иммунокомплекса будет наблюдаться только в удаленных зонах с достаточно высокой концентрацией сорбированных антител, наоборот, при больших концентрациях антигена в образце эффективность связывания в иммунокомплекс и количество проявляемых линий будет увеличиваться и включать начальные зоны с относительно малым содержанием сорбированных на мембране антител. Ввиду того, что золотые наночастицы имеют ярко выраженную розовую окраску, количество окрашенных линий в тестовой зоне мембраны будет пропорционально концентрации определяемого соединения в анализируемом растворе. При достижении контрольной линии 6 избыток конъюгата задерживается на ней, проявляя окраску, свидетельствующую о работоспособности теста. Таким образом количество видимых линий в аналитической зоне будет пропорционально определяемой концентрации анализируемого соединения.
Количество линий с иммобилизованными антителами можно варьировать от двух до 10, тем самым изменяя число диапазонов определяемых концентраций антигена. Количество наносимых линий с увеличивающейся вдоль мембраны концентрацией сорбированных антител может зависеть от требуемого (заданного) числа диапазонов определения анализируемого соединения. При нанесении двух тестовых линий устанавливается три области исследуемых концентраций (низкая, в случае отсутствия окрашивания двух линий, средняя - при наличии окрашивания второй линии и высокая - в случае одновременного окрашивания первой и второй линий). В общем случае при нанесении п тестовых линий количество определяемых диапазонов концентраций составляет (n+1).
Таким образом, основным отличительным существенным признаком изобретения является наличие в тестовой зоне множества линий с сорбированными антителами с градиентным увеличением количества сорбированных антител в направлении движения образца в виде дискретных (неперекрывающихся) линий. Градиентное распределение концентрации сорбированных моноклональных антител на поверхности мембраны (или числа линий с изменяющейся концентрацией антител) можно устанавливать в зависимости от природы анализируемого объекта и необходимого диапазона измеряемых концентраций, а также нижней границы определяемого содержания вещества. В частности, если необходимо получить ответ по принципу «да-нет» (например, в случае анализов на присутствие вирусов, антител, наркотиков, токсикантов, наличие беременности и т.д.) можно в каждом конкретном случае задать такой закон изменения концентрации антител на носителе, согласно которому при окрашивании числа полосок более некоторой критической длины ответ положительный, или наоборот.
Возможность варьирования концентрации сорбированных антител и числа наносимых линий в тестовой зоне позволяет установить взаимозависимость между диапазонами определяемых концентраций и числом окрашенных линий в тестовой зоне.
Совокупность перечисленных отличительных признаков ранее для решения задачи визуального иммунохроматографического анализа не использовалась, и поэтому отвечает критерию существенные отличия.
Пример 1
Получение наночастиц коллоидного золота.
В колбу с магнитной мешалкой добавляют 99 мл бидистиллированной воды и 1 мл 1%-ного раствора золотохлористоводородной кислоты. Раствор нагревают до кипения, после чего быстро при перемешивании добавляют 1,6 мл 1%-ного водного раствора цитрата натрия. Раствор кипятят еще 15 минут при перемешивании, затем охлаждают в темноте до комнатной температуры.
Получение конъюгата частиц золота с антителами
К 2 мл раствора коллоидного золота добавляют при перемешивании необходимое количество 0,1 М раствора Na2CO3 до достижения значения pH=7,0-7,5 (около 20 мкл). Затем по каплям при перемешивании добавляют 200 мкл раствора первых мышиных моноклональных антител против определяемого антигена с концентрацией 15 мг/мл, перемешивают и инкубируют при комнатной температуре в течение 40 минут. Далее добавляют 20%-ный раствор бычьего сывороточного альбумина (БСА) до конечной концентрации 0,2%, инкубируют 20 минут и добавляют сахарозу до конечной концентрации 10% и азида натрия до конечной концентрации 0,01%.
Для удаления несвязавшихся антител конъюгат центрифугируют 30 минут при 10000 об/мин и температуре +4°C. Супернатант удаляют, осадок перерастворяют в требуемом объеме 0,01М фосфатного буфера (ФБ), содержащего 0,1% БСА, 10% сахарозы. Полученный раствор конъюгата коллоидного золота с антителами с оптической плотностью 2 опт.ед. наносят на полоску стекловолоконной мембраны для конъюгата размером 5×260 мм со скоростью 50 мм/сек с помощью автоматического устройства AirJet Quanti 3000 («BioDot», США). Мембрану с нанесенным конъюгатом высушивают в течение 0,5 ч в суховоздушном термостате при температуре 50-60°C и относительной влажности 25-30%.
Получение иммунохроматографического композита для проведения анализа простато-специфического антигена
На аналитическую нитроцеллюлозную мембрану размером 25×260 мм на расстоянии 5 мм от края и на расстоянии 5 мм друг от друга с помощью автоматического устройства BioJet Quanti 3000 с использованием двух насосов наносят одновременно две тестовые линии со следующими концентрациями специфических вторых мышиных моноклональных антител в 0,01М фосфатно-солевом буферном растворе (ФСБР; фосфатный буфер, содержащий 0,14 М NaCl): 1 линия - 0,5 мг/мл; 2 линия - 0,1 мг/мл.
Затем на расстоянии 5 мм от первой линии наносят контрольную линию с раствором аффинно очищенных антивидовых антител овцы против мыши (1 мг/мл в ФСБР). При нанесении линий используют следующие параметры насоса BioJet Quanti 3000: размер капли - 30 нл, шаг - 0,3 мм, скорость - 50 мм/сек. Количество иммобилизуемых антител 1 мкл раствора на 1 см линии.
Мембрану высушивают в течение 2 ч в суховоздушном термостате при температуре 37°C и относительной влажности 25-30%.
С помощью ламинатора на пластиковую подложку с клеящим слоем прикрепляют полоски мембрану для образца, мембрану для конъюгата, нитроцеллюлозную мембрану и отсасывающую мембрану таким образом, чтобы край последующей мембраны перекрывался с краем предыдущей мембраны на 2 мм. После ламинирования мембран проводят ламинирование прозрачной пленкой с нанесенными стрелками, указывающими направление погружения полоски в буферный раствор.
Пластиковую подложку с ламинированными мембранами разрезают с помощью резака на полоски шириной 4 мм. Готовые тест-полоски помещают в пакеты из фольги с силикагелевым осушителем и хранят при температуре 4-20°C.
Проведение анализа общего ПСА в сыворотке крови
Вскрыть упаковку с тест-полосками перед анализом, извлечь необходимое для анализа количество тест-полосок из упаковки. Внести по 150 мкл ФБ в лунки планшета для иммуноферментного анализа. Аккуратно пипеткой нанести 30 мкл анализируемой сыворотки крови на нижний край тест-полоски (на расстоянии 0,5-1,0 см от края, см. фиг.3), осторожно погрузить конец тест-полоски в лунку планшета с буферным раствором (направление погружения в раствор указано стрелками) и включить секундомер. Через 15 мин извлечь тест-полоску из буферного раствора и визуально оценить результат (появление окрашенных в розовый цвет линий).
Если в тестовой зоне наблюдается ярко выраженное окрашивание только одной контрольной линии - концентрация ПСА составляет менее 3 нг/мл (фиг.3а).
Если помимо окрашивания контрольной линии наблюдается заметное окрашивание только одной тестовой линии - концентрация ПСА находится в диапазоне от 3 до 10 нг/мл (рис.3б).
Если помимо контрольной линии наблюдается окрашивание в тестовой зоне двух тестовых линий - концентрация ПСА равна или превышает 10 нг/мл (фиг.3в).
Отсутствие окрашивания контрольной линии (фиг.3г, д, е, ж) свидетельствует о нарушении работы набора и требует проведения повторного анализа с использованием другой тест-полоски. Возможные причины этого - неправильное выполнение процедуры анализа или нарушение условий хранения набора.
Пример 2
Получение наночастиц коллоидного золота и конъюгата частиц золота с антителами
Используют методику приготовления коллоидного золота и его конъюгата со специфическими первыми моноклональными антителами против белка, связывающего жирные кислоты (БСЖК), согласно описанию Примера 1.
Получение иммунохроматографического композита для проведения анализа БСЖК
На аналитическую нитроцеллюлозную мембрану в виде двух тестовых линий на расстоянии 5 мм друг от друга наносят растворы специфических антител в 0,01 М фосфатно-солевом буферном растворе (ФСБР) с помощью программируемого автоматического диспенсера BioJet Quanti 3000 для формирования аналитической зоны: 1 линия - 0,5 мг/мл; 2 линия - 0,2 мг/мл. Для формирования контрольной зоны иммунохроматографической системы на расстоянии 5 мм от аналитической зоны наносяти раствор аффинно очищенных антивидовых антител овцы против мыши с концентрацией 1 мг/мл. Используют следующие параметры насоса BioJet Quanti 3000 для нанесения образцов: размер капли - 30 нл, шаг - 0,3 мм, скорость - 50 мм/сек. Высушивание полосок проводили в течение 24 ч при +37°С. Ламинирование осуществляют согласно описанию Примера 1.
Проведение иммунохроматографического анализа БСЖК
Предварительно на мембрану для нанесения образца каждой тест-полоски наносят по 30 мкл анализируемых образцов сывороток крови. Далее готовые полоски с нанесенным исследуемым образцом вертикально помещают в лунки микропланшета для иммуноферментного анализа со 150 мкл 0,01 М ФСБР, содержащего 0,1% твин-20. Через 15 минут тест-полоски помещают на горизонтальную поверхность и визуально оценивают результат (появление окрашенных в розовый цвет линий).
Интерпретация результатов
При концентрации БСЖК в исследуемом образце менее 2 нг/мл наблюдается появление только одной окрашенной контрольной линии. Появление только одной тестовой линии в аналитической зоне соответствует концентрации БСЖК от 2 нг/мл до 15 нг/мл. Дополнительное появление второй тестовой линии в аналитической зоне наблюдается при концентрации БСЖК в образце >15 нг/мл, что является положительным результатом и свидетельствует о превышении диагностического уровня некроза миокарда.
Пример 3
Получение наночастиц коллоидного золота и конъюгата частиц золота с антителами
Используют методику приготовления коллоидного золота и его конъюгата со специфическими первыми моноклональными антителами против IgE человека, согласно описанию Примера 1.
Получение иммунохроматографического композита
На аналитическую нитроцеллюлозную мембрану размером 25×260 мм на расстоянии 5 мм от края и на расстоянии 2 мм друг от друга с помощью автоматического устройства BioJet Quanti 3000 наносят пять тестовых линий со следующими концентрациями специфических вторых мышиных моноклональных антител в 0,01М ФСБР: 1 линия - 1 мг/мл; 2 линия - 0,5 мг/мл; 3 линия - 0,25 мг/мл; 4 линия - 0,1 мг/мл; 5 линия - 0,05 мг/мл.
Затем на расстоянии 5 мм от первой линии наносят контрольную линию с раствором аффинно очищенных антивидовых антител овцы против мыши (1 мг/мл в ФСБР). При нанесении линий используют следующие параметры насоса BioJet Quanti 3000: размер капли - 30 нл, шаг - 0,3 мм, скорость - 50 мм/сек. Количество иммобилизуемых антител 1 мкл раствора на 1 см линии.
Мембрану высушивают в течение 2 ч в суховоздушном термостате при температуре 37°C и относительной влажности 25-30%.
На аналитическую нитроцеллюлозную мембрану наносят раствор специфических вторых моноклональных антител против IgE человека в 0,01 М ФСБР с помощью программируемого автоматического диспенсера BioJet Quanti 3000 для формирования аналитической зоны. Используют следующие параметры насоса для нанесения образцов; размер капли - 30 нл, шаг - 0,3 мм, скорость - 50 мм/сек. Концентрации специфических антител против IgE человека в растворах составляли, соответственно: 0,05 мг/мл, 0,1 мг/мл, 0,25 мг/мл, 0,5 мг/мл, 1 мг/мл. Для формирования контрольной зоны иммунохроматографической системы на расстоянии 4 мм от аналитической зоны наносят раствор аффинно-очищенных антивидовых антител овцы против мыши с концентрацией 1 мг/мл. Высушивание полосок проводят в течение 1 ч при +37°C.
Ламинирование осуществляют согласно описанию Примера 1.
Проведение иммунохроматографического анализа общего IgE человека
Предварительно на мембрану для нанесения образца каждой тест-полоски наносят по 30 мкл стандартных растворов IgE, а затем анализируемых образцов сывороток крови. Далее готовые полоски с нанесенным исследуемым образцом вертикально помещают в лунки полистиролового планшета для иммуноферментного анализа со 150 мкл ФСБР. Через 15 минут тест-полоски кладут на горизонтальную поверхность и высушивают. Проводят визуальное определение результатов анализа путем подсчета числа видимых линий в тестовой зоне аналитической мембраны и сравнение полученных результатов со стандартными значениями концентраций IgE (см. Табл.1).
|