Результат интеллектуальной деятельности: СПОСОБЫ ПОЛУЧЕНИЯ ТРАНСДЕРМАЛЬНЫХ ТЕРАПЕВТИЧЕСКИХ СИСТЕМ НА ОСНОВЕ СОПОЛИМЕРОВ МОЛОЧНОЙ И ГЛИКОЛЕВОЙ КИСЛОТ (ВАРИАНТЫ)
Вид РИД
Изобретение
Изобретение относится к области фармацевтической промышленности, в частности к способам получения трансдермальных терапевтических систем на основе сополимеров молочной и гликолевой кислот.
Трансдермальная терапевтическая система (ТТС) представляет собой дозированную лекарственную форму для наружного применения в виде пластырей, нетканого материала или пленок. ТТС способны непрерывно и атравматично подавать в организм лекарственное средство (ЛС) со скоростью, создающей в кровотоке постоянный уровень концентрации ЛС, близкий к оптимальному терапевтическому уровню.
Трансдермальные терапевтические системы являются альтернативой парентеральному и пероральному введению лекарственных средств. По сравнению с пероральным приемом, трансдермальное введение обеспечивает быстрое действие препарата и помогает избежать снижения его активности в результате прохождения через печень. Кроме того, при таком введении появляется возможность снизить частоту назначения лекарства, уменьшить необходимые дозы и при этом избежать колебаний его концентрации в крови, а при развитии нежелательных реакций - немедленно прекратить лечение. Для некоторых лекарств трансдермальная доставка является единственным способом введения.
Задача, положенная в основу создания настоящего изобретения, состоит в дальнейшем совершенствовании трансдермальных терапевтических систем, при этом технический результат, полученный при решении такой задачи, состоит в создании биодеградируемых трансдермальных терапевтических систем на основе сополимеров лактида и гликолида.
Для достижения поставленного результата предлагаются варианты способов получения трансдермальной терапевтической системы (ТТС) на основе сополимеров молочной и гликолевой кислот, первый из которых включает растворение сополимера лактид-гликолида и фармакологически активного вещества в органическом растворителе, перемешивание полученного раствора до полного растворения, высушивание горячим воздухом до полного высыхания и постоянной массы с получением пленки, разрезание полученной пленки на части и упаковку; второй включает растворение сополимера лактид-гликолида и фармакологически активного вещества в органическом растворителе, перемешивание полученного раствора в магнитной мешалке до полного растворения, заливку в устройство подачи, подачу на капилляр напряжением 5-40 кВ, сбор волокна на приемное устройство с получением нетканого материала, разрезание полученного нетканого материала на части и упаковку; третий из вариантов способа включает этап экструдирования сополимера лактид-гликолида с получением нити и последующим изготовлением из нити тканого материала, этап растворения сополимера лактид-гликолида в органическом растворителе, растворение фармакологически активного вещества, смешивание и гомогенизацию таких растворов с получением итогового раствора, и этап погружения в итоговый раствор тканного материала с последующим его охлаждением и сушкой; четвертый из заявленных вариантов способа включает растворение сополимера лактид-гликолида в этилацетате, добавление фармакологически активного вещества в буфере, перемешивание, центрифугирование полученной смеси, удаление супернатанта с растворением осадка в этилацетате, получением суспензии и приготовлением на ее основе спрея.
Предпочтительные, но не обязательные варианты реализации первого, второго и третьего вариантов способа предполагают соотношение лактида и гликолида выбрать в пределах от 95:5 до 5:95, предпочтительно 75:25, наиболее предпочтительно 50:50; использование в качестве сополимера лактид-гликолид-полиэтиленгликоль (ПЭГ) или - лактид-гликолид-поливинилпирролидон (ПВП), где ПЭГ или ПВП имеет молекулярную массу от 400 до 40000 Да; дополнительное использование в качестве пластификаторов веществ из группы ε-капролактон, сложные эфиры дикарбоновые кислоты, глицерин, в качестве эмульгаторов - веществ из группы полоксамер, твин-80 (полиоксиэтилен-сорбитан моноолеат); использование для создания заданных параметров высвобождения фармакологически активного вещества аэросила и/или диметилсульфоксида, а в качестве органического растворителя -веществ, выбранных из группы, включающей дихлорметан, хлороформ, хлористый метилен, этилацетат, тетрагидрофуран, диметилсульфоксид, диметилформамид, ацетон или их смеси; кроме того, фармакологически активным веществом может являться терапевтическое или диагностическое средство, при этом в случае, если фармакологически активное вещество является терапевтическим средством, его выбирают из группы, включающей ранозаживляющие средства; противомикробные средства; обезболивающие и анестезирующие средства местного действия; противовоспалительные средства; трофические факторы; лекарства для лечения привыкания и злоупотребления лекарственными средствами; лекарства для лечения привыкания и злоупотребления табаком; лекарства для лечения привыкания и злоупотребления алкоголем; гормональные средства; стимуляторы; лекарства против ожирения; кардиотропные средства, в случае, если фармакологически активное вещество является диагностическим средством, то это средство для диагностики в радиационной медицине и/или лучевой терапии; следует также отметить, что для предотвращения изменения рН в кислую сторону первый-третий варианты заявленного способа могут дополнительно характеризоваться использованием волластонита или биогласса (bioglass 45S5).
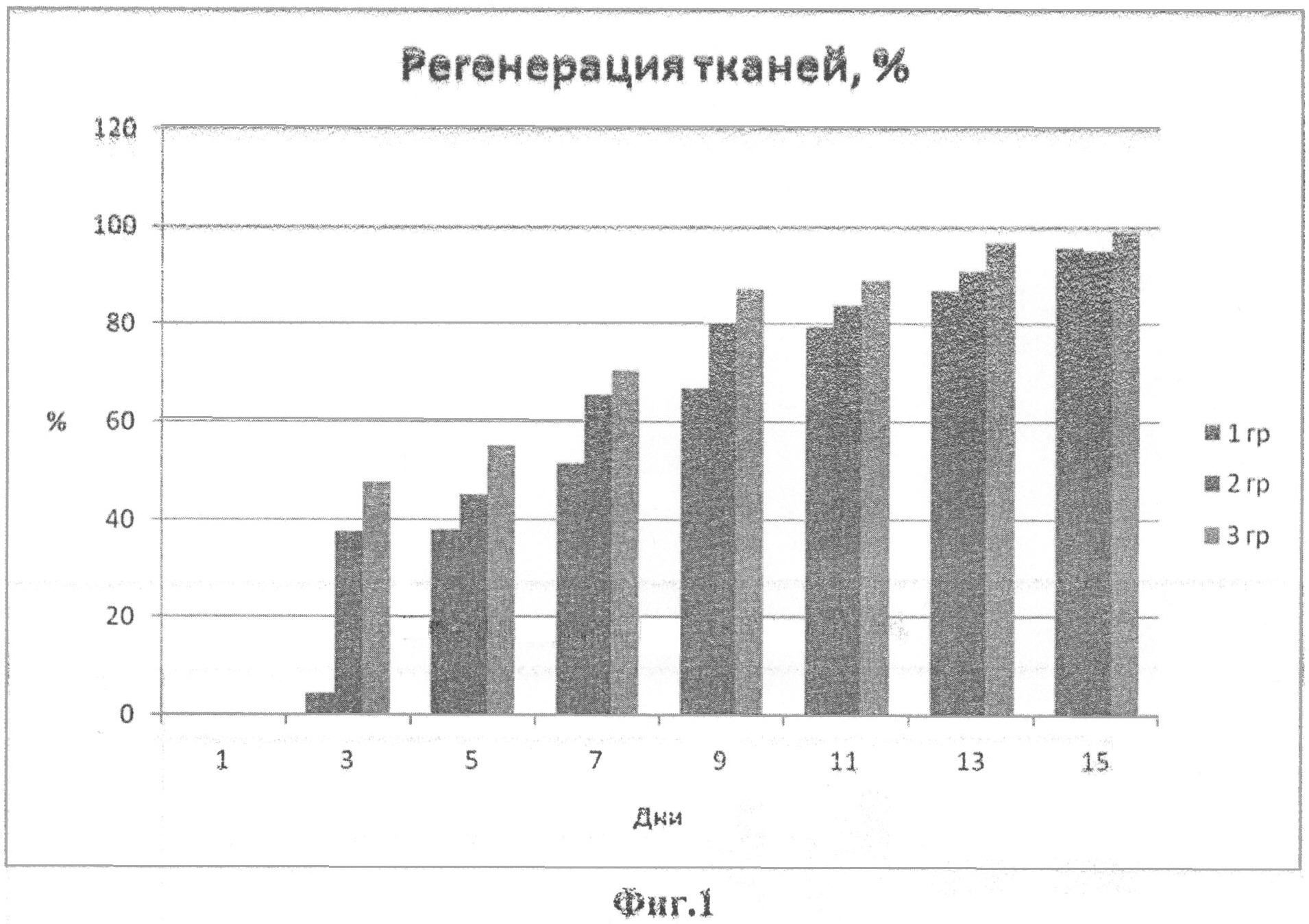
Изобретение иллюстрируется фиг.1 с графиком регенерации тканей.
Возможность достижения поставленного результата обусловлена тем, что сополимеры лактида и гликолида являются поддающимися биологическому разложению полимерами, цепи которых состоят из звеньев молочной и гликолевой кислот, процентное содержание которых оказывает влияние на скорость разложения и, как следствие, высвобождения фармакологически активного вещества. Молекула полилактида является оптически активной, D и L-изомеры могут присутствовать в любых пропорциях, исключением является сополимер L-лактида и D-лактида с относительным содержанием звеньев 50/50. Молекулярная масса сополимеров может варьироваться от 30000 до 100000 Да (массы определены методом гель-проникающей хроматографией). Также возможен синтез олигомеров с молекулярной массой от 2500 до 10000 Да. Для повышения биодеградируемости могут использоваться сополимеры, содержащие помимо сополимеров полилактидов и/или полигликолидов полиэтиленгликоли (ПЭГ) различной молекулярной массы, начиная от 400 Да до 40000 Да.
В общем виде, согласно заявленным вариантам способа, могут быть получены трансдермальные терапевтически системы (ТТС), на основе сополимера лактид-гликолида и, при необходимости, дополнительно полиэтиленгликоля, и/или поливинилпиролидона различной молекулярной массы, и/или пластификатора, и/или поверхностно-активных веществ, и/или аэросила, и/или диметилсульфоксида (ДМСО), в который добавлено фармакологически активное вещество, при этом в общем виде такие способы подразделяются на:
- метод испарения органического растворителя;
- метод электроспиннинга;
- метод получения композитных материалов;
- получение спрея.
Пример 1. Получение биодеградируемой ТТС методом испарения органического растворителя.
1.1. Растворяли 195 мг сополимера лактид-гликолида (50:50; М=10000 Да) и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф, сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.2. Растворяли 486 мг сополимера лактид-гликолид-ε-капролактона (71:22:7; М=5000 Да) и 15 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф и сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.3. Растворяли 972 мг сополимера лактид-гликолид-ПЭГ (50:45:5; М=50000 Да; МПЭГ=1000 Да) и 20 мг фармакологически активного вещества в 60 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф, сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.4. Растворяли 972 мг сополимера лактид-гликолид-ПЭГ-ε-капролактона (70:20:5:5; М=60000 Да; МПЭГ1000 Да) и 20 мг фармакологически активного вещества в 100 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф и сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.5. Растворяли 195 мг сополимера лактид-гликолида (50:50; М=70000 Да), 10 мг глицерина и 10 мг фармакологически активного вещества в 30 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф и сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.6. Растворяли 195 мг сополимера лактид-гликолида (50:50; М=80000 Да), 20 мл полоксамера 188 и 15 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалки до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф и сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.7. Растворяли 195 мг сополимера лактид-гликолида (50:50; М=90000 Да), 10 мг аэросила и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф и сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
1.8. Растворяли 195 мг сополимера лактид-гликолида (50:50; М=100000 Да), 10 мл диметилсульфоксид (ДМСО) и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, затем раствор сушили горячим воздухом до полного высыхания, после чего помещали в вакуумный шкаф и сушили от остатков ацетона до постоянной массы. Полученную пленку разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
Пример 2. Получение биодеградируемой ТТС методом электроспиннинга.
2.1. Растворяли 1 г сополимера лактид-гликолида (50:50; М=35000 Да) и 10 мг фармакологически активного вещества в 10 мл этилацетата; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.2. Растворяли 1 г сополимера лактид-гликолид-ε-капролактона (75:20:5; М=40000 Да) и 15 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.3. Растворяли 1 г сополимера лактид-гликолид-ПЭГ (50:45:5; М=50000 Да; МПЭГ=1000 Да) и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.4. Растворяли 1,0 г сополимера лактид-гликолид-ПЭГ-ε-капролактона (70:20:5:5; М=60000 Да; МПЭГ=1000 Да) и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.5. Растворяли 1 г сополимера лактид-гликолида (50:50; М=70000 Да), 0,2 мг глицерина и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.6. Растворяли 1 г сополимера лактид-гликолида (50:50; М=80000 Да), 0,2 мл полоксамера 188 и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.7. Растворяли 1 г сополимера лактид-гликолида (50:50; М=90000 Да), 0,2 мг аэросила и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
2.8. Растворяли 1 г сополимера лактид-гликолида (50:50; М=100000 Да), 0,2 мл ДМСО и 10 мг фармакологически активного вещества в 10 мл ацетона; полученный раствор тщательно перемешивали на магнитной мешалке до полного растворения, заливали в устройство подачи, подавали на капилляр напряжением 20 кВ и собирали волокна на приемное устройство. Полученный нетканый материал разрезали на части и помещали в стерильный полиэтиленовый мешок, который потом запаивали.
Пример 3. Получение биодеградируемой ТТС методом композитных материалов.
3.1. 5 г сополимера лактид-гликолида (50:50; М=50000 Да) засыпали в экструдер, нагретый до 100°C; затем на выходе из фильеры нить собирали на барабан и на ткацком станке готовили тканый материал.
Растворяли 196 мг сополимера лактид-гликолида (50:50; М=40000 Да) в 30 мл хлороформа; 10 мг фармакологически активного вещества растворяли в 4 мл воды очищенной; смешивали полученные растворы и гомогенизировали при 16000 об/мин. В полученный раствор опускали тканный материал, полученный на ткацком станке и сразу же охлаждали жидким азотом при -196°C. Полученный композитный материал с фармакологически активным веществом помещали в лиофильную сушку и сушили при -85°C.
3.2. 5 г сополимера лактид-гликолида (75:25; М=50000 Да) засыпали в экструдер, нагретый до 100°C; затем на выходе из фильеры нить собирали на барабан и на ткацком станке готовили тканый материал.
Растворяли 196 мг сополимера лактид-гликолида (50:50; М=60000 Да) в 30 мл хлороформа; 10 мг фармакологически активного вещества растворяли в 4 мл воды очищенной; смешивали полученные растворы и гомогенизировали при 16000 об/мин. В полученный раствор опускали тканный материал и сразу же охлаждали жидким азотом при -196°C. Полученный композитный материал с фармакологически активным веществом помещали в лиофильную сушку и сушили при -85°C.
3.3. 5 г сополимера лактид-гликолид-ε-капролактона (75:20:5; М=70000 Да) засыпали в экструдер, нагретый до 100°C; затем на выходе из фильеры нить собирали на барабан и на ткацком станке готовили тканый материал.
Растворяли 196 мг сополимера лактид-гликолида (50:50; М=80000 Да) в 30 мл хлороформа; 10 мг фамкакологически активного вещества растворяли в 4 мл воды очищенной; смешивали полученные растворы и гомогенизировали при 16000 об/мин. В полученный раствор опускали тканный материал и сразу же охлаждали жидким азотом при -196°C. Полученный композитный материал с фармакологически активным веществом помещали в лиофильную сушку и сушили при -85°C.
3.4. 5 г сополимера лактид-гликолид-ПЭГ (70:25:5; М=90000 Да; МПЭГ=1000 Да) засыпали в экструдер, нагретый до 100°C; затем на выходе из фильеры нить собирали на барабан и на ткацком станке готовили тканый материал.
Растворяли 196 мг сополимера лактид-гликолида (50:50; M=30000 Да) в 30 мл хлороформа; 10 мг фармакологически активного вещества растворяли в 4 мл воды очищенной; смешивали полученные растворы и гомогенизировали при 16000 об/мин. В полученный раствор опускали тканный материал и сразу же охлаждали жидким азотом при -196°C. Полученный композитный материал с фармакологически активным веществом помещали в лиофильную сушку и сушили при -85°C.
3.5. 5 г сополимера лактид-гликолид-ПЭГ-ε-капролактона (70:20:5:5; М=50000 Да; МПЭГ=1000 Да) засыпали в экструдер, нагретый до 100°C; затем на выходе из фильеры нить собирали на барабан и на ткацком станке готовили тканый материал.
Растворяли 196 мг сополимера лактид-гликолида (50:50; М=30000 Да) в 30 мл хлороформа; 10 мг фармакологически активного вещества растворяли в 4 мл воды очищенной; смешивали полученные растворы и гомогенизировали при 16000 об/мин. В полученный раствор опускали тканный материал и сразу же охлаждали жидким азотом при -196°C. Полученный композитный материал с фармакологически активным веществом помещали в лиофильную сушку и сушили при -85°C.
3.6. 5 г сополимера лактид-гликолида (50:50; М=30000 Да), 0,1 г аэросила засыпали в экструдер, нагретый до 100°C; затем на выходе из фильеры нить собирали на барабан и на ткацком станке готовили тканый материал.
Растворяли 196 мг сополимера лактид-гликолида (50:50; М=60000 Да), в 30 мл хлороформа; 10 мг фармакологически активного вещества растворяли в 4 мл воды очищенной; смешивали полученные растворы и гомогенизировали при 16000 об/мин. В полученный раствор опускали тканный материал и сразу же охлаждали жидким азотом при -196°C. Полученный композитный материал с фармакологически активным веществом помещали в лиофильную сушку и сушили при -85°C.
4. Получение спрея с фармакологически активным веществом на основе сополимеров молочной и гликолевой кислот
5 г сополимера лактид-гликолида растворяют в 20 мл этилацетата, добавляют 20 мг фармакологическиактивного вещества в буфере, интенсивно перемешивают, полученную смесь центрифугируют, удаляют супернатант, осадок растворяют в 40 мл этилацетата, получая суспензию, на основе которой готовят спрей пригодный для распыления на кожу.
Для исследования эффективности полученных трансдермальных терапевтических систем в виде пленок, нетканого материала, пластырей, содержащих сополимер лактид-гликолида и ацексамовую кислоту в качестве ранозаживляющего фармакологически активного вещества, моделировали раневую поверхность удалением у животных шерсти на месте нанесения раны, затем скальпелем вырезался кусок кожи для получения полнослойной раны размером 225 мм2.
Для эксперимента использовали взрослых самцов крыс Вистар весом 200-250 г в течении 1 недели выдерживали с целью акклиматизации в клетках группами по 5 особей. Животных делили на 3 группы по 6 животных в каждой группе:
1 группа контрольная; животные со стандартными полнослойными ранами (225 мм2) на боковой поверхности тела, которым на область дефекта не воздействуют никакими физическими и химическими факторами.
2 группа, животные со стандартными полнослойными ранами (225 мм2) на боковой поверхности тела, которым на область дефекта наносят спрей «Пантенол».
3 группа, животные со стандартными полнослойными ранами (225 мм2) на боковой поверхности тела, которым на область дефекта наносят полимерную пленку, содержащую сополимер лактид-гликолида (50:50 М=30000 Да) и ацексамовую кислоту в соответствии с заявленными вариантами способа (фиг.1).
Исследование вели в течение 15 дней. Ежедневно измеряли площадь ран у всех экспериментальных животных. У всех животных были взяты мазки-отпечатки с поверхности ран через 6, 12 и 24 часа. У всех животных была взята биопсия через 5, 10 15 сутки с последующим изготовлением гистологических препаратов по стандартным прописям.
Нижеследующие примеры иллюстрируют также возможность реализации заявленных ТТС с различными фармакологически активными веществами.
Пример 4. Анальгетическая активность веществ, высвобождаемых из ТТС.
Тест «отдергивания хвоста». Животное помещали в индивидуальную пластиковую камеру, хвост погружали на 5 см в воду с температурой 55±1°C. В тесте фиксировали латентный период избавления от болевого раздражителя -период времени (сек), в течение которого животное выдергивало хвост из воды полностью. Максимальное время предъявления болевого раздражителя - 30 сек. Исходную болевую чувствительность определяли как среднее арифметическое из показателей, зафиксированных на 60, 40, и 20 минут до применения ТТС. Латентный период избавления от болевого раздражителя фиксировали через 20, 40, 60 и 120 минут после применения. Анальгетическую активность оценивали по изменению латентного периода реакции по формуле: А=ЛПоп-ЛПисх, где ЛПоп - латентный период избавления после применения ТТС, ЛПисх- среднее арифметическое латентных периодов избавления до применения ТТС.
Проводили аппликацию ТТС самцам нелинейных белых крыс весом 200-300 г. Контрольным животным аппликацию не проводили. Полученные результаты приведены в таблице 1.
|
Из представленных результатов следует, что применение ТТС вызывает достоверное увеличение латентного периода реакции отдергивания хвоста в ответ на болевое раздражение.
Пример 5. Испытания эффективности ТТС в тесте воспаления, вызванного конканавалином А.
Реакция воспаления на конканавалин А (Кон А) основана на способности пектинов растительного происхождения высвобождать медиаторы воспаления. Делали аппликацию ТТС или вводили известный противовоспалительный агент в/б за 20 минут до Кон А. Кон А вводили субплантарно в дозе 100 мкг/20 г массы тела (20 мкл раствора в концентрации 5 мг/мл), в контрлатеральную конечность - тот же объем физиологического раствора. Через 1 час мышей забивали, определяли массу лап и подсчитывали индекс реакции воспаления (Ир) по формуле: Ир=(Роп-Рк)*100/Рк, где Роп - масса стопы задней лапы, в подушечку которой вводили Кон А, Рк - физиологический раствор. Статистически достоверную разницу между данными опытных и контрольных групп, превышающая 20%, считали значимой (Любимов Б.И. и др. 2000).
Контрольным животным вводили внутрибрюшинно дистиллированную воду. Полученные результаты приведены в таблице 2.
|
Полученные результаты показывают, что применение противовоспалительного агента в ТТС по сравнению с его в/б вызывает достоверное снижение индекса воспалительной реакции в ответ на введение конканавалина А.
Пример 6. Изучение противомикробной активности В качестве активного компонента для ТТС был взят Хлорамфеникол 3% Изучение противомикробной активности проводили в соответствии с требованиями ГФ XI, in vitro методом диффузии в агар. Стерильные чашки Петри устанавливали на строго горизонтальную поверхность, наливали в них 2% мясопептонный агар (рН=7,2-7,4) в количестве 20 мл для создания оптимальной толщины слоя, равной 4-5 мм. Для тех видов микробов, которые не растут на мясопептонном агаре, как, например, стрептококки, пневмококки и другие, применяли 5% кровяной или сывороточный агар. Перед посевом чашки со средой подсушивали в термостате.
Толстый слой агара засеивали 1-2 мл взвеси испытуемых микроорганизмов и растирали шпателем до равномерного распределения микроорганизмов по всей поверхности чашки Петри и на одинаковом расстоянии. Излишек взвеси полностью удаляли, подсушивали в течение 30 мин. Затем сверлом (d=6 мм) проделывали отверстия на расстоянии 2,5 см от стенки чашки Петри и на одинаковых расстояниях друг от друга, которые затем заполняли исследуемыми объектами. После этого чашки ставили в термостат при 37°C не переворачивая, строго горизонтально, чтобы образовались круглые зоны.
Лекарственное вещество диффундирует из полимерного носителя в агар, формируя вокруг диска зону угнетения роста чувствительных к нему микроорганизмов, четко выделяющуюся на фоне сплошного роста. Через 24 часа измеряли диаметры зоны угнетения роста. Полученные результаты приведены в таблице 3.
|
|
Критерий Крускала-Уоллиса Р>0,05
Более 10 - высокая активность, 10 - умеренная активность, менее 10 - отсутствие активности.
Результаты эксперимента свидетельствуют о противомикробной активности активного компонента, входящего в состав ТТС. Противомикробная активность в форме ТТС не уступает по величине противомикробной активности хлорамфеникола.