КОМБИНАЦИЯ, ВКЛЮЧАЮЩАЯ ФУЛЬВОВУЮ КИСЛОТУ И АНТИБИОТИКИ
Вид РИД
Изобретение
Предпосылки создания изобретения
Настоящее изобретение относится к комбинации, включающей фульвовую кислоту и один или несколько антибиотиков из классов пенициллинов и аминогликозидов, которая предназначена для применения при лечении различных состояний.
Гумусные субстанции образуются в результате разложения остатков растительного и животного происхождения в окружающей среде (MacCarthy и др., 1985). Указанные субстанции можно подразделять на гуминовую кислоту, фульвовую кислоту и гумин на основе их растворимости в воде в зависимости от значения pH. Фульвовая кислота представляет собой фракцию, которая растворима в воде во всем диапазоне значений pH, и в целом она характеризуется меньшими молекулярными размерами и массой и менее интенсивной окраской, чем гуминовые кислоты.
Фульвовая кислота в естественных условиях присутствует в почве и воде в низких концентрациях и ее трудно выделять. Большинство выполненных до настоящего времени исследований, касающихся медицинского применения фульвовой кислоты, были проведены с использованием продукта, который представлял собой фульвовую кислоту, полученную из битуминозного (жирного) угля с помощью контролируемого процесса влажного окисления (Bergh и др., 1997). Наиболее пригодный процесс получения фульвовых кислот из угля методом влажного окисления описан в US 4912256. Фульвовые кислоты, получаемые с помощью такого процесса, часто называют оксифульвовыми кислотами.
В публикации международной заявке на патент WO 00/19999 описано применение фульвовой кислоты при лечении воспаления, угрей, экземы и бактериальных, грибных и вирусных инфекций.
В US 4999202 и US 5204368 описаны композиции, содержащие фульвовую кислоту, ее соль или производное, которые обладают бактериостатическими или бактерицидными свойствами и которые можно применять в качестве дезинфицирующих средств.
Фульвовые кислоты, полученные путем окисления угля, содержат в высоких концентрациях тяжелые металлы, в том числе алюминий, ртуть, кадмий, хром и свинец, которые вредны для человека и которые не должны присутствовать в фармацевтических препаратах. В публикации международной заявки на патент WO 2007/125492 описана композиция, содержащая фульвовую кислоту, полученную из углеводородного сырья методом влажного окисления, которая имеет низкое содержание указанных вредных элементов, и метод получения такой композиции. Указано, что такую композицию можно применять в качестве фармацевтического средства.
Краткое изложение сущности изобретения
Одним из объектов изобретения является комбинация, содержащая фульвовую кислоту, ее соль, эфир или производное и один или несколько антибиотиков из классов пенициллинов и аминогликозидов.
Предпочтительно антибиотик выбирают из группы, включающей оксациллин и гентамицин и их комбинацию.
Фульвовая кислота, ее соль, эфир или производное может иметь любое значение pH от кислотного до основного, как правило, значение pH находится в диапазоне от кислотного до нейтрального. Фульвовая кислота может находиться в форме раствора, забуференного до пригодного значения pH. Предпочтительно фульвовая кислота находится либо в форме кислоты, либо в форме соли, например, калиевой соли.
Предпочтительная фульвовая кислота представляет собой полученную из углевода фульвовую кислоту, такую, как кислота, описанная в WO 2007/125492. Фульвовая кислота, описанная в этой публикации, имеет молекулярную массу, не превышающую 20000 Да, и низкое содержание таких элементов, как алюминий, ртуть, кадмий, хром и свинец. Предпочтительно содержание этих элементов не превышает 20 част./млн. Фульвовую кислоту получают из углевода, такого как сахарид. Предпочтительным сахаридом является сахароза, глюкоза или фруктоза.
Комбинацию можно приготавливать в виде фармацевтической лекарственной формы, более конкретно, в форме жидкости, таблетки, капсулы, крема, геля или т.п.
Другой объект изобретения относится к комбинации, предлагаемой в изобретении, которая предназначена для применения в способе лечения или ингибирования заболевания или состояния у индивидуума, заключающемся в том, что индивидууму вводят комбинацию.
Следующий объект изобретения относится к применению комбинации, предлагаемой в изобретении, для изготовления фармацевтической композиции, предназначенной для применения в способе лечения или ингибирования заболевания или состояния у индивидуума, заключающемся в том, что индивидууму вводят комбинацию.
Еще один объект изобретения относится к комбинации, предлагаемой в изобретении, которая предназначена для применения в способе уничтожения бактерий, ингибирования или предупреждения их роста.
Еще один объект изобретения относится к способу уничтожения бактерий, ингибирования или предупреждения их роста, заключающемуся в том, что применяют комбинацию, предлагаемую в изобретении.
Еще один объект изобретения относится к способу лечения, ингибирования или предупреждения заболевания или состояния у индивидуума, заключающемуся в том, что индивидууму вводят в эффективном количестве комбинацию, предлагаемую в изобретении.
Заболевание или состояние может представлять собой бактериальную инфекцию, предпочтительно инфекцию, вызываемую бактериями, устойчивыми к антибиотикам, более конкретно, бактериями, которые представляют собой устойчивые ко многим лекарственным средствам бактерии, такие как MRSA (устойчивый ко многим лекарственным средствам золотистый стафилококк Staphylococcus aureus).
Бактерии могут обладать устойчивостью к одному или нескольким антибиотикам из классов пенициллинов и аминогликозидов. Предпочтительно антибиотики выбирают из группы, включающей оксациллин и гентамицин и их комбинацию.
Введение можно осуществлять путем орального, местного применения или любым другим пригодным путем введения.
Индивидуум может представлять собой животное или человека.
Применение или введение комбинации, предлагаемой в изобретении, может быть более эффективным, чем применение или введение индивидуально фульвовой кислоты, ее соли, эфира или производного или антибиотика.
При разработке одного из вариантов осуществления изобретения было установлено, что у бактерий может не развиваться устойчивость к комбинации, включающей фульвовую кислоту, ее соль, эфир или производное и оксациллин, при воздействии на бактерию указанной комбинации в течение периода времени, составляющего вплоть до примерно 5 дней, более предпочтительно при воздействии на бактерию указанной комбинации в течение периода времени, составляющего вплоть до примерно 10 дней, еще более предпочтительно при воздействии на бактерию указанной комбинации в течение периода времени, составляющего вплоть до примерно 20 дней.
Было установлено, что применение фульвовой кислоты, ее соли, эфира или производного повышает антибиотические свойства двух классов антибиотиков, прежде всего оксациллина и гентамицина или любой их комбинации.
Краткое описание чертежей
На чертежах показано:
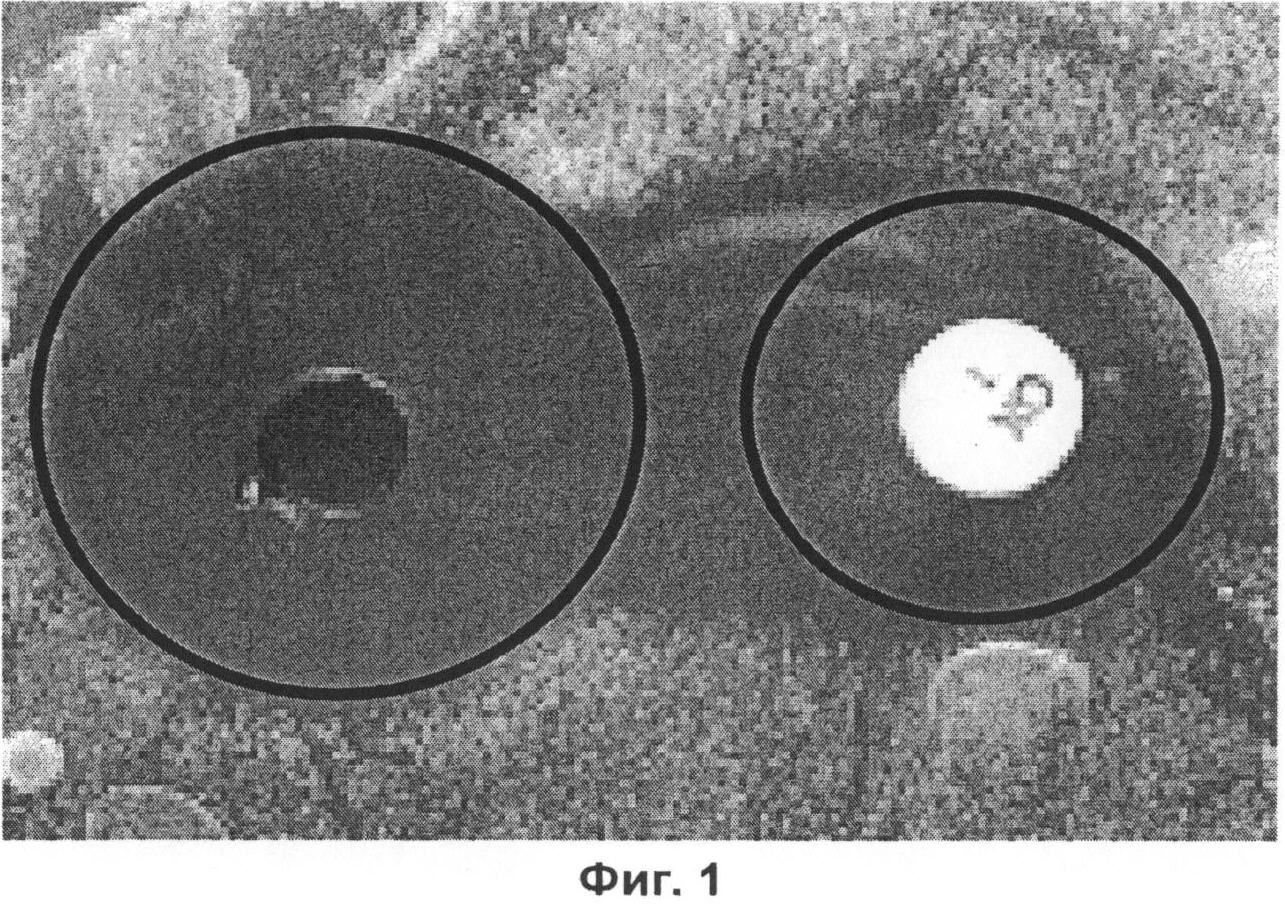
на фиг.1 - синергетическое действие фульвовой кислоты и оксациллина, проиллюстрированное на примере газона штамма S. aureus ATCC 12600;
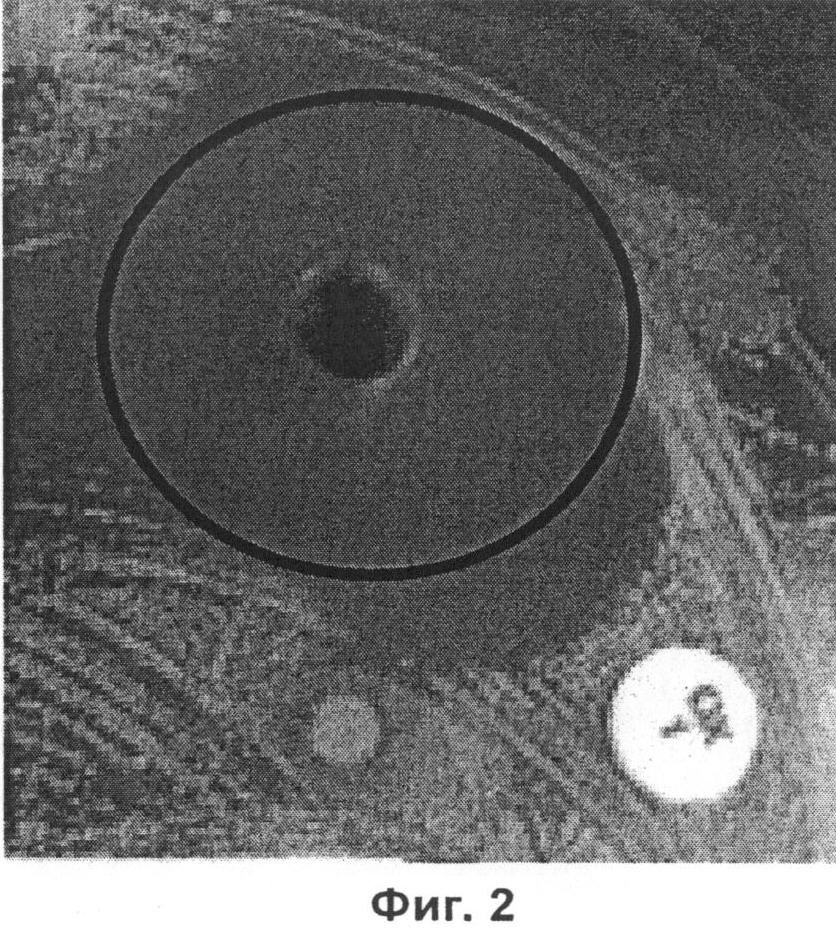
на фиг.2 - синергетическое действие фульвовой кислоты и оксациллина, проиллюстрированное на примере газона устойчивого к метициллину штамма Staphylococcus aureus Р39380;
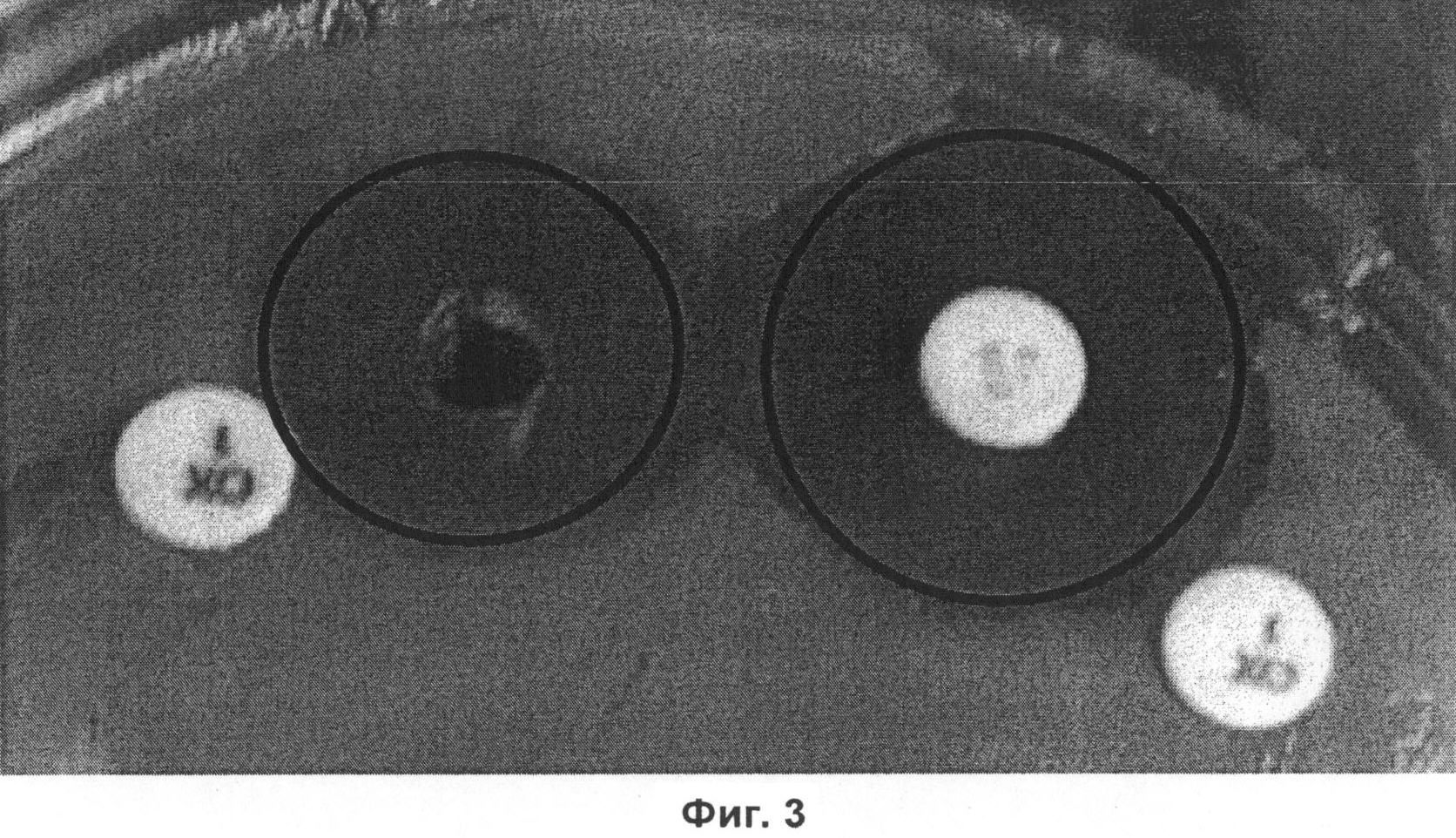
на фиг.3 - синергетическое действие фульвовой кислоты и гентамицина, проиллюстрированное на примере газона штамма P. aeruginosa ATCC 9027;
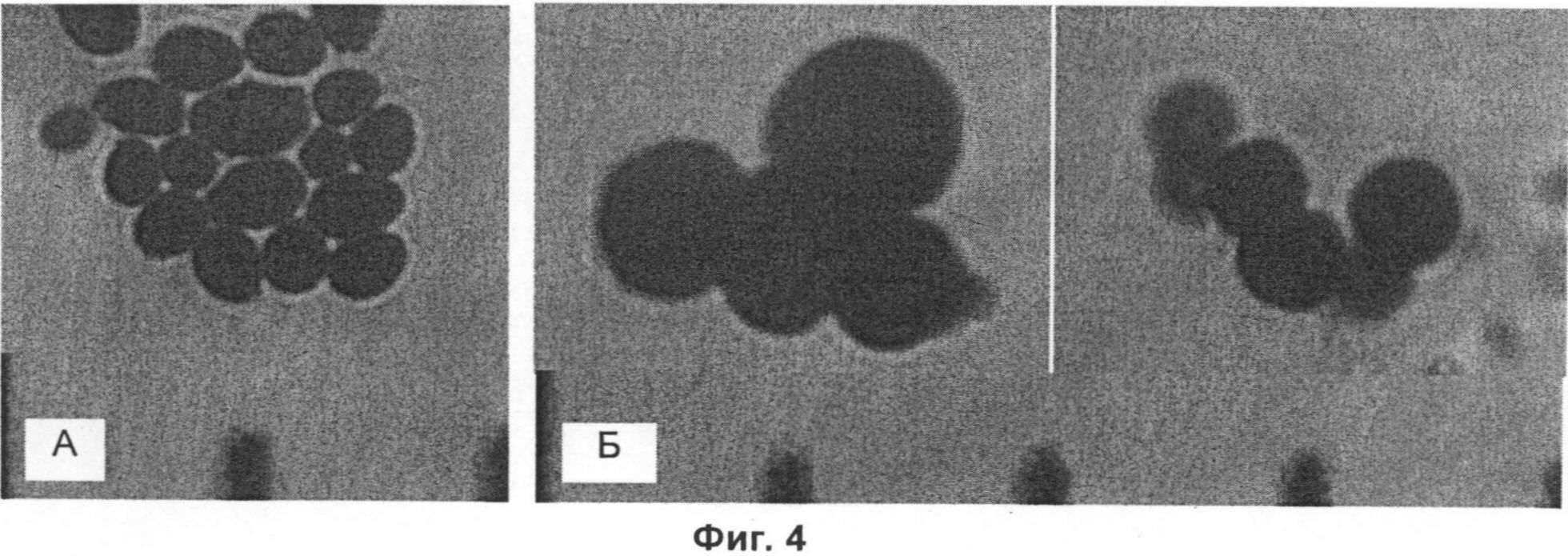
на фиг.4 - результаты окрашивания по Граму С. albicans, не обработанного фульвовой кислотой (а), и собранного из зоны ингибирования обусловленного действием фульвовой кислоты (б);
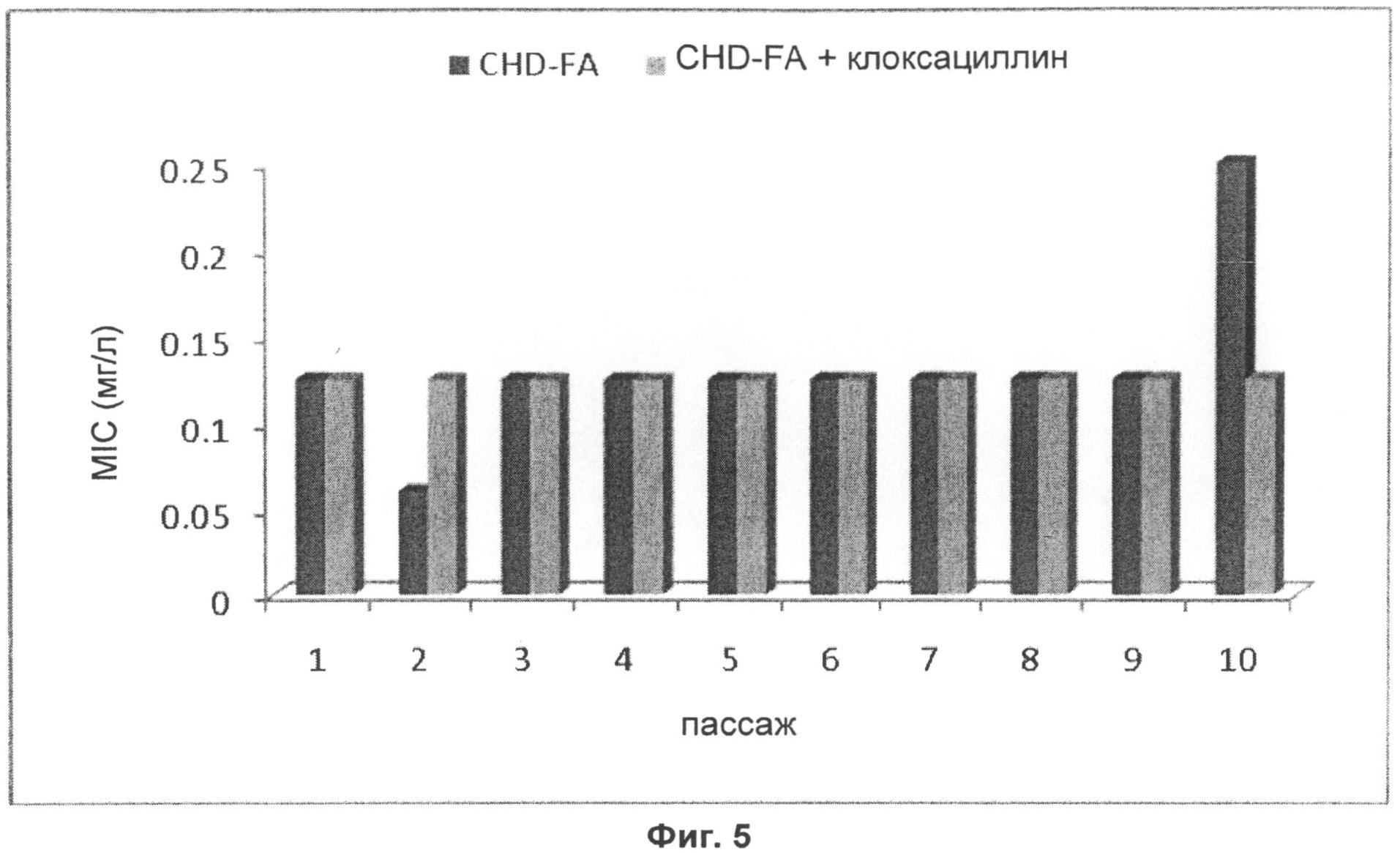
на фиг.5 - окончательные результаты определения величин MIC для CHD-FA (pH 3,0)+/- оксациллин;
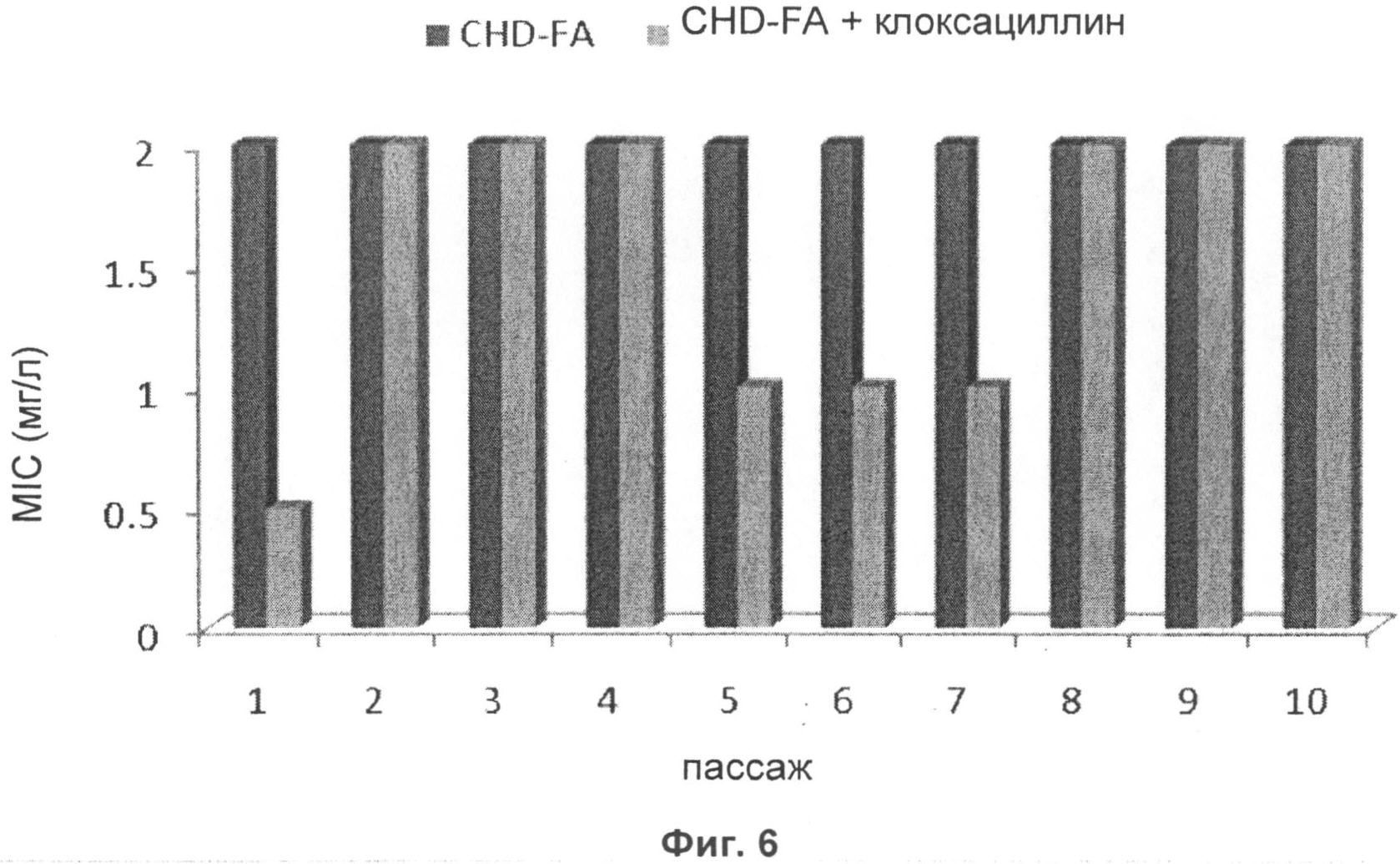
на фиг.6 - окончательные результаты определения величин MIC для CHD-FA (рН 5,0)+/- оксациллин;
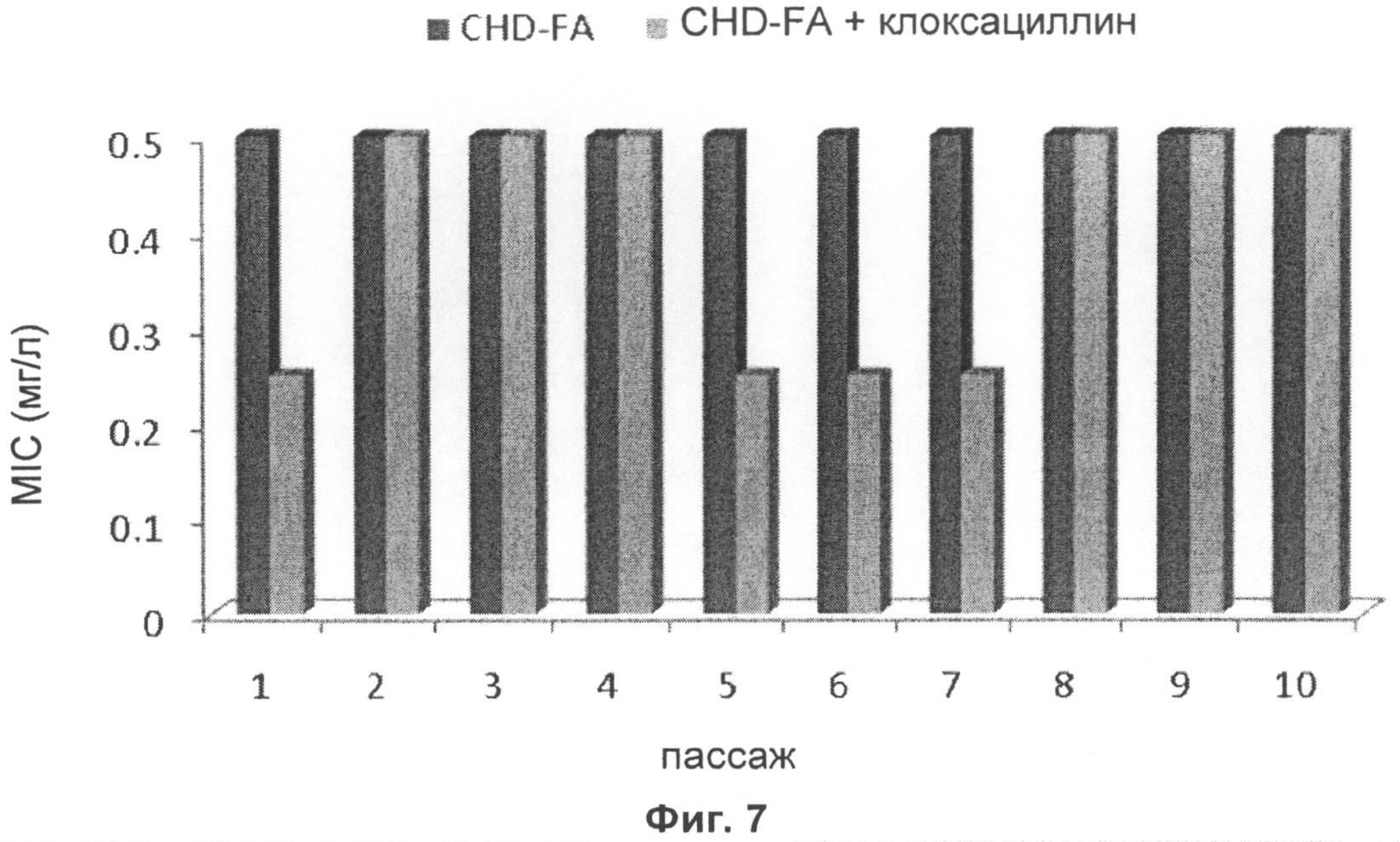
на фиг.7 - окончательные результаты определения величин MIC для CHD-FA (рН 7,0)+/- оксациллин.
Описание предпочтительных вариантов осуществления изобретения
Устойчивость к лекарственным средствам, прежде всего устойчивость ко многим лекарственным средствам (MDR), превратилась в одну из основных проблем при лечении различных заболеваний и состояний, прежде всего тех, которые вызываются бактериальными агентами. Таким образом, существует необходимость в разработке стратегии лечения, эффективной в отношении таких устойчивых штаммов.
Для оценки антибактериальных свойств фульвовой кислоты при ее применении индивидуально или в сочетании с антибиотиками из классов пенициллинов и аминогликозидов в отношении конкретных организмов, в частности бактерий, более конкретно определенных устойчивых к антибиотикам бактерий, были проведены два исследования. Исследования были выполнены с использованием фульвовой кислоты, которая была описана в WO 2007/125492 и получена методом, описанным в этой заявке, ниже в настоящем описании она обозначена как CHD-FA.
В первом исследовании оценивали антибактериальную эффективность фульвовой кислоты при ее применении индивидуально или в сочетании с оксациллином или гентамицином.
Во втором исследовании проводили оценку развития с течением времени устойчивости бактерий к фульвовой кислоте в сочетании с антибиотиком или без него.
Представленные ниже примеры даны только с целью иллюстрации и никоим образом не направлены на ограничение объема изобретения.
Пример 1: Антибактериальные характеристики фульвовой кислоты
Данное исследование проводили с целью определения антибактериальных характеристик фульвовой кислоты. Для оценки противомикробной активности рассматриваемого продукта применяли метод определения радиальных зон ингибирования роста микроорганизмов и метод серийных разведений в бульоне. Результаты продемонстрировали, что фульвовая кислота обладает противомикробной активностью в отношении Enterococcus faecalis (ATCC 51575), Salmonella enterica (ATCC 700565), Staphylococus aureus (ATCC 12600), устойчивого ко многим лекарственным средствам Staphylococcus aureus (MRSA) (ATCC) (Р3938), Escherichia coli (ATCC 1173) и Pseudomonas aeruginosa (ATCC 6027). Было продемонстрировано, что спектр противомикробной активности CHD-FA характеризуется наличием синергизма с гентамицином и оксациллином (метициллином) (фиг.1-3). Окрашивание по Граму С. albicans, выращенного в присутствии фульвовой кислоты, позволило выявить наличие округлых увеличенных не обладающих способностью к делению телец, что свидетельствует о том, что рассматриваемый продукт оказывает воздействие на клеточную мембрану микроорганизмов (фиг.4).
Методы
Тестируемый образец
Тестируемый образец представлял собой полученную из углевода фульвовую кислоту (CHD-FA). CHD-FA представляла собой жидкость коричневого цвета с содержанием 3,5% фульвовой кислоты при pH 2,14. Фульвовая кислота содержала такие элементы, как алюминий, ртуть, кадмий, хром и свинец, в концентрации менее 20 част./млн. и ее получали методом, описанным в WO 2007/125492.
Применяемые штаммы микроорганизмов
Исследование проводили с использованием следующих штаммов:
Escherichia coli (ATCC 1173), P. aeruginosa (ATCC 6027), S. aureus (ATCC 12600), недавно выделенный отрицательный по коагулазе S. aureus, Staphylococcus epidermidis (недавно выделенный изолят) и Е. coli (ATCC 1173). Штаммы S. aureus, которые применяли для сравнительных исследований, проводимых с использованием предписываемых в настоящее время антибиотиков, представляли собой клинический изолят, обозначенный как 22225 (устойчивый к эритромицину) и два устойчивых к метициллину штамма S. aureus (MRSA), а именно 2606 (устойчивый к ампициллину, оксациллину (метициллину) и обладающий слабой чувствительностью к гентамицину) и Р3938 (MRSA-штамм, устойчивый к эритромицину, оксациллину (метициллину), клиндамицину и обладающий слабой чувствительностью к фуцидовой кислоте). Тестировали также два штамма С.albicans (ATCC 10231 и ATCC 9027) и пять других недавно выделенных штаммов С.albicans, которые в проводимом исследовании обозначали как 42, 43, 44, U1 и U7.
Оценка противомикробной активности путем определения ингибирования по методу радиальной диффузии
Радиальную зону ингибирования роста микроорганизмов в результате воздействия CHD-FA определяли, следуя в целом методу Кирби-Бауэра (Kirby-Bauer). В целом метод заключался в следующем. Для количественного анализа вносили по 50 мкл чистой CHD-FA в лунки диаметром 4,5 мм и глубиной 4 мм, сделанные в агаре Мюллера-Хинтона (Mueller Hinton) (фирма Mast Group Ltd, Мерсейсайд, Великобритания), на который высевали газон соответствующего микроорганизма, и затем инкубировали в течение 16 ч при 37°С.Газон создавали путем высевания на поверхность агаровой пластины 50 мкл стандартизованной суспензии микроорганизмов в соляном растворе. Использовали суспензию, для которой при измерении с помощью колориметра (типа Sherwood, 254), снабженного фильтром оптической плотности при длине волны 520 нм, показатель составлял 0,07, что соответствовало 35×106 колониеобразующих единиц на 1 мл. Зону ингибирования измеряли дважды в двух взаимно перпендикулярных направлениях и регистрировали средние значения.
Антибиотики наносили на агаровые пластины с помощью пропитанных антибиотиком дисков (фирма Mast Group Ltd, Мерсейсайд, Великобритания) согласно стандартной процедуре, применяемой при получении лабораторных антибиограмм.
Оценка противомикробной активности методом серийных разведений в бульоне
Минимальную смертельную концентрацию (MLC) CHD-FA для различных организмов определяли с использованием двукратных серийных разведений 0,5 мл CHD-FA в соляном растворе с последующим добавлением 0,5 мл бульона Мюллера-Хинтона двойной крепости (2×) (фирма Mast Group Ltd, Мерсейсайд, Великобритания). Бульоны инокулировали, используя по 25 мкл описанной выше стандартизованной суспензии микроорганизмов, и инкубировали в течение 16 ч. Конечную точку определяли как разведение в последней пробирке, содержимое которой после нанесения в виде капель на агар Мюллера-Хинтона и инкубации в течение 16 ч характеризовалось отсутствием роста. В опыт включали соответствующие положительные и отрицательные контроли.
Оценка синергетического действия
Лунки, содержащие CHD-FA и диски антибиотика, размещали на различных расстояниях друг от друга на пластине с агаром Мюллера-Хинтона, на которую высевали соответствующий микроорганизм согласно описанной выше процедуре; картины ингибирования сравнивали с картинами, описанными ранее у Lorian (1991).
Все указанные выше исследования проводили в трех повторностях и результаты усредняли.
Морфологические исследования С. albicans
Микрофотографии получали с помощью микроскопа типа Reichert Jung, снабженного цифровой камерой (типа Motic Images Plus Version 2.0 ML), соединенной с окуляром микроскопа. Изображения получали в идентичных условиях работы микроскопа и подвергали обработке с использованием одного и того же программного обеспечения.
Результаты
Синергетическая активность CHD-FA в отношении различных микроорганизмов
Синергетическая активность полученной из углевода фульвовой кислоты и оксациллина (метициллина) в отношении газона S. aureus (ATCC 12600) продемонстрирована на фиг.1. На фиг.2 представлены данные, характеризующие наличие синергетической активности CHD-FA и оксациллина (метициллина) в отношении газона MRSA-штамма (Р3938), а на фиг.3 - данные, характеризующие наличие синергетической активности фульвовой кислоты и гентамицина в отношении газона P. aeruginosa (ATCC 9027).
Воздействие CHD-FA на морфологию С. albicans
На фиг.46 представлены результаты окрашивания по Граму штамма С. albicans, собранного из зоны ингибирования, обусловленного действием CHD-FA, которые можно сравнить с представленными на фиг.4а результатами окрашивания по Граму штамма С. albicans, который не подвергали противомикробному воздействию CHD-FA.
Обсуждение
Результаты, полученные путем оценки ингибирования по методу радиальной диффузии и методом серийных двукратных разведений в бульоне, демонстрируют, что CHD-FA является противомикробным средством, обладающим широким спектром действия в отношении грамположительных кокков, грамотрицательных бацилл и дрожжей. Такой спектр ингибирования не характерен для обычных предписываемых в настоящее время антибиотиков. Было установлено также, что CHD-FA обладала эффективностью в отношении трех выделенных недавно штаммов S. aureus, два из которых относились к MRSA-штаммам. Три выделенных недавно штамма S. aureus постепенно приобретали устойчивость к эритромицину, ампициллину, оксациллину (метициллину), клиндамицину, гентамицину и обладали слабой чувствительностью к CHD-FA.
Фульвовая кислота обладает синергетическим действием при ее применении совместно с оксациллином (метициллином) и гентамицином, тем самым, повышая их противомикробную эффективность, возможно за счет того, что облегчает проникновение антибиотика в микроорганизм в результате неспецифического ославляющего воздействия на клеточные мембраны микроорганизмов, что проиллюстрировано на фиг.4.
Пример 2: Развитие устойчивости к CHD-FA
Физические характеристики CHD-FA, также известной под называнием фульвовая кислота CHD-FA, которую применяли в примере 2, восстанавливали в виде 4%-ного раствора. Растворы хранили при комнатной температуре в темноте. Все эксперименты, результаты которых представлены в настоящем описании, проводили с использованием третьей бутыли, которую получили в декабре 2008 г. непосредственно из Южной Африки.
4%-ный раствор CHD-FA представлял собой слегка вязкий раствор желтого/коричневого цвета, обладающий сильным запахом, и он имел значение pH 1,9 при 25°C. В данном исследовании значение pH CHD-FA регулировали с помощью 10 M гидроксида натрия, получая 4%-ный маточный раствор CHD-FA, забуференный до значения pH 3, 5 или 7.
Методы
Бактериальные изоляты
Тесты по оценке чувствительности проводили на бактериальном изоляте, представляющем собой устойчивый к метициллину штамм Staphylococcus aureus EMRSA16. Штамм EMRSA16 выделяли после продолжительного хранения на гранулах при -80°C и выращивали на агаровой среде Мюллера-Хинтона (фирма Oxoid) при 37°C в течение 24 ч.
Среды
Все эксперименты проводили с использованием бульона или агаровых препаратов на основе среды Мюллера-Хинтона (фирма Oxoid), восстановленной согласно инструкциям производителя.
Приготовление инокулята
а) Штамм EMRSA16 культивировали в обычных атмосферных условиях при 37°C на агаре Мюллера-Хинтона в течение 24 ч перед проведением тестирования.
б) Инокулят каждого штамма приготавливали путем отбора отдельных колоний с культуральных планшетов и их суспендирования в 2 мл бульона Мюллера-Хинтона. Затем концентрацию регулировали до достижения мутности согласно стандарту МакФарланда, до уровня, составляющего 0,5.
в) Инокулят полностью ресуспендировали путем интенсивного встряхивания на вихревом смесителе в течение 15 с.
г) Затем инокулят разводили в соотношении 1:100 в бульоне Мюллера-Хинтона для проведения тестов по оценке MIC.
Условия анализа
Применяли стерильные пластиковые одноразовые титрационные 96-луночные плоскодонные микропланшеты.
Стадия 1. Добавление CHD-FA
Маточный раствор CHD-FA содержал 4% нативного соединения. Для каждого тестируемого штамма в каждую из лунок 2-12 добавляли по 100 мкл среды. Затем в лунки, находящиеся в колонке 1, добавляли по 200 мкл 4%-ной CHD-FA. Из лунок в колонке 1 брали по 100 мкл и разводили в два раза путем переноса в лунки колонки 2 с помощью многоканальной пипетки (коэффициент вариации ±2%). Затем из лунок в колонке 2 брали образцы по 100 мкл и переносили в лунки колонки 3, и т.д. вплоть до колонки 10. Последние 100 мкл лекарственной субстанции отбрасывали. Колонка 11 представляла собой положительный контроль, не содержащий CHD-FA, а колонка 12 представляла собой отрицательный контроль, содержащий только разбавитель.
Стадия 2. Добавление оксациллина
Приготавливали маточный раствор оксациллина с концентрацией 1600 мг/л путем добавления 5 мл стерильной дистиллированной воды к 8 мг оксациллина. Затем приготавливали разведение маточного раствора в соотношении 1:100, после чего осуществляли серийные разведения в соотношении 1:2 с получением разведений оксациллина в диапазоне от 16 до 0,06 мг/л. После этого добавляли 50 мкл разведенного оксациллина к разведенной CHD-FA для тех вариантов, когда это требовалось, получая конечные концентрации оксациллина, составляющие от 4 до 0,015 мг/л.
Стадия 3. Добавление штамма EMRSA16
В соответствующие лунки добавляли разведенную суспензию инокулята в бульоне Мюллера-Хинтона в объеме, составляющем либо 100 мкл, либо 50 мкл, для оценки эффективности либо CHD-FA, либо комбинации CHD-FA+оксациллин соответственно. В результате конечный объем в лунке составлял 200 мкл (он включал 100 мкл разведенной CHD-FA или разбавителей и 100 мкл инокулята в соответствующем бульоне для штамма или только бульона).
Стадия 4. Инкубация планшетов
Все планшеты инкубировали на воздухе при температуре 37°C и затемненном термостате в течение 48 ч.
Стадия 5. Анализ планшетов
Осуществляли визуальный анализ планшетов, конечная цель которого заключалась в том, чтобы определить наименьшую концентрацию лекарственного средства, вызывающую ингибирование роста на 50% по сравнению с ростом в контрольной среде, не содержащей лекарственное средство.
Стадия 6. Устойчивость, приобретаемая в результате пассажей
Для оценки влияния устойчивости, приобретаемой в результате пассажей, на ингибирующее воздействие комбинации CHD-FA+/-оксациллин на EMRSA16, осуществляли инокуляцию 100 мкл содержащейся в последней лунке культуры, которая была выращена на планшете с MIC (минимальная ингибирующая концентрация), на половину планшета с агаровой средой Мюллера-Хинтона и инкубировали при 37°C в течение 24 ч. Затем продукт, полученный на этом планшете, использовали в качестве свежей суспензии для осуществления следующего пассажа. Эту процедуру повторяли, осуществляя в общей сложности 10 пассажей, при этом после каждого пассажа проводили оценку эффективности комбинации CHD-FA+/-оксациллин в отношении EMRSA16.
Результаты
MIC для комбинации CHD-FA+/-оксациллин
Результаты оценки MIC продемонстрировали, что эффективность комбинации CHD-FA+/-оксациллин оставалась стабильной при осуществлении вплоть до 10 пассажей. Подробные данные о величинах MIC для комбинации CHD-FA+/-оксациллин представлены в таблице 1.
|
|
Окончательные величины MIC для CHD-FA при pH 3,0.
Окончательные величины MIC свидетельствуют о том, что эффективность комбинации CHD-FA (pH 3,0)+/-оксациллин оставалась стабильной при осуществлении вплоть до 10 пассажей, т.е. результаты оценок MIC при каждом пассаже отличались не более чем в одной лунке по сравнению с результатами первоначальной оценки MIC (пассаж 1). Подробные данные о полученных в результате исследования величинах MIC для комбинации CHD-FA (pH 3,0)+/-оксациллин представлены на фиг.5.
Окончательные величины MIC для CHD-FA при pH 5,0.
Окончательные величины MIC свидетельствуют о том, что эффективность комбинации CHD-FA (pH 5,0)+/-оксациллин оставалась на близком уровне при осуществлении вплоть до 10 пассажей, т.е. результаты оценок MIC при каждом пассаже отличались не более чем в одной лунке по сравнению с результатами первоначальной оценки MIC (пассаж 1). Подробные данные о полученных в результате исследования величинах MIC для комбинации CHD-FA (pH 5,0)+/-оксациллин представлены на фиг.6.
Окончательные величины MIC для CHD-FA при pH 7,0.
Окончательные величины MIC свидетельствуют о том, что эффективность комбинации CHD-FA (pH 7,0)+/-оксациллин оставалась стабильной при осуществлении вплоть до 10 пассажей, т.е. результаты оценок MIC при каждом пассаже отличались не более чем в одной лунке по сравнению с результатами первоначальной оценки MIC (пассаж 1). Подробные данные о полученных в результате исследования величинах MIC для комбинации CHD-FA (pH 7,0)+/-оксациллин представлены на фиг.7.
Выводы:
- CHD-FA обладает эффективностью в отношении EMRSA16 по данным анализа in vitro при забуферивании до pH 3,0, 5,0 или 7,0.
- Комбинация CHD-FA плюс оксациллин обладает эффективностью в отношении EMRSA16 по данным анализа in vitro при забуферивании до pH 3,0, 5,0 или 7.0.
- Последовательно осуществляемые пассажи EMRSA16 в присутствии лишь субингибирующих уровней CDH-FA не оказывали влияния на величину MIC.
- Последовательно осуществляемые пассажи EMRSA16 в присутствии лишь субингибирующих уровней комбинации CDH-FA плюс оксациллин не оказывали влияния на величину MIC комбинации.
- Величины MIC CHD-FA в отношении EMRSA16 оставались стабильными после воздействия соединения при осуществлении серийных пассажей в течение периода >20 дней.
- Не было выявлено заметного развития устойчивости как в случае применения монотерапии с использованием CHD-FA, так и при использовании CHD-FA в комбинации с оксациллином, в отношении MRSA16.
Библиография
Bergh J.J., Cronje I.J., Dekker J., Dekker T.G., Gerritsma L.M. и Mienie L.J., Non-catalytic oxidation of water-slurried coal with oxygen: identification of фульвовую кислоту and acute toxicity. Fuel 76, 1997, cc. 149-154.
Lorian V., Antibiotics in Laboratory Medicine, 3-е изд., 1991, с.44 и с.447.
MacCarthy Р, Clapp СЕ, Malcolm RL, Bloom PR., Humic substances in soil and crop sciences: selected readings. Proceedings of a symposium by International Humic Substances Society, Soil Science Society of America, American Society of Agronomy and Crop Science Society of America, Chigaco, Illinois, 2 декабря 1985 г.