Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ЛЕЧЕНИЯ ВИЧ-ИНФЕКЦИИ, СПОСОБ ЕЕ ПОЛУЧЕНИЯ И СПОСОБ ЛЕЧЕНИЯ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к области химико-фармацевтической промышленности, конкретно к фармацевтической композиции для лечения ВИЧ-инфекции, которая включает в качестве активного вещества, по меньшей мере, один ингибитор ВИЧ протеазы, а также фармацевтически приемлемые вспомогательные вещества при определенном количественном соотношении компонентов. Кроме того, изобретение относится к способу ее получения и способу лечения.
Предшествующий уровень техники
По данным ООН, число людей, живущих с ВИЧ, составило 34,2 миллиона человек. Ни одна страна не избежала страшных последствий этой поистине глобальной эпидемии.
В Российской Федерации эпидемиологическая обстановка по ВИЧ-инфекции остается напряженной, продолжается распространение вируса иммунодефицита человека среди населения и увеличение кумулятивного числа инфицированных и больных.
По данным Роспотребнадзора в настоящее время в Российской Федерации проживает 617018 ВИЧ-инфицированных.
За десять месяцев 2012 года выявлено 62865 новых случаев ВИЧ-инфекции, что на 12,5% больше, чем в прошлом году. Случаи ВИЧ-инфекции зарегистрированы во всех субъектах Российской Федерации (официальный сайт Роспотребнадзора http://rospotrebnadzor.ru/bytag2/-/asset_publisher/01Cv/content)
Ингибиторы протеазы (ИП) ВИЧ - это вещества, обладающие сродством к активному центру протеазы ВИЧ, которая должна расщеплять полипротеин вируса Gag-Pol на отдельные функциональные белки. В результате действия ингибиторов протеаза не выполняет свою функцию, и образуются вирусные частицы, не способные заражать новые клетки. ИП нередко оказывают побочное действие на ЖКТ. При длительном применении возможны нарушения липидного обмена разной степени тяжести и развитие липодистрофии.
Среди ингибиторов ВИЧ-протеазы известны такие вещества, как нелфинавир, саквинавир, типранавир, дарунавир, индинавир, атазанавир, ритонавир, лопинавир, палинавир, фосампренавир.
Известно, что практически все ингибиторы протеазы ВИЧ являются малорастворимыми в воде субстанциями. В связи с этим возникают технологические сложности в процессе создания готовых лекарственных форм на основе этих субстанций. Кроме того, очень трудной задачей является подобрать состав вспомогательных веществ таким образом, чтобы не произошло ухудшение фармакокинетических параметров готовой лекарственной формы и соответственно биодоступности.
Из уровня техники известен препарат Калетра® таблетки, покрытые пленочной оболочкой (Лопинавир 200 мг + Ритонавир 50 мг)» производства Эбботт ГмбХ и Ко.КГ, Германия, который описан в патенте ЕА 011924 и принят авторами настоящего изобретения за прототип.
Как следует из патента ЕА 0011924 авторами была предпринята попытка улучшить биодоступность твердой лекарственной формы лопинавира+ритонавира. Данная задача была решена путем введения в состав готовой лекарственной формы водорастворимых полимеров в достаточно большом количестве от примерно 50 до примерно 85 мас.% и фармацевтически приемлемое поверхностно-активное вещество в количестве от примерно 2 до примерно 20 вес.% относительно веса дозированной формы.
Применение относительно больших количеств дорогостоящих вспомогательных веществ увеличивает себестоимость препарата.
Кроме того, важным недостатком лопинавира/ритонавира является его способность вызывать не только желудочно-кишечные расстройства (диарею, тошноту), но и выраженную дислипопротеидемию - даже более значительную, чем наблюдаемая на фоне приема других ИП. Подобно прочим ИП, лопинавир/ритонавир вызывает липодистрофический синдром, частота которого, по данным одного долговременного исследования, составляет 15% через 5 лет. Кроме того, назначая этот препарат, следует принимать во внимание многочисленные лекарственные взаимодействия. В комбинациях с эфавирензом и невирапином, а возможно и с ампренавиром, его дозу следует повышать. По последним данным, лопинавир/ритонавир допустимо назначать раз в сутки (800/200 мг), хотя в этом случае он несколько чаще провоцирует диарею. Таким образом, в настоящее время существует необходимость разработки новых готовых лекарственных форм, обладающих противовирусной активностью, ингибирующих активность ВИЧ протеазы, с улучшенными фармакокинетическими и технологическими свойствами, а также с увеличенной биодоступностью и следовательно улучшенной терапевтической эффективностью.
Авторы настоящего изобретения поставили перед собой следующую техническую задачу: разработка новых и более эффективных(по сравнению с прототипом) лекарственных форм препарата(ингибитора протеазы ВИЧ), обладающих следующими свойствами: 1) лекарственная форма должна обладать улучшенными технологическими свойствами(прочность, пластичность, распадаемость и т.п.), а также высокой стабильностью; 2) лекарственная форма должна обладать улучшенной кинетикой растворения и повышенной(по сравнению с прототипом) биодоступностью.
Достигаемый технический результат предлагаемого изобретения соответствует поставленным задачам и заключается в расширении арсенала качественных доступных отечественных лекарственных средств для лечения ВИЧ-инфекции, обладающих улучшенной кинетикой растворения и повышенной биологической доступностью по сравнению с лекарственным препаратом по прототипу. Кроме того, полученные лекарственные формы обладали улучшенными технологическими свойствами и высокой стабильностью при хранении. Полученные технические результаты не являются очевидными и их нельзя было предвидеть специалисту на основании имеющегося уровня техники.
Подробное описание сущности изобретения
Поставленная задача решается тем, что авторами настоящего изобретения была разработана фармацевтическая композиция для лечения ВИЧ-инфекции, включающая, по меньшей мере, один ингибитор протеазы ВИЧ и фармацевтически приемлемые вспомогательные вещества при определенном количественном
соотношении компонентов.
В результате проведенных экпериментальных исследований авторам настоящего изобретения удалось значительно снизить содержание водорастворимых полимеров в составе фармацевтической композиции. При этом было неожиданно обнаружено, что кинетика растворения и биологическая доступность заявляемой фармацевтической композиции значительно улучшилась, по сравнению с препаратом по прототипу. Таким образом, фармацевтическая композиция в соответствии с настоящим изобретением обеспечивает сокращение времени до наступления лечебного эффекта и достигается тщательно подобранным качественным составом и количественным соотношением вспомогательных компонентов.
Авторами настоящего изобретения к настоящему моменту времени до конца не изучена причина улучшения фармакокинетических свойств и увеличения биодоступности при снижении содержания в готовой лекарственной форме водорастворимых полимеров.
Авторы не исключают возможность влияния на данные улучшения содержание водонерастворимых полимеров и поверхностно-активных веществ и их взаимодействие.
В результате создания различных вариантов заявляемой фармацевтической композиции было установлено, что указанный технический результат достигается при условии, если в одном из вариантов заявляемая фармацевтическая композиция содержит от 0,4 до 49 масс.% (в пересчете на 100 мас.% всей твердой лекарственной формы) водорастворимых полимеров, а также содержит по меньшей мере один водонерастворимый полимер в количестве от 0,39 до 28 масс.% от массы всей готовой лекарственной формы. В результате проведенных экспериментов было обнаружено, что при ином содержании водорастворимых и водонерастворимых полимеров получаемая готовая лекарственная форма получается с иными(сниженными по сравнению с прототипом) характеристиками.
В результате экспериментальной разработки возможных составов готовых лекарственных форм было найдено, что сами активные вещества, которые могут входить в состав заявляемой фармацевтической композиции включают нелфинавир, саквинавир, типранавир, дарунавир, индинавир, ритонавир, лопинавир, палинавир, фосампренавир или их комбинации друг с другом, являются известными из уровня техники и применяются для лечения ВИЧ-инфекций.
Согласно изобретению, предлагаемое противовирусное лекарственное средство содержит активного вещества в количестве от 5,0 масс.% до 60,5% от массы лекарственной формы, а также фармацевтически приемлемые вспомогательные вещества в количестве от 39,5% до 95,0% от массы активного вещества.
Эффективное количество активного вещества-ингибитора протеазы ВИЧ в лекарственной форме составляет от 5 мг до 1500 мг.
Предпочтительно, что заявляемая противовирусная фармацевтическая композиция дополнительно содержит, по меньшей мере, еще одно противовирусное средство(ингибитор ВИЧ-протеазы) для достижения синергетического действия. Ингибиторы ВИЧ-протеазы, которые могут входить в состав фармацевтической композиции по настоящему изобретению могут включать нелфинавир, саквинавир, типранавир, дарунавир, индинавир, ритонавир, лопинавир, палинавир или фосампренавир и/или их комбинации.
Наряду с активным веществом фармацевтическая композиция может при этом содержать обычные вспомогательные вещества, принятые в технологии приготовления лекарственных средств, такие как связующие, наполнители, консерванты, регуляторы текучести, смягчители, смачиватели, диспергаторы, эмульгаторы, растворители, антиокислители и/или пропелленты, пролонгаторы действия Sucker et al.: Pharmazeutische Technologie, Thieme-Verlag, Stuttgard, 1991.
В качестве наполнителя фармацевтическая композиция содержит одно или несколько веществ из следующих: сахара и их производные (лактоза, модифицированная лактоза, сахароза, глюкоза, маннит, модифицированный маннит, сорбит, фруктоза), полисахариды (целлюлоза и ее производные, крахмал, модифицированный крахмал, декстрин, декстроза, декстрат, мальтодекстрин, кальций и его соли (фосфаты, карбонаты, хлориды), магний и его производные (оксид, карбонат, стеарат), кросповидон, коповидоны, циклодекстрины, альгиновая кислота и ее соли, сахарин и его соли, натрий и его соли (хлорид, цитрат, фумарат, карбонат), аспартам, молочная кислота и ее соли, янтарная кислота, аскорбиновая кислота, тартаровая кислота, коллоидная двуокись кремния, цикламат, бензойная кислота и ее соли, парабены и их соли.
Предпочтительно, фармацевтическая композиция содержит от 0,3 до 56 масс.% перечисленных выше наполнителей (в пересчете на 100 мас.% всей твердой лекарственной формы).
Водорастворимые полимеры, подходящие для использования в составе фармацевтической композиции по настоящему изобретению, включают, но не ограничиваются следующими веществами: гомополимеры и сополимеры N-виниллактамов, особенно гомополимеры и сополимеры N-винилпирролидона, например поливинилпирролидон (PVP), сополимеры N-винилпирролидона и винил-ацетата или винилпропионата; высокомолекулярные полиалкилен-оксиды, такие как полиэтиленоксид и полипропиленоксид и сополимеры этиленоксида и пропиленоксида;полиакрилаты и полиметакрилаты, такие как метакриловая кислота/этилакрилатные сополимеры, метакриловая кислота/метилметакрилатные сополимеры, бутилметакрилат/2-диметиламиноэтилметакрилатные сополимеры, поли(гидроксиалкилакрилаты), поли(гидроксиалкилметакрилаты); полиакриламиды;винилацетатные полимеры, такие как сополимеры винилацетата и кротоновой кислоты;поливиниловый спирт; олиго- и полисахариды, такие как каррагинаны; сложные эфиры целлюлозы и простые эфиры целлюлозы, в частности метилцеллюлозу и этилцеллюлозу, гидроксиалкилцеллюлозы, в частности гидроксипропилметилцеллюлозу, сукцинаты целлюлозы, в частности сукцинат гидроксипропилметилцеллюлозы или ацетатсукцинат гидроксипропилметилцеллюлозы.
Водонерастворимые полимеры, которые могут использоваться в настоящем изобретении включают, но не ограничиваются следующими веществами: целлюлоза микрокристаллическая, гипролоза(гидрокси-пропилцеллюлоза) низкозамещенная.
Предпочтительно, фармацевтическая композиция содержит от 0,4 до 4 9 масс.% перечисленных выше водорастворимых полимеров,по меньшей мере, один водонерастворимый полимер от 0,39 до 28 масс.% от массы всей готовой лекарственной формы, поверхностно-активные вещества, наполнители до массы 100% всей готовой лекарственной формы.
В одном из вариантов осуществления заявленного изобретения фармацевтическая композиция содержит от 0,4 до 20 масс.% перечисленных выше водорастворимых полимеров (в пересчете на 100 мас.% всей твердой лекарственной формы).
Поверхностно-активные вещества, подходящие для использования в составе фармацевтической композиции по настоящему изобретению, включают, но не ограничиваются следующими веществами: полисорбат 8 0 (например, полисорбат марки ТВИН-80), макрогол 6000(полиэтиленгликоль 6000).
Предпочтительно, фармацевтическая композиция содержит от 0,3 до 1,0 масс.% поверхностно-активных веществ (в пересчете на 100 мас.% всей твердой лекарственной формы).
Предпочтительно лекарственное средство может быть изготовлено в виде порошков, таблеток, комбинированных таблеток, капсул, драже, гранул, покрытых оболочкой, суппозиторий, порошков для приготовления суспензий. Лекарственные формы могут быть выполнены традиционным способом («Фармацевтическая технология. Технология лекарственных форм», 2-ое изд., Москва, 2006 г).
Фармацевтическая композиция по изобретению может вводиться перорально. Дозировка зависит от возраста, состояния и веса пациента.
Для пациентов, ранее не получавших антиретровирусную терапию, рекомендуемая дозировка комбинированного препарата лопинавир/ритонавир составляет 400/100 мг 2 раза в день или 800/200 мг 1 раз в день.
Для пациентов, получавших ранее антиретровирусную терапию, рекомендуемая дозировка комбинированного препарата лопинавир/ритонавир составляет 400/100 мг. Применение препарата 1 раз в день у этих пациентов не рекомендуется.
Эффективная дозировка активного вещества-ингибитора протеазы ВИЧ-нелфинавира в лекарственной форме составляет 750 мг.
Эффективная дозировка активного вещества-ингибитора протеазы ВИЧ-дарунавира в лекарственной форме составляет 300 мг.
Эффективная дозировка активного вещества-ингибитора протеазы ВИЧ-саквинавира в лекарственной форме составляет 500 мг.
Эффективная дозировка активного вещества-ингибитора протеазы ВИЧ-индинавира в лекарственной форме составляет 400 мг.
Эффективная дозировка активного вещества-ингибитора протеазы ВИЧ-типранавира в лекарственной форме составляет 500 мг.
Эффективная дозировка активного вещества-ингибитора протеазы ВИЧ-фосампренавира в лекарственной форме составляет 14 00 мг.
Также в соответствии с настоящим изобретением заявляется способ лечения ВИЧ-инфекции, включающий введение млекопитающему, нуждающемуся в таком лечении, фармацевтической композиции в соответствии с настоящим изобретением.
Представленные ниже примеры иллюстрируют (без ограничения объема притязаний) наиболее предпочтительные варианты осуществления изобретения, а также подтверждают возможность получения заявляемой фармацевтической композиции и достижения указанных технических результатов.
Пример 1
Описание технологии получения таблеток покрытых пленочной оболочкой:
Активные фармацевтические субстанции ингибитора протеазы ВИЧ нелфинавир, саквинавир, типранавир, дарунавир, индинавир, ритонавир, лопинавир, палинавир или фосампренавир раздельно микронизируют в водно-спиртовом растворе поверхностно-активных ингредиентов полисорбат 80 и макрогол 6000 в течение 10 минут, с последующим растворением субстанций в шестиатомном спирте сорбитола и макрогол 6000 в течение 10 минут, с последующим растворением субстанций в шестиатомном спирте сорбитола и углеводе дисахарида лактозы и гранулированием. Сушат влажную смесь обычным способом, в псевдоожиженном слое при температуре до 60°C до остаточной влаги не более 2-3%. Затем смешивают и опудривают вспомогательными ингредиентами до однородности в следующей последовательности: целлюлоза микрокристаллическая, карбоксиметилкрахмал натрия, кроскармеллоза натрия, коповидон(например, коповидон марки коллидон VA 64), гипролоза низкозамещенная, кремния диоксид коллоидный, натрия стеарилфумарат или магния стеарат.Из полученной массы для таблетирования получают ядра-таблетки, которые покрывают водорастворимой оболочкой.
Пример 2
Методика исследования пероральной биологической доступности
Исследование биологической доступности проводили на собаках самцах и самках массой примерно 10 кг. Все животные при проведении эксперимента получали сбалансированный кормовой рацион, содержащий 27% жира, и воду в неограниченном количестве. Каждой собаке (примерно за 30 мин до введения исследуемого средства) перорально вводили 100 мкг/кг гистамина. Каждой собаке вводили перорально дозы, содержащие 200 мг лопинавира и 50 мг ритонавира соответственно. Затем вводили примерно 10 мл воды. У каждого животного до введения и через 0,25, 0,5, 1,0, 1,5, 2, 3, 4, 6, 8, 10, 12 и 24 ч после введения лекарственного средства брали пробы крови.
Плазму отделяли от эритроцитов с помощью центрифугирования и до проведения анализа замораживали (-30°C). Концентрации ингибиторов протеазы ВИЧ определяли с помощью высокоэффективной жидкостной хроматографии с обращенной фазой с детектированием в коротковолновом УФ-диапазоне, а затем образцы плазмы подвергали жидкостной экстракции. В течение проведения исследования площадь под кривой (AUC) рассчитывали по методике трапеций. Для изучения каждой дозированной формы использовали группу, содержащую 11-13 собак; приведенные значения являются средними для каждой группы собак. Дозозависимые показатели препарата AUC по прототипу у собак составили 10,22 мкг·ч/мл/100 мг для ритонавира и 50,2 мкг·ч/мл/100 мг для лопинавира. Дозозависимые показатели препарата AUC фармацевтической композиции в соответствии с настоящим изобретением у собак составили 30,36 мкг-ч/мл/100 мг для ритонавира и 66,2 мкг·ч/мл/100 мг для лопинавира.
Результаты этого исследования показали, что биологическая доступность фармацевтической композиции в соответствии с изобретением была выше, чем у лекарственного препарата по прототипу.
Пример 3
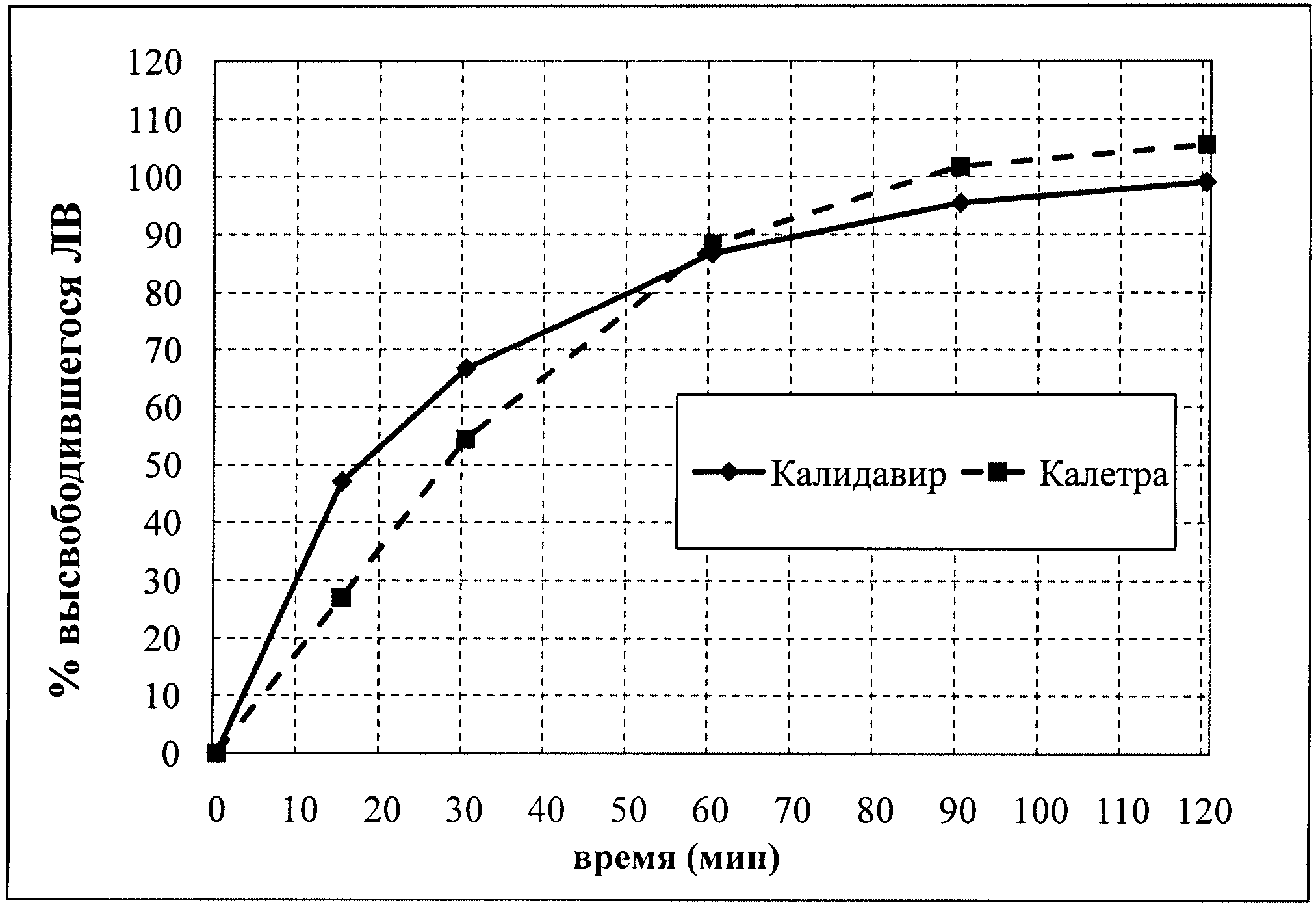
Изучение сравнительной кинетики растворения лекарственных средств «Калидавир® таблетки, покрытые пленочной оболочкой (Лопинавир 100 мг + Ритонавир 25 мг)» производства ОАО «Фармасинтез», Россия, и «Калетра таблетки, покрытые пленочной оболочкой (Лопинавир 200 мг + Ритонавир 50 мг)» производства Эбботт ГмбХ и Ко.КГ, Германия
Исследование проводили согласно ОФС 42-0003-04 «Растворение» на аппарате «лопастная мешалка» при скорости вращения 75 об/мин при температуре 37±0,5°C. Среда растворения - 1% раствор натрия додецилсульфата. Объем среды растворения - 900 мл. Временные точки отбора проб: 15 мин, 30 мин, 60 мин, 90 мин, 120 мин. Количественное определение высвободившихся лопинавира и ритонавира проводили методом ВЭЖХ.
Профиль растворения лекарственных средств Калидавир и Калетра приведен на Рисунке 1.
Среднее значение количества лопинавира, высвободившегося в течение 15 мин из лекарственного средства Калидавир (производства ОАО «Фармасинтез») составило 47,09% (т.е. менее 85%), ритонавира - 107,27% (более 85%), из лекарственного средства Калетра(производства Эбботт ГмбХ) высвобождение лопинавира составило 27,03%, ритонавира - 25,81% (т.е. менее 85%).
Таким образом, исходя из полученных результатов видно, что фармацевтическая композиция в соответствии с настоящим изобретением обладает улучшенным по сравнению с прототипом профилем высвобождения, что и позволяет достигнуть увеличения биодоступности заявляемой фармацевтической композиции.
Пример 4(получение таблеток лопинавир+ритонавир 100 мг + 25 мг покрытых оболочкой)
Активные фармацевтические субстанции лопинавира и ритонавира раздельно микронизируют в водно-спиртовом растворе поверхностно-активных ингредиентов полисорбат 80 и макрагол 6000 в течение 10 минут, с последующим растворением субстанций в шестиатомном спирте маннитола и углеводе дисахарида лактозы и гранулированием. Сушат влажную смесь обычным способом, в псевдоожиженном слое при температуре до 60°С до остаточной влаги не более 2-3%. Затем смешивают и опудривают вспомогательными ингредиентами до однородности в следующей последовательности: целлюлоза микрокристаллическая, карбоксиметилкрахмал натрия, кроскармеллоза натрия, коповидон, гипролоза низкозамещенная, кремния диоксид коллоидный, натрия стеарилфумарат или магния стеарат.Из полученной массы для таблетирования получают ядра-таблетки, которые покрывают водорастворимой оболочкой. Получаемые таблетки имеют следующий состав(соотношения всех компонентов даны в пересчете на 100 мас.% всей таблетки):
|
|
Пример 5 (получение таблеток лопинавир + ритонавир 200 мг + 50 мг и 100 мг + 25 мг покрытых оболочкой)
Согласно методике, описанной в примере 1, получена фармацевтическая композиция, выполненная в форме таблетки (лопинавир + ритонавир 200 мг + 50 мг, 100 мг + 25 мг покрытые оболочкой), имеет следующий состав и соотношение компонентов, масс.% (соотношения всех компонентов даны в пересчете на 100 мас.% всей таблетки):
|
Пример 6 (получение капсул 5 мг, 10 мг, 25 мг, 50 мг, 100 мг ризюнавира)
Просеянные порошки ритонавира в количестве 50,0 г, кросповидона в количестве 10,0 г, макрогола 6000 в количестве 8,0 г загружают в шаровую мельницу и микронизируют в течение 30 минут.Микронизированный ритонавир в смеси с макроголом 6000 и кросповидоном гранулируют в псевдоожиженном слое 20% раствор лактозы и маннита. Полученный гранульный порошок опудривают натрия стеарилфумаратом в количестве 2,0 г в конусном смесителе. Капсулы обеспыливают и упаковывают в банки полимерные или контурные односторонние упаковки. Получают 1000 капсул лекарственного средства по изобретению с общей массой содержимого 200,0 г или 0,200 г ± 10% каждая капсула с содержимым активного ингредиента 0,050 г ± 10%.
Получаемые капсулы имеют следующий состав(соотношения всех компонентов даны в пересчете на 100 мас.% всей капсулы):
|
Пример 7
Исследование влияния содержания водорастворимых и водонерастворимых полимеров на биодоступность
Самцы неинбрендных крыс весом в пределах 300-350 г были выбраны для исследования пероральной биодоступности in vivo. Крыс содержали в условиях вивария с естественным световым режимом на стандартной диете лабораторных животных (ГОСТ Р502 58-92) с соблюдением Международных рекомендаций Европейской конвенции по защите позвоночных животных, используемых при экспериментальных исследованиях (1997), а также правил лабораторной практики при проведении доклинических исследований в РФ. Каждую крысу подготавливали хирургической имплантацией постоянного катетера в верхнюю полую вену. Крысы были разделены на четыре группы по 9 особей в каждой группе. I группе крыс вводили перорально композицию, содержащую 0,4% водорастворимых полимеров и 0,39% водонерастворимых полимеров следующего состава:
|
Водонерастворимых полимеров 0,39% (1,04 мг), водорастворимых полимеров 0,4% (1,068 мг), II группе крыс вводили перорально композицию, содержащую 49% водорастворимых полимеров и 28% водонерастворимых полимеров следующего состава:
|
Водорастворимых полимеров(повидон) - 49%
Водонерастворимых полимеров (гипролоза низкозамещенная, целлюлоза микрокристаллическая) - 28%
III группе крыс вводили перорально композицию, содержащую 0,4% водорастворимых полимеров и 3,75% водонерастворимых полимеров. Состав фарм. композиции соответствует составу, раскрытому в примере 4.
В качестве препарата сравнения, который вводили перорально IV группе(контрольная группа) крыс, использовали таблетки Калетра® следующего состава (г):
|
Коповидон К 28 - 426,9 мг; сорбитана лаурат - 41,95 мг; кремния диоксид коллоидный - 6,0 мг; второй слой: натрия стеарилфумарат - 6,15 мг; кремния диоксид коллоидный - 4,0 мг;
пленочное покрытие: Опадрай® II розовый 85 F 14399 - 15,0 мг (поливиниловый спирт - 40,00%, титана диоксид - 24,85%, тальк - 14,80%, макрогол 3350 - 20,20%, краситель железа оксид красный Е172 - 0,15%.
Сравниваемые препараты давали однократно в дозе, которая номинально соответствует 1/5 дозы, рекомендованной для человека.
Последовательные пробы крови 0,25 мл получали из постоянного катетера при 0,25, 0,5, 1, 2, 4, 6, 8, 12 и 24 часах после дозирования. Эти пробы крови анализировали при помощи ВЖХ-анализа, специфического для тестируемых соединений. Концентрации каждой из трех композиций в крови тестируемых крыс наносили на график зависимости от времени после введения композиции пероральным путем и AUC (площадь под кривой зависимости концентрации в плазме от времени) интегрировали с применением правила трапеций для расчета абсолютной биодоступности, показанной в таблице 1.
|
Таким образом, в результате проведенных исследований неожиданно было установлено, что фармацевтическая композиция, содержащая в своем составе 0,4 масс.% водорастворимых полимеров и 0,39% водонерастворимых полимеров позволила увеличить абсолютную биодоступность на 11% по сравнению с композицией по прототипу. Фармацевтическая композиция, содержащая в своем составе 49 масс.% водорастворимых полимеров и 2 8 масс.% водонерастворимых полимеров позволила увеличить абсолютную биодоступность на 21% по сравнению с композицией по прототипу.
Авторами настоящего изобретения неожиданно было обнаружено, что содержание водорастворимых и водонерастворимых полимеров в составе заявляемых композиций оказывает влияние на такие технологические свойства, как прочность лекарственной формы и пластичность. В результате проведенных исследований было установлено, что готовые лекарственные формы(таблетки), содержащие в своем составе водорастворимые полимеры в диапазоне от 0,4 до 49 масс.%, а также от 0,3 до 28 масс.% водонерастворимых полимеров, являются более прочными по сравнению с прототипом. Кроме того, таблетки в соответствии с настоящим изобретением также имеют высокую пластичность за счет использования высокопластичных полимеров, что в свою очередь приводит к меньшим потерям при таблетировании, позволяет увеличить скорость таблетирования и обеспечивает лингвальность (легкую проглатываемость) таблеток.
Механическую прочность таблеток измеряли по истираемости таблеток. Исследование прочности таблеток на истираемость проводили на приборе Agilent Friability Tester. Прочность таблеток по прототипу на истираемость составила 98%. Прочность таблеток, содержащих в своем составе 0,4% водорастворимых полимеров и 0,39% водонерастворимых полимеров составила 99,4%. Прочность таблеток, содержащих в своем составе 49% водорастворимых полимеров и 28% водонерастворимых полимеров составила 99,8%.
Таким образом, заявленное изобретение позволяет получить новую и более эффективную(по сравнению с прототипом) фармацевтическую композицию, обладающую улучшенными технологическими свойствами (прочность, пластичность, распадаемость), а также улучшенной кинетикой растворения и повышенной(по сравнению с прототипом) биодоступностью.