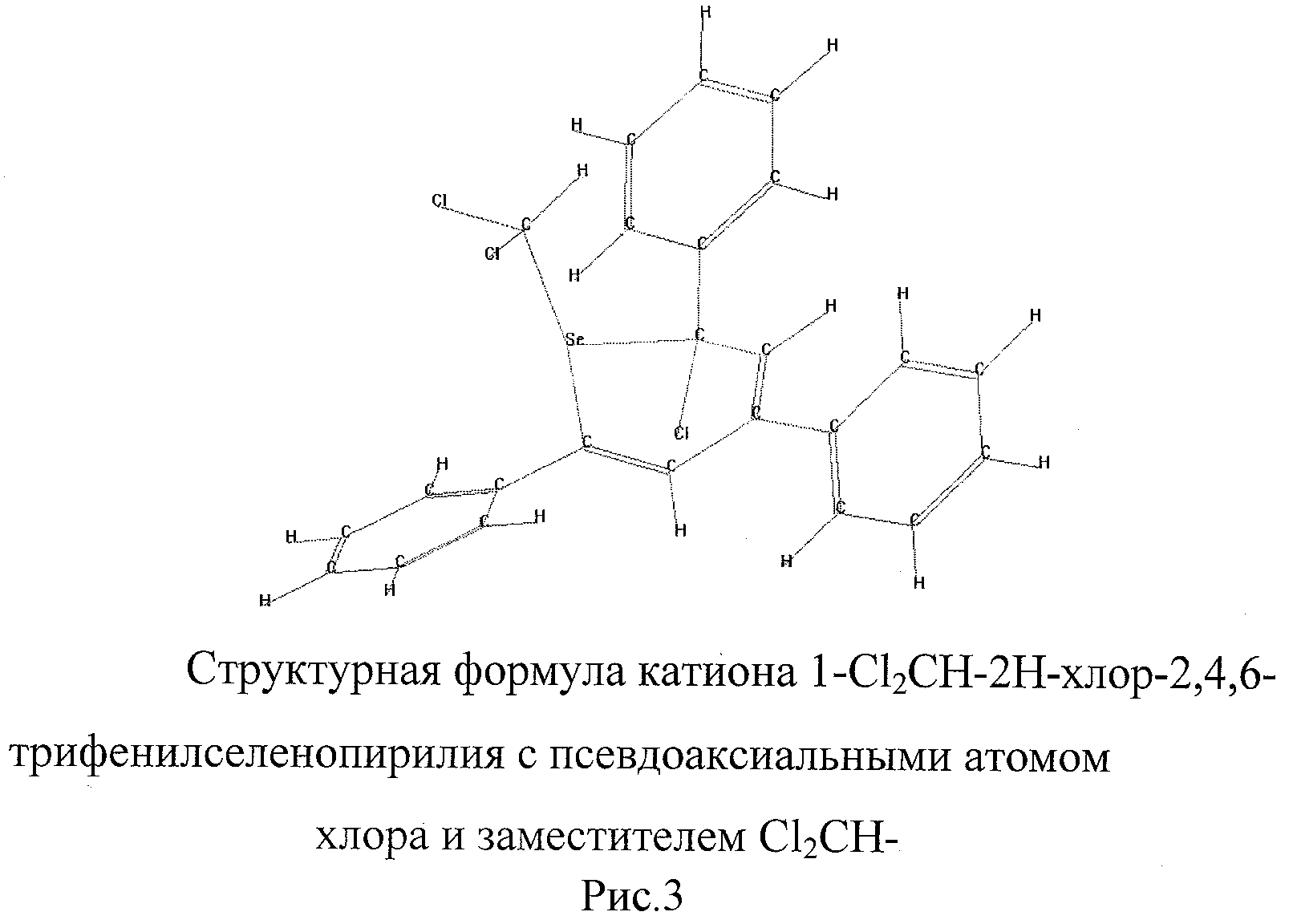Результат интеллектуальной деятельности: СПОСОБ ФОТОХИМИЧЕСКОГО ОКИСЛЕНИЯ О-ИЗОБУТИЛ-S-2-(N,N-ДИЭТИЛАМИНО)ЭТИЛМЕТИЛТИОФОСФОНАТА (ВЕЩЕСТВА ТИПА Vx) В ПРИСУТСТВИИ ПЕРХЛОРАТА 2,4,6-ТРИФЕНИЛСЕЛЕНОПИРИЛИЯ И ХЛОРОФОРМА
Вид РИД
Изобретение
I. Область применения.
В настоящее время согласно международным договоренностям запасы O-изобутил-S-2-(N,N-диэтиламино)этилметилтиолфосфоната (вещество типа Vx) должны быть уничтожены [Федеральный закон от 2 мая 1997 г.№76 ФЗ «Об уничтожении химического оружия»]. Однако данный токсичный химикат предполагается уничтожать гидролизом, который не может дать полноту детоксикации и часто в виде конечных продуктов приводит к высокотоксичным соединениям [Шантроха А.В., Гормай В.В., Холстов В.И., Данилкин В.И. идр. Пути решения проблемы уничтожения фосфор-органических веществ типа Ви-газов. // Российский химический журнал. - 1995. - XXXVIII, №2. - С.16-19], а использование агрессивных реактивов непригодно для дегазации электронного и другого оборудования, на которое в нештатных ситуациях может попасть данный токсикант. В соответствии с вышеуказанными требованиями должны быть дегазированы и корпуса боеприпасов [Васильев С. В., Жданов В.А., Завьялова Н.В., Холстов В.И. Анализ и сравнительная характеристика существующих подходов к оценке технологий и методов уничтожения химического оружия. // Информационный сборник ВИНИТИ «Федеральные и региональные проблемы уничтожения химического оружия», вып №2, Москва, 2000, С.66-77]. Кроме того, возможно использование данного соединения террористами, поэтому разработка метода его уничтожения без повреждения дегазируемых поверхностей актуальна в настоящее время.
II. Предшествующий уровень техники
Разработка процессов, обеспечивающих высокие степени конверсии Vx, ранее проводилась, в основном, в рамках проблем дегазации [Франке З. Химия отравляющих веществ. T.1. M.: Химия, 1973, 440 с.], которые подразумевали использование агрессивных сред (сильные окислители, концентрированные растворы щелочей и т.д.), приводящих к безвозвратной потере многих видов оборудования (например, электронного).
Ранее в США проводились эксперименты по высокотемпературному сжиганию Vx, которые показали неприемлемость данного метода для уничтожения указанного вида соединений [Дудаева Е.М. Уничтожение запасов химического оружия США: базовая и альтернативные технологии. // Информационный сборник ВИНИТИ «Федеральные и региональные проблемы уничтожения химического оружия», вып. №2, Москва, 2000, С.77-84].
Известны технологии уничтожения Vx при помощи рецептуры, содержащей изобутилат калия, изобутиловый спирт, N-метилпирролидон и е-капролактам [Исходные данные по разработке технической документации промышленной зоны объекта уничтожения химического оружия. - M., ГосНИИОХТ. - 1997]. Данная рецептура агрессивна, имеет высокую себестоимость и вызывает определенные трудности при хранении.
Весьма простая технология уничтожения веществ типа Vx - гидролиз, который не может дать полноту детоксикации и часто в виде конечных продуктов приводит к высокотоксичным соединениям. Данная реакция в значительной степени ускоряется в присутствии поверхностно-активных веществ. Так, в отсутствии ПАВ период полураспада Vx при рН=9,5-1100 мин., а в присутствии оксима 1-н-додецил-3-пиридинийиодида в концентрации 0,05 моль/л и рН=9,5~9 мин. [Шантроха А.В., Гормай В.В., Холстов В.И., Данилкин В.И. идр. Пути решения проблемы уничтожения фосфорорганических веществ типа Ви-газов. // Российский химический журнал. - 1995. - XXXVIII, №2. - С.16-19].
Одним из перспективных путей уничтожения отравляющих веществ по оценкам специалистов из США является окисление с УФ облучением [Дудаева Е.М. Уничтожение запасов химического оружия США: базовая и альтернативные технологии. // Информационный сборник ВИНИТИ «Федеральные и региональные проблемы уничтожения химиического оружия», вып. №2, Москва, 2000, С.77-84].
По мнению специалистов РФ [Демидюк В.В., Демидюк Н.В. Технологии уничтожения химического оружия. - М.: ЗАО «Агенство Ракурс», 2004] при разработке технологических процессов уничтожения химического оружия необходимо:
- исключить высокие температуры в зоне переработки отравляющих веществ;
- проводить детоксикацию отравляющих веществ в мягких строго контролируемых условиях;
- исключить переработку отравляющих веществ под давлением;
- проводить процесс уничтожения с ограниченным количеством отравляющих веществ, что исключает развитие неконтролируемой аварийной ситуации;
- проводить поштучное расснаряжение химических боеприпасов, обеспечивая блокировку процесса уничтожения отравляющих веществ на каждой стадии;
- применять только двухстадийный процесс уничтожения отравляющих веществ, в котором на первой стадии проводить детоксикацию отравляющих веществ и только потом, на второй стадии, утилизировать реакционную массу.
Известен метод фотохимического окисления иприта в присутствии четырехбромистого углерода, который на конечном этапе предполагает реакции с разрывом C-S-C связей и образованием смеси легкокипящих галогенированных углеводородов [Патент РФ №2288765, Б.И. - 2006. - №34].
При интенсивном облучении Vx (длина волны 278 нм) была обнаружена его незначительная деструкция с разрывом P-S и Р-O связей [Zuo, Guo-Min; Cheng, Zhen-Xing; Li, Guo-Wen; Wang, Lian-Yuan; Chen, Hong. Journal of Physical Chemistry A, 2005, 109(31), P.6912-6918 (Chem. Abst. Vol.143:295433].
Известен метод фотохимического окисления вещества типа Vx в присутствии четырехбромистого углерода, который предполагает его уничтожение с образованием малотоксичных продуктов реакции [Патент РФ №2355452, Бюлл. №14 за 2009 г. «Способ уничтожения O-изобутил-S-2-(N,N-диэтил-амино)этилметилтиолфосфоната (вещества типа Vx)»]. Недостатком данного способа является использование относительно дорогостоящего реагента - четырехбромистого углерода.
III. Сущность изобретения
Целью данного изобретения является создание нового метода уничтожения O-изобутил-S-2-(N,N-диэтиламино)-этилметилтиолфосфоната, который позволял бы полностью дегазировать поверхности, не нанося им существенного ущерба и был бы безопасен для персонала.
Поставленная цель достигается путем использования реакции фотохимического окисления O-изобутил-S-2-(N,N-диэтиламино)этилметилтиолфос-фоната (Vx) под действием излучения в видимой области спектра в присутствии перхлората 2,4,6-трифенилселенопирилия, которая вследствие нестабильности промежуточных аддуктов, сопровождается рядом спонтанных перегруппировок. В результате была получена сложная смесь продуктов деструкции исходного серусодержащего соединения. При этом, в силу своего строения, полученные продукты не обладают биологической активностью, характерной для фосфорорганических отравляющих веществ.
Фотодиссоциация хлороформа не происходит из-за того, что это соединение не имеет поглощения в данной области спектра.
В молекулярной электронике используются сенсибилизаторы с высоким квантовым выходом на основе солей халькогенопирилия [Tang Ching Wan. Multilayer organic photovoltaic elements // Res. Disel. - 1977. - Vol.162. - P.71-73.; Бабенко В.А., Дядюша Г.Г., Кудинова М.А., Малышев В.И., Сломинский Ю.Л., Сычев А.А., Толмачев А.И. Новые соединения для пассивных затворов лазеров ближнего ИК-диапазона // Квантовая электроника. - 1980. - Т.7. - С.1796-1802]. Однако используемые сенсибилизаторы являются весьма дорогостоящими, поэтому представлял интерес оценить использование в подобных целях триарилзамещенные соли селенопирилия, которые имеют поглощение в области 380-460 нм, являются легкодоступными реагентами и должны иметь высокий квантовый выход [А.С.1816762 СССР. - Бюл. №19. 1993. c.111. A.C. 1167184 СССР. Бюл. №26. С.85. 1985.; Патент РФ №2276150. Бюлл. №13 за 2006 г.; Патент РФ №2367658. Бюлл. №26 за 2009 г.].
В наших исследованиях показано, что перспективным соединением в данном классе веществ является перхлорат 2,4,6-трифенилселенопирилия, который используется многими отечественными и зарубежными исследователями при изучении теоретических и практических вопросов в химии [Murphy, P.J. Selenopyrylium and benzoselenopyrylium salts // Science of Synthesis. - 2003. - Vol.14. - P.817-854]. Это соединение и было использовано в наших экспериментах при изучении фотохимической реакции фосфорилтиохолинов.
При проведении экспериментов были записаны спектры данной соли в видимой и УФ-области. В этаноле для данного соединения λmax=392 нм, а в хлороформе λmax=388 нм. Указанное свойство свидетельствует о том, что при растворении исследуемого соединения в хлороформе могут происходить некоторые процессы, влияющие на спектр поглощения.
Для приведенных длин волн энергия кванта равна:
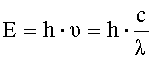 ,
,
а энергия рассчитанная на моль вещества составляет:
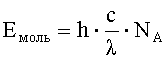 ,
,
где h - постоянная Планка, Дж·с;
NA - число Авогадро, моль-1;
с - скорость света, м/с;
λ - длина волны, м.
Известно, что данный перхлорат 2,4,6-трифенилселенопирилия плохо растворим в четыреххлористом углероде, однако хорошо растворим в хлороформе, поэтому из этих двух наиболее доступных субстратов был выбран последний.
Подставим известные значения в выражение и рассчитаем энергию, которую может получить 1 моль хлороформа при облучении видимым светом:
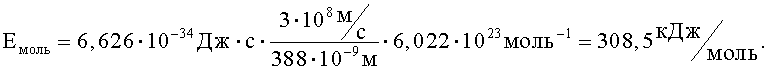
Энергия диссоциации хлороформа на свободные радикалы равна ~ 320 кДж/моль [Рабинович В.А., Хавин З.Я. Краткий химический справочник. - Л.: Химия, 1978. - 392 с.]. Однако хлороформ при ассоциации с солью селенопирилия может давать дополнительный выигрыш энергии, поэтому было решено провести соответствующие квантово-химические расчеты.
Полуэмпирическим методом квантовой химии РМ3 проведено исследование возможности протекания реакции катиона 2,4,6-трифенилселенопирилия с хлороформом в газовой фазе в стандартных условиях. Расчеты проводили по программе из пакета Hyper Chem 7.0 с полной оптимизацией геометрии. При квантово-химических расчетах задавали условие, чтобы норма градиента не превышала 0,05 ккал/(моль.·А) (0,2092 кДж/(моль·A)).
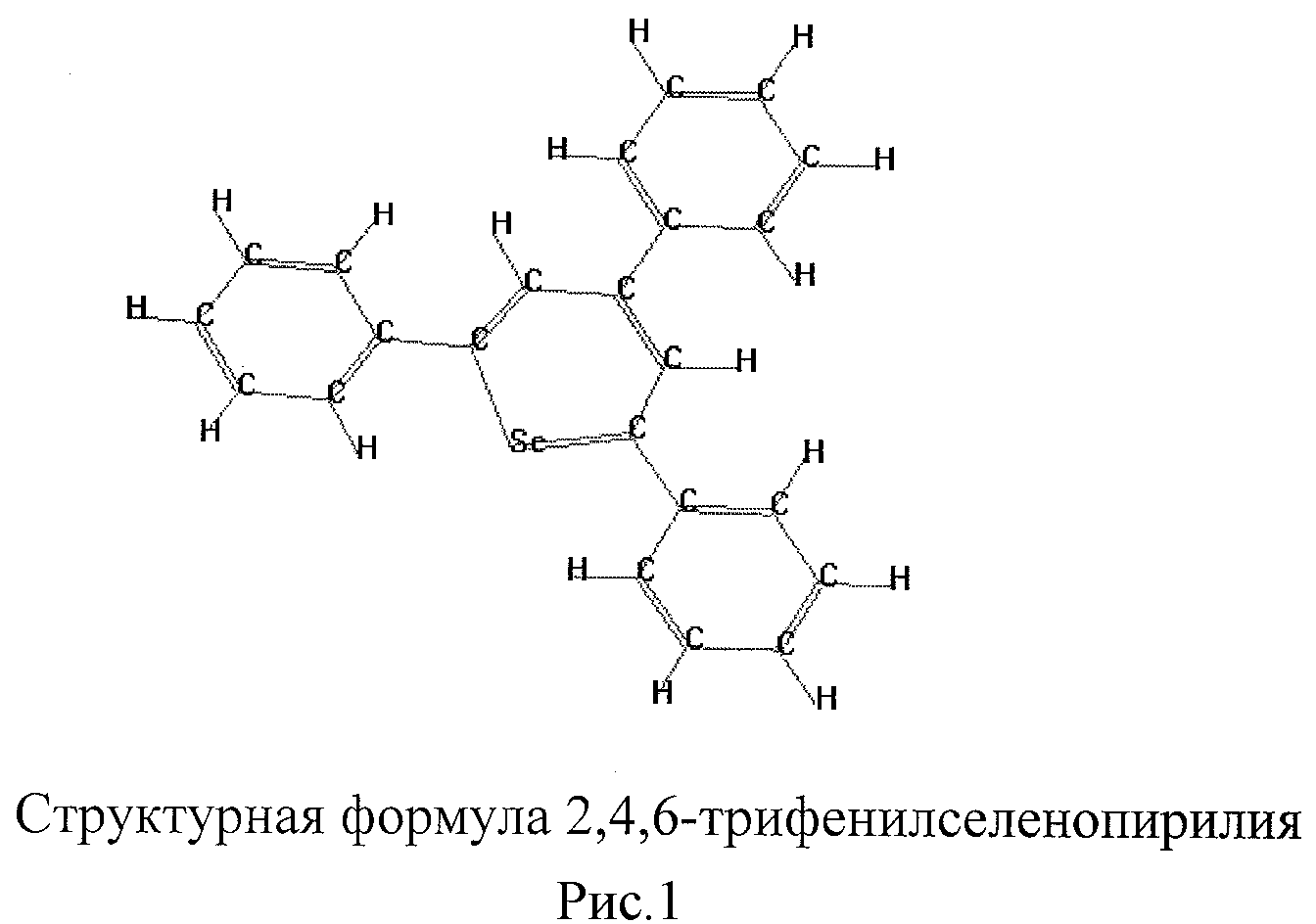
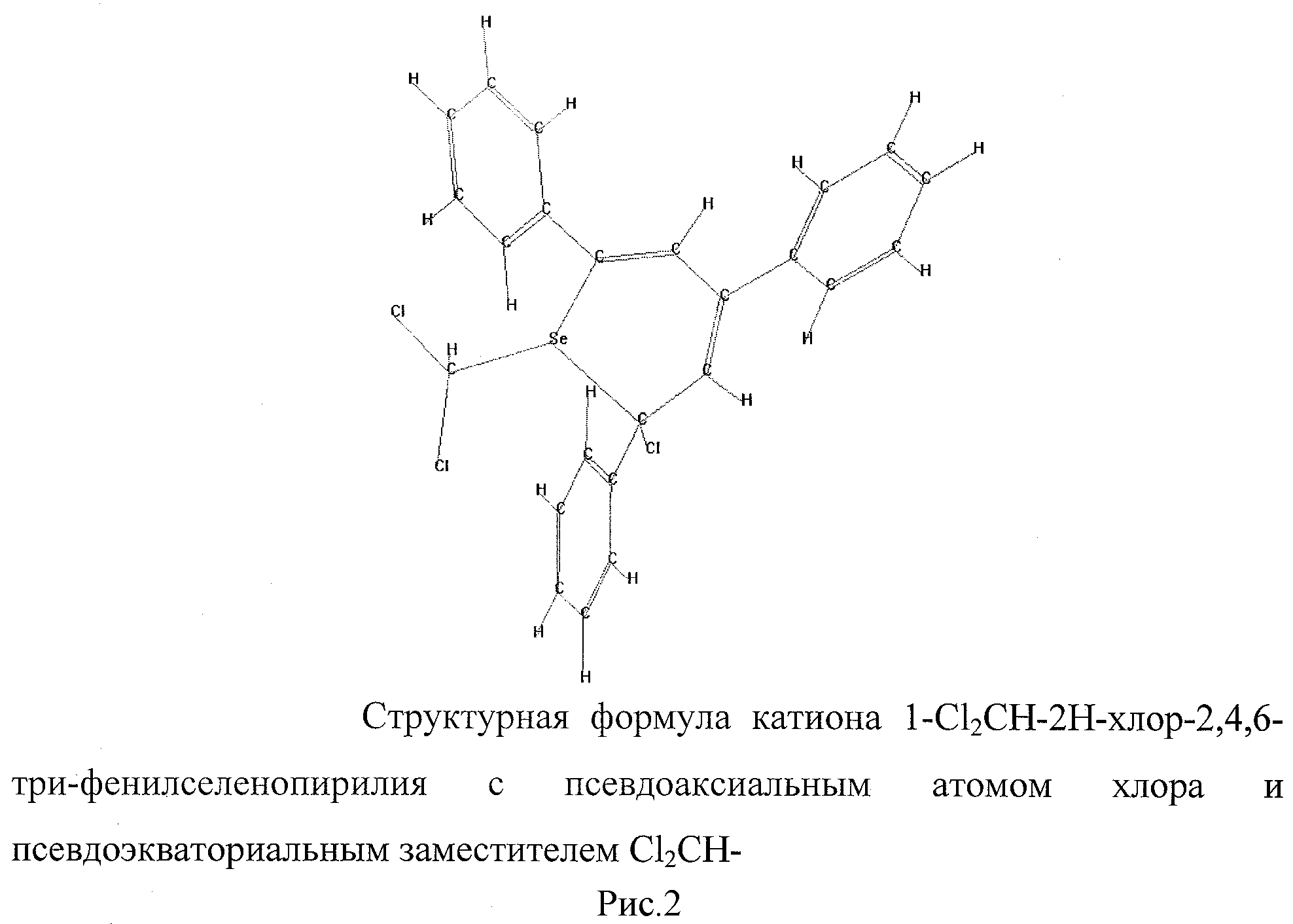
Рассчитаны показатели теплоты образования катиона 2,4,6-трифенилселенопирилия (рисунок 1), хлороформа, возможных продуктов реакции - катионов 1-Cl2CH-2Н-хлор-2,4,6-трифенилселенопирилия с псевдоаксиальным атомом хлора и псевдоэкваториальным заместителем Cl2CH (рисунок 2) и псевдоаксиальными атомом хлора и заместителем Cl2CH (рисунок 3.)
Рассчитаны тепловые эффекты реакций взаимодействия изомеров катиона 2,4,6-трифенилселенопирилия и хлороформа. Показано, что эти реакции протекают с отрицательными тепловыми эффектами.
Более энергетически выгодным процессом является образование катиона 1-Cl2CH-2Н-хлор-2,4,6-трифенилселенопирилия с псевдоаксиальными атомом хлора и заместителем Cl2CH-, тепловой эффект которого составляет -9,72 ккал/моль (-40,67 кДж/моль) по сравнению со значением - 2,70 ккал/моль (-11,30 кДж/моль) для другого.
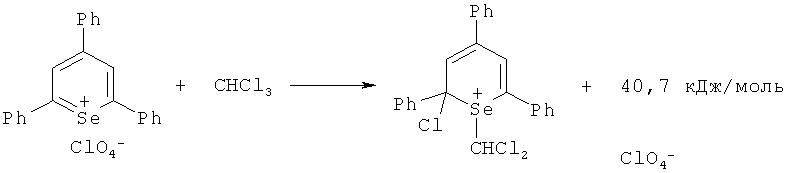
В результате установлено, что при облучении хлороформенного раствора перхлората 2,4,6-трифенилселенопирилия общая энергия, которая будет выделяться в реакционную среду, равна Еобщ=349,2 кДж/моль. Следовательно, при использовании в качестве сенсибилизатора перхлората 2,4,6-трифенилселенопирилия возможен распад молекулы хлороформа на свободные радикалы (учитывая брутто-эффект).
Таким образом, гомолитический распад молекулы хлороформа можно представить в виде следующей схемы:
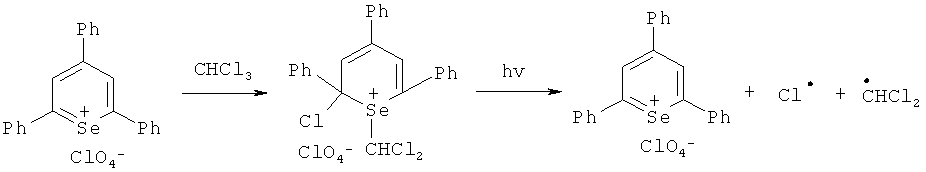
Квантово-химические расчеты подтвердили наши предположения, поэтому было решено провести эксперименты по фотохимическому окислению вещества типа Vx в присутствии перхлората 2,4,6-трифенилселенопирилия и хлороформа с использованием излучения в видимой области спектра.
Перед началом исследования был проведен контрольный эксперимент, в котором раствор вещества типа Vx (содержание массовой доли основного вещества 88%) и соли селенопирилия в хлороформе не подвергались электромагнитному облучению в видимой области спектра. В результате установлено, что деструкция вещества типа Vx в течение 7 суток протекает на 14%.
В результате проведенных экспериментов было установлено, что вследствие фотохимического окисления вещества типа Vx в присутствии перхлората 2,4,6-трифенилселенопирилия в среде хлороформа, он подвергается практически полной деструкции (в пределах детектирования).
Первую серию экспериментов проводили следующим образом:
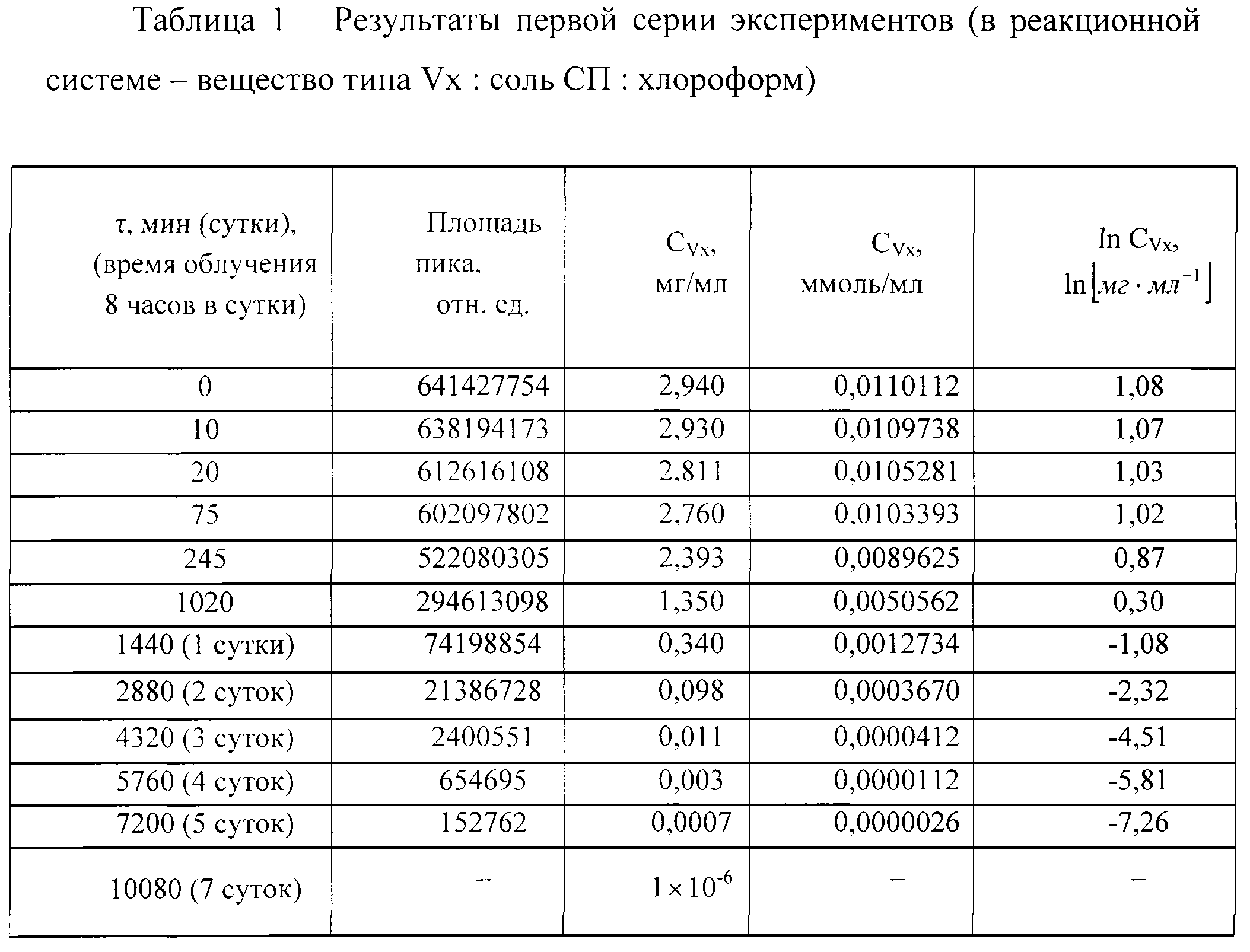
раствор вещества типа Vx (содержание массовой доли основного вещества 88%) и перхлората 2,4,6-трифенилселенопирилия в мольном соотношении 1:0,1 в хлороформе помещали в реактор из стекла, снабженный магнитной мешалкой, при комнатной температуре. Реакционную смесь подвергали воздействию видимым светом (лампа накаливания, длина волны 350-1000 нм), проводя регулярные отборы проб. Анализ проводили методом ГХ с масс-селективным детектированием. Реакция закончилась практически полной деструкцией вещества типа Vx (в пределах детектирования) с образованием сложной смеси продуктов деструкции (таблица 1).
Представленные в таблице 1 данные свидетельствуют о том, что деструкция вещества типа Vx (в пределах детектирования), содержащего массовую долю основного вещества 88%, под действием электромагнитного излучения в видимой области спектра в присутствии перхлората 2,4,6-трифенилселенопирилия в мольном соотношении 1:0,1 в хлороформе протекает в течение 5-7 суток.
Во второй серии экспериментов было использовано ОВ типа Vx (содержание массовой доли основного вещества 81%), включающее до 15% меркаптопроизводных. Меркаптопроизводные органические соединения являются хорошей «ловушкой» свободных радикалов, поэтому длина цепи в изучаемой реакции должна в значительной степени уменьшаться из-за присутствия большого количества меркаптанов. Известно, что Меркаптопроизводные способны вступать в реакции с бромпроизводными галогеноводородными соединениями.
Эксперимент проводили аналогично первому в тех же соотношениях и условиях. Установлено, что реакция деструкции вещества типа Vx в определенный момент времени начала протекать медленнее из-за присутствия в смеси меркаптопроизводных органических соединений. Реакция закончилась практически полной деструкцией вещества типа Vx (в пределах детектирования) с образованием сложной смеси продуктов деструкции (таблица 2).
Представленные в таблице 2 данные показывают, что деструкция вещества типа Vx (в пределах детектирования), содержащего массовую долю основного вещества 81%, под действием электромагнитного излучения в видимой области спектра в присутствии перхлората 2,4,6-трифенилселенопирилия в мольном соотношении 1:0,1 в хлороформе протекает в течение 5-7 суток.
В подтверждение предложенной ранее схемы деструкции вещества типа Vx мы заменили растворитель хлороформ на этанол.
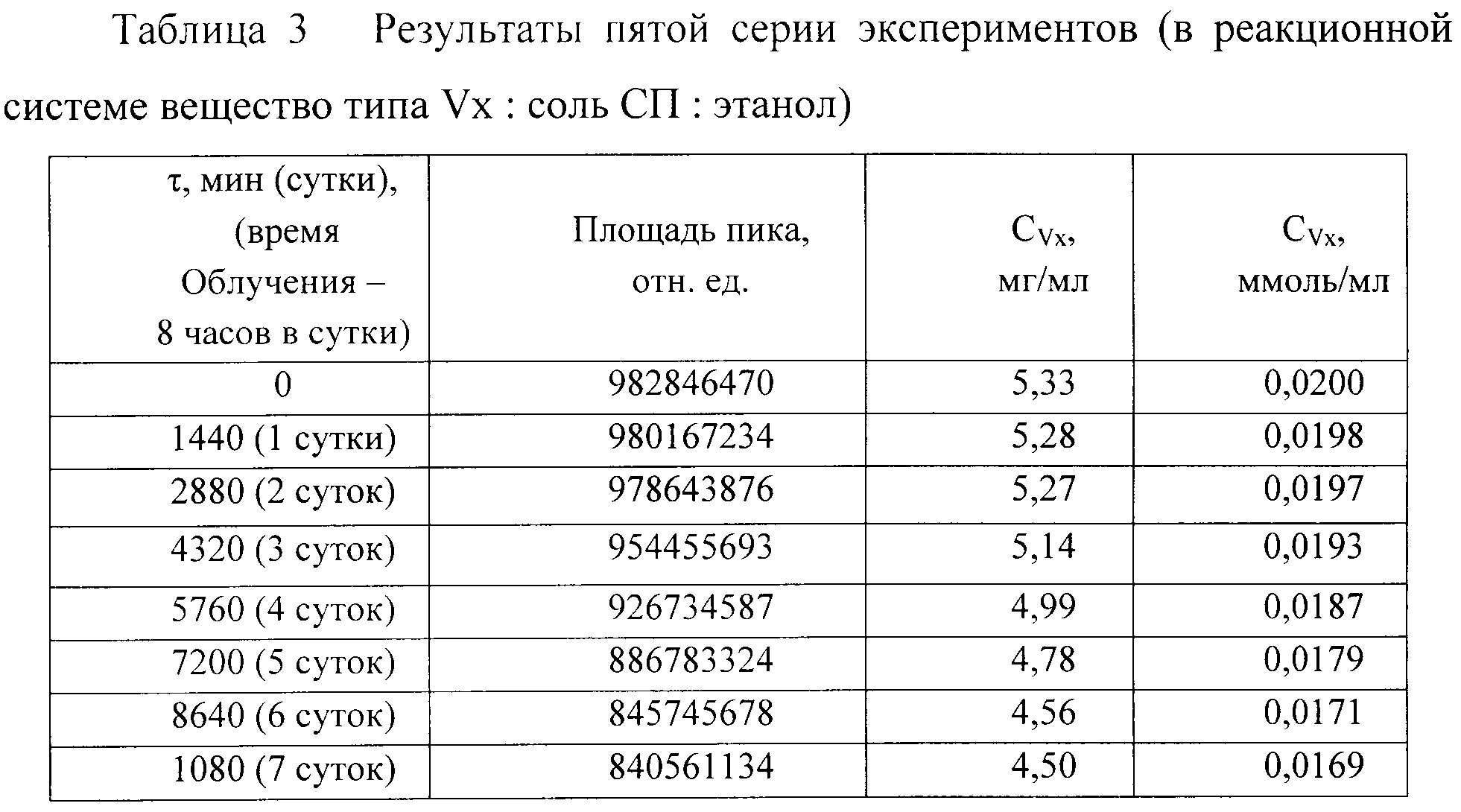
Эксперимент проводили следующим образом: раствор вещества типа Vx (содержание массовой доли основного вещества типа Vx 88%) и перхлората 2,4,6-трифенилселенопирилия в мольном соотношении 1:0,1 в этаноле помещали в реактор из стекла, снабженный магнитной мешалкой, при комнатной температуре. Реакционную смесь подвергали воздействию видимым светом (лампа накаливания, длина волны 350-1000 нм), проводя регулярные отборы проб. Анализ проводили методом ГХ с масс-селективным детектированием. По истечении 7 суток реакция деструкции вещества типа Vx прошла на 16% с образованием сложной смеси продуктов деструкции (таблица 5), что доказывает наше предположение о поведении хлороформа и соли селенопирилия в реакционной среде.
Данные таблицы 3 показывают, что деструкция вещества типа Vx прошла на 16%, под действием электромагнитного излучения в видимой области спектра в присутствии перхлората 2,4,6-трифенилселенопирилия, в мольном соотношении 1:0,1 в этаноле.
Таким образом, полученные результаты по изучению фотохимической реакции O-изобутил-S-2-(N,N-диэтиламино)этилметилтиолфосфоната в присутствии солей селенопирилия под воздействием электромагнитного излучения в видимой области спектра доказывают, что соль селенопирилия является сенсибилизатором и катализатором реакции фотохимической деструкции фосфорилтиохолинов.