СИНХРОНИЗИРОВАННАЯ С ДЫХАТЕЛЬНЫМИ ДВИЖЕНИЯМИ ОЦЕНКА ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ С ПРИМЕНЕНИЕМ УЛЬТРАЗВУКОВЫХ КОНТРАСТНЫХ ВЕЩЕСТВ
Вид РИД
Изобретение
По настоящей заявке испрашивается приоритет по предварительной заявке США под серийным номером 61/022888, поданной 23 января 2008 г., которая включена в настоящее описание путем ссылки.
Данное изобретение относится к ультразвуковым системам диагностической визуализации и, в частности, к использованию ультразвуковых систем диагностической визуализации с целью оценки процесса протекания лечения опухолей.
В международной патентной публикации WO 2006/090309 (Bruce и др.) описана технология ультразвуковой визуализации для обнаружения патологических изменений в печени с использованием ультразвукового контрастного вещества. В организм вводится болюс контрастного вещества и определяется время прибытия контрастного вещества в печень. Когда болюс контрастного вещества проходит по кровеносным сосудам организма и появляется в определенном органе или месте в организме, увеличение контраста на изображениях называют «поступлением» контрастного вещества. Когда инфузия контрастного вещества стабилизируется в этом месте в организме, а затем снижается, поскольку контрастное вещество уносится из данного места током крови, такое снижение называют «вымыванием» контрастного вещества. В вышеупомянутой патентной публикации авторы изобретения используют тот факт, что кровоток, поступающий в печень, имеет два источника: печеночную артерию и воротную вену. Поскольку кровоток на первой артериальной фазе тока крови осуществляет перфузию HCC (гепато-целлюлярной карциномы) и метастаза в печени первым, авторы изобретения идентифицируют подобные патологические изменения путем определения времени прибытия контрастного вещества в печень в течение артериальной и поздней портальной фазы кровотока. Область с ранним поступлением контрастного вещества в печень может служить симптомом патологического изменения.
Когда патологическое изменение или метастаз выявлены с помощью этого и/или иного средства, врач обычно выписывает схему лечения. Лечение может включать в себя, например, гипер-/гипотермическую терапию, цитотоксическую химиотерапию или применение антиангиогенных веществ. Лечение обычно проводится не за одну процедуру, а за несколько процедур в течение недель или месяцев. При проведении каждой терапевтической процедуры врачу обычно желательно оценить процесс протекания лечения, чтобы определить его эффективность для пациента. Патологическое изменение или метастаз может быть визуализирован(о) в диагностических целях, чтобы видеть, например, произошло ли сокращение их размера. Но часто процесс протекания лечения проявляется медленно, и со времени предыдущей процедуры проявляются лишь малые изменения патологического изменения или метастаза. В этих случаях желательно оценить процесс протекания лечения количественно, путем измерения определенных характеристик опухоли. Одним из таких количественных показателей является снижение ангиогенеза опухоли. По мере того как патологическое изменение или метастаз уменьшаются в размере с некрозом их клеток, микроваскуляторное русло, развитое для питания патологического изменения, будет обеспечивать меньшую подачу крови к патологическому изменению и может само начать сокращаться в размере. Один из количественных подходов заключается в оценке такого снижения ангиогенеза, снижения деятельности микроваскуляторного русла патологического изменения. Желательно, чтобы такие количественные измерения обладали повторяемостью и не зависели от изменений в проведении процедур визуализации от одной к другой, например изменений во введении болюса, функционального состояния сердца пациента, наладочных параметров ультразвуковой установки, которые могут разниться от одного дня проведения обследования к другому. Устранение влияния таких вариаций обеспечит возможность сравнения результатов измерений от одной терапевтической процедуры к другой. Задача настоящего изобретения заключается в создании новых и более совершенных технологий оценки ангиогенеза в патологическом изменении или метастазе в период лечения опухоли.
Согласно принципам настоящего изобретения формируются и используются кривые времени-интенсивности поступления и вымывания ультразвуковых контрастных веществ в целях количественного определения ангиогенеза опухоли по результатам лечения. Изображение патологического изменения или метастаза получают с помощью ультразвуковой системы визуализации, при этом осуществляется непрерывная визуализация патологии, по мере того как контрастное вещество поступает в ткань или обследуемый орган и вымывается из них. Для точного измерения данного процесса требуется стабильное получение ультразвуковых сигналов из одного и того же местоположения в метастазе, по мере того как контрастное вещество поступает и вымывается, так чтобы информация по сигналам для расчета кривой времени-интенсивности постоянно исходила из одной и той же точки патологического изменения. Согласно первому аспекту настоящего изобретения влияние дыхательных движений устраняется путем синхронизации с дыхательными движениями во время сбора данных для построения кривой времени-интенсивности. Предпочтительная технология синхронизации с дыхательными движениями выполняется путем анализа изображения, при этом наличие или отсутствие анатомического ориентира на изображении, такого как диафрагма, используется для решения того, использовать или не использовать изображение для обработки кривой времени-интенсивности.
Согласно следующему аспекту настоящего изобретения кривая времени-интенсивности строится как для ультразвуковых данных, полученных от опухоли, так и для ультразвуковых данных, полученных от нормальной ткани. Параметр времени поступления (WIT) рассчитывается для каждой кривой времени-интенсивности. Из двух параметров формируется отношение времен поступления (WITR), которое снижает вариативность количественной оценки времени поступления вследствие таких факторов, как различия болюсов, функционального состояния сердца, а также наладочных параметров ультразвуковой системы. Таким образом, WITR предоставляет точный и поддающийся сравнению индикатор процесса протекания лечения.
Согласно еще одному аспекту настоящего изобретения кривые времени-интенсивности для опухоли и нормальной ткани вычитаются одна из другой для получения разностной кривой времени-интенсивности. Форма разностной кривой времени-интенсивности и ее изменение во времени являются еще одним индикатором процесса протекания лечения.
На чертежах:
на фиг.1 в виде блок-схемы показана ультразвуковая система диагностической визуализации, построенная согласно принципам настоящего изобретения;
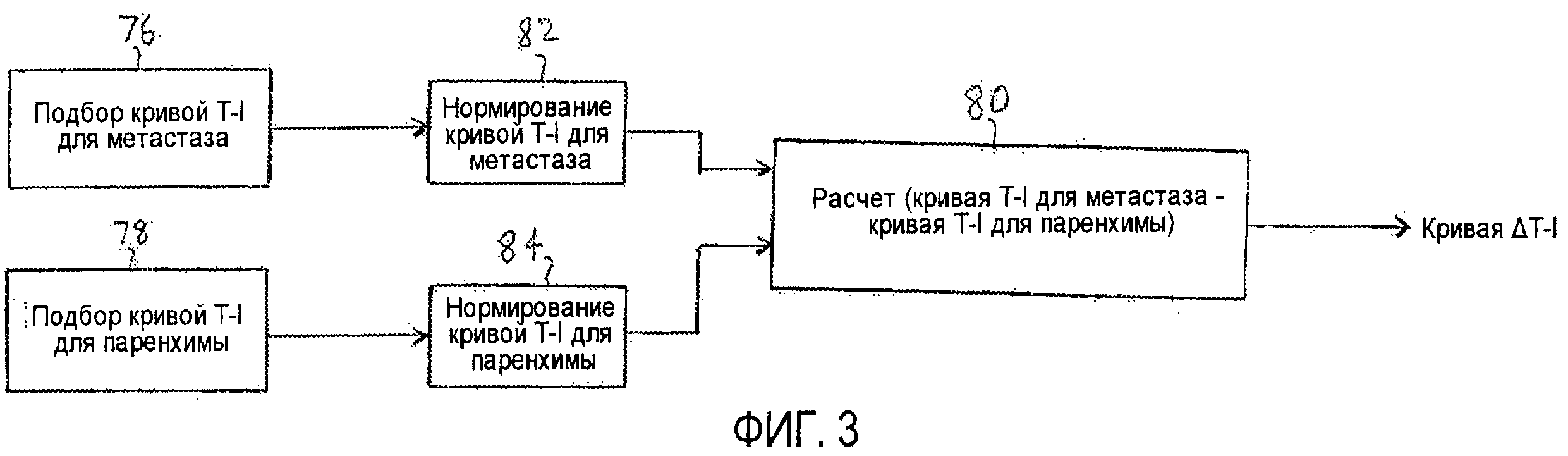
на фиг.2 и 3 подробно показана работа qLab-процессора, представленного на фиг.1, согласно принципам настоящего изобретения;
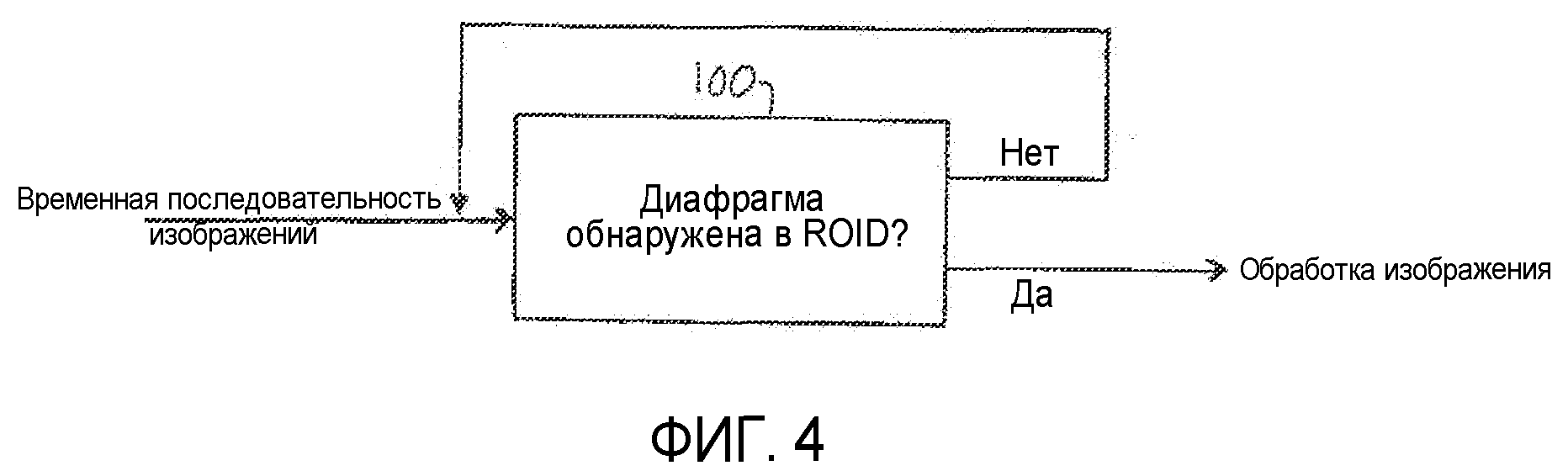
на фиг.4 показана синхронизация с дыхательными движениями посредством обработки изображения согласно принципам настоящего изобретения;
на фиг.5 показаны области интереса для кривых времени-интенсивности согласно настоящему изобретению на изображении печени, полученном в течение артериальной фазы;
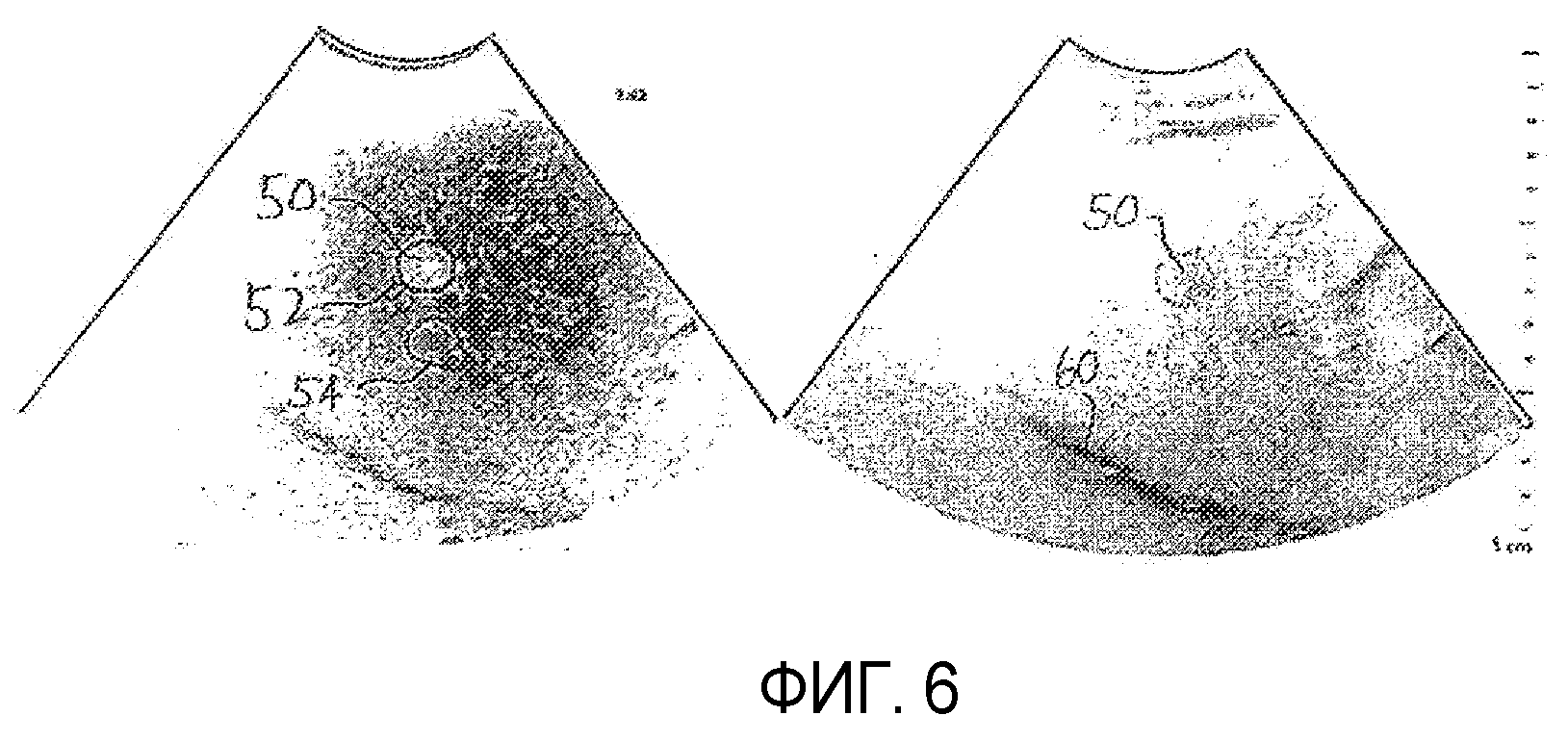
на фиг.6 показаны области интереса для кривых времени-интенсивности согласно настоящему изобретению на изображении печени, полученном в течение поздней портальной фазы;
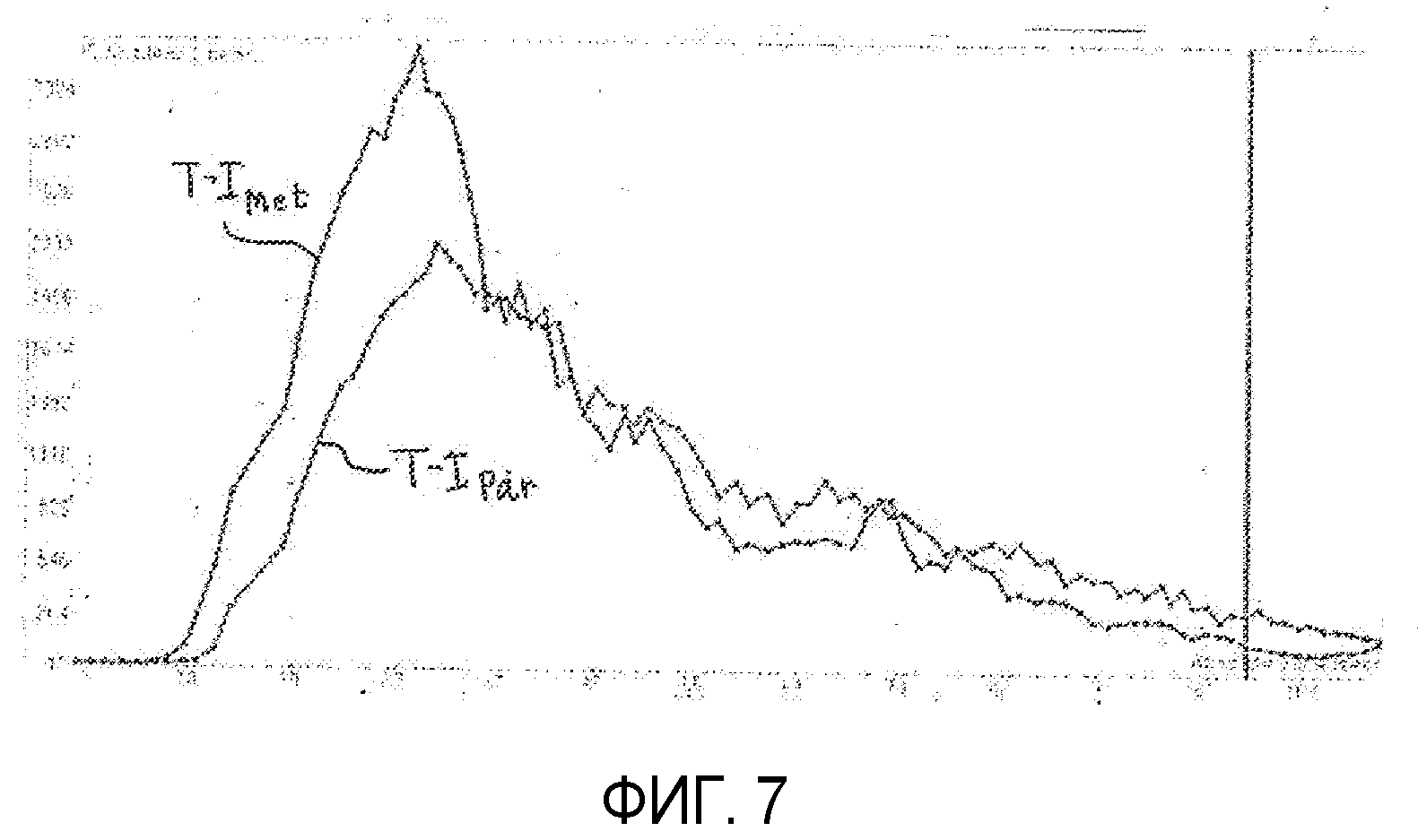
на фиг.7 показаны кривые времени-интенсивности для метастатического поражения и нормальной паренхимы;
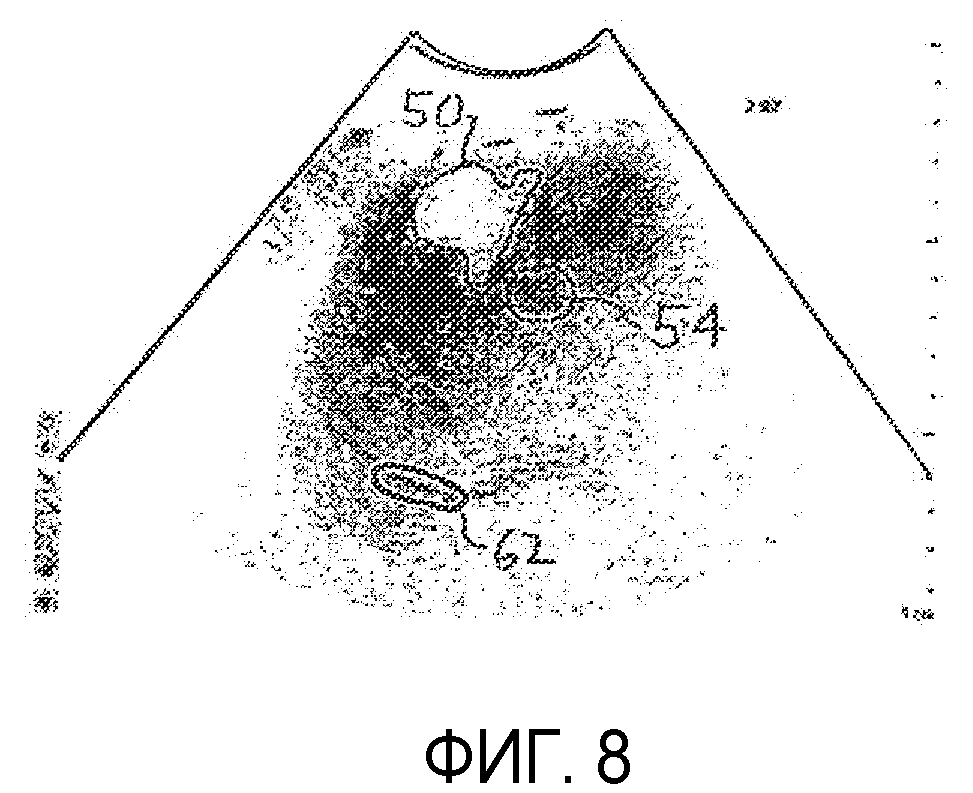
на фиг.8 показана идентификация диафрагмы на ультразвуковом изображении для синхронизации с дыхательными движениями согласно принципам настоящего изобретения;
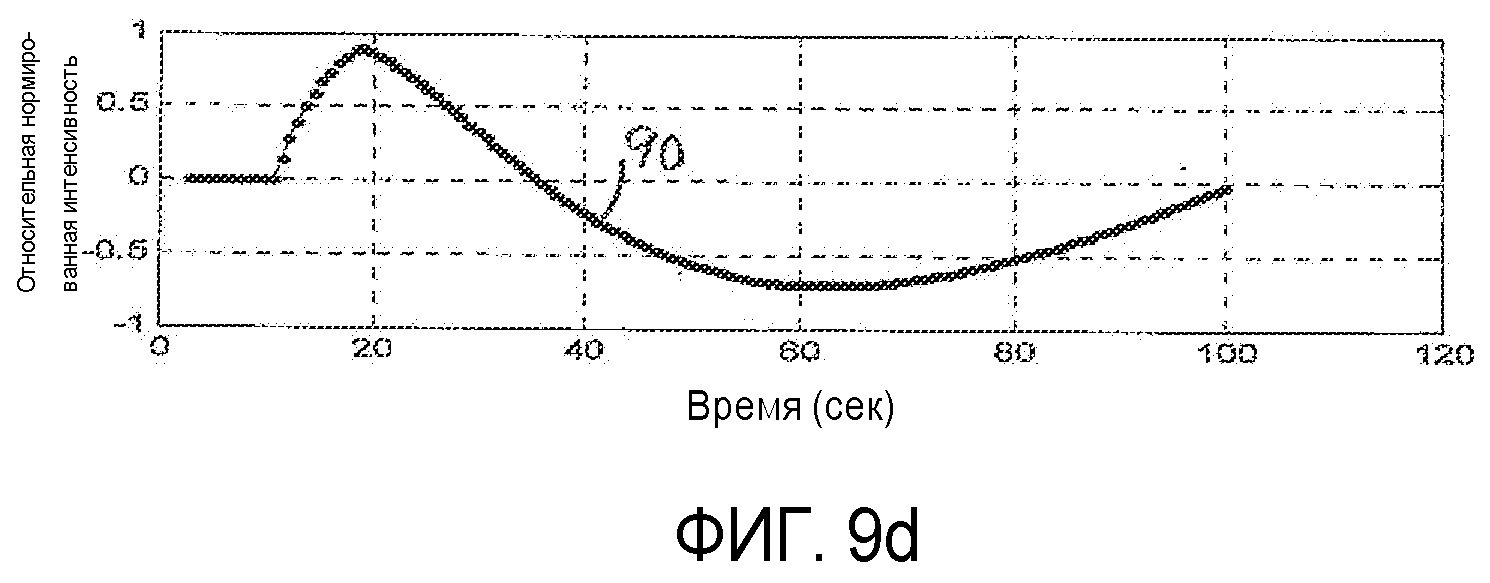
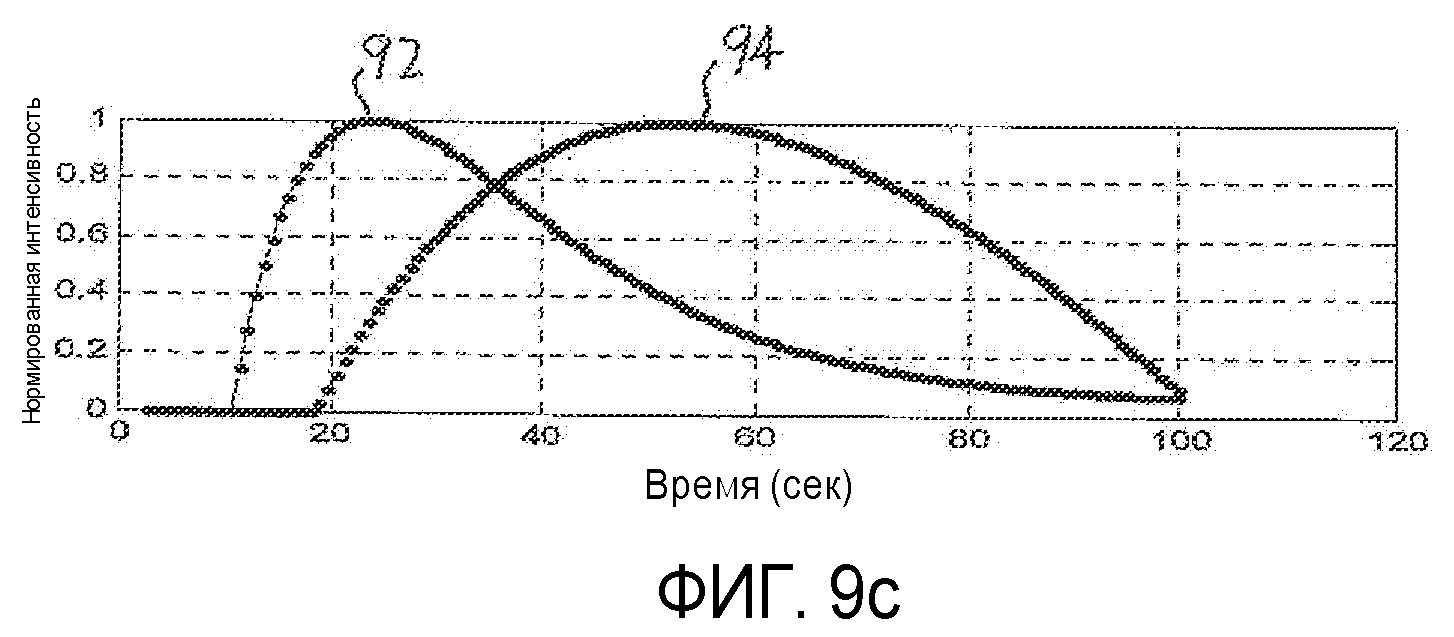
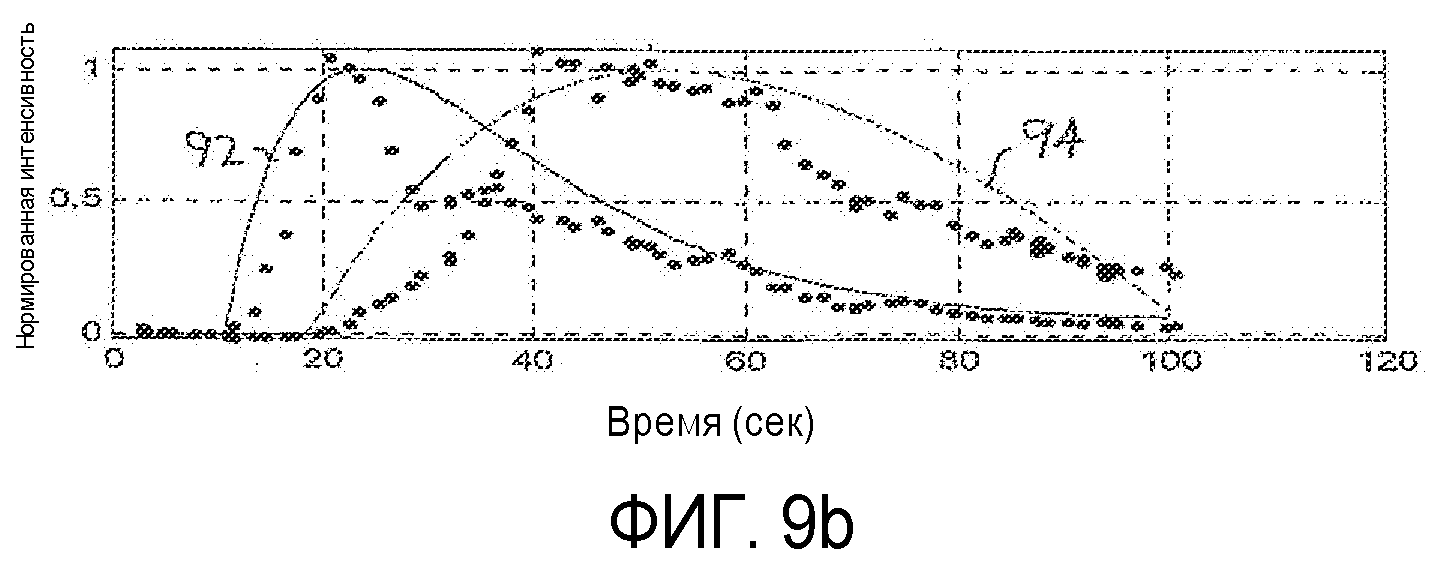
на фиг.9а-9d показано построение и вычитание кривых времени-интенсивности для образования разностной кривой времени-интенсивности согласно принципам настоящего изобретения;
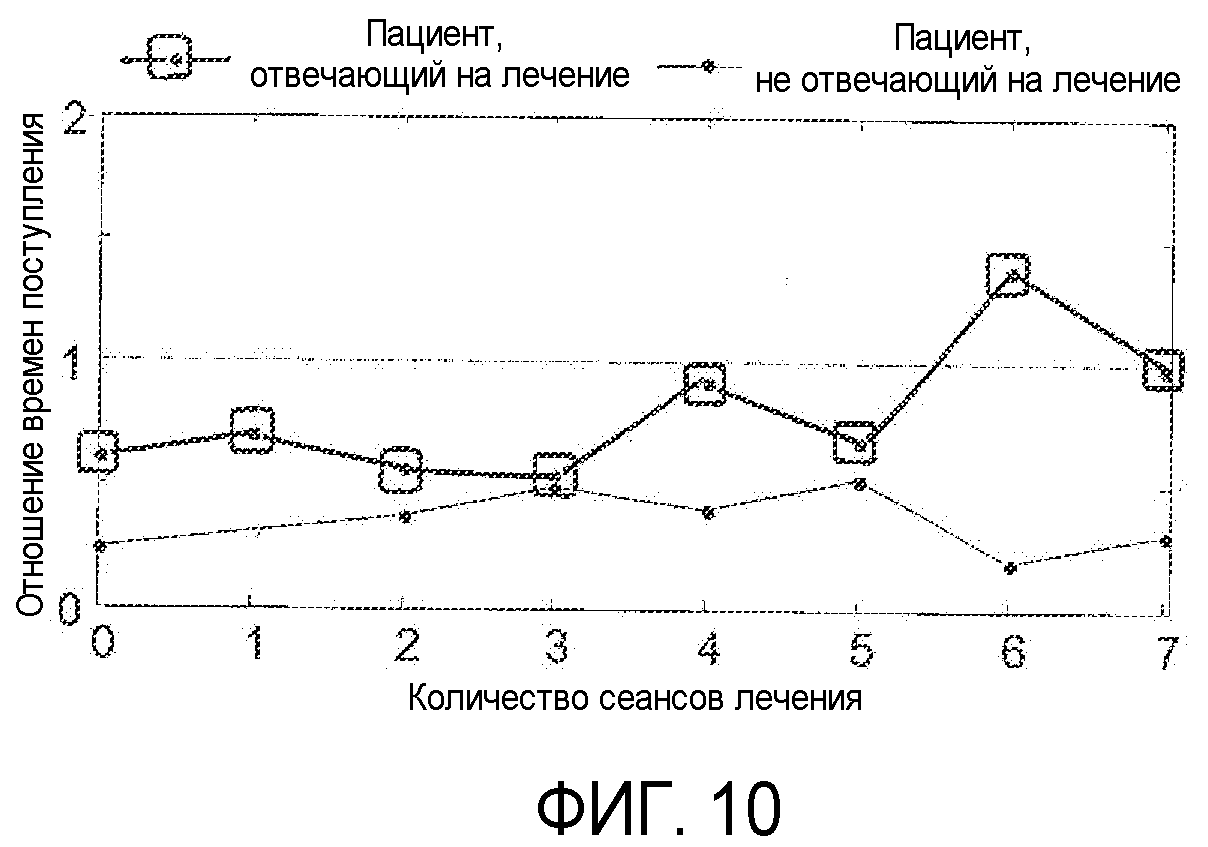
на фиг.10 показаны клинические результаты оценки процесса протекания лечения согласно принципам настоящего изобретения.
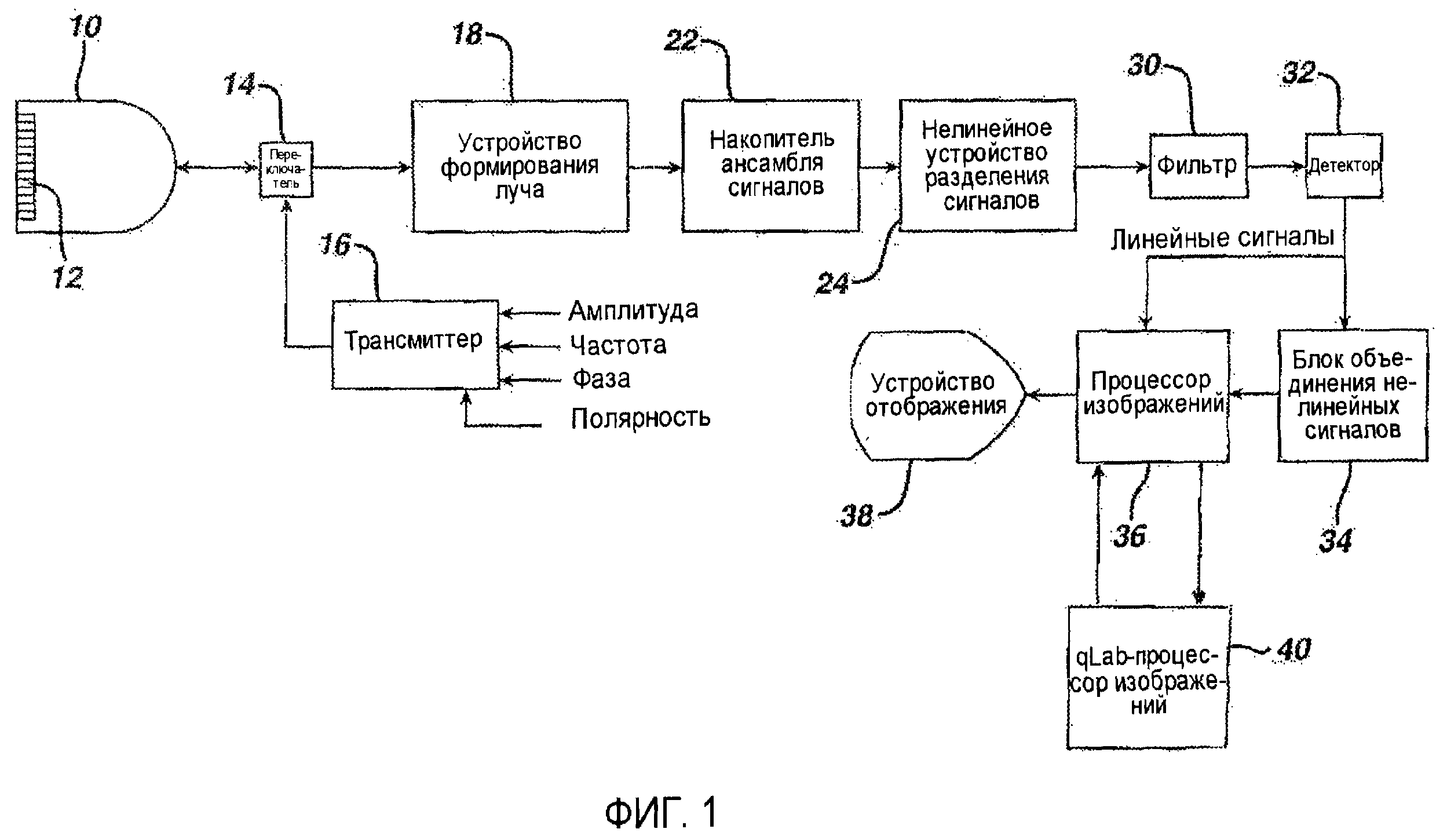
Согласно фиг.1 ультразвуковая система, построенная согласно принципам настоящего изобретения, показана в виде блок-схемы. Данная система функционирует посредством сканирования двух- или трехмерной области организма, визуализируемой с помощью прохождения ультразвуковых лучей. По мере того как каждый луч проходит по своей регулируемой траектории через тело, он дает эхо-сигналы с линейной и нелинейной (основной частотой и частотой гармоники) составляющими, соответствующими переданным частотным составляющим. Переданные сигналы модулируются посредством нелинейного отклика микропузырьков контрастного вещества, находящихся на пути луча, что, таким образом, приводит к генерированию эхо-сигналов с гармоническими составляющими.
В ультразвуковой системе на фиг.1 используется трансмиттер 16, который передает волны или импульсы с выбранными модуляционными характеристиками в требуемом направлении луча с целью возврата гармонических составляющих эхо-сигнала от рассеивающих объектов в организме. Трансмиттер воспринимает ряд параметров управления, определяющих характеристики передаваемых лучей, в том числе частотные составляющие передаваемого луча, их относительные интенсивности и амплитуды, а также фазу и полярность передаваемых сигналов. Трансмиттер соединен посредством переключателя 14 передачи/приема с элементами матричного преобразователя 12 ультразвукового зонда 10. Матричный преобразователь может представлять собой одномерную матрицу для плоской (двумерной) визуализации или двумерную матрицу для двумерной или объемной (трехмерной) визуализации.
Матричный преобразователь 12 принимает эхо-сигналы из организма, содержащие основную (линейную) и гармонические (нелинейные) частотные составляющие, находящиеся в полосе пропускания преобразователя. Эти эхо-сигналы поступают с помощью переключателя 14 в устройство 18 формирования луча, которое осуществляет соответствующую задержку эхо-сигналов от различных элементов преобразователя, а затем объединяет их для образования последовательности линейного и гармонических сигналов вдоль луча от меньших до больших глубин. Предпочтительно устройство формирования луча представляет собой цифровое устройство формирования луча, работающее на оцифрованных эхо-сигналах для формирования последовательности дискретных когерентных цифровых эхо-сигналов от глубин ближней зоны до глубин дальней зоны изображения. Устройство формирования луча может представлять собой многоканальное устройство формирования луча, которое формирует две или более последовательности эхо-сигналов вдоль множества пространственно раздельных принимающих линий сканирования под действием одного передаваемого луча, что особенно ценно для 3D-визуализации. Обработанные устройством формирования луча эхо-сигналы поступают в накопитель 22 ансамбля сигналов.
В ультразвуковой системе на фиг.1 множество волн или импульсов передается в каждом направлении луча с использованием различных способов модуляции, что приводит к приему множества эхо-сигналов для каждой сканируемой точки в поле изображения. Эхо-сигналы, соответствующие общему пространственному местоположению, в настоящем описании будут называться ансамблем эхо-сигналов, и хранятся в накопителе 22 ансамбля сигналов, из которого они могут выводиться и обрабатываться совместно. Эхо-сигналы ансамбля объединяются различным образом с помощью нелинейного устройства 24 разделения сигналов для формирования требуемых нелинейных или гармонических сигналов. Например, два импульса с различной фазовой или полярной модуляцией могут быть переданы в каждую точку поля изображения. Когда эхо-сигналы от этих двух импульсов принимаются ультразвуковой системой и аддитивно объединяются, различие в модуляции приводит к тому, что основные частотные составляющие эхо-сигналов исчезают, а гармонические составляющие усиливают друг друга. Это позволяет выделить гармонические составляющие эхо-сигналов. Наоборот, когда два эхо-сигнала вычитаются один из другого, основные частотные составляющие усиливаются, а гармонические составляющие исчезают. Это позволяет выделить основные частоты для построения стандартного изображения в B-режиме. Такую модуляцию называют «импульсной инверсией», и она может выполняться с помощью фазовой, полярной или амплитудной модуляции, как описано в патентах США 5706819 (Hwang и др.), 5951478 (Hwang и др.), а также 5577505 (Brock Fisher др.).
Разделенные сигналы фильтруются с помощью фильтра 30 для дальнейшего устранения нежелательных частотных составляющих, а затем подвергаются детектированию в B-режиме или допплеровскому детектированию с помощью детектора 32. Детектированные сигналы поступают в блок 34 объединения нелинейных сигналов для уменьшения содержания спекл-структур изображения. Затем сигналы обрабатываются для формирования двумерного, трехмерного, спектрального, параметрического или иного требуемого изображения в процессоре 36 изображений, и далее изображение выводится на устройство 38 отображения. Детектированные основные (линейные) сигналы, которые не требуют обработки по уменьшению спекл-структур, поступают непосредственно на процессор 36 изображений для формирования изображения и его отображения.
Согласно принципам настоящего изобретения ультразвуковые данные изображений также поступают в qLab-процессор 40 изображений для построения кривых времени-интенсивности и характеристик поступления и вымывания контрастного вещества. Кривые времени-интенсивности и характеристики, выданные qLab-процессором, снова поступают в процессор изображений, где они могут воспроизводиться в цифровой форме или графически на устройстве 38 отображения вместе с ультразвуковыми изображениями. Стандартный qLab-процессор, пригодный для расчета кривых времени-интенсивности, поставляемый компанией Philips Healthcare of Andover, Массачусетс.
Стандартный qLab-процессор выдает известные кривые времени-интенсивности, которые также называют кривыми перфузии или кривыми реперфузии. См. патент США 5833613 (Averkiou и др.), международную патентную публикацию WO 2005/099579 (Rafter), а также международную патентную публикацию WO 2005/054898 (Garg и др.). Как показывают эти публикации, накопление контрастного вещества в точках ткани (точках на изображении) контролируется во время прибытия контрастного вещества в определенные места в организме. Количество контрастного вещества в некоторой точке определяется интенсивностью эхо-сигналов, возвращенных от микропузырьков контрастного вещества в каждой точке, и присутствует в последовательности изображений, собранных с помощью передачи низкой мощности (low MI), по мере того как контрастное вещество поступает в ткань. Кривая времени-интенсивности может быть построена на основании этого повышения интенсивности контраста и его последующего снижения в процессе вымывания контрастного вещества для каждой точки в ткани, которая возвращает временную последовательность эхо-сигналов в покадровом режиме. Качественное представление кривых времени-интенсивности для изображаемой ткани в целом может быть сформировано путем окрашивания каждого пикселя в анатомическом изображении некоторым цветом, который представляет параметр кривых времени-интенсивности в каждой точке изображения. Например, в заявке Garg и др. показано образование параметрического изображения миокарда, где цвет каждого пикселя на изображении представляет пиковый уровень, достигнутый кривой времени-интенсивности в каждой точке миокарда. См. также патент США 6692438 (Skyba и др.).
В реализации настоящего изобретения данные эхо-сигналов при перфузии контрастного вещества собираются из последовательности изображений, по мере того как контрастное вещество прибывает в месторасположение метастаза в организме, накапливается, а затем вымывается. Величины интенсивности эхо-сигналов, таким образом, начинаются от некоторого уровня базовой линии, соответствующего отсутствию контрастного вещества, затем возрастают, выходят на горизонтальный участок, а далее снижаются, по мере того как контрастное вещество вымывается. С помощью алгоритма подбора кривой такое изменение данных затем согласуется с функцией ошибок, что определяется следующим образом
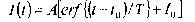 (1)
(1)
где I(t) - линейная интенсивность в момент времени t, А - максимальная интенсивность со смещением базовой линии, Т - временной параметр поступления, линейно пропорциональный времени поступления (например, от 5% до 95%), I0 - смещение базовой линии, t0 - сдвиг времени. Время поступления предпочтительно получают из аппроксимированной кривой, а не из искаженных данных изображения. Предпочтительно эхо-данные контрастного вещества не подвергаются сжатию до этой обработки, так чтобы данные сохраняли приобретенную линейную зависимость. Другой подход заключается в подборе для всей кривой времени-интенсивности (а не только ее части, соответствующей поступлению) соответствующих математических моделей, например логарифмически нормального распределения, что определяется следующим образом
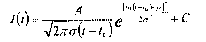 (2)
(2)
где μ и σ - средняя и стандартная девиация нормального распределения, из которого получено логарифмическое преобразование. Кривая может быть отмасштабирована по горизонтали, а также изменена в плане асимметрии. А - площадь под кривой, t0 - сдвиг времени, а C - смещение базовой интенсивности. Аппроксимированная кривая логарифмически нормального распределения используется для выделения времени поступления.
На фиг.5 показана одна пара изображений в последовательности кадров изображения метастаза 50 в окружающей ткани печени. Эта пара изображений получена из одних эхо-данных, при этом левое изображение представляет собой изображение на основе второй гармоники, в котором усиливается контрастное вещество, а правое изображение представляет собой изображение той же анатомической структуры с использованием основной частоты. Когда осуществляется перфузия печени контрастным веществом, перфузированный метастаз 50 отчетливо выделяется на гармоническом изображении и его границы могут быть очерчены с помощью маркировки 52. Вычерчивание может выполняться вручную или путем автоматической или полуавтоматической обработки, такой как определение границы, процесс определения порога или технология наращивания областей, запускаемая указанием начальной точки на границе метастаза. Маркировка 52 границы, таким образом, определяет область интереса (ROI) метастаза в пределах его границы. Можно видеть, что метастаз 50 менее отчетлив на показанном справа изображении в B-режиме, полученном с использованием основной частоты, поскольку гармонический отклик контрастного вещества здесь подавлен. Когда ROI метастаза очерчена маркировкой 52 границы, интенсивность, определяемая контрастным веществом в метастазе, во время получения изображения может быть измерена путем объединения значений пикселей в пределах границы 52 путем интегрирования, суммирования, осреднения или иной выбранной технологии объединения.
Изображения на фиг.5 были собраны в течение артериальной фазы кровотока к печени. На фиг.6 представлена пара изображений, полученных на основе гармоник и основной частоты, для той же ткани и метастаза 50, собранные на поздней портальной фазе. Как упоминалось ранее, HCC и метастатические поражения печени обычно получают большую часть своей перфузии кровью в течение артериальной фазы, в то время как нормальная паренхима печени получает большую часть своей перфузии кровью в течение портальной фазы, что отмечается более сильным затенением печени на левом изображении на фиг.6. Для ясности объяснения ультразвуковые изображения в настоящем описании показаны, будучи визуализированными в серой шкале «черное на белом», а не традиционно «белое на черном».
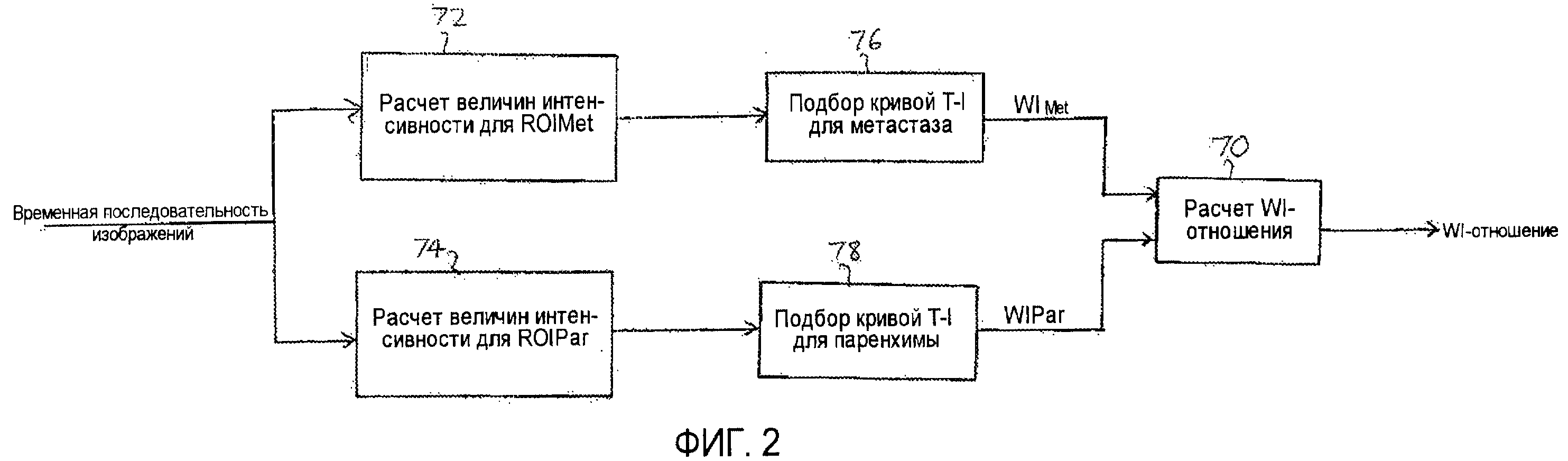
Согласно принципам настоящего изобретения параметр, который в настоящем описании называется «отношением времен поступления» (WITR), рассчитывается как количественная мера перфузии метастаза. Расчет WITR производят согласно блок-схеме на фиг.2. Из временной последовательности изображений метастаза или патологического изменения в ходе поступления и вымывания контрастного вещества, как показано на фиг.5 и 6, величины интенсивности контрастного вещества вычисляются для ROIMet метастаза 50, как показано в блоке 72. Как объяснялось выше, эти величины могут быть рассчитаны путем объединения значений пикселей ROI метастаза для каждого изображения последовательности. В блоке 74 величины интенсивности рассчитываются для ROIPar нормальной паренхимы ткани. Это может быть сделано путем маркировки области нормальной ткани, как показано с помощью маркировок 54 на фиг.5 и 6, и использования значений пикселей перфузии нормальной ткани в пределах этой второй маркировки. Эти величины, таким образом, представляют собой величины перфузии нормальной ткани. В блоке 76 кривая времени-интенсивности подбирается для величин перфузии ROIMet, а в блоке 78 кривая времени-интенсивности подбирается для величин перфузии ROIPar. Подбор не всегда необходим, но он позволяет лучше оценить WITR. Хотя WITR может быть измерено непосредственно из данных, искажение данных может понизить точность измерений, поэтому предпочтительно использовать вычерчивание кривой. На фиг.7 показаны две такие кривые времени-интенсивности, кривая Т-IMet ROI метастаза, а также T-IPar паренхимы. Параметр времени поступления WIT находится для каждой из кривых, например, с использованием функции ошибок или логарифмически нормального распределения, которые описаны выше. Это определяет параметр времени поступления как для метастаза, так и для нормальной паренхимы, WITMet, WitPar, соответственно. Отношение времен поступления WITR далее вычисляется из двух этих параметров поступления путем деления WITMet на WitPar. Эффект нормирования WITMet параметром времени поступления для нормальной ткани призван уменьшить или исключить влияние переменных в процедуре, таких как размер болюса, функциональное состояние сердца и наладочные параметры ультразвуковой системы, которые могут разниться от одной терапевтической процедуры к другой. Таким образом, поддающиеся сравнению количественные показатели роста или сокращения размеров метастаза, определяемые его ангиогенезом, могут быть получены для каждой терапевтической процедуры на период недель или месяцев, в течение которых проводится лечение пациента.
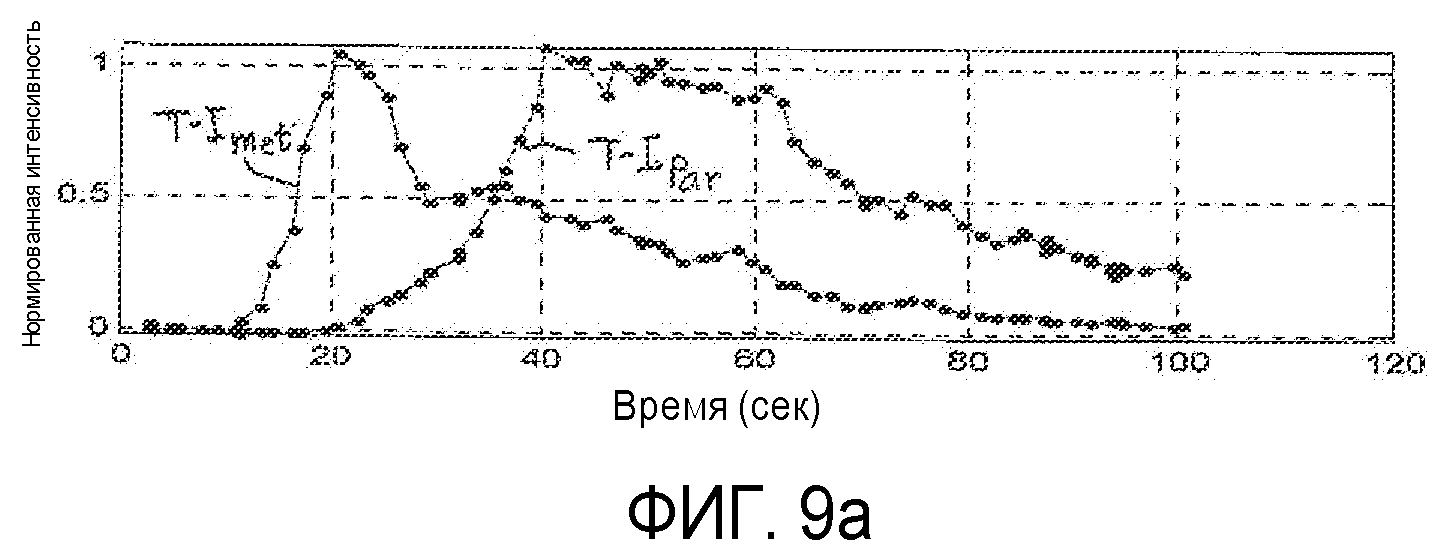
Другой выраженный количественно показатель ангиогенеза в метастазе, который снижает или устраняет влияние скорости введения болюса, функционального состояния сердца пациента или изменений наладочных параметров установки, показан на фиг.3. Кривая времени-интенсивности подбирается для каждой из областей интереса метастаза и паренхимы, как показано в блоках 76 и 78. В блоках 82 и 84 размах каждой кривой времени-интенсивности нормируется. Удобная шкала нормирования составляет от нуля до единицы. В блоке 80 вычисляется разностная кривая ΔТ-I, представленная в виде разности между двумя нормированными кривыми, Т-I кривойMet и Т-I кривойPar. Этот процесс и его результаты показаны на фиг.9а-9d. На фиг.9а точками показаны величины интенсивности перфузии метастаза (Т-IMet) и нормальной паренхимы (Т-IPar), собранные за период поступления и вымывания контрастного вещества, равный ста секундам. Два набора величин нормированы по одной шкале от нуля до единицы, где пиковая величина интенсивности каждого набора данных на шкале имеет уровень единицы. Эти кривые демонстрируют характерную особенность раннего поступления контрастного вещества в течение артериальной фазы для метастаза и более поздней перфузии паренхимы печени в течение портальной фазы. На фиг.9b кривая 92 (например, функция ошибок или логарифмически нормальное распределение) аппроксимирует величины перфузии метастаза, а кривая 94 аппроксимирует величины перфузии паренхимы. На фиг.9с две кривые 92 и 94 показаны более темными линиями, при этом величины собранных данных интенсивности отсутствуют. На фиг.9d показана кривая 90, которая представляет собой вычисленную разностную кривую ΔТ-I двух кривых 92 и 94, представленных на фиг.9с. Когда лечение опухоли проводится успешно и ангиогенез в метастазе снижается по мере лечения, кривая ΔТ-I будет становиться все более плоской и достигнет формы прямой. Этого результата следует ожидать, поскольку когда патологическое изменение устранено, его местоположение в организме будет давать отклик как нормальная паренхима, и разность между двумя (теперь виртуально идентичными) кривыми, соответствующими нормальной ткани и местоположению патологического изменения, станет равной нулю. Разностная кривая может быть также выражена в виде величины параметра, такого как максимальный угол наклона разностной кривой. Когда максимальная величина наклона достигает нуля (т.е. наклон отсутствует), это является признаком того, что разностная кривая стремится к прямой.
Шкала времени на графиках фиг.9а-9d показывает, что типичный период времени поступления и вымывания контрастного вещества может составлять 100 секунд. Это означает, что клинический сбор данных изображения должен поддерживать то же самое изображение патологического изменения устойчиво в течение 100 секунд, так чтобы каждая величина интенсивности соответствовала одной и той же области патологического изменения. Если, например, зонд перемещается в процессе сбора данных, патологическое изменение может выйти из плоскости изображения, и собранные данные не могут быть использованы. Даже если зонд устойчиво удерживается по отношению к телу пациента, патологическое изменение все же может перемещаться относительно поля обзора зонда вследствие дыхательных движений пациента. Один из способов преодоления влияния дыхательных движений заключается в синхронизации получения изображений с дыхательным циклом. Сигналы дыхания могут быть получены с помощью известного средства, такого как эластичная повязка с датчиками деформации или давления вокруг грудной клетки пациента. Другая технология заключается в передаче малых сигналов между датчиками по грудной клетке пациента и измерении изменений импеданса грудной клетки пациента. Эти и другие технологии способны сформировать циклические сигналы дыхательного цикла и могут использоваться для синхронизации получения изображений с той же фазой дыхательного цикла. Согласно другому аспекту настоящего изобретения синхронизация с дыхательными движениями выполняется путем обработки изображения, как показано на блок-схеме, представленной на фиг.4. На изображениях, полученных с использованием основной частоты, справа на фиг.5 и 6 показана отчетливо затененная область 60 в нижней части каждого изображения (которая была бы яркой областью на стандартных ультразвуковых изображениях в серой шкале «белое на черном»). Этим ориентиром 60 на изображении является диафрагма пациента на данных изображениях. На фиг.8 диафрагма на изображении выделена с помощью маркировки 62. В показанном примере маркировка 62 воспроизведена в том же положении на каждом изображении последовательности кадров изображений. Если анатомическая структура на изображении не перемещается относительно зонда при получении последовательности изображений, ориентир 60 диафрагмы будет присутствовать в маркировочном контуре 62 на каждом изображении. Однако дыхательные движения могут перемещать диафрагму 60 внутрь маркировочного контура или выводить наружу, особенно при глубоком дыхании. Процессор 100 изображений на фиг.4 детектирует такое изменение путем поиска ориентира диафрагмы в том же местоположении, ROID, которое является маркировочным контуром 62 в примере, представленном на фиг.8. Когда ориентир 60 диафрагмы найден в его ожидаемом местоположении на изображении («Да»), изображение направляется для обработки и количественной оценки. Однако если дыхательные движения приводят к тому, что ориентир 60 диафрагмы покидает свое ожидаемое местоположение ROID на изображении («Нет»), такое изображение не подвергается обработке. Этот прием применяется для всех изображений последовательности, так что влияние дыхательных движений на визуализацию метастаза, что выражается движением диафрагмы, исключается путем выбраковывания тех изображений, которые не согласуются с постоянным месторасположением диафрагмы. Существуют также другие возможные пути выполнения синхронизации с дыхательными движениями. Например, кривая времени-интенсивности может быть образована из ROI, которая точно следует части диафрагмы, и определяются пороговые значения. Всякое изображение, величина интенсивности которого ниже порогового, выбраковывается. Иные алгоритмы, основанные на компенсации движений, могут также применяться для детектирования дыхательных движений и синхронизации с ними.
Количественные измерения по настоящему изобретению были использованы в клинических условиях для контроля результатов лечения опухолей у восьми пациентов, прошедших от трех до пяти терапевтических процедур. Результат измерения WITR вычислялся для каждого пациента и для каждой терапевтической процедуры. На фиг.10 представлены результаты в отношении пациента, отвечающего на лечение, и пациента, не отвечающего на лечение. Как видно из графика, WITR стремится к единице у пациента с благополучным ходом лечения с каждой терапевтической процедурой. Для пациента из группы, который полностью не способен воспринимать лечение (обозначен как пациент, не отвечающий на лечение), WITR не приближается к единице. Этот график показывает, что результаты измерения WITR хорошо скоррелированы с действительными клиническими результатами лечения и могут использоваться в качестве биомаркера.