Результат интеллектуальной деятельности: СПОСОБ ФОТОЭЛЕКТРОКОЛОРИМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ СУЛЬФАНИЛАМИДНЫХ ПРЕПАРАТОВ
Вид РИД
Изобретение
Изобретение относится к фармацевтическому анализу и может быть использовано для фотоэлектроколориметрического определения сульфаниламидных препаратов - стрептоцида, сульфадимезина, этазола, сульфалена, фталазола, сульфатиазола, сульфадиметоксина, сульфамонометоксина в центральных заводских лабораториях, в контрольно-аналитических лабораториях, в биохимических лабораториях клиник и судебно-химических лабораториях.
Качественное определение сульфаниламидных препаратов - порошков стрептоцида и этазола проводится методом их реакции с салициловой кислотой и цитралем [А.С. 1086373]. Также ряд качественных реакций на сульфаниламидные препараты представлен в других источниках [Тезисы докладов IV съезда фармацевтов УССР. Копийчук И.И., Шкадова А.И. Запорожье, 1984].
Количественное определение сульфаниламидных препаратов (сульфатиазол, сульфадимезин, этазол, стрептоцид) в субстанциях и лекарственных формах (таблетки) проводят методом нитритометрии. Фталазол количественно определяют титрованием препарата в растворе ДМФА раствором натрия гидроксида в смеси метилового спирта и бензола в присутствии тимолового синего до появления синего окрашивания [Государственная Фармакопея СССР. 10-е изд. - М.: Медицина, 1968; ФС 42-1594-81 Сульфапиридазин].
Разработаны также другие методы количественного определения исследуемых соединений: потенциометрическое титрование хлорной кислотой в неводных растворителях (ледяная уксусная кислота, ацетонитрил, уксусный ангидрид); полярографическое восстановление; ПМР-спектроскопия; УФ-спектрофотометрический метод; метод непрямого титрования с использованием насыщенного водного раствора брома; титриметрическое и спектрофотометрическое титрование; спектрофотометричекий метод.
Приведенные выше способы количественного определения исследуемых препаратов являются малочувствительными и неспецифическими.
Технический результат изобретения заключается в повышении чувствительности, селективности и точности определения лекарственных веществ в фармакопейных препаратах.
Технический результат достигается тем, что способ количественного определения сульфаниламидных препаратов в субстанциях и таблетках, в случае с сульфаленом или фталазолом, согласно изобретению включает растворение лекарственного препарата в 0,1 М растворе HCl, выдерживание на нагретой водяной бане при перемешивании до полного растворения, охлаждение и прибавление того же растворителя до метки, дальнейшую обработку аликвотной части приготовленного раствора 0,1 М раствором калия гидроксида, щелочным 1% раствором натрия нитропруссида, 3% раствором водорода перекиси и последующее фотоэлектроколориметрирование окрашенных растворов при длине волны 670 нм; а в случае со стрептоцидом, сульфадимезином, этазолом, сульфатиазолом, сульфадиметоксином или сульфамонометоксином, согласно изобретению включает растворение лекарственного препарата в 0,1 М растворе КОН, выдерживание на нагретой водяной бане при перемешивании до полного растворения, охлаждение и прибавление того же растворителя до метки, дальнейшую обработку аликвотной части приготовленного раствора щелочным 1% раствором натрия нитропруссида, 3% раствором водорода перекиси и последующее фотоэлектроколориметрирование окрашенных растворов при длине волны 670 нм.
Предлагаемый способ фотоэлектроколориметрического определения сульфаниламидных препаратов в субстанциях и таблетках основан на их взаимодействии со свежеприготовленным 1% щелочным раствором химического реактива (натрия нитропруссида) и раствором водорода перекиси.
Щелочной раствор химического реактива получают следующим образом: 1 г натрия нитропруссида растворяют в 100 мл 0,1 М раствора КОН в склянке из темного стекла. После полного растворения вещества постепенно прибавляют каплями из градуированной пипетки 0,20-0,30 мл 30%-го раствора водорода перекиси при перемешивании (светло-оранжевый прозрачный раствор еще раз перемешивается и хранится в склянке из темного стекла в холодильнике в течение месяца).
Продукты реакции окрашивают растворы в светло-зеленый (сульфадиметоксин) и темно-зеленый (фталазол, стрептоцид, этазол, сульфадимезин, сульфамонометаксин, сульфален и сульфатиазол) цвета, устойчивые на протяжении 2 часов. Оптическую плотность поглощения окрашенных растворов измеряют при длине волны 670 нм с помощью фотоэлектроколориметра КФК-2.
Количественное содержание сульфаниламидных препаратов в субстанциях вычисляют методом наименьших квадратов после статистической обработки калибровочных графиков.
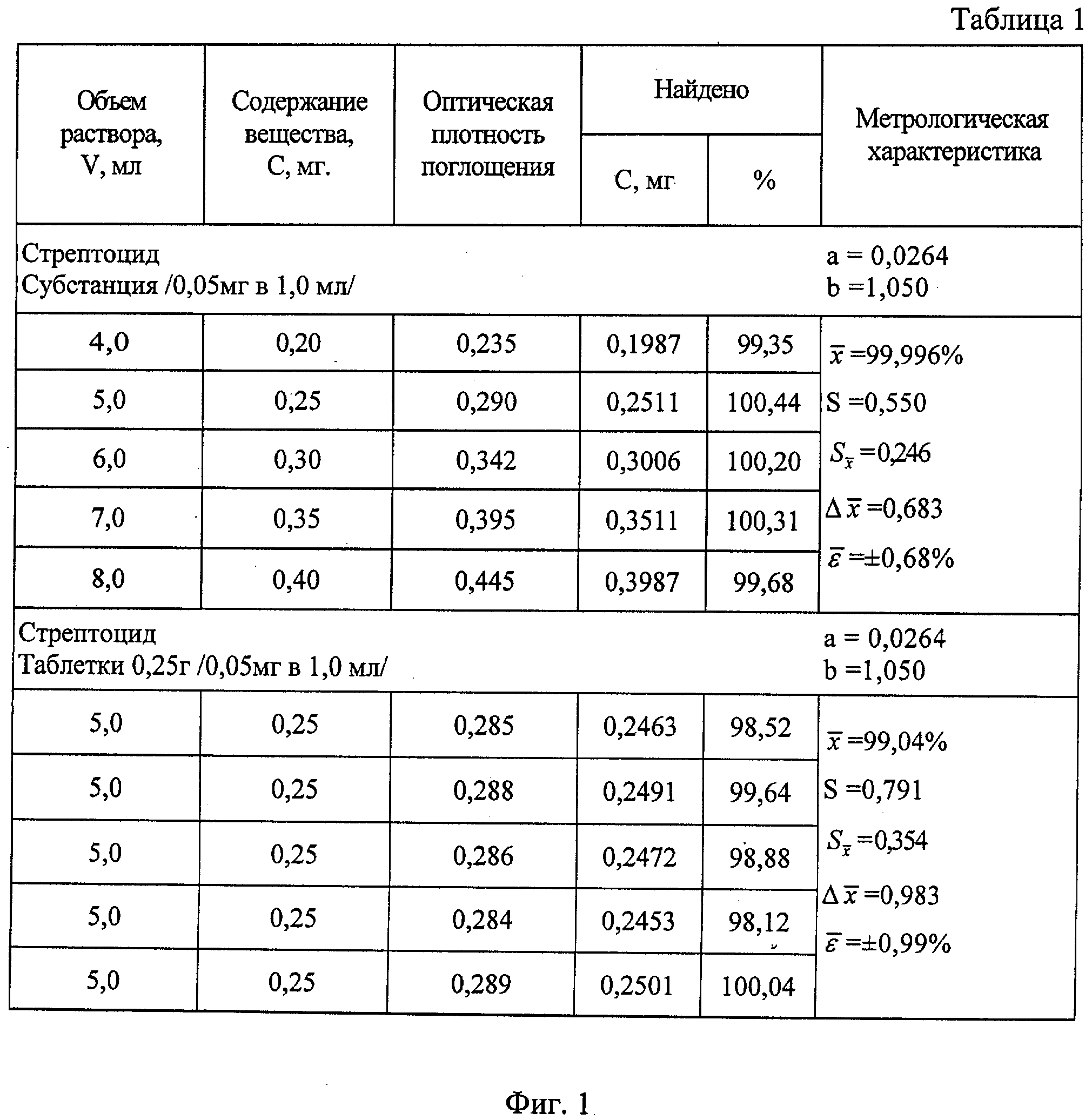
На фиг.1 приведена таблица результатов количественного определения стрептоцида в субстанции и таблетках.
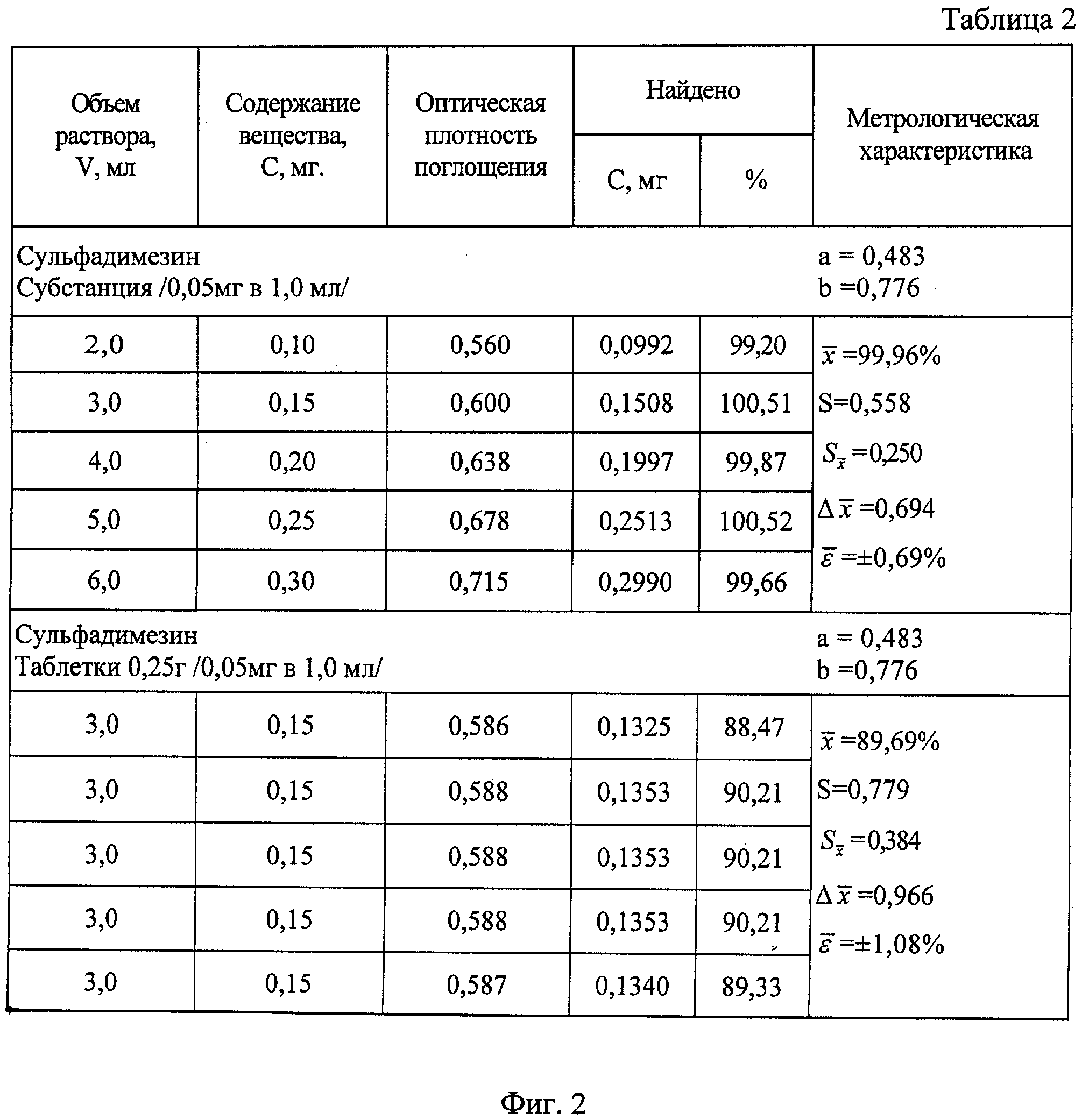
На фиг.2 приведена таблица результатов количественного определения сульфадимезина в субстанции и таблетках.
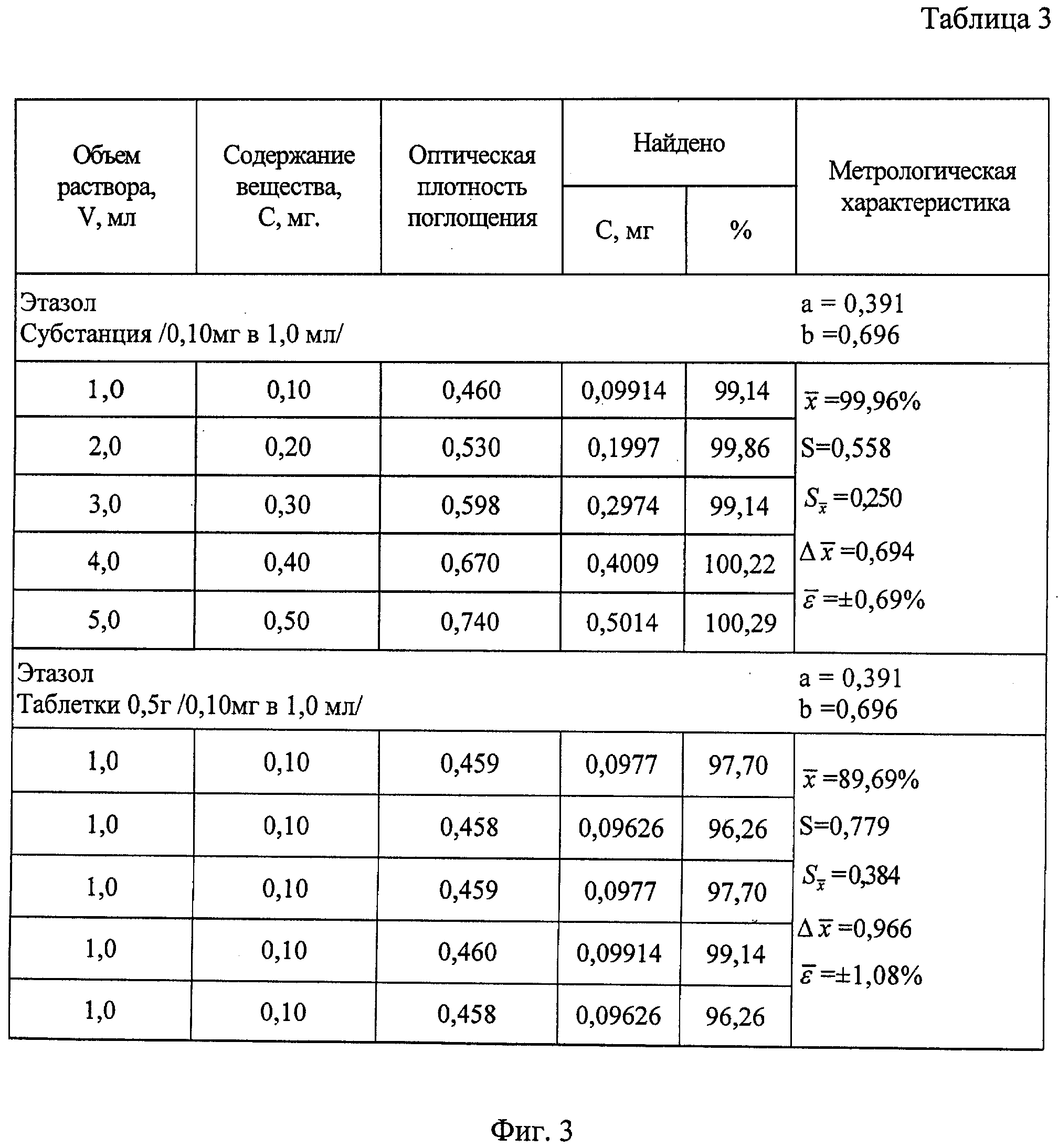
На фиг.3 приведена таблица результатов количественного определения этазола в субстанции и таблетках.
На фиг.4 приведена таблица результатов количественного определения сульфалена в субстанции и таблетках.
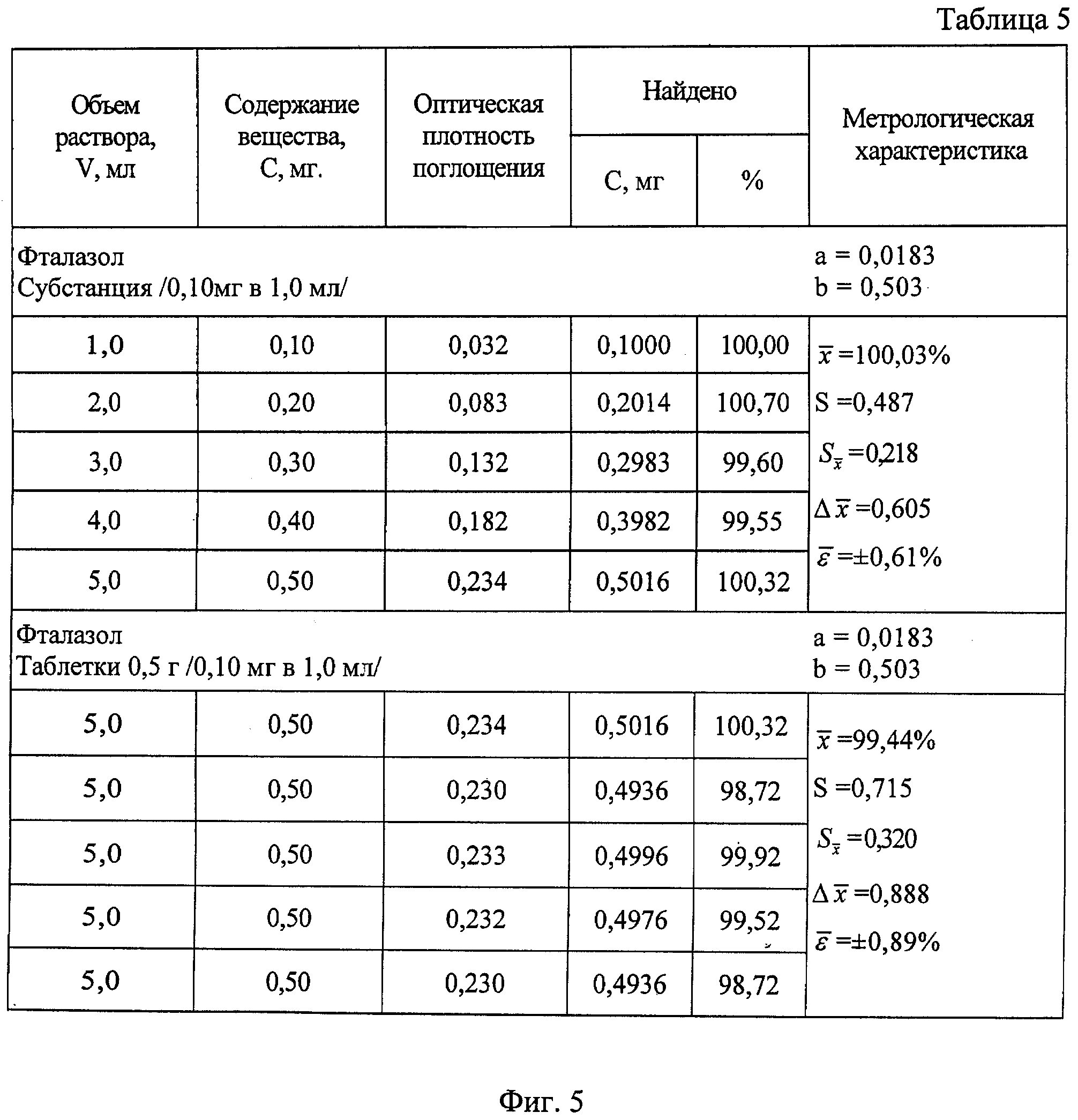
На фиг.5 приведена таблица результатов количественного определения фталазола в субстанции и таблетках.
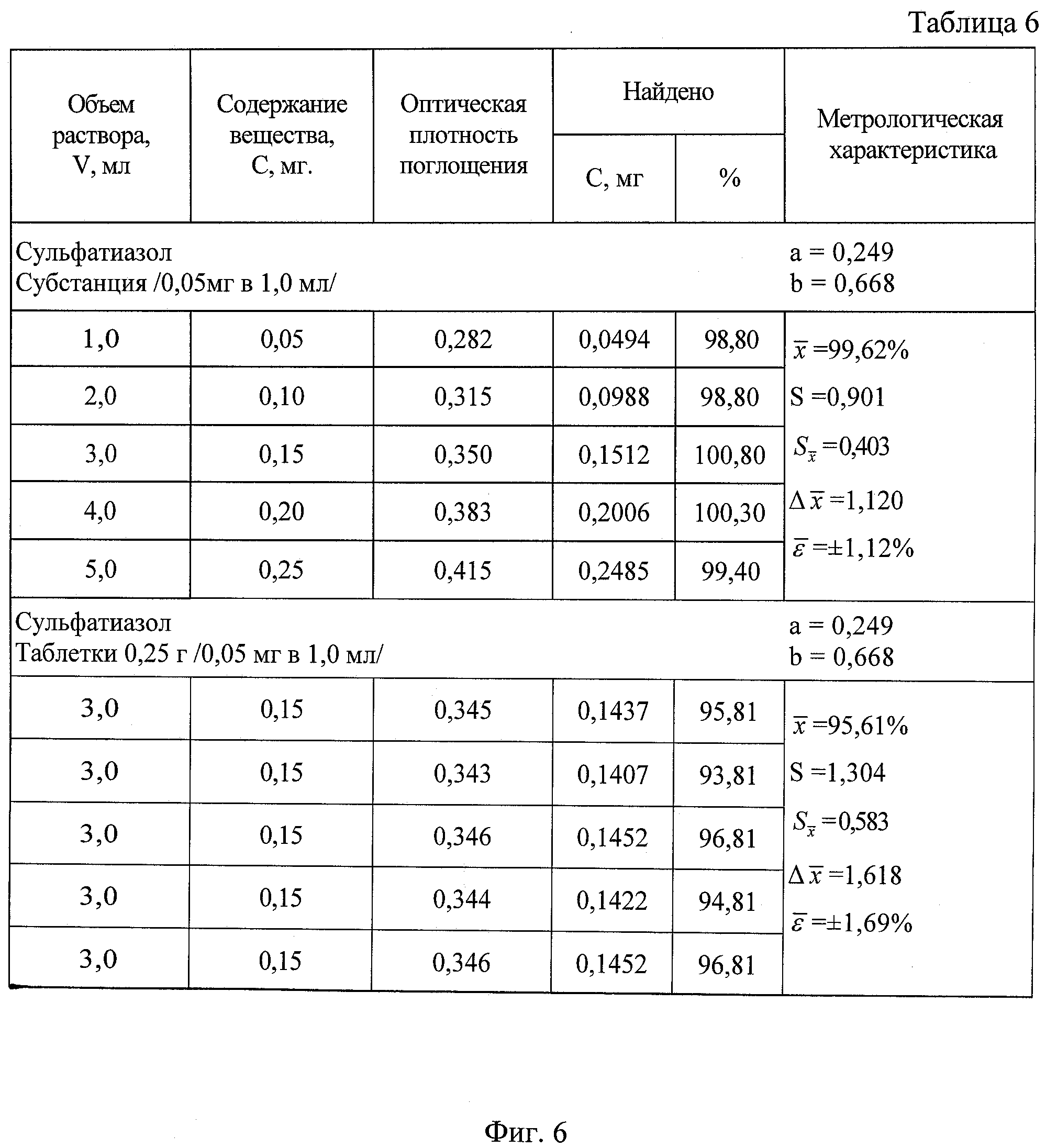
На фиг.6 приведена таблица результатов количественного определения сульфатиазола в субстанции и таблетках.
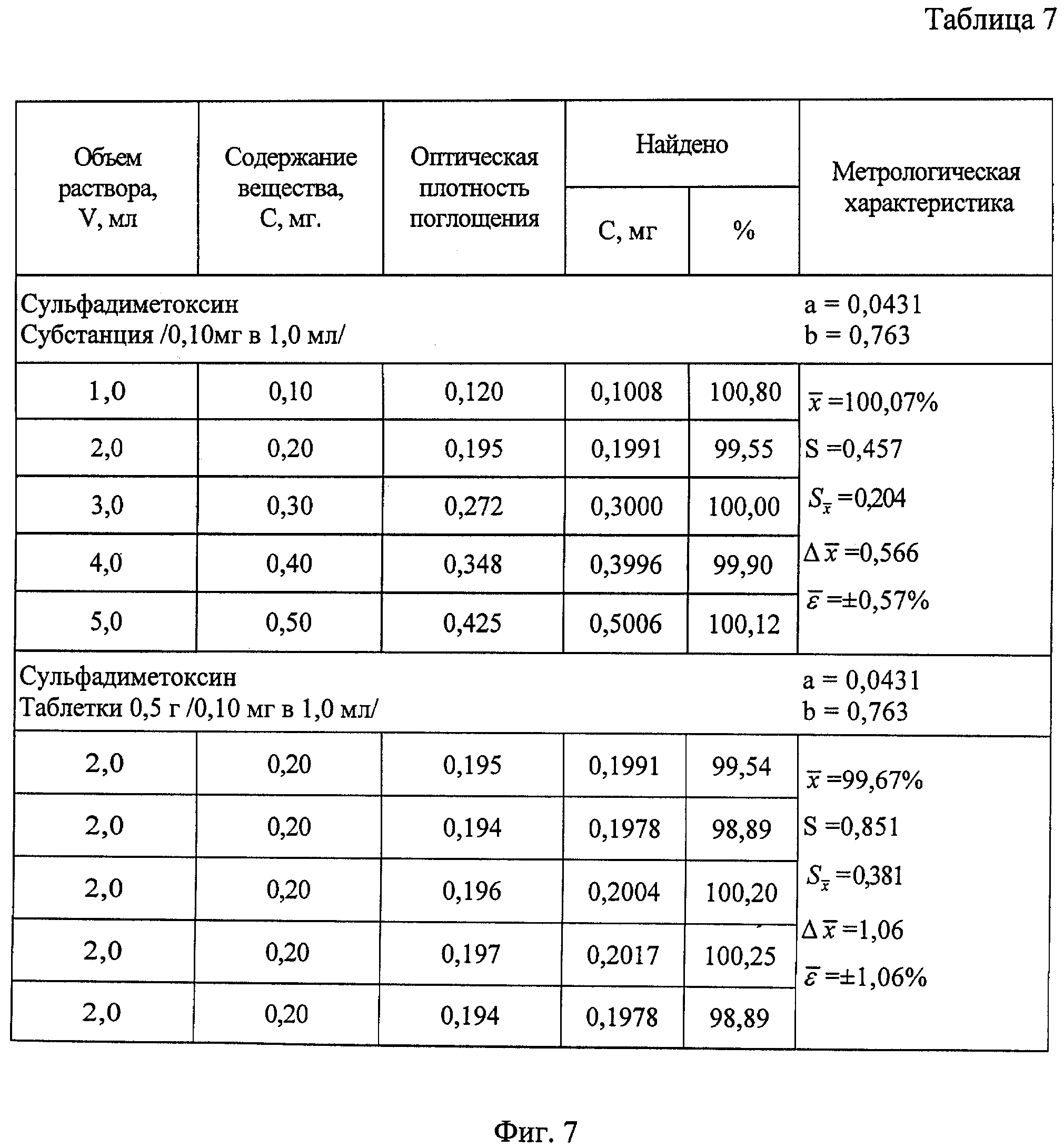
На фиг.7 приведена таблица результатов количественного определения сульфадиметоксина в субстанции и таблетках.
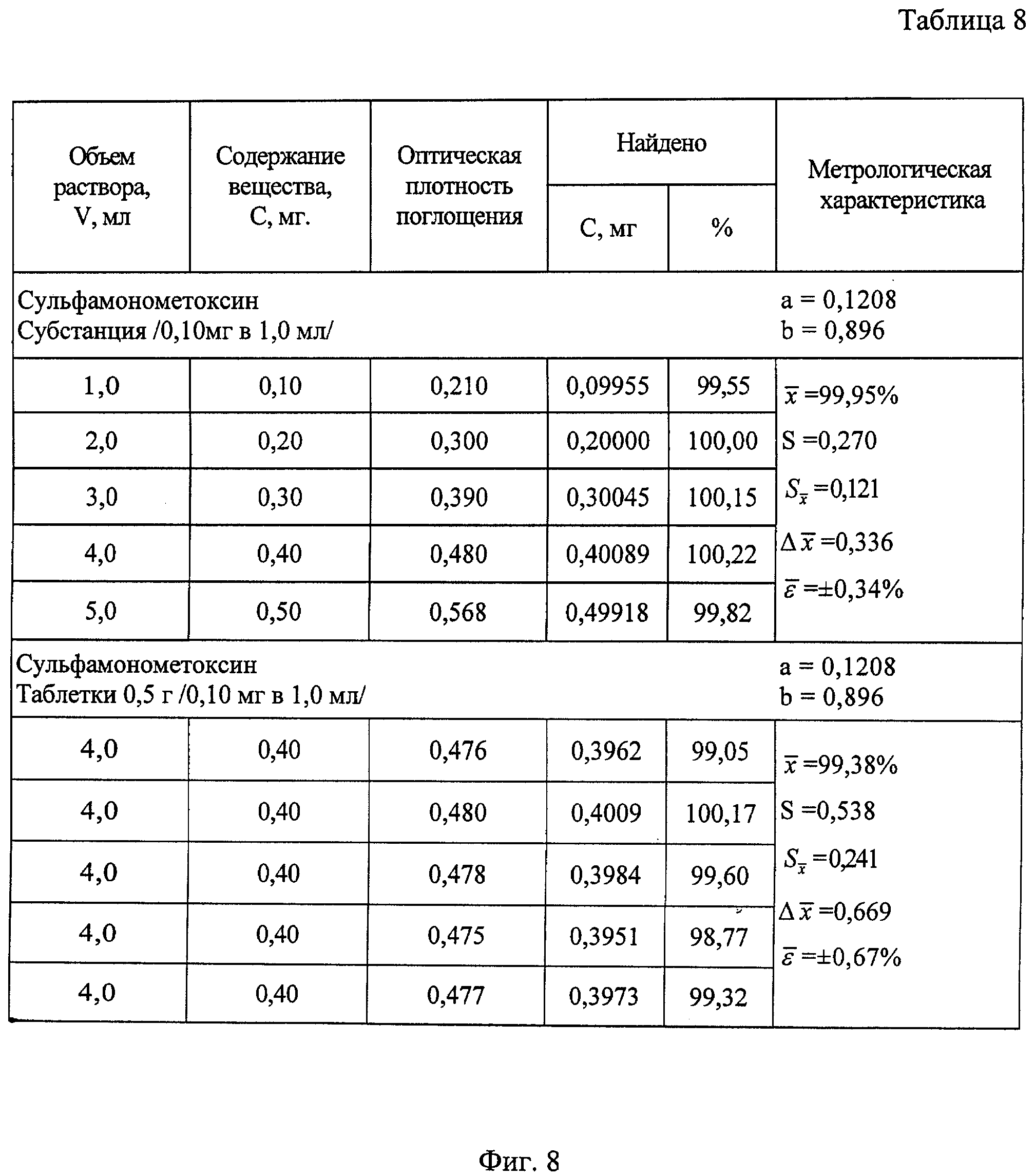
На фиг.8 приведена таблица результатов количественного определения сульфамонометоксина в субстанции и таблетках.
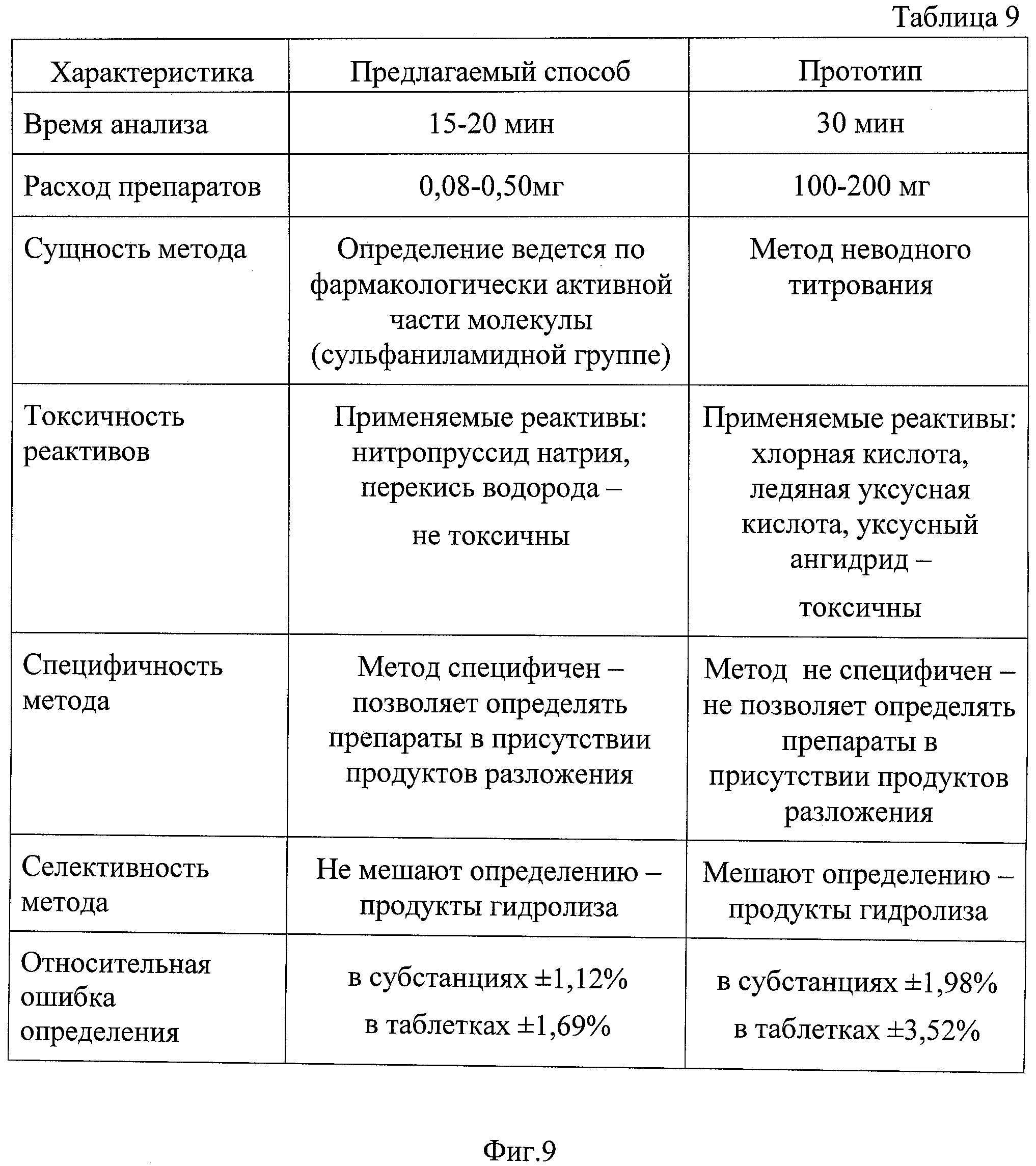
На фиг.9 приведена таблица со сравнительными данными, подтверждающими преимущества предлагаемого способа фотоэлектроколориметричекого определения сульфаниламидных препаратов.
Пример 1. Для количественного определения сульфаниламидных препратов в субстанциях точную навеску (около 0,2-0,5 г) растертого порошка исследуемого препарата растворяют в 50 мл 0,1 М раствора HCl (в случае с сульфаленом или фталазолом) или в 50 мл 0,1 М раствора КОН (в случае со стрептоцидом, сульфадимезином, этазолом, сульфатиазолом, сульфадиметоксином или сульфамонометоксином) в мерной колбе вместимостью 100 мл и выдерживают на нагретой водяной бане при 30-40°С до полного растворения (в случае со фталазолом - 30 мин для прохождения гидролиза). После охлаждения объемы растворов доводят тем же растворителем до метки и перемешивают.
Для построения калибровочных графиков отмеренные объемы 4,0; 5,0; 6,0; 7,0; 8,0 мл стрептоцида, 2,0; 3,0; 4,0; 5,0; 6,0 мл сульфадимезина, 1,0; 2,0; 3,0; 4,0; 5,0 мл этазола, сульфалена, фталазола, сульфатиазола, сульфадиметоксина, сульфамонометоксина приготовленных растворов помещают в мерные колбы емкостью 25 или 50 мл, последовательно каплями при перемешивании прибавляют 2,0 мл свежеприготовленного щелочного 1% раствора натрия нитропруссида видоизмененной формы и 0,2 мл 3% раствора водорода перекиси.
В случае с сульфаленом и фталазолом перед добавлением щелочного раствора натрия нитропруссида вносят от 1,0 до 7,0 мл 0,1 М раствора КОН для щелочности среды.
Окрашивание продуктов взаимодействия проявляется при комнатной температуре в течение 1-2 мин в виде светло-зеленого (сульфадиметоксин) или темно-зеленого (фталазол, стрептоцид, этазол, сульфадимезин, сульфамонометаксин, сульфален и сульфатиазол) цветов.
Оптическую плотность поглощения окрашенных растворов измеряют с помощью фотоэлектроколориметра КФК-2 в кювете с поглощающим слоем 10,0 мм при длине волны 670 нм относительно растворов натрия нитропруссида и калия гидроксида. Подчинения интенсивности поглощения окрашенных растворов закону Бугера-Ламберта-Бера находятся в пределах концентраций для субстанций стрептоцида 0,20-0,40 мг/мл, сульфадимезина 0,10-0,30 мг/мл, этазола 0,10-0,50 мг/мл, сульфалена 0,08-0,40 мг/мл, фталазола 0,10-0,50 мг/мл, сульфатиазола 0,05-0,25 мг/мл, сульфадиметоксина 0,10-0,50 мг/мл и сульфамонометаксина 0,10-0,50 мг/мл.
Коэффициенты a и b исследуемых субстанций вычислены при обработке калибровочных графиков методом наименьших квадратов.
Пример 2. Для количественного определения сульфаниламидных препаратов в лекарственных формах (таблетках) точную навеску (около 0,2-0,5 г) растертой в порошок массы таблетки сульфаниламидного препарата растворяют в 50 мл 0,1 М раствора HCl (в случае с сульфаленом или фталазолом) или в 50 мл 0,1 М раствора КОН (в случае со стрептоцидом, сульфадимезином, этазолом, сульфатиазолом, сульфадиметоксином или сульфамонометоксином) в мерной колбе вместимостью 100 мл и выдерживают на нагретой водяной бане при 30-40°С до полного растворения (в случае со фталазолом - 30 мин для прохождения гидролиза). После охлаждения объемы растворов доводят тем же растворителем до метки, взбалтывают и фильтруют через стеклянный фильтр №4 во вторую мерную колбу вместимостью 100 мл. Отбирают соответственно объемы от 1,0 до 5,0 мл приготовленных растворов и проводят все операции, приведенные выше в Примере 1.
Результаты количественного определения исследуемых веществ в субстанциях и таблетках указывают на воспроизводимость разработанной методики. Относительная ошибка для субстанции и таблетки соответственно не превышает ±0,68% и ±0,99% у стрептоцида, ±0,69% и ±1,08%) у сульфадимезина, ±0,70% и ±1,54%) у этазола, ±0,60% и ±1,54%) у сульфалена, ±0,61% и ±0,89% у фталазола, ±1,12% и ±1,69% у сульфатиазола, ±0,57% и ±1,06%) у сульфадиметоксина, ±0,34% и ±0,67% у сульфамонометоксина.
Вспомогательные вещества таблеток (желатин, тальк, магния стеарат, лактоза и др.) не мешают количественному определению исследуемых препаратов.
Разработанный способ фотоэлектроколориметрического определения сульфаниламидных препаратов в субстанциях и таблетках прост в выполнении, не требует дорогостоящей аппаратуры, дефицитных реактивов и дает воспроизводимые результаты.