Результат интеллектуальной деятельности: ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
Вид РИД
Изобретение
Настоящее изобретение относится к получению фармацевтических средств, более конкретно к способу снижения тенденции тонкоизмельченного лекарственного вещества агрегировать и/или образовывать агломераты.
Для активных ингредиентов, чьи физико-химические свойства затрудняют получение состава, часто желательным является использование наиболее термодинамически стабильной кристаллической формы по сравнению с активным ингредиентом. К сожалению, некоторые лекарственные вещества, особенно тонкоизмельченные лекарственные вещества, имеют тенденцию агрегировать при хранении и/или абсорбировать воду из атмосферы и образовывать агломераты. Эта агрегация и/или образование агломератов затрудняет дальнейшую обработку или, по крайней мере, делает ее менее эффективной. Это даже может значительно ухудшать физико-химические свойства лекарственного вещества, включая стабильность.
Тонкоизмельченный гликопирролат, в частности, имеет сильную тенденцию агрегировать и/или образовывать агломераты, что затрудняет дальнейшее получение лекарственного препарата, особенно получение сухих порошковых составов для введения ингаляцией.
Были предложены различные способы обработки тонкоизмельченных лекарственных веществ для изменения некоторых физико-химических свойств лекарственного вещества. Однако некоторые из этих способов включают применение воспламеняющихся растворителей, которые не подходят идеально для крупномасштабного коммерческого производства. Другие известные способы обработки растворителем, включающие способы с использованием воды или водяного пара, вызывают процессы локальной сольватации, что приводит к росту частиц, агрегации и агломерации.
В статье Brodka-Pfeiffer и др., Drug Development and Industrial Pharmacy, 2003, Т.29, No. 10, c.1077-1084 описано, что тонкоизмельченный сульфат сальбутамола вызывает образование аморфных частиц и нагревание тонкоизмельченного вещества в течение 5 часов при 70°C в духовом шкафу, к сожалению, приводит к перекристаллизации, и, следовательно, стабильного продукта не образуется.
Неожиданно было обнаружено, что обработка тонкоизмельченного лекарственного вещества сухим теплом может снижать его тенденцию агрегировать и/или образовывать агломераты. Это происходит, даже когда лекарственное вещество не содержит никакого существенно определимого количества аморфного вещества.
Соответственно, в первом варианте настоящее изобретение относится к способу снижения тенденции лекарственного вещества агрегировать и/или образовывать агломераты в процессе хранения, включающему стадии:
(а) тонкого измельчения лекарственного вещества с получением среднего размера частиц менее около 10 мкм и
(б) обработку тонкоизмельченного лекарственного вещества сухой средой при повышенной температуре от 40 до 120°C в течение по крайней мере шести часов.
Лекарственное вещество может быть тонкоизмельченным вместе или “совместно тонкоизмельченным” с одним или несколькими другими лекарственными веществами и/или с одним или несколькими противосклеивающими агентами.
Предпочтительно повышенная температура составляет от 60 до 100°C, или обычно от 60 до 90°C.
Предпочтительно тонкоизмельченное лекарственное вещество подвергают обработке сухой средой при повышенных температурах в течение от 12 до 96 часов, более предпочтительно от 24 до 50 часов, особенно около 24 часов.
В некоторых предпочтительных вариантах осуществления, когда лекарственное вещество присутствует в кристаллической форме, которая содержит аморфные частицы, способ может снижать наличие аморфным частиц в лекарственном веществе.
Предпочтительно лекарственное вещество представляет собой соль гликопирролиния, особенно гликопирролат.
Во втором варианте осуществления настоящее изобретение относится к ингалируемому составу сухого порошка, который содержит лекарственное вещество, обработанное описанным выше способом согласно настоящему изобретению.
В третьем варианте осуществления настоящее изобретение относится к ингалируемому составу для применения в ингаляторе с отмеренной дозой, который содержит лекарственное вещество, суспендированное в газе-вытеснителе, где лекарственное вещество обработано описанным выше способом согласно настоящему изобретению.
Термины, использующиеся в описании, имеют следующие значения:
“Агрегат”, как здесь используется, обозначает собираться или объединяться вместе. Свежеприготовленные тонкоизмельченные лекарственные вещества имеют тенденцию образовывать тонкоизмельченный порошок, который имеет тенденцию спонтанно объединяться в течение времени с образованием агрегатов лекарственного вещества. Эти агрегаты напоминают менее тонкоизмельченный или даже крупный порошок.
“Агломерат”, как здесь используется обозначает, формирование массы или комка, особенно в присутствии влажности. Тонкоизмельченные лекарственные вещества или их агрегаты при хранении, особенно в присутствии влажности, имеют тенденцию образовывать крупный порошок, комки или даже по существу единую массу лекарственного вещества.
“Аморфный”, как здесь используется, описывает нарушенное твердое состояние, которое может появляться в процессе изготовления лекарственного вещества (стадия кристаллизации, сушки, измельчения) или лекарственного препарата (гранулирование, прессование). Образец дифракции рентгеновских лучей на порошке аморфного твердого вещества не показывает острых пиков.
“Противосклеивающий агент”, как здесь используется, обозначает материал, который снижает сцепление частиц и предотвращает соединение тонкоизмельченных частиц с внутренними поверхностями устройства для ингаляции, или смеси таких материалов. Противосклеивающие агенты также включают антифрикционные агенты или глиданты, которые придают порошковому составу лучшие свойства текучести в ингаляторе. Он и обычно приводят к лучшей воспроизводимости дозы и более высоким фракциям тонкоизмельченных частиц. Обычные противосклеивающие агенты включают аминокислоты, такие как лейцин, фосфолипиды, такие как лецитин или производные жирной кислоты, такие как стеарат магния или стеарат кальция.
“Соль гликопиррония”, как здесь используется, обозначает любую форму соли или противоиона гликопиррония, включая, но не ограничиваясь ими, бромид гликопиррония (гликопирролат), хлорид гликопиррония или йодид гликопиррония, а также любые и все выделенные стереоизомеры и их смеси стереоизомеров. Производные солей гликопиррония также включены. Подходящими противоионами являются фармацевтически приемлемые противоионы, включая, например, фторид, хлорид, бромид, йодид, нитрат, сульфат, фосфат, формиат, ацетат, трифторацетат, пропионат, бутират, лактат, цитрат, тартрат, малат, малеат, сукцинат, бензоат, п-хлорбензоат, дифенилацетат или трифенилацетат, о-гидроксибензоат, п-гидроксибензоат, 1-гидроксинафтален-2-карбоксилат, 3-гидроксинафтален-2-карбоксилат, метансульфонат и бензолсульфонат.
“Средний размер частиц” представляет собой среднее значение диаметра частиц, что измерено лазерной дифракцией. Средний размер частиц ×90 обозначает средний размер частиц, ниже которого 90% частиц образца имеют меньший средний размер частиц. Средний размер частиц ×50 обозначает средний размер частиц, ниже которого 50% частиц образца имеют меньший средний размер частиц. Средний размер частиц ×10 обозначает средний размер частиц, ниже которого 10% частиц образца имеют меньший средний размер частиц.
В этом описании и в последующей формуле изобретения, если контекстом не указано иное, слово “включать” или варианты, такие как “включает” или “включающий”, должно пониматься как включающее указанное значение или группу значений, но не исключая любое другое значение или группу значений.
Настоящее изобретение относится к способу снижения тенденции лекарственного вещества агрегировать и/или образовывать агломерат. Способ включает (а) тонкое измельчение лекарственного вещества с получением среднего размера частиц менее около 10 мкм; (б) обработку тонкоизмельченного лекарственного вещества сухой средой при повышенной температуре от 40 до 120°C в течение по крайней мере 6 часов.
Лекарственным веществом может быть любой фармакологически активный ингредиент, хотя способ по изобретению особенно подходит для кристаллических лекарственных веществ, чьи физико-химические свойства затрудняют получение обычного состава, особенно при получении составов сухого порошка для введения ингаляцией. Обычно такие вещества имеют активированные поверхности и достаточную химическую стабильность для того, чтобы выдержать обработку используемой температурой.
Такие лекарственные вещества включают противовоспалительные, бронхорасширяющие, антигистаминные, противоотечные и противокашлевые лекарственные вещества, например агонисты β2-адренорецептора, антимускариновые агенты, стероиды, ингибиторы PDE4, агонисты A2a или блокаторы кальция. Предпочтительные лекарственные вещества (включая их соли, полиморфы или гидраты или сольваты) включают антимускариновые агенты, такие как бромид ипратропия, бромид тиотропия, другие соли тиотропия, кристаллический гидрат бромида тиотропия, бромид окситропия, бромид аклидиния, даротропий, BEA-2180, BEA-2108, CHF 4226 (Chiesi), GSK423405, GSK202423, LAS35201, SVT-40776, (R)-3-(2-гидрокси-2,2-дифенилацетокси)-1-(изоксазол-3-илкарбамоилметил)-1-азониабицикло[2.2.2]октанбромид и соли гликопиррония; агонисты β2-адренорецептора, такие как формотерол, индакатерол, альбутерол (сальбутамол), метапротеренол, тербуталин, сальметерол, фенотерол, прокатерол, кармотерол, мильветерол, BI-1744-CL, GSK159797, GSK-159802, GSK642444, PF-610355 и их соли; и стероиды, такие как будесонид, дипропионат бекламетазона, пропионат флутиказона, фуроат мометазона, циклезонид, GSK-685698 и (6S,9R,10S,11S,-13S,16R,17R)-9-хлор-6-фтор-11-гидрокси-17-метоксикарбонил-10,13,16-триметил-3-оксо-6,7,8,9,10,11,12,13,14,15,16,17-додекагидро-3H-циклопента[a]фенантрен-17-иловый эфир 3-метилтиофен-2-карбоновой кислоты. Растворимость и другие физико-химические характеристики этих веществ могут хорошо показывать условия, которые необходимы для снижения тенденции конкретного лекарственного вещества агрегировать и/или образовывать агломерат.
В некоторых вариантах осуществления лекарственное вещество может быть тонкоизмельченным вместе или “совместно тонкоизмельченным” с одним или несколькими другими лекарственными веществами и/или одним или несколькими противосклеивающими агентами.
В предпочтительном варианте осуществления способа настоящего изобретения лекарственное вещество представляет собой соль гликопиррония, особенно бромид гликопиррония или гликопирролат.
Гликопирролат, который имеет химическое название бромид 3-[(циклопентилгидроксифенилацетил)окси]-1,1-диметилпирролидиня, является антимускариновым агентом, который в настоящее время вводится инъекцией для снижения секреций в процессе анестезии или принимается перорально для лечения язвы желудка. Однако позднее он был предложен для лечения заболеваний дыхательного тракта.
Гликопирролат имеет следующую химическую структуру:
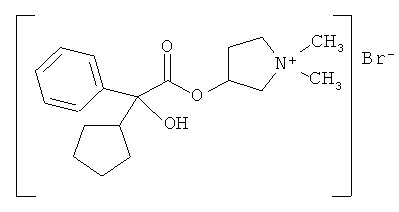
Гликопирролат является коммерчески доступным или может быть получен методикой, описанной в патенте US 2956062, содержание которого приведено здесь в качестве ссылки. Он предпочтительно является кристаллическим и не содержит определимые аморфные части.
Гликопирролат содержит два стереогенных центра и, следовательно, существует в четырех изомерных формах, а именно бромид (3R,2'R)-, (3S,2'R)-, (3R,2'S)- и (3S,2'S)-3-[(циклопентилгидроксифенилацетил)окси]-1,1-диметилпирролидиния, как описано в патентах US 6307060 и US 6613795. Содержания этих описаний к патентам приведены здесь в качестве ссылки. Настоящее изобретение включает использование одной или нескольких этих изомерных форм, особенно 3S,2'R изомера, 3R,2'R изомера или 2S,3'R изомера, таким образом включая отдельные энантиомеры, смеси диастереомеров или рацематы, особенно бромид (3S,2'R/3R,2'S)-3-[(циклопентилгидроксифенилацетил)окси]-1,1-диметилпирролидиния.
Лекарственное вещество может быть тонко измельчено любыми подходящими средствами с получением среднего размера частиц менее 10 мкм, но предпочтительно менее 5 мкм. Обычно частицы лекарственного вещества такого размера подходят для введения ингаляцией. Тонкое измельчение, общими словами, обозначает растирание или другое уменьшение лекарственного вещества механическими средствами, так что по крайней мере 90%, но предпочтительно по крайней мере 95% полученного измельченного материала имеют средний размер частиц менее около 10 микрон в диаметре. В некоторых вариантах осуществления средний размер частиц составляет менее около 7 микрон в диаметре, а другие частицы имеют размер менее около 5 микрон в диаметре.
Частицы, имеющие средний размер частиц больше около 10 мкм, вероятно, ударяются о стенки гортани, и обычно не достигают легких. Частицы, имеющие средний размер частиц от около 2 мкм до около 5 мкм обычно размещаются в дыхательных бронхиолах, тогда как меньшие частицы, имеющие средний размер частиц от около 0,05 мкм до около 2 мкм, вероятно, выдыхаются или размещаются на альвеолах и абсорбируются в кровь.
Устройство для тонкого измельчения является хорошо известным из предшествующего уровня техники и включает различные измельчающие машины и мельницы, например мельницы компрессионного типа, такие как механические мельницы с плавлением, ударные мельницы, такие как шаровые мельницы, гомогенизаторы и микрофлуидизаторы, и струйные мельницы. В предпочтительном варианте осуществления кристаллическая соль гликопиррония измельчается на струйной мельнице с помощью Hosokawa Alpine® 100 AFG псевдоожиженного слоя в струйной мельнице. Другое подходящее оборудование струйного измельчения включает струйные мельницы Hosokawa Alpine® AFG140, AFG200, AFG280 и AFG400 и спиральные струйные мельницы или другое мельничное оборудование, включая оборудование с использованием азота, воздуха или других мельничных газов или их смесей.
В некоторых вариантах осуществления для лекарственного вещества может подходить тонкое измельчение вместе с противосклеивающим агентом для дальнейшего снижения тенденции лекарственного вещества образовывать агломераты и, следовательно, для повышения стабильности полученного лекарственного вещества. Предпочтительно противосклеивающим агентом является один или несколько стеаратов металла, один или несколько кристаллических сахаров или их смесь. Особенно предпочтительные стеараты металлов включают стеарат магния и стеарат кальция или аминокислоты, такие как лейцин. Особенно предпочтительные кристаллические сахара включают лактозу, более предпочтительно моногидрат лактозы или безводную лактозу.
Ключевая стадия способа настоящего изобретения включает обработку тонкоизмельченного лекарственного вещества сухой средой при повышенной температуре от 40 до 120°C по крайней мере в течение 6 часов. Такая среда не содержит или по крайней мере по существу не содержит никакого растворителя или пара растворителя, включая любые органические растворители или воду. При этом не происходит никаких локальных процессов сольватации (вследствие более высокого сродства водяного пара активированных сайтов на поверхности частицы), которые могут приводить к росту, агрегации и/или агломерации частицы.
Тонкоизмельченное лекарственное вещество предпочтительно размазывают тонким слоем по поддону для повышения доступной площади поверхности, и эти поддоны помещают в камеру, где их обрабатывают сухой средой при повышенной температуре от 40 до 120°C по крайней мере в течение 6 часов.
Неожиданно, способ настоящего изобретения повысил поверхностную стабильность лекарственного вещества, особенно кристаллического лекарственного вещества. На фотографиях сканирующей электронной микроскопии (SEM) показано, что обработка свежеприготовленных тонкоизмельченных лекарственных веществ, таких как гликопирролат, для повышения текучести приводит к агрегации частиц и сглаживанию поверхности частиц. Однако свежеприготовленные тонкоизмельченные лекарственные вещества, такие как гликопирролат, которые обрабатывали в соответствии со способом настоящего изобретения, не показывают заметной агрегации частиц, и поверхности частиц остаются неровными. Это сохраняется в случае, когда тот же материал последовательно обрабатывают для повышения текучести, объясняя изменение свойств поверхности на более стабильные при использовании способа настоящего изобретения.
Не основываясь на какой-либо теории, обработка лекарственного вещества сухой средой, как оказывается, вызывает быструю перегруппировку поверхностей лекарственного вещества. Это исключает местные эффекты диссоциации и агрегации, которые могут наблюдаться, когда тонкоизмельченные лекарственные вещества обрабатывают растворителями или парами растворителей, особенно когда лекарственное вещество растворимо в используемом растворителе.
Повышенная температура и длительность обработки может изменяться в зависимости от обрабатываемого лекарственного вещества. Предпочтительно повышенная температура составляет от 40 до 120°C, более предпочтительно от 60 до 100°C, но особенно от 60 до 90°C. Предпочтительно тонкоизмельченное лекарственное вещество обрабатывают сухой средой при повышенной температуре в течение от 12 до 96 часов, more предпочтительно от 24 до 50 часов, особенно около 24 часов.
Когда лекарственное вещество представляет собой гликопирролат, повышенная температура предпочтительно составляет от 60 до 120°C, более предпочтительно от 70 до 90°C, но особенно около 75°C. Тонкоизмельченный гликопирролат предпочтительно обрабатывают сухой средой при повышенной температуре в течение от 12 до 72 часов, more предпочтительно в течение от 20 до 60 часов, но особенно около 24 часов.
В некоторых предпочтительных вариантах осуществления, в которых лекарственное вещество присутствует в кристаллической форме, которая содержит аморфные частицы, способ может снижать наличие аморфных частиц лекарственного вещества. Известно, например, из статьи Burnett и др., International Journal of Pharmaceutics, 2004, 287, c. 123-133, что аморфный материал может быть получен непреднамеренно в процессе измельчения или прессования и наличие этого материала в фармацевтических системах может непосредственно влиять на свойства обработки, хранения, биодоступности и доставки материала.
Когда лекарственное вещество представляет собой гликопирролат, снижение тенденции образовывать агрегаты и агломераты не может объясняться удалением аморфных частиц, поскольку гликопирролат не содержит видимых аморфных частей. Снижение тенденции образовывать агрегаты и агломераты, как оказывается, является результатом перегруппировки и снижения поверхностной энергии на поверхности лекарственного вещества или около нее.
Лекарственные вещества, которые были обработаны в соответствии со способом настоящего изобретения, имеют пониженную тенденцию образовывать агрегаты и/или агломераты и, таким образом, обеспечивают по существу стабильную твердую массу лекарственного вещества, что облегчает дальнейшую обработку, то есть смешение частиц носителя лактозы с получением ингалируемого сухого порошка. Обработка также может повышать способность лекарственного вещества немного сопротивляться умеренным повышениям относительной текучести в силу того, что способ настоящего изобретения изменяет поверхность частиц лекарственного вещества.
Настоящее изобретение иллюстрируется следующим примером.
Пример 1
Тонкое измельчение и тепловая обработка гликопирролата без растворителя
1 кг кристаллического гликопирролата тонко измельчали с 5% стеарата магния, используя противоточную струйную мельницу Hosokawa Alpine® 100 AFG с псевдоожиженным слоем со следующими параметрами: классификатор скорости 17000 об/мин; давление газа мельницы 4 бар. Мельница оснащена 3 насадками диаметром 1,9 мм.
Размер частиц стонкоизмельченного гликопирролата и стеарата магния измеряли лазерной световой дифракцией, используя анализатор размера частиц HELOS от Sympatec GmbH, Germany, и средний размер частиц составлял 2,5 мкм.
Аморфное содержание тонкоизмельченного гликопирролата и стеарата магния измеряли дифференциальной сканирующей калориметрией (ДСК), гипер-ДСК и микрокалориметрией. Аморфный состав не наблюдался.
Тонкоизмельченный гликопирролат и стеарат магния растирали тонким слоем по поддону и помещали в сушильную камеру при атмосферных условиях. Температуру в сушильной камере повышали до 70°C в течение одного часа и поддерживали эту температуру в течение 48 часов. После этого поддоны удаляли из сушильной камеры и оставляли охлаждаться.
Аморфное содержание сухого обработанного теплом тонкоизмельченного гликопирролата и стеарата магния измеряли ДСК, гипер-ДСК и микрокалориметрией, и аморфного состава не наблюдалось. Соответственно гликопирролат не подвергался фазовому изменению в отношении перекристаллизации аморфных частиц. Однако реструктуризация поверхности и снижение поверхностной энергии показано обращенной газовой хроматографией (ОГХ), используя обращенную газовую хроматографию (ОГХ, Surface Measurement Systems) с помощью алканов н-декана, н-нонана, н-октана, гептана, гексана и ацетонитрила и используя этанол и этилацетат в качестве молекул пробы для измерения дисперсионной поверхностной энергии и кислотно-основных свойств поверхности.
До тонкого измельчения материал показал дисперсионную поверхностную энергию 48 мДж/м2, которая повышалась в процессе измельчения до приблизительно 70 мДж/м2. После обработки материала при повышенной температуре эта поверхностная энергия, как оказалось, снижалась до 52 мДж/м2.
Изменение ka/kb-значения (кислотно-основное соотношение, описывающее поверхностные свойства) также определяли путем измерения с помощью ОГХ, используя ацетонитрил, этанол и этилацетат в качестве полярных молекул пробы. Грубое неизмельченное лекарственное вещество показало соотношение ka/kb 1,0. После тонкого измельчения соотношение ka/kb составило около 1,2, возможно, в результате образования новой поверхности. После тепловой обработки соотношение ka/kb составляло около 0,9. Эти изменения дисперсионной поверхностной энергии и соотношения ka/kb ясно показывают изменение поверхностных свойств. Они показывают поверхностную перегруппировку в отношении повышения термодинамического состояния. Изменений размера частиц в процессе не наблюдалось, что измерено лазерной световой дифракцией с помощью анализатора размера частиц HELOS от Sympatec GmbH, Germany.
Если, наоборот, материал не обрабатывали, как описано выше, но обрабатывали повышенной температурой в комбинации с повышенной влажностью способом, при котором тонкоизмельченный гликопирролат и стеарат магния растирали тонким слоем на поддонах и помещали в камеру при атмосферных условиях; температуру в камере повышали до 30°C и относительную влажность доводили до значения 75% RH в течение одного часа и поддерживали при этой температуре в течение 72 часов, дисперсионная поверхностная энергия снижается только до приблизительно 65 мДж/м2 при соотношении ka/kb 1,4, показывая другие поверхностные свойства. Это объясняет положительный эффект и потенциал описанного способа в отношении получения тонкоизмельченного материала, который является термодинамически стабильным и, таким образом, снижает поверхностную энергию.
Полученный материал отличается от материала, который не обработан описанным способом. Например, если свежий тонкоизмельченный (или совместно тонкоизмельченный с некоторыми контрольными агентами, такими как стеарат магния) материал обрабатывают при повышенной влажности, наблюдается агрегация частиц и сглаживание поверхности частиц (например, по данным фотографий SEM). Наоборот, если материал обрабатывают описанным способом при повышенной температуре после процесса измельчения, агрегации частиц не наблюдается, если материал обрабатывают после при повышенной влажности, а также поверхности остаются неровными.

