Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ВОДОРАСТВОРИМЫХ ОЛИГОМЕРНЫХ ГОМОЛОГОВ ХИТОЗАНА В ГЕТЕРОГЕННОЙ СИСТЕМЕ
Вид РИД
Изобретение
Изобретение относится к области химии биополимеров-аминоглюканов и может быть использовано в фармации, медицине, ветеринарии, космецевтике.
Известны разработки, публикации, посвященные изучению процесса пероксидного гидролиза хитозана с целью получения его низкомолекулярных гомологов. Определены закономерности развития процесса деструкции хитозана в гетерогенных системах. Установлена зависимость степени деструкции аминогликана от технологических параметров процесса. Эксперементально определена следующая зависимость DD=ln(M0/M)=f{[H2O2]}·τ}, где DD - степень деструкции, M0 и M - средневязкостная молекулярная масса (ММ) соответственно исходного и деструктированного кислоторастворимого хитозана, τ - время в мин, позволяет установить условия деструкции для заданной ММ целевого хитозана при любых значениях ММ исходного полимера. Показано, что степень деацетилирования исходного хитозана в процессе его пероксидной деструкции практически не изменяется (Шийчук А.В. Универсальный показатель глубины деструкции полимера. Логарифм отношения молекулярных масс. Укр. Хим. журн. 1991. Т.57. 11. С.1229; Gamzazade A.I., Slimak V.M., Sklar A.M., Shtikova E.V., Pavlova S.V., Rogojin S.V. // Acta Polymerica. 1985. V.36. 8. P.420). Деструкция жесткоцепного аминогликана хитозана в гетерогенной системе приводит к снижению ММ и расширению молекулярно-массового распределения (ММР) ввиду возрастания содержания олигомерной фракции гомологов. Данные, полученные методом экслюзионной хроматографии показывают, что при изменении отношения M0/М от ~6,7 (DD=1,9) до ~21,1 (DD=3,1) в условиях гетерогенного пероксидного гидролиза-деполимеризации хитозана наблюдается расширение ММР, а содержание в продуктах гидролиза олигомерных фракций, в том числе мономера, возрастает до 30%. Для хитозана, деструктированного в гетерогенных условиях со средневязкостной ММ ~80-100 кДа, характерно широкое ММР - от 150 кДа до олигомерной фракции; для варианта ММ хитозана ≤25 кДа ММР включает фракции от ~50 кДа до мономера.
Наиболее близким к предлагаемому способу получения водорастворимых олигомерных гомологов хитозана является метод пероксидного гидролиза аминогликана с ММ ~350-600 кДа в гетерогенной системе, применяющийся для получения гомологов хитозана с пониженной молекулярной массой в диапазоне от ~80 кДа до олигомерных структур со степенью полимеризации 1-10. Этот метод включен в описание патента на способ получения водорастворимых форм хитозана (патент РФ 2215749, С08В 37/08, A61K 32/722, 2003). Сущностью заявляемого способа является получение образцов смесей гомологов хитозана с диапазоном молекулярных масс от ~100 кДа до олигомерной группы, включая мономер (глюкозамин). Конечной целью изобретения являлась подготовка препаратов с расширенным спектром биологического действия для использования в медицине, ветеринарии и косметике.
Гомологи хитозана использовались так же для проведения гидролиза и солеобразования с органическими (янтарная, L-глютаминовая) и неорганическими (хлористоводородная, ортофосфорная) кислотами, а также с ангидридами органических кислот. Кроме указанных методов обработки высокомолекулярного хитозана проводились способы аморфизации полимера с целью повышения его реакционной способности и гидрофильности путем переосаждения из растворов в кислотах в условиях повышения рН. С этой же целью использован метод гомогенизации суспензии хитозана в водных растворах органических кислот в режиме создания кавитационных механических полей со сдвиговым воздействием на рабочий объем.
Описание способов деполимеризации хитозана в гетерогенной системе с участием в качестве окислителя гликозидных центров (межзвеньевых связей) пероксида водорода приводится в двух вариантах:
а) Гидролиз хитозана с ММ ~600 кДа в системе, содержащей 0,15% H2O2 при 80°С в течение 25 мин. В результате образуется смесь гомологов хитозана нерастворимых в воде с Mср ~80 кДа.
б) Гидролиз хитозана с ММ ~300 кДа в системе, содержащей 0,2% H2O2 при 80°С в течение 34 мин. Образующаяся смесь гомологов хитозана характеризуется Мср ~20-25 кДа (нерастворимы в воде).
Олигомерную фракцию гомологов хитозана получали в условиях кислотного гидролиза аминогликанов в среде водного раствора ортофосфорной кислоты.
а) Гидролиз хитозана с ММ ~350 кДа. Ортофосфорная кислота использовалась при соотношении с хитозаном 0,6:1. Процесс проводили при 70°С в течение 4 часов. После нейтрализации смеси (Ca(OH)2), фазового разделения, лиофильной сушки и лиофилизации выделена смесь водорастворимых олигомеров хитозана (степень полимеризации=1-10); выход 13,4%.
б) Гидролиз хитозана с ММ ~25 кДа. Соотношение введенной в процесс гидролиза ортофосфорной кислоты и хитозана (водная среда) идентично методу (а). Температурный режим и длительность процесса идентичны методу (а). После обработки методом, указанным в (а) выделена олигомерная водорастворимая фракция гомологов хитозана (степень полимеризации=1-10) с выходом 20%.
Недостатками известной методики получения водорастворимых олигомерных и кислоторастворимых низкомолекулярных гомологов хитозана является усложнение процесса кислотного гидролиза (ортофосфорная кислота); стадии - гидролиз, нейтрализация кислоты, лиофилизация целевого продукта, а также низкий выход олигомерной фракции (степень полимеризации=1-10) до 20%.
Варианты известной методики пероксидного гидролиза хитозана имеют ограниченную возможность ввиду образования только гидрофобных фракций гомологов хитозана с Мср ~20-80 кДа. Возможность получения фракций водорастворимых олигомеров методом пероксидной деполимеризации хитозана не осуществлена.
Задачей предлагаемого изобретения является разработка способа пероксидной деполимеризации хитозана для получения фракций водорастворимых олигомеров.
Технический результат заключается в возможности количественно устанавливать степень превращения исходного высокомолекулярного аминогликана в олигомерные и низкомолекулярные структуры его гомологов.
Технический результат достигается тем, что в способе получения водорастворимых олигомерных гомологов хитозана в гетерогенной системе путем деполимеризацей высокомолекулярного хитозана перекисью водорода, согласно изобретению, процесс деполимеризации хитозана проводится в двухфазной системе, твердой фазой которой является активированный хитозан с Мср=450-650 кДа и средним размером частиц 0,05-0,20 мм, жидкая фаза - водный раствор H2O2 с концентрацией H 2 O 2 в реакционной системе 1-7%, длительностью реакции 120-180 - мин и температуре 70°С, далее проводят фазовое разделение образующихся гомологов хитозана путем фильтрации через бумажную или текстильную поверхность, полученный фильтрат содержит водорастворимые олигомеры хитозана.
В результате деполимеризации образуются две фракции низкомолекулярных гомологов хитозана. Фракция гомологов хитозана, растворимых в воде (нейтральная среда), представляет собой смесь олигомеров со степенью полимеризации в диапазоне 3-8; фракция, не растворимая в воде, но растворимая в 1-2% водной
СН3СООН, является смесью низкомолекулярных гомологов аминогликана со средневязкостной ММ до 25-46 кДа. Определена возможность регулирования процесса пероксидного гидролиза хитозана путем варьирования технологических параметров: концентрации Н2O2 в реакционной системе и длительности реакции. В качестве постоянных значений технологических параметров этого процесса приняты показатели: температура, соотношение твердой и жидкой фазы в системе на начальный период взаимодействия, размер частиц хитозана.
Таким образом, разработанный метод гидролиза позволяет количественно устанавливать степень превращения исходного высокомолекулярного аминогликана в олигомерные и низкомолекулярные структуры его гомологов. По разработанным показателям выход целевой фракции гомологов хитозана водорастворимых олигомеров со степенью полимеризации 3-8 достигает более 53% (масс).
Фазовое разделение образующихся гомологов хитозана осуществляется фильтрацией через бумажную или текстильную поверхность и дополнительной экстракцией путем обработки соответствующими растворителями. Реальной является возможность дополнительного фракционирования смесей водорастворимых олигомерных гомологов хитозана путем обработки выделенной первичной соответствующей фракции водными растворами этилового спирта (экстракция и седиментация при пониженных температурах). Этим путем достигается выделение смесей, состоящих из 2-3 олигомеров.
Оценка средней степени полимеризации фракции олигомеров хитозана производится по данным химического метода определения содержания редуцирующих звеньев в тестируемом образце полимер-гомолога. Количественное блокирование альдегидных групп (полуацетальных гидроксилов) осуществляется действием гидразида изоникотиновой кислоты в водной среде с применением йодометрии. Для характеристики гидрофобной фракции гомологов хитозана, образующихся по предлагаемому методу, использовался вискозиметрический способ, включающий расчет средневязкостной Мср по уравнению Марка-Куна-Хаувинка: [η]=KMα, где K=3,5·10-4, α=0,76.
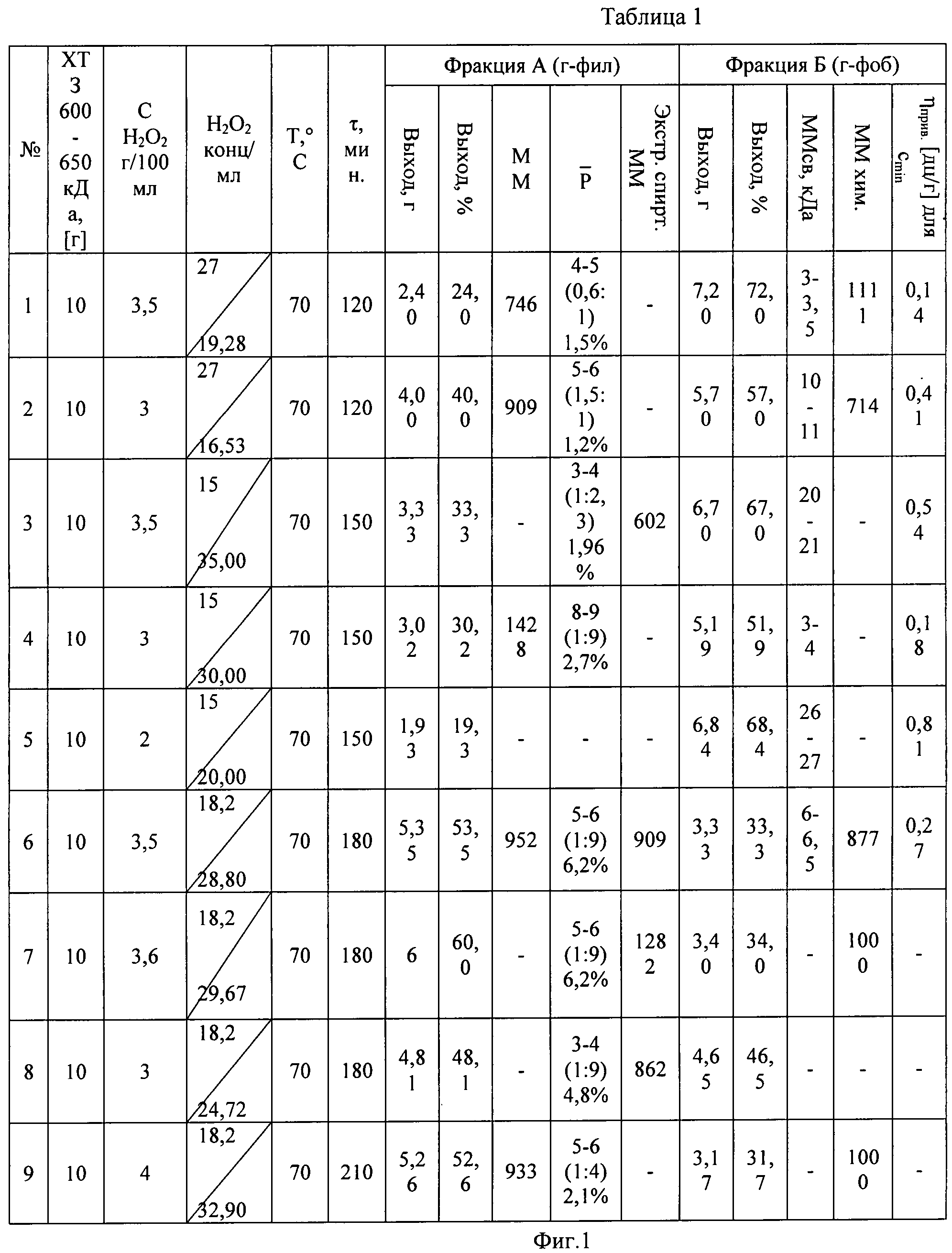
Данные по условиям пероксидного гидролиза хитозана и результатам процесса приведены в таблице (фиг.1).
Пример
10 г (0,06 моль) Хитозана (ХТЗ) (СДА>90%; [η]=29 дл/г, в 2% СН3СООН. Мср=600-650 кДа), гранулометрически подготовленного путем истирания со средним размером частиц 0,05-0,20 мм и 100 мл дистиллированной воды поместили в трехгорлую колбу, снабженную перемешивающим устройством и обратным воздушным холодильником. Образовавшуюся при перемешивании суспензию термостатировали при 40-50°С в течение 30 мин 5,46 г (0,16 моль) пероксида водорода в виде 50 мл водного раствора, добавляли в водную суспензию хитозана и продолжали перемешивание при 70°С в течение 180 мин. Концентрация H 2 O 2 3,6% масс. Жидкостной модуль реакционной системы 15; соотношение реагентов 1:2,6 моль (избыток H2O2) (табл.1). На заключительной стадии обработки визуально отмечено возрастание объема твердых частиц полимера. Образовавшуюся реакционную смесь охладили до 25-30°С и провели фазовое разделение путем фильтрации на воронке Бюхнера с бумажной фильтрующей поверхностью (-0,3-(-0,4) атм). Остаток на фильтре - мягкие, слегка окрашенные в желтый цвет частицы полимергомолога хитозана, не растворимые в воде, промывали дистиллированной водой в объеме 150-200 мл до исчерпывающей экстракции водорастворимой фракции полимерного гидролизата. Выделенную твердую фазу в виде набухших гранул сушили на воздухе при комнатной температуре в течение 48-50 часов. Остаточную влажность (5-6%) в составе полученного полимергомолога определяли путем дополнительного извлечения летучих продуктов из состава полимера в вакууме (-0,6 атм; 50°С). Выделен твердый порошкообразный продукт, окрашенный в слабо желтый цвет, растворимый в 1-2% водной уксусной кислоте, но практически не растворимый в воде. Для последующих аналитических испытаний проводили дополнительную экстракцию низкомолекулярных фракций из состава полимера путем обработки дистиллированной водой в колбе с магнитной мешалкой при 40-45°С в течение 30-45 мин. Выход гидрофобной фракций полимергомологов хитозана - 3,4 г (34% от массы исходного хитозана).
Фильтрат, полученный при фазовом разделении реакционной массы, образовавшегося после пероксидного гидролиза хитозана, помещали в стеклянный кристаллизатор (диаметр 17 см). Удаление летучих продуктов реакции производили в открытой системе при 40-45°С в течение 48-50 часов. Наблюдали образование бесцветного твердого вещества «по визуальной оценке» с аморфной структурой. Полученную смесь гидрофильных олигомеров хитозана экстрагировали 95% этанолом (40-45°С); остаток после экстракции высушивали под вакуумным колоколом (15 мм рт.ст.) при температуре окружающей среды. Выделен бесцветный порошкообразный продукт с признаками кристаллоидной структуры (наблюдение под микроскопом при 16-кратном увеличении). Полученная смесь олигомеров легко растворима в воде при 20-30°С. Для растворов установлена характерно выраженная редуцирующая способность, что подтверждалось реакцией образования серебряного зеркала при добавлении в раствор аммиачного AgNO3. Выход олигомеров составляет 6 г (60% от массы исходного хитозана).
Определение степени полимеризации и Мср синтезированного олигохитозана по редуцирующим звеньям
А. 0,5 г смеси олигомеров хитозана и 0,17 г (0,0012 моль) изониазида (фармакопейный) растворили в 40 мл дист, воды, раствор поместили в плоскодонную колбу с обратным воздушным холодильником. Раствор нагревали при 60-70°С в течение 90 мин. Полученный раствор слабожелтоватого цвета поместили в колбу Вюрца, присоединенную к системе с вакуумом -0,6-(-0,7) атм и вакуумировали при 60-70°С до образования гелеобразного остатка, который экстрагировали 95% этанолом в целях исчерпывающего экстрагирования избытка изониазида. Образовавшуюся при этом двухфазную систему разделили обработкой на фильтре из пористого стекла с бумажной прокладкой (вакуум -0,3 атм). Твердый остаток на поверхности фильтра - смесь гидразонов изониазида на основе олигохитозана. Фильтрат поместили в колбу Вюрца (100 мл) и отогнали этанол при 60-70°С (-0,4 атм). Остаток после удаления этанола (избыток изониазида) растворили в 100 мл дист. воды. Концентрацию изониазида в растворе определяли йодометрическим методом (ГФ XI). 2 г NaHCO3 и 50 мл 0,1 н раствора I2 смешивали с полученным раствором изониазида. Смесь термостатировали при 30°С в условиях светозащиты в течение 30 мин. В полученную смесь при охлаждении ее добавили 20 мл водного раствора HCl 1:2 (нейтрализация бикарбоната натрия). Остаточный I2 титровали 0,1 н раствором тиосульфата натрия. На титрование израсходовано 34 мл раствора Na2S2O3 (K=1, индикатор крахмал). Таким образом, 16 мл йода вступило во взаимодействие с избытком изониазида. Учитывая, что на 0,003428 г изониазида, расходуется 1 мл 0,1 н йода, количество изониазида, вступившего во взаимодействие с олигохитозаном - 0,054 г (0,0039 моль). Количество моль изониазида соответствует количеству редуцирующих звеньев в синтезированном олигохитозане. Мср. полученного олигохитозана составляет 1282. Рассчитанная молекулярная масса олигомера хитозана со степенью полимеризации (Р) равной 7, составляет 1177.
Б. Описание вискозиметрического метода определения Мср. 1,0 г гидрофобной фракции пероксидного гидролиза хитозана растворили в 100 мл 2% водной
СН3СООН. Уточненную концентрацию полученного раствора определяли по среднему значению сухого остатка (1,0 г/дл). Образовавшийся раствор фильтровали.
Для вискозиметрической оценки раствора хитозана в 2% СН3СООН использовали вискозиметр Оствальда (диаметр капилляра 0,9 мм, емкость 10 мл), помещенный в водный термостат с температурой 20°С. Время истечения растворителя и растворов с различной концентрацией (C1-C4) определяли трехкратным тестированием после термостатирования в течение 10 мин. Для этого использовались концентрации растворов, полученные разбавлением исходного раствора 2% уксусной кислотой: C1=0,13, С2=0,05, С3=0,04, С4=0,032 г/дл. Графическим методом определена характеристическая вязкость раствора хитозана ([η] 0,54 дл/г). Для расчета Мср использовали уравнение Марка-Куна-Хаувинка; Мср=20-21 кДа.
Определение степени деацетилирования (СДА)
Приготовили 100 мл водного раствора, содержащего 0,2 г олигомерной фракции хитозана. Потенциометрическое титрование 50 мл полученного раствора производили 0,1Н раством NaOH с использованием рН метра рН-150М с универсальным электродом ЭСКЛ 08М.1 при фиксированной температуре 20°С. По полученным данным строили график. Проведен анализ графической зависимости рН=f (D), где D - количество ммоль NaOH. Результаты анализа полученного графика и соответствующий расчет показывают, что на титрование солевой формы олигохитозана (0,10 г) израсходовано 5,6 ммоль NaOH, что соответствует степени деацетилирования олигохитозана 0,91-0,92 т(91-92%).
Способ получения водорастворимых олигомерных гомологов хитозана в гетерогенной системе путем деполимеризации высокомолекулярного хитозана перекисью водорода, отличающийся тем, что процесс деполимеризации хитозана проводится в двухфазной системе, твердой фазой которой является активированный хитозан с Мср=450-650 кДа и средним размером частиц 0,05-0,20 мм, жидкая фаза - водный раствор HOс концентрацией НО в реакционной системе 1-7%, длительностью реакции 120-180 мин и температурой 70°С, далее проводят фазовое разделение образующихся гомологов хитозана путем фильтрации через бумажную или текстильную поверхность полученной реакционной смеси, образовавшийся фильтрат содержит водорастворимые олигомеры хитозана.