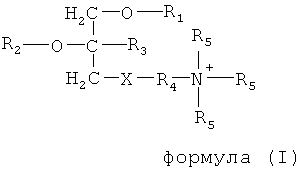Результат интеллектуальной деятельности: ПРИМЕНЕНИЕ ТРИЗАМЕЩЕННЫХ СОЕДИНЕНИЙ ГЛИЦЕРИНА ДЛЯ ЛЕЧЕНИЯ ГЕМАТОЛОГИЧЕСКИХ ЗЛОКАЧЕСТВЕННЫХ ОПУХОЛЕЙ
Вид РИД
Изобретение
Настоящее изобретение относится к применению тризамещенных соединений глицерина в производстве лекарственных средств для лечения гематологических злокачественных опухолей. Изобретение также относится к набору из частей, содержащему такое лекарственное средство. Наконец, изобретение также относится и к соответствующему способу лечения таких состояний, и к in vitro способам определения чувствительности таких опухолевых клеток к лекарственному средству, как определено в изобретении.
Гематологические злокачественные опухоли, такие как лейкоз и лимфома, относятся к разновидностям рака, которые затрагивают кровь, костный мозг и лимфоузлы. На хромосомные транслокации сильно влияет этиология этих заболеваний, тогда как для солидных опухолей это нехарактерно. Это приводит к различным подходам в диагностике и лечении гематологических злокачественных заболеваний (см., например, Dewald G.W. et al (1995) Semin. Oncol. 22, 341-354; Grimwade, D. et al (1998) Blood 92, 2322-2333; Jaffe, E.S. et al (2001) Tumors of hematopoietic and lymphoid tissue. International Agency for Research on Cancer, IARC Press, Lyon, France; Grimwade, D et al (2004) Ann. Hematol. 83, Suppl. 1, S45-S48).
Лечение многих пациентов с диссеминированными гематологическими злокачественными опухолями проводили посредством химиотерапии (возможно в сочетании с облучением) в некоторый момент в течение заболевания. Хотя степень ответных реакций при лечении некоторых злокачественных опухолей, таких как лимфоидные злокачественные опухоли, обычно высока, курс лечения будет приводить к выздоравливанию только подгруппы пациентов. Даже среди лимфоидных злокачественных опухолей некоторые заболевания (например, хронический лимфолейкоз (ХЛЛ); фолликулярная лимфома III/IV стадии, представленная малыми расщепленными клетками; лимфома маргинальной зоны III/IV стадии; лимфома из клеток мантийной зоны III/IV стадии и множественная миелома) в настоящее время не поддаются лечению химиотерапией со стандартными дозировками.
Однако доступные в настоящее время нехирургические терапевтические альтернативы лечения связаны с побочными эффектами препаратов, некоторые из которых довольно тяжелые, которые представляют собой ограничительный фактор для химиотерапевтических подходов для сильно постаревшей части населения с множественными патологиями.
Одной проблемой, связанной с лечением таких злокачественных новообразований, является то, что ремиссия этих опухолей неизбежна даже при или несмотря на применение агрессивного лечебного режима. Длительная терапия химиопрепаратами невозможна, так как степень ответа затем приближается к нулю. Предел дозы облучения также достигается относительно быстро, если планируется эффективно лечить даже первичные опухоли. Таким образом, ситуация в настоящее время такова, что после завершения первого лечебного режима необходимо «ждать» до тех пор, пока не произойдет рецидива.
В настоящее время химиотерапевтические протоколы лечения гематологических злокачественных опухолей включают в себя назначение одного или более антинеопластических агентов (то есть цитостатических и/или цитотоксических химиопрепаратов), таких как алкилирующие агенты, растительные алкалоиды, антиметаболиты, антибиотики, ингибиторы топои-зомераз I и/или II, ингибиторы тирозинкиназ, ингибиторы протеосом и стероиды (см., например, Alexanian, R. et al (1969) JAMA 208, 1680-1685; Rai, K.R. et al. (1981) Blood 58, 1203-1212; Alexanian, R. et al. (1990) Am. J. Hematol. 33, 86-89; Bassan, R. et al., 1992, Leukemia 6 (suppl.2), 186-190; Keating, M.J. et al (1993) Chemotherapy of chronic lymphocytic leukemia, in: Cheson, B.D. (ed.) Chronic Lymphocytic Leukemia. Scientific Advances and Clinical Developments. Marcel Dekker, New York, NY, p.297 ff.; Boulard, F. et al (1993) Cancer Invest. 11, 534-553; Smith, M. et al (1996) J. Clin. Oncol. 14, 18-24; Noordijk, E. et al (1997) Int. J. Radiat. Oncol. Biol. Phys. 39, 173; Miller, T.P. et al (1998) N. Eng. J. Med. 339, 21-26; Drucker, B.J. (2001) N. Engl. J. Med. 344, 1031-1037; Richardson, P.O. et al (2002) ASCO Annual Meeting Proceedings, 11а). Все обычные антинеопластические агенты должны вводиться систематически, так как они представляют собой молекулы, оказывающие также неселективные эффекты на их физиологические мишени. Однако это подразумевает, что такие антинеопластические (цитостатические) агенты, особенно при применении в течение длительного периода времени, будут оказывать пагубный эффект на здоровые клетки организма, то есть их применение связано с серьезными побочными эффектами, в основном проявляющимися на быстро делящихся клетках организма. Обычные побочные эффекты включают в себя, среди прочих, генетические нарушения, тошноту, рвоту, диарею, запоры, выпадение волос, нарушение функций иммунной системы, подавление пролиферации миелоцитов, анемию, геморрагию, цитотоксичность, появление вторичных неоплазий и так далее.
Таким образом, по-прежнему существует необходимость или в альтернативных химиопрепаратах, вызывающих побочные эффекты в меньшей степени при сохранении их фармакологической эффективности, или в любых соединениях, которые необходимо вводить в сочетании с вышеуказанными антинеопластическими агентами, где их комбинация приводит к синергетическим цитостатическим и/или цитотоксическим эффектам на опухолевую клетку по сравнению с индивидуальным применением каждого препарата. Такое комбинирование позволило бы заново назначить уменьшенные дозы антинеопластических препаратов с достижением такой же терапевтической эффективности, но при менее серьезных побочных эффектах.
Тризамещенные соединения глицерина, принадлежащие к классу синтетических алкиллизофосфолипидов с простоэфирной связью, могли бы быть объектами для такого комбинаторного подхода.
Такие синтетические алкиллизофосфолипиды с простоэфирной связью, как известно, проявляют антиканцерогенную активность (описано, например, у Arthur, G. and Bittman, R. (1998) Biochim. Biophys. Acta 1390, 85-102; Jendrossek, V., and Handrick, R. (2003) Curr. Med. Chem. Anti-Canc. Agents 3, 343-353; Mollinedo, F. et al (2004) Curr. Med. Chem. 11, 3163-3184). 1-O-октадецил-2-О-метилглицеро-3-фосфохолин (на который также ссылаются как на ЕТ-18-OCHS, АР-121 или эдельфозин) считается прототипом таких липидов. 1-О-октадецил-2-О-метилглицеро-3-фосфохолин представляет собой синтетический аналог тромбоцит-активирующего фактор (PAF; 1-O-алкил-2-ацетил-sn-глицеро-3-фосфохолин), потенциальный активатор фосфолипидного ряда и посредник во многих функциях лейкоцитов, включая агрегацию тромбоцитов, воспаление и анафилаксию. В отличие от наиболее распространенных химиопрепаратов, эти синтетические липиды с простой эфирной связью не действуют непосредственно на клеточную ДНК, а скорее оказывают эффект на липидный состав плазматической мембраны и/или действуют на различные сигнальные пути. Таким образом, их тип действия не зависит от присутствия определенных клеточных рецепторов или же он зависит от клеточного цикла.
Химиотерапия рака главным образом направлена на замедление роста или на разрушение опухолевых клеток, в то же время избегая коллатеральных повреждений у окружающих клеток и тканей. Следовательно, наиболее эффективными противоопухолевыми агентами являются те, которые могут селективно действовать на раковые клетки, оставляя здоровые клетки незатронутыми. Было показано, что синтетические липиды с простой эфирной связью вызывают подобный эффект (см., например, Magistrelli, A. et al (1995) Drug. Metab. Dispos. 23, 113-118). Некоторые механизмы действия были объяснены токсичным действием липидов с простой эфирной связью на раковые клетки, включая также недостаток у клеток ферментов алкильного расщепления. Итоговая неспособность к гидролизу липидов с простой эфирной связью ведет к их внутриклеточному накоплению и к последующему нарушению организации липидов в клеточной мембране. Другие потенциальные механизмы действия липидов с простой эфирной связью включают в себя эффекты на уровне внутриклеточного фосфорилирования белков и нарушения клеточного метаболизма липидов. Здоровые клетки, в отличие от раковых, обычно обладают способностью избежать или преодолеть потенциальный токсический эффект липидов с простой эфирной связью.
Таким образом, синтетические липиды с простой эфирной связью применялись для лечения солидных опухолей различного типа, таких как опухоли мозга или молочной железы (см., например, German Patent DE 2619686 и Международные Патентные Заявки WO 99/59599 и WO 00/01392 соответственно). Однако, хотя противоопухолевая активность этих липидов с простой эфирной связью была экспериментально показана на отдельных животных опухолевых моделях, их клиническому применению обычно препятствуют системные цитотоксические эффекты, включающие в себя гемолиз, особенно в желудочно-кишечном тракте, и также, среди прочих, в легких, печени и почках.
В настоящее время в большинстве клинических испытаний синтетических липидов с простой эфирной связью соединения вводят пациентам перорально или внутривенно. В этом случае было показано, что внутривенное введение липосомального препарата и липофильной эмульсии «масло-в-воде», соответственно, более благоприятно по сравнению со свободным соединением для улучшения терапевтической эффективности наряду с уменьшением токсического эффекта (см., например, Ahmad, I. et al (1997) Cancer Res.57, 1915-1921 и Международная Патентная Заявка WO 91/09590).
Однако из уровня техники также известно, что определенный фосфолипид с простой эфирной связью и карбамоильные соли наряду с терапевтическим действием у пациентов как конкурентный ингибитор PAF или опухолевого роста при однократной или повторной инъекции вызывают пагубные эффекты в области инъекции. Очевидно, что эти побочные эффекты включают в себя лизис красных кровяных телец, сильный отек, воспаление и некроз в месте инъекции. Эти побочные эффекты часто называют "детергентными" эффектами. В том случае, если требуются повторные инъекции, эти вредные эффекты являются особенно неблагоприятными, так как они делают места введения неприемлемыми и требуются новые места для инъекций. Так как число подходящих мест у пациента ограничено, было бы очень желательно избежать вышеупомянутых побочных эффектов, связанных с внутривенным введением 1-О-октадецил-2-O-метилглицеро-3-фосфохолина.
Довольно недавно было показано, что для того чтобы снизить системные побочные эффекты, возможно также вводить липиды с простой эфирной связью перорально вместе с жидкостью-носителем, годной для питья. В Международной Патентной Заявке WO 99/59599 было описано, что 1-O-октадецил-2-О-метилглицеро-3-фосфохолин может вводиться вместе с носителем на водной или молочной основе, содержащей, по меньшей мере, 3% (масса/масса) жира и/или белка. Заманчивым является предположение, что эффективное связывание 1-O-октадецил-2-O-метилглицеро-3-фосфохолина с белками и/или другими липидами «маскирует» липид с простой эфирной связью, что приводит к уменьшению побочных эффектов.
Тем не менее в 10-20% случаев у пациентов, лечение которых проводилось таким носителем на водной или молочной основе, наблюдалась желудочно-кишечная несовместимость, с которой были связаны потеря аппетита, тошнота и/или рвота, запоры и прочее (см., например, Drings, P. et al (1992) Onkologie 15, 375-382).
Таким образом, остается необходимость в лекарственном средстве для лечения гематологических злокачественных опухолей, которое преодолевает вышеуказанные ограничения. В частности, необходимо лекарственное средство, которое подходит для легкого и удобного введения и обеспечит требуемую фармацевтическую эффективность без серьезных побочных эффектов.
Соответственно, целью настоящего изобретения является поиск такого препарата для лечения гематологических злокачественных опухолей.
Эта цель достигается путем применения тризамещенного соединения глицерина, имеющего признаки независимой формулы 1 для производства соответствующего лекарственного средства, которое может применяться индивидуально или в сочетании с одним или более другими фармацевтическими средствами. Некоторые из предпочтительных вариантов выполнения настоящего изобретения определяются объектами зависимых формул.
По настоящему изобретению было обнаружено, что тризамещенные соединения глицерина, такие как 1-O-октадецил-1-O-метил-глицеро-3-фосфохолин, подходят не только в качестве препарата для селективного лечения гематологических злокачественных опухолей, но также усиливают цитостатический и/или цитотоксический эффекты некоторых известных химиопрепаратов на опухолевые клетки в синергетической манере. Таким образом, эти синергетические эффекты позволяют вводить уменьшенные дозы препаратов для того, чтобы достичь такой же фармацевтической эффективности по сравнению с индивидуальным назначением, что снова будет уменьшать риск появления системных побочных эффектов.
В контексте настоящего изобретения любое определенное числовое значение обычно связано с интервалом точности, который, как будет понятно специалисту в данной области техники, гарантирует технический эффект рассматриваемого признака. Как применяется здесь, отклонение от определенного числового значения лежит в интервале ±10%, и предпочтительно ±5%.
В первом объекте настоящее изобретение относится к применению тризамещенного соединения глицерина по формуле (I) или его энантиомера, диастереомера или фармацевтически приемлемой соли, для производителя лекарственного средства для лечения гематологических злокачественных опухолей
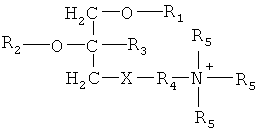
Х выбирается из группы, состоящей из фосфата и сульфата;
R1 выбирается из группы, состоящей из алкилов с 16-20 атомами углерода;
R2 выбирается из группы, состоящей из алкилов с 1-3 атомами углерода и гидроксиалкилов с 1-3 атомами углерода;
R3 выбирается из группы, состоящей из водорода и алкилов с 1-3 атомами углерода;
R4 выбирается из группы, состоящей из алкилов с 1-3 атомами углерода и циклоалкилов с 3-6 атомами углерода;
R5 выбирается из группы, состоящей водорода и метила.
Тризамещенное соединение глицерина по изобретению может применяться в аморфной или кристаллической форме. Использующийся здесь термин «аморфный» обозначает твердое тело, в котором нет расположения атомов дальнего порядка, то есть некристаллический материал. В предпочтительном варианте выполнения изобретения тризамещенное соединение глицерина находится в кристаллической форме.
Термины "Cn алкил","Cn гидроксиалкил" и "Cn циклоалкил", применяемые здесь, обозначают алкильную группу, гидроксиалкильную группу или циклоалкильную группу, имеющую n атомов углерода, соответственно. Например, термин "C18 алкил" относится к алкильной группе, имеющей 18 атомов углерода. Алкильные или гидроксиалкильные группы по изобретению могут быть прямыми или разветвленными.
У тризамещенных соединений глицерина формулы (I) есть один или более асимметрических центров и таким образом они могут существовать в виде энантиомеров или диастереомеров. Соответственно, лекарственное средство, применяемое в настоящем изобретении, может содержать либо один или более отдельных индивидуальных изомеров (таких как L-форма и D-форма), либо смесь изомеров, предпочтительно рацемические смеси.
Тризамещенные соединения глицерина формулы (I) могут содержаться в лекарственном средстве в виде фармацевтически приемлемых солей. Такие соли могут содержать любой фармацевтически приемлемый анион, "нейтрализующий" положительный заряд азота (например, хлорид, бромид или иодид) или фармацевтически приемлемый катион, "нейтрализующий" отрицательный заряд фосфатной группы или сульфогруппы (например, катионы натрия или калия).
В отдельном предпочтительном варианте выполнения настоящего изобретения лекарственное средство содержит тризамещенное соединение глицерина по формуле (I), где Х представляет собой фосфатную группу или сульфогруппу, R1 представляет собой -(СН2)17-СН3, R2 представляет собой СН3, R3 представляет собой Н, R4 представляет собой -(СН2)2- и R5 представляет собой СН3.
Лекарственное средство по настоящему изобретению может находиться в любой фармацевтической лекарственной форме, которая является терапевтически эффективной. Примерами таких фармацевтических лекарственных форм являются среди прочих таблетки, пилюли, капсулы, суспензии, эмульсии, растворы для инъекций или для вливания, настойки, порошки и тому подобное.
Лекарственные средства, применяемые в настоящем изобретении, содержат в себе по меньшей мере один фармацевтически приемлемый эксципиент. Под применяемым здесь термином «фармацевтически приемлемый эксципиент» понимается любое вещество, применяемое для приготовления фармацевтических лекарственных форм, такие как вещества для покрытия, пленкообразующие вещества, наполнители, дезинтегрирующие агенты, вещества, изменяющие высвобождение, вещества-носители, растворители, связывающие агенты и другие адьюванты, каждый из которых хорошо известен в области технике (см. ссылки, указанные ниже). Предпочтительно эксципиент, применяемый в изобретении, содержит по меньшей мере один наполнитель, по меньшей мере один связывающий агент, по меньшей мере один дезинтегрирующий агент, по меньшей мере один агент, контролирующий текучесть и по меньшей мере одно смазывающее вещество.
Лекарственное средство может вводиться любым парентеральным или непарентеральным путем введения. Парентеральные способы применения содержат, например, способы внутрикожных, подкожных, внутримышечных или внутривенных инъекций и вливаний. Непарентеральные способы введения включают, например, пероральное или местное введение. Более того, лекарственное средство может вводиться как местно, так и системно.
Предпочтительно, лекарственное средство, применяемое по настоящему изобретению, находится в твердой лекарственной форме, особенно предпочтительно в форме фармацевтического твердого препарата, подходящего для перорального применения. Примеры таких лекарственных форм включают среди прочих таблетки, пилюли, капсулы, горошки, гранулы, порошки, мультичастичные формы (например, шарики, гранулы или кристаллы) и драже. Стандартные дозы мультичастичных форм могут быть включены в фармацевтическую твердую лекарственную форму, например, посредством сжатия или формования в таблетки, или помещения необходимого количества компонентов внутрь желатиновой капсулы.
Все эти твердые лекарственные формы для перорального применения, так же как и способы их приготовления, хорошо известны в области технике (см., например, Gennaro, A.L. and Gennaro, A.R. (2000) Remington: The Science and Practice of Pharmacy, 20th Ed., Lippincott Williams & Wilkins, Philadephia, PA; Ritschet, W.A. & Bauer-Brandl, A. (2002) Die Tablette: Hand-buch der Ehtwicklung, Herstellung und Qualitatssicherung. Editio-Cantor Verlag, Auendorf, Germany; Crowder, T.M. et al (2003) A Guide to Pharmaceutical Particulate Science. Interpharm/CRC, Boca Raton, FL; Stricker, H. (2003) Arzneiformenentwicklung, Springer Verlag, Berlin, Germany; Niazi, S.K. (2004) Handbook of Pharmaceutical Manufacturing Formulations, CRC Press, Boca Raton, FL).
В предпочтительном варианте выполнения изобретения фармацевтическая твердая лекарственная форма выбирается из группы, состоящей из таблеток, пилюль, капсул и гранул, причем таблетки являются наиболее предпочтительными.
В другом предпочтительном варианте выполнения изобретения твердая лекарственная форма представляет собой энтеральную лекарственную форму. То есть лекарственная форма остается стабильной в желудке, то есть в сильнокислой среде, со значениями рН≤2.5. Это может достигаться путем применения твердой лекарственной формы, содержащей пленочное покрытие. Например, изобретенная лекарственная форма может быть в форме так называемой таблетки с пленочным покрытием.
Способы приготовления лекарственных форм с пленочным покрытием также хорошо известны в области технике (см., например, Gennaro, A.L. and Gennaro, A.R. (2000) Remington: The Science and Practice of Pharmacy, 20th Ed., Lippincott Williams & Wilkins, Philadephia, PA; Ritschet, W.A. & Bauer-Brandl, A. (2002) Die Tablette: Handbuch der Ehtwicklung, Herstellung und Qualitätssicherung. Editio-Cantor Verlag, Auendorf, Germany; Crowder, T.M. et al (2003) A Guide to Pharmaceutical Particulate Science. Interpharm/CRC, Boca Raton, FL; Stricker, H. (2003) Arzneiformenentwicklung, Springer Verlag, Berlin, Germany; Niazi, S.K. (2004) Handbook of Pharmaceutical Manufacturing Formulations, CRC Press, Boca Raton, FL). Более того, специалист в данной области также знает, как создать пленочные покрытия со специфическими свойствами, как, например, энтеросолюбильные покрытия, пленочные покрытия, которые растворяются при контакте с жидкостями организма, покрытия, контролирующие высвобождение лекарственного средства, покрытия, маскирующие вкус, и дезинтегрирующие покрытия. В особенно предпочтительном варианте выполнения изобретения твердая лекарственная форма изобретения содержит энтеросолюбильное покрытие.
По настоящему изобретению, необходимо понимать, что тризамещенное соединение глицерина присутствует в лекарственном средстве в любом количестве, эффективном для достижения желаемого фармацевтического эффекта, такого как остановка прогрессии опухоли или индуцирование апоптотического эффекта в опухолевых клетках при введении пациенту. Эффективные количества обычно выбираются по ряду факторов, например возраст, рост и общее состояние пациента, и медицинское состояние, подлежащее лечению, и определяются разнообразными средствами, например испытания по систематизации доз, хорошо известные и легко применяемые на практике специалистом в данной области технике.
Обычно количество тризамещенного соединения глицерина формулы (I) в лекарственном средстве по настоящему изобретению составляет менее 400 мкг, предпочтительней в интервале от 30 до 250 мкг и наиболее предпочтительно в интервале от 50 до 150 мкг. В отдельных вариантах выполнения данного изобретения количество тризамещенного соединения глицерина формулы (I) в лекарственном средстве составляет 75 и 100 мкг соответственно.
Суточная доза тризамещенного соединения глицерина в лекарственном средстве, вводимом пациенту, составляет менее 1200 мкг, обычно менее 900 мкг, предпочтительней в интервале от 30 до 600 мкг, еще более предпочтительно в интервале от 40 до 400 мкг и наиболее предпочтительно в интервале от 50 до 350 мкг. В специфических вариантах выполнения данного изобретения суточная доза составляет 75, 100, 150, 200, 225 и 300 мкг. Предпочтительно, чтобы суточная доза тризамещенного соединения глицерина вводилась как однократная доза в виде 1-4 таблеток или капсул. Однако также возможно вводить соединение в форме многократных доз, например двух или трех индивидуальных доз в течение дня, например утром, в обед и вечером.
Применяемый здесь термин «гематологические злокачественные опухоли» (или «гематологические неоплазмы») обозначает все разновидности рака, затрагивающие кровеносную систему, костный мозг или органы лимфатической системы. Гематологические злокачественные опухоли включают среди прочих лейкоз, лимфому, множественную миелому и миелодиспластический синдром.
Применяемый здесь термин «лейкоз» подразумевает под собой все разновидности рака кровеносной системы или костного мозга, характеризующиеся аномальной пролиферацией клеток крови, обычно белых кровяных телец (то есть лейкоцитов). В объеме данного изобретения этот термин включает в себя все острые и хронические формы лейкозов так же как или все формы лимфо- или миелолейкозов. Разновидности лимфолейкозов (или лимфоцитарных лейкозов) характеризуются воздействием на лимфоидные клетки (то есть агранулоциты), такие как лимфоциты и моноциты, в то время, как когда затронуты миелоидные клетки (то есть гранулоциты), такие как эозинофилы, нейтрофилы и базофилы, болезнь относят к миелолейкозам (или к миелогенным лейкозам). В предпочтительных вариантах выполнения изобретения лейкоз выбирается из группы, состоящей из острого миелолейкоза (ОМЛ), острого лимфолейкоза (ОЛЛ), хронического миелолейкоза (ХМЛ) и хронического лимфолейкоза (ХЛЛ).
Применяемый здесь термин «лимфома» подразумевает под собой все формы рака лимфоцитарного происхождения, которые включают в себя лимфому Ходжкина, характеризующуюся обычно происхождением от одного лимфатического узла и присутствием клеток Рида-Стернберга, так же как и все виды неходжкинских лимфом. В предпочтительных вариантах выполнения изобретения, гематологическая злокачественная опухоль выбирается из группы, состоящей из лимфомы Ходжкина и неходжкинской лимфомы.
Применяемый здесь термин «множественная миелома» (так же упоминаемая как «миелома» или «плазмоцитома») обозначает разновидность рака клеток плазмы, то есть клеток иммунной системы в костном мозге, продуцирующих антитела.
Применяемый здесь термин «миелодиспластический синдром» (прежде известный как «предлейкоз») обозначает отличное накопление гематологических состояний, объединенных неэффективным продуцированием клеток крови и различными видами риска трансформации в острый миелолейкоз. Часто присутствует анемия, требующая постоянного переливания крови. Не являясь действительной злокачественной неоплазмой, миелодиспластический синдром тем не менее классифицируется как относящийся к гематологическим неоплазмам.
Лекарственное средство по изобретению можно применять для лечения гематологических опухолей индивидуально или в комбинации с по меньшей мере одним другим фармацевтическим средством, содержащим по меньшей мере один дополнительный активный ингредиент. То есть, такое дополнение тоже находится в объеме настоящего изобретения, где лекарственное средство, содержащее тризамещенное соединение глицерина, применяется совместно с по меньшей мере одним другим фармацевтическим средством, содержащим один или более дополнительные активные ингредиенты, то есть активные ингредиенты, отличные от тризамещенных соединений глицерина, заявленных в пункте 1. В предпочтительных вариантах выполнения изобретения один или более дополнительные активные ингредиенты выбираются из группы, состоящей из антител к одному или более эпитопам на поверхности гематологических клеток (гематопоэтической клетки).
Применяемый здесь термин «антинеопластические агенты» (так же упоминаемый здесь как «цитостатические лекарственные средства») подразумевает под собой фармацевтические средства, которые действует на клеточный кариокинез (то есть митоз) и цитокинез (то есть деление клетки), в частности, в злокачественных клетках (то есть опухолевых клетках), в которых он вызывает замедление, задержку или угнетение вышеуказанных процессов. Также сюда включены цитостатические лекарственные средства, проявляющие еще и цитотоксический эффект, то есть фармацевтические средства, вызывающие гибель клетки путем воздействия на кариокинез и/или цитокинез.
Примерами антинеопластических агентов (цитостатических лекарственных средств), которые можно применять в настоящем изобретении, являются среди прочих алкилирующие агенты, антиметаболиты, растительные алкалоиды, антибиотики, ингибиторы топоизомераз I и/или II, ингибиторы тирозикиназ, ингибиторы протеасом и ДНК интеркалирующие агенты.
Применяемый здесь термин «алкилирующие агенты» обозначает соединения, способные присоединять алкильные группы к различным электроотрицательным группам, присутствующим в клеточных молекулах, таких как нуклеиновые кислоты или белки. Обычно эти соединения воздействуют на рост и прогрессию опухоли через поперечные сшивки гуанина в цепях ДНК. Такая модификация предотвращает раскручивание ДНК и разделение цепей и, следовательно, репликацию ДНК.
В предпочтительных вариантах выполнения изобретения алкилирующие агенты выбираются из группы, содержащей азотистые иприты, нитрозомочевины, производные платины и алкилсульфонаты. Примерами азотистых ипритов являются среди прочих хлорамбуцил (ХЛЛ), циклофосфамид (лимфомы), мелфалан (множественная миелома) и мехлоретамин (лимфомы Ходжкина). Примерами нитрозомочевин среди прочих являются кармустин (лимфомы) и карбоплатин (лимфомы, ОЛЛ). Примерами алкилсульфонатов являются среди прочих бусульфан (ХМЛ) и треосульфан (лимфомы).
Применяемый здесь термин «антиметаболиты» подразумевает под собой химические соединения со структурой, подобной соединению (метаболиту), которое требуется для клеточных биохимических реакций, однако достаточно отличающиеся для того, чтобы не воздействовать на нормальные клеточные функции.
В предпочтительных вариантах выполнения изобретения антиметаболиты выбираются из группы, состоящей из метотрексата (ОЛЛ), аналогов пурина и пиримидиновых аналогов. Примерами аналогов пурина являются среди прочих флударабин (Неходжкинская лимфома, ОМЛ), пентостатин (ХЛЛ) и кладрибин (ХЛЛ), а примерами пиримидиновых аналогов являются среди прочих цитарабин (лийкоз, неходжкинские лимфомы) и децитабин (миелодиспластический синдром).
Примерами растительных алкалоидов (то есть встречающихся в природе или полученных синтетическим путем растительные амины), которые могут быть применены в настоящем изобретении, являются среди прочих винкристин (неходжкинские лимфомы, ОЛЛ) и винбластин (лимфома Ходжкина). Примеры антибиотиков, которые могут быть применены в настоящем изобретении, включают среди прочих митоксантрон (ОМЛ), эпирубицин (лимфомы), доксорубицин (лимфома Ходжкина), даунорубицин (ОМЛ, ОЛЛ) и блеомицин (лимфома Ходжкина). Ингибиторы топоизомераз действуют на нормальную функцию топоизомераз типа I и/или типа II, то есть на ферменты, которые действуют на топологию ДНК. В объеме настоящего изобретения предпочтительным ингибитором топоизомеразы II является этопозид (лимфомы, ОМЛ, ХМЛ) или тенипозид (ОЛЛ).
Остальные антинеопластические агенты, которые необходимо использовать в изобретении, включают в себя среди прочих стероидный гормон дексаметазон (неходжкинские лимфомы), ингибитор тирозинкиназ иматиниб (ХМЛ), ингибитор протеасом бортезомиб (множественная миелома) и ДНК интеркалирующие агенты амсакрин (ОЛЛ, ОМЛ) и талидомид (множественная миелома).
Соответствующее первичное медицинское применение вышеупомянутых антинеопластических агентов в объеме настоящего изобретения указано в скобках. Однако это не препятствует применению любого из этих препаратов для лечения любых других гематологических злокачественных опухолей. Более того, также возможно применять сочетание двух или более этих препаратов для лечения любой гематологической злокачественной опухоли.
В отдельном предпочтительном варианте настоящего изобретения антинеопластические агенты выбираются из группы, состоящей из хлорамбуцила, циклофосфамида, мелфалана, мехлоретамина, кармустина, цисплатина, карбоплатина, бусульфана, треосульфана, метотрексата, флударабина, клофарабина, пентостатина, кладрибина, цитарабина, децитабина, винкристина, винбластина, митоксантрона, эпирубицина, доксорубицина, даунорубицина, блеомицина, этопозида, тенипозида, дексаметазона, иматиниба, бортезомиба, амсакрина и талидомида.
Антитела, применяемые в настоящем изобретении, включают моноклональные и поликлональные антитела к одному или более эпитопам на поверхности гематологических (гематопоэтической) клеток. Применяемый здесь термин «гематологические (гематопоэтические) клетки» обозначает все клетки гематопоэтического происхождения, включая клетки миелоидного и лимфоцитарного происхождения. Применяемый здесь термин «к одному или более эпитопам на поверхности клетки» подразумевает под собой тот факт, что антитело, применяемое в настоящем изобретении, может распознавать/связывать одну или более молекул клеточной поверхности (то есть эпитопов) гематологической клетки.
В предпочтительных вариантах выполнения изобретения антитело является моноклональным антителом, то есть антителом к специфическому антигену, которое производится популяцией В-лимфоцитов, которые все являются клонами одной первоначальной клетки, продуцирующей антитела. Антитело может быть человеческим или химерным (гуманизированным) антителом, например химерным антителом мыши/человека. Способы получения таких «сконструированных» моноклональных антител хорошо известны в области техники (см., например, Colligan, J.E. et al (2002) Current Protocols in Immunology, Wiley & Sons, Hoboken, NJ).
Примерами таких антител, которые могут быть применены в настоящем изобретении, являются среди прочих алемтузумаб (анти-CD52; ХЛЛ, лимфомы), ритуксимаб (анти-CD20; ХЛЛ, неходжкинская лимфома), гентузумаб озогамицин (анти-CD33, ОМЛ).
Во втором объекте настоящее изобретение относится к соответствующим способам для предотвращения и/или для лечения гематологических злокачественных опухолей, где способ содержит:
(a) введение пациенту лекарственного средства или комбинации лекарственных средств, как определено в изобретении.
Как схематически описано выше, лекарственное средство или комбинация лекарственных средств по настоящему изобретению могут вводиться любым парентеральным или непарентеральным путем. В случае применения комбинации лекарственных средств, индивидуальные фармацевтические средства могут вводиться одним и тем же или разными путями. Предпочтительно лекарственное средство, содержащее тризамещенное соединение глицерина, вводится перорально, и еще более предпочтительно, если лекарственное средство находится в твердой лекарственной форме. Более того, лекарственное средство предпочтительно вводится в виде однократной дозы в форме одной таблетки или одной капсулы в день. Однако также возможно вводить лекарственное средство в форме многократных доз, так, например, как две или три индивидуальные дозы в течение дня. В случае применения комбинации лекарственных средств (как, например, в форме набора из частей), индивидуальные фармацевтические средства (то есть лекарственное средство, содержащее тризамещенное соединение глицерина и по меньшей мере одно другое фармацевтическое средство) могут вводиться одновременно, отдельно или по очереди. Например, возможно вводить одно лекарственное средство во время еды, а другой через один или более часов.
В предпочтительном варианте выполнения изобретения, способ, кроме того, содержит:
(b) определение степени экспрессии гена Fas рецептора в одной или более злокачественных клетках у пациента, которому необходимо проводить курс лечения, перед введением лекарственного средства или комбинации лекарственных средств.
Как уже схематично описывалось выше, рецептор клеточной гибели Fas (так же известный как АРО-1 или CD95) был идентифицирован как клеточная мишень для 1-O-октадецил-1-O-метил-глицеро-3-фосфохолина (см., например, Gajate, С.et al (2004) J. Exp. Med. 200, 353-365; Nieto-Miguel, T. et al (2006) J. Biol. Chem. 281, 14833-14840). В объеме настоящего изобретения было обнаружено, что злокачественные гематологические клетки (то есть опухолевые клетки), гиперэкспрессирующие Fas рецептор, показывают увеличенную чувствительность к лечению лекарственным средством, как определено в формуле изобретения.
Применяемый здесь термин «экспрессия» или «экспрессия генов» подразумевает под собой сумму регуляторных сигнальных путей, превращающих информацию, закодированную в последовательности нуклеиновых кислот гена, в первую очередь, в матричную-РНК (мРНК), а затем в белок. Соответственно, экспрессия гена содержит его транскрипцию в первичную гетерогенную ядерную РНК (гяРНК), процессинг этой гяРНК в зрелую матричную РНК и трансляцию последовательности мРНК в соответствующую аминокислотную последовательность белка.
Применяемый здесь термин «гиперэкспрессирующий» подразумевает под собой уровень экспрессии, составляющий по меньшей мере 100% от уровня экспрессии у незлокачественных (нетуморогенных) клеток контроля (то есть клеток дикого типа). Соответственно, в одном из вариантов выполнения изобретения способ, кроме того, содержит сравнение результатов измерения, полученных на опухолевых клетках, с результатами, полученными на одной или более контрольных клеток здорового организма.
Термин «определение» подразумевает под собой любой способ для определения «продукта экспрессии гена». В объеме настоящего изобретения термин «продукт экспрессии гена» подразумевает не только белок, закодированный в гене, но и соответствующую мРНК, которую можно назвать «первым продуктом экспрессии гена» во время экспрессии генов. Эти способы содержат хорошо известные в области технике стандартные процедуры (см., например, Sambrook, J. et al (1989) Molecular Cloning: A Laboratory Manual. 2nd ed. Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY; Ausubel, F.M. et al (2001) Current Protocols in Molecular Biology. Wiley & Sons, Hoboken, NJ). Примерами таких способов являются ОТ-ПЦР, тест, основанный на защите от РНКазы, Нозерн блоттинг, Вестерн блоттинг, иммуноферментный анализ, радиоиммунный анализ или флуоресцентное титрование.
Например, содержание мРНК можно определить путем гибридизации с меченым зондом нуклеиновых кислот (ДНК или РНК) и последующего анализа с помощью либо Нозерн блоттинга, либо с помощью теста, основанного на защите от РНКазы. Альтернативно может быть получена соответствующая кДНК из клеточной РНК (либо общей РНК, либо мРНК) путем обратной транскрипции и проанализирована в отсутствии и присутствии отдельных видом нуклеиновых кислот путем ПЦР-амплификации (то есть ОТ-ПЦР). Белки можно легко детектировать, используя специфические антитела, которые могут быть моноклональными или поликлональными. Для визуализации можно пометить антитело или использовать конъюгат вторичного антитела с подходящей меткой. Определение может быть проведено, например, путем Вестерн блоттинга или иммуноферментного анализа ELISA. Подходящие метки для осуществления способов, указанных в изобретении, включают в себя ферментные метки, радиоактивные метки, флуоресцентные метки, хромогенные метки, люминесцентные метки, ди-гоксигенин, биотин, малые органические молекулы, металлы, комплексы металлов и коллоидное золото.
В другом предпочтительном варианте выполнения изобретения, способ, кроме того, содержит:
(с) определение одного или более из следующего в одной или более злокачественных клетках пациента, которому необходимо провести курс лечения, перед введением лекарственного средства или комбинации лекарственных средств:
(i) присутствие или отсутствие одной или более мутаций в гене ras;
(ii) присутствие или отсутствие одной или более мутаций в гене FGFR3;
(iii) присутствие или отсутствие одной или более мутаций в гене PTEN.
В одном из вариантов выполнения способ, кроме того, содержит сравнение результатов, полученных от одной или более злокачественных клеток, с результатами, полученными от одной или более клеток контроля, то есть нетуморогенных клеток, от здорового организма.
Применяемый здесь термин «мутация в гене ras» подразумевает любое генетическое изменение члена семейства генов ras, то есть генов Н-ras, К-ras, N-ras, в частности генов ras человека (см. Land, H. et al (1983) Science 222, 771-778). Генетические изменения по настоящему изобретению включают в себя добавление, удаление и замещение одного или более нуклеотидов в соответствующей последовательности ДНК. Предпочтительно, чтобы такие одна или более мутаций приводили к измененной аминокислотной последовательности соответствующего белка Ras, что также включает образование усеченного или удлиненного белка. Такие мутации также могут затрагивать функции белка. Например, они могут вызывать (конститутивную) активацию белка Ras или могут приводить к доминантно-негативной разновидности белка Ras. Примерами таких мутаций в генах ras являются среди прочих мутации, затрагивающие кодоны 12, 13 и 61 в человеческом N-ras, так же как и кодоны 12 и 71 в человеческом К-ras (см. ссылки ниже).
В предпочтительном варианте выполнения изобретения одна или более мутаций в гене ras вызывают активацию соответствующего белка Ras (то есть увеличение активности белка Ras). Особенно предпочтительные примеры таких мутаций в гене ras содержат среди прочих мутации в кодоне 61 человеческого N-ras, включая CAA→CGA и САА→САС, так же как и мутации в кодоне 12 человеческого К-ras, включающие GGT→GCT и GGT→GAT (см., например, Воз, J.L. et all (1984) Nucl. Acids Res. 12, 9155-9163; Pilz, R.B. et al (1997) Cell Growth Diff. 8, 53-59; Delgado, M.D. et al (2000) Oncogene 19, 783-790; Chesi, M. et al (2001) Blood 97, &29-736).
Применяемый здесь термин «мутация в гене FGFR3» подразумевает под собой любое генетическое изменение в гене рецептора 3 фактора роста фибробластов (FGFR3), в частности в гене FGFR3 человека (Ornitz, D.M. and ltoh, N. (2001) Genome Biol. 2, обзоры 3005.1-3005.12). Генетические изменения по настоящему изобретению включают добавление, удаление и замещение одного или более нуклеотидов соответствующей последовательности ДНК. Предпочтительно, чтобы одна или более мутаций приводила к измененной аминокислотной последовательности соответствующего белка FGFR3, что также включает образование усеченного или удлиненного белка. Такие мутации также могут влиять на функции белка. Например, они могут вызывать (конститутивную) активацию белка FGFR3 или могут приводить к доминантно-негативной разновидности белка FGFR3. Примерами таких мутаций в гене FGFR3 являются среди прочих мутации, затрагивающие кодоны 373, 384 и 650 в человеческом FGFR3, так же как и делеция стоп-кодона в человеческом FGFR3 (см. ссылки ниже).
В предпочтительном варианте выполнения изобретения одна или более мутаций в гене FGFR3 вызывают активацию соответствующего белка FGFR3 (то есть увеличение активности белка FGFR3). Особенно предпочтительные примеры таких мутаций в гене FGFR3 содержат среди прочих мутации в кодоне 373 человеческого FGFR3, включающие TAT→TGT, мутации в кодоне 650 человеческого FGFR3, включающие AAG→GAG, и делецию стоп-кодона в человеческом FGFR3 (см., например, Chesi, M. et al (1997) Nat. Genet. 16, 260-264, Chesi, M. etal (2001) Blood 97, 729-736).
В отдельных предпочтительных вариантах выполнения присутствие или отсутствие одной или более мутаций в гене FGFR3 определяется в сопутствующем присутствии t(4; 14) хромосомной транслокации. То есть последовательность гена FGFR3 анализируется на одной или более злокачественных клетках (таких как гематопоэтические клетки), несущих указанную хромосомную транслокацию.
Применяемый здесь термин «t(4; 14) хромосомная транслокация» обозначает кариотипически «молчащую» генетическую транслокацию, то есть аномальное хромосомное перерасположение, вызванное взаимным обменом участками между негомологичными хромосомами, в человеческой хромосоме 14, в частности это обозначает транслокацию t(4; 14)(p16; q32), которая ведет к дисрегуляции экспрессии гена рецептора 3 фактора роста фибробластов FGFR3 (см., например, Richelda, R. et al (1997) Blood 90, 4062-4070, Chesi, M. et al (2001) Blood 97, 729-736).
Присутствие t(4; 14) хромосомной транслокации в одной или более злокачественных клетках, которые необходимо проанализировать, могут среди прочего быть определено путем классического анализа по Саузерну (см., например, Sambrook, J. et al (1989), supra; Ausubel, F.M. et al (2001), supra) или методиками гибридизации in situ, предпочтительно, флуоресцентной гибридизации in situ (FISH) (см., например, van der Ploeg, M. (2000) Eur. J. Histochem. 44, 7-42; Levsky, J.M. and Singer, R.H. et al (2003) J. Cell Sci. 116, 2833-2838).
Применяемый здесь термин «мутация в гене PTEN» подразумевает любое генетическое изменение гена опухолевого супрессора PTEN, в частности человеческого гена PTEN (см., например, Sakai, A. et al (1998) Blood 92, 3410-3415; Wu, H. et al (2003) Oncogene 22, 3113-3122). Генетические изменения по настоящему изобретению включают в себя добавление, удаление и замещение одного или более нуклеотидов соответствующей последовательности ДНК. Предпочтительно, чтобы одна или более мутаций приводила к измененной аминокислотной последовательности соответствующего белка PTEN, что также включает образование усеченного или удлиненного белка. Такие мутации также могут влиять на функции белка. Например, они могут вызывать активацию (конститутивную) белка PTEN или могут приводить к доминантно-негативной разновидности белка PTEN.
Предпочтительные примеры мутаций в гене PTEN, которые необходимо определить в настоящем изобретении, включают среди прочих делецию экзонов 2-5 в гене PTEN человека, делецию двух пар оснований и инсерцию 9 пар оснований в кодоне 234 и инсерцию 39 пар оснований в кодоне 246 гена PTEN человека, соответственно.
Соответственный анализ генов ras, FGFR3 и PTEN производится по установленным стандартным лабораторным способам обычно путем полимеразной цепной реакции (ПЦР), рестрикционного анализа и/или анализа последовательности ДНК (см., например, Sambrook, J. et al (1989), supra; Ausubel, F.M. et al (2001), supra).
Вместо или в дополнение к определению присутствия или отсутствия одной или более мутаций в генах ras, FGFR3 и/или PTEN, соответственно, каждый из которых влияет на MAPK/ERK- и/или Р13/АКТ- сигнальные пути (описано в Johnson, G.L. and Lapadat, R. (2002) Science 298, 1911-1913; Lee, J.T., and McCubrey, J.A. (2002) Leukemia 16, 486-507; Platanias, L.C. (2003) Blood 101, 4667-4679; Meier, F. et al (2005) Front. Biosci. 10, 2986-3001; Martelli, A.M. et al (2006) Leukemia 20, 911-928), также возможно в объеме данного изобретения определить «статус активности» (то есть происходит активация или нет) в соответствующих сигнальных путях "как таковых". Например, активация MAPK/ERK сигнального пути может быть определена путем измерения фосфорилирования ERK-1/2 с помощью иммунохимических способов, хорошо известных в этой области техники, таких как Вестерн блоттинг, иммунопреципитация и иммуноферментный анализ ELISA, предпочтительно с применением специфических фосфорилирующих анти-ERK-1/2 антител, коммерчески доступных от разных производителей (обзор иммунологических методов можно посмотреть в Coico, R. et а (2006) Current Protocols in Immunology. Wiley & Sons, Hoboken, NJ).
В третьем объекте настоящее изобретение относится к in vitro способу определения чувствительности одной или более злокачественных клеток к лекарственному средству или к комбинации лекарственных средств, как определено в изобретении, способ содержит:
(а) определение степени экспрессии гена рецептора Fas в одной или более злокачественных клетках.
В предпочтительном варианте выполнения изобретения способ, кроме, того содержит:
(b) определение одного или более из следующего в одной или более злокачественных клетках
(i) присутствие или отсутствие одной или более мутаций в гене ras;
(ii) присутствие или отсутствие одной или более мутаций в гене FGFR3; и
(iii) присутствие или отсутствие одной или более мутаций в гене PTEN.
В предпочтительных вариантах выполнения изобретения присутствие или отсутствие одной или более мутаций в гене FGFR3 определяется в сопутствующем присутствии t(4; 14) хромосомной транслокации.
Возможно, но не обязательно, способ далее содержит:
(c) сравнение результатов измерений, полученных в (а) и/или (b) с результатами, полученными в одной или более контрольных клетках.
В четвертом объекте настоящее изобретение относится к тризамещенному соединению глицерина, как определено здесь, для лечения гематологических злокачественных опухолей. В предпочтительных вариантах выполнения изобретения гематологические злокачественные группы выбираются из группы, состоящей из лейкоза, лимфомы, множественной миеломы и миелодиспластического синдрома.
В пятом объекте настоящее изобретение относится к набору из частей, содержащему лекарственное средство для лечения гематологических злокачественных опухолей, причем лекарственное средство содержит тризамещенное соединение глицерина, как определено в изобретении.
В предпочтительных вариантах выполнения набор из частей, кроме того, содержит другое лекарственное средство, содержащее один или более дополнительных активных ингредиентов. Особенно предпочтительно, один или более дополнительных активных ингредиентов выбираются из группы антинеопластических агентов, либо выбираются из группы антител, где указанные антитела направлены против одного или более эпитопов на поверхности гематологических клеток, как определено выше.
Компоненты (части) набора (то есть индивидуальные лекарственные средства или активные ингредиенты) могут вводиться в течение комбинированного лечения (протокола) одновременно, раздельно или по очереди (см., например, Sambrook, J. et al (1989), supra; Ausubel, F.M. et al (2001), supra).
Далее изобретение описывается следующими рисунками и примерами, которые представлены только для того, чтобы проиллюстрировать специфические варианты выполнения этого изобретения и не должны быть истолкованы как ограничивающие объем этого изобретения каким-либо образом.
Вещества, примененные при тестировании, являются либо коммерчески доступными, либо могут быть легко приготовлены из коммерчески доступных веществ специалистами в данной области техники.
ЧЕРТЕЖИ
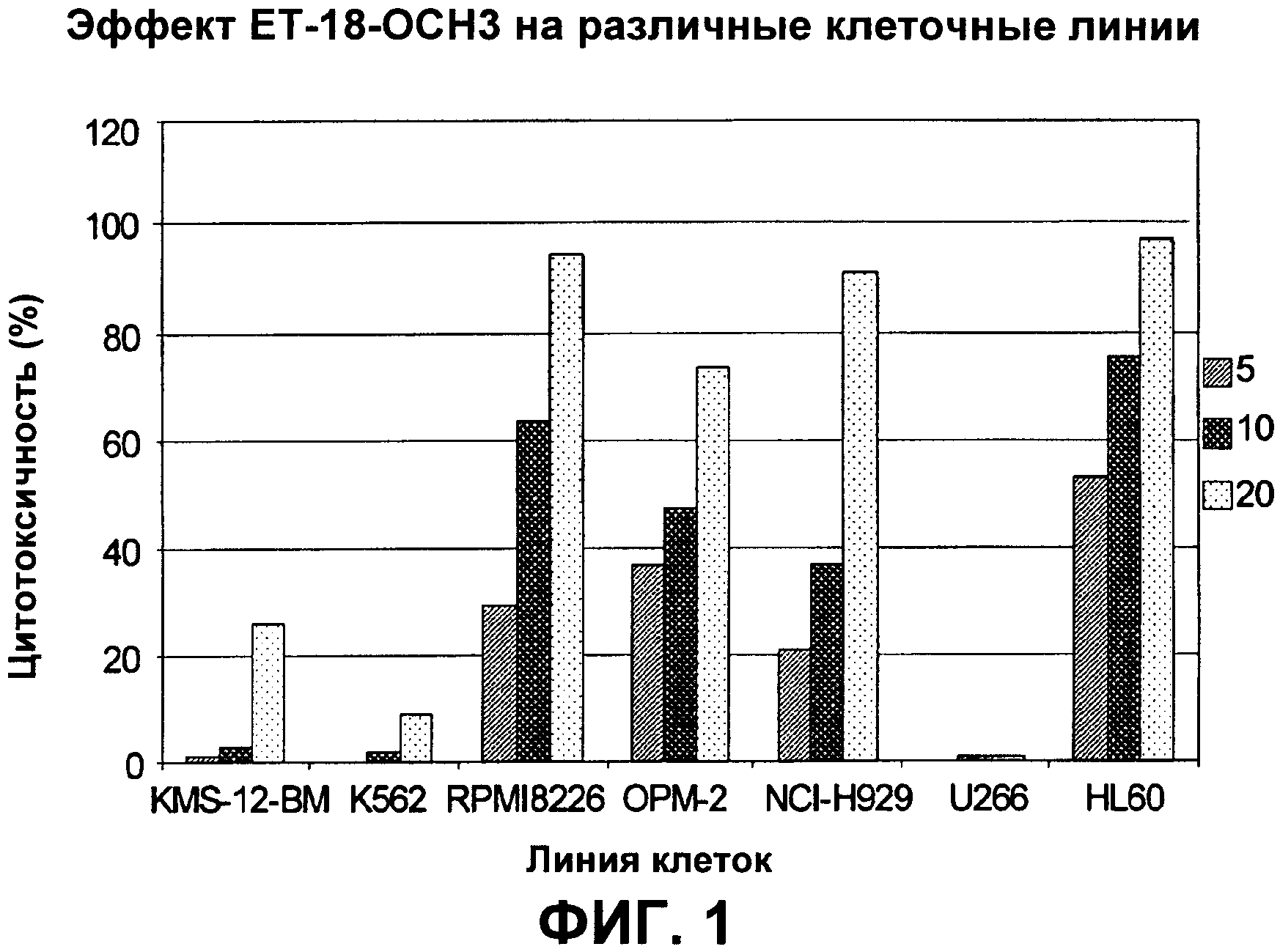
Фиг.1 показывает цитотоксические эффекты ЕТ-18-ОСН3 (1-O-октадецил-2-O-метилглицеро-3-фосфохолин) на различные линии опухолевых клеток. Были применены следующие клеточные линии: KMS-12-BM, К562, RPMI8226, ОРМ-2, NCl-H929, U266 и HL60. Клетки культивировали на 96-луночных планшетах объемом 200 мкл до концентрации 1×106 клеток/мл. Затем клетки инкубировали в течение 20 ч с 5 мкг/мл, 10 мкг/мл и 20 мкг/мл ЕТ-18-ОСН3 (конечные концентрации), соответственно. Гибель клеток наблюдали, окрашивая клетки 7-аминоактиномицином D (конечная концентрация 200 мкг/мл), анализ проводили путем проточной цитофлуориметрии, как описано в литературе (см., например, Schmid, I. et al (1994) J. Immunol. Meth. 170, 145-157; Ayuk, F.A. et al (2005) Exp. Hematol. 33, 1531-1536).
Фиг.2 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в сочетании с бортезомибом (Velcade®), ингибитором протеасомы 26S, на клетки Jurkat. Клетки культивировали, как описано для Фиг.1. ЕТ-18-ОСН3 добавляли в конечной концентрации 2.5 или 5.0 мкг/мл («Е2.5» и «Е5», соответственно) без или в комбинации с 5 или 10 нг/мл бортезомиба («Vel5» и «Vel10», соответственно), затем клетки инкубировали в течение 20 ч. Гибель клеток наблюдали, как описано для Фиг.1. Результаты представлены как среднее значение ± стандартное отклонение из трех независимых экспериментов.
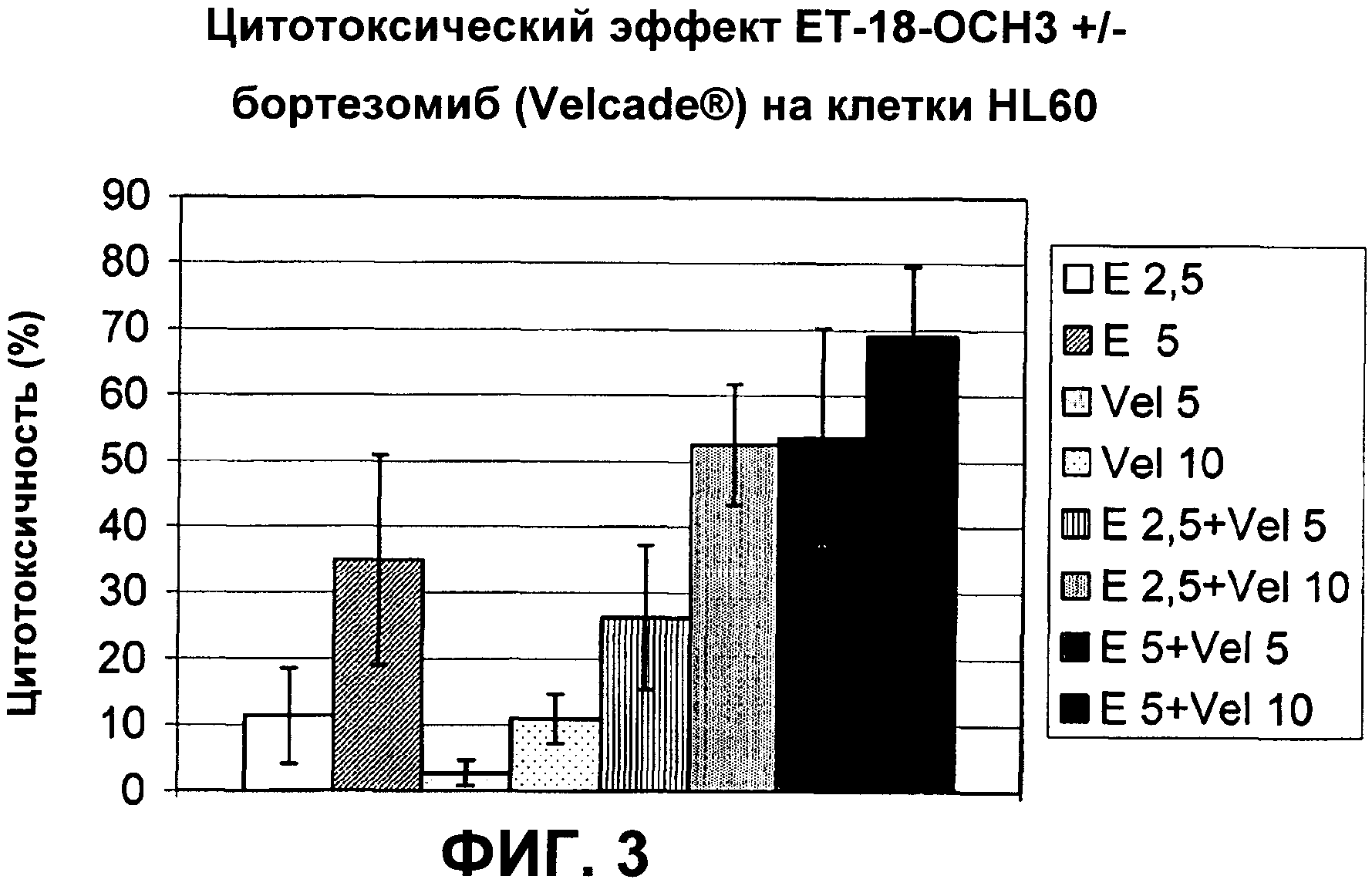
Фиг.3 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с бортезомибом на клетки HL60. Культуру клеток, концентрации соединений и условия эксперимента были идентичны описанным для Фиг.2. Результаты представлены как среднее значение ± стандартное отклонение из четырех независимых экспериментов.
Фиг.4 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с бортезомибом на клетки RPMI8226. Культуры клеток, концентрации соединений и условия эксперимента были идентичны описанным для Фиг.2. Результаты представлены как среднее значение ± стандартное отклонение из трех независимых экспериментов.
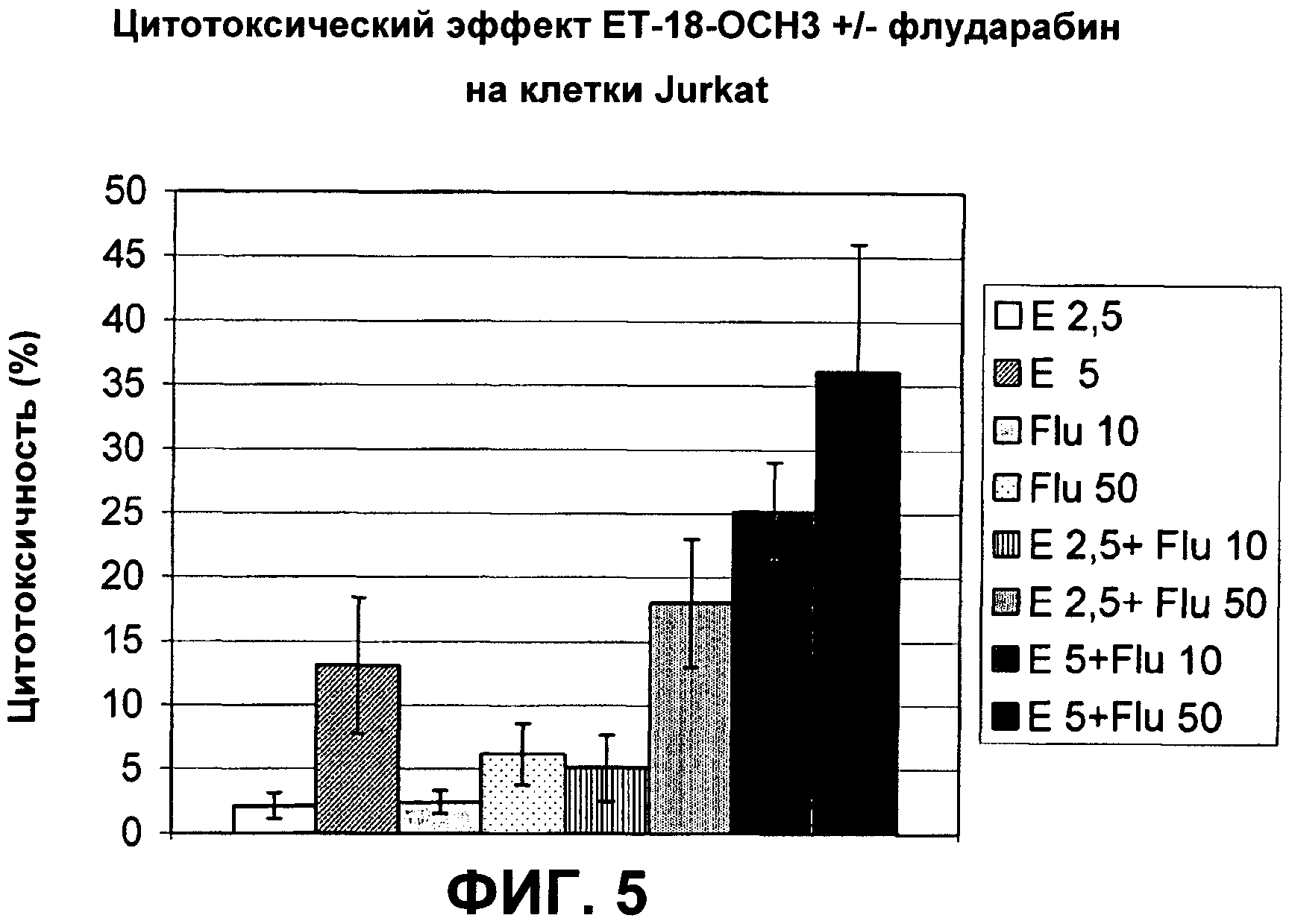
Фиг.5 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с флударабином, аналогом пурина, на клетки Jurkat. Клетки культивировали, как описано для Фиг.1. ЕТ-18-ОСН3 добавляли в конечной концентрации 2.5 или 5.0 мкг/мл («Е2.5» и «Е5», соответственно) без или в комбинации с 10 или 50 мкМ флударабина («Flu5» и «Flu10», соответственно), затем клетки инкубировали в течение 20 ч. Гибель клеток наблюдали, как описано для Фиг.1. Результаты представлены как среднее значение ± стандартное отклонение из трех независимых экспериментов.
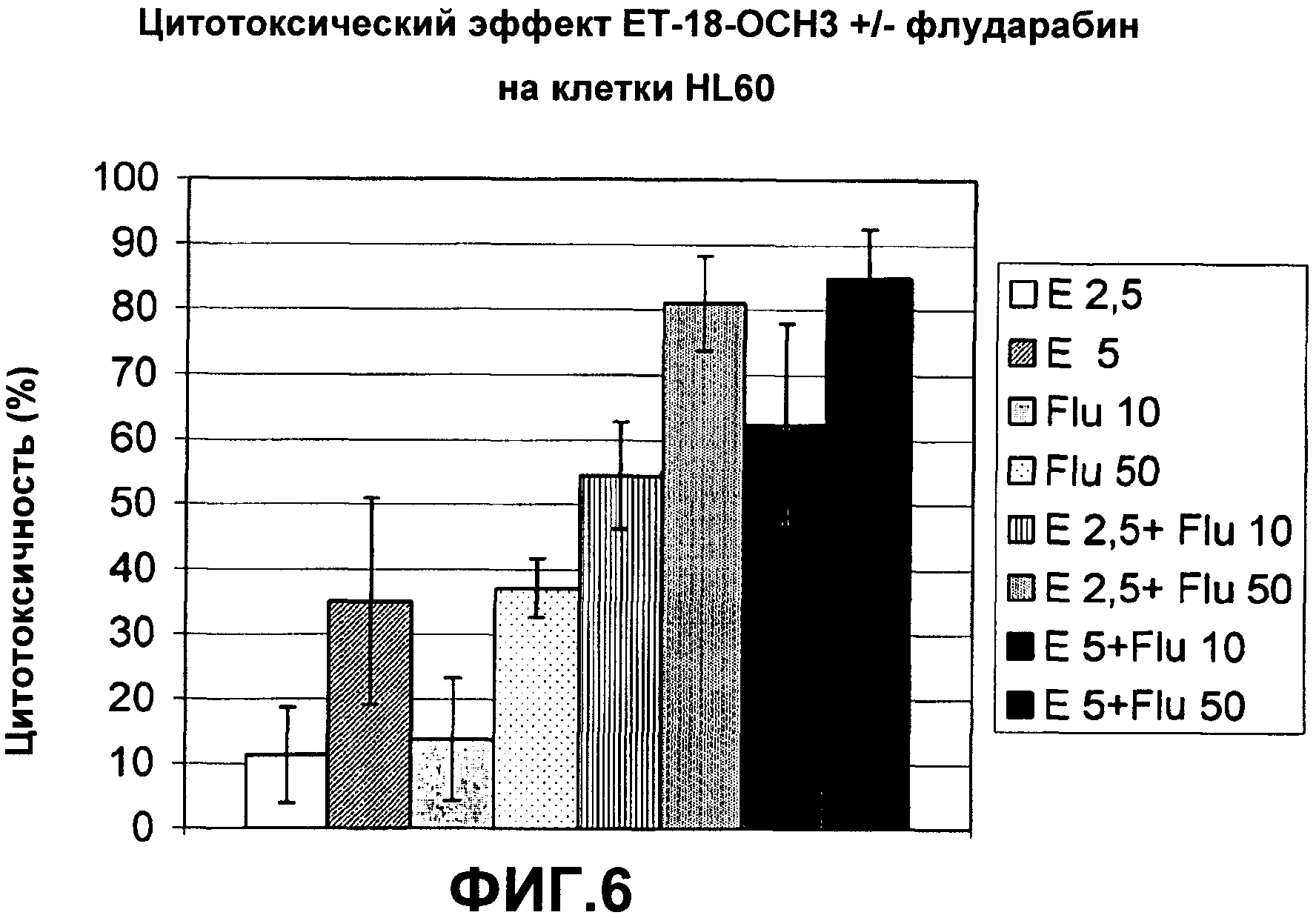
Фиг.6 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с флударабином на клетки HL60. Культуры клеток, концентрации соединений и условия эксперимента были идентичны описанным для Фиг.2. Результаты представлены как среднее значение ± стандартное отклонение из четырех независимых экспериментов.
Фиг.7 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в сочетании с цитарабином, аналогом пиримидина, на клетки Jurkat. Клетки культивировали, как описано в Фиг.1. ЕТ-18-ОСН3 добавляли в конечной концентрации 2.5 или 5.0 мкг/мл («Е2.5» и «Е5», соответственно) без или в комбинации с 10 или 40 мкМ цитарабина («Ara-С10» и «Ara-С40», соответственно), затем клетки инкубировали в течение 20 ч. Гибель клеток наблюдали, как описано для Фиг.1. Результаты представлены как среднее значение ± стандартное отклонение из трех независимых экспериментов.
Фиг.8 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с цитарабином на клетки HL60. Культуры клеток, концентрации соединений и условия эксперимента были идентичны описанным для Фиг.7. Результаты представлены как среднее значение ± стандартное отклонение из четырех независимых экспериментов.
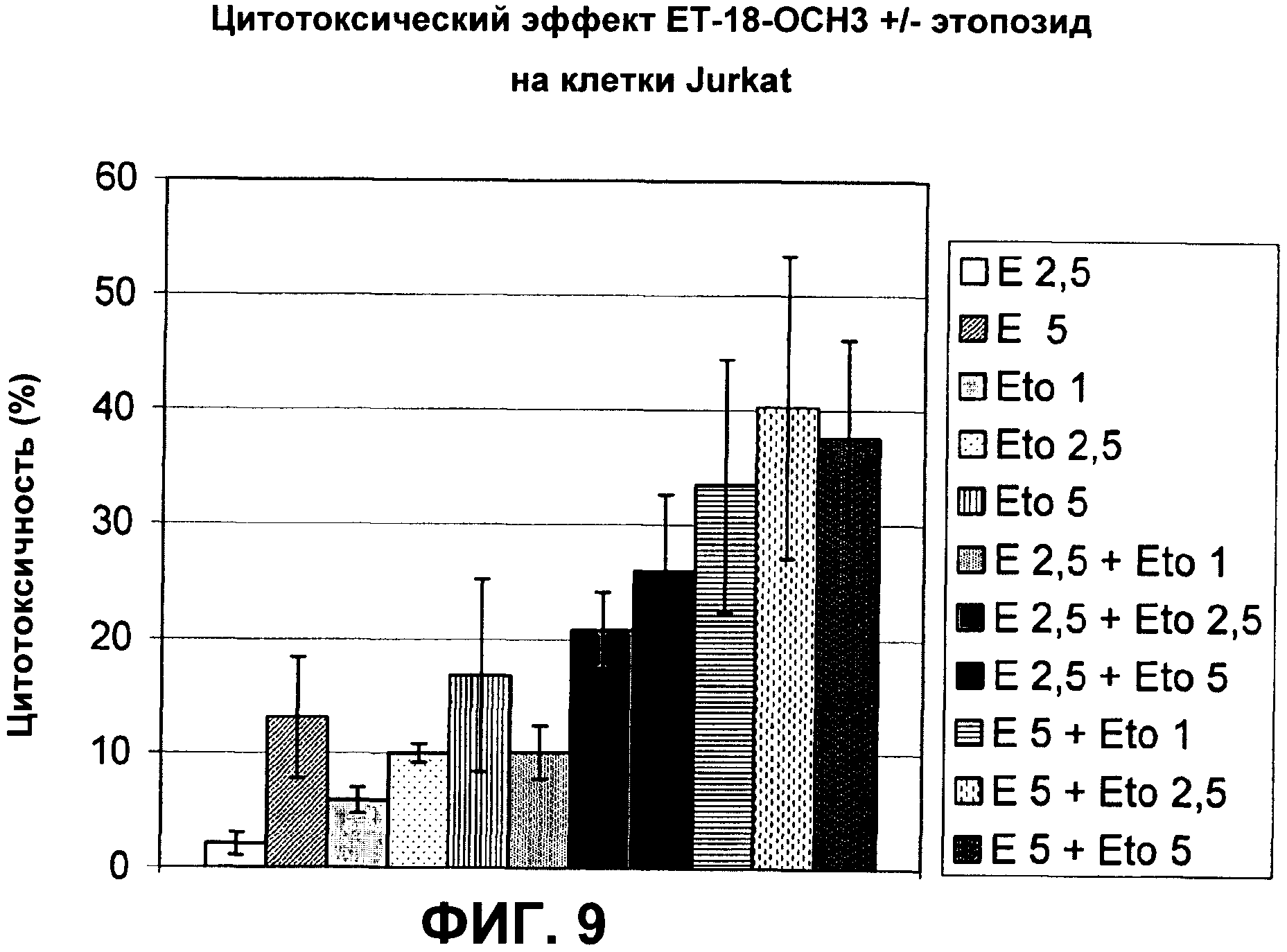
Фиг.9 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с этопозидом, ингибитором топоизомеразы II, на клетки Jurkat. Клетки культивировали, как описано для Фиг.1. ЕТ-18-ОСН3 добавляли в конечной концентрации 2.5 или 5.0 мкг/мл («Е2.5» и «Е5», соответственно) без или в комбинации с 1.0, 2.5 или 5.0 мкМ этопозида («Eto1», «Eto2.5» и «Eto5», соответственно), затем клетки инкубировали в течение 20 ч. Гибель клеток наблюдали, как описано для Фиг.1. Результаты представлены как среднее значение ± стандартное отклонение из трех независимых экспериментов.
Фиг.10 показывает цитотоксические эффекты ЕТ-18-ОСН3 индивидуально и в комбинации с этопозидом на клетки HL60. Культуры клеток, концентрации соединений и условия эксперимента были идентичны описанным для Фиг.7. Результаты представлены как среднее значение ± стандартное отклонение из четырех независимых экспериментов.
ПРИМЕРЫ
Пример 1: Определение цитотоксического эффекта 1-O-октадецил-2-О-метилглицеро-3-фосфохолина на различные линии гематологических опухолевых клеток человека
Были применены следующие линии клеток человека:
1. KMS-12-BM (DMSZ № АСС 551), клетки костного мозга; миелома/плазмоцитома; не содержат никаких генетических изменений, отмеченных здесь; Chesi, M. et al (2001), supra.
2. К562 (АТСС № CCL-243); клетки костного мозга; ХМЛ; не содержат генетических изменений, отмеченных в настоящем изобретении; Delgado, M.D. et al (2001), supra.
3. RPMI8226 (АТСС № CCL-155); клетки периферической крови; миеломы/плазмоцитома; K-12-G>A мутация в гене K-ras (GGT→GCT в кодоне 12); Chesi, M. et al (2001), supra.
4. ОРМ-2 (АТСС № CRL-13007); лимфобластные клетки; миелома; t(4; 14) хромосомная транслокация; К650Е мутация в гене FGFR3 (AAG→GAG в кодоне 650); Chesi, M. et al (2001), supra.
5. NCI-H929 (АТСС № CRL-9068); клетки костного мозга; миелома/плазмоцитома; t(4;14) хромосомная транслокация; N13-G>D мутация в гене N-ras (GGT→GAT в кодоне13); Chesi, M. et al (2001), supra.
6. U266 (АТСС № TIB-196); клетки периферической крови; миелома/плазмоцитома; не содержит никаких генетических изменений, указанных здесь; Chesi, M. et al (2001), supra.
7. HL60 (АТСС № CCL-240); клетки периферической крови; ОМЛ; N61-Q>R мутация в гене N-ras (CAA→CGA в кодоне 61); Bos, J.L. et al (1984), supra.
8. Jurkat (АТСС № TIB-152); клетки периферической крови; ОЛЛ; делеция 2 пар нуклеотидов и инсерция 9 пар нуклеотидов в кодоне 234 в экзоне 7 в гене PTEN (что приводит к понижению стоп-кодона); Sakai, A. et al (1998), supra.
Клетки культивировали на 96-луночных плашках в объеме 200 мкл до концентрации 1×106 клеток/мл. Затем клетки инкубировали в течение 20 ч с конечными концентрациями 1-O-октадецил-2-O-метилглицеро-3-фосфохолина (ЕТ-18-ОСН3) 5 мкг/мл, 10 мкг/мл и 20 мкг/мл, соответственно. Клеточную гибель оценивали с помощью окрашивания клеток 7-аминоактиномицином D (Calbiochem, Darmstadt, Germany; конечная концентрация 200 мкг/мл) и анализировали путем проточной цитофлуоримет-рии на проточном цитометре FACS-Scan (BD Biosciences, San Jose, California, USA) (как описано, например, в Schmid, I. et al (1994), J. Immunol. Meth. 170, 145-157; Ayuk, F.A. etal (2005) Exp. Hematol. 33, 1531-1536).
Результаты, полученные в типичном эксперименте, суммированы на Фиг.1. За исключением клеток U266, которые, по-видимому, не реагируют на ЕТ-18-ОСН3 совсем, все клеточные линии при воздействии ЕТ-18-ОСН3 показывали дозозависимый эффект. Применение 20 мкг/мл ЕТ-18-ОСН3 приводило к практически полной гибели клеток RPMI8226, NCl-H929 и HL60, соответственно. В клетках ОРМ-2 около 75% клеток погибало при воздействии 20 мг/мл ЕТ-18-ОСН3. Интересно, что в тех клетках, которые не содержат никаких генетических изменений, определенных здесь, а именно t(4; 14) хромосомную транслокацию, мутации в генах ras, FGFR3 и PTEN, соответственно (то есть клетки KMS-12-BM, К562 и U266), цитотоксичность значительно уменьшается или почти исчезает. Эти результаты показывают, что присутствие одного или более генетического изменения является строгим показателем чувствительности данной клетки к обработке ЕТ-18-ОСН3.
Пример 2: Определение цитотоксического эффекта 1-O-октадецил-2-О-метилглицеро-3-фосфохолина в сочетании с различными антинеопластическими агентами на различных клеточных линиях
Были применены следующие цитостатические лекарственные средства: бортезомиб (Velcade®; Janssen Cilag, Neuss, Germany), ингибитор 26S протеасомы, который обычно используется для лечения множественной миеломы; флурарабин (Sigma, St. Louis, USA), аналог пурина, в основном применяемый при лечении ОМЛ и ХЛЛ; цитарабин (так же известный как «цитозин арабинозид» или «Ara-C», Sigma, St. Louis, USA), в основном применяемый для лечения ОМЛ и неходжкинских лимфом, и этопозид (Sigma, St. Louis, USA), ингибитор топоизоомеразы II, который обычно используется в лечении лимфом.
Клетки культивировали на 96-луночных плашках в объеме 200 мкл до концентрации 1×106 клеток/мл. Затем клетки инкубировали в течение 20 ч с соответствующими лекарственными средствами. Применялись следующие конечные концентрации (в общем, применяемые концентрации приводили к менее чем 50% цитотоксичности при введение индивидуально): 2.5 мкг/мл и 5.0 мкг/мл 1-O-октадецил-2-O-метилглицеро-3-фосфохолина (ЕТ-18-ОСН3); 5 нг/мл и 10 нг/мл бортезомиба; 10 мкМ и 50 мкМ флударабина; 10 мкМ и 40 мкМ цитарабина и 1 мкМ, 2.5 мкМ и 10 мкМ этопозида, соответственно. Цитотоксический эффект ЕТ-18-ОСН3 в комбинации с бортезомибом был определен в клетках Jurkat, клетках HL60 и клетках RPMI8226, в то время как цитотоксический эффект ЕТ-18-ОСН3 в комбинации с цитарабином, флударабином и этопозидом, соответственно, в клетках Jurkat и HL60. Гибель клеток определяли так же, как описано в примере 1.
Полученные результаты суммированы в таблицах 1-4 (данные представляют собой среднее значение ± стандартное отклонение от 3 (клетки Jurkat и RPMI8226) или 4 (HL60)независимых экспериментов):
|
|
|
Из приведенных выше результатов очевидно, что добавление 1-O-октадецил-2-О-метилглицеро-3-фосфохолина (ЕТ-18-ОСН3) к любому протестированному антинеопластическому агенту давало улучшенный цитотоксический эффект во всех примененных клеточных линиях. Важно, что разные комбинации активных ингредиентов действовали не только в дополняющей, но и в синергетической манере. Таким образом, этот синергетический режим действия позволяет вводить уменьшенные дозы препаратов для того, чтобы достичь такой же фармацевтической эффективности по сравнению с индивидуальным введением, что опять же уменьшит риск появления неблагоприятных побочных эффектов.
Настоящее изобретение, иллюстративно описанное здесь, может быть осуществлено на практике подходящим образом в отсутствие какого-либо элемента или элементов, ограничения или ограничений, неспецифично раскрытых здесь. Так, например, термины «содержащий», «включающий», «содержащий в себе» и т.д. должны пониматься расширенно и без ограничений.
В дополнение, термины и выражения, примененные здесь, были применены как описательные термины, но не ограничивающие, и нет намерения применять такие термины и выражения, которые исключают любые эквиваленты показанных и описанных признаков или их частей, но указано, что различные модификации возможны в объеме заявленного изобретения. Таким образом, следует понимать, что хотя настоящее изобретение было специфически раскрыто предпочтительными вариантами выполнения и необязательными признаками, модификация и вариация изобретений, воплощенных и раскрытых здесь, могут быть сделаны специалистами в данной области техники, и такие модификации и вариации, как считают, будут лежать в объеме изобретения.
Все цитируемые здесь документы и ссылки, включая любые инструкции производителя, описания, спецификации продуктов и бланки к продуктам, для любых продуктов, упомянутых здесь, или в любом документе, на которые здесь ссылаются, в настоящем документе включены посредством ссылки и могут быть применены при осуществлении изобретения на практике. Цитирование или идентификация любого документа в настоящей заявке не является признанием того, что такой документ доступен в качестве уровня техники для настоящего изобретения.
Изобретение было описано здесь широко и в общем. Каждая из более узких областей и подродовых группировок, лежащих внутри общего открытия, также образуют часть изобретения. Это включает общее описание изобретения с условием или отрицательным ограничением, удаляющим любой объект из рода, не обращая внимания, цитируется ли здесь исключенный материал или нет.
Другие варианты выполнения изобретения лежат внутри следующей формулы изобретения. В дополнение, когда признаки или объекты изобретения описываются на основе групп Маркуша, то специалисты в данной области техники поймут, что изобретение также описывается на основе любого отдельного члена или подгруппы членов группы Маркуша.