Результат интеллектуальной деятельности: СПОСОБ ПРОИЗВОДСТВА ГАЛОГЕНИРОВАННОГО АЛКЕНОВОГО СОЕДИНЕНИЯ И ФТОРИРОВАННОГО АЛКИНОВОГО СОЕДИНЕНИЯ
Вид РИД
Изобретение
Область техники
[0001]
Настоящее изобретение относится к способам производства галогенированного алкенового соединения и фторированного алкинового соединения.
Область техники
[0002]
В качестве способа производства галогенированного алкенового соединения, например, в патентном документе (ПД (PTL)) 1 исходный материал, такой как CF3CHClCHClCCl3, CF3CCl2CH2CCl3, CF3CClHCHFCCl3 или CF3CClFCH2CCl3, вводят в реакцию с фторидом водорода в присутствии катализатора на основе оксифторида хрома, а дегидрофторирование проводят во время фторирования, получая в результате CF3CF=CHCF3.
Список цитирования
Патентный документ
[0003]
ПД 1: WO 2012/067864.
Сущность изобретения
Техническая задача
[0004]
Цель настоящего изобретения состоит в разработке способов, в которых можно получать галогенированное алкеновое соединение и фторированное алкиновое соединение с высокой степенью конверсии и высокой селективностью.
Решение задачи
[0005]
Настоящее изобретение включает следующие конфигурации.
Пункт 1. Способ производства галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
и этот способ включает введение галогенированного бутанового соединения, представленного формулой (1A):
CX1X2X3CHX4CFHCX5X6X7 (1A),
где X1, X2, X3, X4, X5, X6 и X7 имеют значения, определенные выше, в реакцию дегидрофторирования.
Пункт 2. Способ производства галогенированного бутинового соединения, представленного формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
и этот способ включает введение галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше, и X4 представляет собой атом галогена, в реакцию дегидрогалогенирования.
Пункт 3. Способ производства галогенированного бутинового соединения, представленного формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
и этот способ включает:
(IA) введение галогенированного бутанового соединения, представленного формулой (1A):
CX1X2X3CHX4CFHCX5X6X7 (1A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше, и X4 представляет собой атом галогена, в реакцию дегидрофторирования с получением галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 имеют значения, определенные выше;
(IIA) после стадии (IA) удаление фторида водорода; и
(IIIA) после стадии (IIA) введение полученного галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 имеют значения, определенные выше, в реакцию дегидрогалогенирования с получением галогенированного бутинового соединения, представленного формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше.
Пункт 4. Способ производства в соответствии с любым из пунктов 1-3, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят в присутствии катализатора и/или основания.
Пункт 5. Способ производства в соответствии с любым из пунктов 1-4, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят в жидкой фазе.
Пункт 6. Способ производства в соответствии с пунктом 5, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят в замкнутом реакционном процессе.
Пункт 7. Способ производства в соответствии с любым из пунктов 1-4, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят в газовой фазе.
Пункт 8. Способ производства в соответствии с пунктом 7, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят в присутствии, по меньшей мере, одного катализатора, выбираемого из группы, состоящей из катализатора на основе активированного угля, катализатора на основе оксида хрома, цеолитного катализатора и алюмосиликатного катализатора.
Пункт 9. Способ производства галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу, и X8 представляет собой атом галогена,
и этот способ включает введение галогенированного алканового соединения, представленного формулой (1B):
CHX8A1CHX9A2 (1B),
где A1 и A2 имеют значения, определенные выше, и X8 и X9 являются одинаковыми или разными и каждый представляет собой атом галогена, в реакцию дегидрогалогенирования в присутствии катализатора в газовой фазе.
Пункт 10. Способ производства фторированного алкинового соединения, представленного формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу,
и этот способ включает введение галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 имеют значения, определенные выше, и X8 представляет собой атом галогена, в реакцию дегидрогалогенирования в присутствии катализатора.
Пункт 11. Способ производства в соответствии с пунктом 10, где стадию реакции дегидрогалогенирования проводят в газовой фазе.
Пункт 12. Способ производства фторированного алкинового соединения, представленного формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу,
и этот способ включает:
(IB) введение галогенированного алканового соединения, представленного формулой (1B):
CHX8A1CHX9A2 (1B),
где A1 и A2 имеют значения, определенные выше, и X8 и X9 являются одинаковыми или разными и каждый представляет собой атом галогена, в реакцию дегидрогалогенирования в присутствии катализатора в газовой фазе с получением галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1, A2 и X8 имеют значения, определенные выше;
(IIB) после стадии (IB) удаление галогенида водорода; и
(IIIB) после стадии (IIB) введение полученного галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1, A2 и X8 имеют значения, определенные выше, в реакцию дегидрогалогенирования в присутствии катализатора в газовой фазе с получением фторированного алкинового соединения, представленного формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 имеют значения, определенные выше.
Пункт 13. Способ производства в соответствии с любым из пунктов 1-12, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят с помощью газофазного непрерывного поточного процесса.
Пункт 14. Способ производства в соответствии с любым из пунктов 1-13, где стадию реакции дегидрофторирования и/или реакции дегидрогалогенирования проводят в присутствии циклического галогенкарбидного соединения, в котором все атомы водорода, связанные с атомами углерода, в углеводородном соединении замещены атомами галогена.
Пункт 15. Композиция, содержащая галогенированное бутеновое соединение, представленное формулой (1A):
CX1X2X3CX4=CHCX5X6X7 (1A),
где X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
причем галогенированное бутеновое соединение, представленное формулой (1A), содержится в количестве от 80,00 до 99,99% мол. из расчета на общее количество композиции, которое принимают за 100% мол.
Пункт 16. Композиция в соответствии с пунктом 15, содержащая в качестве галогенированного бутенового соединения, представленного формулой (1A), (Е)-галогенированное бутеновое соединение в количестве от 85,00 до 99,98% мол. из расчета на общее количество композиции, которое принимают за 100% мол.
Пункт 17. Композиция, содержащая:
галогенированное алкеновое соединение, представленное формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу, и X8 представляет собой атом галогена; и,
по меньшей мере, одно гидрофторуглеродное (HFC) соединение, за исключением галогенированного алкенового соединения, представленного формулой (2B).
Пункт 18. Композиция в соответствии с пунктом 17, где галогенированное алкеновое соединение, представленное формулой (2B), содержится в количестве 80% мол. или больше, и гидрофторуглеродное (HFC) соединение содержится в количестве 20% мол. или меньше из расчета на общее количество композиции, которое принимают за 100% мол.
Пункт 19. Композиция в соответствии с пунктом 17 или 18, где гидрофторуглеродное (HFC) соединение представляет собой, по меньшей мере, одно соединение, выбираемое из группы, состоящей из гексафторбутена, гексафторбутана и октафторбутана.
Пункт 20. Композиция, содержащая:
фторированное алкиновое соединение, представленное формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу; и,
по меньшей мере, одно гидрофторуглеродное (HFC) соединение, за исключением фторированного алкинового соединения, представленного формулой (3B).
Пункт 21. Композиция, содержащая:
галогенированное бутиновое соединение, представленное формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена; и
по меньшей мере, одно гидрофторуглеродное (HFC) соединение, за исключением галогенированного бутинового соединения, представленного формулой (3A).
Пункт 22. Композиция в соответствии с пунктом 20 или 21, где фторированное алкиновое соединение, представленное формулой (3B), или галогенированное бутиновое соединение, представленное формулой (3A), содержится в количестве 80% мол. или больше, и гидрофторуглеродное (HFC) соединение содержится в количестве 20% мол. или меньше из расчета на общее количество композиции, которое принимают за 100% мол.
Пункт 23. Композиция в соответствии с любым из пунктов 20-22, где гидрофторуглеродное (HFC) соединение представляет собой, по меньшей мере, одно соединение, выбираемое из группы, состоящей из трифторметана, дифторметана, тетрафторметана и монофторметана.
Пункт 24. Композиция в соответствии с любым из пунктов 15-23, которую используют в качестве очищающего газа, травильного газа, хладагента, теплопередающей среды или строительного блока для органического синтеза.
Положительные эффекты изобретения
[0006]
В соответствии с настоящим изобретением галогенированное алкеновое соединение и фторированное алкиновое соединение могут быть синтезированы с высокой степенью конверсии и высокой селективностью.
Краткое описание чертежей
[0007]
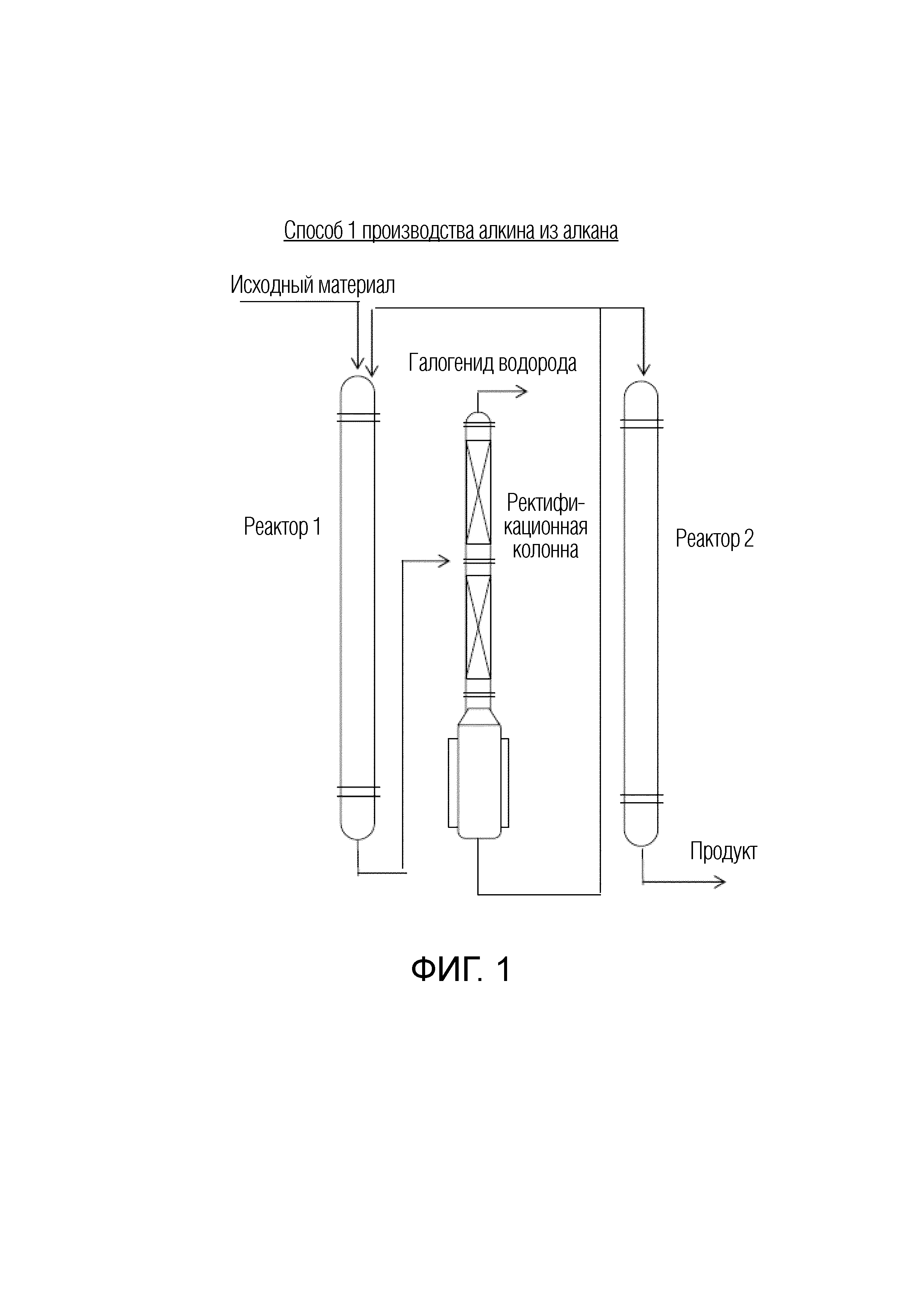
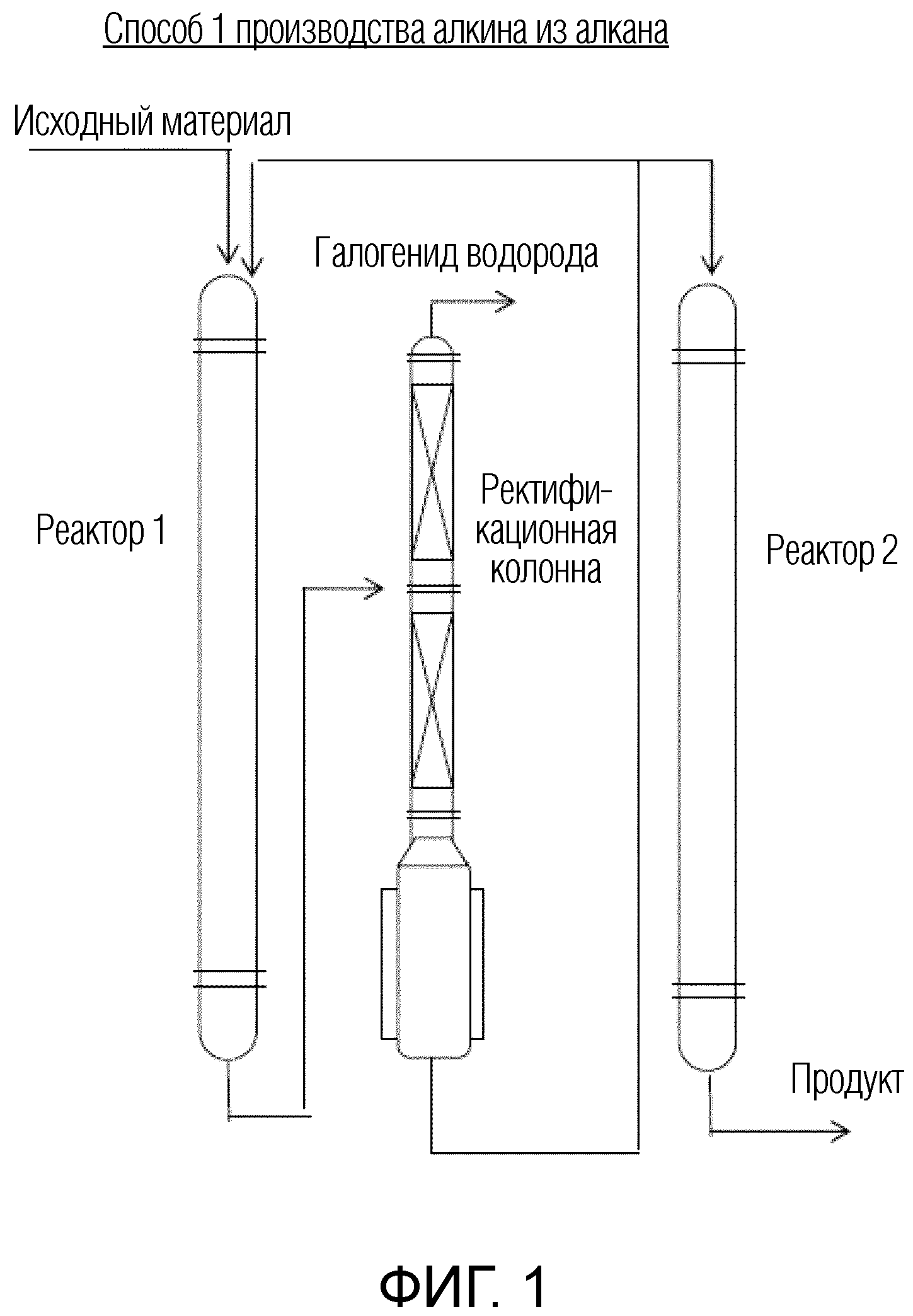
ФИГ. 1 представляет собой вид, схематично показывающий способ производства алкена (галогенированного бутенового соединения или галогенированного алкенового соединения) и алкина (галогенированного бутинового соединения или фторированного алкинового соединения) по настоящему изобретению. На ФИГ. 1 образующийся фторид водорода может быть отделен в ректификационной колонне.
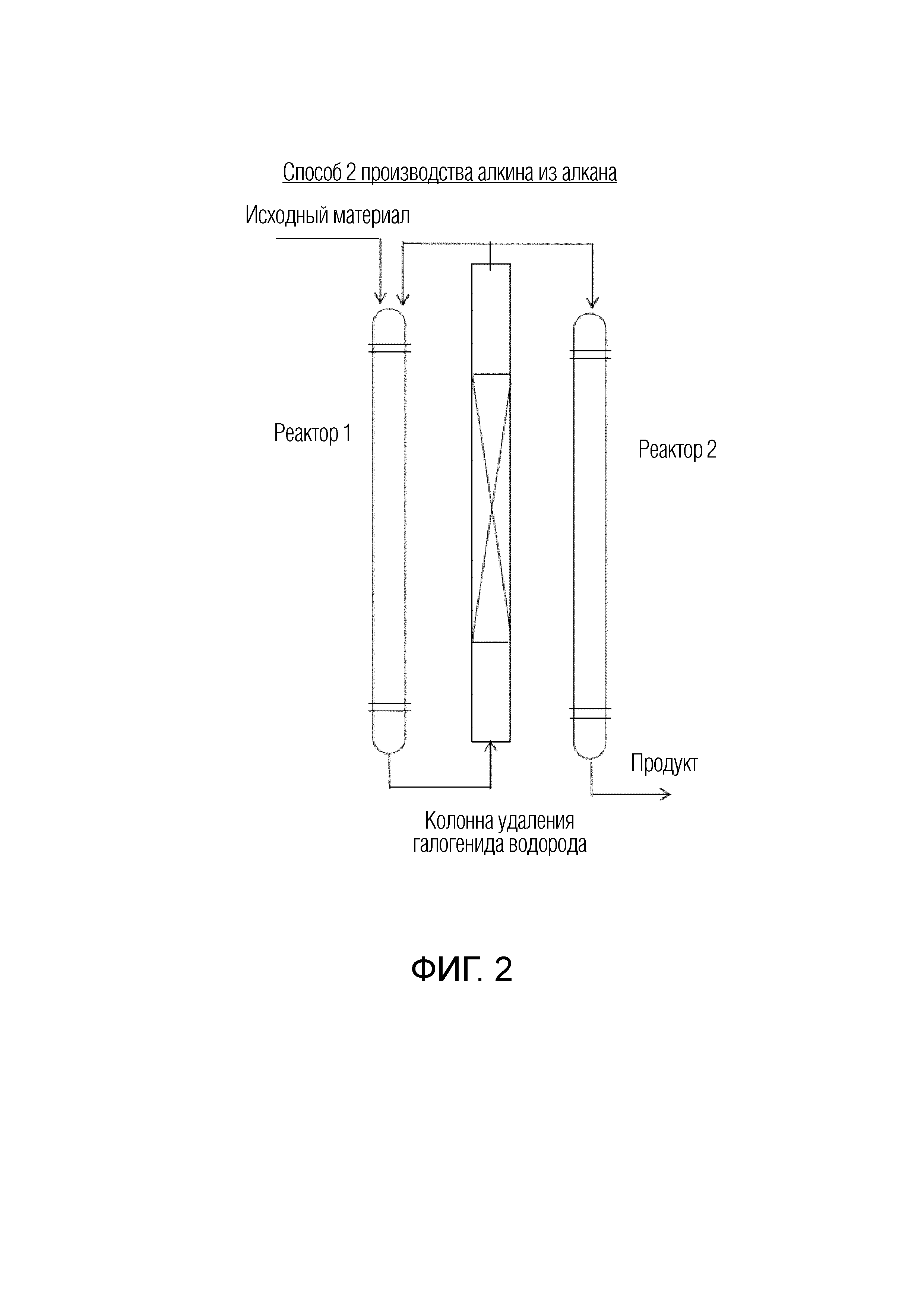
ФИГ. 2 представляет собой вид, схематично показывающий способ производства алкена (галогенированного бутенового соединения или галогенированного алкенового соединения) и алкина (галогенированного бутинового соединения или фторированного алкинового соединения) по настоящему изобретению. На ФИГ. 2 образующийся галогенид водорода может быть удален с использованием агента удаления галогенида водорода (колонна для удаления).
Описание вариантов осуществления
[0008]
В данном описании термин «содержит» представляет собой понятие, включающее «содержащий», «состоящий по существу из» и «состоящий из». В настоящем описании числовой интервал, обозначенный «от A до B», означает A или больше и B или меньше.
[0009]
В данном описании «селективность» означает показатель (% мол.) общего молярного количества целевого соединения, находящегося в выходящем газе из выходного отверстия реактора, из расчета на общее молярное количество соединений, отличных от соединения исходного материала, в выходящем газе.
[0010]
В настоящем описании «степень конверсии» означает показатель (% мол.) общего молярного количества соединений, отличных от соединения исходного материала, находящихся в выходящем газе из выходного отверстия реактора, из расчета на молярное количество соединения исходного материала, поданного в реактор.
[0011]
Традиционно (см. ПД 1) исходный материал, такой как CF3CHClCHClCCl3, CF3CCl2CH2CCl3, CF3CClHCHFCCl3 или CF3CClFCH2CCl3, вводят в реакцию с фторидом водорода в присутствии катализатора на основе оксифторида хрома, и дегидрофторирование проводят одновременно с фторированием, получая в результате CF3CF=CHCF3. Однако его выход составляет только 14,8%.
[0012]
Исходя из вышеизложенного, в традиционном способе выход составляет только 14,8%. В соответствии со способом производства по настоящему изобретению галогенированное алкеновое соединение и фторированное алкиновое соединение могут быть синтезированы с более высокой степенью конверсии и более высокой селективностью по сравнению с обычным способом.
[0013]
1. Способы производства галогенированного бутенового соединения и галогенированного бутинового соединения
1-1: Способ производства галогенированного бутенового соединения из галогенированного бутанового соединения
Способ производства галогенированного бутенового соединения по настоящему изобретению представляет собой способ производства галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
и этот способ включает введение галогенированного бутанового соединения, представленного формулой (1A):
CX1X2X3CHX4CFHCX5X6X7 (1A),
где X1, X2, X3, X4, X5, X6 и X7 имеют значения, определенные выше, в реакцию дегидрофторирования.
[0014]
В соответствии с настоящим изобретением, когда галогенированное бутановое соединение, представленное формулой (1A), вводят в реакцию дегидрофторирования, может быть селективно получено галогенированное бутеновое соединение, представленное формулой (2A), в котором 1 моль фторида водорода отщепляют на 1 моль галогенированного бутанового соединения, представленного формулой (1A). Кроме того, реакция отщепления галогенида водорода, представленного как HX4, от галогенированного бутенового соединения, представленного формулой (2A), вряд ли будет происходить непрерывно. Кроме того, в соответствии с настоящим изобретением в качестве галогенированного бутенового соединения, представленного формулой (2A), может быть селективно синтезирован E-изомер среди геометрических изомеров. Причина этого состоит в следующем. Так как α-углерод тригалогенированных метильных групп, таких как CF3 группа, становится электронодефицитным из-за эффекта притяжения электронов тригалогенированных метильных групп, таких как CF3 группа, галогенированные анионы, такие как анионы фтора, менее склонны к десорбции. В результате получают галогенированный бутен вместо галогенированного бутина. Кроме того, селективный синтез E-изомера происходит потому, что транс-конфигурация энергетически более стабильна вследствие стерических затруднений тригалогенированных метильных групп, таких как CF3 группа.
[0015]
(1-1-1) Соединение исходного материала (Галогенированное бутановое соединение).
Галогенированное бутановое соединение в качестве субстрата, который может быть использован в способе производства по настоящему изобретению, представляет собой, как описано выше, галогенированное бутановое соединение, представленное формулой (1A):
CX1X2X3CHX4CFHCX5X6X7 (1A),
где X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена.
[0016]
В формуле (1A) примеры атома галогена, обозначенного X1, X2, X3, X4, X5, X6 и X7, включают атом фтора, атом хлора, атом брома и атом йода.
[0017]
В галогенированном бутановом соединении, которое является субстратом, все из X1, X2, X3, X4, X5, X6 и X7 предпочтительно представляют собой атомы фтора или атомы хлора, и более предпочтительно атомы фтора, с той точки зрения, что галогенированное бутеновое соединение может быть получено особенно с высокой степенью конверсии, высоким выходом и высокой селективностью.
[0018]
X1, X2, X3, X4, X5, X6 и X7 могут быть одинаковыми или разными.
[0019]
Конкретные примеры галогенированного бутанового соединения в качестве субстрата, который удовлетворяет приведенным выше условиям, включают CF3CFHCFHCF3, CCl3CClHCFHCCl3, CBr3CBrHCFHCBr3 и т.п. Эти галогенированные бутановые соединения могут быть использованы по отдельности или в комбинации из двух или более. Такие галогенированные бутановые соединения могут быть известными или коммерчески доступными продуктами.
[0020]
(1-1-2) Реакция дегидрофторирования
На стадии введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении, например, в галогенированном бутановом соединении, представленном формулой (1A), в качестве субстрата X1, X2, X3, X4, X5, X6 и X7 более предпочтительно представляют собой атомы фтора.
[0021]
То есть, эта реакция предпочтительно представляет собой реакцию дегидрофторирования в соответствии со следующим уравнением реакции:
CF3CFHCFHCF3 → CF3CF=CHCF3+HF
[0022]
Стадия введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении может быть проведена в жидкой фазе или газовой фазе. Особенно с точки зрения производительности предпочтительно проведение этой стадии в газовой фазе.
[0023]
Стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении предпочтительно проводят в присутствии катализатора и/или основания с точки зрения того, что целевое соединение может быть получено с более высокой селективностью и более высокой степенью конверсии. Более конкретно, когда используют жидкофазную реакцию, эту стадию предпочтительно проводят в присутствии основания и необязательно катализатора, и, когда используют газофазную реакцию, эту стадию предпочтительно проводят в присутствии катализатора. Подробная информация по катализатору и основанию в каждом случае описана позднее.
[0024]
(1-1-2-1) Жидкофазная реакция
Когда стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении проводят в жидкой фазе, выход целевого соединения может быть дополнительно улучшен, например, за счет использования металлического контейнера и увеличения жидкого компонента за счет прикладывания давления и повышения температуры кипения исходного материала.
[0025]
Когда стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении проводят в жидкой фазе, предпочтительно вначале готовить раствор галогенированного бутанового соединения, представленного формулой (1A), а затем переходить к реакции в присутствии основания.
[0026]
Растворитель
В качестве растворителя в растворе галогенированного бутанового соединения могут быть использованы как водные, так и неводные растворители. Предпочтительные примеры неводных растворителей включают карбонатные сложные эфиры, такие как диметилкарбонат, этилметилкарбонат, диэтилкарбонат, метилпропил-карбонат и этилпропилкарбонат; сложные эфиры, такие как этил-ацетат, пропилацетат, бутилацетат, метилпропионат, этилпропионат и бутилпропионат; кетоны, такие как ацетон, этилметилкетон и диэтилкетон; лактоны, такие как γ-бутиролактон, γ-валеролактон, тетрагидрофуран и тетрагидропиран; простые эфиры, такие как диэтиловый эфир, дибутиловый эфир, диизопропиловый эфир, 1,2-диметоксиэтан, 1,2-диэтоксиэтан и тетрагидрофуран; нитрилы, такие как ацетонитрил, пропионитрил и бензонитрил; амиды, такие как N, N-диметилформамид; сульфоны, такие как диметилсульфоксид и сульфолан; и т.п. Эти водные и неводные растворители могут быть использованы по отдельности или в комбинации из двух или более. Из них предпочтительно использовать растворители, которые имеют высокую температуру кипения и которые плохо разлагают основания, описанные позже. Говоря точнее, неводный растворитель предпочтителен, простой эфир более предпочтителен и дибутиловый эфир особенно предпочтителен.
[0027]
Основание
Когда стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении проводят в жидкой фазе, эту стадию предпочтительно проводят в присутствии основания, как описано выше.
[0028]
С точки зрения степени конверсии реакции и селективности, а также выхода галогенированного бутенового соединения основание предпочтительно представляет собой гидроксид или алкоксид щелочного металла или щелочноземельного металла, и более предпочтительно алкоксид щелочного металла или щелочноземельного металла. Конкретные примеры включают гидроксид натрия, гидроксид калия, метоксид натрия, трет-бутоксид калия и т.п.; и предпочтительно метоксид натрия, трет-бутоксид калия и т.п. На этой стадии предпочтительно использовать водный раствор гидроксида или алкоксида щелочного металла или щелочноземельного металла и более предпочтительно водный раствор алкоксида щелочного металла или щелочноземельного металла. Говоря точнее, особенно предпочтительными являются водный раствор метоксида натрия, метоксида калия, этоксида калия, трет-бутоксида калия или т.п. Благодаря использованию такого основания целевое соединение может быть получено с более высокой селективностью и более высокой степенью конверсии.
[0029]
Содержание основания в реакционном растворе не ограничено, но составляет предпочтительно от 20 до 60% масс. и более предпочтительно от 40 до 55% масс. из расчета на весь реакционный раствор, который принимают за 100% масс. Когда содержание основания в реакционном растворе находится в пределах этих интервалов, целевое соединение может быть получено с более высокой селективностью и более высокой степенью конверсии.
[0030]
Катализатор
На этой стадии может быть использован катализатор, если это необходимо. Катализатор, используемый на этой стадии, предпочтительно представляет собой алкоксид на основе углеводорода. Примеры алкоксидов на основе углеводорода включают тетраметиламмонийфторид, тетраметиламмонийхлорид, тетраметил-аммонийбромид, тетраметиламмониййодид, тетраэтиламмонийфторид, тетраэтиламмонийхлорид, тетраэтиламмонийбромид, тетраэтил-аммониййодид, тетрапропиламмонийфторид, тетрапропиламмоний-хлорид, тетрапропиламмонийбромид, тетрапропиламмониййодид, тетрабутиламмонийфторид, тетрабутиламмонийхлорид, тетрабутил-аммонийбромид, тетрабутиламмониййодид, бензилтриэтиламмоний-фторид, бензилтриэтиламмонийхлорид, бензилтриэтиламмонийбромид, бензилтриэтиламмониййодид, бензилтрибутиламмонийфторид, бензил-трибутиламмонийхлорид, бензилтрибутиламмонийбромид, бензил-трибутиламмониййодид, метилтрибутиламмонийфторид, метилтрибутил-аммонийхлорид, метилтрибутиламмонийбромид, метилтрибутиламмоний-йодид, метилтриоктиламмонийфторид, метилтриоктиламмонийхлорид (товарный знак: Aliquat 336), метилтриоктиламмонийбромид, метилтриоктиламмониййодид и т.п. Катализаторы могут быть использованы по отдельности или в комбинации из двух или более. Благодаря использованию такого катализатора целевое соединение может быть получено с более высокой селективностью и более высокой степенью конверсии.
[0031]
Циклическое галогенкарбидное соединение
В настоящем изобретении стадия введения галогенированного бутанового соединения в реакцию дегидрофторирования может быть проведена в присутствии циклического галогенкарбидного соединения. Циклическое галогенкарбидное соединение относится к циклическому галогенкарбидному соединению, в котором все атомы водорода, связанные с атомами углерода, в углеводородном соединении замещены атомами галогена. Другими словами, это соединение относится к циклическому галогенкарбидному соединению, состоящему из атомов углерода и атомов галогена и не содержащему атомы водорода.
[0032]
Когда стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования проводят в присутствии такого циклического галогенкарбидного соединения, можно сдвигать равновесие реакции в сторону продукта, и галогенированное бутеновое соединение, которое является целевым продуктом, может быть получено с более высокой степенью конверсии и более высоким выходом.
[0033]
Примеры атома галогена в подходящем для использования циклическом галогенкарбидном соединении включают любые из атомов фтора, атомов хлора, атомов брома и атомов йода. Из них с точки зрения эффективности реакции предпочтительно, чтобы присутствовал тот же тип атома галогена, что и атом галогена (X1, X2, X3, X4, X5, X6 и X7), находящийся в галогенированном бутановом соединении, которое является соединением исходного материала. Когда галогенированное бутановое соединение имеет множество атомов галогена (когда не все из X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми), предпочтительно, чтобы циклическое галогенкарбидное соединение содержало один, или два, или больше из атомов галогена, находящихся в галогенированном бутановом соединении, и более предпочтительно один из атомов галогена, находящихся в галогенированном бутановом соединении.
[0034]
Количество атомов углерода в подходящем для использования циклическом галогенкарбидном соединении не ограничено. С точки зрения степени конверсии, селективности и выхода галогенированного бутенового соединения как целевого продукта число атомов углерода в циклическом галогенкарбидном соединении составляет предпочтительно от 1 до 10, более предпочтительно от 2 до 7 и даже более предпочтительно от 3 до 5.
[0035]
Подходящее для использования циклическое галогенкарбидное соединение может представлять собой насыщенное циклическое галогенкарбидное соединение без ненасыщенной связи или ненасыщенное циклическое галогенкарбидное соединение с ненасыщенной связью. Из них насыщенное циклическое галоген-карбидное соединение предпочтительно с точки зрения степени конверсии, селективности и выхода галогенированного бутенового соединения как целевого продукта.
[0036]
Исходя из вышесказанного, циклическое галогенкарбидное соединение предпочтительно представляет собой насыщенное циклическое галогенкарбидное соединение. Такое насыщенное циклическое галогенкарбидное соединение предпочтительно представляет собой насыщенное циклическое галогенкарбидное соединение, представленное формулой (4):
[0037]

[0038]
где A3, A4, A5, A6, A7, A8, A9 и A10 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу.
[0039]
В формуле (4) перфторалкильная группа, обозначенная как A3, A4, A5, A6, A7, A8, A9 и A10, относится к алкильной группе, в которой все атомы водорода замещены атомами фтора. Такая перфторалкильная группа, например, представляет собой перфторалкильную группу, имеющую от 1 до 20 атомов углерода, предпочтительно от 1 до 12 атомов углерода, более предпочтительно от 1 до 6 атомов углерода, даже более предпочтительно от 1 до 4 атомов углерода и особенно предпочтительно от 1 до 3 атомов углерода. Перфторалкильная группа предпочтительно представляет собой линейную или разветвленную перфторалкильную группу. Такой перфторалкильной группой предпочтительно является трифторметильная группа (CF3-) или пентафторэтильная группа (C2F5-).
[0040]
Конкретные примеры циклического галогенкарбидного соединения, которое удовлетворяет приведенным выше условиям, включают:
[0041]

[0042]
[0043]
В способе производства по настоящему изобретению, когда галогенированное бутановое соединение вводят в реакцию дегидрофторирования в жидкой фазе, например, в присутствии циклического галогенкарбидного соединения, циклическое галоген-карбидное соединение может быть вдуто в газообразном состоянии в раствор галогенированного бутанового соединения, или в него может быть подана жидкая фаза (например, сжиженный газ).
[0044]
В способе производства по настоящему изобретению, когда галогенированное бутановое соединение вводят в реакцию дегидрофторирования в присутствии циклического галогенкарбидного соединения, количество используемого циклического галоген-карбидного соединения не ограничено. С точки зрения степени конверсии, селективности и выхода галогенированного бутенового соединения как целевого продукта количество циклического галогенкарбидного соединения предпочтительно является избыточным количеством в пересчете на галогенированное бутановое соединение, которое представляет собой соединение исходного материала, и, говоря точнее, используют предпочтительно от 1 до 20 молей, более предпочтительно от 2 до 10 молей и даже более предпочтительно от 3 до 5 молей на моль галогенированного бутанового соединения, которое является соединением исходного материала.
[0045]
Замкнутый реакционный процесс
В настоящем изобретении галогенированное бутеновое соединение, представленное формулой (2A), как целевое соединение имеет низкую температуру кипения и существует в виде газа при комнатной температуре. Соответственно, в настоящем изобретении на стадии проведения реакции дегидрофторирования, когда используют замкнутый реакционный процесс в качестве реакционной системы, давление внутри замкнутого реакционного процесса растет естественным образом, и реакция может быть проведена в условиях повышенного давления. Следовательно, галогенированное бутеновое соединение, представленное формулой (2A), как целевое соединение может быть получено с более высокой селективностью и более высокой степенью конверсии.
[0046]
Таким образом, замкнутый реакционный процесс находится под давлением из-за низкой температуры кипения целевого соединения, и концентрация субстрата (соединение исходного материала) в реакционном растворе (раствора основания) растет, что может улучшить реакционную способность. В замкнутом реакционном процессе предпочтительно проводить реакцию, одновременно герметизируя реакционную систему с использованием устойчивого к давлению реакционного сосуда периодического действия. Когда реакцию проводят в периодическом процессе, предпочтительно, например, помещать соединение исходного материала, раствор основания (щелочной водный раствор), катализатор и др., в сосуд высокого давления, такой как автоклав, повышать температуру до соответствующей реакционной температуры с помощью нагревателя и проводить реакцию при перемешивании в течение некоторого периода времени. Что касается реакционной атмосферы, то предпочтительно проводить реакцию в атмосфере инертного газа, такого как азот, гелий или диоксид углерода.
[0047]
В настоящем изобретении на стадии проведения реакции дегидрофторирования температура реакции в замкнутом реакционном процессе обычно составляет предпочтительно 0°C или выше, более предпочтительно 10°C или выше и даже более предпочтительно 15°C или выше с точки зрения того, что реакция отщепления может протекать более эффективно, а целевое соединение может быть получено с более высокой селективностью, и с точки зрения подавления снижения степени конверсии.
[0048]
На стадии проведения реакции дегидрофторирования в настоящем изобретении температура реакции в замкнутом реакционном процессе обычно составляет предпочтительно 100°C или ниже и более предпочтительно 80°C или ниже с точки зрения того, что реакция дегидрофторирования может протекать более эффективно, а целевое соединение может быть получено с более высокой селективностью, и с точки зрения дополнительного подавления падения селективности из-за разложения или полимеризации продукта реакции.
[0049]
Реакционный процесс при повышенном давлении
На стадии проведения реакции дегидрофторирования в настоящем изобретении реакция может быть проведена в реакционном процессе при повышенном давлении путем установки температуры реакции на 10°C или выше и давления реакции на 0 кПа или больше. В результате галогенированное бутеновое соединение, представленное формулой (2A), как целевое соединение может быть получено с более высокой селективностью и более высокой степенью конверсии. Когда давление в реакционной системе повышают таким образом, концентрация субстрата (соединения исходного материала) в реакционном растворе (раствора основания, щелочного водного раствора) растет, что может улучшить реакционную способность. В реакционном процессе при повышенном давлении предпочтительно проводить реакцию, одновременно герметизируя реакционную систему с использованием устойчивого к давлению реакционного сосуда периодического типа. Когда реакцию проводят в периодическом процессе, предпочтительно, например, помещать соединение исходного материала, раствор основания (щелочной водный раствор), катализатор и др. в реакционный сосуд, такой как автоклав, повышать температуру до соответствующей температуры реакции с помощью нагревателя и проводить реакцию при одновременном перемешивании в течение некоторого периода времени.
[0050]
На стадии проведения реакции отщепления в настоящем изобретении условия повышения давления предпочтительно являются такими, чтобы давление реакции было 0 кПа или больше. Давление реакции представляет собой давление внутри реакционного сосуда, используемого в случае реакционного процесса при повышенном давлении. На стадии проведения реакции дегидрофторирования в настоящем изобретении давление реакции составляет предпочтительно 0 кПа или больше, более предпочтительно 5 кПа или больше, даже более предпочтительно 10 кПа или больше и особенно предпочтительно 15 кПа или больше. Верхняя граница давления реакции не ограничена, и, как правило, равна приблизительно 2 МПа. В настоящем изобретении давление является избыточным, если не указано иное.
[0051]
В случае создания повышенного давления в реакционной системе давление может быть увеличено путем подачи в реакционную систему инертного газа, такого как азот, гелий или диоксид углерода.
[0052]
На стадии проведения реакции дегидрофторирования в настоящем изобретении температура реакции в реакционном процессе при повышенном давлении составляет обычно предпочтительно 0°C или выше, более предпочтительно 10°C или выше и даже более предпочтительно 15°C или выше с точки зрения того, что реакция отщепления может протекать более эффективно и целевое соединение может быть получено с более высокой селективностью, и с точки зрения подавления снижения степени конверсии.
[0053]
На стадии проведения реакции дегидрофторирования в настоящем изобретении температура реакции в замкнутом реакционном процессе составляет обычно предпочтительно 100°C или ниже и более предпочтительно 80°C или ниже с точки зрения того, что реакция дегидрофторирования может протекать более эффективно и целевое соединение может быть получено с более высокой селективностью, а также с точки зрения дополнительного подавления снижения селективности из-за разложения или полимеризации продукта реакции.
[0054]
Комбинация замкнутого реакционного процесса и реакционного процесса при повышенном давлении
На стадии проведения реакции дегидрофторирования в настоящем изобретении также можно проводить реакцию в формате непрерывной реакции под давлением при одновременном извлечении жидкости или извлечении превращенного в газ продукта за счет подключения клапана обратного давления к реактору непрерывного действия с перемешиванием (CSTR).
[0055]
После окончания реакции дегидрофторирования необязательно может быть проведена очистка в соответствии с традиционными методами с получением в результате галогенированного бутенового соединения, представленного формулой (2A).
[0056]
(1-1-2-2) Газофазная реакция
Когда в настоящем изобретении стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования проводят в газовой фазе, то это выгодно тем, что использование растворителя не требуется, промышленные отходы не образуются, а производительность является отличной.
[0057]
Стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении предпочтительно проводят в газовой фазе, особенно с помощью газофазного непрерывного поточного процесса с использованием реактора с неподвижным слоем. При использовании газофазного непрерывного поточного процесса устройство, работа и т.д. могут быть упрощены, что экономически выгодно.
[0058]
Катализатор
Стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении предпочтительно проводят в присутствии катализатора.
[0059]
Предпочтительные катализаторы, используемые в способе производства по настоящему изобретению, включают катализаторы на основе активированного угля, хромоксидные катализаторы, цеолитные катализаторы, алюмосиликатные катализаторы и т.п. Такие катализаторы могут представлять собой как нефторированные катализаторы, так и фторированные катализаторы.
[0060]
Катализаторы на основе активированного угля не ограничены, и примеры включают порошкообразный активированный уголь, такой как измельченный уголь, формованный уголь, гранулированный уголь и сферический уголь. В качестве порошкообразного активированного угля предпочтительно использовать порошкообразный активированный уголь, который показывает размер частиц от 4 меш (4,75 мм) до 100 меш (0,150 мм) в соответствии с JIS испытанием (JIS Z8801). Такие активированные угли могут представлять собой известные или коммерчески доступные продукты.
[0061]
Так как активированный уголь показывает более высокую активность при фторировании, также можно использовать, в качестве катализатора на основе активированного угля фторированный активированный уголь, полученный путем предварительного фторирования активированного угля перед его использованием в реакции. То есть, в качестве катализатора на основе активированного угля может быть использован как нефторированный активированный уголь, так и фторированный активированный уголь.
[0062]
Подходящие примеры фторирующих агентов для фторирования активированного угля включают HF и подобные неорганические фторирующие агенты, а также гидрофторуглерод (HFC), такой как гексафторпропен, хлорфторуглерод (CFC), такой как хлорфторметан, гидрохлорфторуглерод (HCFC), и подобные органические фторирующие агенты.
[0063]
Способ фторирования активированного угля представляет собой, например, фторирование путем циркуляции упомянутого выше фторирующего агента при атмосферном давлении при температуре от комнатной температуры (25°C) до приблизительно 400°C.
[0064]
Хромоксидные катализаторы не ограничены; однако, когда оксид хрома представлен формулой CrOm, предпочтительно, чтобы он удовлетворял условию 1,5<m<3, более предпочтительно условию 2<m<2,75 и даже более предпочтительно условию 2<m<2,3. Кроме того, когда оксид хрома представлен формулой CrOm⋅nH2O, он может быть гидрирован так, чтобы значение n составляло 3 или меньше, особенно от 1 до 1,5.
[0065]
Фторированный хромоксидный катализатор может быть приготовлен путем фторирования упомянутого выше хромоксидного катализатора. Такое фторирование может быть выполнено с помощью, например, HF или фторуглерода. Такой фторированный хромоксидный катализатор может быть синтезирован, например, в соответствии со способом, описанным в документе JPH 05-146680A.
[0066]
Ниже приведен пример способа синтеза хромоксидного катализатора и фторированного хромоксидного катализатора.
[0067]
В начале может быть получен осадок гидроксида хрома путем смешения водного раствора соли хрома (нитрата хрома, хлорида хрома, хромовых квасцов, сульфата хрома и т.д.) с водным аммиаком. В это время физические свойства гидроксида хрома могут быть проконтролированы за счет скорости реакции для реакции осаждения. Скорость реакции предпочтительно является высокой. Скорость реакции зависит от температуры реакционного раствора, способа смешения водного аммиака (скорость смешения), уровня смешения и т.д.
[0068]
Осадок может быть отфильтрован и промыт, а затем высушен. Сушка может быть проведена, например, на воздухе при температуре от 70 до 200°C в течение от 1 до 100 часов. Катализатор на этой стадии иногда называют «состоянием гидроксида хрома». Затем этот катализатор может быть измельчен. С точки зрения прочности гранул, активности катализатора и т.д. предпочтительно регулировать скорость реакции осаждения так, чтобы плотность порошка измельченного порошка (например, 95% порошка, имеющего размер частиц 1000 мкм или меньше, особенно от 46 до 1000 мкм) составляла от 0,6 до 1,1 г/мл и предпочтительно от 0,6 до 1,0 г/мл. Удельная площадь поверхности порошка (удельная площадь поверхности по методу БЭТ) составляет предпочтительно 100 м2/г или больше и более предпочтительно 120 м2/г или больше, например, при условиях обезгаживания при 200°C в течение 80 минут. Верхняя граница удельной площади поверхности равна, например, 220 м2/г.
[0069]
При необходимости этот порошок гидроксида хрома может быть смешан 3% масс. или меньше графита, и могут быть сформованы гранулы с помощью таблеточной машины. Размер и прочность гранул могут быть скорректированы соответствующим образом.
[0070]
Формованный катализатор может быть прокален в инертной атмосфере (например, в потоке азота) с получением аморфного оксида хрома. Температура прокаливания составляет предпочтительно 360°C или выше и предпочтительно от 380 до 460°C с точки зрения подавления кристаллизации. Время прокаливания может быть установлено, например, на период от 1 до 5 часов.
[0071]
Удельная площадь поверхности прокаленного катализатора составляет предпочтительно, например, 170 м2/г или больше, более предпочтительно 180 м2/г или больше и даже более предпочтительно 200 м2/г или больше с точки зрения активности катализатора. Верхняя граница удельной площади поверхности обычно равна предпочтительно приблизительно 240 м2/г и более предпочтительно приблизительно 220 м2/г.
[0072]
Затем оксид хрома может быть фторирован с получением фторированного оксида хрома. Температура фторирования может находиться в температурном интервале, в котором образующаяся вода не конденсируется, и верхняя граница может представлять собой температуру, при которой катализатор не кристаллизуется из-за теплоты реакции. Температура фторирования может быть установлена, например, на 100-460°C. Хотя давление во время фторирования не ограничено, предпочтительно проводить фторирование при давлении во время введения в каталитическую реакцию.
[0073]
В качестве цеолитных катализаторов могут быть широко использованы известные типы цеолита. Например, предпочтительны кристаллические гидратированные алюмосиликаты щелочных металлов или щелочноземельных металлов. Кристаллическая форма цеолита не ограничена, и примеры включают A тип, X тип, LSX тип и т.п. Щелочной металл или щелочноземельный металл в цеолите не ограничен, и примеры включают калий, натрий, кальций, литий и т.п.
[0074]
Так как цеолитный катализатор показывает более высокую активность за счет фторирования, цеолитный катализатор может быть предварительно фторирован перед применением в реакции и использован в виде фторированного цеолитного катализатора.
[0075]
Подходящие для использования примеры фторирующих агентов для фторирования цеолитных катализаторов включают неорганические фторирующие агенты, такие как F2 и HF; органические фторирующие агенты на основе фторуглеродов, такие как гексафторпропен, и т.п.
[0076]
Способ фторирования цеолитного катализатора представляет собой, например, фторирование путем циркуляции упомянутого выше фторирующего агента при атмосферном давлении при температуре от комнатной температуры (25°C) до приблизительно 400°C.
[0077]
Алюмосиликатный катализатор представляет собой катализатор на основе сложного оксида, содержащий диоксид кремния (SiO2) и оксид алюминия (Al2O3). Когда общее количество диоксида кремния и оксида алюминия принимают за 100% масс., подходящий катализатор имеет, например, содержание диоксида кремния от 20 до 90% масс. и особенно от 50 до 80% масс.
[0078]
Так как алюмосиликатный катализатор показывает более высокую активность за счет фторирования, алюмосиликатный катализатор может быть предварительно фторирован перед применением в реакции и использован в виде фторированного алюмосиликатного катализатора.
[0079]
Подходящие для использования примеры фторирующих агентов для фторирования алюмосиликатных катализаторов включают неорганические фторирующие агенты, такие как F2 и HF; органические фторирующие агенты на основе фторуглеродов, такие как гексафторпропен, и т.п.
[0080]
Способ фторирования алюмосиликатного катализатора представляет собой, например, фторирование путем циркуляции упомянутого выше фторирующего агента при атмосферном давлении при температуре от комнатной температуры (25°C) до приблизительно 400°C.
[0081]
Описанные выше катализаторы могут быть использованы по отдельности или в комбинации из двух или более. С точки зрения степени конверсии, селективности и выхода предпочтительными из них являются катализаторы на основе активированного угля (активированный уголь или фторированный активированный уголь), хромоксидные катализаторы (оксид хрома или фторированный оксид хрома) и т.д.; и более предпочтительны катализаторы на основе активированного угля (активированный уголь или фторированный активированный уголь).
[0082]
Когда упомянутые выше хромоксидный катализатор, цеолитный катализатор, алюмосиликатный катализатор или т.п., используют в качестве катализатора, он может быть также нанесен на носитель. Подходящие примеры таких носителей включают углерод, оксид алюминия (Al2O3), оксид циркония (ZrO2), диоксид кремния (SiO2), оксид титана (TiO2) и т.п. В качестве углерода могут быть использованы активированный уголь, аморфный углерод, графит, алмаз и т.д.
[0083]
В способе производства по настоящему изобретению, когда галогенированное бутановое соединение вводят в реакцию дегидрофторирования в газовой фазе в присутствии катализатора, например, предпочтительно катализатор в твердом состоянии (твердая фаза) приводить в контакт с галогенированным бутановым соединением. В этом случае форма катализатора может представлять собой порошок; однако форма гранул предпочтительна, когда катализатор используют в реакции газофазного непрерывного поточного процесса.
[0084]
Удельная площадь поверхности катализатора (здесь и далее также называемая «удельной площадью поверхности по БЭТ»), измеренная по методу БЭТ, обычно составляет предпочтительно от 10 до 3000 м2/г, более предпочтительно от 10 до 2500 м2/г, даже более предпочтительно от 20 до 2000 м2/г и особенно предпочтительно от 30 до 1500 м2/г. Когда удельная площадь поверхности по БЭТ катализатора находится в пределах этих интервалов, плотность частиц катализатора не является слишком маленькой. Следовательно, галогенированное бутеновое соединение может быть получено с более высокой селективностью. Кроме того, степень конверсии галогенированного бутанового соединения может быть дополнительно улучшена.
[0085]
Циклическое галогенкарбидное соединение
В настоящем изобретении стадии введения галогенированного бутанового соединения в реакцию дегидрофторирования также могут быть проведены в присутствии циклического галогенкарбидного соединения. Циклическое галогенкарбидное соединение относится к циклическому галогенкарбидному соединению, в котором все атомы водорода, связанные с атомами углерода, в углеводородном соединении замещены атомами галогена. Другими словами, это соединение относится к циклическому галогенкарбидному соединению, состоящему из атомов углерода и атомов галогена и не содержащему атомы водорода.
[0086]
Когда стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования проводят в присутствии такого циклического галогенкарбидного соединения, можно сдвинуть равновесие реакции в сторону продукта, и галогенированное бутеновое соединение, которое является целевым продуктом, может быть получено с более высокой степенью конверсии и более высоким выходом.
[0087]
В качестве такого циклического галогенкарбидного соединения могут быть одобрены соединения, описанные в разделе «(1-1-2-1) Жидкофазная реакция». То же самое относится к предпочтительным конкретным примерам и используемым количествам.
[0088]
В способе производства по настоящему изобретению, когда галогенированное бутановое соединение подвергают реакции дегидрофторирования в газовой фазе в присутствии циклического галогенкарбидного соединения, например, предпочтительно циклическое галогенкарбидное соединение в форме газа (газовая фаза) приводить в контакт с галогенированным бутановым соединением.
[0089]
Температура реакции
На стадии введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении температура реакции обычно составляет предпочтительно 230°C или выше, более предпочтительно 280°C или выше и даже более предпочтительно 320°C или выше с точки зрения того, что реакция дегидрофторирования может протекать более эффективно, степень конверсии может быть дополнительно улучшена, а галогенированное бутеновое соединение как целевое соединение может быть получено с более высокой селективностью. Когда активированный уголь используют в качестве катализатора и когда циклическое галоген-карбидное соединение не используют, температура реакции предпочтительно является более высокой, чтобы стимулировать реакцию дегидрофторирования более эффективно, и составляет предпочтительно 400°C или выше и более предпочтительно 420°C или выше. Даже когда активированный уголь используют в качестве катализатора и когда галогенированное бутановое соединение подвергают реакции дегидрофторирования в газовой фазе в присутствии циклического галогенкарбидного соединения, реакция дегидрофторирования может протекать более эффективно; таким образом, температура реакции может быть установлена немного ниже и обычно составляет предпочтительно 230°C или выше, более предпочтительно 280°C или выше и даже более предпочтительно 320°C или выше.
[0090]
Температура реакции для введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении, как правило, составляет предпочтительно 500°C или ниже и более предпочтительно 450°C или ниже с точки зрения того, что реакция дегидрофторирования может протекать более эффективно, степень конверсии может быть дополнительно улучшена, а галогенированное бутеновое соединение в качестве целевого соединения может быть получено с более высокой селективностью.
[0091]
Время реакции
Что касается времени реакции в случае введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении, например, когда используют газофазный проточный процесс, время контакта соединения исходного материала с катализатором (W/F) [W: масса (г) катализатора, F: расход (куб.см/сек) соединения исходного материала] составляет предпочтительно от 5 до 100 г.сек/куб.см, более предпочтительно от 10 до 90 г.сек/куб.см и даже более предпочтительно от 15 до 80 г.сек/куб.см, с точки зрения того, что степень конверсии реакции является особенно высокой, а галогенированное бутеновое соединение может быть получено с более высоким выходом и более высокой селективностью. Когда галогенированное бутановое соединение подвергают реакции дегидрофторирования в газовой фазе в присутствии циклического галогенкарбидного соединения, реакция дегидрофторирования может протекать более эффективно; следовательно, нижняя граница времени контакта может быть дополнительно понижена, и время контакта составляет предпочтительно от 1 до 100 г.сек/куб.см, более предпочтительно от 2 до 90 г.сек/куб.см и даже более предпочтительно от 3 до 80 г.сек/куб.см. Время контакта относится ко времени контакта между соединением исходного материала и катализатором.
[0092]
Давление реакции
Давление реакции при введении галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении составляет предпочтительно 0 кПа или больше, более предпочтительно 10 кПа или больше, даже более предпочтительно 20 кПа или больше и особенно предпочтительно 30 кПа или больше, с точки зрения того, что реакция дегидрофторирования может протекать более эффективно, степень конверсии может быть дополнительно улучшена, а галогенированное бутеновое соединение в качестве целевого соединения может быть получено с более высокой селективностью. Верхняя граница давления реакции не ограничена и обычно равна приблизительно 2 МПа. В настоящем изобретении давление является избыточным, если не указано иное.
[0093]
В реакции дегидрофторирования галогенированного бутанового соединения в настоящем изобретении реактор для взаимодействия галогенированного бутанового соединения и предпочтительно катализатора и циклического галогенкарбидного соединения не ограничен по его форме и структуре, пока он может выдерживать описанные выше температуру и давление. Примеры реактора включают вертикальный реактор, горизонтальный реактор, многотрубчатый реактор и т.п. Примеры материала реактора включают стекло, нержавеющую сталь, железо, никель, железоникелевые сплавы и т.п.
[0094]
Примеры реакции дегидрофторирования
Реакция дегидрофторирования галогенированного бутанового соединения в настоящем изобретении может быть проведена в периодическом процессе или проточном процессе, в котором галогенированное бутановое соединение в качестве соединения исходного материала непрерывно подают в реактор, а галогенированное бутеновое соединение в качестве целевого соединения непрерывно выводят из реактора. Если галогенированное бутеновое соединение в качестве целевого соединения остается в реакторе, реакция отщепления может протекать дальше; следовательно, предпочтительно проводить реакцию в поточном процессе. Стадию введения галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении предпочтительно проводят в газовой фазе, особенно с помощью газофазного непрерывного поточного процесса с использованием реактора с неподвижным слоем. При использовании газофазного непрерывного поточного процесса устройство, работа и т.д. могут быть упрощены, что экономически выгодно. При применении периодического процесса также можно использовать замкнутый реакционный процесс или реакционный процесс при повышенном давлении, рассмотренные выше в разделе «Жидкофазная реакция».
[0095]
Атмосфера при введении галогенированного бутанового соединения в реакцию дегидрофторирования в настоящем изобретении предпочтительно представляет собой атмосферу инертного газа, атмосферу газообразного фторида водорода или т.п., с точки зрения подавления деградации катализатора. Примеры инертного газа включают азот, гелий, аргон и т.п. Из этих инертных газов азот является предпочтительным с точки зрения сокращения затрат. Концентрация инертного газа составляет предпочтительно от 0 до 50% мол. газового компонента, введенного в реактор.
[0096]
После завершения реакции дегидрофторирования необязательно может быть проведена очистка в соответствии с традиционными методами с получением в результате галогенированного бутенового соединения, представленного формулой (2A).
[0097]
(1-1-3) Целевое соединение (Галогенированное бутеновое соединение)
Целевым соединением по настоящему изобретению, полученным описанным выше образом, является галогенированное бутеновое соединение, представленное формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена.
[0098]
В формуле (2A) X1, X2, X3, X4, X5, X6 и X7 являются такими же, как X1, X2, X3, X4, X5, X6 и X7 в формуле (1A), соответственно. Следовательно, конкретные примеры получаемого галогенированного бутенового соединения, представленного формулой (2A), включают CF3CF=CHCF3, CCl3CCl=CHCCl3, CBr3CBr=CHCBr3 и т.п. Эти соединения содержат как Z-, так и E-изомеры.
[0099]
Полученное таким образом галогенированное бутеновое соединение может быть эффективно использовано для разных областей применения, таких как травильные газы для формирования новейших микроструктур в полупроводниках, жидкие кристаллы и т.д., а также в качестве очищающих газов, осаждающих газов, хладагентов, теплопередающих сред и строительных блоков для органического синтеза. Осаждающий газ и строительный блок для органического синтеза описаны ниже.
[0100]
1-2: Способ производства галогенированного бутинового соединение из галогенированного бутенового соединения
Способ производства галогенированного бутинового соединения по настоящему изобретению представляет собой способ производства галогенированного бутинового соединения, представленного формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
и этот способ включает введение галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше, и X4 представляет собой атом галогена, в реакцию дегидрогалогенирования.
[0101]
В соответствии с настоящим изобретением, когда галогенированное бутеновое соединение, представленное формулой (2A), подвергают реакции дегидрогалогенирования, может быть получено селективно галогенированное бутиновое соединение, представленное формулой (3A), в котором отщеплен 1 моль галогенида водорода на моль галогенированного бутенового соединения, представленного формулой (2A).
[0102]
(1-2-1) Соединение исходного материала (Галогенированное бутеновое соединение)
Галогенированное бутеновое соединение в качестве субстрата, который может быть использован в способе производства по настоящему изобретению, представляет собой, как описано выше, галогенированное бутеновое соединение, представленное формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена, и соответствует целевому соединению в разделе «1-1: Способ производства галогенированного бутенового соединения из галогенированного бутанового соединения».
[0103]
В формуле (2A) в качестве атома галогена, представленного X1, X2, X3, X4, X5, X6 и X7, могут быть использованы атомы галогена, упомянутые выше. То же самое относится к предпочтительным типам.
[0104]
Конкретные примеры галогенированного бутенового соединения в качестве субстрата, который удовлетворяет приведенным выше условиям, включают CF3CF=CHCF3, CCl3CCl=CHCCl3, CBr3CBr=CHCBr3 и т.п. Эти соединения содержат как Z- и E-изомеры. Эти галогенированные бутеновые соединения могут быть использованы по отдельности или в комбинации из двух или более. Такие галогенированные бутеновые соединения могут представлять сбой известные или коммерчески доступные продукты.
[0105]
(1-2-2) Реакция дегидрогалогенирования
На стадии введения галогенированного бутенового соединения в реакцию дегидрогалогенирования в настоящем изобретении, например, в галогенированном бутеновом соединении, представленном формулой (2A), в качестве субстрата X1, X2, X3, X4, X5, X6 и X7 более предпочтительно представляют собой атомы фтора.
[0106]
То есть, эта реакция предпочтительно представляет собой реакцию дегидрофторирования в соответствии со следующим уравнением реакции:
CF3CF=CHCF3 → CF3C≡CCF3+HF.
[0107]
Стадия введения галогенированного бутенового соединения в реакцию дегидрогалогенирования в настоящем изобретении может быть проведена в жидкой фазе или газовой фазе. Особенно с точки зрения производительности предпочтительно проводить эту стадию в газовой фазе.
[0108]
Стадию введения галогенированного бутенового соединения в реакцию дегидрогалогенирования в настоящем изобретении предпочтительно проводят в присутствии катализатора и/или основания с точки зрения получения целевого соединения с более высокой селективностью и более высокой степенью конверсии. Более конкретно, когда используют жидкофазную реакцию, эту стадию предпочтительно проводят в присутствии основания и необязательно катализатора, и когда используют газофазную реакцию, эту стадию предпочтительно проводят в присутствии катализатора. Для получения подробной информации по жидкофазной реакции (растворитель, основание, катализатор, циклическое галогенкарбидное соединение, условия замкнутого реакционного процесса и реакционного процесса при повышенном давлении и т.д.) и подробной информации по газофазной реакции (катализатор, циклическое галогенкарбидное соединение, температура реакции, время реакции, давление реакции и т.д.) может быть применено объяснение раздела «1-1: Способ производства галогенированного бутенового соединения из галогенированного бутанового соединения», за исключением того, что выражение «реакция для получения галогенированного бутенового соединения из галогенированного бутанового соединения реакцией дегидрофторирования» читается как «реакция для получения галогенированного бутинового соединения из галогенированного бутенового соединения реакцией дегидрогалогенирования». То же самое относится к предпочтительным типам и содержаниям.
[0109]
После завершения реакции дегидрогалогенирования необязательно может быть проведена очистка в соответствии с традиционными методами, с получением в результате галогенированного бутинового соединения, представленного формулой (3A).
[0110]
(1-2-3) Целевое соединение (Галогенированное бутиновое соединение)
Целевым соединение по настоящему изобретению, получаемым описанным выше образом, является галогенированное бутиновое соединение, представленное формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена.
[0111]
В формуле (3A) X1, X2, X3, X5, X6 и X7 являются такими же, как X1, X2, X3, X5, X6 и X7 в формуле (2A), соответственно. Таким образом, конкретные примеры галогенированного бутинового соединения, представленного формулой (3A), которое производят, включают CF3C≡CCF3, CCl3C≡CCCl3, CBr3C≡CCBr3 и т.п.
[0112]
Полученное таким образом галогенированное бутиновое соединение может быть эффективно использовано для разных областей применения, таких как травильные газы для формирования новейших микроструктур в полупроводниках, жидкие кристаллы и т.д., а также в качестве очищающих газов, осаждающих газов, хладагентов, теплопередающих сред и строительных блоков для органического синтеза. Осаждающий газ и строительный блок для органического синтеза описаны позднее.
[0113]
1-3: Способ производства галогенированного бутинового соединения из галогенированного бутанового соединения через галогенированное бутеновое соединение
Способ производства галогенированного бутинового соединения по настоящему изобретению представляет собой способ производства галогенированного бутинового соединения, представленного формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 являются одинаковыми или разными и каждый представляет собой атом галогена,
и этот способ включает:
(IA) введение галогенированного бутанового соединения, представленного формулой (1A):
CX1X2X3CHX4CFHCX5X6X7 (1A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше, и X4 представляет собой атом галогена, в реакцию дегидрофторирования с получением галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 имеют значения, определенные выше;
(IIA) после стадии (IA) удаление фторида водорода; и
(IIIA) после стадии (IIA) введение полученного галогенированного бутенового соединения, представленного формулой (2A):
CX1X2X3CX4=CHCX5X6X7 (2A),
где X1, X2, X3, X4, X5, X6 и X7 имеют значения, определенные выше, в реакцию дегидрогалогенирования с получением галогенированного бутинового соединения, представленного формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше.
[0114]
(1-3-1) Стадия (IA)
В способе производства галогенированного бутинового соединения по настоящему изобретению объяснение раздела «1-1: Способ производства галогенированного бутенового соединения из галогенированного бутанового соединения» может быть применено к стадии (IA), как оно есть.
[0115]
(1-3-2) Стадия (IIA)
Способ производства галогенированного бутинового соединения по настоящему изобретению включает введение галогенированного бутанового соединения, представленного формулой (1A), в реакцию дегидрофторирования с получением галогенированного бутенового соединения, представленного формулой (2A) (стадия (IA)), и затем удаление фторида водорода из смеси, содержащей галогенированное бутеновое соединение и фторид водорода (стадия (IIA)).
[0116]
В способе производства галогенированного бутинового соединения по настоящему изобретению после стадии (IA) фторид водорода, образовавшийся в результате реакции дегидрофторирования на стадии (IA), отделяют и/или удаляют, после чего следует производство галогенированного бутинового соединения на следующей стадии (IIIA), посредством чего галогенированное бутиновое соединение, которое является целевым соединением, может быть получено путем дегидрофторирования с высокой степенью конверсии (выход) и высокой селективностью.
[0117]
Фторид водорода может быть удален из смеси, содержащей галогенированное бутеновое соединение и фторид водорода, полученной на стадии (IA), предпочтительно путем отделения фторида водорода в ректификационной колонне (ФИГ. 1) или путем удаления фторида водорода с использованием агента удаления галогенида водорода (колонна для удаления), такого как щелочь, Secard, алюминий или диоксид кремния (ФИГ. 2).
[0118]
В способе производства галогенированного бутинового соединения по настоящему изобретению непрореагировавшие исходные материалы (галогенированное бутановое соединение и т.д.), отделенные путем ректификации, предпочтительно использовать повторно. В способе производства галогенированного бутинового соединения по настоящему изобретению непрореагировавшее галогенированное бутановое соединение, отделенное ректификацией, может быть возвращено (использовано повторно) в реактор и использовано для дегидрофторирования.
[0119]
Способ отделения фторида водорода в ректификационной колонне
Температура кипения фторида водорода (HF), который должен быть отделен, составляет 19,54°C.
[0120]
Чтобы удалить фторид водорода из смеси, содержащей галогенированное бутеновое соединение и фторид водорода, которая получена на стадии (IA), галогенированное бутеновое соединение и фторид водорода разделяют в ректификационной колонне на основании температур кипения обоих соединений и на основании разницы температур кипения обоих соединений. Затем галогенированное бутеновое соединение собирают, а фторид водорода может быть отделен. При производстве галогенированного бутинового соединения на следующей стадии (IIIA) содержание фторида водорода может быть уменьшено, и галогенированное бутиновое соединение как целевое соединение может быть произведено с высокой степенью конверсии (выход) и высокой селективностью.
[0121]
Способ удаления фторида водорода с использованием агента удаления галогенида водорода
Фторид водорода, который необходимо отделить, может быть удален с помощью агента удаления фторида водорода. В качестве агента удаления фторида водорода предпочтительно использовать щелочь, оксид алюминия, диоксид кремния, цеолит, Secard и подобные агенты удаления фторида водорода. Secard представляет собой адсорбент (синтетический цеолит), в котором используется в качестве основного сырьевого материала аморфный глинистый минералоид (оксид алюминия/силикагель), называемый «аллофаном», и который состоит из гидратированного алюмосиликата от аморфного до слабо кристаллического.
[0122]
Чтобы удалить фторид водорода из смеси, содержащей галогенированное бутеновое соединение и фторид водорода, которая получена на стадии (IA), фторид водорода удаляют с использованием агента удаления фторида водорода, а галогенированное бутеновое соединение может быть собрано. При производстве галогенированного бутинового соединения на следующей стадии (IIIA) содержание фторида водорода может быть уменьшено, и галогенированное бутиновое соединение как целевое соединение может быть произведено с высокой степенью конверсии (выход) и высокой селективностью.
[0123]
Концентрация фторида водорода
В способе производства галогенированного бутинового соединения по настоящему изобретению после стадии (IA) фторид водорода, образовавшийся в результате дегидрофторирования на стадии (IA), отделяют и/или удаляют, после чего следует производство галогенированного бутинового соединения на следующей стадии (IIIA), в результате чего галогенированное бутиновое соединение, которое является целевым соединением, может быть получено путем дегидрофторирования с высокой степенью конверсии (выход) и высокой селективностью.
[0124]
При производстве галогенированного бутинового соединения на следующей стадии (IIIA) галогенированное бутеновое соединение, представленное формулой (2A), используют в качестве соединения исходного материала. В этом случае помимо галогенированного бутенового соединения, представленного формулой (2A), смесь, содержащая фторид водорода, образовавшийся при дегидрофторировании, может быть введена в производство галогенированного бутинового соединения на следующей стадии (IIIA).
[0125]
В способе производства галогенированного бутинового соединения по настоящему изобретению с точки зрения того, что при производстве галогенированного бутинового соединения на следующей стадии (IIIA) галогенированное бутиновое соединение, которое является целевым соединением, производят путем дегидрофторирования с высокой степенью конверсии (выход) и высокой селективностью, в композиции, используемой в качестве сырьевого материала на следующей стадии (IIIA), из расчета на смесь, содержащую галогенированное бутеновое соединение, представленное формулой (2A), и фторид водорода (100% мол.), содержание фторида водорода (концентрация) составляет предпочтительно 50% мол. или меньше, более предпочтительно 20% мол. или меньше, даже более предпочтительно 3% мол. или меньше, и особенно предпочтительно 0,1% мол. или меньше. Когда смесь, содержащая галогенированное бутеновое соединение, представленное формулой (2A), и фторид водорода, имеет низкое содержание фторида водорода, галогенированное бутиновое соединение, которое является целевым соединением, может быть произведено с высокой степенью конверсии (выход) и высокой селективностью.
[0126]
(1-3-3) Стадия (IIIA)
В способе производства галогенированного бутинового соединения по настоящему изобретению объяснение раздела «1-2: Способ производства галогенированного бутинового соединения из галогенированного бутенового соединения» применимо к стадии (IIIA), как оно есть.
[0127]
(1-3-4) Примеры дегидрофторирования
На стадии проведения дегидрофторирования в настоящем изобретении реакция может быть проведена в периодическом процессе или в поточном процессе, в котором соединение исходного материала (галогенированное бутановое соединение) непрерывно подают в реактор, а целевое соединение (галогенированное бутеновое соединение) непрерывно выводят из реактора на стадии (IA). Затем фторид водорода удаляют из смеси, содержащей галогенированное бутеновое соединение или фторид водорода (стадия (IIA)). Стадия (IIIA) может быть проведена в периодическом процессе или проточном процессе, в котором соединение исходного материала (галогенированное бутеновое соединение) непрерывно подают в реактор, а целевое соединение (галогенированное бутиновое соединение) непрерывно выводят из реактора. На каждой стадии целевое соединение (галогенированное бутеновое соединение или галогенированное бутиновое соединение) не остается в реакторе, и дегидрофторирование может протекать дальше; следовательно, предпочтительно проводить реакцию в поточном процессе.
[0128]
На стадии проведения дегидрофторирования в настоящем изобретении реакцию предпочтительно проводят в газовой фазе, особенно с помощью газофазного непрерывного поточного процесса с использованием реактора с неподвижным слоем. При использовании газофазного непрерывного поточного процесса устройство, работа и т.д. могут быть упрощены, что экономически выгодно.
[0129]
На стадии проведения дегидрофторирования в настоящем изобретении атмосфера при проведении реакции предпочтительно представляет собой атмосферу инертного газа с точки зрения подавления деградации катализатора (активированного угля, металлического катализатора и т.д.). В настоящем изобретении инертный газ предпочтительно представляет собой, по меньшей мере, один газ, выбираемый из группы, включающей азот, гелий, аргон и диоксид углерода. Из этих инертных газов азот более предпочтителен с точки зрения сокращения затрат. Концентрация инертного газа составляет предпочтительно от 0 до 50% мол. газового компонента, введенного в реактор.
[0130]
На стадии проведения дегидрофторирования в настоящем изобретении после окончания реакции, как описано выше, необязательно может быть проведена очистка в соответствии с традиционными методами с получением целевого соединения (галогенированного бутенового соединения или галогенированного бутинового соединения).
[0131]
2. Способы производства галогенированного алкенового соединения и фторированного алкинового соединения
2-1: Способ производства галогенированного алкенового соединения из галогенированного алканового соединения
Способ производства галогенированного алкенового соединения по настоящему изобретению представляет собой способ производства галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу, и X8 представляет собой атом галогена,
и этот способ включает введение галогенированного алканового соединения, представленного формулой (1B):
CHX8A1CHX9A2 (1B),
где A1 и A2 имеют значения, определенные выше, и X8 и X9 являются одинаковыми или разными и каждый представляет собой атом галогена, в реакцию дегидрогалогенирования в присутствии катализатора в газовой фазе.
[0132]
В соответствии с настоящим изобретением, когда галогенированное алкановое соединение, представленное формулой (1B), подвергают реакции дегидрогалогенирования в присутствии катализатора в газовой фазе, может быть получено селективно галогенированное алкеновое соединение, представленное формулой (2B), в котором 1 моль галогенида водорода отщеплен на моль галогенированного алканового соединения, представленного формулой (1B). Более того, реакция отщепления галогенида водорода, представленного как HX8, от галогенированного алкенового соединения, представленного формулой (2B), вряд ли будет проходить непрерывно. Кроме того, в соответствии с настоящим изобретением в качестве галогенированного алкенового соединения, представленного формулой (2B), E-изомер может быть синтезирован селективно среди других геометрических изомеров. Этот эффект более выражен, когда A1 и A2 представляют собой перфторалкильные группы. Так как α-углерод тригалогенированных метильных групп, таких как CF3 группа, становится электронодефицитным из-за эффекта притяжения электронов тригалогенированных метильных групп, таких как CF3 группа, галогенированные анионы, такие как анионы фтора, десорбируются с меньшей вероятностью. Как результат, галогенированный бутен должен образовываться с большей вероятностью, чем галогенированный бутин. Кроме того, селективный синтез E-изомера более выражен, когда A1 и A2 представляют собой трифторметильные группы. Это обусловлено тем, что транс-конфигурация энергетически более стабильна из-за стерического затруднения тригалогенированных метильных групп, таких как CF3 группа.
[0133]
(2-1-1) Соединение исходного материала (Галогенированное алкановое соединение)
В настоящем изобретении соединение исходного материала в способе производства галогенированного алкенового соединения из галогенированного алканового соединения представляет собой галогенированное алкановое соединение, представленное формулой (1B):
CHX8A1CHX9A2 (1B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу, и X8 и X9 являются одинаковыми или разными и каждый представляет собой атом галогена.
[0134]
В формуле (1B) в качестве перфторалкильной группы, обозначенной как A1 и A2, и атома галогена, обозначенного как X8 и X9, могут быть использованы те, что упомянуты выше. То же самое применимо к предпочтительным конкретным примерам.
[0135]
Примеры галогенированного алканового соединения в качестве соединения исходного материала, которое удовлетворяет приведенным выше условиям, включают CF3CHClCHClCF3 (336mdd), CF3CHClCHFCl, CHFClCHFCl, CF3CHFCHFCF3 (338mee), CF3CHFCHF2, CHF2CHF2, CF3CHClCHClC2F5, C2F5CHClCHClC2F5, C2F5CHClCHFCl, CF3CHFCHFC2F5, C2F5CHFCHFC2F5, C2F5CHFCHF2 и т.п. Эти галогенированные алкановые соединения могут быть использованы по отдельности или в комбинации из двух или более. Такие галогенированные алкановые соединения могут представлять сбой известные или коммерчески доступные продукты.
[0136]
(2-1-2) Реакция дегидрогалогенирования
На стадии введения галогенированного алканового соединения в реакцию дегидрогалогенирования в настоящем изобретении с точки зрения способности давать галогенированное алкеновое соединение из галогенированного алканового соединения с высокой степенью конверсии (выход) и высокой селективностью, например, в галогенированном алкановом соединении, представленном формулой (1B), в качестве субстрата A1 и A2 предпочтительно оба представляют собой трифторметильные группы (CF3-), и X8 и X9 более предпочтительно представляют собой атомы фтора или атомы хлора.
[0137]
То есть, эта реакция представляет собой предпочтительно реакцию дегидрофторирования или дегидрохлорирования в соответствии со следующими уравнениями реакции:
CF3CHClCHClCF3 (336mdd) → CF3CCl=CHCF3 ((Z) или (E)-1326mxz) + HCl
CF3CHFCHFCF3 (338mee) → CF3CF=CHCF3 ((Z) или (E)-1327myz) + HF
[0138]
Катализатор
Стадию введения галогенированного алканового соединения в реакцию дегидрогалогенирования с получением галогенированного алкенового соединения в настоящем изобретении проводят в присутствии катализатора в газовой фазе.
[0139]
Катализатор, используемый на этой стадии, представляет собой предпочтительно, по меньшей мере, один катализатор, выбираемый из группы, состоящей из активированного угля и металлического катализатора, с точки зрения степени конверсии, селективности и выхода.
[0140]
Когда в качестве катализатора, используемого на этой стадии, используют металлический катализатор, металлический катализатор представляет собой предпочтительно, по меньшей мере, один катализатор, выбираемый из группы, состоящей из оксида хрома, фторированного оксида хрома, фторида хрома, оксида алюминия, фторированного оксида алюминия, фторида алюминия, оксида железа, фторированного оксида железа, фторида железа, оксида никеля, фторированного оксида никеля, фторида никеля, оксида магния, фторированного оксида магния и фторида магния.
[0141]
На этой стадии с точки зрения способности взаимодействовать с галогенированным алкановым соединением, в качестве соединения исходного материала, с высокой степенью конверсии (выход) и давать галогенированное алкеновое соединение, в качестве целевого соединения, с высокой селективностью из этих катализаторов более предпочтительны активированный уголь, оксид хрома, фторированный оксид хрома, оксид алюминия, фторированный оксид алюминия и т.д.
[0142]
На этой стадии, когда соединение исходного материала вводят в контакт с катализатором в газовой фазе, предпочтительно вводить катализатор в твердом состоянии (твердая фаза) в контакт с соединением исходного материала.
[0143]
На этой стадии катализатор может находиться в порошковой форме; однако форма гранул предпочтительна в случае реакции газофазного непрерывного поточного процесса.
[0144]
Удельная площадь поверхности катализатора (далее называемая «удельной площадью поверхности по БЭТ»), измеренная по методу БЭТ, обычно составляет предпочтительно от 10 до 3000 м2/г, более предпочтительно от 100 до 2000 м2/г, даже более предпочтительно от 500 до 1500 м2/г и особенно предпочтительно от 1000 до 1300 м2/г. Когда удельная площадь поверхности по БЭТ катализатора находится в пределах этого интервала, плотность частиц катализатора не является слишком низкой. Следовательно, целевое соединение может быть получено с более высокой селективностью. Кроме того, степень конверсии соединения исходного материала может быть дополнительно улучшена.
[0145]
Когда активированный уголь используют в качестве катализатора, предпочтительно использовать порошкообразный активированный уголь, такой как измельченный уголь, формованный уголь, гранулированный уголь и сферический уголь. В качестве порошкообразного активированного угля, предпочтительно использовать порошкообразный активированный уголь, который показывает размер частиц от 4 меш (4,76 мм) до 100 меш (0,149 мм) в соответствии с испытанием JIS.
[0146]
Когда активированный уголь используют как катализатор, в качестве формы активированного угля (например, удельная площадь поверхности приблизительно 1200 м2/г), предпочтительно использовать или порошкообразный или гранулированный активированный уголь, и более предпочтительно использование гранулированного активированного угля.
[0147]
Когда металлический катализатор используют в качестве катализатора, его предпочтительно наносят на носитель. В качестве носителя, например, предпочтительно могут быть использованы углерод, оксид алюминия (Al2O3), оксид циркония (ZrO2), диоксид кремния (SiO2), оксид титана (TiO2) и т.п. Кроме того, в качестве углерода предпочтительно может быть использован активированный уголь, аморфный углерод, графит, алмаз и т.п.
[0148]
Оксид хрома и фторированный оксид хрома описаны в настоящем изобретении в качестве примеров катализатора. Например, когда оксид хрома представлен как Cr2O3.nH2O, n имеет значение предпочтительно 3 или меньше и более предпочтительно от 1 до 1,5. Кроме того, в случае оксида хрома предпочтительно, чтобы в формуле состава CrOm значение m удовлетворяло условию 1,5<m<3. В качестве катализатора может быть приготовлен фторированный оксид хрома путем фторирования оксида хрома. Примеры фторирования включают фторирование с помощью фторида водорода (HF), фторирование с помощью фторуглерода и др.
[0149]
Оксид хрома в качестве катализатора может быть получен в соответствии с методом, описанным, например, в документе JP 3412165B. Оксид хрома может быть фторирован фторидом водорода (обработка HF) с получением фторированного оксида хрома. Температура фторирования, например, составляет предпочтительно от 100 до 460°C. Давление при фторировании предпочтительно представляет собой давление во время проведения каталитической реакции. В настоящем изобретении особенно предпочтительно использовать высокофторированный хромоксидный катализатор с высоким содержанием фтора. Высокофторированный хромоксидный катализатор может быть получен путем фторирования оксида хрома при более высокой температуре, чем обычно, в течение длительного периода времени.
[0150]
Высокофторированный хромоксидный катализатор предпочтительно имеет содержание фтора 30% масс. или больше и более предпочтительно от 30 до 45% масс. Содержание фтора может быть измерено по изменению массы катализатора или с помощью метода обычного количественного анализа оксида хрома.
[0151]
Циклическое галогенкарбидное соединение
В настоящем изобретении стадия введения галогенированного алканового соединения в реакцию дегидрогалогенирования может быть проведена в присутствии циклического галогенкарбидного соединения. Циклическое галогенкарбидное соединение относится к циклическому галогенкарбидному соединению, в котором все атомы водорода, связанные с атомами углерода, в углеводородном соединении замещены атомами галогена. Другими словами, это соединение относится к циклическому галогенкарбидному соединению, состоящему атомов углерода и атомов галогена и не содержащему атомы водорода.
[0152]
Когда стадию введения галогенированного алканового соединения в реакцию дегидрогалогенирования проводят в присутствии такого циклического галогенкарбидного соединения, галогенированное алкеновое соединение как целевой продукт может быть получено с более высокой степенью конверсии и более высоким выходом.
[0153]
В качестве циклического галогенкарбидного соединения могут быть использованы упоминавшиеся выше соединения. То же самое применимо к предпочтительным конкретным примерам, используемым количествам, методам введения в жидкофазную реакцию и газофазную реакцию и т.п.
[0154]
Температура реакции
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении нижняя граница температуры реакции обычно равна 50°C, предпочтительно 70°C и более предпочтительно 100°C с точки зрения более эффективного стимулирования реакции дегидрогалогенирования и получения целевого соединения (галогенированного алкенового соединения) с более высокой селективностью, а также с точки зрения подавления снижения степени конверсии из соединения исходного материала (галогенированного алканового соединения).
[0155]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении верхняя граница температуры реакции обычно равна 500°C, предпочтительно 450°C и более предпочтительно 400°C с точки зрения того, что реакция дегидрогалогенирования может протекать более эффективно, и целевое соединение (галогенированное алкеновое соединение) может быть получено с более высокой селективностью, а также с точки зрения подавления снижения селективности из-за разложения или полимеризации продукта реакции.
[0156]
Время реакции
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении, что касается времени реакции, то, если время контакта соединения исходного материала с катализатором (W/F0) [W: масса (г) катализатора, F0: расход (куб.см/сек) соединения исходного материала] более длительное, степень конверсии соединения исходного материала может быть увеличена; однако растет количество катализатора и требуется крупногабаритное оборудование, что неэффективно.
[0157]
Следовательно, на стадии проведения реакции дегидрогалогенирования в настоящем изобретении, что касается времени контакта, то время контакта (W/F0) соединения исходного материала (галогенированного алканового соединения) с катализатором предпочтительно составляет от 0,1 до 200 г.сек/куб.см, более предпочтительно от 0,2 до 150 г.сек/куб.см, даже более предпочтительно от 0,4 до 100 г.сек/куб.см и особенно предпочтительно от 0,5 до 50 г.сек/куб.см, с точки зрения улучшения степени конверсии соединения исходного материала (галогенированного алканового соединения) и снижения стоимости оборудования.
[0158]
Время контакта соединения исходного материала с катализатором относится ко времени контакта между соединением исходного материала и катализатором.
[0159]
Когда реакцию дегидрогалогенирования по настоящему изобретению проводят в присутствии катализатора в газовой фазе, целевое соединение (галогенированное алкеновое соединение) может быть получено с более высокой селективностью особенно за счет соответствующего регулирования температуры реакции и времени реакции (времени контакта) в зависимости от катализатора.
[0160]
В реакции дегидрогалогенирования по настоящему изобретению, когда оксид хрома используют в качестве катализатора, температура реакции составляет предпочтительно 300°C или выше и более предпочтительно 350°C или выше. Кроме того, время контакта составляет предпочтительно 10 г.сек/куб.см или больше, более предпочтительно 20 г.сек/куб.см или больше и даже более предпочтительно 40 г.сек/куб.см или больше.
[0161]
В реакции дегидрогалогенирования по настоящему изобретению, когда оксид алюминия используют в качестве катализатора, температура реакции составляет предпочтительно 300°C или выше, и время контакта равно предпочтительно 5 г.сек/куб.см или больше.
[0162]
В реакции дегидрогалогенирования по настоящему изобретению, когда активированный уголь используют в качестве катализатора, температура реакции составляет предпочтительно от 50 до 600°C и более предпочтительно от 100 до 400°C. Кроме того, время контакта составляет предпочтительно от 0,2 до 100 г.сек/куб.см, более предпочтительно от 0,3 до 50 г.сек/куб.см и даже более предпочтительно от 0,5 до 43 г.сек/куб.см.
[0163]
Давление реакции
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении давление реакции предпочтительно составляет от -0,05 до 2 МПа, более предпочтительно от -0,01 до 1 МПа и даже более предпочтительно от нормального давления до 0,5 МПа с точки зрения более эффективного стимулирования реакции дегидрогалогенирования. В настоящем изобретении давление является избыточным, если не указано иное.
[0164]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении реактор для взаимодействия соединения исходного материала (галогенированного алканового соединения) и катализатора (активированного угля, металлического катализатора и т.д.) путем введения их в контакт друг с другом не ограничен по форме и структуре, пока он может выдерживать описанные выше температуру и давление. Примеры реактора включают вертикальный реактор, горизонтальный реактор, многотрубчатый реактор и т.п. Примеры материала реактора включают стекло, нержавеющую сталь, железо, никель, железоникелевые сплавы и т.п.
[0165]
Примеры реакции дегидрогалогенирования
Стадия проведения реакции дегидрогалогенирования в настоящем изобретении может быть проведена в периодическом процессе или проточном процессе, в котором соединение исходного материала (галогенированное алкановое соединение) непрерывно подают в реактор, а целевое соединение (галогенированное алкеновое соединение) непрерывно выводят из реактора. Целевое соединение (галогенированное алкеновое соединение) не остается в реакторе, и реакция дегидрогалогенирования может протекать дальше; таким образом, предпочтительно проводить реакцию в поточном процессе.
[0166]
Стадию проведения реакции дегидрогалогенирования в настоящем изобретении предпочтительно проводят в газовой фазе, особенно с помощью газофазного непрерывного поточного процесса с использованием реактора с неподвижным слоем. При использовании газофазного непрерывного поточного процесса устройство, работа и т.д. могут быть упрощены, что экономически выгодно.
[0167]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении атмосфера при проведении реакции предпочтительно представляет собой атмосферу инертного газа с точки зрения подавления деградации катализатора (активированного угля, металлического катализатора и т.д.). В настоящем изобретении инертный газ представляет собой предпочтительно, по меньшей мере, один газ, выбираемый из группы, включающей азот, гелий, аргон и диоксид углерода. Из этих инертных газов азот более предпочтителен с точки зрения сокращения затрат. Концентрация инертного газа составляет предпочтительно от 0 до 50% мол. газового компонента, введенного в реактор.
[0168]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении после окончания реакции необязательно может быть проведена очистка в соответствии с традиционными методами с получением в результате галогенированного алкенового соединения, представленного формулой (2B), которое является целевым соединением.
[0169]
(2-1-3) Целевое соединение (Галогенированное алкеновое соединение)
Целевое соединение по настоящему изобретению, полученное описанным выше образом, представляет собой галогенированное алкеновое соединение, представленное формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу, и X8 представляет собой атом галогена.
[0170]
В формуле (2B) A1, A2 и X8 являются такими же, как A1, A2 и X8 в формуле (1B), соответственно. Следовательно, конкретные примеры галогенированного алкенового соединения, представленного формулой (2B), которое производят, включают CF3CCl=CHCF3 ((Z) или (E)-1326mxz), CF3CCl=CHF, CFCl=CHF, CF3CF=CHCF3 ((Z) или (E)-1327myz), CF3CF=CHF, CF2=CHF, CF3CCl=CHC2F5, C2F5CCl=CHC2F5, C2F5CCl=CHF, CF3CF=CHC2F5, C2F5CF=CHC2F5, C2F5CF=CHF и т.п. Эти соединения содержат как Z-, так и E-изомеры.
[0171]
Полученное таким образом галогенированное алкеновое соединение может быть эффективно использовано для разных областей применения, таких как травильные газы для формирования новейших микроструктур в полупроводниках, жидкие кристаллы и т.д., а также в качестве очищающих газов, осаждающих газов, хладагентов, теплопередающих сред и строительных блоков для органического синтеза. Осаждающий газ и строительный блок для органического синтеза описаны позднее.
[0172]
2-2: Способ производства фторированного алкинового соединения из галогенированного алкенового соединения
Способ производства фторированного алкинового соединения по настоящему изобретению представляет собой способ производства фторированного алкинового соединения, представленного формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу,
и этот способ включает введение галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 имеют значения, определенные выше, и X8 представляет собой атом галогена, в реакцию дегидрогалогенирования в присутствии катализатора.
[0173]
(2-2-1) Соединение исходного материала (Галогенированное алкеновое соединение)
Галогенированное алкеновое соединение в качестве субстрата, который может быть использован в способе производства по настоящему изобретению, представляет собой, как описано выше, галогенированное алкеновое соединение, представленное формулой (2B):
CX8A1=CHA2 (2B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу, и X8 представляет собой атом галогена. Это соединение соответствует целевом соединению раздела «2-1: Способ производства галогенированного алкенового соединения из галогенированного алканового соединения».
[0174]
В формуле (2B) в качестве перфторалкильной группы, обозначенной, как A1 и A2, и атома галогена, обозначенного как X8, могут быть использованы те, что упомянуты выше. То же самое относится к предпочтительным типам.
[0175]
Конкретные примеры галогенированного алкенового соединения в качестве субстрата, который удовлетворяет приведенным выше условиям, включают CF3CCl=CHCF3 ((Z) или (E)-1326mxz), CF3CCl=CHF, CFCl=CHF, CF3CF=CHCF3 ((Z) или (E)-1327myz), CF3CF=CHF, CF2=CHF, CF3CCl=CHC2F5, C2F5CCl=CHC2F5, C2F5CCl=CHF, CF3CF=CHC2F5, C2F5CF=CHC2F5, C2F5CF=CHF и т.п. Эти соединения содержат как Z-, так и E-изомеры. Эти галогенированные алкеновые соединения могут быть использованы по отдельности или в комбинации из двух или более. Такие галогенированные алкеновые соединения могут представлять собой известные или коммерчески доступные продукты.
[0176]
(2-2-2) Реакция дегидрогалогенирования
На стадии введения галогенированного алкенового соединения в реакцию дегидрогалогенирования в настоящем изобретении с точки зрения способности давать фторированное алкиновое соединение из галогенированного алкенового соединения с высокой степенью конверсии (выход) и высокой селективностью, например, в галогенированном алкеновом соединении, представленном формулой (2B), в качестве субстрата, A1 и A2 предпочтительно оба представляют собой трифторметильные группы (CF3-), и X8 более предпочтительно представляет собой атом фтора или атом хлора.
[0177]
То есть, эта реакция представляет собой предпочтительно реакцию дегидрофторирования или реакцию дегидрохлорирования в соответствии со следующими уравнениями реакции:
CF3CCl=CHCF3 ((Z) или (E)-1326mxz) → CF3C≡CCF3 (PF2B) + HCl
CF3CF=CHCF3 ((Z) или (E)-1327myz) → CF3C≡CCF3 (PF2B) + HF
[0178]
Стадия введения галогенированного алкенового соединения в реакцию дегидрогалогенирования в настоящем изобретении может быть проведена в жидкой фазе или газовой фазе. Особенно с точки зрения производительности предпочтительно проводить эту стадию в газовой фазе.
[0179]
Стадию введения галогенированного алкенового соединения в реакцию дегидрогалогенирования в настоящем изобретении предпочтительно проводят в присутствии катализатора и/или основания с точки зрения получения целевого соединения с более высокой селективностью и более высокой степенью конверсии. Говоря точнее, когда используют жидкофазную реакцию, эту стадию предпочтительно проводят в присутствии основания и необязательно катализатора, и когда используют газофазную реакцию, эту стадию предпочтительно проводят в присутствии катализатора. Для получения подробной информации по жидкофазной реакции (растворитель, основание, катализатор, циклическое галоген-карбидное соединение, условия замкнутого реакционного процесса и реакционного процесса при повышенном давлении и т.д.) объяснение раздела «1-1: Способ производства галогенированного бутенового соединения из галогенированного бутанового соединения» может быть применено, за исключение того, что выражение «реакция с получением галогенированного бутенового соединения из галогенированного бутанового соединения реакцией дегидрофторирования» читается как «реакция с получением фторированного алкинового соединения из галогенированного алкенового соединения реакцией дегидрогалогенирования». Кроме того, для получения подробной информации по газофазной реакции (катализатор, циклическое галогенкарбидное соединение, температура реакции, время реакции, давление реакции и т.д.) объяснение раздела «2-1: Способ производства галогенированного алкенового соединения из галогенированного алканового соединения» может быть применено, за исключением того, что выражение «реакция с получением галогенированного алкенового соединения из галогенированного алканового соединения реакцией дегидрогалогенирования» читается как «реакция с получением фторированного алкинового соединения из галогенированного алкенового соединения реакцией дегидрогалогенирования». То же самое относится к предпочтительным типам и содержаниям.
[0180]
После завершения реакции дегидрогалогенирования необязательно может быть проведена очистка в соответствии с традиционными методами с получением в результате фторированного бутинового соединения, представленного формулой (3B).
[0181]
(2-2-3) Целевое соединение (Фторированное бутиновое соединение)
Целевое соединение по настоящему изобретению, полученное описанным выше образом, представляет собой фторированное бутиновое соединение, представленное формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу.
[0182]
В формуле (3B) A1 и A2 являются такими же, как A1 и A2 в формуле (2B), соответственно. Таким образом, конкретные примеры фторированного бутинового соединения, представленного формулой (3B), которое получают, включают CF3C≡CCF3 (PF2B), CF3C≡CF, CF≡CF, CF3C≡CC2F5, C2F5C≡CC2F5, C2F5C≡CF и т.п.
[0183]
Полученное таким образом фторированное бутиновое соединение может быть эффективно использовано для разных областей применения, таких как травильные газы для формирования новейших микроструктур в полупроводниках, жидкие кристаллы и т.д., а также в качестве очищающих газов, осаждающих газов, хладагентов, теплопередающих сред и строительных блоков для органического синтеза. Осаждающий газ и строительный блок для органического синтеза описаны позднее.
[0184]
2-3: Способ производства фторированного алкинового соединения из галогенированного алканового соединения через галогенированное алкеновое соединение
Способ производства фторированного алкинового соединения по настоящему изобретению представляет собой способ производства фторированного алкинового соединения, представленного формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 являются одинаковыми или разными и каждый представляет собой атом фтора или перфторалкильную группу,
и этот способ включает:
(IB) введение галогенированного алканового соединения, представленного формулой (1B):
CHX8A1CHX9A2 (1B),
где A1 и A2 имеют значения, определенные выше, и X8 и X9 являются одинаковыми или разными и каждый представляет собой атом галогена, в реакцию дегидрогалогенирования в присутствии катализатора в газовой фазе с получением галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1, A2 и X8 имеют значения, определенные выше;
(IIB) после стадии (IB) удаление галогенида водорода; и
(IIIB) после стадии (IIB) введение полученного галогенированного алкенового соединения, представленного формулой (2B):
CX8A1=CHA2 (2B),
где A1, A2 и X8 имеют значения, определенные выше, в реакцию дегидрогалогенирования в присутствии катализатора в газовой фазе с получением фторированного алкинового соединения, представленного формулой (3B):
CA1≡CA2 (3B),
где A1 и A2 имеют значения, определенные выше.
[0185]
(2-3-1) Стадия (IB)
В способе производства фторированного бутинового соединения по настоящему изобретению объяснение раздела «2-1: Способ производства галогенированного алкенового соединения из галогенированного алканового соединения» может быть применено к стадии (IB), как оно есть.
[0186]
(2-3-2) Стадия (IIB)
Способ производства фторированного алкинового соединения по настоящему изобретению включает введение галогенированного алканового соединения, представленного формулой (1B), в реакцию дегидрогалогенирования с получением галогенированного алкенового соединения, представленного формулой (2B) (стадия (IB)), и затем удаление галогенида водорода из смеси, содержащей галогенированное алкеновое соединение и галогенид водорода (стадия (IIB)).
[0187]
В способе производства фторированного алкинового соединения по настоящему изобретению после стадии (IB) галогенид водорода, образовавшийся в результате реакции дегидрогалогенирования на стадии (IB), отделяют и/или удаляют, после чего следует производство фторированного алкинового соединения на следующей стадии (IIIB), в результате чего фторированное алкиновое соединение, которое является целевым соединением, может быть произведено помощью реакции дегидрогалогенирования с высокой степенью конверсии (выход) и высокой селективностью.
[0188]
Для способа удаления галогенида водорода из смеси, содержащей галогенированное алкеновое соединение и галогенид водорода, полученной на стадии (IB), объяснение раздела «(1-3-2) Стадия (IIA)» раздела «Способ производства галогенированного бутинового соединения из галогенированного бутанового соединения через галогенированное бутеновое соединение» может быть применено, как оно есть, за исключением того, что оно читается, как отделение галогенида водорода вместо отделения фторида водорода.
[0189]
(2-3-3) Стадия (IIIB)
В способе производства фторированного алкинового соединения по настоящему изобретению объяснение раздела «2-2: Способ производства фторированного алкинового соединения из галогенированного алкенового соединения» может быть применено к стадии (IIIB), как оно есть.
[0190]
(2-3-4) Примеры реакции дегидрогалогенирования
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении реакция может быть проведена в периодическом процессе или в поточном процессе, в котором соединение исходного материала (галогенированное алкановое соединение) непрерывно подают в реактор, а целевое соединение (галогенированное алкеновое соединение) непрерывно выводят из реактора на стадии (IB). Затем галогенид водорода удаляют из смеси, содержащей галогенированное алкенового соединения и галогенид водорода (стадия (IIB)). Стадия (IIIB) может быть проведена в периодическом процессе или проточном процессе, в котором соединение исходного материала (галогенированное алкеновое соединение) непрерывно подают в реактор, а целевое соединение (фторированное алкиновое соединение) непрерывно выводят из реактора. На каждой стадии целевое соединение (галогенированное алкеновое соединение или фторированное алкиновое соединение) не остается в реакторе, и реакция дегидрогалогенирования может протекать дальше; таким образом, предпочтительно проводить реакцию в поточном процессе.
[0191]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении реакцию предпочтительно проводят в газовой фазе, особенно с помощью газофазного непрерывного поточного процесса с использованием реактора с неподвижным слоем. При использовании газофазного непрерывного поточного процесса устройство, работа и т.д. могут быть упрощены, что экономически выгодно.
[0192]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении атмосфера при проведении реакции предпочтительно представляет собой атмосферу инертного газа с точки зрения подавления деградации катализатора (активированного угля, металлического катализатора и т.д.). В настоящем изобретении инертный газ представляет собой предпочтительно, по меньшей мере, один газ, выбираемый из группы, включающей азот, гелий, аргон и диоксид углерода. Из этих инертных газов азот более предпочтителен с точки зрения сокращения затрат. Концентрация инертного газа составляет предпочтительно от 0 до 50% мол. газового компонента, введенного в реактор.
[0193]
На стадии проведения реакции дегидрогалогенирования в настоящем изобретении после окончания реакции, как описано выше, необязательно может быть проведена очистка в соответствии с традиционными методами с получением в результате целевого соединения (галогенированного алкенового соединения или фторированного алкинового соединения).
[0194]
3. Композиция
Галогенированное бутеновое соединение, галогенированное бутиновое соединение, галогенированное алкеновое соединение или фторированное алкиновое соединение могут быть получены, как описано выше; однако эти соединения могут быть получены в форме композиций, содержащих соответствующие целевые соединения.
[0195]
3-1: Композиции, содержащие галогенированное бутеновое соединение или галогенированное алкеновое соединение
В соответствии со способом производства по настоящему изобретению, например, когда используют способ, описанный выше в разделе «1-1: Способ производства галогенированного бутенового соединения из галогенированного бутанового соединения», например, галогенированное бутеновое соединение, представленное формулой (2A), может быть получено в виде композиции, содержащей как E-, так и Z-изомеры. Кроме того, эта композиция может содержать галогенированное бутиновое соединение, представленное формулой (3A):
CX1X2X3C≡CCX5X6X7 (3A),
где X1, X2, X3, X5, X6 и X7 имеют значения, определенные выше, и
галогенированное бутадиеновое соединение, представленное формулой (4):
CX1X2=CX4CF=CX5X6 (4),
где X1, X2, X4, X5 и X6 имеют значения, определенные выше.
[0196]
В формулах (2A), (3A) и (4) примеры атома галогена, обозначенного как X1, X2, X3, X4, X5, X6 и X7, включают атом фтора, атом хлора, атом брома и атом йода; предпочтительно атом фтора и атом хлора; и более предпочтительно атом фтора.
[0197]
Когда общее количество композиции по настоящему изобретению принимают за 100% мол., содержание галогенированного бутенового соединения, представленного формулой (2A), составляет предпочтительно от 80,00 до 99,99% мол., более предпочтительно от 90,00 до 99,98% мол. и даже более предпочтительно от 92,00 до 99,97% мол. Кроме того, содержание галогенированного бутинового соединения, представленного формулой (3A), составляет предпочтительно от 0,00 до 3,00% мол. и более предпочтительно от 0,01 до 2,00% мол., но может составлять от 1,00 до 10,00% мол. (особенно от 2,00 до 8,00% мол.) в зависимости от условий синтеза. Более того, содержание галогенированного бутадиенового соединения, представленного формулой (4), составляет предпочтительно от 0,00 до 0,50% мол. и более предпочтительно от 0,01 до 0,30% мол. Когда галогенированное бутеновое соединение, представленное формулой (2A), содержит как E-, так и Z-изомеры, указанное выше содержание относится к их общему количеству.
[0198]
В соответствии со способом производства по настоящему изобретению в качестве галогенированного бутенового соединения, представленного формулой (2A), E-изомер может быть синтезирован селективно. Таким образом, содержание (E)-галогенированного бутенового соединения составляет предпочтительно от 85,00 до 99,98% мол. (особенно от 86,00 до 99,00% мол.), и содержание (Z)-галогенированного бутенового соединения составляет предпочтительно от 0,01 до 15,00% мол. (особенно от 1,00 до 14,00% мол).
[0199]
В соответствии со способом производства по настоящему изобретению, даже будучи полученным в виде композиции галогенированного бутена, галогенированное бутеновое соединение, представленное формулой (2A), может быть получено с высокой степенью конверсии, с высоким выходом и высокой селективностью, как описано выше. Таким образом, можно уменьшить компоненты, отличные от галогенированного бутенового соединения, представленного формулой (2A), в композиции галогенированного бутена, что может сократить работу по очистке для получения галогенированного бутенового соединения, представленного формулой (2A).
[0200]
Напротив, при применении способа, описанного в разделе «2-1: Способ производства галогенированного алкенового соединения из галогенированного алканового соединения», например, может быть образована композиция, содержащая галогенированное алкеновое соединение, представленное формулой (2B), и, по меньшей мере, одно дополнительное соединение, содержащее, по меньшей мере одно, гидрофторуглеродное (HFC) соединение, помимо галогенированного алкенового соединения, представленного формулой (2B).
[0201]
Дополнительное соединение предпочтительно представляет собой, по меньшей мере, одно соединение, выбираемое из группы, состоящей из гексафторбутена, гексафторбутана и октафторбутана.
[0202]
Говоря точнее, в способе производства галогенированного алкенового соединения из галогенированного алканового соединения настоящего изобретения, когда 2-хлор-1,1,1,4,4,4-гексафтор-2-бутен (1326mxz) получают в качестве целевого продукта, может быть получен (Z)-1,1,1,4,4,4-гексафторбут-2-ен (HFO-1336mzz(Z)).
[0203]
В композиции, содержащей галогенированное алкеновое соединение, представленное формулой (2B), по настоящему изобретению, когда общее количество композиции принимают за 100% мол., содержание галогенированного алкенового соединения, представленного формулой (2B), составляет предпочтительно 80% мол. или больше, и содержание дополнительного соединения составляет предпочтительно 20% мол. или меньше. В композиции, содержащей, галогенированное алкеновое соединение, представленное формулой (2B), по настоящему изобретению, когда общее количество композиции принимают за 100% мол., содержание галогенированного алкенового соединения, представленного формулой (2B), составляет предпочтительно 85% мол. или больше, более предпочтительно 90% мол. или больше и даже более предпочтительно 95% мол. или больше. В композиции, содержащей, галогенированное алкеновое соединение, представленное формулой (2B), по настоящему изобретению, когда общее количество композиции принимают за 100% мол., содержание галогенированного алкенового соединения, представленного формулой (2B), составляет предпочтительно от 80 до 99,9% мол., более предпочтительно от 85 до 99,9% мол., даже более предпочтительно от 90 до 99,9% мол. и особенно предпочтительно от 95 до 99,9% мол.
[0204]
3-2: Композиция, содержащая галогенированное бутиновое соединение или фторированное алкиновое соединение
В соответствии со способом производства по настоящему изобретению, например, когда применяют способ, описанный в разделе «2-2: Способ производства фторированного алкинового соединения из галогенированного алкенового соединения», например, может быть получена композиция, содержащая фторированное алкиновое соединение, представленное формулой (3B), и, по меньшей мере, одно дополнительное соединение, содержащее, по меньшей мере, одно гидрофторуглеродное (HFC) соединение, помимо фторированного алкинового соединения, представленного формулой (3B). Когда используют способ, описанный в разделе «1-2: Способ производства галогенированного бутинового соединения из галогенированного бутенового соединения», может быть получена композиция, содержащая галогенированное бутиновое соединение, представленное формулой (3A), и, по меньшей мере, одно дополнительное соединение, содержащее гидрофторуглеродное (HFC) соединение, помимо галогенированного бутинового соединения, представленного формулой (3A).
[0205]
Дополнительное соединение предпочтительно представляет собой, по меньшей мере, одно соединение, выбираемое из группы, состоящей из трифторметана, дифторметана, тетрафторметана и монофторметана.
[0206]
В способе производства галогенированного бутинового соединения из галогенированного бутенового соединения и способе производства фторированного алкинового соединения из галогенированного алкенового соединения по настоящему изобретению, когда 1,1,1,4,4,4-гексафтор-2-бутин (PF2B) получают в качестве целевого продукта, может быть получен трифторметан (HFC-23, R23).
[0207]
В композиции, содержащей галогенированное бутиновое соединение или фторированное алкиновое соединение, в настоящем изобретении, когда общее количество композиции принимают за 100% мол., содержание галогенированного бутинового соединения или фторированного алкинового соединения составляет предпочтительно 80% мол. или больше, и содержание дополнительного соединения составляет предпочтительно 20% мол. или меньше. В композиции, содержащей галогенированное бутиновое соединение или фторированное алкиновое соединение, когда общее количество композиции принимают за 100% мол., содержание галогенированного бутинового соединения или фторированного алкинового соединения составляет предпочтительно 85% мол. или больше, более предпочтительно 90% мол. или больше и даже более предпочтительно 95% мол. или больше. В композиции, содержащей галогенированное бутиновое соединение или фторированное алкиновое соединение, по настоящему изобретению, когда общее количество композиции принимают за 100% мол., содержание галогенированного бутинового соединения или фторированного алкинового соединения составляет предпочтительно от 80 до 99,9% мол., более предпочтительно от 85 до 99,9% мол., даже более предпочтительно от 90 до 99,9% мол. и особенно предпочтительно от 95 до 99,9% мол.
[0208]
3-3: Применение композиции, содержащей галогенированное бутеновое соединение, галогенированное бутиновое соединение, галогенированное алкеновое соединение или фторированное алкиновое соединение
В соответствии со способами производства по настоящему изобретению даже при получении в виде композиции, содержащей галогенированное бутеновое соединение, галогенированное бутиновое соединение, галогенированное алкеновое соединение или фторированное алкиновое соединение, галогенированное бутеновое соединение, галогенированное бутиновое соединение, галогенированное алкеновое соединение или фторированное алкиновое соединение могут быть получены особенно с высокой селективностью. Как результат, содержание компонентов, отличных от галогенированного бутенового соединения, галогенированного бутинового соединения, галогенированного алкенового соединения и фторированного алкинового соединения, в композиции может быть уменьшено. В соответствии со способами производства по настоящему изобретению можно сократить работы по очистке для получения галогенированного бутенового соединения, галогенированного бутинового соединения, галогенированного алкенового соединения или фторированного алкинового соединения.
[0209]
Композиция, содержащая галогенированное бутеновое соединение, галогенированное бутиновое соединение, галогенированное алкеновое соединение или фторированное алкиновое соединение, по настоящему изобретению может быть эффективно использована для разных областей применения, таких как травильные газы для формирования новейших микроструктур в полупроводниках, жидкие кристаллы и т.д., а также в качестве очищающих газов, осаждающих газов, хладагентов, теплопередающих сред и строительных блоков для органического синтеза, как и в случае галогенированного бутенового соединения, галогенированного бутинового соединения, галогенированного алкенового соединения или фторированного алкинового соединения отдельно.
[0210]
Осаждающий газ представляет собой газ, которые осаждает устойчивый к травлению полимерный слой.
[0211]
Строительный блок для органического синтеза относится к веществу, которое может быть предшественником соединения, имеющего высоко реакционноспособный скелет. Например, когда композицию по настоящему изобретению вводят в реакцию с фторсодержащим кремнийорганическим соединением, таким как CF3Si(CH3)3, можно вводить фторалкильную группу, такую как CF3 группа, превращая его в вещество, которое может быть очистителем или фторсодержащим фармацевтическим промежуточным продуктом.
[0212]
Хотя выше описаны варианты осуществления изобретения, могут быть выполнены разнообразные изменения в форме и деталях без отступления от сути и объема формулы изобретения.
Примеры
[0213]
Характерные признаки настоящего изобретения пояснены ниже при рассмотрении примеров. Настоящее изобретение этими примерами не ограничено.
[0214]
В способах производства галогенированного бутенового соединения примеров 1-7 соединение исходного материала представляет собой галогенированное бутановое соединение, представленное формулой (1A), где X1, X2, X3, X4, X5, X6 и X7 представляет собой атомы фтора, и галогенированное бутеновое соединение получают по реакции дегидрофторирования в соответствии со следующим уравнением реакции:
CF3CFHCFHCF3 → CF3CF=CHCF3+HF.
[0215]
В способах производства галогенированного алкенового соединения и фторированного бутинового соединения примера 8 соединение исходного материала представляет собой галогенированное алкановое соединение, представленное формулой (1B), где X8 и X9 представляют собой атомы хлора, и A1 и A2 представляют собой трифторметильные группы, и галогенированное алкеновое соединение и галогенированное бутиновое соединение получают по реакции дегидрохлорирования в соответствии со следующими уравнениями реакции:
CF3CHClCHClCF3 (336mdd) → CF3CCl=CHCF3 ((Z) или (E)-1326mxz) + HCl
CF3CCl=CHCF3 ((Z) или (E)-1326mxz) → CF3C≡CCF3 (PF2B) + HCl.
[0216]
В способах производства галогенированного алкенового соединения и фторированного бутинового соединения примеров 9-20 соединение исходного материала представляет собой галогенированное алкановое соединение, представленное формулой (1B), где X8 и X9 представляют собой атомы фтора, и A1 и A2 представляют собой трифторметильные группы, и галогенированное алкеновое соединение и фторированное бутиновое соединение получают по реакции дегидрофторирования в соответствии со следующими уравнениями реакции:
CF3CHFCHFCF3 (338mee) → CF3CF=CHCF3 ((Z) или (E)-1327myz) + HF
CF3CF=CHCF3 ((Z) или (E)-1327myz) → CF3C≡CCF3 (PF2B) + HF.
[0217]
Примеры 1-3: Жидкофазная реакция
В качестве реакционной системы используют автоклав (200 куб.см).
[0218]
Вследствие использования автоклава в качестве реакционной системы эта реакционная система относится к (1) замкнутому реакционному процессу в присутствии основания или (2) реакционному процессу при повышенном давлении, проводимому в присутствии основания при температуре реакции 10°C или выше и при давлении реакции 0 кПа или больше. Повышение давления таким путем включает герметизацию.
[0219]
В автоклав в качестве реакционного раствора добавляют 7,0 г 50%-ного (масс) водного раствора KOH или 50%-ного (масс.) раствора тетра-бутоксида калия (t-BuOK) в дибутиловом эфире (Bu2O). При необходимости 0,28 г хлорида метилтриоктиламмония (товарный знак: Aliquat 336) добавляют в качестве катализатора. Кроме того, добавляют 8,0 г соединения исходного материала (CF3CFHCFHCF3). После того, как крышку закрывают для создания замкнутой системы, подают азот и повышают давление. Давление в это время равно 20 кПа. Затем для стимулирования реакции проводят перемешивание при комнатной температуре (25°C). После начала реакции дегидрофторирования по мере необходимости отбирают пробы. Реакцию останавливают, когда в реакционной системе отсутствуют изменения. Давление в конце реакции равно 80 кПа.
[0220]
После остановки перемешивания продукт реакции охлаждают до 0°C. Затем проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС (GC/MS)), используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»). Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают CF3CF=CHCF3. Результаты представлены в таблице 1.
[0221]
Примеры 4-6: Газофазная реакция (Активированный уголь)
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) в качестве реакционной трубки заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (производства компании Osaka Gas Chemicals Co., Ltd.; удельная площадь поверхности 1200 м2/г). После сушки при 200°C в течение 2 час в атмосфере азота соединению CF3CFHCFHCF3 (соединение исходного материала) позволяют протекать через реакционную трубку при нормальном давлении, так что время контакта (W/F) CF3CFHCFHCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет 15 г.сек/куб.см, 30 г.сек/куб.см или 47 г.сек/куб.см.
[0222]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0223]
Реакционную трубку нагревают при 450°C, чтобы начать реакцию дегидрофторирования.
[0224]
Через час после начала реакции дегидрофторирования собирают дистиллят, который прошел через колонну очистки.
[0225]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС), используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»). Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают CF3CF=CHCF3. Результаты представлены в таблице 1.
[0226]
Пример 7: Газофазная реакция (Хромоксидный катализатор)
Реакции дают возможность протекать таким же образом, как в примерах 4-6, за исключением того, что катализатор на основе оксида хрома (Cr2O3) используют в качестве катализатора, температура реакции равна 350°C, а время контакта (W/F) CF3CFHCFHCF3 (соединение исходного материала) и хромоксидного катализатора равно 47 г.сек/куб.см. Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают CF3CF=CHCF3. Результаты представлены в таблице 1.
[0227]
Таблица 1
|
[0228]
Пример 8 (Дегидрохлорирование)
336mdd (CF3CHClCHClCF3) → 1326mxz (CF3CCl=CHCF3) → PF2B (CF3C≡CCF3)
(1) 336mdd (CF3CHClCHClCF3) → 1326mxz (CF3CCl=CHCF3)
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) используют в качестве реакционной трубки и заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (удельная площадь поверхности 1200 м2/г). После сушки при 200°C в течение 2 час в атмосфере азота соединению CF3CHClCHClCF3 (соединение исходного материала) дают возможность протекать через реактор при нормальном давлении, так что время контакта (W/F0) CF3CHClCHClCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет 5 г.сек/куб.см или 25 г.сек/куб.см.
[0229]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0230]
Реактор нагревают при 300°C или 400°C, чтобы начать дегидрохлорирование.
[0231]
(2) Удаление хлорида водорода
Через один час после начала дегидрохлорирования собирают дистиллят, который прошел через колонну очистки.
[0232]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС), используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»).
[0233]
Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получено галогенированное алкеновое соединение (1326mxz: CF3CCl=CHCF3).
[0234]
Кроме того, в способе производства галогенированного алкенового соединения из галогенированного алканового соединения в качестве целевого продукта получают (Z)-1,1,1,4,4,4-гексафторбут-2-ен (HFO-1336mzz(Z)) помимо 1326mxz (CF3CCl=CHCF3).
[0235]
Таблица 2
336mdd (CF3CHClCHClCF3) → 1326mxz (CF3CCl=CHCF3)
|
336mdd: CF3CHClCHClCF3
1326mxz: CF3CCl=CHCF3
R23: CHF3
PF2B: CF3C≡CCF3
1327myz: CF3CF=CHCF3
Z1336mzz: CF3CH=CHCF3
1316mxx: CF3CCl=CClCF3
[0236]
(3) 1326mxz (CF3CCl=CHCF3) → PF2B (CF3C≡CCF3)
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) используют в качестве реакционной трубки и заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (удельная площадь поверхности 1200 м2/г).
[0237]
В этой операции реакцию проводят путем возвращения реакционного газа, содержащего галогенированное алкеновое соединение, полученного описанным выше образом, в реактор (первый реактор), или позволяя ему протекать в следующий реактор (второй реактор), заполненный катализатором на основе активированного угля.
[0238]
В это время концентрация хлорида водорода в реакционном газе, содержащем галогенированное алкеновое соединение, равна 50% мол. Реакционный газ из первого реактора подвергают ректификации, обработке щелочью, обработке Secard, обработке оксидом алюминия или т.п., чтобы довести концентрацию хлорида водорода до 20% мол., 3% мол. или 0,1% мол.
[0239]
После сушки при 200°C в течение 2 час в атмосфере азота, соединению CF3CCl=CHCF3 (соединение исходного материала) дают возможность протекать через реактор при нормальном давлении, так что время контакта (W/F0) CF3CCl=CHCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет 0,5 г.сек/куб.см, 20 г.сек/куб.см или 43 г.сек/куб.см.
[0240]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0241]
Реактор нагревают при 400°C, чтобы начать дегидрохлорирование.
[0242]
Через один час после начала дегидрохлорирования собирают дистиллят, который прошел через колонну очистки.
[0243]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС), используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»).
[0244]
Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают фторированное алкиновое соединение (PF2B (CF3C≡CCF3)).
[0245]
Кроме того, в способе производства фторированного алкинового соединения из галогенированного алкенового соединения в качестве целевого продукта получают трифторметан (HFC-23, R23) помимо PF2B.
[0246]
Таблица 3:
1326mxz (CF3CCl=CHCF3) → PF2B (CF3C≡CCF3)
|
1326mxz: CF3CCl=CHCF3
PF2B: CF3C≡CCF3
R23: CHF3
1327myz: CF3CF=CHCF3
[0247]
Пример 9 (Дегидрофторирование)
338mee (CF3CHFCHFCF3) → 1327myz (CF3CF=CHCF3) → PF2B (CF3C≡CCF3)
(1) 338mee (CF3CHFCHFCF3) → 1327myz (CF3CF=CHCF3).
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) используют в качестве реакционной трубки и заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (удельная площадь поверхности 1200 м2/г).
[0248]
После сушки при 200°C в течение 2 час в атмосфере азота соединению CF3CHFCHFCF3 (соединение исходного материала) дают возможность протекать через реактор при нормальном давлении, так что время контакта (W/F0) CF3CHFCHFCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет 5 г.сек/куб.см или 25 г.сек/куб.см.
[0249]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0250]
Реактор нагревают при 100°C, 200°C, 300°C или 400°C, чтобы начать дегидрофторирование.
[0251]
(2) Удаление фторида водорода
Через один час после начала дегидрофторирования собирают дистиллят, который прошел через колонну очистки.
[0252]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС) используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»).
[0253]
Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают галогенированное алкеновое соединение (1327myz: CF3CF=CHCF3).
[0254]
(3) 1327myz (CF3CF=CHCF3) → PF2B (CF3C≡CCF3)
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) используют в качестве реакционной трубки и заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (удельная площадь поверхности 1200 м2/г).
[0255]
В этой операции реакцию проводят путем возвращения реакционного газа, содержащего галогенированное алкеновое соединение, полученное описанным выше образом, в реактор (первый реактор), или позволяя ему протекать в следующий реактор (второй реактор), заполненный катализатором на основе активированного угля.
[0256]
В это время концентрация хлорида водорода в реакционном газе, содержащем галогенированное алкеновое соединение, равна 50% мол. Реакционный газ из первого реактора подвергают ректификации, обработке щелочью, обработке Secard, обработке оксидом алюминия или т.п., чтобы довести концентрацию хлорида водорода до 20% мол., 3% мол. или 0,1% мол.
[0257]
После сушки при 200°C в течение 2 час в атмосфере азота соединению CF3CF=CHCF3 (соединение исходного материала) дают возможность протекать через реактор при нормальном давлении, так что время контакта (W/F0) CF3CCl=CHCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет 0,5 г.сек/куб.см, 20 г.сек/куб.см или 43 г.сек/куб.см.
[0258]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0259]
Реактор нагревают при 400°C, чтобы начать дегидрофторирование.
[0260]
Через один час после начала дегидрофторирования собирают дистиллят, который прошел через колонну очистки.
[0261]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС) используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»).
[0262]
Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают фторированное алкиновое соединение (PF2B (CF3C≡CCF3)).
[0263]
Кроме того, в способе производства фторированного алкинового соединения из галогенированного алкенового соединения в качестве целевого продукта получают трифторметан (HFC-23, R23) помимо PF2.
[0264]
Таблица 4
1327myz (CF3CF=CHCF3) → PF2B (CF3C≡CCF3)
|
1327myz: CF3CF=CHCF3
PF2B: CF3C≡CCF3
R23: CHF3
[0265]
Примеры 10-16 (Дегидрофторирование)
338mee (CF3CHFCHFCF3) → 1327myz (CF3CF=CHCF3)
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) используют в качестве реакционной трубки и заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (удельная площадь поверхности 1200 м2/г). После сушки при 200°C в течение 2 час в атмосфере азота соединению CF3CHFCHFCF3 (соединение исходного материала) дают возможность протекать через реактор при нормальном давлении, так что время контакта (W/F0) CF3CHFCHFCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет от 2 до 47 г.сек/куб.см. После этого в примерах 10-13 через реактор позволяют протекать 4 молям октафторциклобутана (ц-C4F8; C318) из расчета на моль CF3CHFCHFCF3 (соединение исходного материала).
[0266]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0267]
Реактор нагревают при 400°C, чтобы начать дегидрохлорирование.
[0268]
Через один час после начала дегидрохлорирования собирают дистиллят, который прошел через колонну очистки.
[0269]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС) используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»).
[0270]
Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают галогенированное алкеновое соединение (1327myz: CF3CF=CHCF3).
[0271]
Кроме того, в способе производства галогенированного алкенового соединения из галогенированного алканового соединения в качестве целевых продуктов получают 1,1,1,4,4,4-гексафторбут-2-ен (HFO-1336mzz), 1,1,1,4,4,4-гексафтор-2-бутин (PF2B) и т.д. помимо 1327myz (CF3CF=CHCF3).
[0272]
Таблица 5
338mee (CF3CHFCHFCF3) → 1327myz (CF3CF=CHCF3)
|
336mee: CF3CHFCHFCF3
1327myz: CF3CF=CHCF3
PF2B: CF3C≡CCF3
1336mzz: CF3CH=CHCF3
[0273]
Примеры 17-20 (Дегидрофторирование)
1327myz (CF3CF=CHCF3) → PF2B (CF3C≡CCF3)
Трубку из нержавеющей стали (наружный диаметр 1/2 дм) используют в качестве реакционной трубки и заполняют, в качестве катализатора, 10 г катализатора на основе активированного угля (удельная площадь поверхности 1200 м2/г). После сушки при 200°C в течение 2 час в атмосфере азота соединению CF3CF=CHCF3 (соединение исходного материала) дают возможность протекать через реактор при нормальном давлении, так что время контакта (W/F0) CF3CF=CHCF3 (соединение исходного материала) и катализатора на основе активированного угля составляет 2 г.сек/куб.см, 2,8 г.сек/куб.см или 10 г.сек/куб.см. После этого в примерах 17-18 через реактор позволяют протекать 4 молям октафторциклобутана (ц-C4F8; C318) из расчета на моль CF3CF=CHCF3 (соединение исходного материала).
[0274]
Реакция протекает с помощью газофазного непрерывного поточного процесса.
[0275]
Реактор нагревают при 400°C, чтобы начать дегидрохлорирование.
[0276]
Через один час после начала дегидрохлорирования собирают дистиллят, который прошел через колонну очистки.
[0277]
После этого проводят масс-спектрометрию с помощью комбинации газовая хроматография/масс-спектрометрия (ГХ/МС) используя газовый хроматограф (производства компании Shimadzu Corporation, торговое наименование «GC-2014»). Структурный анализ с помощью спектров ЯМР выполняют, используя прибор ЯМР (производства компании JEOL Ltd., торговое наименование «400YH»).
[0278]
Результаты масс-спектрометрии и структурного анализа подтверждают, что в качестве целевого соединения получают фторированное алкиновое соединение (PF2B: CF3C≡CCF3).
[0279]
Кроме того, в способе производства галогенированного алкенового соединения из галогенированного алканового соединения в качестве целевого продукта получают трифторметан (HFC-23, R23) помимо PF2B (CF3C≡CCF3).
[0280]
Таблица 6
1327myz (CF3CF=CHCF3) → PF2B (CF3C≡CCF3)
|
1327myz: CF3CF=CHCF3
PF2B: CF3C≡CCF3
R23: CHF3