Результат интеллектуальной деятельности: ДЕТСКАЯ СМЕСЬ C МОЛОЧНЫМ ЖИРОМ ДЛЯ СТИМУЛИРОВАНИЯ ЗДОРОВОГО РОСТА
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Изобретение относится к питанию для детей, в частности к детским смесям, предназначенным для применения в качестве единственного источника питания.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Женское грудное молоко, бесспорно, является золотым стандартом детского питания. Однако в некоторых случаях грудное вскармливание является неполноценным или неблагоприятным по медицинским причинам или вследствие отказа кормить грудью. Для таких ситуаций были разработаны молочные смеси первого уровня (для детей первого полугодия жизни) или второго уровня (для детей второго полугодия жизни). В настоящее время коммерческие детские смеси обычно используются для обеспечения дополнительного или единственного источника питания детей в раннем возрасте. Эти смеси содержат ряд питательных веществ для удовлетворения пищевых потребностей растущего ребенка и обычно включают в себя жиры, углеводы, белки, витамины, минеральные и другие питательные вещества, полезные для оптимального роста и развития ребенка. Коммерческие детские смеси предназначены для максимальной, насколько это возможно, имитации состава и функций женского грудного молока.
Давно было признано, что характер или кривая увеличения массы тела детей на естественном вскармливании отличается от характера или кривой увеличения массы тела детей на искусственном вскармливании. После первой недели жизни, во время которой дети, вскармливаемые грудью, сначала, как правило, теряют большую массу тела, чем дети на искусственном вскармливании, и им требуется немного более длительный период времени для достижения массы тела, которая была при рождении, в течение первых 4 месяцев жизни характер увеличения массы тела детей на искусственном вскармливании аналогичен характеру увеличения массы тела детей вскармливающихся грудью. В 3-месячном возрасте масса тела детей, вскармливающихся грудью, как правило, несколько больше (Andres et al., 2013, J. Pediatrics 163: 49-54). После достижения детьми примерно 4-месячного возраста скорость увеличения массы тела детей, вскармливающихся грудью, и детей на искусственном вскармливании заметно различается. Разница средней массы тела в 12 месяцев достигает примерно 500-650 г (Dewey et al., 1993 Am. J. Clin. Nutr. 57: 140-145). В ряде исследований, проведенных в различных регионах по всему миру, сообщалось, что в развитых странах Запада, а также в незападных развивающихся странах у детей, вскармливающихся грудью, в возрасте от 4 до 12 месяцев масса тела возрастает медленнее. Увеличение роста детей, вскармливающихся грудью, и детей на искусственном вскармливании, как правило, отличается меньше, и в результате дети, вскармливающиеся грудью, в возрасте 12 месяцев более худощавы (Dewey et al., 1993). Таким образом, в данной области техники было показано, что кривая роста грудных детей, вскармливающихся коммерческими смесями, отличается от кривой роста детей, вскармливающихся грудью. Обычно детская смесь ускоряет рост в первый год жизни, в особенности с 4-месячного возраста и далее, что приводит к более высокой массе тела в возрасте 12 месяцев (Dewey et al., 1993; Dewey et al., 1992 Pediatrics 89:1035).
В предшествующем уровне в области разработки детских смесей для улучшения кривой роста для большего ее приближения к кривой роста детей, вскармливающихся грудью, основное внимание было направлено на детскую смесь с более низким содержанием белков/или более низкой калорийностью. В WO 2008/071667 раскрывается питательная композиция для детей с риском развития ожирения в более позднем возрасте, содержащая источник белков, источник липидов и источник углеводов. Содержание белков составляет менее 1,8 г/100 ккал, энергетическая ценность составляет менее 650 ккал/л. В WO 2010/070613 раскрывается, что меньшее увеличение массы тела в течение первой недели жизни наблюдалось при использовании детской смеси с очень низкой калорийностью и низким содержанием белка из расчета на объем. В публикации Koletzko et al., 2009, Am. J. Clin. Nutr. 89:1836-1845 раскрывается, что использование изокалорийной детской смеси первого уровня и второго уровня с содержанием белков 1,77 и 2,1 г/100 ккал приводит к меньшему увеличению массы тела, чем в группе детей, вскармливающихся детскими смесями первого уровня и второго уровня с высокой концентрацией белка 2,9 и 4,4 г/100 ккал. В возрасте 24 месяцев у детей в группе, потребляющей смесь с более низким содержанием белка, значение показателя z-score отношения массы тела к росту (z-score масса тела/рост) было ниже значения этого показателя z-score группы, потребляющей смесь с высоким содержанием белка, и не отличалось от значения этого показателя z-score контрольной группы грудного вскармливания. В WO 2015/078505 раскрывается, что меньшее увеличение массы тела наблюдается в период от 3 до 6 месяцев, когда вводится смесь с более низким содержанием белка, чем в смеси контрольной группы. WO 2015/091789 относится к олигосахаридным смесям, содержащим N-ацетилированный олигосахарид, галакто-олигосахарид и/или сиалилированный олигосахарид и стимулирующим скорость роста, которая приближается к скорости роста детей, вскармливающихся грудью.
WO 2013/153071 раскрываются тестированные детские смеси, содержащие сиаловую кислоту, холестерин, сфингомиелин, с более низкой калорийностью и более низким содержанием белка по сравнению с контрольной смесью. Когда для вскармливания использовались эти смеси, не наблюдалось никаких различий в росте в сравнении с грудным вскармливанием в 6 месяцев при рассмотрении скорректированных по возрасту значений z-score. В публикации Timby et al., 2014, Am. J. Clin. Nutr. 99:860-868 представлены данные аналогичного исследования в течение 12 месяцев, которые показывали, что обе группы, которые вскармливались детскими смесями, показали статистически значимую более высокую скорость роста по массе тела и росту по сравнению с контрольной группой грудного вскармливания. В WO 2009/051502 раскрыты детские смеси, обогащенные источником ганглиозидов, для повышения или поддержания здорового роста. Постнатальное увеличение массы тела наблюдалось у крыс, получавших гель, обогащенный ганглиозидами.
Детские молочные смеси включают в себя преимущественно растительные масла в качестве источника липидов, а пальмитиновая кислота в растительных маслах находится, главным образом, в sn-1 и sn-3 положениях молекулы триглицерида. Молочный жир млекопитающих, в том числе женского грудного молока, содержит большое количество пальмитиновой кислоты, и пальмитиновая кислота по большей части находится в sn-2 положении молекулы триглицерида. Под действием панкреатических липаз пальмитиновая кислота высвобождается в форме 2-моноглицерида, а не в форме свободной жирной кислоты, что приводит к более высокой абсорбции кальция и пальмитиновой кислоты. В WO 2011/071371 раскрывается применение в рационе питания детей раннего возраста триглицеридов с повышенной долей остатков пальмитиновой кислоты в sn-2 положении для улучшения развития здорового композиционного состава организма, в особенности для профилактики ожирения, в более позднем возрасте. В WO 2012/173467 раскрывается применение специально разработанного липидного компонента с оптимальным профилем жирных кислот и повышенной долей остатков пальмитиновой кислоты в sn-2 положении, который представлен в виде липидных глобул определенного размера и/или с покрытием, в питании детей раннего возраста для улучшения развития здорового композиционного состава организма, в частности профилактики ожирения, в более позднем возрасте.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
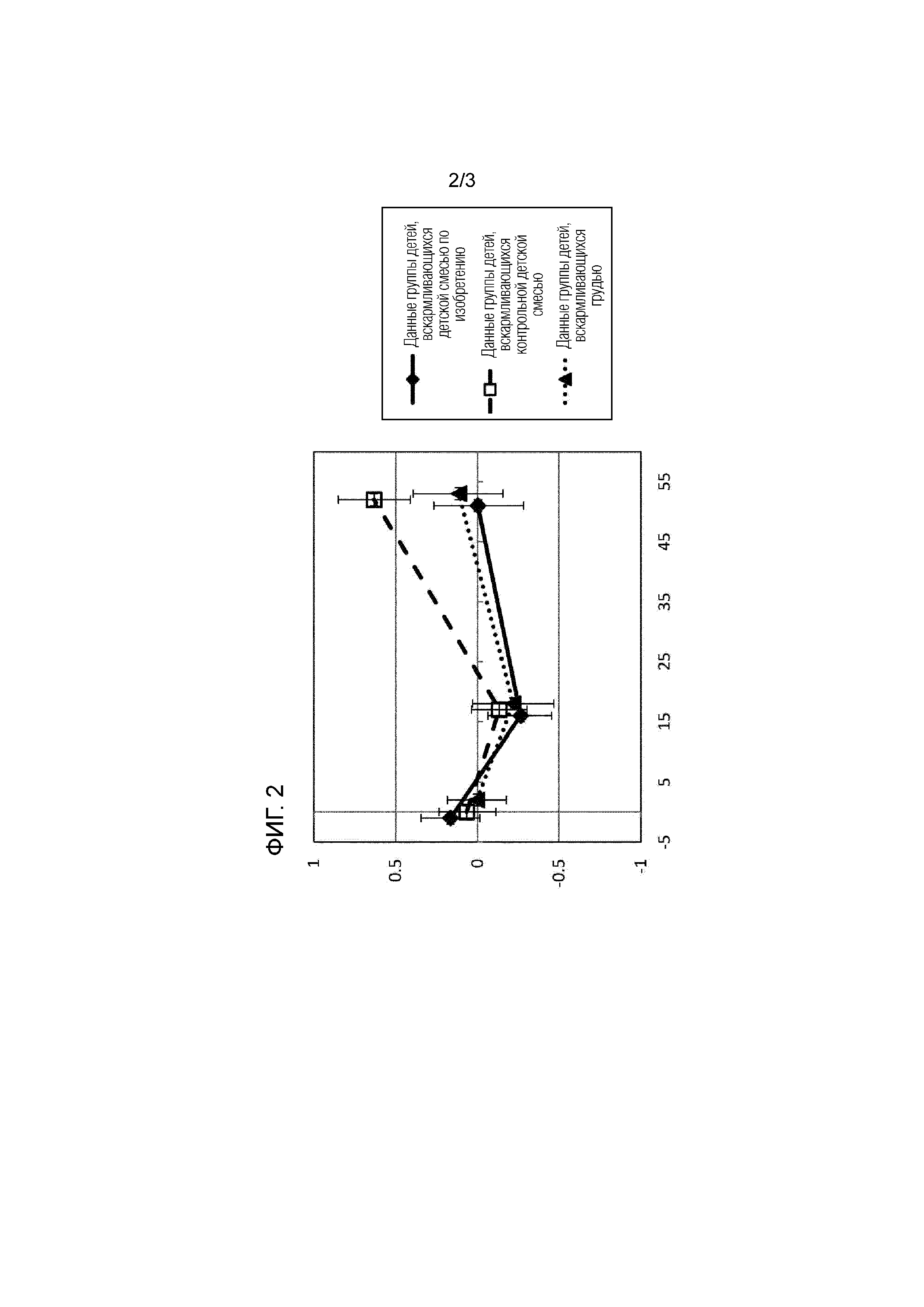
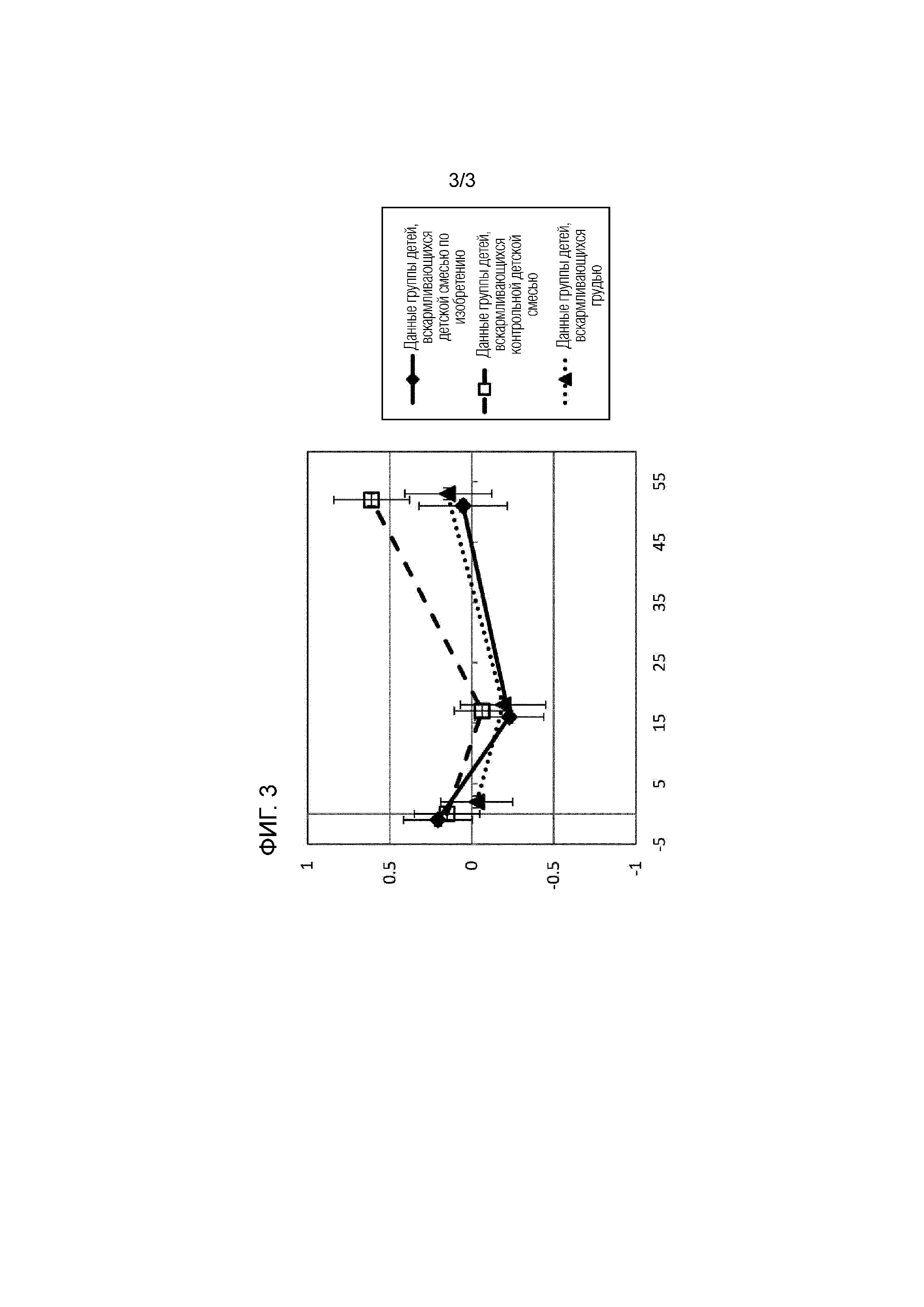
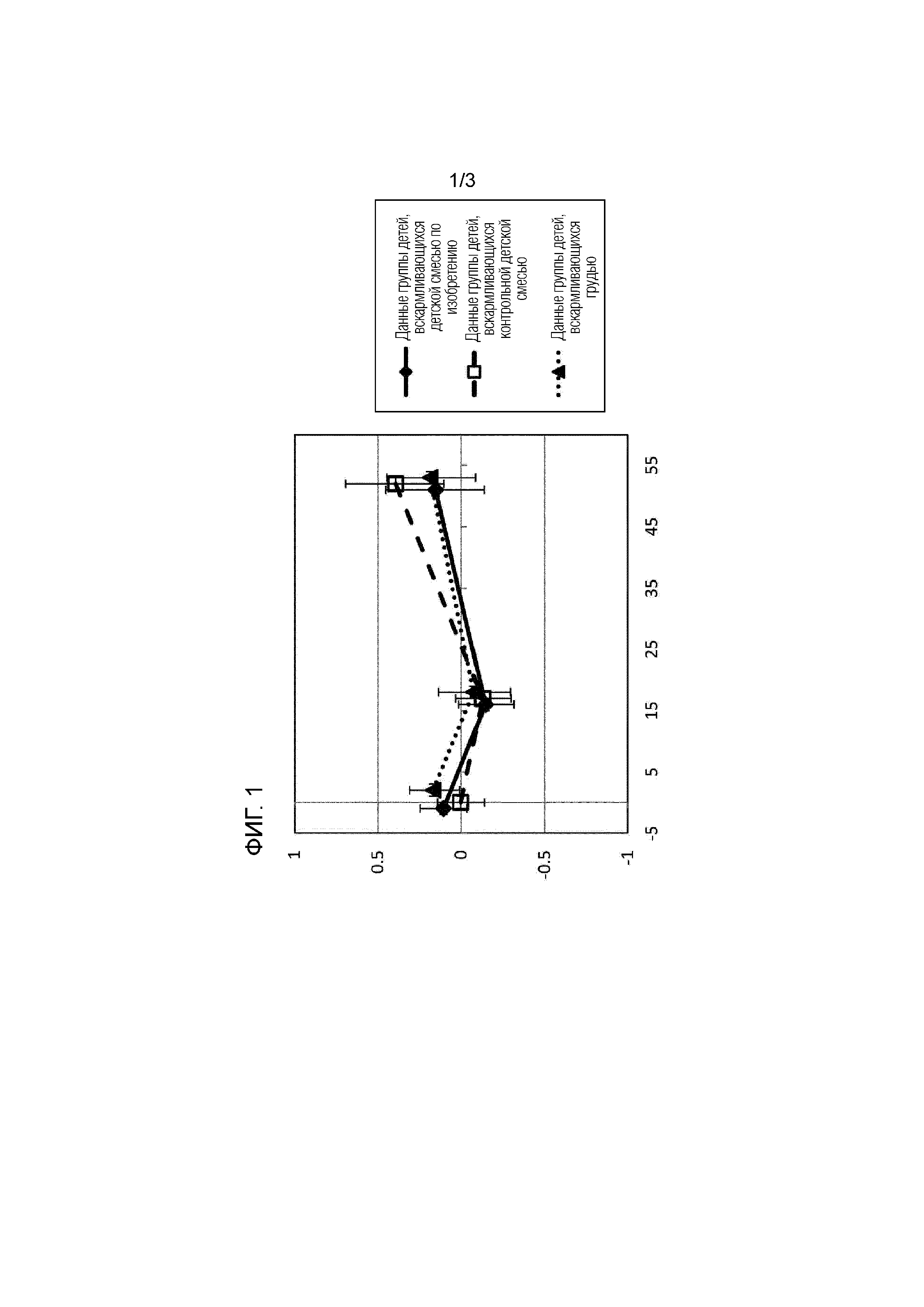
Авторы настоящего изобретения сравнили характер роста или кривые роста здоровых доношенных детей в 3 группах в течение первых 12 месяцев и сравнили их с Нормами роста детей грудного вскармливания, разработанными ВОЗ. Одна группа представляла собой нерандомизированную контрольную группу детей грудного вскармливания, другая группа получала экспериментальную детскую смесь, содержащую липидный компонент в форме смеси растительных жиров и жира коровьего молока, и еще одна группа получала контрольную детскую смесь, содержащую липидный компонент в форме, главным образом, растительного жира. Обе смеси вводили до 17 недель жизни. Контрольная и экспериментальная молочные смеси были аналогичны по калорийности, а также по содержанию жиров, углеводов и белков.
Авторы настоящего изобретения неожиданно обнаружили, что при анализе кривых роста в течение всего периода исследования до 12-месячного возраста популяции «в соответствии с протоколом» (PP) с кривой параметрического роста (PGC) группа детей, получающих экспериментальную смесь, статистически не отличалась от контрольной группы детей, вскармливающихся грудью, при сравнении массы тела или индекса массы тела (- BMI) в возрасте 12 месяцев. С другой стороны, группа, получающая контрольную смесь, показала статистически значимое повышение BMI в возрасте 12 месяцев по сравнению с контрольной группой детей, вскармливающихся грудью. Кроме того, группа, получающая контрольную смесь, показала в возрасте 12 месяцев статистически значимое повышение BMI по сравнению с группой детей, вскармливающихся экспериментальной смесью.
В контрольной группе детей в возрасте 12 месяцев при анализе популяции «назначенного лечения» ( ITT) средние значения показателя z-score отношения массы тела к возрасту (z-score масса тела/возраст), показателя z-score отношения массы тела к росту (z-score масса тела/рост) и z-score отношения BMI к возрасту (z-score BMI/возраст) были значительно выше Норм роста детей грудного вскармливания, разработанных ВОЗ. В контрольной группе при анализе популяции «назначенного лечения» (ITT) среднее значение показателя z-score отношения окружности головы к возрасту (z-score окружность головы/возраст) значительно превосходило Нормы роста детей грудного вскармливания, разработанные ВОЗ. С другой стороны, экспериментальная группа была близка к контрольной группе детей, вскармливающихся грудью, по всем этим значениям z-score, как показывает перекрывающийся доверительный интервал, и для обеих групп (группа детей, вскармливающихся экспериментальной смесью, и контрольная группа детей, вскармливающихся грудью) не было никаких данных, указывающих на их отличие от Норм роста детей грудного вскармливания, разработанных ВОЗ.
Это свидетельствует о том, что вскармливание детской смесью в начале жизни с аналогичным содержанием калорий и макро-ингредиентов может оказывать различное и благоприятное воздействие на модель роста или кривую роста в начале жизни, делая ее больше схожей с моделью или кривой роста детей, вскармливающихся грудью. Это обусловлено различием способа, которым сконфигурирован липидный компонент, то есть способом, при котором он более напоминает липид женского молока, содержащий повышенное количество пальмитиновой кислоты в sn-2 положении молекулы триглицерида.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Таким образом, настоящее изобретение относится к способу стимулирования кривой постнатального роста или постнатального развития организма ребенка до кривой постнатального роста или постнатального развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью, причем указанный способ включает введение питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
и где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В качестве альтернативы, настоящее изобретение относится к способу стимулирования кривой постнатального роста или постнатального развития организма ребенка до кривой постнатального роста или постнатального развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью, причем указанный способ включает введение питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
В одном варианте осуществления настоящего изобретения кривая роста или развитие организма ребенка, которые подобны кривой роста или развитию организма ребенка, наблюдаемым у детей, вскармливающихся грудью, представляет собой кривую роста или развитие организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма ребенка согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ. В контексте настоящего изобретения Нормы роста детей грудного вскармливания, разработанные ВОЗ, представляют собой Нормы роста детей, разработанные ВОЗ, которые опубликованы в Acta Paediatrica, April 2006, volume 95, supplement 450.
В контексте настоящего изобретения термин «подобна (похожа)» или «ближе (приближена)» относится к сравнению с введением стандартной детской смеси первого уровня или стандартной детской смеси второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находятся в sn-2 положении триглицеридов.
В качестве альтернативы «стимулирования кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью», настоящее изобретение относится также к улучшению кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно по сравнению с кривой роста или развитием организма детей, вскармливающихся смесью первого уровня или смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находится в sn-2 положении триглицеридов.
Таким образом, в одном варианте осуществления настоящее изобретение относится к способу улучшения кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно по сравнению с кривой роста или развитием организма детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находится в sn-2 положении триглицеридов, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
и где липид включает 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В альтернативном варианте осуществления настоящее изобретение относится к способу улучшения кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, наблюдаемым у детей, вскармливающихся женским грудным молоком, предпочтительно при сравнении с кривой роста или развитием организма детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находится в sn-2 положении триглицеридов, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, и где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
В качестве альтернативы, настоящее изобретение относится к способу стимулирования кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ, причем указанный способ включает введение питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида,
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
и где липид включает 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В альтернативном варианте осуществления настоящее изобретение относится к способу стимулирования кривой постнатального роста или развития организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ, причем указанный способ включает введение питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
В некоторых юрисдикциях введение питательной композиции ребенку считается нетерапевтическим введением. В этих случаях изобретение может быть сформулировано, как определено выше, как относящееся к способу, включающему введение питательной композиции. Для наглядности, способ также может быть определен как нетерапевтический способ стимулирования кривой постнатального роста или развития организма ребенка, как определено выше. По определению термин «нетерапевтический» исключает любой терапевтический эффект.
В некоторых юрисдикциях введение питательной композиции ребенку считается терапевтическим само по себе. В этих случаях изобретение может быть сформулировано следующим образом.
В одном варианте осуществления настоящее изобретение относится к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в стимулировании кривой постнатального роста или развития организма ребенка до кривой роста или развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
и где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В альтернативном варианте осуществления настоящее изобретение относится к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в стимулировании кривой постнатального роста или постнатального развития организма ребенка до кривой постнатального роста или постнатального развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
В одном варианте осуществления настоящее изобретение относится к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в улучшении кривой постнатального роста или постнатального развития организма до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно в сравнении с кривой роста или развитием организма детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты, находится в sn-2 положении триглицеридов, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
и где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В качестве альтернативы, изобретение относится к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в стимулировании кривой постнатального роста или постнатального развития организма до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно в сравнении с кривой роста или развитием организма детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находится в sn-2 положении триглицеридов, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
В одном варианте осуществления настоящее изобретение относится к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в стимулировании кривой постнатального роста или постнатального развития организма до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, и где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В альтернативном варианте осуществления настоящее изобретение относится к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в стимулировании кривой постнатального роста или развития организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, включающие в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
Изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20,
для применения в стимулировании кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью.
В альтернативном варианте осуществления изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов,
для применения в стимулировании постнатальной кривой роста или постнатального развития организма ребенка до кривой роста или развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью.
Изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20,
для применения в улучшении кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно в сравнении с кривой роста или развитием организма детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находится в sn-2 положении триглицеридов.
Изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов,
для применения в улучшении кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно в сравнении с кривой роста или развитием организма детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты находится в sn-2 положении триглицеридов.
Изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20,
для применения в стимулировании кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
В качестве альтернативы, изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов,
для применения в стимулировании кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
В предпочтительном варианте осуществления способа, применения или композиции для применения согласно настоящему изобретению кривая роста или развитие организма представляет собой кривую роста или развитие организма в первые 12 месяцев жизни ребенка.
В предпочтительном варианте осуществления способа, применения или композиции для применения согласно настоящему изобретению в 12 месяцев масса тела ребенка и/или индекс массы тела (BMI) и/или отношение массы тела к росту приблизительно представляет собой массу тела и/или BMI и/или отношение массы тела к росту детей, вскармливающихся грудью, в 12 месяцев. В предпочтительном варианте осуществления способа, применения или композиции для применения согласно настоящему изобретению в 12 месяцев масса тела ребенка и/или BMI и/или отношение массы тела к ростe приблизительно представляет собой массу тела и/или индекс массы тела и/или отношение массы тела к росту ребенка в 12 месяцев согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ. В контексте настоящего изобретения термин «приблизительно» означает, что статистически не отличается.
В другом варианте осуществления способа, применения или композиции для применения согласно настоящему изобретению окружность головы ребенка в 12 месяцев приблизительно равна окружности головы ребенка, вскармливающегося грудью, в 12 месяцев. В предпочтительном варианте осуществления способа, применения или композиции для применения согласно настоящему изобретению окружность головы ребенка в 12 месяцев приблизительно равна окружности головы ребенка в 12 месяцев, вскармливающегося грудью, согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ. В контексте настоящего изобретения термин «приблизительно» означает, что статистически не отличается.
В другом варианте осуществления способа, применения или композиции для применения согласно настоящему изобретению толщина кожной складки ребенка в 12 месяцев, предпочтительно толщина подлопаточной кожной складки или толщина кожной складки над трехглавой мышцей или обе указанной толщины, приблизительно равна толщине кожной складки ребенка в 12 месяцев, вскармливающегося грудью. В предпочтительном варианте осуществления способа, применения или композиции для применения согласно настоящему изобретения толщина подлопаточной кожной складки или толщина кожной складки над трехглавой мышцей или обе указанные толщины складок у ребенка в 12 месяцев приблизительно равна толщине подлопаточной кожной складки или толщине над трехглавой мышцей ребенка в 12 месяцев согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ. В контексте настоящего изобретения термин «приблизительно» означает, что статистически не отличается.
В одном варианте осуществления настоящее изобретение относится к способу i) стимулирования сбалансированной кривой роста или сбалансированного развития организма ребенка и/или ii) предотвращения или снижения риска несбалансированной кривой роста или несбалансированного развития организма ребенка, причем указанный способ включает введение ребенку питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, где питательная композиция включает от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
В одном варианте осуществления настоящее изобретение относится к способу i) стимулирования сбалансированной кривой роста или сбалансированного развития организма ребенка и/или ii) предотвращения или снижения риска несбалансированной кривой роста или несбалансированного развития организма ребенка, причем указанный способ включает введение ребенку питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, причем указанный способ включает введение ребенку питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, где питательная композиция включает от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
Изобретение также может быть сформулировано как относящееся к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в i) стимулировании сбалансированной кривой роста или сбалансированного развития организма ребенка и/или ii) предотвращения или снижения риска несбалансированной кривой роста или несбалансированного развития организма ребенка, где питательная композиция включает от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
Изобретение также может быть сформулировано как относящееся к применению липидных глобул в производстве питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня, для применения в i) стимулировании сбалансированной кривой роста или сбалансированного развития организма ребенка и/или ii) предотвращении или снижении риска несбалансированной кривой роста или несбалансированного развития организма ребенка, где питательная композиция включает от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов.
Изобретение также может быть сформулировано как относящееся к питательной композиции, выбранной из детской смеси первого уровня и детской смеси второго уровня и включающей от 3 до 7 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где липид включает
i) от 30 до 90% масс. растительного жира из расчета на общее количество липида, и
ii) от 10 до 70% масс. молочного липида млекопитающих, полученного из группы, состоящей из коровьего масла, жира коровьего масла, топленого коровьего масла и безводного молочного жира, из расчета на общее количество липида,
где липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20,
для применения в i) стимулировании сбалансированной кривой роста или сбалансированного роста организма ребенка и/или ii) предотвращении или снижения риска несбалансированной кривой роста или несбалансированного развития организма ребенка.
Изобретение также может быть сформулировано как питательная композиция, выбранная из детской смеси первого уровня и детской смеси второго уровня и включающая от 3 до 7 г липида/100 ккал, 1,25 до 5 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, где
i) липид включает от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20, и
ii) липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов,
для применения в i) стимулировании сбалансированной кривой роста или сбалансированного развития организма ребенка и/или ii) предотвращения или снижения риска несбалансированной кривой роста или несбалансированного развития организма ребенка.
Предпочтительно сбалансированная кривая роста или сбалансированное развитие организма сравнимы с кривой роста или развитием организма или подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью. В одном варианте осуществления настоящего изобретения сбалансированная кривая роста или сбалансированное развитие организма приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
В контексте настоящего изобретения питательная композиция не является женским молоком. Кроме того, в контексте настоящего изобретения питательная композиция не является коровьим молоком, в частности коровьим молоком, которое не гомогенизировано.
Рост
Настоящее изобретение относится к стимулированию кривой постнатального роста или постнатального развития организма ребенка до кривой роста или развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью. Синонимами термина «кривая роста» являются «картина роста» и «рост для возраста». В контексте настоящего изобретения кривая роста включает картину изменения массы тела, т.е. массу тела по возрасту, картину изменения массы тела по росту, то есть отношение масса тела-рост-возраст, и картину индекса массы тела (BMI), т.е. BMI по возрасту. В одном варианте осуществления настоящего изобретения кривая роста ребенка также включает в себя кривую увеличения окружности головы по возрасту. В одном варианте осуществления кривая роста ребенка также включает толщину подлопаточной кожной складки по возрасту или толщину складки трехглавой мышцы по возрасту или обе эти величины.
Всемирная организация здравоохранения (ВОЗ) в 2006 г. выпустила новое статистическое распределение международных норм роста, которые описывают рост детей в возрасте от 0 до 59 месяцев, живущих в условиях, которые, как полагают исследователи ВОЗ, поддерживают оптимальный рост детей в шести странах мира, включая США. Распределение показывает, как дети грудного возраста и маленькие дети растут в этих условиях, но не как они растут в условиях, которые могут не поддерживать оптимальный рост. Стандарты ВОЗ устанавливают рост ребенка, вскармливающегося грудью, как норму роста. Диаграммы ВОЗ отражают кривую роста детей, которые в основном находились на грудном вскармливании по меньшей мере 4 месяца и вскармливались грудью в течение еще 12 месяцев. Нормы ВОЗ обеспечивают лучшее описание физиологического роста в младенчестве. Диаграммы роста ВОЗ представляют собой стандарты в том смысле, что они определяют, как ребенок должен расти при обеспечении оптимальных условий. Нормы ВОЗ основаны на высококачественном исследовании, разработанном специально для создания диаграмм роста. Стандарты ВОЗ были разработаны с использованием данных о продольной длине (росте) и массе тела, определяемых через повторяющиеся интервалы времени. Также представлены значения показателей z-score. z-Показатель или стандартный показатель представляет собой число стандартных отклонений, когда результаты исследований или полученные данные результат лежат выше среднего значения (для положительного z показателя) или ниже среднего значения (для отрицательного z показателя).
ЛИПИД
Растительный жир и липид молока млекопитающих
Питательная композиция для введения в способе или применении согласно настоящему изобретению включает липид. Липиды согласно настоящему изобретению представляют собой один или несколько компонентов, выбранных из группы, состоящей из триглицеридов, полярных липидов (таких как фосфолипиды, холестерин, гликолипиды, сфингомиелин), свободных жирных кислот, моно- и диглицеридов. Предпочтительно композиция включает по меньшей мере 70% масс., более предпочтительно по меньшей мере 80%% масс., более предпочтительно по меньшей мере 85% масс., триглицеридов, еще более предпочтительно по меньшей мере 90% масс. триглицеридов из расчета на общее количество липида.
Питательная композиция включает от 3 до 7 г липида/100 ккал, предпочтительно от 4 до 6 г липидов/100 ккал, более предпочтительно от 4,5 до 5,5 г липидов/100 ккал. Липид включает предпочтительно от 80 до 100% масс. триглицеридов из расчета на общее количество липида, более предпочтительно от 90 до 100% масс. триглицеридов.
В первом способе определения питательной композиции липид, включенный в определение, включает растительные липиды. Наличие растительных липидов предпочтительно обеспечивает оптимальный профиль жирных кислот, высокое содержание полиненасыщенных жирных кислот и большее приближение к жиру женского молока. Использование липидов молока жвачных животных, в частности только коровьего молока или других домашних жвачных млекопитающих, не обеспечивает оптимальный профиль жирных кислот. Предпочтительно, композиция по настоящему изобретению включает по меньшей мере один, предпочтительно по меньшей мере два источника липидов, выбранных из группы, в которую входят масло семян льна (льняное масло), рапсовое масло (такое как масло ярового рапса, рапсовое масло с низким содержанием эруковой кислоты и масло канолы), масло шалфея, перилловое масло, портулаковое масло, масло семян брусники, облепиховое масло, конопляное масло, подсолнечное масло, подсолнечное масло с высоким содержанием олеиновой кислоты, сафлоровое масло, сафлоровое масло с высоким содержанием олеиновой кислоты, оливковое масло, масло семян черной смородины, масло синяка подорожникового, кокосовое масло, пальмовое масло и косточковое пальмовое масло. Предпочтительно композиция по настоящему изобретению включает по меньшей мере один, предпочтительно по меньшей мере два источника липидов, выбранных из группы, в которую входят рапсовое масло с низким содержанием эруковой кислоты, льняное масло, каноловое масло, кокосовое масло, подсолнечное масло и высокоолеиновое подсолнечное масло.
Предпочтительно компонент растительного жира включает по меньшей мере 90% масс. триглицеридов. Предпочтительно композиция включает от 30 до 90% масс. растительных липидов из расчета на общее количество липидов, более предпочтительно от 40 до 85% масс., еще более предпочтительно от 50 до 75% масс., из расчета на общее количество липидов.
Кроме того, в первом способе определения питательной композиции для введения в способе или применении согласно настоящему изобретению липиды, включенные в нее, включают липиды молока млекопитающих, предпочтительно молока жвачных животных, предпочтительно коровьего молока, козьего молока, овечьего молока, молока буйволиц, молока ячих, оленьего молока и верблюжьего молока, наиболее предпочтительно коровьего молока. Предпочтительно, молоко млекопитающих не является женским молоком. Предпочтительно компонент молока млекопитающих включает по меньшей мере 70% масс. триглицеридов, более предпочтительно по меньшей мере 90% масс., еще более предпочтительно по меньшей мере 97% масс. триглицеридов.
Предпочтительно липид молока млекопитающих получен из группы, в которую входят коровье масло, жир коровьего масла, топленое коровье масло и безводный молочный жир, более предпочтительно безводный молочный жир и топленое коровье масло. Такие источники липида молочного жира являются источниками с высоким содержанием триглицеридов. Кроме того, эти источники липидов представлены в форме непрерывной жировой фазы или в форме эмульсии типа «вода-в-масле». Использование этих источников молочного жира в процессе производства питательной композиции по настоящему изобретению позволяет получить липидные глобулы, каждая из которых включает в себя смесь растительного жира и молочного жира. Когда используются источники молочного жира, которые представляют собой эмульсию типа «масло-в-воде», будут получены липидные глобулы, состоящие из молочного жира или из растительного жира, которые считаются менее эффективными.
Термин «молочный жир» в настоящем изобретении относится ко всем липидным компонентам молока, которое произведено млекопитающим, таким как корова, и обнаруживается в коммерческом молоке и продуктах, полученных из молока.
Коровье масло в настоящем изобретении представляет собой эмульсию типа вода-в-масле, которое включает в себя более 80% масс. молочного жира.
Термин «жир коровьего масла» в настоящем изобретении относится ко всем жировым компонентам в молоке, которые отделимы взбиванием, другими словами, присутствуют в коровьем масле.
Термин «безводный молочный жир (AMF)» известен в данной области техники и относится к экстрагированному молочному жиру. Обычно AMF включает более 99% масс. липидов из расчета на общую массу. Он может быть получен экстракцией молочного жира из сливок или коровьего масла. Безводное топленое масло в настоящем изобретении является синонимом AMF.
Термин «топленое коровье масло» известен в данной области техники. Он обычно относится к экстракту молочного липида с содержание липидов более 98% масс. и, как правило, является предшественником в способе получения безводного молочного жира или безводного топленого масла.
Предпочтительно композиция включает от 10 до 70% масс. молочных липидов из расчета на общее количество липидов, более предпочтительно от 15 до 60% масс., еще более предпочтительно от 25 до 50% масс., из расчета на общее количество липидов. Предпочтительно эти молочные липиды выбраны из группы, в которую входят коровье масло, молочный жир, топленое коровье масло и безводный молочный жир. Предпочтительно соотношение растительного жира и молочного жира составляет от 3/7 до 9/1.
Питательная композиция также может включать нерастительные липиды и немолочный жир, такие как животный жир, отличный от молочного жира, например рыбий жир, яичный липид, и масла микробов, водорослей, грибов или масла изолированных клеток. Предпочтительно, нерастительный немолочный жир присутствует в количестве не более 10% масс. из расчета на общую массу липидов, более предпочтительно не более 5% масс. Предпочтительно липид в питательной композиции включает источник жира, содержащий длинноцепочечные полиненасыщенные жирные кислоты ( - LC-PUFA), выбранные из группы, в которую входят рыбий жир, жир морских млекопитающих, масла водорослей, микробов, масла изолированных клеток и яичные липиды, в количестве 0,25 до 10% масс. из расчета на общее количество липида, предпочтительно в количестве от 0,5 до 10% масс.
Пальмитиновая кислота в sn-2 положении триглицерида
В качестве альтернативы, питательная композиция для введения в способе или применении согласно настоящему изобретению включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положение триглицеридов.
Триглицериды включают молекулу глицерида, к которой с помощью эфирных связей присоединены три остатка жирных кислот, которые могут быть одинаковыми или разными и которые обычно выбраны из насыщенных и ненасыщенных жирных кислот, содержащих от 6 до 26 атомов углерода, включая, но без ограничения, LA, ALA, олеиновую кислоту (С18:1), PA и/или стеариновую кислоту (С18:0). Такие жирно-кислотные триглицериды могут отличаться остатками жирных кислот, которые присутствуют, и/или соответствующим(и) положением(ями) остатка(ов) жирных кислот, например, в sn-1, -2 и/или -3 положении. Предпочтительно триглицериды, используемые в питательной композиции, выбраны таким образом, что количество остатков РА, которые присутствуют в триглицеридах, составляет 10% масс. или более из расчета на общее количество жирных кислот, присутствующих в триглицеридах, предпочтительно более 15% масс. Таким образом, в одном варианте осуществления настоящего изобретения в питательной композиции в способе или применении согласно настоящему изобретению липид включает триглицериды, которые включают в себя по меньшей мере 10% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, где по меньшей мере 15% пальмитиновой кислоты находится в sn-2 положении триглицеридов. Предпочтительно количество остатков PA, которые присутствуют в триглицеридах, составляет менее 30% масс., более предпочтительно от 16 до 24%. Предпочтительно триглицериды, используемые в питательной композиции, выбраны таким образом, что из всего количества остатков PA, присутствующих в триглицериде, по меньшей мере 15%, предпочтительно по меньшей мере 20%, более предпочтительно по меньшей мере 30%, еще более предпочтительно по меньшей мере 35%, наиболее предпочтительно по меньшей мере 40% находятся в sn-2 или бета-положении триглицерида.
Подходящие триглицериды для питательной композиции в способе или применении согласно настоящему изобретению являются коммерчески доступными, например от Loders Croklaan под названием Betapol™, и/или могут быть получены известным способом, например как описано в ЕР 0698078 и/или ЕР 0758846. Другим подходящим источником является InFat™ от Enzymotec. В случае, если указанные липиды получены путем транс- или переэтерификации растительных триглицеридов, эти источники в контексте настоящего изобретения рассматриваются как растительные липиды. Предпочтительно количество триглицерида с повышенном количеством остатков пальмитиновой кислоты в sn-2 положении молекулы триглицерида, который включен в липидную фракцию композиции, подлежащей введению в соответствии с настоящим способом или применением, составляет от 10 до 100% масс., предпочтительно от 20 до 100% масс., более предпочтительно от 20 до 80% масс., еще более предпочтительно от 50 до 80% масс.
Предпочтительным источником триглицеридов, содержащих пальмитиновую кислоту в sn-2 или бета-положении триглицерида, является животный жир нечеловекоподобного животного, более предпочтительно молочный жир нечеловекоподобного млекопитающего, еще более предпочтительно молочный жир коровьего молока. Предпочтительно молочный жир нечеловекоподобного млекопитающего, в частности молочный жир коровьего молока, используется в форме безводного молочного жира или топленого коровьего (сливочного) масла. Предпочтительно источник молочного жира представляет собой гомогенную жировую фазу, такую как топленое коровье масло или безводный молочный жир, и не представлен в форме эмульсии типа «масло в воде», такой как сливки, поскольку липидные глобулы питательной композиции по настоящему изобретению проще получать при использовании гомогенной жировой фазы. Предпочтительно количество молочного жира находится в интервале от 10 до 70% масс. молочных липидов из расчета на общее количество липидов, более предпочтительно от 15 до 60% масс., еще более предпочтительно от 25 до 50% масс., из расчета на общее количество липида.
Улучшенное стимулирование кривой роста и/или развития организма, аналогичное динамике роста и/или развитию при вскармливании грудью, наблюдалось при применении такого липидного компонента с повышенными количествами остатков пальмитиновой кислоты, расположенных в sn-2 положении молекул триглицеридов.
Состав жирных кислот
Термин ʺLAʺ в настоящем описании относится к линолевой кислоте и/или ацильной цепи (18:2 n6); термин ʺALAʺ в настоящем описании относится к α-линоленовой кислоте и/или ацильной цепи (18:3 n3); термин ʺPUFAʺ относится к полиненасыщенным жирным кислотам и/или ацильным цепям; термин «MUFA» относится к мононенасыщенным жирным кислотам и/или ацильным цепям; термин ʺLC-PUFAʺ относится к длинноцепочечным полиненасыщенным жирным кислотам и/или ацильным цепям, содержащим по меньшей мере 20 атомов углерода в жирной ацильной цепи и 2 или более ненасыщенных связей; термин ʺDHAʺ относится к докозагексаеновой кислоте и/или ацильной цепи (22:6, n3); термин ʺЕРАʺ относится к эйкозапентаеновой кислоте и/или ацильной цепи (20:5 n3); термин ʺАRАʺ относится к арахидоновой кислоте и/или ацильной цепи (20:4 n6); термин ʺDPAʺ относится к докозапентаеновой кислоте и/или ацильной цепи (22:5 n3). Термин ʺPAʺ относится к пальмитиновой кислоте и/или ацильным цепям (С16:0). Термин «жирные кислоты средней длины цепи» ( MCFA) относится к жирным кислотам и/или ацильным цепям с длиной цепи в 6, 8 или 10 атомов углерода.
Липид, который присутствует в питательной композиции в способе или применении согласно настоящему изобретению, предпочтительно включает PUFA, более предпочтительно LC-PUFA, поскольку LC-PUFA дополнительно улучшают картину роста и развитие организма. Питательная композиция предпочтительно включает от 5 до 35% масс. PUFA, более предпочтительно от 10 до 30% масс. PUFA, наиболее предпочтительно от 15 до 20% масс. PUFA, из расчета на общее количество липида. В одном варианте осуществления настоящего изобретения липид в питательной композиции для способа или применения согласно настоящему изобретению включает по меньшей мере 10% масс. полиненасыщенных жирных кислот из расчета на общее количество жирных кислот. Также предпочтительно, питательная композиция включает MUFA, предпочтительно от 10 до 80% масс. MUFA, более предпочтительно от 20 до 70% масс. MUFA, наиболее предпочтительно от 35 до 55% масс. MUFA, из расчета на общее количество липида.
LA присутствует в количестве, достаточном для способствования здоровому росту и развитию организма, но по возможности в малом количестве для предотвращения возникновения дисбаланса в росте или развитии организма. Таким образом, питательная композиция предпочтительно включает в себя менее 20% масс. LA из расчета на общее количество липида, предпочтительно от 5 до 16% масс., более предпочтительно от 10 до 14,5% масс. Предпочтительно питательная композиция включает по меньшей мере 5% масс. LA из расчета на общее количество липида. На 100 ккал питательная композиция предпочтительно включает 350-1400 мг LA. ALA присутствует в количестве, достаточном для стимулирования здорового роста и развития ребенка. Таким образом, питательная композиция предпочтительно включает по меньшей мере 1,0% масс. ALA из расчета на общее количество липида. Предпочтительно питательная композиция включает по меньшей мере 1,5% масс. ALA из расчета на общее количество липида, более предпочтительно по меньшей мере 2,0% масс. Предпочтительно питательная композиция включает менее 12,5% масс. ALA, более предпочтительно менее 10,0% масс., наиболее предпочтительно менее 5,0% масс. Предпочтительно в питательной композиции массовое соотношение LA/ALA составляет от 2 до 20, более предпочтительно от 3 до 16, более предпочтительно от 4 до 14, еще более предпочтительно от 5 до 12. Липид, который присутствует в питательной композиции в способе или применении в соответствии с изобретением, предпочтительно включает липиды, который включает в себя от 5 до 35% масс. полиненасыщенных жирных кислот (PUFA) из расчета на общее количество жирных кислот, включая линолевую кислоту (LA) и альфа-линоленовую кислоту (ALA) в массовом соотношении от 2 до 20.
Предпочтительно питательная композиция включает менее 10% масс. короткоцепочечных жирных кислот из расчета на общее количество жирных кислот, предпочтительно менее 8% масс., предпочтительно менее 6% масс., предпочтительно менее 5% масс. Предпочтительно питательная композиция включает по меньшей мере 0,5% масс. короткоцепочечных жирных кислот из расчета на общее количество жирных кислот, предпочтительно по меньшей мере 0,6% масс., менее 0,8% масс., предпочтительно по меньшей мере 0,9% масс., более предпочтительно по меньшей мере 1,2% масс., более предпочтительно по меньшей мере, 2,0% масс. Короткоцепочечные жирные кислоты представляют собой жирные кислоты с ацильной цепью, содержащей от 2 до 6 атомов углерода. Предпочтительно, питательная композиция включает в себя менее 10% масс. масляной кислоты (ацильная цепь, содержащая 4 атома углерода) из расчета на общее количество жирных кислот, предпочтительно менее 8% масс., предпочтительно менее 6% масс., предпочтительно менее 5% масс., предпочтительно менее 4% масс. Предпочтительно питательная композиция включает по меньшей мере 0,5% масс. масляной кислоты из расчета на общее количество жирных кислот, предпочтительно по меньшей мере 0,6% масс., предпочтительно по меньшей мере 0,9% масс., более предпочтительно по меньшей мере 1,2% масс. Питательная композиция предпочтительно включает по меньшей мере 3% масс. MCFA из расчета на общее количество жирных кислот, более предпочтительно по меньшей мере 10% масс., еще более предпочтительно 15% масс. Настоящая композиция предпочтительно включает менее 50% масс. MCFA из расчета на общее количество жирных кислот, более предпочтительно менее 30% масс., еще более предпочтительно менее 20% масс.
Согласно настоящему изобретению, питательная композиция предпочтительно включает LC-PUFA, более предпочтительно n-3 LC-PUFA, поскольку n-3 LC-PUFA стимулирует полезную кривую роста. Более предпочтительно питательная композиция включает EPA, DPA и/или DHA, еще более предпочтительно DHA. Поскольку низкая концентрация DHA, DPA и/или EPA уже является эффективной, и нормальный рост и развитие играют важную роль, содержание n-3 LC-PUFA в питательной композиции, более предпочтительно DHA, предпочтительно не превышает 15% масс. из расчета на общее содержание жирных кислот, предпочтительно не превышает 10% масс., еще более предпочтительно не превышает 5% масс. Предпочтительно питательная композиция включает по меньшей мере 0,15% масс., предпочтительно по меньшей мере 0,35% масс., более предпочтительно по меньшей мере 0,75% масс. n-3 LC-PUFA, более предпочтительно DHA, из расчета на общее содержание жирных кислот. В одном варианте осуществления настоящего изобретения композиция по настоящему изобретению включает по меньшей мере 0,15% масс. n-3 LC-PUFA из расчета на общее количество жирных кислот, выбранных из группы, в которую входят DHA, EPA и DPA, более предпочтительно DHA.
Поскольку группа n-6 жирных кислот, в особенности арахидоновая кислота (ARA) и LA в качестве ее предшественника, противодействует группе n-3 жирных кислот, в частности DHA и EPA, а также ALA в качестве ее предшественника, питательная композиция содержит относительно небольшие количества ARA. Содержание n-6 LC-PUFA, более предпочтительно ARA, предпочтительно не превышает 5% масс., более предпочтительно не превышает 2,0% масс., более предпочтительно не превышает 0,75% масс., еще более предпочтительно не превышает 0,5% масс., из расчета на общее количество жирных кислот. Поскольку присутствие ARA не является необходимым для стимулирования кривой роста и развития организма до кривой роста и развития, аналогичных кривой роста и развитию при вскармливании грудью, ARA может также отсутствовать.
Фосфолипиды
Предпочтительно питательная композиция для введения в способе или применении согласно настоящему изобретению включает фосфолипиды, предпочтительно питательная композиция включает фосфолипиды, полученные из молока нечеловекоподобных млекопитающих. Фосфолипиды, полученные из молока нечеловекоподобных млекопитающих, включают фосфолипиды, выделенные из молочного липида, липида сливок, липида плазмы сливок, липида плазмы масла, липида бета-сыворотки, липида молочной сыворотки, сырного липида и/или липида пахты. Липид пахты обычно получают в процессе производства пахты. Липид плазмы масла или липид бета-сыворотки обычно получают в процессе производства безводного молочного жира из сливок или сливочного (коровьего) масла. Предпочтительно фосфолипиды получают из молочных (коровьих) сливок. Фосфолипиды предпочтительно получают из молока коров, кобыл, овец, коз, буйволиц, лошадей и верблюдиц, наиболее предпочтительно из коровьего молока. Наиболее предпочтительно применение липидного экстракта, выделенного из коровьего молока. Подходящий источник фосфолипидов, полученных из молока нечеловекообразных млекопитающих, представляет собой фракцию, которая может быть выделена из молока, называемую мембраной жировых глобул молока (milk fat globule membrane - MFGM). Таким образом, в одном варианте осуществления настоящего изобретения фосфолипиды, которые будут использоваться в питательной композиции в способе или применении согласно настоящему изобретению, предоставлены как MFGM. Предпочтительно питательная композиция включает в себя от 0,5 до 20% масс. фосфолипидов из расчета на общее количество липида, более предпочтительно от 0,5 до 10% масс., более предпочтительно от 1 до 10% масс., еще более предпочтительно от 2 до 10% масс., еще более предпочтительно от 3 до 8% масс. фосфолипидов из расчета на общее количество липида.
Размер липидных глобул
Предпочтительно согласно настоящему изобретению, питательная композиция включает липидные глобулы. В жидкой форме композиции эти липидные глобулы эмульгированы в водной фазе. В качестве альтернативы, липидные глобулы представлены в форме порошка, и порошок подходит для восстановления с водой или другой водной фазой пищевого сорта, предпочтительно для получения смеси, готовой для питья. В одном варианте осуществления настоящего изобретения питательная композиция для введения в способе или применении согласно настоящему изобретению включает липидные глобулы, взвешенный по объему модальный диаметр которых составляет по меньшей мере 1,0 мкм, и/или в которых глобулы диаметром в интервале от 2 до 12 мкм составляют по меньшей мере 45% об. из расчета на общий объем липида. Липидные глобулы состоят из ядра и внешней поверхности. Ядро предпочтительно включает растительный жир и предпочтительно включает по меньшей мере 90% масс. триглицеридов, более предпочтительно по существу состоит из триглицеридов. Не все растительные жиры, которые присутствуют в композиции, обязательно должны содержаться в ядре липидных глобул, но предпочтительно основная часть, предпочтительно более 50% масс., более предпочтительно более 70% масс., еще более предпочтительно более 85% масс., еще более предпочтительно более 95% масс., наиболее предпочтительно болеее 98% масс. растительных липидов, которые присутствуют в композиции, включены в ядро липидных глобул. В одном варианте осуществления настоящего изобретения ядро липидных глобул включает по меньшей мере 40% масс. триглицеридов растительного происхождения, более предпочтительно по меньшей мере 50% масс., еще более предпочтительно по меньшей мере 70% масс. триглицеридов растительного происхождения, более предпочтительно ядро липидных глобул включает по меньшей мере 85% масс., более предпочтительно по меньшей мере 95% масс. триглицеридов растительного происхождения. Взвешенный по объему модальный диаметр липидных глобул в питательной композиции в способе или применении по настоящему изобретению составляет более 1,0 мкм, предпочтительно более 3,0 мкм, более предпочтительно 4,0 мкм или более, предпочтительно в интервале от 1,0 до 10 мкм, более предпочтительно в интервале от 2,0 до 8,0 мкм, еще более предпочтительно в интервале от 3,0 до 8,0 мкм, наиболее предпочтительно в интервале от 4,0 до 8,0 мкм. Предпочтительно также, распределение по размерам таково, что глобулы диаметром в интервале от 2 до 12 мкм составляют по меньшей мере 45% по объему, предпочтительно по меньшей мере 55% по объему, еще более предпочтительно по меньшей мере 65% по объему, еще более предпочтительно по меньшей мере 75% по объему. Более предпочтительно глобулы диаметров в интервале от 2 до 10 мкм составляют по меньшей мере 45% по объему, предпочтительно по меньшей мере 55% по объему, еще более предпочтительно по меньшей мере 65% по объему, еще более предпочтительно по меньшей мере 75% по объему. Еще более предпочтительно глобулы диаметром в интервале от 4 до 10 мкм составляют по меньшей мере 45% по объему, предпочтительно по меньшей мере 55% по объему, еще более предпочтительно по меньшей мере 65% по объему, еще более предпочтительно по меньшей мере 75% по объему. Предпочтительно глобулы диаметром более 12 мкм составляют менее 5% по объему.
Диаметр липидных глобул стандартных детских смесей первого уровня или второго уровня составляет менее 0,5 мкм. Было установлено, что крупные липидные глобулы стимулируют кривую роста или развитие организма, которые более похожи на кривую роста или развитие организма детей, вскармливающихся грудью. Процент липидных глобул представляет собой процент из расчета на общий объем липида. Термин «модальный диаметр» относится к диаметру, который является наиболее распространенным из расчета на общий объем липида, или к пиковому значению в графическом изображении, где Х представляет собой диаметр, и Y представляет собой объем (%).
Объем липидных глобул и их распределение по размерам может соответствующим образом определяться с использованием анализатора размера частиц, такого как Mastersizer (Malvern Instruments, Malvern, UK), например методом, описанным в публикации Michalski et al, 2001, Lait 81: 787-796.
Покрытие липидных глобул фосфолипидами
Предпочтительно согласно настоящему изобретению, питательная композиция включает полярные липиды. Полярные липиды являются амфипатическими по своей природе и включают в себя глицерофосфолипиды, гликосфинголипиды, сфингомиелин и/или холестерин. Более предпочтительно питательная композиция включает фосфолипиды (глицерофосфолипиды и сфингомиелин). Термин «полярные липиды» в настоящем изобретении относится к глицерофосфолипидам, гликосфинголипидам, сфингомиелину и холестерину. Полярные липиды, более предпочтительно фосфолипиды, предпочтительно присутствуют в виде покрытия на поверхности липидных глобул. Термин «покрытие» означает, что наружный поверхностный слой липидных глобул содержит полярные липиды, в то время как эти полярные липиды практически отсутствуют в ядре липидных глобул. Было установлено, что наличие полярных липидов, в частности фосфолипидов, в качестве покрытия или внешнего слоя липидной глобулы во вводимом питании преимущественно стимулирует кривую роста или развитие организма, которые боле похожи на кривую роста или развитие организма детей, вскармливающихся грудью. В одном варианте осуществления питательная композиция для введения в способе или применении согласно настоящему изобретению включает липидные глобулы, содержащие на поверхности, по меньшей мере частично, слой фосфолипидов. Не все фосфолипиды и/или полярные липиды, которые присутствуют в композиции, обязательно должны находиться в покрытии, но предпочтительно большая их часть находится в покрытии. Предпочтительно свыше 30% масс., более предпочтительно свыше 50% масс., более предпочтительно свыше 70% масс., еще более предпочтительно свыше 85% масс., наиболее предпочтительно свыше 95% масс. фосфолипидов и/или полярных липидов, которые присутствуют в композиции, находятся в покрытии липидных глобул. В предпочтительном варианте осуществления настоящего изобретения питательная композиция в способе или применении согласно настоящему изобретению включает фосфолипиды, предпочтительно питательная композиция содержит по меньшей мере 0,5% масс. фосфолипидов из расчета на общее количество липида. И еще более предпочтительно фосфолипиды включают по меньшей мере 15% масс. сфингомиелина из расчета на общее количество фосфолипидов.
В одном варианте осуществления настоящего изобретения в питательной композиции в способе или применении согласно настоящему изобретению взвешенный по объему модальный диаметр липидных глобул составляет 1,0 мкм или более, и поверхность липидных глобул, по меньшей мере частично, покрыта фосфолипидами. Комбинация липидных глобул большого размера и покрытия дополнительно стимулирует кривую роста или развитие организма, которые более похожи на кривую роста или развитие организма детей, вскармливающихся грудью, по сравнению с малыми липидными глобулами без фосфолипидного покрытия.
Согласно настоящему изобретению, питательная композиция предпочтительно включает в себя глицерофосфолипиды. Глицерофосфолипиды представляют собой класс липидов, полученных из жирных кислот, этерифицированных по гидроксильным группам на 1 или 2 атоме углерода основной цепи глицеринового фрагмента, и отрицательно заряженной фосфатной группы, присоединенной к 3 атому углерода глицерина посредством сложноэфирной связи, и необязательно, холиновой группы (в случае фосфатидилхолина (phosphatidylcholine - РС)), сериновой группы (в случае фосфатидилсерина (phosphatidylserine - SС)), этаноламиновой группы (в случае фосфатидилэтаноламина (phosphatidylethanolamine - PE), инозитоловой группы (в случае фосфатидилинозитола (phosphatidylinositol - PI)) или глицериновой группы (в случае фосфатидилглицерина (phosphatidylglycerol - PG), присоединенной к фосфатной группе. Лизофосфолипиды представляют собой класс фосфолипидов с одной жирной ацильной цепью. Предпочтительно композиция по настоящему изобретению включает PC, PS, PI и/или PE, более предпочтительно по меньшей мере PC.
Предпочтительно питательная композиция включает сфингомиелин. Молекулы сфингомиелинов представляют собой фосфорилхолиновую или фосфорилэтаноламиновую молекулу, этерифицированную по 1-гидроксильной группы церамида. Они относятся к классу фосфолипидов, а также сфинголипидов, но не классифицируются как глицерофосфолипиды и гликосфинголипиды. Предпочтительно питательная композиция включает от 0,05 до 10% масс. сфингомиелина из расчета на общее количество липида, более предпочтительно от 0,1 до 5% масс., еще более предпочтительно от 0,2 до 2% масс.
Согласно настоящему изобретению, питательная композиция предпочтительно включает гликосфинголипиды. Термин «гликосфинголипиды», когда используется в настоящем изобретении, относится, в частности, к гликолипидам с аминоспиртовым сфингозином. Основная цепь сфингозина представляет является О-связанной с заряженной головной группой, такой как этаноламиновая, сериновая или холиновая цепь. Основная цепь представляет собой также амид, связанный с жирной ацильной группой. Гликосфинголипиды представляют собой церамиды с одним или несколькими остатками сахаров, соединенных в бета-гликозидной связи при гидроксильной группе в положении 1. Предпочтительно питательная композиция содержит ганглиозиды, более предпочтительно по меньшей мере один ганглиозид, в которую входят GM3 и GD3.
Термин «сфинголипиды» в настоящем изобретении относится к сфингомиелинам и гликосфинголипидам. Термин «фосфролипиды» в настоящем изобретении относится к сфингомиелину и глицерофосфолипидам. Предпочтительно фосфолипиды получены из молочных липидов. Предпочтительно массовое отношение фосфолипиды: гликосфинголипиды составляет от 2:1 до 10:1, более предпочтительно от 2:1 до 5:1.
Предпочтительно питательная композиция включает от 0,1 до 10% масс. гликосфинголипидов из расчета на общее количество липида, более предпочтительно от 0,5 до 5% масс., еще более предпочтительно от 2 до 4% масс. Предпочтительно питательная композиция включает от 0,5 до 10% масс. гликосфинголипидов и фосфолипидов из расчета на общее количество липида, более предпочтительно от 1,0 до 10% масс. гликосфинголипидов и фосфолипидов из расчета на общее количество липида. В одном варианте осуществления питательная композиция для способа или применения согласно настоящему изобретению включает фосфолипиды, где фосфолипид включает гликолипиды и/или получен из либо составляет часть мембран жировых глобул молока (MFGM), предпочтительно MFGM коровьего молока.
Согласно настоящему изобретению, питательная композиция предпочтительно включает холестерин. Питательная композиция предпочтительно включает по меньшей мере 0,005% масс. холестерина из расчета на общее количество липида, более предпочтительно по меньшей мере 0,01% масс., более предпочтительно по меньшей мере 0,02% масс., более предпочтительно по меньшей мере 0,05% масс., еще более предпочтительно по меньшей мере, 0,1% масс. Предпочтительно количество холестерина не превышает 10% масс. из расчета на общее количество липида, более предпочтительно не превышает 5% масс., еще более предпочтительно не превышает 1% масс. из расчета на общее количество липида.
Согласно настоящему изобретению, питательная композиция предпочтительно включает от 0,6 до 25% масс. полярных липидов из расчета на общее количество липида, где полярные липиды включают фосфолипиды, гликосфинголипиды и холестерин, более предпочтительно от 0,6 до 12% масс., более предпочтительно от 1 до 10% масс., еще более предпочтительно от 2 до 10% масс., еще более предпочтительно от 3,0 до 10% масс. полярных липидов из расчета на общее количество липида, где полярные липиды включают фосфолипиды, гликосфинголипиды и холестерин.
Предпочтительными источниками фосфолипидов, гликосфинголипидов и/или холестерина являются яичные липиды, молочный жир, жир пахты и жир сыворотки масла, такой как жир бета-сыворотки. Предпочтительным источником фосфолипидов, в частности PC, является соевый лецитин и/или лецитин подсолнечника. Как упоминалось выше, согласно настоящему изобретению, питательная композиция предпочтительно включает фосфолипиды, полученные из молока млекопитающих, предпочтительно молока нечеловекообразных млекопитающих. Предпочтительно питательная композиция включает фосфолипиды и гликосфинголипиды, полученные из молока. Предпочтительно также, холестерин получен из молока. Предпочтительно полярные липиды, в частности фосфолипиды, получены из молока. Полярные липиды, в частности фосфолипиды, полученные из молока, включают полярные липиды, в частности фосфолипиды, выделенные из молочного липида, липида сливок, липида сыворотки сливок, липида плазмы масла, липида бета-сыворотки, липида молочной сыворотки, липида сыра и/или липида пахты. Липид пахты обычно получают в процессе производства пахты. Липид плазмы масла и липид бета-сыворотки обычно получают в процессе производства безводного молочного жира из сливочного (коровьего) масла. Предпочтительно фосфолипиды, гликосфинголипиды и/или холестерин получают из молочных сливок (сливок коровьего молока). Питательная композиция предпочтительно включает фосфолипиды, гликосфинголипиды и/или холестерин из коровьевого молока, молока кобылиц, овец, коз, буйволиц, лошадей и верблюдиц. Наиболее предпочтительно применение липидного экстракта, выделенного из коровьего молока. Применение полярных липидов из молочного жира преимущественно включает полярные липиды из мембран жировых глобул молока (MFGM), которые больше всего напоминают грудное молоко. Полярные липиды, в частности фосфолипиды, полученные из молочного жира, преимущественно стимулируют кривую роста более эффективно чем полярные липиды из других источников. Подходящий источник фосфолипидов, полученных из молока нечеловекообразных млекопитающих, представляет собой фракцию, которая может быть выделена из указанных мембран жировых глобул молока (MFGM). Таким образом, в одном варианте осуществления настоящего изобретения фосфолипиды, которые будут использоваться в питательной композиции в способе или применении согласно настоящему изобретению, предоставлены как MFGM. Полярные липиды, в частности фосфолипиды, предпочтительно расположены на поверхности липидных глобул, т.е. как покрытие или наружный слой. Было обнаружено, что, когда полярные липиды или фосфолипиды присутствуют в покрытии липидных глобул, они более эффективны, чем когда они смешаны в сухом виде в порошкообразном продукте, т.е. присутствует в качестве ингредиента как такового. Подходящим способом определения, расположены ли полярные липиды на поверхности липидных глобул, является лазерная сканирующая микроскопия. Таким образом, совместное применение полярных липидов, в частности фосфолипидов, полученных из молока домашних животных, и триглицеридов, полученных из растительных липидов, позволяет получать липидные глобулы с покрытием, которое более похоже на грудное молоко, обеспечивая при этом оптимальный профиль жирных кислот. Подходящими коммерчески доступными источниками молочных полярных липидов являются BAEF, SM2, SM3 и SM4 порошок от Corman, Salibra от Glanbia и LacProdan MFGM-10 или PL20 от Aria. Предпочтительно источник молочных полярных липидов включает по меньшей мере 4% масс. фосфолипидов из расчета на общее количество липида, более предпочтительно от 7 до 75% масс., наиболее предпочтительно от 20 до 70% масс. фосфолипидов из расчета на общее количество липида. Предпочтительно массовое отношение фосфолипидов к белкам составляет свыше 0,10, более предпочтительно свыше 0,20, еще более предпочтительно свыше 0,3. Предпочтительно по меньшей мере 25% масс., более предпочтительно по меньшей мере 40% масс., наиболее предпочтительно по меньшей мере 75% масс. полярных липидов, в частности фосфолипидов, получены из молочных полярных липидов.
Способы получения липидных глобул увеличенного размера и/или с покрытием фосфолипидов раскрыты в WO 2010/0027258, WO 2010/0027259 и WO 2013/135738.
Предпочтительно, питательная композиция в способе или применении согласно настоящему изобретению включает липидные глобулы увеличенных размеров по сравнению с размером в стандартной детской смеси, а также, по меньшей мере частично, покрыты фосфолипидами. Таким образом, в одном варианте осуществления настоящего изобретения питательная композиция в способе или применении согласно настоящему изобретению включает липидные глобулы, у которых
а) взвешенный по объему модальный диаметр составляет по меньшей мере 1,0 мкм, и/или глобулы диаметром от 2 мкм до 12 мкм составляют по меньшей мере 45% по объему из расчета на общий объем липида, и
b) поверхность, по меньшей мере частично, покрыта слоем фосфолипидов.
Все предпочтительные варианты осуществления, описанные для размера липидных глобул и покрытий фосфолипидами, описанные выше, применимы также к комбинации обоих отличительных признаков.
Детская смесь первого уровня и детская смесь второго уровня
Питательная композиция для введения в способе или применении согласно настоящему изобретению выбрана из детской смеси первого уровня и детской смеси второго уровня. Это означает, что питательная композиция по настоящему изобретению не является женским молоком. В качестве альтернативы, термин «детская смесь» относится к композиции, которая получена искусственно или, другими словами, является синтетической. Таким образом, в одном варианте осуществления настоящего изобретения питательная композиция выбрана из искусственной детской смеси первого уровня и искусственной детской смеси второго уровня или синтетической детской смеси первого уровня и синтетической детской смеси второго уровня. В контексте настоящего изобретения термин «молочная смесь первого уровня» относится к питательным композициям, искусственно изготовленным и предназначенным для детей от 0 до примерно 4-6 месяцев в качестве замены женского молока. Обычно детские смеси первого уровня подходят для применения в качестве единственного источника питания. Такие детские смеси также известны как молочные смеси начального периода жизни. Питательная смесь для детей с 4-6 месяцев жизни до 12 месяцев жизни предназначена для докорма детей, которых начинают отлучать от груди с переходом на другие продукты. Такие детские смеси также известны как молочные смеси второго уровня. Детские смеси первого и второго уровней подчиняются строгим правилам, например Директивам Комиссии ЕС 2006/141/EC.
Питательная композиция включает от 3 до 7 г липида/100 ккал, предпочтительно от 4 до 6 г липида/100 ккал, более предпочтительно от 4,5 до 5,5 г липида/100 ккал, от 1,25 до 5 г белка/100 ккал, предпочтительно от 1,35 до 4 г белка/100 ккал, более предпочтительно от 1,5 до 3 г белка/100 ккал, более предпочтительно от 1,25 до 2,5 г белка/100 ккал, более предпочтительно от 1,25 до 2,25 г белка/100 ккал, еще более предпочтительно от 1,25 до 2,1 г белка/100 ккал и от 6 до 18 г усвояемого углевода/100 ккал, предпочтительно от 8 до 16 г усвояемого углевода/100 ккал, более предпочтительно от 10 до 15 г усвояемого углевода/100 ккал.
Белок
Питательная композиция включает в себя белки, предпочтительно в количествах, указанных выше, в частности от 1,25 до 5 г белка/100 ккал, предпочтительно от 1,35 до 4 г белка/100 ккал, более предпочтительно от 1,5 до 3 г белка/100 ккал, более предпочтительно от 1,25 до 2,5 г белка/100 ккал, более предпочтительно от 1,25 до 2,25 г белка/100 ккал, еще более предпочтительно от 1,25 до 2,1 г белка/100 ккал. Источник белка должен быть выбран таким образом, чтобы удовлетворять минимальным требования к содержанию незаменимых аминокислот и обеспечивать удовлетворительный рост. Поэтому предпочтительными источниками белка являются белки молока коров, такие как молочная сыворотка, казеин и их смеси, и белки сои, картофеля или гороха. В случае использования белков молочной сыворотки источником белка предпочтительно является кислая молочная сыворотка или сладкая молочная сыворотка, изолят сывороточного белка или их смеси, он и может включать α-лактальбумин и β-лактоглобулин. Более предпочтительно, источник белка основан на кислой молочной сыворотке или сладкой молочной сыворотке, из которой удален казеино-гликомакропептид (caseino-glyco-macropeptide - CGMP). Предпочтительно композиция включает по меньшей мере 3% масс. казеина из расчета на сухую массу. Предпочтительно казеин является интактным и/или негидролизованным. Для настоящего изобретения белки включают пептиды и свободные аминокислоты.
Усвояемые углеводы
Питательная композиция включает усвояемые углеводы, предпочтительно в количествах, указанных выше, в частности от 6 до 18 г усвояемого углевода/100 ккал, предпочтительно от 8 до 16 г усвояемого углевода/100 ккал, более предпочтительно от 10 до 15 г усвояемого углевода/100 ккал. Предпочтительными источниками усвояемых углеводов являются лактоза, глюкоза, сахароза, фруктоза, галактоза, мальтоза, крахмал и мальтодекстрин. Лактоза представляет собой основной усвояемый углевод, который присутствует в женском грудном молоке. Лактоза преимущественно имеет низкий гликемический индекс. Питательная композиция предпочтительно включает лактозу. Питательная композиция предпочтительно содержит усвояемый углевод, где лактоза составляет по меньшей мере 35% масс., более предпочтительно по меньшей мере 50% масс., более предпочтительно по меньшей мере 75% масс., еще более предпочтительно по меньшей мере 90% масс., наиболее предпочтительно по меньшей мере 95% масс. усвояемого углевода. Настоящая композиция предпочтительно включает по меньшей мере 25% масс. лактозы, предпочтительно по меньшей мере 40% масс. лактозы, из расчета на сухую массу.
Неусвояемые углеводы
В одном варианте осуществления настоящего изобретения питательная композиция включает неусвояемые олигосахариды. Предпочтительно, питательная композиция включает неусвояемые олигосахариды со степенью полимеризации (degree of polymerization - DP) от 2 до 250, более предпочтительно от 3 до 60.
Предпочтительно композиция по настоящему изобретению включает фруктоолигосахариды, инулин и/или галактоолигосахариды, более предпочтительно галактоолигосахариды, наиболее предпочтительно трансгалактоолигосахариды. В предпочтительном варианте осуществления композиция включает смесь трансгалактоолигосахаридов и фруктоолигосахаридов или инулина. Подходящими неусвояемыми олигосахаридами являются, например, Vivinal GOS (FrieslandCampina DOMO), Raftilin HP или Raftilose (Orafti).
Предпочтительно питательная композиция включает от 80 мг до 2 г неусвояемых олигосахаридов на 100 мл, более предпочтительно от 150 мг до 1,50 г, еще более предпочтительно от 300 мг до 1 г на 100 мл. Питательная композиция предпочтительно включает от 0,25% масс. до 20% масс., более предпочтительно от 0,5% масс. до 10% масс., еще более предпочтительно 1,5% масс. до 7,5% масс. неусвояемых олигосахаридов из расчета на сухую массу.
Применение
В способе или применении согласно настоящему изобретению питательная композиция вводится ребенку или используется ребенком. В контексте настоящего изобретения термин «ребенок» относится к ребенку возраста до 12 месяцев. Предпочтительно питательная композиция вводится доношенному ребенку или используется доношенным ребенком. Термин «доношенный ребенок» означает ребенка, рожденного в гестационном возрасте от 37 до 42 недель. Предпочтительно питательная композиция вводится здоровому ребенку или используется здоровым ребенком. Предпочтительно питательная композиция вводится ребенку мужского пола. Хотя влияние питательной композиции по настоящему изобретению на кривую постнатального роста и постнатальное развитие организма наблюдался у детей как мужского, так и женского пола, наибольший эффект наблюдался у детей мужского пола. Предпочтительно, питательная композиция используется по меньшей мере в течение первых 2 месяцев жизни ребенка, предпочтительно по меньшей мере в течение первых 3 месяцев жизни ребенка, более предпочтительно по меньшей мере в течение первых 4 месяцев жизни ребенка. Предпочтительно питательная композиция вводится ребенку в возрасте менее 6 месяцев, более предпочтительно в возрасте менее 4 месяцев.
Согласно настоящему изобретению, стимулируется кривая постнатального роста или постнатальное развитие организма ребенка до кривой роста или развития организма, которые подобны кривой роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью. В качестве альтернативы, согласно настоящему изобретению, стимулируется кривая постнатального роста или постнатальное развитие организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
В качестве альтернативы «стимулирования постнатальной кривой роста или постнатального развития организма ребенка до кривой роста или развития организма, подобных динамике роста или развитию организма, наблюдаемым у детей, вскармливающихся грудью», настоящее изобретение относится также к улучшению постнатальной кривой роста или постнатального развития организма до кривой роста или развития организма, наблюдаемых у детей, вскармливающихся грудью, предпочтительно при сравнении с кривой роста или развитием организма детей, вскармливающихся молочной смесью первого уровня или молочной смесью второго уровня, включающей молочный жир или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, но в которой менее 15% остатков пальмитиновой кислоты, находится в sn-2 положении триглицеридов.
Предпочтительно, кривая роста или развитие организма выбраны из группы, в которую входят кривая или развитие массы тела, массы для роста (длины тела) и/или индекса массы тела (BMI). В предпочтительном варианте осуществления настоящего изобретения кривая роста или развитие организма представляют собой кривую роста или развитие организма в первые 12 месяцев жизни ребенка. Предпочтительно, масса и/или BMI и/или масса тела для роста ребенка в 12 месяцев приближены к массе и/или BMI и/или массе тела для роста (длины) ребенка, вскармливающегося грудью, в 12 месяцев. Предпочтительно, масса тела и/или BMI и/или масса для роста (длины) ребенка в 12 месяцев приближены к массе тела и/или BMI и/или массе для роста (длины) ребенка в 12 месяцев согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
Предпочтительно кривая роста или развитие организма представляет собой кривую роста или развитие окружности головы. В предпочтительном варианте кривая роста или развитие организма представляет собой кривую роста или развитие организма в первые 12 месяцев жизни ребенка. Предпочтительно окружность головы ребенка в 12 месяцев приблизительно равна окружности головы ребенка, вскармливающегося грудью. Предпочтительно окружность головы ребенка в 12 месяцев приблизительно равна окружности головы ребенка в 12 месяцев согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
Предпочтительно кривая роста или развитие организма представляет собой кривую роста или развитие толщины кожной складки, предпочтительно кривую роста или развитие толщины подлопаточной кожной складки и/или толщину складки над трехглавой мышцей. В предпочтительном варианте кривая роста или развитие организма представляют собой кривую роста или развитие организма в первые 12 месяцев жизни ребенка. Предпочтительно в 12 месяцев у ребенка толщина кожной складки, предпочтительно толщина подлопаточной кожной складки и/или толщина кожной складки над трехглавой мышцей, приблизительно равна толщине кожной складки ребенка, вскармливающегося грудью, в 12 месяцев. Предпочтительно, в 12 месяцев у ребенка толщина подлопаточной кожной складки и/или толщина кожной складки над трехглавой мышцей приблизительно равна толщине подлопаточной кожной складки и/или толщине кожной складки над трехглавой мышцей ребенка в 12 месяцев согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ.
В одном варианте осуществления согласно настоящему изобретению стимулируется i) сбалансированная кривая роста или сбалансированное развитие организма ребенка и/или предотвращается несбалансированная кривая роста или несбалансированное развитие организма ребенка либо снижается их риск.
ОПИСАНИЕ ФИГУР
На графиках фигур 1-3 ось х представляет собой число недель жизни ребенка после рождения. Ось у представляет собой значения z-score по сравнению с Нормами роста детей грудного вскармливания, разработанными ВОЗ. Точки данных на 0, 17 неделях и 52 неделях представлены слегка сдвинутыми относительно друг друга таким образом, чтобы доверительные интервалы стали видимыми.
На фигуре 1 представлены средние значения и доверительные интервалы для 0,95 доверительной вероятности (confidence interval - CI) показателя z-score масса тела/возраст по возрастной категории ITT группы.
На фигуре 2 представлены средние значения и доверительные интервалы для 0,95 доверительной вероятности показателя z-score BMI/возраст по возрастной категории ITT группы.
На фигуре 3 представлены средние значения и доверительные интервалы для 0,95 доверительной вероятности показателя z-score масса тела/возраст по возрастной категории ITT группы.
В примерах данные собраны у детей возраста 17 недель и 52 недель. Они интерпретируются как соответствующие 4 месяцам и 12 месяцам, соответственно. Другими словами, в контексте настоящего изобретения 4-месячный возраст рассматривается как возраст 17 недель, а 12-месячный возраст рассматривается как возраст 52 недели.
ПРИМЕРЫ
Пример 1: Экспериментальная и контрольная детские смеси
Диета 1: Стандартный Nutrilon 1
Детская смесь с энергетической ценностью 66 ккал на 100 мл готовой к употреблению смеси, содержащая 1,3 г белка (белок молочной сыворотки и казеин в соотношении 6/4 масс./масс.), 7,3 г усвояемого углевода (в основном, лактозы), 3,4 г жира и 0,8 г короткоцепочечных галакто-олигосахаридов (от VivinalGOS) и длинноцепочечных галактоо-олигосахаридов (от RaftilinHP) в соотношении 9/1 масс./масс., а также минералы, витамины, следовые микроэлементы и другие питательные микроэлементы, которые известны в данной области техники и соответствуют директивам для детской смеси. Смесь поставляется в виде порошка с инструкцией для восстановления с водой. Примерно 13,6 г порошка восстанавливают до 100 мл готовой для питья детской смеси.
Жировой компонент включает, главным образом, растительный жира (смесь пальмового масла, рапсового масла низким содержанием эруковой кислоты, кокосового масла, подсолнечного масла с высоким содержанием олеиновой кислоты, подсолнечного масла, небольшого количества соевого лецитина (0,13% масс.)) и примерно 1,5% масс. премикса LC-PUFA (рыбий жир и микробное масло).
Взвешенный по объему модальный диаметр липидных глобул составляет примерно 0,5 мкм, и липидные глобулы со взвешенным по объему модальным диаметром в интервале от 2 до 12 мкм составляют менее 10% об.
Диета 2: Экспериментальная детская смесь
Детская смесь, аналогичная смеси диеты 1, но со следующими отличиями:
жировой компонент включает примерно 51% масс. растительного жира (смесь рапсового масла с низких содержанием эруковой кислоты, кокосового масла, подсолнечного масла с высоким содержание олеиновой кислоты, подсолнечного масла), примерно 44% масс. безводного жира коровьего молока, 1,5% масс. LC-PUFA-содержащего масла (рыбий жир и микробное масло), 0,13% масс. соевого лецитина, примерно 3,6% масс. молочного жира, полученного из пахты, обогащенной молочными фосфолипидами, или мембран жировых глобул молока (молочные фосфолипиды составляют примерно 1,5% масс. из расчета на общее количество липида);
взвешенный по объему модальный диаметр липидных глобул составляет примерно 5,6 мкм, и липидные глобулы со взвешенным по объему модальным диаметром в интервале от 2 до 12 мкм составляют более 45% об.
Составы жирных кислот диеты 1 и диеты 2 очень близки по содержанию насыщенных, моно- и полиненасыщенных кислот и содержанию n3 и n6 PUFA. Количество пальмитиновой кислоты в диете 1 и диете 2 составляет 18,4% масс. и 17,7% масс. (из расчета на общее количество жирных кислот), соответственно. В диете 2 примерно 36% масс. остатков пальмитиновой кислоты находится в положении sn2, в диете 1 этот показатель составляет 13% масс. Количество C4:0 (масляная кислота) составляет 0,10% масс. в диете 1 и 1,39% масс. в диете 2, количество С6:0 (капроновая кислота) составляет 0,24% масс. в диете 1 и 0,98% масс. в диете 2. Проценты по массе представлены из расчета на общее количество липида в молочной смеси.
Пример 2: Протокол исследования и популяции исследования
После подписания родителем(ями)/законным(и) опекуном(ами) информированного согласия, детей, участвующих в эксперименте и вскармливающихся исключительно детской смесью, рандомизируют для введения им экспериментального продукта или контрольного продукта для двойного слепого исследования в течение периода максимально 17 недель (в зависимости от возраста на момент начала исследования). В контрольную группу включают только детей, вскармливающихся грудью, и график их посещения и оценочные исследования соответствуют графику посещения и оценочным исследованиям рандомизированных детей. В ходе первого посещении собирают исходные данные и данные о рождении и предоставляют родителю(ям) исследуемый продукт и журналы ежедневных записей. Последующие посещения для исследования детей проводят в возрасте 5, 8, 13 и 17 недель. В ходе этих посещений собирают информацию и антропометрические данные. Во время посещения на 52 неделе (необязательное продление исследования) проводят сбор антропометрических данных. В исследовании задействовано 17 центров в 4 странах, и всего в исследование принимают участие 313 пациентов: 6 центров в Нидерландах (121 пациентов), 3 центра во Франции (13 пациентов), 7 центров в Бельгии (158 пациентов) и 1 центр в Сингапуре (21 пациент). Из общего числа 313 зарегистрированных пациентов 223 пациента включают в рандомизированные исследования и 88 включают в контрольную группу грудного вскармливания, 2 пациента исключают из рандомизированного исследования по результатам скрининга.
Совокупность данных по всем обработанным пациентам (All-Subjects-Treated - AST) включает данные всех пациентов, принимающих участие в рандомизированных испытаниях (ASR, n=223), которые получают по меньшей мере некоторые исследуемые продукты. Пациенты (n=8) с достаточными доказательствами того, что ни в одном исследовании не получили ни одного продукта, не включают в AST группу (n=215).
Совокупность данных ITT популяции включает данные всех пациентов ASR группы (ITT=ASR). Результаты анализа ITT данных отражают воздействие на целевую популяцию в реальной клинической ситуации/оценивают эффект (эффективность) способа лечения. Данные пациентов анализируют как «как рандомизированные».
Анализ «в соответствии с протоколом» (Per-Protocol (PP) - РР) ограничен анализом данных пациентов, которые выполняют условия протокола с точки зрения приемлемости, вмешательств, инструкций/ограничений и оценки результатов. Совокупность данных PP популяции состоит из данных всех субъектов и/или посещений субъектов из совокупности данных ITT популяции, полученных без каких-либо серьезных отклонений от условий протокола. Таким образом, совокупность данных РР популяции не ограничивается субъектами, которые прошли полное исследование, и количество субъектов на посещение меняется. Результаты анализа данных РР популяции оценивают эффект (эффективность) лечения. Данные обследования субъектов анализируют как данные «обработанных» пациентов. Для исключения из совокупности данных РР популяции используют следующие правила отбора пациентов: возраст в начале исследования (1 посещение) >35 дней, отсутствуют данные о массе тела при рождении или она составляет <9,96 или >90,04 процентилей (исходя из Норм роста детей грудного вскармливания, разработанных ВОЗ), окружность головы при включении находится вне ±2,04 SD процентилей (исходя из Норм роста детей грудного вскармливания, разработанных ВОЗ), отсутствие по меньшей мере одного значимого посещения после получения данных исходного уровня. Исследование потребления продукта начинают через≥6 дней после определения данных исходного уровня с получением результатов другого исследования продукта в качестве двойника, ни один продукт исследования не потребляется в соответствии с историей болезни, то есть болезнями/состояниями, которые определены медицинским контролем. Для исключения данных различных посещений из совокупности данных РР популяции применяют следующие правила: любое посещение более чем через 3 дня после приостановки приема исследуемого продукта, независимо от того, является приостановка временной или нет, любое посещение более чем через 3 дня после начала вскармливания другой детской смесью, любое посещение через более чем 3 дня после начала кормления твердой пищей. Из исследования исключают данные рандомизированных исследований 49 субъектов и данные некоторых посещений.
Для контрольной группы нерандомизированного исследования, получающей грудное вскармливание, также определяют совокупности данных, соответствующие ITT и PP популяциям рандомизированных детей. Соответственно, в качестве совокупности данных ITT популяции определены данные полной группы детей, вскармливающихся грудью, ни один пациент не исключен из группы детей, вскармливающихся грудью. Соответственно совокупности данных РР популяции, определяют совокупность данных популяции соответствия протоколу контрольной группы грудного вскармливания (Protocol Compliant Breastfed Ref - PCBF*), применяя соответствующие правила, определенные для формирования набора данных PP популяции. Для исключения данных пациента из совокупности PCBF данных используют следующие правила: возраст при определении данных исходного уровня >35 дней, отсутствуют данные о массе тела при рождении или составляют <9,96-ю или >90,04-ю процентиль (исходя из Норм роста детей грудного вскармливания, разработанных ВОЗ), окружность головы при включении вне ± 2,04 SD (исходя из Норм роста детей грудного вскармливания, разработанных ВОЗ), отсутствие по меньшей мере одного значимого посещения после посещения для определения исходных данных или соответствующий анамнез, то есть болезни/состояния, выявленные медицинским контролем. Для исключения данных различных посещений из совокупности PCBF популяции используют следующие правила: любое посещение более чем через 3 дня после остановки грудного вскармливания в случае, если прекращение грудного вскармливания происходит до 13-недельного возраста, любое посещение более чем через 3 дня после начала другого вскармливания в случае, когда начало вскармливания другой смесью присходит до 13-недельного возраста, любое посещение более чем через 3 дня после начала вскармливания твердой пищей в случае, когда начало вскармливания другим твердым питанием происходит до 4-го посещения. 11 пациентов, вскармливающихся грудью, а также данные некоторых посещений исключают.
Данные пациентов (рандомизированных или вскармливающихся грудью), которые включены в совокупность PP/PCBF данных до и включая посещение в 17-недельном возрасте, и включенных в необязательно продолженное исследование, включены в совокупность данных РР популяции при посещении в возрасте 52 недель.
Статистически значимые различия между этими группами в рамках различных совокупностей данных (PP, ITT) по стратификации факторов пола, возрасту на исходном уровне (<14 дней/> 14 дней), регионам (Европа или Азия) отсутствуют. Нет разницы в продолжительности исследования этих групп.
Анализ роста пациентов (определение массы тела и BMI в 52 недель) проводят с использованием параметрических кривых роста (parametric growth curves - PGC), корректируя факторы стратификации, описанные выше. Такой подход предполагает параметрическую функцию времени (т.е. возраста субъекта) и, таким образом, описывает развитие параметров роста (т.е. массы тела BMI) во времени с помощью полиномиальной функции второго порядка. Она не требует, чтобы параметры субъектов исследования определялись в одном и том же множестве временных точек. Полученные параметры сравнивают для оценки различий полученных кривых. Анализы чувствительности для подтверждения пригодности модели выполняют с использованием общего линейного моделирования (ANCOVA) и моделей произвольных средних значений (Arbitrary Mean Models), где время моделируется как категориальная переменная.
Для анализа значений показателей z-score каждое из антропометрических измерений субъектов нормализуют, используя стандартные значения показателей z-score согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ, которые представляют собой зависимые от возраста и пола стандартизированные значения. Макрос SAS (предоставлен ВОЗ, http://www.who.int/childgrowth/software/en/) используют при нормализации абсолютных данных антропометрических измерений субъектов, никакой коррекции для стратификации факторов не производят. Анализ z-score проводят посредством возрастной категории, выбирая антропометрические данные, собранные в интервале ±10 дней со дня посещения, принимая во внимание реальный возраст исследуемых пациентов. Возрастные категории: новорожденные, 10 ± 10 дней при вступлении в исследовании, 35 ± 10 дней на 5 неделе, 56 ± 10 дней на 8 неделе, 91 ± 10 дней на 13 неделе, 119 ± 10 дней на 17 неделе и 365 ± 10 дней на 52 неделе.
Для резюмирования эквивалентности увеличения массы тела по сравнению с исходным уровнем (рандомизация) до возраста 17 недель у детей, получающих экспериментальный продукт, по сравнению с детьми, получающими контрольный продукт, двусторонние доверительные интервалы при доверительной вероятности 0,95 для различий среднего увеличения массы тела должны находиться в пределах от -0,5 SD до +0,5 SD с минимальным значением 3 г/день и максимальным значением 5 г/день. Анализ эквивалентности проводят с использованием параметрических кривых роста, корректируя факторы стратификации, описанные выше. Такой подход предполагает параметрическую функцию времени (т.е. возраста субъекта) и, таким образом, описывает развитие параметров роста (т.е. массы тела) с течением времени полиномиальной функцией второго порядка. Она не требует, чтобы параметры субъектов исследования определялись в одном и том же множестве временных точек. Полученные параметры сравнивают для оценки различий между кривыми. Анализы чувствительности для подтверждения пригодности модели выполняют с использованием общего линейного моделирования (ANCOVA) и моделей произвольных средних значений (Arbitrary Mean Models), где время моделируется как категориальная переменная.
Пример 3: Результаты оценки кривой роста и развития организма
Масса тела
Результаты показывают, что средняя масса тела (кг) мальчиков и девочек (включены в три исследуемые группы) находится в пределах z-score -1 и +1 Норм роста детей грудного вскармливания, разработаны[ ВОЗ, для совокупности данных ITT и PP популяций (данные не показаны).
Увеличение массы тела в сутки в экспериментальной группе эквивалентно контрольной группе грудного вскармливания (ретроспективный анализ) с момента посещения для определения данных исходного уровня до возраста 17 недель в совокупности данных как РР популяции, так и ITT популяции при использовании границы эквивалентности ±3 г/день. Эквивалентность увеличения массы тела в день показана для экспериментальной детской смеси по сравнению с группой, принимающей стандартную детскую смесь (РР и ITT популяции), даже при выборе только тех детей, которые поступили в возрасте до 14 дней.
Средние значения показателей z-score масса/возраст на посещение и соответствующие доверительные интервалы (confidence intervals - CI) для доверительной вероятности 0,95 показывают, что рост массы тела контрольной группы детей, вскармливающихся грудью, не отличается от разработанных ВОЗ Стандартов роста ребенка. В период от исходного уровня до возраста 13 недель контрольная группа и экспериментальная группа показали более низкое значение показателей z-score масса/возраст по сравнению с Нормами роста детей грудного вскармливания, разработанными ВОЗ. Для ITT группы значения показателя z-score ближе к показателями группы, вскармливаемой грудью, но никакая статистически значимая разница между этими двумя группами не предполагается (данные не показаны). В возрасте 17 недель отсутствуют статистически значимые различия между экспериментальной и контрольной группами и Нормами роста детей грудного вскармливания, разработанными ВОЗ. Но в возрасте 52 недель контрольная группа показывает значительно более высокое значение показателя z-score масса тела/возраста по сравнению со значениями z-score Норм роста детей грудного вскармливания, разработанными ВОЗ. Экспериментальная же группа на 52 неделе более похожа на контрольную группу грудного вскармливания, как показано перекрывающимися CI, и для обеих групп не предполагается отличий от Норм роста детей грудного вскармливания, разработанных ВОЗ. На фигуре 1 показаны результаты, полученные для ITT популяции по возрастной категории (при рождении, в возрасте 17 и 52 недель). Совокупность данных PP популяции показывает аналогичные результаты (данные не показаны). Интересно, что несмотря на то, эффекты имеют место как для девочек, так и для мальчиков, наибольший эффект наблюдается для мальчиков как в PP, так и в ITT популяции (данные не показаны).
В возрасте 52 недель разницу массы тела исследуемых групп сравнивают с использованием PGC анализа, принимая во внимание общий период исследования (от посещения для определения данных исходного уровня до 52 недель) и корректируя факторы стратификации. Результаты (в граммах за весь период), представленные в таблице 1, показывают, что как в ITT популяции, так и в РР популяции группы, получающей контрольную детскую смесь, масса тела выше, но нет статистически значимого различия массы тела по сравнению с группой, получающей экспериментальную смесь. Однако сравнение контрольной группы с контрольной группой грудного вскармливания показывает статистически значимую более высокую массу тела в контрольной группе для ITT и PP популяций, соответственно (оценка разности массы тела контрольной группы относительно массы тела группы грудного вскармливания 551,09 г (р=0,0009) для ITT популяции и 593,03 г (р=0,0009) для PP популяции). Сравнение экспериментальной группы с контрольной группой грудного вскармливания показывает большую массу тела в экспериментальной группе, которая статистически не различима для совокупности данных PP популяции (оценка разности массы тела 254,89 (р=0,1027)). По сравнению с контрольной группой экспериментальная группа ближе к группе грудного вскармливания.
Таблица 1: Различия в массе тела (граммы) детей в исследуемых группах в возрасте 52 недель согласно PGC анализу
|
PGC анализ, учитывающий общий период исследования (посещения для определения данных исходного уровня до 52 недель) и корректирующий факторы стратификации.
BMI
Среднее значение BMI для мальчиков и для девочек, включенных в три исследуемые группы, находятся в пределах значения z-score от -1 до +1 z-score показателей Норм роста детей грудного вскармливания, разработанных ВОЗ, для совокупности данных ITT и PP популяций (данные не показаны).
Средние значения z-score BMI/возраста и соответствующие доверительные интервалы при доверительной вероятности 0,95 показывают, что рост BMI в контрольной группе грудного вскармливания не отличается от Норм роста детей грудного вскармливания, разработанных ВОЗ. Для ITT группы в возрасте 17 недель нет статистически значимой разницы между контрольной группой и Нормами роста детей грудного вскармливания, разработанными ВОЗ, в то время как значение показателя z-score BMI экспериментальной группы ниже и статистически значимо отличается от Норм роста детей, вскармливающихся грудью, разработанных ВОЗ. Однако в возрасте 52 недель контрольная группа показывает значительно более высокий BMI для данного возраста по сравнению с Нормами роста детей грудного вскармливания, разработанными ВОЗ. С другой стороны, экспериментальная группа более близка к контрольной группе грудного вскармливания, как показывают перекрывающиеся CI, и для обеих групп отсутствует значимое отличие от Норм роста детей грудного вскармливания, разработанных ВОЗ. На фигуре 2 представлены результаты, полученные для совокупности данных ITT популяции. Совокупность данных PP популяции показывает аналогичные результаты (данные не показаны). Интересно, что эффекты имеют место как для девочек, так и мальчиков, однако наибольший эффект наблюдается для мальчиков как для PP, так и для ITT популяции (данные не показаны).
В возрасте 52 недель различие в BMI исследуемых групп сравнивают с использованием PGC анализа, принимая во внимание общий период исследования (от посещения для определения данных исходного уровня до возраста 12 месяцев) и корректируя факторы стратификации. Полученные результаты, представленные в таблице 2, показывают, что для совокупностей данных ITT и PP популяций группа, получающая контрольную детскую смесь, показывает самый высокий BMI, что статистически значимо отличается от группы, получающей экспериментальную смесь, и от контрольной группы грудного вскармливания. Сравнение экспериментальной группы с контрольной группой грудного вскармливания показывает большее, но статистически значимо не отличающее значение BMI в экспериментальной группе для ITT популяции и PP популяции.
Таблица 2: Различия значений BMI (кг/м2) детей в возрасте 52 недель в исследуемых группах согласно PGC анализу
|
PGC анализ, учитывающий общий период исследования (от посещения для определения данных исходного уровня до 52 недель) и корректирующий факторы стратификации.
Отношение массы тела к росту
Средние значения масса тела/рост для мальчиков и для девочек, включенных в три исследуемых группы, находятся в пределах значения z-score от -1 до +1 z-score Норм роста детей грудного вскармливания, разработанных ВОЗ, для совокупности данных ITT и PP популяций (данные не показаны).
В границе значений z-score BMI/возраст, ни одна из исследуемых групп не показывает значение показателя z-score масса тела/рост при рождении, который значительно отличается от Норм роста детей грудного вскармливания, разработанных ВОЗ. Средние значения z-score масса тела/роста опытной группы несколько ниже и значительно отличаются от Норм роста детей грудного вскармливания, разработанных ВОЗ, для возраста 17 недель. В возрасте 52 недель не наблюдаются различия между экспериментальной группой и Нормами роста детей, вскармливающихся грудью, разработанными ВОЗ. Напротив, средние значения z-score массы тел/рост контрольной группы в 52 недельном возрасте выше и значительно отличаются от Норм роста детей грудного вскармливания, разработанных ВОЗ. На фигуре 3 представлены результаты, полученные для совокупности данных ITT популяции. Совокупность PP данных показывает аналогичные результаты (данные не показаны). Интересно, что эффекты имели место как для девочек, так и мальчиков, однако наибольший эффект наблюдается для мальчиков как для PP, так и для ITT популяции (данные не показаны).
Следует отметить, что различия между группой, вскармливающейся контрольной смесью, и группой грудного вскармливания соответствуют наблюдениям, содержащимся в научной литературе, при сравнении детей, вскармливающихся грудью, с детьми, вскармливаемыми молочными смесями (Dewey et al., 1993, Am J Clin Nutr 57: 140-145). Все средние значения (массы тела, BMI, массы для роста, окружности головы и складок кожи) находятся в пределах диапазона нормальных здоровых детей, которые не подвержены риску ожирения.
Толщина кожной складки и окружность головы
Толщина кожной складки является неинвазивным показателем содержания жира в организме детей раннего возраста и является показателем развития организма. На 52 неделе измеряют толщину кожной складки над бицепсом, над трицепсом, над подвздошной костью и под лопаткой, и вычисляют сумму толщин этих кожных складок. Кожные складки контрольной группы грудного вскармливания (ITT популяция) были меньше над бицепсом, над трицепсом, над подвздошной костью и по сумме толщин кожных складок были больше подлопаточной кожной складки по сравнению с контрольной группой. Во всех случаях кожные складки экспериментальной группы являются промежуточными и ближе к контрольной группе грудного вскармливания по сравнению с контрольной группой. z-Показатель толщины кожной складки трицепса и подлопаточной кожной складки контрольной группы грудного вскармливания был самым близким к Нормам роста детей грудного вскармливания, разработанным ВОЗ, и толщины всех кожных складок у экспериментальной группы ближе к Нормам роста детей грудного вскармливания, разработанным ВОЗ, чем у контрольная группы.
Кроме того, показатель z-score окружность головы/возраст экспериментальной группы (ITT) очень близок к z-score контрольной группы грудного вскармливания и Норм роста детей грудного вскармливания, разработанных ВОЗ. С другой стороны, z-score контрольной группы (ITT) выше в возрасте 12 месяцев, чем у двух других групп, и значительно превосходит z-score Норм роста детей грудного вскармливания, разработанных ВОЗ.
Эти результаты показывают эффект детской смеси по стимулированию постнатальной кривой роста или развития организма ребенка до кривой роста или развития организма, которые близки к кривой роста или развитию организма, наблюдаемым у детей при вскармливании грудью, и/или на стимулирование постнатальной кривой роста или развития организма ребенка до кривой роста или развития организма, которые приближены к оптимальной кривой роста или оптимальному развитию организма согласно Нормам роста детей грудного вскармливания, разработанным ВОЗ. Кроме того, эти результаты показывают влияние детской смеси на улучшение постнатальной кривой роста или постнатального развития организма ребенка до кривой роста или развития организма, наблюдаемых при грудном вскармливании, в частности по сравнению с кривой роста или развития организма у детей, вскармливающихся детской смесью первого уровня или детской смесью второго уровня, не содержащей молочного жира или содержащей от 15 до 20% масс. пальмитиновой кислоты из расчета на общее количество жирных кислот, в которой менее 15% остатков пальмитиновой кислот находится в sn-2 положении триглицеридов. Полученные результаты показывают также эффект детской смеси на стимулирование сбалансированной кривой роста или сбалансированного развития организма ребенка и/или предотвращения или снижения риска несбалансированной кривой роста или развития организма ребенка.