Результат интеллектуальной деятельности: МАЛОИНВАЗИВНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ ЧУВСТВИТЕЛЬНОСТИ ОПУХОЛЕЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ К ЛУЧЕВОЙ ТЕРАПИИ НА ОСНОВАНИИ ИЗМЕНЕНИЯ КОПИЙНОСТИ ГЕНОВ BRCA2 И RAD50
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к молекулярной онкологии, и может быть использовано для малоинвазивного определения чувствительности опухолей предстательной железы к лучевой терапии.
Во всем мире рак предстательной железы (РПЖ) занимает лидирующие позиции в структуре онкологической патологии. В России рост заболеваемости за 10 лет превысил 140%, а смертности 45%, это самые высокие значения среди всей онкологической патологии (см. Зинькович М.С., Максимов А.Ю., Розенко Л.Я., Гусарева М.А., Карнаухова Е.А., Фаенсон А.В., Тимошкина Н.Н., Кутилин Д.С. Радиорезистентность как фактор эволюции лучевой терапии рака предстательной железы // Современные проблемы науки и образования. - 2019. - №2.; URL: http://www.science-education.ru/ru/article/view?id=28627 (дата обращения: 14.03.2019)). Устойчивый рост данных показателей делает как никогда актуальной задачу разработки новых методологических подходов к лечению данной патологии. Лучевая терапия является одним из основных методов лечения РПЖ. Облучение используется главным образом у пациентов с локализованными или местно-распространенными формами рака с противопоказаниями для хирургического вмешательства (см. Кутилин Д.С., Сагакянц А.Б., Зинькович М.С., Максимов А.Ю., Гусарева М.А., Бондаренко Е.С., Потемкин Д.С., Васильченко Н.Г. Влияние различных доз лучевой терапии на выживаемость опухолевых клеток предстательной железы линии РС-3 // Современные проблемы науки и образования. - 2019. - №2.; URL: http://science-education.ru/ru/article/view?id=28740 (дата обращения: 11.10.2019)).
Эффективность подобной терапии зависит от исходная радиорезистентности опухолевых клеток, которая обеспечивается определенными молекулярно-генетическими особенностями этих клеток (Ярмоненко С.П., Вайнсон А.А. Радиобиология человека и животных. М., 2004. 549 с). К подобным особенностям можно отнести показатель копийности генов (Copy Number Variation (CNV)) - вид генетического полиморфизма, результатом которого может явиться снижение или повышение числа копий определенного гена, и, следовательно, пониженная или повышенная экспрессия продукта гена - белка или не кодирующей РНК (Кутилин Д.С., Айрапетова Т.Г., Анистратов П.А., Пыльцин С.П., Лейман И.А., Карнаухов Н.С., Кит О.И. Изменение копийности генов в опухолевых клетках и внеклеточной ДНК у больных аденокарциномой легкого // Бюллетень экспериментальной биологии и медицины. - 2019. - Т. 167. - №6. - С. 731-738; Zarrei М., MacDonald J.R., Merico D., Scherer S.W. A copy number variation map of the human genome // Nature Reviews Genetics. - 2015. - №16(3). - PP. 172-83.).
CNV определяемые в операционном материале имеют высокий потенциал в качестве молекулярных предикторов чувствительности клеток опухоли к лучевой терапии. Однако этот потенциал ограничен высоким уровнем инвазивности при получении биоматериала. Возможное решение этой проблемы находится в переходе на исследование копийности генов во внеклеточной ДНК (внДНК) плазмы крови. К внДНК в организме относят: клеточную и митохондриальную ДНК из соматических и из опухолевых клеток, подвергающихся процессам апоптоза и некроза; ДНК из эритробластов, ядра которых энуклеируются в процессе дифференцировки в эритроциты, ДНК из лимфоцитов в процессе их апоптотической гибели после стимуляции, ДНК эмбрионов в крови матери, бактериальную и вирусную ДНК. При онкологических заболеваниях часто определяется повышенный уровень нДНК в периферической крови. При этом прогресс заболевания часто связан с постепенным повышением уровня внДНК. (см. Козлов В.А. Свободная внеклеточная ДНК в норме и при патологии. Медицинская иммунология. 2013, Т. 15, №5, с. 399-412).
Изменение числа копий генов BRCA2 и RAD50 ассоциировано с чувствительностью опухолевых клеток к лучевой терапии.
Продукт гена BRCA2 необходим для восстановления поврежденной ДНК. BRCA2 связывает одноцепочечную ДНК и напрямую взаимодействует с рекомбиназой RAD51, чтобы стимулировать важный этап гомологичной рекомбинации (см. Wang С.Х., Jimenez-Sainz J., Jensen R.B., Mazin A.V. The Post-Synaptic Function of Brca2 // Scientific Reports. - 2019. - V. 9(1). - P. 4554. doi: 10.1038/s41598-019-41054-у). Перемещение RAD51 к двухцепочечному разрыву ДНК требует образования комплекса BRCA1-PALB2-BRCA2 (см. Holloman W.K. Unraveling the mechanism of BRCA2 in homologous recombination // Nat. Struct. Mol. Biol. - 2011. - V. 18(7). P 748-54.). Также BRCA2 играет важную роль в защите от Mre11-зависимой нуклеолитической деградации реверсированных репликационных вилок, которые образуются при остановке вилки репликации ДНК, вызванной излучением (см. Mijic S., Zellweger R., Chappidi N., Berti M., Jacobs K., Mutreja K., Ursich. S, Ray Chaudhuri A., Nussenzweig A., Janscak P., Lopes M. Replication fork reversal triggers fork degradation in BRCA2-defective cells // Nature Communications. - 2017. - V. 8(1). - P. 859).
Белок, кодируемый геном RAD50 участвует в репарации двойных разрывов цепочки ДНК. Этот белок образует комплекс с MRE11 и NBS1. Этот комплекс MRN связывается с поврежденными концами ДНК и представляет многочисленные ферментативные активности, необходимые для репарации двойных разрывов цепи путем присоединения негомологичного конца или гомологичной рекомбинацией (см. Chen С, Wang Y, Mei JF, Li SS, Xu HX, Xiong HP, Wang XH, He X. Targeting RAD50 increases sensitivity to radiotherapy in colorectal cancer cells. Neoplasma. 2018; 65(1): 75-80. doi: 10.4149/neo_2018_170219N128).
Поэтому, в качестве маркеров для определения чувствительности опухолей предстательной железы к лучевой терапии допустимо использование показателя относительной копийности BRCA2 и RAD50.
Анализ патентных источников (www.fips.ru) показал отсутствие действующих патентов и заявок на «Малоинвазивный способ определения чувствительности опухолей предстательной железы к лучевой терапии на основании изменения копийности генов BRCA2 и RAD50», а также отсутствие изобретений, близких (подобных) нашему.
Техническим результатом заявляемого изобретения является создание нового, простого в исполнении, не дорогостоящего и точного способа с уникальными высокоспецифичными последовательностями синтетических олигонуклеотидов (праймеров) для определения чувствительности опухолей предстательной железы к лучевой терапии.
Сущность способа заключается в том, что образцы крови (10 мл крови и 3 мл 10 мМ фосфатного буфера, рН 7,5, с 0,15 М NaCl и 50 мМ ЭДТА) разделяют на плазму и фракцию клеток центрифугированием в течение 20 минут при 400 g при 15°С. Из плазмы крови выделяют внДНК фенол-хлороформным методом и проводят амплификацию с высокоспецифичными праймерами для генов BRCA2, RAD50 и GAPDH, анализируют первичные данные и вычисляют относительную копийность (rC) по формуле 2-ΔCt, где ΔCt=Ct(BRCA2 или RAD50) - Ct(GAPDH). Затем сравнивают полученные значения rC с прогностическими значениями копийности, и при значениях в интервале rCBRCA2>(497,9±5,1)*10-3 и rCRAD50>(12,6±0,4)*10-3 у пациента диагностируют радиорезистентную форму рака предстательной железы (чувствительность 90%, специфичность 91%), а при значениях в интервале rCBRCA2<(497,9±5,1)*10-3 и rCRAD50<(12,6±0,4)*10-3 у пациента определяют чувствительную к лучевой терапии форму рака предстательной железы (чувствительность 89%, специфичность 95%).
Заявленный анализ основан на определении количества копий генов BRCA2 и RAD50 относительно референсного гена GAPDH во внДНК плазмы крови больных раком предстательной железы, и последующем сравнении полученных значений с интервалом копийности rCBRCA2 и rCRAD50 характерным для радиорезистентной или чувствительной к лучевой терапии формы рака предстательной железы.
Заявленный способ включает следующие приемы:
• выделение внеклеточной ДНК из плазмы крови с помощью метода фенол-хлороформной экстракции;
• определение относительной копийности генетических локусов BRCA2 и RAD50 методом ПЦР-РВ в присутствии красителя EVA-Green и специфичных праймеров на матрице выделенной внДНК;
• анализ первичных данных с помощью программного продукта амплификатора;
• расчет относительной копийности гена (rC) на основании соотношения сигналов, продуцируемых амплификатами изучаемой и референсной последовательностей,
• сравнением rC пробы с прогностическими значениями копийности rCстандарт, определенными для радиорезистентной и чувствительной к лучевой терапии формы рака предстательной железы.
Для осуществления способа были разработаны специфичные олигонуклеотидные прямые и обратные праймеры для генов BRCA2, RAD50 и GAPDH. Дизайн специфичных олигонуклеотидных праймеров (таблица 1) осуществлялся с использованием референсных последовательностей NCBI GenBank.

Заявленный способ осуществляется следующим образом:
На первом этапе образцы крови (10 мл крови и 3 мл 10 мМ фосфатного буфера, рН 7,5, с 0,15 М NaCl и 50 мМ ЭДТА) разделяют на плазму и фракцию клеток центрифугированием в течение 20 минут при 400 g при 15°С. Из плазмы крови ДНК выделяют фенол-хлороформным методом в нашей модификации. К плазме крови добавляют равный объем лизирующего буфера (2% SDS и 1% меркаптоэтанол) и 20 мкл протеиназы К, инкубируют в термостате при 58°С 1 час. К полученному лизату добавляют равный объем щелочного фенола и хлороформа (соотношение 1:1), центрифугируют 20 минут 3000 об/мин. После разделения фаз отбирают водную фазу в отдельную стерильную пробирку. К водной фазе добавляют равный объем 95% изопропилового спирта и раствор 5М NaCl до концентрации 100 mM, пробирку помещают в холодильник на -20°С на 60 минут. Далее центрифугируют 15 минут при 12700 об/мин, при -10°С, декантируют супернатант, а осадок промывают 80% этиловым спиртом, центрифугированием удаляют остатки этанола, высушивают осадок в твердотельном термостате и растворяют в 10 мМ ТЕ буфере.
Амплификацию проводят в 20 мкл ПЦР-смеси, содержащей 3 нг внДНК, 0,20 мМ dNTPs, 2,5 мМ MgCl2, 1x ПЦР-буфер, 1x краситель EvaGreen, и 0,1 е.а./мкл реакционной смеси ДНК-полимеразы Thermus aquaticus, и по 500 нМ прямого и обратного праймеров для референсного гена или гена-мишени.
Количественную ПЦР-РВ амплификацию проводят на термоциклере по следующей программе: t=95°C в течение 3 мин. 40 циклов: t=95°C в течение 10 с, t=58°C (чтение сигнала) в течение 30 с, t=72°C в течение 30 с.
Относительная копийность генов BRCA2 и RAD50 вычисляется следующим образом:
- рассчитывается Ct для целевого (BRCA2 или RAD50) и референсного локуса (GAPDH),
- рассчитывается величина ΔCt=Ct(целевой локус) - Ct(референсный локус);
- рассчитывается копийность целевого локуса относительно референсного (rC) по формуле 2-ΔCt.
Полученные значения rC сравнивают с интервалом прогностического коэффициента копийности:
• при значениях rCBRCA2>(497,9±5,1)*10-3 и rCRAD50>(12,6±0,4)*10-3 у пациента диагностируют радиорезистентную форму рака предстательной железы,
• при значениях rCBRCA2<(497,9±5,1)*10-3 и rCRAD50<(12,6±0,4)*10-3 у пациента определяют чувствительную к лучевой терапии форму рака предстательной железы.
Предлагаемым способом было осуществлено обследование 20 пациентов, у которых был диагностирован рак предстательной железы. Для доказательства прогностической ценности предлагаемого способа приводятся две выписки из историй болезни.
1. Пациент С. 81 год.
Из анамнеза: 24.10.08 - радикальная простатэктомия (ОКБ №2). Гистологический анализ - билатеральная умеренно-дифференцированная аденокарцинома, опухоль врастает в капсулу, стенку семенных пузырьков. В лимфоузлах опухоли нет. При обследовании 29.01.18 отмечен рост ПСА до 5,1 нг/мл. Рекомендована гормональная терапия. МРТ (от 07.08.18) - МР-картина неравномерного утолщения цистуретрального анастомоза. Структурно соответствует рецидиву, размерами 14×17 мм.
На основании морфологического заключения, данных анамнеза и клинико-лабораторных данных установлен диагноз: (С61) Рак предстательной железы T3N0M0, St. III, состояние после хирургического лечения (2008), рецидив, кл. гр. 2.
В сентябре 2018 года в условиях отделения радиологии РНИОИ после предварительной компьютерно-томографической топометрической подготовки проведена дистанционная лучевая терапия на область тазовых лимфоузлов и ложе предстательной железы и семенных пузырьков на линейном ускорителе Novalis ТХ, Varian.
Перед началом лечения взята кровь для выделения внДНК. Результаты молекулярно-генетического анализа образцов внДНК: rCBRCA2=507,2*10-3 и rCRAD50=15,3*10-3 соответствуют прогностическим коэффициентам радиорезистентной формы рака предстательной железы.
Состояние при выписке: удовлетворительное, лучевых реакций нет.
Динамика показателя общего ПСА представлена в таблице 2:
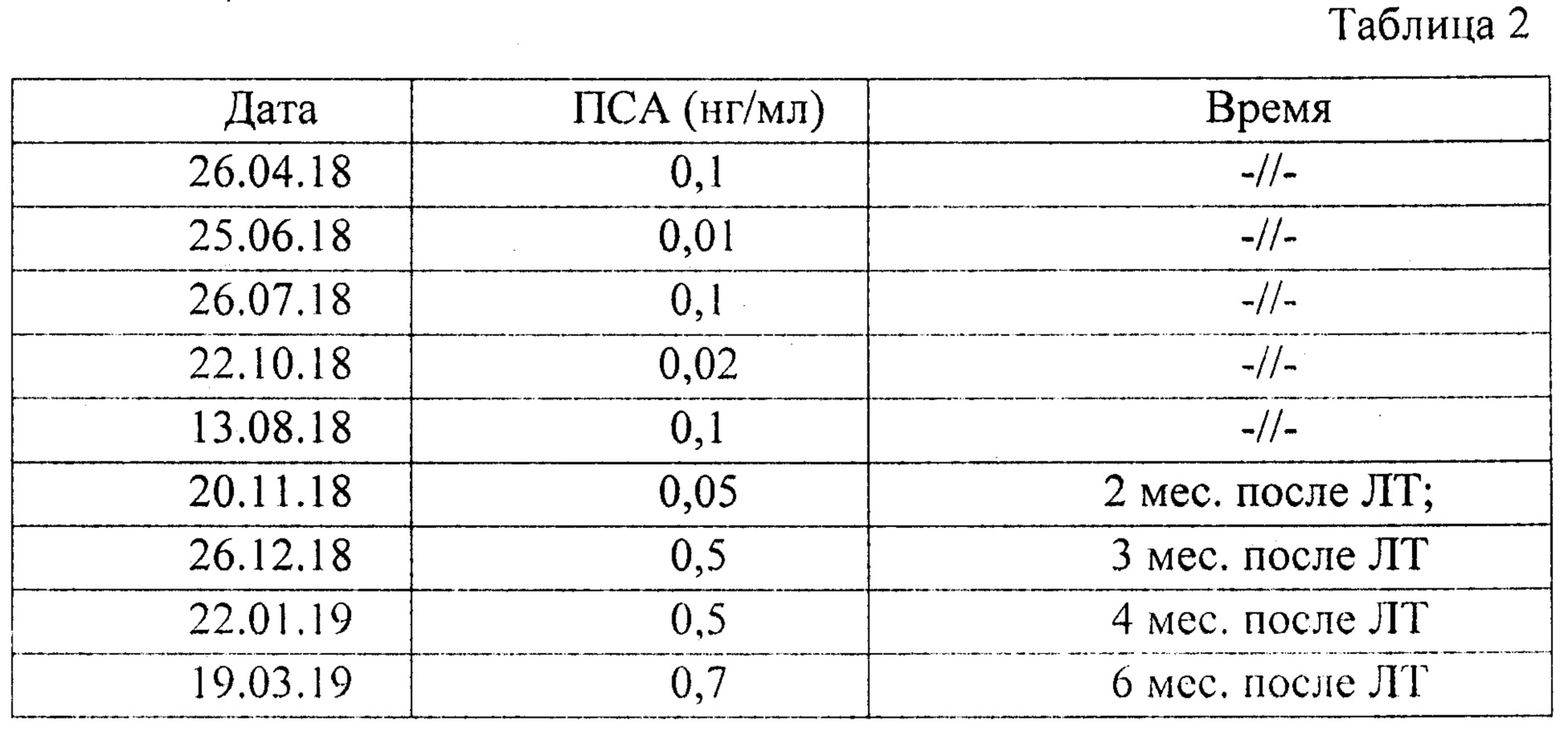
Как видно из представленных данных через 2 месяца после окончания лучевой терапии у пациента было отмечено снижение уровня ПСА в связи с чем была отменена гормональная терапия. Однако уже к 3 месяцу произошел резкий скачек ПСА, через месяц при контрольном исследовании показатель без динамики, однако к 6 месяцу отмечено продолжение роста ПСА. Ситуация расценена как биохимический рецидив, пациенту назначена гормональная терапия, на фоне которой отмечается снижение уровня ПСА. Таким образом, в данном случае мы видим отсутствие ожидаемого эффекта после проведенной лучевой терапии.
2. Пациент М. 83 года.
Из анамнеза: в сентябре 2018 г выявлено повышение ПСА до 5 нг/мл. УЗИ ОБП и ОМТ (13.09.18 г) - Умеренная гиперплазия, структурные изменения предстательной железы (4.0×3.6×4.2 см объем: 31.8 см3), объем остаточной мочи 8 мл. МРТ ОМТ (17.09.18 г) - MP-картина фокуса карциномы простаты слева с распространением за пределы капсулы.
02.10.2018 г выполнена трансректальная биопсия простаты. Г/а: в правой доле, в двух биоптатах - очаги ацинарной аденокарциномы. На основании морфологического заключения, данных анамнеза и клинико-лабораторных данных установлен диагноз: (C61) Рак предстательной железы T3aN0M0, St. III, кл. гр. 2.
Перед началом лечения взята кровь для выделения внДНК. Результаты молекулярно-генетического анализа образцов внДНК: rCBRCA2=300,5*10-3 и rCRAD50=5,9*10-3 соответствуют прогностическим коэффициентам чувствительной к лучевой терапии форме рака предстательной железы.
С 22.10. по 16.11.2018 г в условиях отделения радиологии РНИОИ после предварительной компьютерно-томографической топометрической подготовки проведен курс дистанционной лучевой терапии на линейном ускорителе Novalis ТХ, Varian на зону предстательной железы и семенных пузырьков. Состояние при выписке: удовлетворительное, лучевых реакций нет.
Динамика показателя общего ПСА представлена в таблице 3:

Как мы можем видеть, уже через 2 недели после лучевой терапии уровень ПСА снизился практически вдвое. К 5 месяцу был отмечено ярко выраженное снижение. При последнем клиническом осмотре 17.09.19 пациент чувствовал себя удовлетворительно, патологических реакций со стороны органов риска отмечено не было.
Заявляемый способ, включает разработанные нами синтетические олигонуклеотиды (праймеры) и является экономически оправданным для определения чувствительности опухолей предстательной железы к лучевой терапии, осуществляется в условиях стандартной лаборатории молекулярной биологии (ПЦР), без использования специального дорогостоящего оборудования; обладает высокой чувствительностью и специфичностью, осуществление анализа возможно с плазмой крови, занимает не более 4-5 часов.
--->
Перечень последовательностей
<110> Kutilin, Denis; Rostovskij nauchno-issledovatelskij onkologicheskij institut
<120> Low invasive method for determining the sensitivity of prostate tumors to radiation therapy based on changes in the copy number of BRCA2 and RAD50 genes
<140>RU2019135781
<141>2019-11-06
<160> 1
<210> 1
<211> 21
<212> DNA
<213> Homo sapiens
<400> 1
TGCATCCCTG TGTAAGTGCA T 21
<110> Kutilin, Denis; Rostovskij nauchno-issledovatelskij onkologicheskij institut
<120> Low invasive method for determining the sensitivity of prostate tumors to radiation therapy based on changes in the copy number of BRCA2 and RAD50 genes
<140>RU2019135781
<141>2019-11-06
<160> 2
<210> 1
<211> 22
<212> DNA
<213> Homo sapiens
<400> 1
ACGTACTGGG TTTTTAGCAA GC 22
<110> Kutilin, Denis; Rostovskij nauchno-issledovatelskij onkologicheskij institut
<120> Low invasive method for determining the sensitivity of prostate tumors to radiation therapy based on changes in the copy number of BRCA2 and RAD50 genes
<140>RU2019135781
<141>2019-11-06
<160> 3
<210> 1
<211> 20
<212> DNA
<213> Homo sapiens
<400> 1
TGGCTGGCAG GATCTTTTGG 20
<110> Kutilin, Denis; Rostovskij nauchno-issledovatelskij onkologicheskij institut
<120> Low invasive method for determining the sensitivity of prostate tumors to radiation therapy based on changes in the copy number of BRCA2 and RAD50 genes
<140>RU2019135781
<141>2019-11-06
<160> 4
<210> 1
<211> 20
<212> DNA
<213> Homo sapiens
<400> 1
GCTTAACTGA GGCCGAAGCA 20
<110> Kutilin, Denis; Rostovskij nauchno-issledovatelskij onkologicheskij institut
<120> Low invasive method for determining the sensitivity of prostate tumors to radiation therapy based on changes in the copy number of BRCA2 and RAD50 genes
<140>RU2019135781
<141>2019-11-06
<160> 5
<210> 1
<211> 19
<212> DNA
<213> Homo sapiens
<400> 1
GCTGAACGGG AAGCTCACT 19
<110> Kutilin, Denis; Rostovskij nauchno-issledovatelskij onkologicheskij institut
<120> Low invasive method for determining the sensitivity of prostate tumors to radiation therapy based on changes in the copy number of BRCA2 and RAD50 genes
<140>RU2019135781
<141>2019-11-06
<160> 6
<210> 1
<211> 21
<212> DNA
<213> Homo sapiens
<400> 1
GCAGGTTTTT CTAGACGGCA G 21
<---
Малоинвазивный способ определения чувствительности опухолей предстательной железы к лучевой терапии на основании изменения копийности генов BRCA2 и RAD50, включающий выделение внеклеточной ДНК из плазмы крови, заключающийся в том, что проводят определение копийности генов BRCA2 и RAD50 относительно референсного гена GAPDH методом ПЦР-РВ в присутствии красителя EVA-Green и высокоспецифичных праймеров: для BRCA2 SEQ ID NO 1 и SEQ ID NO 2, для RAD50 SEQ ID NO 3 и SEQ ID NO 4, для GAPDH SEQ ID NO 5 и SEQ ID NO 6 на матрице выделенной внДНК, рассчитывают относительную копийность гена (rC) по формуле rC=2, где Ct - медиана сигналов флюоресценции, ΔC=C(BRCA2 или RAD50) - C(GAPDH), и сравнивают полученные значения rC с прогностическим интервалом копийности, и при значениях rC>(497,9±5,1)*10 и rC>(12,6±0,4)*10 у пациента диагностируют радиорезистентную форму рака предстательной железы, а при значениях rC<(497,9±5,1)*10 и rC<(12,6±0,4)*10 у пациента определяют чувствительную к лучевой терапии форму рака предстательной железы.
