Результат интеллектуальной деятельности: Способ выделения и очистки нафтохиноновых противогрибковых антибиотиков астолидов А и В
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к области биотехнологии и химии природных соединений, а именно к способу получения биологически активных веществ, обладающих антифунгальной активностью и цитотоксичностью.
Предшествующий уровень техники
Микроорганизмы обладают высочайшей способностью к развитию резистентности к антибиотикам, что преставляет растущую угрозу в современном здравоохранении. Особенную тревогу вызывают грибковые патогены, которые вызывают смертельные инвазивные микозы, способы лечения которых ограничены тремя известными классами антибиотиков. Эти классы включают азолы, которые игибируют биосинтез эргостерола, эхинокандины, ингибирующие биосинтез клеточной стенки, и мембрано-активные полиены [Revie, N.M.; Iyer, K.R.; Robbins, N.; Cowen, L.E. Antifungal drug resistance: evolution, mechanisms and impact. Current Opinion in Microbiology 2018, 45, 70-76], причем темп возникновения резистентности к этому ограниченному числу антифунгальных препаратов в последнее время принимет беспрецедентный масштаб [Fisher, М.С.; Hawkins, N.J.; Sanglard, D.; Gurr, S.J. Worldwide emergence of resistance to antifungal drugs challenges human health and food security. Science 2018, 360, 739]. Таким образом, поиск новых антифунгальных препаратов и разработка лекарственных средств на их основе является крайне актуальной задачей.
Ранее был обнаружен новый штамм-продуцент нафтохиноновых антибиотиков астолидов А и В, обладающих выраженной противогрибковой активностью в отношении широкого спектра грибов и дрожжей [Alferova, V.A.; Novikov, R.A.; Bychkova, О.P.; Rogozhin, E.A.; Shuvalov, M.V.; Prokhorenko, I.A.; Sadykova, V.S.; Kulko, A.B.; Dezhenkova, L.G.; Stepashkina, E.A.; et al. Astolides A and B, antifungal and cytotoxic naphthoquinone-derived polyol macrolactones from Streptomyces hygroscopicus. Tetrahedron 2018, 74, 7442-7449]. Также был разработан метод культивирования штамма и метод выделения индивидуальных антибиотиков астолидов А и В [Патент RU 2 681 828 С1].
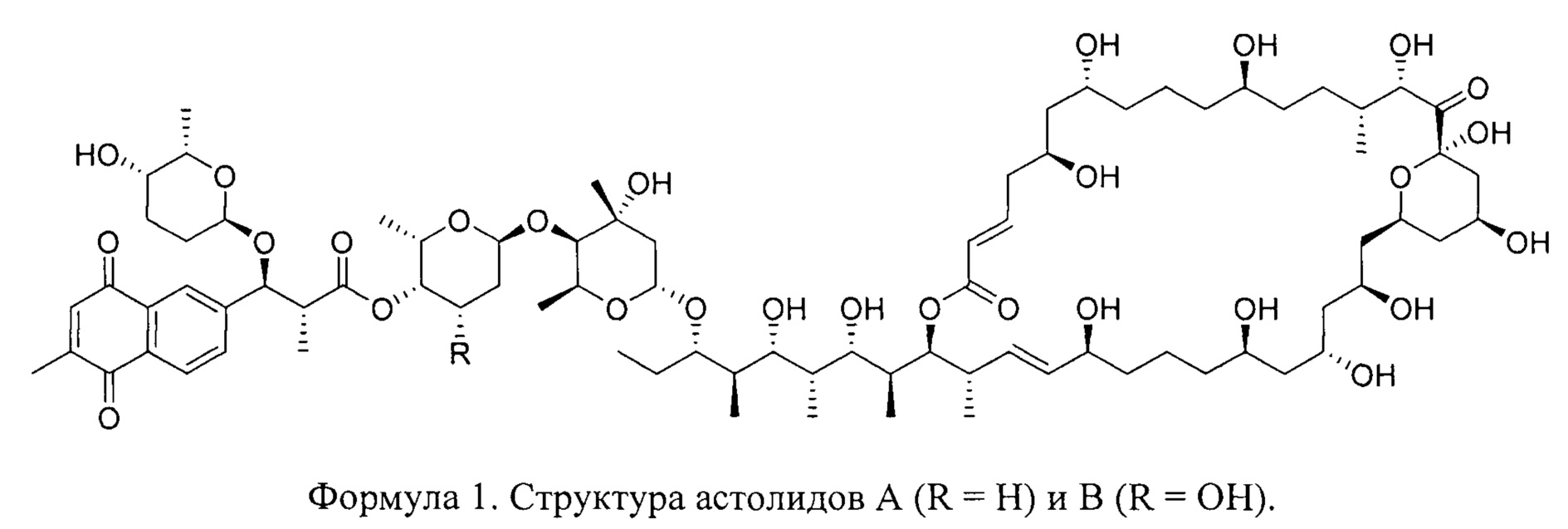
Астолиды А, В имеют структуру, изображенную на формуле 1, и принадлежат к классу нафтохиноновых полиольных макролидов [Алферова, В.А.; Шувалов, М.В.; Коршун, В.А.; Тюрин, А.П. Нафтохиноновые полиольные макролиды из природных источников. Известия Академии Наук. Серия Химическая 2018, 5, 955-966.]. Широкий спектр биологической активности - антипролиферативная, антифунгальная, противопаразитарная, иммуносупрессорная - позволяет рассматривать нафтохиноновые полиольные макролиды как перспективную основу для разработки соответствующих лекарственных средств. Благодаря своим необычным биологическим свойствам и структурым особенностям, антибиотики этого структурного класса вызывают существенный интерес в последние годы [ -Victoria, I.; Oves-Costales, D.; Lacret, R.; Martin, J.;
-Victoria, I.; Oves-Costales, D.; Lacret, R.; Martin, J.;  -Hidalgo, M. et al. Structure elucidation and biosynthetic gene cluster analysis of caniferolides A-D, new bioactive glycosylated 36-membered polyol macrolides from the marine-derived Streptomyces caniferus CA-271066. Org. Biomol. Chem. 2019, 17, 2954-2971; Takeuchi, Т.; Hatano, M.; Umekita, M.; Hayashi, C.; Wada, S.; Nagayoshi, M.; Sawa, R.; Kubota, Y.; Kawada, M.; Igarashi, M.; et al. ATP Depletion Assay Led to the Isolation of New 36-Membered Polyol Macrolides Deplelides A and В from Streptomyces sp.MM581-NF15. Org. Lett. 2017, 19, 4207-1210].
-Hidalgo, M. et al. Structure elucidation and biosynthetic gene cluster analysis of caniferolides A-D, new bioactive glycosylated 36-membered polyol macrolides from the marine-derived Streptomyces caniferus CA-271066. Org. Biomol. Chem. 2019, 17, 2954-2971; Takeuchi, Т.; Hatano, M.; Umekita, M.; Hayashi, C.; Wada, S.; Nagayoshi, M.; Sawa, R.; Kubota, Y.; Kawada, M.; Igarashi, M.; et al. ATP Depletion Assay Led to the Isolation of New 36-Membered Polyol Macrolides Deplelides A and В from Streptomyces sp.MM581-NF15. Org. Lett. 2017, 19, 4207-1210].
Раскрытие изобретения
Сущность изобретения заключается в новом способе извлечения антифунгальных антибиотиков астолидов А и В из культуры штамма-продуцента, включающем отделение мицелия, экстракцию мицелия с обработкой ультразвуком, жидкостно-жидкостную экстракцию водной фазы и флеш-хроматографию на обращенно-фазовом сорбенте с дальнейшей препаративной хроматографией.
Найденный метод обеспечивает более полное выделение антибиотиков из культуры штамма-продуцента. Средняя эффективность нового метода составляет 60-90% (суммарный выход вещества при выделении по отношению к содержанию в культуре), что позволяет использовать его для работы с низкопродуктивными линиями штамма-продуцента и отходами производства. При этом эффективность ранее описанного метода выделения не превышала 25%, в том числе из-за того, что мицелий не обрабатывался. В примерах 1-2 приведены данные для линий со сниженной продуктивностью (менее 20 мг/л); в примере 3 - для линии с нормальной продуктивностью (20-40 мг/л). Во всех случаях описанный препаративный подход показал свою применимость и высокую эффективность. Также следует отметить более простое аппаратурное оформление данного метода в сравнении с ранее описанным: он не требует использования высокоэффективной жидкостной хроматографии на заключительном этапе очистки, а позволяет ограничиться изократическим элюированием при среднем давлении.
Осуществление изобретения
Пример 1. Выделение астолидов из культуральной жидкости штамма Streptomyces hygroscopicus 18 (ВКПМ Ас2079)
По ранее описанной методике было получено 0,7 л культуры продуцента. После центрифугирования (4000g, 10 мин) водную фазу декантировали и экстрагировали н-бутанолом (2×200 мл). Мицелий (36 г сырой биомассы) суспендировали в метаноле (150 мл) и озвучивали на ультразвуковой бане (40 кГц, 60 Вт, 30 мин при температуре 25°С). Метанольный экстракт декантировали, упаривали в вакууме с помощью роторного испарителя. Экстракт из водной фазы также упаривали досуха в вакууме. Температура бани при упаривании не должна превышать 50°С, в противном случае наблюдается деградация антибиотика. Массы после упаривания: бутанольный экстракт - 0,44 г, спиртовой экстракт - 0,51 г.
Объединенные экстракты растворяли в минимальном количестве метанола и наносили на октадецил-силикагель (использовался сорбент Macherey-Nagel POLYGOPREP 100-50С18, колонка с внутр. диаметром 4 см, высота слоя сорбента 4 см) «сухим» способом: сорбент (10-15% общего количества) добавляли небольшими порциями к метанольному раствору, при перемешивании, затем полученную взвесь высушивали в вакууме роторного испарителя и наносили остаток ровным слоем на верх хроматографической колонки. Элюировали смесью ацетонитрила с водой (по 200 мл, содержащих 30, 45 и 60% ацетонитрила). Активные вещества содержались только во фракции с 60% ацетонитрила. Данную фракцию упаривали в вакууме до удаления ацетонитрила (темп, бани не выше 35°С), полученный водный раствор замораживали и лиофильно высушивали в вакууме.
Полученный концентрат массой 28 мг растворяли в 1 мл 50% ацетонитрила и хроматографировали на препаративной колонке Waters ХВridge Prep C18 5 μm OBD 19×150 мм, детекция по поглощению при 250 нм, элюент - 45% ацетонитрил в воде (изократическое элюирование), скорость потока - 6 мл/мин. Фракции, содержащие чистые астолиды А и Б, собирали отдельно, упаривали в вакууме до удаления ацетонитрила (темп, бани не выше 35°С), остаток замораживали и лиофильно высушивали. В результате получали 7,1 мг астолида А (чистота 98,5%), и 7.0 мг астолида Б (чистота 99,0%).
Пример 2. Выделение астолидов из культуральной жидкости штамма Streptomyces hygroscopicus 18 (ВКПМ Ас2079)
По ранее описанной методике было получено 1,0 л культуры продуцента. После центрифугирования (4000 g, 10 мин) водную фазу декантировали и экстрагировали изо-бутанолом (2×250 мл). Мицелий (45 г сырой биомассы) суспендировали в этаноле (200 мл) и озвучивали на ультразвуковой бане (40 кГц, 60 Вт, 30 мин при температуре 22°С). Этанольный экстракт декантировали с мицелия, упаривали в вакууме роторного испарителя. Экстракт из водной фазы также упаривали досуха в вакууме (температура бани при упаривании не должна превышать 50°С). Массы после упаривания: бутанольный экстракт - 0,81 г, спиртовой экстракт - 0,92 г.
Объединенные экстракты растворяли в минимальном количестве метанола и наносили на октадецил-силикагель (использовался сорбент Quingdao Hi-Tech BANGKAI 100А 40-60 мкм C18, колонка с внутр. диаметром 5 см, высота слоя сорбента 4 см) «сухим» способом как описано в Примере 1. Элюировали смесью ацетонитрила с водой (по 200 мл, содержащих 30, 45 и 60% ацетонитрила). Активные вещества содержались только во фракции с 60% ацетонитрила. Данную фракцию упаривали в вакууме до удаления ацетонитрила (темп, бани не выше 35°С), остаток замораживали и лиофилизовали.
Полученный концентрат массой 33 мг растворяли в 1 мл 50% ацетонитрила и хроматографировали на препаративной колонке Waters ХВ ridge Prep C18 5 μm OBD 19×150 мм, детекция по поглощению при 250 нм, элюент - 45% ацетонитрил в воде (изократическое элюирование), скорость потока - 6 мл/мин. Фракции, содержащие чистые астолиды А и Б, собирали отдельно, упаривали в вакууме до удаления ацетонитрила (темп, бани не выше 35°С), остаток замораживали и лиофилизовали. В результате получали 9,6 мг астолида А (чистота 98,7%), и 7,6 мг астолида Б (чистота 99,3%).
Пример 3. Выделение астолидов из культуральной жидкости штамма Streptomyces hygroscopicus 18 (ВКПМ Ас2079)
По ранее описанной методике было получено 1,1 л культуры продуцента. После центрифугирования (4000 g, 10 мин) водную фазу декантировали и экстрагировали н-бутанолом (2×250 мл). Мицелий (42 г сырой биомассы) суспендировали в этаноле (200 мл) и озвучивали на ультразвуковой бане (40 кГц, 60 Вт, 30 мин при температуре 24°С). При меньшем времени экстракции наблюдается заниженный выход антибиотика. Этанольный экстракт декантировали с мицелия, упаривали в вакууме роторного испарителя. Экстракт из водной фазы также упаривали досуха в вакууме. Температура бани при упаривании не должна превышать 50°С. Массы после упаривания: бутанольный экстракт - 0,77 г, спиртовой экстракт - 1,08 г.
Объединенные экстракты растворяли в минимальном количестве метанола и наносили на метилированный силикагель (использовался сорбент Merck Silanized silica С2 40-60 мкм, колонка с внутр. диаметром 5 см, длина слоя сорбента 4 см) «сухим» способом. Элюировали смесью ацетонитрила с водой (по 200 мл, содержащих 20, 35 и 50% ацетонитрила). Фракцию с 50% ацетонитрила упаривали в вакууме до удаления ацетонитрила (темп, бани не выше 35°С), остаток замораживали и лиофилизовали.
Полученный концентрат массой 56 мг растворяли в 2 мл 50% ацетонитрила и хроматографировали на препаративной колонке Waters XBridge Prep C18 5 μm OBD 19×150 мм, детекция при 250 нм, элюент - 42% ацетонитрил в воде (изократическое элюирование), скорость потока - 6 мл/мин. Фракции, содержащие чистые астолиды А и Б, собирали отдельно, упаривали в вакууме до удаления ацетонитрила (темп, бани не выше 35°С), остаток замораживали и лиофилизовали. В результате получено 9,8 мг астолида А (чистота 98,5%), и 20,4 мг астолида Б (чистота 99,5%).
Промышленная применимость
Изобретение может быть использовано для выделения астолидов А и В для применения в медицине и ветеринарии, в качестве лекарственного средства, а также в научно-исследовательских лабораториях.
Способ выделения и очистки нафтохиноновых противогрибковых антибиотиков астолидов А и В, отличающийся дополнительной экстракцией полярными органическими растворителями с ультразвуковой обработкой из мицелия штамма S. hygroscopicus ВКПМ Ас2079 сырца антибиотиков астолидов А и В, обогащением сырца антибиотиков астолидов А и В с помощью флеш-хроматографии на обращенно-фазовом сорбенте, разделением обогащенного сырца антибиотиков на индивидуальные антибиотики астолиды А и В путем препаративной хроматографии на обращенно-фазовой колонке при среднем давлении до 50 бар в изократических условиях.
