Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ПРОМЕЖУТОЧНОГО СОЕДИНЕНИЯ ДЛЯ ПОЛУЧЕНИЯ АВИБАКТАМА
Вид РИД
Изобретение
Область техники
[001] Настоящее изобретение относится к области фармацевтической биохимической инженерии, в частности, относится к способу получения промежуточного соединения для получения авибактама и, более конкретно, относится к способу получения (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида.
Уровень техники
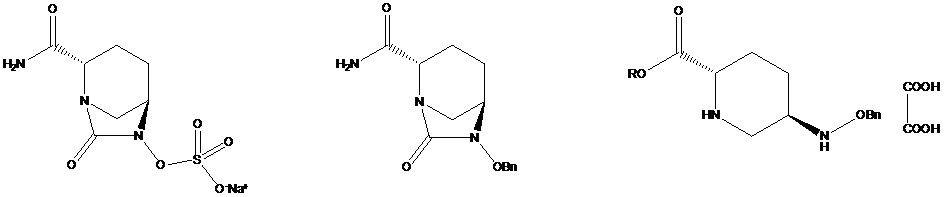
[002] Авибактам, поскольку он является одним из ингибиторов диазабициклооктаноновых соединений не на основе β-лактама, может ингибировать β-лактамазы типа A (в том числе ESBL и KPC) и типа C. При введении в комбинации с различными типами антибиотиков, представляющих собой цефалоспорины и карбапенем, авибактам обладает активностью широкого спектра действия в отношении бактерий, в частности, обладает значительной активностью в отношении Escherichia coli и Klebsiella pneumoniae, содержащих расширенный спектр β-лактамаз, Escherichia coli, содержащей избыточное количество фермента AmpC, и Escherichia coli, содержащей как AmpC, так и расширенный спектр β-лактамаз. Авибактам (I), характеризующийся номером CAS № 1192491-61-4 и химическим названием [(1R,2S,5R)-2-(аминокарбонил)-7-оксо-1,6-диазабицикло[3.2.1]окт-6-ил]сульфат натрия, характеризуется структурной формулой, представленной на формуле I:
|
[003] В патентных литературных источниках CN 103649051 A, CN 105294690 A, CN 106866668 A, WO 2012086241, US 8148540, US 9284273 и US 9567335 авибактам (I) во всех случаях получали с применением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II) в качестве промежуточного соединения. Осуществляли дебензилирование (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II) при катализе с помощью палладия на угле в присутствии различных восстановителей (таких как водород, триэтилсилан, формиат натрия и гидрат гидразина), затем осуществляли сульфатирование с помощью комплекса триоксида серы, и преобразовывали продукт в солевую форму четвертичного аммония с последующим ионным обменом с получением авибактама (I), как показано на схеме 1.
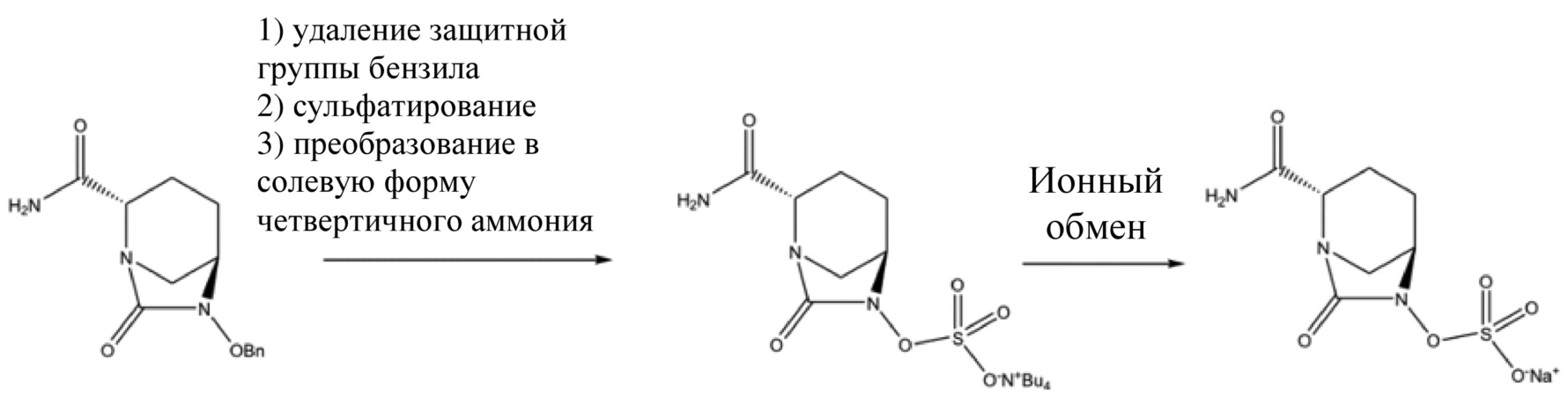
Схема 1
[004] Различные способы получения (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II) главным образом делятся на две схемы: амидирование с последующей циклизацией мочевины и циклизация мочевины с последующим амидированием, как показано на схеме 2.
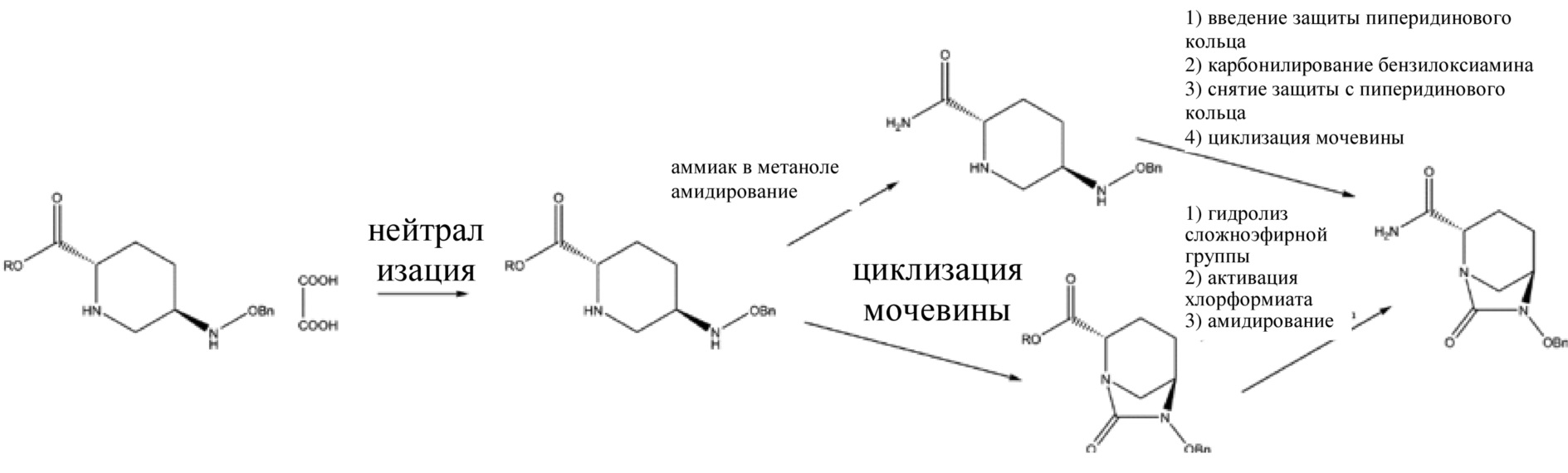
Схема 2
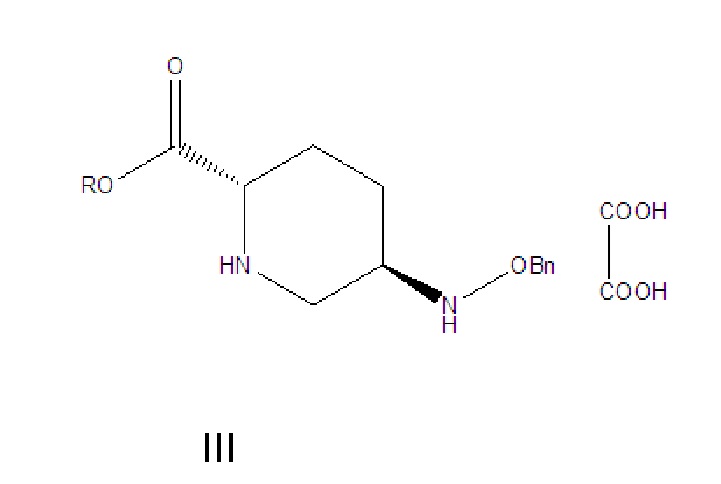
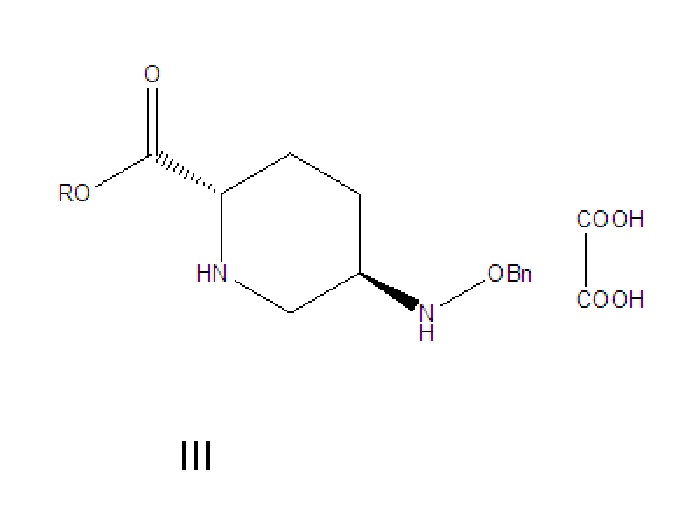
[005] В патентах CN 103649051 A и CN 105294690 A применяется схема амидирования с последующей циклизацией мочевины. 5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалат (III) в качестве исходного вещества амидировали в метанольном растворе газообразного аммиака или в водном растворе аммиака в спирте, и реакционную смесь фильтровали для удаления оксалата аммония; осадок на фильтре, представляющий собой оксалат аммония, промывали метанолом, и полученный метанольный раствор концентрировали; продукт экстрагировали с помощью метилбензола и перекристаллизовывали с использованием подходящего растворителя с получением (2S,5R)-5-[(бензилокси)амино]пиперидин-2-карбоксамида (выход: 68-99%); затем проводили реакцию карбонилирования с участием карбонилдиимидазола и бензилосиламина в присутствии защитной группы при аминогруппе в пиперидиновом кольце полученного (2S, 5R)-5-[(бензилокси)амино]пиперидин-2-карбоксамида с помощью 9-фторенилметилхлорформиата (FMOC-CI), и после удаления защитной группы в пиперидиновом кольце с помощью диэтиламина проводили циклизацию мочевины с получением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II) (выход: 90%, общий выход: 61,2-89,1%). В данном способе получения обработка после амидирования осложнена, и защитное средство, представляющее собой 9-фторенилметилхлорформиат, применяемое для циклизации мочевины, является дорогостоящим. Кроме того, 9-фторенилметилхлорформиат и карбонилдиимидазол обеспечивают только один карбонил, так что реакция характеризуется низкой атомной эффективностью, что не способствует защите окружающей среды и снижению затрат. Дополнительно, прямая циклизация мочевины в отношении (2S, 5R)-5-[(бензилокси)амино]пиперидин-2-карбоксамида с применением трифосгена и карбонилдиимидазола без введения защитной группы для аминогруппы в пиперидиновом кольце характеризовалась низким выходом (50-56%) с отсутствием промышленного значения.
[006] Помимо этого, все из патентов CN 102834395 A, CN 103649051 A, CN 103328476 A, CN 106279163 A, CN 106565712 A, US 9284273 и US 9567335 относятся к способу циклизации мочевины с последующим амидированием. Осуществляли циклизацию мочевины в отношении 5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) в качестве исходного вещества с применением трифосген-органического основания, карбонилдиимидазола или других средств карбонилирования, затем гидролизовали в щелочной среде, такой как водный раствор гидроксида лития, с получением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоновой кислоты; затем карбоксил активировали до ангидрида с применением триметилацетилхлорида или других средств, и затем ангидрид амидировали с применением водного раствора аммиака с получением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II) с общим выходом 34,5-65,5%. (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-формиат, полученный циклизацией мочевины, характеризуется низкой реакционной способностью, и его невозможно непосредственно амидировать в метанольном растворе газообразного аммиака. Вместо этого, для эффективного амидирования сложноэфирную группу необходимо гидролизовать до карбоксила, и затем карбоксил активируют до ангидрида. Данный способ предусматривает трудоемкую рабочую процедуру и низкую атомную эффективность, что, таким образом, не способствует защите окружающей среды и осуществлению промышленного производства.
Краткое описание
[007] Для устранения недостатков предшествующего уровня техники, в настоящем изобретении предусмотрен способ получения промежуточного соединения для получения авибактама, а именно (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II). Исходный материал для настоящего изобретения является недорогим и легкодоступным; способ получения является простым и в высокой степени пригодным к применению без необходимости в специальном защитном средстве или реагенте для карбонилирования; кроме того, реакция характеризуется высокой атомной эффективностью и низкой стоимостью; способ получения является экологичным и безвредным для окружающей среды; полученный в результате продукт (II) характеризуется высоким показателем чистоты и высоким выходом; полученный в результате 2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамид (II) можно применять для получения авибактама (I).
[008] Определение терминов:
[009] соединение формулы III: 5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалат, где -Bn означает бензил;
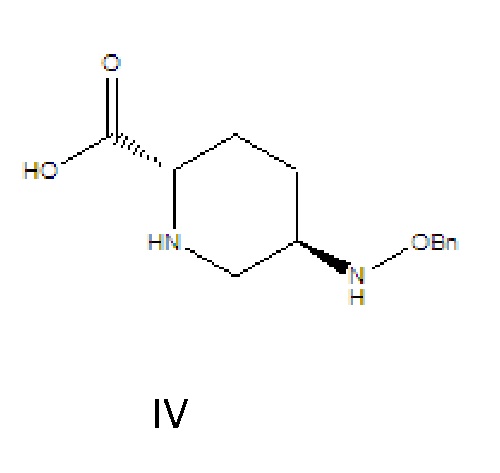
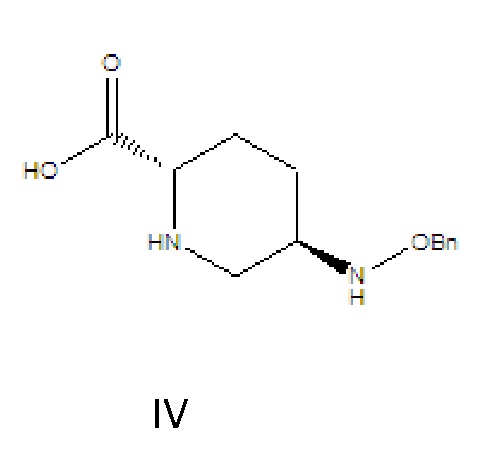
[0010] соединение формулы IV: 5R-[(бензилокси)амино]пиперидин-2S-карбоновая кислота, где -Bn означает бензил;
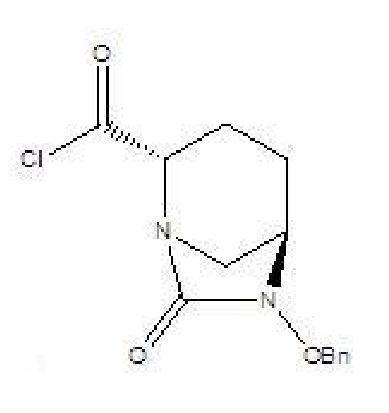
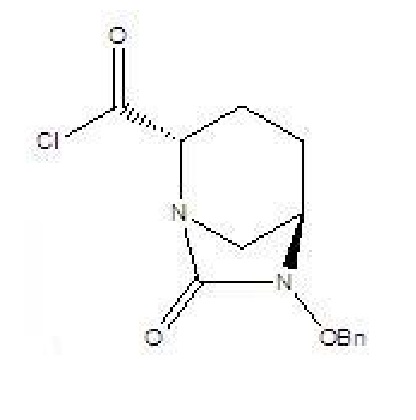
[0011] соединение формулы V: (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-формилхлорид, где -Bn означает бензил.
[0012] Номера соединений в описании полностью соответствуют номерам их структурных формул, и они имеют одни и те же ссылки.
[0013] Техническое решение в соответствии с настоящим изобретением представлено ниже.
[0014] Способ получения промежуточного соединения для получения авибактама, предусматривающий следующие стадии, на которых:
[0015] (1) соединение формулы III растворяют в растворителе A, гидролизуют в присутствии основания A и затем подкисляют с получением соединения формулы IV;
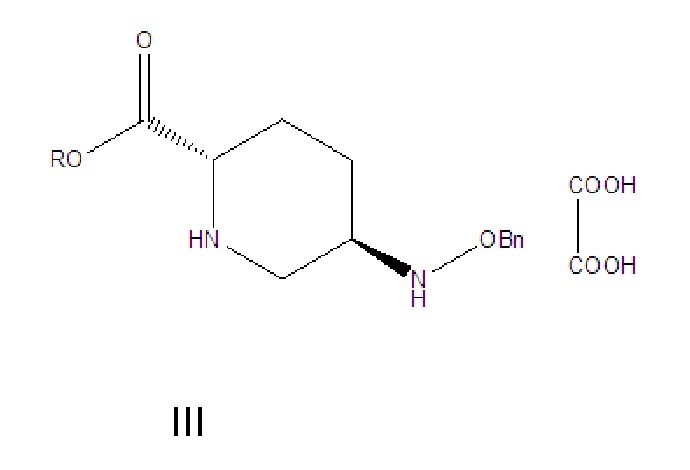
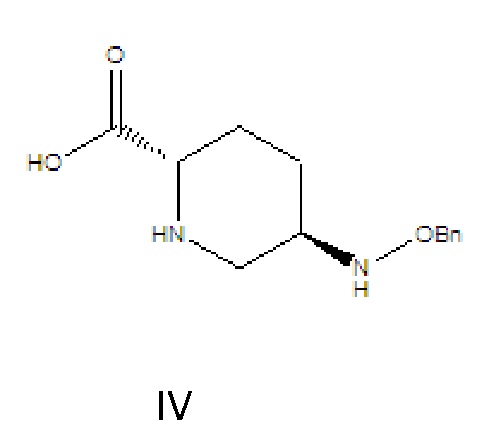
[0016] где R в соединении формулы III означает C1-6-алифатическую группу или -алкилзамещенный фенил; предпочтительно R выбран из группы, состоящей из метила, этила, н-пропила, изопропила, н-бутила, изобутила, трет-бутила, н-пентила, изопентила, трет-пентила, гексила, бензила, о-метилбензила и п-метилбензила;
[0017] 2) соединение формулы IV и твердый фосген или дифосген параллельно вводят в реакцию циклизации мочевины и реакции хлорформилирования в присутствии органического основания B и катализатора в растворителе B с получением соединения формулы V, которое применяли непосредственно на следующей стадии реакции без очистки;
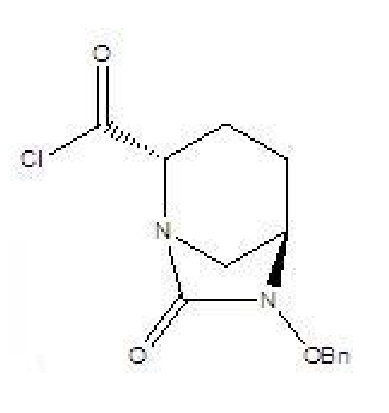
V
[0018] (3) проводят реакцию амидирования с участием соединения формулы V и аммиака с получением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II).
[0019] В соответствии с настоящим изобретением, предпочтительно после гидролиза соединения формулы III на стадии (1) в щелочной среде и его подкисления получают экстракт, содержащий соединение формулы IV, с применением экстрагирующего средства; экстракт, содержащий соединение формулы IV, подвергают перегонке с удалением экстрагирующего средства с получением соединения формулы IV, или экстракт, содержащий соединение формулы IV, непосредственно применяют на следующей стадии реакции без перегонки.
[0020] Предпочтительно, в соответствии с настоящим изобретением, растворитель A на стадии (1) выбран из группы, состоящей из дихлорметана, 1,2-дихлорэтана, трихлорметана, тетрахлорметана, тетрагидрофурана, 2-метилтетрагидрофурана, метоксициклопентана, метилбензола и комбинаций из двух или более из них.
[0021] Предпочтительно, в соответствии с настоящим изобретением, на стадии (1) массовое соотношение растворителя A и соединения формулы III составляет 3-4,5:1.
[0022] Предпочтительно, в соответствии с настоящим изобретением, используемое на стадии (1) основание A выбрано из группы, состоящей из гидроксида натрия, гидроксида калия, гидроксида лития, карбоната калия, карбоната натрия, гидрокарбоната калия, гидрокарбоната натрия и смеси двух или более из них; предпочтительно основание A представляет собой водный раствор, содержащий основание при концентрации 5-15% по массе.
[0023] Предпочтительно, в соответствии с настоящим изобретением, на стадии (1) молярное соотношение основания A и соединения формулы III составляет 2,0-5,0:1.
[0024] Предпочтительно, в соответствии с настоящим изобретением, на стадии (1) реакцию гидролиза осуществляют при температуре 0-80°C; на стадии (1) реакцию гидролиза предпочтительно осуществляют при температуре 10-40°C. Длительность реакции составляет 2-5 часов.
[0025] Предпочтительно на стадии (1) подкисление осуществляют при температуре 20-25°C в течение 1-2 часов.
[0026] Предпочтительно на стадии (1) подкисление предусматривает регулирование значения pH системы до 2-3 с применением подкисляющего средства, при этом подкисляющее средство представляет собой водный раствор хлористоводородной кислоты, серной кислоты или азотной кислоты при концентрации 10-40% по массе.
[0027] Предпочтительно на стадии (2) растворитель B выбран из группы, состоящей из дихлорметана, 1,2-дихлорэтана, трихлорметана, тетрахлорметана, тетрагидрофурана, 2-метилтетрагидрофурана, метоксициклопентана, метилбензола и комбинаций из двух или более из них.
[0028] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) массовое соотношение растворителя B и соединения формулы IV составляет 4-20:1.
[0029] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) органическое основание B выбрано из группы, состоящей из триэтиламина, три-н-бутиламина, диизопропилэтиламина и комбинаций из двух или более из них.
[0030] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) молярное соотношение органического основания B и соединения формулы IV составляет 3,0-8,0:1.
[0031] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) катализатор выбран из группы, состоящей из N, N-диметилформамида, пиридина, 4-диметиламинопиридина и комбинаций из двух или более из них.
[0032] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) катализатор присутствует в количестве 0,1-5,0% по массе соединения формулы IV.
[0033] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) молярное соотношение твердого фосгена или дифосгена и соединения формулы IV составляет 0,6-2,5:1.
[0034] Предпочтительно, в соответствии с настоящим изобретением, молярное соотношение твердого фосгена и соединения формулы IV составляет 0,6-2,0:1.
[0035] Предпочтительно, в соответствии с настоящим изобретением, молярное соотношение дифосгена и соединения формулы IV составляет 1,0-2,5:1.
[0036] Предпочтительно, в соответствии с настоящим изобретением, на стадии (2) как реакцию циклизации мочевины, так и реакцию хлорформилирования предпочтительно осуществляют при температуре −20-60°C; на стадии (2) как реакцию циклизации мочевины, так и реакцию хлорформилирования осуществляют при температуре 0-40°C. Длительность реакции составляет 1-8 часов.
[0037] Предпочтительно, в соответствии с настоящим изобретением, на стадии (3) соединение аммония выбрано из группы, состоящей из аммиака, раствора газообразного аммиака в метаноле или водного раствора аммиака.
[0038] Предпочтительно, в соответствии с настоящим изобретением, на стадии (3) молярное соотношение аммиака и соединения формулы IV составляет 1,0-5,0:1.
[0039] Предпочтительно, в соответствии с настоящим изобретением, на стадии (3) реакцию амидирования осуществляют при температуре −20-80°C; на стадии (3) реакцию амидирования предпочтительно осуществляют при температуре 10-50°C. Длительность реакции составляет 1-6 часов.
[0040] В соответствии с настоящим изобретением, 5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалат (III) в качестве исходного материала гидролизуют в щелочной среде, затем окисляют с получением 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV) и полученное соединение формулы IV и твердый фосген или дифосген одновременно вводят в реакцию циклизации мочевины и хлорформилирования в присутствии органического основания и катализатора с получением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-формилхлорида (V), который затем амидируют с получением (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II), при этом реакции циклизации мочевины, хлорформилирования и амидирования осуществляют посредством “однореакторного” способа, и промежуточные продукты не нужно разделять и очищать. Схема (схема 3) представлена ниже.
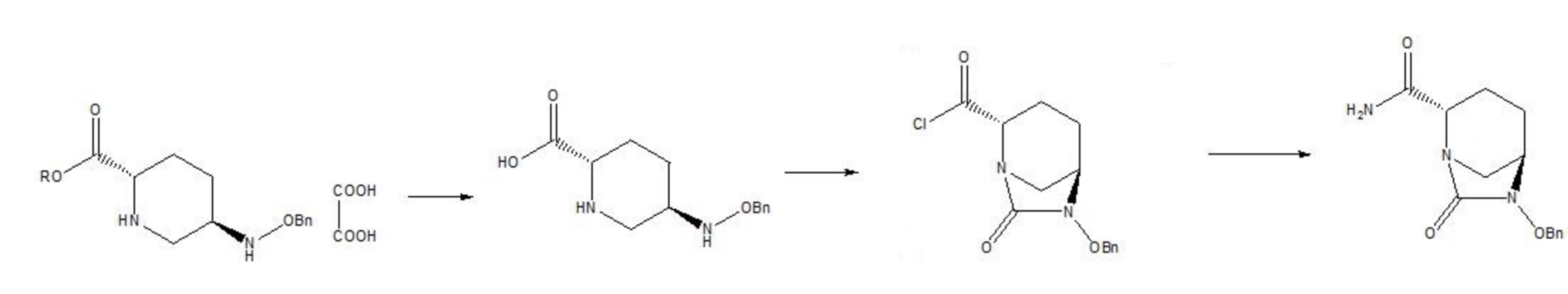
|
Схема 3
[0041] В настоящем изобретении предусмотрены следующие преимущественные эффекты.
[0042] 1. По сравнению с предшествующим уровнем техники, в настоящем изобретении отсутствуют недостатки способа амидирования с последующей циклизацией мочевины, для которого необходимы защита пиперидинового кольца и применение специфического реагента для карбонилирования, и дополнительно отсутствуют трудоемкие операции циклизации мочевины с последующим амидированием, для чего необходимы гидролиз сложноэфирной группы, активация с образованием ангидрида и амидирование. В настоящем изобретении применяется «однореакторный» способ реакций циклизации мочевины, хлорформилирования и амидирования, и промежуточные продукты не нужно подвергать последующим видам обработки, таким как разделение и очистка; способ предусматривает простые стадии, экологичные и безвредные для окружающей среды процедуры и низкую стоимость.
[0043] 2. В настоящем изобретении применяется недорогой и легкодоступный исходный материал, и типы применяемых реакций являются типичными реакциями; условия реакции являются легко контролируемыми; операции являются простыми; пригодность к применению является высокой; способ является простым. В способе циклизации мочевины не требуется специальная защита или реагент для карбонилирования; реакция характеризуется высокой атомной эффективностью; способ получения является экологичным и безвредным для окружающей среды; продукт, получаемый в результате циклизации мочевины, характеризуется соответствующей активностью, при этом он может быть амидирован с помощью газообразного аммиака, водного раствора аммиака и т. д., так что стадии являются простыми, и стоимость является низкой. Кроме того, (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамид (II), полученный в соответствии со способом по настоящему изобретению, характеризуется высокими показателями чистоты и выхода, что способствует снижению стоимости и экологичному получению авибактама (I).
Примеры
[0044] Далее в данном документе настоящее изобретение будет подробно проиллюстрировано со ссылкой на примеры; однако настоящее изобретение не ограничено ими.
[0045] Если не указано иное, все значения процентного содержания в примерах означают массовые процентные доли.
[0046] Исходный материал, представляющий собой 5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалат (III), является коммерчески доступным (от фармацевтической компании Jinan Qinsi), при этом он представляет собой белый порошок с оптической чистотой, составляющей 99,6%.
[0047] Протекание реакции и чистоту продукта контролируют с помощью газового хроматографа или жидкостного хроматографа. Жидкостный хроматограф, оснащенный хиральной колонкой (ES-OVS, 150 мм x 4,6 мм, Agilent), применяют для определения оптической чистоты (отношение значений площади %) и расчета выхода, а также % значения энантиомерной чистоты.
Пример 1. Получение 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV)
[0048] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г дихлорметана, 150 г 10% (по массе) водного раствора гидроксида натрия, 43,0 г (0,1 моль) бензил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-30°C в течение 3 часов. Затем реакционную смесь подкисляли до значения pH 2,5-3,0 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и один раз промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы получали 24,5 г 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты с выходом 98,0% и чистотой 99,9%, определенными с помощью HPLC.
[0049] Данные ЯМР (ядерного магнитного резонанса) полученного продукта приведены ниже: 1H-ЯМР (400 МГц, DMSO-d6), δ: 1,10 (1H, q), 1,27 (1H, q), 1,82 (2H, d), 2,23 (1H, t), 2,76 (1H, m), 2,90 (1H, d), 3,13 (1H, d), 4,70 (2H, s), 6,54 (1H, d), 7,35 (5H, m), 13,51 (1H, br).
Пример 2. Получение 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV)
[0050] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г 1,2-дихлорэтана, 80 г 10% (по массе) водного раствора гидроксида лития, 43,0 г (0,1 моль) бензил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-25°C в течение 4 часов. Затем реакционную смесь подкисляли до значения pH 2,5-3,0 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали 1,2-дихлорэтаном (каждый раз по 50 г). Органические фазы объединяли и один раз промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы получали 24,6 г 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты с выходом 98,5% и чистотой 99,9%, определенными с помощью HPLC.
Пример 3. Получение 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV)
[0051] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г дихлорметана, 120 г 10% (по массе) водного раствора гидроксида натрия, 37,0 г (0,1 моль) этил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-25°C в течение 4 часов. Затем реакционную смесь подкисляли до значения pH 2,5-3,0 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и один раз промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы получали 24,1 г 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты с выходом 96,4% и чистотой 99,9%, определенными с помощью HPLC.
Пример 4. Получение 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV)
[0052] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г дихлорметана, 150 г 10% (по массе) водного раствора гидроксида натрия, 39,5 г (0,1 моль) трет-бутил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-30°C в течение 3 часов. Затем реакционную смесь подкисляли до значения pH 2,5-3,0 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и один раз промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы получали 24,3 г 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты с выходом 97,2% и чистотой 99,9%, определенными с помощью HPLC.
Пример 5. Получение (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II)
[0053] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 200 г тетрагидрофурана, 12,5 г (0,05 моль) 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты, полученной в примере 2, 50 г три-н-бутиламина и 0,1 г N,N-диметилформамида. После охлаждения добавляли по каплям раствор 23,8 г (0,08 моль) твердого фосгена в 80 г тетрагидрофурана при −10-0°C. После завершения добавления реакционную смесь перемешивали при 10-20°C в течение 4 часов. Вводили 3,0-3,5 г газообразного аммиака при 10-20°C. Затем реакционную смесь перемешивали при 15-20°C в течение 3 часов. Реакционную жидкость выливали в 300 г смеси воды и льда и разделяли и затем водную фазу дважды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и дважды промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы добавляли 10,0 г холодного хлорбутана; затем смесь растирали, промывали и фильтровали с получением 12,6 г (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло [3.2.1] октан-2-карбоксамида с выходом 91,6% и чистотой 99,9%, определенными с помощью HPLC.
[0054] Данные ЯМР (ядерного магнитного резонанса) полученного продукта приведены ниже: 1H-ЯМР (400 МГц, DMSO-d6), δ: 1,65 (2H, m), 1,84 (1H, br), 2,06(1H, m), 2,90 (2H, s), 3,62 (1H, s), 3,68 (1H, d), 4,93 (2H, dd), 7,30-7,46 (7H, m).
Пример 6. Получение (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II)
[0055] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 200 г дихлорметана, 12,5 г (0,05 моль) 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты, полученной в примере 2, 60 г диизопропилэтиламина и 0,1 г N,N-диметилформамида. После охлаждения добавляли по каплям раствор 23,8 г (0,08 моль) твердого фосгена в 80 г дихлорметана при −10-0°C. После завершения добавления реакционную смесь перемешивали при 10-20°C в течение 4 часов. Добавляли 25 г 10% (по массе) раствора газообразного аммиака в метаноле при 10-20°C. Затем реакционную смесь перемешивали при 15-20°C в течение 3 часов. Реакционную жидкость выливали в 300 г смеси воды и льда и разделяли и затем водную фазу дважды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и дважды промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы добавляли 10,0 г холодного хлорбутана; затем смесь растирали, промывали и фильтровали с получением 12,7 г (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло [3.2.1] октан-2-карбоксамида с выходом 92,5% и чистотой 99,9%, определенными с помощью HPLC.
Пример 7. Получение (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II)
В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 200 г дихлорметана, 12,5 г (0,05 моль) 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты, полученной в примере 2, 60 г диизопропилэтиламина и 0,1 г N,N-диметилформамида. После охлаждения добавляли по каплям раствор 24,0 г (0,12 моль) дифосгена в 60 г дихлорметана при −10-0°C. После завершения добавления реакционную смесь перемешивали при 20-25°C в течение 3 часов. Добавляли 25 г 10% (по массе) раствора газообразного аммиака в метаноле при 20-25°C. Затем реакционную смесь перемешивали при 20-25°C в течение 3 часов. Реакционную жидкость выливали в 300 г смеси воды и льда и разделяли и затем водную фазу дважды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и дважды промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы добавляли 10,0 г холодного хлорбутана; затем смесь растирали, промывали и фильтровали с получением 12,5 г (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло [3.2.1] октан-2-карбоксамида с выходом 91,0% и чистотой 99,9%, определенными с помощью HPLC.
Пример 8. Получение (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II)
[0056] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 200 г дихлорметана, 12,5 г (0,05 моль) 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты, полученной в примере 2, 40 г триэтиламина и 0,1 г N,N-диметилформамида. После охлаждения добавляли по каплям раствор 23,8 г (0,08 моль) твердого фосгена в 80 г дихлорметана при −10-0°C. После завершения добавления реакционную смесь перемешивали в течение 4 часов при температуре 10-20°C. Добавляли 25 г 10% (по массе) водного раствора аммиака при 10-20°C. Затем реакционную смесь перемешивали при 15-20°C в течение 3 часов. Реакционную жидкость выливали в 200 г смеси воды и льда и разделяли и затем водную фазу дважды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и дважды промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы добавляли 10,0 г холодного хлорбутана; затем смесь растирали, промывали и фильтровали с получением 12,1 г (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло [3.2.1] октан-2-карбоксамида с выходом 88,0% и чистотой 99,8%, определенными с помощью HPLC.
Пример 9. Получение (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло[3.2.1]октан-2-карбоксамида (II)
[0057] При получении 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV) смешанную жидкость полученной органической фазы непосредственно подвергали следующим стадиям.
[0058] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г дихлорметана, 120 г 10% (по массе) водного раствора гидроксида натрия, 37,0 г (0,1 моль) этил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-25°C в течение 4 часов. Затем реакционную смесь подкисляли до значения pH 2,5-3,0 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли с получением смешанного раствора органических фаз.
[0059] Полученный смешанный раствор органической фазы переносили в другую 4-горлую колбу объемом 500 мл, в которую загружали 60 г диизопропилэтиламина и 0,1 г N,N-диметилформамида. После охлаждения добавляли по каплям раствор 26,7 г (0,09 моль) твердого фосгена в 80 г дихлорметана при −10-0°C. После завершения добавления реакционную смесь перемешивали при 10-20°C в течение 4 часов. Добавляли 25 г 10% (по массе) раствора газообразного аммиака в метаноле при 10-20°C. Затем реакционную смесь перемешивали при 15-20°C в течение 3 часов. Реакционную жидкость выливали в 300 г смеси воды и льда и разделяли и затем водную фазу дважды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и дважды промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы добавляли 10,0 г холодного хлорбутана; затем смесь растирали, промывали и фильтровали с получением 24,9 г (2S,5R)-6-бензилокси-7-оксо-1,6-диазабицикло [3.2.1] октан-2-карбоксамида с общим выходом 90,5% и чистотой 99,9%, определенными с помощью HPLC.
Сравнительный пример 1. Получение 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV)
[0060] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г дихлорметана, 70 г 10% (по массе) водного раствора гидроксида натрия, 43,0 г (0,1 моль) бензил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-30°C в течение 3 часов. Затем реакционную смесь подкисляли до значения pH 2,5-3,0 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и один раз промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы получали 9,5 г 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты с выходом 38,1% и чистотой 98,1%, определенными с помощью HPLC.
[0061] В данном сравнительном примере показано, что если во время процедуры получения 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты количество основания является слишком низким, гидролиз будет неполным, что приводит к значительному снижению выхода 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты.
Сравнительный пример 2. Получение 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты (IV)
[0062] В 4-горлую колбу объемом 500 мл, оснащенную мешалкой и термометром, добавляли 150 г дихлорметана, 150 г 10% (по массе) водного раствора гидроксида натрия, 43,0 г (0,1 моль) бензил-5R-[(бензилокси)амино]пиперидин-2S-карбоксилата оксалата (III) и затем реакционную смесь перемешивали при 20-30°C в течение 3 часов. Затем реакционную смесь подкисляли до значения pH 1,5-1,9 с помощью 30% (по массе) водного раствора хлористоводородной кислоты и перемешивали при комнатной температуре в течение 1-2 часов. Смешанный раствор разделяли и затем водную фазу трижды экстрагировали дихлорметаном (каждый раз по 50 г). Органические фазы объединяли и один раз промывали насыщенным раствором хлорида натрия (каждый раз по 20 г). После извлечения растворителя из полученной органической фазы получали 18,2 г 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты с выходом 72,8% и чистотой 99,7%, определенными с помощью HPLC.
[0063] В данном сравнительном примере показано, что если во время процедуры получения 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты значение pH при подкислении является слишком низким, часть продукта превратится в гидрохлорид, который растворяется в воде, что приводит к снижению выхода 5R-[(бензилокси)амино]пиперидин-2S-карбоновой кислоты.